随着工业的发展,难降解有机物带来的水污染日益严重,传统方法难以去除[1]。阿特拉津(ATZ)是一种广泛使用的三嗪类除草剂,广泛分布于自然水系中,给人类带来严重的致癌风险[2]。现已发展出多种废水处理技术,例如吸附[3]、絮凝[4]、超滤[5]、生物[6]、光电催化[7,8]和高级氧化技术(Advanced oxidation processes,AOPs)[9-11]。其中,AOPs因其高效的污染物降解能力而受到广泛应用[12]。芬顿(Fenton)反应是基于过氧化氢(H2O2)的一种高效清洁的高级氧化技术,是近年来应用最广泛的高级氧化技术之一[13]。如式(1)所示,在此Fenton反应过程中,羟基自由基(·OH)由Fe2+和H2O2在酸性溶液中共同作用产生[14],其具有很强的氧化能力(E0=1.8~2.7 V),可与多种有机化合物发生反应[15]。然而,Fenton反应会消耗Fe2+,少部分可以通过H2O2原位还原Fe3+再生产生Fe2+,如式(2)所示。在这2个反应中,式(1)的速率常数在63~76 mol·L-1·s-1之间,而式(2)的速率常数约为0.01~0.02 mol·L-1·s-1,这表明Fe2+的消耗比再生快很多[16]。这导致在Fenton过程中Fe2+需求量较高。此外,为了保持Fe2+的强催化作用,溶液的pH值需保持在3.0~4.0,在pH值较高的情况下,由于氢氧化铁沉淀的生成会导致溶液中Fe离子的浓度降低[17]。在此过程中还会形成大量的氢氧化铁污泥,从而带来额外的分离和处理问题。
近年来,人们提出了各种方法来提高Fenton氧化工艺的效率,其中电-芬顿(electro-Fenton)工艺受到广泛关注[18]。传统的芬顿氧化工艺需要添加Fe(Ⅱ)盐,与之相比,电芬顿工艺可以通过以下2种方式更有效地提供Fe2+:(1)在阴极添加一定量的外部来源的Fe(Ⅲ)盐,从而进行Fe(Ⅱ)持续再生,如式(3)所示;(2)将铁作阳极,通过电化学氧化作用生成Fe(Ⅱ),如式(4)所示。在此基础上,通过添加H2O2和电化学还原,可以在适当pH值下有效去除有机污染物[19]。
然而,根据此种方法,在水处理过程中依旧会引入大量的Fe离子。因此,需要寻找一种无须向溶液中引入Fe(Ⅱ)离子也可激活H2O2的系统。根据相关报道,Fe的硫化物是一种高效的电激活H2O2的催化剂,将其原位负载在基底材料上可以合成自支撑阴极催化剂。采用此自支撑电极作阴极催化剂的电芬顿系统不仅可以减少铁离子的添加量和相应铁淤泥的生成量,还可以通过直接阳极氧化和Fe(Ⅲ)阴极还原促进污染物的降解。此外,该过程中外加电压的存在也能减缓催化剂的氧化失活与浸出。在电芬顿过程中,施加在催化剂表面的电压很大程度上影响了降解污染物的效率,但电压增加也会增加能量消耗。因此,降低在电芬顿过程中催化剂上的电压可以有效减少能量消耗,从而降低成本。
碳材料因其良好的导电性、高比表面积和环境友好,已成为电芬顿过程中常用的支撑电极基底[20]。有关研究表明,在碳材料中,石墨毡(GF)在低电流密度和中等电流密度下表现出更好的性能[21]。目前,相比于单一的Fe基催化剂,复合催化剂受到越来越多的关注,将Fe与其他过渡金属结合制备复合催化剂可以显著提高其对Fenton反应的催化活性。Mn基材料以其低成本、无毒性和多价态等优势,在催化领域得到了广泛的应用[22]。最近的研究表明,将Mn引入Fe中形成Fe-Mn复合材料对污染物的降解表现出了优异的活性[23]。这是由于Mn元素的引入可以加速各种价态Fe的相互转换,以生成更多有电芬顿活性的Fe(Ⅱ)物种。
本研究通过原位还原和硫化合成了自支撑电极材料。通过改变Mn元素的添加量以及硫化时间,获得了不同的催化剂,对材料的化学成分和形貌结构进行了表征和分析,将材料用作电激活H2O2的阴极催化剂,用于ATZ的降解,对系统降解ATZ的性能和稳定性进行了测试和分析。通过改变外加电压来探究不同系统在低电压下电激活H2O2的效果。通过对活性氧物种生成途径的分析,提出了H2O2在此电芬顿体系中的活化机理。总体而言,本研究通过调控阴极材料结构提升了电芬顿系统在低电压下的降解性能,因此在电芬顿过程的实际应用中具有巨大潜力。
1 实验部分
1.1 实验用主要试剂
无水乙醇(C2H5OH,分析纯)购于天津市江天化工有限公司。六水合三氯化铁(FeCl3·6H2O,99%,质量分数,下同)、β-胡萝卜素(96%)、过氧化氢(H2O2,30%)购于麦克林生化科技有限公司。硼氢化钠(NaBH4,分析纯)购于天津市大茂化学试剂有限公司。阿特拉津(ATZ,97%)购于天津希恩思生化有限公司。甲醇(MeOH,色谱级)购于天津科密欧化学试剂有限公司。一水合硫酸锰(MnSO4·H2O,99%)、硫酸钠(Na2SO4,99%)、九水合硫化钠(Na2S·9H2O,99.9%)、叔丁醇(TBA,99%)、对苯醌(p-BQ,99.5%)和甲基苯基亚砜(PMSO,98%)购于上海阿拉丁生化有限公司。
1.2 自支撑催化剂的制备
将石墨毡(GF)切割成所需的尺寸(1 cm× 2 cm)。分别用去离子水和乙醇反复清洗,并在热硝酸溶液(70 ℃)中浸泡2 h。处理后的GF基底用去离子水清洗后,在60 ℃鼓风干燥箱中干燥6 h,取出备用。x%Mn-FeS/GF(x=1, 5, 10)的制备流程如下:将前处理后的GF基底浸入100 mL含有0.015 mol·L-1 FeCl3·6H2O和一定浓度的MnSO4·H2O(0.15、0.75和1.50 mmol·L-1)的溶液中超声处理30 min。然后在上述溶液中逐渐滴加15 g·L-1的NaBH4溶液,在GF上沉积复合金属。密封反应一段时间后,将负载金属的GF通过去离子水和乙醇反复清洗多次得到前驱体。然后将制备的前驱体在1 mol·L-1的Na2S溶液中浸泡硫化一定时间(10~100 min),清洗完成后在60 ℃下真空干燥6 h得到x%Mn-FeS/GF样品。
1.3 催化剂表征测试
采用扫描电子显微镜(SEM,S4800)对制备材料的形貌结构进行表征。采用Bruker-Nonius D8 Focus型X射线衍射仪(XRD,Cu_Ka, λ= 0.154 nm)对材料的晶体结构进行表征。X射线光电子能谱(XPS,Thermo K-Alpha)用于对样品表面的元素组成、化学价态等方面进行分析。采用电感耦合等离子体发射光谱仪(ICP-OES,Aglient 5110)对测试样品的元素含量进行痕量分析。
1.4 电化学降解实验
室温下,在100 mL的电解池中进行电激活H2O2降解ATZ实验。在CHI 760电化学工作站上使用安培时间法(Amperometic,i-t)采用两电极体系进行电化学催化氧化反应。除非另有说明,降解系统的电压均为-1.5 V。将制备好的自支撑样品作阴极(催化剂浸入液面面积为1 cm× 1 cm),石墨棒作阳极。将ATZ溶液(10 mg·L-1,50 mL)置于电解池中,并以500 r·min-1的速率磁力搅拌降解。加入20 mmol·L-1 Na2SO4溶液作为支持电解质,并调节溶液pH值到3。加入5 mmol·L-1 H2O2后,通过电化学工作站在阴阳极施加一定电压开始反应。在降解过程中,每隔一定时间(1、2、5、10、20、30和60 min)取出0.5 mL溶液,然后与0.5 mL甲醇充分混合。通过微滤膜(0.22 μm)过滤后,使用配备C18色谱柱的高效液相色谱(HPLC)对混合溶液进行分析。HPLC流动相为甲醇/水(体积比为7∶3),流速为1.0 mL·min-1。在循环实验中,使用过的材料经去离子水和乙醇充分清洗并真空干燥后用于下一循环实验。
1.5 电化学测试
电化学测试是在CHI 760电化学工作站上采用标准三电极体系进行的。将制备好的自支撑样品(液面下面积1 cm×1 cm)作工作电极,石墨棒作对电极,Ag/AgCl电极作参比电极。支持电解质为50 mmol·L-1 Na2SO4溶液。开路电位测试(OCP)用于确定体系是否存在非自由基过程。电化学阻抗谱(EIS)用于测定催化剂的电化学交流阻抗,频率范围为0.01~106 Hz,交流电压振幅为5 mV。
2 结果与讨论
2.1 材料表征测试
2.1.1 材料微观形貌表征
在成功制备材料后,对其进行了扫描电子显微镜(SEM)测试,结果如图1所示。如图1(a)和图1(b)所示,金属硫化物活性物质以团簇的形式生长在碳纤维表面,且双金属的样品Mn-FeS/GF团簇的密集程度高于单金属样品FeS/GF。根据图1(c)和图1(d),团簇放大后由片状物质堆叠而成。相比于FeS/GF样品,由于Mn元素的引入,Mn-FeS/GF样品中片状结构明显增加。SEM的结论证明了催化剂的成功合成。

图1 (a);(c)FeS/GF和(b);(d)Mn-FeS/GF的SEM图像
Fig.1 SEM images of (a); (c) FeS/GF and (b); (d) Mn-FeS/GF
2.1.2 材料结构表征
为了进一步分析材料中的物质成分及组成,进行了XRD测试。如图2所示,GF基底的衍射峰是经典的C峰峰型。在GF的基础上,FeS/GF和Mn-FeS/GF 2种样品在17.6°、30.1°和40.0°处均有衍射峰的出现,这分别对应于FeS(PDF#10-037)的(001)、(101)和(111)晶面。而对于双金属复合材料Mn-FeS/GF,其在27.5°和45.7°处出现衍射峰,这分别对应于MnS(PDF#40-1288)的(111)和(220)晶面。分析XRD衍射结果可以得出,在样品中金属元素以及硫元素主要存在形式为FeS和MnS,这表明了双金属硫化物材料的成功合成。
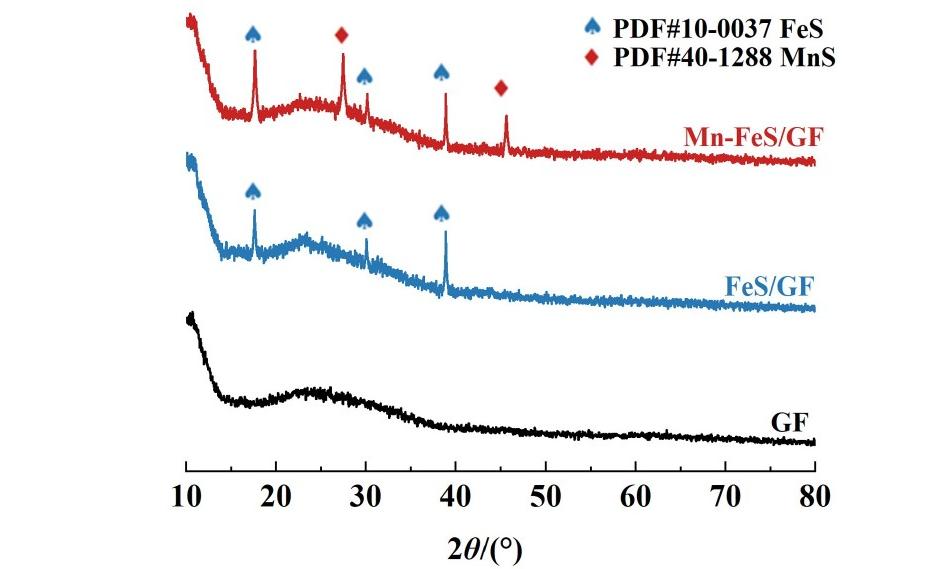
图2 FeS/GF和Mn-FeS/GF的XRD谱图
Fig.2 XRD spectra of FeS/GF and Mn-FeS/GF
2.1.3 材料元素分析
为了进一步分析样品表面的元素价态,进行了X射线光电子能谱(XPS)测试。Mn-FeS/GF样品的XPS全谱如图3(a)所示,O 1s的峰可能来自测试过程中材料被氧化或吸附了氧气。如图3(b)所示,在C 1s光谱中,有3个主峰位于284.3、285.6和287.9 eV处,分别对应于C![]() C、C—O和C
C、C—O和C![]() O[24]。含氧基团可能是在GF预处理过程中浓硝酸活化造成的,其存在可能会增强电极的亲水性[25]。
O[24]。含氧基团可能是在GF预处理过程中浓硝酸活化造成的,其存在可能会增强电极的亲水性[25]。
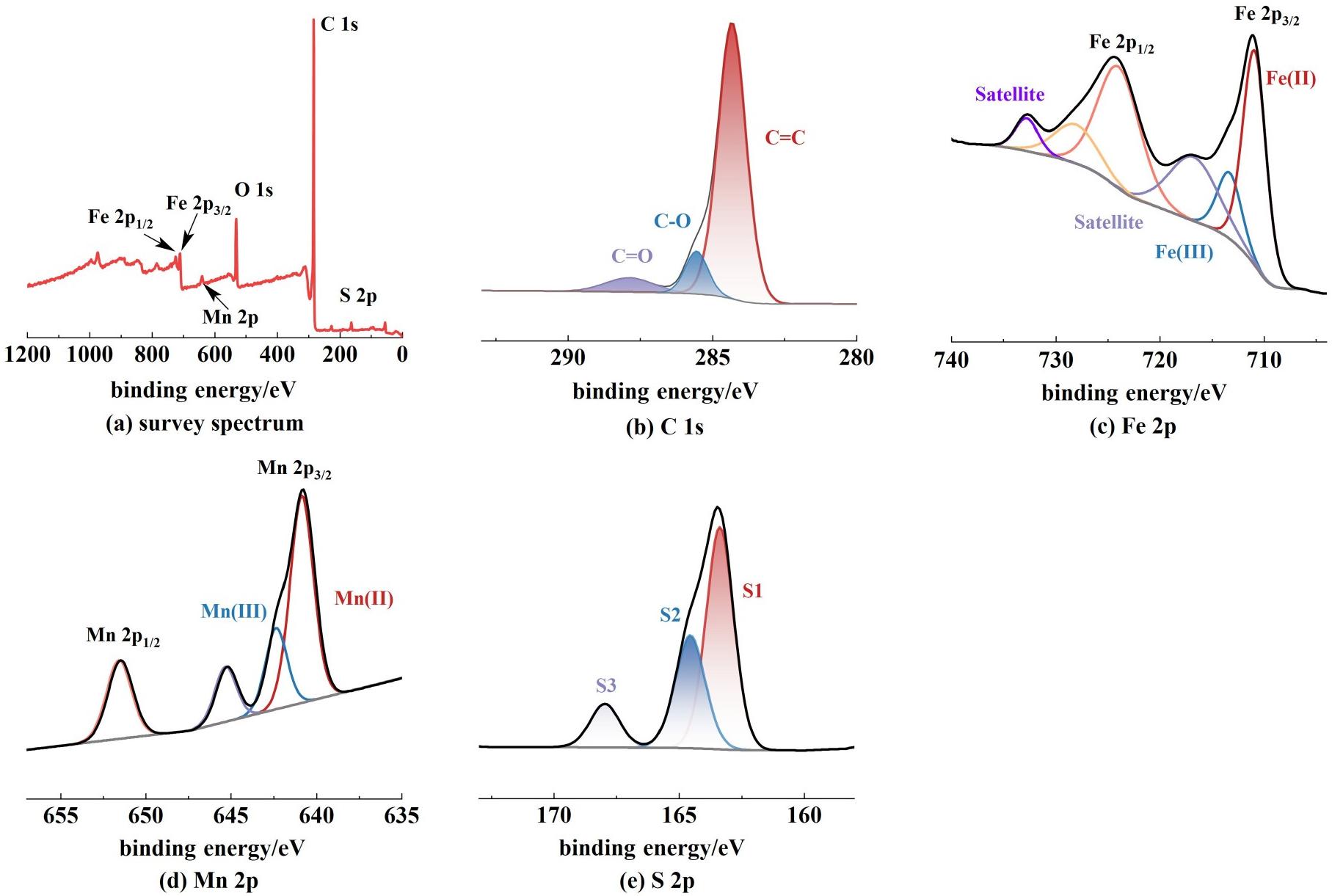
图3 Mn-FeS/GF的XPS谱图和精细谱
Fig.3 XPS spectra and high-resolution spectra of Mn-FeS/GF
根据图3(c),位于711.2和723.4 eV处的峰分别对应Fe 2p3/2和Fe 2p1/2,且Fe 2p3/2光谱可以分解Fe(Ⅱ)(710.9 eV)和Fe(Ⅲ)(711.3 eV)[26]。Fe(Ⅱ)含量较高的原因可能是在制备过程中Fe未完全硫化。如图3(d)显示,Mn 2p光谱出现了2个主要衍射峰Mn 2p3/2(641.2 eV)和Mn 2p1/2(651.5 eV),且Mn 2p3/2衍射峰可以分解为Mn(Ⅱ)(640.7 eV)和Mn(Ⅲ)(642.7 eV)[27]。Mn 2p的卫星峰(645.2 eV)的出现进一步证明了Mn(Ⅱ)的存在[28]。
如图3(e)所示,S 2p光谱出现了3个衍射峰,分别标记为S1、S2和S3。根据相关报道,S1(163.4 eV)对应于硫与金属的结合,对于Mn-FeS/GF催化剂即为S与Fe和Mn结合[27]。S2(164.6 eV)对应于材料合成过程中使用的硫源的残留物。S3(168.0 eV)则对应于S氧化后的产物![]() ,这是由于催化剂制备过程一直在空气条件下表层的S元素遭到氧化[29]。综上所述,XPS分析进一步证明了Mn-FeS材料的成功合成。
,这是由于催化剂制备过程一直在空气条件下表层的S元素遭到氧化[29]。综上所述,XPS分析进一步证明了Mn-FeS材料的成功合成。
2.2 降解性能测试
2.2.1 材料制备条件的优化
图4探究了不同条件下制备的Mn-FeS/GF催化剂,包括硫化时间以及Mn比例对激活H2O2降解ATZ性能的影响。
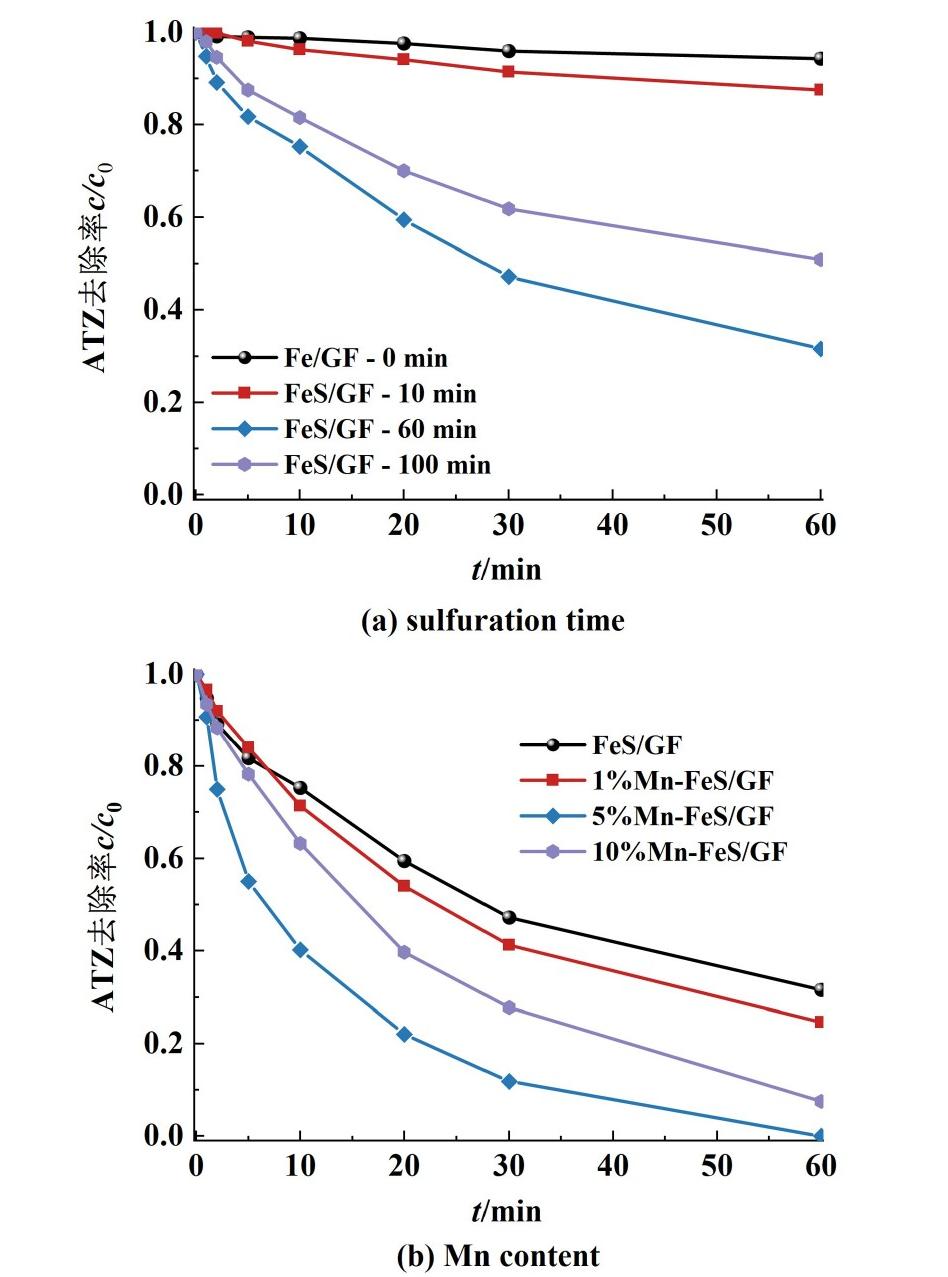
图4 不同制备条件下的催化剂性能
Fig.4 The performance of catalysts under different preparation condition
如图4(a)所示,以不同硫化时间的不含Mn的FeS/GF材料为目标催化剂,当不硫化或者硫化时间过短(10 min)时,体系对ATZ的去除率极低,这代表未经硫化或者硫化不完全的催化剂基本不具备阴极电激活H2O2的活性。而随着硫化时间的延长,在经过60 min硫化的FeS/GF催化剂具有相对最高的ATZ去除率,在60 min内达到70%。随着硫化时间的进一步延长,催化剂性能略微下降,这可能是因为长时间的硫化使得其内部结构遭到了破坏。因此,催化剂制备过程中最合适的硫化时间为60 min。
图4(b)探究了材料制备过程中不同Mn比例对制备的Mn-FeS/GF催化剂的性能的影响,硫化时间均为60 min。可以看出,Mn元素的引入增强了催化剂的降解性能。添加了5%Mn元素[n(Mn)/n(Fe)]制备出的催化剂具有最好的电激活H2O2性能,在30 min可以降解90%的ATZ。然而,随着Mn比例进一步升高,制备的催化剂的降解性能有所降低。根据SEM分析的结果,这可能是由于过量的Mn覆盖了Fe活性位点,影响到了电-芬顿反应的进行。因此5%的Mn添加比例制备出的催化剂具有相对最好的活性。综上所述,后续的目标催化剂均在Mn添加量5%,硫化时间60 min的条件下制备,并且统一命名为Mn-FeS/GF。
2.2.2 电激活H2O2性能
如图5(a)所示,探究了GF基底以及不同催化剂对ATZ的吸附效果。结果显示,对于每种催化剂和GF基底,其对于目标污染物ATZ均几乎没有吸附作用。因此,在该体系中,可以完全忽略吸附作用对于ATZ去除率的影响。图5(b)显示了不同催化剂在体系中电激活H2O2降解ATZ性能,可以看出GF基底对于ATZ几乎没有催化性能,且不含Fe的MnS/GF的性能较差。不含Mn的FeS/GF催化剂在60 min内可以约降解70%的ATZ。随着Mn元素的引入,催化剂降解性能得到了极大提升,可以在60 min内实现对污染物的完全降解。上述实验证明了Fe与Mn元素在阴极活化H2O2的协同作用。
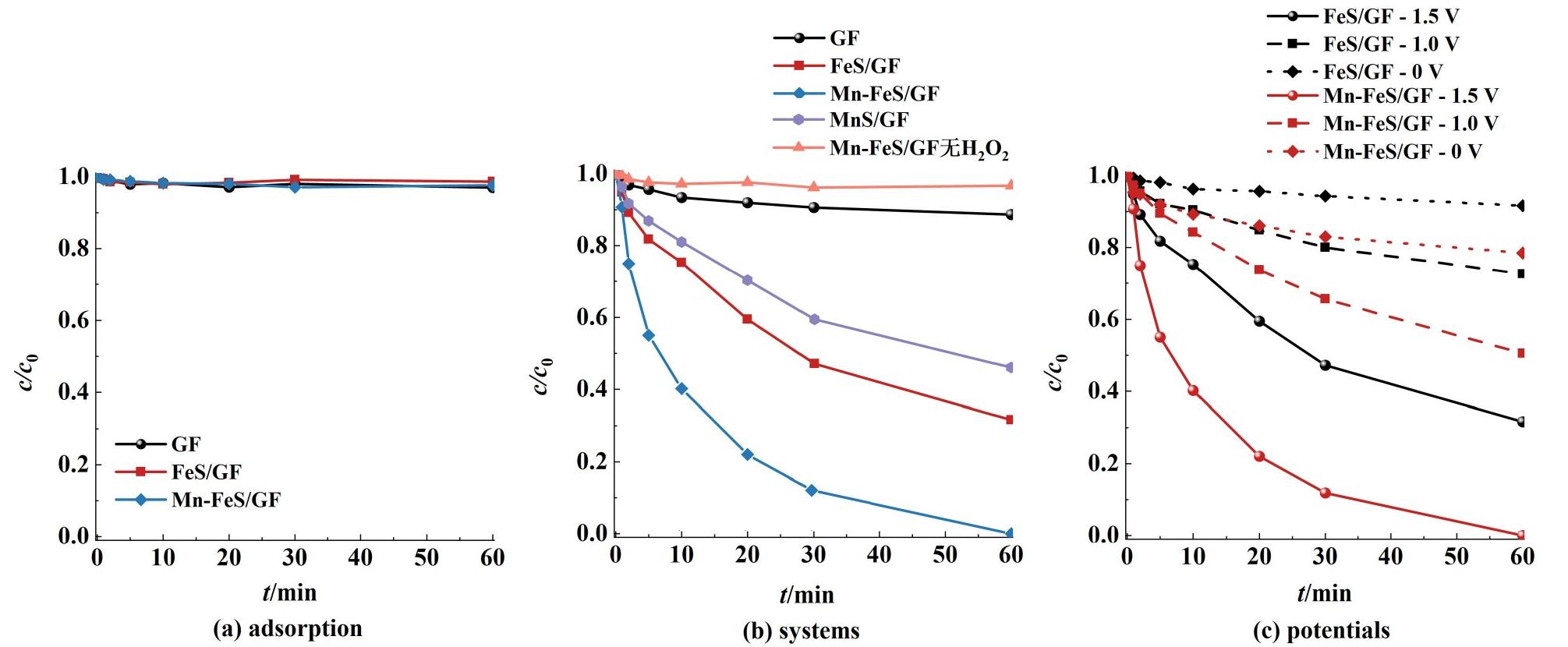
图5 不同催化剂的降解性能
Fig.5 Degradation performance of different catalysts
为了探究不同外加电压下2种催化剂的实际降解性能,在对外加电压降低的条件下进行了降解过程,结果如图5(c)所示。对于FeS/GF和Mn-FeS/GF 2种催化剂,在无外加电压情况下,其催化性能均较弱。随着电压从-1.5降低至-1.0 V,催化剂的性能都有所降低,但是含Mn的Mn-FeS/GF催化剂的性能明显优于不含Mn的FeS/GF催化剂。这表明Mn元素的引入可以使得催化剂在低电压下具有更高的电激活H2O2性能。
此外,对不同催化剂及外加电压下的降解性能进行了一阶反应动力学拟合,得到了相应的一阶反应速率。如图6所示,在引入Mn后,Mn-FeS/GF的反应速率提高至FeS/GF的3倍。且在较低电压下,Mn-FeS/GF的反应速率也是FeS/GF的2倍。因此,Mn的引入提升了催化剂的性能。
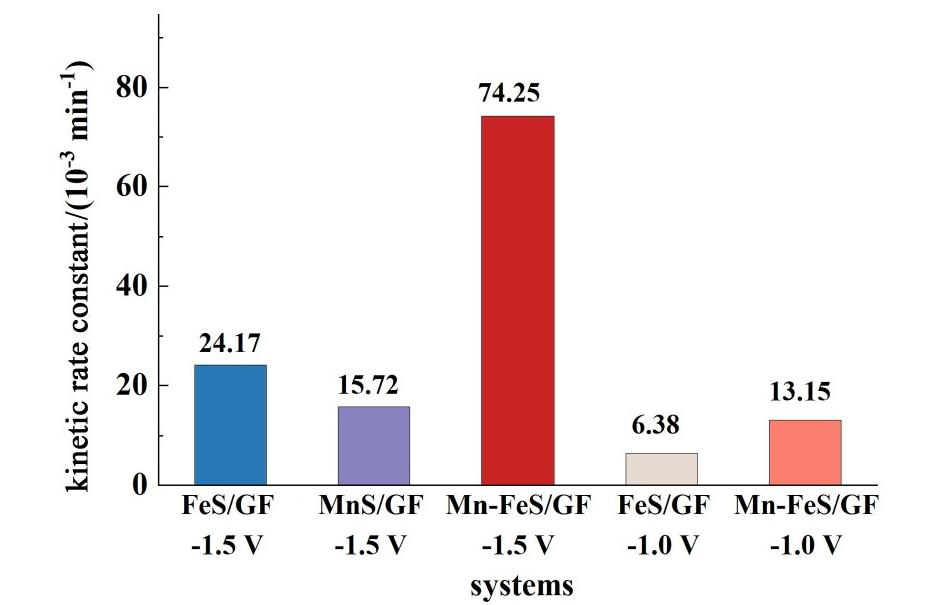
图6 不同系统的一阶反应速动力学常数
Fig.6 The first-order kinetic rate constants in different systems
对催化剂的稳定性进行了测试,如图7所示。结果显示,FeS/GF催化剂在3次反应循环中,ATZ去除率从70%下降至不足50%。而Mn-FeS/GF催化剂在第2次循环使用中仍可在60 min内降解90%的ATZ,且在第3圈循环使用中可以在60 min内降解超80%的ATZ。这表明了Mn的引入提升了催化剂的循环稳定性。
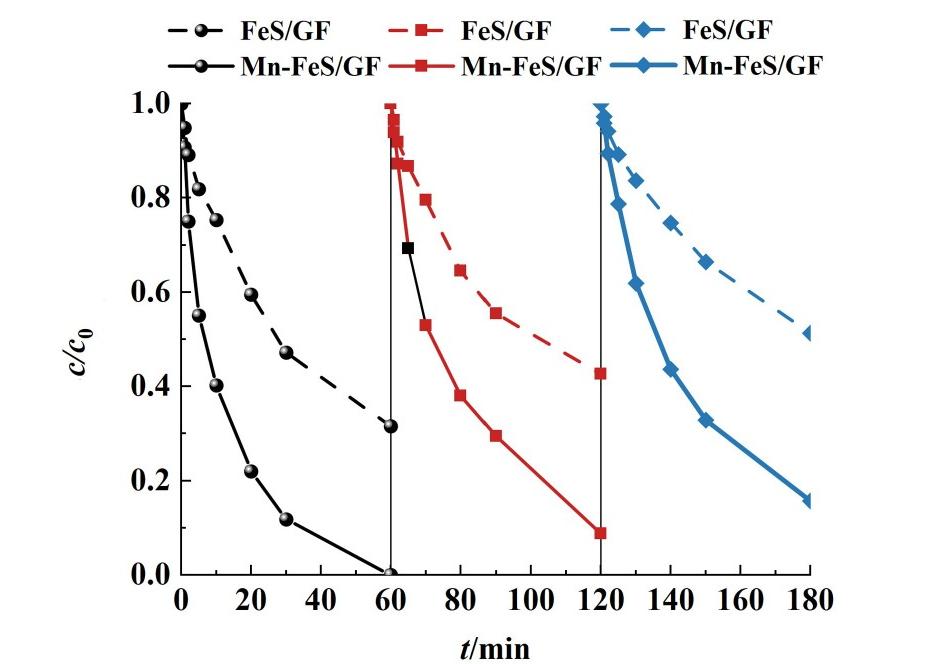
图7 FeS/GF和Mn-FeS/GF的稳定性测试
Fig.7 Stability and reusability test of FeS/GF and Mn-FeS/GF
2.2.3 离子浸出分析
为了探究Mn-FeS/GF催化剂的失活原因,通过ICP测试检测了降解反应后溶液中的Fe和Mn离子浓度。如表1所示,对于Mn-FeS/GF样品,其在第1次循环实验中浸出了1.695 mg·L-1的Fe离子。而在后续2次循环中,Fe离子的浸出浓度均小于0.4 mg·L-1。这表明大部分金属浸出发生于第1次循环反应中,后2次循环反应的金属浸出较少。通过结合稳定性测试的结果,Mn-FeS/GF样品在第2次循环反应中性能出现明显下降,而第3次循环反应前后的性能并没有较大差别。因此,金属浸出问题是催化剂性能降低的重要因素。通过与SEM分析的结果结合,第1次循环实验中,外层的金属硫化物脱落并浸出,导致催化剂的性能显著下降。除此之外,通过ICP测试,经过10 min硫化的Mn-Fe/GF样品的浸出远远高于正常样品,浸出离子浓度超过了100 mg·L-1。这可能是催化剂外层硫化不完全,导致其内部金属也浸出。此外,正常样品的离子浸出均较小,具有一定环境友好性。
表1 金属离子浸出浓度
Table 1 The concentration of metal leaching ions
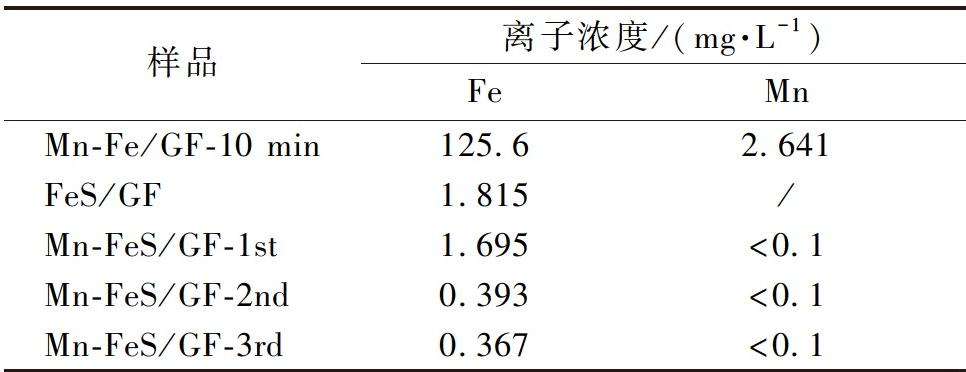
Mn-Fe/GF-10 min 125.62.641 Mn-FeS/GF-2nd0.393<0.1 Mn-FeS/GF-3rd0.367<0.1样品离子浓度/(mg·L-1)FeMn FeS/GF1.815/Mn-FeS/GF-1st1.695<0.1
2.2.4 电化学阻抗分析
为了探究不同催化剂的电化学反应电子转移步骤动力学差异,进行了电化学交流阻抗谱(EIS)测试。将测试得到数据使用Zview软件进行拟合分析,拟合模型及结果如图8所示。引入了Mn元素后的Mn-FeS/GF催化剂的阻抗比FeS/GF有所减小。这表明Mn元素的存在可以加快催化剂的电子转移。
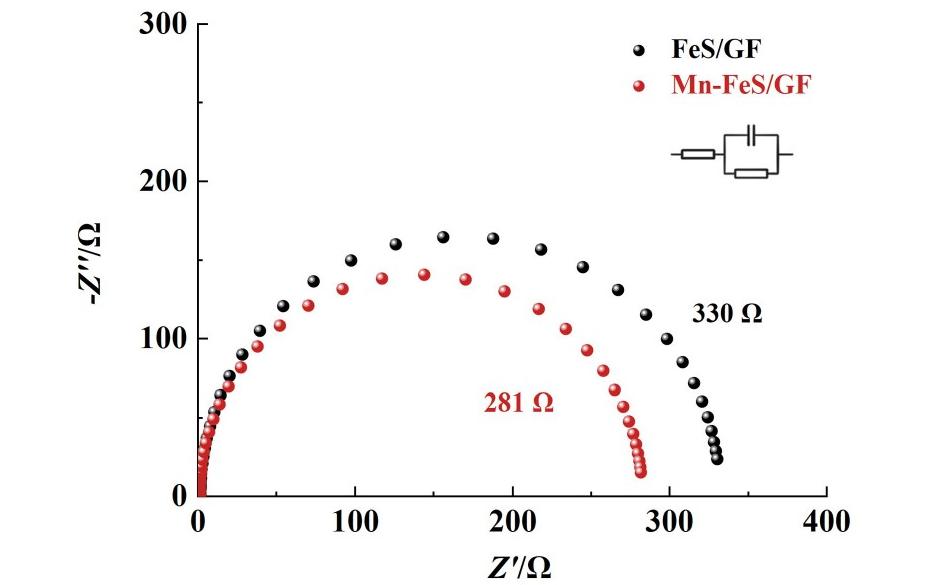
图8 样品的EIS曲线
Fig.8 EIS Nyquist plots of samples
2.3 降解机理研究
2.3.1 猝灭实验
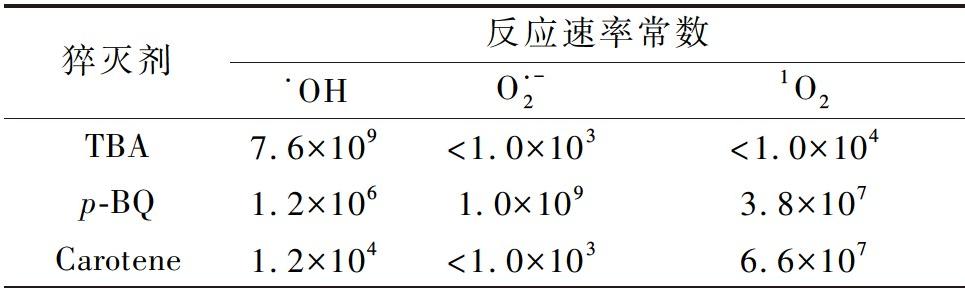
为了探究各种活性氧物种(ROSs)在电激活H2O2反应中的作用,进行了自由基猝灭实验。一些特定的自由基猝灭剂可以与相应的自由基快速反应并使其无法参与污染物降解,以达到在反应中猝灭相应自由基的作用。叔丁醇(TBA)可以与·OH快速发生反应,是一种理想的·OH猝灭剂。对苯醌(p-BQ)可以有效猝灭超氧自由基![]() 胡萝卜素(carotene)被广泛应用于单线氧自由基(1O2)的猝灭。由于催化剂中主要成分为Fe元素,因此在反应过程中可能有高价铁的影响。根据相关报道,甲基苯基亚砜(PMSO)是一种有效猝灭高价铁物种的猝灭剂[30]。各ROSs猝灭剂与相应自由基的反应速率常数如表2所示[31]。
胡萝卜素(carotene)被广泛应用于单线氧自由基(1O2)的猝灭。由于催化剂中主要成分为Fe元素,因此在反应过程中可能有高价铁的影响。根据相关报道,甲基苯基亚砜(PMSO)是一种有效猝灭高价铁物种的猝灭剂[30]。各ROSs猝灭剂与相应自由基的反应速率常数如表2所示[31]。
表2 ROSs猝灭剂与相应自由基的反应速率常数
Table 2 Rate constants for the reaction of ROSs scavengers with the corresponding radicals
猝灭剂反应速率常数·OHO·-21O2TBA7.6×109<1.0×103<1.0×104 p-BQ1.2×1061.0×1093.8×107 Carotene1.2×104<1.0×1036.6×107
自由基猝灭实验的结果如图9所示,从图9中可以看出,各种猝灭剂加入后,催化剂的性能均受到一定影响。加入TBA后,催化反应的降解速率降低得最显著,从100%下降至不足10%。这表明·OH在反应中占主导地位。除此之外,p-BQ的加入也使反应降解率降低至约20%,这表明![]() 在反应中也起到一定作用。β-胡萝卜素对反应的猝灭有一定作用但是效果不明显,这表明1O2存在于反应系统中,但是作用不明显。PMSO加入后,体系的反应速率并没有太多影响,这表明高价铁氧化作用的贡献很小,基本不在系统中出现。因此,猝灭实验结果显示,
在反应中也起到一定作用。β-胡萝卜素对反应的猝灭有一定作用但是效果不明显,这表明1O2存在于反应系统中,但是作用不明显。PMSO加入后,体系的反应速率并没有太多影响,这表明高价铁氧化作用的贡献很小,基本不在系统中出现。因此,猝灭实验结果显示,![]() 和1O2均存在于反应中,且·OH和
和1O2均存在于反应中,且·OH和![]() 对电激活H2O2降解ATZ过程起到关键作用。
对电激活H2O2降解ATZ过程起到关键作用。
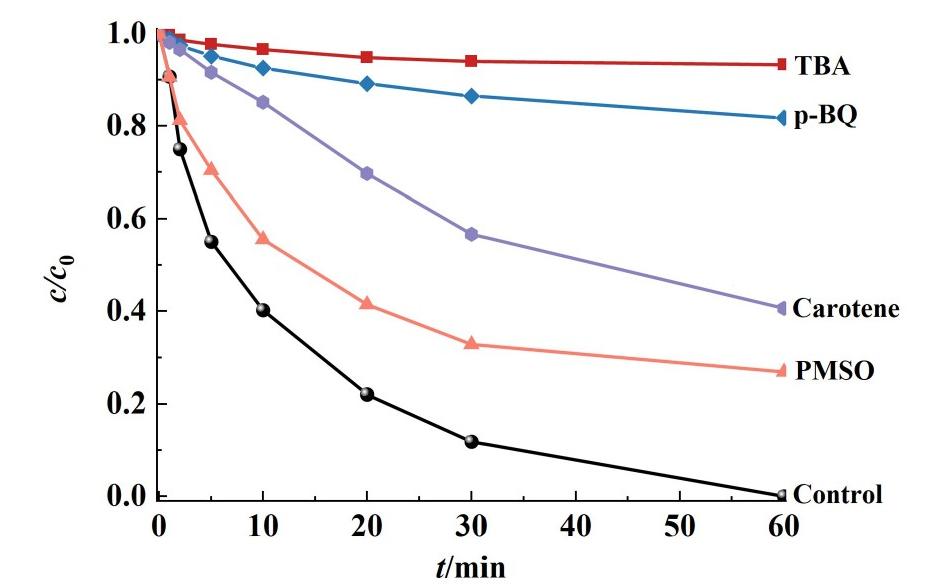
图9 不同猝灭剂对ATZ降解的影响
Fig.9 Inhibition effect of various scavengers on ATZ degradation
2.3.2 开路电位测试
为了探究电激活H2O2降解ATZ过程中的直接电子转移过程(Direct electron-transfer,DET)的作用,进行了开路电位测试(Open circuit potential,OCP)。为了确保溶液的导电性,测试开始之前,向体系中加入50 mmol·L-1的Na2SO4溶液作为支持电解质。如图10所示,在200 s时,向体系中加入5 mmol·L-1 H2O2后,体系的电位出现明显上升,这表明出现了催化剂电激活H2O2产生ROSs的过程,引起了催化剂表面电荷的重新排布。此外,在400 s时,向溶液中加入污染物ATZ,体系的电位几乎没有变化,这说明电化学系统中没有发生直接电子转移过程。此外,根据图5(b),不添加H2O2的系统对ATZ的去除率很低,这表明了系统中不存在直接阳极氧化过程。因此,综上所述,Mn-FeS/GF电活化H2O2系统中不存在直接电子转移过程。
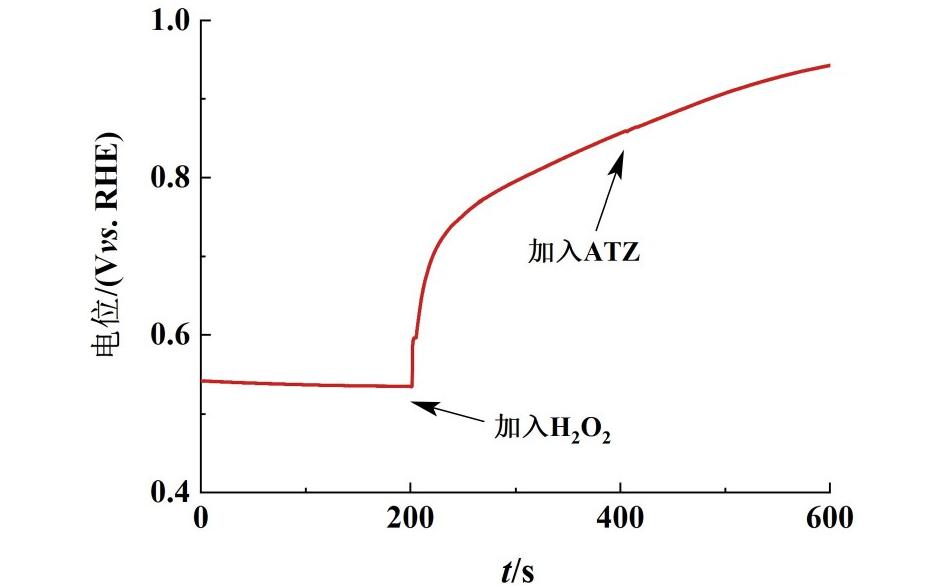
图10 Mn-FeS/GF的开路电位测试
Fig.10 OCP curves of Mn-FeS/GF
2.3.3 催化剂反应失活分析
为了研究催化剂失活过程的机制,比较了反应前后Mn-FeS/GF催化剂的XPS光谱。如图11所示,反应后,Fe(Ⅱ)的相对含量从76.05%下降至69.20%,Fe(Ⅲ)的相对含量从23.95%上升到了30.80%。相似的,Mn(Ⅱ)的含量从73.51%下降至63.42%,Mn(Ⅲ)的相对含量从26.49%上升到了36.58%。证明了Fe(Ⅱ)/Fe(Ⅲ)和Mn(Ⅱ)/Mn(Ⅲ)之间的价态转换,此过程可以用式(5)和式(6)来表明。此外,反应后的Mn 2p光谱强度相对于反应前明显降低。这表明反应后Mn元素浸出较为严重,这也与ICP测试的结果保持一致。
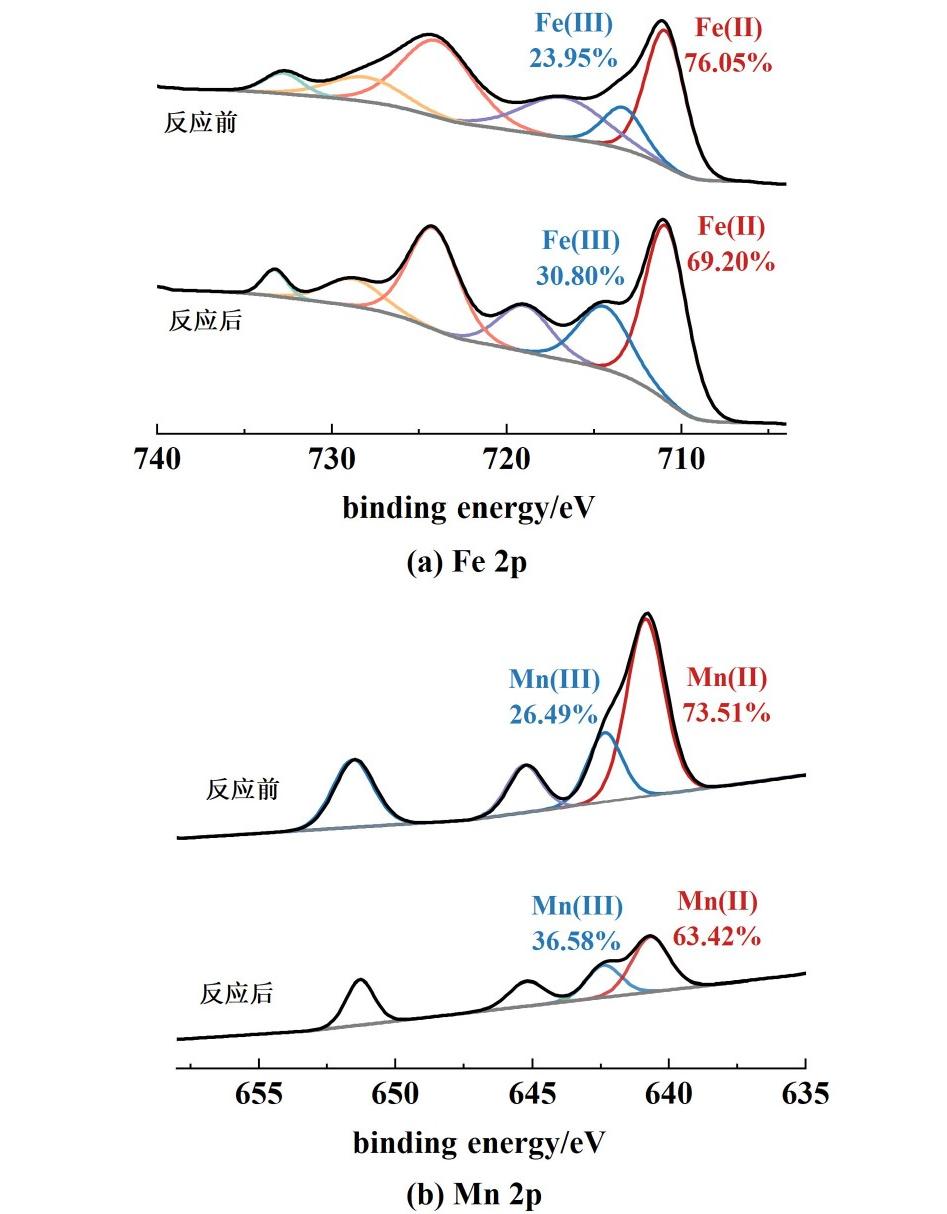
图11 反应前后Mn-FeS/GF的XPS谱图
Fig.11 XPS spectra of Mn-FeS/GF before and after the reaction
Mn元素具有多种价态,可以与Fe(Ⅲ)反应,将其还原为具有芬顿活性的Fe(Ⅱ)[25]。在Mn(Ⅲ)和Mn(0)的作用下,Fe(Ⅱ)和Mn(Ⅱ)通过式(11)和式(12)所示的反应产生。此外,阴极的电流还会将无催化活性的Fe(Ⅲ)/Mn(Ⅲ)还原为有活性的Fe(Ⅱ)/Mn(Ⅱ),也可以增加催化剂的活性及稳定性。
2.3.4 活化机理的提出
一般情况下,1O2可以通过3种路径生成,分别是空气中O2溶解、H2O2自分解和·OH与H2O2反应产生[32-34]。向反应体系中通入氮气以去除溶解氧,降解性能基本没有增强。在图5(b)中,用GF基底取代催化剂的体系对ATZ的降解性能大幅度降低。这表明1O2无法通过前2种路径生成,因此大部分是由·OH于H2O2反应生成。因此,Mn-FeS/GF电激活H2O2系统中的自由基催化氧化途径如下:
3 结论
本研究通过原位还原并硫化合成了复合双金属硫化物样品Mn-FeS/GF。将其用作自支撑阴极电激活H2O2降解ATZ。其在电化学系统中表现出优异的ATZ降解性能,可以在30 min内降解90%的污染物,对比无Mn元素的FeS/GF催化剂性能具有显著提升。通过探究改变外加电压对降解结果的影响,发现了Mn的引入还会使得低电压下的催化剂性能保持在一定水平。该阴极催化剂具有良好的稳定性及较低的金属离子浸出。猝灭实验结果显示,反应系统中存在![]() 和1O2,且·OH和
和1O2,且·OH和![]() 对反应过程起到关键作用。本研究合成出了一种用于电激活H2O2降解污染物的高效自支撑催化剂Mn-FeS/GF,且Fe和Mn之间存在协同作用,为电-芬顿过程的实际应用提供了一种有效策略。
对反应过程起到关键作用。本研究合成出了一种用于电激活H2O2降解污染物的高效自支撑催化剂Mn-FeS/GF,且Fe和Mn之间存在协同作用,为电-芬顿过程的实际应用提供了一种有效策略。
[1] WANG J, WANG S. Activation of persulfate (PS) and peroxymonosulfate (PMS) and application for the degradation of emerging contaminants[J]. Chemical Engineering Journal, 2018, 334: 1502-1517
[2] ZENG X, SHI X, SUN Z. Degradation of atrazine by electroactivation of persulfate using FeCuO@C modified composite cathode:Synergistic activation mechanism[J]. Chemosphere, 2023, 332:138860
[3] ROBATI D, MIRZA B, RAJABI M, et al. Removal of hazardous dyes-BR 12 and methyl orange using graphene oxide as an adsorbent from aqueous phase[J]. Chemical Engineering Journal, 2016, 284: 687-697
[4] FAN J, GRANDE C D, RODRIGUES D F. Biodegradation of graphene oxide-polymer nanocomposite films in wastewater[J]. Environmental Science: Nano, 2017, 4(9): 1808-1816
[5] YANG C, WANG P, LI J, et al. Photocatalytic PVDF ultrafiltration membrane blended with visible-light responsive Fe(Ⅲ)-TiO2 catalyst: Degradation kinetics, catalytic performance and reusability[J]. Chemical Engineering Journal, 2021, 417: 129340
[6] JIANG L, LUO C, ZHANG D, et al. Shifts in a phenanthrenedegrading microbial community are driven by carbohydrate metabolism selection in a ryegrass rhizosphere[J]. Environmental Science & Technology, 2021, 55(2): 962-973
[7] SONG R, CHI H, MA Q, et al. Highly efficient degradation of persistent pollutants with 3D nanocone TiO2-based photoelectrocatalysis[J]. Journal of the American Chemical Society, 2021, 143(34): 13664-13674
[8] SU L, WANG D, MA D, et al. Regulating local electron density of iron single sites by introducing nitrogen vacancies for efficient photo-Fenton process[J]. Angewandte Chemie International Edition, 2021, 60(39): 21261-21266
[9] XIE M, DAI F, LI J, et al. Tailoring the electronic metal-support interactions in supported atomically dispersed gold catalysts for efficient Fenton-like reaction[J]. Angewandte Chemie International Edition, 2021, 60(26): 14370-14375
[10] LI X, HUANG X, XI S, et al. Single cobalt atoms anchored on porous N-doped graphene with dual reaction sites for efficient Fenton-like catalysis[J]. Journal of the American Chemical Society, 2018, 140(39): 12469-12475
[11] CHEN D, ZHANG D, LIU P, et al. Confining free radicals in close vicinity to contaminants enables ultrafast Fenton-like processes in the interspacing of MoS2 membranes[J]. Angewandte Chemie International Edition, 2019, 58(24): 8134-8138
[12] LI M, LI W, BOLTON J R, et al. Organic pollutant degradation in water by the vacuum-ultraviolet/ultraviolet/H2O2 process: Inhibition and enhancement roles of H2O2[J]. Environmental Science & Technology, 2019, 53(2): 912-918
[13] WENG C, CHUANG Y H, DAVEY B, et al. Reductive electrochemical activation of hydrogen peroxide as an advanced oxidation process for treatment of reverse osmosis permeate during potable reuse[J]. Environmental Science & Technology, 2020, 54(19): 12593-12601
[14] LI Y, MILLER C J, WU L, et al. Hydroxyl radical production via a reaction of electrochemically generated hydrogen peroxide and atomic hydrogen: An effective process for contaminant oxidation?[J]. Environmental Science & Technology, 2022, 56(9): 5820-5829
[15] XIE M, DAI F, WANG Y, et al. Electronic metal-support interaction directing the design of Fe(Ⅲ)-based catalysts for efficient advanced oxidation processes by dual reaction paths[J]. Small,2022, 18(33): 2203269
[16] BABUPONNUSAMI A, MUTHUKUMAR K. Advanced oxidation of phenol: A comparison between Fenton, electro-Fenton, sonoelectro-Fenton and photo-electro-Fenton processes[J]. Chemical Engineering Journal, 2012, 183: 1-9
[17] GALLARD H, DE LAAT J, LEGUBE B. Spectrophotometric study of the formation of iron(Ⅲ)-hydroperoxy complexes in homogeneous aqueous solutions[J]. Water Research, 1999, 33(13): 2929-2936
[18] BRILLAS E, SIRÉS I, OTURAN M A. Electro-Fenton process and related electrochemical technologies based on Fenton’s reaction chemistry[J]. Chemical Reviews, 2009, 109(12): 6570-6631
[19] KURT U, APAYDIN O, GONULLU M T. Reduction of COD in wastewater from an organized tannery industrial region by Electro-Fenton process[J]. Journal of Hazardous Materials, 2007, 143(1/2): 33-40
[20] SONG H R, YAN L, JIANG J, et al. Enhanced degradation of antibiotic sulfamethoxazole by electrochemical activation of PDS using carbon anodes[J]. Chemical Engineering Journal, 2018,344: 12-20
[21] SOPAJ F, RODRIGO M A, OTURAN N, et al. Influence of the anode materials on the electrochemical oxidation efficiency. Application to oxidative degradation of the pharmaceutical amoxicillin[J]. Chemical Engineering Journal, 2015, 262: 286-294
[22] WAN Z, WANG J. Degradation of sulfamethazine using Fe3O4-Mn3O4/reduced graphene oxide hybrid as Fenton-like catalyst[J]. Journal of Hazardous Materials, 2017, 324: 653-664
[23] DU J, BAO J, LIU Y, et al. Facile preparation of porous Mn/Fe3O4 cubes as peroxymonosulfate activating catalyst for effective bisphenol A degradation[J]. Chemical Engineering Journal,2019, 376: 119193
[24] LAI C, HUANG F, ZENG G, et al. Fabrication of novel magnetic MnFe2O4/bio-char composite and heterogeneous photo-Fenton degradation of tetracycline in near neutral pH[J]. Chemosphere,2019, 224: 910-921
[25] LI B, YAN Z, LIU X, et al. Enhanced bio-electro-Fenton degradation of phenolic compounds based on a novel Fe-Mn/graphite felt composite cathode[J]. Chemosphere, 2019, 234: 260-268
[26] XI Y, XIE T, LIU Y, et al. Carboxymethyl cellulose stabilized ferrous sulfide@extracellular polymeric substance for Cr(Ⅵ) removal: Characterization, performance, and mechanism[J].Journal of Hazardous Materials, 2022, 425: 127837
[27] HEIBA Z K, DEYAB M A, FARAG N M, et al. Electrochemical performance of nano CuCo2O4 and MnS solid solution[J].Journal of Sol-Gel Science and Technology, 2022, 103(3): 843-852
[28] QI K, WANG Y, RENGARAJ S, et al. MnS spheres: Shapecontrolled synthesis and its magnetic properties[J]. Materials Chemistry and Physics, 2017, 193: 177-181
[29] GE Y, WU J, XU X, et al. Facile synthesis of CoNi2S4 and Cu-Co2S4 with different morphologies as prominent catalysts for hydrogen evolution reaction[J]. International Journal of Hydrogen Energy, 2016, 41(44): 19847-19854
[30] YAO J, WU N, TANG X, et al. Methyl phenyl sulfoxide (PM-SO) as a quenching agent for high-valent metal-oxo species in peroxymonosulfate based processes should be reconsidered[J]. Chemical Engineering Journal Advances, 2022, 12: 100378
[31] WANG J, LI B, LI Y, et al. Facile synthesis of atomic Fe-N-C materials and dual roles investigation of Fe-N4 sites in Fenton-like reactions[J]. Advanced Science, 2021, 8(22): 2101824
[32] HUANG Y, TIAN X, NIE Y, et al. Enhanced peroxymonosulfate activation for phenol degradation over MnO2 at pH 3.5 to 9.0 via Cu(Ⅱ) substitution[J]. Journal of Hazardous Materials,2018, 360: 303-310
[33] ZHOU Y, JIANG J, GAO Y, et al. Activation of peroxymonosulfate by benzoquinone: A novel nonradical oxidation process[J].Environmental Science & Technology, 2015, 49(21):12941-12950
[34] GAO Y, DUAN X, LI B, et al. Fe containing template derived atomic Fe-N-C to boost Fenton-like reaction and charge migration analysis on highly active Fe-N4 sites[J]. Journal of Materials Chemistry A, 2021, 9(26): 14793-14805