环己烷和乙醇为典型的二元共沸体系,在化工生产过程中经常出现[1,2],共沸物中环己烷的摩尔分率为55%,采用普通的精馏方法无法实现其二元组分的清晰分离。萃取精馏作为一种用于分离共沸和近沸混合物体系的有效分离方法,在工业上得到了广泛应用[3]。
离子液体(ILs)作为一种新型的萃取剂,具有溶解能力强、热稳定高、蒸汽压低、环境友好以及易于回收循环使用等优点[4],近年来受到了广泛关注[5-7]。
王孝科等[8]分别选用离子液体[BMIM][Cl]、[BMIM][BF4]和[BMIM][PF6]作为萃取剂,研究了3种离子液体对环己烷-乙醇二元体系相对挥发度的影响,发现[BMIM][PF6]的效果最好,可将环己烷对乙醇相对挥发度提高至4.94。丁瀚忠等[9]以[N14111][OAc]为萃取剂对环己烷-乙醇共沸体系进行萃取精馏分离研究,利用Aspen Plus软件对该分离过程进行了模拟,得到了最适宜工艺参数。此外,张羽等[10]也对采用3种不同的离子液体作为萃取剂萃取精馏分离环己烷-乙醇二元体系进行了研究,发现萃取精馏的分离效果顺序为:[N1,8,8,8][Ac]>[DMIM][Ac]>[C16MIM][Ac]。当[N1,8,8,8][Ac]的物质的量分数达到0.10时,共沸现象被完全消除。李焕新等[11]基于COSMO-RS理论模型采用COSMOthermX软件筛选出[1,3-dihydroxylimidazolium][PF6]作为萃取剂,研究了离子液体萃取剂对环己烷-乙醇体系汽液平衡的影响。
本研究针对环己烷-乙醇共沸体系,采用COS-MOthermX19版本软件,基于COSMO-RS理论模型[12-17],根据选择性与溶解度等因素对20种阳离子和23种阴离子组成的460种离子液体进行了萃取剂筛选,结果表明,三丁基乙基膦丙酸盐([P2,4,4,4][Pr])作为萃取剂最为适宜。测定了乙醇-环己烷-[P2,4,4,4][Pr]三元体系的等压汽液相平衡数据,使用NRTL模型进行关联,用Aspen Plus V11版本软件对萃取精馏进行了工艺模拟并对过程参数进行了优化,基于σ-profiles图分析了萃取精馏的分离机理。
1 实验部分
1.1 实验仪器及试剂
实验中的乙醇和环己烷均购自国药集团化学试剂有限公司,质量分数≥99.7%;[P2,4,4,4][Pr]购自兰州雨陆精细化学有限公司,质量分数≥99%。实验前,离子液体在真空干燥箱中干燥48 h,干燥温度为333.15 K,干燥压力2 kPa。干燥后含水量低于5× 10-4 (Karl-Fischer法测定)。
实验和测试的设备包括北洋化工有限公司提供的CE-2型汽液相平衡釜,安捷伦7820A气相色谱仪,上海思达分析仪器有限公司HS-9顶空进样器,奥豪斯仪器(常州)有限公司PR224ZH电子天平。
气相色谱条件为:FID检测,进样口及检测器温度分别为473.15和453.15 K,柱箱温度为315.15 K,载气流速20.1 cm3·min-1。
1.2 实验过程和理论分析方法
采用标准不确定度为0.000 1 g的电子天平称量环己烷、乙醇和[P4442][Pr],配制液相样品并注入平衡釜中。加热平衡釜中溶液至部分汽化,由标准不确定度为0.01 K的温度计进行温度测量,当蒸汽温度在30 min内不发生变化时,系统被认为达到了平衡,进行汽液相取样。采用连接顶空进样器的气相色谱对样品中环己烷和乙醇含量进行测定。由于离子液体的蒸汽压极低,可以忽略不计,通过差重法计算了离子液体的含量。每个样品至少重复测量3次,3种组分的物质的量分数不确定度为0.001。
气相常压下按理想气体处理,液相的非理想性采用NRTL模型描述。NRTL模型计算公式如下[18,19]:
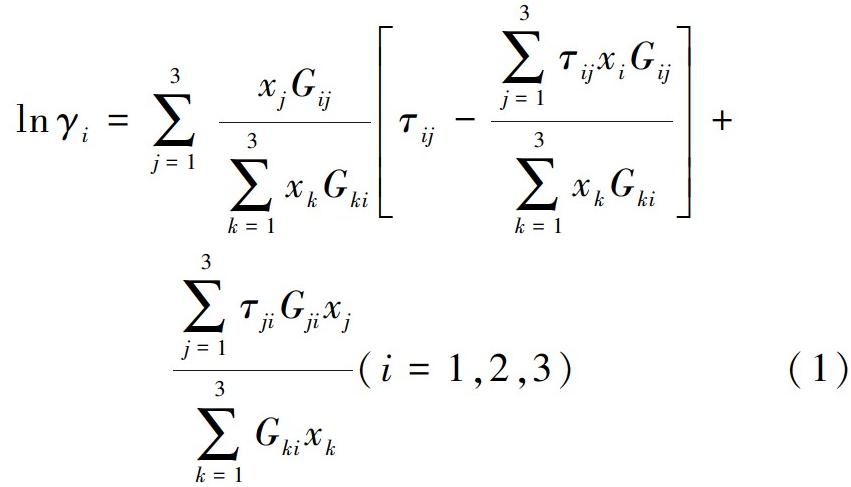
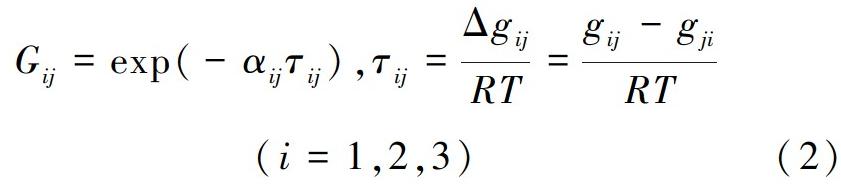
式(2)中:αij为非随机参数,Δgij是相互作用能参数,R是理想气体常数,T是平衡温度。通过最小化γi的平均相对偏差(ARD)获得NRTL模型的9个参数(α12,α13,α23,Δg12,Δg21,Δg23,Δg32,Δg13,Δg31)。ARD表达式为:
式(3)中:n为总点数;![]() 为组分i活度系数的实验值;
为组分i活度系数的实验值;![]() 是基于NRTL关联式的组分活度系数的计算值。
是基于NRTL关联式的组分活度系数的计算值。
依据平均相对挥发度(![]() )对离子液体的分离能力做出评价,其计算公式为公式(4)。
)对离子液体的分离能力做出评价,其计算公式为公式(4)。
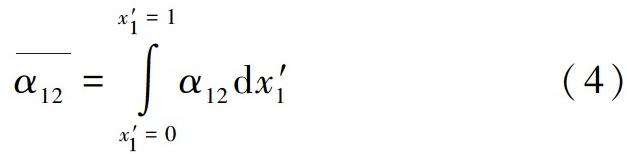
软件COSMO-thermX以分子表面的极化电荷密度、氢键强度和氢键阈值等微观信息的量化计算为基础,与离子液体分离在无限稀释浓度下的选择性和针对真实溶剂类导体构建屏蔽模型结合,计算出分子的电荷密度,应用于分离过程的物性预测。其中分子表面等面积片段的屏蔽电荷密度称为σ,单个分子表面的三维空间电荷密度的分布函数 ρs (σ) 为该分子表面上 σ 的相对量,σ-profile 为体系中的三维空间电荷密度的分布函数与溶剂分子表面积AS的加权平均值。
2 结果与讨论
2.1 实验数据
为了检验实验设备和方法的可靠性,在101.3 kPa下测量了环己烷(1)+乙醇(2)体系的二元汽液相平衡数据,测得的结果和文献值[20]基本一致,采用Herington的面积检验法[21],得到D=12.086,J=3.191,![]() D-J
D-J![]() ≤10,符合热力学一致性,表明实验方法和装置是可靠的。
≤10,符合热力学一致性,表明实验方法和装置是可靠的。
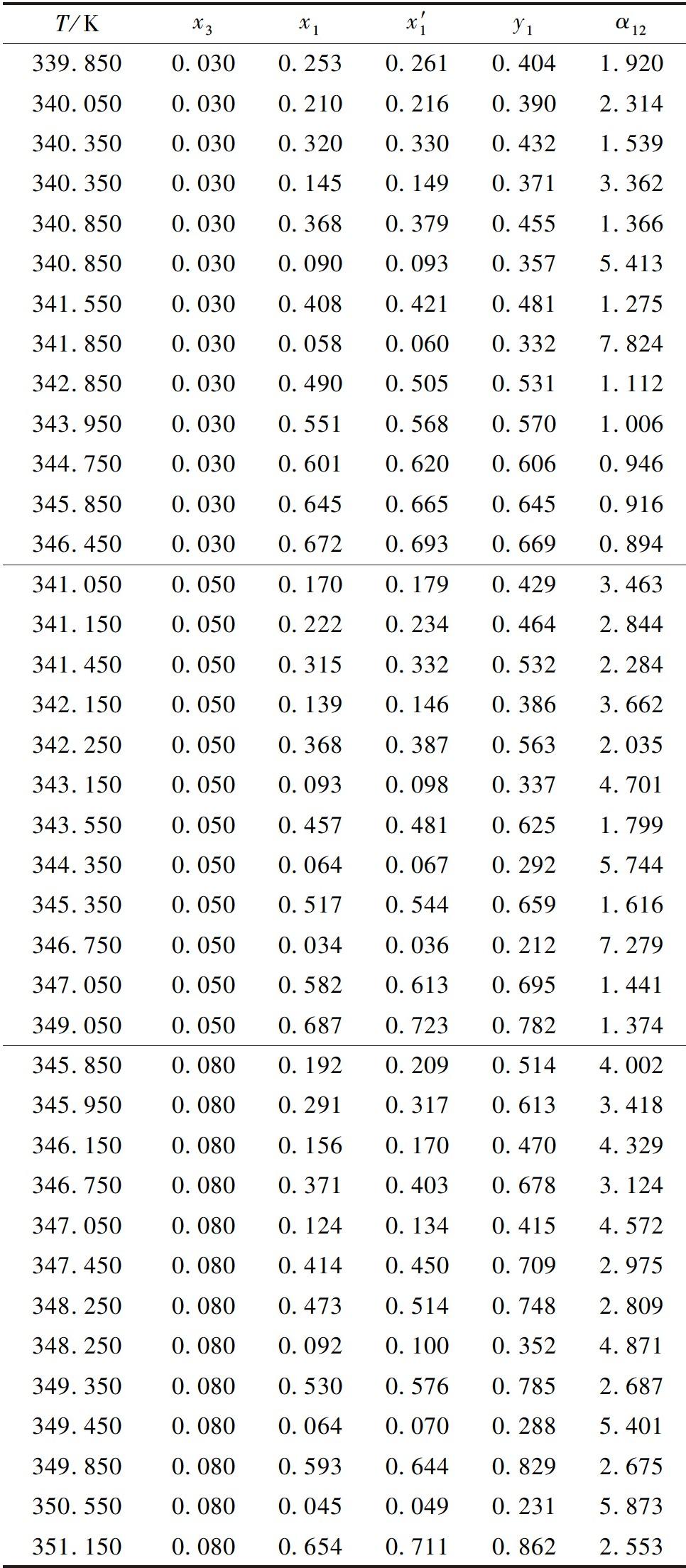
表1和图1显示了三元体系环己烷(1)+乙醇(2)+[P2,4,4,4][Pr](3)在101.3 kPa条件下的汽液相平衡数据。离子液体的物质的量分数(x3)分别是0.03、0.05和0.08。其中T为系统平衡温度,x1是液相中环己烷的物质的量分数,![]() 是除去离子液体后环己烷的物质的量分数,y1为气相中环己烷的物质的量分数;α12为组分环己烷对乙醇的相对挥发度;γ1和γ2分别为液相中环己烷和乙醇的活度系数。
是除去离子液体后环己烷的物质的量分数,y1为气相中环己烷的物质的量分数;α12为组分环己烷对乙醇的相对挥发度;γ1和γ2分别为液相中环己烷和乙醇的活度系数。
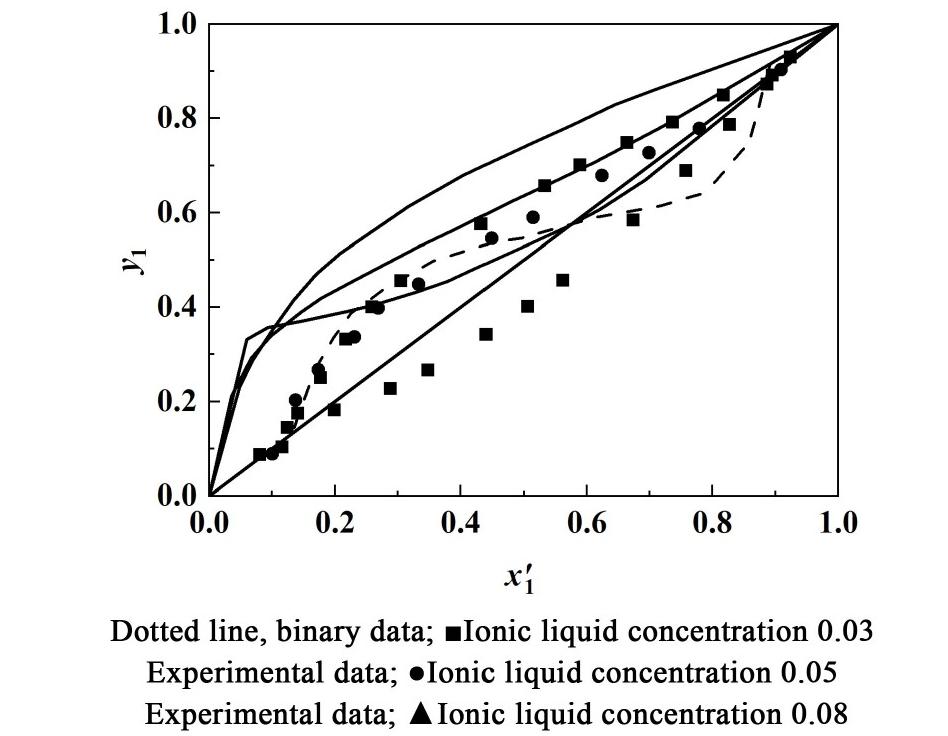
图1 环己烷(1)+乙醇(2)+[P2,4,4,4][Pr](3)三元体系在101.325 kPa下的![]() 图
图
Fig.1 ![]() of cyclohexane (1) + ethanol (2) +[P2,4,4,4][Pr] (3) ternary system at 101.325 kPa
of cyclohexane (1) + ethanol (2) +[P2,4,4,4][Pr] (3) ternary system at 101.325 kPa
表1 三元体系汽-液平衡实验数据
Table 1 Experimental data of vapor-liquid equilibrium in ternary system
340.350 0.030 0.320 0.330 0.432 1.539 341.550 0.030 0.408 0.421 0.481 1.275 342.150 0.050 0.139 0.146 0.386 3.662 346.750 0.050 0.034 0.036 0.212 7.279 347.050 0.050 0.582 0.613 0.695 1.441 349.050 0.050 0.687 0.723 0.782 1.374 345.850 0.080 0.192 0.209 0.514 4.002 345.950 0.080 0.291 0.317 0.613 3.418 347.050 0.080 0.124 0.134 0.415 4.572 347.450 0.080 0.414 0.450 0.709 2.975 350.550 0.080 0.045 0.049 0.231 5.873 351.150 0.080 0.654 0.711 0.862 2.553 T/Kx3x1x1′y1α12339.850 0.030 0.253 0.261 0.404 1.920 340.050 0.030 0.210 0.216 0.390 2.314 340.350 0.030 0.145 0.149 0.371 3.362 340.850 0.030 0.368 0.379 0.455 1.366 340.850 0.030 0.090 0.093 0.357 5.413 341.850 0.030 0.058 0.060 0.332 7.824 342.850 0.030 0.490 0.505 0.531 1.112 343.950 0.030 0.551 0.568 0.570 1.006 344.750 0.030 0.601 0.620 0.606 0.946 345.850 0.030 0.645 0.665 0.645 0.916 346.450 0.030 0.672 0.693 0.669 0.894 341.050 0.050 0.170 0.179 0.429 3.463 341.150 0.050 0.222 0.234 0.464 2.844 341.450 0.050 0.315 0.332 0.532 2.284 342.250 0.050 0.368 0.387 0.563 2.035 343.150 0.050 0.093 0.098 0.337 4.701 343.550 0.050 0.457 0.481 0.625 1.799 344.350 0.050 0.064 0.067 0.292 5.744 345.350 0.050 0.517 0.544 0.659 1.616 346.150 0.080 0.156 0.170 0.470 4.329 346.750 0.080 0.371 0.403 0.678 3.124 348.250 0.080 0.473 0.514 0.748 2.809 348.250 0.080 0.092 0.100 0.352 4.871 349.350 0.080 0.530 0.576 0.785 2.687 349.450 0.080 0.064 0.070 0.288 5.401 349.850 0.080 0.593 0.644 0.829 2.675
从表1和图1可以看出:随着离子液体浓度的增大,共沸点向上移动。当离子液体浓度达到0.05时,共沸点消失。说明[P2,4,4,4][Pr]可显著提高环己烷-乙醇共沸物系的分离效果。
表2示出了NRTL[22]方程非随机参数及相互作用能参数拟合的结果,最小化ARD的值是1.85,图1中的实线为NRTL方程的拟合曲线。表2中很小的ARD值和图1中拟合线与实验点非常吻合,表明NRTL方程具有较高的拟合精度。利用NRTL方程计算出[P2,4,4,4][Pr]打破共沸所需最小物质的量分数为0.046,效果优于文献报道的[N1,8,8,8][Ac]、[DMIM][Ac]、[C16MIM][Ac]、[N14,1,1,1][OAc]等离子液体。计算获得离子液体在物质的量分数为0.05、0.08处![]() 值分别为1.77和2.29。说明离子液体的加入能有效提高环己烷对乙醇的相对挥发度,且随着离子液体加入量的添加,相对挥发度也相应增加,分离效果提高。
值分别为1.77和2.29。说明离子液体的加入能有效提高环己烷对乙醇的相对挥发度,且随着离子液体加入量的添加,相对挥发度也相应增加,分离效果提高。
表2 NRTL模型的参数
Table 2 Parameters of NRTL model

注:αij and Δgji are NRTL model parameters; R is the ideal gas constant; ARD is the average relative deviation.
componentjαijΔgij/R Δgji/R ARD/%cyclohexanethanol0.499674.422492.4060.60 Cyclohexan[P2,4,4,4][Pr]0.118-3 711.9367 5001.85 ethanol[P2,4,4,4][Pr]0.600-771.711965.4701.85
2.2 [P2,4,4,4][Pr]萃取精馏分离环己烷-乙醇过程模拟
采用Aspen Plus V11版本软件,以[P2,4,4,4][Pr]为萃取剂,原料离子液体和共沸体系在常温(298.15 K)常压(101.3 kPa)下分别以5 kmol·h-1和100 kmol·h-1的流量[n(环己烷)∶ n(乙醇)为1∶1)]进入萃取精馏塔,产品要求环己烷和乙醇产品的物质的量分数要求达到99.7%,操作压力为常压。萃取精馏分离环己烷-乙醇工艺流程由萃取精馏塔(EDC)和溶剂回收塔(SRC)等设备组成,如图2所示。
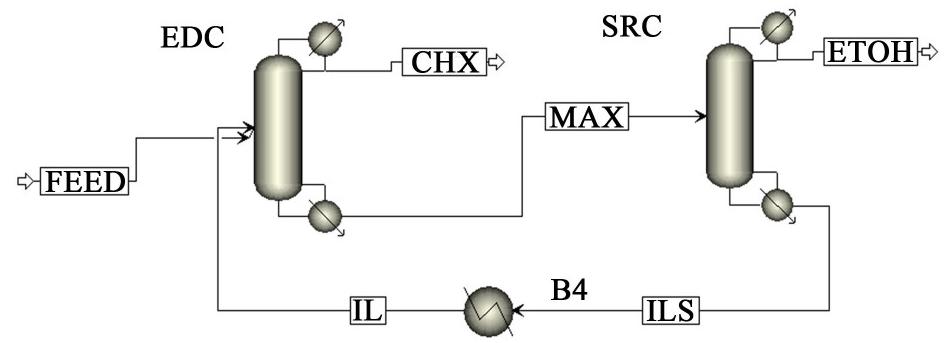
图2 萃取精馏工艺流程图
Fig.2 Process flow chart of extractive distillation
离子液体的物质的量分数选择需要在实验范围内能够消除共沸现象,所以离子液体的物质的量分数应高于最小打破共沸0.046。离子液体和共沸体系在常温(298.15 K)常压(101.3 kPa)下分别以5和100 kmol·h-1的流量[n(环己烷)∶n(乙醇)为1∶1)]进入EDC,轻组分环己烷从精馏段塔顶馏出,乙醇和[P2,4,4,4][Pr]由EDC塔底进入SRC,SRC顶部馏出乙醇,塔底流出[P2,4,4,4][Pr]进入SRC循环使用。通过对产品对纯度、冷凝器和再沸器热负荷的研究对2个塔的塔板数、进料位置和回流比进行了优化,其中环己烷和乙醇产品的物质的量分数要求达到99.7%,在此前提下冷凝器和再沸器热负荷越小越好。
模拟过程中使用的离子液体[P4,4,4,2][Pr]不是常见化合物,需要新建于Aspen Plus软件数据库中有关于 [P4,4,4,2][Pr]的热力学参数的物性参数(Tb、Tc、pc、Vc和ω),其物性参数采用由 Valderrama等修正的可确保离子液体关键特性预测值准确的基团贡献法[23]进行预测。预测结果列于表3中。
表3 [P2,4,4,4][Pr]的物性参数
Table 3 The Physical parameter of [P2,4,4,4][Pr]
MTb/KTc/Kpc/kPaVc/(mL·mol-1)ω304.5683.7855.31 3521 120.80.939 9
图3示出了EDC塔板数对环己烷物质的量分数、冷凝器和再沸器热负荷的影响。
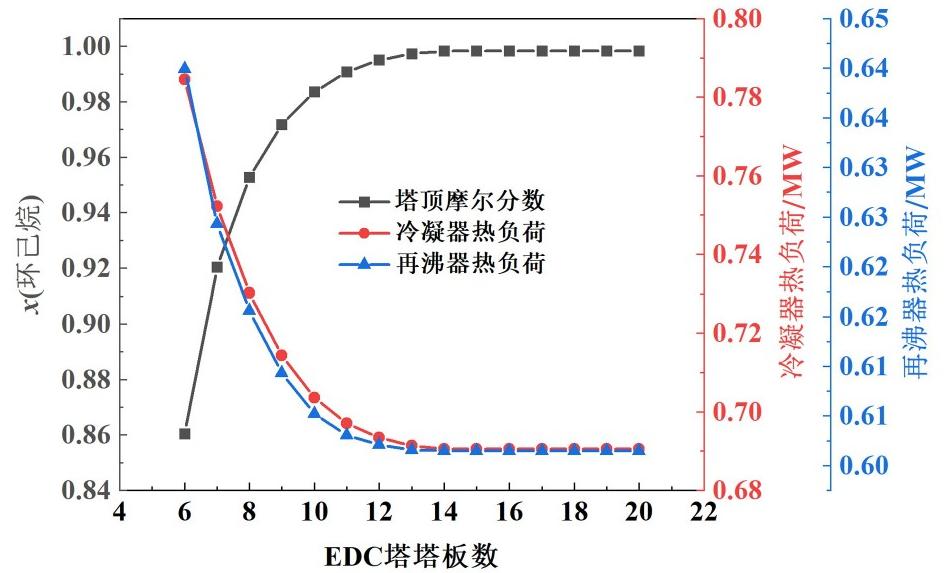
图3 萃取精馏塔塔板数的影响
Fig.3 Influence of EDC plate count
从图3中可见在EDC总塔板数少于12块时,环己烷的物质的量分数随塔板数的增多而明显提高,冷凝器和再沸器的热负荷随塔板数的增加显著下降。在EDC总塔板数多于12块后,环己烷的物质的量分数、冷凝器和再沸器的热负荷随塔板数增多的变化不明显。塔板数为12块时环己烷物质的量分数可达99.50%, 当塔板数为13块时,环己烷物质的量分数高达99.73%。因为塔板数的增加将导致精馏塔的设备费用升高,同时,在产品纯度、冷凝器和再沸器的热负荷不随塔板数的增加发生明显变化时,增多塔板数也会使萃取精馏过程的总费用提高。因此,在可达到环己烷体积分数大于99.7%的产品要求条件下,适宜的EDC塔板数为13。
图4为原料的进料位置对环己烷物质的量分数、冷凝器和再沸器热负荷的影响。
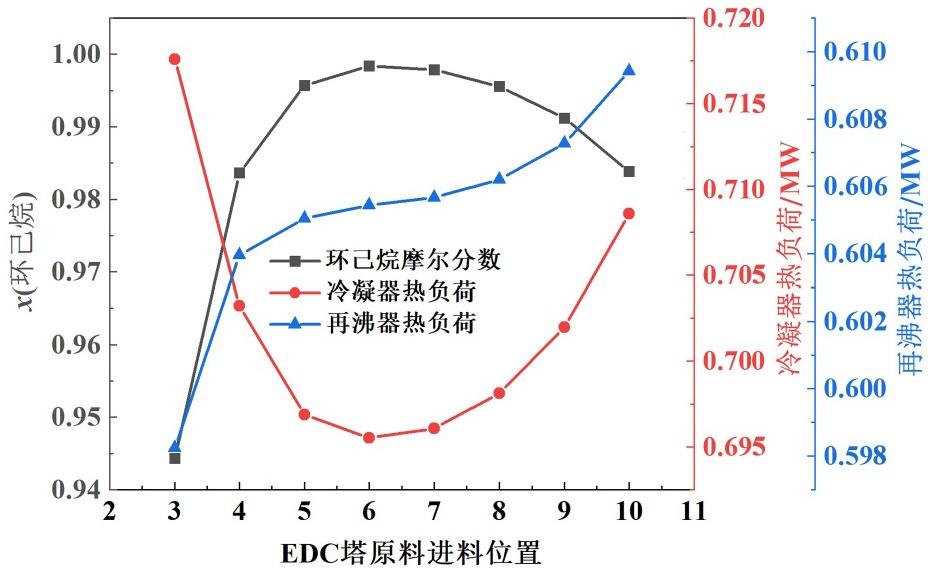
图4 原料进料位置的影响
Fig.4 Influence of raw material feeding position
环己烷物质的量分数随着进料板板数的增加先变大后减小,从第5块塔板进料时,环己烷物质的量分数为99.57%,从第6块塔板进料时,环己烷物质的量分数是99.84%,从第7块塔板进料时,环己烷物质的量分数为97.88%。冷凝器热负荷随进料板板数先减小后增大,从第6块塔板进料时热负荷最小。再沸器热负荷随进料塔板板数增加而增大,增大的速率是先减小后增加。
此外,从图4中可以看出只有从第6块塔板进料才能满足产品体积分数达到99.7%的要求,因此,进料板确定为第6块。环己烷物质的量分数随进料板板数变化出现最大值,以及冷凝器热负荷随进料板板数变化出现最小值,这是因为总塔板数已经确定,进料位置过高会降低精馏段的分离效率,而进料位置过低会降低提馏段分离效率。再沸器热负荷随进料板位置增加而升高是由于提馏段被减小。再沸器热负荷增加速率的变化也和总塔板数已被固定有关,当精馏段或提馏段太短时,再沸器热负荷的变化都会更加明显。
图5示出了EDC回流比对环己烷物质的量分数、冷凝器和再沸器热负荷的影响。
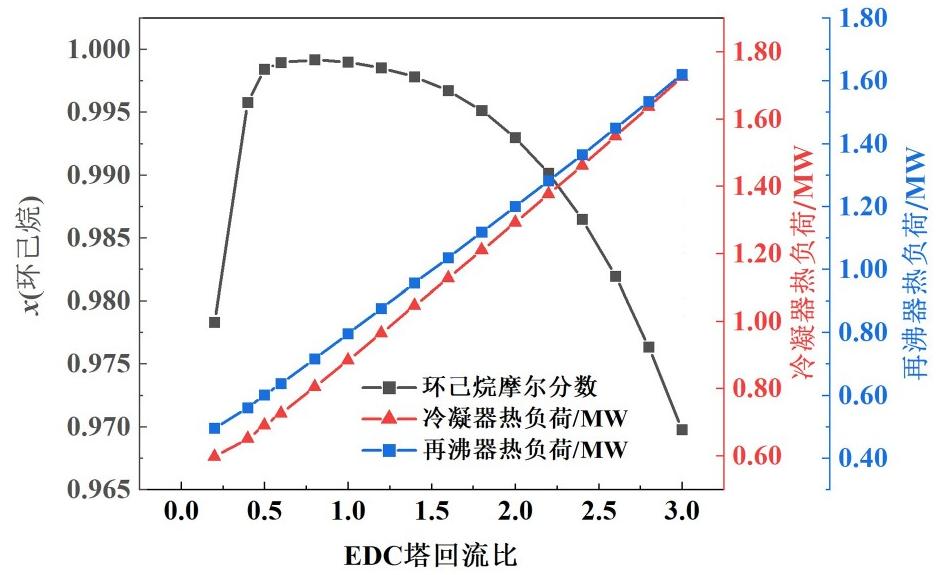
图5 萃取精馏塔回流比对萃取精馏的影响
Fig.5 Effect of reflux ratio on extractive distillation
从图5中可见,在回流比低于0.5时,环己烷物质的量分数随回流比增加显著提高,当回流比大于0.5时,环己烷物质的量分数随回流比的增大而下降。冷凝器和再沸器热负荷均随回流比增加而显著升高。回流比为0.4时,产品环己烷物质的量分数为99.58%,回流比为0.5时环己烷物质的量分数可达99.84%,回流比0.6时环己烷物质的量分数为99.89%。
由于回流比为0.5或0.6时,环己烷物质的量分数均高于设计要求的99.7%,但0.5时冷凝器热负荷和再沸器热负荷明显小于0.6时的热负荷,因此回流比选用0.5。
综合考虑产品的物质的量分数、冷凝器和再沸器热负荷,EDC理论板数确定为13块,原料的进料位置选定为第6塔板,回流比选择为0.5。采用同样方法可得到SRC的塔板数为6,进料位置为第3块塔板,回流比选择为0.2。
2.3 机理分析
图6是[P2,4,4,4]+、[Pr]-、环己烷和乙醇的σ谱图。纵坐标ρ (σ)为分子表面的三维空间电荷密度的分布函数 ,也就是该分子表面上 σ 的相对量。
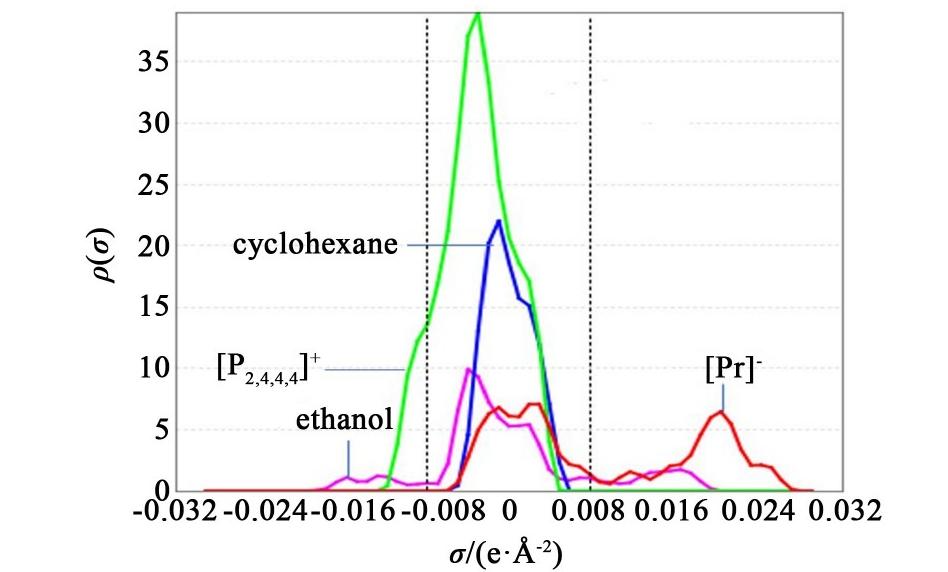
图6 环己烷、乙醇和[P2,4,4,4][Pr]的σ-profiles图
Fig.6 σ-profiles of cyclohexane, ethanol and [P2,4,4,4][Pr]
图6中垂直虚线所示的 0.0082和-0.0082分别为氢键受体区和氢键给体区的边界,σ峰值越大、峰的位置越向右对应的氢键受体能力越强,σ峰值越大、峰的位置越向左对应的氢键给体能力越强,σ在-0.008~0.008 e·Å-2(1 Å=0.1 nm)范围内表现为非极性[24-27]。从图6中可见离子液体和乙醇在3个区域均具有较强的表面电荷分布,而环己烷的σ峰处于非极性区(-0.008<σ<0.008 e·Å-2)。因为环己烷的σ峰处于非极性区,所以环己烷与乙醇之间的共沸主要是由于它们分子间的非极性力作用。而离子液体[P2,4,4,4][Pr]与乙醇相同即可以作为氢键受体,又可以作为氢键给体形成氢键,当[P2,4,4,4][Pr]被加入环己烷-乙醇混合液时,[P2,4,4,4][Pr]与乙醇分子之间能够形成比非极性分子间作用更强的氢键,乙醇与[P2,4,4,4][Pr]形成结合力更强的氢键会导致乙醇与环己烷之间较弱的非极性作用力被打破。因此,当加入环己烷-乙醇混合物中的[P2,4,4,4][Pr]的量达到一定值时,环己烷-乙醇混合物的共沸将会被打破。
3 结论
在101.3 kPa下测定了环己烷+乙醇+ILs三元体系的汽液相平衡数据,采用NRTL模型对实验数据进行了拟合,得到了方程参数。基于NRTL方程计算得到了[P2,4,4,4][Pr]打破环己烷-乙醇体系共沸的最小物质的量分数为0.046,该值低于文献报道的数值0.10。当离子液体在物质的量分数分别为0.05和0.08时,平均相对挥发度![]() 值分别为1.77和2.29,共沸体系均可实现清晰分离。利用Aspen Plus V11软件对萃取精馏过程进行了模拟和过程参数优化,确定了适宜的理论塔板数、进料位置和回流比,分别为13、6和0.5。基于σ谱图对离子液体[P2,4,4,4][Pr]的分离机理进行了分析,发现[P2,4,4,4][Pr]能够打破环己烷-乙醇体系的共沸主要是由于[P2,4,4,4][Pr]和乙醇具有更强的生成氢键能力。
值分别为1.77和2.29,共沸体系均可实现清晰分离。利用Aspen Plus V11软件对萃取精馏过程进行了模拟和过程参数优化,确定了适宜的理论塔板数、进料位置和回流比,分别为13、6和0.5。基于σ谱图对离子液体[P2,4,4,4][Pr]的分离机理进行了分析,发现[P2,4,4,4][Pr]能够打破环己烷-乙醇体系的共沸主要是由于[P2,4,4,4][Pr]和乙醇具有更强的生成氢键能力。
[1] GHIMBEU C M, GADIOU R, DENTZER J, et al. A TPD-MS study of the adsorption of ethanol/cyclohexane mixture on activated carbons[J]. Adsorption, 2011, 17(1): 227-233
[2] MISRA R, BHATTACHARYYA S P, MANDAL A. Spectral response of 4-methyl-2, 6-dicarbomethoxyphenol, an excited-state intramolecular proton-transfer probe in cyclohexane-ethanol mixtures: Signatures of medium microheterogeneity[J]. The Journal of Physical Chemistry B, 2011, 115(41): 11840-11851
[3] AYUSO M, NAVARRO P, PALMA A M, et al. Separation of benzene from methylcycloalkanes by extractive distillation with cyano-based ionic liquids: Experimental and CPA EoS modelling[J]. Separation and Purification Technology, 2020, 234: 116128
[4] YANG J, PAN X, YU M, et al. Vapor-liquid equilibrium for binary and ternary systems of tetrahydrofuran, ethyl acetate and N-methyl pyrrolidone at pressure 101.3 kPa[J]. Journal of Molecular Liquids, 2018, 268: 19-25
[5] AKINLUA A, JOCHMANN M A, SCHMIDT T C. Ionic liquid as green solvent for leaching of polycyclic aromatic hydrocarbons from petroleum source rock[J]. Industrial & Engineering Chemistry Research, 2015, 54(51): 12960-12965
[6] ZHANG Y, SU Z, XUE K, et al. Efficient separation of methyl tert-butyl ether using ionic liquids from computational thermodynamics to process intensification[J]. Industrial & Engineering Chemistry Research, 2022, 61(48): 17631-17643
[7] BRODERICK E M, SERBAN M, MEZZA B, et al. Scientific approach for a cleaner environment using ionic liquids[J]. ACS Sustainable Chemistry & Engineering, 2017, 5(5): 3681-3684
[8] 王孝科, 田敉. 离子液体萃取精馏分离乙醇-环己烷共沸物[J]. 过程工程学报, 2009, 9(2): 269-273
WANG Xiaoke, TIAN Mi. Extractive distillation of ethanol-cyclohexane azeotrope using ionic liquid as extractant[J]. The Chinese Journal of Process Engineering, 2009, 9(2): 269-273(in Chinese)
[9] 丁忠瀚, 李文秀, 张羽, 等. 萃取精馏分离环己烷-乙醇共沸体系的模拟[J]. 沈阳化工大学学报, 2021, 35(4): 304-308
DING Zhonghan, LI Wenxiu, ZHANG Yu, et al. Simulation of cyclohexane-ethanol azeotrope separation by extractive distillation[J]. Journal of Shenyang University of Chemical Technology, 2021, 35(4): 304-308(in Chinese)
[10] LI W, ZHANG Y, LI H, et al. Measurement and correlation of the vapor-liquid equilibrium of cyclohexane + ethanol containing ILs and the thermophysical properties of these ILs at 101.3 kPa[J]. The Journal of Chemical Thermodynamics, 2020, 150: 106203
[11] 李焕新, 刘笑琛, 王岳昕, 等. 分离环己烷-乙醇的离子液体萃取剂的筛选[J]. 化学研究与应用, 2023, 35(4): 779-784
LI Huanxin, LIU Xiaochen, WANG Yuexin, et al. Screening of ionic liquid extractant for separation of cyclohexane-ethanol[J]. Chemical Research and Application, 2023, 35(4): 779-784(in Chinese)
[12] KLAMT A, JONAS V, BÜRGER T, et al. Refinement and parametrization of COSMO-RS[J]. Journal of Physical Chemistry A,1998, 102(26): 5074-5085
[13] KLAMT A. Conductor-like screening model for real solvents: A new approach to the quantitative calculation of solvation phenomena[J]. The Journal of Physical Chemistry, 1995, 99(7): 2224-2235
[14] KLAMT A. The COSMO and COSMO-RS solvation models[J].Wiley Interdisciplinary Reviews: Computational Molecular Science, 2018, 8(1): e1338
[15] LI J, YANG X, CHEN K X, et al. Sifting ionic liquids as additives for separation of acetonitrile and water azeotropic mixture u-sing the COSMO-RS method[J]. Industrial & Engineering Chemistry Research, 2012, 51(27): 9376-9385
[16] 刘潜, 张香兰, 李巍. 基于COSMO-RS模型的分离油酚混合物的离子液体萃取剂筛选[J]. 化工学报, 2018, 69(12): 5100-5111
LIU Qian, ZHANG Xianglan, LI Wei. Screening ionic liquids solvent for separation of oil and hydroxybenzene mixtures based on COSMO-RS model[J]. CIESC Journal, 2018, 69(12): 5100-5111(in Chinese)
[17] BANERJEE T, SINGH M K, KHANNA A. Prediction of binary VLE for imidazolium based ionic liquid systems using COSMO-RS[J]. Industrial & Engineering Chemistry Research, 2006, 45(9): 3207-3219
[18] RENON H, PRAUSNITZ J M. Local compositions in thermodynamic excess functions for liquid mixtures[J]. AIChE Journal,1968, 14(1): 135-144
[19] 李文秀, 王丽达, 温情, 等. 含离子液体苯-正丙醇物系等压气液相平衡[J]. 化学工程, 2020, 48(10): 58-62
LI Wenxiu, WANG Lida, WEN Qing, et al. Isobaric vapor-liquid equilibrium for benzene-n-propanol-1-octyl-3-methyl imidazolium acetate ternary system[J]. Chemical Engineering (China),2020, 48(10): 58-62(in Chinese)
[20] 李宏辉, 李文秀, 张志刚, 等. 离子液体-环己烷(乙醇)二元体系气液相平衡研究[J]. 沈阳化工大学学报, 2020, 34(3): 198-204, 254
LI Honghui, LI Wenxiu, ZHANG Zhigang, et al. Vapor-liquid equilibrium of ionic liquids with cyclohexane or ethanol binary system[J]. Journal of Shenyang University of Chemical Technology, 2020, 34(3): 198-204, 254(in Chinese)
[21] KLAMT A, ECKERT F. Prediction of vapor liquid equilibria u-sing COSMOtherm[J]. Fluid Phase Equilibria, 2004, 217(1):53-57
[22] LI Y, BAI P, ZHUANG Q. Isobaric vapor-liquid equilibrium for binary system of methanol and acetonitrile[J]. Fluid Phase Equilibria, 2013, 340: 42-45
[23] VALDERRAMA J O, SANGA W W, LAZZÚS J A. Critical properties, normal boiling temperature, and acentric factor of another 200 ionic liquids[J]. Industrial & Engineering Chemistry Research, 2008, 47(4): 1318-1330
[24] VERDÍA P, GONZÁLEZ E J, MORENO D, et al. Deepening of the role of cation substituents on the extractive ability of pyridinium ionic liquids of N-compounds from fuels[J]. ACS Sustainable Chemistry & Engineering, 2017, 5(2): 2015-2025
[25] ISLAM M R, CHEN C. COSMO-SAC sigma profile generation with conceptual segment concept[J]. Industrial & Engineering Chemistry Research, 2015, 54(16): 4441-4454
[26] RUIZ E, FERRO V R, PALOMAR J, et al. Interactions of ionic liquids and acetone: Thermodynamic properties, quantum-chemical calculations, and NMR analysis[J]. The Journal of Physical Chemistry B, 2013, 117(24): 7388-7398
[27] 李文秀, 张利月, 李继鹏, 等. 离子液体分离能力与其分子结构间的构效关系研究[J]. 沈阳化工大学学报, 2017, 31(4): 289-294
LI Wenxiu, ZHANG Liyue, LI Jipeng, et al. Study on the structure activity relationship of ionic liquid separation ability and its molecular structure[J]. Journal of Shenyang University of Chemical Technology, 2017, 31(4): 289-294(in Chinese)