锂(Li)作为当今最具战略意义的能源金属,被广泛应用于润滑脂、光学元件和锂电池等领域[1]。随着节能减排政策的持续推进,锂资源成为新能源工业的核心材料。仅2023年全球电动汽车的销售量就突破了1 400万辆,较2022年增长了35%,这一发展趋势直接驱动锂资源的需求激增[2]。其作为电池的核心材料,仅锂元素成本就占正极材料成本的40%以上。磷酸铁锂和三元锂2大技术路线每年对锂资源的需求超过了80万t[3]。值得注意的是,全球锂矿资源主要分布在智利、阿根廷和玻利维亚3国,呈现密集型分布的特点,这就导致身为全球最大锂电生产和消费市场的中国受到了前所未有的挑战[4]。而我国锂资源主要存在于盐湖中,占总储量的85%,这就凸显了盐湖提锂技术的不断优化的重要性[5]。
盐湖提锂传统方法主要包括液-液萃取、电渗析以及化学沉淀等,存在回收率低、环境污染大和能耗过高等问题[6-8]。近些年,随着科学研究的不断进步,基于离子交换机制的锂离子筛(Lithium Ion Sieve,简称 LIS)得到了广泛的关注。LIS技术具备毒性小、化学稳定性高、吸附容量大和成本低廉等明显优势,被认为是盐湖提锂最具潜力的技术[9-12]。LIS主要涉及锰基LIS以及钛基LIS这2类材料,其中锰基LIS虽然具备高的选择性,但是LIS结构中的锰元素在酸性溶液中会发生严重的歧化反应,导致锰溶解损失,使其重复利用价值下降[13]。相反,钛基LIS因其由稳定的Ti-O骨架结构组成,在酸性介质中展现出优异的耐酸性和化学稳定性。因此,研究人员聚焦于优化钛基LIS的提锂技术,例如Qin等[14]利用十二烷基硫酸钠的刻蚀作用,改变LIS对溶液的亲和性,显著改善了其吸附性能;Jin等[15]通过非金属元素W掺杂的策略,修饰LIS的层间结构,进一步降低了钛溶损;Zhang等[16]通过金属元素Cu的引入扩展了LIS的Li+传输通道,增加了对Li+吸附速率。就目前而言,现有研究大多围绕H2TiO3体系展开,而对于H2Ti3O7材料的研究,仍处于空白状态。
本研究创新性采用低温水热合成技术(40~160 ℃,调控H2Ti3O7型钛基LIS微观结构和形貌)。Li+吸附实验表明,80 ℃合成的LIS HTO80在pH值为6.5条件下对Li+吸附容量为14.1 mg·g-1。并且采用XRD、BET、TEM、XPS和吸附动力学模型表征了LIS的晶体结构、比表面积、微观形貌和Li+吸附机制。本研究丰富了钛基LIS材料体系,也为高效盐湖提锂技术开发提供了新思路。
1 实验部分
1.1 原料
实验所用试剂如下:二氧化钛[P25(TiO2),德国德固赛公司];氢氧化钠(NaOH,AR,沪试);盐酸(HCl,AR,沪试);氯化锂(LiCl,无水级,质量分数为98%,阿拉丁试剂有限公司);无水乙醇(C2H5OH,AR,沪试)。
1.2 锂离子筛制备过程
采用传统水热法制备LIS前驱体Na2Ti3O7,首先配制10 mol·L-1的NaOH溶液,将16 g的片状NaOH加入含有40 mL去离子水烧杯中,搅拌1 h,直至溶液温度降至室温,将其命名为A溶液。然后称取1.0 g的P25分多次少量加入A溶液中,搅拌2 h保证其分散均匀。将其转入水热合成反应釜中,并放入鼓风烘箱,在一定温度(40~160 ℃)下反应48 h。最后将得到的白色固体用大量的去离子水洗涤数次,直到溶液pH值介于7~8之间,然后将其放入真空烘箱中过夜,即得到干燥的Na2Ti3O7(用NTOx表示,其中x代表水热温度)。
将前驱体NTOx分散到0.5 mol·L-1的HCl溶液中,搅拌2 h,为保证Na+和H+充分置换,将该步骤重复3次。最后利用大量的去离子水洗涤数次,直到溶液pH值介于7~8之间,将其放入真空烘箱中过夜,即得到锂离子筛H2Ti3O7(用HTOx表示,其中x代表水热温度)。
1.3 锂离子筛的表征
采用DX-2007B 型X射线衍射仪进行XRD表征,并使用Jade.9软件分析晶体结构,与粉末衍射标准联合委员会衍射图谱对比进行物相鉴别;采用日本电子株式会社生产的JEM-2100透射电子显微镜(TEM)对样品形貌结构进行了分析;采用美国康塔仪器公司Quantachrome Autosorb iQ物理吸附仪分析了样品的比表面积(BET)和孔结构;采用美国赛默飞世尔科技公司生产的K-ALPHA型X射线电子能谱仪(XPS)分析样品的电子化学状态;采用中国生产的电感耦合等离子体发射光谱仪(ICP-OES)分析了溶液中离子浓度。
1.4 锂离子筛吸附能力评价
称取HTOx 100 mg于离心管中,然后将配制好浓度的LiCl溶液10 mL加入到其中,将离心管放置于旋转混匀仪上,在室温下旋转吸附24 h,离心后取上层清液并用0.22 μm PVDF膜进行过滤。将获得的含Li+溶液用ICP-OES测定其浓度,并根据式(1)计算其平衡吸附容量。
式(1)中:ρ0代表Li+的初始浓度值,mg·L-1;ρe代表吸附后溶液中离子的平衡浓度值,mg·L-1;V代表吸附实验中溶液的体积,L;m代表吸附实验中LIS的质量,g;Qe代表LIS在溶液中对目标离子的平衡吸附容量,mg·g-1。
1.5 吸附等温线模型
1.5.1 Langmuir吸附等温线模型
Langmuir方程可表述为线性化形式,可以通过式(2)的斜率和截距计算Qm和kL参数[17]。
式(2)中:ρe代表吸附平衡时Li+浓度值,mg·L-1;Qe代表LIS对Li+的平衡吸附容量,mg·g-1;Qm代表LIS对Li+的最大吸附容量,mg·g-1;kL代表该模型的平衡吸附常数,L·mg-1。
1.5.2 Freundlich吸附等温线模型
Freundlich吸附等温线作为异质表面吸附体系的经典描述模型,在固-液界面吸附研究中具有广泛适用性。通过引入吸附强度参数(n)与吸附常数(kF),成功实现了对非均质表面多层吸附行为的数学表征[17]:
式(3)中:ρe代表吸附平衡时Li+浓度值,mg·L-1;Qe代表LIS对Li+的平衡吸附容量,mg·g-1;n和kF为Freundlich常数。
1.6 动力学模型
1.6.1 准一阶动力学模型
准一阶动力学模型本质上描述的是扩散主导型吸附过程,方程如式(4)[17]:
式(4)中:Qe代表LIS对Li+的平衡吸附容量,mg·g-1;Qt 代表某一时刻t,LIS对Li+的吸附容量,mg·g-1;K1是准一阶动力学模型的吸附速率常数,h-1。通过对时间t和吸附容量Qt进行拟合可以计算得出K1和Qe的值。
1.6.2 准二阶动力学模型
准二阶动力学模型基于表面化学吸附控制假设,其核心认为吸附速率由吸附质与吸附剂表面活性位点形成化学键过程主导,其方程如式(5)[17]:
式(5)中:K2是准二阶动力学模型的吸附速率常数,g·mg-1·h-1。通过对时间t和吸附量Qt进行拟合可以计算得出K2和Qe的值。
2 结果与讨论
2.1 锂离子筛的结构与形貌分析
通过XRD对水热法合成的LIS前驱体系列样品进行表征,结果如图1(a)所示。原料P25展现出锐钛矿和金红石混合相衍射峰,符合商业P25的特征且未检测出其他杂峰,表明原料纯度较高。当水热温度升至40 ℃时(NTO40),其XRD图谱仍然保留P25的特征峰,各峰强度显著降低,但未出现新相的衍射信号。说明40 ℃时,碱性条件下可部分破坏TiO2的表面晶格,导致其结晶度下降。但是,该温度下难以形成足够的[TiO6]八面体组成NTOx。当温度提升至80 ℃及以上时(NTO80~NTO160),所有样品在10.0°、24.5°、28.5°和48.5°出现强衍射峰,分别属于单斜晶系NTOx(PDF 31—1329)的(001)、(201)、(111)和(020)晶面,与文献报道的NTOx标准谱高度吻合[18]。这些结果表明当水热温度≥80℃时,P25在强碱环境中解离成众多[TiO6]八面体,随后通过共享棱和顶点的方式重组形成NTOx。
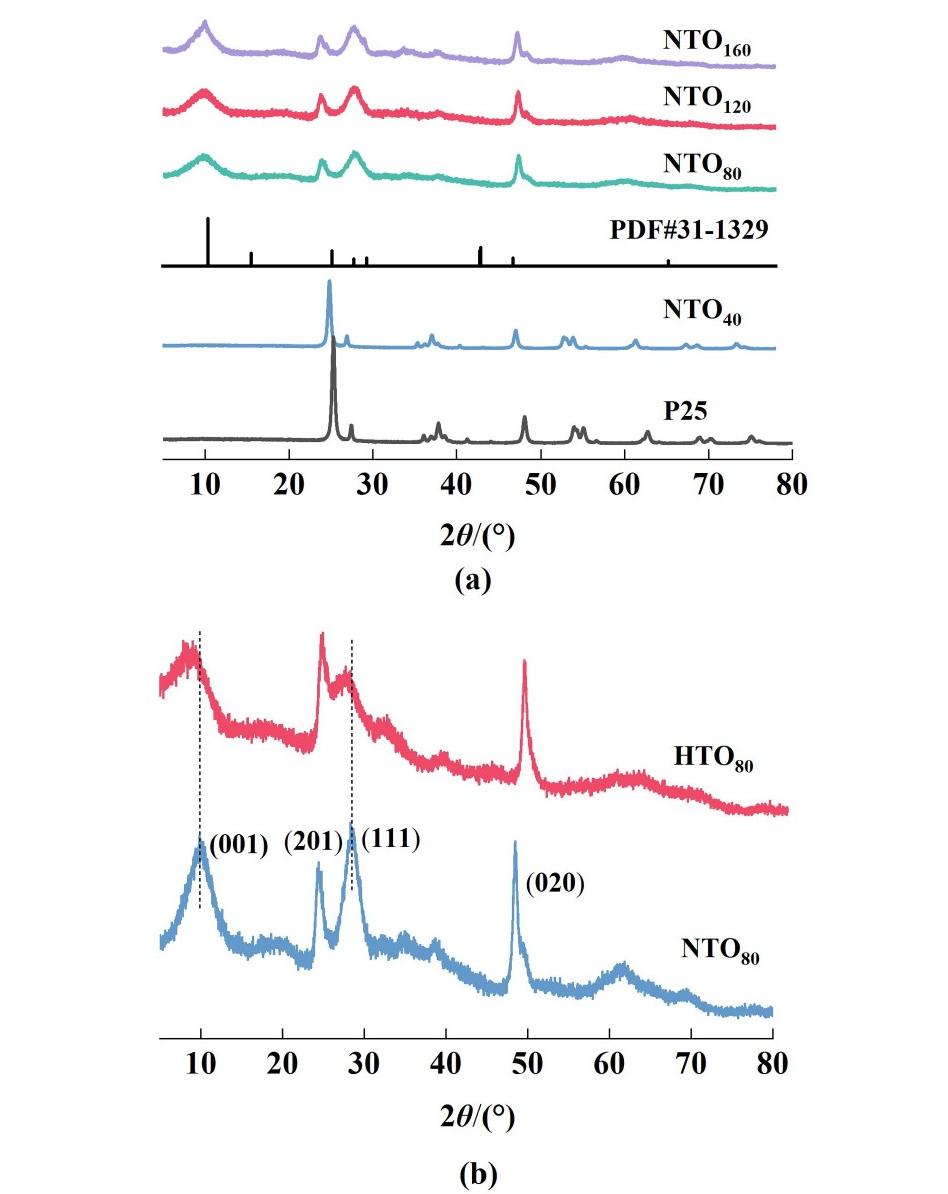
图1 (a)P25、NTO40、NTO80、NTO120和NTO160的XRD图谱;(b)NTO80和HTO80的XRD图谱
Fig.1 (a) XRD patterns of P25, NTO40, NTO80, NTO120,and NTO160; (b) XRD patterns of NTO80 and HTO80
LIS前驱体NTO80中的Na+和H+完全交换后形成LIS HTO80,由图1(b)所示,相比于NTO80的特征峰图谱,HTO80的(001)和(111)晶面所对应的特征峰向低角度略微偏移,由布拉格方程2dsinθ=nλ可知,当nλ不变时,角度减小将会导致层间距d变大,可归因于H+进入层间占据原来Na+的位置,H+和上下层间的静电作用力小于Na+,从而对上下2层的束缚力减小,导致层间距变大。此外,HTO80特征峰强度整体变弱,这是因为H+的对X射线的散射能力远低于Na+,导致层间离子相关衍射峰强度减弱[19]。
通过TEM对前驱体NTOx的形貌演变进行观察。原料P25以直径28.3 nm的颗粒形式存在[图2(a)],经过40 ℃的碱性水热(NTO40),OH-对P25晶格引发强烈的刻蚀,引发表面重构,使颗粒直径增至约32.3 nm[图2(b)]。NTO40依然维持P25的基本颗粒形貌,表明该温度下并未发生结构性转变,这与XRD结果一致。温度提升至80 ℃(NTO80)时,形貌发生了显著的改变,结合XRD结果分析,此时已经彻底转变为钛酸盐相,并呈现出宽阔二维纳米带状形貌。而NTO120和NTO160则发生卷曲折叠形成纳米管状形貌,并且从120 ℃时的直径8.8 nm增大至160 ℃时的10.3 nm,这是由于高温化学驱动力增强,促使管壁结构趋于致密化。此外,前驱体NTO80经过质子化处理转变为HTO80,其依然保持轻薄的纳米带状结构,没有发生显著的形貌变化,仅仅表面粗糙度略有增加。

图2 (a) P25,(b)NTO40,(c)NTO80,(d)NTO120,(e)NTO160和(f)HTO80的TEM图
Fig.2 TEM images of (a) P25, (b) NTO40, (c) NTO80, (d) NTO120, (e) NTO160, and (f) HTO80
众所周知,比表面积决定着LIS表面可及活性位点数目,进而影响LIS对Li+的吸附性能[20]。为此,将不同温度合成的前驱体NTOx经过酸处理形成HTOx,并通过N2吸附-脱附测试其比表面积和孔径分布。如图3(a)所示,所有LIS样品均展现出典型的Ⅳ型等温线特征,并且在相对压力p/p0=0.7~1.0的范围内,存在明显的H4型回滞环,这证实了材料内部主要以介孔结构为主[21]。
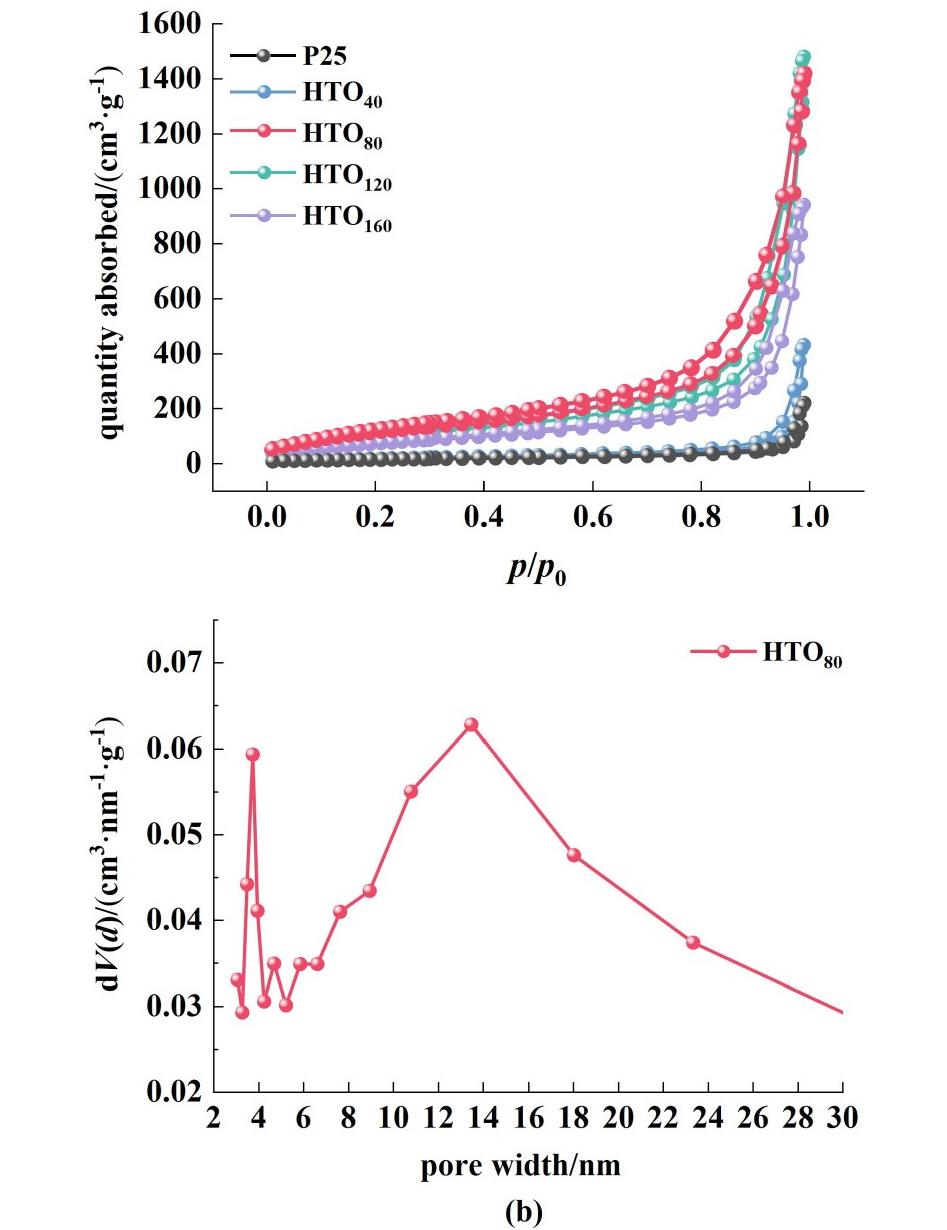
图3 (a)P25、HTO40、HTO80、HTO120和HTO160的N2吸附-解吸等温线;(b)HTO80的孔径分布
Fig.3 (a) N2 adsorption-desorption isotherms of P25,HTO40, HTO80, HTO120, and HTO160; (b) Pore size distribution of HTO80
进一步分析HTO80的孔径分布曲线,如图3(b)所示,位于2~3 nm处的假峰由仪器的毛细作用所造成。而6~30 nm范围内的峰归因于HTO80纳米带部分发生卷曲折叠形成中空管状结构所致。并且由表1的BET数据可知,HTO80比表面积高达422.0 m2·g-1,显著高于其他温度处理的样品。这种高比表面积可归因于80 ℃条件下化学驱动力不足,难以将HTO80纳米带完全卷曲折叠成管状结构,二维展开片层暴露大量表面,从而显著提高比表面积,这将有利于为Li+吸附提供更多表面可交换活性位点。
表1 P25、HTO40、HTO80、HTO120和HTO160的表面积参数
Table 1 Specific surface area parameters of P25, HTO40, HTO80, HTO120, and HTO160

samplesBET/(m2·g-1)P2550.4 HTO4078.0 HTO80422.0 HTO120381.3 HTO160281.1
2.2 锂离子筛的Li+吸附性能
探究了不同水热温度下制备的LIS与Li+吸附量之间的变化关系,结果如图4(a)所示。原材料P25由于缺乏LIS的离子交换能力,仅表现出0.35 mg·g-1的吸附量。水热温度40~60 ℃制备的HTO40和HTO60对Li+的吸附量分别增加至1.89和5.90 mg·g-1,归因于该温度下还未完全生成具备离子交换能力的钛酸盐相。值得注意的是,HTO80展现出显著的吸附性能跃升(14.1 mg·g-1),与P25相比,LIS HTO80对Li+的吸附能力提升40倍以上,这主要归因于HTO80纳米带形貌提供高比表面积,使其离子交换活性位点以最大程度暴露,增强了对Li+的捕获速率和能力。但是,水热温度进一步增加,高温导致HTO80纳米带发生卷曲和剥离形成管状结构,活性位点利用率被降低,致使吸附能力下降。这一现象也验证了LIS的晶体结构和微观形貌对Li+吸附性能的影响和关联性。如图4(b)所示,LIS的加入量和吸附液体积之间存在明显关系,随着固液比增大,LIS之间由于范德华力的存在会发生一定程度的团聚,吸附位点利用率下降,使得固液比和吸附性能之间呈现负相关[27]。此外,LIS对Li+的吸附量还受pH值的影响,如图4(c)所示,pH值和吸附量间存在正相关线性关系,其机理源于H+/Li+交换反应:![]() ,酸性条件下不利于反应正向进行,从而抑制了对Li+的吸附,碱性条件则相反。
,酸性条件下不利于反应正向进行,从而抑制了对Li+的吸附,碱性条件则相反。
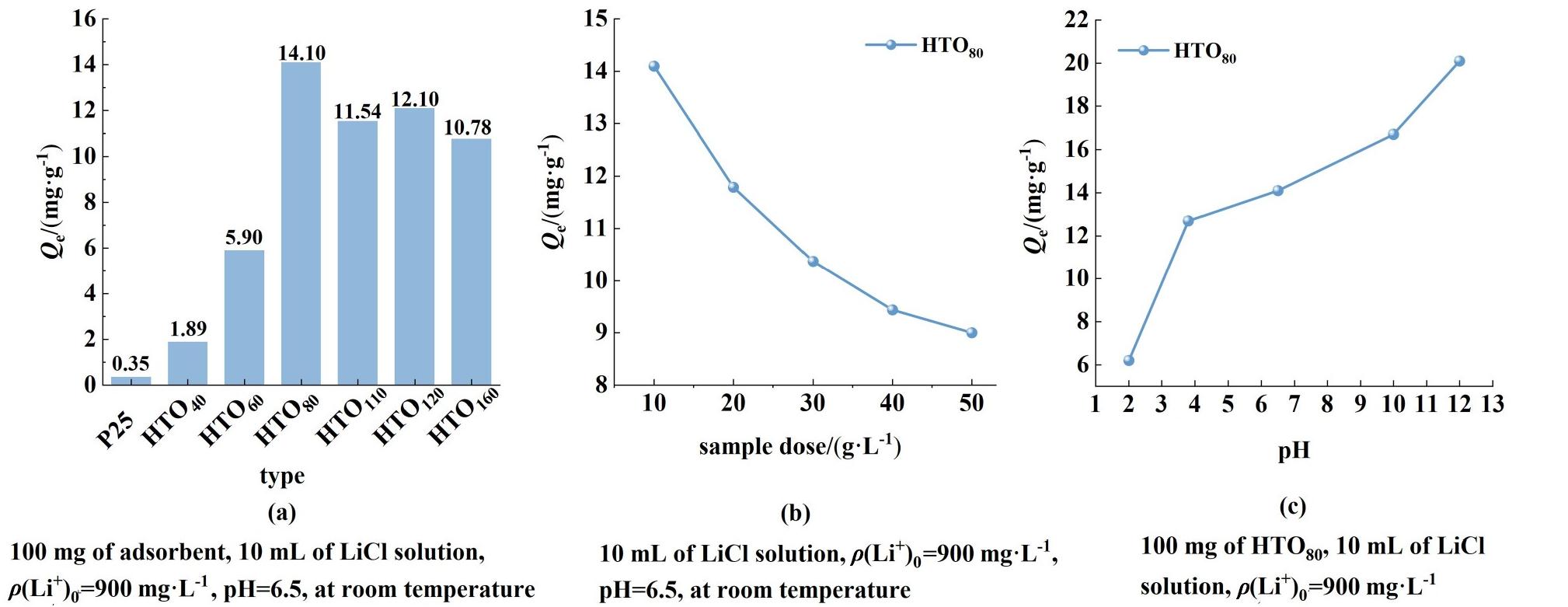
图4 (a)P25、HTO40、HTO60、HTO80、HTO10、HTO120和HTO160的对Li+的平衡吸附容量(室温);(b)HTO80在不同固液比下的平衡吸附容量(室温);(c)HTO80在不同pH值下的平衡吸附容量(室温)
Fig.4 (a) Equilibrium adsorption capacities of P25, HTO40, HTO60, HTO80, HTO100, HTO120, and HTO160 for Li+ ions; (b) Equilibrium adsorption capacities of HTO80 at different solid-liquid ratios;(c) Equilibrium adsorption capacities of HTO80 at different pH values
此外,本研究制备的LIS HTO80吸附容量和吸附条件与近年来H2TiO3型LIS的数据进行对比,列于表2。显然利用低温水热策略合成的HTO80具备显著的快速吸附动力学优势,可以在极短时间内(0.17 h)完成对Li+的摄取。在pH=6.5、固液比为10的温和条件下,反应0.17 h可有效吸附Li+(13.2 mg·g-1),有望在中性甚至弱酸性卤水中实现对Li+的摄取。值得注意的是,当我们把吸附条件改变为与其他工作吸附条件相近时(pH=12、固液比为2),其对Li+的吸附容量骤升至37.6 mg·g-1,这一结果表明所制备的HTO80型LIS具备出色Li+吸附容量。
表2 其他文献中H2TiO3与本研究H2Ti3O7型LIS吸附性能参数对比
Table 2 Comparison of adsorption performance parameters between H2TiO3in other literatures and H2Ti3O7-type LIS in this work
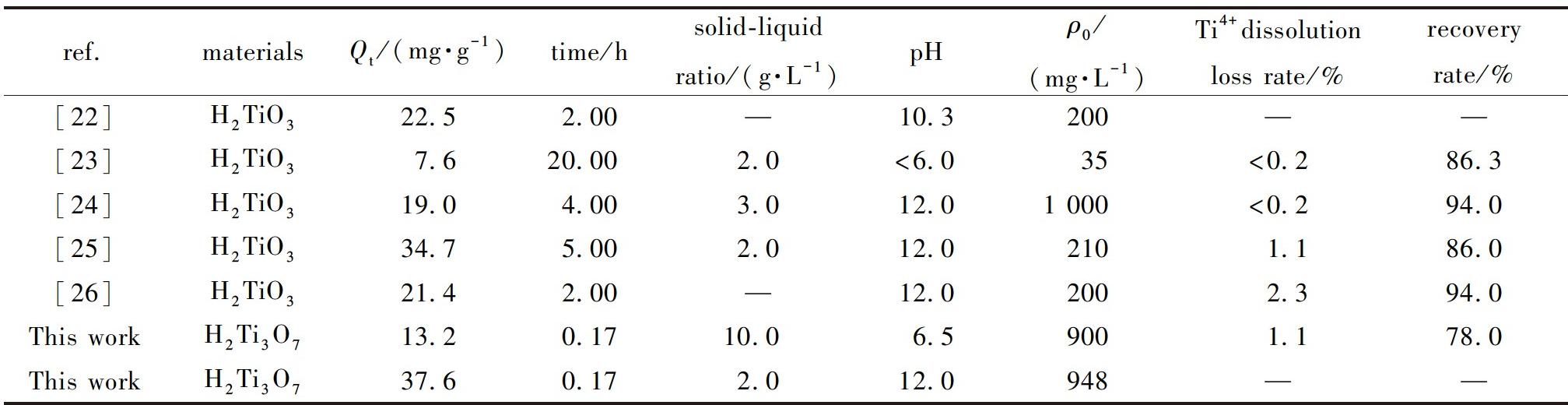
注:“—”为无数据。
ref.materialsQt/(mg·g-1)time/hsolid-liquid ρ0/Ti 4+dissolution recovery ratio/(g·L-1)pH(mg·L-1)loss rate/%rate/%[22]H2TiO322.52.00—10.3200——[23]H2TiO37.620.002.0<6.035<0.286.3[24]H2TiO319.04.003.012.01 000<0.294.0[25]H2TiO334.75.002.012.02101.186.0[26]H2TiO321.42.00—12.02002.394.0 This workH2Ti3O713.20.1710.06.59001.178.0 This workH2Ti3O737.60.172.012.0948——
2.3 锂离子筛的Li+吸附动力学
通过对HTO80进行吸附动力学和等温线拟合,进一步探究其Li+离子的吸附行为。如图5(a)所示,展示了HTO80对Li+吸附量和吸附时间的关系。可以看出该LIS的一个显著特点是其快速吸附动力学,在最初10 min对Li+的吸附量迅速增加达到13.20 mg·g-1。利用准一阶和准二阶动力学模型对吸附数据进行拟合,如图5(b)和图5(c)所示,相关动力学拟合参数总结在表3中。与准一阶动力学模型相比,HTO80的吸附行为更符合准二阶动力学模型,拟合精度![]() 。此外,该吸附条件计算得到的Li+离子理论吸附容量(Qcal=13.28 mg·g-1)与实验值(Qexp=13.32 mg·g-1)更为一致。这充分证实了HTO80对Li+离子的吸附过程由化学吸附机制控制,也就是Li+离子通过形成化学键的方式与HTO80结合[28]。此外,如图5(d)所示,HTO80的吸附量,随Li+离子初始浓度增加而增加,当Li+达到一定浓度时,吸附容量增速变得缓慢。该现象归因于Li+浓度增加,化学驱动力变大,从而促进对Li+的吸附。但是,HTO80的活性位点数目有限,Li+浓度过高时,其吸附量增加变得缓慢。使用朗缪尔(Langmuir)和弗伦德里希(Freundlich)等温模型对吸附平衡等温线进行拟合,如图5(e)和图5(f)所示,相关拟合参数总结在表4中。可以看出吸附平衡数据和Langmuir模型拟合效果更优
。此外,该吸附条件计算得到的Li+离子理论吸附容量(Qcal=13.28 mg·g-1)与实验值(Qexp=13.32 mg·g-1)更为一致。这充分证实了HTO80对Li+离子的吸附过程由化学吸附机制控制,也就是Li+离子通过形成化学键的方式与HTO80结合[28]。此外,如图5(d)所示,HTO80的吸附量,随Li+离子初始浓度增加而增加,当Li+达到一定浓度时,吸附容量增速变得缓慢。该现象归因于Li+浓度增加,化学驱动力变大,从而促进对Li+的吸附。但是,HTO80的活性位点数目有限,Li+浓度过高时,其吸附量增加变得缓慢。使用朗缪尔(Langmuir)和弗伦德里希(Freundlich)等温模型对吸附平衡等温线进行拟合,如图5(e)和图5(f)所示,相关拟合参数总结在表4中。可以看出吸附平衡数据和Langmuir模型拟合效果更优![]() 。这意味着所制备的HTO80对Li+的吸附主要由单层吸附为主导[29]。
。这意味着所制备的HTO80对Li+的吸附主要由单层吸附为主导[29]。
表3 HTO80的准一阶和准二阶动力学模型拟合参数
Table 3 Fitting parameters of pseudo-first-order and pseudo-second-order kinetic models for HTO80

Pseudo-first-orderPseudo-second-order QexpK1QcalR21K2QcalR2213.320.011.100.2830.2613.280.999
表4 HTO80的Langmuir和Freundlich模型拟合参数
Table 4 Fitting parameters of the Langmuir and Freundlich models for HTO80

QmLangmuirFreundlich bR21kFnR2215.130.0190.9982.713.830.962
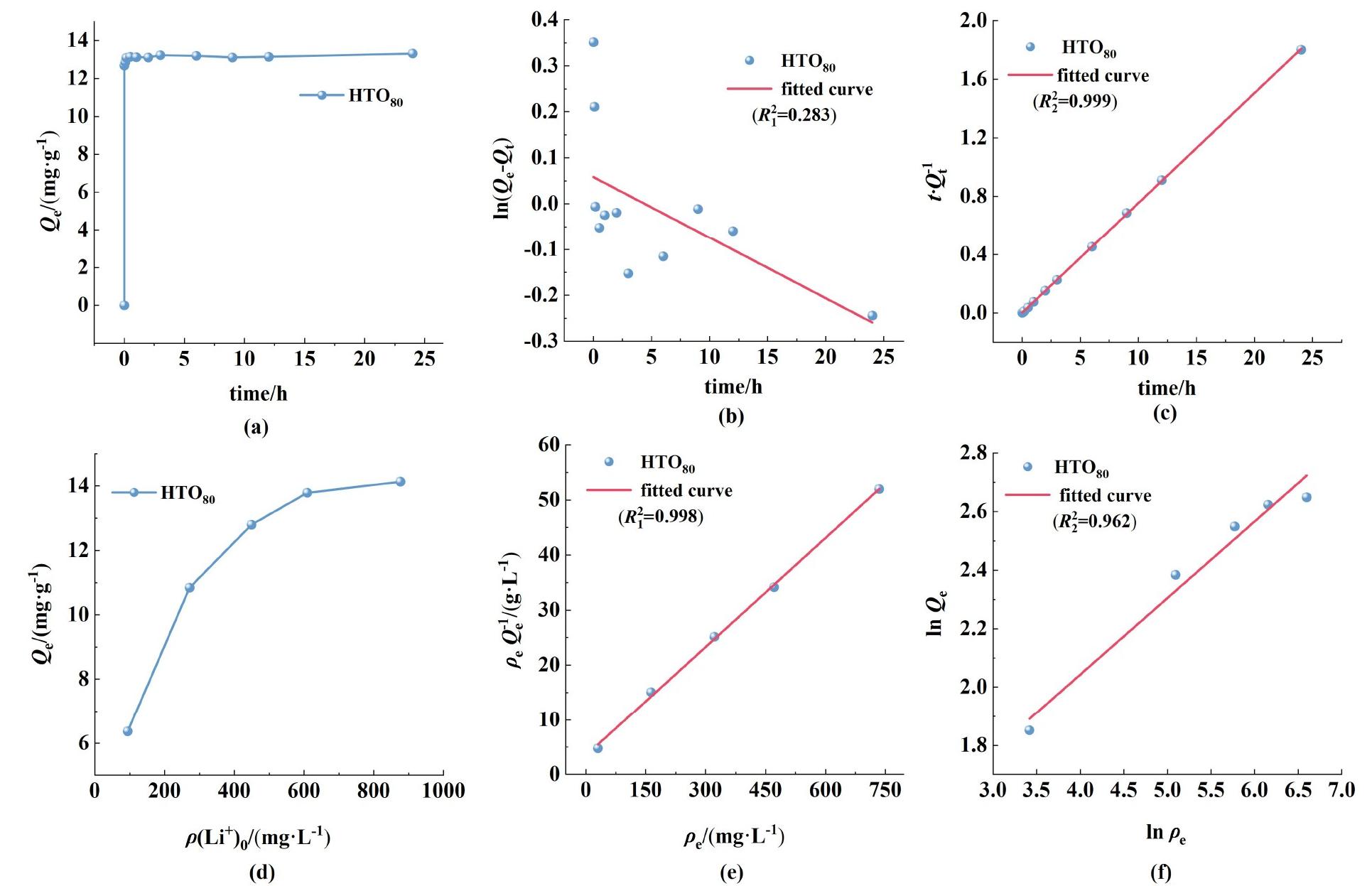
图5 (a)HTO80对Li+的吸附量随吸附时间的变化规律;Li+在HTO80上吸附的(b)准一阶动力学和(c)准二阶动力学图;(d)HTO80的Li+吸附等温线;HTO80的(e)Langmuir和(f)Freundlich模型拟合图
Fig.5 (a) The variation law of the adsorption amount of Li+ ions on HTO80 with the adsorption time; (b) Pseudo-firstorder kinetic and (c) pseudo-second-order kinetic diagrams of the adsorption of Li+ ions on HTO80; (d) The adsorption isotherm of Li+ ions on HTO80; (e) Fitting diagrams of the Langmuir and (f) Freundlich models for HTO80
2.4 锂离子筛的Li+吸附选择性和稳定性探究
由于卤水中存在许多与Li+共存的阳离子,主要有Na+、K+和Mg2+,这些竞争离子的存在会在一定程度上影响LIS的吸附选择性。如图6(a)所示,实验结果可以看出多种离子共存时,HTO80对Li+的吸附量(10.31 mg·g-1)远大于对其他离子的吸附量,这归因于空间位阻效应,使得其他离子难以扩散到晶体内部[30]。此外,材料的循环稳定性在实际应用过程中起重要作用,为了评估材料的稳定性,本研究对HTO80进行了5次吸附/解吸循环实验,如图6(b)所示,LIS HTO80经历5次循环后对Li+的吸附容量降至初始吸附容量的78%,吸附率的下降可能有2种原因:一是在酸洗过程中,发生Ti4+溶损(Ti4+的溶损率小于2.1%),导致HTO80的[TiO6]八面体骨架部分遭到破坏;二是循环过程中Li+未完全解吸,导致吸附位点减少。
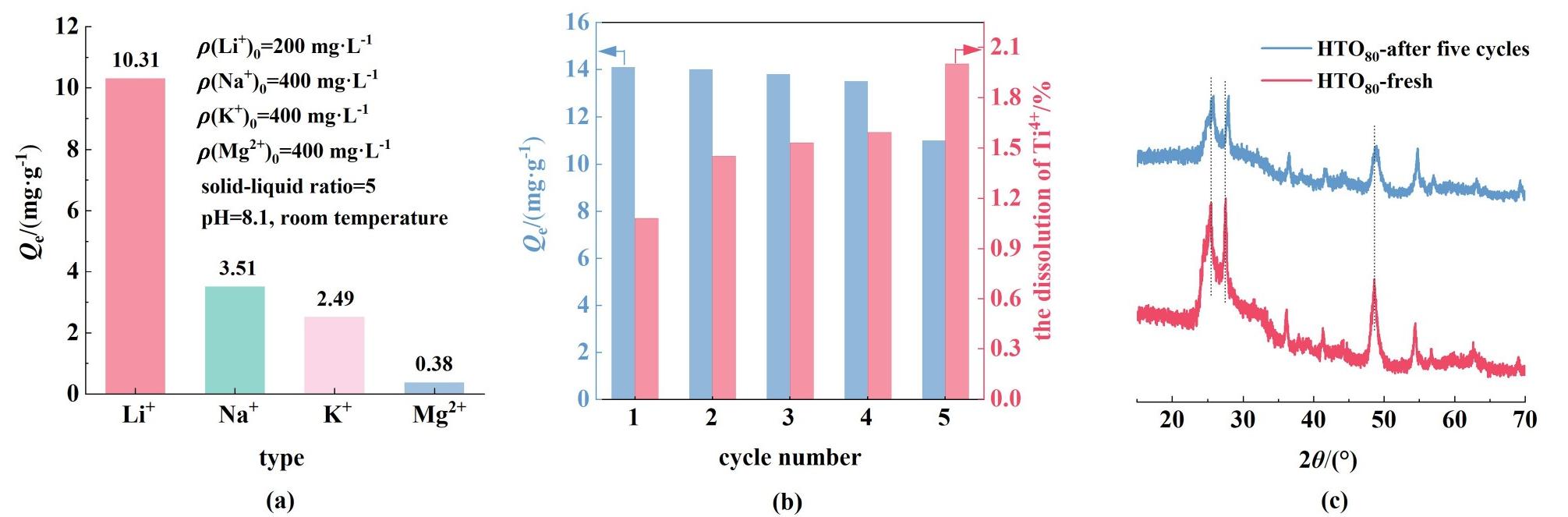
图6 (a)HTO80对不同阳离子的吸附容量(室温);(b)HTO80的循环稳定性以及Ti4+溶解情况;(c)循环反应前后HTO80的XRD
Fig.6 (a) Adsorption capacity of HTO80 for different cations; (b) Cycling stability of HTO80 and dissolution of Ti4+; (c) XRD patterns of HTO80 before and after cyclic reactions
值得注意的是,如图6(c)所示,与新鲜的LIS(HTO80-fresh)相比,循环后的LIS(HTO80-after five cycles)XRD特征峰发生整体右移0.15°,归因于离子交换反应的发生,不可避免地导致晶格收缩[31,32]。且没有发生明显的特征峰出现或消失,仅结晶度有所下降,表明LIS的基本骨架未被完全破坏,且没有杂相生成,只是晶格发现部分畸变,导致其晶体有序性下降[33]。因此,酸洗不会显著改变LIS的晶体结构,其仍然具备一定的循环稳定和回收性。
2.5 锂离子筛的Li+吸附机制
为了揭示LIS HTO80吸附Li+的机制,我们通过X射线电子能谱(XPS)对吸附Li+前后HTO80的电子化学状态进行表征。如图7(a)所示,在Li 1s精细谱中,可以清楚地观察到吸附Li+之前,HTO80样品中没有检测出Li元素的存在,而吸附Li+后,在55.25 eV处出现明显的Li 1s特征峰[34]。此外,通过图7(b)和图7(c) O 1s和Ti 2p的XPS谱图可以看出,HTO80吸附Li+之前O 1s和Ti 2p结合能分别为530.17和458.78 eV,吸附Li+之后O 1s和Ti 2p的特征峰出现在530.41和458.52eV。表明吸附Li+后,O 1s结合能增加0.24 eV,而Ti 2p轨道结合能则降低0.26 eV,这可归因于H—O—Ti键转变为Li—O—Ti键后化学环境发生变化[35-37]。这有力地证明HTO80吸附Li+的机制为H+和Li+之间发生离子交换反应,与动力学拟合结果一致。综上所述,本研究初步提出HTO80吸附Li+机制。
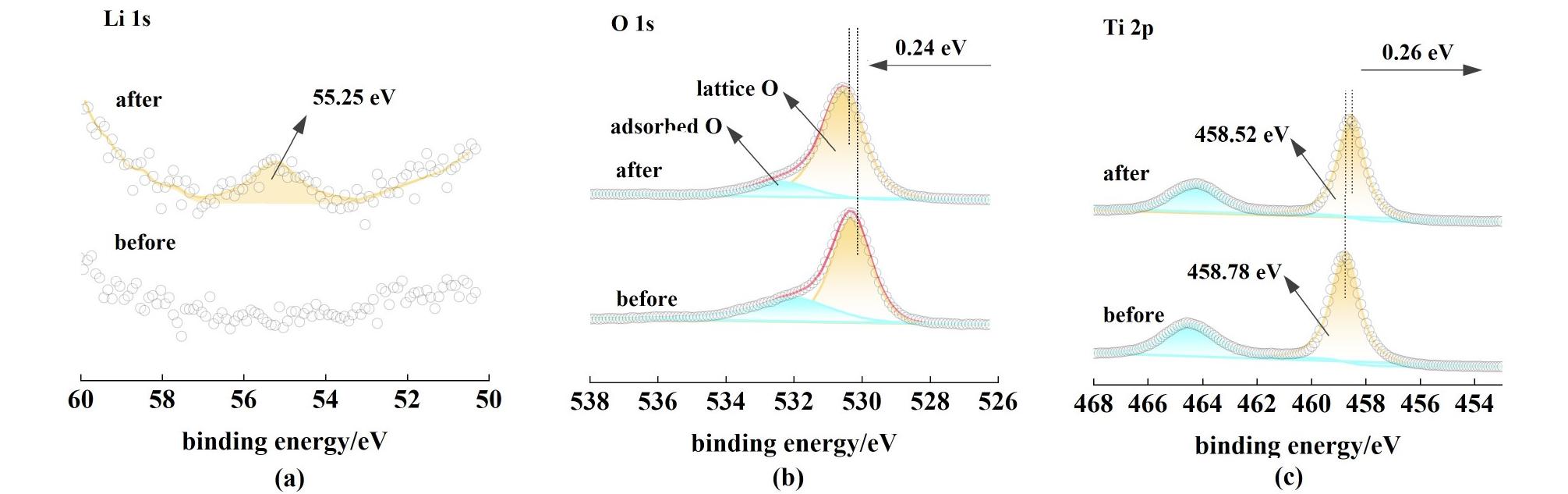
图7 HTO80吸附Li+前后(a)Li 1s;(b)O 1s和(c)Ti 2p的XPS谱图
Fig.7 XPS spectra of (a) Li 1s; (b) O 1s and (c) Ti 2p of HTO80 before and after the adsorption of Li+ ions
如图8所示,在Li+吸附阶段,HTO80与含Li+溶液接触,溶液中的Li+通过浓度梯度扩散至材料表面,在固-液界面处发生离子交换反应:H2Ti3O7+xLi+→LixH2-xTi3O7+xH+。脱附再生阶段,将吸附饱和的HTO80置于酸性环境时,高浓度的H+再次置换层间Li+,从而实现脱锂再生。
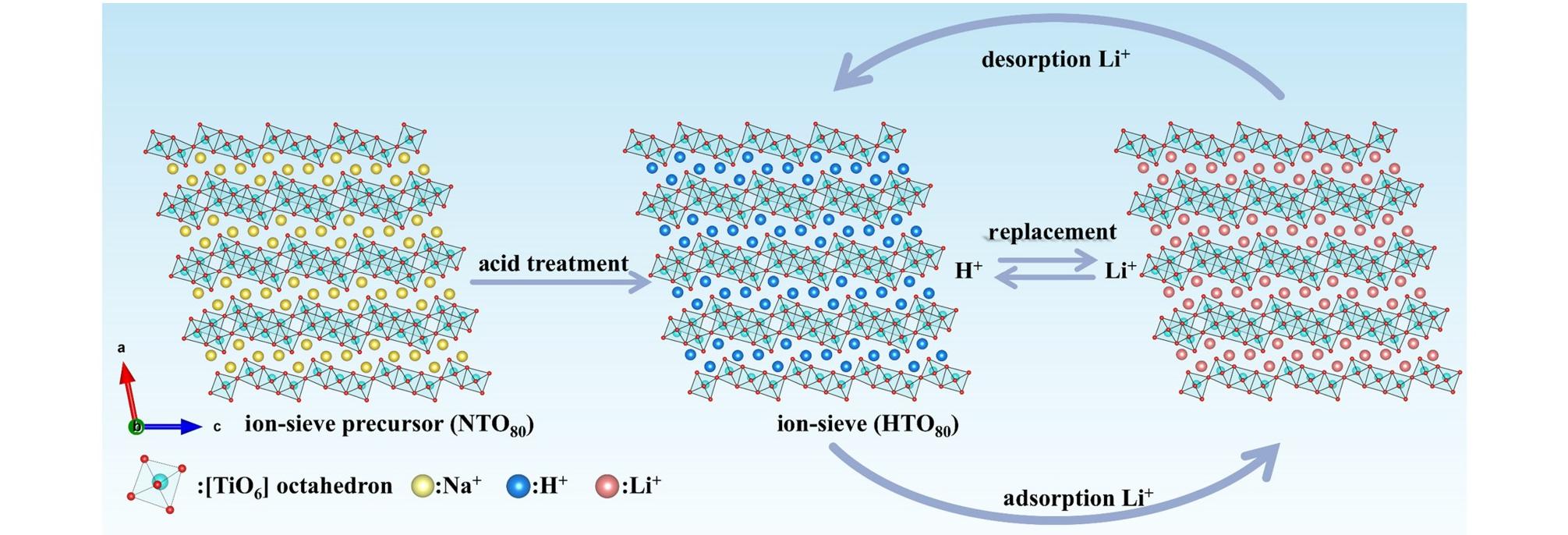
图8 HTO80的结构模型及其Li+吸附机制
Fig.8 The structural model of HTO80 and its adsorption mechanism for Li+ ions
3 结论
本研究通过低温水热合成技术成果制备了H2Ti3O7型钛基锂离子筛HTO80,展现出比表面积高达422.0 m2·g-1,在温和条件下对Li+的吸附容量达14.1 mg·g-1,快速吸附动力学,即10 min可达平衡容量的93.6%,5次循环后容量保持78%。其吸附机制符合准二阶动力学和Langmuir单层模型,证实通过H+/Li+交换实现特异性吸附,且对Li+表现出明显选择性。该研究为高效盐湖提锂技术开发提供了新思路,H2Ti3O7在工业化提锂中具有重要应用潜力。
[1] WANG Y, HE P, ZHOU H. Olivine LiFePO4: Development and future[J]. Energy & Environmental Science, 2011, 4(3): 805-817
[2] CELADON A, SUN H, SUN S, et al. Batteries for electric vehicles: Technical advancements, environmental challenges, and market perspectives[J]. SusMat, 2024, 4(5): e234
[3] DING Y, FU J, ZHANG S, et al. Advances in recycling LiFe-PO4 from spent lithium batteries: A critical review[J]. Separation and Purification Technology, 2024, 338: 126551
[4] YAN J, QIAN J, LI Y, et al. Toward sustainable lithium iron phosphate in lithium-ion batteries: Regeneration strategies and their challenges[J]. Advanced Functional Materials, 2024, 34(44): 2405055
[5] DING H, YUAN S, LEI S, et al. Technology and principle on preferentially selective lithium extraction for spent ternary lithium batteries: A review[J]. Separation and Purification Technology, 2025, 355: 129691
[6] ZHOU B, SU H, LIU W, et al. Solvent extraction of metal ions from the leaching solutions of waste lithium-ion battery materials:A review[J]. Separation and Purification Technology, 2025,354: 129173
[7] CHAN K, MALIK M, AZIMI G. Separation of lithium, nickel,manganese, and cobalt from waste lithium-ion batteries using e-lectrodialysis[J]. Resources, Conservation and Recycling,2022, 178: 106076
[8] YANG Y, SUN M, YU W, et al. Recovering Fe, Mn and Li from LiMn1-xFexPO4 cathode material of spent lithium-ion battery by gradient precipitation[J]. Sustainable Materials and Technologies, 2023, 36: e00625
[9] CHITRAKAR R, KANOH H, MIYAI Y, et al. A new type of manganese oxide (MnO2·0.5H2O) derived from Li1.6Mn1.6O4 and its lithium ion-sieve properties[J]. Chemistry of Materials,2000, 12(10): 3151-3157
[10] OOI K, MIYAI Y, KATOH S. Lithium-ion sieve property of λ-type manganese oxide[J]. Solvent Extraction and Ion Exchange,1987, 5(3): 561-572
[11] WANG S, CHEN X, ZHANG Y, et al. Lithium adsorption from brine by iron-doped titanium lithium ion sieves[J]. Particuology, 2018, 41: 40-47
[12] LIU J, ZHANG Y, MIAO Y, et al. Alkaline resins enhancing Li+/H+ ion exchange for lithium recovery from brines using granular titanium-type lithium ion-sieves[J]. Industrial & Engineering Chemistry Research, 2021, 60(45): 16457-16468
[13] GAO Y, WANG S, GAO F, et al. Al and Cr ions Co-doped spinel manganese lithium ion-sieve with enhanced Li+ adsorption performance and structural stability[J]. Microporous and Mesoporous Materials, 2023, 351: 112492
[14] QIN Y, YANG X, ZENG L, et al. Hydrophilic surface-modified titanium-based lithium ion sieve adsorbents for efficient lithium extraction[J]. Journal of Molecular Liquids, 2024,412: 125896
[15] JIN Z, MA T, LIU Y, et al. Preparation of tungsten-doped Tibased lithium ion sieves with excellent adsorption performance by hydrothermal method[J]. Journal of Alloys and Compounds,2024, 1005: 176058
[16] ZHANG H, DONG B, YANG Y, et al. Cu-doped titanium lithium-ion sieves with cell expansion and improved hydrophilicity for efficient extraction of lithium from aqueous resources[J]. Chemical Engineering Journal, 2024, 495: 153545
[17] WANG L, MENG C, HAN M, et al. Lithium uptake in fixed-pH solution by ion sieves[J]. Journal of Colloid and Interface Science, 2008, 325(1): 31-40
[18] ZAKI A H, ABDEL HAFIEZ M, EL ROUBY W M A, et al. Novel magnetic standpoints in Na2Ti3O7 nanotubes[J]. Journal of Magnetism and Magnetic Materials, 2019, 476: 207-212
[19] LOA I, LANDGREN F. On: X-ray diffraction from the electron gas in monatomic metallic hydrogen[J]. Journal of Physics: Condensed Matter, 2024, 36(18): 185401
[20] ZHOU J, GUAN B, GUO J, et al. Inhibition of Cu-SSZ-13 for NH3 selective catalytic reduction by K/Na poisoning[J]. Catalysis Letters, 2024, 154(6): 2761-2776
[21] MOLAEI S, GHADERMAZI M. Comparative study of two mesoporous magnetic and MCM-41 supported Cu complex: High-performance heterogeneous catalysts for aqueous synthesis of tetrazole[J]. Inorganic Chemistry Communications, 2024, 169: 113022
[22] YANG Z, LI Y, MA P. Impact of sintering temperature on H2TiO3 lithium-ion sieves synthesised via the solid-phase method[J]. Journal of Materials Science: Materials in Electronics, 2022, 33(29): 23128-23136
[23] LIU J, XU N, SHI D, et al. Preparation, characterization, and adsorption performance of H2TiO3 lithium ion sieves with homogeneous nanoparticles: Kinetics, thermodynamics, and mechanism analysis[J]. ChemistrySelect, 2024, 9(39): e202402440
[24] QU W, FU Y, ZHANG Y, et al. Structural/surficial dual regulated granular H2TiO3 lithium-ion sieves for lithium extraction from salt lake brine[J]. Journal of Cleaner Production, 2024, 449: 141789
[25] WU M, WANG S, JIANG M, et al. Preparation of W-doped titanium lithium ion sieve by hydrothermal method and enhanced adsorption performance for Li+[J]. Ionics, 2025, 31(4): 3421-3432
[26] YANG Z, LI Y, MA P. Synthesis of H2TiO3-PVC lithium-ion sieves via an antisolvent method and its adsorption performance[J]. Ceramics International, 2022, 48(20): 30127-30134
[27] YU C, BAO S, ZHANG Y, et al. Separation and adsorption of V(V) from canadium-containing solution by TOMAC-impregnated resins[J]. Chemical Engineering Research and Design, 2021,174: 405-413
[28] WANG S, LI P, ZHANG X, et al. Selective adsorption of lithium from high Mg-containing brines using HxTiO3 ion sieve[J].Hydrometallurgy, 2017, 174: 21-28
[29] RASEE A I, AWUAL E, REHAN A I, et al. Efficient separation, adsorption, and recovery of Samarium(Ⅲ) ions using novel ligand-based composite adsorbent[J]. Surfaces and Interfaces,2023, 41: 103276
[30] TANG D, ZHOU D, ZHOU J, et al. Preparation of H2TiO3-lithium adsorbent using low-grade titanium slag[J]. Hydrometallurgy, 2015, 157: 90-96
[31] WANG L, WANG L, WANG J, et al. Synthesis of zirconiumcoated lithium ion sieve with enhanced cycle stability[J]. Separation and Purification Technology, 2022, 303: 121933
[32] IDEMOTO Y, MOCHIZUKI T, UI K, et al. Properties, crystal structure, and performance of o-LiMnO2 as cathode material for Li secondary batteries[J]. Journal of the Electrochemical Society, 2006, 153(2): A418
[33] BAO L, TANG W, SUN S. Semi-wet synthesis of high-performance Li1.6Mn1.6O4 for selective lithium extraction from Salt Lakes Brine[J]. Desalination, 2024, 584: 117730
[34] SUN H, YANG Z, GHOSH R, et al. Thermal processing to modulate surface chemistry and bulk charge distribution in nickelrich layered lithium positive electrodes[J]. Nature Communications, 2025, 16(1): 1478
[35] PU X, DU X, JING P, et al. Interface and defect engineering enable fast and high-efficiency Li extraction of metatitanic acid adsorbent[J]. Chemical Engineering Journal, 2021,425: 130550
[36] CHEN S, CHEN Z, WEI Z, et al. Titanium-based ion sieve with enhanced post-separation ability for high performance lithium recovery from geothermal water[J]. Chemical Engineering Journal,2021, 410: 128320
[37] LIU J, XU N, BIAN S, et al. Design and adsorption performance of hollow structure nano-metatitanic acid lithium ion sieve with strong structure stability and large adsorption capacity[J].Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2024, 692: 133960