乙二醇(EG,HOCH2CH2OH)作为最简单的二元醇,其化学性质活泼,可发生酯化反应、醚化反应、氧化反应、缩醛反应、脱水反应等[1],广泛应用于聚酯纤维、塑料等工业的生产,也是防冻剂、冷却剂、保湿剂、增塑剂、软化剂、液压油以及化学工业中常用的溶剂[2-4]。 目前,乙二醇的工业生产常采用石油路线和合成气路线,相比之下,经济性更好、不依赖石油的合成气路线受到了更为广泛的关注。该路线先从煤、天然气、生物质和其他原料制备合成气,然后通过CO羰基化偶联反应得到草酸二甲酯(DMO),进而加氢制得乙二醇[5]。 其中,草酸二甲酯加氢技术作为乙二醇生产的核心技术之一,高性能加氢催化剂的开发更是其中的关键。
铜催化剂作为应用最广泛的草酸二甲酯加氢催化剂,国内外学者对其进行了大量的研究工作,得到了许多有重大参考价值的结论。 研究表明,催化剂的制备工艺影响铜物种的分布、铜物种与载体之间的相互作用以及铜颗粒的化学状态,进而影响其催化反应性能。 Dong等[6]分别采用蒸氨法和沉淀法制备了AE-Cu/SiO2催化剂和CP-Cu/SiO2催化剂。 其中蒸氨法制备的催化剂AE-Cu/SiO2有利于形成具有片状结构的页硅酸铜,提供大量的铜纳米粒子和酸位点[7],可以进一步提高催化剂的活性和选择性。 而沉淀法合成的CP-Cu/SiO2催化剂,由于铜颗粒较大,反应过程中会发生铜的聚集和流失严重问题,导致催化性能较差。 另外,Song等[8]分别以蒸氨法、蒸氨水热法、改进的水热法和沉淀凝胶法合成了一系列高分散的铜硅催化剂,对比了4种合成方法对于碳酸乙烯酯加氢活性的影响,改进的水热法性能较好,甲醇的选择性可达到89%,经研究发现在水热合成过程中Cu与SiO2的相互作用更强,可以生成更多的层状硅酸铜物种,使还原后的催化剂含有更多的Cu+,这会有利于加氢反应的进行。 为了防止铜颗粒在热处理过程中快速迁移、聚集和流失导致催化剂的稳定性下降,人们不断探索研究Cu/SiO2催化剂的制备过程,将蒸氨法和水热法相结合来制备Cu/SiO2催化已得到了广泛的研究。
载体作为催化剂的重要组成部分,在维持催化剂活性,提高催化剂稳定性方面发挥着重要的作用[9]。 当前传统的Cu/SiO2催化剂多以硅溶胶作为载体材料,其孔道不发达,在扩散方面存在劣势。相比而言介孔二氧化硅以其丰富多孔的结构,为分子提供扩散途径。 Xu等[10]采用介孔二氧化硅制备了Cu/SiO2催化剂,利用介孔二氧化硅来创建活跃的金属-载体界面来促进催化,通过调控介孔二氧化硅制备出了具有丰富Cu-O-SiOx界面,其在DMO选择性加氢到EG中是一个非常活跃的界面,因此表现出了相对较好的催化性能。 鉴于目前草酸二甲酯选择性加氢反应催化剂多采用蒸氨法制备,且二氧化硅的载体效应对选择性加氢反应性能的影响研究较少,本研究拟进行水热条件下介孔二氧化硅载体效应的探究。
本研究采用改进水热法制备了系列Cu/SiO2催化剂,并与传统蒸氨法对比,在此基础上探讨了水热时间及介孔SiO2载体尺寸对催化性能的影响。通过XRD、FTIR、H2-TPR、TEM、XPS等表征方法对催化剂的物化结构进行表征分析,探讨其对催化性能的影响。
1 实验
1.1 实验药品
硝酸铜[Cu(NO3)2·3H2O,质量分数为99%]、氨水(质量分数为25%~28%)、十六烷基三甲基溴化铵(CTAB)、正硅酸四乙酯(TEOS)购自国药化学试剂有限公司。 胶体二氧化硅(质量分数为40%)由阿拉丁试剂提供。
1.2 催化剂的制备
1.2.1 介孔二氧化硅的制备
介 孔 二 氧 化 硅 采 用Stöber法 制 备[11,12]。 将0.16 g CTAB,30 mL乙醇,1 mL TEOS,适量氨水,和一定量的H2O依次加入三口烧瓶中,于室温下搅拌,然后将悬浊液离心洗涤至中性,放于110 ℃烘箱中干燥过夜。 研磨后于600 ℃下煅烧6 h,以去除模板剂。 得到的硅球分散在一定量水中,以待制备催化剂时使用。
1.2.2 蒸氨法制备Cu/SiO2-EA催化剂
称取适量Cu(NO3)2·3H2O溶于适量的去离子水中,向其溶液加入一定量的氨水,使铜氨络合物溶液的pH值在11 ~12之间。 然后,将硅溶胶逐滴滴加到铜氨溶液中,滴加完毕后老化4 h。 老化结束后,将水浴温度升至80 ℃,开始蒸氨,待溶液pH值达到中性左右停止蒸氨。 接着将蒸氨后的悬浊液过滤、洗涤,100 ℃干燥过夜。 最后,将干燥后的固体研磨,于马弗炉中600 ℃煅烧5 h,得到的催化剂记为Cu/SiO2-EA。
1.2.3 水热法制备Cu/SiO2-HY催化剂
水浴温度在30 ℃下,将适量Cu(NO3)2·3H2O溶于去离子水中,向其中加入一定量的氨水溶液,使初始铜氨溶液的pH值在11左右。 然后将一定量的硅球加入去离子水中,超声数分钟使其分散均匀后,在40 ℃下逐滴滴加到铜氨溶液中,滴加完毕后老化4 h。 将老化后的悬浊液转移到反应釜中,140 ℃水热合成数小时。 将水热后的悬浊液离心、洗涤至中性,真空干燥过夜。 将干燥后的固体研磨后,于马弗炉中450 ℃煅烧4 h。 得到的催化剂记为Cu/SiO2-HY。
1.3 催化剂的评价
本实验采用实验室自制的固定床反应器对催化剂的加氢性能进行评价,使用质量分数为10%DMO的甲醇溶液作为原料液。 催化剂取2 mL(40 ~80目),两端装填适量的石英砂(40 ~80目)防止管内气体沟流。 然后对催化剂进行在线还原,还原结束后进行反应,产物用气相色谱(SP-3420A,色谱柱HP-INNOWAX, 毛 细 管 柱: 30 m × 0.320 mm ×0.50 μm,FID)进行分析。 采用外标法对DMO加氢产物进行分析,DMO的转化率、EG的选择性按式(1)和式(2)计算。
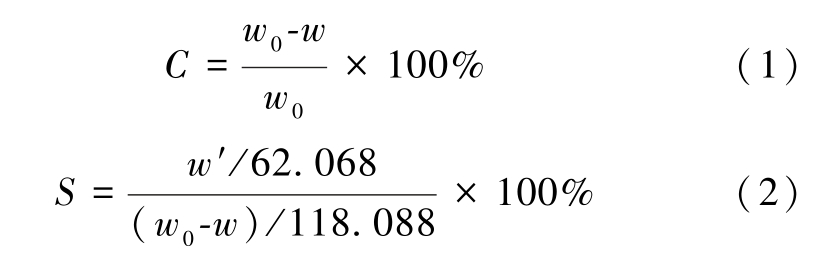
式(1)和式(2)中:C为DMO转化率;S为EG选择性;w0为原料液DMO的质量分数;w为产物中的DMO质量分数;w′为产物中EG的质量分数。
1.4 表征
1.4.1 X射线衍射
煅烧样品和还原样品的X射线衍射(XRD)分析在D/MAX/2500PC型X射线粉末衍射仪上进行,使用Cu_Kα 辐射(λ = 0.154 06 nm),扫描角(2θ)范围为10°~90°。
1.4.2 傅里叶变换红外吸收光谱
催化剂结构采用型号为Nicolet IS10的红外光谱仪(美国赛默飞公司)进行测定。 扫描范围为400 ~4 000 cm-1。 样品制备:需要将样品与KBr在研钵中研磨混合均匀,压片后放入仪器中进行测试。
1.4.3 透射电子显微镜
采用JEM-2100 PLUS透射电子显微镜(日本电子公司)对催化剂结果进行表征分析。 测试之前要将催化剂样品在室温下在乙醇中超声分散20 min。
1.4.4 H2程序升温还原
程序升温还原(H2-TPR)使用Auto Chem Ⅱ2920型化学吸附仪和导热系数探测器(TCD)。 将样品放置在U型管中,在氩气气氛下以2 ℃·min-1的升温速率将温度升至150 ℃,再以1 ℃·min-1的速率将样品温度升至350 ℃,预处理1 h。 冷却至室温后,将体积分数为10%的H2/Ar混合气通入仪器中,以10 ℃·min-1的速率将温度升至600 ℃。
1.4.5 X射线光电子能谱
采用XPS及AES进行测试催化剂表面铜物种价态分布,仪器型号为ESCALAB Ⅺ+的电子能谱仪。 样品于350 ℃和体积分数为10%的H2/N2气氛下预处理8 h,冷却至室温后以N2保护转移至密闭容器中。 选取284.8 eV处的C 1s结合能作为基准,校准催化剂所有结合能。
2 结果与讨论
2.1 不同制备方法对Cu/SiO2-HY 催化剂加氢性能的影响
图1 是在200 ℃、3 MPa、氢酯比为80的条件下,对3组催化剂进行DMO加氢性能的评价图。
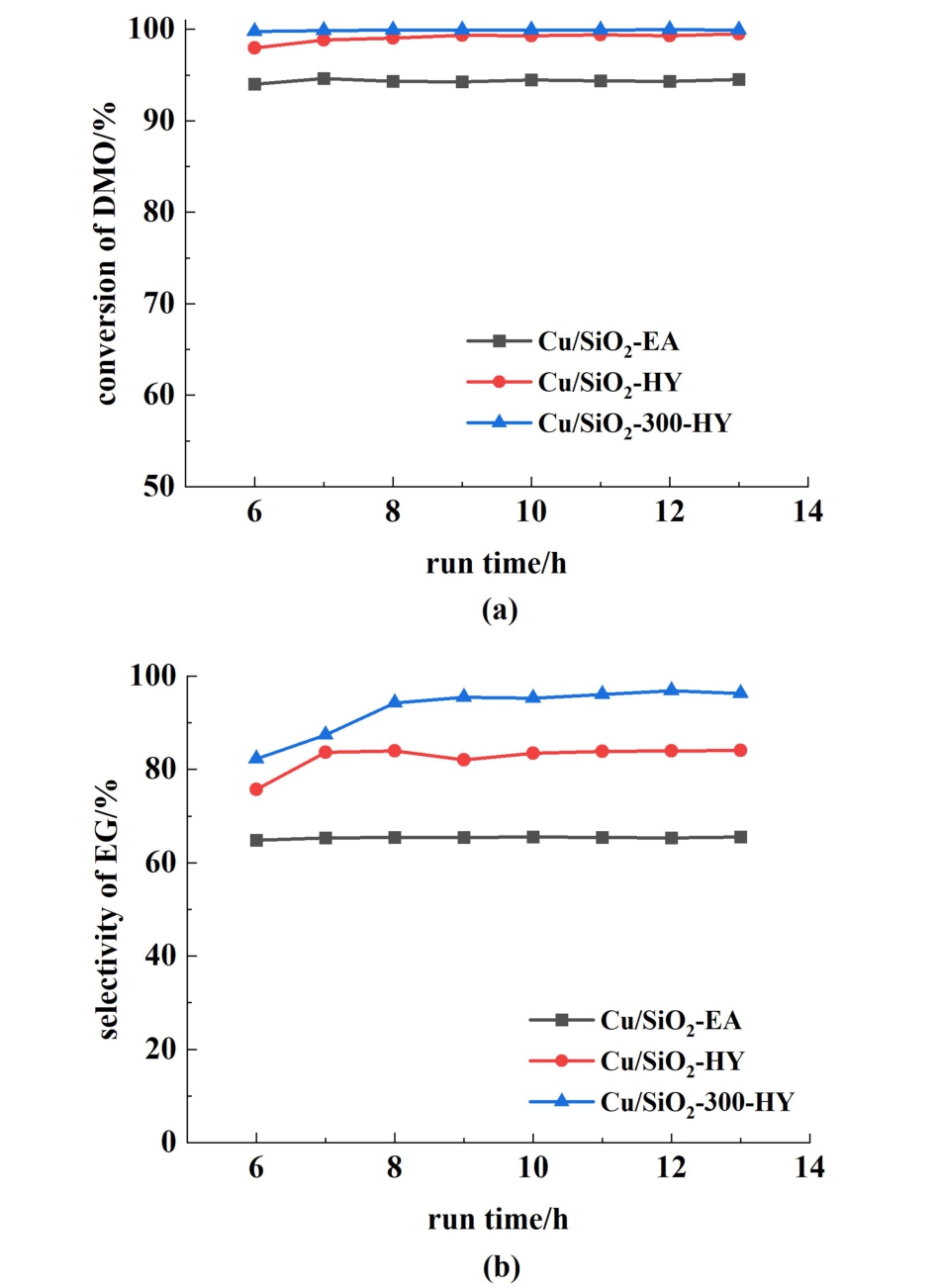
图1 不同制备方法及硅源对(a)DMO的转化率和(b)EG的选择性的影响
Fig.1 Effect of different preparation methods on the(a) conversion of DMO and (b) the selectivity of EG
本研究以硅溶胶为硅源,采用蒸氨法和水热法分别制备了Cu/SiO2-EA和Cu/SiO2-HY 2组催化剂,然后选取300 nm尺寸的介孔硅球为载体,采用水热法制备了Cu/SiO2-300-HY催化剂进行对比。 从图1中可以看出,在硅源相同的情况下,水热法制备的Cu/SiO2-HY催化剂的催化活性显著优于蒸氨法制备的Cu/SiO2-EA催化剂,其DMO的转化率达到99%,EG的选择性达到80%以上。 另外,以介孔硅球为载体的Cu/SiO2-300-HY催化剂性能明显优于以硅溶胶为硅源的Cu/SiO2-HY催 化 剂, 其 中, DMO转 化 率 达 到99%,EG选择性达到96%。 这可能与硅球的介孔结构强化了反应的传质过程有关系,详细原因需根据表征数据进一步分析。
2.2 Cu/SiO2-300-HY 催化剂制备工艺优化
2.2.1 水热时间对Cu/SiO2-300-HY催化剂加氢性能的影响
水热时间是影响催化剂结构和性能的重要因素,我们在5 ~20 h水热条件下,探究了水热时间对Cu/SiO2-300-HY催化性能的影响, 结果如图 2所示。
从图2中可以看出随着水热时间的增加,催化剂的性能逐渐提升并达到稳定,水热时间为15 h的Cu/SiO2-300-HY-15催化剂性能最优,其中DMO转化率达到99%,EG选择性达到96%。 继续增加水热时间,Cu/SiO2-300-HY-20催化剂的性能开始下降,这可能是因为水热时间过长对催化剂结构产生不利影响。
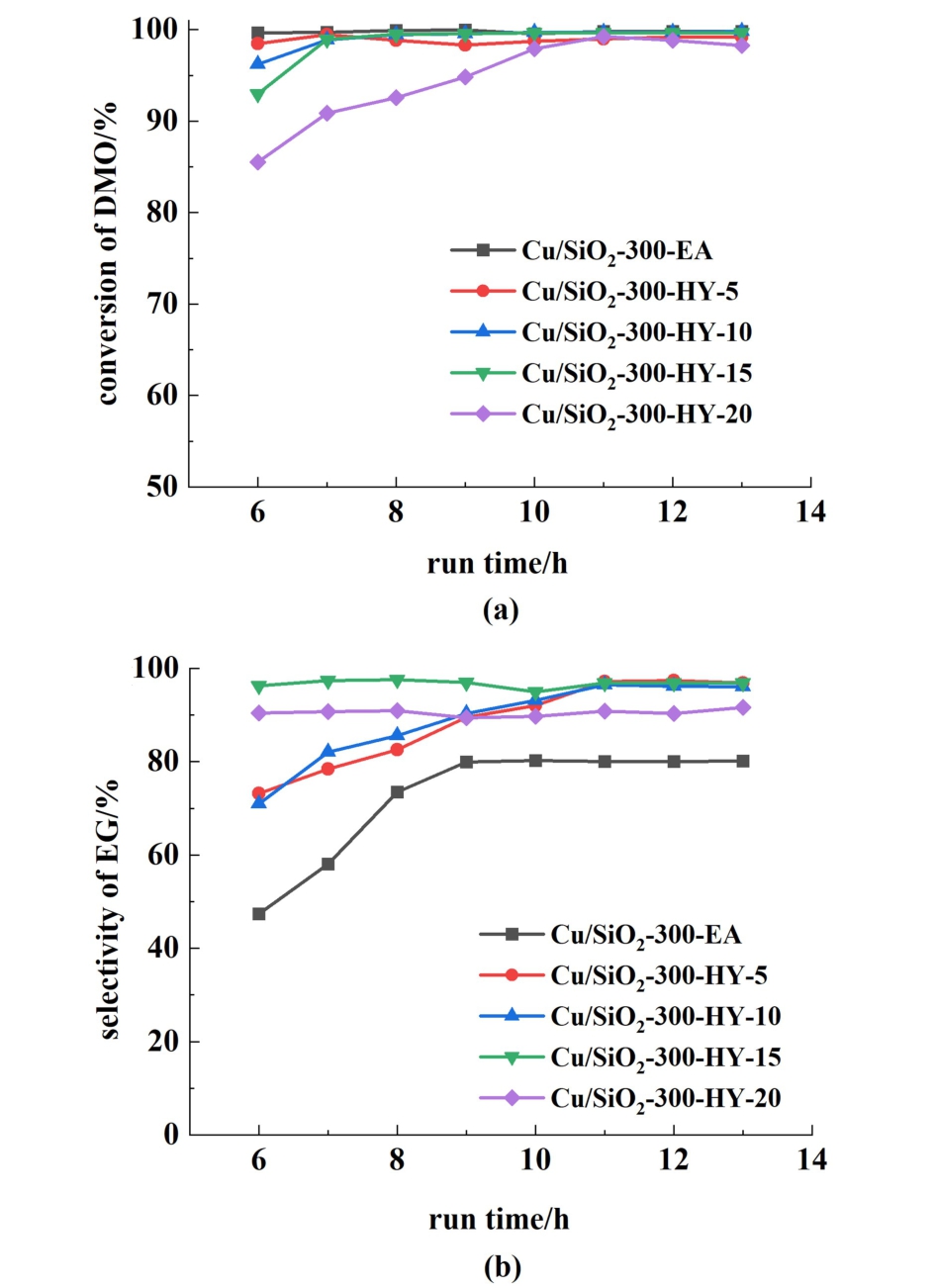
图2 不同水热时间对(a)DMO的转化率和(b)EG的选择性的影响(Cu/SiO2-300-HY-x,x为水热时间)
Fig.2 Effect of different hydrothermal times on (a) the conversion of DMO and (b) the selectivity of EG(Cu/SiO2-300-HY-x,x represents the hydrothermal time)
2.2.2 载体尺寸对Cu/SiO2-HY催化剂加氢性能的影响
在最适宜水热时间的基础上,我们通过控制水解条件制备了不同尺寸的介孔硅纳米微球,探讨了载体的尺寸对催化加氢反应性能的影响,结果如图3所示。
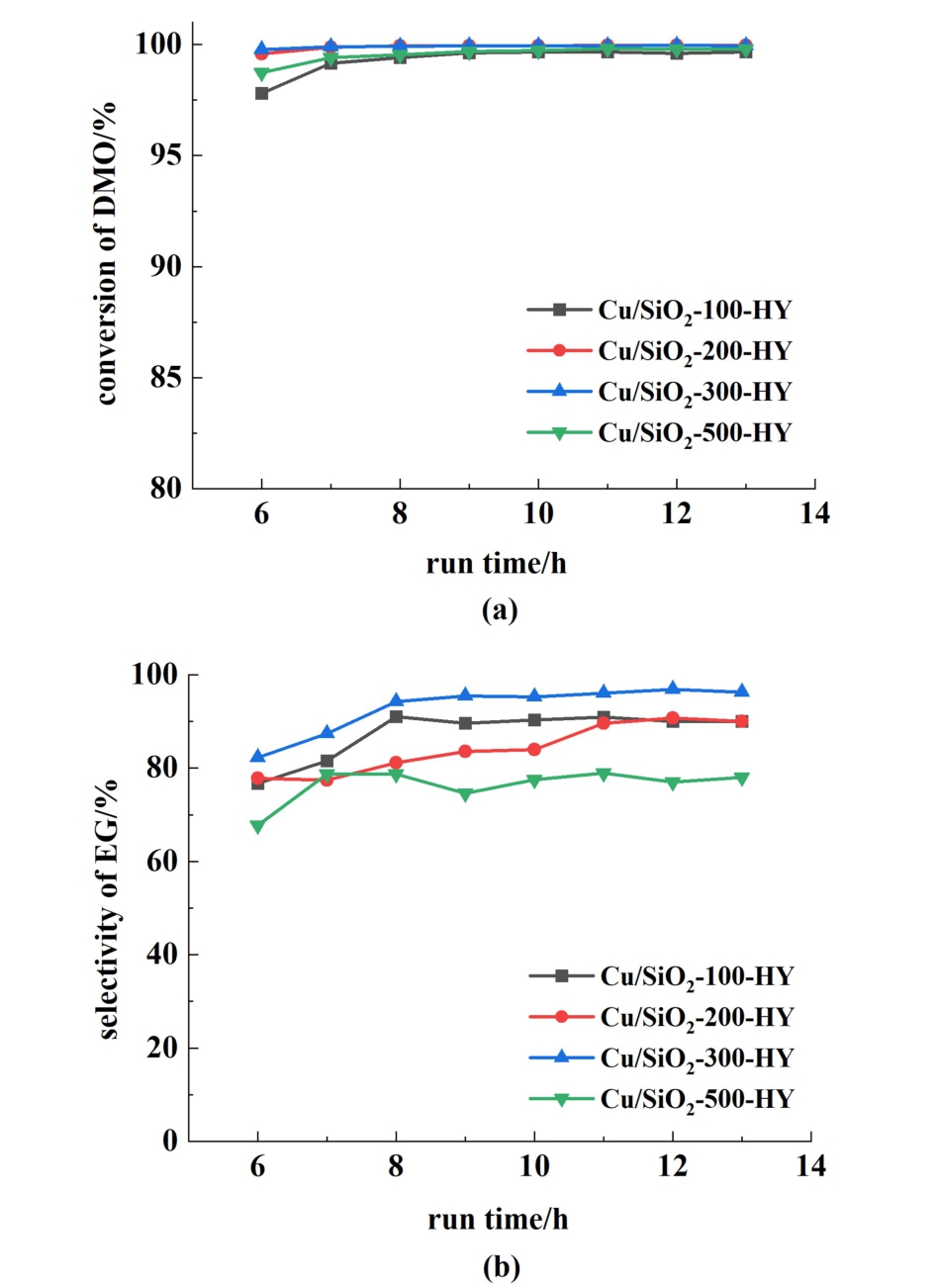
图3 不同载体尺寸对(a)DMO的转化率和(b)EG的选择性的影响(Cu/SiO2-y-HY,y为硅球尺寸)
Fig.3 Effect of different carrier sizes on (a) the conversion of DMO and (b) the selectivity of EG(Cu/SiO2-y-HY,y represents the size of the silicon sphere)
由图3可以看出,与转化率相比,载体尺寸对选择性的影响更加显著,随着载体尺寸的增加,选择性先升高后降低,载体尺寸在300 nm左右,催化性能最佳,DMO的转化率可达99%,EG的选择性达到96%。 根据药大卫等[11]的研究结果,载体尺寸影响反应物的富集和扩散,两者的平衡效应导致具有中等尺寸载体的催化剂表现出最优的催化性能。
2.3 Cu/SiO2 催化剂的结构性质和活性物质
2.3.1 氧化态催化剂的X射线粉末衍射
氧化态的Cu/SiO2-y-HY催化剂和Cu/SiO2-300-EA催化剂的XRD图谱如图4所示。
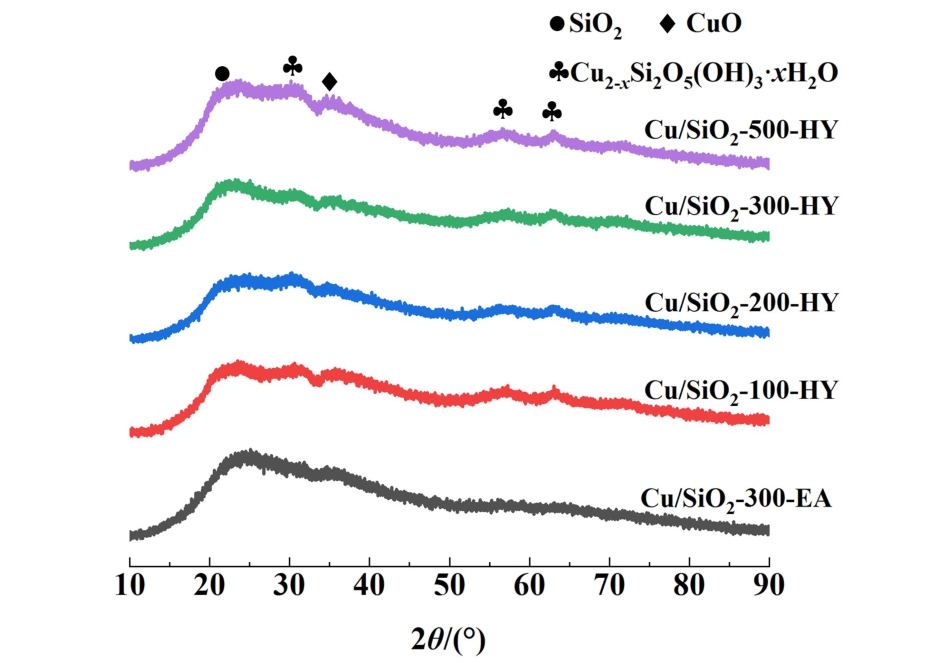
图4 氧化态催化剂的XRD图谱
Fig.4 XRD patterns of the oxidation state catalysts
从图4可以看出,各样品在2θ=21.8°处的峰归属为无定型SiO2的衍射峰,2θ=35.5°处的峰为CuO的衍射峰,在2θ=30.8°、57.0°和63.1°处的峰归属于Cu2Si2O5(OH)2。 可以看出相对于各Cu/SiO2-y-HY样品,Cu/SiO2-300-EA催化剂中硅酸铜的特征峰不明显,说明制备方法影响催化剂上硅酸铜的含量或结晶度,从而影响其催化加氢性能。
2.3.2 傅里叶变换红外吸收光谱
煅烧后催化剂的红外吸收谱图如图5所示。
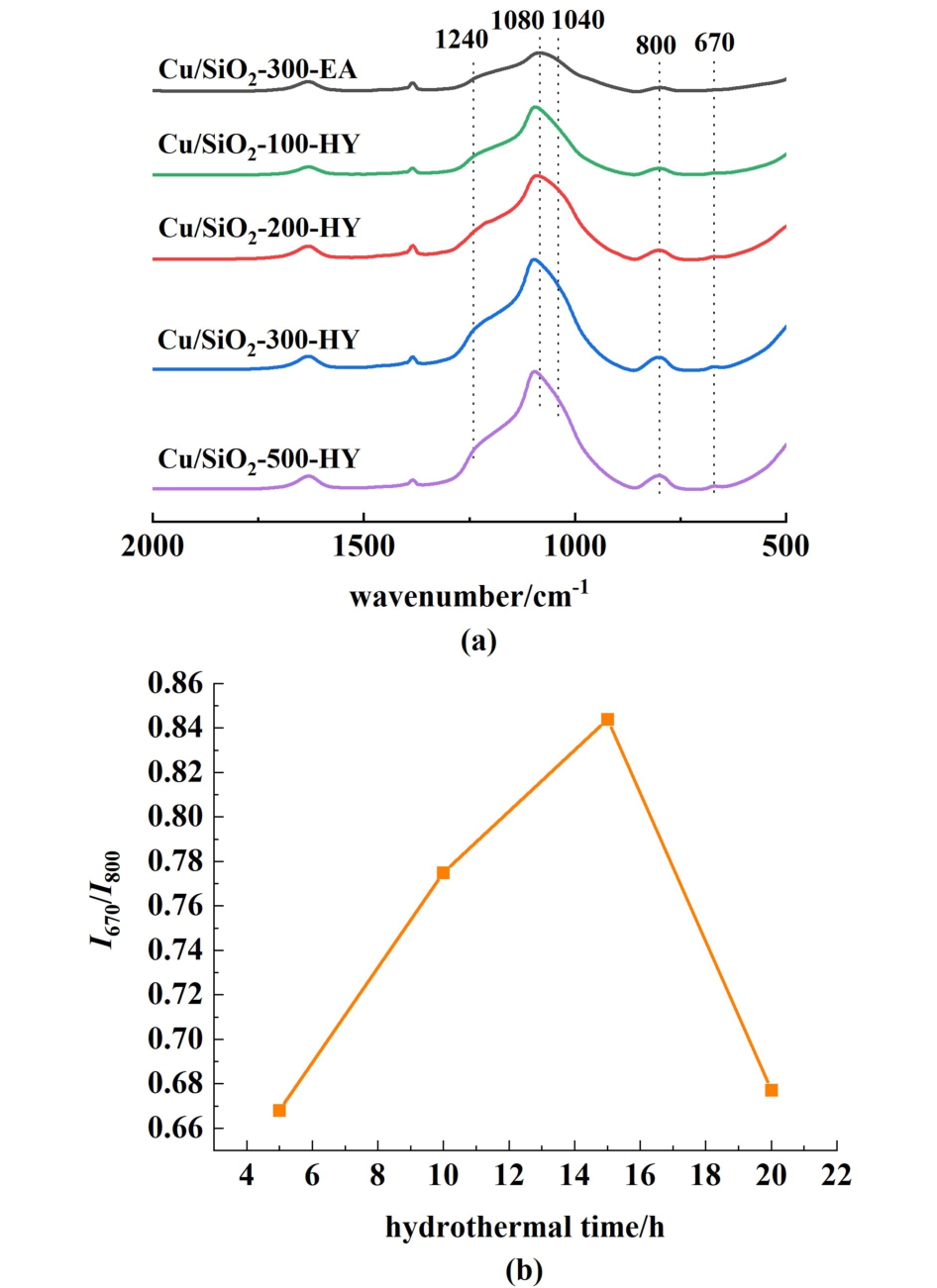
图5 (a)氧化态催化剂的FTIR图谱和(b)氧化态催化剂的I670/I800
Fig.5 (a) FTIR profile of oxidation state catalyst and(b) I670/I800 of oxidation state
由图5(a)可知,在无定形二氧化硅的振动峰中,1 080和1 240 cm-1处的2个吸收带属于Si—O—Si结构的非对称伸缩振动峰,而800 cm-1处的吸收带属于Si—O—Si结构的对称伸缩振动峰[13]。 当670和1 040 cm-1处都存在吸收峰时,可以确定催化剂样品中含有层状硅酸铜[14],其中670 cm-1处的吸收峰属于层状硅酸铜中的—OH基团的振动峰(δOH),而1 040 cm-1处的吸收峰则属于层状硅酸铜中Si—O的振动峰(νSiO)[14,15]。通过比较670cm-1处δOH带和800cm-1处νSiO带的强度,即I670/I800[16,17],可以定性计算出不同载体制备的Cu/SiO2-y-HY样品中层状硅酸铜的相对含量[18]。如图5(b)所示,不同载体尺寸的Cu/SiO2-y-HY催化剂的I670/I800比值差异显著,随着载体尺寸从100增加到500 nm,I670/I800比值先增大后减小,说明样品中层状硅酸铜的含量是呈先增加后减少的趋势。其中,Cu/SiO2-300-HY催化剂的I670/I800含量最高,说明Cu/SiO2-300-HY催化剂中层状硅酸铜相对含量最高,而层状硅酸铜增多可以提供更多的高分散活性位点,因此Cu/SiO2-300-HY表现出了最佳催化性能。
2.3.3 还原态催化剂的X射线粉末衍射
还原态的Cu/SiO2-y-HY催化剂和Cu/SiO2-300-EA催化剂的XRD图谱见图6。
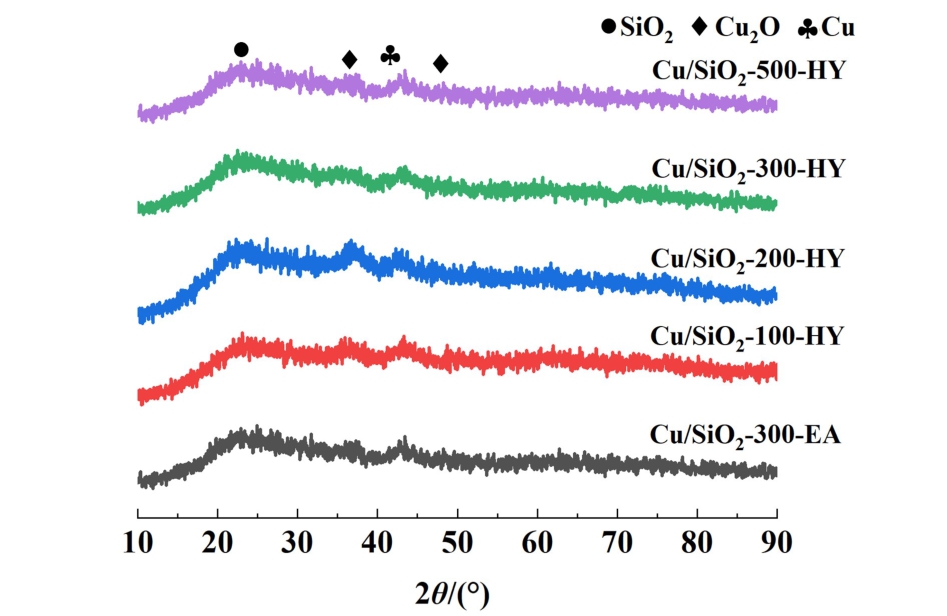
图6 还原态催化剂的XRD图谱
Fig.6 XRD patterns of reduced catalysts
在2θ=22.9°处的峰归属为无定型SiO2的衍射峰,2θ=36.8°和48.6°处的峰为Cu+的衍射峰,2θ=43.1°处的峰为Cu0的衍射峰,在整个图谱中没有观察到CuO的衍射峰,这说明催化剂还原结束后Cu2+已全部被还原为Cu0和Cu+。 可以看到Cu/SiO2-300-HY催化剂的Cu2O的衍射峰比其他几组催化剂的衍射峰宽,这说明Cu+在载体SiO2上分散度较高,而Cu+是由硅酸铜前驱体还原而成的,Cu2+与硅酸铜表面的Si—O—Cu键形成了强相互作用,使得Cu2+不易被还原为Cu0,从而以高度分散的Cu+分散在载体表面[19,20]。
2.3.4 透射电子显微镜
为了进一步探究水热时间对催化剂性能的影响,采用了TEM表征来进行分析,见图7。
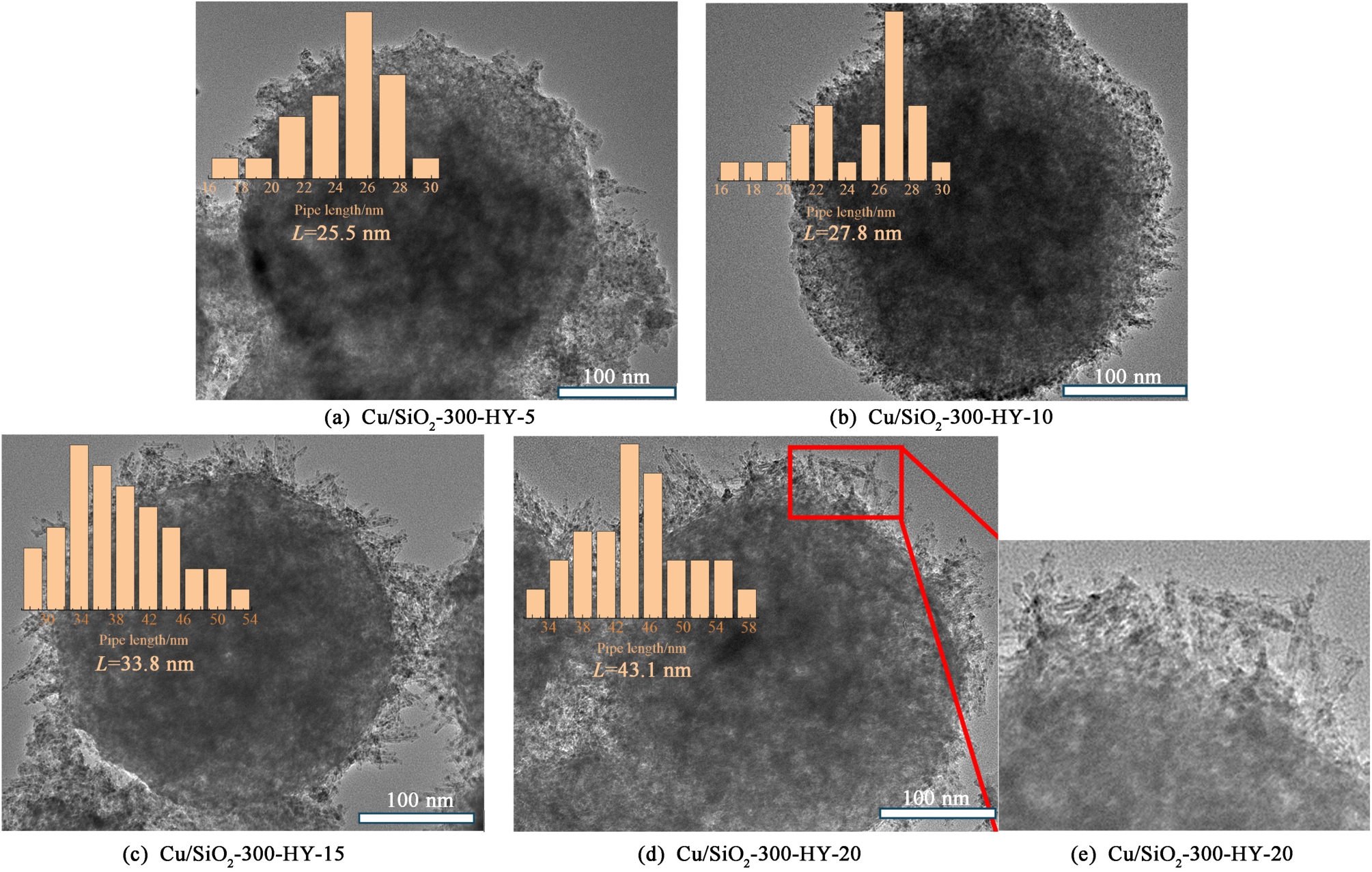
图7 还原态的Cu/SiO2-300-HY-x催化剂TEM图
Fig.7 TEM images of reduced Cu/SiO2-300-HY-x catalysts
图7 所示是经过还原后的Cu/SiO2-300-HY-x催化剂TEM图。 从TEM图中可以观察到,水热时间的不断增加,在载体硅球的表面生长出尺寸不同硅酸铜的纳米管。 在水热时间为5 h的条件下,载体表面的硅纳米管长仅有25.5 nm,随着水热时间延长到10 h时,载体表面的硅纳米管生长到27.8 nm,并且与水热5 h制备的催化剂相比,其表面的硅纳米管生长得比较均匀。 随着水热时间的进一步延长,载体表面的硅纳米管的长度也随之增加,这与催化剂活性评价结果相对应,说明催化剂制备过程中的水热时间可以影响催化剂表面硅纳米管的长度。 如图7(e)是Cu/SiO2-300-HY-20催化剂的局部放大图,可以看到当水热时间增加到20 h后,硅纳米管在载体上有部分堆积在载体表面,阻碍了硅纳米管的生成,这可能是Cu/SiO2-300-HY-20催化剂性能下降的原因。 因此后续实验将水热时间设置在15 h,不仅能保证硅纳米管的生长时间,还能避免纳米管的沉积。
2.3.5 H2程序升温还原
为了进一步研究铜的氧化还原特性对催化性能的影响,对各氧化态催化剂进行了H2-TPR表征,如图8所示。
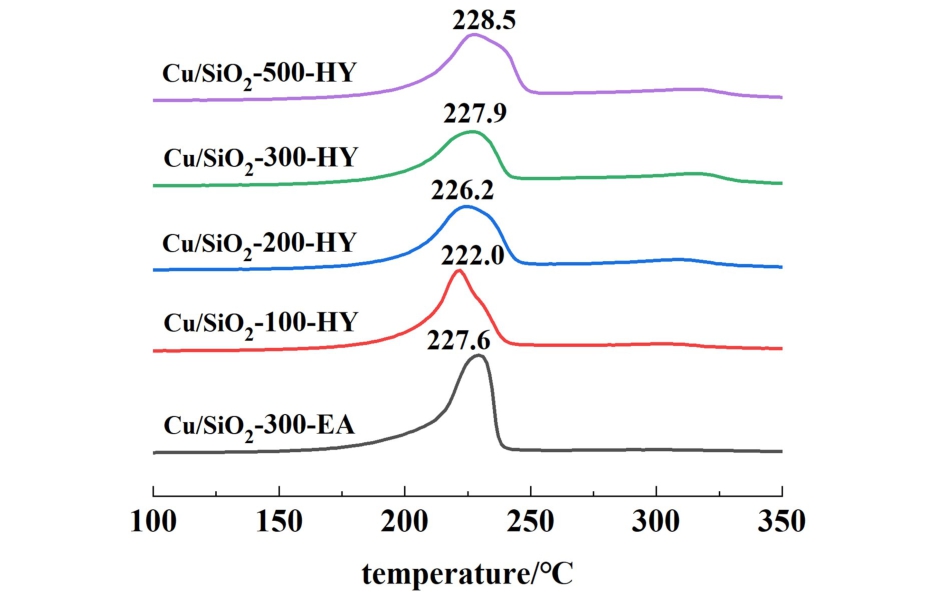
图8 氧化态化剂的H2-TPR图谱
Fig.8 H2-TPR profiles of oxidation state catalysts
由图8可知,所有催化剂在200 ~250 ℃范围内均出现1个不对称的还原峰,不同制备方法和不同硅球尺寸的还原温度呈现出不同的规律。 随着二氧化硅尺寸的增加,还原峰的温度不断升高,这表明硅球尺寸对铜物种的还原有一定的影响。 另外可以观察到,Cu/SiO2-300-HY催化剂的还原温度比Cu/SiO2-300-EA催化剂的高,这表明,在水热过程中,Cu/SiO2-300-HY催化剂表面Cu与载体之间的相互作用更加紧密,从而导致催化剂表面的铜颗粒更难以还原[21,8]。 催化剂在200 ~250 ℃之间的还原峰与硅酸铜还原为Cu+有关[22],还原峰向更高温度移动,这表明形成了更多的硅酸铜[23,24]。 根据TEM和XRD表征结果,在煅烧催化剂中没有发现大块氧化铜,由页硅酸铜还原衍生的Cu+通常是在600 ℃左右,因此,在310 ℃左右的峰值可能属于部分Cu+的还原,很可能是由Cu—O—Si的还原形成的Cu+[25]。
2.3.6 X射线光电子能谱
大量研究表明催化剂表面还原态铜物种的价态和含量对催化加氢反应有重要的影响,为了进一步证明不同价态的活性组分在草酸二甲酯加氢反应中的作用,对蒸氨法制备的Cu/SiO2-300-EA催化剂和水热方法制备的Cu/SiO2-y-HY催化剂进行了XPS表征,如图9所示。
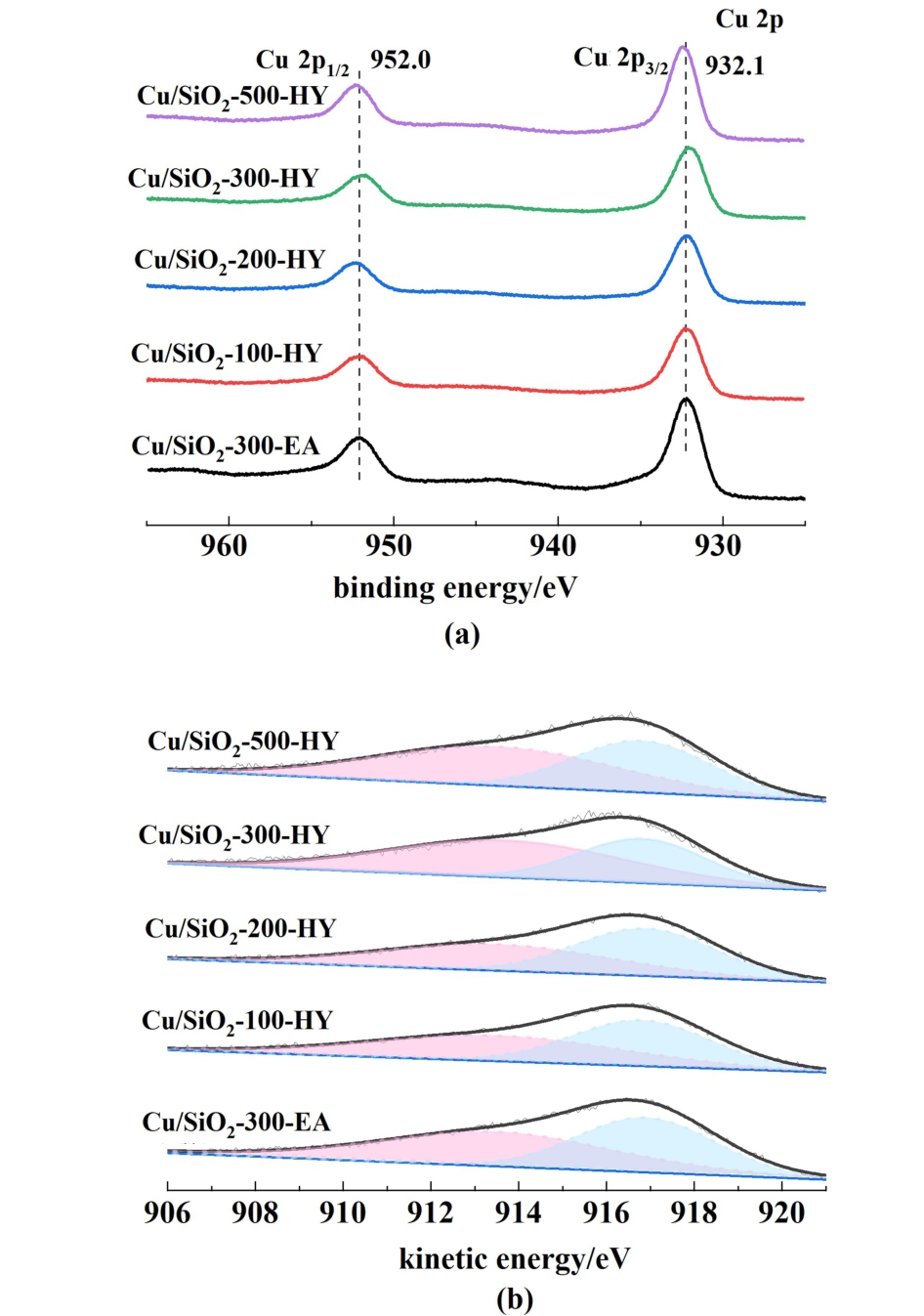
图9 (a)还原态催化剂的Cu 2p XPS光谱;(b)还原态催化剂的铜LMM XEAS光谱
Fig.9 (a) Cu 2p XPS spectra of reduced catalysts;(b) Cu LMM XEAS spectra of reduced catalysts
如图9(a)所示,各还原态催化剂均呈现2个峰,中心分别为932和952 eV,分别对应Cu 2p3/2和Cu 2p1/2。 在结合能为942 ~944 eV之间没有观察到氧化态Cu 2p→3d的卫星峰,说明催化剂表面Cu2+物种均被还原为Cu0或Cu+[5,26]。 可以观察到在改变制备方法后,由水热法制备的催化剂的Cu 2p3/2的结合能略向高结合能方向移动,表明水热合成过程中Cu与载体间的结合更加紧密。
由于Cu+和Cu0的Cu 2p3/2和Cu 2p1/2结合能几乎相同,难以通过XPS进行区分,所以需要采用Cu LMM XEAS来区分[27]。 还原后的Cu/SiO2-300-EA催化剂和Cu/SiO2-300-HY催化剂上[图9(b)]均出现一个位于906 ~920 eV的不对称宽峰,此峰为还原态Cu0和Cu+物种的特征峰[28]。 为了更好地计算出Cu0和Cu+2个物种的比例,对其进行了高斯拟合如图9(b),在912.7和916.8 eV处得到2个对称峰,它们分别对应的是Cu+和Cu0[8],分峰结果如表1所示。 可以看出,Cu/SiO2-y-HY催化剂表面Cu+/(Cu++Cu0)物种的比例略高于Cu/SiO2-300-EA催化剂,说明水热方法制备的催化剂表面Cu+浓度更高[5]。 而水热法制备的一系列催化剂中,Cu/SiO2-300-HY的Cu+/(Cu++Cu0)物种的比例最大,表现出了最佳的催化性能,这与评价数据相一致。另外通过对比,以介孔二氧化硅为载体更利于催化剂表面Cu+的生成。
表1 Cu/SiO2-300-EA 催化剂和Cu/SiO2-y-HY 催化剂的XPS 和Cu LMMXEAS 的高斯拟合分峰结果
Table 1 Gaussian fitting peak splitting result of XPS and Cu LMMXEAS for Cu/SiO2-300-EA catalysts and Cu/SiO2-y-HY catalysts
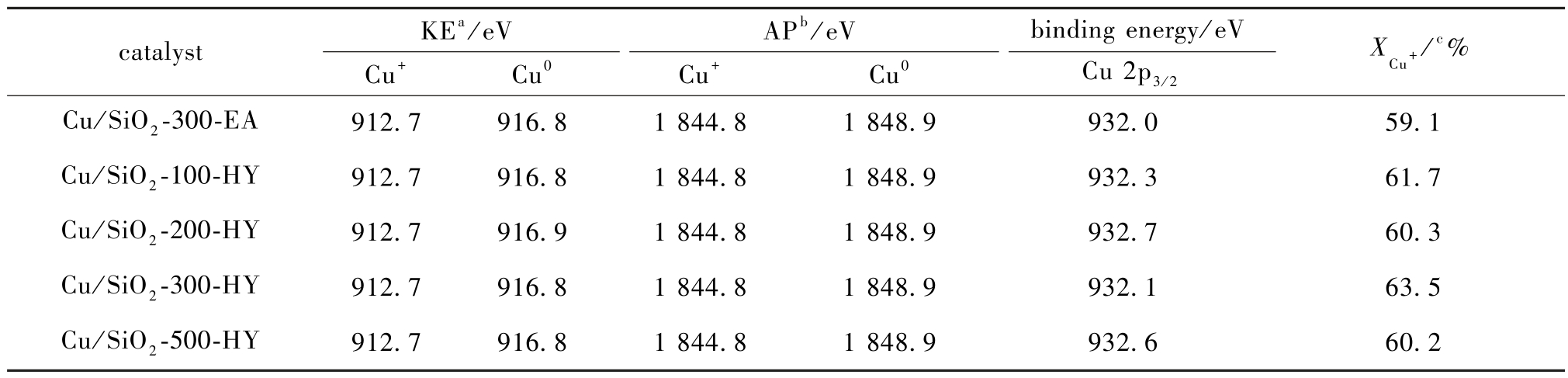
a Kinetic energy (KE);b Auger parameter (AP);c Obtained by Cu LMM AES spectra.
catalyst KEa/eV APb/eV binding energy/eV Cu+ Cu0 Cu+ Cu0 Cu 2p3/2 XCu+/c%Cu/SiO2-300-EA 912.7 916.8 1 844.8 1 848.9 932.0 59.1 Cu/SiO2-100-HY 912.7 916.8 1 844.8 1 848.9 932.3 61.7 Cu/SiO2-200-HY 912.7 916.9 1 844.8 1 848.9 932.7 60.3 Cu/SiO2-300-HY 912.7 916.8 1 844.8 1 848.9 932.1 63.5 Cu/SiO2-500-HY 912.7 916.8 1 844.8 1 848.9 932.6 60.2
2.4 Cu/SiO2-300-HY 催化剂的稳定性测试
催化剂的稳定性是影响其产业化应用的关键因素之一,需在长时间、高强度反应条件下保持高活性和选择性,以确保经济性和可持续性。图10是Cu/SiO2-300-HY催化剂的稳定性测试。
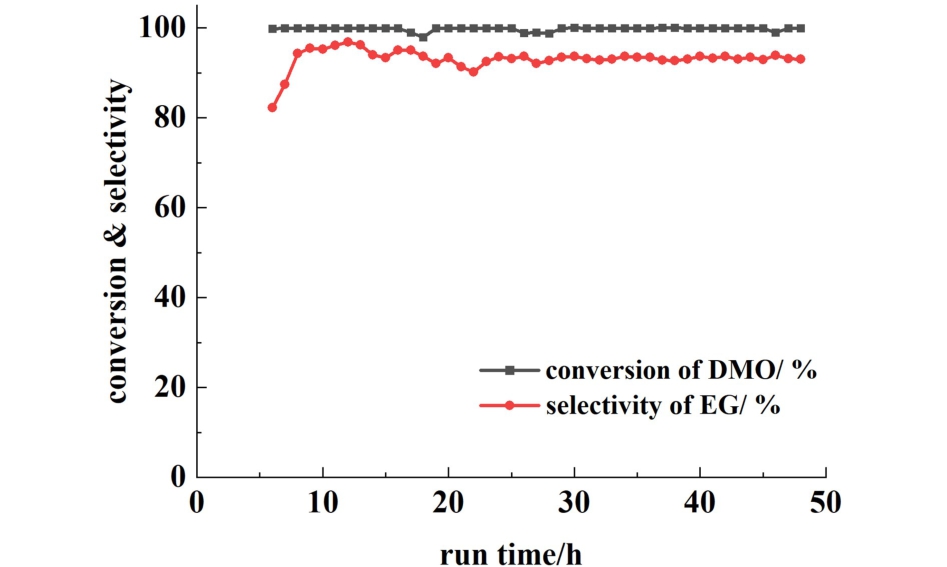
图10 Cu/SiO2-300-HY催化剂的催化性能随时间的变化
Fig.10 The catalytic performance of Cu/SiO2-300-HY catalyst varies with time
在200 ℃、3 MPa、氢酯比为80、液时空速为0. 9 h-1的条件下,我们对Cu/SiO2-300-HY催化剂进行了48 h的稳定性测试。 从图10中可以看出,该催化剂表现出优异的稳定性,DMO转化率维持在99%以上,同时EG选择性保持在93%左右且无明显波动。
3 结论
采用水热法合成系列Cu/SiO2催化剂,研究结果表明其催化反应性能与水热时间和载体尺寸密切相关。 TEM、XRD及H2-TPR表征结果显示,水热时间影响催化剂的结构及活性组分铜的分散度,不同尺寸载体催化剂表面铜物种还原度也不同。 水热时间为15 h,二氧化硅载体尺寸为300 nm时,催化剂的催化加氢效果最好,DMO转化率达到99%,EG选择性达到96%,较传统蒸氨法制备的Cu/SiO2催化剂,其选择性增加了20%左右。 氧化态Cu/SiO2-HY-300催化剂表面较高的页硅酸铜含量、适宜的氧化铜还原度及相应还原态催化剂表面较高Cu+/(Cu++Cu0)物种比例,是其显示良好催化性能的主要原因。
[1] 杜周. 乙二醇加氢精制催化剂的制备与开发研究[D]. 北京: 北京化工大学, 2017 DU Zhou. Study on preparation and development of ethylene glycol hydrofining catalyst [D]. Beijing: Beijing University of Chemical Technology, 2017 (in Chinese)
[2] YANG Q, XU S, YANG Q, et al. Optimal design and exergy analysis of biomass-to-ethylene glycol process[J]. Bioresource Technology, 2020, 316: 123972
[3] ZHANG L, AI P, GAO Z, et al. Enhanced catalytic stability of Cu-based catalyst for dimethyl oxalate hydrogenation[J]. Fuel,2022, 324: 124536
[4] AI P, TAN D, ISHIKURO Y, et al. Design of an autoreduced copper in carbon nanotube catalyst to realize the precisely selective hydrogenation of dimethyl oxalate [J]. ChemCatChem,2017, 9(6): 1067-1075
[5] ZHENG X, LIN H, ZHENG J, et al. Lanthanum oxide-modified Cu/SiO2 as a high-performance catalyst for chemoselective hydrogenation of dimethyl oxalate to ethylene glycol[J]. ACS Catalysis, 2013, 3(12): 2738-2749
[6] DONG F, DING G, ZHENG H, et al. Highly dispersed Cu nanoparticles as an efficient catalyst for the synthesis of the biofuel 2-methylfuran[J]. Catalysis Science & Technology, 2016, 6(3):767-779
[7] 牛鸿宇. Cu 基催化剂在糠醛选择加氢反应机制研究[D]. 辽宁大连: 大连理工大学, 2020 NIU Hongyu. Study on selective hydrogenation reaction mechanism of Cu-based catalyst in furfural[D]. Liaoning Dalian:Dalian University of Technology, 2020 (in Chinese)
[8] SONG T, CHEN W, QI Y, et al. Efficient synthesis of methanol and ethylene glycol via the hydrogenation of CO2-derived ethylene carbonate on Cu/SiO2 catalysts with balanced Cu+-Cu0 sites[J].Catalysis Science & Technology, 2020, 10(15): 5149-5162
[9] GUO W, LI G, ZHENG Y, et al. Influence of La2 O3 addition on activity and coke formation over Ni/SiO2 for acetic acid steam reforming[J]. International Journal of Hydrogen Energy, 2022, 47(6): 3633-3643
[10] XU C, CHEN G, ZHAO Y, et al. Interfacing with silica boosts the catalysis of copper[J]. Nature Communications, 2018, 9(1): 3367
[11] 药大卫. 草酸酯加氢铜基催化剂多尺度结构设计与构效关系研究[D]. 天津: 天津大学, 2019 YAO Dawei. Multi-scale structure design and structure-activity relationship of copper-based catalyst for oxalate hydrogenation[D]. Tianjin: Tianjin University, 2019 (in Chinese)
[12] 滕兆刚. 介孔SiO2 及介孔磁性复合物的制备与性质研究[D]. 长春: 吉林大学, 2009 TENG Zhaogang. Preparation and properties of mesoporous SiO2 and mesoporous magnetic composites[D]. Changchun: Jilin University, 2009 (in Chinese)
[13] 薛婧, 武朦朦, 宋有为, 等. Ag 改性层状硅酸铜催化剂的草酸二甲酯加氢合成乙醇酸甲酯性能研究[J]. 燃料化学学报, 2022, 50(8): 1014-1022 XUE Jing, WU Mengmeng, SONG Youwei, et al. Study on performance of Ag-modified layered copper silicate catalyst for hydrogenation of dimethyl oxalate to methyl glycolate[J]. Journal of Fuel Chemistry and Technology, 2022, 50(8): 1014-1022(in Chinese)
[14] LI B, LIU J, LIU Y, et al. Copper nanoparticles confined in hollow silica spheres: Understanding the confinement effect and enhanced catalytic performance for the selective hydrogenation of dimethyl oxalate[J]. Microporous and Mesoporous Materials,2025, 386: 113490
[15] 武朦朦. Cu/SiO2 催化剂制备及其DMO 加氢性能研究[D].太原: 太原理工大学, 2021 WU Mengmeng. Preparation of Cu/SiO2 catalyst and its DMO hydrogenation performance[D]. Taiyuan: Taiyuan University of Technology, 2021 (in Chinese)
[16] TOUPANCE T, KERMAREC M, LAMBERT J F, et al. Conditions of formation of copper phyllosilicates in silica-supported copper catalysts prepared by selective adsorption[J]. The Journal of Physical Chemistry B, 2002, 106(9): 2277-2286
[17] TOUPANCE T, KERMAREC M, LOUIS C. Metal particle size in silica-supported copper catalysts. Influence of the conditions of preparation and of thermal pretreatments[J]. The Journal of Physical Chemistry B, 2000, 104(5): 965-972
[18] LIU Z, LI Z, MA Z, et al. Histidine-derivate modified Cu/SiO2 catalyst for selective hydrogenation of dimethyl oxalate to methyl glycolate[J]. Fuel, 2025, 381: 133701
[19] WANG Y, SHEN Y, ZHAO Y, et al. Insight into the balancing effect of active Cu species for hydrogenation of carbon-oxygen bonds[J]. ACS Catalysis, 2015, 5(10): 6200-6208
[20] GONG J, YUE H, ZHAO Y, et al. Synthesis of ethanol via syngas on Cu/SiO2 catalysts with balanced Cu0-Cu+sites[J]. Journal of the American Chemical Society, 2012, 134(34): 13922-13925
[21] CHEN Z, ZHANG J, ABBAS M, et al. Effect of configuration addition of precursors on structure and catalysis of Cu/SiO2 catalysts prepared by ammonia evaporation-hydrothermal method[J].Industrial & Engineering Chemistry Research, 2017, 56(33):9285-9292
[22] GONG Z, WANG H, LAN T, et al. Dehydrogenation of methyl glycolate to methyl glyoxylate over a Cu/SiO2 catalyst[J]. Applied Catalysis A: General, 2025, 697: 120219
[23] LI Y, ZHAO J, YAN A, et al. Highly selective dehydrogenation of methanol to methyl formate over copper catalysts supported on hierarchical hollow silica spherical [J].Fuel,2025,388: 134520
[24] WANG H, ZHAO W, REHMAN M U, et al. Copper phyllosilicate nanotube catalysts for the chemosynthesis of cyclohexane via hydrodeoxygenation of phenol[J]. ACS Catalysis, 2022, 12(8): 4724-4736
[25] ZHAO Y, ZHANG Y, WANG Y, et al. Structure evolution of mesoporous silica supported copper catalyst for dimethyl oxalate hydrogenation[J]. Applied Catalysis A: General, 2017, 539:59-69
[26] ZHANG P, HUANG L, YANG J, et al. The regulation of surface copper species coupled with ammonia-evaporation and hydrothermal aging process to enhance catalytic hydrogenation properties of Cu-SiO2 catalysts[J]. Catalysis Letters, 2024, 154(3):1007-1017
[27] HUANG H, WANG B, WANG Y, et al. Partial hydrogenation of dimethyl oxalate on Cu/SiO2 catalyst modified by sodium silicate[J]. Catalysis Today, 2020, 358: 68-73
[28] JIMÉNEZ-GÓMEZ C P, CECILIA J A, ALBA-RUBIO A C, et al. Tailoring the selectivity of Cu-based catalysts in the furfural hydrogenation reaction: Influence of the morphology of the silica support[J]. Fuel, 2022, 319: 123827