恶性肿瘤的存在对人类的生命、健康和安全造成了巨大的威胁。根据世界卫生组织的全球癌症报告,肺癌和乳腺癌严重威胁着人类的生命和健康,结肠癌、胃癌和肝癌的患病概率也在逐年提升,预计到2040 年,癌症负担将增加50%,新发癌症病例也将接近3 000 万[1-3]。现阶段,通过放疗、药物治疗、手术治疗和局部治疗等手段,肿瘤患者的生活质量得到了一定的保障,但是现今治疗手段仍不理想,一些常用的治疗方式,如使用化疗药物阿霉素、顺铂甚至是放疗,都会给患者带来严重的不良反应,产生一系列毒副作用[4-6]。
高分子聚合物在肿瘤治疗领域具有较高的应用价值,聚合物纳米颗粒因其可以良好地保护负载药物,克服治疗过程中的生物学障碍受到了广泛的关注。壳聚糖(CS)是一种天然存在的可生物降解的高分子聚合物,在自然界中含量丰富。由于其良好的物理化学特性和独特的生物学特性,壳聚糖在许多行业中都有应用,包括医疗、食品、化工、化妆品、水处理、金属提取和回收、生化和生物医学工程行业,生物有机体中的CS 可以被生物酶催化解聚,降解产物为N-乙酰葡萄糖和葡萄糖胺,对人体无毒,降解中间体不会在体内积聚,也没有免疫原性[6-8]。羧甲基壳聚糖(CMCS)是一种水溶性壳聚糖衍生物,通过在CS 结构中引入羧甲基使其具有比CS 更好的生物相容性,并且不改变CS 原有的良好特性。此外,CMCS 易于制成纳米颗粒,在Ca2+、Al3+等离子的作用下可以形成纳米粒子(NPs),现已有CaCO3/CMCS 杂化纳米微球在肿瘤纳米药物递送的应用[5]。CMCS 在药物递送、生物成像和基因治疗等方面具有广阔的应用前景。
目前聚合物/金属复合纳米材料受到了广泛关注,利用金属氧化物可以有效改性高分子聚合物,使其展现出与原材料不同的机械强度和溶胀性能等特性[9]。在生物医学领域MgO NPs 和ZnO NPs 因其具有出色的稳定性、无毒、高表面反应性和良好的生物相容性有较高的应用价值,因此掺杂这2 种NPs 改性的聚合物分子也在纳米药物递送领域有着广泛的应用[10,11]。叶酸(FA)也被称为维生素B9,是基本生物学功能所必需的B 族维生素,在DNA 和RNA 合成、细胞分裂和生长以及造血过程中有着重要作用[12],叶酸受体的过表达也是恶性肿瘤的标志,过表达的叶酸受体也常用作抗肿瘤纳米药物的靶点,FA 可以与叶酸受体结合,使叶酸结合物在内化作用下进入肿瘤细胞,且叶酸结合物并不会改变FA 与其受体的结合能力[13-15],因此在肿瘤治疗领域FA 常被用作纳米药物的靶向分子。本工作设计了一种新型pH 值响应型纳米材料,CM/FCB NPs 本身不负载任何抗癌药物,通过自组装的方式将叶酸偶联壳聚糖(FC)和氟硼荧(BODIPY)包覆在CM NPs 外制成CM/FCB NPs,并利用荧光分子BODIPY 示踪。
本研究制备的CM/FCB NPs 以肿瘤细胞中的溶酶体为作用目标,在被肿瘤细胞溶酶体摄入后,CM/FCB NPs 会在溶酶体酸性环境中触发溶胀使自身体积迅速膨胀,并触发质子海绵效应,破坏溶酶体膜,将其中水解酶释放至细胞质中,触发肿瘤细胞线粒体凋亡途径的激活,从而导致细胞死亡[16-18],达到抗肿瘤目的。本研究对其进行了研究与表征。
1 实验部分
1.1 实验原料
羧甲基壳聚糖,壳聚糖(Mw:50 ku),上海麦克林生化科技有限公司;无水氯化钙,叶酸,N-羟基琥珀酰亚胺,1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐,氢氧化钠,上海阿拉丁生化科技股份有限公司;纳米氧化镁(20 nm),先锋纳米材料科技有限公司;吐温80,天津市科密欧化学试剂有限公司;冰乙酸,二甲基亚砜,无水乙醇,PBS 缓冲液,二氯甲烷,天津市江天化工技术有份有限公司。
1.2 实验设备
傅里叶变换红外光谱仪,Nicolet 6700,美国热电公司;纳米粒度及Zeta 电位仪,Nano ZS,马尔文仪器有限公司;紫外可见分光光度计,UV-1800,日本岛津公司;荧光分光光度计,F-2500,日本Hitchi公司;真空冷冻干燥机,LGJ-10N,北京亚星仪科科技发展有限公司;场发射扫描电子显微镜,Apreo S LoVac,美国FEI;超声波细胞粉碎机,11-0634,宁波Scientz 生物科技有限公司。
1.3 材料制备
1.3.1 叶酸活性酯的合成
首先合成了叶酸活性酯,具体步骤如下:量取三乙胺(TEA,2.8 mL)和无水二甲基亚砜(DMSO,38.5 mL)置于250 mL 三口烧瓶中充分混合,称取叶酸(FA,1.950 g)加入三口烧瓶于25 ℃避光的条件下以500 r·min-1的转速机械搅拌2 h 至FA 充分溶解,称取N-羟基琥珀酰亚胺(NHS,0.800 g)加入三口烧瓶搅拌至溶解,再称取1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDCl,1.330 g)加入其中,继续避光机械搅拌48 h,量筒量取丙酮(18 mL)和无水乙醚(42.0 mL)在0 ℃冰水浴条件下充分混匀,用滴管将混合溶液逐滴加入正在反应的三口烧瓶中,溶液颜色逐渐加深,滴至不再生成棕色沉淀,停止搅拌,在0 ℃冰水浴条件下避光冷却2 h,以12 000 r·min-1的转速离心15 min 去除上清液中的杂质,用去离子水反复洗涤固体沉淀并离心3 次,避光冷冻干燥48 h,得到棕黄色胶状固体,避光保存[19]。
1.3.2 叶酸偶联壳聚糖(FC)的合成
叶酸偶联壳聚糖(FC)的合成具体操作步骤如下:称取叶酸活性酯(0.500 g)加入DMSO(5.0 mL)磁力搅拌2 h 至固体充分溶解成棕色溶液,超声10 min 备用。称取壳聚糖(CS,1.000 g)置于500 mL三口烧瓶中,配制浓度1%的冰醋酸(200.0 mL)滴管逐滴加入三口烧瓶中,机械搅拌4 h 至CS 充分溶解,配制氢氧化钠溶液(0.5 mol·L-1,60.0 mL),滴管逐滴加入三口烧瓶直至pH 试纸显示溶液pH 值5.0~6.0,快速加入充分溶解后的叶酸活性酯溶液,控制温度不超过45 ℃条件下500 r·min-1避光机械搅拌充分反应60 h,逐滴滴加NaOH 溶液(0.5 mol·mL-1)至pH 试纸显示溶液pH 值为8.0~9.0,以12 000 r·min-1的转速离心15 min,去除上清液并用去离子水重复洗涤3 遍,避光条件下在PBS 缓冲液(pH 值为7.4)透析72 h,再置于去离子水中透析72 h,冷冻干燥固体沉淀,得到浅黄色片状FC,避光保存。
1.3.3 CMCS NPs 和CM NPs 的制备
CMCS NPs 和CM NPs 的具体制备过程如下:采用离子交联法制备CM NPs,称取羧甲基壳聚糖(CMCS,20.0 mg)加入去离子水中(20.0 mL)磁力搅拌1 h 至完全溶解备用。称取纳米氧化镁(MgO NPs,5.0 mg)溶于去离子水(500 μL)中磁力搅拌10 min 再超声分散10 min 成白色溶液,在磁力搅拌的条件下,将MgO 溶液用滴管逐滴缓慢滴加至CMCS 溶液中,按顺序滴加丙酮(500 μL)和吐温80(0.5 mL)使其均匀分散,磁力搅拌1 h 后,使用超声细胞粉碎仪(功率35%)超声粉碎20 min。称取无水氯化钙(CaCl2,4.0 mg)溶于去离子水(4.0 mL)中,室温磁力搅拌条件下,滴管逐滴滴入上述乳白色溶液中,继续搅拌1.5 h,静置15 min 后离心(11 000 r·min-1,10 min),去离子水反复洗涤3 遍,冷冻真空干燥(24 h)得到白色CM NPs,并以相同方法制备CMCS NPs。
1.3.4 CM/FCB NPs 的制备
采用浸渍法制备CM/FCB NPs 的过程如下:称取FC(40.0 mg)加入3%的HAc 溶液(5.0 mL)中避光磁力搅拌2 h 至充分溶解,再超声10 min 得到橘黄色透明溶液备用,参照文献中方法[20]制备BODIPY,称取BODIPY(1.0 mg)溶于丙酮(500 μL)中,滴管逐滴加入至上述溶液中搅拌混匀。称取CM NPs(16.0 mg)加入去离子水(8.0 mL),使用超声细胞粉碎仪(功率45%)超声粉碎20 min 得到乳白色液体,滴管逐滴加入至FC 溶液中,在避光条件下涡旋混匀1 h,静置3 h 后离心(12 000 r·min-1,15 min),用去离子水反复洗涤3 遍,真空冷冻干燥24 h 得到棕黄色CM/FCB NPs。
1.4 材料表征
1.4.1 CM/FCB NPs 的透射电镜和扫描电镜测试
透射电镜(TEM)和扫描电镜(SEM)分别观察CMCS NPs、CM NPs 和CM/FCB NPs 的外观形貌。
1.4.2 CM/FCB NPs 的红外光谱测试
分别称取适量的CM NPs、CMCS NPs、FA、FC、CS 和MgO NPs,在白炽灯充分干燥后,与适量KBr粉末共同研磨,分别经过压片处理后进行红外光谱测试。
1.4.3 CM/FCB NPs 的纳米粒度和Zeta 电位测试
分别称量1 mg 的CM/FCB NPs、CM NPs 和CMCS NPs 加入15 mL 不 同pH 值的PBS 缓 冲液(pH 值为7.4、6.5 和4.5)中,使用超声细胞粉碎仪(功率30%)超声粉碎20 min 使NPs 充分分散均匀备用,将样品分别滴入塑料皿和Zeta 电位样品池,在3 种不同pH 值下分别测定3 种纳米粒子的纳米粒度和Zeta 电位值。
1.4.4 紫外可见吸收光谱和荧光发射光谱测试
分别称取适量CM/FCB NPs 和BODIPY 溶于二氯甲烷中,将样品滴入玻璃比色皿中,分别测定紫外-可吸收光谱(波长250 ~650 nm),将紫外-可吸收光谱的最大吸收波长作为荧光发射光谱的激发波长,并再次将二氯甲烷溶液分别滴入玻璃比色皿中,进行荧光发射光谱测试。
1.4.5 CM/FCB NPs 的生物性能评价
使用MTT 比色法检测了2.5、5.0、10.0、20.0、40.0、60.0、80.0、100.0 μg·mL-1 浓 度 下CM/FCB NPs、CM NPs、CMCS NPs、MgO NPs、BODIPY 以及FC 对Hela 肿瘤细胞的毒性。
采用激光共聚焦显微镜对CM/FCB NPs 的摄取情况进行了分析。
2 结果与讨论
2.1 红外光谱分析
如图2 所示,观察叶酸的红外光谱,其中3 546 cm-1 的吸收峰为FA 中羟基(—OH)的吸收峰,3 413 和3 324 cm-1 处的吸收峰为FA 中氨基(—NH2)与N—H 的伸缩振动所产生的,羧基中的![]() 的伸缩振动在1 695 cm-1 处产生强吸收峰。
的伸缩振动在1 695 cm-1 处产生强吸收峰。
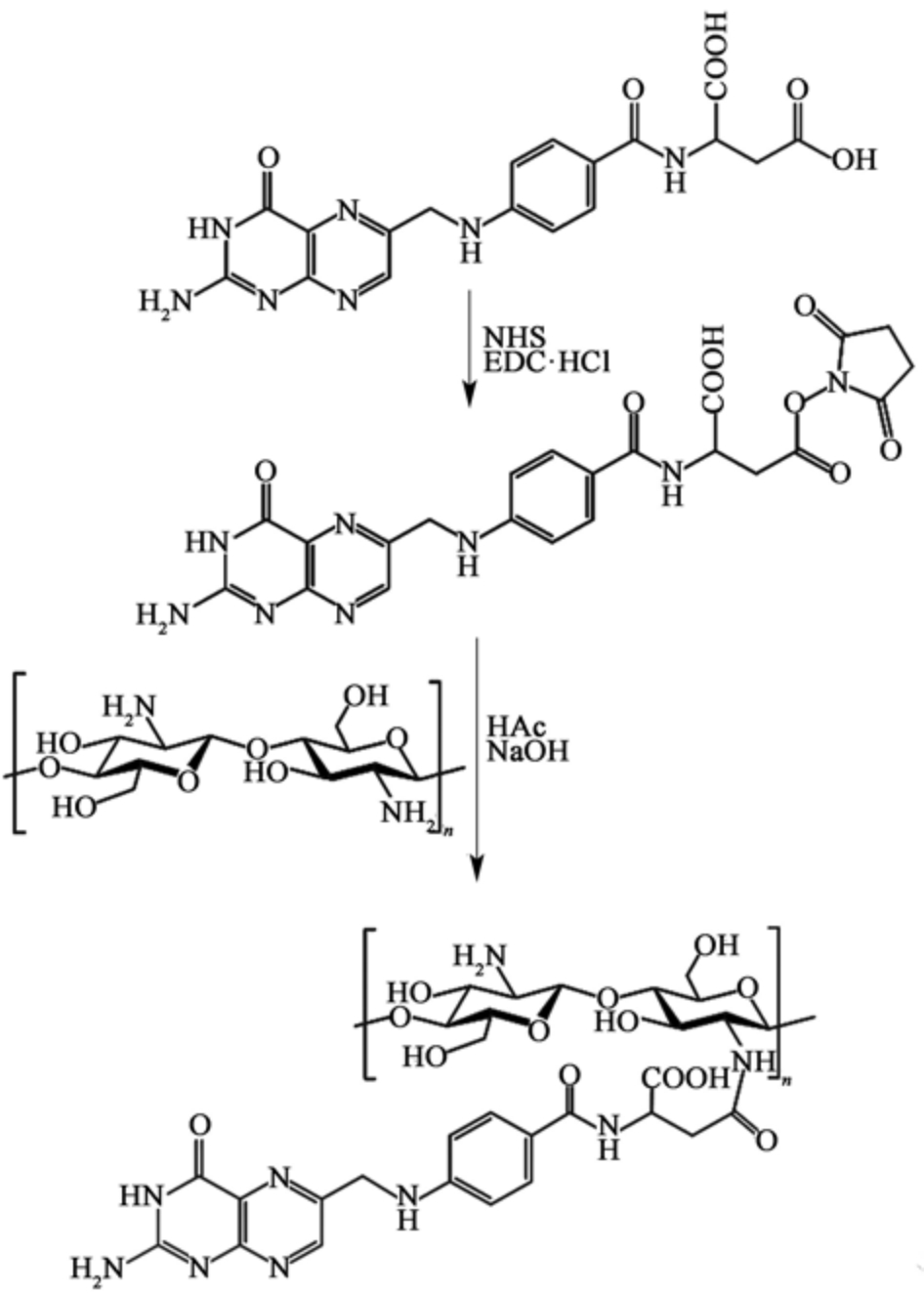
图1 FC 的合成
Fig.1 The synthesis of FC
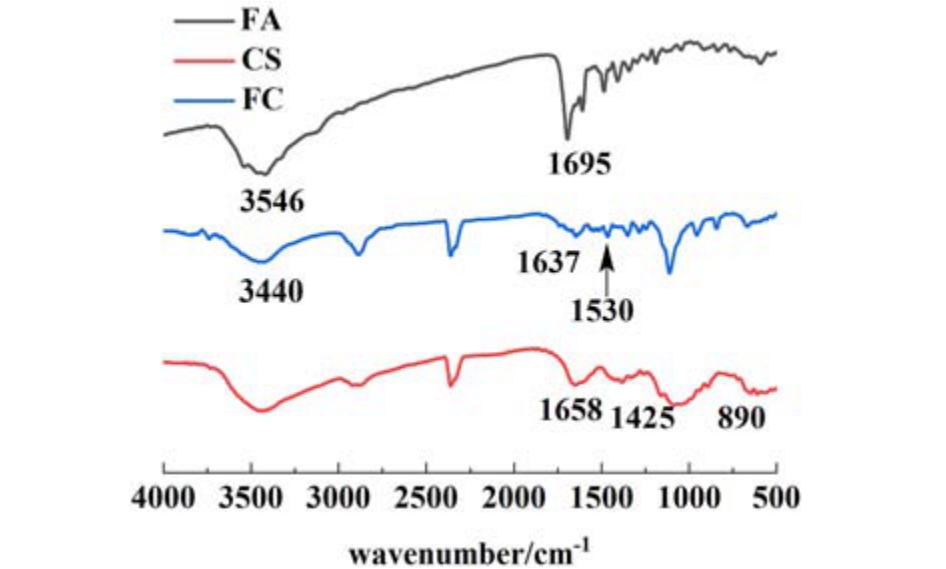
图2 FA、CS 和FC 的红外吸收光谱
Fig.2 FTIR spectra of FA, CS and FC
壳聚糖红外光谱中,由于形成氢键缔合的O—H的伸缩振动与N—H 的伸缩振动的重叠,使得在3 440 cm-1 处形成增宽的吸收峰,在2 869 ~2 919 cm-1处C—H 的伸缩振动形成了宽吸收峰,在1 658 cm-1处为仲酰胺的羰基伸缩振动(酰胺I 带)的吸收峰,1 425 cm-1 处吸收峰为![]() 弯曲振动和—CH3 变形振动引起的。
弯曲振动和—CH3 变形振动引起的。
在叶酸偶联壳聚糖的红外光谱中,由于CS的—NH2 基团与FA 中—COOH 基团发生静电自组装,在3 440 cm-1 处仅形成了1 个仲酰胺吸收峰,由于CS 上—NH2 基团被FA 取代,在1 658 和1 596 cm-1处吸收峰明显减弱,在1 637 cm-1 处出现吸收峰,由于FC 中形成新的—CO—NH—键,在1 530 cm-1 处形成新吸收峰。通过进一步对比标准红外谱图,确定合成化合物为FC。
如图3 所示,在羧甲基壳聚糖的红外光谱中,由于—COOH 基团的不对称伸缩振动,在1 641 cm-1处出现吸收峰,1 066 cm-1 处的吸收峰为伯醇所生成的 醚 键(—O—) 伸 缩 振 动 产 生 的,2 908 和1 324 cm-1 处分别为C—H 键伸缩振动和弯曲振动的吸收峰,3 457 cm-1 处宽吸收峰为O—H 与N—H伸缩振动叠加产生。
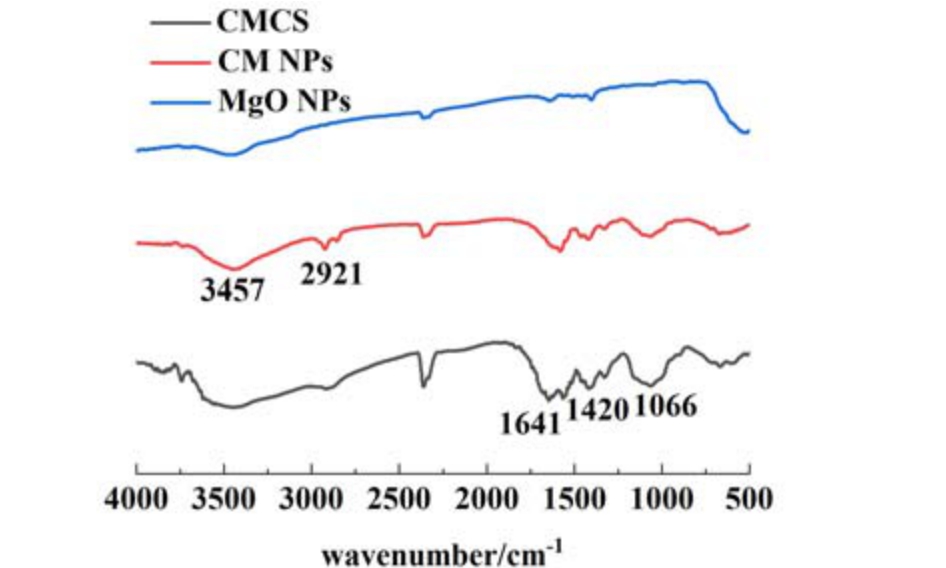
图3 MgO NPs、CMCS 和CM NPs 的红外吸收光谱
Fig.3 FTIR spectra of MgO NPs, CMCS and CM NPs
在CM NPs 的红外光谱中,由于Ca2+与CMCS离子交联作用,3 457 cm-1 处吸收峰强度变低、宽度变窄,由于在Ca2+与去质子化的—COOH 基团产生离子键,1 641 cm-1 处吸收峰强度降低,C—H 键在2 921 cm-1 处由于MgO NPs 的掺杂峰强明显增大,这也表明CM NPs 被成功制备。
如图4 所示,通过对比 CM/FC NPs 与FC、CM NPs 的红外光谱,可以发现FC 中1 530 cm-1 和1 637 cm-1 处特征吸收峰在CM/FC NPs 谱图中显现,CM/FCB NPs 中2 921 和3 457 cm-1 处吸收峰与CM NPs 相近,由于FC 外壳与CM NPs 核之间通过静电作用自组装结合,3 457 与1 637 cm-1 处吸收峰强度进一步降低。因此,通过结构表征可以确定制备CM/FC NPs。
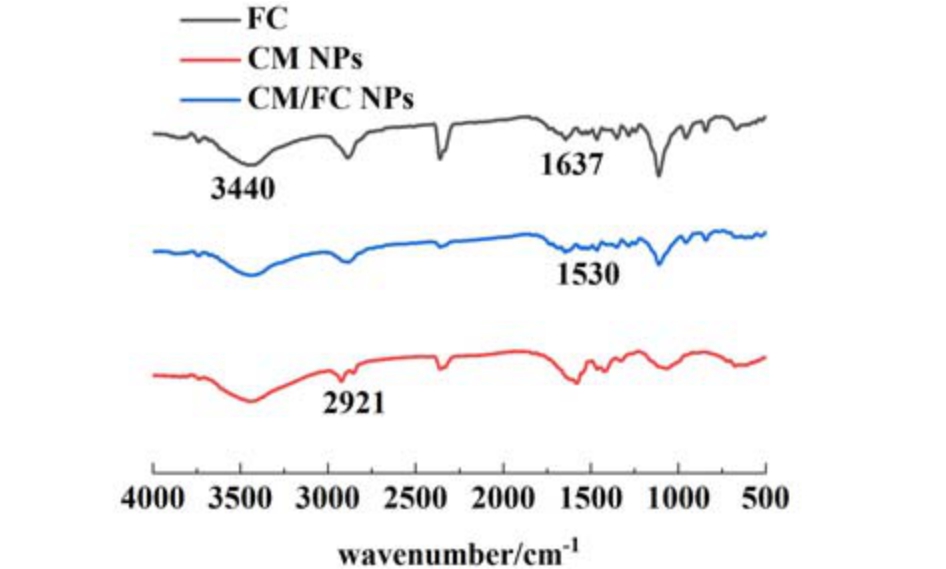
图4 CM/FC NPs、FC 和CM NPs 的红外吸收光谱
Fig.4 FTIR spectra of CM/FC NPs, FC and CM NPs
2.2 CM/FCB NPs 的形貌表征
如图5 所示,TEM 图中3 种NPs 都大致呈现球形,形貌较为接近,且粒径都在200 ~400 nm 之间,由于CM/FCB NPs 的核-壳结构,图5(c)中TEM图中外侧存在圆形阴影。

图5 (a) CMCS NPs; (b) CM NPs 和(c) CM/FCB NPs 的TEM 图
Fig.5 TEM images of (a) CMCS NPs; (b) CM NPs and (c) CM/FCB NPs
如图6 所示,CMCS NPs、CM NPs 和CM/FCB NPs 都是球型纳米粒子,其中且3 种NPs 都具有凹凸不平的粗糙表面,图6 中3 组NPs 的粒径分别为287.4、301.8 和315.4 nm。通过对比发现,图6(c)中CM/FCB NPs 的表面褶皱更为明显,其原因可能是由于核-壳结构的CM/FCB NPs 在制备过程中由于真空冷冻干燥后,使其中核-壳结构中冷冻水从纳米复合珠中迅速升华,聚合物网络部分塌陷所导致的。而图6(b)中,CM NPs 的表面相对光滑紧密,其原因可能因为MgO NPs 的掺杂使得CMCS 链和MgO NPs 之间产生界面相互作用,MgO NPs 可以收缩并阻碍CMCS 链的可移动性,进而改变表面形貌,使其表面相对光滑。

图6 (a) CMCS NPs; (b) CM NPs 和(c) CM/FCB NPs 的SEM 图
Fig.6 SEM image of (a) CMCS NPs; (b) CM NPs and (c) CM/FCB NPs
2.3 CM/FCB NPs 的溶胀性能分析
为了分析CM/FCB NPs 的溶胀性能以及稳定性,通过测定不同pH 值环境下,3 种NPs 的粒径、Zeta 电位进行表征。利用PBS 缓冲液模拟正常血管条件下(pH 值为7.4)、肿瘤微环境条件下(pH 值为6.5)和肿瘤细胞溶酶体内条件下(pH 值为4.5)的不同环境,3 种NPs 在不同环境中的粒径如表1所示,其中3 种NPs 在正常条件下的平均粒径均在300 ~360 nm 之间,与TEM 和SEM 图中所显示的一致,均符合可以被细胞内化的条件。随着pH 值从7.4 降至4.5,CMCS NPs 的平均粒径从359.8 增大至519.5 nm,由于CMCS 链上的—NH2 在酸性环境中不断解离为—![]() ,—
,—![]() 与—COOH 的静电排斥作用使得CMCS NPs 的体积增大、孔隙率提高,从而使H2O 渗透至NPs 中,使得CMCS NPs 的粒径随pH 值不断增大。通过掺杂MgO NPs,CM NPs 的溶胀能力进一步得到提升,其平均粒径从中性条件下的324.7 nm 溶胀至pH 值为4.5 条件下的796.3 nm,带电的MgO NPs 导致更多H2O 的渗透,以中和积聚的离子渗透压,从而使NPs 溶胀性能提升,同时MgO NPs 的掺杂会影响Ca2+与CMCS 链间的作用,使其交联程度降低、孔隙率增大,因而CM NPs 的溶胀性能得到提升。核-壳结构的CM/FCB NPs 显示出极佳的溶胀性能,当pH 值从7.4 降至4.5 时,CM/FCB NPs 的粒径从329.6 增大至1 254.0 nm,扩大了近4 倍,其良好的溶胀性能不仅依赖于其核中CM NPs 结构自身的溶胀能力,同时也因为外壳FC 中在酸性环境中不断解离的—
与—COOH 的静电排斥作用使得CMCS NPs 的体积增大、孔隙率提高,从而使H2O 渗透至NPs 中,使得CMCS NPs 的粒径随pH 值不断增大。通过掺杂MgO NPs,CM NPs 的溶胀能力进一步得到提升,其平均粒径从中性条件下的324.7 nm 溶胀至pH 值为4.5 条件下的796.3 nm,带电的MgO NPs 导致更多H2O 的渗透,以中和积聚的离子渗透压,从而使NPs 溶胀性能提升,同时MgO NPs 的掺杂会影响Ca2+与CMCS 链间的作用,使其交联程度降低、孔隙率增大,因而CM NPs 的溶胀性能得到提升。核-壳结构的CM/FCB NPs 显示出极佳的溶胀性能,当pH 值从7.4 降至4.5 时,CM/FCB NPs 的粒径从329.6 增大至1 254.0 nm,扩大了近4 倍,其良好的溶胀性能不仅依赖于其核中CM NPs 结构自身的溶胀能力,同时也因为外壳FC 中在酸性环境中不断解离的—![]() 与核中—COOH 产生的静电排斥,使得大量H2O 进入NPs核-壳间,因此,CM/FCB NPs 具有出色的溶胀性能。
与核中—COOH 产生的静电排斥,使得大量H2O 进入NPs核-壳间,因此,CM/FCB NPs 具有出色的溶胀性能。
表1 在不同pH 值(7.4、6.5 和4.5)条件下,CMCS NPs、CM NPs 和CM/FCB NPs 的粒径变化
Table 1 Size changes of CMCS NPs, CM NPs and CM/FCB NPs at different pH (7.4, 6.5, 4.5)
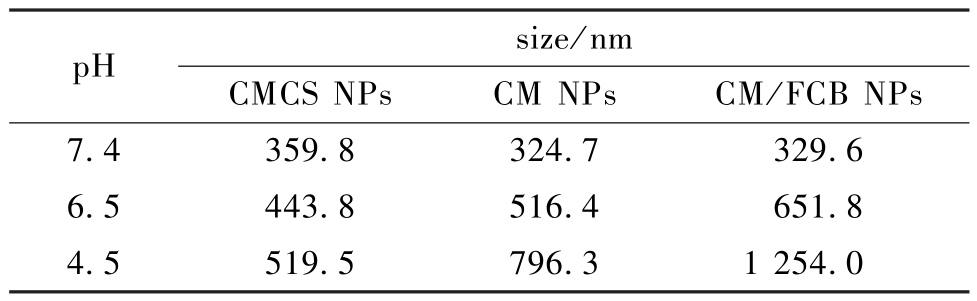
pH size/nm CMCS NPs CM NPs CM/FCB NPs 7.4 359.8 324.7 329.6 6.5 443.8 516.4 651.8 4.5 519.5 796.3 1 254.0
通过分析NPs 的Zeta 电位判断NPs 的稳定性,如表2 所示,在中性环境下,3 种NPs 的Zeta 电位绝对值均大于20 mV,这表明3 种NPs 均具有良好的稳定性。随pH 值降低CMCS NPs 的电位均随之上升,这是因为CMCS 链上电离出的—COO-在酸性环境中不断转变为—COOH,使其电位不断上升。由于引入带正电的MgO NPs,CM NPs 的电位较CMCS NPs 进一步上升。CM/FCB NPs 由于其核-壳间静电斥力随pH 值降低而不断增大,导致其电位随pH值降低上升得更为明显。
表2 在不同pH 值(7.4、6.5 和4.5)条件下,CMCS NPs、CM NPs 和CM/FCB NPs 的Zeta 电位变化
Table 2 Changes in the Zeta potential of CMCS NPs,CM NPs and CM/FCB NPs at different pH (7.4,6.5,4.5)
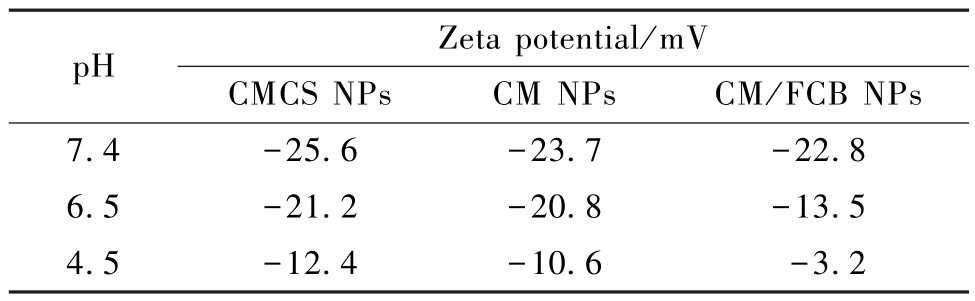
pH Zeta potential/mV CMCS NPs CM NPs CM/FCB NPs 7.4 -25.6 -23.7 -22.8 6.5 -21.2 -20.8 -13.5 4.5 -12.4-10.6 -3.2
2.4 CM/FCB NPs 的紫外光谱和荧光光谱分析
BODIPY 染料作为光敏介质因其良好的生物相容性被广泛应用于生物成像以及癌症诊断领域,本工作通过在CM/FCB NPs 中掺杂BODIPY,对NPs在细胞摄取过程和活体生物成像中进行示踪。如图7 所示,利用紫外-可见分光光度计分别检测溶于二氯甲烷的CM/FCB NPs 与BODIPY,在250 ~600 nm 范围内,二者的最大紫外吸收峰均在501 nm处出现,这表明BODIPY 被成功掺杂于NPs 中,并且本身性质并未在制备过程中受到影响。
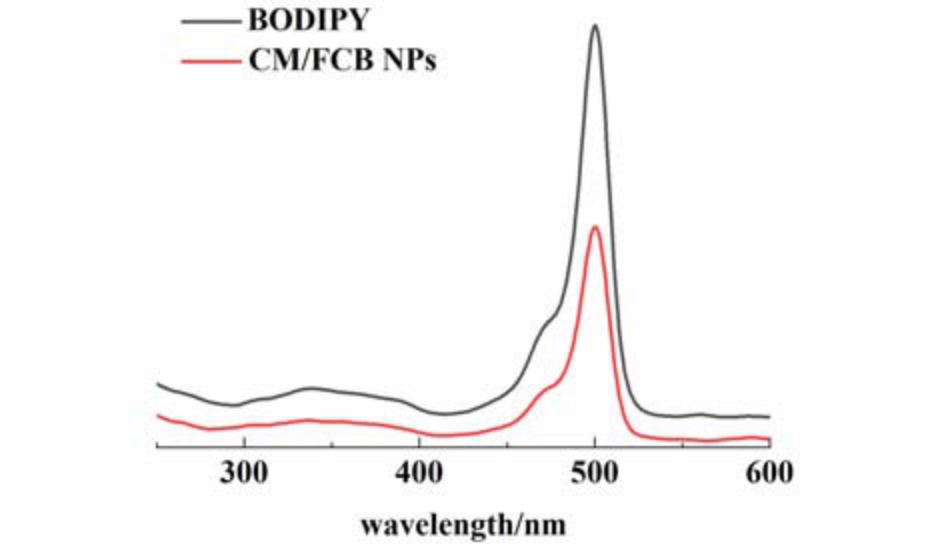
图7 BODIPY 和CM/FCB NPs 在二氯甲烷中的紫外可见吸收光谱
Fig.7 The UV-Vis absorption spectra of BODIPY and CM/FCB NPs in dichloromethane
如图8 所示,利用荧光分光光度计分别测定500 nm 至650 nm 的CM/FCB NPs 与BODIPY 的荧光发 射 光 谱, 在 激 发 电 压400 V、狭 缝 宽 度 为2.5 mm、490 nm 光源激发条件下,BODIPY 的最大荧光发射波长为523 nm,CM/FCB NPs 的最大荧光发射波长为518 nm,二者最大发射波长相差5 nm,均可在激发光作用下发出绿色荧光,进一步表明BODIPY 被成功掺杂于NPs 中并且并未改变其自身化学结构,因此BODIPY 的掺杂使CM/FCB NPs 具备在细胞和生物体内示踪的条件,可以应用于后续实验。
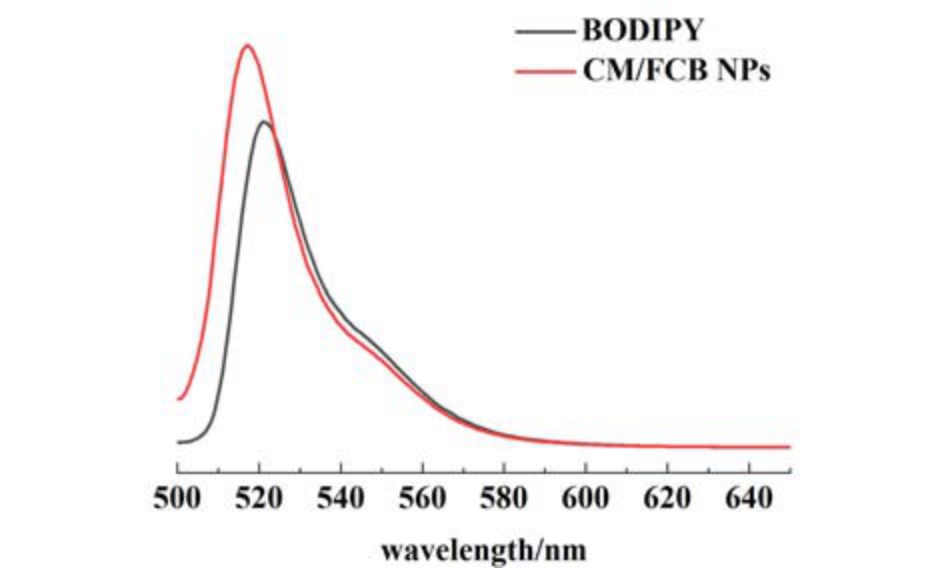
图8 BODIPY 和CM/FCB NPs 的荧光发射光谱
Fig.8 The fluorescence emission spectra of BODIPY and CM/FCB NPs
2.5 CM/FCB NPs 的生物性能分析
利用MTT 法评估CM/FCB NPs 的体外细胞毒性。首先对NPs 中各组分对肿瘤细胞的毒性进行了研究。
如图9(a)所示,随BODIPY 浓度从低到高,Hela 细胞在BODIPY 浓度小于80 μg·mL-1 时,细胞存活率均在82%以上,因此,BODIPY 对本实验几乎不产生影响。如图9(b)所示,当FC 浓度从0 ~100 μg·mL-1 逐渐升高时,Hela 细胞存活率都随浓度增大成梯度减小,当FC 浓度低于80 μg·mL-1时,细胞存活率均在80% 以上,当FC 浓度达到100 μg·mL-1时,Hela 细胞存活率分别为74.4%,实验表明FC 在较高浓度下也对肿瘤细胞表现出较低的毒性,而且CS 和FA 本身生物相容性极佳且容易代谢,因此FC 自身毒性并不会对CM/FCB NPs 的细胞毒性产生较大影响。如图9(c)所示,CMCS NPs 对Hela 细胞存活率在87%以上,CMCS NPs 在pH 值为4.5 时平均粒径为519.5 nm,随pH 值下降并未产生剧烈溶胀,同时CMCS 自身生物相容性极佳,Ca 元素作为人体必需元素,在调节细胞功能中发挥了重要作用,参与人体新陈代谢,不会对组织器官造成伤害,因此CMCS NPs 对肿瘤细胞基本不会造成伤害。如图9(d)所示,CM NPs 随浓度增加对2 种肿瘤细胞的毒性成梯度增大,当CM NPs 浓度达到100 μg·mL-1 时,Hela 细胞存活率下降至41.1%,CM NPs 随pH 值下降至4.5 时,平均粒径可增大至796.3 nm,粒径增大至原先2 倍以上,因此,通过实验表明NPs 随pH 值下降触发自身溶胀可以对肿瘤细胞产生伤害,CM NPs 也通过该机制获得了杀灭肿瘤细胞的能力。
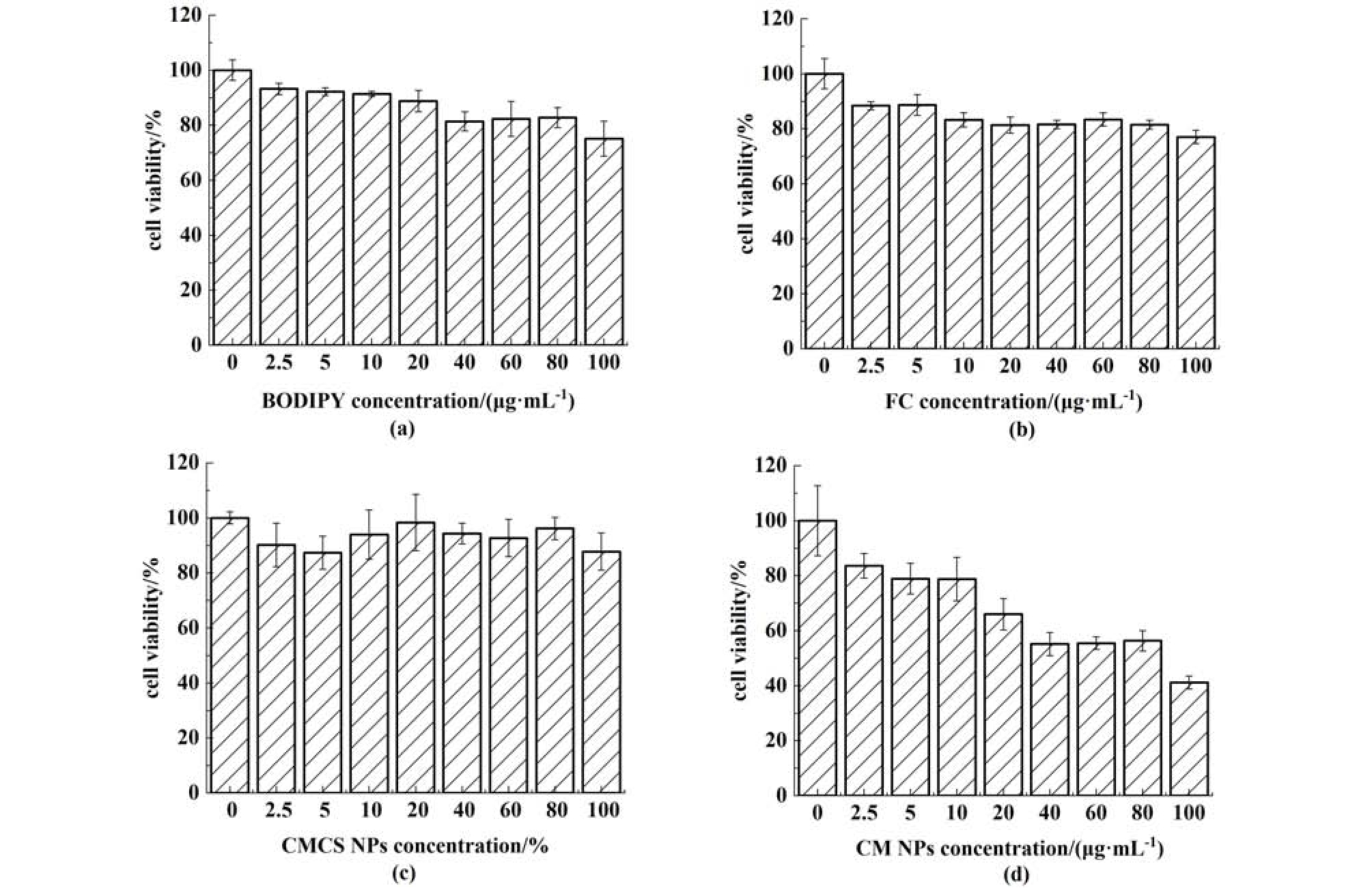
图9 (a)BODIPY; (b)FC; (c)CMCS NPs 和(d)CM/FCB NPs 的Hela 细胞存活率
Fig.9 Viabilities of cancer cell lines (Hela) incubated with (a) BODIPY; (b) FC; (c)CMCS NPs and (d)CM NPs
进一步探究CM/FCB NPs 对肿瘤细胞的杀伤效果,如图10 所示,CM/FCB NPs 对Hela 细胞的毒性随给药浓度成线性梯度增加,且抗肿瘤效果明显,当NPs 浓度为80 μg·mL-1 时,Hela 细胞存活率已降至21.3%,当浓度达到100 μg·mL-1时,Hela 细胞存活率降至17.2%,CM/FCB NPs 在pH 值为 4.5的条件下粒径增大至1 254.0 nm,粒径较中性条件下增大了4 倍,NPs 良好的溶胀性能使其具有了优异的抗肿瘤能力。
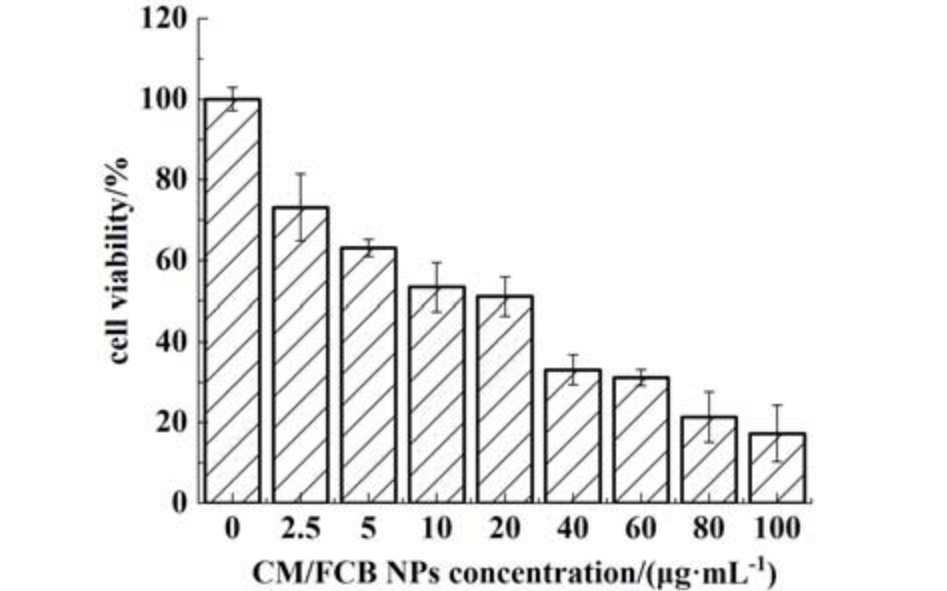
图10 CM/FCB NPs 的Hela 细胞存活率
Fig.10 Viabilities of cancer cell lines (Hela)incubated with CM/FCB NPs
为了成功发挥治疗作用,纳米粒子必须先被目标细胞摄取,因此内化机制对纳米粒子非常重要,大部分纳米粒子主要通过受体介导的胞吞作用被细胞摄取,通过修饰配体以增加细胞靶向性也会明显增大细胞内化纳米颗粒的效率[14]。CM/FCB NPs的平均粒径为329.6 nm,并且在NPs 表面修饰了肿瘤特异性叶酸靶向,因此NPs 满足肿瘤细胞的内化条件,为了进一步探究NPs 的肿瘤细胞摄取情况,利用激光扫描共聚焦显微镜在NPs 分别与Hela 细胞共孵育2、4 和6 h 后进行了对比分析。
DAPI 的发射波长为400 nm,染核后在激发光作用下可产生蓝色荧光;CM/FCB NPs 的发射波长为519 nm,可在激光作用下产生绿色荧光。如图11所示,随孵育时间增加,CM/FCB NPs 在Hela 细胞中的荧光信号显著增强,在2 h 时绿色荧光并未完全与蓝色荧光重合,大部分包裹在蓝色荧光的表面,并且绿色荧光较弱,而蓝色荧光较明显,这表明Hela 细胞正处于内化CM/FCB NPs 的初级阶段,在4 h 时,绿色荧光已经与蓝色荧光基本完全重合,这表明此时NPs 已经成功被Hela 细胞内化,而在6 h时的绿色荧光强度比4 h 时更强,证明随着时间增加,Hela 细胞对NPs 的内化作用不断增大,细胞内的NPs 浓度不断上涨。
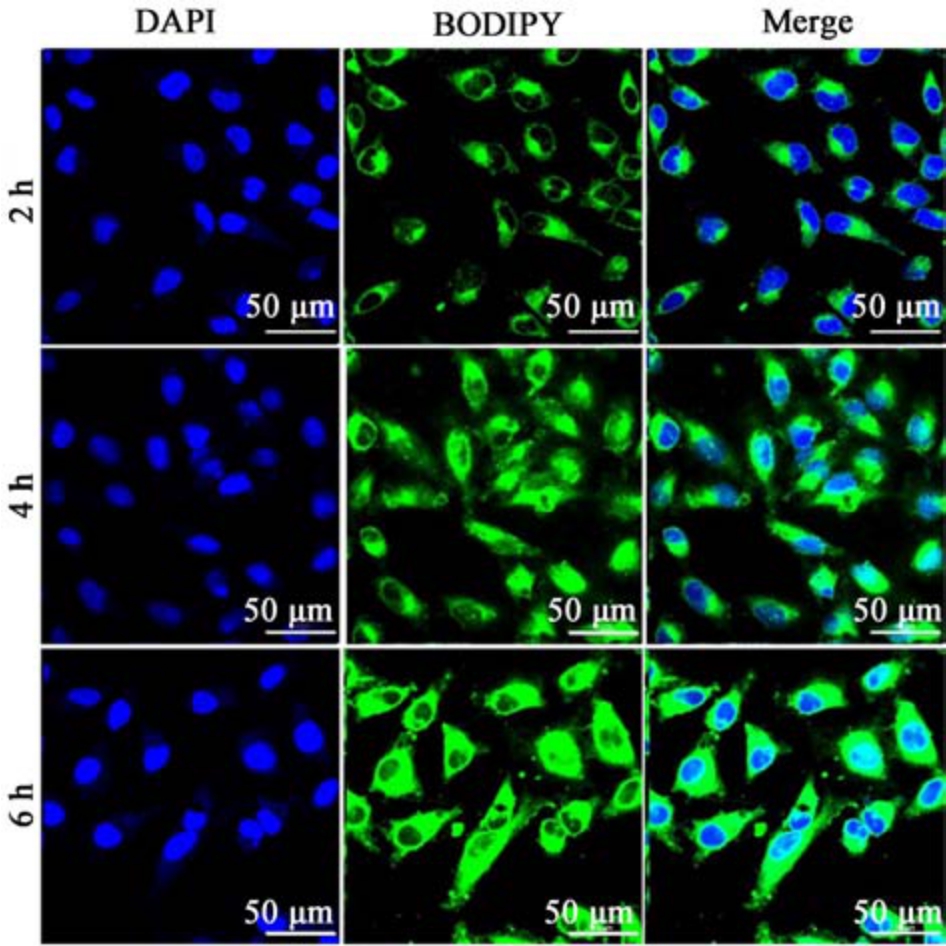
图11 分别给药2、4 和6 h 后,CM/FCB NPs 在Hela细胞中的细胞摄取荧光图片
Fig.11 Cellular uptake of CM/FCB NPs on Hela cells after incubation for 2, 4 and 6 h, as displayed in fluorescence microscopy images
CM/FCB NPs 主要作用于肿瘤细胞溶酶体,通过在酸性条件下剧烈溶胀触发溶酶体膜破裂,使其中的组织蛋白酶释放至细胞质中,从而诱导肿瘤细胞的凋亡。其中组织蛋白酶是溶酶体中一种高活性蛋白酶,研究表明,组织蛋白酶参与细胞凋亡的内部线粒体途径的激活,通过破坏溶酶体膜的稳定性,可以导致组织蛋白酶D 在细胞质中释放,组织蛋白酶D 可以触发细胞凋亡线粒体途径的激活,凋亡途径的激活将导致细胞死亡,从而抑制肿瘤生长,除组织蛋白酶D 外,组织蛋白酶B 和L 也可在细胞质的中性pH 值下发挥作用,诱导内在凋亡途径的激活[16]。为了进一步证明CM/FCB NPs 在肿瘤细胞溶酶体中的作用情况,利用激光扫描共聚焦显微镜对肿瘤细胞溶酶体定位分析。Lyso-Tracker Red 的最大激发波长为577 nm,最大发射波长为590 nm,在激发光下可产生红色荧光。如图12 所示,当Hela 细胞与NPs 共孵育2 h 时,绿色荧光与红色荧光分离度较高,只有较少的绿色荧光与红色荧光重合,表明2 h 时进入Hela 细胞溶酶体的NPs较少,Hela 细胞的摄取实验结果一致。当共孵育4 h 后,红色荧光已基本与绿色荧光完全重合,这表明在4 h 时,大部分NPs 已被成功运送至Hela 细胞溶酶体中,但此时荧光面积较低,可能因为NPs 在溶酶体中还未发生剧烈溶胀。当共孵育9 h 后,红、绿色荧光呈现高度重合,并且红色荧光面积明显增大且呈不规则形状,而绿色荧光表现出极高的荧光强度且面积显著增大,并与红色荧光的不规则形状高度一致,这表明NPs 在9 h 时成功在Hela 细胞溶酶体中发生剧烈溶胀,并使溶酶体体积膨胀,荧光的不规则形状显示Hela 细胞的溶酶体膜可能已经被NPs 破坏。
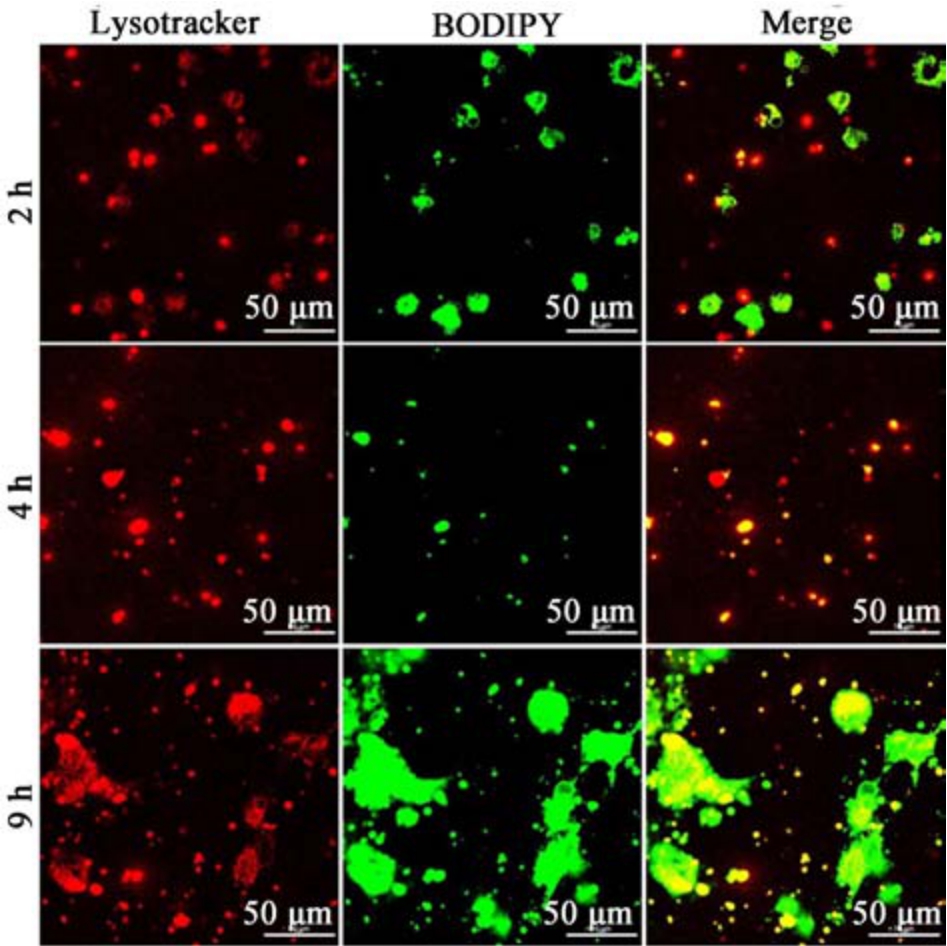
图12 CM/FCB NPs 在Hela 细胞溶酶体中的定位
Fig.12 Lysosomes localization of CM/FCB NPs on Hela cells
3 结论
设计并制备一种新型pH 值响应型纳米粒子CM/FCB NPs,该纳米粒子具有核-壳结构,本身没有负载抗肿瘤药物,以肿瘤细胞溶酶体为作用对象,利用溶酶体内特殊的酸性环境(pH 值为4.5),触发纳米粒子自身溶胀使其体积迅速增大,同时触发质子海绵效应,造成肿瘤细胞溶酶体膜破裂,使大量水解酶被释放至细胞质,激活细胞线粒体凋亡途径,从而导致肿瘤细胞凋亡。利用各种表征对CM/FCB NPs 的结构、形貌等进行了探究,并对其细胞和生物水平的抗肿瘤效果进行了探究。得出结论如下。
(1)CM/FCB NPs 以CM NPs 为核,以FC 为外壳,利用静电作用将其自组装为球形纳米粒子。通过红外、紫外、荧光分析了其结构、光学性质和元素组成,通过TEM 和SEM 观察其形貌结构,结果表明,CM/FCB NPs 为球型纳米颗粒,表面有褶皱,荧光发射峰在518 nm 处。
(2)通过纳米粒度和Zeta 电位测试对CM/FCB NPs 的pH 值响应型溶胀性能进行了分析,在PBS缓冲液模拟的正常血管环境下(pH 值为7.4),CM/FCB NPs 平均粒径为329.6 nm,在模拟的肿瘤细胞溶酶体环境下(pH 值为4.5),其平均粒径增长至1 254.0 nm,具有优异的溶胀性能。
(3)细胞实验结果表明,CM/FCB NPs 对Hela肿瘤细胞都有较强的细胞毒性,在100 μg·mL-1 的CM/FCB NPs 处理下,细胞存活率为17.2%。
[1] NAN Y, SU H, ZHOU B, et al.The function of natural compounds in important anticancer mechanisms[J].Frontiers in Oncology, 2023, 12: 1049888
[2] DUBE A, REYNOLDS J L, LAW W C, et al.Multimodal nanoparticles that provide immunomodulation and intracellular drug delivery for infectious diseases[J].Nanomedicine: Nanotechnology, Biology and Medicine, 2014, 10(4): 831-838
[3] XIAO Y, YU D.Tumor microenvironment as a therapeutic target in cancer [J].Pharmacology &Therapeutics,2021,221: 107753
[4] ONGNOK B, CHATTIPAKORN N, CHATTIPAKORN S C.Doxorubicin and cisplatin induced cognitive impairment: The possible mechanisms and interventions[J].Experimental Neurology, 2020, 324: 113118
[5] WANG J, CHEN J, ZONG J, et al.Calcium carbonate/carboxymethyl chitosan hybrid microspheres and nanospheres for drug delivery[J].The Journal of Physical Chemistry C, 2010, 114(44): 18940-18945
[6] ZHAO D, YU S, SUN B, et al.Biomedical applications of chitosan and its derivative nanoparticles[J].Polymers, 2018, 10(4): 462
[7] BYRNE J D, BETANCOURT T, BRANNON-PEPPAS L.Active targeting schemes for nanoparticle systems in cancer therapeutics[J].Advanced Drug Delivery Reviews, 2008, 60 ( 15):1615-1626
[8] FERNÁNDEZ M, JAVAID F, CHUDASAMA V.Advances in targeting the folate receptor in the treatment/imaging of cancers[J].Chemical Science, 2018, 9(4): 790-810
[9] SINGH S R, RAMESHWAR P, SIEGEL P.Targeting tumor microenvironment in cancer therapy[J].Cancer Letters, 2016,380(1): 203-204
[10] MICHIELS C, TELLIER C, FERON O.Cycling hypoxia: A key feature of the tumor microenvironment[J].Biochimica et Biophysica Acta (BBA)-Reviews on Cancer, 2016, 1866(1):76-86
[11] 叶君, 郭园, 熊犍.CMC/金属(金属氧化物)复合纳米材料的研究进展[J].高分子材料科学与工程, 2012, 28(12):169-172, 178 YE Jun, GUO Yuan, XIONG Qian.Progress in CMC/metal(metal oxide) nanocomposites[J].Polymer Materials Science &Engineering, 2012, 28(12): 169-172, 178(in Chinese)
[12] YOUNG O, NGO N, LIN L, et al.Folate receptor as a biomarker and therapeutic target in solid tumors[J].Current Problems in Cancer, 2023, 47(1): 100917
[13] 李书芹, 杨志勇.叶酸受体介导靶向治疗肿瘤[J].医学综述, 2008, 14(13): 2041-2043 LI Shuqin, YANG Zhiyong.Targeted therapy of tumor mediated by the folate receptor [J].Medical Recapitulate, 2008, 14(13): 2041-2043(in Chinese)
[14] LU Y, LOW P S.Folate-mediated delivery of macromolecular anticancer therapeutic agents[J].Advanced Drug Delivery Reviews, 2012, 64: 342-352
[15] YANG M, DENG J, GUO D, et al.A folate-conjugated platinum porphyrin complex as a new cancer-targeting photosensitizer for photodynamic therapy[J].Organic & Biomolecular Chemistry,2019, 17(21): 5367-5374
[16] WANG X, LI L, LI L, et al.Interplay of nanoparticle properties during endocytosis[J].Crystals, 2021, 11(7): 728
[17] GYPARAKI M T, PAPAVASSILIOU A G.Lysosome: The cell’s‘suicidal bag’ as a promising cancer target[J].Trends in Molecular Medicine, 2014, 20(5): 239-241
[18] MO R, SUN Q, XUE J, et al.Multistage pH-responsive liposomes for mitochondrial-targeted anticancer drug delivery[J].Advanced Materials, 2012, 24(27): 3659-3665
[19] 刘举慧, 赵峰, 周海玲, 等.载姜黄素/阿霉素叶酸偶联壳聚糖纳米粒的制备[J].科学技术与工程, 2018, 18(4):239-244 LIU Juhui, ZHAO Feng, ZHOU Hailing, et al.Preparation of folate modified chitosan nanoparticles loaded with curcumin and adriamycin[J].Science Technology and Engineering, 2018, 18(4): 239-244(in Chinese)
[20] MENG Y, DU Y, LIN Y, et al.A two-fold interpenetration pillar-layered metal-organic frameworks based on BODIPY for chemo-photodynamic therapy[J].Dyes and Pigments, 2021,188: 109174