面对化石能源的过度消耗以及由此引起的环境污染问题,人类须加快新能源的开发和利用。近年来,世界各国积极推进新能源战略部署,风能、太阳能和氢能等清洁能源的运用技术已逐步成熟。氢作为一种可再生能源载体,具有来源丰富、能量密度高(142 MJ·kg-1)、燃烧热值高以及零碳排放等诸多优点, 被认为是未来最理想的清洁能源之一[1-3]。
氢能产业发展主要包括高效的氢制备技术、安全可靠的氢存储与运输以及先进的氢应用技术。然而氢气体积密度小、易燃易爆等特点对其储运提出了较高要求。因此,寻求安全高效的储氢方法是实现氢能规模化、产业化发展的重要一环。目前常用的氢储存方式包括高压气态储氢、低温液态储氢和以储氢材料为媒介的固态储氢[4-7]。固态储氢因其安全性好、运输便捷和储氢密度高等优点,被认为是极具发展前景的储氢方式之一[8-10]。尽管固态储氢研究已取得了较为丰硕的成果,但其发展仍面临诸多瓶颈,需要进一步开发和优化固态储氢材料,以实现更为高效的氢存储。理想的储氢材料必须具备经济实惠、高储能密度、快速吸/放氢和循环稳定性好等特点。固态储氢材料通常可分为物理吸附储氢材料和化学吸附储氢材料2 大类[11,12]。物理吸附储氢主要依靠范德华力对氢气进行吸附,主要的储氢材料包括无机多孔材料和碳基材料等[13,14],而化学吸附储氢材料主要是通过氢原子或离子与其他元素结合形成亚稳态化合物实现氢的存储, 如金属氢化物( MgH2) 和络合氢化物(LiBH4)[15,16]。
在已报道的固态储氢材料中,镁基储氢材料凭借其高储氢密度(7.6%)、Mg 资源丰富(地壳中Mg元素占2.3%)以及相对廉价的成本而备受瞩目,成为研究最为广泛的储氢材料之一[17,18]。然而,MgH2作为储氢材料在实际应用中仍面临挑战。具体而言,纯镁在储氢过程中存在吸放氢热力学稳定(放氢焓ΔH=75 kJ·mol-1)以及动力学缓慢(放氢活化能Ea=160 kJ·mol-1)的问题,同时在吸放氢循环过程中Mg/MgH2 的颗粒团聚与长大都限制着镁基储氢材料的进一步发展[19,20]。近年来,国内外研究者从结构优化和成分调控2 方面对提升镁基储氢材料吸放氢性能进行了探索,并取得了丰硕的研究成果。
本论文基于国内外镁基储氢材料的研究现状,综合概括了合金化、纳米化、添加催化剂、薄膜化及复合化5 种改性策略(图1),分类讨论了不同策略所取得的研究进展;总结了5 种策略的优点与不足,为设计、制备具有更优性能的镁基固态储氢材料提供依据。
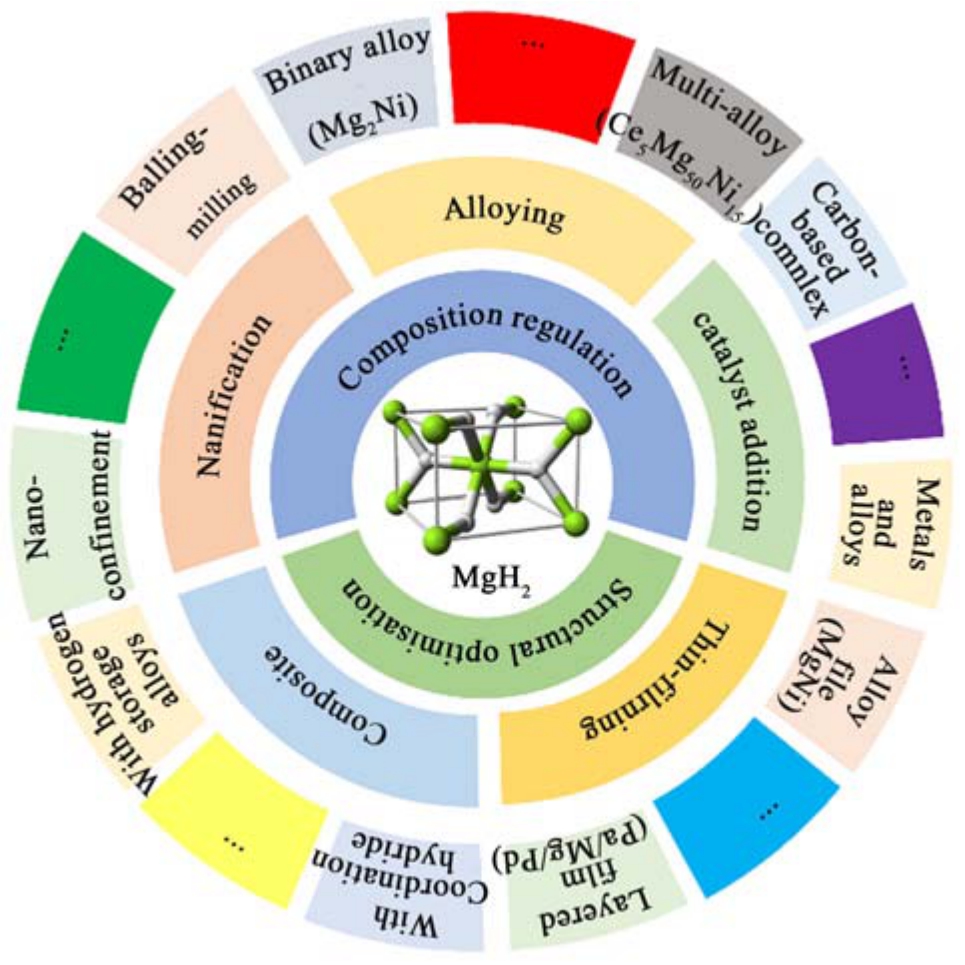
图1 镁基储氢材料性能改性方法分类
Fig.1 Modification strategies of magnesium-based materials for hydrogen storage
1 合金化
MgH2 热力学稳定性高,放氢焓达75 kJ·mol-1,而通过合金化,可显著改善镁基储氢材料的热力学性能,并对改善动力学性能起到积极影响。合金化引入的金属元素与镁和氢结合生成次稳定氢化物能削弱Mg—H 键,多相边界的生成为体系吸放氢提供更多的活性位点,可促进体系吸放氢;部分金属与镁反应生成的合金在储氢过程中发生可逆转换(如Mg2Ni/Mg2NiH4、Mg2Co/Mg2CoH5),产生“氢泵”效应,有效改善吸放氢动力学。
Mg-Ni 合金作为典型的镁基储氢体系,具备优异的吸放氢性能。早在1968 年,Reilly 等[21]首次报告了以熔炼法制备的Mg2Ni 储氢性能,结果表明Mg2Ni 可在2 MPa 氢压、250 ℃下与H2 反应生成热力学稳定性较低的Mg2NiH4。此外,进一步研究发现在吸放氢过程中Mg2Ni 与Mg2NiH4 的可逆转化,Mg2NiH4 的 放 氢 焓 低 至64.5 kJ·mol-1。为 提 高Mg2Ni 储氢性能,Yu 等[22]采用真空感应熔炼法制备了Mg95- x-Nix-Y5 (x= 5, 10, 15)。Mg-Ni-Y 氢化得到Mg2NiH4、YH3 和MgH2 三相纳米晶结构,原位形成的YH3 在放氢过程中未发生分解,均匀分散在母合金中,促进了体系吸/放氢过程中Mg2Ni 和Mg2NiH4 的相互转化。一定范围内随着Ni 含量的增加,体系吸放氢动力学明显改善,Mg80-Ni15-Y5 放氢活化能低至63.5 kJ·mol-1,200 ℃下60 s 内可吸氢5.4%。
镁基固溶体比纯镁具有更高的平衡氢压,通过Mg 与其他金属形成固溶体,可有效降低MgH2热稳定性[23,24]。特别地,Mg(In) 体系由于其完全可逆性,使其成为研究焦点之一[23-25]。Liang等[26]将Mg 分别与Zn、Al、Ag、Ga、Cd 和In 进行机械合金化来改善体系吸放氢性能,研究表明,Mg(Cd)和Mg(In)固溶体表现出更为突出的效果。Ma 等[27] 采用直流电弧等离子体法制备了Mg(In)固溶体,其吸/放氢焓分别降低至(-67.6±1.9)和(68.4 ±2.4)kJ·mol-1。进一步分析发现,In在MgH2 中有效降低了H 扩散能垒,抑制了Mg—H键的收缩,从而显著改善了Mg-In 体系的热力学和动力学性能。
稀土元素由于特殊的4f 电子层结构,引入储氢合金材料能有效削弱合金元素与H 的键合强度,从而降低氢扩散和解吸的能量势垒,有效改善体系储氢性能[28]。Hou 等[29]采用熔融纺丝法在Mg2Ni 合金中加入Cu 和La,制备了(Mg24Ni10Cu2)100- xLax。研究了La 含量对储氢性能的影响,在一定范围内放氢活化能随着 La 含量的增加而降低,Mg24Ni10Cu2: 65.54 和(Mg24Ni10Cu2)80La20: 48.26 kJ·mol-1。
总之,合金化能有效改善镁基储氢体系吸放氢热/动力学,但合金化过程大量金属元素的引入使体系储氢容量降低,表1 列举了部分镁基合金储氢性能,可以看出随着除Mg 以外的其他金属相对比重增加,体系储氢容量呈下降趋势,合金化削弱了Mg—H 键合强度,不同程度地降低了吸放氢反应焓。
表1 镁基合金储氢性能总结
Table 1 Summary of hydrogen storage properties of magnesium-based alloys
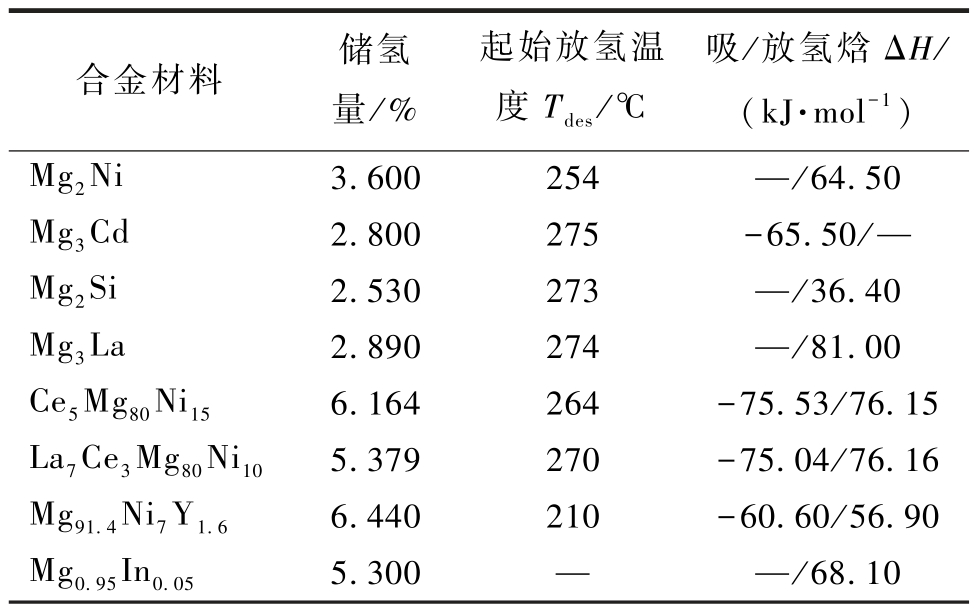
注:“—”表示无有关实验数据。
合金材料 储氢量/%起始放氢温度Tdes/℃吸/放氢焓ΔH/(kJ·mol-1)Mg2Ni 3.600 254 —/64.50 Mg3Cd 2.800 275 -65.50/—Mg2Si 2.530 273 —/36.40 Mg3La 2.890 274 —/81.00 Ce5Mg80Ni15 6.164 264 -75.53/76.15 La7Ce3Mg80Ni10 5.379 270 -75.04/76.16 Mg91.4Ni7Y1.6 6.440 210 -60.60/56.90 Mg0.95In0.05 5.300 — —/68.10
2 纳米化
纳米化为镁基储氢材料赋予更小的晶粒尺度,有效缩短了氢扩散距离;提供了更多的相界面,拓宽了氢扩散通道,从而降低了吸放氢反应的动力学障碍。同时,增加的表/界面能量可进一步优化热力学性能,是改善镁基储氢材料性能的主要策略之一[37-39]。Wagemans 等[39] 研 究 了 晶 粒 度 对 Mg/MgH2 颗粒热/动力学性能的影响,结果表明,当晶粒尺寸小于1.3 nm,放氢活化能显著降低,粒径为0.9 nm 的MgH2 可在200 ℃下放氢,放氢焓低至63kJ·mol-1 H2。近年来,国内外科研工作者致力发展高效纳米化技术以改善镁基储氢材料的性能,其中包括球磨法、化学合成法和纳米限域法等。
2.1 球磨法
球磨法是制备纳米材料的有效方法之一,可通过调节球磨介质、球料比以及球磨时长来控制纳米颗粒的粒径及分布。采用球磨法制备镁基储氢材料不仅能有效提高材料的比表面积,还能在一定程度上增加材料的晶格缺陷[40],这些改变可有效改善储氢材料吸放氢特性。Yuan 等[41]采用真空感应熔炼法制备了LaMg11Ni 合金,并对其进行充分球磨以提升吸放氢性能。研磨20 h 的合金氢化动力学明显改善,储氢容量从4.5%提高至5.4%。Liu 等[42]利用高能球磨机的机械能将镁粉和镍粉研磨,制备了纳米晶与部分非晶相共存、成分单一且粒径~10 μm 的Mg2Ni 合金;研究表明,通过控制球磨时间,合金粉的冷焊和破碎达到平衡,粒度基本保持在~10 μm 不变,其储氢密度接近理论值3.6%。
然而,值得注意的是,并非球磨时间越长,转速越高,得到的镁基储氢材料粒径越小,储氢性能越好。随着研磨时间的延长,颗粒细化,发生氧化的可能性增加,颗粒间应力变大,发生重新结合,导致材料储氢容量降低。因此,根据材料特性设置合理的球磨参数是制备良好储氢材料的关键。
2.2 气相沉积
气相沉积基于电弧放电产生的高温使金属瞬间激烈蒸发的原理,在H2 等气体的介入下,金属原子历经蒸发、形核、大幅度成长及凝聚等一系列过程[43]。可通过调控气压和冷凝速率等参数,合成纳米结构材料。Mao 等[44]采用电弧等离子体气相沉积技术,制备了核壳结构的Mg-MFx(M=V、Ni、La 和Ce)复合体系。研究发现,相较于纯Mg,这些复合体系吸氢动力学性能均得到明显改善,尤其是Mg-NiF2 在制备和吸放氢过程中原位形成了Mg2Ni 和MgF2,使其在较低温度下表现出最显著的改善;在200 ℃下60 s 内吸收3.85% H2,吸/放氢活化能分别降低至67.00 和139.21 kJ·mol-1。Chen 等[45]通过气相沉积法将V 修饰的Mg 纳米颗粒限制在1 nm 的碳壳中[图2(a)]。通过调节Mg 和V 的蒸发速率和元素质量比,制备了Mg92V8@C 纳米复合材料。平均粒径为~32 nm 的Mg92V8@C 表现出优异的储氢性能,氢储存量达6.6%[图2(b)~图2(c)],吸/放氢活化能分别降低到41 和67 kJ·mol-1[图2(d)],经10 次氢循环测试,可逆储氢容量仍大于5.2%[图2(e)]。进一步研究发现,碳壳的“纳米效应”和吸放氢过程中VH2/V2H起到“氢泵”作用,是储氢性能改善的关键因素。
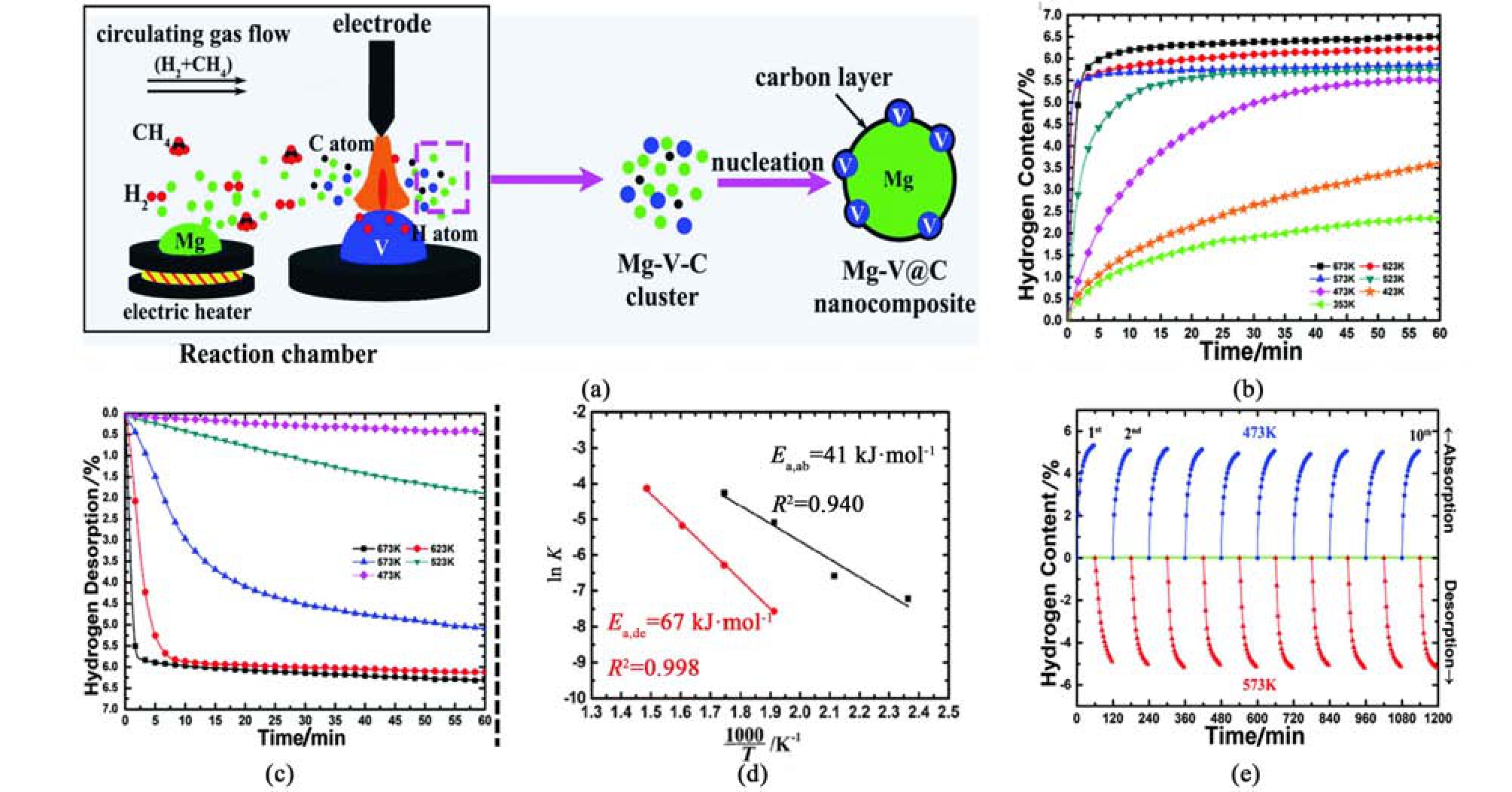
图2 (a) Mg-V@C 纳米复合材料合成工艺示意图;(b) Mg92V8@C 不同温度下的吸氢动力学曲线和(c) 放氢动力学曲线;(d) Mg92V8@C 吸/放氢ln k vs.1000/T 曲线和 (e) 吸/放氢循环曲线[45]
Fig.2 (a) Schematic diagram of the synthesis process of Mg-V@C nanocomposites, (b) the isothermal hydrogen absorption; (c) desorption curves of Mg92V8@C under different temperatures;(d) Mg92V8@C hydrogen absorption/desorption ln k vs.1000/T curves; (e) hydrogen absorption/desorption cycling curves[45]
2.3 化学合成
化学合成是制备Mg/MgH2 纳米颗粒的重要方法之一,其包括但不限于化学还原和氢化法等。化学合成效率高、可控性强,通过调控反应参数,如温度、压力与时间等,可以实现对反应进程和最终目标产物的有效调控。
化学还原法制备镁基储氢材料:通常以碱金属作为还原剂,还原Mg2+前驱体得到镁纳米材料。Liu等[46,47]先后报道了用萘作为电子载体,通过碱金属锂、钠和钾还原正二丁基镁(MgBu2),制备了粒径为7 ~52 nm 碱包覆的镁纳米颗粒。研究发现合理控制碱金属/萘比有助于镁纳米颗粒的成核和生长,制备的Mg 纳米颗粒热力学得到显著改善(钾包覆镁纳米颗粒吸氢焓: -63.2 kJ·mol-1)。此外,在钠和钾包覆的镁纳米颗粒上析出了具有钙钛矿结构的NaMgH3 和KMgH3 物质/相,发现钾包覆镁纳米颗粒具有更快的动力学,这很大程度上与KMgH3 具有更高的催化活性有关。Zhang 等[48]在超声的辅助下,诱导LiH 与MgCl2 在四氢呋喃中发生复分解反应,合成了粒径约4 ~5 nm 的MgH2 颗粒。该MgH2 颗粒在30 ℃低温下可逆吸放氢容量高达6.7%,在150 ℃下经50 次氢循环仍能保持99%的储氢量;与传统块状MgH2 相比,此方法制备的MgH2 热/动力学均有显著改善;吸、放氢活化能分别降低至28 和80 kJ·mol-1,放氢焓下降至59.5 kJ·mol-1。接近室温的吸放氢性能,良好的循环稳定性为其商业化应用提供了可能。
氢化 法 指 在 高 压 H2 (>3.5 MPa) 和 高 温(>150 ℃)下 将 镁 盐 转 化 为MgH2。Zhang 等[49] 将MgBu2 溶液渗透到孔径~13 nm 的碳气凝胶中,随后转移至高压釜中,在170 ℃,5.0 ~5.5 MPa 氢压下将MgBu2 转化为超细的MgH2。结合XRD 和TEM 研究表明,15%~17%的MgH2 以纳米颗粒的形式被限制在碳气凝胶中,其中~12%的MgH2 吸/放氢可逆循环超10 次,且其放氢速率是与石墨混合球磨MgH2 的5倍。结果表明,该储氢体系优异的放氢动力学行为和循环稳定性与其较小的Mg/MgH2 颗粒尺寸以及纳米碳气凝胶抑制了颗粒的团聚密切相关。
2.4 纳米限域
与球磨和化学合成制备方法不同,纳米限域通过将氢化物颗粒限制在框架材料的孔洞中,多孔框架起到抑制纳米颗粒的团聚和长大的作用[50]。纳米限域制备的储氢材料优点在于:(1)增加材料的比表面积,加速氢的吸附/解吸;(2)有效抑制颗粒的团聚,提升体系循环稳定性;(3)增加晶界处氢原子比例,提升氢扩散速度[51]。当前,研究较为广泛的纳米限域框架材料主要有多孔碳材料、金属有机框架材料(MOFs)、二维过渡金属碳化物(MXene)等。
金属有机骨架(MOFs)是一种由无机单元(金属离子或团簇)与有机配体通过配位键结合而成的高比表面积多孔框架材料,凭借其结构可控、高比表面积等特性,广泛应用于储氢材料体系[52,53]。Wang 等[54]采用沉积-还原法制备了Mg/MOFs 纳米复合材料(MOFs 为ZIF-8、MOF-74 和ZIF-67),MOFs 的引入可大幅度提升体系的储氢性能。特别是Mg/ZIF-67,表现出优异的吸放氢动/热力学性能;在175 ℃下吸收2% H2 仅2 051 s (纯Mg 需要3 124 s),吸氢态的Mg/ZIF-67 在300 ℃条 件 下,5 000 s 可 释 放3.7%H2,吸、放氢焓分别降低至-67.5 和77.8 kJ·mol-1。此外,Mg/ZIF-67 体系还表现出良好的循环稳定性(经100 次吸放氢循环其储氢容量无明显衰减)。研究表明,Mg/ZIF-67 呈现出良好的动/热力学及循环稳定性,这归因于其独特的核壳结构在一定程度上限制了Mg/MgH2 颗粒的长大。
MXene 是一类具有二维层状结构的金属碳化物或氮化物,得益于独特的官能团及片状结构,将其引入Mg/MgH2 体系,可有效改善其储氢性能[55]。Liu 等[56]通过剥离Ti3AlC2 粉体成功制备了二维Ti3C2(MXene),研究表明,二维Ti3C2 引入Mg/MgH2 储氢体系,储氢活性得到明显提升,其特有的二维层状结构和原位形成的Ti0 是改善储氢性能的主要因素。MgH2-5% Ti3C2 复合材料起始放氢温度下降至185 ℃,300 ℃下60 s 内能快速释放6.2% H2。同时,该复合材料可在室温下实现吸氢,150 ℃下吸收6.1% H2 仅需30 s。Ali 等[57]通过球磨MgH2 和三维双金属 MXene (d-TiNbCTx) 的混合物制备了MgH2@d-TiNbCTx 复合材料[图3(a)];该复合材料起始放氢温度低至150 ℃,在200 ℃下5 min 内能吸收7.2% H2,在低温30 ℃下吸收5.5% H2 仅需120 min[图3(b)]。此外,该复合材料在250 ℃下经150 次氢循环,仍具有6.5%的储氢容量。研究表明,元素Ti 和Nb 的电负性分别为1.54 和1.62,介于Mg(1.31)和H (2.20)之间,能有效促进Mg—H键的断裂,锚定在MXene 表面的Mg/MgH2 颗粒与原位形成的Ti/Nb 相互作用,从而有效改善了Mg/MgH2 吸放氢动力学,提升了体系的氢循环稳定性[图3(c)]。
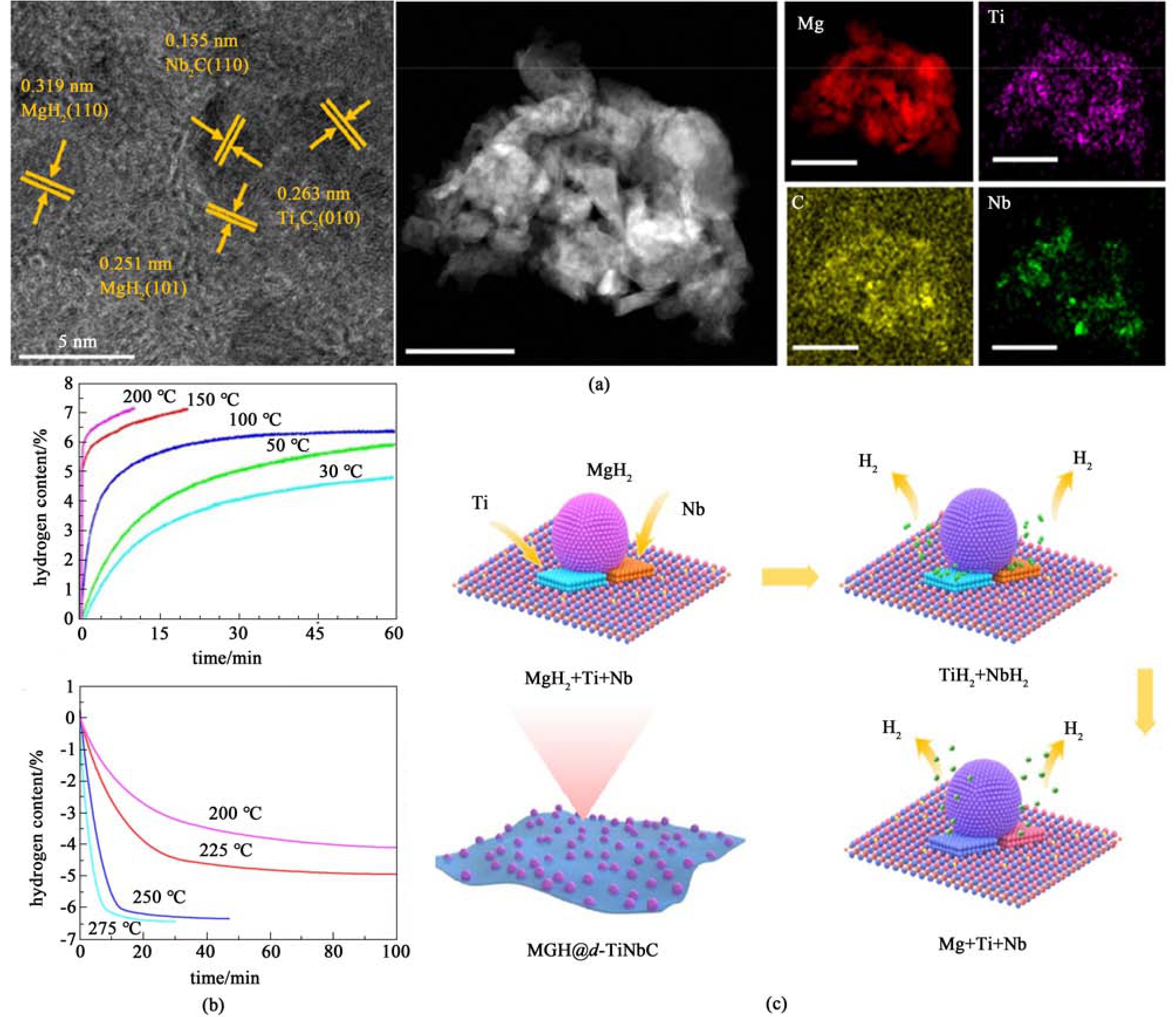
图3 (a)MgH2@d- TiNbCT 复合材料的微观结构和(b)不同温度下的吸/放氢动力学曲线;(c)TiH2/NbH2 对MgH2吸放氢性能增强机理图[57]
Fig.3 (a) Microstructure and (b) the isothermal hydrogen absorption/desorption curves of MgH2@d- TiNbCT composites under different temperatures; (c) mechanism of TiH2/NbH2 enhancement on MgH2 hydrogen absorption/desorption properties [57]
综上所述,实现镁基储氢材料纳米化的方法各有优劣。虽然球磨制备工艺简单,但制备的镁基储氢材料尺寸不均匀、氢化物颗粒经多次吸/放氢循环易发生团聚,从而影响体系循环稳定性。气相沉积技术可以制备出具有较高限域程度的镁基储氢材料,但制备条件难以控制。化学合成法具有操作简便、效率高等优点,但化学反应的微环境不均匀,导致颗粒尺寸不均匀,且化学反应物残存于储氢Mg/MgH2 颗粒中,迟滞了体系的吸/放氢行为。纳米限域通过将Mg/MgH2 纳米团簇限制在多孔支架中,缩短了H2 的扩散距离,改善了体系的储氢动力学行为,同时,减少了颗粒团聚从而提高了材料的循环稳定性。纳米限域技术经过几十年的发展,虽然取得了较为丰硕的研究成果,仍有进一步发展的空间。
3 添加催化剂
添加催化剂已被证实是改善Mg/MgH2 体系储氢性能的重要途径之一[58],通常可用“溢流”[59,60]、“氢泵”[17,61]、“通道”效应[62,63]和“电子转移”[64,65]4 种机理来解释。简单来说,催化剂的添加可削弱MgH2 的稳定性,为吸/放氢提供更多的活性位点、增加氢扩散通道。此外,部分催化相价态变化产生的电子转移促进了MgH2 的解离,从而有效改善体系吸放氢动力学性能。目前研究较为广泛的Mg/MgH2 体系催化剂大致可分为过渡金属单质/合金、过渡金属氧/硫化物、其他过渡金属化合物以及碳基复合材料等。
3.1 过渡金属单质/合金
储氢材料吸放氢动力学性能主要受H2 的解离和氢原子在储氢材料内的扩散影响。而过渡金属对氢原子具有较强的亲和力,外层电子易与氢的电子产生相互作用,该作用可使Mg—H 键结合力降低,从而改善镁基储氢材料放氢性能。此外部分过渡金属催化剂可以促进氢扩散、掺杂到MgH2 晶格中形成新相,对体系吸放氢都产生积极影响。
Pozzo 等[66]通过密度泛函理论(DFT)计算了系列过渡金属(TM)催化剂担载在Mg(0001)表面上对H2 解离和氢原子扩散的影响(TM=Ti、V、Zr、Fe、Rh、Ag、Cu、Pd、Ni 和Co)。研 究 表 明,在Mg 金属中掺入元素周期表偏左侧的TM 有利于H2 的解离,但TM 与氢原子结合力强,阻碍了氢原子的扩散。相反,元素周期表偏右侧的TM 与氢原子结合力较低,但对促进H2 的解离是有限的。然而位于第八族的Fe、Ni、Rh、Co 和Pd 掺杂在Mg 中既能有效促进H2 的解离,也能加速氢原子的扩散;氢分子在Pd、Ni、Fe 金属上的分解能垒分别为0.39、0.06 和0.03 eV,远低于Mg 的1.15 eV。Cui 等[67]使用湿化学法合成了过渡金属(Ti、V、Co、Ni、Nb、Mo)包裹镁的核壳结构纳米材料。这些材料均具有良好的放氢性能,放氢动力学 按Mg-Mo、Mg-Co、Mg-V、Mg-Ni、Mg-Nb、Mg-Ti 顺序依次增强。基于理论分析,这种动力学上的差异与元素电负性密切相关(除Ni 外,TM 电负性越小,Mg-TM 放氢活化能越低),而Mg-Ni 体系中Mg2 Ni 的形成直接影响了吸放氢的进行。
Chen 等[68]通过静电纺丝技术结合后续热处理的方法制备了多孔镍纳米纤维,该纳米纤维能有效促进MgH2 的分解。MgH2-4% Ni 纳米纤维起始放氢温度仅143 ℃(球磨MgH2 ~350 ℃),放氢峰值温度为244 ℃(球磨MgH2 ~383 ℃),在325 ℃下11 min 可 释 放 7.02% H2, 放 氢 活 化 能 降 低 至81.5 kJ·mol-1,较球磨制备的MgH2-4% Ni 粉体系(141.3 kJ·mol-1)性能明显提升。研究表明,这种性能的改善主要归因于多孔Ni 纳米纤维在Mg/MgH2表面的均匀分散,增强了Ni 与氢化物之间的接触面积,从而提供了更多的催化活性位点。
Ni 和Zr 单质在一定程度上能有效改善Mg/MgH2 体系吸放氢性能[68,69]。然而研究发现,通过共沉淀和熔盐还原制备的10 ~60 nm ZrNi 合金表现出较单一Zr 或Ni 更好的催化效果[70],球磨制备的MgH2-ZrNi 复合材料可在178 ℃下放氢,在250 ℃下10 min 内可释放5.6% H2,且能在室温(25 ℃)下开始再吸氢,放氢活化能仅88.6 kJ·mol-1。El-Eskandarany 等[71]将MgH2 与TiMn2 在Ar 气环境下球磨制备了MgH2-10% TiMn2 纳米复合材料,该体系在275 ℃下100 s 内 可 吸 氢5.1%;250 ℃下1 400 h 氢循环测试后储氢容量无明显衰减,在1 200 ~1 400 h 的 测 试 过 程 中 储 氢 容 量 维 持 在4.95%不变。
近年来,高熵合金(HEA)成为研究者普遍关注的前沿课题。HEA 通过“氢泵”效应和密切的电子转移显著增强了Mg/MgH2 体系的储氢动力学性能[72]。Wan 等[73]通过球磨法制备了MgH2-FeCoNi-CrMn(HEA)的复合材料。该复合材料在吸放氢过程中,部分Ni 和Co 分别与Mg 发生反应生成Mg2Ni/Mg2NiH4 和Mg2Co/ Mg2CoH5,产生“氢泵”效应,有效改善了体系的吸放氢动力学,放氢活化能降低至90.2 kJ·mol-1。在150 ℃下,该复合材料30 s 内可吸收5.5% H2,并能在280 ℃下600 s 内放氢5.6%;此外,HEA 的加入可有效抑制Mg/MgH2颗粒的团聚,从而提高体系循环稳定性(20 次氢循环后仍能保持98.6%的容量)。
3.2 过渡金属氧化物
与金属单质、合金不同,过渡金属氧化物催化剂脆性更好,采用普遍使用的球磨技术将其引入Mg/MgH2 体系,能获得更好的分散性,从而起到更好的改性效果[74]。表2 列举了部分过渡金属氧化物催化剂的添加对体系储氢性能的影响,良好的分散性使催化位点在体系中分布更均,有效提升了吸放氢动力学性能。
表2 金属氧化物掺杂对Mg/MgH2 体系储氢性能的影响
Table 2 Effect of doped metal oxides on the properties of the Mg/MgH2 system
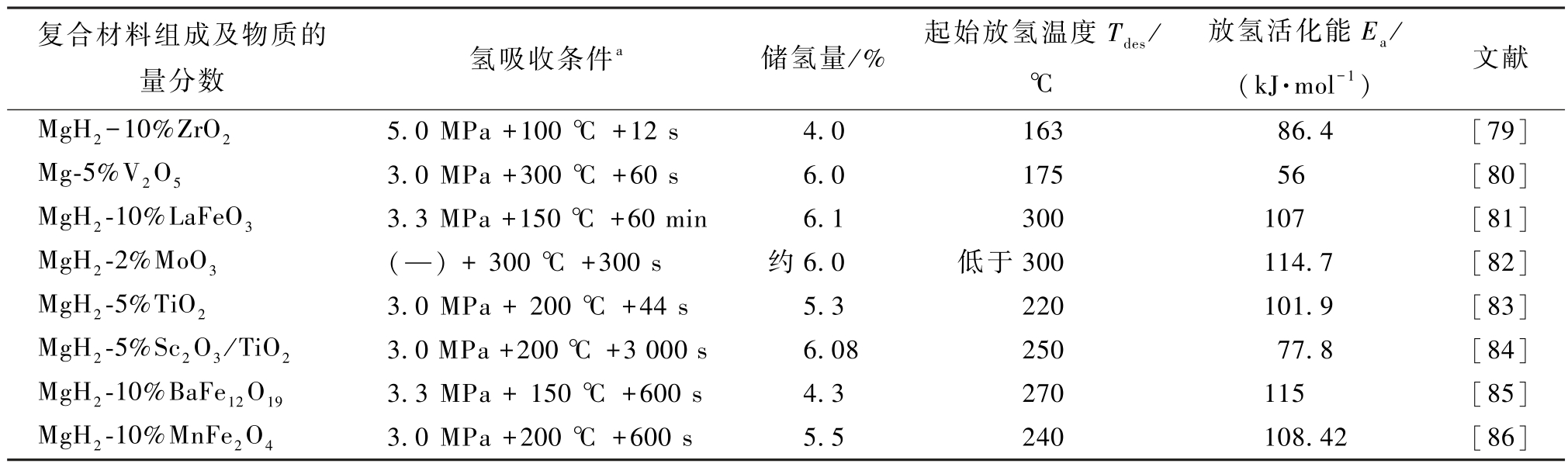
注:a“—”表示无有关实验数据。
复合材料组成及物质的量分数 氢吸收条件a 储氢量/% 起始放氢温度Tdes/℃放氢活化能Ea/(kJ·mol-1) 文献MgH2-10%ZrO2 5.0 MPa +100 ℃ +12 s 4.0 163 86.4 [79]Mg-5%V2O5 3.0 MPa +300 ℃ +60 s 6.0 175 56 [80]MgH2-10%LaFeO3 3.3 MPa +150 ℃ +60 min 6.1 300 107 [81]MgH2-2%MoO3 (—) + 300 ℃ +300 s 约6.0 低于300 114.7 [82]MgH2-5%TiO2 3.0 MPa + 200 ℃ +44 s 5.3 220 101.9 [83]MgH2-5%Sc2O3/TiO2 3.0 MPa +200 ℃ +3 000 s 6.08 250 77.8 [84]MgH2-10%BaFe12O19 3.3 MPa + 150 ℃ +600 s 4.3 270 115 [85]MgH2-10%MnFe2O4 3.0 MPa +200 ℃ +600 s 5.5 240 108.42 [86]
Long 等[75]采用直流电弧等离子体蒸发法制备了Ce2O3 包覆Mg 颗粒的核壳结构纳米复合材料。与纯MgH2 相比,该复合材料对吸放氢热力学改善甚微(吸/放氢焓分别为-71 和75.41 kJ·mol-1),但有效改善了吸氢动力学(吸氢活化能降低至47.75 kJ·mol-1),在150 ℃下该复合材料10 h 内能吸收4.07% H2。Guemou 等[76]研究了Mn3O4/ZrO2双金属氧化物对Mg/MgH2 储氢性能的影响,MgH2-Mn3O4/ZrO2 复合材料起始放氢温度低至219 ℃,在250 ℃下10 min 内可释放6.4% H2(纯MgH2 即使在335 ℃下仅释放1.4% H2),其放氢活化能降低至64.52 kJ·mol-1,再吸氢活化能低至16.79 kJ·mol-1;值得注意的是,放氢后的复合材料能在室温下开始吸氢,且在250 ℃下可吸氢6.0%。研究表明,均匀分散的 ZrO2 有效限制了Mg/MgH2 的长大,吸放氢过程中原位形成的Mn 则起到了“氢泵”的作用,加速了氢在Mg/MgH2 界面上的吸收/释放。
此外,二元金属氧酸盐催化剂对Mg/MgH2 体系的储氢性能也显示出优异的改善效果。Zhang等[77]制备了微米尺度的分层多孔TiNb2O7 球体,添加多孔TiNb2O7 球的Mg/MgH2 储氢体系在室温下开始吸氢,150 ℃下吸收4.5% H2 仅需3 min,在250 ℃下10 min 内能快速放出5.5%的氢。进一步研究发现,该储氢体系在吸放氢过程中,TiNb2O7 部分被还原为低价金属氧化物(TiO2、Nb2O5 等)或零价金属(Ti0),这些原位生成的氧化物/金属在储氢体系中起到了强的协同作用,从而改善该储氢体系吸放氢动力学(相对于仅由TiO2 或Nb2O5 催化的储氢体系,含TiNb2O7 的体系具有较低温度下的吸/放氢过程)。催化相的组成对体系性能提升极为重要,此外,催化剂的微观形貌和结构对储氢体系的吸放氢性能也存在影响。Xian 等[78]研究表明,添加3%的二维纳米片状TiNb2O7 能使Mg/MgH2 储氢体系起始放氢温度降低至178 ℃,在300 ℃下放氢量高达7.0%;且该储氢体系表现出良好的循环稳定性,经30 次吸/放氢循环,储氢容量仍保持在96 %以上。DFT 计算表明,MgH2 和TiNb2O7 之间强的电荷转移改变了Mg 和H 的电荷分布,削弱了Mg—H 键。
3.3 过渡金属硫化物
过渡金属硫化物对镁基材料的储氢性能具有良好的增强作用,这种增强作用源自吸放氢过程中原位生成的MgS 及其它新相为储氢体系提供了可持续催化作用[87,88]。Jia 等[88] 研究了MoS2 和MoO2 对MgH2 的吸放氢的催化作用。结果表明,相较于MoO2,MoS2 更好地改善了镁基储氢体系的动力学。同MoO2 球磨的MgH2,其放氢活化能为101.34 kJ·mol-1,而同MoS2 球磨的MgH2 活化能降低至87.19 kJ·mol-1。
Wang 等[89]研究了系列过渡金属硫化物(TiS2、NbS2、MoS2、MnS、CoS2 和CuS)对MgH2 的储氢性能的影响。结果表明,以上硫化物都能明显优化MgH2 的吸放氢动力学,放氢活化能按CuS、CoS2、MoS2、MnS、NbS2、TiS2 的 顺 序 依 次 降 低。其 中,MgH2-TiS2 可在204 ℃下放氢,放氢活化能低至50.8 kJ·mol-1。研究表明,原位形成的MgS、TiH2、NbH、Mo、Mn、Mg2CoH5 和MgCu2 促进了催化活性的提升。Fu 等[90]采用水热法合成了FeNi2S4,并通过球磨法制备了MgH2-FeNi2S4 复合材料。该复合材料起始放氢温度低至267 ℃,比球磨的纯MgH2低80 ℃[图4(a)],放氢活化能仅65.5 kJ·mol-1(纯MgH2 ∶ 161.2 kJ·mol-1)[图4(b)~图4 (c)]。通过对吸放氢前后物相、微观结构的进一步研究表明,吸/放氢过程中原位生成的Mg2NiH4/Mg2Ni 充当“氢泵”作用,而MgS 和Fe 组分可持续地为系统提供催化作用,研究者认为这是改善Mg/MgH2 的储氢性能的关键因素[图4(d)~图4 (f)]。
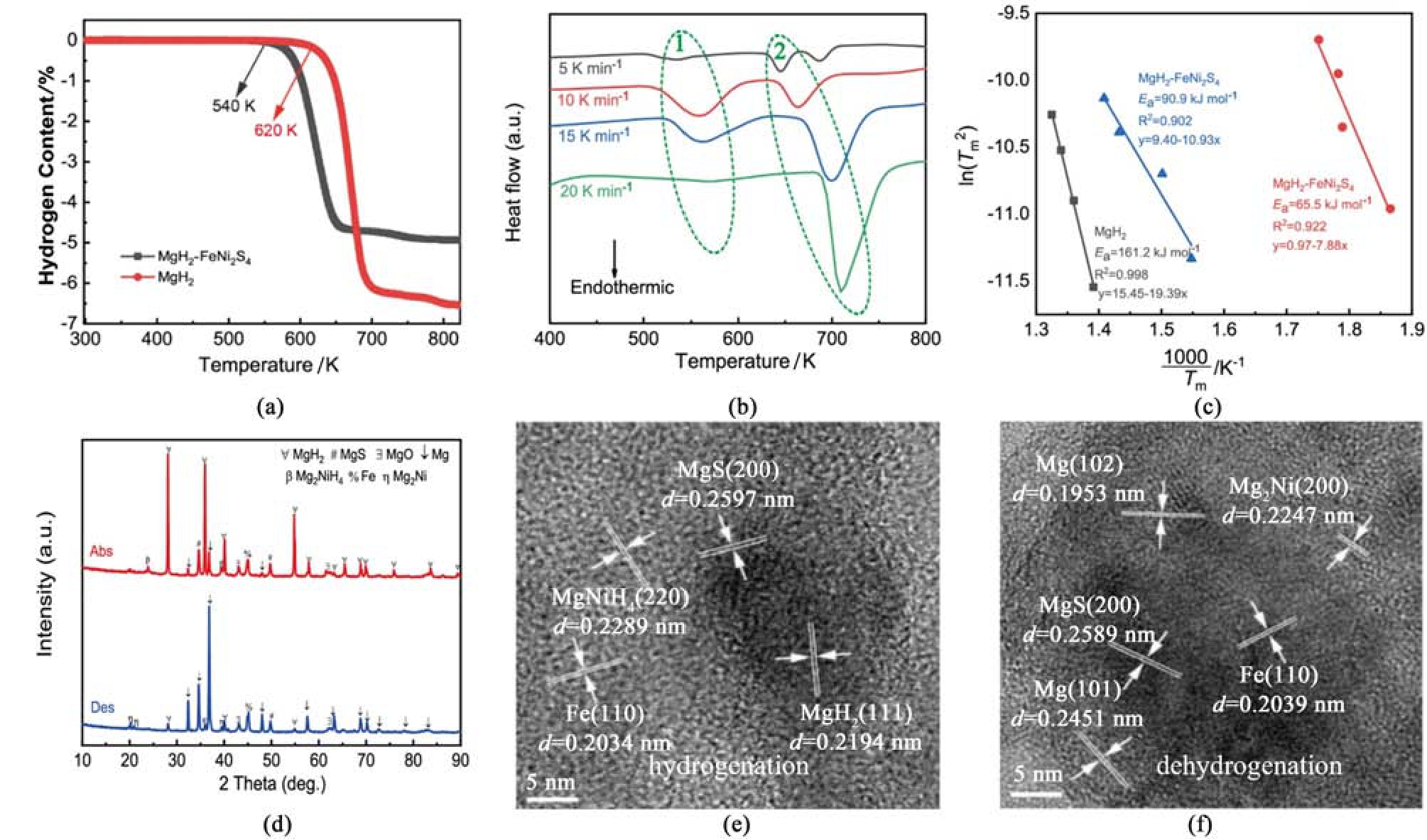
图4 (a)MgH2-FeNi2S4 和MgH2 TPD 曲线;(b)MgH2-FeNi2S4 DSC 放氢曲线;(c)MgH2-FeNi2S4 和MgH2 Kissinger 图;(d)MgH2-FeNi2S4 10 次氢循环后的吸/放氢态XRD 图谱;(e-f)MgH2-FeNi2S4 吸/放氢后的HRTEM 图[90]
Fig.4 (a) MgH2-FeNi2S4 and MgH2 TPD curves; (b) MgH2-FeNi2S4 DSC dehydrogenation curves; (c) MgH2-FeNi2S4 and MgH2 Kissinger plots;(d) XRD profiles of the absorbed/desorbed states of MgH2-FeNi2S4 after 10 cycles of hydrogenation;(e-f) HRTEM image of MgH2-FeNi2S4 after hydrogen absorption/desorption[90]
3.4 其他过渡金属化合物
除过渡金属单质/合金、金属氧/硫化物外,金属卤化物、金属碳化物、金属氮化物等同样表现出良好的催化作用。Zhang 等[91]采用熔盐法制备了包含Nb3+和Nb5+的NbN 纳米颗粒,并将其用于Mg/MgH2 储氢体系。MgH2-NbN 复合材料吸放氢动力学得到明显改善,低至100 ℃时,24 min 内能快速吸氢5.0%。
Tian 等[92] 通过机械球磨将 5% 的碳化物(Ti3C2、Ni3C、Mo2C、Cr3C2、NbC)引入MgH2 中,均对MgH2 的吸放氢动力学起到了积极影响,其动力学改善效果按以下顺序依次减弱:Ti3C2、Ni3C、NbC、Mo2C、Cr3C2。其中,MgH2-Ti3C2 起始放氢温度低至205 ℃,放氢活化能降低至57.5 kJ·mol-1。Lan等[93]通过刻蚀V4AlC3 制备了二维VC。研究表明,掺杂VC 的MgH2 可在170 ℃放氢,并在室温下吸氢,放氢活化能降低至89.3 kJ·mol-1,远低于纯MgH2 (138.5 kJ·mol-1)。DFT 计算表明,VC 可以拉伸Mg—H 键,使得Mg—H 键更容易断裂,有助于降低放氢温度并促进氢原子的扩散速率,从而使储氢体系吸放氢动力学得到改善。
据研究发现镁基储氢体系掺入适量金属卤化物催化剂能有效改善吸放氢性能[94]。Malka 等[95]采用球磨法将金属卤化物(TiCl3、ZrF4、TaF5 和NbF5)作为催化剂掺杂在Mg/MgH2 体系中,研究了这些金属卤化物的添加对体系储氢性能的影响机制。结果表明,金属卤化物的添加很大程度上提高了体系吸放氢动力学,特别是ZrF4、NbF5 的添加引入了F 离子,削弱了Mg—H 键,形成了MgF2,有效改善了体系储氢性能。
3.5 碳基复合催化剂
碳材料高度无序的多孔结构、良好的分散性和强吸附性被视为工业中最受欢迎的添加剂之一[96]。目前已被应用于镁基储氢体系进行研究,与其他添加剂相比,碳基金属复合催化剂的添加不仅改善Mg/MgH2 的储氢动力学性能,同时,能够有效抑制颗粒的团聚,显著提升了镁基储氢体系的循环稳定性。常见的碳基金属复合催化剂载体有金属有机框架衍生的多孔碳[97,98]、石墨烯[99-102] 和碳纳米管[103]等。不同碳基复合材料的掺杂对镁基储氢体系放氢性能的和氢循环稳定性的影响如表3 所示。
表3 碳基复合材料掺杂对Mg/MgH2 体系储氢性能的影响
Table 3 Effect of doped Carbon-based composites on the properties of the Mg/MgH2 system
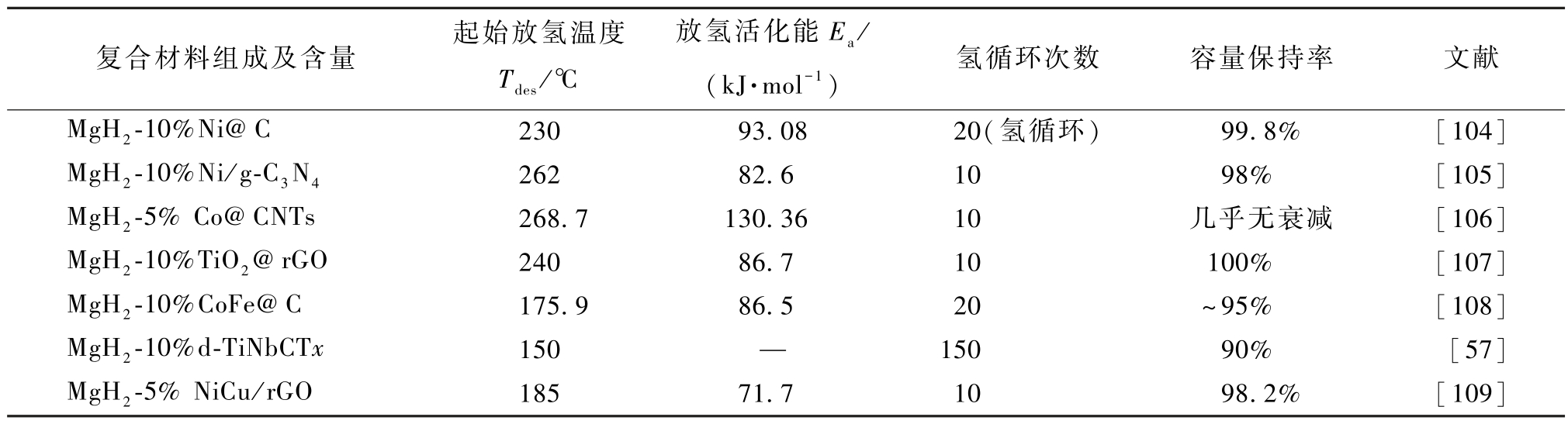
注:“—”表示无有关实验数据。
复合材料组成及含量 起始放氢温度Tdes/℃放氢活化能Ea/(kJ·mol-1)氢循环次数 容量保持率 文献MgH2-10%Ni@C 230 93.08 20(氢循环) 99.8% [104]MgH2-10%Ni/g-C3N4 262 82.6 10 98% [105]MgH2-5% Co@CNTs 268.7 130.36 10几乎无衰减 [106]MgH2-10%TiO2@rGO 240 86.7 10 100% [107]MgH2-10%CoFe@C 175.9 86.5 20~95% [108]MgH2-10%d-TiNbCTx 150 — 150 90% [57]MgH2-5% NiCu/rGO 185 71.7 10 98.2% [109]
石墨烯(GR)由于独特的结构、质轻、多孔和大比表面积被众多学者用于储能体系[99]。GR 对镁基储氢体系的催化作用机理主要在于Mg 与C 之间的电子转移[100]。Zhang 等[101] 采用球磨 法 制 备 了MgH2-10% GR 的复合材料,通过SEM 观察发现,GR 成片状弥散分散在MgH2 颗粒间,有效地控制了球磨过程中MgH2 颗粒的团聚。GR 的加入有效改善了MgH2 的储氢性能。根据差示扫描量热法(DSC)测得,相同条件下,该复合储氢体系较纯MgH2 体系放氢温度低近100 ℃。单纯添加GR 对于MgH2 储氢性能的改善是有限的,Yao 等[102]采用化学还原法合成了还原氧化石墨烯包裹镍(Ni@rGO)纳米复合材料,并通过球磨制备了MgH2-10%Ni@rGO 复合材料。该复合材料起始放氢温度低至190 ℃,在100 ℃下20 min 内能快速吸氢5.0%,放氢活化能降低至117.8 kJ·mol-1。研究表明,Ni@rGO 的加入有效改善了体系吸放氢动力学,rGO 的存在提供了更多的“催化位点”和H“扩散通道”,提高了体系循环稳定性。
综上所述,添加催化剂能为储氢材料吸放氢过程中氢吸附及解吸提供更多的活性位点,有效改善动力学行为,是目前广泛研究的一种储氢材料改性手段。但催化剂的添加对体系热力学的改善是有限的,MgH2 的高热稳定性仍然是当下面临的一个重大障碍。
4 薄膜化
薄膜储氢材料相对于块状材料具有表面积大、吸放氢速率快、表面易于改性以及导热系数高等优点[110,111]。纯镁薄膜的吸放氢性能相较于块状镁有所提高,但想要实现商业化应用通过简单的薄膜化处理显然是不够的。
为了弥补纯镁薄膜的不足,研究者将具有较好氢吸附/解吸活性的Pd 包覆于镁薄膜表面,一方面起到保护层的作用,有效防止镁在空气中发生氧化。同时,Pd 还能充当催化剂加快表面氢分子的解离,有效降低吸放氢温度。早在2009 年,Kumar等[112]通过热蒸发法成功制备了Pd 包覆Mg 薄膜,该薄膜储氢容量高达7.0%。但吸放氢循环稳定性得不到保证,在前2 次循环中效果很好,但在第3 次循环过程中,储氢容量显著降低。研究发现,Pd/Mg界面反应是引起储氢容量降低的关键因素。因此,阻断Pd 与Mg 薄膜的界面混合是解决体系循环稳定性的有效方法,于是Reddy 等[113]采用电子束蒸发法制备了Pd 和Ti 薄膜,采用电阻蒸发法制备了Mg 薄膜,并将Ti 薄膜置于Pd 与Mg 薄膜层中间,在300 ℃下真空处理;该复合膜在150 ℃,0.15 MPa氢压下可吸收7.0% H2,在200 ℃下能实现完全放氢。此外,经18 次氢循环,该复合膜仍能保持约2.2%储氢容量。
镁基合金材料相较于纯镁储氢热力学性能有明显的改善,并具有更好的循环稳定性[114]。Qin等[115]为克服镁基合金放氢热力学稳定和动力学缓慢的障碍,通过超高真空磁控溅镀设备制备了具有超晶格结构的Mg-Zr 调制膜。研究表明,沉积的Mg-Zr 调制膜具有超薄的相干层,能在室温下吸氢,并在81 ℃时开始放氢[图5(a)],较传统MgH2 放氢性能得到显著提升。上述性能的显著改善主要在于Zr 的催化作用和相干异质界面应变的协同作用,Mg-Zr 调制膜具有原子尺度分布均匀的高界面密度,提供了快速的H2 吸收/释放通道和催化位点,有效改善了体系动力学性能[图5(b)]。MgNi合金作为一种代表性的储氢材料,一直受到广泛的关注和研究。吴等[116]采用磁控溅射技术制备了以Pd 封 盖、Si 为 基 底 的Mg1- xNix (x=0.1,0.2,0.3 和0.5)薄膜。研究表明Ni 的引入显著降低了体系的放氢温度,当x=0.5 时,体系可在低至113 ℃下实现放氢,比纯Mg 薄膜低98 ℃,在250 ℃条件下Mg0.8Ni0.2 放氢量达3.09%。
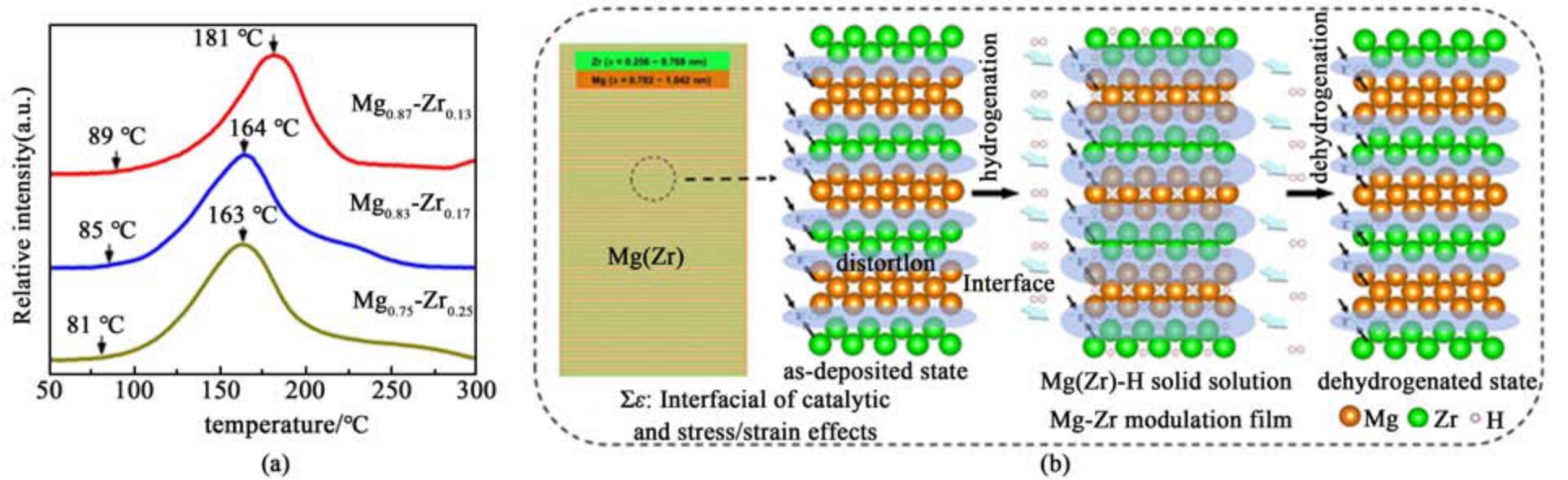
图5 (a)Mg-Zr 调制膜TPD-MS 曲线和 (b)吸/放氢机理图[115]
Fig.5 (a) TPD-MS curves and (b) hydrogen absorption/desorption mechanism diagrams of Mg-Zr modulated membranes[115]
近年来,在科研工作者努力下,镁基储氢薄膜的研究取得了一定的进展,但薄膜易氧化、添加改性材料价格昂贵、改性后体系容量降低明显和循环稳定性较差等问题仍亟待解决。
5 复合化
近年来,固态储氢体系取得了多元化发展。研究人员为解决镁基储氢材料吸放氢热力学稳定、动力学缓慢的问题,寻求更为理想的储氢体系,构建了“MgH2+轻金属配位氢化物”、“MgH2+合金氢化物”等复合体系。
轻金属配位氢化物具有相较于其他固态储氢材料具有更为突出的储氢容量,因此构建以“MgH2+轻金属配位氢化物”复合材料能有效提升体系的储氢容量[5]。MgH2+LiBH4 复合体系储氢性能的改善主要有:(1)复合体系“反应失稳”生成稳定性更高的MgB2,改变了放氢途径,实现热力学性能的改善。(2)LiBH4 有效提升了体系储氢容量[117-119]。Leon团队[120-122]通过在球磨过程中进行原位气溶胶喷涂技术制备了纳米“MgH2+LiBH4”复合材料,充分混合的复合材料可在低至265 ℃下实现可逆吸/放5.0% H2。Chen 等[123]研究了Al3Ti 掺杂Al 纳米颗粒催化2LiBH4-MgH2 体系储氢性能,复合体系两步放氢活化能分别降低至110.1(纯MgH2: 165.5)和119.6 kJ·mol-1(纯LiBH4:153.1 kJ·mol-1),经10 次氢循环,仍能保持9.2%的储氢容量。
除 LiBH4 外, Mg/MgH2 复 合 LiAlH4[124,125]、NaBH4[126,127]等体系的研究均取得了一定进展。Lin等[128]采用球磨将MgH2、LiBH4 和Li3AlH6 三相复合,复合材料初始放氢温度仅276 ℃,在360 ℃实现完全放氢, 可逆氢容量高达 8.0%, 脱氢焓低至62.8 kJ·mol-1。LiBH4 和Li3AlH6 破坏了MgH2 的稳定性,改善了体系热力学性能,吸放氢过程中原位生成的Li3Mg7、Mg17Al12 和MgAlB4 加快了氢扩散速率,提升了反应动力学性能,改善了体系循环稳定性。
储氢合金通常具有较好的热/动力学性能,但合金元素本身质量占比重,储氢容量低。将其与镁基储氢材料复合,一方面起到催化Mg/MgH2 吸放氢的作用,另一方面在于镁基储氢合金的生成,改变Mg/MgH2 吸放氢反应途径,降低吸放氢反应焓,实现两者性能优势的互补。常见的复合体系有“MgH2+AB5 型 合 金”[129,130] 和“MgH2 +AB2 型 合金”[131,132]等。
Márquez 等[133]采用冷轧工艺制备了后0.1 mm的“MgH2+AB5 型合金(LaNi5)”复合薄片,该复合材料在300 ℃,30 min 实现完全放氢,而冷轧MgH2 在330 ℃下,相同时间仅能释放复合体系50% 的H2。DSC 测试结果表明MgH2 在452 ℃左右出现放氢峰,而复合材料放氢温度在350 ℃附近。10 次吸放氢循环后,仍具有较好的动力学性能,保持4.0%的储氢容量。分析表明,吸放氢过程Mg2NiH4 和LaH3新相的生成对体系吸放氢动力学起到了积极作用。
与添加催化剂改性不同,轻金属配位氢化物和合金等体系也具有一定的储氢能力。特别地,引入轻金属配位氢化物,能显著提升镁基储氢的储氢量。同时,改变镁基储氢材料吸放氢反应途径,改善体系的热力学性能。但复合体系动力学性能、吸放氢循环稳定性仍有待提升。
6 镁基固态储氢工程化进展
近年来,在科研工作者不断努力之下,镁基储氢材料的工程化取得了初步进展,为实现大规模商业化应用奠定了坚实的基础。2023 年,上海交通大学氢科学中心和上海氢枫能源科技有限公司联合研发的全球首台吨级镁基固态储运氢车MH-100 T首次亮相,车辆搭载的镁基固态储氢装置可储存1.03 t H2,储氢量是传统高压气态储氢的3 ~4 倍,运输成本为其1/3,提供了高效、安全的氢气储运方案。该技术的应用示范为降低氢能源成本开辟新途径,拓宽了氢的高安全性应用范围[134]。2024 年,江苏华镁时代科技有限公司投产的全球首条百吨级镁基固态储氢材料生产线在我国投料试产一次性开车成功,氢化镁的年产量可达100 t,试生产中下线材料储氢密度可以达到6.5%。
尽管镁基固态储氢技术在工程化方面已取得初步成果,但要实现进一步产业化仍需面临诸多挑战。具体来说,储氢材料的制备成本较高,且必须在特定的环境条件下应用,目前大多数储氢材料的吸氢温度仍超过150 ℃。其次,储氢设备有待升级,特别是在气密性等关键性能指标上。此外,储氢材料的循环稳定性仍需提高。这些难题的攻克将是推动镁基固态储氢技术走向产业化升级的关键。
7 总结与展望
开发高效、廉价的固态储氢材料是推动“氢经济”的关键环节之一。镁基储氢材料因储氢容量高、成本低廉等优点备受关注,然而较高的放氢温度、缓慢的动力学性能阻碍了其进一步应用。为改善镁基储氢材料的性能,科研工作者开展了大量研究并取得了较为丰硕的成果。
(1)合金化通过成分调控能有效改善热/动力学性能,特别是热力学性能的提升。然而,在合金化过程中引入的大量金属元素会极大地降低储氢容量。同时,吸放氢过程中的金属键的断裂也会直接影响合金的循环稳定性。因此,提升储氢合金的容量、探索储氢合金工作机制,寻找循环稳定性更好的合金是当下需要解决的难点课题。
(2)通过材料纳米化获得高孔隙率、高比表面积以及更多的缺陷结构,能显著改善材料表面活性和吸放氢热/动力学性能。然而,针对不同的纳米化方法存在的缺陷仍需要进一步优化。例如,球磨过程中材料易发生团聚,化学合成难以做到可控制备,得到的纳米材料易于氧化等。
(3)催化剂的引入可能会激发“溢流”、“氢泵”、“通道”效应和“电子转移”,从而提高催化活性。合适的催化剂可有效促进氢的吸附/解吸,从而改善动力学性能,同时能维持良好的循环稳定性。例如,碳与金属的复合催化剂在一定程度上既能改善吸放氢动力学性能降低吸放氢温度,又能提高体系循环稳定性。然而,目前开发的催化剂对储氢体系的热力学影响甚微,尽管现阶段通过原位合成的纳米级催化剂有一定的提升,但仍有很大的发展空间。因此,设计、制备有效改善镁基储氢材料热/动力学性能、高度分散以及活性位点丰富的新型催化剂是未来发展重点。
(4)薄膜化可增加比表面积、加快氢扩散速度,能显著改善镁基储氢材料的吸放氢性能,是当前最具前景的改性方法之一。抑制膜表面的氧化是提升储氢材料性能的关键所在。对薄膜表面进行处理,如化学镀等,更好地抑制薄膜氧化同时起到催化作用。
(5)复合化通过改变储氢材料反应途径和原位形成新相(提供更多的催化活性位点)等原理改善镁基储氢材料热/动力学性能,但复合体系氢循环稳定性较差仍是当前面临的主要问题。
需要说明的是以上5 种改性方法并不是独立存在的。纳米化和薄膜化从制备方法上进行调整,利用纳米效应、薄膜化结构特征优化动力学性能,合金化和添加催化剂通过成分调控达到改性的目的。虽然以上4 种改性方法对于镁基储氢材料的性能优化都有一定的效果,然而仅仅通过单一策略提高性能显然难以取得令人满意的成效。随着研究的进一步深入,合金化-纳米化、添加催化剂-纳米化、合金化-薄膜化等结合的改性策略都取得了较单一方法更好的调控效果。
未来想要实现镁基固态储氢材料的进一步发展,可从以下方面出发。首先,研究储氢机制,提升储氢效果:深入研究储氢材料的储氢机制,包括吸附、扩散和反应过程,以指导更高效的储氢体系的设计开发。其次,开发新的储氢材料、优化改性策略:在进一步改善催化剂活性、控制纳米颗粒尺寸、设计更合适的合金以及探索新结构材料方面,还有很多工作可以开展,例如MOFs 和MXene 材料不仅能起到纳米限域的作用,同时具有良好的催化性能等。此外,优化储氢材料的制备工艺、提升材料制备效率:例如利用等离子球磨技术替代传统的球磨工艺,以提高材料的制备效率和质量、通过将溶剂反应与球磨工艺相结合,实现材料的协同改性,提高储氢性能等。
[1] WANG Y, XUE Y, ZÜTTEL A.Nanoscale engineering of solidstate materials for boosting hydrogen storage[J].Chemical Society Reviews, 2024, 53(2): 972-1003
[2] SCHLAPBACH L, ZÜTTEL A.Hydrogen-storage materials for mobile applications[J].Nature, 2001, 414(6861): 353-358
[3] ABDIN Z, ZAFARANLOO A, RAFIEE A, et al.Hydrogen as an energy vector[J].Renewable and Sustainable Energy Reviews, 2020, 120: 109620
[4] 邹建新.氢气储存和运输[M].北京: 机械工业出版社, 2023 ZOU Jianxin.Hydrogen storage and transportation[M].Beijing:China Machine Press, 2023 (in Chinese)
[5] WANG H, LI J, WEI X, et al.Thermodynamic and kinetic regulation for Mg-based hydrogen storage materials: Challenges,strategies, and perspectives[J].Advanced Functional Materials,2024, 34(42): 2406639
[6] 朱敏.先进储氢材料导论[M].北京: 科学出版社, 2015 ZHU Min.Introduction to advanced hydrogen storage materials[M].Beijing: Science Press, 2015 (in Chinese)
[7] 巴纳姆, Darren P, 刘永锋, 等.储氢材料: 储存性能表征[M].北京: 机械工业版社, 2013
[8] 敖鸣, 王启东.储氢材料的研究与应用[J].材料导报,1992, 6(1): 63-66 AO Ming, WANG Qidong.Research and application of hydrogen storage materials[J].Materials Review, 1992, 6(1): 63-66(in Chinese)
[9] SADHASIVAM T, KIM H T, JUNG S, et al.Dimensional effects of nanostructured Mg/MgH2 for hydrogen storage applications: A review[J].Renewable and Sustainable Energy Reviews, 2017, 72: 523-534
[10] 彭苏萍, 陈立泉.氢能与储能导论[M].北京: 中国科学技术出版社, 2023 PENG Suping, CHEN Liquan.Introduction to hydrogen energy and storage energy[M].Beijing: China Science and Technology Press, 2023 (in Chinese)
[11] 王艺强, 刘录强, 张志成, 等.化学储氢介质实现“西氢东送” 的可行性研究[J].储能科学与技术, 2024, 13(3):1050-1058 WANG Yiqiang, LIU Luqiang, ZHANG Zhicheng, et al.Feasibility of “West-to-East Hydrogen Transmission” through chemical hydrogen storage media[J].Energy Storage Science and Technology, 2024, 13(3): 1050-1058(in Chinese)
[12] 殷伊琳.我国氢能产业发展现状及展望[J].化学工业与工程, 2021, 38(4): 78-83 YIN Yilin.Present situation and prospect of hydrogen energy industry[J].Chemical Industry and Engineering, 2021, 38(4):78-83(in Chinese)
[13] XU W, TAKAHASHI K, MATSUO Y, et al.Investigation of hydrogen storage capacity of various carbon materials[J].International Journal of Hydrogen Energy, 2007, 32(13): 2504-2512
[14] SAEED M, MARWANI H M, SHAHZAD U, et al.RETRACTED: Nanoscale silicon porous materials for efficient hydrogen storage application [J].Journal of Energy Storage, 2024,81: 110418
[15] XU N, WANG K, ZHU Y, et al.PdNi biatomic clusters from metallene unlock record-low onset dehydrogenation temperature forbulk-MgH2 [J].AdvancedMaterials,2023,35(38): 2303173
[16] GUO Y, YU X, GAO L, et al.Significantly improved dehydrogenation of LiBH4 destabilized by TiF3[J].Energy & Environmental Science, 2010, 3(4): 464-469
[17] REN L, ZHU W, ZHANG Q, et al.MgH2 confinement in MOFderived N-doped porous carbon nanofibers for enhanced hydrogen storage[J].Chemical Engineering Journal, 2022, 434: 134701
[18] 李谦, 潘复生.镁基储氢材料[M].重庆: 重庆大学出版社, 2023 LI Qian, PAN Fusheng.Magnesium-based hydrogen storage materials[M].Chongqing: Chongqing University Press, 2023 (in Chinese)
[19] REN L, LI Y, ZHANG N, et al.Nanostructuring of Mg-based hydrogen storage materials: Recent advances for promoting key applications[J].Nano-Micro Letters, 2023, 15(1): 93
[20] LU Z, YU H, LU X, et al.Two-dimensional vanadium nanosheets as a remarkably effective catalyst for hydrogen storage in MgH2[J].Rare Metals, 2021, 40(11): 3195-3204
[21] REILLY J J, WISWALL R H.Reaction of hydrogen with alloys of magnesium and nickel and the formation of Mg2 NiH4[J].Inorganic Chemistry, 1968, 7(11): 2254-2256
[22] YU Y, JI Y, ZHANG S, et al.Microstructure characteristics,hydrogen storage thermodynamic and kinetic properties of Mg-Ni-Y based hydrogen storage alloys[J].International Journal of Hydrogen Energy, 2022, 47(63): 27059-27070
[23] MAO J, HUANG T, PANDA S, et al.Direct observations of diffusion controlled microstructure transition in Mg-In/Mg-Ag ultrafine particles with enhanced hydrogen storage and hydrolysis properties [J].Chemical Engineering Journal,2021,418: 129301
[24] ZHOU C, FANG Z, LU J, et al.Thermodynamic destabilization of magnesium hydride using Mg-based solid solution alloys[J].The Journal of Physical Chemistry C, 2014, 118 ( 22):11526-11535
[25] ZHAO D, ZHANG Y.Research progress in Mg-based hydrogen storage alloys[J].Rare Metals, 2014, 33(5): 499-510
[26] LIANG G.Synthesis and hydrogen storage properties of Mg-based alloys[J].Journal of Alloys and Compounds, 2004, 370(1/2):123-128
[27] MA Z, HUANG Z, LI Z, et al.Insights into thermodynamic destabilization in Mg-In-D hydrogen storage system: A combined synchrotron X-ray and neutron diffraction study[J].Energy Storage Materials, 2023, 56: 432-442
[28] UCHIDA H, TADA M, HUANG Y.The influence of cerium,praseodymium, neodymium and samarium on hydrogen absorption in LaNi5 alloys[J].Journal of the Less Common Metals, 1982,88(1): 81-87
[29] HOU Z, ZHANG W, WEI X, et al.Hydrogen storage behavior of nanocrystalline and amorphous Mg-Ni-Cu-La alloys[J].RSC Advances, 2020, 10(55): 33103-33111
[30] SKRIPNYUK V M, RABKIN E.Mg3 Cd: A model alloy for studying the destabilization of magnesium hydride[J].International Journal of Hydrogen Energy, 2012, 37(14): 10724-10732
[31] VAJO J J, MERTENS F, AHN C C, et al.Altering hydrogen storage properties by hydride destabilization through alloy formation: LiH and MgH2 destabilized with Si[J].ChemInform,2004, 108(37):13977-13983
[32] OUYANG L Z, QIN F, ZHU M.The hydrogen storage behavior of Mg3 La and Mg3 LaNi0.1[J].Scripta Materialia, 2006, 55(12): 1075-1078
[33] QI Y, ZHANG X, LI J, et al.Hydrogen storage thermodynamics and kinetics of as-cast Ce-Mg-Ni-based alloy[J].Journal of Iron and Steel Research International, 2024, 31(3): 752-766
[34] ZHANG Y, SUN H, ZHANG W, et al.A comparison study of hydrogen storage performances of as-cast La10 - x REx Mg80 Ni10 (x=0 or 3; RE=Sm or Ce) alloys[J].Journal of Alloys and Compounds, 2021, 884: 160905
[35] PANG X, RAN L, CHEN Y, et al.Enhancing hydrogen storage performance via optimizing Y and Ni element in magnesium alloy[J].Journal of Magnesium and Alloys, 2022, 10(3): 821-835
[36] ZHONG H, WANG H, LIU J, et al.Altered desorption enthalpy of MgH2 by the reversible formation of Mg(In) solid solution[J].Scripta Materialia, 2011, 65(4): 285-287
[37] SHAO H, XIN G, ZHENG J, et al.Nanotechnology in Mgbased materials for hydrogen storage[J].Nano Energy, 2012, 1(4): 590-601
[38] PASQUINI L.The effects of nanostructure on the hydrogen sorption properties of magnesium-based metallic compounds: A review[J].Crystals, 2018, 8(2): 106
[39] WAGEMANS R W P, VAN LENTHE J H, DE JONGH P E, et al.Hydrogen storage in magnesium clusters: Quantum chemical study[J].ChemInform, 2005, 127(47): 16675-1668
[40] RÉVÉSZ Á, KÁNYA Z, VEREBÉLYI T, et al.The effect of high-pressure torsion on the microstructure and hydrogen absorption kinetics of ball-milled Mg70 Ni30[J].Journal of Alloys and Compounds, 2010, 504(1): 83-88
[41] YUAN H, AN Y, XU G, et al.Hydriding behavior of magnesium-based hydrogen storage alloy modified by mechanical ballmilling[J].Materials Chemistry and Physics, 2004, 83(2/3):340-344
[42] LIU X, ZHOU L, LI W, et al.Preparation of Mg2 Ni hydrogen storage alloy materials by high energy ball milling[J].Advances in Materials Science and Engineering, 2022, 2022: 2661424
[43] 张秋雨, 任莉, 李映辉, 等.镁基固态储氢材料研究进展[J].科技导报, 2022, 40(23): 6-23 ZHANG Qiuyu, REN Li, LI Yinghui, et al.Solid state Mgbased hydrogen storage materials: Research progress and future perspective[J].Science & Technology Review, 2022, 40(23):6-23(in Chinese)
[44] MAO J, ZOU J, LU C, et al.Hydrogen storage and hydrolysis properties of core-shell structured Mg-MFx (M = V, Ni, La and Ce) nano-composites prepared by arc plasma method[J].Journal of Power Sources, 2017, 366: 131-142
[45] CHEN M, HU M, XIE X, et al.High loading nanoconfinement of V-decorated Mg with 1 nm carbon shells: Hydrogen storage properties and catalytic mechanism[J].Nanoscale, 2019, 11(20): 10045-10055
[46] LIU W, AGUEY-ZINSOU K F.Size effects and hydrogen storage properties of Mg nanoparticles synthesised by an electroless reduction method[J].Journal of Materials Chemistry A, 2014, 2(25): 9718-9726
[47] LIU W, AGUEY-ZINSOU K F.Hydrogen storage properties of in situ stabilised magnesium nanoparticles generated by electroless reduction with alkali metals[J].International Journal of Hydrogen Energy, 2015, 40(47): 16948-16960
[48] ZHANG X, LIU Y, REN Z, et al.Realizing 6.7 wt% reversible storage of hydrogen at ambient temperature with non-confined ultrafine magnesium hydrides[J].Energy & Environmental Science, 2021, 14(4): 2302-2313
[49] ZHANG S, GROSS A F, VAN ATTA S L, et al.The synthesis and hydrogen storage properties of a MgH2 incorporated carbon aerogel scaffold[J].Nanotechnology, 2009, 20(20): 204027
[50] 邹勇进, 向翠丽, 邱树君, 等.纳米限域的储氢材料[J].化学进展, 2013, 25(1): 115-121 ZOU Yongjin, XIANG Cuili, QIU Shujun, et al.Nanoconfined materials for hydrogen storage[J].Progress in Chemistry, 2013,25(1): 115-121(in Chinese)
[51] SUI Y, YUAN Z, ZHOU D, et al.Recent progress of nanotechnology in enhancing hydrogen storage performance of magnesiumbased materials: A review[J].International Journal of Hydrogen Energy, 2022, 47(71): 30546-30566
[52] GANGU K K, MADDILA S, MUKKAMALA S B, et al.Characteristics of MOF, MWCNT and graphene containing materials for hydrogen storage: A review[J].Journal of Energy Chemistry,2019, 30: 132-144
[53] CHEN Z, KIRLIKOVALI K O, IDREES K B, et al.Porous materials for hydrogen storage[J].Chem, 2022, 8(3): 693-716
[54] WANG Y, LAN Z, HUANG X, et al.Study on catalytic effect and mechanism of MOF (MOF=ZIF-8, ZIF-67, MOF-74) on hydrogen storage properties of magnesium[J].International Journal of Hydrogen Energy, 2019, 44(54): 28863-28873
[55] BOLARIN J A, ZOU R, LI Z, et al.MXenes for magnesiumbased hydrides: A review[J].Applied Materials Today, 2022,29: 101570
[56] LIU Y, DU H, ZHANG X, et al.Superior catalytic activity derived from a two-dimensional Ti3 C2 precursor towards the hydrogen storage reaction of magnesium hydride[J].Chemical Communications, 2016, 52(4): 705-708
[57] ALI W, LI X, YANG Y, et al.In situ formed Ti/Nb nanocatalysts within a bimetal 3D MXene nanostructure realizing long cyclic lifetime and faster kinetic rates of MgH2[J].ACS Applied Materials & Interfaces, 2023, 15(30): 36167-36178
[58] JAIN I P, LAL C, JAIN A.Hydrogen storage in Mg: A most promising material[J].International Journal of Hydrogen Energy, 2010, 35(10): 5133-5144
[59] GUO J, LI S, SU Y, et al.Theoretical study of hydrogen storage by spillover on porous carbon materials[J].International Journal of Hydrogen Energy, 2020, 45(48): 25900-25911
[60] GENG Z, WANG D, ZHANG C, et al.Spillover enhanced hydrogen uptake of Pt/Pd doped corncob-derived activated carbon with ultra-high surface area at high pressure[J].International Journal of Hydrogen Energy, 2014, 39(25): 13643-13649
[61] HUANG T, HUANG X, HU C, et al.MOF-derived Ni nanoparticles dispersed on monolayer MXene as catalyst for improved hydrogen storage kinetics of MgH2[J].Chemical Engineering Journal, 2021, 421: 127851
[62] ZHANG L, CHEN L, FAN X, et al.Enhanced hydrogen storage properties of MgH2 with numerous hydrogen diffusion channels provided by Na2 Ti3 O7 nanotubes[J].Journal of Materials Chemistry A, 2017, 5(13): 6178-6185
[63] PUKAZHSELVAN D, CAPURSO G, MADDALENA A, et al.Hydrogen storage characteristics of magnesium impregnated on the porous channels of activated charcoal scaffold[J].International Journal of Hydrogen Energy, 2014, 39(35): 20045-20053
[64] GAO H, SHI R, ZHU J, et al.Interface effect in sandwich like Ni/Ti3 C2 catalysts on hydrogen storage performance of MgH2[J].Applied Surface Science, 2021, 564: 150302
[65] WU Z, FANG J, LIU N, et al.The improvement in hydrogen storage performance of MgH2 enabled by multilayer Ti3 C2[J].Micromachines, 2021, 12(10): 1190
[66] POZZO M, ALFÈ D.Hydrogen dissociation and diffusion on transition metal (=Ti, Zr, V, Fe, Ru, Co, Rh, Ni, Pd, Cu,Ag)-doped Mg(0001) surfaces[J].International Journal of Hydrogen Energy, 2009, 34(4): 1922-1930
[67] CUI J, LIU J, WANG H, et al.Mg-TM (TM: Ti, Nb, V, co,Mo or Ni) core-shell like nanostructures: Synthesis, hydrogen storage performance and catalytic mechanism[J].Journal of Materials Chemistry A, 2014, 2(25): 9645-9655
[68] CHEN J, XIA G, GUO Z, et al.Porous Ni nanofibers with enhanced catalytic effect on the hydrogen storage performance of MgH2[J].Journal of Materials Chemistry A, 2015, 3(31):15843-15848
[69] HAN B, WANG J, TAN J, et al.First-principles study on the dehydrogenation thermodynamics and kinetics of Ti, Zr, V and Nb doped MgH2 [J].Journal of Energy Storage, 2024,83: 110612
[70] ZHANG L, ZHANG X, ZHANG W, et al.Nanoparticulate Zr-Ni: in situ disproportionation effectively enhances hydrogen cycling of MgH2[J].ACS Applied Materials & Interfaces, 2023,15(34): 40558-40568
[71] EL-ESKANDARANY M S, SHABAN E, ALDAKHEEL F, et al.Synthetic nanocomposite MgH2/5 wt.% TiMn2 powders for solidhydrogen storage tank integrated with PEM fuel cell[J].Scientific Reports, 2017, 7: 13296
[72] SINGH S, BHATNAGAR A, SHUKLA V, et al.Ternary transition metal alloy FeCoNi nanoparticles on graphene as new catalyst for hydrogen sorption in MgH2[J].International Journal of Hydrogen Energy, 2020, 45(1): 774-786
[73] WAN H, YANG X, ZHOU S, et al.Enhancing hydrogen storage properties of MgH2 using FeCoNiCrMn high entropy alloy catalysts[J].Journal of Materials Science & Technology, 2023, 149: 88-98
[74] BARKHORDARIAN G, KLASSEN T, BORMANN R.Catalytic mechanism of transition-metal compounds on Mg hydrogen sorption reaction[J].The Journal of Physical Chemistry B, 2006,110(22): 11020-11024
[75] LONG S, ZOU J, LIU Y, et al.Hydrogen storage properties of a Mg-Ce oxide nano-composite prepared through arc plasma method[J].Journal of Alloys and Compounds, 2013, 580: S167-S170
[76] GUEMOU S, GAO D, WU F, et al.Enhanced hydrogen storage kinetics of MgH2 by the synergistic effect of Mn3 O4/ZrO2 nanoparticles[J].Dalton Transactions, 2023, 52(3): 609-620
[77] ZHANG L, WANG K, LIU Y, et al.Highly active multivalent multielement catalysts derived from hierarchical porous TiNb2 O7 nanospheres for the reversible hydrogen storage of MgH2 [J].Nano Research, 2021, 14(1): 148-156
[78] XIAN K, WU M, GAO M, et al.A unique nanoflake-shape bimetallic Ti-Nb oxide of superior catalytic effect for hydrogen storage of MgH2[J].Small, 2022, 18(43): 2107013
[79] ZHANG X, ZHANG X, ZHANG L, et al.Ultrafast hydrogenation of magnesium enabled by tetragonal ZrO2 hierarchical nanoparticles[J].Materials Today Nano, 2022, 18: 100200
[80] 戴敏, 雷钢铁, 张钊, 等.五氧化二钒促进MgH2/Mg 室温吸氢[J].化学学报, 2022, 80(3): 303-309 DAI Min, LEI Gangtie, ZHANG Zhao et al.Room temperature hydrogen absorption of V2 O5 catalyzed MgH2/Mg [J].Acta Chimica Sinica, 2022, 80(3): 303-309(in Chinese)
[81] SAZELEE N A, IDRIS N H, MD DIN M F, et al.LaFeO3 synthesised by solid-state method for enhanced sorption properties of MgH2[J].Results in Physics, 2020, 16: 102844
[82] DAN L, HU L, WANG H, et al.Excellent catalysis of MoO3 on the hydrogen sorption of MgH2[J].International Journal of Hydrogen Energy, 2019, 44(55): 29249-29254
[83] MA Z, LIU J, ZHU Y, et al.Crystal-facet-dependent catalysis of anatase TiO2 on hydrogen storage of MgH2[J].Journal of Alloys and Compounds, 2020, 822: 153553
[84] HUANG H, YUAN J, ZHANG B, et al.A noteworthy synergistic catalysis on hydrogen sorption kinetics of MgH2 with bimetallic oxide Sc2 O3/TiO2[J].Journal of Alloys and Compounds, 2020,839: 155387
[85] SAZELEE N A, IDRIS N H, MD DIN M F, et al.Synthesis of BaFe12 O19 by solid state method and its effect on hydrogen storage properties of MgH2[J].International Journal of Hydrogen Energy, 2018, 43(45): 20853-20860
[86] IDRIS N H, MUSTAFA N S, ISMAIL M.MnFe2 O4 nanopowder synthesised via a simple hydrothermal method for promoting hydrogen sorption from MgH2[J].International Journal of Hydrogen Energy, 2017, 42(33): 21114-21120
[87] WANG L, HU Y, LIN J, et al.The hydrogen storage performance and catalytic mechanism of the MgH2-MoS2 composite[J].Journal of Magnesium and Alloys, 2023, 11(7): 2530-2540
[88] JIA Y, HAN S, ZHANG W, et al.Hydrogen absorption and desorption kinetics of MgH2 catalyzed by MoS2 and MoO2[J].International Journal of Hydrogen Energy, 2013, 38 ( 5 ):2352-2356
[89] WANG P, TIAN Z, WANG Z, et al.Improved hydrogen storage properties of MgH2 using transition metal sulfides as catalyst[J].International Journal of Hydrogen Energy, 2021, 46 ( 53):27107-27118
[90] FU Y, ZHANG L, LI Y, et al.Effect of ternary transition metal sulfide FeNi2 S4 on hydrogen storage performance of MgH2[J].Journal of Magnesium and Alloys, 2023, 11(8): 2927-2938
[91] ZHANG M, XIAO X, HANG Z, et al.Superior catalysis of NbN nanoparticles with intrinsic multiple valence on reversible hydrogen storage properties of magnesium hydride[J].International Journal of Hydrogen Energy, 2021, 46(1): 814-822
[92] TIAN Z, WANG Z, YAO P, et al.Hydrogen storage behaviors of magnesium hydride catalyzed by transition metal carbides[J].International Journal of Hydrogen Energy, 2021, 46 ( 80):40203-40216
[93] LAN Z, LIANG H, WEN X, et al.Experimental and theoretical studies on two-dimensional vanadium carbide hybrid nanomaterials derived from V4 AlC3 as excellent catalyst for MgH2[J].Journal of Magnesium and Alloys, 2023, 11(10): 3790-3799
[94] BHAT V V, ROUGIER A, AYMARD L, et al.Catalytic activity of oxides and halides on hydrogen storage of MgH2[J].Journal of Power Sources, 2006, 159(1): 107-110
[95] MALKA I E, PISAREK M, CZUJKO T, et al.A study of the ZrF4, NbF5, TaF5, and TiCl3 influences on the MgH2 sorption properties[J].International Journal of Hydrogen Energy, 2011,36(20): 12909-12917
[96] YANG L, ZENG W, LI Y Q.Advancements in the modification of magnesium-based hydrogen storage materials[J].Progress in Natural Science: Materials International, 2024, 34 ( 3 ):540-554
[97] LI Z, SUN L, XU F, et al.Modulated noble metal/2D MOF heterostructures for improved hydrogen storage of MgH2[J].Rare Metals, 2024, 43(4): 1672-1685
[98] GAO H, SHI R, SHAO Y, et al.Catalysis derived from flowerlike Ni MOF towards the hydrogen storage performance of magnesium hydride[J].International Journal of Hydrogen Energy,2022, 47(15): 9346-9356
[99] GEORGAKILAS V, OTYEPKA M, BOURLINOS A B, et al.Functionalization of graphene: Covalent and non-covalent approaches, derivatives and applications [J].Chemical Reviews,2012, 112(11): 6156-6214
[100] SHRINIWASAN S, KAR T, NEERGAT M, et al.Mg-C interaction induced hydrogen uptake and enhanced hydrogen release kinetics in MgH2-rGO nanocomposites [J].The Journal of Physical Chemistry C, 2018, 122(39): 22389-22396
[101] ZHANG J, YU X, MAO C, et al.Influences and mechanisms of graphene-doping on dehydrogenation properties of MgH2: Experimental and first-principles studies[J].Energy, 2015, 89:957-964
[102] YAO P, JIANG Y, LIU Y, et al.Catalytic effect of Ni@rGO on the hydrogen storage properties of MgH2[J].Journal of Magnesium and Alloys, 2020, 8(2): 461-471
[103] LIU B, ZHANG B, CHEN X, et al.Remarkable enhancement and electronic mechanism for hydrogen storage kinetics of Mg nano-composite by a multi-valence co-based catalyst[J].Materials Today Nano, 2022, 17: 100168
[104] MENG Q F, HUANG Y, YE J, et al.Electrospun carbon nanofibers with in situ encapsulated Ni nanoparticles as catalyst for enhanced hydrogen storage of MgH2[J].Journal of Alloys and Compounds, 2021, 851: 156874
[105] LI X, FU Y, XIE Y, et al.Effect of Ni/tubular g-C3 N4 on hydrogen storage properties of MgH2[J].International Journal of Hydrogen Energy, 2021, 46(66): 33186-33196
[106] LIU M, XIAO X, ZHAO S, et al.ZIF-67 derived Co@CNTs nanoparticles: Remarkably improved hydrogen storage properties of MgH2 and synergetic catalysis mechanism[J].International Journal of Hydrogen Energy, 2019, 44(2): 1059-1069
[107] LIU G, WANG L, HU Y, et al.Enhanced catalytic effect of TiO2@rGO synthesized by one-pot ethylene glycol-assisted solvothermal method for MgH2[J].Journal of Alloys and Compounds, 2021, 881: 160644
[108] LI F, HUANG Z, WANG Y, et al.Effect of MOF-derived nanoparticle-cumulated flower-like CoFe@C coated composites on hydrogenation/dehydrogenation performance of MgH2 [J].Chemical Engineering Journal, 2024, 485: 150008
[109] LIU J, LIU Y, LIU Z, et al.Effect of rGO supported NiCu derived from layered double hydroxide on hydrogen sorption kinetics of MgH2 [J].Journal of Alloys and Compounds, 2019,789: 768-776
[110] LYU J, M LIDER A, N KUDIIAROV V.An overview of progress in Mg-based hydrogen storage films[J].Chinese Physics B, 2019, 28(9): 098801
[111] SUNITHA Y, REDDY G L N, KUMAR S, et al.Studies on interdiffusion in Pd/Mg/Si films: Towards improved cyclic stability in hydrogen storage[J].Applied Surface Science, 2009, 256(5): 1553-1559
[112] KUMAR S, REDDY G L N, RAJU V S.Hydrogen storage in Pd capped thermally grown Mg films: Studies by nuclear resonance reaction analysis[J].Journal of Alloys and Compounds,2009, 476(1/2): 500-506
[113] REDDY G L N, KUMAR S.Hydrogen storage studies in Pd/Ti/Mg films[J].International Journal of Hydrogen Energy,2018, 43(5): 2840-2849
[114] MATHEUS F H, ZEPON G, OLIVEIRA V B, et al.Highly reactive hydrogen storage Mg2 Ni alloy prepared by mechanochemistry and H-cycling[J].International Journal of Hydrogen Energy, 2024, 51: 320-328
[115] QIN J, ZHOU X, FU Y, et al.Construction of Mg/Zr superlattice structure to achieve efficient hydrogen storage via atomicscale interaction in Mg-Zr modulation films[J].Acta Materialia, 2024, 263: 119470
[116] 吴海燕.Mg-Ni 储氢薄膜的控制制备、微观结构及脱氢性能[D].广州: 华南理工大学, 2021 WU Haiyan.Controlled preparation, microstructure and dehydrogenation properties of Mg-Ni hydrogen storage thin films[D].Guangzhou: South China University of Technology, 2021(in Chinese)
[117] 丁晓丽, 庞刚.“反应失稳” 复合储氢材料的研究进展[J].安徽工业大学学报(自然科学版), 2011, 28(2): 166-170 DING Xiaoli, PANG Gang.Research progress on reactive hydrides destabilized composites[J].Journal of Anhui University of Technology (Natural Science), 2011, 28(2): 166-170(in Chinese)
[118] VAJO J J, SALGUERO T T, GROSS A F, et al.Thermodynamic destabilization and reaction kinetics in light metal hydride systems[J].Journal of Alloys and Compounds, 2007, 446:409-414
[119] BÖSENBERG U, DOPPIU S, MOSEGAARD L, et al.Hydrogen sorption properties of MgH2-LiBH4 composites[J].Acta Materialia, 2007, 55(11): 3951-3958
[120] DING Z, SHAW L.Enhancement of hydrogen desorption from nanocomposite prepared by ball milling MgH2 with in situ aerosol spraying LiBH4 [J].ACS Sustainable Chemistry & Engineering, 2019, 7(17): 15064-15072
[121] DING Z, LI H, SHAW L.New insights into the solid-state hydrogen storage of nanostructured LiBH4-MgH2 system [J].Chemical Engineering Journal, 2020, 385: 123856
[122] DING Z, WU P, SHAW L.Solid-state hydrogen desorption of 2 MgH2 + LiBH4 nano-mixture: A kinetics mechanism study[J].Journal of Alloys and Compounds, 2019, 806: 350-360
[123] CHEN W, SUN Y, XU T, et al.Enhancing reversible hydrogen storage performance of 2LiBH4-MgH2 via in situ building heterogeneous nucleation sites[J].Rare Metals, 2024, 43(9):4367-4376
[124] DING X, ZHU Y, WEI L, et al.Synergistic hydrogen desorption of HCS MgH2 + LiAlH4 composite[J].Energy, 2013, 55:933-938
[125] ZHANG Y, XIAO X, LUO B, et al.Synergistic effect of LiBH4 and LiAlH4 Additives on improved hydrogen storage properties of unexpected high capacity magnesium hydride[J].The Journal of Physical Chemistry C, 2018, 122(5): 2528-2538
[126] KATO S, BORGSCHULTE A, BIELMANN M, et al.Interface reactions and stability of a hydride composite (NaBH4 + MgH2)[J].Physical Chemistry Chemical Physics, 2012, 14(23):8360-8368
[127] MAZLAN N S C, HALIM YAP F A, YAHYA M S, et al.Influence of TiF3 catalyst on the enhancement of hydrogen storage properties of Mg-Na-Al-Li-B composite system[J].Journal of Energy Storage, 2023, 71: 108097
[128] LIN W, XIAO X, WANG X, et al.Extreme high reversible capacity with over 8.0 wt% and excellent hydrogen storage properties of MgH2 combined with LiBH4 and Li3 AlH6[J].Journal of Energy Chemistry, 2020, 50: 296-306
[129] THIANGVIRIYA S, THONGTAN P, THAWEELAP N, et al.Heat charging and discharging of coupled MgH2-LaNi5 based thermal storage: Cycling stability and hydrogen exchange reactions[J].International Journal of Hydrogen Energy, 2024, 49:59-66
[130] LIANG G, HUOT J, BOILY S, et al.Hydrogen storage in mechanically milled Mg-LaNi5 and MgH2-LaNi5 composites[J].Journal of Alloys and Compounds, 2000, 297(1/2):261-265
[131] ZHOU C, FANG Z, BOWMAN R C.Stability of catalyzed magnesium hydride nanocrystalline during hydrogen cycling.part I:Kinetic analysis[J].The Journal of Physical Chemistry C,2015, 119(39): 22261-22271
[132] ZHANG L, CAI Z, YAO Z, et al.A striking catalytic effect of facile synthesized ZrMn2 nanoparticles on the de/rehydrogenation properties of MgH2[J].Journal of Materials Chemistry A,2019, 7(10): 5626-5634
[133] MÁRQUEZ J J, LEIVA D R, FLORIANO R, et al.Hydrogen storage in MgH2 LaNi5 composites prepared by cold rolling under inert atmosphere[J].International Journal of Hydrogen Energy,2018, 43(29): 13348-13355
[134] 邹建新, 丁文江.2023 年镁基储氢材料研究热点回眸[J].科技导报, 2024, 42(1): 204-216 ZOU Jianxin, DING Wenjiang.Review of research hotspots in magnesium-based hydrogen storage materials in 2023[J].Science & Technology Review, 2024, 42 ( 1): 204 - 216(in Chinese)