聚对苯二甲酸乙二醇酯(Polyethylene terephthalate,PET)作为典型的热塑性聚酯材料,凭借其优异的机械强度、显著的热稳定性及突出的光学透明性[1],已成为纺织工业[2]、包装工程[3]及食品科学领域的关键基础材料。 该材料的工业化进程可追溯至1941年英国化学家Whinfield和Dickson提出的合成专利,随后由杜邦公司完成技术转化并于1951年实现规模化生产[4]。 截至2024年末,全球PET年需求量已突破70 Mt量级,其生产网络呈现全球化分布特征,有效支撑了现代工业体系的材料需求。 然而,该材料的全生命周期管理面临严峻挑战——基于其低成本加工特性,大量短周期消费品在单次使用后即被废弃,导致全球范围内塑料固废激增与资源错配问题并存[5]。 我国当前PET闭环回收体系仍处于相对滞后状态(图1),约68%的废弃材料通过填埋或焚烧等热值利用效率低下的方式处理[6,7],这不仅造成二次能源浪费,更引发土壤微塑料污染等环境风险[8,9]。 因此,构建PET高效循环利用技术体系已成为实现材料领域可持续发展的关键。
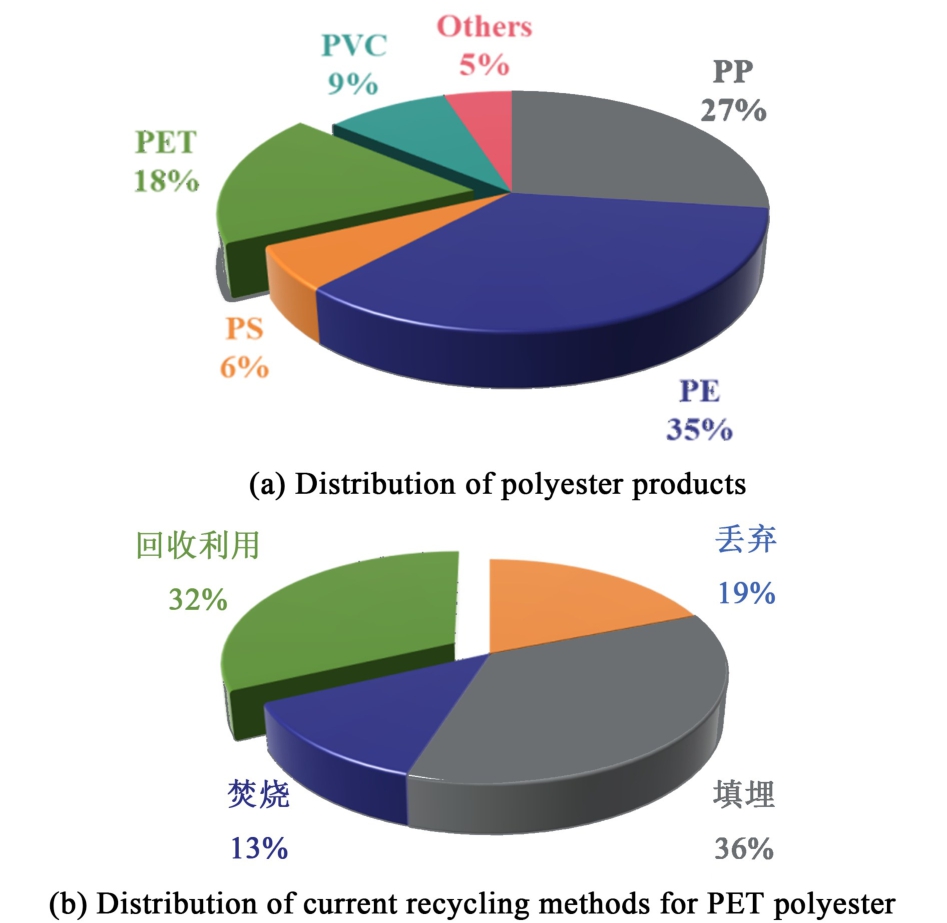
图1 聚酯产物的分布情况和目前PET聚酯的回收方式分布
Fig.1 Distributions of polyester products and the current recycling methods for PET polyester
1 PET 的现行回收技术
PET回收技术体系可分为4类基础路径(图2):物理回收(Mechanical recycling)[10]、热化学转化(Thermochemical conversion)[11]、生物降解(Biological degradation)[12]及化学解聚(Chemical depolymerization)[13]。 其中物理回收通过熔融挤出等基础物理改性处理实现材料再生,虽因操作简便占据主流应用,但其反复加工导致的材料性能不可逆劣化严重制约再生品价值[14]。 热化学转化技术基于PET高热值特性(23 ~28 kJ·g-1)进行能量回收,虽然提供简易的能量转化路径,但存在碳足迹增加及经济可行性不足等固有缺陷。 生物降解技术依托特异性水解酶(如IsPETase、LCC等)在温和反应条件下的催化作用实现材料降解,但受限于酶活性稳定性及反应周期较长等技术瓶颈,其工业化应用仍需突破。 相比之下,化学解聚技术通过选择性断键技术(如水解、糖酵解等)实现PET可控解聚,在特定溶剂体系与催化系统作用下,可将材料高效转化为对苯二甲酸衍生物等高值化学品。 该技术路线因产物价值提升潜力显著及闭环循环可行性突出,已被证实具有显著的循环经济价值,目前正加速向工业化应用阶段推进。
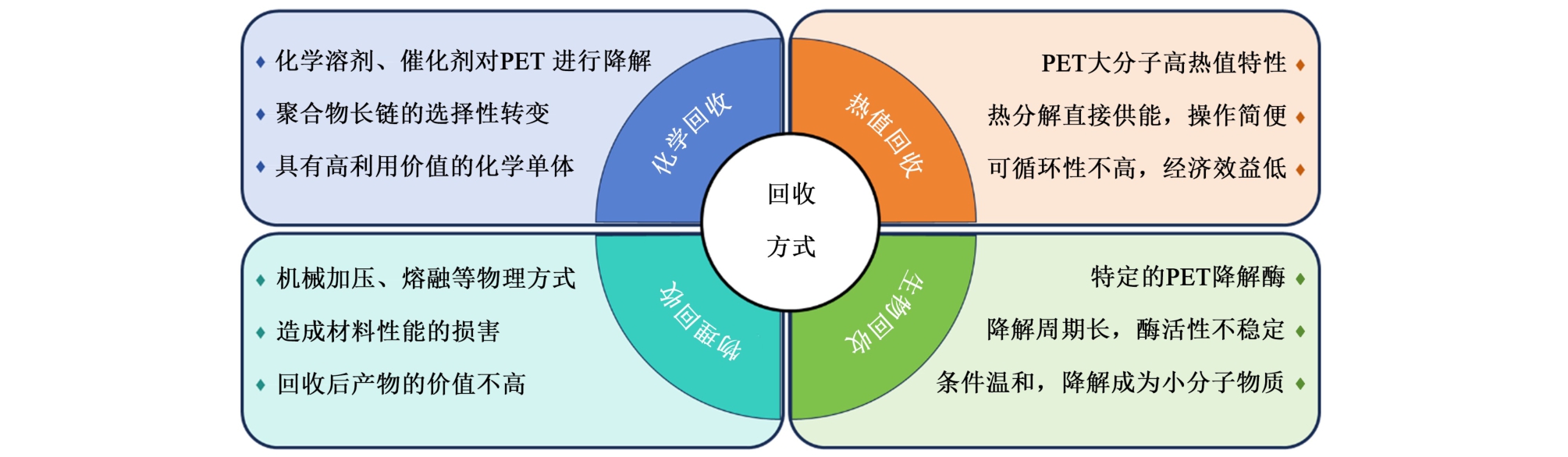
图2 现行PET回收技术的优势与缺陷
Fig.2 Advantages and shortcomings of the current PET recycling technologies
PET的化学回收技术依据反应介质与断裂机制差异可分为5大类:水解(Hydrolysis)、醇解(Methanolysis)、糖酵解(Glycolysis)、氨解(Aminolysis)及氢解(Hydrogenolysis)。 前3类方法遵循酰氧基断裂的双分子亲核取代机制(图3),其核心路径为亲核试剂(H2O、ROH或EG)攻击酯键羰基碳,引发电子重排并断裂C—O键[15]。 具体而言:(1)水解反应在酸性/碱性条件下生成对苯二甲酸(TPA)和乙二醇(EG),但TPA的强极性导致其易与金属离子络合,后续纯化能耗较高;(2)醇解以甲醇为介质生成对苯二甲酸二甲酯(DMT),需通过酯交换步骤再生PET,存在工艺链延长缺陷;(3)糖酵解以EG为反应介质,通过可逆酯交换反应直接生成对苯二甲酸双羟乙酯(BHET)单体,其产物与原生PET合成原料同源,可实现“单体-聚合物”的闭环循环,且BHET结晶特性显著简化了分离纯化流程[16]。 相较之下,氨解通过胺基亲核攻击生成对苯二甲酸二酰胺衍生物[17],而氢解在H2氛围下催化断裂C—O键生成二甲苯等高值化学品[18],这2类方法虽具有产物功能化潜力,但通常需要贵金属催化剂(如Ru/C)或超临界条件(>300 ℃),其工业化经济性与能耗控制面临严峻挑战[19]。 因此,糖酵解凭借其温和条件、与现有PET产业链的高度兼容性以及BHET单体的直接利用,成为目前唯一实现千吨级工业化应用的PET化学回收路线。
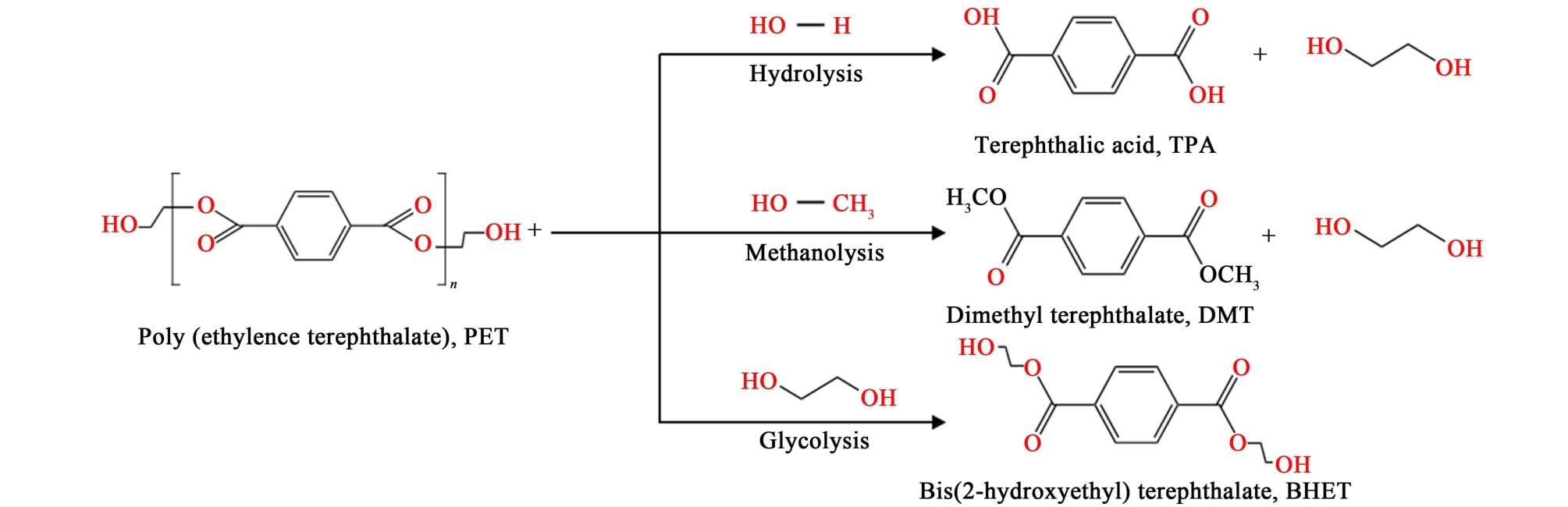
图3 PET化学解聚反应路径以及目标产物
Fig.3 PET chemical depolymerization reaction pathways and target products
2 PET 的糖酵解解聚
作为PET化学回收领域工业化应用最成熟的技术路线之一,糖酵解凭借其较低的工艺设备要求及可控的能耗成本,展现出显著的工业化优势。 动力学研究进一步揭示其多阶段解聚机制[20]:初始阶段,PET大分子链在过量乙二醇(EG)溶胀作用下发生非晶区优先解离,生成末端含羟基的低聚物;随着反应进程推进,酯交换反应主导的链式解聚逐步将低聚物转化为目标产物BHET。 值得注意的是,解聚-再聚合动态平衡的存在导致BHET单体存在临界停留时间窗口,超过该阈值后逆反应速率显著上升。 这一特性对工艺参数精确控制提出挑战,同时也驱动研究者开发抑制逆反应的高选择性催化剂,或通过构建连续化反应体系实现产物即时分离,从而突破传统间歇式反应的热力学限制。
2.1 金属盐类催化剂
金属盐类催化剂作为PET糖酵解反应中应用最早且研究最广泛的催化体系,其催化效能与金属离子的价态及电子结构密切相关。 研究表明,不同价态的金属离子通过独特的电子传递机制和配位作用,显著影响PET解聚反应的动力学过程及产物分布。 根据金属离子价态的差异,其催化机理可系统归纳为3类。
2.1.1 离子极化构建醇盐配位活化机制
一价金属离子(Na+和K+等)的离子极化机制:此类碱金属离子通过与醇类溶剂(如乙二醇)形成稳定的金属醇盐配合物(M+-OR-),显著改变溶剂分子的电子分布。 具体而言,金属离子与醇羟基氧原子通过静电相互作用形成配位共价键,导致羟基氧的电子云密度向金属中心偏移,从而增强其亲核攻击能力(图4)。 这种电子结构的重构使得羟基氧更易对PET分子链中酯基的羰基碳(C  O)发起亲核进攻,促使β-消除反应的发生[21]。 实验证实,该过程遵循SN2双分子亲核取代机理,金属离子的半径大小直接影响配合物稳定性,其中K+相较于Na+形成的金属醇盐具有更优的催化活性。
O)发起亲核进攻,促使β-消除反应的发生[21]。 实验证实,该过程遵循SN2双分子亲核取代机理,金属离子的半径大小直接影响配合物稳定性,其中K+相较于Na+形成的金属醇盐具有更优的催化活性。
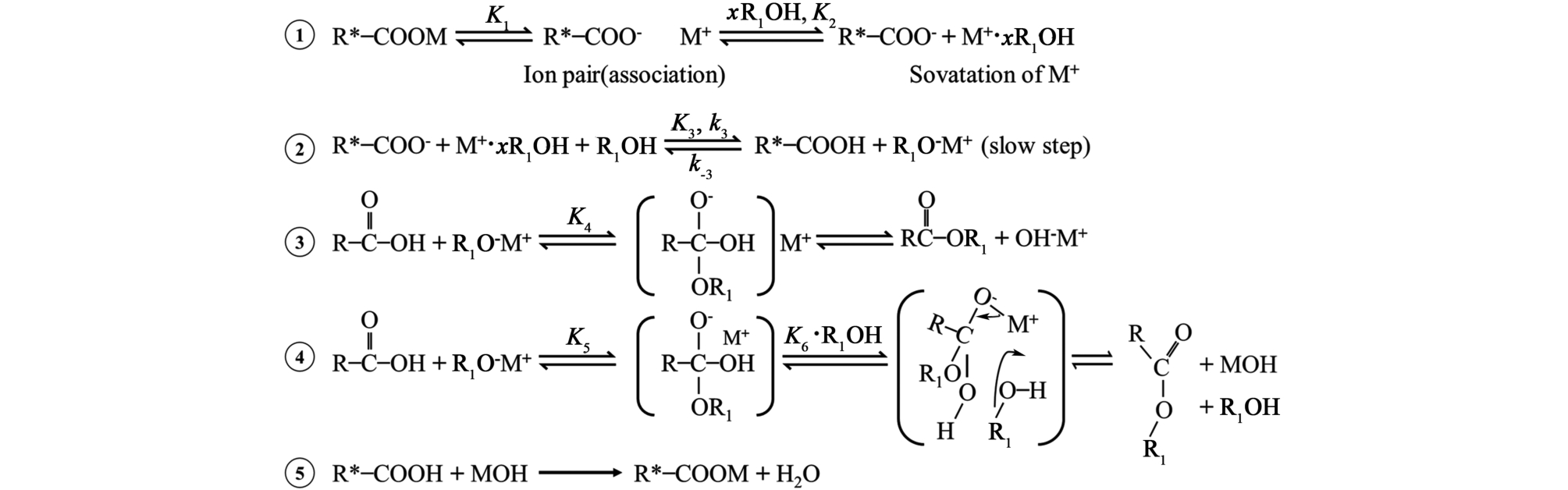
图4 1和2价金属糖酵解机理[21]
Fig.4 Mechanism of glycolysis catalyzed by mono- and di-valent metals[21]
2.1.2 路易斯酸调控羰基电子云密度机制
2 价过渡金属离子(Ni2+、Zn2+和Co2+等)的路易斯酸活化机制:具有d8电子构型的2价金属离子作为典型的路易斯酸,通过空d轨道与PET酯基中羰基氧的孤对电子发生配位作用[22]。 这种配位作用导致C  O双键的电子云向金属中心偏移,显著增强羰基碳原子的电正性(δ+)。 密度泛函理论(DFT)计算表明,当Zn与羰基氧配位时,C
O双键的电子云向金属中心偏移,显著增强羰基碳原子的电正性(δ+)。 密度泛函理论(DFT)计算表明,当Zn与羰基氧配位时,C  O键长由0.122延伸至0.124 nm,证明羰基的活化程度显著提升[23]。 同时,金属离子的电荷密度与其催化活性呈正相关,其中Zn2+具有较高的电荷密度,因此2价金属离子中表现出良好的催化活性。 Vaidya等[24]报道了醋酸锌催化PET与乙二醇(EG)的酯交换反应,成功实现聚酯解聚并合成聚酯多元醇。随后的系统性研究表明[25],2价金属醋酸盐(Zn2+、Co2+、Mn2+和Pb2+)的催化活性呈现显著差异性,其活性顺序遵循Zn2+>Mn2+>Co2+>Pb2+的规律。 在优化反应条件[196 ℃,m(EG)/m(PET)为5,催化剂负载量1%]下,醋酸锌体系可将BHET单体收率提升至87.30%,展现出优异的解聚动力学特性[26]。值得注意的是,金属氯化物(如ZnCl2)与醋酸盐具有相似的Lewis酸催化机制[27],证实金属离子的电子结构特性是决定催化活性的关键因素。 尽管2价金属盐展现出高效催化性能,但其环境风险引发学界关注。 Shukla等[28] 率先采用碱金属碳酸盐(Na2CO3、NaHCO3)构建绿色催化体系,在190 ℃、m(EG)/m(PET)为2的条件下反应8 h,BHET收率达62.18%。 尽管催化效率较传统金属盐体系降低约25%,但其生物相容性优势为食品级再生PET生产提供了新路径。
O键长由0.122延伸至0.124 nm,证明羰基的活化程度显著提升[23]。 同时,金属离子的电荷密度与其催化活性呈正相关,其中Zn2+具有较高的电荷密度,因此2价金属离子中表现出良好的催化活性。 Vaidya等[24]报道了醋酸锌催化PET与乙二醇(EG)的酯交换反应,成功实现聚酯解聚并合成聚酯多元醇。随后的系统性研究表明[25],2价金属醋酸盐(Zn2+、Co2+、Mn2+和Pb2+)的催化活性呈现显著差异性,其活性顺序遵循Zn2+>Mn2+>Co2+>Pb2+的规律。 在优化反应条件[196 ℃,m(EG)/m(PET)为5,催化剂负载量1%]下,醋酸锌体系可将BHET单体收率提升至87.30%,展现出优异的解聚动力学特性[26]。值得注意的是,金属氯化物(如ZnCl2)与醋酸盐具有相似的Lewis酸催化机制[27],证实金属离子的电子结构特性是决定催化活性的关键因素。 尽管2价金属盐展现出高效催化性能,但其环境风险引发学界关注。 Shukla等[28] 率先采用碱金属碳酸盐(Na2CO3、NaHCO3)构建绿色催化体系,在190 ℃、m(EG)/m(PET)为2的条件下反应8 h,BHET收率达62.18%。 尽管催化效率较传统金属盐体系降低约25%,但其生物相容性优势为食品级再生PET生产提供了新路径。
2.1.3 多齿配位诱导酯键断键机制
3 价和4价金属离子(Ti4+、Sb3+等)的配体交换-断键机制:高电荷密度的3价和4价金属离子通过多齿配位模式与PET分子中的酯基形成五元环或六元环过渡态[29]。 具体反应路径包括:(1)金属离子与酯基氧原子发生配位,形成稳定四面体中间体(如氧负离子过渡态),减少能量壁垒;(2)配位作用诱导酯键中C O键的电子云重新分布,导致键能降低;(3)在热力学驱动下,金属中心通过配体交换过程夺取酯基氧原子,促使酯键的断裂。
O键的电子云重新分布,导致键能降低;(3)在热力学驱动下,金属中心通过配体交换过程夺取酯基氧原子,促使酯键的断裂。
钛基催化剂由于其独特结构,通过多齿配位模式与PET分子中的酯基形成五元环或六元环过渡态,在PET糖酵解领域取得重要突破[30,31]。 Wen等[32]通过水热合成法开发了苯甲酸钛16(Ti-BA)催化剂,并创新性地采用一锅法构建异苯二酸钛(Ti-IPA)催化体系[图5(a)]。 通过系统性优化钛源选择(钛酸四丁酯、钛酸异丙酯)及溶剂体系(乙醇、乙二醇等),成功实现了Ti-IPA的可控合成。 结合响应面法(RSM) 对反应参数进行多变量分析[图5(b)],确定最适宜工艺条件为: m (EG)/m(PET)为3.59、反应温度217 ℃、时间3.3 h、Ti-BA负载量2%,此时BHET收率达90.01%。 进一步研究表明[33],Ti-IPA体系在优化条件(催化剂负载量0.86%、EG用量13 mL、温度194 ℃、时间3 h)下仍可实现84.86%的BHET产率。 对比分析显示,该催化剂在循环稳定性(经5次重复使用后活性保持率>92%)、反应动力学及产物选择性等方面均优于传统金属盐体系,其单位质量PET处理成本较商业化催化剂降低17.3%,展现出显著的工业化应用前景。 这一突破性进展为开发高效、可持续的聚酯循环利用技术提供了新材料基础。
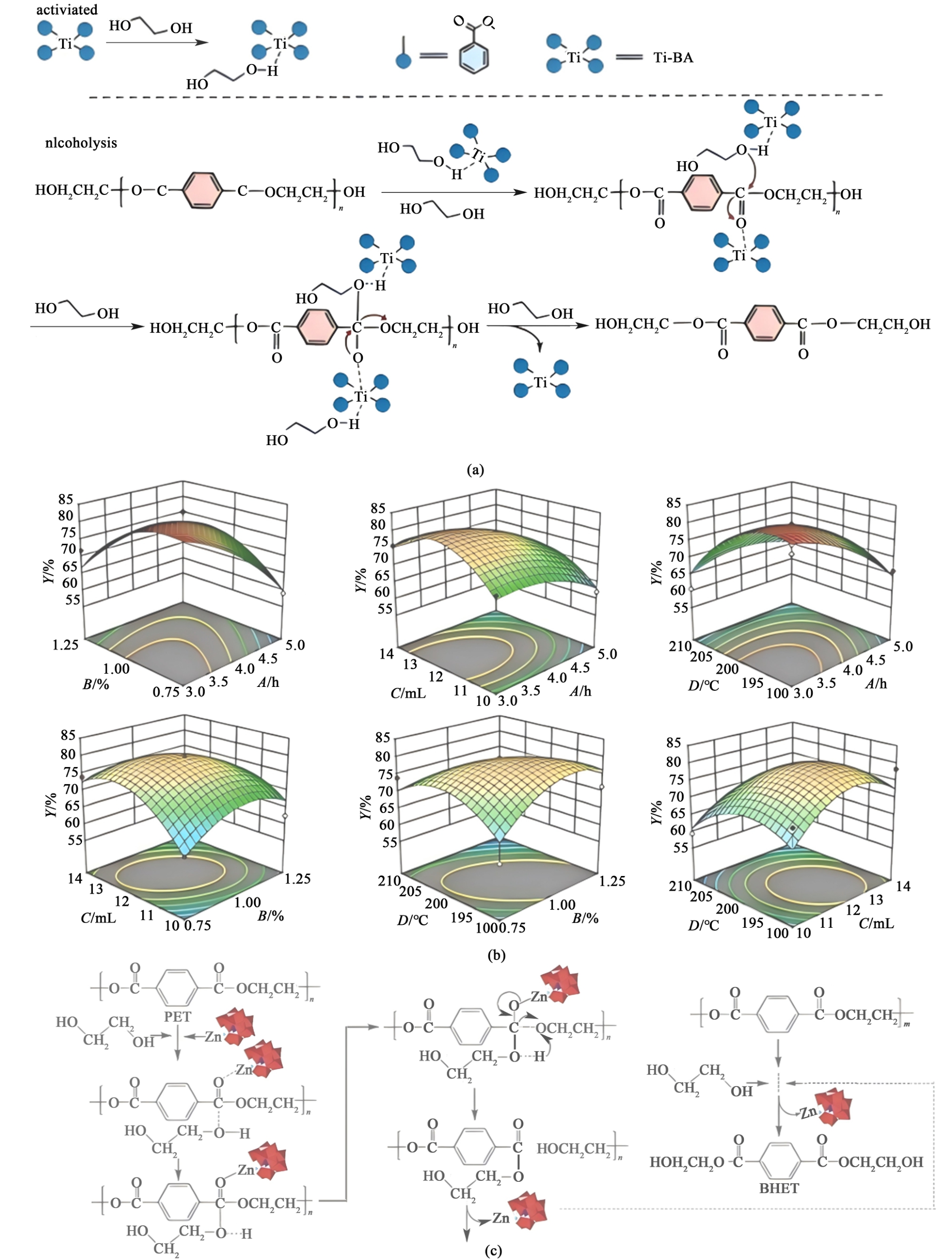
图5 (a)Ti-BA催化PET醇解反应机理[32];(b)不同条件对Ti-IPA催化体系影响的RSM图[33];(c)SiW11Zn催化PET解聚机理[35]
Fig.5 (a) Mechanism of Ti-BA-catalyzed PET glycolysis reaction[32]; (b) RSM plots of the effect of different conditions on the Ti-IPA catalytic system[33]; (c) Mechanism of SiW11Zn-catalyzed PET depolymerization[35]
2.1.4 新型金属盐催化体系
多金属氧酸盐(POMs)作为具有可调控酸性和氧化还原特性的纳米级金属氧簇[34],为PET催化解聚提供了新思路。 过渡金属取代型POMs通过引入Zn2+、Mn2+等活性位点,有效增强表面电荷密度以强化底物吸附能力。 Geng等[35] 开发的Keggin型POMs[K6SiW11MO39(H2O),M=Zn2+、Mn2+等]体系,不仅通过金属-EG配位作用促进酯交换反应动力学[图5(c)],更创新性地实现催化剂与溶剂的同步循环利用——经5次循环后仍保持85%以上催化活性,这一自稳定特性显著降低了操作成本。
虽然金属盐催化体系表现出优异的催化能力,但仍面临着双重挑战:(1)均相催化机制导致催化剂难以高效分离回收,增加工艺复杂性和再生成本;(2)重金属离子残留可能对再生PET的食品/医药领域应用形成制约。 因此,开发兼具高活性、易回收和环境友好特性的新型催化体系,仍是该领域亟待突破的关键科学问题。
2.2 离子液体类催化剂
为克服传统催化剂的局限性,离子液体(ILs)作为新型催化介质逐渐进入公众的研究视野。 离子液体类催化剂根据其所含组分不同又分为金属离子液体与非金属离子液体,所对应的解聚机理也具有一定的差异。
2.2.1 离子液体(ILs)催化体系的作用机制
Ju等[36]对24种不同阴离子和阳离子对的咪唑基和叔铵基离子液体研究(图6),通过对ILs与二聚体之间的相互作用进行密度泛函理论(DFT)计算去探究ILs对糖酵解PET相互作用的影响。 其中金属ILs催化剂的机理核心在于阴阳离子协同作用。阴离子(如Cl-)通过与EG中羟基氢的相互作用,增强羟基氧的亲核性;阳离子则通过活化PET长链中的羰基碳,使羰基中的碳显正电性,更易被EG中的羟基氧攻击。 同时,金属离子作为路易斯酸进一步活化羰基,稳定反应中间体,促进酯键断裂并形成单体BHET[37]。 此类催化剂因阴阳离子与金属的协同作用表现出高效催化活性,但金属的引入可能增加成本或环境负担。
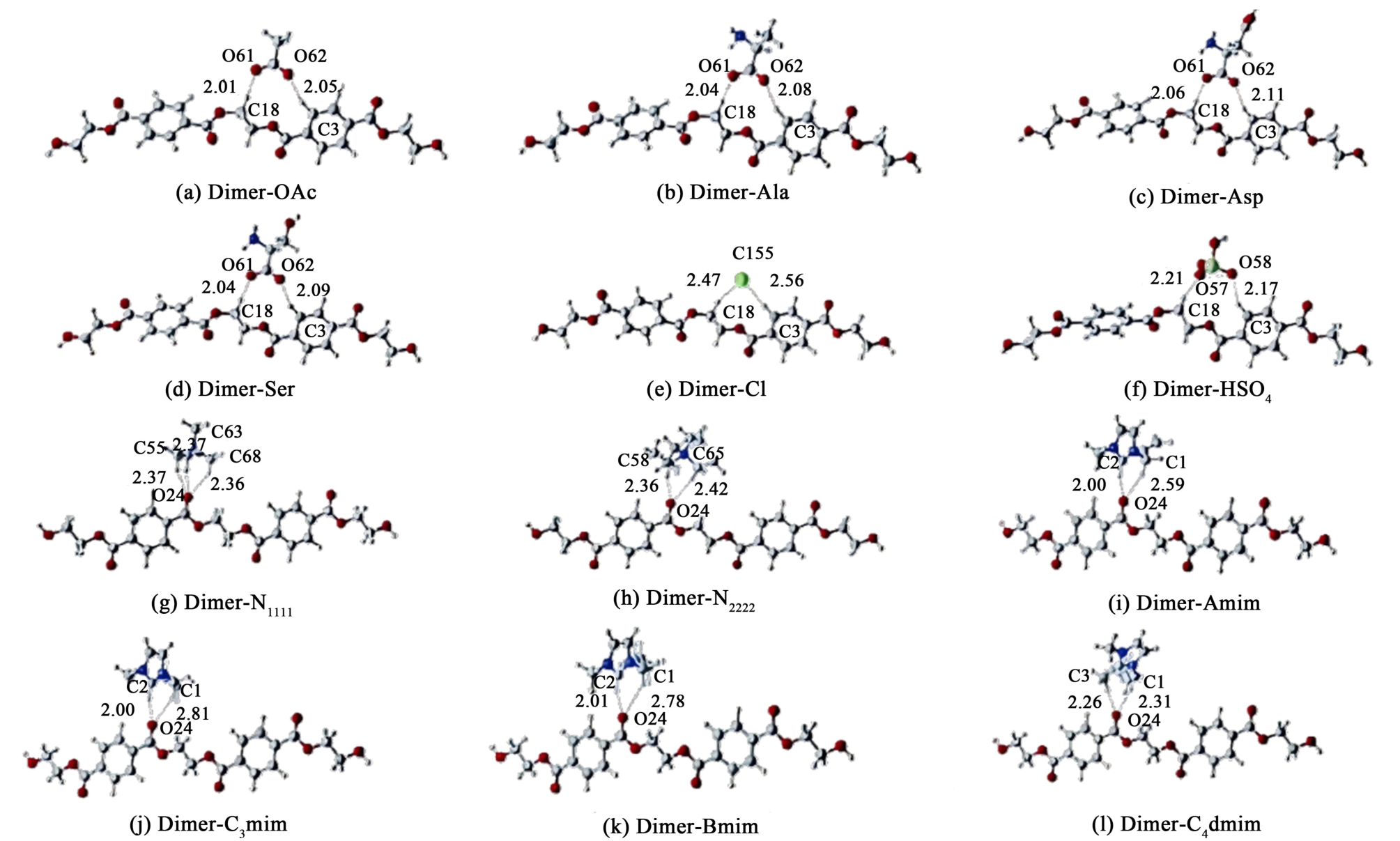
图6 (a ~f)优化后阴离子-二聚体的理论模型;(g ~l)优化后阳离子离子-二聚体的理论模型 (虚线表示氢键的形成距离以Å 为单位)[36]
Fig.6 (a—f) Theoretical models of optimized anionic-dimers; (g—l) Theoretical models of optimized cationic-ionic-dimers (dashed lines indicate the formation of hydrogen bonds, distance in Å)[36]
非金属ILs催化剂的催化机理主要由阳离子主导。 阳离子通过静电作用攻击PET的羰基氧,极化C O键,使羰基碳更易接受EG羟基氧的亲核进攻,从而断裂酯键并生成新键。 重复此过程可实现PET长链的逐步降解,最终形成目标单体[38]。 此类催化剂无需金属参与,合成简单且避免金属残留问题,但其催化效率通常低于金属ILs,且反应条件要求较高。
O键,使羰基碳更易接受EG羟基氧的亲核进攻,从而断裂酯键并生成新键。 重复此过程可实现PET长链的逐步降解,最终形成目标单体[38]。 此类催化剂无需金属参与,合成简单且避免金属残留问题,但其催化效率通常低于金属ILs,且反应条件要求较高。
2.2.2 离子液体催化 PET糖酵解的技术进展
Wang等[39]在2009年首次提出了使用离子液体类催化剂对PET的糖酵解反应,采用1-丁基-3-甲基咪唑卤化物([Bmim]X, X=Cl/Br/HSO4/H2PO4)体系催化PET糖酵解以来,离子液体(Ionic Liquids, ILs)作为绿色催化介质在聚酯解聚领域持续发展。 该团队在195 ℃、m(EG)/m(PET)= 5、反应6 h条件下实现PET转化率>99%,BHET收率达90% 以 上。 Yue等[40] 合 成 了[Bmim] ZnCl3和[Bmim]MnCl3,2种金属离子液体,由于Zn2+与Mn2+的加入,在190 ℃,催化剂添加量为0.16%时,就可以高效地催化PET降解,BHET产率可以达到83.3%。 并且实验表明2种催化剂在共同使用时,表现出更好的催化效果,表明2种金属离子之间会存在某种协同作用,促进反应的进行。 但体系中卤素残留引发的环境风险制约其实际应用。 为此,Zhou等[41]通过改变引入其他阴离子,开发无氯金属醋酸盐ILs,其中[deim][Zn(OAc)3]在180 ℃、m(EG)/m(PET)= 6、2.5 h条件下将PET转化率提升至98.05%,BHET选择性达70.94%。 该工作首次证实无氯金属醋酸盐ILs兼具环境友好性与高效催化性能,为发展绿色无氯PET化学回收技术提供了理论依据与工艺范式,具有显著的工业应用潜力。
为进一步优化催化效率,Wang等[42]系统研究阳离子结构效应,发现1-烯丙基-3-甲基咪唑氯化金属盐([amim][MCl3], M=Zn/Co)。 通过结合原位红外技术表明,因其阳离子空间位阻降低及缺电子特性(烯丙基共轭效应),显著增强对PET羰基氧的亲电攻击能力[图7(a)]。 实验表明,[amim][ZnCl3]在175 ℃、常压、75 min条件下即可实现PET完全转化,BHET选择性达80.1%,且产物可通过简单相分离获得质量分数>99%。 然而,金属离子的引入虽提升催化活性,却带来二次污染风险及产物色度问题。 针对此瓶颈,Zhang等[43]设计出对苯二甲酸基ILs(如[EMIm]2TPA)。 其阴离子TPA与PET结构单元同源,通过π-π 堆积效应定向吸附于PET表面,同时羧基与EG形成氢键网络降低活化能。 在197 ℃、106 min条件下实现PET 100%转化及83.6%的BHET收率,且催化剂经15次循环后活性保持率>95%。 所得BHET再聚合生成的rPET色度(L*值>85)显著优于金属基体系,证实无金属ILs在产物品质控制方面的优势[图7(b)]。 Zhang等[44]进一步开发全有机磷酸酯ILs,通过量子化学计算阐明其作用机制:磷酸基团与PET羰基形成强偶极-偶极相互作用,促使EG对羰基碳的亲核攻击。 在200 ℃、2 h条件下实现PET完全解聚,BHET产率40.80%,表观活化能(89.73 kJ·mol-1)较传统金属盐体系降低约25%。 尽管产物收率尚待提升,但其环境兼容性为闭环回收提供新思路。
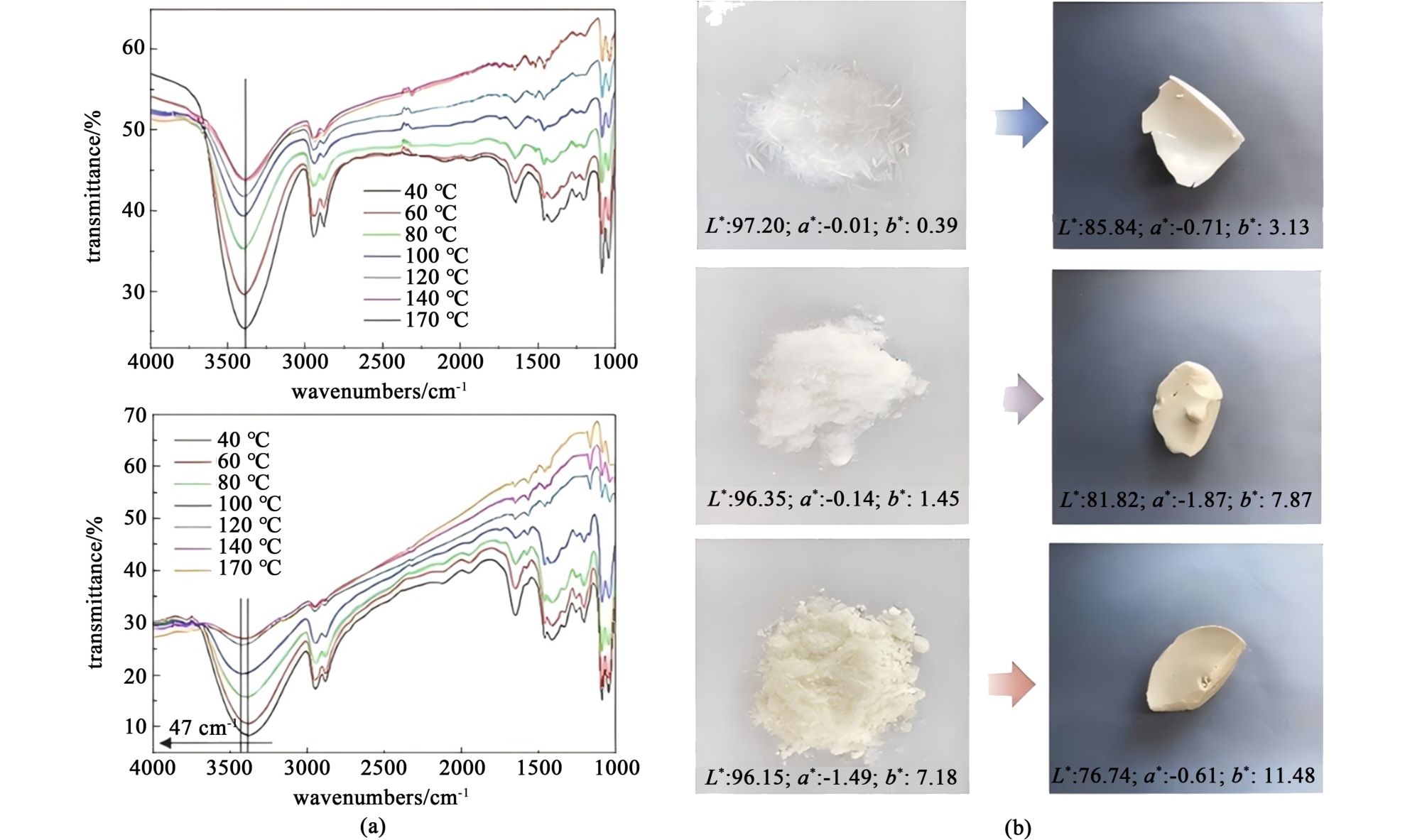
图7 (a)ILs催化剂糖酵解反应的原位红外光谱[42];(b)不同ILs催化剂降解所得到的BHET与rPET图[43]
Fig.7 (a) In situ infrared spectra of glycolysis reaction of ILs catalysts[42]; (b) BHET vs rPET plots obtained from the degradation of different ILs catalysts[43]
2.2.3 低共熔溶剂(DES)的绿色催化优势
随着对ILs本征性质的深入认知,研究者发现传统认知中ILs的“绝对绿色”属性存在理论局限。大量研究表明,部分ILs实际具有挥发性、易燃性及生物毒性,这种特性异质性源于其阳离子-阴离子的组合多样性。 在此背景下,低共熔溶剂(DES)作为新型绿色介质进入研究视野,其优势体现在可生物降解性、制备经济性及热稳定性等方面[45]。 DES由氢键受体(HBA)和氢键供体(HBD)按固定化学计量比组成[图8(a)],形成二元或三元混合体系,其冰点低于各组分的冰点[46]。 通过氢键网络与路易斯酸碱协同作用实现催化[47]。 其中,DES的氢键供体(如尿素)与EG羟基氢形成动态氢键,增强羟基氧的亲核性;同时,其组分中的金属离子(如Zn2+)作为路易斯酸配位PET的羰基氧,极化酯键以促进攻击。 氢键网络还可稳定中间体,降低反应能垒。Abbott等[48]通过混合2种具有高冰点的固体物质[氯化胆碱(ChCl)和尿素]首次制备出DESs。 2015年Wang等[49]开发的尿素/ZnCl2 DES体系应用于PET的糖酵解反应,在190 ℃、30 min内实现PET完全转化,收率达83.2%。 这种优异性能可能是由于DESs与EG之间形成的氢键和配位键之间的协同催化作用。 Liu等[50]通过系统研究1,3-DMU/Zn(OAc)2 DES的催化机制,发现尿素衍生物氨基的碱度与空间位阻显著影响催化活性[图8(b)],金属盐与有机组分间的酸碱协同作用使体系在190 ℃、20 min条件下达成100%的PET转化率,BHET收率82%。 动力学分析表明该过程符合收缩核模型,表观活化能为148.89 kJ·mol-1。 Li等[51]通过构建L-脯氨酸(Pro)及其衍生物与金属盐协同作用的DESs催化体系,实现了废弃PET的高效糖酵解及产物高值化利用。 实验筛选出Pro/Zn(Ac)2为最适宜催化剂,在210 ℃、常压、15 min的优化条件下[催化剂负载量2%,m(BDO)/m(PET)为5](BDO为1,4-丁二醇),实现PET完全解聚,获得67.1%的BHBT收率,并将解聚产物BHET与BHBT作为扩链剂,制备芳香族聚氨酯弹性体(PUEs),证实PET糖酵解产物在工程材料领域的应用潜力。该工作为PET闭环回收提供了新型催化体系设计策略,同时拓展了再生高分子材料的高性能化途径。
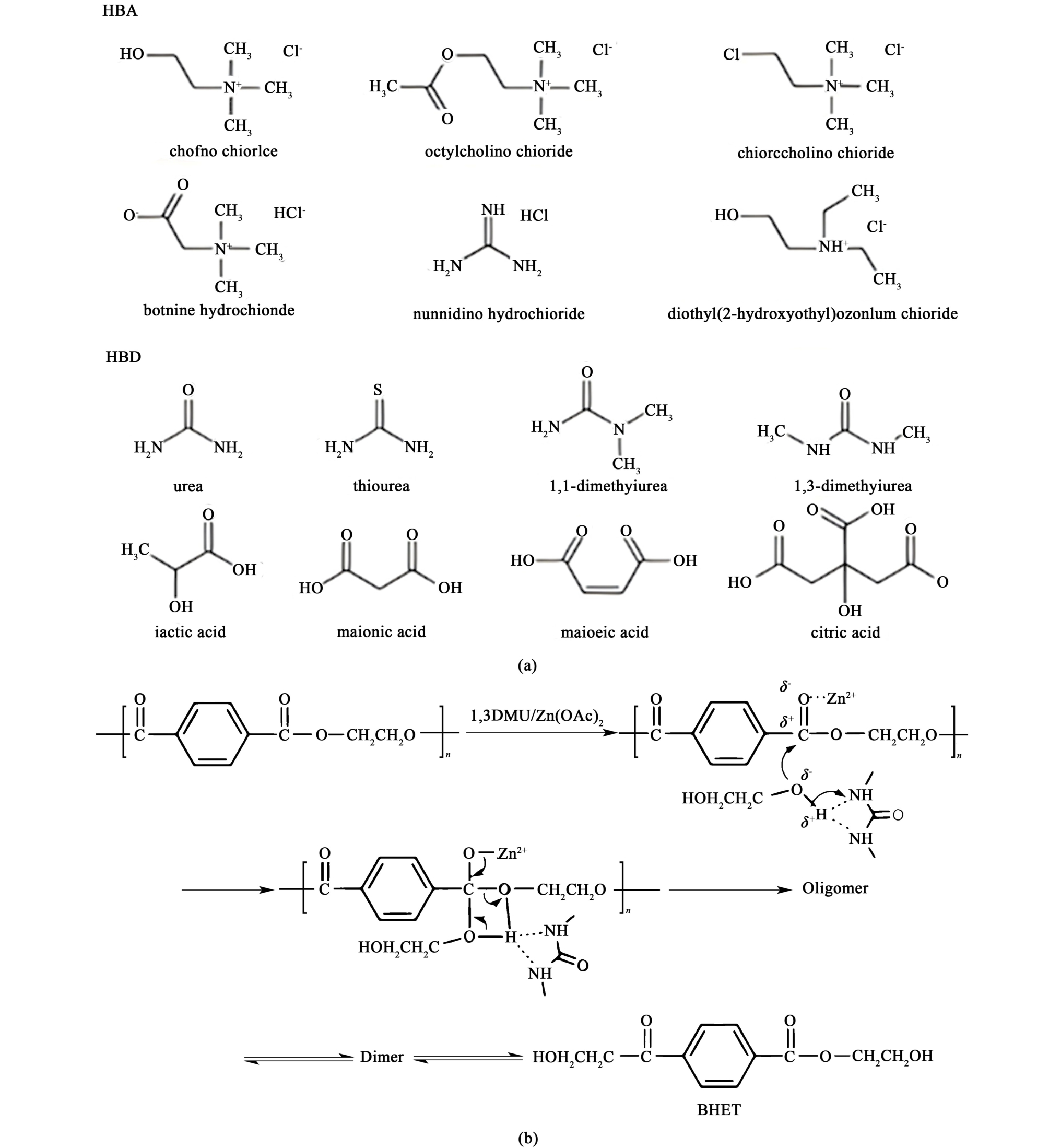
图8 (a)常见的DESs的氢键受体与氢键供体[46];(b)1,3-DMU/Zn(OAc)2催化PET糖酵解的反应机制[50]
Fig.8 (a) Hydrogen bond acceptors and hydrogen bond donors of common DESs[46]; (b) Reaction mechanism of 1,3-DMU/Zn(OAc)2-catalyzed PET glycolysis[50]
DESs体系通过氢键重构破坏PET结晶结构,其绿色合成工艺与高效催化性能为工业化应用提供了新方向。 然而,金属基ILs的潜在生态毒性及DESs体系的长周期稳定性仍需深入评估。
2.3 非均相类催化剂
针对均相催化剂的分离难题,近年来非均相催化体系发展迅速。 非均相催化剂在PET糖酵解反应中通过表面酸性位点活化、孔隙限域效应及金属-配体协同作用实现高效催化:其表面Bronsted酸(如沸石的羟基)或Lewis酸位点(如ZIF-8的Zn2+)通过质子化或配位作用极化PET的羰基键,增强乙二醇(EG)羟基氧的亲核攻击能力;微孔/介孔结构选择性吸附反应物并限域反应空间,提升局部浓度与传质效率,而金属-配体协同能够进一步稳定过渡态并降低活化能。
2.3.1 沸石催化剂
Shukla等[52]研究发现γ 沸石在197 ℃、EG回流条件下反应8 h可获得65%的BHET收率,虽低于均相体系,但其5次循环后活性保持率超90%,展现出良好的工业适用性。 Yang等[53]通过低温无模板绿色合成策略制备了具有高比表面积和开放孔道结构的100-FAU催化剂。 该催化剂具有显著增强的Lewis酸-碱双功能特性及活性位点可及性,这有效解决了传统沸石催化剂在PET降解中存在的酸性位点失配和传质受限问题[图9(a)]。 实验表明,在197 ℃,反应1 h后,实现PET的完全解聚并高效转化BHET,初始产率达64.2%。 通过优化反应时间至1.5 h,BHET产率可进一步提升至72.1%。后经简单过滤即可回收并保持5次循环的催化活性稳定性,且在商业化废PET塑料降解中表现出普适性。
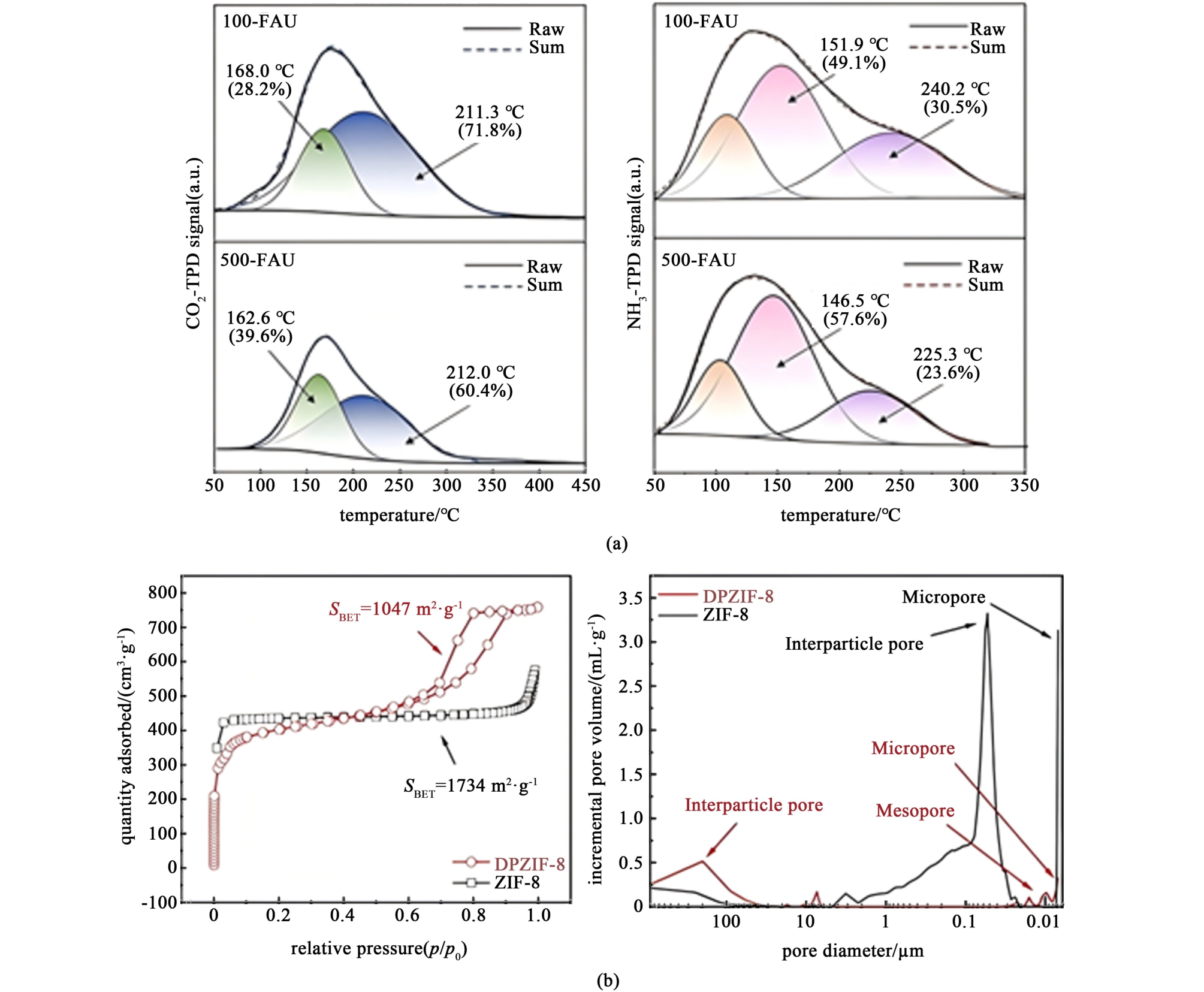
图9 (a)FAU沸石的CO2-TPD与NH3-TPD图谱[53];(b)ZIF-8和DPZIF-8纳米颗粒的N2吸附-脱附曲线以及孔径分布[55]
Fig.9 (a) CO2-TPD versus NH3-TPD mappings of FAU zeolites[53]; (b) N2 adsorption-desorption curves and pore size distributions of ZIF-8 and DPZIF-8 nanoparticles[55]
2.3.2 金属有机框架催化剂
金属有机框架(MOFs)材料因其超高比表面积和可调控活性位点成为研究热点。 Suo等[54]对比ZIF-8、ZIF-67和MOF-5的催化性能,发现ZIF-8在197 ℃、1%负载量下反应1.5 h即实现PET完全转化,BHET收率达76.5%,活化能降至137.6 kJ·mol-1。其优异性能归因于Zn2+路易斯酸位点与介孔结构的协同作用,为反应物扩散和中间体稳定提供理想微环境。 Han等[55] 使用三乙胺调节剂制备得到DPZIF-8纳米颗粒,该调节剂可以调控ZIF-8纳米颗粒的成核和生长机制。 DPZIF-8纳米颗粒包括本征微孔和颗粒黏附诱导的介孔,可以在 ZIF-8结构中提供更大的锌位点外表面积[图9(b)]。 DPZIF-8在180 ℃,常压,催化4 h后PET转化率为91.7%,BHET产率为76.1%,其远高于传统的非均相ZIF-8催化剂。 双孔结构合理的设计策略也为其他金属有机框架,以增加界面催化反应位点提供了思路。Wang等[56]创新性地开发了CoFe2O4@ ZIF-8/ZIF-67双金属沸石咪唑酯骨架(ZIF)复合催化剂,并系统探究其糖酵解催化性能。 实验结果表明,在200 ℃、1 h反应条件下,该催化剂对PET/PBT混合塑料展现出优异的催化效率,实现100%塑料转化率及84.3%的BHET产率,且产物纯度达到92%。尤为突出的是,本研究首次实现了混合塑料体系的高效降解,磁性CoFe2O4核的引入赋予催化剂快速磁分离特性,循环使用5次后仍保持催化活性稳定,Zn、Co元素流失率低于10%,实现了混合塑料体系的高效降解,突破了传统单一塑料降解研究的局限性。
2.3.3 介孔负载型催化剂
介孔载体与活性组分的界面效应研究为催化剂设计提供了新思路。 Yao等[57]通过超声浸渍法制备了一系列M/SBA-15(M=Zn2+、Mg2+、Co2+、Ni2+、Cu2+等)介孔催化剂,其中5%的ZnO/SBA-15表现出良好的稳定性与催化能力,在反应温度197 ℃、反应时间1 h、m(EG)/m(PET)为 4和催化剂用量为5%的条件下,BHET的最佳收率为91.0%,并且该催化剂在循环过程中仍然具有较高的活性。 Mo等[58]开发的Ti/SBA-15催化剂在190 ℃、1 MPa压力下45 min内实现PET完全解聚,BHET收率达87.2%。 对比研究表明,Ti4+通过强电子效应活化PET羰基,而Nb基催化剂因活性位点易失活导致性能下降,这为活性金属筛选提供了理论依据。 Dai等[59]利用离子交换法制备了各种Zn负载的介孔沸石(SBA-15、 MCM-41-25、 MCM-41-Silicon、 Mesoporous Y)作为PET糖酵解的催化剂。 其中,基于MCM-41的催化剂表现出优异的活性,并被选中进行进一步评估。 在最佳条件下,使用Si/Al比为25和Zn负载量为8%的Zn-MCM-41-25催化剂进行PET糖酵解反应:催化剂用量为5%(与PET的质量比),反应温度为200 ℃,m(EG)/m(PET)为6,反应时间为105 min,PET转化率和BHET产率可达到100%和81.4%。
相较于均相催化体系在产物分离与纯化方面存在的固有缺陷,非均相催化剂的引入显著提升了催化体系的分离效率,为解决这一技术难题提供了有效途径。 然而,由于非均相催化体系中传质过程的限制,其在PET糖酵解反应中的应用仍面临诸多挑战,主要体现在反应条件苛刻(如高温、高压等)以及催化效率偏低等方面。 因此,未来非均相催化剂的研究重点应聚焦于催化体系的优化设计,通过构建高效温和的催化系统,实现PET糖酵解过程在温和条件下的高效进行。 这一关键科学问题的解决,将推动非均相催化体系在PET糖酵解领域的进一步发展与应用。
2.4 助溶剂对糖酵解体系的促进
在PET糖酵解反应体系中,其解聚动力学过程遵循缩核模型(Shrinking Core Model)。 反应初期,由于PET分子链的逐步解聚,反应表面积变化并不显著;随着解聚过程的深入,PET开始逐渐变薄并发生溶胀,导致反应表面积显著增加[60],从而加速解聚速率[图10(a)]。 因此,PET的溶胀速率是影响糖酵解反应效率的关键因素之一。
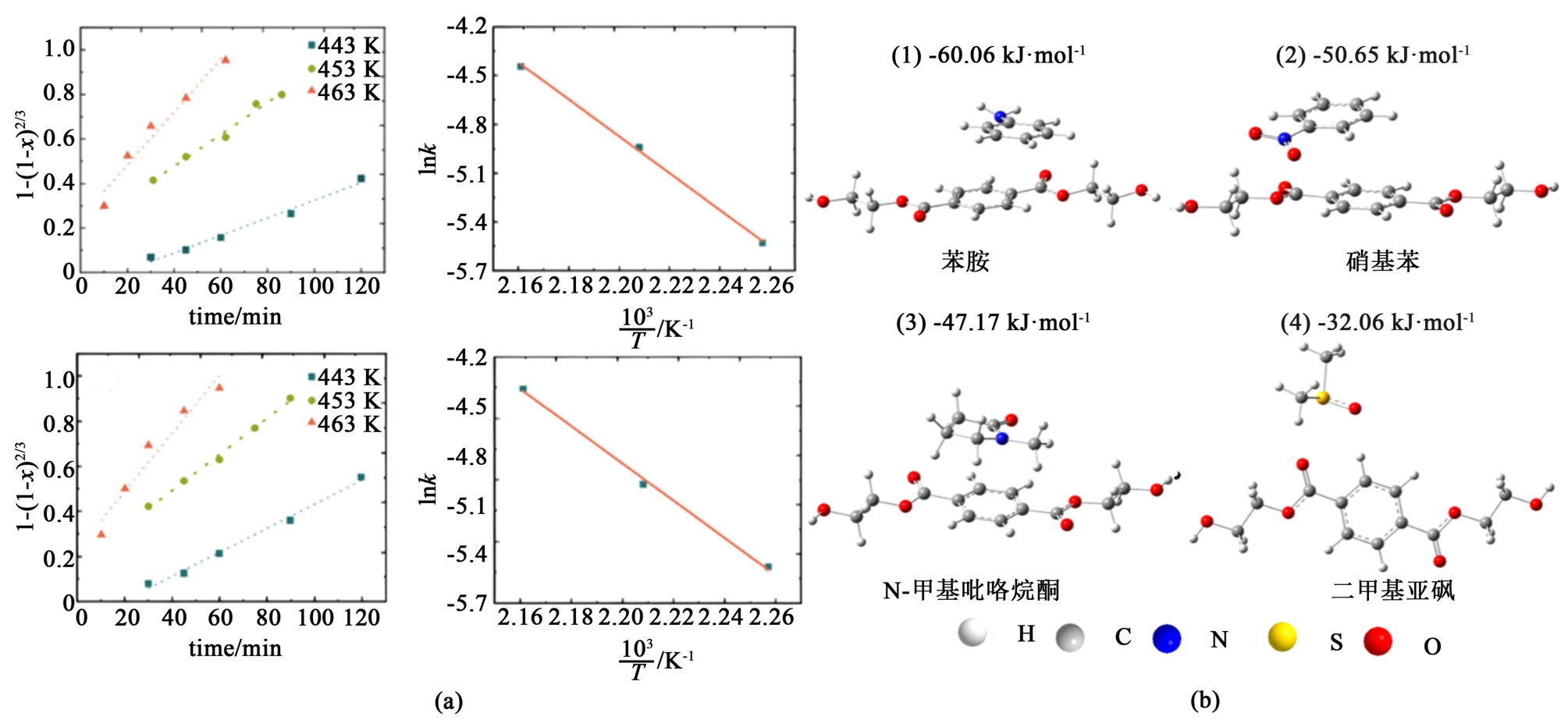
图10 (a)有无助溶剂条件下PET糖酵解动力学[60];(b)溶剂与BHET之间的相互作用结构与相对能量[61]
Fig.10 (a) Kinetics of PET glycolysis with and without co-solvents[60]; (b) Structures and relative energies of the interaction between solvents and BHET[61]
Liu等[61]研究者系统考察了苯胺、硝基苯、NMP和DMSO等助溶剂在乙酸锌催化体系中的作用。实验结果表明,在DMSO体系中,170 ℃反应1 min即可实现PET的完全解聚,BHET单体产率达82%。通过理论计算与红外光谱表征,研究发现芳香族溶剂中的π-π 相互作用对PET溶解具有重要贡献,而DMSO的溶解机制则归因于DMSO中的硫原子与PET羰基氧之间形成氢键[图10(b)],起到了增加PET溶解度的作用。 Le等[62]采用苯甲醚作为绿色助溶剂,在碱金属乙酸酯催化体系中将反应温度从197 ℃显著降低至153 ℃,反应2 h后BHET产率达86%。 研究者建立了共溶剂辅助反应体系的机理动力学模型,揭示了PET解聚的2步过程:首先,PET经历从固态聚合物到可溶性低聚物的相变,这一过程以酯键的随机断裂为特征,由乙二醇(EG)促进,导致反应体系黏度瞬时增加;随后,低聚物进一步分解为二聚体和单体,主要产物为线性BHET三聚体。 该模型指出,酯键断裂总数与消耗的EG量相等,且降解过程通过不可逆的异相反应步骤完成,为优化PET乙二醇解反应的反应器设计和操作参数提供了理论依据。 Luna等[63]系统研究了不同溶剂与聚合物基体的相互作用,最终选择与PET具有最强相互作用的1,3-二氧五环作为助溶剂,在65 ℃反应1 h后获得88%的BHET产率。 研究表明,在高亲和力溶剂(如DMSO、m-THF)作用下,PET颗粒表面形成溶胀层,松弛聚合物链结构,增加对亲核攻击的暴露性,从而提高反应效率;而低产率溶剂则受限于固-液界面反应或传质效率,表现出较弱的PET转化能力。 同时,助溶剂通过调控聚合物溶胀状态、传质效率及离子活性,显著影响PET解聚动力学路径与效率。 因此,在溶剂选择过程中,需要综合考虑溶胀能力、传质优化及化学活化作用之间的平衡[64]。 上述研究进展表明,通过合理选择助溶剂并优化反应条件,可显著提升PET糖酵解反应的效率,为PET的绿色回收提供了重要的理论指导和技术支持。
3 结论
PET的糖酵解技术作为化学回收领域工业化应用最成熟的路径之一,通过选择性断键与可控解聚机制实现了废弃PET的高值化再生。 本研究系统性解析了PET糖酵解反应中金属盐、离子液体(ILs)及非均相催化体系的构效关系与作用机制,总结了当前该反应的研究现状,揭示了不同催化路径下羰基活化与亲核攻击的动态耦合规律,并通过工艺-催化协同优化策略,利用助溶剂辅助糖酵解催化体系突破了传统解聚技术的效率瓶颈。 但在实际应用中,该技术仍面临诸多挑战:金属盐类催化剂因均相特性导致难以回收,且存在重金属残留风险,制约了食品级再生应用;ILs催化剂的产物收率与反应效率仍需优化,DESs体系的稳定性能与长期使用能力有待评估;非均相催化的成本问题与较为苛刻的使用条件,仍是制约其工业化发展的主要问题。 针对上述挑战,可探索以下可行解决思路:(1)对于金属盐类催化剂的回收与残留问题,可研究将均相金属盐催化剂通过化学键合、负载等方式固载到载体上,转化为非均相催化剂,既保留其催化活性,又实现催化剂的高效回收,同时通过选择低毒或无毒金属盐替代重金属盐,降低残留风险。(2)针对ILs催化剂产物收率与反应效率的优化,可通过分子设计对ILs的阳离子、阴离子结构进行修饰,增强其对PET的溶解与催化活性,例如引入具有强亲核性的官能团;对于DESs体系的稳定性问题,可筛选更优的氢键供体与受体组合,或通过添加稳定剂提高其在反应条件下的稳定性,并开展长期循环使用实验评估其寿命。 (3)关于非均相催化的成本与使用条件问题,可开发低成本的天然材料作为载体,降低催化剂制备成本;通过引入助催化剂或优化反应介质,降低反应所需的温度、压力等苛刻条件,提高反应的经济性与可行性。
未来的研究中PET糖酵解技术的发展需聚焦3个核心方向:(1)构建绿色催化体系,通过活性位点精准调控与计算化学辅助设计,开发高效、低毒、可循环的催化材料;(2)创新产物分离与高值化利用模式,突破BHET单体闭环再生的局限,探索其作为共聚酯、离子液体或碳基功能材料前驱体的新路径,形成“降解-升级”一体化体系;(3)建立全生命周期评价框架,从原料、反应到产物应用全链条平衡技术可行性、经济性与环境效益。 通过推动上述方向,PET糖酵解技术有望成为破解全球塑料污染难题的关键抓手,为循环经济体系的构建提供兼具科学严谨性与工业可行性的解决方案。
[1] DE MELLO SOARES C T, EK M, EMMA Ö, et al. Recycling of multi-material multilayer plastic packaging: Current trends and future scenarios[J]. Resources, Conservation and Recycling,2022, 176: 105905
[2] MIR MOHAMAD SADEGHI G, SHAMSI R, SAYAF M. From aminolysis product of PET waste to novel biodegradable polyurethanes[J]. Journal of Polymers and the Environment, 2011, 19(2): 522-534
[3] 王章薇, 宋鹏宇, 游波. 改性聚酯涂层的制备及在食品包装材料中的应用[J]. 包装工程, 2022, 43(9): 1-10 WANG Zhangwei, SONG Pengyu, YOU Bo. Preparation of modified polyester coating and its application in food packaging materials[J]. Packaging Engineering, 2022, 43(9): 1-10(in Chinese)
[4] XIN J, ZHANG Q, HUANG J, et al. Progress in the catalytic glycolysis of polyethylene terephthalate[J]. Journal of Environmental Management, 2021, 296: 113267
[5] PERSSON L, CARNEY ALMROTH B M, COLLINS C D, et al.Outside the safe operating space of the planetary boundary for novel entities[J]. Environmental Science & Technology, 2022, 56(3): 1510-1521
[6] BORRELLE S B, RINGMA J, LAW K L, et al. Predicted growth in plastic waste exceeds efforts to mitigate plastic pollution[J]. Science, 2020, 369(6510): 1515-1518
[7] CHEN Y, LI Y, LIANG X, et al. Effects of microplastics on soil carbon pool and terrestrial plant performance[J]. Carbon Research, 2024, 3(1): 37
[8] NAQASH N, PRAKASH S, KAPOOR D, et al. Interaction of freshwater microplastics with biota and heavy metals: A review[J]. Environmental Chemistry Letters, 2020, 18(6): 1813-1824
[9] 郭琛龙, 彭正奇, 姜冰雪, 等. 退役PET 高值回用的研究进展[J]. 化工学报, 2025, 76(2): 532-542 GUO Chenlong, PENG Zhengqi, JIANG Bingxue, et al. Advances in upcycling of post-consumer PET[J]. CIESC Journal,2025, 76(2): 532-542(in Chinese)
[10] PARK S H, KIM S H. Poly (ethylene terephthalate) recycling for high value added textiles[J]. Fashion and Textiles, 2014, 1(1): 1
[11] NOLASCO CRUZ J, DONJUAN MARTÍNEZ K, ÁLVARO ZAVARIZ D, et al. Review of the thermochemical degradation of PET: An alternative method of recycling[J]. Journal of Ecological Engineering, 2022, 23(9): 319-330
[12] 刘欣悦, 崔颖璐. PET 塑料废弃物及微塑料生物降解与转化的研究现状与展望[J]. 生物加工过程, 2022, 20(2):226-234 LIU Xinyue, CUI Yinglu. Biodegradation and conversion of polyethylene terephthalate(PET) wastes and microplastics: A review[J]. Chinese Journal of Bioprocess Engineering, 2022, 20(2):226-234(in Chinese)
[13] BARNARD E, RUBIO ARIAS J J, THIELEMANS W. Chemolytic depolymerisation of PET: A review[J]. Green Chemistry,2021, 23(11): 3765-3789
[14] YAMAYE M, HASHIME T, YAMAMOTO K, et al. Chemical recycling of poly (ethylene terephthalate). 2. Preparation of terephthalohydroxamic acid and terephthalohydrazide[J]. Industrial & Engineering Chemistry Research, 2002, 41(16): 3993-3998
[15] SCHEIRS J, LONG T. Modern polyesters: Chemistry and technology of polyesters and copolyesters [M]. Chichester, England:John Wiley & Sons, Ltd., 2005
[16] IMRAN M, KIM B K, HAN M, et al. Sub- and supercritical glycolysis of polyethylene terephthalate (PET) into the monomer bis(2-hydroxyethyl) terephthalate (BHET)[J]. Polymer Degradation and Stability, 2010, 95(9): 1686-1693
[17] PETERSON R L, NEPPEL E P, PEEREBOOM L, et al. Upcycling waste PET: I. Ammonolysis kinetics of model dimethyl terephthalate and the catalytic effects of ethylene glycol[J]. ACS Sustainable Chemistry & Engineering, 2025, 13(10): 4120-4131
[18] 邹雨翀, 陈伟鹏, 麦耀舜, 等. 废弃PET 催化氢解材料[J].离子交换与吸附, 2025, 41(1): 27-45 ZOU Yuchong, CHEN Weipeng, MAI Yaoshun, et al. Catalysts for hydrogenesis of PET waste[J]. Ion Exchange and Adsorption, 2025, 41(1): 27-45(in Chinese)
[19] 刘吉星, 龚智婷, 聂思恒. 聚对苯二甲酸乙二醇酯解聚为高附加值化学品的研究进展 [J]. 化学工程与技术, 2024, 14(2): 98-105 LIU Jixing, GONG Zhiting, NIE Siheng. Progress in the depolymerization of polyethylene terephthalate into high value-added chemicals [J]. Chemical Engineering and Technology, 2024, 14(2): 98-105
[20] WANG L, LAN S, HUANG Z, et al. Reaction kinetic model of glycolysis of polyethylene terephthalate[J]. Chemical Engineering Science, 2025, 309: 121463
[21] OTTON J, RATTON S. Investigation of the formation of poly(ethylene terephthalate) with model molecules: Kinetics and mechanism of the catalytic esterification and alcoholysis reactions. I. Carboxylic acid catalysis (monofunctional reactants)[J]. Journal of Polymer Science Part A: Polymer Chemistry,1988, 26(8): 2183-2197
[22] AGURA K, HAYASHI Y, WADA M R, et al. Studies of the electronic effects of zinc cluster catalysts and their application to the transesterification of β-keto esters[J]. Chemistry, an Asian Journal, 2016, 11(10): 1548-1554
[23] NILWANNA K, SITTIWONG J, SRIFA P, et al. Theoretical insights into poly(ethylene terephthalate) glycolysis catalyzed by acid-base pairs in Zn-supported MOF-808 metal-organic framework[J]. Chemical Physics Letters, 2024, 836: 141034
[24] VAIDYA U R, NADKARNI V M. Polyester polyols from glycolyzed PET waste: Effect of glycol type on kinetics of polyesterification[J]. Journal of Applied Polymer Science, 1989, 38(6):1179-1190
[25] CHEN J, CHEN L, CHENG W. Kinetics of glycolysis of polyethylene terephthalate with zinc catalyst[J]. Polymer International, 1999, 48(9): 885-888
[26] XI G, LU M, SUN C. Study on depolymerization of waste polyethylene terephthalate into monomer of bis ( 2-hydroxyethyl terephthalate)[J]. Polymer Degradation and Stability, 2005, 87(1): 117-120
[27] PINGALE N D, PALEKAR V S, SHUKLA S R. Glycolysis of postconsumer polyethylene terephthalate waste[J]. Journal of Applied Polymer Science, 2010, 115(1): 249-254
[28] SHUKLA S R, HARAD A M. Glycolysis of polyethylene terephthalate waste fibers[J]. Journal of Applied Polymer Science,2005, 97(2): 513-517
[29] APICELLA B, DI SERIO M, FIOCCA L, et al. Kinetic and catalytic aspects of the formation of poly(ethylene terephthalate)(PET) investigated with model molecules[J]. Journal of Applied Polymer Science, 1998, 69(12): 2423-2433
[30] ZAHOVA S, TSACHEVA I, TROEV K, et al. Conventional and MW assisted PET glycolysis promoted by titanium based catalyst[J]. Polymer Degradation and Stability, 2023, 212: 110353
[31] WANG S, WANG C, WANG H, et al. Sodium titanium tris(glycolate) as a catalyst for the chemical recycling of poly(ethylene terephthalate) via glycolysis and repolycondensation[J].Polymer Degradation and Stability, 2015, 114: 105-114
[32] WEN R, SHEN G, YU Y, et al. Optimization of Ti-BA efficiently for the catalytic alcoholysis of waste PET using response surface methodology[J]. RSC Advances, 2023, 13(25): 17166-17178
[33] WEN R, SHEN G, ZHANG M, et al. One-pot synthesis of titanium isophthalate and highly active catalytic glycolysis of waste PET[J]. New Journal of Chemistry, 2024, 48(39): 17254-17260
[34] ZHANG H, ZHAO W, LI H, et al. Latest progress in covalently modified polyoxometalates-based molecular assemblies and advanced materials[J]. Polyoxometalates, 2022, 1(2): 9140011
[35] GENG Y, DONG T, FANG P, et al. Fast and effective glycolysis of poly(ethylene terephthalate) catalyzed by polyoxometalate[J]. Polymer Degradation and Stability, 2015, 117: 30-36
[36] JU Z, XIAO W, LU X, et al. Theoretical studies on glycolysis of poly(ethylene terephthalate) in ionic liquids[J]. RSC Advances, 2018, 8(15): 8209-8219
[37] WANG H, YAN R, LI Z, et al. Fe-containing magnetic ionic liquid as an effective catalyst for the glycolysis of poly(ethylene terephthalate)[J]. Catalysis Communications, 2010, 11(8):763-767
[38] WANG H, LIU Y, LI Z, et al. Glycolysis of poly(ethylene terephthalate) catalyzed by ionic liquids[J]. European Polymer Journal, 2009, 45(5): 1535-1544
[39] WANG H, LI Z, LIU Y, et al. Degradation of poly(ethylene terephthalate) using ionic liquids[J]. Green Chemistry, 2009,11(10): 1568-1575
[40] YUE Q, XIAO L, ZHANG M, et al. The glycolysis of poly(ethylene terephthalate) waste: Lewis acidic ionic liquids as high efficient catalysts[J]. Polymers, 2013, 5(4): 1258-1271
[41] ZHOU X, LU X, WANG Q, et al. Effective catalysis of poly(ethylene terephthalate) (PET) degradation by metallic acetate ionic liquids [J]. Pure and Applied Chemistry, 84 ( 3):789-801
[42] WANG Q, LU X, ZHOU X, et al. 1-Allyl-3-methylimidazolium halometallate ionic liquids as efficient catalysts for the glycolysis of poly(ethylene terephthalate)[J]. Journal of Applied Polymer Science, 2013, 129(6): 3574-3581
[43] ZHANG R, ZHENG X, YAO X, et al. Light-colored rPET obtained by nonmetallic TPA-based ionic liquids efficiently recycle waste PET[J]. Industrial & Engineering Chemistry Research,2023, 62(30): 11851-11861
[44] ZHANG C, HE H, SHEN Y, et al. Green catalytic ionic liquids containing organophosphorus for efficient glycolysis of waste PET bottle flakes[J]. Industrial & Engineering Chemistry Research,2024, 63(25): 10903-10913
[45] PŁOTKA-WASYLKA J, DE LA GUARDIA M, ANDRUCH V,et al. Deep eutectic solvents vs ionic liquids: Similarities and differences[J]. Microchemical Journal, 2020, 159: 105539
[46] HANSEN B B, SPITTLE S, CHEN B, et al. Deep eutectic solvents: A review of fundamentals and applications[J]. Chemical Reviews, 2021, 121(3): 1232-1285
[47] ZHANG P, DOERT P T, WANG P et al. Inorganic synthesis based on reactions of ionic liquids and deep eutectic solvents[J].Angewandte Chemie International Edition, 2021, 60 ( 41):22148-22165
[48] ABBOTT A P, CAPPER G, DAVIES D L, et al. Novel solvent properties of choline chloride/urea mixtures[J]. Chemical Communications, 2003(1): 70-71
[49] WANG Q, YAO X, GENG Y, et al. Deep eutectic solvents as highly active catalysts for the fast and mild glycolysis of poly(ethylene terephthalate) (PET) [J]. Green Chemistry, 2015, 17(4): 2473-2479
[50] LIU B, FU W, LU X, et al. Lewis acid-base synergistic catalysis for polyethylene terephthalate degradation by 1, 3-dimethylurea/Zn(OAc)2 deep eutectic solvent[J]. ACS Sustainable Chemistry& Engineering, 2019, 7(3): 3292-3300
[51] LI F, YAO X, DING R, et al. Directional glycolysis of waste PET using deep eutectic solvents for preparation of aromaticbased polyurethane elastomers[J]. Green Chemistry, 2024, 26(18): 9802-9813
[52] SHUKLA S R, PALEKAR V, PINGALE N. Zeolite catalyzed glycolysis of poly(ethylene terephthalate) bottle waste[J]. Journal of Applied Polymer Science, 2008, 110(1): 501-506
[53] YANG G, WU H, HUANG K, et al. The recyclable dual-functional zeolite nanocrystals promoting the high efficiency glycolysis of PET[J]. Journal of Polymers and the Environment, 2024, 32(10): 5071-5085
[54] SUO Q, ZI J, BAI Z, et al. The glycolysis of poly(ethylene terephthalate) promoted by metal organic framework (MOF) catalysts[J]. Catalysis Letters, 2017, 147(1): 240-252
[55] HAN N, LEE K, LEE J, et al. Dual-porous ZIF-8 heterogeneous catalysts with increased reaction sites for efficient PET glycolysis[J]. Chemosphere, 2024, 364: 143187
[56] WANG T, SHEN C, YU G, et al. Fabrication of magnetic bimetallic Co-Zn based zeolitic imidazolate frameworks composites as catalyst of glycolysis of mixed plastic [J]. Fuel, 2021,304: 121397
[57] YAO H, LIU L, YAN D, et al. Colorless BHET obtained from PET by modified mesoporous catalyst ZnO/SBA-15[J]. Chemical Engineering Science, 2022, 248: 117109
[58] MO S L, GUO Y, LIU X, et al. Efficient depolymerization of PET over Ti-doped SBA-15 with abundant Lewis acid sites via glycolysis[J]. Catalysis Science & Technology, 2023, 13(22):6561-6569
[59] DAI C, LIU Y, WANG Z, et al. Efficient glycolysis of waste polyethylene terephthalate textiles over Zn-MCM-41 catalysts[J].Catalysis Today, 2024, 440: 114827
[60] WEI X, ZHENG W, SUN W, et al. Modeling the enhanced swelling behaviors of poly(ethylene terephthalate) glycolysis with mixed EG/CHDM using experiments and molecular dynamics simulation[J]. Industrial & Engineering Chemistry Research,2024, 63(12): 5148-5159
[61] LIU B, LU X, JU Z, et al. Ultrafast homogeneous glycolysis of waste polyethylene terephthalate via a dissolution-degradation strategy[J]. Industrial & Engineering Chemistry Research,2018, 57(48): 16239-16245
[62] LE N, NGOC VAN T T, SHONG B, et al. Low-temperature glycolysis of polyethylene terephthalate[J]. ACS Sustainable Chemistry & Engineering, 2022, 10(51): 17261-17273
[63] LUNA E, OLAZABAL I, ROOSEN M, et al. Towards a better understanding of the cosolvent effect on the low-temperature glycolysis of Polyethylene Terephthalate (PET)[J]. Chemical Engineering Journal, 2024, 482: 148861
[64] AGUADO A, BECERRA L, MARTÍNEZ L. Glycolysis optimisation of different complex PET waste with recovery and reuse of ethylene glycol[J]. Chemical Papers, 2023, 77(6): 3293-3303