随着全球碳中和战略的推进及《巴黎协定》减排目标的迫切需求,基于可再生能源驱动的电催化二氧化碳还原(eCO2RR)技术已成为可再生电力能源以储存在化学键中的形式转化为高附加值的燃料和化工原料提供了一种可行的方法[1]。 目前,碳二(C2)产物由于其较高能量密度和经济价值,受到科研人员的广泛关注[2]。 铜基催化剂凭借其对*CO中间体的独特吸附能及C—C耦合能力,在eCO2RR制备C2+产物方面表现出优异的催化性能[3,4]。 然而,在H型电解池中,受限于传质导致热力学势垒相近的析氢反应(HER)[5]竞争以及复杂的多电子/质子耦合路径(可产生16种以上产物),实现高选择性、高电流密度的C2+产物仍面临严峻挑战。
目前, 多种策略被用于提升铜基材料在eCO2RR生成C2+产物中的性能,例如界面微环境调控[6,7]、形貌与晶面结构工程[8-10]以及铜的价态调控[11]等。 eCO2RR的限速步骤通常是CO2的吸附和质子化和/或*CO中间体的形成[12-14],而铜基材料的优势在于通过C—C偶联反应生成C2+产物。因此,除了上述策略外,设计和构建用于协同eCO2RR的Cu基串联催化剂也是一种有前途的策略。 用于CO2还原的含铜串联电催化剂通常涉及2个或更多活性中心,这些活性中心具有合适的CO2某些关键中间体的结合能[15]。 铜基双组分串联催化剂由主体铜基材料和客体材料组成,用于协同CO2还原生成C2+产物。 关键的*CO中间体通常在客体材料上生成,并可以转移到铜位点进行后续的C—C偶联反应。 在已报道的铜基串联催化剂中,主体材料通常是铜单质及其纳米结构如纳米颗粒[16]、纳米线[17]或纳米片[18],铜的氧化物及其纳米结构以及铜基金属有机框架,但是以泡沫铜基纳米阵列结构使用较少。 实际上,这种具有三维多孔结构自支撑结构和高比表面积的材料易于修饰、掺杂,并在反应过程中保持较高的局部pH值。 泡沫铜基底的氧化亚铜纳米阵列通常具有高比表面积和有序的纳米结构,纳米结构化后高表面粗糙度带来的电化学活性比表面积的增加,获得了较多的活性位点,且这为C—C偶联提供了丰富的反应位点,且Cu2O在还原环境中可形成Cu0/Cu+界面,调控表面电荷分布,优化中间体吸附强度[19]。 客体材料空间限域效应:金属有机框架(MOF)衍生的微孔/介孔结构可限制反应中间体的扩散,延长其在活性位点的停留时间,增加后续在主体材料上C2产物生成概率。 因此,通过用MOF衍生的Ni-N-C与铜基阵列进行复合,有望得到一种性能优良的铜基串联催化剂,用于eCO2RR制C2产物。
本研究通过简单的液相法设计了一种MOF基衍生物Ni-N-C为客体、Cu2O@ CF纳米阵列为主体材料的Ni-N-C-Cu2O@ CF串联催化剂。 结合物理化学 表 征、 电 化 学 表 征 以 及 eCO2RR性 能, 与Cu2O@ CF相 比,研 究Ni-N-C-Cu2O@ CF的 CO2还原活性和C2产物选择性的影响。 本研究为设计高效铜基串联电催化剂提供了新策略。
1 实验部分
1.1 实验材料
六水合硝酸锌(Zn(NO3)2·6H2O,分析纯,重庆川东化工有限公司);二甲基咪唑(MelM,分析纯,上海麦克林生化科技股份有限公司);氯化镍(NiCl2,分析纯,上海麦克林生化科技股份有限公司);过硫酸铵(H8N2O8S2,分析纯,上海阿拉丁生化科技有限公司);氢氧化钠(NaOH,分析纯,上海阿拉丁生化科技有限公司);盐酸(HCl,分析纯,重庆川东化工有限公司);硫酸(H2SO4,分析纯,重庆川东化工有限公司);无水乙醇(CH3CH2OH,分析纯,天津大茂试剂有限公司);甲醇(CH3OH,分析纯,天津大茂试剂有限公司);丙酮(C3H6O,分析纯,成都市科隆化学品有限公司);氯化钾(KCl,分析纯,上海麦克林生化科技股份有限公司);碳酸氢钾(KHCO3,分析纯,上海阿拉丁生化科技有限公司); 泡沫铜(99.99%,130 ppi)购自苏州科盛和金属材料。 H型电解池配件如质子交换膜、钛夹、参比电极、铂网等均购自天津高仕睿联科技有限公司。
1.2 催化剂制备
1.2.1 Ni-N-C的制备
将3.76 g的六水合硝酸锌与80 mL甲醇溶液和100 mL超纯水混合,同时,将8 g 2-二甲基咪唑溶于80 mL的甲醇溶液中。 通过蠕动泵将含有六水合硝酸锌的甲醇溶液匀速滴入含有2-甲基咪唑的甲醇溶液后,持续搅拌3 h后静置2 h。 白色产物Zn-N-C产物通过高速离心机在1 200 r·min-1下10 min获得,随后用甲醇溶液洗涤2 ~3次。 将所收集产物在真空干燥箱中60 ℃干燥过夜。 将产物在900 ℃下氩气气氛中退火3 h。 将热解的产物在60 ℃的0.5 mol·L-1 H2SO4溶液中处理6 h,以除去多余的纳米锌颗粒。 最后用水和乙醇洗涤2 ~3次后干燥,获得Zn-N-C黑色粉末。 镍源(NiCl2)和前驱体Zn-N-C按照质量比2 ∶5密封在真空条件下的石英管中。 将密封好的石英管放置于马弗炉中,确保NiCl2粉末不与Zn-N-C直接接触,在760 ℃中热解10 h,得到黑色Ni-N-C粉末。
1.2.2 Cu2O@CF纳米阵列的制备
纳米阵列采用在泡沫铜原位生长的方法。 首先,分别用丙酮冲洗泡沫铜并浸入1.0 mol·L-1的盐酸中浸泡5 min,以除去泡沫铜表面的氧化层。 然后依次用乙醇和去离子水对泡沫铜进行清洗。 用氩气干燥后,将泡沫铜在0.133 mol·L-1的过硫酸铵和2.667 mol·L-1氢氧化钠的混合溶液中浸泡30 min。在这个刻蚀过程中,泡沫铜的表面逐渐变为蓝色,表示生成氢氧化铜纳米线。 取出样品,用去离子水和乙醇洗涤数次。 最后,将氢氧化铜纳米阵列在氩气气氛下550 ℃的管式炉中退火3 h,得到砖红色的Cu2O@ CF纳米阵列[11]。
1.2.3 Ni-N-C-Cu2O@CF纳米阵列的制备
称取5 mg Ni-N-C催化剂加入940 μL无水乙醇溶液,滴加60 μL Nafion溶液(质量分数5%),超声30 min使其分散均匀,得到催化剂的ink溶液。 用移液枪滴加50 μL ink溶液均匀涂覆在0.5 cm×0.5 cm的Cu2O@ CF上,在室温下晾干。
1.3 催化剂物理化学和电化学表征
采用场发射扫描电子显微镜(SEM,Sigma300,德国ZEISS)和透射电子显微镜(TEM,200S,美国FEI Talos)分别对催化剂的微观形貌及颗粒分布进行表征。 通过X射线衍射仪(XRD,D8-Focus,德国Bruker)分析催化剂的物相组成及晶体结构。 采用X射线光电子能谱(XPS,K-Alpha+,英国Thermo Fisher)进一步表征其表面元素化学态及配位环境。
电化学表征均通过电化学工作站(660E,CHI)进行分析,在进行CO2电解反应前,在H型电解池中利用线性伏安扫描(Linear voltametric scanning,LSV)对催化剂的CO2还原活性进行比较。 测试电压范围为-0.1 ~-1.2 V vs. RHE,电解质为Ar2(体积分数为99.999%)饱和的0.5 mol·L-1 KCl溶液中,对上述电极进行循环LSV扫描。
对于电化学表征所用的 H型电解池, 以0.5 mol·L-1KCl为 阴 极 电 解 液,以0.5 mol·L-1 KHCO3为阳极电解液。 研究发现,与KHCO3电解液相比,由于KCl中的Cl-离子在催化剂表面的选择性吸附及局部pH值升高对HER的抑制作用[20,21],CO2转化效率显著提高。 以质子交换膜(Nafion 211)将阴阳极电解液隔开。 对电极为铂网电极,参比电极为饱和氯化钾溶液填充的银/氯化银电极,参比电极通过鲁金毛细管与阴极室隔开,催化剂Ni-N-C-Cu2O@ CF纳米阵列作为电极片。在CO2电解过程中,CO2原料气均通过气体流量计控制以20 mL·min-1的速度持续通入电解池中。在-0.8 ~-1.2 V vs. RHE的电压范围内,每个测试电位间隔0.1 V气相产物进入气相色谱仪进行定量分析,电解结束后,收集液相产物,用于核磁分析,并记录电流随时间变化曲线。
本研究所报道的电位均转化为相对于可逆氢电极(Reversible hydrogen electrode,RHE)的电位,未进行Ir补偿,转换公式为:
式(1)中: E1表示Evs. RHE, 相对于RHE的电位; E2表示Evs. Ag/AgCl, 相对于Ag/AgCl参比电极的测量电位;pH为电解液的酸碱度。
电化学活性表面积(Electrochemical active surface area, ECSA)通过不同扫速的循环伏安法(Cyclic voltammetry, CV)计算双电层电容(Double-layer capacitance, Cdl)法评估,对中位电压处电流差值和扫速拟合得到的直线斜率即为Cdl。
1.4 产物分析
在电解过程中,气相产物通过配备有火焰离子化检测器(FID)和热导检测器(TCD)的在线气相色谱仪(GC 9790 Plus,福立分析仪器有限公司)每15 min进行定量分析。 液相产物在20 min后收集适量阴极电解液与内标物二甲基亚砜和氘代水混合,通过1H NMR(Avance NEO 400 MHz,德国Bruker)进行测量分析。 二氧化碳还原产物i的法拉第效率(FE)根据公式(2)计算。
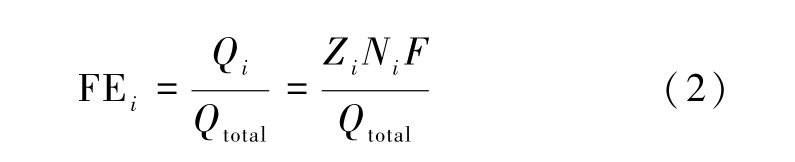
式(2) 中: Qi为生成产物i的电荷量; Qtotal为总通过电荷量(C); Zi为生成产物i转移的电子数;Ni为通过气相色谱(GC)或核磁共振(NMR)测量的产物量(mol); F为法拉第常数(96 485 C·mol-1)。
2 结果与讨论
2.1 物理化学表征
Ni-N-C-Cu2O@ CF纳米阵列串联催化剂的制备过程如图1(a)所示。 通过扫描电子显微镜(SEM)图像可以观察到所得样品的形貌,图1(b)以及插图显示了在CF上形成的Cu(OH)2纳米阵列,直径为100 ~300 nm,长度约为5 μm。 图1(c)证明了在Cu(OH)2@ CF脱水后,Cu2O@ CF呈现出带状结节结构,其平均虽直径减小到约250 nm,但阵列结构得以保持,这有助于传质和活性位点的暴露。 图1(d)为正十二面体的Ni-N-C,图1(e)可以看到Ni-N-C均匀串联在Cu2O@ CF纳米阵列上,图1(f)中的高分辨率透射电镜(HRTEM)清楚地显示了间距为0.213和0.246 nm的晶格,分别对应于Cu2O晶体的(200)和(111)晶面。 在图1(g)中,Ni-N-CCu2O@ CF串联催化剂具有与Cu2O@ CF相同的形貌和结构。 然而,在相应的元素映射图中可以发现Ni和N原子,它们仅存在于Ni-N-C中,并且它们在Cu2O@ CF上的分布与Cu和O原子一致。 这些现象证明了Ni-N-C串联在Cu2O@ CF纳米阵列的成功制备以及Ni-N-C在Cu2O@ CF纳米阵列上的均匀分布。

图1 (a) Ni-N-C-Cu2O@CF纳米阵列的合成示意图;(b) Cu(OH)2@CF、(c) Cu2O@CF、(d) Ni-N-C和(e) Ni-N-C-Cu2O@CF的扫描电子显微镜图像;(f) Cu2O@CF的高分辨透射电子显微镜图像;(g) Ni-N-C-Cu2O@CF的高分辨透射电子显微镜图像及其对应的Ni、N、Cu和O元素分布图
Fig.1 (a) Schematic illustration for the synthesis of Ni-N-C-Cu2O@CF NWs array; SEM images of(b) Cu(OH)2@CF, (c) Cu2O@CF, (d) Ni-N-C and (e) Ni-N-C-Cu2O@CF; (f) HRTEM image of Cu2O@CF;(g) HRTEM image of Ni-N-C-Cu2O@CF and the corresponding elemental mappings of Ni, N, Cu and O atoms
图2(a)显示了CF、Cu2O@ CF、Cu(OH)2@ CF和 Ni-N-C-Cu2O@ CF样品的 XRD图谱可以看出,CF经过湿化学氧化后,Cu(OH)2单晶的 XRD峰(020)、(021)、(002)和(022)面分别出现在16.7°、23.8°、34.0°和38.0°,这意味着在 CF上形成了Cu(OH)2晶体。 Cu(OH)2@ CF进一步热处理后,在36.9°和42.6°处可观察到 Cu2O单晶的(111)和(200)面的特征 XRD峰,同时 Cu(OH)2晶体的(020)和(021)面消失。 上述现象清楚地表明了从Cu、Cu(OH)2到Cu2O的转变。 用 Ni-N-C对 Cu2O@CF纳米阵列进行复合后,Cu2O的典型 XRD峰基本保留,这意味着 Ni-N-C@ CF成功复合在Cu2O@ CF纳米阵列上。 为研究Cu2O@ CF与Ni-N-C之间的相互作用,通过拉曼光谱(Raman)和X射线光电子能谱(XPS)分析了Cu2O@ CF和Ni-N-C-Cu2O@ CF样品的表面组成及化学态。 在图2(b)中,Cu2O@CF样品在217 cm-1处的拉曼峰归属于Cu2O。 对于Ni-N-C-Cu2O@ CF样品,Ni-N-C-Cu2O@ CF样品新出现287 cm-1处的拉曼峰归属于CuO[22]。 通过高分辨率XPS分析了Cu 2p、Cu LMM、Ni 2p和O 1s的化学态,以仔细研究Cu2O与Ni-N-C之间的电子转移关系。 图2(c)中Cu2O@ CF在932.4 eV和952.2 eV处 的Cu XPS峰应来源于Cu0/Cu+的Cu 2p3/2和 Cu 2p1/2轨 道[23], Ni-N-C-Cu2O @ CF在935.3 eV处的Cu XPS峰来源于Cu2+表面,Cu2O在空气中极易氧化成CuO[24]。 图2(d)中的Cu LMM Aguer谱显示,Cu2O@ CF中Cu+的结合能(569.8 eV)在Ni-N-C-Cu-Cu2O@ CF中升至570.1 eV,此处566.9 eV的峰应来源于泡沫铜中的Cu0,Ni-N-CCu2O@ CF中的573.8 eV处的峰来源于Cu2+[25]。图2(e)中Ni-N-C-Cu2O@ CF的高分辨率Ni 2p的XPS谱可分为Ni2+的Ni 2p3/2轨道(855.5 eV)和Ni 2p1/2轨道(873.1 eV)[26]。 与Ni-N-C粉末中的Ni原子相比,Ni-N-C-Cu-Cu2O@ CF中Ni的结合能无明显变化。 图2(f)中,Cu2O@ CF与Ni-N-C-Cu-Cu2O@CF的O 1s XPS峰可归属为金属-氧键(M—O,530.4 eV)、晶格氧(531.8 eV)和吸附水(535.9 eV)。显然,相对于Cu2O@ CF,Ni-N-C-Cu-Cu2O@ CF的M—O组分含量显著减少,这表明Ni-N-C成功复合在Cu2O@ CF,二者在CO2电化学还原反应中能够发挥协同效应。
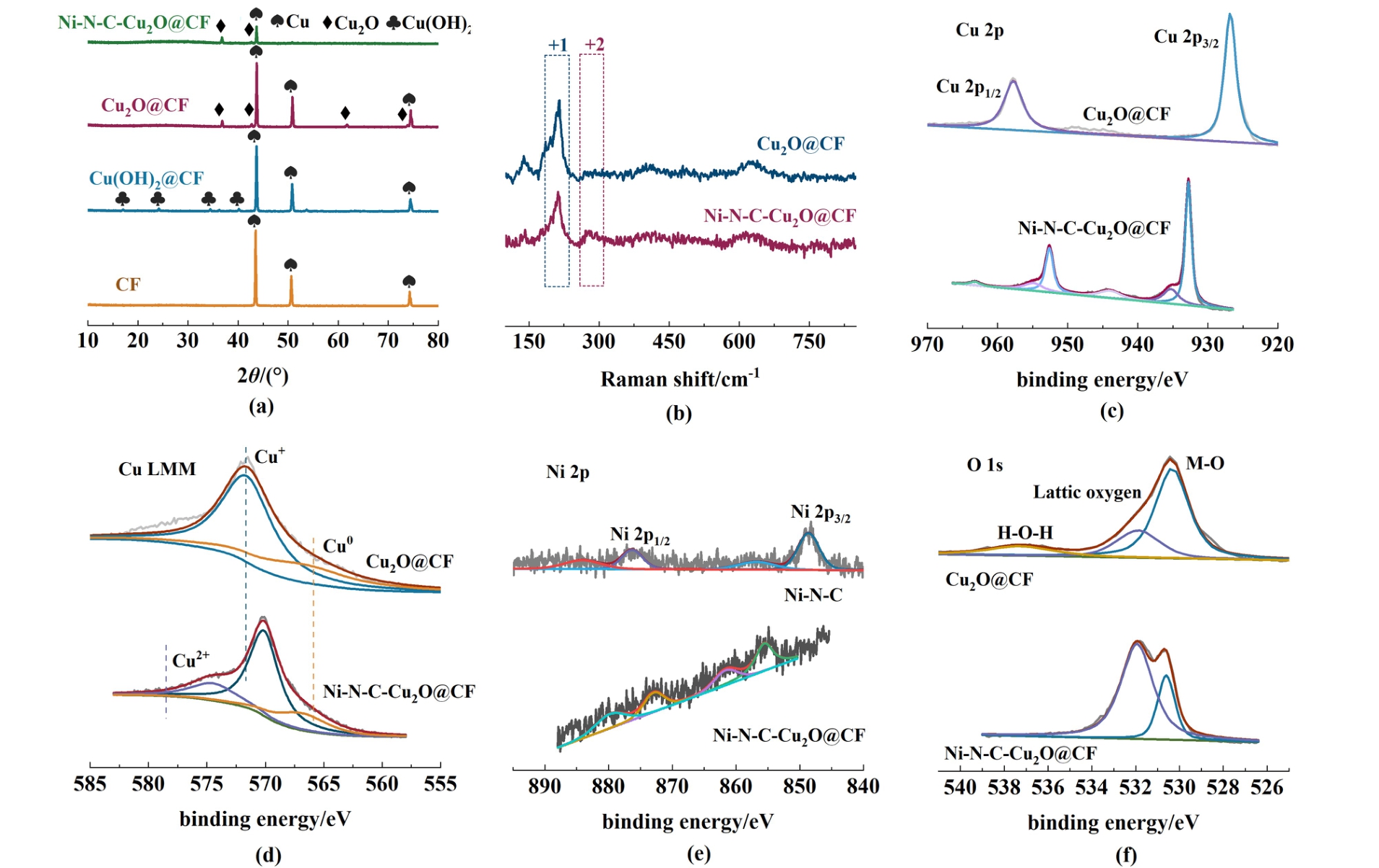
图2 (a) CF、Cu(OH)2@CF、Cu2O@CF和Ni-N-C-Cu2O@CF的X射线衍射图谱;(b) Ni-N-C-Cu2O@CF和Cu2O@CF的拉曼光谱;(c,d) Ni-N-C-Cu2O@CF和Cu2O@CF的Cu 2p X射线光电子能谱及Cu LMM俄歇电子能谱;(e) Ni-N-C和Ni-N-C-Cu2O@CF的Ni 2p X射线光电子能谱;(f) Cu2O@CF和 Ni-N-C-Cu2O@CF样品的O 1s X射线光电子能谱
Fig.2 (a) XRD patterns of CF, Cu(OH)2@CF, Cu2O@CF and Ni-N-C-Cu2O@CF; (b) Raman spectra of Ni-N-C-Cu2O@CF and Cu2O@CF; (c,d) Cu 2p XPS spectra and Cu LMM Auger spectrum of Ni-N-C-Cu2O@CF and Cu2O@CF;(e) Ni 2p XPS spectra of Ni-N-C and Ni-N-C-Cu2O@CF; (f) O 1s XPS spectra of Cu2O@CF and Ni-N-C-Cu2O@CF
通过测量Cu2O@ CF与Ni-N-C-Cu2O@ CF样品的疏水接触角(HCA)的值,可评估其表面CO2扩散能力及HER抑制效应。 研究表明:具备更大HCA的催化剂不仅能有效减弱电解液覆层效应与竞争性HER,还可促进CO2从电解液向催化剂表面迁移及其吸附过程[27]。 图3(a)样品Ni-N-C-Cu2O@ CF的HCA值为131.06°,Cu2O@CF亲水性较强,未能采集到图片,Ni-N-C-Cu2O@ C的串联纳米阵列结构展现出最优的疏水特性。 Ni-N-C-Cu2O@CF较Cu2O@CF的HCA提升,归因于图3(b)中催化剂Ni-N-C的微孔/介孔的本征疏水性[27]。 图3(c)~图3(d)中可以看出催化剂的比表面积关系为:Ni-N-C-Cu2O@ CF>Cu2O@CF>CF。 由此,疏水接触角和比表面积两者趋势与各样品eCO2RR活性及选择性高度匹配。
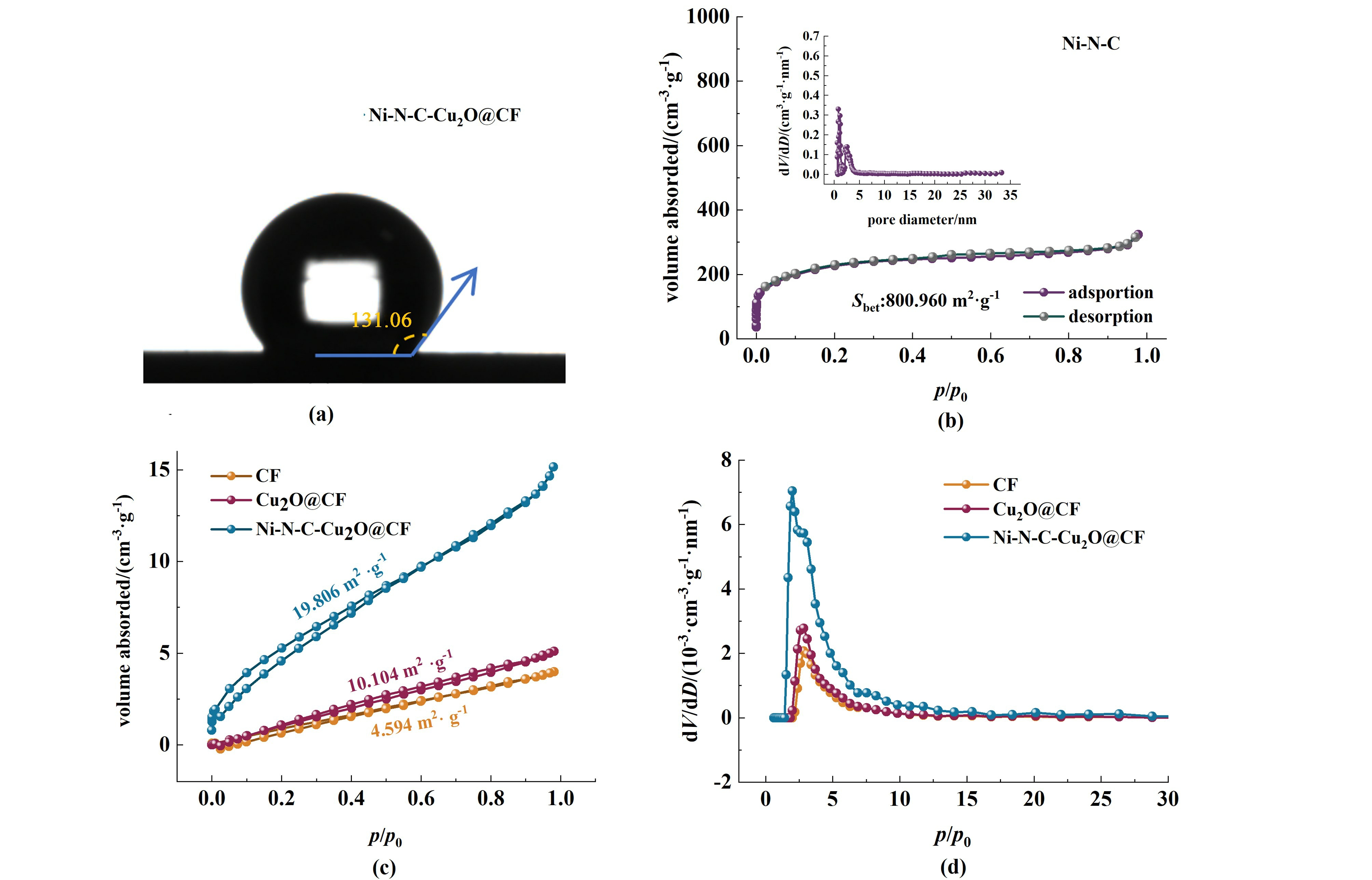
图3 (a) Ni-N-C-Cu2O@CF 表面 0.5 mol·L-1氯化钾水溶液的接触角;(b) Ni-N-C N2 等温吸脱附曲线和孔径分布图;CF、Cu2O@CF 和Ni-N-C-Cu2O@CF 的 (c) N2 等温吸脱附曲线和 (d) 孔径分布图
Fig.3 (a) The contact angle of 0.5 mol·L-1 KCl aqueous solution on Ni-N-C-Cu2O@CF; (b) N2 isothermal desorption curves and pore size distribution of Ni-N-C; (c) N2 isothermal desorption curves and (d) pore size distribution of CF, Cu2O@CF and Ni-N-C-Cu2O@CF
2.2 电化学表征
利用双层电容法对Cu2 O@ CF和Ni-N-CCu2 O@ CF催化剂的电化学活性表面积进行评估,如图 4(a)~图4(b) 所示。 在0.154 ~0.254 V vs. RHE的电位范围内,分别以20、40、60、80和100 mV·s-1的扫描速率对电极进行循环伏安扫描,同一样品可以得到一系列CV曲线,同时对中点电位(0. 204 V vs. RHE)下的电流密度和扫描速率作图,拟合得到的直线斜率即为对应电极的双层电容值。 由于电化学活性表面积与双层电容值呈正比,因此可以利用双层电容值来比较不同电极的电化学活性表面积[28]。 如图 4(c)所示,Cu2 O@ CF和Ni-N-C-Cu2 O@ CF催化剂的双层电容值分别是5. 72和30. 16 mF·cm-2,结果说明Ni-N-C-Cu2 O@ CF具有较大的电化学活性表面积,可以为eCO2 RR提供较多的反应活性位点,提高其CO2电催化性能[29]。 因此由于Ni-N-C的串联,Ni-N-C-Cu2 O@ CF的电化学活性表面积更大,在eCO2 RR中有可能表现出更高的含碳产物活性和选择性[30]。
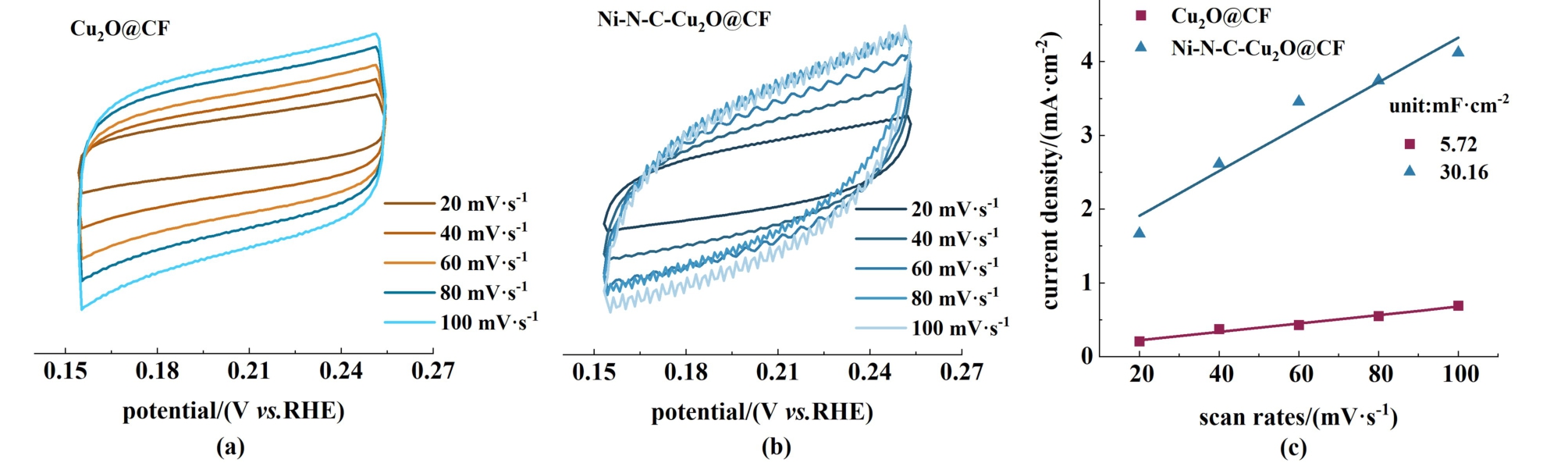
图4 (a) Cu2O@CF和(b) Ni-N-C-Cu2O@CF催化剂的循环伏安曲线;(c) Cu2O@CF与Ni-N-C-Cu2O@CF的双电层充电电流密度
Fig.4 Cyclic voltammetry of (a) Cu2O@CF and (b) Ni-N-C-Cu2O@CF catalysts; (c) Double layer charging current densities of Cu2O@CF and Ni-N-C-Cu2O@CF
2.3 电化学性能测试
在气密H型电解池中,分别测量了Cu2O@ CF和Ni-N-C-Cu2O@ CF样品在Ar2和CO2饱和的0.5 mol·L-1KCl溶液中的LSV曲线,以研究它们的CO2还原活性,如图5(a)所示。 在eCO2RR测试之前,首 先 在 0.5 mol·L-1KCl溶 液 中, 在 电 位-0.7 V vs. RHE对样品进行预还原20 min,以确保催化剂的稳定性。 Ni-N-C-Cu2O@ CF的相应LSV曲线显示出比Cu2O@ CF更正的起始电位和更负的电流密度。 这意味着Ni-N-C-Cu2O@ CF应该是CO2还原的最有效催化剂。
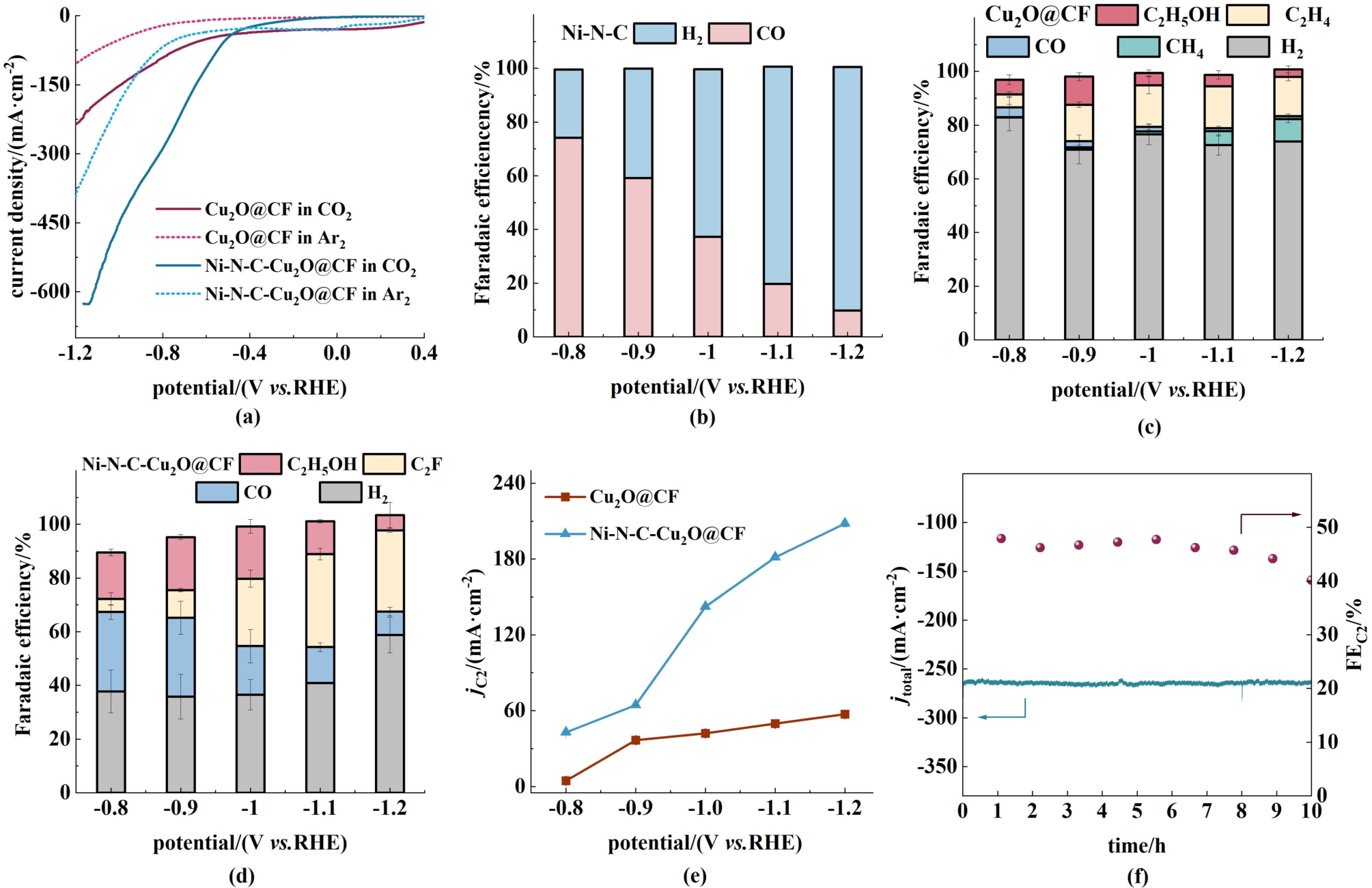
图5 (a) Cu2O@CF和Ni-N-C-Cu2O@CF在Ar2和CO2饱和的0.5 mol·L-1 KCl溶液中的LSV曲线,扫描速率为10 mV·s-1; (b) Ni-N-C、(c) Cu2O@CF和 (d) Ni-N-C-Cu2O@CF样品在不同电位下的产物FE;(e) Cu2O@CF与Ni-N-C-Cu2O@CF的C2产物的分电流密度(jC2)对比;(f) Ni-N-C-Cu2O@CF的FE(C2)与电流密度(j)在10 h内的稳定性变化
Fig.5 (a) LSV curves of Cu2O@CF and Ni-N-C-Cu2O@CF in 0.5 mol·L-1 KCl solution saturated with Ar2 or CO2 at a scan rate of 10 mV·s-1; FE of products for (b) Ni-N-C; (c) Cu2O@CF and (d) Ni-N-C-Cu2O@CF samples at different potentials; (e) Comparison of jC2 between Cu2O@CF and Ni-N-C-Cu2O@CF; (f) Stability of FE(C2) and j for Ni-N-C-Cu2O@CF during 10 h
图5(b)显示,当MOF基衍生物Ni-N-C用作电催化剂时,CO2还原产物为CO和H2。 在-0.8 ~-1.2 V vs.RHE电位范围内,最高可以实现74.1%的CO法拉第效率FE(CO),图5(c)~图5(d)表明了当使用所获得的铜基样品作为催化剂时,CO2还原测试中各种产物的法拉第效率随工作电位的变化。 在Cu2O@ CF、Ni-N-C-Cu2O@ CF样品的测试中,可以检测到H2、CO、CH4、HCOOH、C2H4和C2H5OH产物,由于HCOOH的含量很少,可忽略不计。 所有测试均进行了2次,并以误差棒表示平均值。 对于Cu2O@ CF,由于Cu0/Cu+对CO2RR的协同效应,Cu+促进了C2产物的形成。 从图5(c)所示,随着工作电位从-0.8升至-1.2 V vs. RHE,2e-产品的FE(CO)降低,8e-产品的FE(CH4)升高,12e-产品的FE(C2H4)先升高后降低,12e-产品的FE(C2H5OH)先升高后降低。 而当Ni-N-C串联到Cu2O@ CF后,CH4消失,如图5(d)所示。 Ni-N-C-Cu2O@ CF样品在-1.1 V vs. RHE下,表现出最优的46.9%的C2产物的法拉第效率[FE(C2)],其中,FE(C2H4)为34.7%,FE(C2H5OH) 为12.2%,高于Cu2O@ CF 19.8% 的 FE ( C2 ), FE ( C2H4 ) 为 15.6%, FE(C2H5OH)为4.2%。 同时,在图5(e)显示,Ni-N-CCu2O@ CF样品也表现出C2产物中最高的部分电流密度(- 181.5 mA·cm-2),高于Cu2O@ CF(-49.8 mA·cm-2)。 此外,在电位-1.1 V vs. RHE下,Ni-N-C-Cu2O@ CF如图5(f)所示,在CO2还原过程中的进行了10 h稳定性评估,测试8 h后,C2的法拉第效率下降了10.2%。
2.4 电解后价态分布
反应后的Ni-N-C-Cu2O@ CF XPS以及Raman表征如图6所示,从图6 (a)中Cu 2p的高分辨率光谱可以看到,电解过后催化剂表面出现金属态的铜,归属于Cu2O的特征峰强度降低,这是由于在CO2还原过程中采用负电位,Cu2O被部分还原为Cu0,在953.5和933.2 eV处的峰分别归属于Cu 2p1/2和Cu 2p3/2,对应于Cu(Ⅰ)氧化态。 图6(b)对Cu LMM Aguer进行分峰分析,结果表明Cu+和Cu0共存状态。 综合XPS以及图6(c) Raman结果表明,Cu2O催化剂在CO2还原过程中会被部分还原为Cu0,形成Cu+/Cu0混合价态,有研究也报道了这一现象,同时混合价态也有利于C2产物的生成。综上所述,在负电位下普遍存在部分还原现象,但是仍能保持Cu(Ⅰ)的存在。 在之后的研究中,将针对这一现象研究维持Cu(Ⅰ)的长时间稳定存在、高选择性的催化剂作为重点。
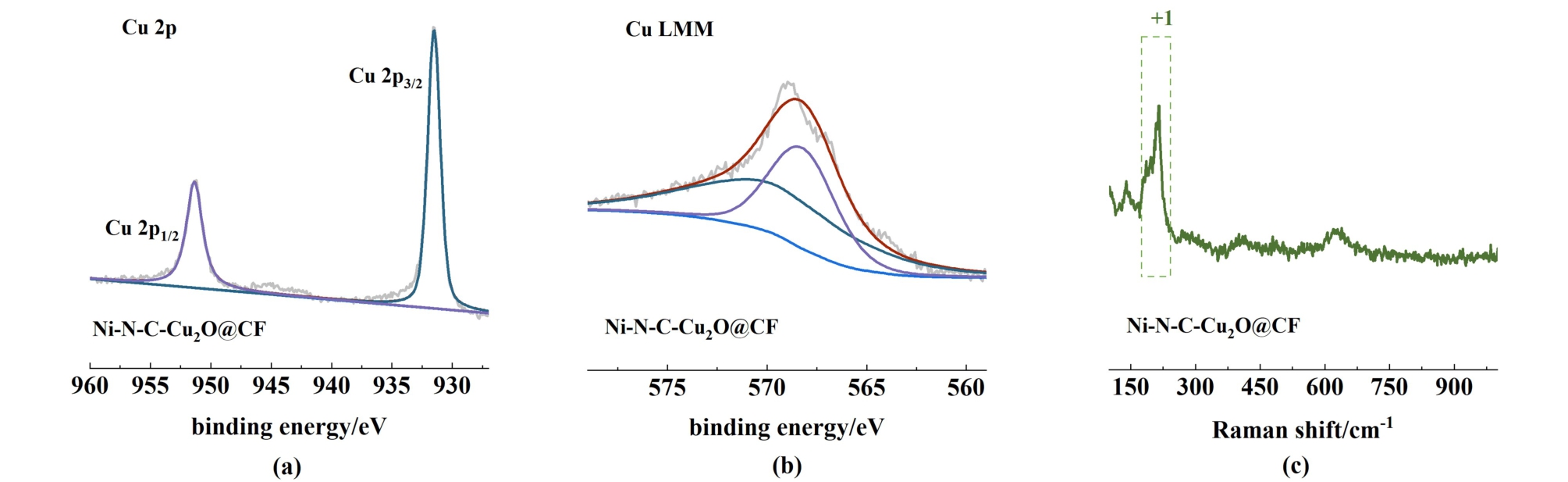
图6 eCO2RR测试后Ni-N-C-Cu2O@CF的 (a) Cu 2p X射线光电子能谱;(b)Cu LMM俄歇电子能谱;(c)拉曼光谱
Fig.6 (a) Cu 2p XPS spectra; (b) Cu LMM Auger spectrum; (c) Raman spectra of Ni-N-C-Cu2O@CF after eCO2RR test
3 结论
总之,本研究首次成功设计了将MOF基衍生物Ni-N-C与Cu2O@CF纳米阵列的复合结构作为自支撑串联电催化剂,用于高效eCO2RR生成C2产物。系列表征证实,Ni-N-C作为客体材料提供的*CO中间体,Cu2O@CF作为主体材料将其吸附并高效转化C2产物。 在H型电解池中,使用Ni-N-C-Cu2O@ CF纳米阵列作为催化剂,在-1.1 V vs.RHE下可以实现46.9%的C2产物的法拉第效率和-181.5 mA·cm-2的分电流密度。 结合以上研究,本研究将Ni-N-CCu2O@ CF更高的C2产物选择性归因于2个方面。首先催化剂Ni-N-C的多孔结构可以促进*CO生成并促进*CO中间体的富集,而主体材料的结节针状结构表面活性位点丰富,进而促进C—C偶联,加大深度转化率。 其次,Cu+在反应过程中动态稳定,Cu0/Cu+有助于C2的转化效率。 本研究为通过构建Ni-N-C-Cu2O@ CF纳米阵列串联催化剂促进*CO中间体的转化增强C—C偶联制备C2产物提供了借鉴。
[1] JIN D, HAO Z, ZHANG P, et al. Advances and challenges for the electrochemical reduction of CO2 to CO: From fundamentals to industrialization[J]. Angewandte Chemie International Edition, 2021, 60(38): 20627-20648
[2] LUO Z, WANG J, NIKOLAOU V, et al. Molecular hybrid materials for selective CO2 electroreduction to multicarbon products[J]. Advanced Energy Materials, 2024, 14(43): 2402070
[3] XIANG K, SHEN F, FU Y, et al. Boosting CO2 electroreduction towards C2+ products via CO* intermediate manipulation on copper-based catalysts[J]. Environmental Science: Nano, 2022, 9(3): 911-953
[4] SHI Y, LI J, MIN Z, et al. Adjusting *CO adsorption configuration over tandem trimetallic AuAgCu heterojunction boosts CO2 electroreduction to ethanol via asymmetric C—C coupling[J].Science China Materials, 2025, 68(1): 173-179
[5] SHAO L, HU B, HAO J, et al. A dendritic Cu/Cu2 O structure with high curvature enables rapid and efficient reduction of carbon dioxide to C2 in an H-cell[J]. Chinese Journal of Catalysis,2024, 63: 144-153
[6] DENG T, JIA S, CHEN C, et al. Polymer modification strategy to modulate reaction microenvironment for enhanced CO2 electroreduction to ethylene[J]. Angewandte Chemie International Edition, 2024, 63(2): e202313796
[7] GE W, CHEN Y, FAN Y, et al. Dynamically formed surfactant assembly at the electrified electrode-electrolyte interface boosting CO2 electroreduction[J]. Journal of the American Chemical Society, 2022, 144(14): 6613-6622
[8] YANG B, LIU K, LI H, et al. Accelerating CO2 electroreduction to multicarbon products via synergistic electric-thermal field on copper nanoneedles[J]. Journal of the American Chemical Society, 2022, 144(7): 3039-3049
[9] GENG Q, FAN L, CHEN H, et al. Revolutionizing CO2 electrolysis: Fluent gas transportation within hydrophobic porous Cu2 O[J]. Journal of the American Chemical Society, 2024, 146(15): 10599-10607
[10] 曹光伟, 曹雪蕊, 王华. 多孔Cu2 O 立方体电催化还原CO2制备乙烯/乙醇[J]. 化学工业与工程, 2023, 40(6): 15-27 CAO Guangwei, CAO Xuerui, WANG Hua. Preparation of ethylene/ethanol by electrocatalytic reduction of CO2 with porous Cu2 O cube[J]. Chemical Industry and Engineering, 2023, 40(6): 15-27(in Chinese)
[11] CHOU T, CHANG C, YU H, et al. Controlling the oxidation state of the Cu electrode and reaction intermediates for electrochemical CO2 reduction to ethylene[J]. Journal of the American Chemical Society, 2020, 142(6): 2857-2867
[12] WEI Z, YUE S, GAO S, et al. Synergetic effects of gold-doped copper nanowires with low Au content for enhanced electrocatalytic CO2 reduction to multicarbon products[J]. Nano Research,2023, 16(5): 7777-7783
[13] KATAYAMA Y, NATTINO F, GIORDANO L, et al. An In situ surface-enhanced infrared absorption spectroscopy study of electrochemical CO2 reduction: Selectivity dependence on surface Cbound and O-bound reaction intermediates[J]. The Journal of Physical Chemistry C, 2019, 123(10): 5951-5963
[14] GUO C, GUO Y, SHI D, et al. Electrocatalytic reduction of CO2 to ethanol at close to theoretical potential via engineering abundant electron-donating Cuδ+species[J]. Angewandte Chemie International Edition, 2022, 61(32): e202205909
[15] HE Q, LI T. Tandem electroreduction of CO2 to C2+ products based on M-SACs/Cu catalysts[J]. Chemistry-A European Journal, 2025, 31(3): e202403297
[16] LUO H, LI B, MA J, et al. Surface modification of nano-Cu2 O for controlling CO2 electrochemical reduction to ethylene and syngas[J]. Angewandte Chemie (International Ed), 2022, 61(11): e202116736
[17] LI X, ZHOU X, LI L, et al. In situ engineering of the core-shell Ag@ Cu structure on porous nanowire arrays for high energy and stable aqueous Ag-Bi batteries[J]. ACS Applied Materials & Interfaces, 2020, 12(9): 10332-10340
[18] ZHANG Z, LIU S, WU Z, et al. High efficiency coupled electrocatalytic CO2 reduction to C2 H4 with 5-hydroxymethylfurfural oxidation over Cu-based nanoflower electrocatalysts[J]. Green Chemistry, 2023, 25(14): 5404-5415
[19] WANG S, WANG D, TIAN B, et al. Synergistic Cu+ /Cu0 on Cu2 O-Cu interfaces for efficient and selective C2+ production in electrocatalytic CO2 conversion[J]. Science China Materials,2023, 66(5): 1801-1809
[20] LIU W, ZHAI P, LI A, et al. Electrochemical CO2 reduction to ethylene by ultrathin CuO nanoplate arrays[J]. Nature Communications, 2022, 13(1): 1877
[21] KIM C, CHO K M, PARK K, et al. Cu/Cu2 O interconnected porous aerogel catalyst for highly productive electrosynthesis of ethanol from CO2[J]. Advanced Functional Materials, 2021, 31(32): 2102142
[22] SANDER T, REINDL C T, GIAR M, et al. Correlation of intrinsic point defects and the Raman modes of cuprous oxide[J].Physical Review B, 2014, 90(4): 045203
[23] KIM Y E, PARK J E, LEE J H, et al. Ag decorated-Cu2 O catalysts with enhanced selectivity for CO2 electroreduction toward C2+ products[J]. Journal of Environmental Chemical Engineering, 2023, 11(5): 111028
[24] CAO X, CAO G, LI M, et al. Enhanced ethylene formation from carbon dioxide reduction through sequential catalysis on Au decorated cubic Cu2 O electrocatalyst[J]. European Journal of Inorganic Chemistry, 2021, 2021(24): 2353-2364
[25] ZHANG W, HUANG C, XIAO Q, et al. A typical oxygen-bearing copper boosts ethylene selectivity toward electrocatalytic CO2 reduction[J]. Journal of the American Chemical Society, 2020,142(26): 11417-11427
[26] BAGUS P S, NELIN C J, BRUNDLE C, et al. Main and satellite features in the Ni 2p XPS of NiO[J]. Inorganic Chemistry,2022, 61(45): 18077-18094
[27] TANG Z, WANG P, XU B, et al. Bioinspired robust water repellency in high humidity by micro-meter-scaled conical fibers:Toward a long-time underwater aerobic reaction[J]. Journal of the American Chemical Society, 2022, 144(24): 10950-10957
[28] LI Z, YADAV R M, SUN L, et al. CuO/ZnO/C electrocatalysts for CO2-to-C2+ products conversion with high yield: On the effect of geometric structure and composition[J]. Applied Catalysis A:General, 2020, 606: 117829
[29] 王磊, 蒋勇, 钟达忠, 等. 碳化的MOF 用于电催化还原二氧化碳制备乙烯和乙醇[J]. 化工学报, 2022, 73(8): 3576-3585 WANG Lei, JIANG Yong, ZHONG Dazhong, et al. Carbonized metal-organic framework for carbon dioxide reduction to ethylene and ethanol[J]. CIESC Journal, 2022, 73(8): 3576-3585(in Chinese)
[30] NOH H, PARK Y, BHADOURIA A, et al. Effects of electrochemical active surface area of Cu on electrochemical CO2 reduction in acidic electrolyte using Cu nanoparticles on surfactanttreated carbon[J]. Journal of Catalysis, 2024, 437: 115662