硝基芳烃化学品在医疗制药、航空航天等高端应用领域具有独特地位。 自21世纪开始,许多国内外的科研工作者开始对多种芳烃化合物的硝化工艺进行微通道过程强化的技术革新,经过改进后的芳烃硝化工艺在安全、高效、环保等方面有着很大的优势[1-3]。 芳烃硝化过程中,反应剧烈且放热量大,微反应器比表面积大,其换热效率极高,可以有效地移走产生的热量,达到控制反应温度的目的,减少因温度失控而引发副反应生成的现象;微反应器的高传质效率可以使物料在短时间内完成混合传质,缩短反应需要的时间,减少物料浓度分布不均匀引起的产物收率降低[4-6]。
芳烃硝化过程常采用间歇反应釜混酸硝化方式进行,但由于其反应速率很快、放热效应显著且为非均相混合的特点,传统反应釜通过控制硝化速率面临生产周期长、产品收率不可控等难题[7-9]。近年来微通道硝化技术的兴起为硝基芳烃化学品的本质安全生产提供重要技术支持,但目前鲜有高通量微通道连续硝化反应技术报道[10]。 面向高通量硝基化学品的微通道连续合成技术特征和工艺探究,将有助于衡量工业化放大效应,为芳烃硝化连续流技术的推广奠定基础[11-13]。
本工作采用苯和氯苯的硝化反应体系,探究其一硝化和二硝化反应工艺条件。 使用叉指结构的预混器和盘管微反应器构建反应装置,对连续流工艺的条件参数进行优化,主要参数条件包括物料流量、反应温度、硝酸用量、混酸物质的量之比、混酸预热温度、反应停留时间和混酸含水量[14-16]。 根据优化工艺条件,在高通量环隙式微通道设备上验证放大效应和工艺试验条件[17,18]。
1 实验部分
如图1所示,本实验通过柱塞泵将混酸与有机相以精确的流速输送到预混器中进行混合,混酸和有机相在实验进料前始终保持常温25 ℃。 预混器采用实验室定制的叉指结构设计,其特征尺寸为0.1 mm,分配比为10 ∶1,持液量为1.5 mL,能够有效增强两相流体的接触面积,促进物料快速混合。混合后的物料通过不同长度的SS316L不锈钢反应管进行反应,反应管规格为ϕ3 mm×1 mm,长度可根据实验需求灵活调整,以实现对反应时间的精确控制。 反应管段通过水浴锅进行加热,物料反应完成后,进入外夹套分液釜进行冷却猝灭,使用低温恒温槽连接夹套釜通入循环冷却液,控制淬灭温度为0 ℃,迅速降低物料温度,终止反应并防止副反应的发生。
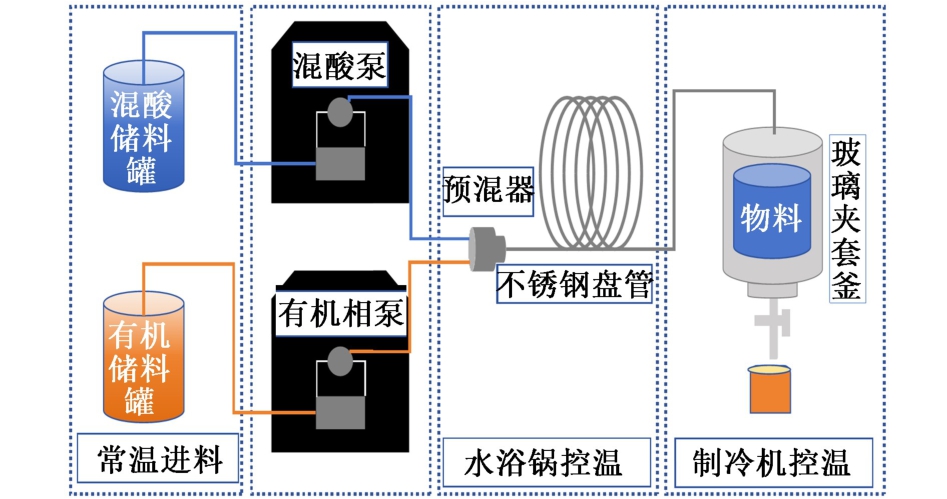
图1 硝化实验设备示意图
Fig.1 Schematic diagram of nitration experimental equipment
用气相色谱进行检测,以氮气作为载气,色谱柱为SE-54毛细色谱柱,色谱进样口温度为250 ℃,柱温箱程序升温由80 ℃升高到260 ℃,检测器为氢离子火焰检测器(FID),温度为300 ℃。 采用标准曲线法计算样品中不同物质的含量。 以苯的硝化实验为例,购买苯(B)、硝基苯(NB)、间二硝基苯(m-DNB)的纯物质样品,制作标准曲线,计算不同物质与苯的相对物质的量校正因子Fi[式(1)],其中邻二硝基苯(o-DNB)和对二硝基苯(p-DNB)由于不常使用难以获得,采用与m-DNB相同的校正因子。

苯的转化率XB通过式(2)计算得出:
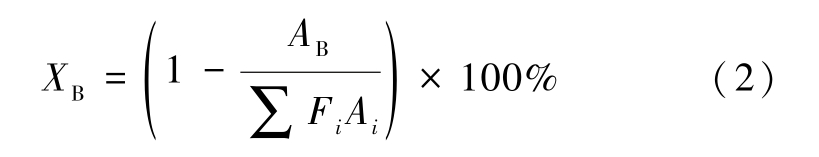
产物的收率Yi由式(3)计算得出:
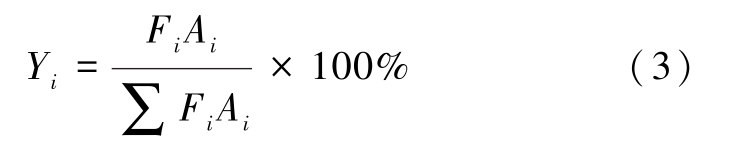
式(1)~式(3)中:ni代表不同物质的物质的量;Ai是各物质的色谱峰面积;Fi为各物质的物质的量校正因子;X为物质转化率;Y为物质收率。
2 结果与讨论
2.1 总流量对硝化反应的影响
2.1.1 总流量对一硝化的影响
通过改变不同流量,探究总流量变化对苯和氯苯一硝化过程的影响。 苯的一硝化条件为:反应温度50 ℃,混酸中硫酸与硝酸的比例n(H2SO4) ∶n(HNO3)= 2.0 ∶1.0,混酸含水量为13%(质量分数),硝酸用量为n(HNO3) ∶n(B)= 1.05 ∶1.00,混酸和苯的进料前温度为25 ℃,设置总流量为3 ~90 mL·min-1,对应停留时间由92.0减少至3.1 s,实验结果如图2(a)。 氯苯的一硝化条件为:反应温度50 ℃,混酸比例为n(H2SO4) ∶n(HNO3)= 2.0 ∶1.0,混酸含水量为13%,硝酸和氯苯的物料配比n(HNO3) ∶n(CB)= 1.20 ∶1.00,同样保 持2种物料的进料温度为25 ℃,总流量为3 ~90 mL·min-1,对应停留时间由92 s减少至3.1 s,实验结果如图2(b)。 由图2可知苯和氯苯的转化率先降低再增加,都存在一个拐点,主要是因为此处发生流型的变化,随着流量的改变,流型可能由液滴流变化为平行流再变化为分散流,两相接触面积先减小后增大。 由于两相反应主要在界面进行,导致转化率会先减小后增大。
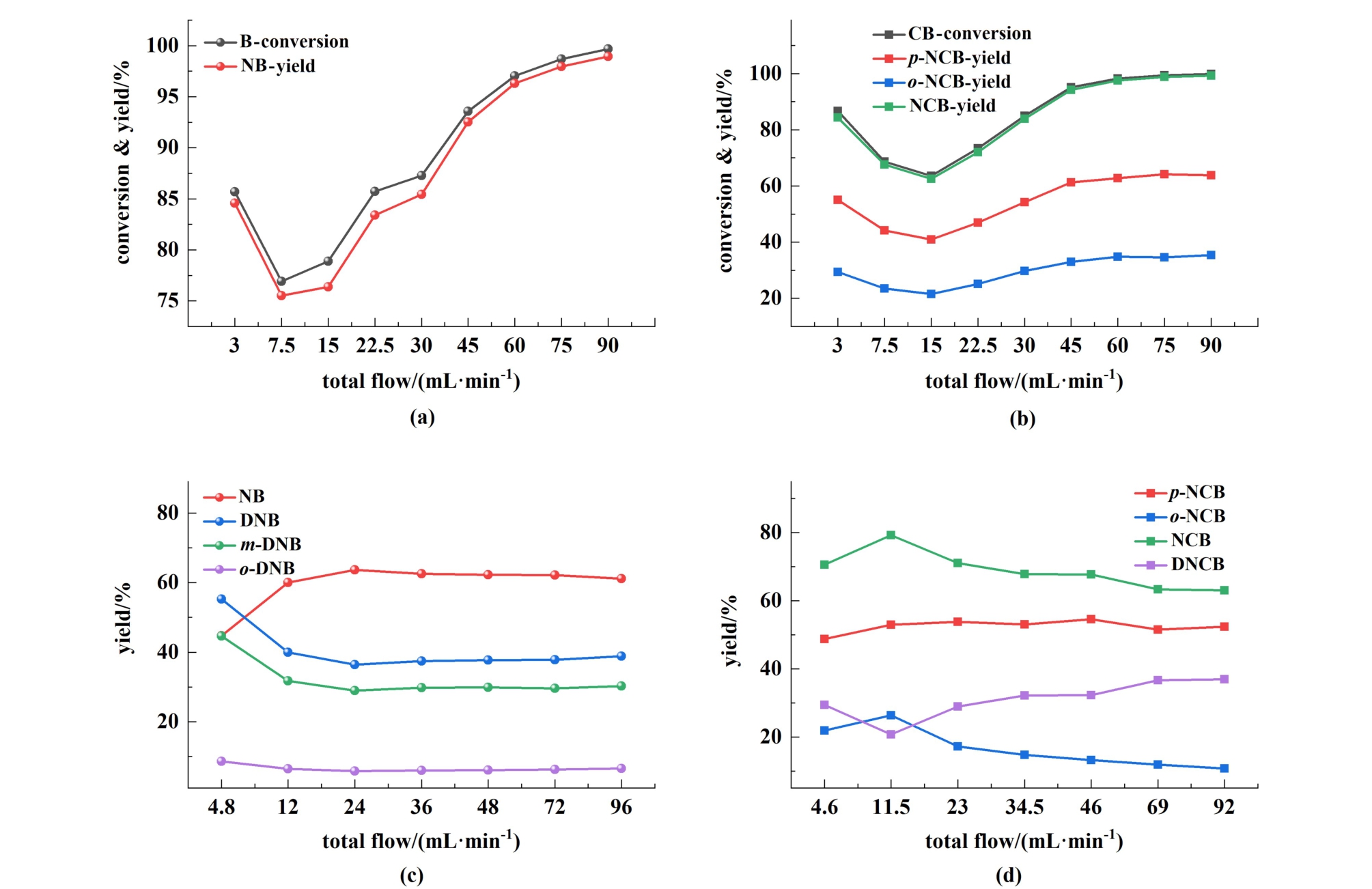
图2 总流量对(a)和(b)苯和氯苯一硝化以及(c)和(d)二硝化反应的影响
Fig.2 Effect of total flow rate on (a) and (b) mononitration; (c) and (d) dinitration of benzene and chlorobenzene
本实验中总流量为3 mL·min-1时,NB的收率为84.6%,NCB的收率为84.4%(p-NCB占54.4%),在总流量为90 mL·min-1时,NB和NCB的收率分别为99%和99.2%(p-NCB占62.2%)。
2.1.2 总流量对二硝化的影响
苯的二硝化条件为:反应温度70 ℃,混酸比例n(H2SO4) ∶n(HNO3)= 2.0 ∶1.0,混酸含水量为8%,硝酸和苯的物料配比n(HNO3) ∶n(B)= 2.05 ∶1.00,2种物料的进料温度为25 ℃,总流量为4.8 ~96 mL·min-1,对应停留时间由58 s减少至2.9 s,实验结果如图2(c)。 氯苯的二硝化条件为:反应温度70 ℃,混酸含水量为8%,混酸比例为n(HNO3) ∶n(B)= 2.00 ∶1.00,硝酸和苯的物料配比n(HNO3) ∶n(CB)= 2.20 ∶1.00,2种物料的进料温度为25 ℃,总流量为4.6 ~92 mL·min-1,对应停留时间由60.5减少至3.0 s,实验结果如图2(d)。 在二硝化反应中,苯和氯苯基本被反应完全,转化率为100%。 氯苯二硝化的产物主要为2,4-二硝基氯苯(DNCB)。由图2(c)可知,在总流量低于24 mL·min-1时,DNB的收率随流量的增大而减小, 当流量大于24 mL·min-1时,DNB的收率略微增高,增高幅度不大,认为没有变化,说明DNB的生成不受流量(混合传质)控制;然而在流量为4.8 mL·min-1时,m-DNB的选择性要比其他流量下高,说明低流量时的流型控制有利于m-DNB生成。 由图2(d)可知,DNCB的收率随着流量的增高先减小后增大,p-NCB变化不大,o-NCB的收率变化与DNCB相反,说明流量的增加促进o-NCB反应为DNCB,o-NCB的反应由混合传质控制,虽然高流量下DNCB的收率明显增高,但氯苯的主要一硝化产物p-NCB。
2.2 反应温度对硝化反应的影响
2.2.1 反应温度对一硝化的影响
苯的一硝化条件为:混酸比例n(H2SO4) ∶n(HNO3)= 2.0 ∶1.0,混酸含水量为13%,n(HNO3)∶n(B)= 1.05 ∶1.00,苯与混酸的进料温度为25 ℃,总流量设定为7.5和90.0 mL·min-1,停留时间分别为37和3.1 s,设定反应温度为30、40、50、60和70 ℃,实验结果如图3(a)和图3(b)。 氯苯的一硝化条件为:n(HNO3) ∶n(CB)= 1.20 ∶1.00,其余参数与苯相同,实验结果如图3(c)和图3(d)。
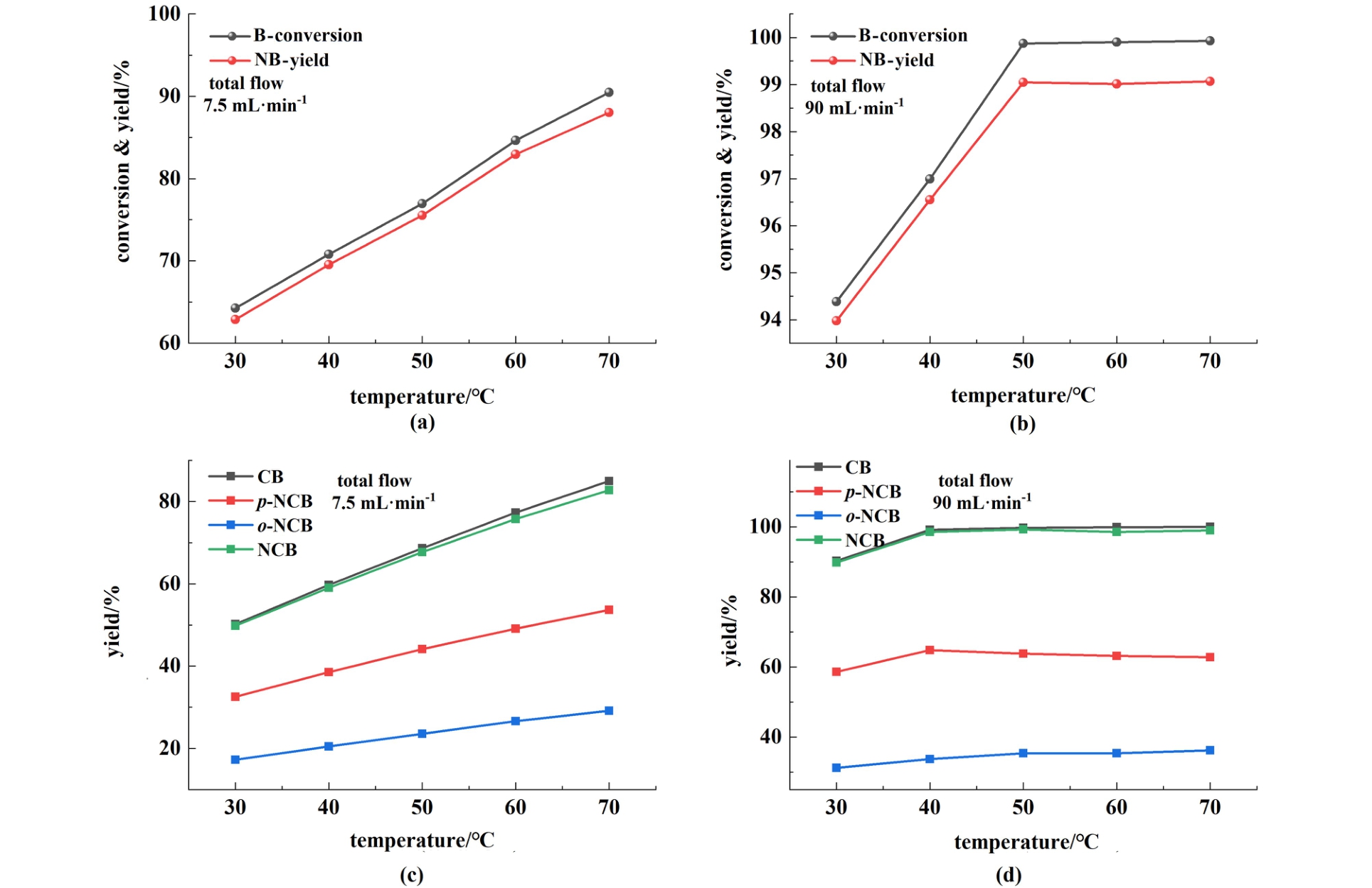
图3 温度对(a)和(b)苯和(c-d)氯苯一硝化反应的影响
Fig.3 Effect of temperature on the mononitration reaction of (a) and (b) benzene; (c) and (d) chlorobenzene
由图3可知温度可以促进硝化反应的进行,在苯和氯苯的一硝化反应中,转化率随温度的增高而增高,在流量7.5 mL·min-1时,由于转化率较低,其对温度的响应较大,高流量下转化率较高,温度影响不大,也会促进原料转化。 反应的选择性越好,原料的转化率与产物的收率越接近,由图3得,高温下引发过硝化产生,二硝化产物增多。 综上对于苯的一硝化适宜温度为50 ℃,对于氯苯的一硝化适宜温度为40 ~50 ℃,在该温度范围下,高流量促进一硝化产物生成(混合传质控制)。
2.2.2 反应温度对二硝化的影响
苯的二硝化条件为:混酸比例n(H2SO4) ∶n(HNO3)= 2.0 ∶1.0,混酸含水量为8%,n(HNO3) ∶n(B)= 2.05 ∶1.00,2种物料的进料温度为25 ℃,总流量设定为4.8和24.0 mL·min-1,停留时间分别为58.0和11.6 s,设定反应温度为50、60、70、80和90 ℃,实验结果如图4(a)和图4(b)。 氯苯的二硝化条件为:n(HNO3) ∶n(CB)= 2.20 ∶1.00,总流量设定为4.5和92.0 mL·min-1,停留时间分别为61和3 s,其余条件参数与苯的参数相同,实验结果如图4(c)和图4(d)。 其中,苯和氯苯的转化率已达到100%。
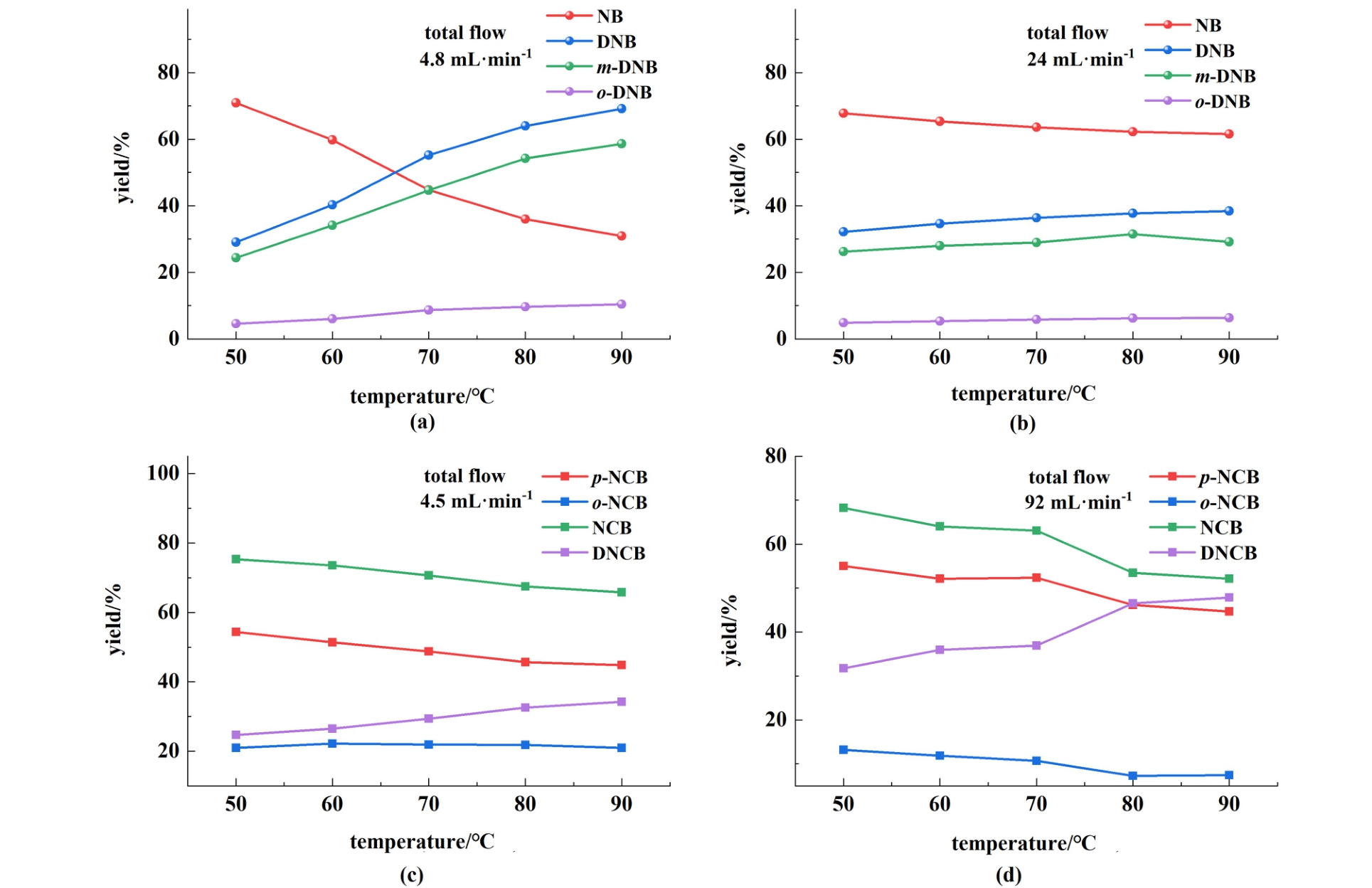
图4 温度对(a)和(b)苯和(c)和(d)氯苯二硝化反应的影响
Fig.4 Effect of temperature on the dinitration reaction of (a) and (b) benzene; (c) and (d) chlorobenzene
由图4可知,随着温度增加,二硝化的收率提高。在苯的二硝化反应中,增高温度对m-DNB影响较大,温度由50增加到90 ℃,总流量为4.8 mL·min-1的DNB收率由30.9%提高到69.0%,而总流量为24.0 mL·min-1的DNB收率变化幅度不大,提高程度在10%以内,说明高温更容易影响低流量下的DNB收率,苯的二硝化采用低流量高温的方法(与2.1节低流量下流型控制m-DNB生成规律一致);对于氯苯的二硝化反应,与苯的情况相反,高温容易影响高流量下的DNCB的收率,且对2种一硝化产物的影响相同,氯苯的二硝化采用高流量高温的方法。
2.3 硝酸用量对硝化反应的影响
2.3.1 硝酸用量对一硝化的影响
苯的一硝化条件为:n(H2SO4) ∶n(HNO3)=2.0 ∶1.0,混酸含水量为13%,反应温度为50 ℃,2种物 料 的 进 料 温 度 为 25 ℃, 总 流 量 设 定 为90.0 mL·min-1(一硝化为混合传质控制,高流量有利于一硝化反应进行),停留时间为3.1 s,硝酸和苯的物料配比n(HNO3) ∶n(B)分别为1.00 ∶1.00、1.05 ∶1.00、1.10 ∶1.00和1.20 ∶1.00,实验结果如图5(a)。 氯苯的一硝化条件为:硝酸和氯苯的物料配比n(HNO3) ∶n(CB)分别为1.10 ∶1.00、1.20 ∶1.00、1.25 ∶1.00和1.30 ∶1.00,其余条件参 数与苯相同,实验结果如图5(b)。 当反应中硝酸用量增多,相当于参与反应的混酸量增多,由图5(a)可知,当硝酸和苯的物料配比n(HNO3) ∶n(B)= 1.00 ∶1.00时,苯的转化率只有95.4%,其他物料配比的转化率均达到99.5%以上,说明需要硝化剂过量,来促进反应正向进行,使原料完全转化,当物料配比大于1.05 ∶1.00时,NB的收率略微下降,此时硝化剂过量引发二硝化反应,产物中DNB的含量增多。 结合实际生产情况,减少混酸的用量可以节约生产成本,因此苯的物料配比取n(HNO3) ∶n(B)= 1.05 ∶1.00为最适宜物料配比。 由图5(b)可知,硝酸和氯苯的物料配比n(HNO3) ∶n(CB)从1.10 ∶1.00变 化 到1.30 ∶1.00时,原料 转 化 率 和 产物收率变化很小,因此选取n(HNO3) ∶n(CB)=1.10 ∶1.00为较适宜条件。
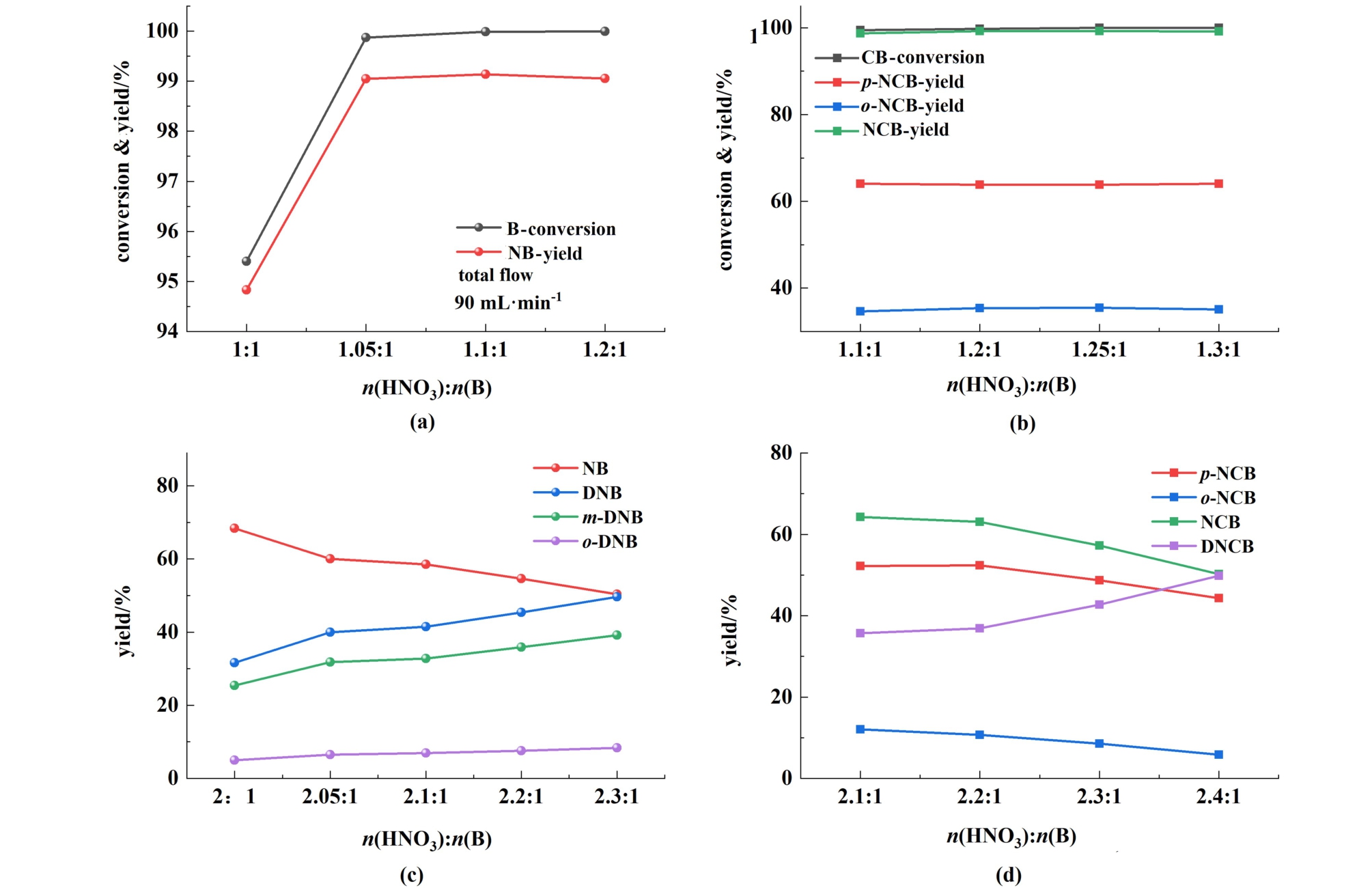
图5 HNO3配比对苯和氯苯(a)和(b)一硝化以及(c)和(d)二硝化反应的影响
Fig.5 Effect of HNO3 ratio on (a) and (b) mononitration; (c) and (d) dinitration of benzene and chlorobenzene
2.3.2 硝酸用量对二硝化的影响
苯的二硝化条件为:n(H2SO4) ∶n(HNO3)= 2.0 ∶1.0,混酸含水量为8%,反应温度为70 ℃,2种物料的进料温度为25 ℃,总流量设定为12.0 mL·min-1,停留时间为23 s,物料配比n(HNO3) ∶n(B)分别为2.00 ∶1.00、2.05 ∶1.00、2.10 ∶1.00、2.20 ∶1.00和2.30 ∶1.00,实验结果如图5(c)。 氯苯的二硝化条件为:总流量设定为92.0 mL·min-1,停留时间为3 s,n(HNO3) ∶n(CB)分 别 为2.10 ∶1.00、2.20 ∶1.00、2.30 ∶1.00和2.40 ∶1.00,其余条件与苯相同,实验结果如图5(d)。 由图5可知,当硝酸用量增多时,二硝化产物的收率增大,主要原因是参与反应的硝化活性相增多,促使二硝化反应进行。 通过增加硝酸用量来增加二硝化产物的收率,会增加生产工艺的成本,同时也增加反应后的废酸量。 增加物料配比只提高参与反应的活性相含量,对活性相硝化能力的强弱影响不大。 底物反应活泼性越低,硝酸用量对硝化反应影响越小,需要通过其他方式强化二硝化反应,因此对于苯和氯苯的二硝化混酸用量需要结合其他实验条件共同优化。
2.4 混酸物质的量之比对硝化反应的影响
芳烃硝化反应中,硫酸相当于催化剂,不直接参与反应,硫酸分子会解离出硫酸根离子,这部分硫酸根离子与硝酸解离的![]() 生成硝化活性相,解离的硝酰阳离子
生成硝化活性相,解离的硝酰阳离子![]() 是硝化主活性相,硫酸根离子是硝化辅助相,当硝化反应体系中,不加入浓硫酸或浓硫酸较少,此时硝化反应靠硝酸解离出的
是硝化主活性相,硫酸根离子是硝化辅助相,当硝化反应体系中,不加入浓硫酸或浓硫酸较少,此时硝化反应靠硝酸解离出的![]() ,需要提供很高的能量才能引发反应,高温下还可能引发氧化反应。 当硝化体系中,硫酸过多时,会增加废酸量,增加后续处理的负担,提高工艺的复杂性和成本。 因此需要探究合适的硫酸用量。
,需要提供很高的能量才能引发反应,高温下还可能引发氧化反应。 当硝化体系中,硫酸过多时,会增加废酸量,增加后续处理的负担,提高工艺的复杂性和成本。 因此需要探究合适的硫酸用量。
2.4.1 混酸物质的量之比对一硝化的影响
苯的一硝化条件为:物料配比n(HNO3) ∶n(B)=1.05 ∶1.00,反应温度为50 ℃,2种物料的进料温度为25 ℃,总流量设定为90 mL·min-1,停留时间为3.1 s,n(H2SO4) ∶n(HNO3)分 别为1.0 ∶1.0、1.5 ∶1.0、2.0 ∶1.0和2.5 ∶1.0,实验结果如图6(a)。 氯苯的一硝化条件为:n(HNO3) ∶n(CB)= 1.20 ∶1.00,n(H2SO4) ∶n(HNO3)分 别 为1.0 ∶1.0、1.5 ∶1.0、2.0 ∶1.0和2.5 ∶1.0,其余条件参 数与苯 相同,实验结果如图6(b)。 由图6可知,n(H2SO4) ∶n(HNO3)从1.0 ∶1.0增加到2.0 ∶1.0,苯的转化率会提高,说明硫酸增多,混酸中的硝化活性相含量增多,促使苯和氯苯发生硝化反应。 当n(H2SO4) ∶n(HNO3)从2.0 ∶1.0增加到2.5 ∶1.0时,苯和氯苯的转化率接近100%,NB和NCB的收率略微下降,说明发生过硝化反应,二硝化产物收率增大,此时活性相可能过多,因此对于苯和氯苯的一硝化,n(H2SO4) ∶n(HNO3)为2.0 ∶1.0最适宜。
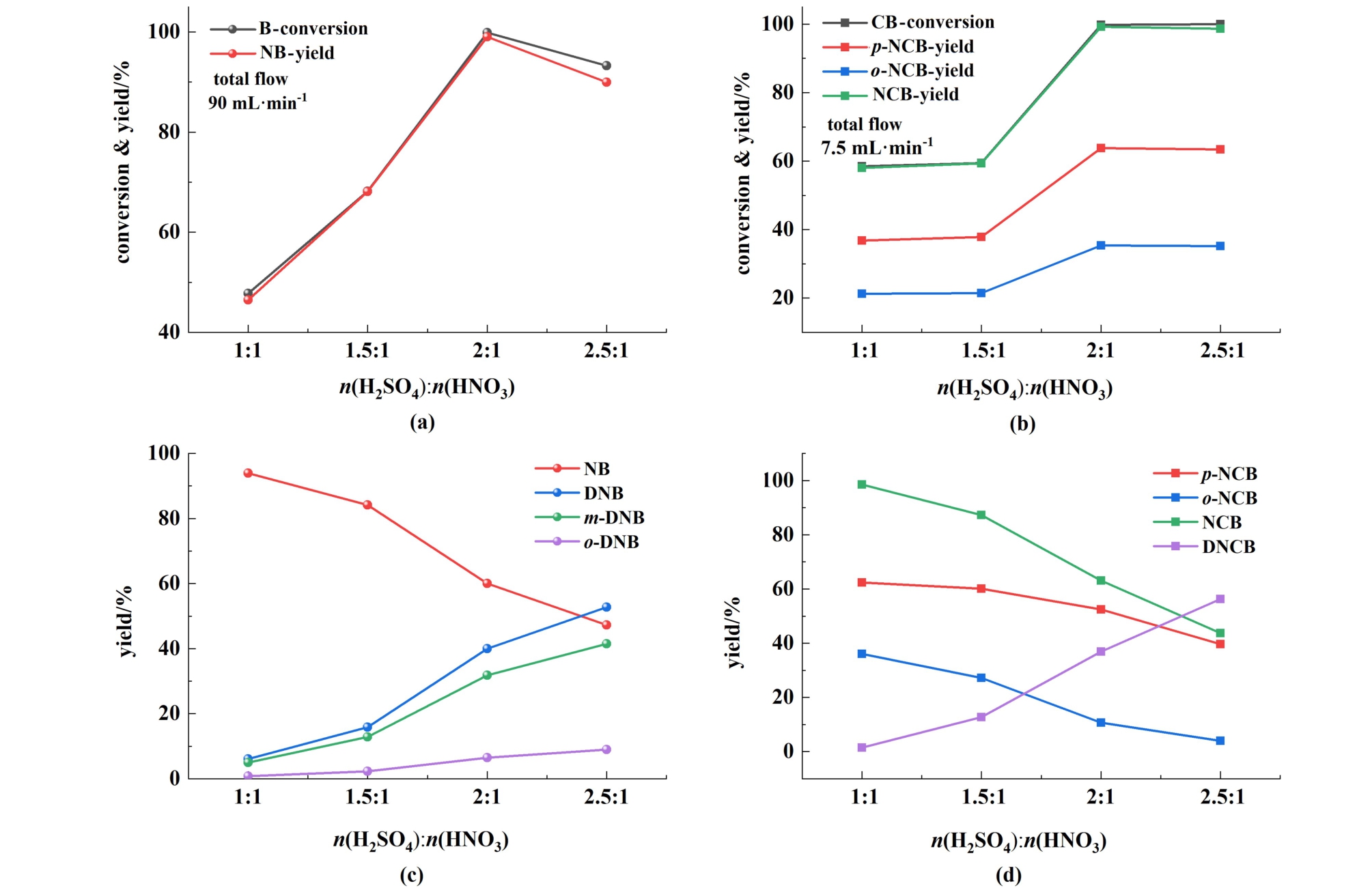
图6 混酸物质的量之比对对苯和氯苯(a)和(b)一硝化以及(c)和(d)二硝化反应的影响
Fig.6 Effect of mixed acid ratio on mononitration and dinitration of (a) and (b) benzene; chlorobenzene (c) and (d)
2.4.2 混酸物质的量之比对二硝化的影响
苯的二硝化条件为:物料配比n(HNO3) ∶n(B)=2.05 ∶1.00,反应温度为70 ℃,2种物料的进料温度为25 ℃,总流量设定为12.0 mL·min-1,停留时间为23 s,n(H2SO4) ∶n(HNO3)分别 为1.0 ∶1.0、1.5 ∶1.0、2.0 ∶1.0和2.5 ∶1.0,实验结果如图6(c)。 氯苯的二硝化条件为:总流量设定为92 mL·min-1,停留时间为3 s,物料配比n(HNO3) ∶n(CB) 设为2.20 ∶1.00,n(H2SO4) ∶n(HNO3)分别为1.0 ∶1.0、1.5 ∶1.0、2.0 ∶1.0和2.5 ∶1.0,其余条件参数与苯相同,实验结果如图6(d)。
由图6可知,随着硫酸用量的增加,二硝化产物的收率呈现上升趋势。 硫酸用量的提升使参与反应的硝化活性相含量增加,推动了二硝化反应的进行。 通过提高硫酸用量来提高二硝化产物收率,可以提升产物收率,但相比于增加混酸物质的量之比提高产物收率,提高硫酸用量会消耗大量混酸。
2.5 混酸预热温度对硝化反应的影响
硝化反应的关键影响因素是混酸中活性相的生成量,改变物料配比和混酸物质的量之比,从本质上讲是增加混酸中活性相的生成量,也可以通过其他途径,提高混酸中活性相的含量。 ![]() 与
与![]() 结合生成
结合生成![]() 活性相的过程是需要吸收热量的,提高混酸的温度,可以为活性相的生成提供足够的能量,有助于混酸在参与反应前生成更多的活性相。
活性相的过程是需要吸收热量的,提高混酸的温度,可以为活性相的生成提供足够的能量,有助于混酸在参与反应前生成更多的活性相。
2.5.1 混酸预热温度比对一硝化的影响
苯的一硝化条件为:n(H2SO4) ∶n(HNO3)=2.0 ∶1.0,混酸含水量为13%,反应温度为50 ℃,n(HNO3) ∶n(B) = 1.05 ∶1.00,苯的进料温度为25 ℃,总流量设定为45 mL·min-1,停留时间为6.2 s,反应前混酸预热温度为20、25、30和35 ℃,实验结果如图7(a)。 氯苯的一硝化条件为:n(HNO3) ∶n(CB)= 1.20 ∶1.00,反应前混酸预热温度为20、25、30和35 ℃,其余条件与苯相同,实验结果如图7(b)。 由图7可知,当混酸预热温度由20提高到35 ℃,2种硝化底物的转化率逐渐增加,说明通过提高混酸的温度,增加混酸中活性相的含量,有助于硝化反应进行。 对于混酸加热,还有其他因素影响,已有相关研究指出,部分芳烃化合物如苯、氯苯等可以溶于浓硫酸,溶解度会随着硫酸的浓度以及混酸的温度提高而增大,因此提高混酸温度,2股物料在经过预混器混合时,更多的苯或者氯苯溶于混酸,加强传质,促进反应进行。 对于苯和氯苯的一硝化,可以提高混酸温度来强化硝化反应。
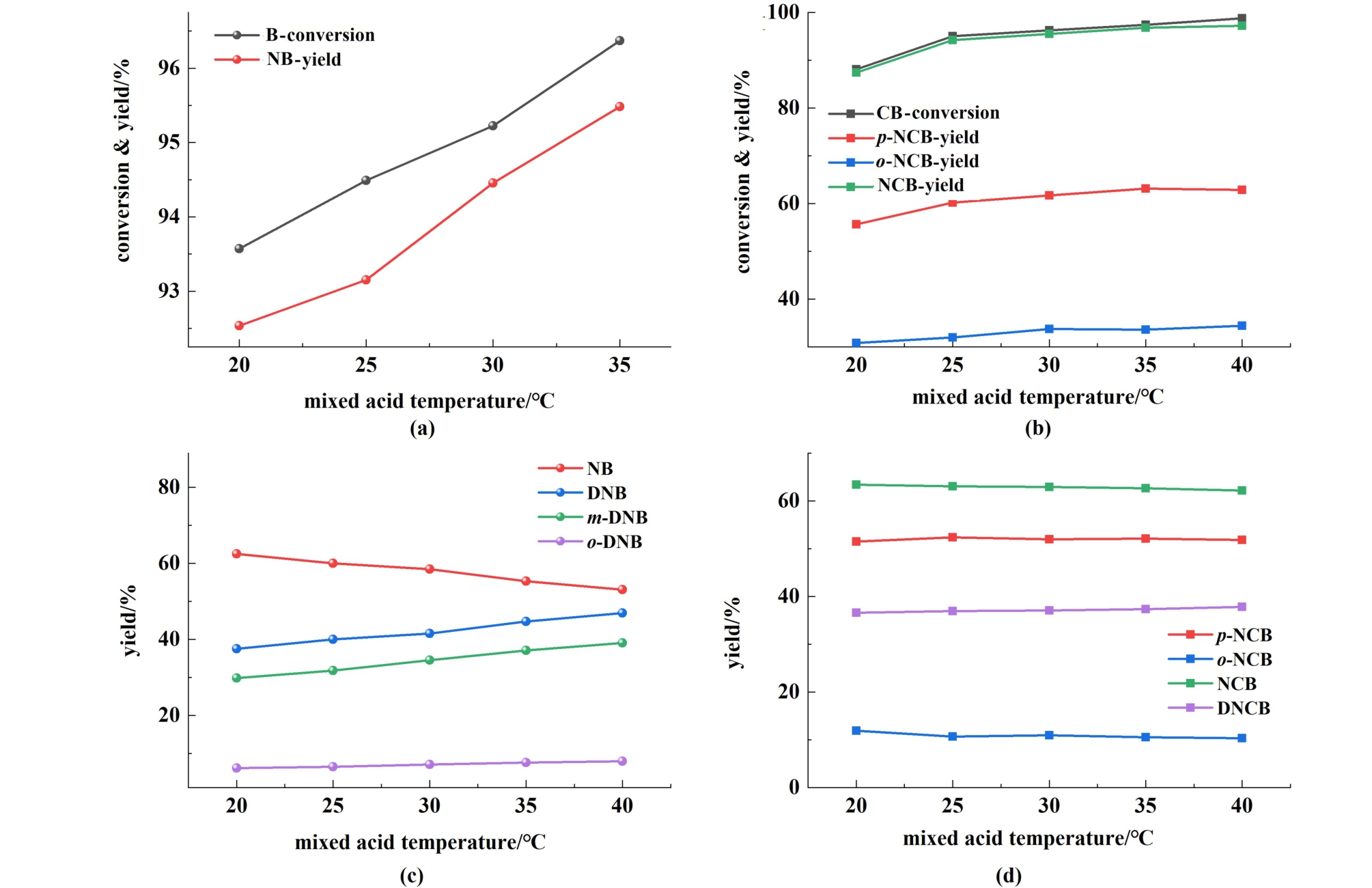
图7 混酸温度对苯和氯苯(a)和(b)一硝化以及(c)和(d)二硝化反应的影响
Fig.7 Effect of mixed acid temperature on mononitration and dinitration of (a) and (b) benzene;chlorobenzene (c) and (d)
2.5.2 混酸预热温度比对二硝化的影响
苯的二硝化条件为:n(H2SO4) ∶n(HNO3)=2.0 ∶1.0,混酸含水量为8%,反应温度为70 ℃,物料配比n(HNO3) ∶n(B)= 2.05 ∶1.00,苯的进料温度为25 ℃,总流量设定为12 mL·min-1,停留时间为23 s,反应前混酸预热温度为20、25、30、35和40 ℃,实验结果如图7(c)。 氯苯的二硝化条件为:总流量设置为92.0 mL·min-1,停留时间为3 s,物料配比n(HNO3) ∶n(CB)= 2.20 ∶1.00,反应前混酸预 热温度为20、25、30、35和40 ℃,其余参数与苯相同,实验结果如图7(d)。
由图7可知,混酸加热对苯的二硝化反应影响较大,DNB的收率由37.5%提高到47%,二硝化产物中m-DNB的提高更为明显,说明混酸加热可以提高m-DNB的选择性。 而氯苯的二硝化几乎不受混酸温度的影响,DNCB的收率略微提高。
2.6 混酸含水量对硝化反应的影响
与混酸温度的相同,混酸的含水量也是影响混酸中活性相的重要因素。 活性相产生的过程是硫酸分子解离出的![]() ,促使硝酸分子解离出
,促使硝酸分子解离出![]() 并与其结合,生成
并与其结合,生成![]() 活性相同时产生一分子的H2O,当混酸中的水含量过高时会使上述反应逆向进行,从而抑制活性相的产生,混酸中含水量越低,混酸中的活性相含量越高,硝化能力越强。硫酸中水含量的不同可以解离出不同的硫酸根形式的活性物,有
活性相同时产生一分子的H2O,当混酸中的水含量过高时会使上述反应逆向进行,从而抑制活性相的产生,混酸中含水量越低,混酸中的活性相含量越高,硝化能力越强。硫酸中水含量的不同可以解离出不同的硫酸根形式的活性物,有![]() 等不同的存在形式,作为硝化辅助活性相,活性相具有的硝化能力也不同。 减少混酸中的水含量,可以使硝化活性相的配位形态发生改变,进而增强混酸硝化能力。 混酸中的水主要来自浓硝酸,使用不同浓度的硝酸可以配置成不同含水量的混酸,探究其对硝化反应的具体影响。 对于苯和氯苯的一硝化,使用含水量为13%的混酸可以完成全部转化,降低含水量会引发过硝化反应,且使用发烟硝酸生产成本过高,因此不探究含水量对一硝化的影响。
等不同的存在形式,作为硝化辅助活性相,活性相具有的硝化能力也不同。 减少混酸中的水含量,可以使硝化活性相的配位形态发生改变,进而增强混酸硝化能力。 混酸中的水主要来自浓硝酸,使用不同浓度的硝酸可以配置成不同含水量的混酸,探究其对硝化反应的具体影响。 对于苯和氯苯的一硝化,使用含水量为13%的混酸可以完成全部转化,降低含水量会引发过硝化反应,且使用发烟硝酸生产成本过高,因此不探究含水量对一硝化的影响。
苯的二硝化实验条件为:n(H2SO4) ∶n(HNO3)=2.0 ∶1.0,反应温度为70 ℃,2种物料的进料温度为25 ℃,总流量设定为4.8 mL·min-1,n(HNO3) ∶n(B)为2.05 ∶1.00,混酸含水量为3.5%和8%,实验结果如图8(a)。 氯苯的二硝化条件为:总流量设定为92.0 mL·min-1,n(HNO3) ∶n(CB)= 2.20 ∶1.00,其余条件与苯相同,实验结果如图8(b)。
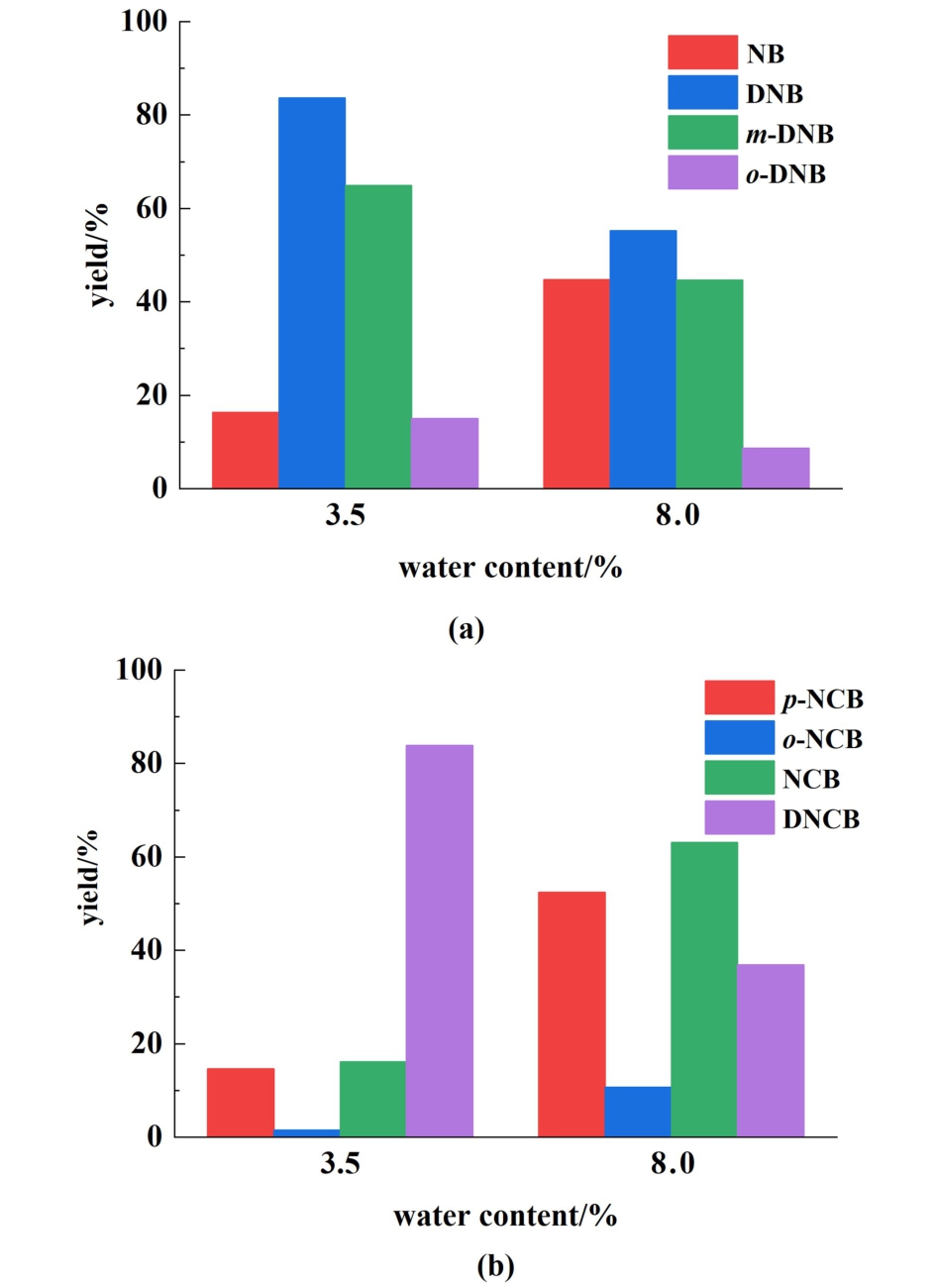
图8 混酸含水量对二硝化反应的影响(a)苯;(b)氯苯
Fig.8 Effect of water content of mixed acid on the dinitration reaction of (a) benzene and (b) chlorobenzene
从图8可以看出,对于苯和氯苯的二硝化,混酸含水量由8.0%降低到3.5%,苯的二硝化产物DNB的收率由55.2%提高到83.7%,氯苯的二硝化产物DNCB收率由36.9%提高到83.9%,说明混酸中含水量对硝化反应影响很大,主要原因是当混酸中水含量高时,硫酸根作为辅助相催化HNO3解离![]() 的速度会下降,同时部分活性相的存在形态也会发生改变,大大降低混酸的硝化能力。 其次含水量高时,硫酸的浓度变低,对芳烃化合物的溶解能力下降,影响传质能力。 对于苯和氯苯的二硝化,需要尽量降低混酸中的含水量。
的速度会下降,同时部分活性相的存在形态也会发生改变,大大降低混酸的硝化能力。 其次含水量高时,硫酸的浓度变低,对芳烃化合物的溶解能力下降,影响传质能力。 对于苯和氯苯的二硝化,需要尽量降低混酸中的含水量。
2.7 停留时间对硝化反应的影响
影响物料在微通道反应器的停留时间的因素有很多,其中最主要的是设备的持液量和物料流量。 由实验可知,改变流量不只是影响物料停留时间,还会影响混合传质、流体的流型等,导致不同停留时间下的结果不够准确,因此对于停留时间的探究,需要通过改变持液量。 微通道反应管的持液量由管长和管径决定,改变管径会影响比表面积,还会改变流型,一般通过延长管长来提高持液量。 对于苯和氯苯的一硝化,主要通过高流量完成传质与反应,该过程速度很快,对增加停留时间完成反应的需求较低,本实验只对二硝化反应进行探究。
苯的二硝化条件为:n(H2SO4) ∶n(HNO3) =2.0 ∶1.0,混酸含水量为8.0%,反应温度为70 ℃,2种物料的进料温度为25 ℃, 总流量设定为4.8 mL·min-1,物料配比n(HNO3) ∶n(B)= 2.05 ∶1.00,总反应管长分别为4、6、10和14 m,实验结果如图9(a)。 氯苯的二硝化条件为:总流量设定为4.6和92.0 mL·min-1,n(HNO3) ∶n(CB)为2.20 ∶1.00,其余条件参数与苯相同,实验结果如图9(b)。
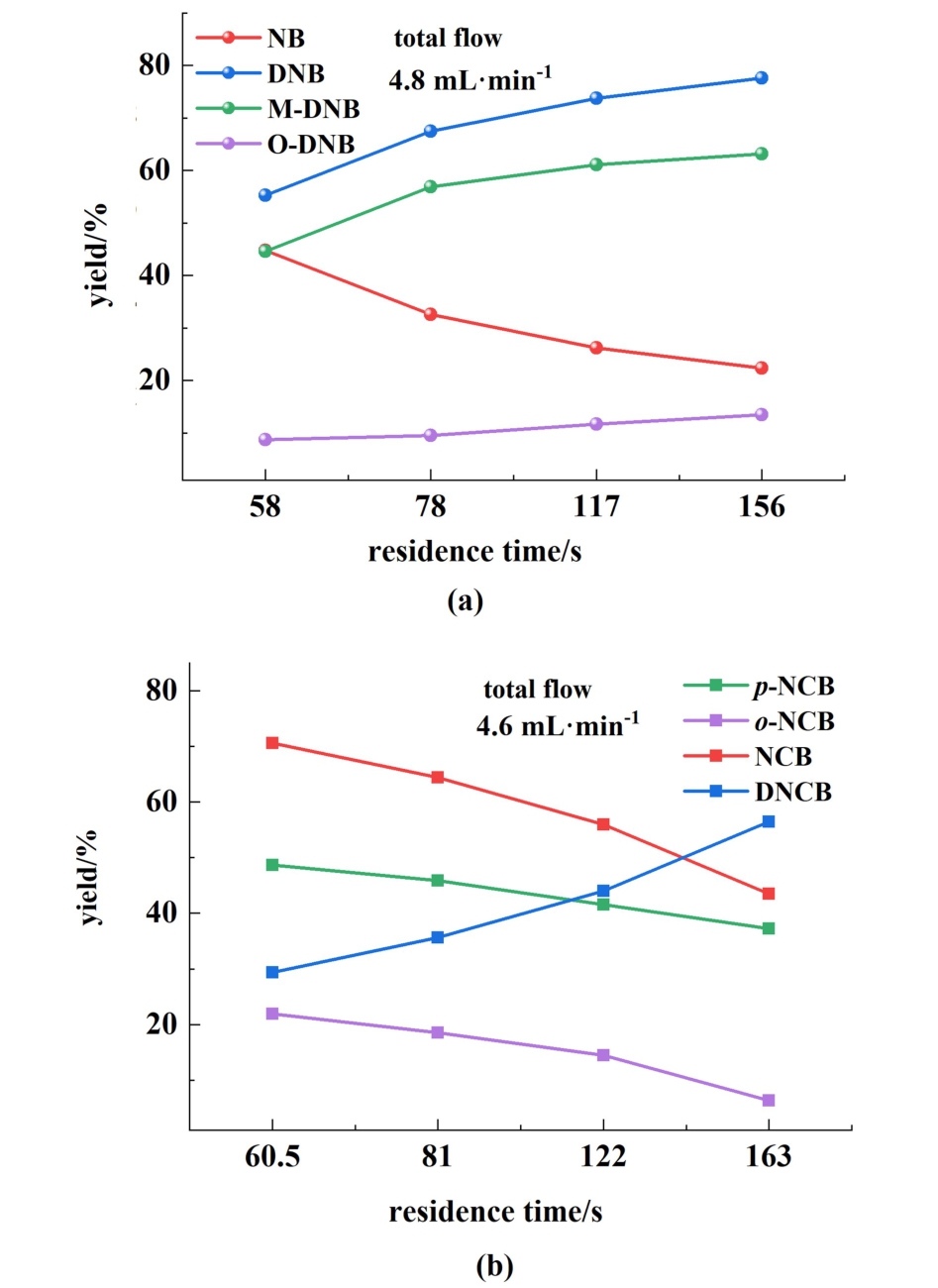
图9 停留时间对二硝化反应的影响(a)苯;(b)氯苯
Fig.9 Effect of residence time on the dinitration reaction of (a) benzene and (b) chlorobenzene
通过图9可以看出,增加停留时间,二硝化产物增多,当混酸的硝化强度较低,也就是混酸含水量较高时,提供足够的反应时间,可以使一硝化产物继续硝化,但很难反应完全,反应过程中会生成水,体系水含量会逐渐增多,降低混酸的硝化强度,最终二硝化产物的收率会停止增长。 相对而言,增加反应时间会降低m-DNB/o-DNB同分异构体比例,对于二硝基苯产物纯化控制有指导意义。对于DNCB,增加反应时间可进一步促进p-NCB的硝化进程,对于突破DNCB总收率瓶颈具有重要作用。
2.8 小中试放大实验以及结果
通过上述优化工艺参数指导苯和氯苯的高通量连续硝化实验(小中试规模),如图10所示。 其中强化混合微反应器带有特殊结构强化混合,会在物料流动的同时增加扰动,进一步提高物料的混合传质效率,特征尺寸相当于物料在环隙内径1.5 mm的套管微通道反应器中进行反应,反应器长度为1 m,整套小中试设备上配备有5根,每根持液量为25 mL,延时熟化微反应器为盘管式结构,规格为ϕ8 mm×1 mm,反应器盘管长度在20 m左右,持液量大约为600 mL,全设备总持液量在750 mL左右。反应过程中的换热介质温度由冷热介质循环机控制,同时会提供介质循环动力,每根反应器内置测温探头,可以实时进行温度检测。 设备尺寸经过放大,在微通道反应器中优化过后的条件得出的结果会有差异,工艺需进一步调整。 苯和氯苯的一硝化由于反应迅速,只使用2根强化混合微反应器,总持液量为50 mL左右,中段取样口接样,反应温度50 ℃,n(H2SO4) ∶n(HNO3) 为2.0 ∶1.0,含水量13%,混酸保温30 ℃,苯和氯苯的一硝化中试实验结果见表1和表2。
表1 苯一硝化和二硝化中试反应结果
Table 1 The results of mononitration and dinitration reaction of benzene in the pilot-scale
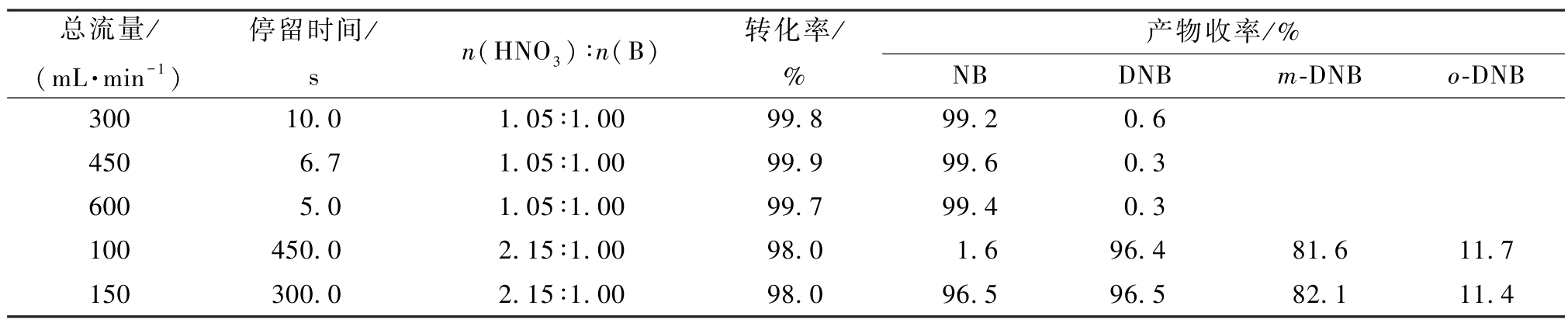
总流量/(mL·min-1)停留时间/s n(HNO3) ∶n(B) 转化率/%产物收率/%NB DNB m-DNB o-DNB 300 10.0 1.05 ∶1.00 99.8 99.2 0.6 450 6.7 1.05 ∶1.00 99.9 99.6 0.3 600 5.0 1.05 ∶1.00 99.7 99.4 0.3 100 450.0 2.15 ∶1.00 98.0 1.6 96.4 81.6 11.7 150 300.0 2.15 ∶1.00 98.0 96.5 96.5 82.1 11.4
表2 氯苯一硝化和二硝化中试结果
Table 2 The results of mononitration and dinitration reaction of chlorobenzene in the pilot-scale
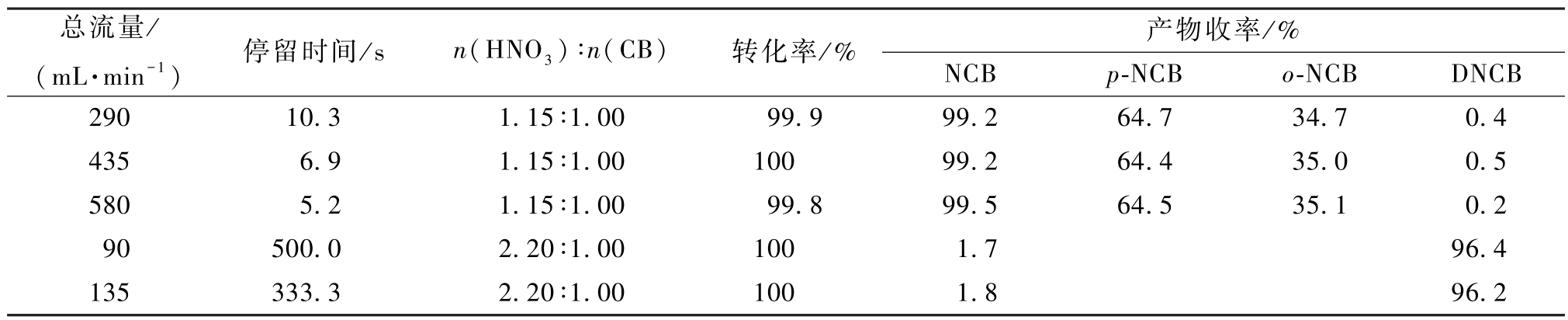
总流量/(mL·min-1) 停留时间/s n(HNO3) ∶n(CB) 转化率/% 产物收率/%NCB p-NCB o-NCB DNCB 290 10.3 1.15 ∶1.00 99.9 99.2 64.7 34.7 0.4 435 6.9 1.15 ∶1.00 100 99.2 64.4 35.0 0.5 580 5.2 1.15 ∶1.00 99.8 99.5 64.5 35.1 0.2 90 500.0 2.20 ∶1.00 100 1.7 96.4 135 333.3 2.20 ∶1.00 100 1.8 96.2
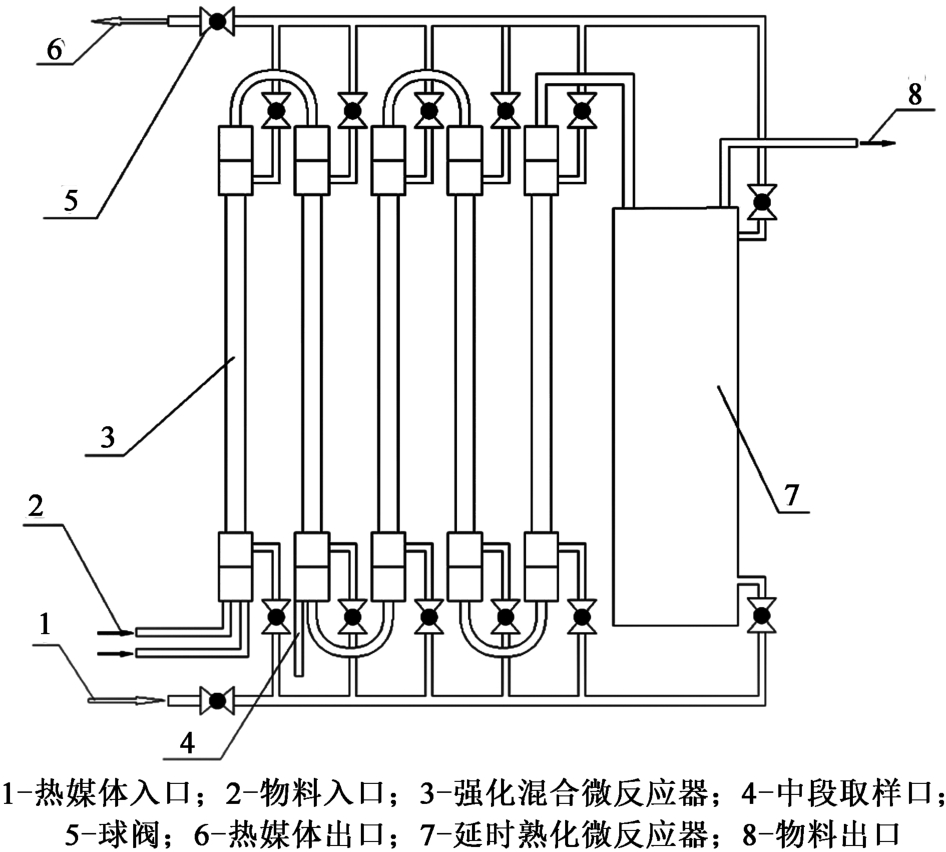
图10 中试设备示意图
Fig.10 Schematic diagram of pilot-scale equipment
苯和氯苯的二硝化使用全部反应器,总持液量为750 mL左右,反应温度80 ℃,硫酸和硝酸的配比为n(H2SO4) ∶n(HNO3)= 2.0 ∶1.0,混酸保温30 ℃。二硝化反应过程中,设备处于高温的状态,大量3.5%含水量的混酸与有机物料混合后,反应过于剧烈,导致原料发生过度氧化反应,生成黑色黏稠状物质。 对于二硝化反应过程,采取分段进料的方法,将中段取样口改为进料口,先使用含水量为8.0%的混酸使有机原料转化为一硝化产物,然后在设备中间进料口通入含水量为3.5%的混酸。 苯和氯苯的二硝化实验见表1和表2。 从小中试放大实验的结果可知,设备仍具有良好的反应性能和产物收率,未出现明显的放大效应,说明本工艺具有良好的工业化应用前景,为苯和氯苯硝化工艺的连续化、自动化和智能化生产提供有力支持。
3 结论
(1)获得苯和氯苯的连续硝化工艺。 苯的一硝化工艺实验条件:反应温度为50 ℃,物料配比n(HNO3) ∶n(B)= 1.05 ∶1.00,混 酸含水量为13%,停留时间控制在3 s左右,苯的转化率达到99.5%以上,NB的收率达到99%,DNB的收率控制在0.3%左右。 氯苯的一硝化工艺条件:n(HNO3) ∶n(CB)= 1.20 ∶1.00,反应停留时间控制在3 s左右,氯苯的转化率达到99.5%以上,NCB的总收率达到99.2%,p-NCB的收率在63.7%左右,o-NCB的收率在35.3%,DNCB的收率控制在0.3%左右。
(2)苯的二硝化工艺条件:反应温度90 ℃,物料配比n(HNO3) ∶n(B)= 2.15 ∶1.00,混酸含水量为3.5%,流量4.8 mL·min-1,停留时间控制在156 s左右,NB的收率在1.5%左右,DNB的总收率达到98.5%,m-DNB的收率在82.5%左右,o-DNB的收率在12.5%左右,p-DNB的收率为3.5%。 氯苯的二硝化实验条件:物料配比n(HNO3) ∶n(CB)=2.20 ∶1.00,混酸含水量为3.5%,流量92 mL·min-1,停留时间控制在163 s(可继续提高)左右,NCB的总收率在1.4%左右,一硝化产物多为p-NCB,DNCB的总收率达到98.6%左右,其中2,4-二硝基氯苯的收率在95%以上。
(3)通过小中试放大实验验证了微通道技术在苯和氯苯硝化工艺中的应用可行性。 实验结果表明,优化后的工艺条件在150 ~750 mL·min-1通量(小中试规模)下仍具有良好的反应性能和产物收率,未出现明显的放大效应。
[1] GEYER K, CODÉE DR J D C, SEEBERGER PROF DR P H.Microreactors as tools for synthetic chemists: The chemists’round-bottomed flask of the 21st century? [J]. Chemistry-A European Journal, 2006, 12(33): 8434-8442
[2] 刘全, 张钊, 邵先钊, 等. 连续流反应技术在药物分子合成中的研究进展[J]. 安徽化工, 2020, 46(5): 11-13, 19 LIU Quan, ZHANG Zhao, SHAO Xianzhao, et al. Study progress of continuous flow technology in drug molecular synthesis[J]. Anhui Chemical Industry, 2020, 46(5): 11-13, 19(in Chinese)
[3] 陈蔚, 冯明杰, 许波, 等. 原料药生产中应用连续流动化学的质量考量[J]. 中国医药工业杂志, 2022, 53(10):1386-1393 CHEN Wei, FENG Mingjie, XU Bo, et al. Quality considerations for application of continuous flow chemistry in API manufacturing[J]. Chinese Journal of Pharmaceuticals, 2022, 53(10):1386-1393(in Chinese)
[4] 李文鹏, 高展鹏, 侯翠红. “双碳” 背景下河南省精细化工行业转型升级现状及发展建议[J]. 当代化工研究, 2023(5):188-190 LI Wenpeng, GAO Zhanpeng, HOU Cuihong. Current situation and development suggestions of the fine chemical enterprises in Henan Province under the background of “double carbon”[J].Modern Chemical Research, 2023(5): 188-190(in Chinese)
[5] HORNUNG C H, NGUYEN X, KYI S, et al. Synthesis of RAFT block copolymers in a multi-stage continuous flow process inside a tubular reactor[J]. Australian Journal of Chemistry, 2013, 66(2): 192
[6] DR K J, DR V H, DR H L P, et al. Chemistry in microstructured reactors[J]. Angewandte Chemie International Edition,2004, 43(4): 406-446
[7] MAE K. Advanced chemical processing using microspace[J].Chemical EngineeringScience,2007,62 ( 18/19/20 ):4842-4851
[8] HAN B, CHEN Y, ZOU H, et al. Study on characteristics of toluene/chlorobenzene nitrification in different microreactors[J].Chemical Engineering Research and Design, 2024, 205:343-353
[9] VOLKER H, STEFFEN H, HOLGER L. Chemical micro process engineering: Fundamentals, modelling and reactions[M]. Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA,2004
[10] JIN N, SONG Y, YUE J, et al. Heterogeneous nitration of nitrobenzene in microreactors: Process optimization and modelling[J]. Chemical Engineering Science, 2023, 281: 119198
[11] 陈光文, 袁权. 微化工技术[J]. 化工学报, 2003, 54(4):427-439 CHEN Guangwen, YUAN Quan. Micro-chemical technology[J].CIESC Journal, 2003, 54(4): 427-439(in Chinese)
[12] ZHANG Q, LIU H, ZHAO S, et al. Hydrodynamics and mass transfer characteristics of liquid-liquid slug flow in microchannels: The effects of temperature, fluid properties and channel size[J]. Chemical Engineering Journal, 2019, 358: 794-805
[13] LV H, YANG Z, ZHANG J, et al. Liquid flow and mass transfer behaviors in a butterfly-shaped microreactor[J]. Micromachines,2021, 12(8): 883
[14] 张经纬, 周弋惟, 陈卓, 等. 微反应器内的有机合成前沿进展[J]. 化工学报, 2022, 73(8): 3472-3482 ZHANG Jingwei, ZHOU Yiwei, CHEN Zhuo, et al. Advances in frontiers of organic synthesis in microreactor[J]. CIESC Journal,2022, 73(8): 3472-3482(in Chinese)
[15] 孙青霞, 苏焕焕, 金晓云. 微通道技术在提升精细化工安全中的应用进展[J]. 浙江化工, 2023, 54(9): 43-48 SUN Qingxia, SU Huanhuan, JIN Xiaoyun. Application progress of microchannel technology in improving the safety of fine chemicals[J]. Zhejiang Chemical Industry, 2023, 54(9): 43-48(in Chinese)
[16] 陈旻. 微通道反应器在聚合领域中的应用研究进展[J]. 浙江化工, 2021, 52(9): 31-36 CHEN Min. Research progress in application of microchannel reactors in the field of polymerization[J]. Zhejiang Chemical Industry, 2021, 52(9): 31-36(in Chinese)
[17] GÜNTHER A, KHAN S A, THALMANN M, et al. Transport and reaction in microscale segmented gas-liquid flow[J]. Lab on a Chip, 2004, 4(4): 278-286
[18] LIU H, YAO C, ZHAO Y, et al. Heat transfer characteristics of CO2 desorption from N-methyldiethanolamine solution in a microchannel reactor[J]. Chemical Engineering & Technology, 2018,41(7): 1398-1405