CO2加氢制甲烷,不仅可以降低碳排放,而且可以将可再生能源经电解水生成的氢气储存于甲烷,实现储能[1-2]。
已报道的CO2加氢制甲烷催化剂有贵金属(钌和铑)催化剂和非贵金属(镍、铁和钴[3]等)催化剂;贵金属催化剂具有较好的活性和选择性,但成本较高、稳定性仍待提高,非贵金属催化剂成本较低、性能较好。Ni基催化剂可以通过组分调控,如载体和助剂选择[4]、添加第二金属[5]等途径改善催化性能,获得优良活性、选择性和稳定性。然而,Ni基催化剂面临如下问题:CO2化学稳定性高,活化较困难,提高反应活性是一个重点;CO2加氢制甲烷是放热反应,在高温反应过程中,反应放热会使催化剂表面局部过热,加速活性组分镍金属颗粒的烧结,导致失活。
氧空位被认为是活化CO2的一类重要活性位点。如Cisneros等[6]研究了Ru/TiO2催化剂上的氧空位的作用,发现氧空位能削弱吸附在其上的CO2分子的C—O键促进其被活化H2还原。Ni的高分散是优良性能的CO2加氢制甲烷催化剂的一项重要特征。氧化物担载镍基催化剂上,氧化物表面的氧空位活化CO2,金属镍活化氢分子和由CO2转化并迁移至镍表面的CO,CO加氢生成甲烷。如Xie等[7]研究了Ni/CeO2纳米催化剂的甲烷化表现,发现Ni能够促进H2分子裂解为活性氢原子;Cortazar等[8]制备Ce0.5Ni0.1Co0.1Cu0.1Zn0.1Mg0.1Ox催化剂,研究其甲烷化的构效关系,发现金属铜和高熵氧化物对CO2转变为CO有关键作用,而金属Ni和Co主要促进了后续的CO加氢转变为CH4。
所以,氧空位和高分散的金属镍对CO2加氢制甲烷催化剂很重要。
高熵氧化物(HEOs)是指5个或更多金属阳离子的单相氧化物[9],其最大构型熵Sconfig≥1.5R(R为气体摩尔常数)。HEOs由多种金属阳离子构成,不仅赋予其高构型熵(高混乱度),使得高熵氧化物表面易于形成氧空位[10],也有利于金属离子均匀混合;若将氧化镍均匀分散于其上,则还原后易于实现金属Ni的高分散。
柠檬酸可以通过络合实现多种金属元素的均匀混合,这样利于煅烧过程中组分之间发生固相反应,是制备复合氧化物的一种有效方法。
基于以上背景,本研究采用柠檬酸络合法制备了含有Ni、Ce、Zr、Y、La和Ti等6种金属元素的混合氧化物,还原得到萤石型HEOs负载Ni催化剂考察其对CO2加氢制甲烷的性能,并借助多种表征方法对制备催化剂进行表征。发现5种金属元素Ce、Zr、Y、La和Ti构成的混合氧化物和萤石型HEOs均易于形成氧空位合和金属镍的高分散;该5种元素构成的混合氧化物由于煅烧温度较低,在形成氧空位方面更具优势。
1 实验部分
1.1 主要试剂
试剂:Ni(NO3)2·6H2O,天津市大茂化学,分析纯;Ce(NO3)3·6H2O、Y(NO3)3·6H2O、La(NO3)3·6H2O和C6H8O7,上海阿拉丁生化科技,分析纯;Zr(NO3)4·5H2O和C16H36O4Ti,迈瑞尔生化科技,分析纯;(HOCH2)2,天津光复精细化工,分析纯。
1.2 催化剂制备
采用柠檬酸络合法合成了不同Ni负载量的x%Ni/(CeZrYLaTi)0.2O2(x=0、5、10和20)催化剂,其中x表示Ni的质量分数(以NiO计)。首先,将各金属硝酸盐、柠檬酸和乙二醇溶解于去离子水中,其中n(金属硝酸盐之和)∶ n(柠檬酸)∶n(乙二醇)=1.0∶1.2∶ 0.2,Ce、Zr、Y、La和Ti为等物质的量;然后,在80 ℃的水浴锅中搅拌上述混合溶液,直到获得凝胶。最后,将凝胶在120 ℃下干燥12 h,煅烧时先在350 ℃的空气中煅烧2 h,然后在550 ℃(650、750、850 和950 ℃)的空气气氛中煅烧4 h。
1.3 催化剂表征
1.3.1 N2吸脱附
使用Tristar3000仪器在-196 ℃下测量了N2物理吸附-脱附等温线。
在测量前将样品在300 ℃下真空脱水4 h,然后在0.05~0.30的相对压力范围内进行N2吸附。使用BET方程和BJH方法计算催化剂的比表面积和孔体积。
1.3.2 程序升温还原(H2-TPR)
使用天津先权TP-5080多功能自动吸附仪上测试了H2程序升温还原曲线。
在测试前用体积分数为5%的H2/Ar吹扫35 mg的催化剂,该催化剂在石英管中被吹扫30 min;然后,将石英管从室温以10 ℃·min-1的速率加热到900 ℃,并在该温度保持3 min,用TCD检测器记录H2的变化。在测试过程中,气体流速维持在30 mL·min-1。
1.3.3 程序升温脱附(TPD)
使用与H2-TPR测试相同的设备进行TPD测试。
将一定质量的还原后催化剂在300 ℃下用H2预处理1 h,然后该温度下用惰性气体He吹扫30 min,冷却至室温。然后,在室温下用相应气体(H2、CO2和CO)处理样品30 min,接着用惰性气体He吹扫30 min,除去未吸附的分子。最后在相同的惰性气氛中以10 ℃·min-1的升温速率从室温升温到900 ℃,并用TCD检测脱附的气体。
1.3.4 X射线衍射(XRD)
X射线衍射(XRD)谱图在Bruker D8焦点X射线衍射仪上记录,配备了过滤Ni的Cu_Kα源,其波长为λ=0.154 06 nm,样品的2θ角度范围为20°~80°。
1.3.5 X射线光电子能谱(XPS)
使用美国Thermo Scientific K-Alpha光电子能谱仪进行X射线光电子谱图测试。光谱仪的X射线发射源在5×10-9 mbar(1 mbar=100 Pa)的压力下为Al_Kα线(hν=1 486.6 eV)。
通过C 1s峰(284.8 eV)校正所有样品的全部结合能数据。
1.3.6 透射电子显微镜(TEM)
使用JEOL JEM-2100F显微镜场发射透射电子显微镜,获得催化剂的TEM图像和元素映射。在测试之前,样品被磨成粉末并分散到乙醇中,然后经过30 min的超声处理,之后滴入双层膜中。
1.3.7 热分析
热重和差示扫描量热使用NETZSCH STA449F3仪器测定。在空气气氛下,以10 ℃·min-1的加热速率从室温升至1 000 ℃分析样品。
稳定性测试后的催化剂在DTG-60AH仪器上测试其热重曲线。在空气气氛中以10 ℃·min-1的升温速率从室温加热至1 000 ℃,记录样品重量变化。
1.4 催化剂性能评价
CO2加氢制甲烷性能测试使用固定床反应器。反应测试时,将40~60目的0.2 g催化剂与0.2 g的石英砂混合加入反应管中,参与反应。反应前,将催化剂在700 ℃下的30 mL·min-1的H2气氛中还原2 h。预处理后,设置反应压力为3 MPa,使用n(H2)∶ n(CO2)=4∶1的反应气,体积分数为3.2%的N2做气相色谱的内标气体。气体空速为15 000 mL·g-1·h-1。反应测试的温度范围为300~550 ℃。通过气相色谱仪(GC,FULI GC 979011)检测出口气体成分(如N2,CO2,CO和CH4),以N2为内标气体。
2 结果与讨论
2.1 XRD表征
对750 ℃制备的不同Ni含量的催化剂x%Ni/(CeZrYLaTi)0.2O2进行XRD测试,结果见图1(a)、图1(c)和图1(e)。
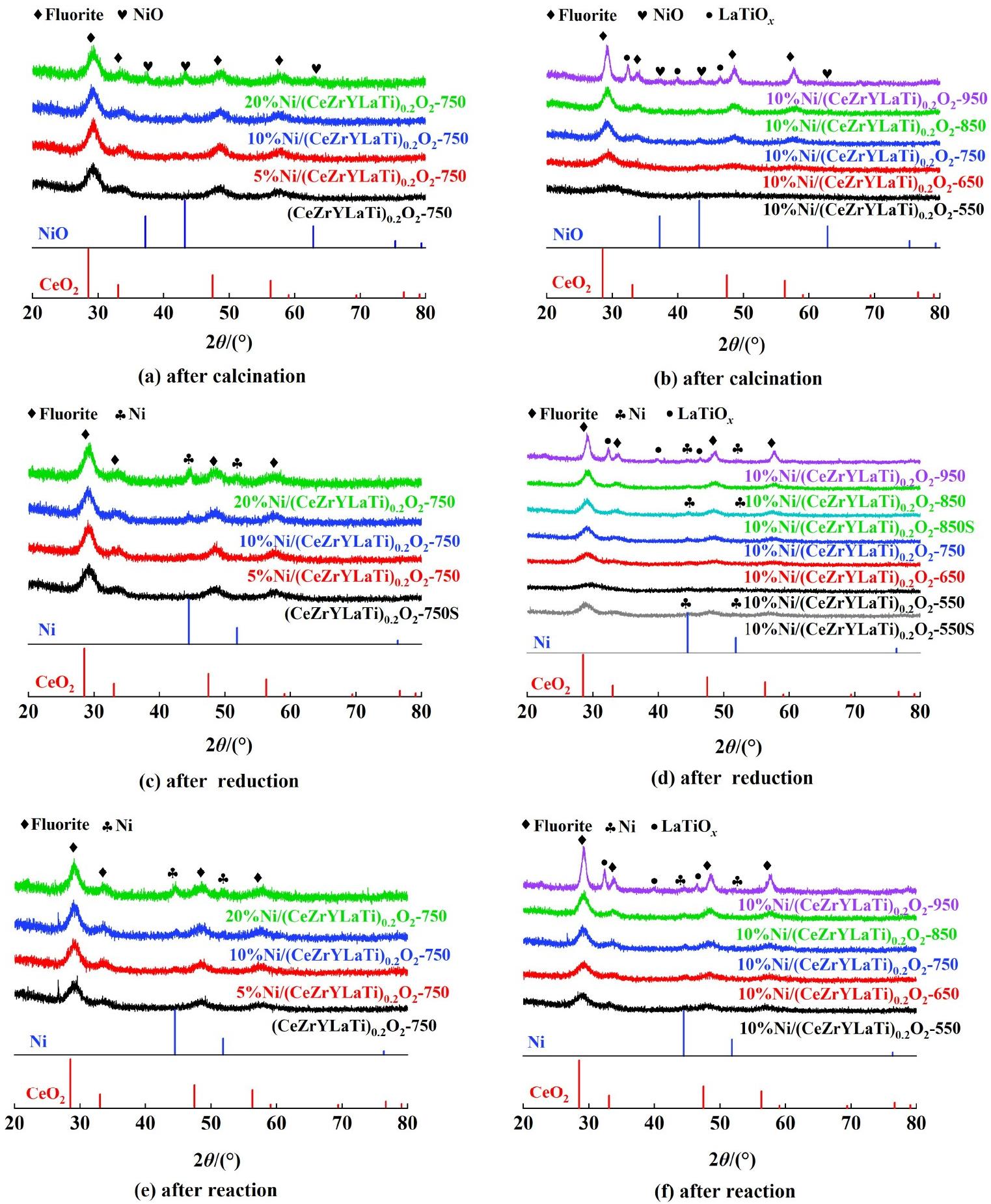
图1 不同Ni含量和不同煅烧温度的催化剂(a)和(b)煅烧后;(c)和(d)还原后和(e)和(f)反应后的XRD图[图1(d)中标记550S、850S的曲线分别表示550和850 ℃煅烧催化剂稳定性测试后的XRD曲线]
Fig.1 XRD patterns of catalysts with different Ni content and different calcination temperatures (a),(b)after calcination;(c), (d)after reduction and (e), (f)after reaction[Curves marked 550S and 850S in Fig.1(d) indicate XRD curves after stability test of calcined catalysts at 550 and 850℃, respectively]
由图1可知煅烧后催化剂中存在萤石特征峰[11],分别是(111)、(200)、(220)和(311)晶面;显示形成了萤石型高熵氧化物[12]。煅烧后的XRD中能看到NiO特征峰,还原后转变为金属Ni,对比还原后与反应后XRD谱图,萤石相与Ni相特征峰无明显变化。根据XRD结果计算得到煅烧后、还原后与反应后的萤石相颗粒尺寸见表1。可以看到750 ℃制备的负载Ni催化剂,其颗粒尺寸在反应前后变化不大,基本没有烧结发生。表明高熵氧化物和其负载的Ni颗粒具有很好的抗烧结性能。
表1 x%Ni/(CeZrYLaTi)0.2O2-750(x=0, 5, 10, 20)催化剂萤石晶型的颗粒尺寸
Table 1 Particle sizes of x%Ni/(CeZrYLaTi)0.2O2-750(x=0,5,10, 20) catalysts fluorite crystal type
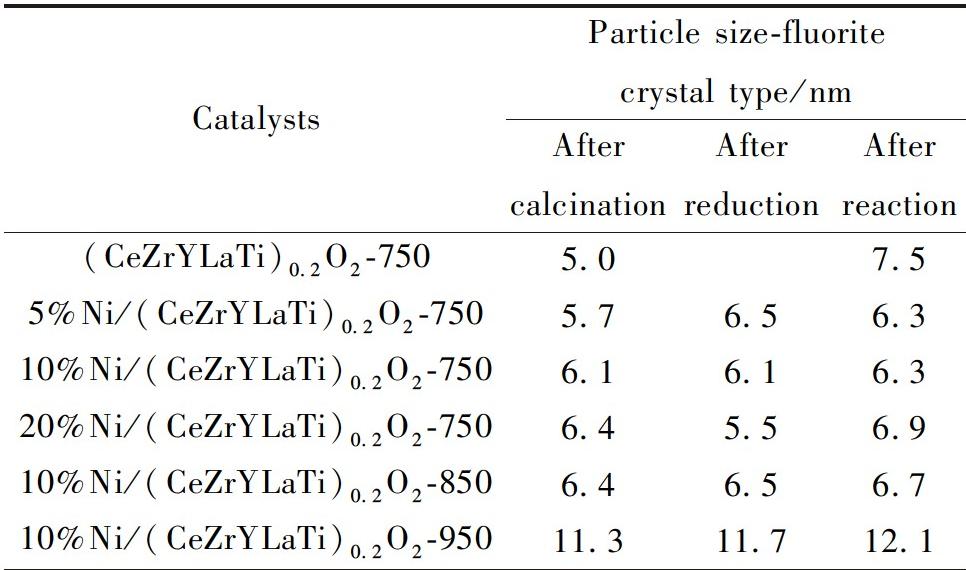
After After After 10%Ni/(CeZrYLaTi)0.2O2-8506.46.56.7Particle size-fluorite Catalystscrystal type/nm calcinationreductionreaction(CeZrYLaTi)0.2O2-7505.07.55%Ni/(CeZrYLaTi)0.2O2-7505.76.56.310%Ni/(CeZrYLaTi)0.2O2-7506.16.16.320%Ni/(CeZrYLaTi)0.2O2-7506.45.56.910%Ni/(CeZrYLaTi)0.2O2-95011.311.712.1
对于10%Ni负载量(质量分数,下同)的催化剂,煅烧温度对高熵氧化物形成的影响,结果见图1(b)、图1(d)和图1(f)。由图1可知,低温550和650 ℃煅烧的催化剂没有出现完整的萤石特征峰,即没有形成高熵氧化物;750和850 ℃制备的催化剂的XRD谱图中出现了萤石特征峰,并且是单相,可以判断形成高熵氧化物;而950 ℃样品谱图中出现萤石特征峰,但同时有归属于镧钛氧化物的物相,即出现了相分离[12],不符合高熵氧化物的单相特征,即没有形成高熵氧化物。而无论是还原后还是反应后,Ni相与萤石相保持稳定,Ni颗粒在载体表面分散性良好,不易烧结。由表1可知,750和850 ℃催化剂煅烧后、还原后和反应后,萤石相颗粒尺寸在6.1~6.7 nm范围,显示这个温度区间HEOs的物相保持稳定、不发生烧结。950 ℃ 催化剂的晶粒尺寸为11.3(煅烧后)、11.7(还原后)和12.1 nm(反应后),明显大于750和850 ℃煅烧的催化剂,表明过高温度煅烧出现相分离的同时,导致萤石相颗粒烧结。
图1(d)中标记有550S与850S 2条曲线分别是催化剂10%Ni/(CeZrYLaTi)0.2O2-550进行200 h稳定性测试后和10%Ni/(CeZrYLaTi)0.2O2-850催化剂进行100 h稳定性测试后的XRD曲线。对于550 ℃催化剂,稳定性后的XRD曲线上出现了明显的萤石特征峰,且是单相存在。还原后萤石特征峰弥散而且强度很弱,稳定性测试后萤石相衍射峰强度显著增大、晶粒尺寸为5.5 nm,表明在长时间的反应中,载体中的混合氧化物部分转变为HEOs。对于850 ℃催化剂,稳定性后XRD曲线与还原后XRD曲线对比,高熵氧化物相与Ni相无明显变化,同时萤石相颗粒尺寸稳定性测试前后均为6.5 nm,表明高熵氧化物及其负载Ni纳米颗粒抗烧结性能优越。
综上所述,在催化剂制备时,较低的煅烧温度无法形成高熵氧化物,主要是多种氧化物微晶的均匀混合;而较高的950 ℃煅烧会导致形成的萤石相发生相分离,也无法得到HEOs;适当的煅烧温度(750~850 ℃)可以形成HEOs,这与Rost等[13]的研究结果一致。而对于形成高熵氧化物的催化剂而言,HEO具备的优良热稳定性发挥作用,使得HEO载体与负载Ni颗粒不发生明显烧结。
2.2 TEM表征
图2与图3为稳定性测试前后的元素能谱图(EDS),显示550和850 ℃煅烧的催化剂,煅烧后、还原后以及稳定性测试后,催化剂中的Ce、Zr、Y、La和Ti 5种元素均分布均匀[14],没有发生团聚;表明所制备催化剂各组分均匀混合。
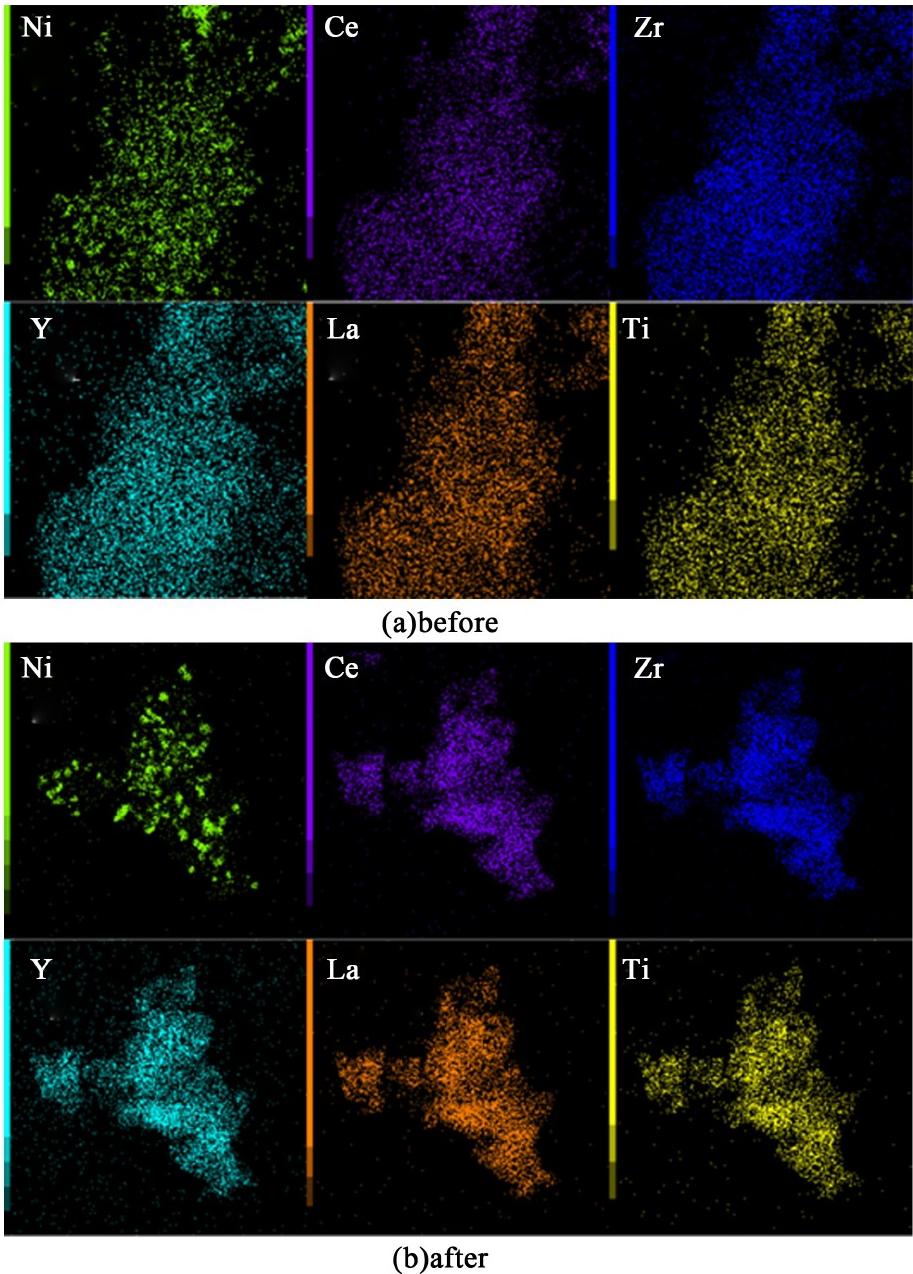
图2 10%Ni/(CeZrYLaTi)0.2O2-550催化剂稳定性前后的元素能谱图(EDS)
Fig.2 Elemental energy spectra (EDS) before and after stability of 10%Ni/(CeZrYLaTi)0.2O2-550 catalyst
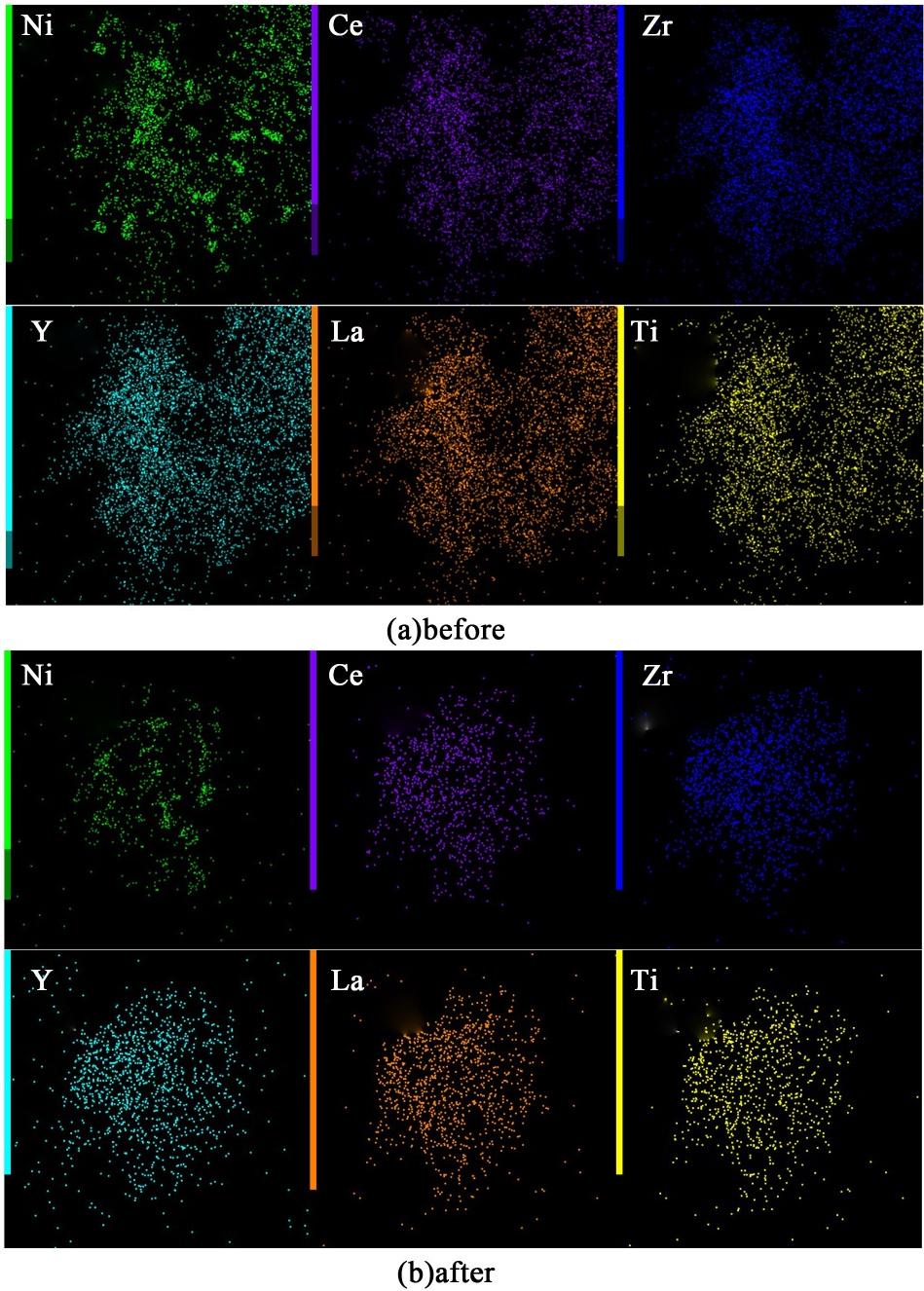
图3 10%Ni/(CeZrYLaTi)0.2O2-850催化剂稳定性前后的元素能谱图(EDS)
Fig.3 Elemental energy spectra (EDS) before and after stability of 10%Ni/(CeZrYLaTi)0.2O2-850 catalyst
还原后催化剂中,Ni元素处于高分散状态;稳定性测试后,镍仍以纳米颗粒形式存在,仍处于高分散状态。表明Ni元素分散性好,稳定性测试后没有烧结。
经由柠檬酸络合法制备的10%Ni/(CeZrYLa-Ti)0.2O2催化剂的元素分散性良好,无论是否形成高熵氧化物,表明本研究的5种金属阳离子的选择合适。
2.3 H2-TPR表征
图4(a)是750 ℃煅烧、不同镍负载量的TPR图,420~430 ℃范围的还原峰属于催化剂表面氧空位上吸附氧的还原,其峰面积随Ni含量增加没有明显变化;500~600 ℃的弱还原峰归属于催化剂表面高分散Ni2+的还原[15],该部分峰面积随Ni含量提高略有增长;700 ℃左右的还原峰归属于与HEOs作用强或进入HEOs晶格的Ni2+的还原,其峰面积随Ni含量增加而线性增加;800~850 ℃区间弥散还原峰,属于形成体相氧空位对应的还原,对应HEOs晶粒内部部分Ce4+或Ti4+被还原为Ce3+或Ti3+[16,17]。
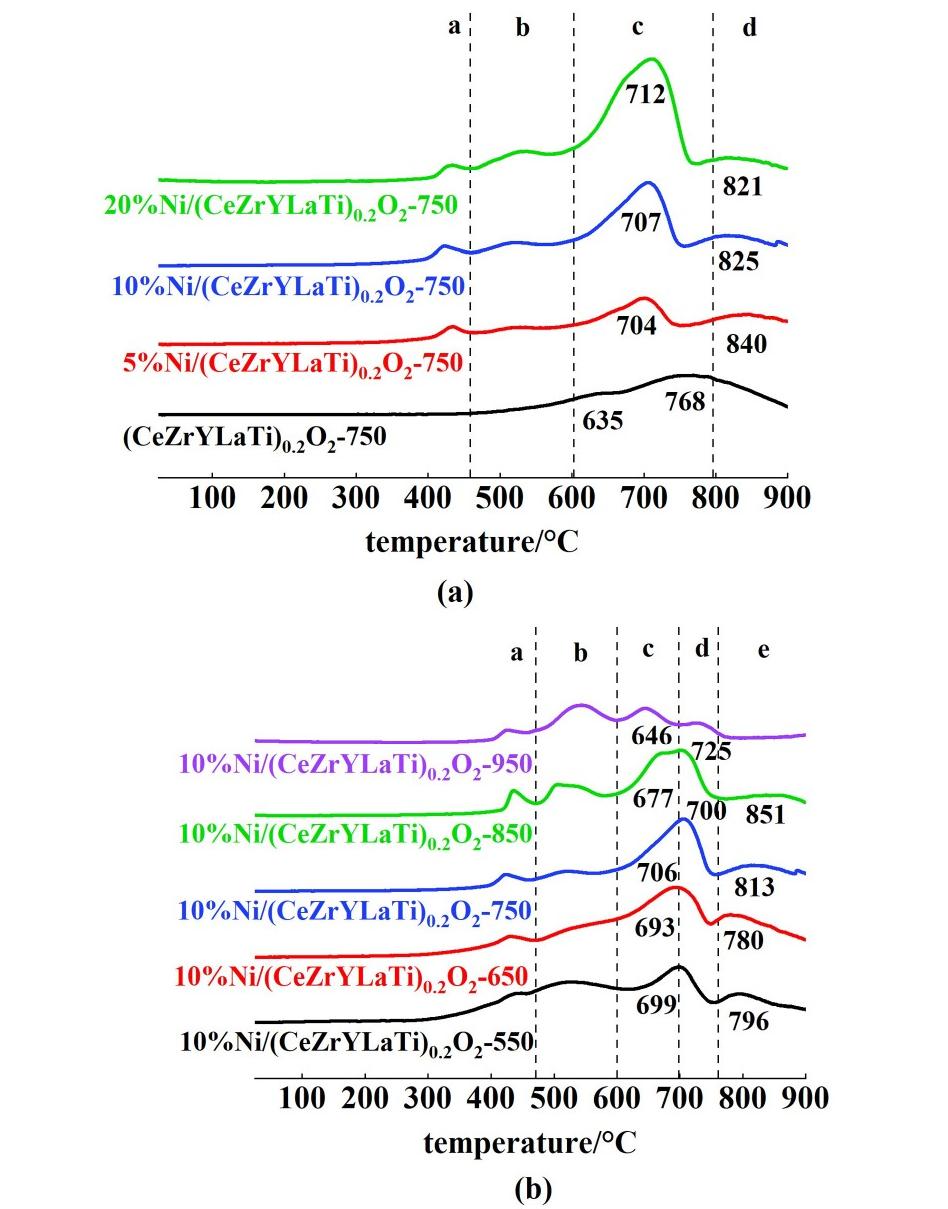
图4 (a)x%/Ni/(CeZrYLaTi)0.2O2-750(x=0,5,10,20)的H2-TPR曲线;(b)10%Ni/(CeZrYLaTi)0.2O2-T(T=550,650,750,850和950)的H2-TPR曲线
Fig.4 (a)H2-TPR curves of x%/Ni/(CeZrYLaTi)0.2 O2-750 (x=0, 5, 10, 20); (b) H2-TPR curves of 10%Ni/(CeZrYLaTi)0.2O2-T (T=550, 650, 750, 850, 950)
可以看出不含Ni的(CeZrYLaTi)0.2O2-750催化剂已经形成了高熵氧化物,其中的2个还原峰位于635和768 ℃,应该分别对应表面氧空位上的吸附氧还原和形成体相氧空位的还原。该还原峰温度显著低于含镍催化剂的对应还原峰,可能是镍与高熵氧化物的相互作用所致。
图4(b)是10%镍含量、不同煅烧温度催化剂的TPR图,550、650和750 ℃煅烧的催化剂,TPR曲线类似于图4(a),区别在于随着煅烧温度的升高,氧化物表面高分散的镍减少,进入HEOs晶格的镍增加,显示升高煅烧温度利于形成HEOs以及利于镍离子进入HEOs晶格。当煅烧温度达到950 ℃时,700 ℃附近归属于HEOs中镍离子的还原峰分裂为2个小峰,表明催化剂在该温度下由于相分离,体相的Ni2+出现了2种存在形式[18],一种是在高熵氧化物内部的Ni2+,另一种是与分离出的氧化物相互作用之中的Ni2+,这与前面XRD结果相符合。对于煅烧温度为850 ℃的催化剂,TPR曲线显示开始出现相分离的苗头,但是仍然主要以HEOs存在。
性能测试前,催化剂在700 ℃氢气中还原,TPR结果显示催化剂中的镍离子全部被还原为金属镍。
2.4 TPD表征
由表2可知,不同煅烧温度负载10%Ni的催化剂中,850 ℃样品还原后分散度最高为24.6%,其他样品基本维持在22%水平。各催化剂还原后的Ni比表面积、Ni平均颗粒尺寸无明显区别。对于稳定性测试后催化剂,可以看到分散度略微下降,Ni平均颗粒尺寸发生略微长大,但烧结情况不明显;Ni比表面积下降幅度也不大,550 ℃的样品从还原后的148.5 m2·g-1降低为稳定性后的140.1 m2·g-1,850 ℃的样品从还原后的146.4 m2·g-1降低为稳定性后的139.3 m2·g-1,分别下降了5.7%和4.8%。考虑到镍分散度、晶粒尺寸和比表面积的测定存在较大的误差,这些小幅度的下降说明催化剂中镍的抗烧结性能较好。
表2 根据H2-TPD和N2吸脱附测试计算的还原后及稳定性测试后10%Ni/(CeZrYLaTi)0.2O2-T(T=550,650,750,850和950)的物理参数
Table 2 Physical parameters of 10%Ni/(CeZrYLaTi)0.2O2-T(T=550, 650, 750, 850, 950) after reduction and stability tests calculated based on H2-TPD and N2 adsorption and desorption tests
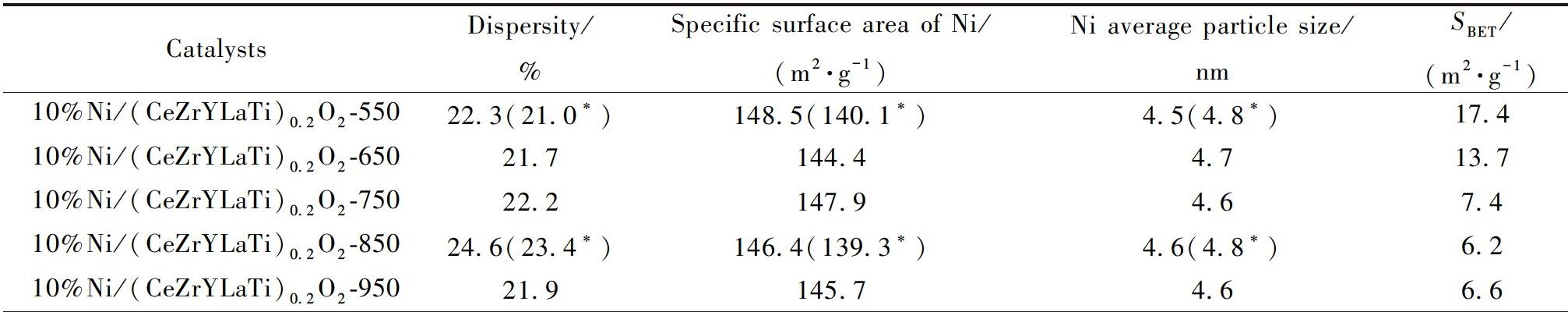
*催化剂在550或850 ℃稳定性测试后的数据。
CatalystsDispersity/Specific surface area of Ni/Ni average particle size/S BET/%(m2·g-1)nm(m2·g-1)10%Ni/(CeZrYLaTi)0.2O2-55022.3(21.0*)148.5(140.1*)4.5(4.8*)17.410%Ni/(CeZrYLaTi)0.2O2-65021.7144.44.713.710%Ni/(CeZrYLaTi)0.2O2-75022.2147.94.67.410%Ni/(CeZrYLaTi)0.2O2-85024.6(23.4*)146.4(139.3*)4.6(4.8*)6.210%Ni/(CeZrYLaTi)0.2O2-95021.9145.74.66.6
550和850 ℃煅烧的10%Ni/(CeZrYLaTi)0.2O2催化剂700 ℃还原后的CO2-TPD结果见图5(a)。由图5(a)可知,还原后催化剂上有3个脱附峰,其分别对应于与催化剂表面结合弱(<270 ℃)、中等(270~540 ℃)、强(>540 ℃)3种碱性位[19][20]。其中,弱碱性位点归因于表面OH组,中等碱性位点归因于Lewis酸碱对,强碱性位点归因于表面吸附的O2-物种[21]。CO2加氢制甲烷过程中,中等碱性位点是活化CO2的活性位,另外2类碱性位点几乎没有作用[22]。与850 ℃ 煅烧催化剂相比,550 ℃煅烧催化剂中等强度碱性位较多,活性也应该更好。
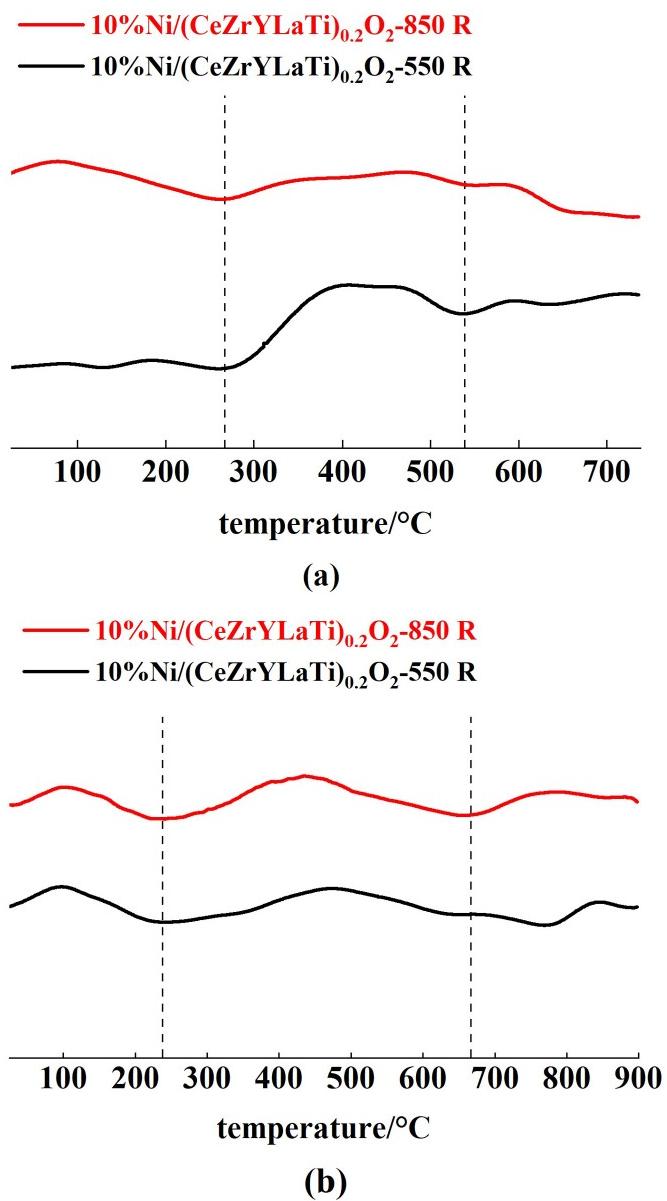
图5 550和850 ℃煅烧的10%Ni/(CeZrYLaTi)0.2O2催化剂700 ℃还原后的(a)CO2-TPD;(b)CO-TPD
Fig.5 (a) CO2-TPD; (b) CO-TPD of 10%Ni/(CeZrYLaTi)0.2O2 catalysts calcined at reduction 550 and 850 ℃ after reduction at 700 ℃
图5(b)是还原后催化剂的CO-TPD,存在3个脱附峰[23],其中中等强度的吸附峰(240~660 ℃)对应可以参与活化反应的CO,其中550 ℃的峰温高于850 ℃制备催化剂,表明550 ℃催化剂表面与CO结合的强度相对更高。中等吸附峰的峰面积对于2种催化剂基本相同,即550和850 ℃煅烧的催化剂对CO的吸附位的浓度相近。作为反应中间体的CO,与550 ℃表面结合更强,表明其更容易进一步加氢转化为CH4,而高温850 ℃的中等CO结合强度相对较低,使得中间体CO相对更多的脱附,作为副产物CO排出,从而使得CH4选择性的下降与CO2转化率的降低。
2.5 热分析表征
550与850 ℃制备的10%Ni/(CeZrYLaTi) 0.2O2催化剂稳定性后的TG结果见图6。由图6可知,550与850 ℃制备的催化剂在稳定性测试后的TG曲线上只有1个质量增加的峰,对应Ni氧化为NiO[24],经计算积碳量相对无碳沉积的理论质量分别为1.3%和0.7%,表明积碳微弱[25]制备的HEOs担载Ni催化剂具有优良的抗积碳性能。
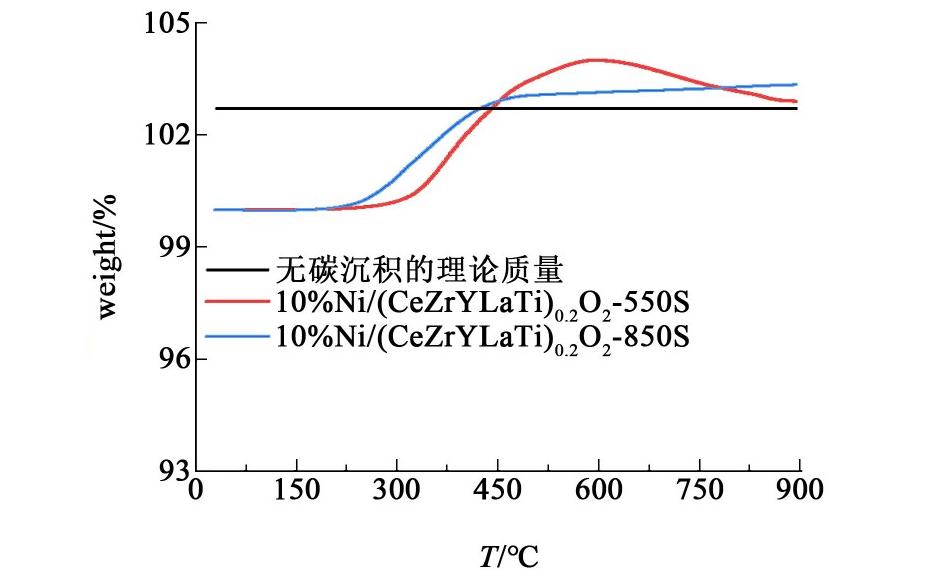
图6 550与850 ℃制备的10%Ni/(CeZrYLaTi)0.2O2催化剂稳定性后的TG
Fig.6 TG curves of 10%Ni/(CeZrYLaTi)0.2O2 catalysts prepared at 550 ℃ and 850 ℃ after stability
利用TG-DSC对负载Ni的氧化物载体形成高熵氧化物的条件进行研究,结果见图7。由图7可知,DSC曲线上峰温在408.7 ℃左右的大放热峰,且伴随着明显的质量损失,应是催化剂预煅烧未完全除去的柠檬酸络合物的燃烧放热[26];而在680 ℃左右,存在由于形成高熵氧化物的相变[27]而产生的微小放热峰。
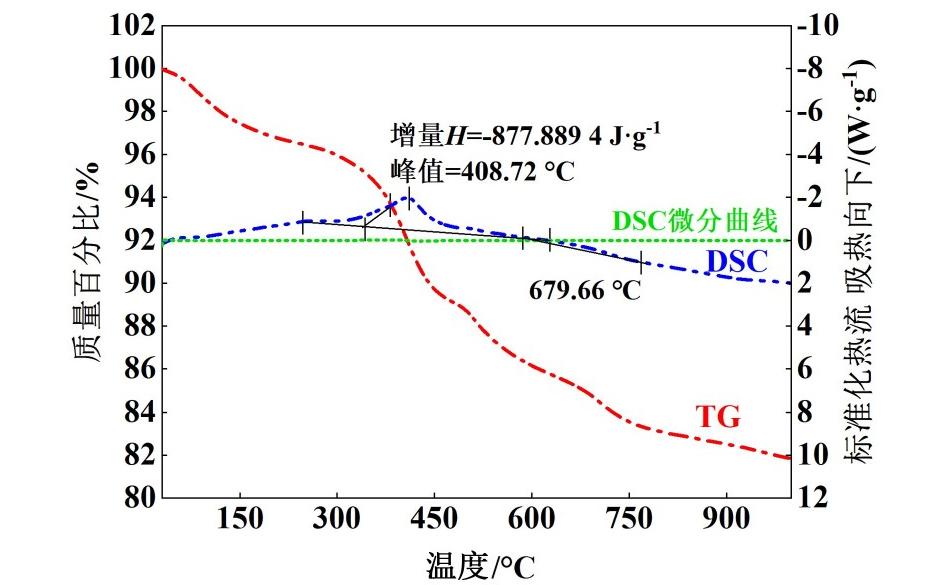
图7 催化剂10%Ni/(CeZrYLaTi)0.2O2经350 ℃煅烧2 h后测试的TG-DSC曲线
Fig.7 TG-DSC curve of catalyst 10%Ni/(CeZrYLaTi)0.2O2 after calcination at 350 ℃ for 2 h
2.6 XPS表征
利用XPS技术研究了稳定性测试前后550与850 ℃制备催化剂的表面电子情况,结果见图8和表3。
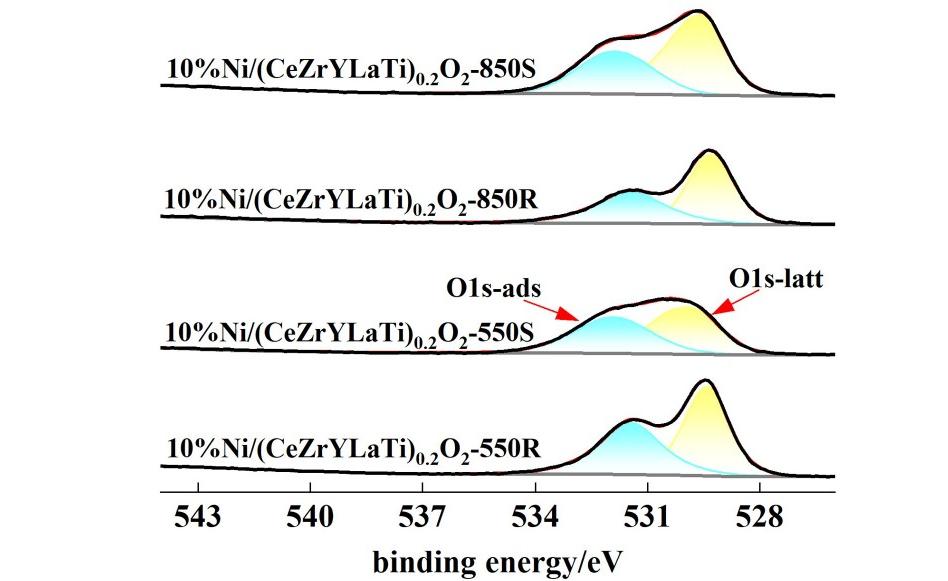
图8 550和850 ℃煅烧的10%Ni/(CeZrYLaTi)0.2O2催化剂稳定性前后的O 1s的X射线光电子能谱
Fig.8 X-ray photoelectron spectra of 10%Ni/(CeZrYLaTi)0.2O2 catalysts calcined at 550 and 850 ℃ before and after stability for O 1s
表3 根据XPS结果计算的550和850 ℃制备的10%Ni/(CeZrYLaTi)0.2O2催化剂稳定性前后的吸附氧与晶格氧的比值
Table 3 Ratio of adsorbed oxygen to lattice oxygen before and after stability of 10%Ni/(CeZrYLaTi)0.2O2 catalysts prepared at 550 and 850 ℃ calculated based on XPS results

Oads/Olatt(After Oads/Olatt(After Catalystsreduction)reactiom)10%Ni/(CeZrYLaTi)0.2O2-5500.840.8510%Ni/(CeZrYLaTi)0.2O2-8500.780.58
对还原后、稳定性测试后550与850 ℃煅烧的催化剂做了XPS测试。镍的出峰位置与镧重叠,而且镧的信号很强,所以不能获得镍的结合能信息。Ce、Zr、Y、La、Ti元素之间的相互作用复杂,结合能的变化找不到规律,也未列出。
对于O 1s给出2个峰,分别对应结合能约529.4 eV的晶格氧(Olatt)与结合能约531.6 eV的吸附氧(Oads)[28]。结合图8与表3可知,550 ℃煅烧的催化剂吸附氧占比更高,且稳定性测试过程中几乎不损失;而850 ℃煅烧的催化剂吸附氧占比低于550 ℃样品,且稳定性过程中损失了相当多的吸附氧。
CO2加氢制甲烷反应过程中,需要氧空位活化CO2。550 ℃催化剂具有更多且稳定的吸附氧位,表明其表面可以形成更多的氧空位;而850 ℃催化剂氧空位含量较低,且在稳定性测试过程中部分消失。这与CO2-TPD结果一致。
2.7 CO2甲烷化催化性能评价
对催化剂的性能进行了评价,具体见图9。
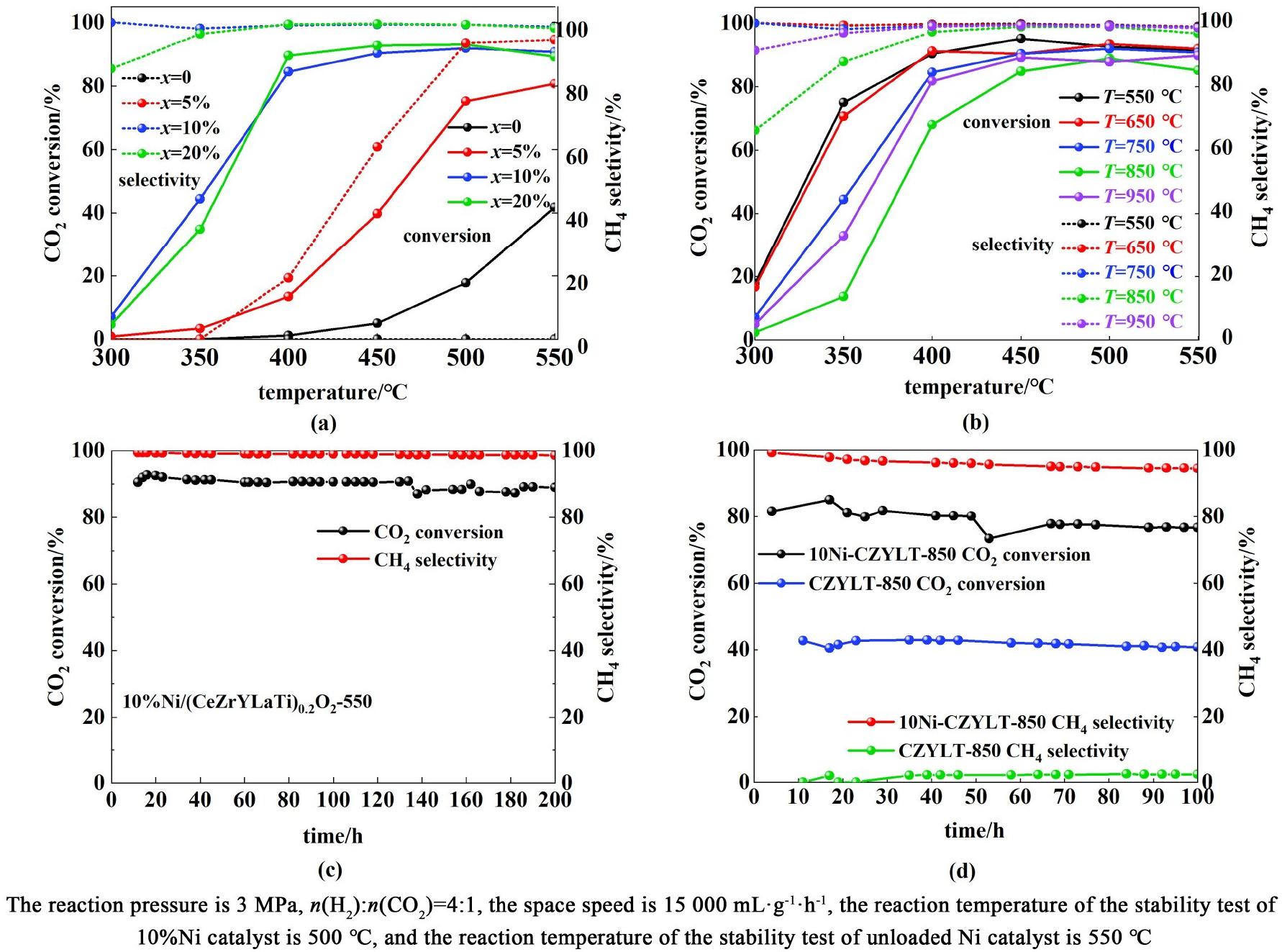
图9 (a)750 ℃煅烧的不同Ni负载量催化剂;(b)10%Ni载量的不同煅烧温度催化剂的CO2转化率、CH4选择性随反应温度的变化;(c)550 ℃;(d)850 ℃煅烧催化剂的稳定性测试结果
Fig.9 CO2 conversion and CH4 selectivity (a) Catalysts with different Ni loading calcined at 750 ℃;(b) Catalysts with 10%Ni loading calcined at different temperatures; Stability test results of catalysts calcined at (c)550 ℃; (d) 850 ℃
由图9(a)可知,当催化剂不负载Ni时,组成为(CeZrYLaTi)0.2O2为氧化物催化剂,在550 ℃的条件下有40%的CO2转化率,产物全部为CO,说明发生了逆水煤气变换反应(r-WGSR)。随着负载Ni的质量分数从5%逐步提高到10%和20%,明显看到CO2转化率和CH4选择性大幅提高,对于负载Ni10%与20%的催化剂,反应温度在400 ℃开始,CO2转化率便保持在85%左右,之后稳定在90%水平,而CH4选择性从350℃开始几乎达到100%水平。可见,不负载Ni的HEOs可以催化r-WGSR,其产物为CO。而负载Ni后,产物逐步转变为CH4,据此推测甲烷化反应是在HEOs表面CO2先转变为CO,之后在金属镍表面由CO加氢生成甲烷,即CO2加氢制甲烷是串联反应,与文献报道一致[29]。
Ni的负载量影响CO2转化率与CH4选择性,10%Ni的催化剂活性和选择性最高;再提高镍含量,催化剂的活性和选择性略有下降,可能是再提高镍含量并未提高镍的表面积而是导致了镍的团聚所致。
图9(c)和图9(d)的稳定性结果,表明低温550 ℃煅烧的催化剂10%Ni/(CeZrYLaTi)0.2O2-550具有优良的稳定性,而且CH4选择性稳定在99%水平。850 ℃煅烧的催化剂10%Ni/(CeZrYLa-Ti)0.2O2-850在前67 h内,CO2转化率有微小波动,之后转化率维持稳定,而其CH4选择性缓慢下降到94%水平,其稳定性表现较低。
850 ℃煅烧、不含Ni的(CeZrYLaTi)0.2O2-850催化剂对CO2加氢具有活性,但是产物是CO,几乎不生成甲烷,说明HEOs具有r-WGSR活性;与上述HEOs上活化CO2、进行逆水煤气变换反应,金属镍上进行CO加氢生成甲烷的观点一致。
图9(b)显示了煅烧温度催化剂性能影响,CO2转化率趋势随催化剂煅烧温度变化顺序是:550 ℃>650 ℃>750 ℃>950 ℃>850 ℃,即煅烧温度越低,CO2加氢制甲烷性能越好。不形成高熵氧化物的催化剂性能较好,而形成高熵氧化物的催化剂性能较差。
850 ℃煅烧的含Ni的10%Ni/(CeZrYLa-Ti)0.2O2-850催化剂与的不含Ni的(CeZrYLa-Ti)0.2O2-850催化剂,在100 h的稳定性期间,CO2转化率下降幅度接近,分别为5.9%、4.6%,表明HEOs活化CO2、进行r-WGSR的活性有比较明显的下降。说明催化剂上CO2转化率降低的关键原因不是活性组分镍的烧结或积碳所致,而是活化CO2的氧空位变化所致。结合前面CO2-TPD和XPS表征结果,当煅烧温度由550升至850 ℃后,吸附活化CO2的表面氧空位下降,认为850 ℃煅烧后,催化剂表面氧空位含量降低是其催化活性较低的主要原因。
550 ℃煅烧的催化剂未形成HEOs,体相组分为混合金属氧化物;由于煅烧温度较低,比表面积较高(见表2),于是表面氧空位浓度高,从而有利于CO2的活化。稳定性测试过程中原先的混合金属氧化物部分转变为HEOs,发生了晶化和晶粒长大,导致表面氧空位含量降低,于是CO2转化率有所下降。高温850 ℃煅烧的催化剂形成HEOs,体相各金属元素分散良好,但是HEOs的晶粒比550 ℃煅烧的催化剂的混合氧化物的晶粒尺寸大,于是导致氧空位数量较少,活性下降。且随着稳定性的进行,部分氧空位消失,导致CO2转化率的下降。
对于850 ℃煅烧的催化剂,由于稳定性测试的温度比较高(500 ℃),CO2加氢制甲烷又是强放热反应,另一方面HEOs的萤石晶粒较大;导致在反应过程中,氧空位被反应气氛中存在的CO2或H2O中的氧离子占据,导致部分氧空位消失。反应温度高、强放热反应形成催化剂表面的局部过热会促进氧空位的消失,所以稳定性较差。对于550 ℃煅烧的催化剂,由于是几种氧化物微粒的均匀混合,阻碍了同一种氧化物长大成为大晶粒的过程,因为其他氧化物微粒阻碍了任何同一种氧化物微粒的接触;另一方面,由于反应温度远低于几种氧化物微粒通过固相反应形成HEOs的温度(680 ℃,见DSC结果),于是形成HEOs的过程也比较缓慢;所以550 ℃煅烧的催化剂具有更好的稳定性。
关联表征结果,各催化剂反应前后的Ni分散度变化不大,均显示出很好的抗烧结性能;低温煅烧的催化剂,氧空位浓度高,更利于活化CO2,具有更高的活性和稳定性。可见对于本研究的混合氧化物/高熵氧化物催化剂,氧空位对催化剂性能更重要。
3 结论
采用柠檬酸络合法制备了Ce、Zr、Y、La、Ti和Ni的混合氧化物以及还原后得到的Ce、Zr、Y、La、Ti的混合氧化物担载Ni催化剂和(CeZrYLaTi)0.2O2高熵氧化物担载Ni催化剂。混合氧化物担载Ni催化剂具有更高的比表面积、更高的氧空位含量,高熵氧化物的晶化比较好、比表面积较低、活化CO2的氧空位含量也较低,于是呈现出较低的活性和稳定性。2种催化剂上,镍纳米颗粒均实现了高度分散,而且镍纳米颗粒具有高抗烧结性能。2种催化剂均具有优良的抗积碳性能,2种氧化物本身具有催化逆水煤气变换反应的活性。
[1] 刘智勇, 周枫然, 张体强, 等. 二氧化碳固体吸附剂材料改性研究进展[J]. 化学试剂, 2025, 47(3): 13-23
LIU Zhiyong, ZHOU Fengran, ZHANG Tiqiang, et al. Research progress on modification of solid adsorbents for carbon dioxide[J]. Chemical Reagents, 2025, 47(3): 13-23(in Chinese)
[2] KARIM S, TANWAR N, DAS S, et al. Shaping the future of green hydrogen production: Overcoming conventional challenges with molecular catalysts, immobilization, and scalable electrolyzers[J]. ACS Catalysis, 2025, 15(2): 1073-1096
[3] ZHOU G, WU T, XIE H, et al. Effects of structure on the carbon dioxide methanation performance of co-based catalysts[J].International Journal of Hydrogen Energy, 2013, 38(24):10012-10018
[4] HU F, TONG S, LU K, et al. Reduced graphene oxide supported Ni-Ce catalysts for CO2 methanation: The support and ceria promotion effects[J]. Journal of CO2 Utilization, 2019, 34: 676-687
[5] TSIOTSIAS A I, CHARISIOU N D, YENTEKAKIS I V, et al.Bimetallic Ni-based catalysts for CO2 methanation: A review[J].Nanomaterials, 2021, 11(1): 28
[6] CISNEROS S, ABDEL-MAGEED A, MOSRATI J, et al. Oxygen vacancies in Ru/TiO2-drivers of low-temperature CO2 methanation assessed by multimodal operando spectroscopy[J].iScience, 2022, 25(3): 103886
[7] XIE Y, CHEN J, WU X, et al. Frustrated lewis pairs boosting low-temperature CO2 methanation performance over Ni/CeO2 nanocatalysts[J]. ACS Catalysis, 2022, 12(17): 10587-10602
[8] CORTAZAR M, LAFUENTE M, NAVARRO-PUYUELO A, et al. Highly selective CO formation via CO2 hydrogenation over novel ceria-based high-entropy oxides (HEOs)[J]. Chemical Engineering Journal, 2025, 507: 160706
[9] SARKAR A, BREITUNG B, HAHN H. High entropy oxides: The role of entropy, enthalpy and synergy[J]. Scripta Materialia, 2020, 187: 43-48
[10] FENG D, DONG Y, ZHANG L, et al. Holey lamellar high-entropy oxide as an ultra-high-activity heterogeneous catalyst for solvent-free aerobic oxidation of benzyl alcohol[J]. Angewandte Chemie International Edition, 2020, 59(44): 19503-19509
[11] ANANDKUMAR M, BHATTACHARYA S, DESHPANDE A S. Low temperature synthesis and characterization of single phase multi-component fluorite oxide nanoparticle sols[J]. RSC Advances, 2019, 9(46): 26825-26830
[12] GILD J, SAMIEE M, BRAUN J L, et al. High-entropy fluorite oxides[J]. Journal of the European Ceramic Society, 2018, 38(10): 3578-3584
[13] ROST C M, SACHET E, BORMAN T, et al. Entropy-stabilized oxides[J]. Nature Communications, 2015, 6: 8485
[14] ZHANG Z, YANG S, HU X, et al. Mechanochemical nonhydrolytic Sol-gel-strategy for the production of mesoporous multimetallic oxides[J]. Chemistry of Materials, 2019, 31(15): 5529-5536
[15] KHAJONVITTAYAKUL C, TONGNAN V, NAMO N, et al. Tar steam reforming for synthesis gas production over Ni-based on ceria/zirconia and La0.3Sr0.7Co0.7Fe0.3O3 in a packed-bed reactor[J]. Chemosphere, 2021, 277: 130280
[16] LEE J, CHRISTOPHER P. Does H2 temperature-programmed reduction always probe solid-state redox chemistry? the case of Pt/CeO2[J]. Angewandte Chemie International Edition, 2025,64(2): e202414388
[17] LI J, LIN Y, PAN X, et al. Enhanced CO2 methanation activity of Ni/anatase catalyst by tuning strong metal-support interactions[J]. ACS Catalysis, 2019, 9(7): 6342-6348
[18] LIU L, LIU Y, SONG J, et al. Plasma-enhanced steam reforming of different model tar compounds over Ni-based fusion catalysts[J]. Journal of Hazardous Materials, 2019, 377: 24-33
[19] MA H, ZENG L, TIAN H, et al. Efficient hydrogen production from ethanol steam reforming over La-modified ordered mesoporous Ni-based catalysts[J]. Applied Catalysis B: Environmental, 2016, 181: 321-331
[20] CHARISIOU N D, SIAKAVELAS G, TZOUNIS L, et al.Ni/Y2O3-ZrO2 catalyst for hydrogen production through the glycerol steam reforming reaction[J]. International Journal of Hydrogen Energy, 2020, 45(17): 10442-10460
[21] WIERZBICKI D, DEBEK R, MOTAK M, et al. Novel Ni-Lahydrotalcite derived catalysts for CO2 methanation[J]. Catalysis Communications, 2016, 83: 5-8
[22] DAI Y, XU M, WANG Q, et al. Enhanced activity and stability of Ni/La2O2CO3 catalyst for CO2 methanation by metal-carbonate interaction[J]. Applied Catalysis B: Environmental, 2020,277: 119271
[23] LIANG G, HE L, ARAI P M, et al. The Pt-enriched PtNi alloy surface and its excellent catalytic performance in hydrolytic hydrogenation of cellulose[J]. ChemSusChem, 2014, 7(5): 1415-1421
[24] LIN J, MA C, LUO J, et al. Preparation of Ni based mesoporous Al2O3 catalyst with enhanced CO2 methanation performance[J].RSC Advances, 2019, 9(15): 8684-8694
[25] CHEN S, FU J, PENG Y, et al. Effective CO2 thermocatalytic hydrogenation with high coke resistance on Ni-CZ/attapulgite composite[J]. Molecules, 2024, 29(19): 4550
[26] ZHANG H, JIA X, YAN Y, et al. The effect of the concentration of citric acid and pH values on the preparation of MgAl2O4 ultrafine powder by citrate sol-gel process[J]. Materials Research Bulletin, 2004, 39(6): 839-850
[27] ANGHEL E M, PETRESCU S, MOCIOIU O C, et al. Influence of ceria addition on crystallization behavior and properties of mesoporous bioactive glasses in the SiO2-CaO-P2O5-CeO2 system[J]. Gels, 2022, 8(6): 344
[28] ARANDIYAN H, WANG Y, SCOTT J, et al. In situ exsolution of bimetallic Rh-Ni nanoalloys: A highly efficient catalyst for CO2 methanation[J]. ACS Applied Materials & Interfaces, 2018, 10(19): 16352-16357
[29] KARELOVIC A, RUIZ P. CO2 hydrogenation at low temperature over Rh/γ-Al2O3 catalysts: Effect of the metal particle size on catalytic performances and reaction mechanism[J]. Applied Catalysis B: Environmental, 2012, 113: 237-249