石化行业的生产、加工过程中会产生大量的硫化氢气体(H2S),H2S是一种剧毒、可燃、具有腐蚀性且恶臭的高度危害性气体,长期接触低浓度的硫化氢会使人体出现头痛、咳嗽、恶心、胸痛和失眠等不良现象[1,2]。 除此之外,其存在还会对生产设备产生极强的腐蚀与“氢脆”作用[3-6]。 因此,研究脱除硫化氢技术对环境保护和经济发展均具有重要意义。
已有的脱硫技术中,克劳斯(Claus)工艺是工业上用于处理大规模、高浓度H2S的首选工艺[7-9]。Claus工艺通过将H2S和空气进行燃烧,发生催化反应生成硫磺。 但Claus反应受到热力平衡学约束,即便是经过3级Claus反应仍有1%~3%的H2S残留,随着我国环保法规的日益严格,亟需对残留的H2S进行高效处理。 其中,H2S选择性催化氧化因不受热力学平衡限制而被认为是一种非常有前途的处理残留H2S的方法,其主要的反应方程式如式(1)。
开发高效催化剂是实现H2S选择氧化技术进一步工业应用的重中之重。 石墨相氮化碳是一种富含氮元素的碳基催化剂(氮元素含量>60%)。 石墨相氮化碳具有三嗪环和七嗪环2种基本的结构单元,均为sp2杂化的N和C原子交替排列构成。 结构单元之间通过桥氮相互连接构成二维平面,再通过弱相互作用堆叠成为三维结构[10]。 氮化碳因其独特的结构而表现出优异的化学稳定性与热稳定性。 其结构中的氮原子可作为结构性碱位点,为材料表面提供丰富的电子密度,从而使氮化碳成为一种具有潜力的脱硫材料[11-13]。 但由于氮化碳缺乏足够的氧气吸附和活化位点,使其选择性催化氧化硫化氢的性能较差。 为了解决该问题,Lyu等[14]通过离子热法制备了具有明确原子结构的结晶性聚三嗪酰亚胺锂(PTI-Li+),并证明其中原子级分散的Li+作为活性位点,通过扩展电子离域和优化能带结构增强了O2和H2S的吸附与活化能力,从而在脱硫反应中表现出优异的活性和稳定性(100%硫化氢转化率和100 h的催化剂寿命)。 Ye等[15]通过构建一系列氮掺杂碳负载的Mn单原子催化剂,发现Mn-N4位点对O2和H2S具有适中且相近的吸附能,符合Sabatier最优原则,从而在宽浓度范围的H2S选择性氧化脱硫反应中表现出优异性能(100%硫化氢转化率和60 h的催化剂寿命)。 因此,利用富含氧活性物种的金属改善氮化碳活化氧的能力是构建高效硫化氢选择性氧化催化剂的有效方法。 例如Koyuncu等[16]在Fe2O3材料中引入铈元素,铈晶格中的氧大幅提升了硫单质的选择性,最终制备的2Fe-2Ce材料的硫化氢转化率与硫单质选择性均达到99%。 Yasyerli等[17]则是在钒基催化剂中掺入了等物质的量的氧化铈(CeO2),其在脱硫反应中也展现出了较高的催化性能(100%硫化氢转化率和97%硫选择性)。
基于以上研究,我们提出了利用具有良好氧捕捉和存储能力的Ce元素来修饰氮化碳,进而构建高效脱硫催化剂。 通过简单的一步法直接制备了不同含量的Ce掺杂CNCex催化剂,并评价了其催化性能。 结果表明,CNCex材料在200 ℃的条件下,可以实现96%的硫磺产率。 同时对H2S的选择氧化过程进行了深入探究,并提出了可能的催化机理。
1 实验部分
1.1 实验材料
三聚氰胺(质量分数99%),购自国药化学试剂有限公司:硝酸铈(分析纯),购自上海麦克林生化科技有限公司;高纯氮气(体积分数99%)、硫化氢和氧气等气体购自北京华元化工气体有限公司。
1.2 催化剂制备
将一定量的硝酸铈混合10 g三聚氰胺在研钵中充分研磨15 min,混合均匀的粉末样品放入50 mL坩埚中,在马弗炉中550 ℃煅烧4 h,升温速率为5 ℃·min-1,自然冷却到室温后将样品取出研磨,将所得固体洗涤并在80 ℃干燥12 h,得到的催化剂记为CNCex(x为Ce的物质的量之比,x=1,2,5)。
将10 g三聚氰胺放入50 mL坩埚中,在马弗炉中550 ℃煅烧4 h,升温速率为5 ℃·min-1,自然冷却到室温后将样品取出研磨,得到的石墨相氮化碳粉末记为CN。
1.3 H2S 选择性催化氧化性能测试
H2S选择性氧化实验装置主要由4部分组成(如图1所示):供气系统、温控系统、气体在线分析系统及尾气吸收系统。 实验流程如下,催化剂置于内径为6 mm石英反应管中,石英反应管置于加热炉中进行反应。 反应温度由2个分别放置于炉内和石英反应管的热电偶控制。 使用体积分数为5.0×10-3/2.5×10-3的H2S/O2混合气(N2为平衡气)作为反应气,反应前后H2S浓度使用配备有火焰光度检测器(FPD)的色谱(GC128)进行检测。 根据式(2) ~式(4)计算H2S转化率、硫选择性和硫产率。
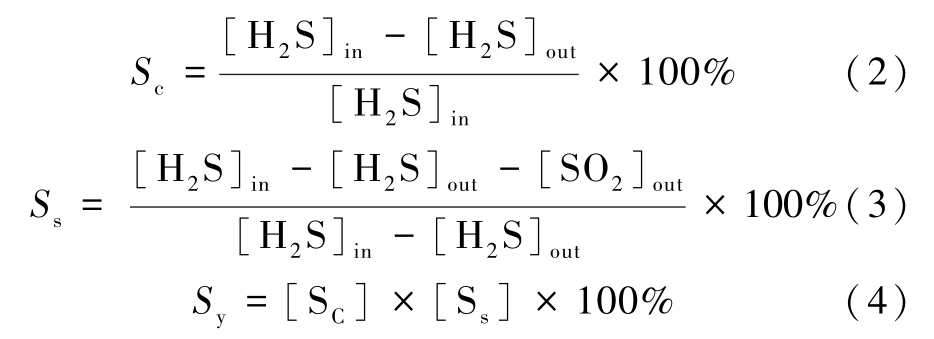
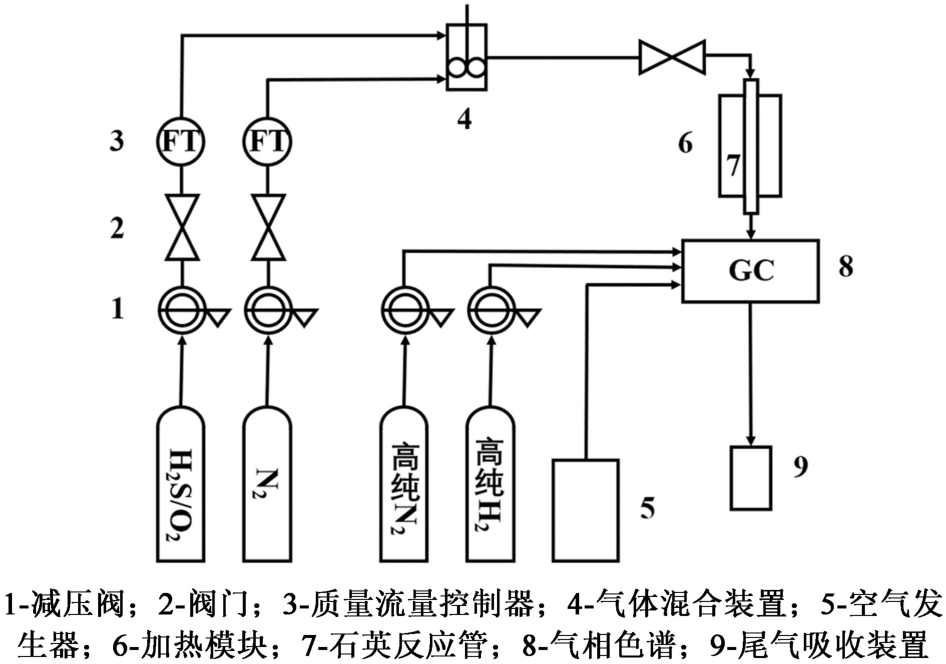
图1 H2S选择性氧化实验流程示意图
Fig.1 Schematic diagram of the experimental process for H2S selective oxidation
式(2)~式(4)中:[H2S]in代表原料气中硫化氢的浓度;[H2S]out代表反应尾气中硫化氢的浓度;[SO2]out代表反应尾气中二氧化硫的浓度;Sc代表H2S的转化率;Ss代表硫选择性;Sy代表硫产率。
1.4 催化剂表征
1.4.1 X射线光电子能谱(XPS)
使用ESCALB 250型 X射线光电子能谱仪分析样品表面的元素组成及其价态。 以Al靶Kα 射线为光源,能量为20 eV,功率为200 W,用导电胶将压成片状的样品固定在样品台上再进行测试。 使用Avantage对测试结果进行处理,以C 1s结合能(284.8 eV)校准电子结合能。
1.4.2 粉末 X射线衍射(XRD)
使用Miniflex600型X射线衍射仪(XRD)对样品的晶体结构进行表征。 光源使用铜靶(Cu_Kα,λ=0.154 nm)X射线管,工作电流40 mA,工作电压40 kV,扫描范围2θ=5°~80°,扫描速率0.2,扫描步长0.02。
1.4.3 拉曼光谱(Raman)
使用 LabRAM HR Evolution型原位共聚焦显微拉曼光谱仪分析样品的分子结构信息。 根据材料的不同性质,采用波长为 325 nm的激光作为激发光源,使用600 grooves·mm-1的光栅分离不同波长的拉曼散射,采集100 ~2 500 cm-1的拉曼位移范围内的信号,曝光时间为20 s(单次采集时间5 s,采集次数4次)。
1.4.4 高分辨率透射电子显微镜(HRTEM)
使用Talos F200s型透射电镜表征样品的形貌结构。 首先将样品分散在乙醇中,超声1 h将使其均匀分散,然后将分散液滴于超薄碳膜上,晾干后用于形貌结构的表征。
1.4.5 程序升温脱附(TPD)
使用华思化学吸附仪对样品进行了程序升温脱附(TPD),表征样品对气体的吸附位点和吸附量。取适量样品在300℃、50mL·min-1的N2流中预处理30min,然后在40mL·min-1的5%O2/N2或5%H2S/N2气流中吸附60min,最后在40mL·min-1的N2流中以10 ℃·min-1的速度将其升温至300 ℃,同时用热导检测器(TCD)检测尾气中的组分变化。
1.4.6 原位红外(In-situ DRIFTS)
使用配备有MCT-A检测器的傅里叶变换红外光谱仪(FTIRNiS50)收集4 000 ~600 cm-1范围内的原位红外光谱。 向原位池中装填大约100 mg的试样。然后在N2的保护下120 ℃热处理60 min,以除去催化剂表面吸附的杂质。 降温至所需温度后,在N2气氛下采集背景,随后通入1.0×10-3H2S/5.0×10-4O2混合气体,并将反应池逐渐升温至200 ℃,以8 cm-1的分辨率采集样品吸附气体后的红外信号。
1.4.7 比表面积和孔径分布分析(BET)
使用ASAP2460仪器(Micromeritics)分析样品的比表面积和孔径分布。 在120 ℃温度条件下,对样品进行12 h真空脱气处理,然后在液氮温度(77 K)下,通过静态吸附法进行分析真空度p/p0为0 ~1的范围内的氮气吸脱附曲线,并通过Barret-Emmett-Teller(BET)法计算样品比表面积。
2 结果与讨论
2.1 催化剂结构表征
为了验证Ce在氮化碳中成功掺杂与否,并探究其对氮化碳物理化学性质的影响,对合成的CNCe1、CNCe2和 CNCe5等3种材料进行了结构表征测试。 图2是3种催化材料的XRD谱图。
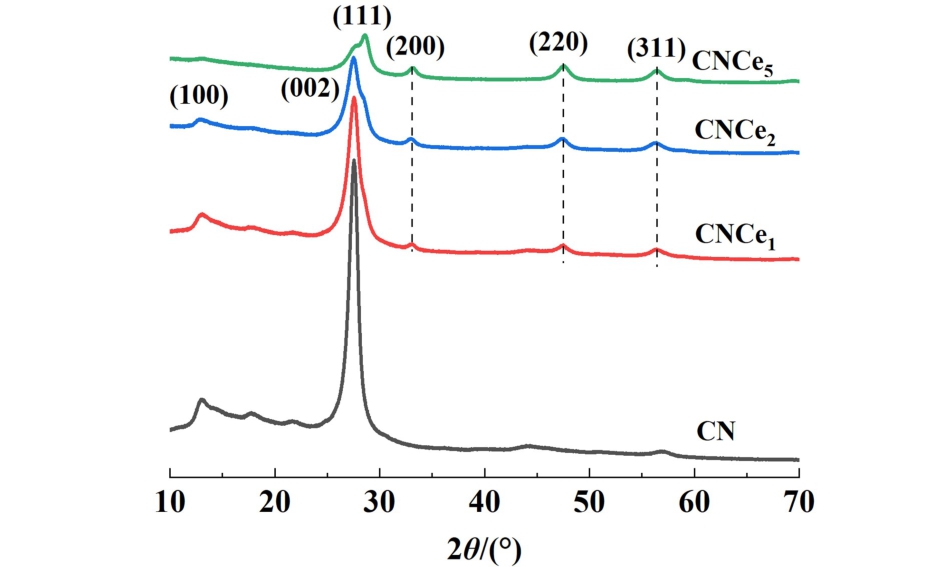
图2 不同CNCex的XRD图谱
Fig.2 XRD patterns of different CNCex catalysts
CN和CNCex样品的XRD谱图均在13.0°和27.5°处有2个较明显的衍射峰,分别对应于氮化碳的(100)晶面和(002)晶面[18],相应的晶面间距分别为0.680和0.325 nm其中13.0°处的衍射峰源于氮化碳面内的周期性重复七嗪单元,而27.5°处的衍射峰对应共轭二维平面之间的层状堆叠。 但随着Ce掺杂量的增加,氮化碳的特征衍射峰逐渐宽化,峰高逐渐降低,这是由于Ce3+离子与g-C3N4骨架之间的相互作用,干扰了其长程有序的周期性排列,引起晶格畸变,导致氮化碳的聚合程度逐渐降低,说明Ce成功地掺杂进了氮化碳的晶格中。 同时,CNCex样品在28.6°、33.1°、47.5°和56.5°出现了逐渐增强的特征峰,分别对应着CeO2结构中的(111)、(200)、(220)和(311)晶面[19]。 表明存在部分Ce未掺杂进氮化碳材料的晶格中,而是以CeO2的形式存在。
CN和CNCex样品的表面形貌和微观结构如图3所示。 CN的TEM图像清楚地显示CN具有不规则堆叠的片状结构[图3(a)]。 CNCex的微观结构与CN类似,图3(d)~图3(h)为CNCe5的能谱元素分布图(EDS),检测到了C、N、Ce和O元素的存在,证明了CNCe5复合催化剂的成功合成。 在CNCe5的HRTEM图[图3(b)~图3(c)]可以观察到CeO2的纳米颗粒的存在,同时,通过图3(c)可以清楚地观察到间距为0.315 nm的晶格条纹,对应于CeO2的(111)晶面[20]。 这些结果进一步证实了部分Ce未引入氮化碳的晶格中,而是以CeO2的形式存在。

图3 (a)CN的TEM图;(b ~c)CNCe5的TEM图;(d ~h)CNCe5的元素分布能谱
Fig.3 (a)TEM image of CN; (b—c) CNCe5; (d—h) elemental distribution spectra of CNCe5
利用氮气等温吸脱附实验研究了样品的比表面积和多孔结构性质,结果见图4和表1。 如图4所示,在相对压力为0.6 ~1.0之间,CN和CNCex样品均显示出典型的Ⅳ型吸附特性与H3型回滞环,反映了材料的介孔结构,图4中孔径分布也表明,在Ce掺杂后,材料中的介孔含量相较于普通氮化碳CN明显增多。 这主要归因于CeO2在高温下促进了三聚氰胺的不完全缩合,释放NH3、CO2等气体,形成气泡模板。 比表面积的增大和介孔的增多可以为催化反应提供更多的活性位点,有利于气体分子的传质从而提高催化活性。
表1 CNCex 催化剂的比表面积和孔结构
Table 1 The specific surface area and pore structure of CNCex catalysts
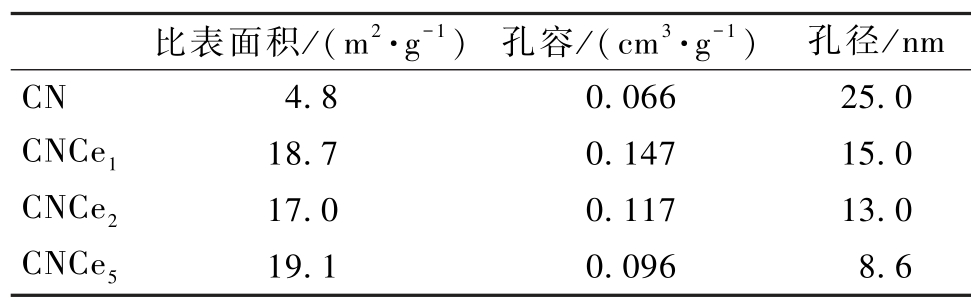
比表面积/(m2·g-1) 孔容/(cm3·g-1) 孔径/nm CN 4.8 0.066 25.0 CNCe1 18.7 0.147 15.0 CNCe2 17.0 0.117 13.0 CNCe5 19.1 0.096 8.6
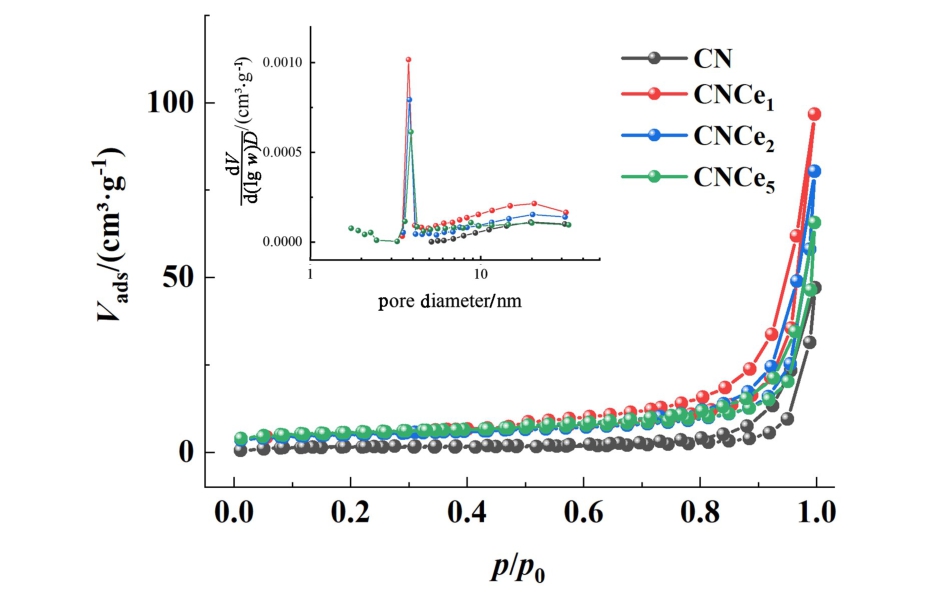
图4 CNCex催化剂的N2吸附-脱附曲线和孔径分布
Fig.4 N2 adsorption-desorption curves and pore size distributions of CNCex catalysts
进一步用XPS分析了催化剂的表面元素组成和化学状态,结果见图5和表2。 通过表2可以看出,C和N是主要元素。 如图5(a)所示,CN样品的C 1s高分辨率谱图可以分为2个峰,1个峰位于284.8 eV,对于氮化碳可能是属于杂质碳;另1个峰位于288.1 eV,对应七嗪结构中sp2杂化的碳原子[21,22]。 在N 1s的高分辨谱图中[图5(c)],所有样品的谱图均可拟合为4个峰。 其中,位于398.6 eV处的峰归属于七嗪结构中 sp2杂化的吡啶氮(C—N  C);400.2 eV处的峰对应于七嗪单元中的N—(C)3结构氮原子;401.2 eV处的峰归因于氨基(—NH2)中的氮原子[23];而404.4 eV处的峰则与π 激发效应有关[24]。 CNCex催化剂相比CN的C峰由288.24 eV处红移到288.33 eV,N峰由398.75 eV处的峰偏移到398.77 eV。 这2处峰都对应了氮化碳的七嗪环特征峰。 表明未引入氮化碳晶格中的CeO2与氮化碳框架之间可能存在强相互作用[25]。强相互作用抑制了CeO2颗粒的团聚,还可以加速Ce物种与CN载体间的电子转移,可进一步提高催化剂的催化性能。 在Ce 3d的图谱[图5(e)]中,可以检测到归属于Ce3+和Ce4+的7个峰,其中在882.23、885.23、888.64、906.70和916.60 eV处的5个峰归属于Ce(Ⅳ)的特征峰,而在898.20和900.85 eV处的峰归属于Ce(Ⅲ)的特征峰[26-29]。 Ce3+和Ce4+的共存表明催化剂表面存在Ce3+/Ce4+氧化还原电子对,且n(Ce3+)/n(Ce4+)随着Ce引入量的增加而减少(表2,分别为0.39、0.33和0.21),这进一步证明了由于氮化碳和Ce之间存在的强相互作用,构建了Ce-CN的电子转移通道,使得材料中Ce4+含量的增加,作为典型的氧化还原反应,高价态Ce4+的存在有利于反应的进行[30]。 CN和CNCex材料的O 1s XPS图谱如图6所示,CN中532.20 eV处的峰通常认为是氮化碳表面结合水中O—H的峰[31]。CNCex材料可在529.23和532.00 eV处检测到2个峰,529.23 eV处的峰被认为于CeO2中晶格氧有关[32],且其含量随着Ce引入量的增加而增加,从0.9% ( 物 质 的 量 分 数) 增 加 到 了 3.88%; 而532.00 eV处的峰则是由CeO2的表面吸附氧和碳氮材料表面结合水中O—H共同作用,其含量由CN材料的2.66%逐渐增加到CNCe5材料的4.54%也证明了这一论断。
C);400.2 eV处的峰对应于七嗪单元中的N—(C)3结构氮原子;401.2 eV处的峰归因于氨基(—NH2)中的氮原子[23];而404.4 eV处的峰则与π 激发效应有关[24]。 CNCex催化剂相比CN的C峰由288.24 eV处红移到288.33 eV,N峰由398.75 eV处的峰偏移到398.77 eV。 这2处峰都对应了氮化碳的七嗪环特征峰。 表明未引入氮化碳晶格中的CeO2与氮化碳框架之间可能存在强相互作用[25]。强相互作用抑制了CeO2颗粒的团聚,还可以加速Ce物种与CN载体间的电子转移,可进一步提高催化剂的催化性能。 在Ce 3d的图谱[图5(e)]中,可以检测到归属于Ce3+和Ce4+的7个峰,其中在882.23、885.23、888.64、906.70和916.60 eV处的5个峰归属于Ce(Ⅳ)的特征峰,而在898.20和900.85 eV处的峰归属于Ce(Ⅲ)的特征峰[26-29]。 Ce3+和Ce4+的共存表明催化剂表面存在Ce3+/Ce4+氧化还原电子对,且n(Ce3+)/n(Ce4+)随着Ce引入量的增加而减少(表2,分别为0.39、0.33和0.21),这进一步证明了由于氮化碳和Ce之间存在的强相互作用,构建了Ce-CN的电子转移通道,使得材料中Ce4+含量的增加,作为典型的氧化还原反应,高价态Ce4+的存在有利于反应的进行[30]。 CN和CNCex材料的O 1s XPS图谱如图6所示,CN中532.20 eV处的峰通常认为是氮化碳表面结合水中O—H的峰[31]。CNCex材料可在529.23和532.00 eV处检测到2个峰,529.23 eV处的峰被认为于CeO2中晶格氧有关[32],且其含量随着Ce引入量的增加而增加,从0.9% ( 物 质 的 量 分 数) 增 加 到 了 3.88%; 而532.00 eV处的峰则是由CeO2的表面吸附氧和碳氮材料表面结合水中O—H共同作用,其含量由CN材料的2.66%逐渐增加到CNCe5材料的4.54%也证明了这一论断。
表2 CNCex 的XPS 元素分析的结果
Table 2 XPS elemental analysis results of CNCex catalysts
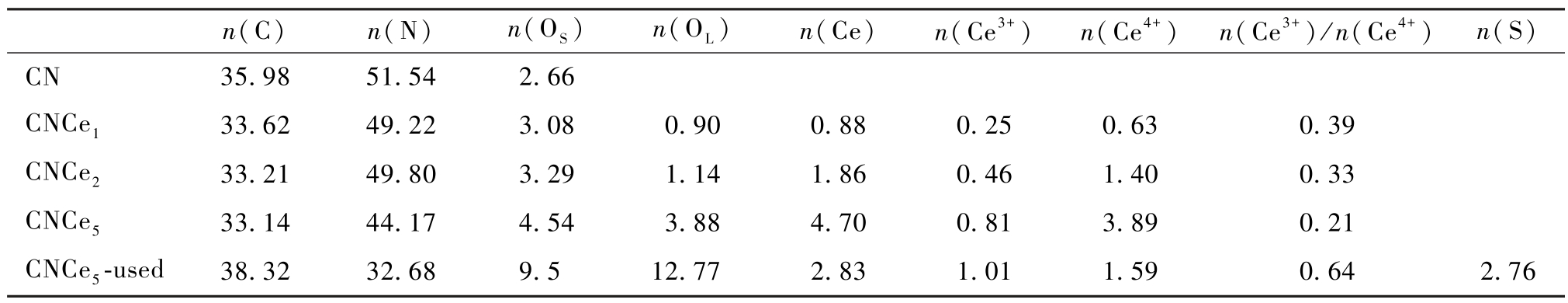
*[Os] Surface active oxygen; [OL] lattice oxygen; [CNCe5-used] CNCe5 after reaction-induced deactivation.
n(C) n(N) n(OS) n(OL) n(Ce)n(Ce3+) n(Ce4+) n(Ce3+)/n(Ce4+) n(S)CN 35.98 51.54 2.66 CNCe1 33.62 49.22 3.08 0.90 0.88 0.25 0.63 0.39 CNCe2 33.21 49.80 3.29 1.14 1.86 0.46 1.40 0.33 CNCe5 33.14 44.17 4.54 3.88 4.70 0.81 3.89 0.21 CNCe5-used 38.32 32.68 9.5 12.77 2.83 1.01 1.59 0.64 2.76
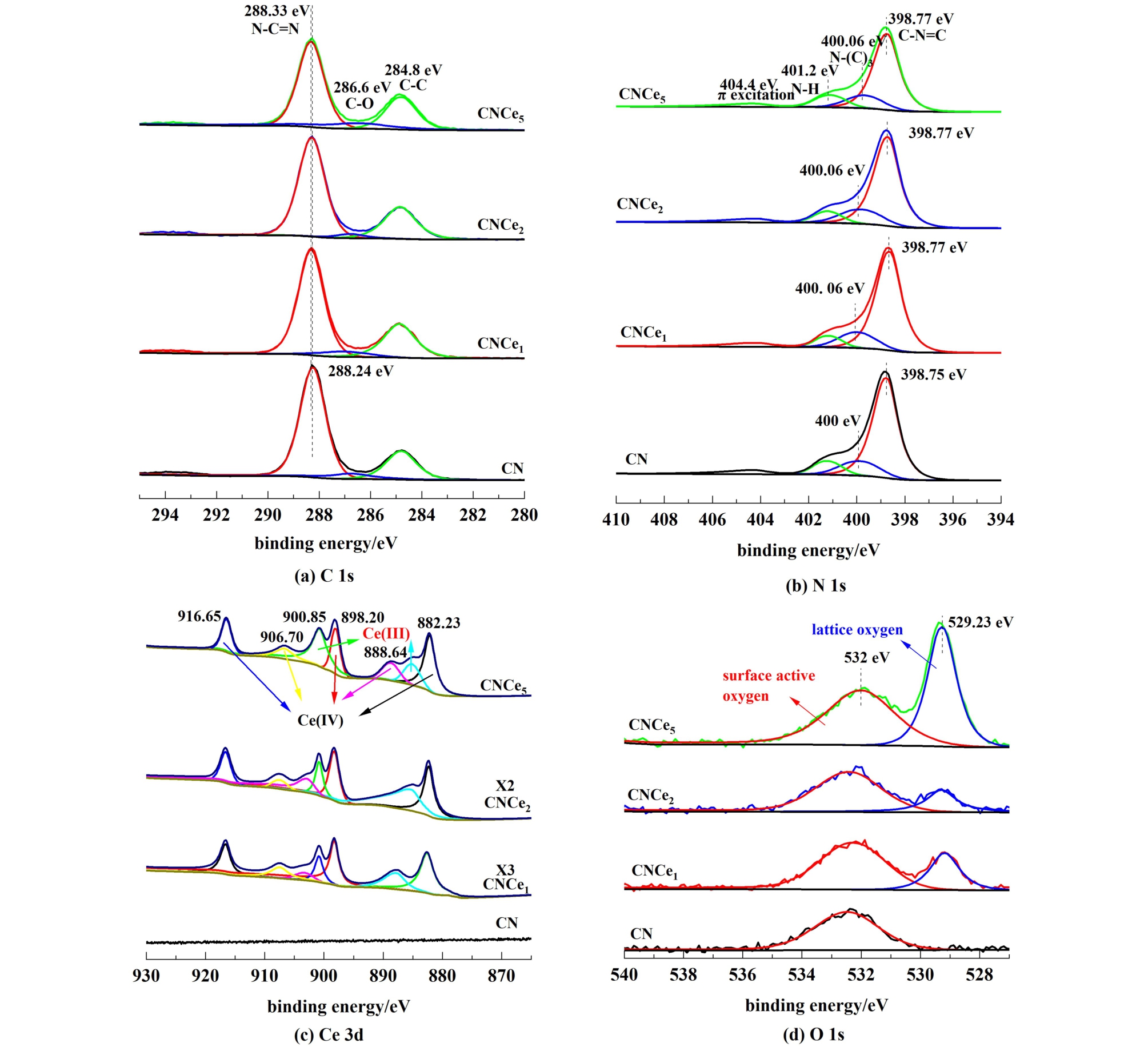
图5 CNCex催化剂的XPS谱图
Fig.5 XPS spectra of CNCex catalysts
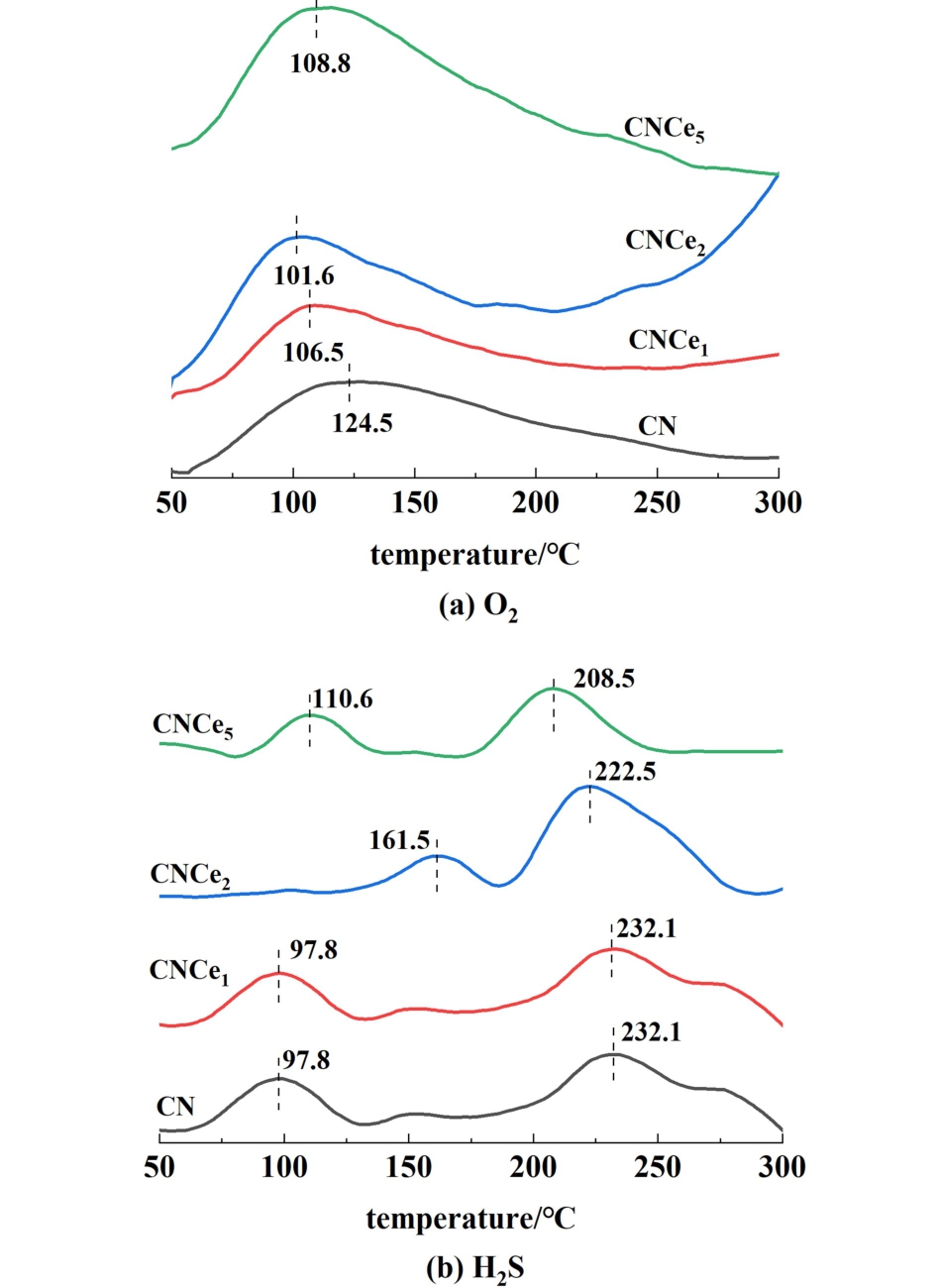
图6 CN和CNCex催化剂的程序升温脱附曲线
Fig.6 TPD of CNCex catalysts
2.2 催化剂表面化学性质
本研究进一步利用氧/硫化氢-程序升温脱附方法(O2/H2S-TPD)探究了CNCex样品表面吸附反应物的能力。 CNCex材料的O2-TPD曲线如图6(a)所示,所有材料均在100 ~200 ℃区间呈现1个宽的氧气脱附峰,对应于材料表面的氧物种,这与XPS的结果相一致。 值得注意的是,随着Ce的引入和含量的增加,氧气的脱附峰从CN材料的124.5 ℃逐渐移动到108 ℃,且随着Ce含量的增加氧脱附峰的面积逐渐增加,说明Ce的掺杂可明显提高氧的活化能力。 H2S-TPD曲线[图6(b)]则显示CNCex材料与CN有着相近的脱附峰面积和脱附温度。 这表明无论引入Ce与否,材料对H2S的吸附能力没有明显的改善,Ce对材料表面的改性主要是通过对氧活化能力的改善来实现的。
通过拉曼光谱测试可以探究材料表面的结构缺陷和石墨化程度[33]。 如图7所示,CNCex材料的拉曼光谱峰均位于1 450和1 610 cm-1附近位置。1 450 cm-1处为D带峰,对应无定型碳中的无序结构,例如边缘缺陷等,1 590 cm-1为G带峰,对应氮化碳材料中规整的石墨结构[34]。 通常使用D峰与G峰强度之比(ID/IG)来衡量氮化碳材料的缺陷程度[35][36],经过测试与拟合计算,CNCe1、CNCe2和CNCe5材料拉曼谱图的 ID/IG值分别为0.83、0.74和 0.92。 铈掺杂后的材料表面缺陷程度均大于原始石墨相氮化碳CN(0.68)。 说明引入氮化碳晶格中的Ce导致氮化碳的部分有序结构畸变或被破坏,进而造成催化剂表面缺陷的增多。 而这一增加会增加材料表面的活性中心,有利于反应物的(O2)吸附的活性,与O2-TPD的结果相一致促进。
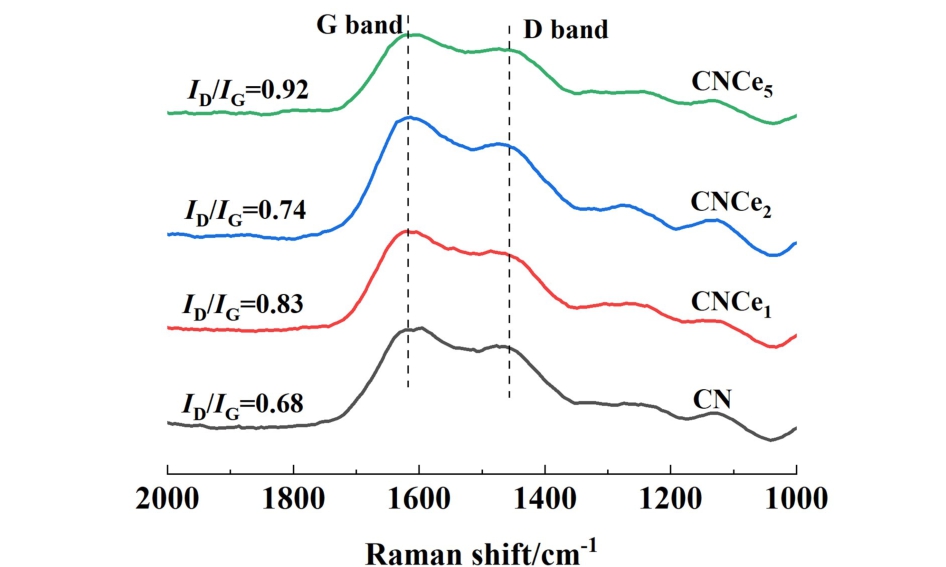
图7 CNCex催化剂的Raman图谱
Fig.7 Raman pattern of CNCex catalysts
3 催化性能测试
本研究在130 ~260 ℃范围内评价了温度对催化剂催化性能的影响。 由图8(a)所示,CN样品在整个温度区间内其H2S的转化率不超过3.7%,说明其本身具有极差的催化性能,且随着反应温度的升高至260 ℃,硫单质选择性会快速降低至40%。而CNCe1和CNCe2样品随温度升高,硫化氢转化率出现逐步的大幅提高,在260 ℃时,转化率分别能达到54.65%和78.33%。 值得注意的是,CNCe5在整个温度区间都能保持88%以上的硫化氢转化率,且在200 ℃表现出最佳的硫化氢转化率(98.8%)。 同时CNCex催化剂在140 ~180 ℃温度区间内保持接近100%的单质硫选择性,随着温度的进一步升高,其单质硫选择性也可保持在89%以上。 Ce的引入极大地改善了催化剂的催化性能,尤其是CNCe5,在200 ℃表现出了最佳的催化效率,可获得96%的硫磺产率。 其催化性能的改善主要源自几个方面:(1)丰富的孔结构可以有效地改善气体分子的传质,而且可以增加活性点位的暴露数量;(2)氧活化能力的明显改善;(3)活性相Ce4+含量的增加。
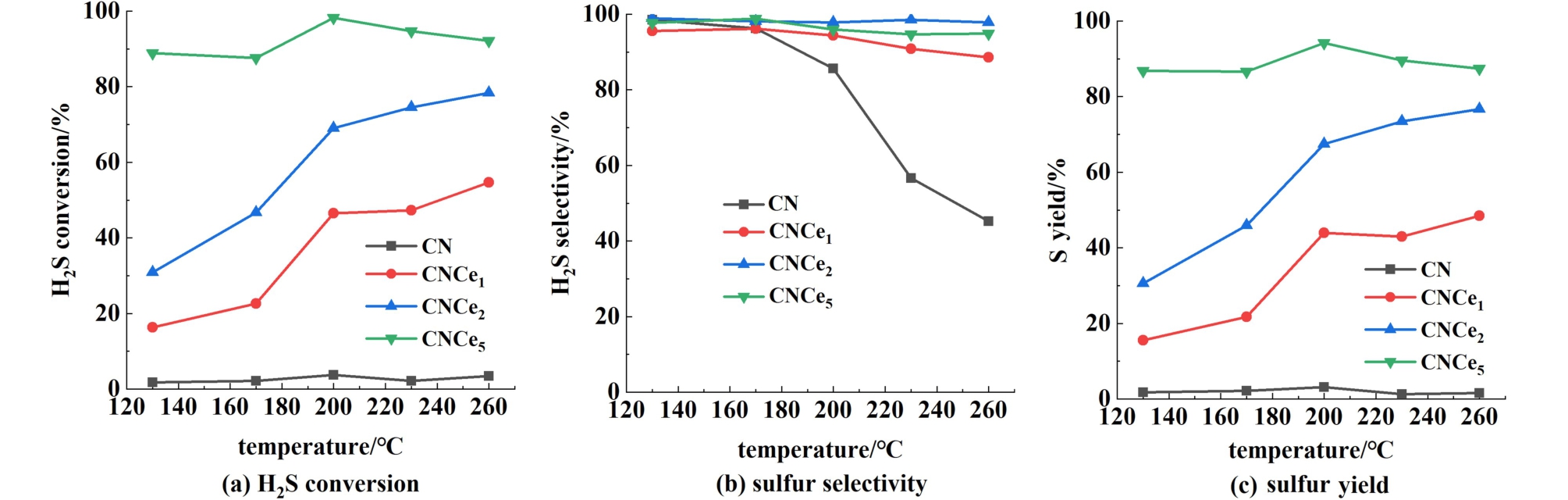
图8 CNCex催化剂的催化性能
Fig.8 Catalytic performance of CNCex catalysts
氧含量对CNCe5材料催化性能的影响如图9所示。 当n(H2S) ∶n(O2)= 3 ∶1(化学计量比)时,H2S转化率仅为 58.14%, 而当氧浓度升高至n(H2S) ∶n(O2)= 2 ∶1时,其H2S转化率可迅速增加至99.16%,且随着氧浓度的进一步增加至n(H2S) ∶n(O2)= 1 ∶3,其H2S转化率基本维持稳定。 这说明氧在该反应中起着重要的作用,氧的不足会严重制约反应的进行。 与此同时,硫单质的选择性则随着氧浓度的增加出现轻微的下降,从99.5%逐渐降至88.7%。 这可能是由于随着氧气的增多,导致反应生成的硫单质在高温下进一步与剩余氧气反应生成SO2和硫酸盐物种。 即便如此,CNCe5材料也可在高氧浓度的条件下[n(H2S) ∶n(O2)= 1 ∶3]维持较高的单质硫选择性(88.7%)。 说明材料具有良好的抗氧波动能力。
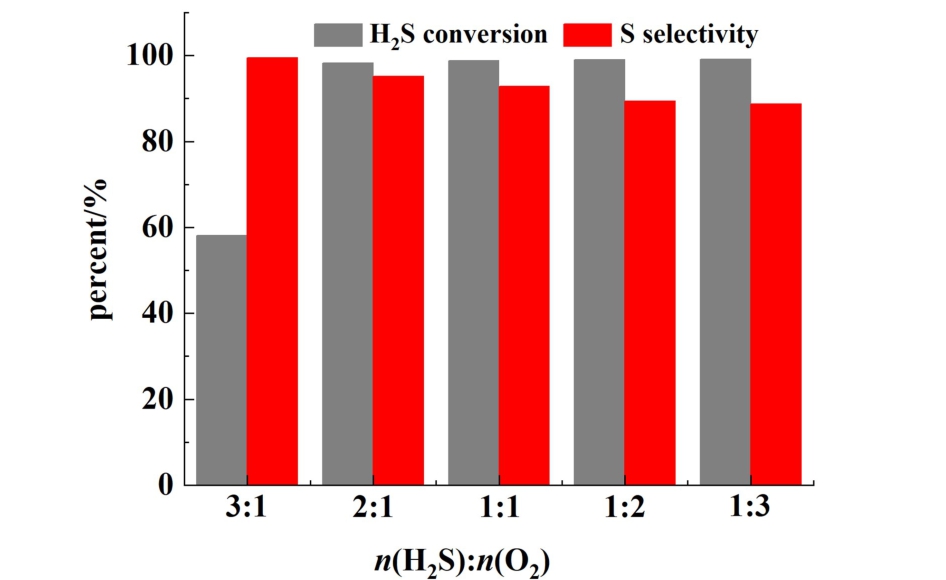
图9 氧含量对CNCe5催化剂催化性能的影响
Fig.9 Influence of O2 concentration on the catalytic performance of CNCe5 catalyst
在实际工况下,H2S气氛中往往伴随着大量的水蒸气。 因此,本研究考察了不同水蒸气含量对催化剂性能的影响,结果如图10所示。 在通入水蒸气后,硫化氢转化率从99.42%(5%的H2O,体积分数,下同)略微下降至98.65%(30%),硫单质选择性从98.47%(5%)略微下降98.04%(30%)。 说明材料具有极好的抗水性能。
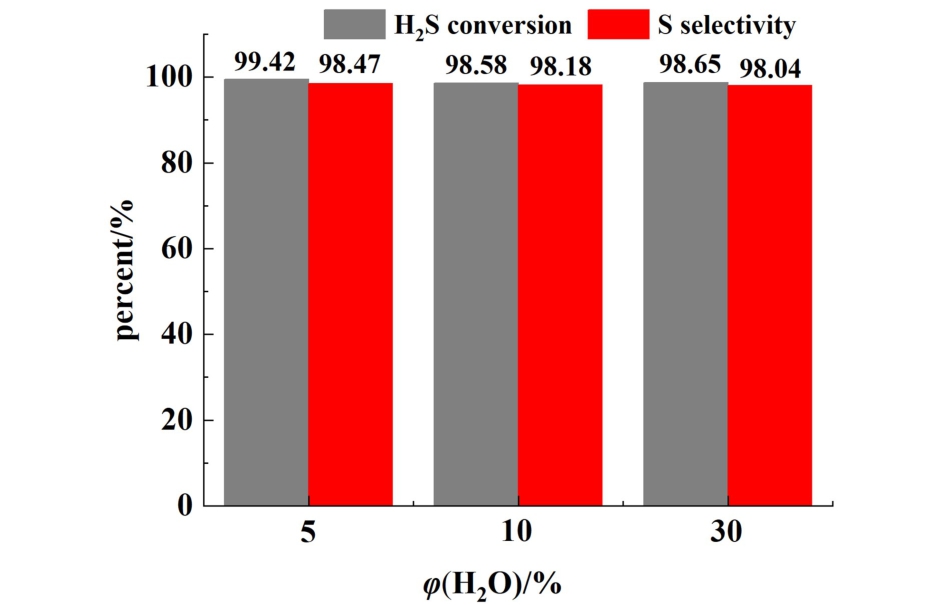
图10 水蒸气含量对CNCe5催化剂催化性能的影响
Fig.10 Influence of H2O concentration on the catalytic
利用热处理的方法(400 ℃条件下氮气吹扫2 h)对失活催化剂进行了再生,并评价了其再生性能,结果如图11所示。 CNCe5催化材料在运行120 min后,其H2S转化率由98%降到89%,此后进行热处理再生。 CNCe5在5次循环后120 min运行后的硫产率仍能维持在90%。
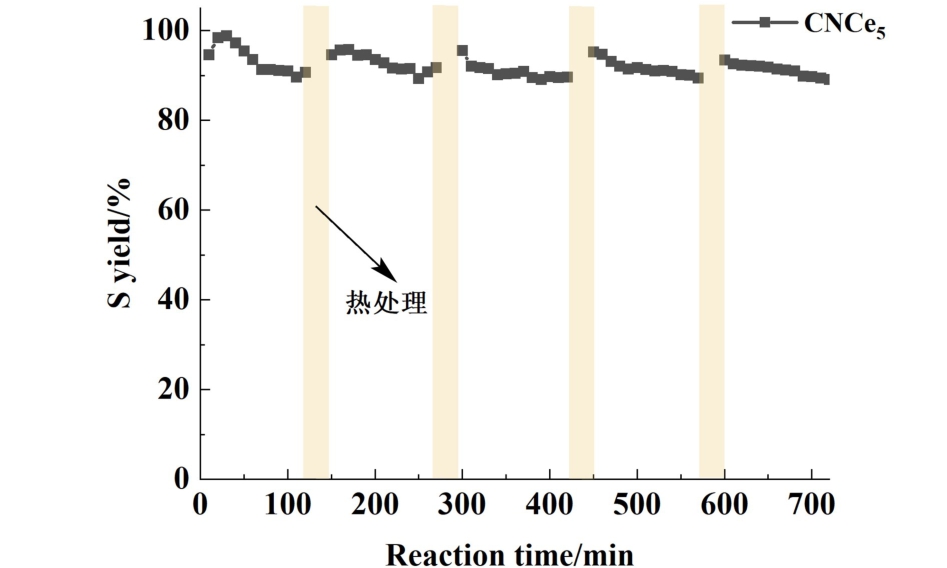
图11 CNCe5催化剂的循环再生性能
Fig.11 Regeneration performance of CNCe5 catalyst
结合以上实验结果,CNCe5材料展现出了优秀的催化性能、抗氧波动能力和抗水蒸气能力,同时表现出了较好的循环再生能力。 这些优点赋予了其较好的实际应用价值。
4 催化机理探究
利用原位红外光谱技术深入地研究了CNCe5材料上该反应机理。 在 CNCe5的原位红外光谱图中(图12),在3 100 ~3 800 cm-1范围内的宽红外吸收带,主要是来自表面O—H伸缩振动,对应了反应过程中生成的H2O,随着反应的进行,该振动峰的强度也逐渐增加,说明反应的发生;在2 700 ~3 400 cm-1范围内的宽红外吸收带,主要是来自表面N—H键的伸缩振动,对应着材料表面的吡啶氮物种,而该物种被认为是吸附位点,可用于H2S的吸附;在2 510 ~2 650 cm-1范围内的宽红外峰,对应于S—H键的振动,说明H2S在材料表面的解离吸附。
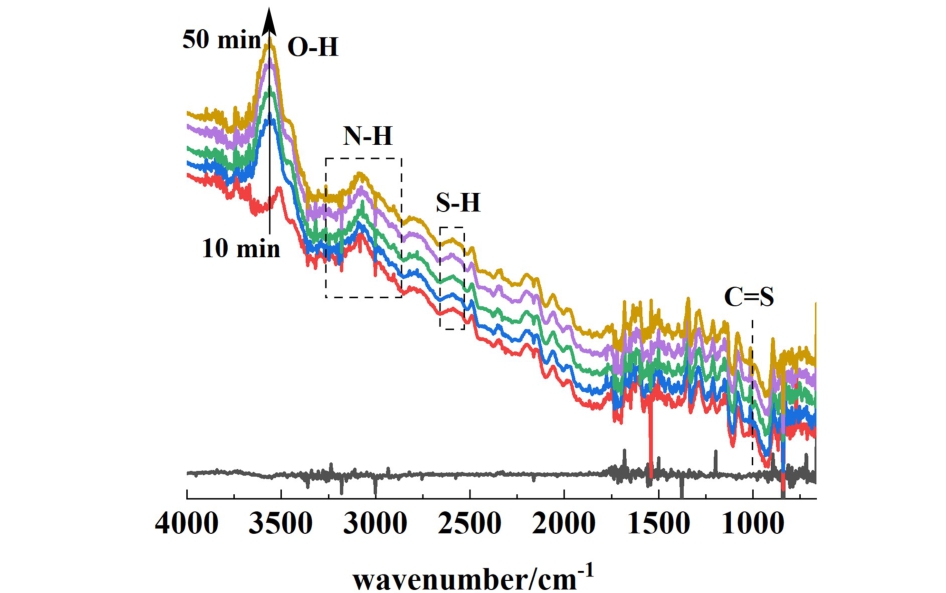
图12 CNCe5催化剂上反应的原位红外谱图
Fig.12 In-situ DRIFTS spectra of the reaction over CNCe5 catalysts
采用XPS进一步分析了CNCe5催化剂反应前后的元素组成和化学状态,结果如图13和表2。 结果表明,反应后材料中n(Ce3+)/n(Ce4+)由0.21上升至0.64,说明随着反应的进行,一部分Ce4+得电子转化为了Ce3+,这预示着Ce4+物种参与了反应,并且发生了氧化还原反应。 同时,在反应后的材料表面检测到了对应于硫酸盐物种的特征峰[169 eV处,图13(c)]。 图13(b)显示反应后O 1s的特征峰红移了约2 eV,说明氧的配位环境的改变,且反应后氧含量从8.22%增加到22.27%也进一步说明了大量的含氧物种沉积在材料表面,对应着硫酸盐生成。
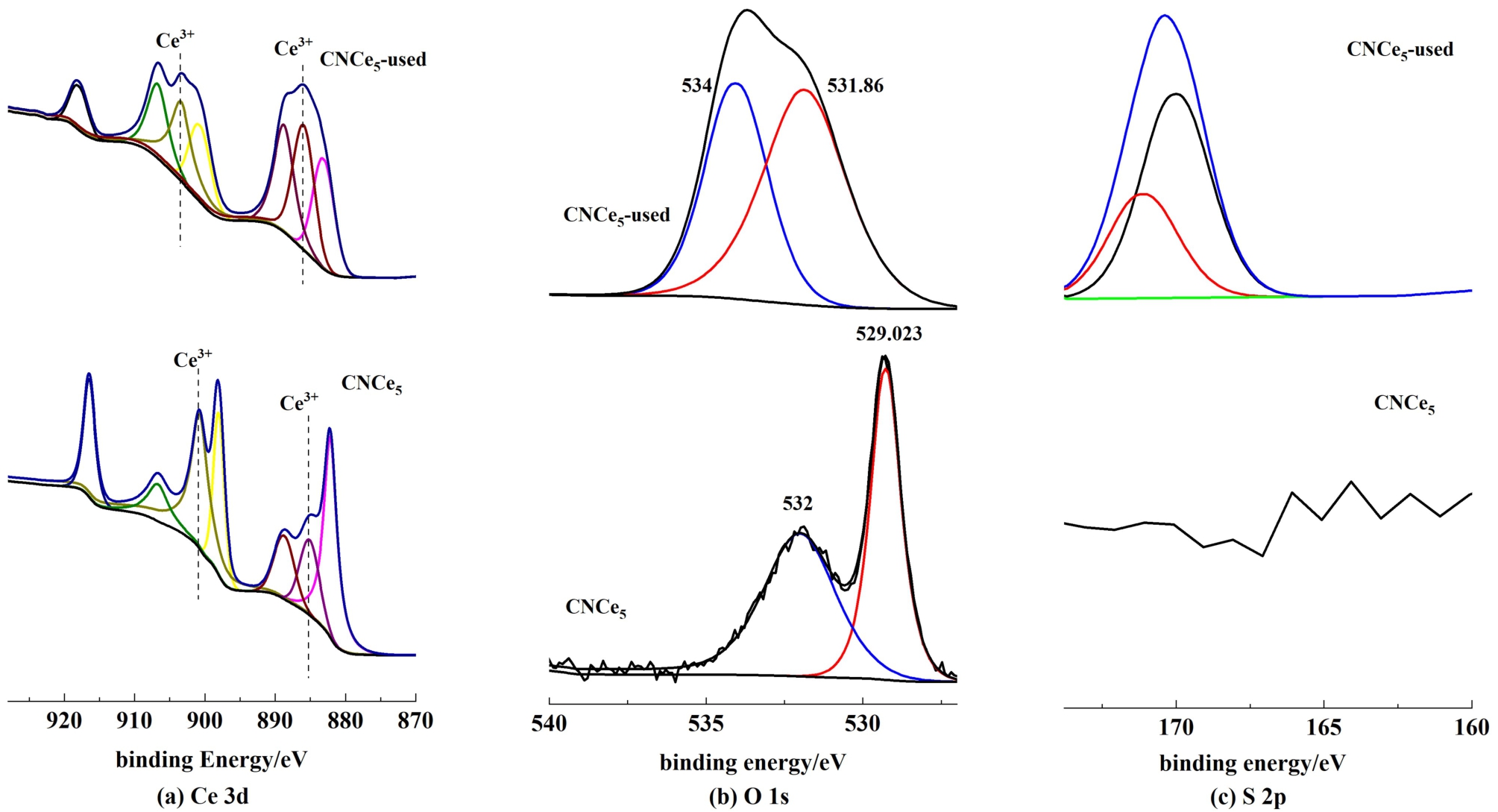
图13 CNCe5样品失活前后XPS谱图
Fig.13 XPS spectra of fresh and used CNCe5 catalyst
综合以上分析,可以推断出H2S在CNCex材料表面发生选择氧化反应的微观过程,如图14所示:(1)氮化碳表面的吡啶氮作为碱性位点,吸附硫化氢,并解离为HS-;(2)HS-进一步被Ce4+氧化为单质硫,同时Ce4+发生还原反应转化为Ce3+;(3)分子氧被表面缺陷活化为活性氧物种;(4)活性氧物种进一步将生成的Ce3+氧化为Ce4+,同时生成H2O。在催化循环中,Ce3+再氧化为Ce4+的速率决定了整个反应的进程。 O2在催化剂表面活性位上的活化效率以及后续活性氧物种的迁移速率共同限制了Ce3+的再氧化速率。 催化剂失活的原因可能是Ce3+被氧化成Ce4+的速率小于Ce4+被还原成Ce3+的速率,同时生成的硫酸盐物种沉积在表面导致活化氧的活性位点的覆盖也是造成催化失活的原因之一。
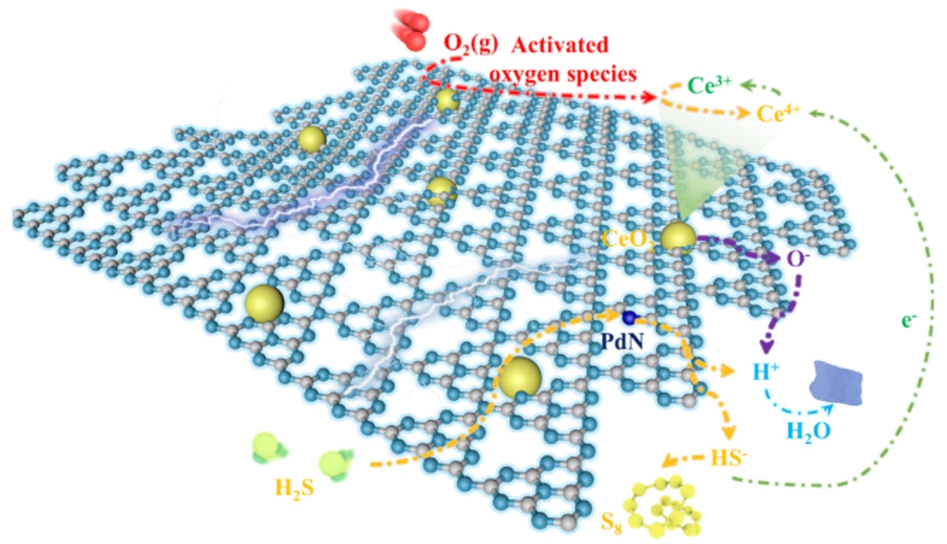
图14 H2S催化氧化反应机理示意图
Fig.14 Reaction mechanism for the catalytic oxidation of H2S
5 结论
通过一步法合成系列Ce掺杂的氮化碳材料,结果表明Ce掺杂后,材料的孔结构得到了明显的改善,有利于气体分子的传质。 部分Ce物种成功地进入了氮化碳材料的晶格中,导致氮化碳材料晶格的畸变或被破坏,从而产生了大量的表面缺陷位,极大地改善了材料对氧的吸附活化能力。 与此同时,部分未掺入晶格中的Ce以CeO2形式存在,其与氮化碳表面存在强相互作用,加速了Ce物种与氮化碳表面的电子转移,从而使得更多Ce4+物种存在。 活性测试表明,Ce掺杂后材料的催化性能得到了显著的提高,CNCe5催化剂可以在200 ℃条件下获得98.8%的硫磺产率,且表现出了极好的抗水性能(30% H2O条件下活性基本不变)、抗氧波动性能和一定循环再生性能。 对催化剂反应机理进行了深入探讨,并初步提出了可能的反应机理为:硫化氢吸附在氮化碳材料的吡啶氮位点上后解离为HS-,其后与Ce4+发生氧化还原反应生成单质硫和Ce3+,最后Ce3+被活性氧物种(缺陷位活化分子氧为活性氧物种)重新氧化为Ce4+并生成水。 Ce3+再氧化为Ce4+作为催化循环的决速步。 Ce3+被氧化成Ce4+的速率小于Ce4+被还原成Ce3+的速率。 同时生成的硫酸盐物种沉积在表面导致活化氧的活性位点被覆盖也是催化剂可能的失活原因。
[1] 刘江红, 石风华. 硫化氢脱除技术的研究进展[J]. 辽宁化工, 2010, 39(3): 292-294 LIU Jianghong, SHI Fenghua. Research progress of removing hydrogen sulfide technology [J]. Liaoning Chemical Industry,2010, 39(3): 292-294(in Chinese)
[2] 张剑锋. 液相氧化还原法脱硫工艺的现状与发展[J]. 石油与天然气化工, 1992, 21(3): 142-149 ZHANG Jianfeng. Present situation and development of liquidphase oxidation-reduction desulfurization process[J]. Chemical Engineering of Oil and Gas, 1992, 21(3): 142-149(in Chinese)
[3] 秦歌, 吴小军, 赵鹏, 等. 硫化氢中毒: 代谢机制及检验方法的研究进展[J]. 环境化学, 2025, 44(5): 1802-1814 QIN Ge, WU Xiaojun, ZHAO Peng, et al. Hydrogen sulfide poisoning: Advances in metabolic mechanisms and examination methods research[J]. Environmental Chemistry, 2025, 44(5):1802-1814(in Chinese)
[4] 王瑶, 张劲松, 范博文, 等. 急性硫化氢中毒合并中枢神经系统损伤的相关危险因素及其预测价值研究[J]. 南京医科大学学报(自然科学版), 2023, 43(12): 1650-1655, 1680 WANG Yao, ZHANG Jinsong, FAN Bowen, et al. Research on the related risk factors and predictive value of acutehydrogen sulfide poisoning combined with central nervous system injury[J].Journal of Nanjing Medical University ( Natural Sciences),2023, 43(12): 1650-1655, 1680(in Chinese)
[5] 薄宇,周洪,贾紫牧,等. 全球大气污染物和温室气体融合排放清单研究趋势分析[J/OL]. 中国环境科学, Doi: org/10.19674/j.cnki.issn1000-6923 BO Yu,ZHOU Hong,JIA Zimu,et al. Trend analysis in global integrated emission inventories of air pollutants and greenhouse gases [J/OL]. China Environmental Science, Doi: org/10.19674/j.cnki.issn1000-6923 (in Chinese)
[6] 洪铭江. 天然气脱硫方法的选择及醇胺法的运用研究[J].中国石油和化工标准与质量, 2020, 40(14): 146-147 HONG Mingjiang. Study on selection of natural gas desulfurization methods and application of alcoholamine method[J]. China Petroleum and Chemical Standard and Quality, 2020, 40(14):146-147(in Chinese)
[7] CHARISIOU N D, BAKLAVARIDIS A, PAPADAKIS V G, et al. Synthesis gas production via the biogas reforming reaction over Ni/MgO-Al2 O3 and Ni/CaO-Al2 O3 catalysts[J]. Waste and Biomass Valorization, 2016, 7(4): 725-736
[8] LIANG S, LIU F, JIANG L. Recent advances on nitrogen-doped metal-free materials for the selective catalytic oxidation of hydrogen sulfide[J]. Current Opinion in Green and Sustainable Chemistry, 2020, 25: 100361
[9] PRASERTCHAROENSUK P,PROMTONGKAEW A,TAWATCHAI M, et al. A review on sensitivity of operating parameters on biogas catalysts for selective oxidation of Hydrogen Sulfide to elemental sulfur[J]. Chemosphere, 2022, 301: 134579
[10] ONG W J, TAN L, NG Y H, et al. Graphitic carbon nitride(g-C3 N4)-based photocatalysts for artificial photosynthesis and environmental remediation: Are we a step closer to achieving sustainability? [J]. Chemical Reviews, 2016, 116 ( 12 ):7159-7329
[11] SHEN L, LEI G, FANG Y, et al. Polymeric carbon nitride nanomesh as an efficient and durable metal-free catalyst for oxidative desulfurization[J]. Chemical Communications, 2018, 54(20): 2475-2478
[12] KAMALI F, ESKANDARI M M, RASHIDI A, et al. Nanorod carbon nitride as a carbo catalyst for selective oxidation of hydrogen sulfide to sulfur[J]. Journal of Hazardous Materials, 2019,364: 218-226
[13] 肖永厚, 王树东, 袁权. 无氧下低浓度硫化氢在浸渍活性炭上的吸附研究[J]. 燃料化学学报, 2006, 34(6): 730-734 XIAO Yonghou, WANG Shudong, YUAN Quan. Adsorption of low concentration H2 S on impregnated activated carbon under anaerobic conditions[J]. Journal of Fuel Chemistry and Technology, 2006, 34(6): 730-734(in Chinese)
[14] LYU S, WANG J, ZHOU Y, et al. Structural lithium incorporated with the crystalline poly(triazine imide) frameworks for selective catalytic oxidative desulfurization[J]. Advanced Functional Materials, 2024, 34(10): 2310286
[15] YE H, XING W, ZHAO F, et al. Sabatier optimal of Mn-N4 single atom catalysts for selective oxidative desulfurization[J]. Angewandte Chemie International Edition, 2025, 64(7): e202419630
[16] PARK N K, HAN D, LEE T J, et al. A study on the reactivity of Ce-based Claus catalysts and the mechanism of its catalysis for removal of H2 S contained in coal gas[J]. Fuel, 2011, 90(1):288-293
[17] ESLEK KOYUNCU D D, YASYERLI S. Selectivity and stability enhancement of iron oxide catalyst by ceria incorporation for selective oxidation of H2 S to sulfur[J]. Industrial & Engineering Chemistry Research, 2009, 48(11): 5223-5229
[18] GASPER-GALVIN L D, ATIMTAY A T, GUPTA R P. Zeolitesupported metal oxide sorbents for hot-gas desulfurization[J]. Industrial & Engineering Chemistry Research, 1998, 37(10):4157-4166
[19] HAIBER D M, LEVIN B D A, TREACY M M J, et al. In-plane structural fluctuations in differently condensed graphitic carbon nitrides[J]. Chemistry of Materials, 2021, 33(1): 195-204
[20] HUMAYUN M, HU Z, KHAN A, et al. Highly efficient degradation of 2, 4-dichlorophenol over CeO2/g-C3 N4 composites under visible-light irradiation: Detailed reaction pathway and mechanism [J]. Journal of Hazardous Materials, 2019, 364:635-644
[21] XU F, LAI C, ZHANG M, et al. Facile one-pot synthesis of carbon self-doped graphitic carbon nitride loaded with ultra-low ceric dioxide for high-efficiency environmental photocatalysis: Organic pollutants degradation and hexavalent chromium reduction[J].Journal of Colloid and Interface Science, 2021, 601: 196-208
[22] YANG D, ZHUZHANG H, WANG R, et al. Carbon vacancies in a melon polymeric matrix promote photocatalytic carbon dioxide conversion [J]. Angewandte Chemie International Edition,2019, 58(4): 1134-1137
[23] WANG R, YANG P, WANG S, et al. Distorted carbon nitride nanosheets with activated n→π*transition and preferred textural properties for photocatalytic CO2 reduction[J]. Journal of Catalysis, 2021, 402: 166-176
[24] CHE W, CHENG W, YAO T, et al. Fast photoelectron transfer in (Cring)-C3 N4 plane heterostructural nanosheets for overall water splitting[J]. Journal of the American Chemical Society,2017, 139(8): 3021-3026
[25] LI M, CHEN C, XU L, et al. Surface defect-rich ceria quantum dots anchored on sulfur-doped carbon nitride nanotubes with enhanced charge separation for solar hydrogen production[J]. Journal of Energy Chemistry, 2021, 52: 51-59
[26] LIN H, TANG X, WANG J, et al. Enhanced visible-light photocatalysis of clofibric acid using graphitic carbon nitride modified by cerium oxide nanoparticles[J]. Journal of Hazardous Materials, 2021, 405: 124204
[27] LIU J, ZHANG T, WANG Z, et al. Simple pyrolysis of urea into graphitic carbon nitride with recyclable adsorption and photocatalytic activity [J]. Journal of Materials Chemistry, 2011, 21(38): 14398-14401
[28] JOURSHABANI M, SHARIATINIA Z, BADIEI A. Facile onepot synthesis of cerium oxide/sulfur-doped graphitic carbon nitride (g-C3 N4) as efficient nanophotocatalysts under visible light irradiation[J]. Journal of Colloid and Interface Science, 2017,507: 59-73
[29] HUANG H, DAI Q, WANG X. Morphology effect of Ru/CeO2 catalysts for the catalytic combustion of chlorobenzene[J]. Applied Catalysis B: Environmental, 2014, 158: 96-105
[30] FU J, ZHU B, JIANG C, et al. Hierarchical porous O-doped g-C3 N4 with enhanced photocatalytic CO2 reduction activity[J].Small, 2017, 13(15): 1603938
[31] WANG X, WU J, WANG J, et al. Methanol plasma-catalytic oxidation over CeO2 catalysts: Effect of ceria morphology and reaction mechanism[J]. Chemical Engineering Journal, 2019, 369:233-244
[32] ZAMAN J, CHAKMA A. Production of hydrogen and sulfur from hydrogen sulfide[J]. Fuel Processing Technology, 1995, 41(2): 159-198
[33] LI M, ZHANG L, WU M, et al. Mesostructured CeO2/g-C3 N4 nanocomposites: Remarkably enhanced photocatalytic activity for CO2 reduction by mutual component activations[J]. Nano Energy, 2016, 19: 145-155
[34] EDLUND D J, PLEDGER W A. Catalytic platinum-based membrane reactor for removal of H2 S from natural gas streams[J].Journal of Membrane Science, 1994, 94(1): 111-119
[35] ZHANG J, ZHANG G, CHEN X, et al. Co-monomer control of carbon nitride semiconductors to optimize hydrogen evolution with visible light [J]. Angewandte Chemie International Edition,2012, 51(13): 3183-3187
[36] ZAMAN J, CHAKMA A. A simulation study on the thermal decomposition of hydrogen sulfide in a membrane reactor[J]. International Journal of Hydrogen Energy, 1995, 20(1): 21-28