壬基酚(NP)是一种重要的精细化工原料和中间体,主要用于生产非离子表面活性剂、润滑油添加剂、纺织印染等。 同时,NP是环境内分泌干扰物(EDCs)[1],具有类雌激素效应,会影响生物体正常的生殖和发育,可导致人类男性精子数量减少[2]。并且,其具有致癌性、致畸性[3]、持久性以及生物蓄积性[4]。 中国和美国已将NP列为优先管控的环境污染物。 加拿大政府为保护环境和人类健康,制定了NP及其乙氧基酸盐的土壤质量标准[5]。 在施用粪肥和污水灌溉土壤中[6,7],NP浓度为0.01 ~7 600 μg·kg-1d. w. (d. w:干质量),其土壤污染受到广泛关注。
现在国内外研究主要采用生物降解、植物修复、电化学等方法去除土壤中壬基酚。 Shan等[8]采用14C示踪技术研究了蚯蚓对土壤中NP矿化、降解转化和残渣形成的影响,结果表明蚯蚓显著抑制了土壤中NP矿化和残渣的形成,但显著促进了土壤中NP及其代谢产物的降解转化。 Shi等[9]研究了铜绿假单胞菌对黑麦草植物修复NP和镉(Cd)复合污染土壤效率的影响,结果表明铜绿假单胞菌可以提高土壤酶活性,从而显著提高NP去除率。Guedes等[10]采用电动法对4-n-壬基酚(4-n-NP)污染土壤进行修复,结果表明污染物的电化学迁移与溶解度、辛醇-水分配系数相关,而4-n-NP的溶解度较低,导致电动法对4-n-NP污染土壤的修复效率较低。 现有研究聚焦于农田土壤NP的修复,化工场地土壤中NP修复相关研究较少。 生物修复、植物修复等技术存在修复效率低、应用范围窄等缺点,难以适用于化工场地土壤中NP修复。
近年来,热脱附技术由于具有去除效率高、修复效果显著等优点[11],广泛应用于持久性有机污染物和低沸点金属污染土壤修复。 有机污染物在土壤热处理过程包括脱附、再吸附、热解为中间产物、矿化(转化为CO2、H2O和C等)[12]。 于天等[13]采用响应面法探究热脱附过程中土壤粒径、含水率和有机质对石油烃及其各组分热脱附效率的影响,发现各因素间有显著的交互作用。 Li等[14]研究了不同矿物对人工含油土壤热解产物和二次污染物的影响,结果表明矿物对含油土壤热解有显著影响,且与热解温度密切相关。 Zhang等[15]研究了在热处理过程中还原性粘土矿物对悬浮液中苯酚的氧化降解机制,阐明Fe2+在升温时加速·OH的产生,并对苯酚进行降解。 然而,目前采用热脱附技术修复NP污染土壤的研究尚未报道。
本研究对4-n-NP污染土壤进行了热脱附处理,考察了温度、时间、含水率、升温速率和污染物浓度等因素对4-n-NP去除率的影响,并基于响应面法进行了工艺参数优化。 在此基础上,探究4-n-NP热脱附处理的化学动力学过程,明晰热脱附废气组成特征,解析4-n-NP热脱附转化途径,为土壤4-n-NP热脱附修复技术工程化应用提供科学依据和技术支撑。
1 材料与方法
1.1 材料与试剂
实验试剂包括4-壬基酚(C15H22O,4-n-NP,CAS:104-40-5);正己烷(C6H14,色谱纯);二氯甲烷(CH2Cl2,色谱纯);乙腈(CH3CN,色谱纯);乙酸乙酯(C4H8O2,色谱纯);去离子水;甲醇(CH4O,色谱纯)。 土壤样品取自某日用化学品生产企业周边区域土壤。 经风干、研磨、过筛和染毒(根据参考文献[16]中土壤壬基酚浓度加入4-n-NP标准样品)等过程制成。
1.2 实验方法
单因素实验设计:在热脱附温度(100~600 ℃)、时间(10 ~ 60 min)、含 水 率(10% ~ 30%)、升 温速率(5~25 ℃·min-1)和污染物浓度(200 ~ 1 200 μg·kg-1)的条件下分别考察热脱附温度、时间、含水率、升温速率和污染物浓度对4-n-NP去除率的影响。
利用Design Expert软件进行热脱附实验参数设计。 基于响应面法(RSM),采用中心复合设计(CCD)分析加热温度、停留时间、升温速率、含水率、4-n-NP浓度与去除率的对应关系,确定了4-n-NP热脱附最适宜参数。 其中,4-n-NP去除率计算见式(1)。 根据单因素的实验结果确定温度、时间、含水率、升温速率和4-n-NP浓度范围,响应面实验设计表格见表1。 采用Design-Expert软件进行多元非线性回归分析,见式(2)。
表1 实验运行参数
Table 1 Experimental operating parameters
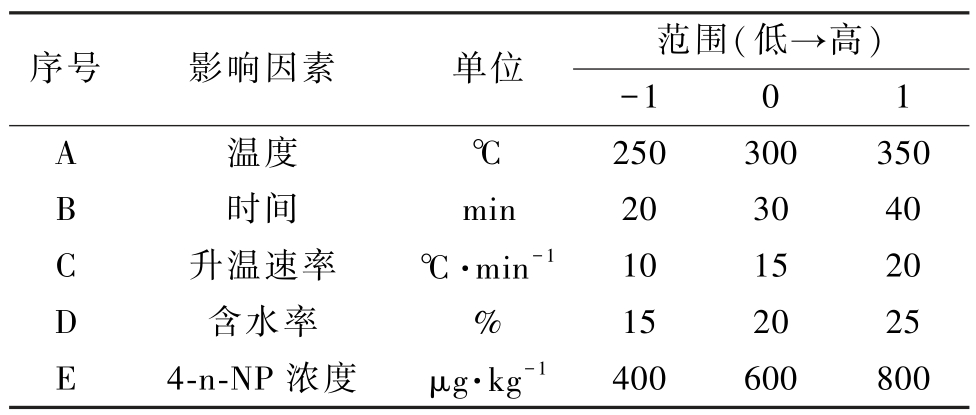
序号 影响因素 单位 范围(低→高)-1 0 1 A 温度 ℃ 250300350 B 时间 min 20 30 40 C 升温速率 ℃·min-1 10 15 20 D 含水率 % 15 20 25 E 4-n-NP 浓度 μg·kg-1 400 600 800
式(1)中:RE为土壤中4-n-NP的去除率,%;c0为4-n-NP的初始质量分数,μg·kg-1;c为热脱附处理后4-n-NP的残留质量分数,μg·kg-1。
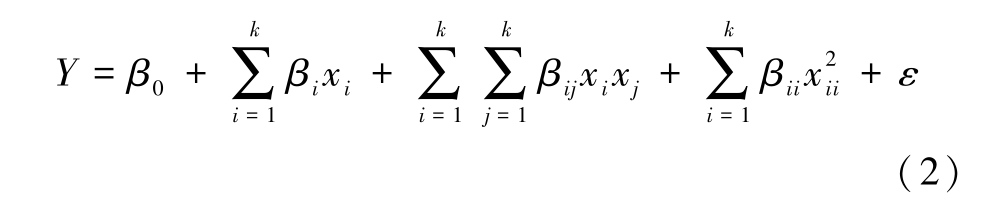
式(2)中:Y是响应变量;β0、βi、βij和βii是截距系数、线性系数、二次系数和相互作用系数的回归常数;xi、xj是自变量或因子;ε 是误差;k为研究变量数。
热脱附实验和 XRD表征: 使用管式炉对4-n-NP污染土壤样品进行热处理。 在实验中,将10 g污染土壤放入加热区,以1.5 L·min-1的速率连续注入高纯氮,温度、时间、升温速率、含水率、4-n-NP浓度等工艺参数见表1。 热处理后,土壤样品冷却至室温(20 ℃)。 土壤在热脱附过程中的物相组成和晶体结构变化由X射线衍射仪(XRD-Bruker)进行表征,扫描角度为3°~80°,步长0.02°。
土壤4-n-NP检测:向土壤中加入10 mL二氯甲烷和乙酸乙酯(体积比为4 ∶1)溶液,在35 ℃下超声提取20 min。 将液相转移到离心管中,以4 000 r·min-1离心10 min,重复以上操作3次,合并上清液。 上清液经旋转蒸发仪浓缩至近干后,立即加入1 mL正己烷。 通过硅胶-无水硫酸钠层析柱净化后,用6 mL二氯甲烷-乙酸乙酯(体积比为4 ∶1)洗脱,经氮吹仪吹干,加入1 mL乙腈定容,采用HPLC检测。
TG-FTIR分析:为研究土壤中4-n-NP的动态热解行为,将约20~30 mg土壤样品装入热重分析仪(NETZSCH STA 449F3) 热解管中,在氩气中以10 ℃·min-1从室温加热至600 ℃。 通过FTIR光谱仪(Bruker Tensor 27,德国)记录4-n-NP热解过程中生成气相产物在500~4 000 cm-1的FTIR光谱。
Py-GC/MS分析:为研究土壤中4-n-NP热解气相产物组成,取约3 ~ 5 mg土壤样品,在热解仪(Frontier-Lab Co,Py-2020iD)中以20 ℃·ms-1在300和500 ℃下进行热解,并保持30 s,以确保4-n-NP充分热解。 气相色谱/质谱仪(Shimadzu GC—2010/QP 2010)配备HP-5毛细管柱(30 m × 250 μm ×0.25 μm),通过NIST质谱库筛查识别m/z 50~500范围内产物。
2 结果与讨论
2.1 工艺参数对壬基酚去除率的影响
加热温度、停留时间、升温速率、初始污染物浓度和初始含水率等因素对热脱附去除率具有不同程度影响。 如图1 (a)和图1(b),在100~600 ℃和10~60 min范围内,4-n-NP去除率与温度和时间呈正相关。 当污染土壤中4-n-NP初始浓度为1 mg·kg-1、温度为200 ℃、时间为20 min时,4-n-NP去除率能达到80%左右;在300 ℃以上温度热处理20 min,去除率接近100%。 4-n-NP热脱附去除率与温度的关系和其他酚类污染物具有相似结果,Zhang等[15]研究了热脱附温度对土壤中苯酚降解的影响,苯酚去除率随着温度升高和时间的增加而增加;Davis等[17]对土壤中五氯酚的去除研究表明,随温度升高,五氯酚去除率逐渐增加,气相产物逐渐减少。
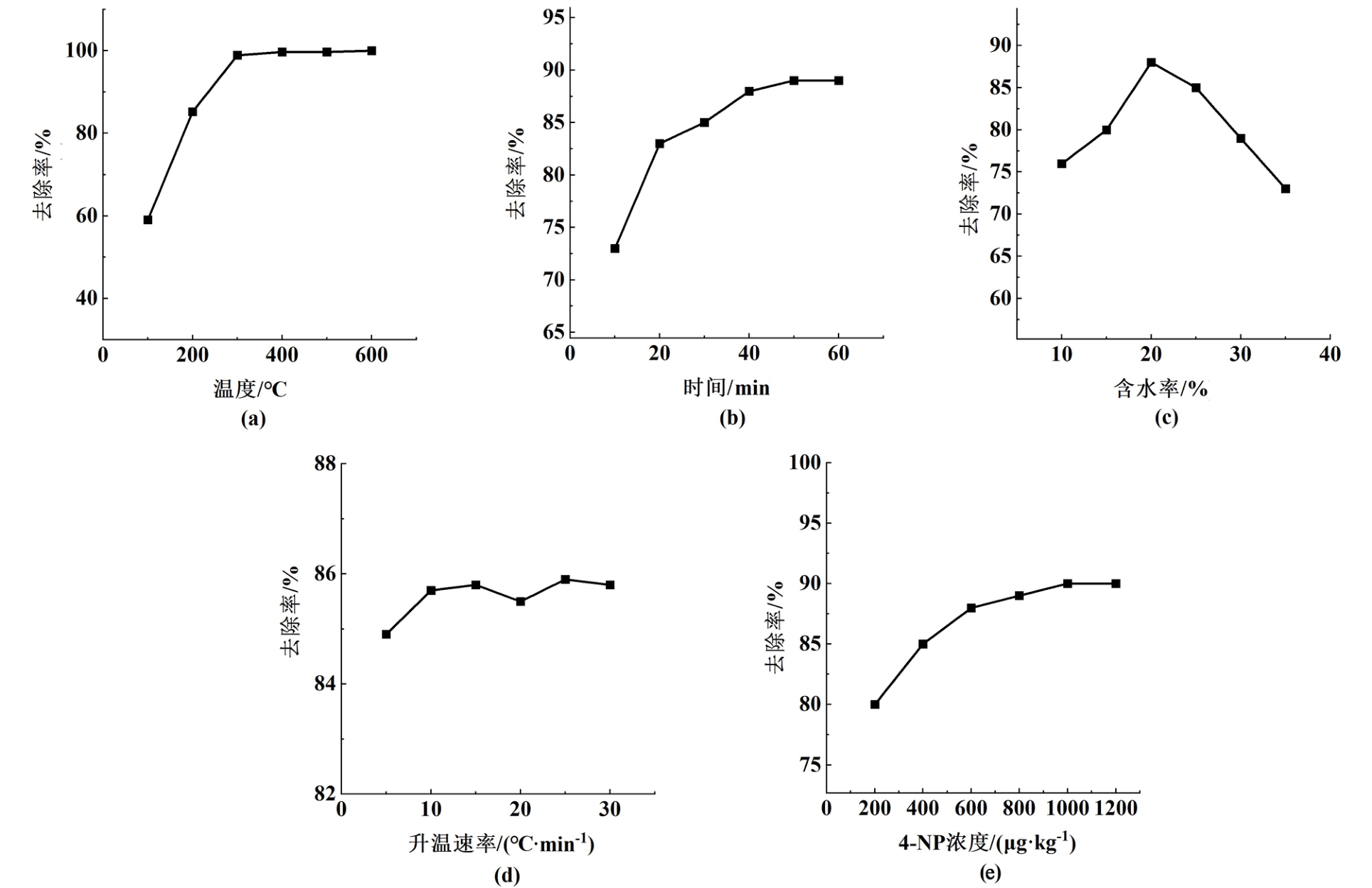
图1 (a)加热温度;(b)停留时间;(c)含水率;(d)加热速率和(e)初始浓度对4-n-NP去除率的影响
Fig.1 (a) Effects of heating temperature; (b) residence time; (c) moisture content; (d) heating rate and (e) initial concentration on 4-n-NP removal rate
含水率对4-n-NP热脱附效率影响较为显著。如图1(c),在含水率为10%~20%时,4-n-NP去除率随含水率增加而增加;在超过20%时,随着含水率增加,4-n-NP去除率下降。 含水率较高的土壤热脱附效率较低,是因为高温下土壤水分迅速蒸发,含水率较高的土壤板结严重,阻碍了内部污染物的扩散迁移[18]。 此外,含水率过高会形成水膜,占据粒间空隙,抑制传质过程,导致4-n-NP去除率下降[19]。 Feeney等[20]在研究中指出,热脱附处理的污染土壤应具有一定含水量(最适宜值为10% ~20%),水分挥发在一定程度上会促进有机物的脱附,因此合适的含水率对于热脱附效率至关重要。
升温速率和4-n-NP浓度对热脱附效率有一定影响。 如图1(d)和图1(e)所示,在5~30 ℃·min-1,200~1 200 μg·kg-1范围内,4-n-NP去除率与升温速率、污染物浓度总体呈现正相关关系,但相比热脱附温度和时间,影响较小。 研究结果与Bai等[21]关于土壤多氯联苯(PCBs)热脱附修复研究结果相似,污染土壤中PCBs的去除效率与升温速率大致呈正线性相关。 污染物浓度对热脱附效率的影响主要体现在土壤对4-n-NP的吸附效应上,高浓度4-n-NP吸附在土壤颗粒表面,热脱附初期表层4-n-NP容易脱附,去除效率高。 但随着时间推移,剩余污染物浓度相对较低,4-n-NP全部被土壤介质包裹和吸附,脱附困难,导致去除率下降[16]。
2.2 响应面法优化工艺参数
根据热脱附实验结果,基于二阶回归模型[22],建立土壤4-n-NP热脱附去除率与影响因子的二次多项回归方程,如式(3)所示。 该模型的回归方程较好地解释了响应面试验结果,并预测了4-n-NP去除最适宜工艺参数。

式(3)中:Y为4-n-NP去除率,%;A为加热温度,℃;B为停留时间,min;C为升温速率,℃·min-1;D为含水率,%;E为4-n-NP浓度,μg·kg-1。
如图2(a)所示,在加热温度、停留时间、升温速率、含水率和污染物浓度因素中,温度对响应面的影响最显著。 4-n-NP去除率的预测值和实际值高度吻合,见图2(b),模型回归预测R2为0.851,表明模型拟合程度较好。 表2显示了回归模型的方差分析和显著性检验结果。 模型中F值为72.92,对应P值<0.000 1,表明该模型具有较高可信度。 失拟项的P值为0.062(P>0.05),说明模型在本实验的拟合度良好。 模型信噪比为32.00(大于4),进一步确认了建立的二次多项式模型合理性和一致性,可用于4-n-NP污染土壤热脱附工艺参数优化。 模型预测当4-n-NP浓度为800 μg·kg-1(文献[7]报道土壤环境NP浓度为ND-7 600 μg·kg-1,中位数约为800 μg·kg-1),工艺参数设置为温度399 ℃、停留时间20 min、含水率16%、升温速率19 ℃·min-1时,4-n-NP热脱附去除率为99%。 在此条件下热脱附实验结果显示4-n-NP去除率为97%,实验结果与预测结果高度吻合。
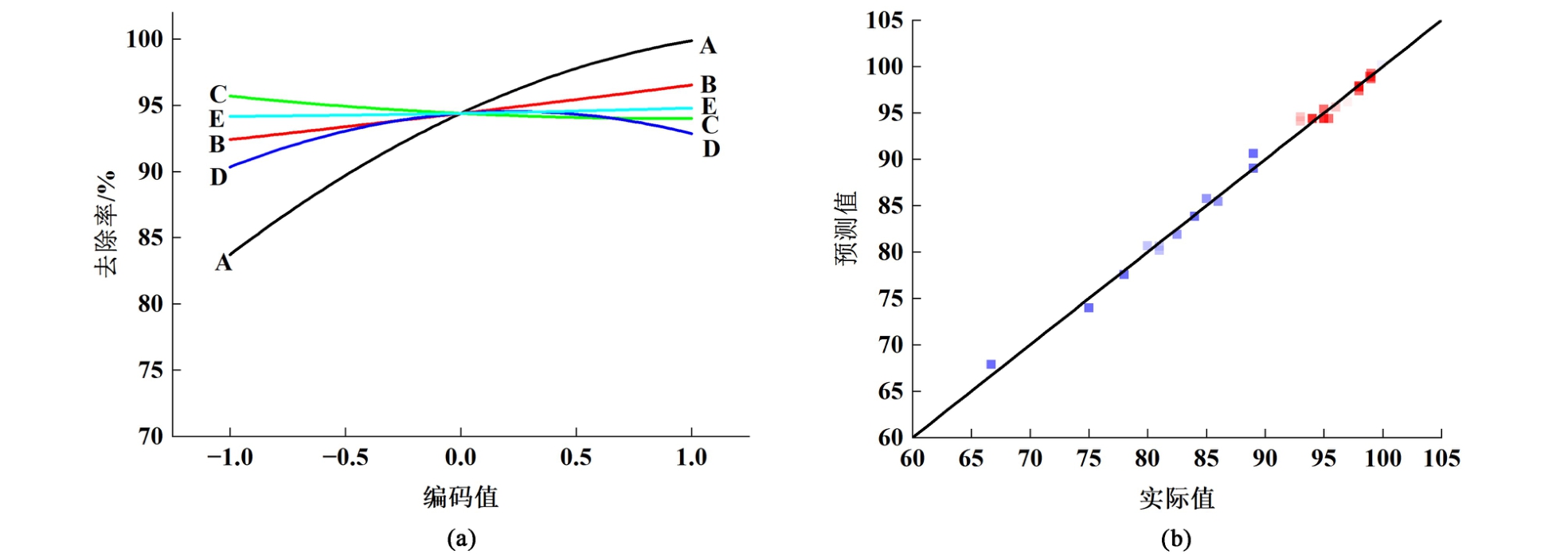
图2 (a) 显示所有参数影响的扰动图;(b) 4-n-NP去除率的实际-预测值曲线图
Fig.2 (a) Perturbation plot showing the effects of all parameters; (b) actual-predicted curve of 4-n-NP removal rate
表2 响应面二次模型方差分析
Table 2 Response surface quadratic model analysis of variance
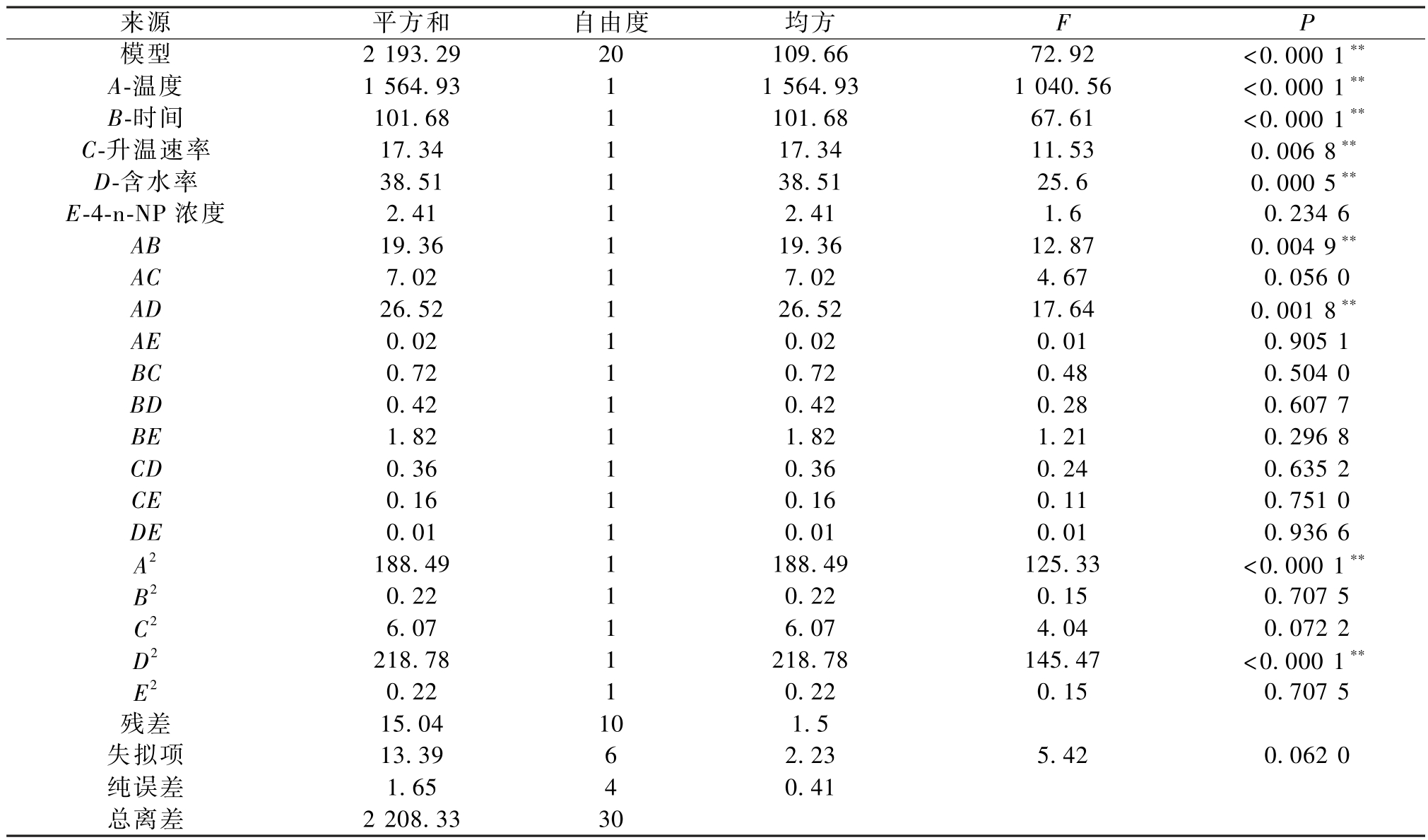
注:∗表示P<0.05;∗∗表示P<0.01。
来源 平方和 自由度 均方 F P模型 2 193.29 20 109.66 72.92 <0.000 1∗∗A-温度 1 564.93 1 1 564.93 1 040.56 <0.000 1∗∗B-时间 101.68 1 101.68 67.61 <0.000 1∗∗C-升温速率 17.34 1 17.34 11.53 0.006 8∗∗D-含水率 38.51 1 38.51 25.6 0.000 5∗∗E-4-n-NP 浓度 2.41 1 2.41 1.6 0.234 6 AB 19.36 1 19.36 12.87 0.004 9∗∗AC 7.02 1 7.02 4.67 0.056 0 AD 26.52 1 26.52 17.64 0.001 8∗∗AE 0.02 1 0.02 0.01 0.905 1 BC 0.72 1 0.72 0.48 0.504 0 BD 0.42 1 0.42 0.28 0.607 7 BE 1.82 1 1.82 1.21 0.296 8 CD 0.36 1 0.36 0.24 0.635 2 CE 0.16 1 0.16 0.11 0.751 0 DE 0.01 1 0.01 0.01 0.936 6 A2 188.49 1 188.49 125.33 <0.000 1∗∗B2 0.22 1 0.22 0.15 0.707 5 C2 6.07 1 6.07 4.04 0.072 2 D2 218.78 1 218.78 145.47 <0.000 1∗∗E2 0.22 1 0.22 0.15 0.707 5残差 15.04 10 1.5失拟项 13.39 6 2.23 5.42 0.062 0纯误差 1.65 4 0.41总离差 2 208.33 30
根据上述5个因素对4-n-NP去除率的综合影响,绘制了三维响应曲面。 如图3所示,加热温度与其余因素的交互作用明显,曲面呈现左下角低、右上角高的形状。 在一定时间与含水率条件下,4-n-NP去除率随温度增加而逐渐增加。 当加热温度超过250 ℃且含水率在15% ~25%时,4-n-NP去除效果最佳。 这是由于随温度升高,传热速度加快,4-n-NP更容易从土壤中挥发,4-n-NP去除效率增加。 如图4所示,升温速率、4-n-NP浓度以及含水率之间三维交互曲面倾斜较小,表明各因素之间交互作用较弱。 曲面倾斜程度表明,温度和时间及温度和含水率之间交互作用对4-n-NP去除率影响最为显著,与模型方差分析结果一致。
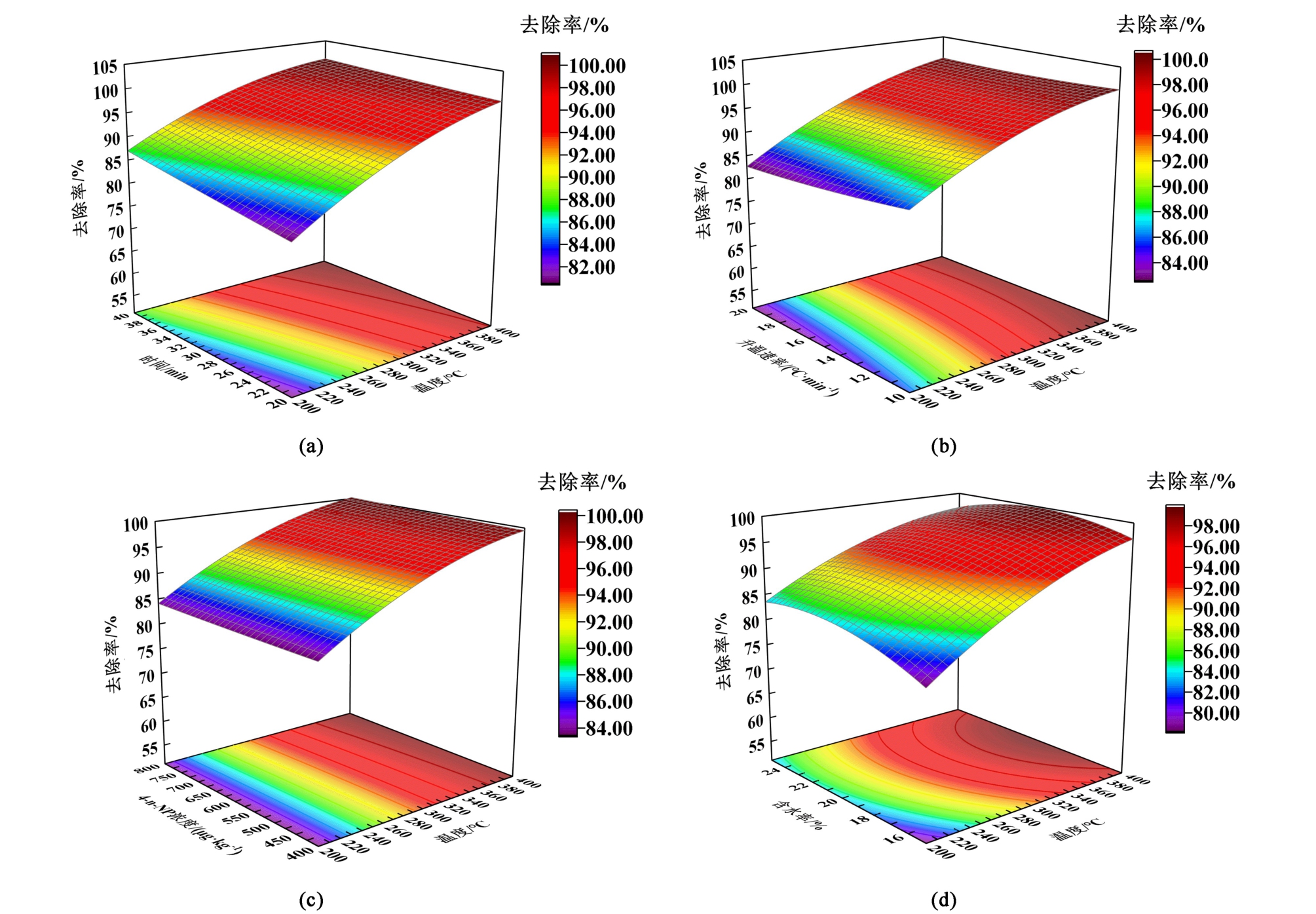
图3 (a)温度与时间;(b)温度与升温速率;(c)温度与4-n-NP浓度和(d)温度与含水率对去除率的交互作用
Fig.3 (a) Interactions between temperature and time; (b) temperature and heating rate; (c) temperature and 4-n-NP concentration and (d) temperature and water content on the removal rate
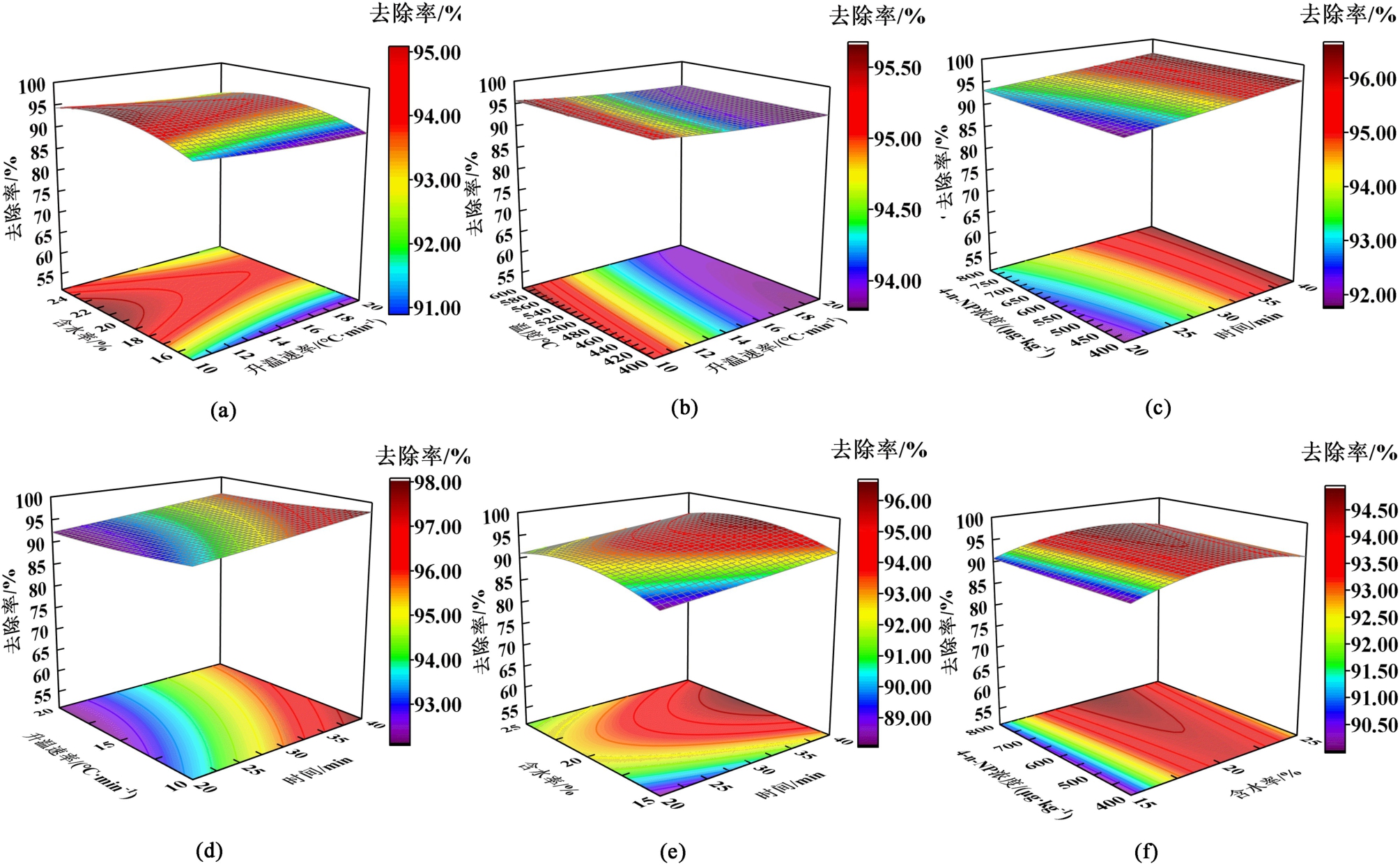
图4 (a)升温速率和时间;(b)含水率和时间;(c) 4-n-NP浓度和时间;(d)含水率和升温速率;(e)4-n-NP浓度和升温速率和(f)4-n-NP浓度和含水率对去除率的交互作用
Fig.4 The interaction of (a) heating rate and time; (b) moisture content and time; (c) 4-n-NP concentration and time; (d) moisture content and heating rate; (e) 4-n-NP concentration and heating rate; (f) 4-n-NP concentration and moisture content on the removal rate
2.3 壬基酚热脱附过程动力学分析
采用一级反应动力学、二级动力学与指数衰减动力学方程拟合不同加热时间下土壤中4-n-NP的总去除效率,动力学方程分别见式(4)、式(5)和式(6)。
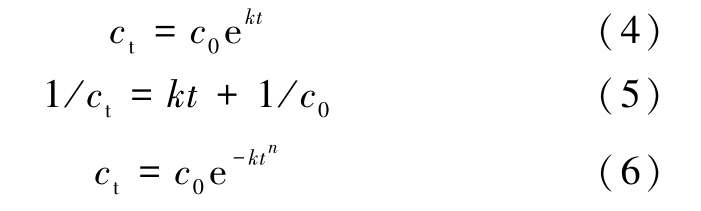
式(4)~式(6)中:ct为加热一定时间后4-n-NP浓度,μg·kg-1;c0为4-n-NP初始浓度,μg·kg-1;t为热脱附时间,min;k为模型速率常数,n是指数衰减模型的阶数。
4-n-NP去除动力学曲线如图5,不同动力学曲线拟合R2均大于0.82。 4-n-NP热脱附过程分为2个解吸阶段,前10 min发生快速解吸,污染物浓度急剧下降,而后解吸速率减缓,30 min左右开始达到解吸平衡。 一级和指数衰减动力学模型对4-n-NP污染土壤热脱附过程拟合效果较好(R2为0.906~0.999),表明4-n-NP热脱附过程由膜扩散和化学解吸共同主导[23]。 4-n-NP热脱附动力学方程可分析4-n-NP残留浓度与处理温度和时间的关系,为4-n-NP热脱附修复工程应用的能量效率和成本衡算提供支撑。
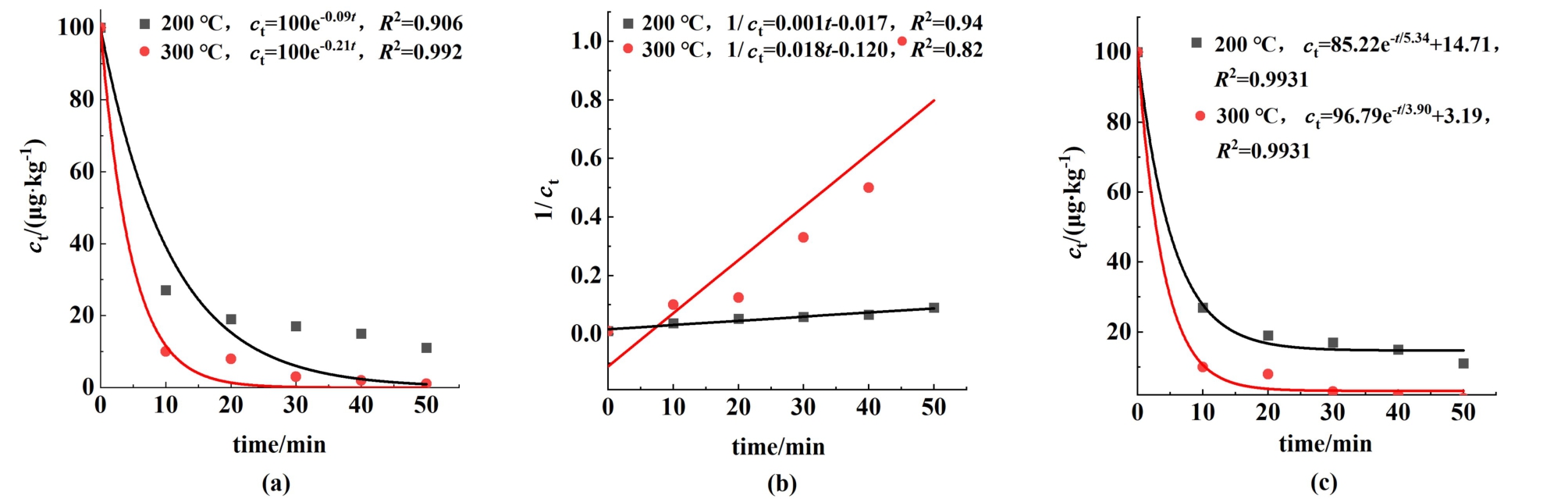
图5 4-n-NP污染土壤热处理的(a)一级动力学;(b)二级动力学;(c)指数衰减动力学拟合曲线
Fig.5 (a) first-order kinetics; (b) second-order kinetics; (c) exponential decay kinetics fitting curve of 4-n-NP contaminated soil heat treatment
2.4 TG-FTIR 分析
TGA-DTG曲线如图6(a)和图6(b)所示,在150 ℃之前,质重量变化较小;在300和500 ℃时存在较为明显的热失量。 FTIR图6(c)表明,随着温度增加,土壤含碳、氧官能团数量增加,伴随着复杂小尖峰频谱带释放。 4 000~3 500 cm-1范围内频谱带与羟基相关[24],表明水蒸气释放。 而2 400 ~2 250 cm-1范围内频谱带是CO不对称拉伸振动,对应CO2排放。 H2O和CO2随温度增加而增加,500 ℃之前主要与水蒸气挥发和含碳、氧官能团的脱氧脱氢反应[25]有关,500 ℃土壤矿物学组分向较小衍射峰移动表明,超过500 ℃时和土壤矿物分解促进H2O和CO2的生成有关,如图6(d)。 随着温度升高,土壤表面组成没有显著变化,见图6(d)。土壤中含有一定量的硅铝酸盐,天然硅铝酸盐可通过质子传递以及授受电子来产生催化作用[26],因此可能存在土壤矿物催化降解4-n-NP路径。 1 750~1 250 cm-1和3 500~3 000 cm-1范围内的小尖峰对应于 C-C (1 520 ~ 1 510 cm-1)、 CO (1 750 ~1 700 cm-1和1 680~ 1 650 cm-1)和CH(3 350 ~3 150 cm-1)官能团,表明在高温下有机物分解并产生含碳、氧官能团的化合物,与Liu等[27]对石油烃污染土壤TG-FTIR研究结果相似。
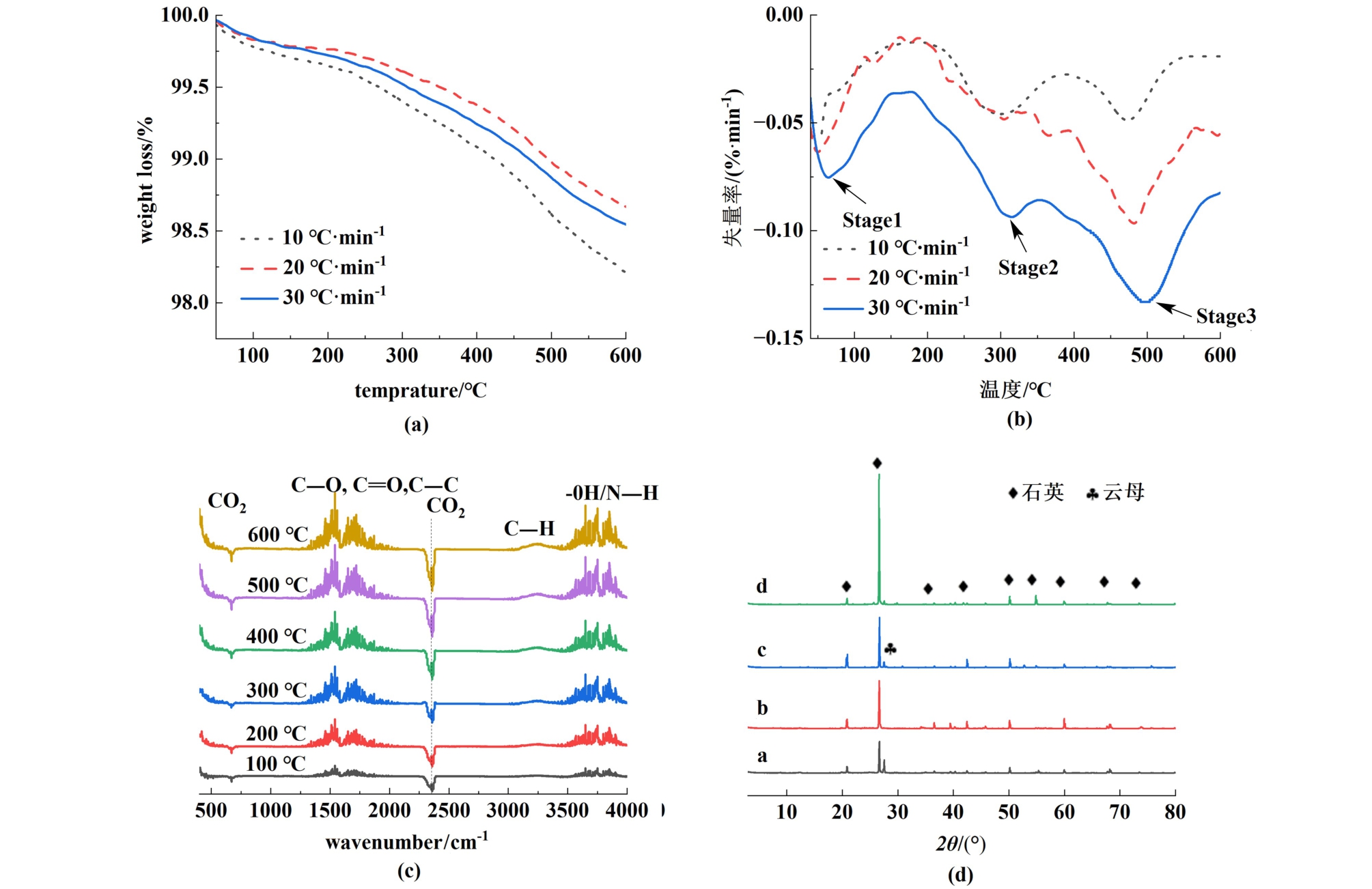
图6 升温速率为10~30 ℃·min-1时,在100~600 ℃范围内4-n-NP的(a)TGA和(b)DTG曲线;4-n-NP污染土壤热解样品的(c)FTIR光谱和(d)XRD图
Fig.6 The TGA (a) and DTG (b) curves of 4-n-NP were obtained in the temperature range of 100-600 ℃ when the heating rate was 10—30 ℃·min-1; FTIR spectra (c) and XRD patterns(d) of 4-n-NP contaminated soil pyrolysis samples
2.5 Py-GC/MS 分析
根据4-n-NP去除效率与TG分析结果,热解温度为300和500 ℃时,热脱附去除效率分别达到90 %和100 %,TG曲线质量变化显著。 在这2个温度下进行Py-GC/MS测试分析,研究其热脱附气相产物。 如图7,在300 ℃时产生气相组分主要以苯甲酸等羧酸、2,5-二甲基-3-乙烯基-1,4-己二烯等烯烃、2,6-二叔丁基对甲酚等为主;在500 ℃时主要为3,5-二甲基-3-己醇、2,2-二甲基-3-戊醇等醇类,只有少量酚类化合物被检出。 由于酚类污染物在热解过程中会转化为烷烃、芳烃等[28],并通过脱烷基以及活性氧物种氧化酚对位甲基等途径[29,30],进一步转化为醇类、羧酸类等,表明4-n-NP在加热过程可能产生2,6-二叔丁基对甲酚、苯甲酸、苯甲酸丙酯、3,5-二甲基-3-己醇等化合物。
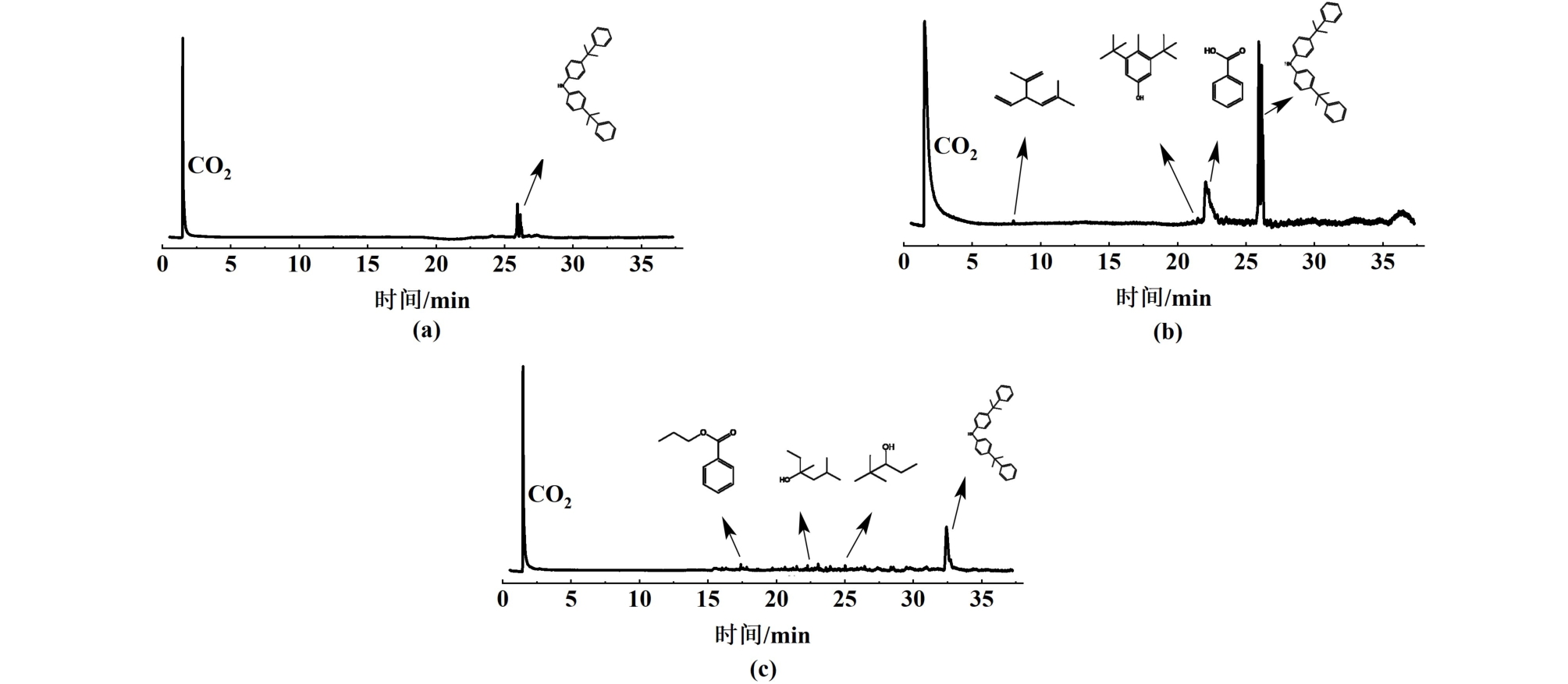
图7 (a)干净土壤300 ℃;(b)4-n-NP污染土壤300 ℃;(c)4-n-NP污染土壤500 ℃的Py-GC-MS分析
Fig.7 (a) Py-GC-MS analysis of clean soil at 300 ℃; (b) 4-n-NP contaminated soil at 300 ℃ and(c)4-n-NP contaminated soil at 500 ℃
结合TG-FTIR分析结果推断,热脱附过程中4-n-NP可能的转化路径如图8,包括脱烷基生成对甲基苯酚和正庚烷,进一步转化为苯甲酸、苯甲酸丙酯、3,5-二甲基-3-己醇等。 在热脱附过程,矿物表面的H2O、O2会形成HO·和O-2·等活性物种[31]。由于4-n-NP键解离能较低的C—C键(苯环与壬基碳之间),在加热状态下容易被自由基攻击断裂生成对甲基苯酚,并进一步氧化生成对羟基苯甲酸[32]。对羟基苯甲酸中的酚羟基容易脱去[29],形成苯甲酸并通过酯化反应生成苯甲酸丙酯。 4-n-NP脱烷基生成的正辛烷、正庚烷等,可以通过质子化环丙烷碳正离子机理转化为同分异构体[33],并在高温下继续发生裂解和自由基链式反应生成3,5-二甲基-3-己醇、2,2-二甲基-3-戊醇等。 4-n-NP高温下烷基链断裂,直链烷烃会进一步断裂成小分子烷烃,进而在苯环上发生亲电取代反应[34],生成2,6-二叔丁基对甲酚。
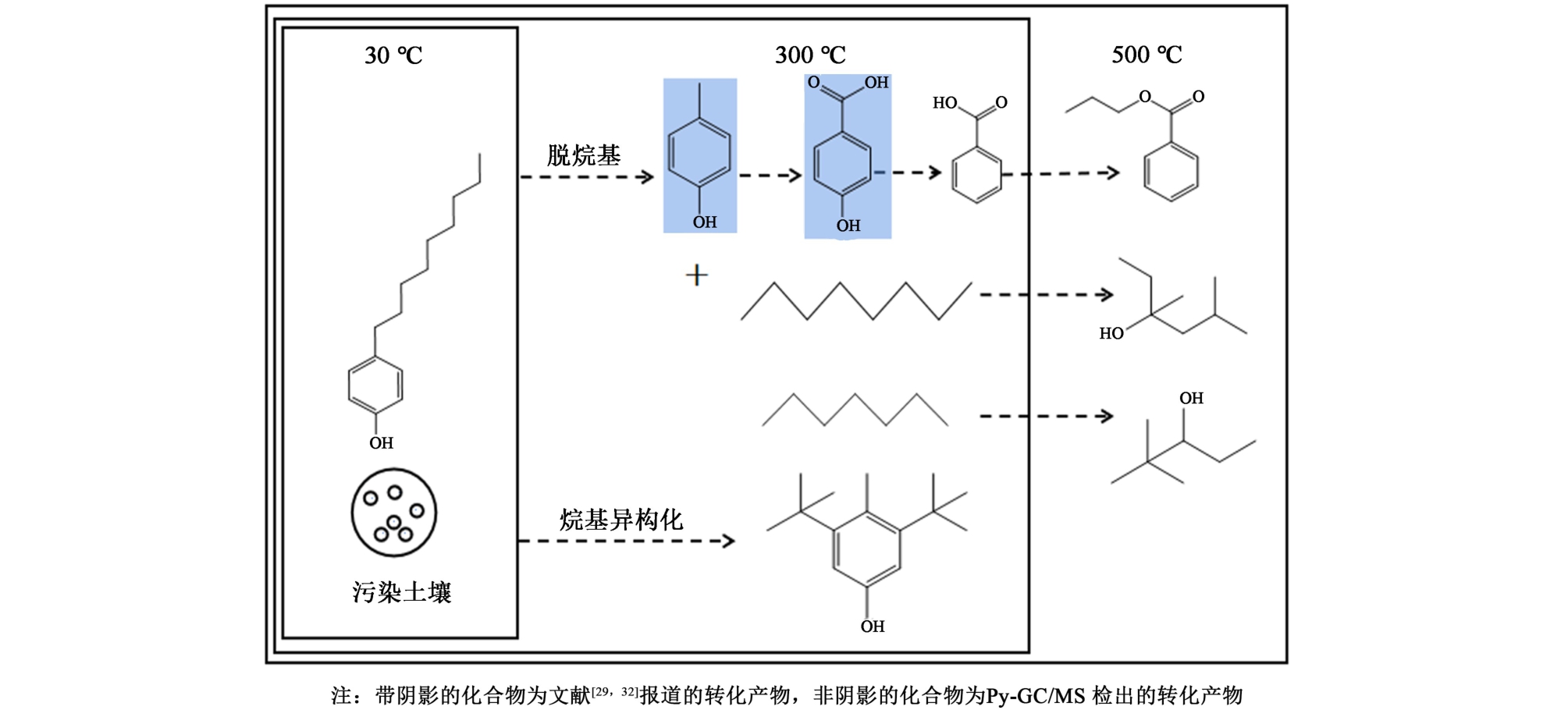
图8 热脱附过程中4-n-NP可能的转化路径
Fig.8 The possible transformation pathway of 4-n-NP in the thermal desorption process
3 结论
(1)温度、时间和含水率对土壤中4-n-NP热脱附去除具有重要影响。 4-n-NP去除率随温度和时间的增加而提高,随着含水率的增加呈先增加后减小的趋势。 针对4-n-NP污染土壤热脱附修复工艺参数优化,响应面实验分析表明,当4-n-NP浓度为800 μg·kg-1时,最适宜工艺参数为温度399 ℃、停留时间20 min、含水率16%、升温速率19 ℃·min-1,在该条件下,4-n-NP降解效率可以达到99 %。
(2)土壤中4-n-NP热脱附行为可以用一级动力学和指数衰减动力学模型描述。 利用TG-FTIR和Py-GC/MS分析发现,热脱附过程产生酚类、烷烃和烯烃等气相产物,推测4-n-NP可能通过脱烷基、氧化、异构化等反应转化为CO2、H2O、3,5-二甲基-3-己醇、苯甲酸丙酯等。
[1] LA MERRILL M A, VANDENBERG L N, SMITH M T, et al.Consensus on the key characteristics of endocrine-disrupting chemicals as a basis for hazard identification[J]. Nature Reviews Endocrinology, 2020, 16(1): 45-57
[2] EVE L, FERVERS B, LE ROMANCER M, et al. Exposure to endocrine disrupting chemicals and risk of breast cancer[J]. International Journal of Molecular Sciences, 2020, 21(23): 9139
[3] KWAK J I, MOON J, KIM D, et al. Species sensitivity distributions for nonylphenol to estimate soil hazardous concentration[J]. Environmental Science & Technology, 2017, 51(23):13957-13966
[4] XU Y, SUN M, XU Y, et al. Nonylphenol exposure affects mouse oocyte quality by inducing spindle defects and mitochondriadysfunction [J].Environmental Pollution,2020,266: 114967
[5] Canadian Council of Ministers of the Environment (CCME). A protocol for the derivation of environmental and human health soil quality guidelines[M]. Ottawa: Canadian Council of Ministers of the Environment, 2006
[6] 杨清伟, 梅晓杏, 孙姣霞, 等. 典型环境内分泌干扰物的来源、环境分布和主要环境过程[J]. 生态毒理学报, 2018, 13(3): 42-55 YANG Qingwei, MEI Xiaoxing, SUN Jiaoxia, et al. Sources,distribution and major transformation process of typical endocrine disruptors in the environment[J]. Asian Journal of Ecotoxicology, 2018, 13(3): 42-55(in Chinese)
[7] METCALFE C D, BAYEN S, DESROSIERS M, et al. An introduction to the sources, fate, occurrence and effects of endocrine disrupting chemicals released into the environment[J]. Environmental Research, 2022, 207: 112658
[8] SHAN J, CORVINI P F, SCHÄFFER A, et al. Influence of the geophagous earthworm Aporrectodea sp. on fate of bisphenol A and a branched 4-nonylphenol isomer in soil[J]. Science of the Total Environment, 2019, 693: 133574
[9] SHI G, HU J, CHENG Y, et al. Pseudomonas aeruginosa improved the phytoremediation efficiency of ryegrass on nonylphenol-cadmium co-contaminated soil[J]. Environmental Science and Pollution Research International,2023,30 ( 10 ):28247-28258
[10] GUEDES P, MATEUS E P, COUTO N, et al. Electrokinetic remediation of six emerging organic contaminants from soil[J].Chemosphere, 2014, 117: 124-131
[11] SANG Y, YU W, HE L, et al. Sustainable remediation of lube oil-contaminated soil by low temperature indirect thermal desorption: Removal behaviors of contaminants, physicochemical properties change and microbial community recolonization in soils[J]. Environmental Pollution, 2021, 287: 117599
[12] TOPP E, STARRATT A. Rapid mineralization of the endocrinedisrupting chemical 4-nonylphenol in soil[J]. Environmental Toxicology and Chemistry, 2000, 19(2): 313-318
[13] 于天, 陈春红, 徐成华, 等. 基于碳数分段法的石油烃污染土壤异位热脱附工艺的优化[J]. 环境工程学报, 2021, 15(6): 1988-1999 YU Tian, CHEN Chunhong, XU Chenghua, et al. Optimization of ex-situ thermal desorption of petroleum hydrocarbon contaminated soil based on carbon number-based fraction approach[J].Chinese Journal of Environmental Engineering, 2021, 15(6):1988-1999(in Chinese)
[14] LI J, ZHENG F, LI Q, et al. Effects of inherent minerals on oily sludge pyrolysis: Kinetics, products, and secondary pollutants[J]. Chemical Engineering Journal, 2022, 431: 133218
[15] ZHANG W, LI X, SHEN J, et al. Insights into the degradation process of phenol during in situ thermal desorption: The overlooked oxidation of hydroxyl radicals from oxygenation of reduced Fe-bearing clay minerals[J]. Journal of Hazardous Materials,2023, 444: 130401
[16] LI D, XU W, MU Y, et al. Remediation of petroleum-contaminated soil and simultaneous recovery of oil by fast pyrolysis[J].Environmental Science &Technology,2018,52 ( 9 ):5330-5338
[17] DAVIS R J, LILJESTRAND H M, KATZ L E. Evidence for multiple removal pathways in low-temperature (200—400 ℃) thermal treatment of pentachlorophenol-laden soils[J]. Journal of Hazardous Materials, 2020, 400: 122870
[18] ZHANG X, MIAO Z, WAN L. Human action categories using motion descriptors[C]/ /2012 19th IEEE International Conference on Image Processing. Orlando, FL, USA. IEEE, 2012:1381-1384
[19] WU L, WU H, QIU S, et al. Insights into removal efficiency and mechanism of microwave remediation of soils contaminated with polyaromatic hydrocarbons of low molecular weight assisted by bluecoke-basedconditioner [J].Chemosphere,2022,301: 134647
[20] FEENEY R J, NICOTRI P J, JANKE D. Overview of thermal desorption technology [R]. 1998, Doi:10.21236/ada352083
[21] BAI S, QI Z, LIU J, et al. Effect of carrier gas flow rate in thermal desorption process of PCBs contaminated soil[J]. Advanced Materials Research, 2014, 878: 731-738
[22] CHEN F, CHEFETZ B, THOMPSON M L. Comparison of adsorption behaviors of selected endocrine-disrupting compounds in soil [J].Journal of Environmental Quality, 2021, 50(3): 756-767
[23] KITHOME M, PAUL J W, LAVKULICH L M, et al. Kinetics of ammonium adsorption and desorption by the natural zeolite clinoptilolite[J]. Soil Science Society of America Journal, 1998,62(3): 622-629
[24] LI T T, SONG F, ZHANG J, et al. Pyrolysis characteristics of soil humic substances using TG-FTIR-MS combined with kinetic models [J].ScienceoftheTotalEnvironment, 2020,698: 134237
[25] MIAO W, LI X, WANG Y, et al. Pyrolysis characteristics of oilfield sludge and the comparison of kinetic analysis with two representative methods[J]. Journal of Petroleum Science and Engineering, 2019, 182: 106309
[26] ZHONG M, HUANG H, XU P, et al. Catalysis of minerals in pyrolysis experiments[J]. Minerals, 2023, 13(4): 515
[27] LIU Y, SUN Z, JI L, et al. Systematic study on dynamic pyrolysis behaviors, products, and mechanisms of weathered petroleumcontaminated soil with Fe2 O3[J]. Science of the Total Environment, 2022, 834: 155197
[28] KIM J Y, MOON J, LEE J H, et al. Conversion of phenol intermediates into aromatic hydrocarbons over various zeolites during lignin pyrolysis[J]. Fuel, 2020, 279: 118484
[29] CHEN Y, SHI R, HU Y, et al. Alkali-thermal activated persulfate treatment of tetrabromobisphenol A in soil: Parameter optimization, mechanism, degradation pathway and toxicity evaluation[J]. Science of the Total Environment, 2023, 903: 166477
[30] YUAN X, LI T, HE Y, et al. Degradation of TBBPA by nZVI activated persulfate in soil systems[J]. Chemosphere, 2021,284: 131166
[31] ODEN C P, WERTH C J, KIENZLE B A, et al. Impact of organic matter on transformation during thermal remediation of pyrene-contaminated substrates[J]. Science of the Total Environment, 2024, 906: 167569
[32] YAN Y, XU J, LIU S, et al. Reactive force-field MD simulation on the pyrolysis process of phenolic with various cross-linked and branched structures[J]. Chemical Engineering Science, 2023,272: 118606
[33] DHAR A, VEKARIYA R L, SHARMA P. Kinetics and mechanistic study of n-alkane hydroisomerization reaction on Pt-doped γ-alumina catalyst[J]. Petroleum, 2017, 3(4):489-495
[34] ALEXANDER R, BERWICK L, PIERCE K. Single carbon surface reactions of 1-octadecene and 2, 3, 6-trimethylphenol on activated carbon: Implications for methane formation in sediments[J]. Organic Geochemistry, 2011, 42(5): 540-547