催化裂化是现代石油炼制过程中的核心技术之一,能够将重质烃类高效转化为汽油、柴油和丙烯等高附加值轻质馏分。在流化催化裂化(FCC)过程中,Y型分子筛作为催化剂的关键活性组分,凭借其良好的水热稳定性、可调酸性以及优异的催化性能,广泛应用于工业装置中[1,2]。
然而,在长期运行过程中,催化剂常受到金属污染物的影响,尤其是铁的沉积会显著加速其失活。铁在催化剂表面沉积后易形成致密的壳层,其厚度通常为1~2 μm,主要富集Fe、Ni和Si等杂质元素[3-5]。该壳层会堵塞催化剂孔道,阻碍反应物分子扩散至活性位点,不仅导致重油转化率下降、油浆产率增加、产品选择性变差,还可能引起催化剂流化性能恶化,给工业装置的长周期稳定运行带来严重挑战[6,7]。
研究表明,污染铁在催化裂化催化剂表面主要以磁赤铁矿(γ-Fe2O3)的形式存在,并且根据粒径的不同表现出铁磁性与超顺磁性(粒径<30 nm)。在FCC反应阶段中,来自FCC催化剂原料高岭土中的结构铁Fe(Ⅲ)还原为Fe(Ⅱ);来自原料油与炼油设备的游离铁主要转化为γ-Fe2O3。在FCC再生阶段中,部分Fe(Ⅱ)被氧化回Fe(Ⅲ),但FCC的氧化环境不足以氧化全部Fe(Ⅱ),导致其部分残留;γ-Fe2O3在完全燃烧条件下更容易使铁磁性γ-Fe2O3形成更小颗粒的超顺磁性γ-Fe2O3,在部分燃烧条件下促进铁磁性γ-Fe2O3向更大颗粒生长[8]。铁的沉积会导致催化剂颗粒变大,表现为胶体铁在外表面堆积或有机铁渗透到基质中,铁在基质内多呈还原态,而表面则多为氧化态[9]。Fe2+较Fe3+具有更高的迁移活性,但在接近分子筛位置后渗透受阻,导致铁在颗粒表面聚集。这种沉积不仅会堵塞分子筛孔道,抑制酸性位点,还可能改变酸性强度和分布,从而降低催化活性和选择性[10]。
γ-Fe2O3是一种具有高磁化率的热力学亚稳态结构的铁氧化物,其在高温下容易发生相变,转化为热力学更稳定但磁化率几乎为零的α-Fe2O3相。据文献报道[11,12],当处理温度超过450 ℃时,γ-Fe2O3纳米粒子会发生相变,转变为非磁性α-Fe2O3相,掺杂不同元素(如Zn、Cu、Co、Ni、Mn)可进一步提高相变温度。例如,掺杂1%Zn使γ-Fe2O3到α-Fe2O3的相变温度从532 ℃提升至640 ℃;掺杂0.89%Mn后,相变温度达到601 ℃。但关于铁在催化剂中具体的作用机理,尤其是γ-Fe2O3与分子筛之间的相互作用机制,仍存在较大的研究空白。为此,深入探索铁在FCC催化剂中的影响机理,尤其是其与分子筛的相互作用,对于理解催化剂的失活过程和铁中毒的抑制机制至关重要,也有助于开发具有更强抗铁中毒能力的催化剂。
本研究旨在通过差热分析(DTA)、X射线衍射(XRD)、比表面积和孔径分析(BET)、傅里叶红外光谱(FTIR)等多种表征手段,系统分析γ-Fe2O3分子筛之间的相互作用。通过这些多维度的表征方法,揭示铁中毒对催化剂结构及性能的影响,为解决FCC催化剂的铁中毒问题提供理论支持,并为抗铁中毒催化剂的设计提供新的研究视角。本研究明确了γ-Fe2O3在分子筛调控下的相变行为及其对磁化率的影响机制,进一步揭示了α-Fe2O3对分子筛骨架结构和热稳定性的破坏路径,填补了高温条件下不同铁物种与分子筛协同演化机制的研究空白。
1 实验部分
1.1 试剂与原料
实验所用原料包括Y型分子筛(中国石化催化剂齐鲁分公司)、γ-Fe2O3(粒径10 nm,购自Adamas公司,质量分数≥99%)、α-Fe2O3(粒径10 nm,购自Adamas公司,质量分数≥99%)。
1.2 催化材料的掺混
用Y型分子筛分别和γ-Fe2O3、α-Fe2O3进行掺混,为了确保铁相在分子筛中的均匀分布,实验采用了分步混合法。以掺混量为20 mg·g-1 Fe的分子筛样品为例,具体操作如下:精确称取40 g分子筛(干基质量),将其置于研钵中备用;精确称量1.194 g γ-Fe2O3,将其分次缓慢加入分子筛中;每次加入少量γ-Fe2O3后,使用研钵手动搅拌均匀,确保两者充分混合直至分散均匀;重复上述步骤,制备不同掺混量的催化材料样品。
将γ-Fe2O3与分子筛的掺混样品称为γ-Fe2O3掺混样(γ-Fe2O3-Zeolite Y),α-Fe2O3与分子筛的掺混样品称为α-Fe2O3掺混样(α-Fe2O3-Zeolite Y),将未经掺混处理的γ-Fe2O3与Y型分子筛分别称为γ-Fe2O3(γ-Fe2O3)与分子筛空白样(Zeolite Y)。由于γ-Fe2O3空白样的铁含量较高,因此在不同温度焙烧后再通过掺入石英砂稀释铁含量后再进行磁化率测量。将γ-Fe2O3空焙烧后与石英砂的掺混样品称为石英砂掺混样(γ-Fe2O3-SiO2)。
为了考察焙烧温度对掺混样品的影响,将制备好的混合样品分别在500、600、700、800、900和1 000 ℃于马弗炉中焙烧4 h,焙烧后在马弗炉中自然冷却至室温,并对所得样品进行密封保存,避免环境湿度和氧化对样品的影响。
1.3 催化材料的表征
利用英国Bartington MS3磁化率仪配MS2B传感器测量样品磁化率,精度达2×10-6 SI,并通过空白校准和3次重复测量确保结果准确可靠;使用德国西门子D5005型X射线衍射仪测定焙烧前后γ-Fe2O3的相变,扫描范围为5°~70°,步宽为0.016 7°;采用美国Micromeritics DIGISORB2500型吸附仪通过BET方法测定分子筛的比表面积、孔体积及孔径大小;采用日本Shimadzu DTG-60/60H热分析仪在空气氛中测定分子筛的崩塌温度,升温速率为10 ℃·min-1,温度区间为室温至1 200 ℃;通过德国Bruker Tensor27型红外光谱仪分析分子筛羟基情况,扫描范围为4 000~400 cm-1,分辨率4 cm-1;采用德国Bruker AVANCE Ⅲ 600WB核磁共振波谱仪测试分子筛29Si NMR,设置共振频率156.4 MHz,样品旋转速率10 kHz,确保谱图准确可靠。
2 结果与讨论
2.1 高温条件下分子筛对γ-Fe2O3相变的影响规律
2.1.1 磁化率
样品磁化率是对其中磁性物质的反映,分子筛的磁化率为0,而γ-Fe2O3具有较高的磁化率,所以掺混样品的磁化率可以反映出其中铁相的变化情况[13]。对γ-Fe2O3空白样及γ-Fe2O3掺混样品在焙烧前后进行磁化率测量,每次测量取样6 g,测量3次后取平均值作为最后结果。结果如图1所示,γ-Fe2O3空白样品在500 ℃焙烧后,铁含量为20 mg·g-1的石英砂掺混样品磁化率从12.03 27×10-3下降到了2.932 02×10-3,下降幅度为75.63%,而在600 ℃焙烧后,样品磁化率降至3.12×10-4,下降幅度为97.41%,在700 ℃焙烧后样品磁化率降到了0附近;而不同的是,γ-Fe2O3掺混样品在500 ℃焙烧后磁化率虽然也有下降,但铁含量为20 mg·g-1的掺混样品磁化率从11.985 33×10-3降到了8.558 785× 10-3,降幅仅为28.59%,在600 ℃焙烧后,掺混样品磁化率为3.945 6×10-3,降幅为67.08%,700 ℃焙烧后,样品磁化率降到0附近。
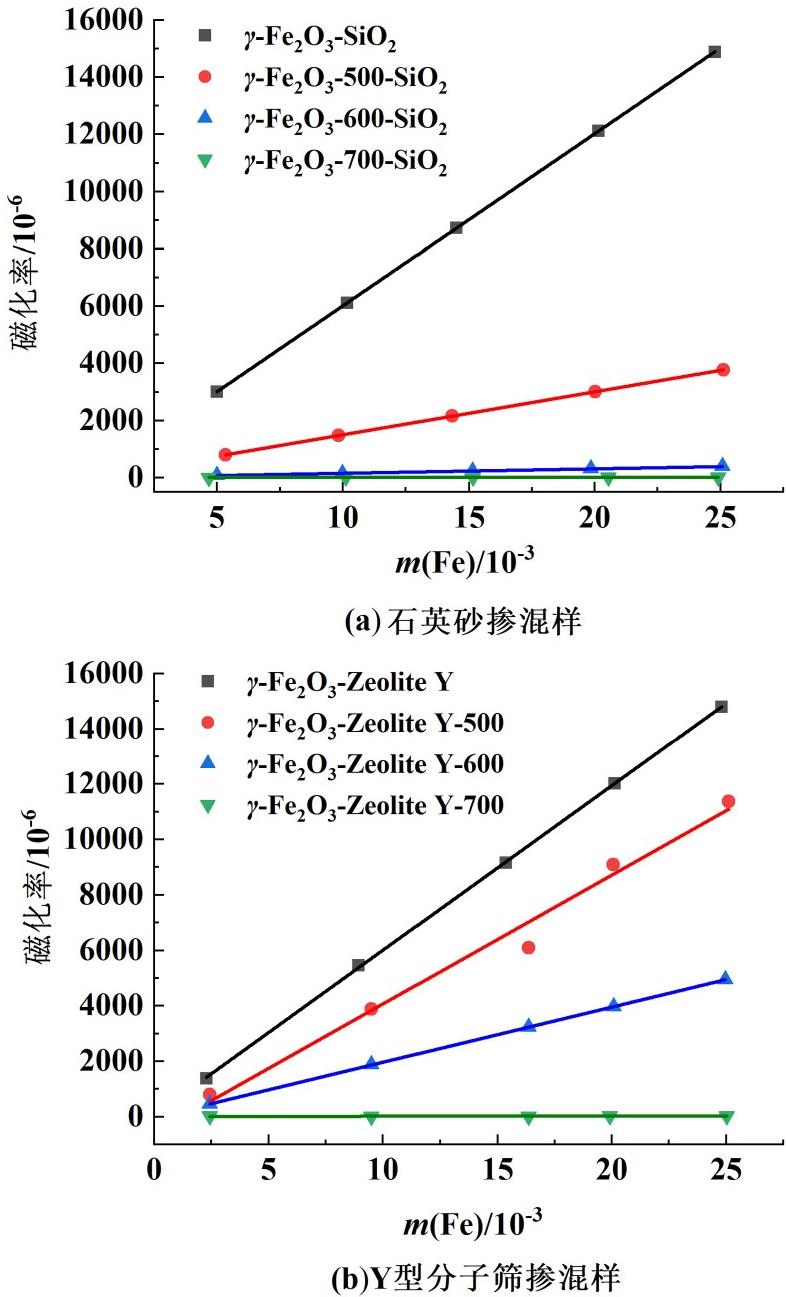
图1 样品不同温度焙烧后的磁化率测量
Fig.1 Magnetic susceptibility measurement of samples after calcination at different temperatures
综上所述,样品的磁化率能够有效反映其中磁性物质的变化情况,并与铁的含量呈现良好的线性关系。通过对γ-Fe2O3空白样品及其与γ-Fe2O3掺混样品在不同温度下的焙烧实验发现,随着焙烧温度的升高,石英砂掺混样品的磁化率显著下降,表明其中γ-Fe2O3相变为了磁化率较低的物质。在相同焙烧条件下,γ-Fe2O3掺混样品的磁化率下降幅度明显小于石英砂掺混样品,说明分子筛可能与γ-Fe2O3发生相互作用,从而抑制其相变进程,减缓磁化率的下降趋势。
2.1.2 XRD
为了研究样品焙烧后磁化率变化的原因,对γ-Fe2O3空白样及铁含量为20 mg·g-1的γ-Fe2O3掺混样品进行XRD表征,观察铁相的变化情况。图2展示了不同样品在焙烧前后XRD谱图的对比。
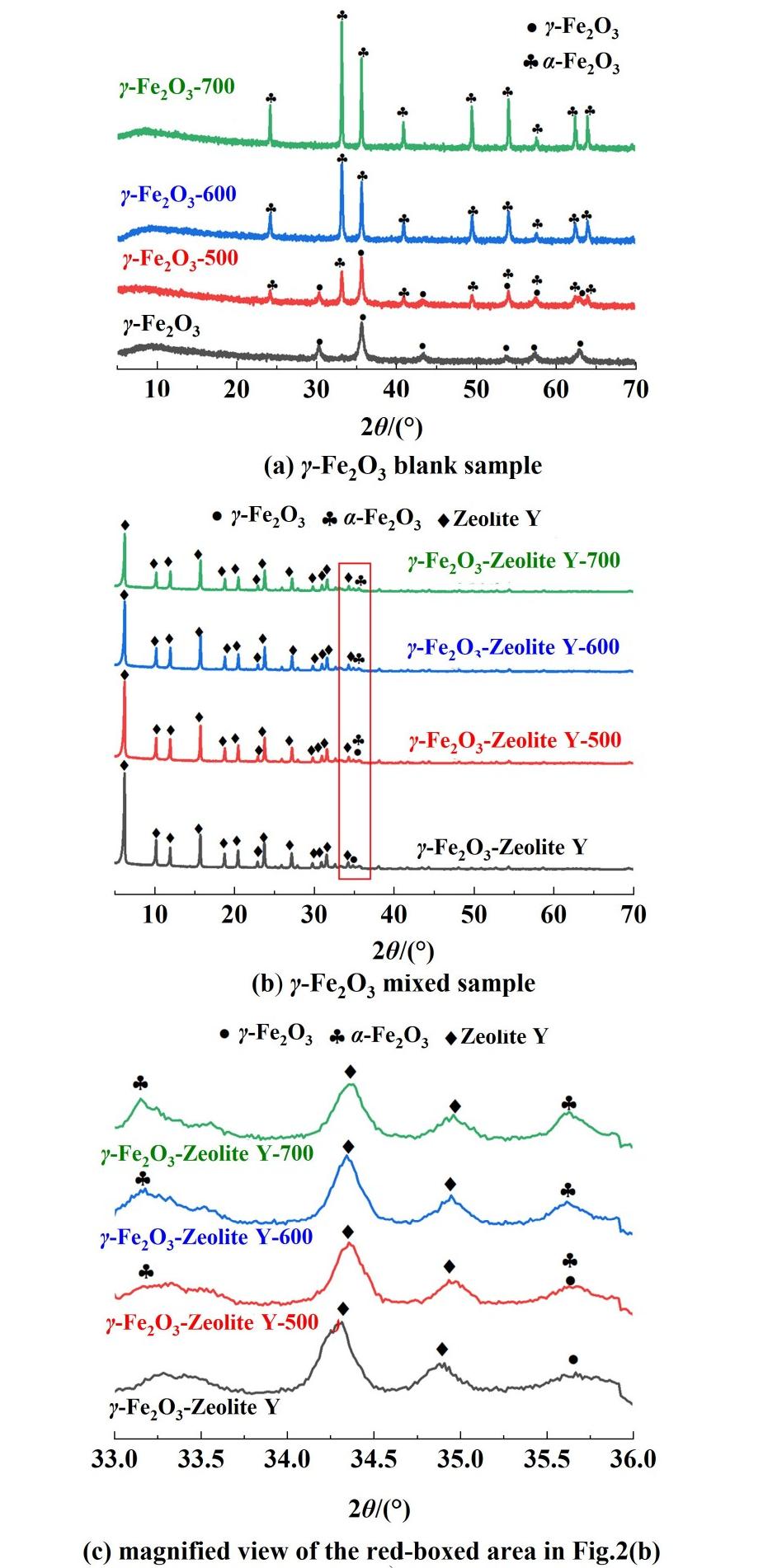
图2 样品不同温度焙烧后的XRD谱图
Fig.2 XRD patterns of samples after calcination at different temperatures
γ-Fe2O3空白样在500 ℃焙烧后,其特征衍射峰强度显著降低,并伴随α-Fe2O3的衍射峰出现,表明部分γ-Fe2O3相变为α-Fe2O3。在600与700 ℃焙烧后,γ-Fe2O3的衍射峰完全消失,仅剩α-Fe2O3的衍射峰,表明γ-Fe2O3完全转变为α-Fe2O3。γ-Fe2O3掺混样品的行为略有不同。在500 ℃焙烧后,分子筛衍射峰保持稳定,同时出现了α-Fe2O3的衍射峰,表明样品中部分γ-Fe2O3转化为了α-Fe2O3。600 ℃焙烧后,α-Fe2O3的衍射峰强度增大,而γ-Fe2O3的衍射峰强度减小。在700 ℃焙烧后,分子筛的衍射峰依然保持稳定,而γ-Fe2O3的衍射峰完全消失,表明此温度下γ-Fe2O3发生了完全相变。
γ-Fe2O3和α-Fe2O3具有显著不同的磁化率特征:前者具有较高磁化率,而后者几乎为0。结合前述实验数据可知,掺混样品在不同焙烧温度下磁化率的变化反映了γ-Fe2O3逐步向α-Fe2O3转变的过程。在500 ℃下,铁含量为20 mg·g-1的掺混样品磁化率仅下降了28.59%,说明γ-Fe2O3仅发生了部分相变;而600 ℃下磁化率下降幅度达67.08%,表明相变程度明显增强;至700 ℃时,磁化率降至接近0,反映出γ-Fe2O3已基本转变为α-Fe2O3。相比之下,γ-Fe2O3空白样在相同温度条件下磁化率下降更为剧烈,表明分子筛的存在有效延缓了γ-Fe2O3的相变进程,从而对其磁性保持起到了抑制高温相变的作用。
2.1.3 FTIR
文献报道[14]γ-Fe2O3与γ-Al2O3具有强相互作用,两者会通过羟基相互作用,导致γ-Fe2O3相变温度升高,γ-Fe2O3与分子筛可能也会通过这种方式相互作用,所以利用傅里叶红外光谱对分子筛空白样与铁含量为20 mg·g-1的γ-Fe2O3掺混样品进行表征,区分不同类型羟基的位置和性质。根据文献报道[15],桥接羟基(B酸羟基,Si—OH—Al)的特征吸收峰通常在3 600~3 650 cm-1处,位于框架中的铝原子附近(Si—O—Al桥键上),酸性较强,是B酸的主要来源;自由羟基(Si—OH),位于分子筛外表面或孔道终端的硅醇基团,红外特征吸收峰在3 740~3 750 cm-1处,酸性较弱,因为它不与铝原子配位,也不参与B酸中心的形成,它的化学环境较为孤立,通常不参与强酸催化反应;弱酸性羟基,主要分布在苏打笼中,与框架氧原子(如Si—O—Al)相连的羟基,红外特征吸收峰在3 530~3 580 cm-1处,酸性较弱,相比桥接羟基活性稍低。
γ-Fe2O3掺混样与分子筛空白样的FTIR谱图如图3所示,在500 ℃焙烧后,γ-Fe2O3掺混样品的3 550 cm-1处的弱酸羟基与3 625 cm-1处的桥接羟基的吸收峰明显比分子筛空白样品的要低,这表明在焙烧后γ-Fe2O3与分子筛的羟基发生了相互作用。样品700 ℃焙烧后,3 625 cm-1处的桥接羟基与3 550 cm-1处的弱酸羟基消失,在3 520~3 650 cm-1处出现了1个大峰,可能是因为高温焙烧会导致分子筛框架中部分铝原子迁移或流失,产生非骨架铝和结构缺失,桥连羟基(Si—OH—Al)减少,使其在红外光谱中表现为更宽、更强的吸收峰。3 740 cm-1处吸收峰的增强主要与焙烧温度升高导致的脱水作用及框架缺陷相关。框架缺陷的增多引入了更多的自由羟基(如Al—OH或Si—OH),导致3 740 cm-1附近的吸收增强。
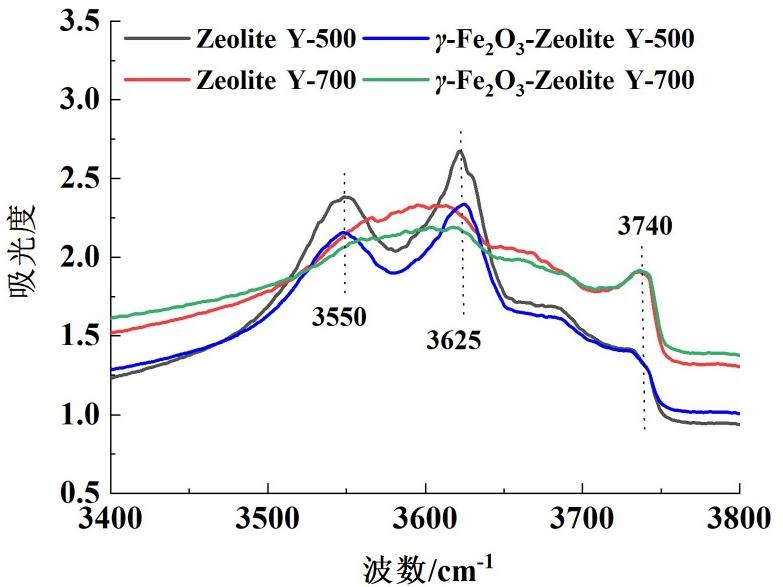
图3 不同焙烧温度下γ-Fe2O3掺混样与分子筛空白样的FTIR谱图
Fig.3 FTIR spectra of γ-Fe2O3 mixed samples and Y-type zeolite blanks after calcination at various temperatures
文献报道[16,17,18],γ-Fe2O3相变过程中会发生聚集,减少比表面积从而降低表面自由能,而FTIR结果表明,γ-Fe2O3与Y型分子筛会通过羟基相互作用,阻止了γ-Fe2O3的聚集,导致其相变温度升高,同时分子筛本身羟基减少,酸性受损。
2.1.4 29Si NMR
本研究采用29Si固态核磁共振(NMR)进行表征。相比于27Al NMR,29Si NMR能够直接提供Si(2Al)、Si(1Al)和Si(0Al)等不同配位Si的化学位移信息,同时也有助于分析骨架铝的脱除过程。对分子筛空白样品以及铁含量为20 mg·g-1的γ-Fe2O3掺混样品进行29Si NMR表征,观察样品焙烧前后Y型分子筛中Si的配位环境是否发生变化。结果如图4所示,Y型分子筛中存在化学位移为-95、-101以及-106处的共振吸收峰,分别归属于Si(2Al)、Si(1Al)、Si(0Al)[19,20]。经过500 ℃焙烧后,发现γ-Fe2O3掺混样品的3个共振吸收峰强度比空白样品的要强,并且化学位移在-50和-152出现了振荡峰,以及在-157处出现了新的共振吸收峰,此处结果与FTIR结果相对应,表明掺混样品中的γ-Fe2O3通过羟基与分子筛相互作用后,改变了分子筛中Si的配位环境。
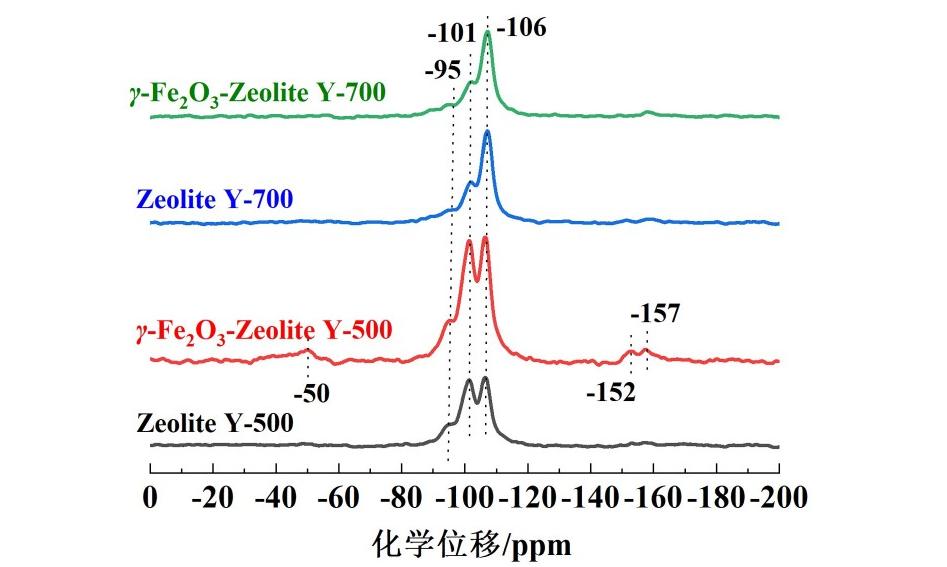
图4 不同焙烧温度下γ-Fe2O3掺混样与分子筛空白样的29Si NMR谱图
Fig.4 29Si NMR spectra of γ-Fe2O3 mixed samples and zeolite blank samples after calcination at different temperatures
分子筛空白样品与γ-Fe2O3掺混样品在经过700 ℃焙烧后,发现Si(2Al)与Si(1Al)的共振吸收峰强度相较于500 ℃焙烧后的样品明显降低,Si(0Al)的共振吸收峰增强,表明随着焙烧温度的升高,分子筛中骨架铝发生脱除,导致Si(0Al)含量增多[21,22]。
2.2 α-Fe2O3对分子筛热稳定性的影响
2.2.1 DTA
由于γ-Fe2O3在700 ℃之前已完全转化为α-Fe2O3,因此对铁含量为20 mg·g-1的α-Fe2O3掺混样品和分子筛空白样进行了差热分析(DTA)表征,以研究在高温条件下α-Fe2O3与分子筛之间的相互作用。结果如图5所示,2条曲线中均观察到1个显著的放热峰,这与分子筛结构崩塌密切相关。随着温度升高,分子筛空白样在1 040 ℃出现放热峰,而掺混样品的分子筛崩塌温度则降低至975 ℃,比空白样低了65 ℃。这一结果表明,α-Fe2O3能够与分子筛发生显著的相互作用,削弱分子筛骨架的热稳定性,从而使分子筛崩塌温度降低。
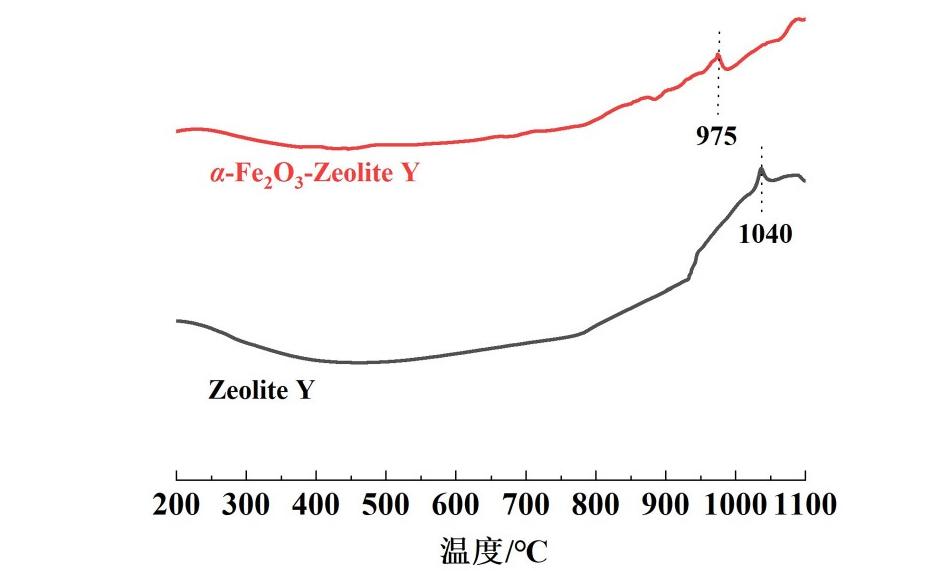
图5 γ-Fe2O3掺混样与分子筛空白样的DTA分析
Fig.5 DTA analysis of α-Fe2O3 mixed samples and zeolite blank samples
α-Fe2O3在高温下可能通过界面应力、骨架元素迁移等多重作用机制破坏分子筛的晶体结构,从而导致其结晶度下降。
2.2.2 结晶度与XRD
对分子筛空白样与铁含量为20 mg·g-1的α-Fe2O3掺混分子筛样品在800、900和1 000 ℃焙烧后进行了XRD结晶度与物相的表征,结晶度结果如图6所示,800℃焙烧后,α-Fe2O3掺混分子筛样品的结晶度为59.9%,低于空白样的73.3%,表明α-Fe2O3对分子筛的结晶度有一定破坏作用。900 ℃焙烧后,α-Fe2O3掺混样品的结晶度进一步下降至4.4%,相比之下,空白样的结晶度仍维持在64%。而1 000 ℃焙烧后,2种样品的结晶度均完全损失,表明分子筛框架在高温下彻底崩塌。
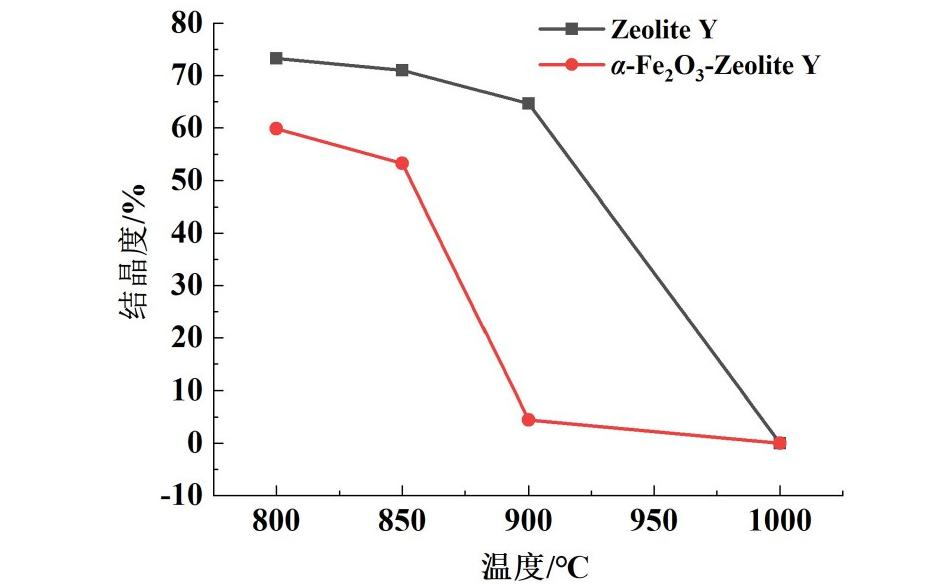
图6 γ-Fe2O3掺混样与分子筛空白样的分子筛结晶度
Fig.6 Crystallinity of zeolites in α-Fe2O3 mixed samples and zeolite blank samples
样品物相结果如图7所示,800~850 ℃焙烧后,2种样品均显示明显的分子筛特征衍射峰,表明此温度范围内分子筛框架结构基本保持完整。900 ℃焙烧后,分子筛空白样中的分子筛衍射峰仍比较明显;而α-Fe2O3掺混样品的衍射峰显著衰减,仅保留少部分衍射峰,该结果与XRD结晶度结果一致,表明在此温度下α-Fe2O3会导致分子筛框架发生严重崩塌。1 000 ℃焙烧后,2种样品中的分子筛衍射峰消失,并且分子筛样品中均出现硅线石(Al2SiO5)的衍射峰,表明分子筛框架在高温下完全失稳,并伴随硅铝组分的重排形成新相[23]。硅线石的生成可能源于高温条件下分子筛骨架硅氧四面体与铝氧八面体的部分分离和重新排列,该组分是低活性、低比表面的组分,可能对铁中毒催化裂化催化剂表面壳层的形成具有直接作用[24,25]。
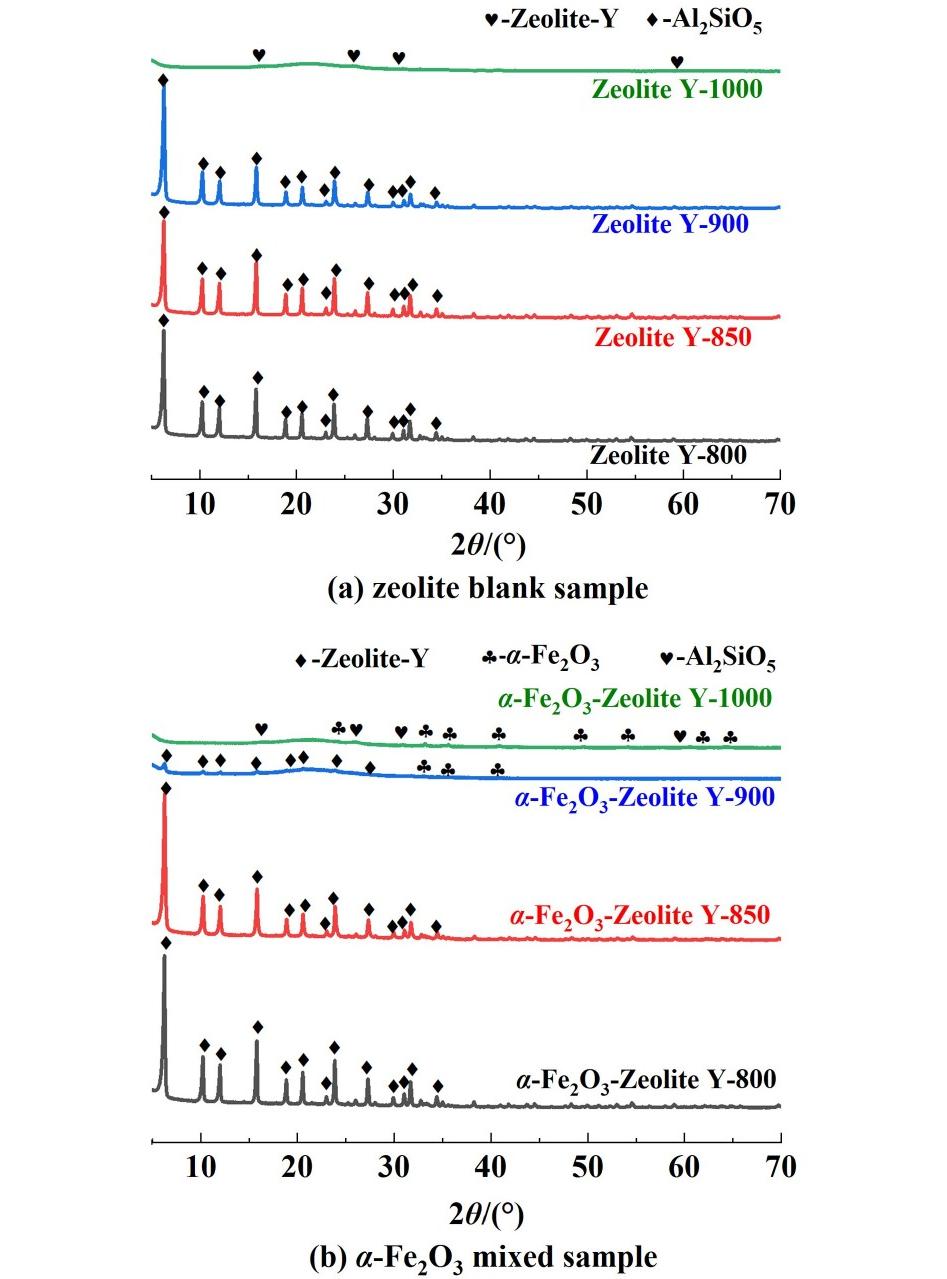
图7 不同温度焙烧下分子筛空白样与α-Fe2O3掺混样的XRD物相谱图
Fig.7 XRD phase patterns of zeolite blank and α-Fe2O3 mixed samples after calcination at different temperatures
2.2.3 BET
对分子筛空白样品与铁含量为20 mg·g-1的α-Fe2O3掺混样品分别进行BET表征,以研究不同温度下α-Fe2O3对分子筛孔结构的影响。结果如图8所示,800与850 ℃焙烧后,α-Fe2O3掺混样品的比表面积和孔体积均略低于空白样,显示铁氧化物的引入对分子筛的孔结构已有一定负面影响,但分子筛框架的主要结构尚未显著受损。900 ℃焙烧后,分子筛空白样品的比表面积和孔体积分别为586.56和0.24 cm3·g-1;α-Fe2O3掺混样品的比表面积为26.00 m2·g-1,孔体积为0.01 cm3·g-1,与空白样品相比,比表面积和孔体积大幅减少,这与其在900 ℃焙烧后分子筛结晶度完全损失的结果一致。1 000 ℃焙烧后,2种样品的比表面积和孔体积均接近于0,表明分子筛框架在高温下已完全坍塌,孔道结构彻底破坏。
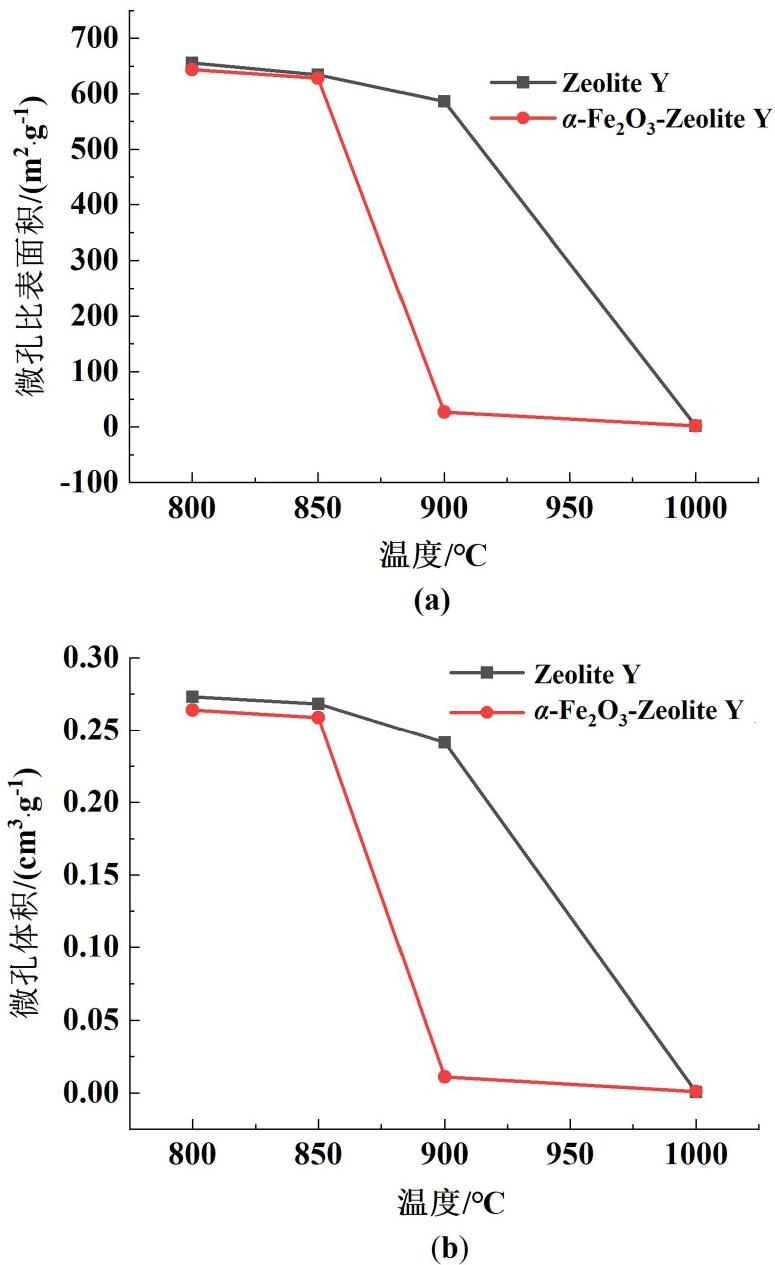
图8 不同温度下α-Fe2O3对分子筛(a)微孔比表面积与(b)微孔体积的影响
Fig.8 Effect of α-Fe2O3 on (a) the microporous specific surface area and (b) micropore volume of zeolites at different calcination temperatures
实验结果表明,α-Fe2O3的引入显著降低了Y型分子筛的热稳定性,导致其在高温条件下结晶度下降、比表面积和孔体积减小。比表面积和孔体积的大幅减少显著削弱了分子筛对反应物分子的吸附和扩散能力,降低了催化剂的活性。孔道坍塌导致酸性功能位点暴露度降低,进而影响重油分子的活化效率,削弱催化裂化反应性能。孔结构的破坏可能导致反应路径改变,轻质油品(如汽油和柴油)的产率下降,同时增加焦炭的生成倾向。
3 结论
(1) γ-Fe2O3的相变行为受到Y型分子筛显著调控。在高温条件下,γ-Fe2O3逐步转变为α-Fe2O3,伴随磁化率下降。但在Y型分子筛存在下,其相变温度显著提高,磁化率下降趋势减缓。这主要归因于分子筛通过桥接羟基和弱酸性羟基与γ-Fe2O3发生相互作用,抑制了颗粒聚集与相变。
(2) γ-Fe2O3与分子筛的相互作用对骨架结构与酸性中心造成影响。上述相互作用改变了分子筛中Si的配位环境,导致骨架羟基减少、酸性中心流失,并生成自由羟基,从而对分子筛的酸性和催化活性造成一定程度的负面影响。
(3) α-Fe2O3的形成加剧了分子筛骨架的崩塌。α-Fe2O3显著降低分子筛的热稳定性,使其崩塌温度从1 040 ℃下降至975 ℃。随着焙烧温度的升高,α-Fe2O3对分子筛骨架的破坏作用逐渐增强。在900 ℃焙烧后,α-Fe2O3掺混样的分子筛结晶度降至4.4%,微孔比表面积和孔体积几乎完全损失,而分子筛空白样仍保留较高的结晶度和孔结构。这表明α-Fe2O3的形成进一步加剧了分子筛框架的坍塌,导致微孔结构严重受损,从而对催化剂性能产生深远影响。
(4) 分子筛结构破坏对催化剂性能产生不利影响。首先,分子筛结构的崩塌造成比表面积和孔体积的急剧下降,使得催化剂的有效活性位点大幅减少,从而削弱了催化剂的裂化能力。其次,酸性中心的流失降低了催化剂的酸性强度,不仅影响碳氢化合物的活化,还可能改变催化反应路径,降低目标产物的选择性。此外,孔道结构的破坏严重影响了反应物的扩散和产物的脱除,导致催化剂更易积炭,加速催化剂的失活。
(5) 未来研究展望。本研究表明,铁源种类和相变行为对分子筛结构稳定性及催化性能具有深远影响。未来研究可从以下方向入手以提升催化剂的抗铁中毒能力:开发可与铁物种形成稳定络合物或包覆层的助剂,从而抑制其对分子筛的侵蚀;构建具备更强铁容忍能力的新型分子筛骨架结构;加强对铁物种迁移行为和破坏机制的原位表征研究,为铁污染的微观调控和抗毒策略提供理论支撑。
[1] 陈俊武. 催化裂化工艺与工程[M]. 2版. 北京: 中国石化出版社, 2005
[2] CLOUGH M, POPE J C, LYNNE T X L, et al. Nanoporous materials forge a path forward to enable sustainable growth: Technology advancements in fluid catalytic cracking[J]. Microporous and Mesoporous Materials, 2017, 254: 45-58
[3] 石磊, 毕林田, 姚远. 铁对催化裂化催化剂的影响[J]. 齐鲁石油化工, 2012, 40(1): 50-53
SHI Lei, BI Lintian, YAO Yuan. Influence of iron on catalytic cracking catalyst[J]. Qilu Petrochemical Technology, 2012, 40(1): 50-53(in Chinese)
[4] 李雪礼, 侯硕旻, 王启飞, 等. 催化裂化催化剂铁污染研究进展[J]. 工业催化, 2020, 28(6): 1-6
LI Xueli, HOU Shuomin, WANG Qifei, et al. Research progress of the iron contamination on the catalytic cracking catalysts[J].Industrial Catalysis, 2020, 28(6): 1-6(in Chinese)
[5] KRUMEICH F, IHLI J, SHU Y, et al. Structural changes in deactivated fluid catalytic cracking catalysts determined by electron microscopy[J]. ACS Catalysis, 2018, 8(5): 4591-4599
[6] 刘倩倩, 达志坚, 吕令玮, 等. 催化裂化催化剂铁中毒问题剖析[J]. 石油炼制与化工, 2022, 53(5): 1-6
LIU Qianqian, DA Zhijian, LÜ Lingwei, et al. Analysis on iron poisoning of FCC catalyst[J]. Petroleum Processing and Petrochemicals, 2022, 53(5): 1-6(in Chinese)
[7] ARAKAWA S, TESHIMA K, WATABE M. Effect of iron compound accumulation on apparent bulk density and catalyst activity of FCC catalyst[J]. Journal of the Japan Petroleum Institute, 2011, 54(4): 258-265
[8] SOUZA N L A, PANIAGO R, ARDISSON J D, et al. Iron contamination of FCC catalysts: Quantification of different crystalline phases and valence states[J]. Applied Catalysis A: General, 2019, 569: 57-65
[9] IHLI D J, FERREIRA SANCHEZ D D, et al. Localization and speciation of iron impurities within a fluid catalytic cracking catalyst[J]. Angewandte Chemie International Edition, 2017, 56(45): 14031-14035
[10] WISE A M, WEKER J N, KALIRAI S, et al. Nanoscale chemical imaging of an individual catalyst particle with soft X-ray ptychography[J]. ACS Catalysis, 2016, 6(4): 2178-2181
[11] PATI S S, HEROJIT SINGH L, MANTILLA OCHOA J C, et al.Facile approach to suppress γ transition beyond 600 ℃ in Fe3O4 nanoparticles[J]. Materials Research Express, 2015, 2(4): 045003
[12] SIDHU P S, GILKES R J, POSNER A M. The behavior of Co, Ni, Zn, Cu, Mn, and Cr in magnetite during alteration to maghemite and hematite[J]. Soil Science Society of America Journal, 1980, 44(1): 135-138
[13] 周公度, 段连运. 结构化学基础[M]. 5版. 北京: 北京大学出版社, 2017
ZHOU Gongdu, DUAN Lianyun. Fundamentals of structural chemistry[M]. 5th ed. Beijing: Peking University Press, 2017(in Chinese)
[14] ZHONG Z, PROZOROV T, FELNER I, et al. Sonochemical synthesis and characterization of iron oxide coated on submicrospherical alumina: A direct observation of interaction between i-ron oxide and alumina[J]. The Journal of Physical Chemistry B, 1999, 103(6): 947-956
[15] WARD J W. The nature of active sites on zeolites[J]. Journal of Catalysis, 1968, 11:251-258
[16] EL MENDILI Y, BARDEAU J F, RANDRIANANTOANDRO N,et al. Insights into the mechanism related to the phase transition from γ-Fe2O3 to α-Fe2O3 nanoparticles induced by thermal treatment and laser irradiation[J]. The Journal of Physical Chemistry C, 2012, 116(44): 23785-23792
[17] LEHTINEN K E J, WINDELER R S, FRIEDLANDER S K. A note on the growth of primary particles in agglomerate structures by coalescence[J]. Journal of Colloid and Interface Science,1996, 182(2): 606-608
[18] LEHTINEN K E J, ZACHARIAH M R. Effect of coalescence energy release on the temporal shape evolution of nanoparticles[J].Physical Review B, 2001, 63(20): 205402
[19] RAMESH K, JIE C, HAN Y F, et al. Synthesis, characterization, and catalytic activity of phosphorus modified H-ZSM-5 catalysts in selective ethanol dehydration[J]. Industrial & Engineering Chemistry Research, 2010, 49(9): 4080-4090
[20] DONG X, SONG Y, LIN W. A new way to enhance the coke-resistance of Mo/HZSM-5 catalyst for methane dehydroaromatization[J]. Catalysis Communications, 2007, 8(3): 539-542
[21] SHEN B, QIN Z, GAO X, et al. Desilication by alkaline treatment and increasing the silica to alumina ratio of zeolite Y[J].Chinese Journal of Catalysis, 2012, 33(1): 152-163
[22] BEYERLEIN R A, MCVICKER G B. Defect structure and acid catalysis of high silica, FAU-framework zeolites: Effects of aluminum removal and of basic metal oxide addition[M]//Fluid Catalytic Cracking V Materials and Technological Innovations. Amsterdam: Elsevier, 2001: 3-40
[23] SILAGHI M C, CHIZALLET C, SAUER J, et al. Dealumination mechanisms of zeolites and extra-framework aluminum confinement[J]. Journal of Catalysis, 2016, 339: 242-255
[24] LIU Q, PENG B, ZHOU Q, et al. Role of iron contaminants in the pathway of ultra-stable Y zeolite degradation[J]. Catalysis Science & Technology, 2022, 12(13): 4145-4156
[25] 刘倩倩.催化裂化催化剂铁中毒机理及抗铁催化剂研究[D].北京:石油化工科学研究院,2020:63-68
LIU Qianqian. The mechanism of iron contamination on FCC catalysts and the development of anti-iron contamination catalyst[D]. Beijing: Research Institute of Petroleum Processing,2020:63-68(in Chinese)