随着现代农业的发展,农药在蔬菜水果种植中的广泛应用导致农产品中农药残留问题日益突出。有机磷、拟除虫菊酯类等农药的长期摄入可能对人体造成神经毒性、内分泌干扰甚至致癌风险[1]。尽管各国制定了严格的农药残留最大限量标准[2],但传统检测方法在应对多残留、复杂基质样品时仍面临灵敏度不足、前处理步骤繁琐等挑战[3]。因此,开发高效、灵敏且环保的农药多残留检测技术,对保障食品安全和消费者健康具有重要意义。
当前,农药残留分析工作主要依托于气相色谱-质谱(GC-MS)[4]和液相色谱-质谱(LC-MS)技术[5]。然而,蔬菜水果中的色素、有机酸等基质成分会干扰检测[6]。传统前处理方法如固相萃取(SPE)存在耗时长、溶剂用量大、回收率不稳定等问题[7]。QuEChERS方法[8]因其快速高效的特点被广泛应用,但其传统吸附剂(如PSA、C18)对部分极性农药的净化效果有限,且难以兼顾多种农药的同步提取[9]。
氨基化多壁碳纳米管(NH2-MWCNTs)[10]因其独特的高比表面积、π-π共轭效应和表面氨基修饰,表现出优异的吸附性能[11]。研究表明,NH2-MWCNTs可通过氢键和静电作用选择性吸附果蔬中的干扰物(如有机酸、糖类),同时保留目标农药分子[12]。本研究将NH2-MWCNTs引入QuEChERS前处理流程,旨在解决传统方法净化效率低的问题,并结合超高效液相色谱-串联质谱(UPLC-MS/MS)的高通量、高灵敏度特性,建立一种更高效的农药多残留分析方法。
1 实验部分
1.1 主要仪器与试剂
XEVO-TQS Cronos型超高效液相色谱-质谱联用仪、0.22 μm微孔滤膜(美国Waters公司);120S型电子天平(德国赛多利斯股份公司);5910R型高速冷冻离心机(德国艾本德股份有限公司)、VORTEX3型漩涡振荡仪(德国IKA公司);强力多管型涡旋混匀仪(北京科德诺斯技术有限公司)。
38种农药残留标准品(天津阿尔塔科技有限公司);乙腈(质谱级,美国默克公司);甲酸铵、甲酸(色谱纯,美国迪马科技有限公司);氨基化多壁碳纳米管(纯度99%,直径8~20 nm,管长5~20 nm,徐州宏武新材料有限公司);无水硫酸镁、氯化钠、柠檬酸钠、柠檬酸氢二钠(分析纯,国药集团化学试剂有限公司);乙二胺-N-丙基硅烷化硅胶(美国安捷伦科技有限公司);Millipore型超纯水系统(美国Millipore公司)。
水果蔬菜样本来自于全省食品安全风险监测项目中实验室日常检测样本,样本来自于全青海省各区县中的农贸市场及超市等,包括蔬菜样品67份,水果样品36份。
1.2 实验方法
1.2.1 流动相的配制
(1)0.1%甲酸+5 mmol甲酸铵+V(水)∶V(甲醇)=98∶2,量取979 mL去离子水,加入1 mL甲酸,加入0.315 g甲酸铵,超声溶解。再加入 20 mL甲醇,超声混匀,过0.22 μm滤膜备用。
(2)0.1%甲酸+5 mmol甲酸铵+V(甲醇)∶V(水)=98∶2,量取19 mL去离子水,加入1 mL甲酸,加入0.315 g甲酸铵,超声溶解。在980 mL甲醇中加入上述液体,超声混匀,过0.22 μm滤膜备用。
1.2.2 基质匹配标准曲线的制备
(1)中间液1(10 μg/mL):移取1.0 mL(100 μg/mL)各标准品储备液于10 mL容量瓶中,乙腈定容,混匀(临用现配)。
(2)中间液2(1 μg/mL):移取1.0 mL中间液1于10 mL容量瓶中,乙腈定容,混匀(临用现配)。
(3)基质匹配标准工作溶液:分别吸取适量中间液,用经1.2.3和1.2.4步骤前处理后的基质空白溶液稀释,按表1配制标准工作溶液。
表1 标准工作溶液配制表
Tab.1 Preparation of standard working solutions
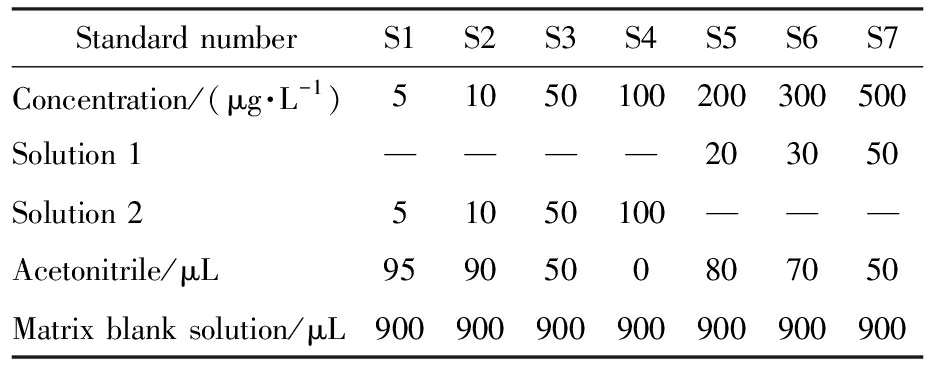
Standard numberS1S2S3S4S5S6S7Concentration/(μg·L-1)51050100200300500Solution 1————203050Solution 251050100———Acetonitrile/μL9590500807050Matrix blank solution/μL900900900900900900900
1.2.3 样品的制备与保存
蔬菜与水果的取样按照《2025年国家食品污染物和有害因素风险监测工作手册》的程序进行采样和取样。样品前处理依据其物理形态差异分别进行:个体较小的样品取全部;个体较大的均匀样品分割为小块;组分不均的样品则从不同部位切取以保障代表性。随后,将所有样品一并均质化为匀浆,置于聚乙烯瓶中,于-18 ℃条件下冷冻保存备用。
1.2.4 样品的前处理
准确称取10.00 g试样于50 mL塑料离心管中,加入10 mL乙腈,涡旋振荡3 min以进行提取。随后,加入4 g无水硫酸镁、1 g氯化钠、1 g柠檬酸钠、0.5 g柠檬酸氢二钠及一颗陶瓷均质子,剧烈振荡1 min,随后于4200 r/min离心 5 min。提取完成后,准确移取1 mL上清液至已装有150 mg无水硫酸镁与20 mg氨基化多壁碳纳米管的净化管中(用于脱水和净化),涡旋混合1 min。该混合物经4200 r/min再次离心5 min后,取0.3 mL上清液,用0.7 mL去离子水稀释并混匀,最终经0.22 μm微孔滤膜过滤,转移至进样瓶以待仪器分析。
1.2.5 色谱及质谱条件
1.2.5.1 色谱条件
色谱分析在Waters ACQUITY UPLC BEH C18色谱柱(100 mm×2.1 mm,1.7 μm)上进行。柱温箱温度维持在40 ℃,自动进样器的进样体积设定为10 μL,流动相流速为0.3 mL/min。流动相由A相(含0.1%甲酸与5 mmol/L甲酸铵的水溶液(含2%甲醇))和B相(甲醇(含2%水))组成。洗脱方式为梯度洗脱,具体程序见表2。
表2 流动相梯度洗脱程序
Tab.2 Mobile phase gradient elution procedure
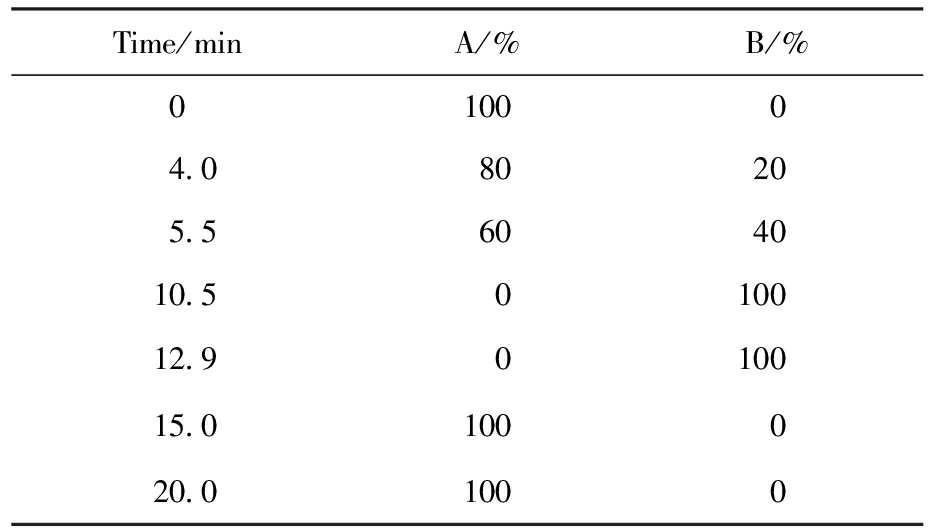
Time/minA/%B/%010004.080205.5604010.5010012.9010015.0100020.01000
1.2.5.2 质谱条件
质谱检测采用电喷雾离子源(ESI),在正离子模式下以多反应监测(MRM)方式进行扫描。关键仪器参数设定如下:毛细管电压2.0 kV,离子源温度150 ℃,脱溶剂温度450 ℃,脱溶剂气流速800 L/h。其他质谱参数见表3。
表3 38种农药的多反应监测(MRM)优化参数
Tab.3 Optimized parameters for multi-response monitoring (MRM) of 38 pesticides
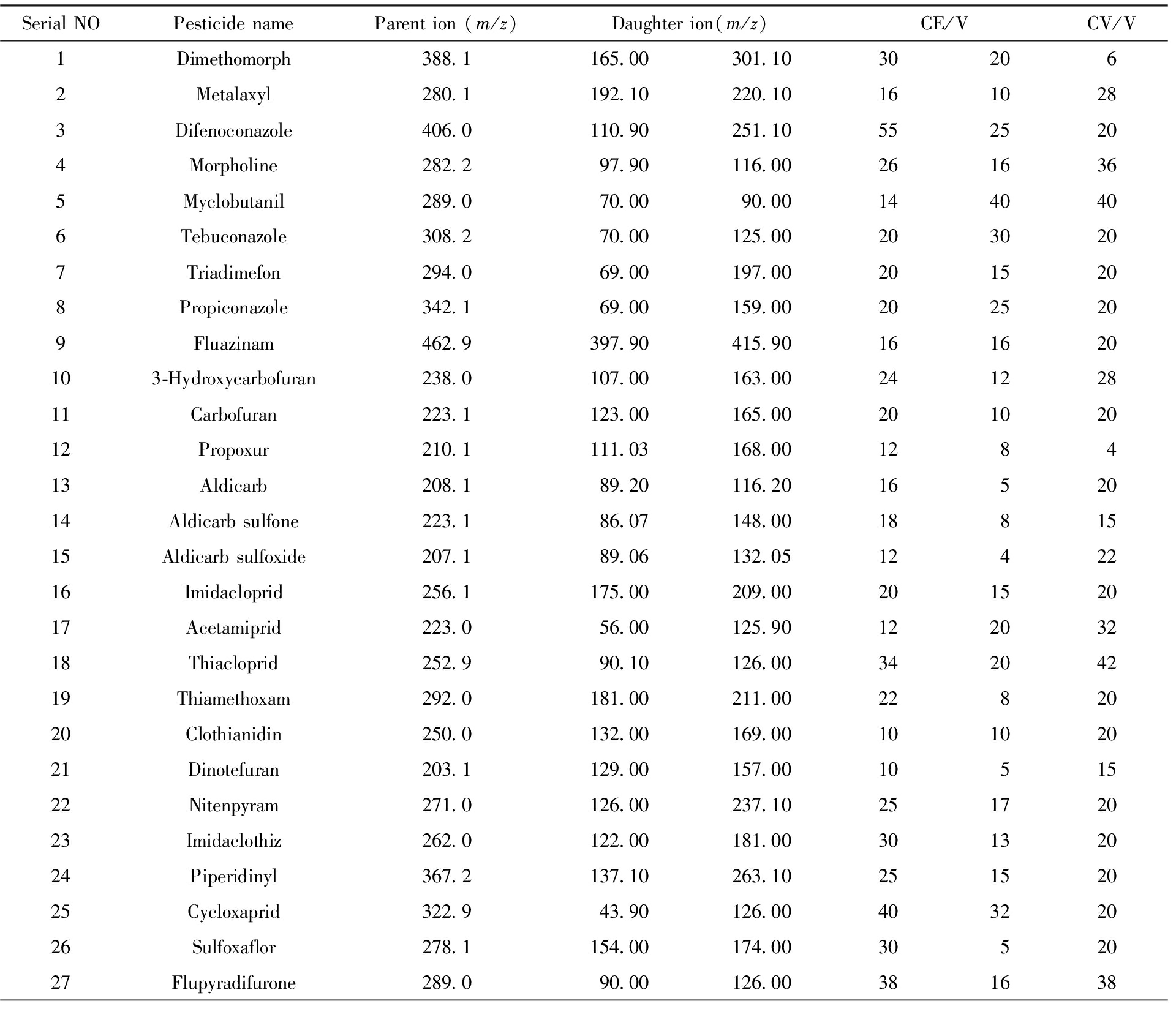
Serial NOPesticide nameParent ion (m/z)Daughter ion(m/z)CE/VCV/V1Dimethomorph388.1165.00301.10302062Metalaxyl280.1192.10220.101610283Difenoconazole406.0110.90251.105525204Morpholine282.297.90116.002616365 Myclobutanil289.070.0090.001440406Tebuconazole308.270.00125.002030207Triadimefon294.069.00197.002015208Propiconazole342.169.00159.002025209Fluazinam462.9397.90415.90161620103-Hydroxycarbofuran238.0107.00163.0024122811Carbofuran223.1123.00165.0020102012Propoxur210.1111.03168.00128413Aldicarb208.189.20116.201652014Aldicarb sulfone223.186.07148.001881515Aldicarb sulfoxide207.189.06132.051242216Imidacloprid256.1175.00209.0020152017Acetamiprid223.056.00125.9012203218Thiacloprid252.990.10126.0034204219Thiamethoxam292.0181.00211.002282020Clothianidin250.0132.00169.0010102021Dinotefuran203.1129.00157.001051522Nitenpyram271.0126.00237.1025172023Imidaclothiz262.0122.00181.0030132024Piperidinyl367.2137.10263.1025152025Cycloxaprid322.943.90126.0040322026Sulfoxaflor278.1154.00174.003052027Flupyradifurone289.090.00126.00381638
续表
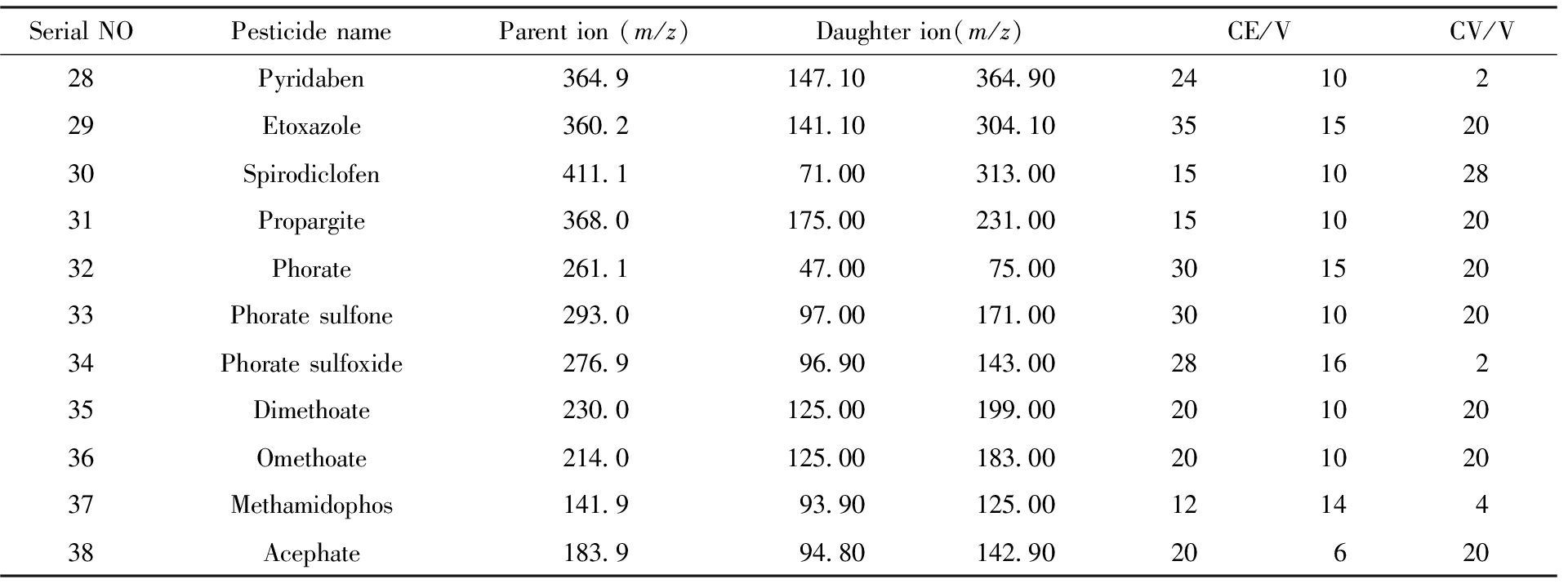
Serial NOPesticide nameParent ion (m/z)Daughter ion(m/z)CE/VCV/V28Pyridaben364.9147.10364.902410229Etoxazole360.2141.10304.1035152030Spirodiclofen411.171.00313.0015102831Propargite368.0175.00231.0015102032Phorate261.147.0075.0030152033Phorate sulfone293.097.00171.0030102034Phorate sulfoxide276.996.90143.002816235Dimethoate230.0125.00199.0020102036Omethoate214.0125.00183.0020102037Methamidophos141.993.90125.001214438Acephate183.994.80142.9020620
2 结果与讨论
2.1 QuEChERS条件的选择和优化
2.1.1 提取剂的选择
本实验分别用10 mL的乙酸乙酯、甲醇、乙腈作为提取试剂,结果发现乙腈作为提取试剂时,回收率在80%~120%之间的农药占比较多,可达到90%以上。因此,本实验选定乙腈作为提取溶剂。为优化提取效率,考察了10 g空白基质中乙腈用量(10、15、20、25、30 mL)对目标农药回收率的影响如图1所示。结果表明,回收率随溶剂用量增加而提升;当用量达到20 mL时,目标化合物的平均回收率高于70%。然而,过量溶剂不仅造成浪费,还会因提取液浓缩后目标物相对浓度降低而影响检测灵敏度。因此,最终确定采用20 mL乙腈提取10 g样品的优化方案。
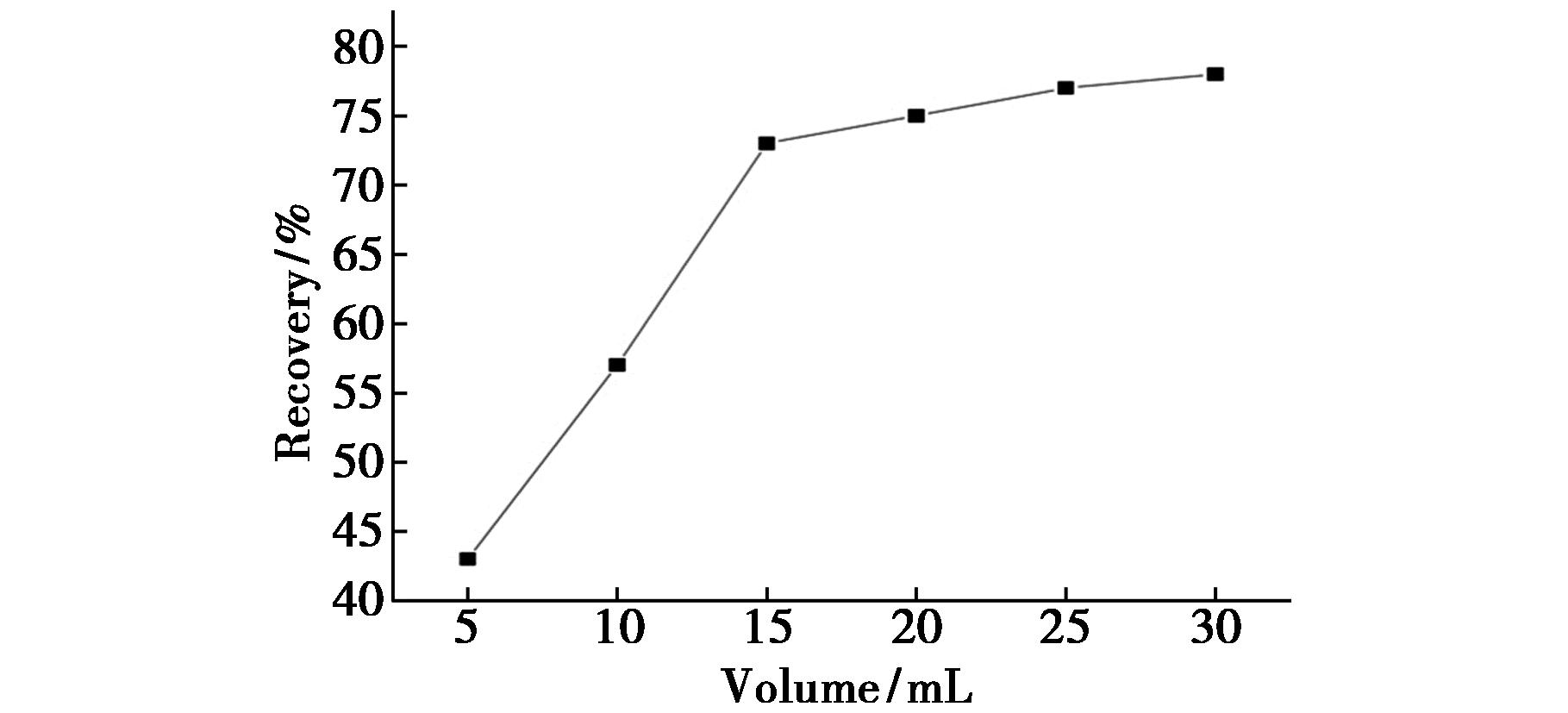
图1 不同提取体积对回收率的影响
Fig.1 Effect of different extraction volumes on recovery
在QuEChERS提取过程中,盐包的组成与用量通过影响水在有机相中的分配而直接关系到萃取效率[13]。为此,本研究评估了4种不同的盐包配比(3 g MgSO4+2 g NaCl、3 g Na2SO4+2 g NaCl、4 g MgSO4+1 g NaCl、4 g Na2SO4+1 g NaCl)对农药回收率的影响。结果表明,采用4 g MgSO4与 1 g NaCl的组合时,可获得最佳的整体回收效果,约88%的目标农药其回收率落在80%~120%的理想区间内。因此,该配比被确定为最终优化条件。
2.1.2 净化试剂的优化
在蔬菜水果中净化试剂的选择至关重要,常用的净化试剂有PSA[14]、GCB[15]、C18[16]等,GCB能够强烈吸附平面结构的农药[17],C18能够吸附非极性类的农药,对除虫菊酯类农药吸附较多[18],PSA粉能够除去一些有机酸、脂肪酸色素等[19]。氨基化多壁碳纳米管有较高的比表面积,有较强的吸附能力,能够实现对多种杂质的定向吸附,能够替代传统的吸附剂,减少基质效应[20]。因此本实验在研究了每mL提取液中组合使用了PSA+氨基化多壁碳纳米管+MgSO4进行回收率实验后,通过加入50 mg的PSA、150 mg的MgSO4和分别加入10、15、20、25、30、35 mg的氨基化多壁碳纳米管进行对比实验,如图2所示。结果表明,在配比为50 mg PSA+25 mg氨基化多壁碳纳米管+150 mg MgSO4时,农药的回收率均在60%以上,且平均回收率>82%。
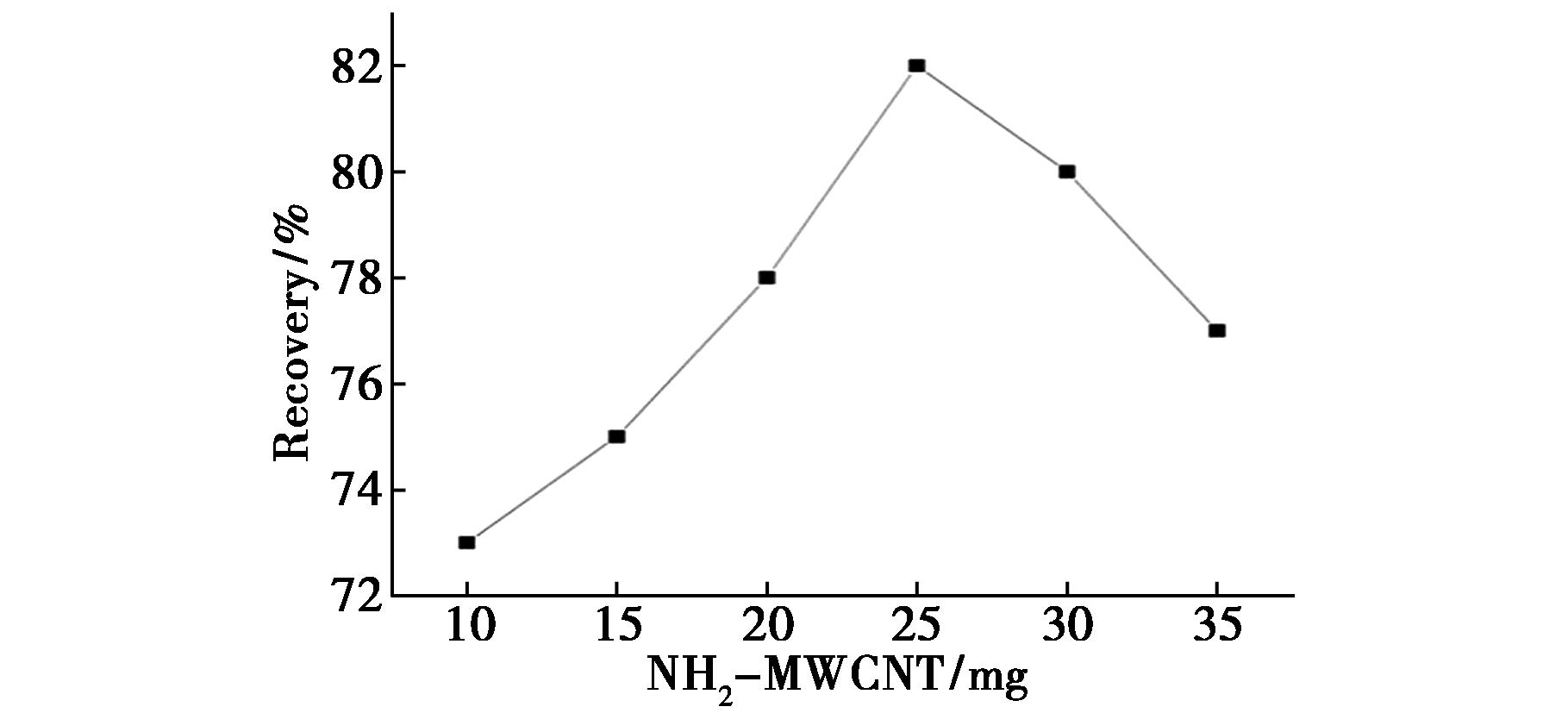
图2 净化试剂含量对回收率的影响
Fig.2 Effect of purification reagent amount on recovery
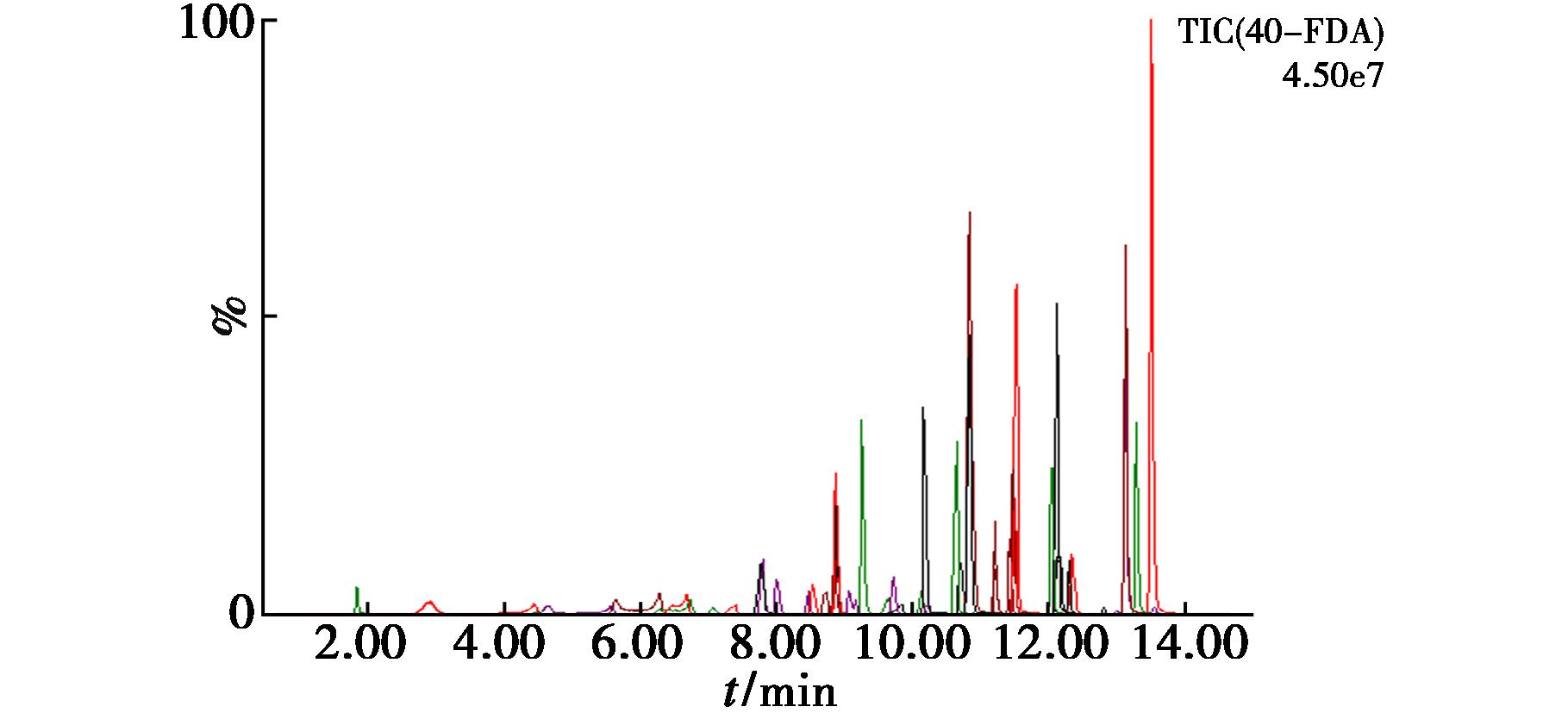
图3 加标100 μg/kg的样品总离子流图
Fig.3 Total ion chromatogram of a sample spiked at 100 μg/kg
2.1.3 流动相及流速的选择
在相同梯度下系统比较了以乙腈或甲醇作为有机相,并与添加不同浓度甲酸或甲酸铵的水相组合的效果。初步实验表明,仅使用甲醇/水或乙腈/水体系时,多数农药响应微弱甚至无响应。通过引入添加剂,其响应与峰形得到显著改善,且作用机制因化合物类别而异:甲酸的加入显著提升了有机磷农药的响应,这源于其促进了目标物的质子化电离;而甲酸铵则更利于有机氯及拟除虫菊酯类农药,因该类化合物易在质谱中形成稳定的[M+NH4]+加合离子,铵盐的存在有效促进了该过程。综合考虑到甲醇作为质子溶剂,可通过氢键作用提供更优的分离选择性,本研究最终选择甲醇作为有机相,并进一步优化其水相中添加剂的浓度。实验表明,随着甲酸浓度(体积分数0.01%~0.2%)升高,甲胺磷的噪声增大,峰形变差;而当甲酸铵浓度超过5 mmol/L(测试范围为 1~10 mmol/L)时,阿维菌素和多杀菌素等农药出现峰展宽和保留时间延迟。综合考量各农药的灵敏度与分离效果,最终确定采用含0.1%甲酸和 5 mmol/L甲酸铵的水溶液与甲醇作为流动相条件。分别对流速为0.2、0.3、0.4 mL/min进行测试,结果发现流速为0.2 mL/min时部分化合物峰宽增加,灵敏度降低。流速为0.4 mL/min时部分峰分离度降低。综合考虑灵敏度和分离度最终选择流速为0.3 mL/min。
2.2 方法学评价
2.2.1 线性关系及检出限
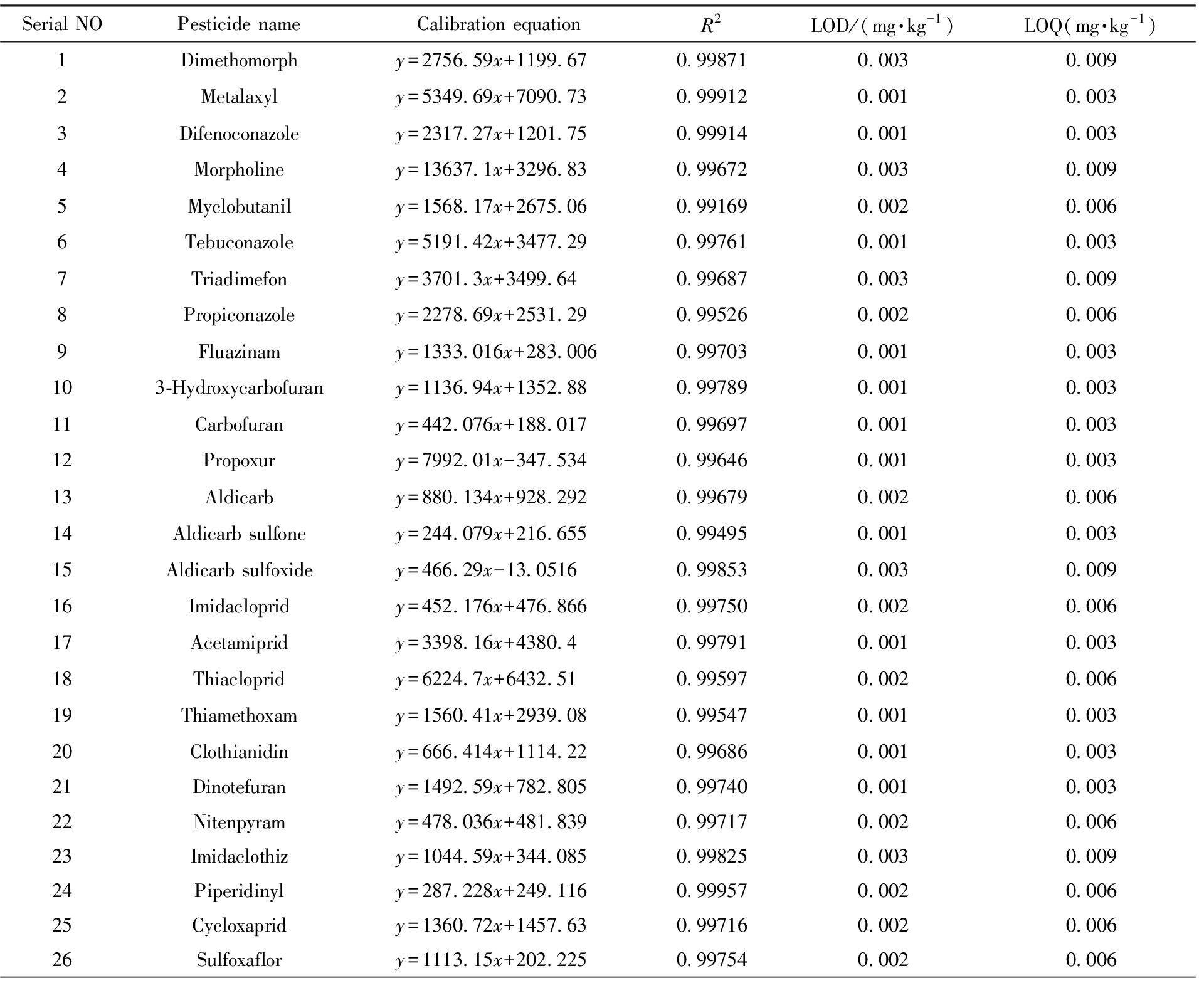
本研究采用空白基质匹配标准溶液配制标准曲线,以目标化合物的质量浓度为横坐标,以其定量离子对的峰面积为纵坐标进行线性拟合。结果表明,各目标化合物在其相应浓度范围内线性关系良好,标准曲线的线性回归相关系数(R2)均大于0.991。方法的检出限(LOD)按信噪比(S/N)为3时对应的浓度进行测定。10倍的信噪比(S/N)计算定量限,检出限(LOD)与定量限(LOQ)范围分别为0.001~0.003 mg/kg和0.003~0.009 mg/kg(表4)。
表4 38种农药残留的线性范围、检出限与定量限
Tab.4 Linear range,detection limit and quantification limit for 38 pesticide residues
Serial NOPesticide nameCalibration equationR2LOD/(mg·kg-1)LOQ(mg·kg-1)1Dimethomorphy=2756.59x+1199.670.998710.0030.0092Metalaxyly=5349.69x+7090.730.999120.0010.0033Difenoconazoley=2317.27x+1201.750.999140.0010.0034Morpholiney=13637.1x+3296.830.996720.0030.0095Myclobutanily=1568.17x+2675.060.991690.0020.0066Tebuconazoley=5191.42x+3477.290.997610.0010.0037Triadimefony=3701.3x+3499.640.996870.0030.0098Propiconazoley=2278.69x+2531.290.995260.0020.0069Fluazinamy=1333.016x+283.0060.997030.0010.003103-Hydroxycarbofurany=1136.94x+1352.880.997890.0010.00311Carbofurany=442.076x+188.0170.996970.0010.00312Propoxury=7992.01x-347.5340.996460.0010.00313Aldicarby=880.134x+928.2920.996790.0020.00614Aldicarb sulfoney=244.079x+216.6550.994950.0010.00315Aldicarb sulfoxidey=466.29x-13.05160.998530.0030.00916Imidaclopridy=452.176x+476.8660.997500.0020.00617Acetamipridy=3398.16x+4380.40.997910.0010.00318Thiaclopridy=6224.7x+6432.510.995970.0020.00619Thiamethoxamy=1560.41x+2939.080.995470.0010.00320Clothianidiny=666.414x+1114.220.996860.0010.00321Dinotefurany=1492.59x+782.8050.997400.0010.00322Nitenpyramy=478.036x+481.8390.997170.0020.00623Imidaclothizy=1044.59x+344.0850.998250.0030.00924Piperidinyly=287.228x+249.1160.999570.0020.00625Cycloxapridy=1360.72x+1457.630.997160.0020.00626Sulfoxaflory=1113.15x+202.2250.997540.0020.006
续表
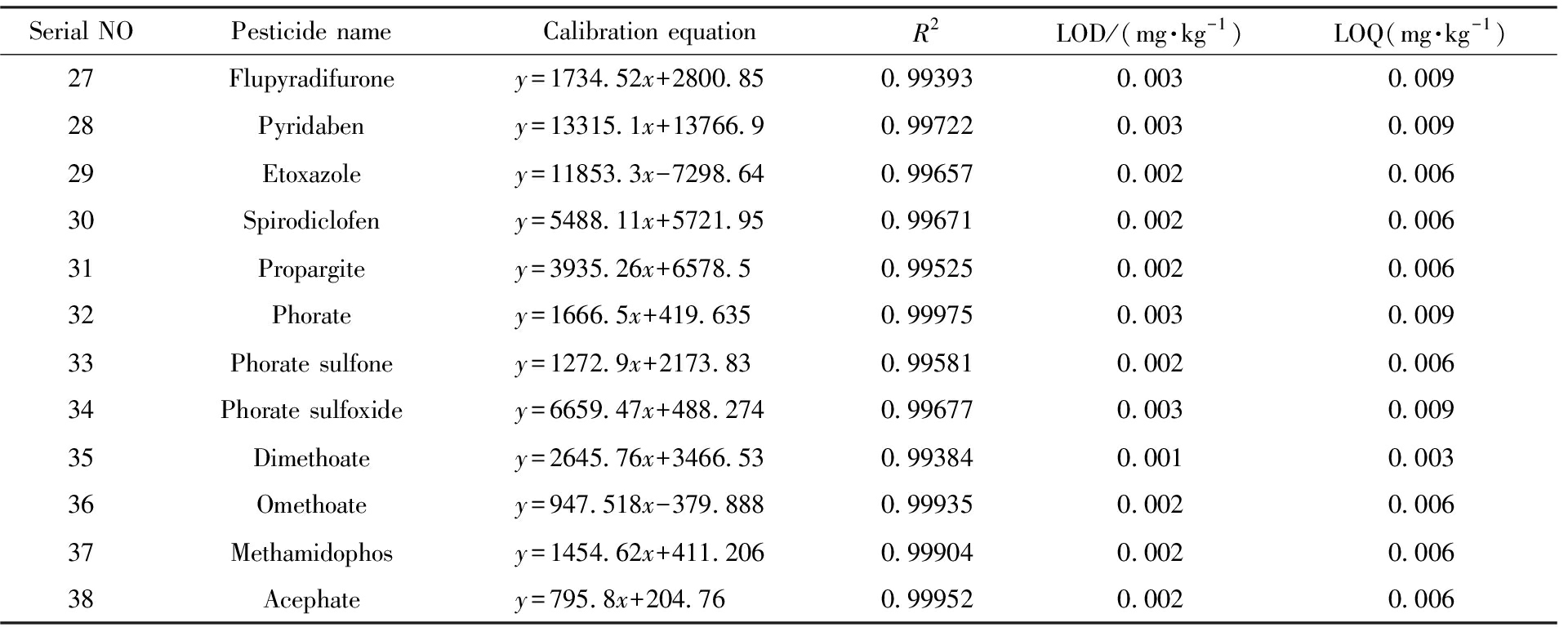
Serial NOPesticide nameCalibration equationR2LOD/(mg·kg-1)LOQ(mg·kg-1)27Flupyradifuroney=1734.52x+2800.850.993930.0030.00928Pyridabeny=13315.1x+13766.90.997220.0030.00929Etoxazoley=11853.3x-7298.640.996570.0020.00630Spirodiclofeny=5488.11x+5721.950.996710.0020.00631Propargitey=3935.26x+6578.50.995250.0020.00632Phoratey=1666.5x+419.6350.999750.0030.00933Phorate sulfoney=1272.9x+2173.830.995810.0020.00634Phorate sulfoxidey=6659.47x+488.2740.996770.0030.00935Dimethoatey=2645.76x+3466.530.993840.0010.00336Omethoatey=947.518x-379.8880.999350.0020.00637Methamidophosy=1454.62x+411.2060.999040.0020.00638Acephatey=795.8x+204.760.999520.0020.006
2.2.2 准确度及精密度
为评估方法的准确度与精密度,进行了空白样品添加回收试验。分别在20、50和100 μg/kg 3个水平进行8次平行实验,并采用标准曲线法定量。结果(表5)表明,所有目标化合物的回收率为63.3%~108.1%,相对标准偏差(RSD)为1.20%~14.0%。并且连续3 d进行了日间精密度的测试,相对标准偏差(RSD)为3.22%~13.06%。该结果证明本方法具有良好的准确度和精密度。
表5 目标化合物加标回收率与相对标准偏差
Tab.5 Recovery and relative standard deviation (RSD) of target compounds (n=8)
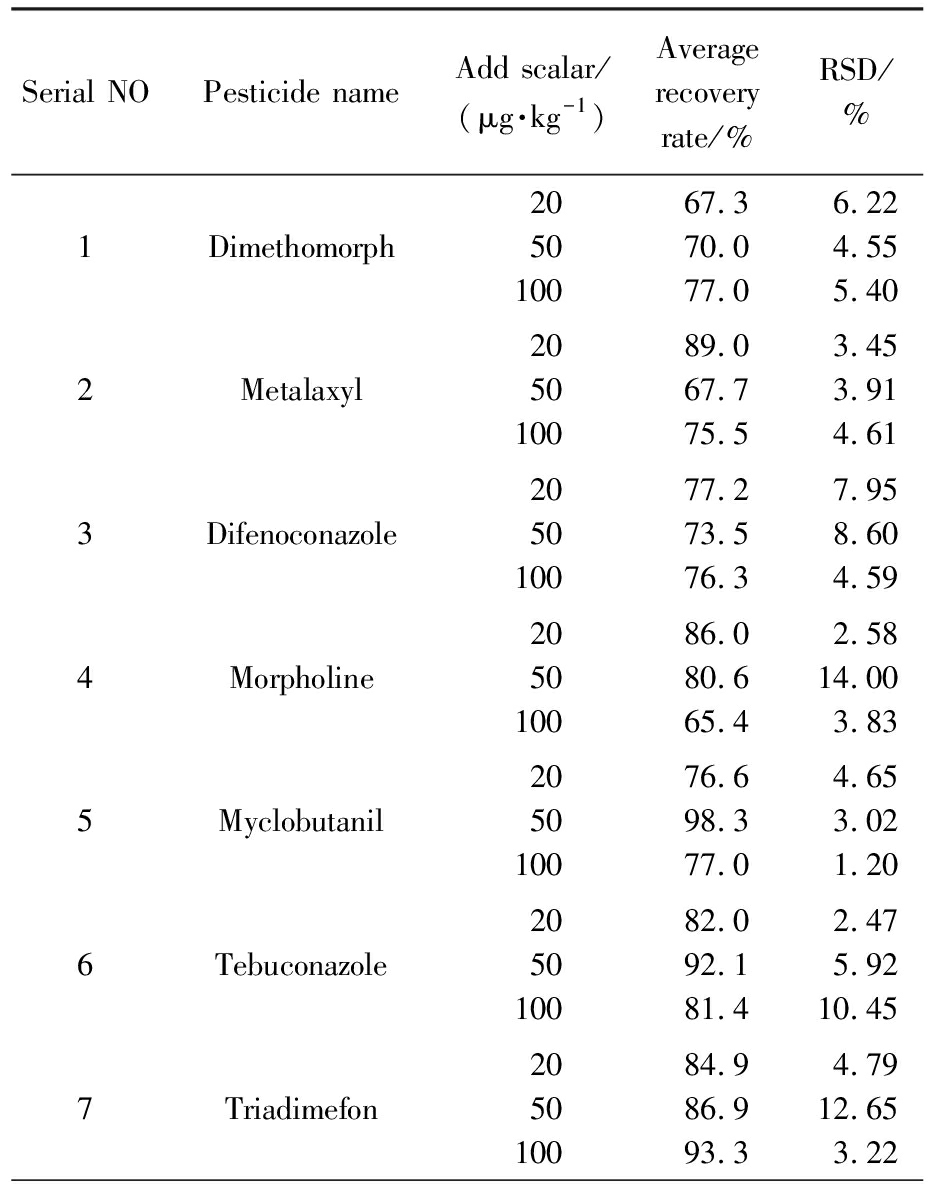
Serial NOPesticide nameAdd scalar/(μg·kg-1)Average recovery rate/%RSD/%1Dimethomorph205010067.370.077.06.224.555.402Metalaxyl205010089.067.775.53.453.914.613Difenoconazole205010077.273.576.37.958.604.594Morpholine205010086.080.665.42.5814.003.835Myclobutanil205010076.698.377.04.653.021.206Tebuconazole205010082.092.181.42.475.9210.457Triadimefon205010084.986.993.34.7912.653.22
续表
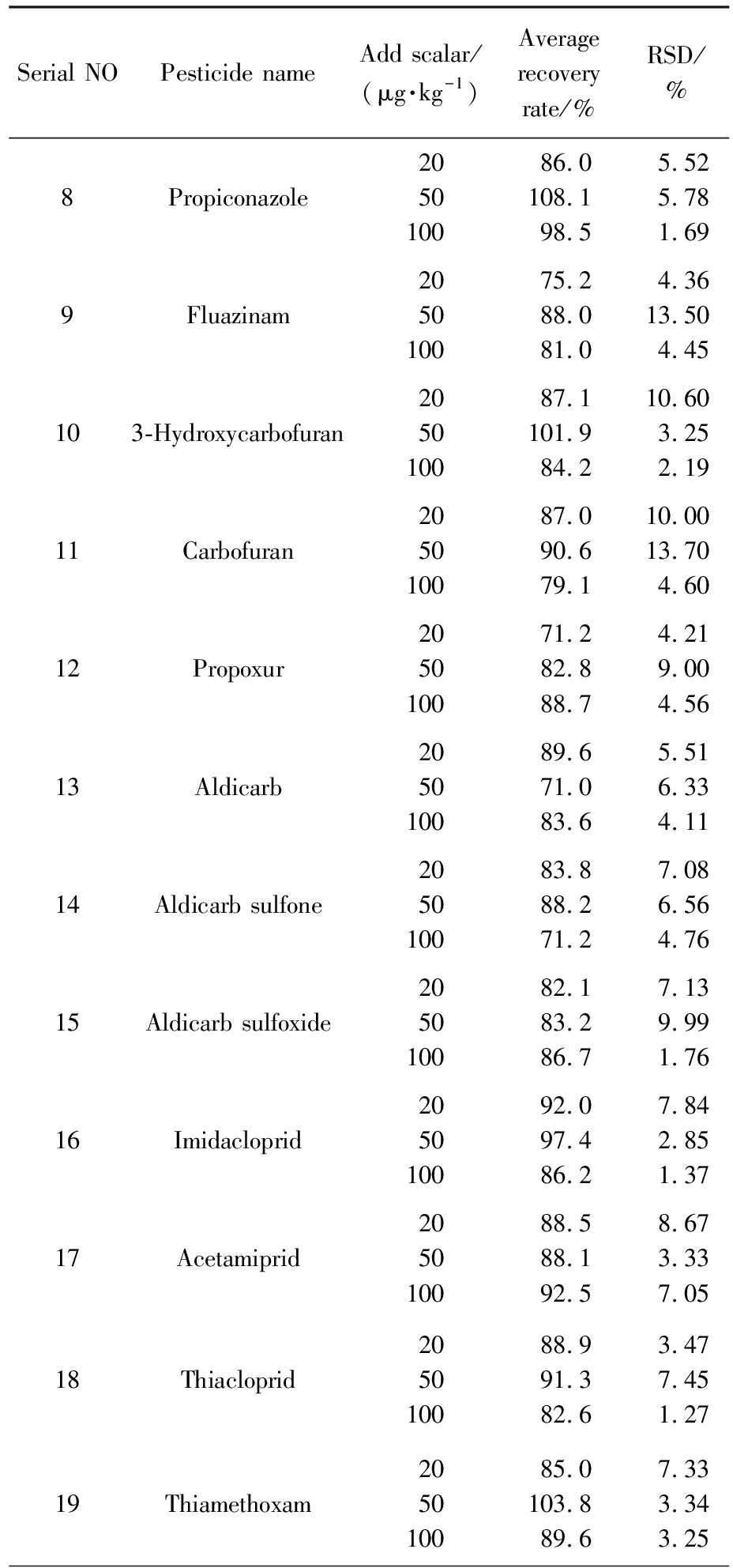
Serial NOPesticide nameAdd scalar/(μg·kg-1)Average recovery rate/%RSD/%8Propiconazole205010086.0108.198.55.525.781.699Fluazinam205010075.288.081.04.3613.504.45103-Hydroxycarbofuran205010087.1101.984.210.603.252.1911Carbofuran205010087.090.679.110.0013.704.6012Propoxur205010071.282.888.74.219.004.5613Aldicarb205010089.671.083.65.516.334.1114Aldicarb sulfone205010083.888.271.27.086.564.7615Aldicarb sulfoxide205010082.183.286.77.139.991.7616Imidacloprid205010092.097.486.27.842.851.3717Acetamiprid205010088.588.192.58.673.337.0518Thiacloprid205010088.991.382.63.477.451.2719Thiamethoxam205010085.0103.889.67.333.343.25
续表

Serial NOPesticide nameAdd scalar/(μg·kg-1)Average recovery rate/%RSD/%20Clothianidin205010090.6101.085.75.443.811.3221Dinotefuran205010087.878.776.59.023.685.2422Nitenpyram205010078.295.287.29.692.572.2123Imidaclothiz205010091.088.075.85.757.729.6024Piperidinyl205010063.386.376.53.213.041.4025Cycloxaprid205010079.486.674.15.788.236.0026Sulfoxaflor205010073.392.984.73.626.261.8227Flupyradifurone205010080.0102.881.52.882.957.0028Pyridaben205010092.191.677.82.112.472.0129Etoxazole205010081.287.381.12.882.473.5630Spirodiclofen205010065.196.684.63.585.392.6931Propargite205010066.266.882.75.537.398.5732Phorate205010084.079.675.04.346.762.6233Phorate sulfone205010087.080.966.73.664.315.2034Phorate sulfoxide205010086.082.875.36.104.813.7035Dimethoate205010076.488.366.88.408.605.2636Omethoate205010083.698.594.15.3813.85.5937Methamidophos205010086.082.093.45.526.156.5438Acephate205010095.580.581.78.295.742.34
2.3 实际样品的检测
本研究采集了103份蔬菜水果样品,样品均来自于青海省各区县各大农贸市场及超市,结果显示部分样品的啶虫脒、噻虫嗪、噻虫胺、乙螨唑等均有检出。阳性样本经过二次复检,通过对保留时间和特征离子比率比进行了复核,并且报上级机构实验室进行了比对,相对相差<20%,部分阳性样本碎片离子色谱图如图4所示,根据国家标准GB 2763—2021《食品安全国家标准 食品中农药最大残留限量》[21]均小于国家限量。
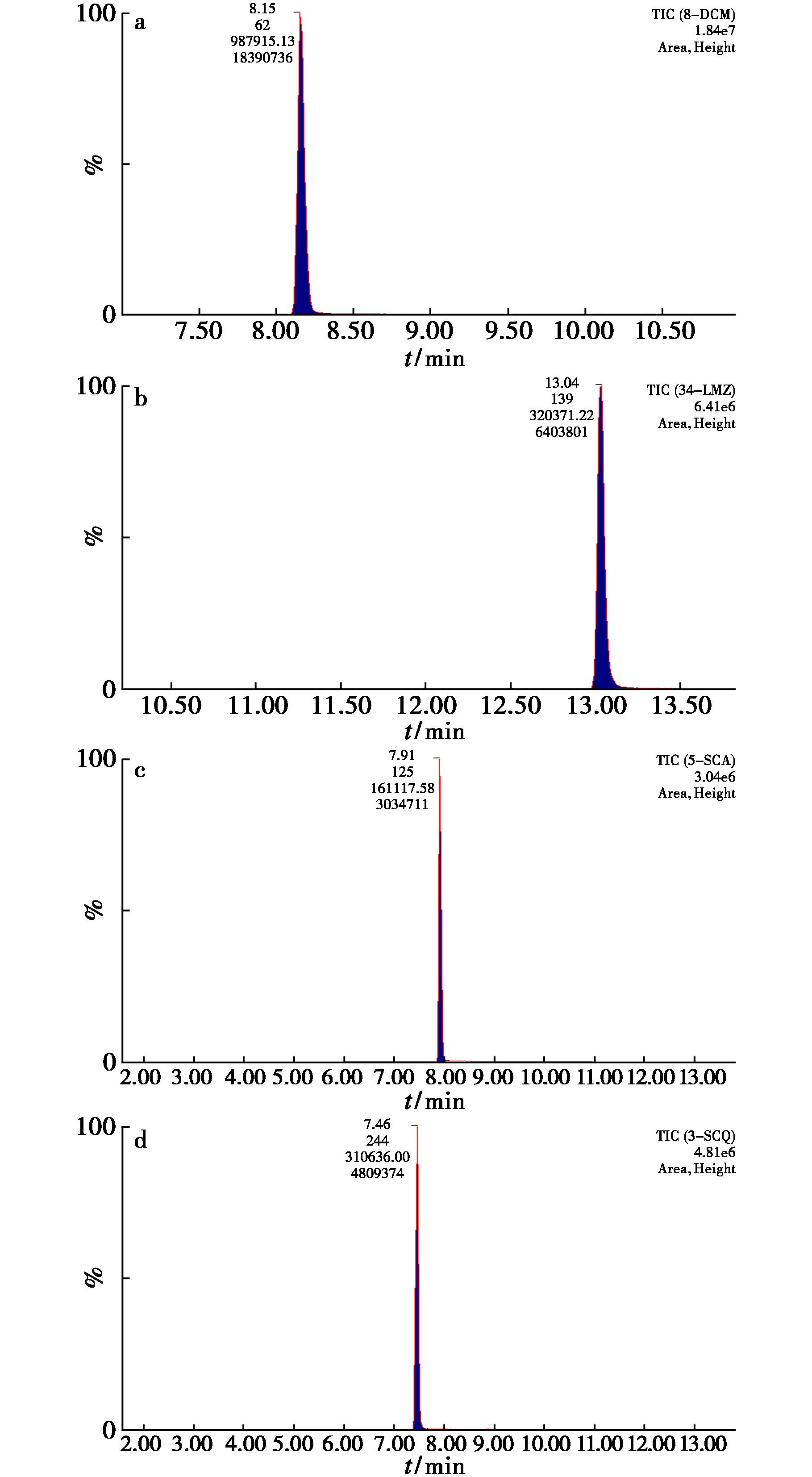
a.15号样品啶虫脒色谱图;b.33号样品螺螨酯色谱图;c.18号样品噻虫胺色谱图;d.11号样品噻虫嗪色谱图
图4 部分阳性样品色谱图
Fig.4 Representative chromatograms of selected positive samples
3 结论
本研究构建了一个高效的分析体系:通过采用氨基化多壁碳纳米管改进QuEChERS前处理净化效果,并利用超高效液相色谱-串联质谱技术,实现了果蔬样品中38种农药残留的同步、快速分析。并且通过优化提取试剂、净化试剂、仪器条件等方式有效地提高了方法的回收率,降低了基质效应的影响。本方法准确、快速、灵敏度高,为蔬菜水果中农药残留的检测提供了方法参考,为市场监管有效管理提供了技术支撑。
[1]Qian X M,Wan L,Li W G,Xue A L.Chin.J.Anal.Lab.,2025,44(4):502-510.
钱晓敏,万玲,李卫国,薛爱龙.分析试验室,2025,44(4):502-510.
[2]Malhat F,Abdel S S S,Saber E S,Saber A N.Food Control,2026,179:111555.
[3]An Q.Preparation of a New Magnetic Mesoporous Composite ODA@Fe3O4-MWCNTS and Its Application in the Analysis of Benzamide Pesticide Residues.Shenyang:China Medical University,2023.
安琪.新型磁性介孔复合材料ODA@Fe3O4-MWCNTs的制备及其在苯甲酰胺类农药残留分析中的应用.沈阳:中国医科大学,2023.
[4]Xu Y,Fang Z W,Yang H J,Huang B Y,Fang F,An J,Liu Q,Huang P X,Yu H B.Chin.J.Anal.Lab.,2025,44(5):725-731.
徐悦,方紫薇,杨红菊,黄宝勇,方芳,安娟,刘茜,黄培鑫,于寒冰.分析试验室,2025,44(5):725-731.
[5]Wang Y,Diao Z,Qu Y.Sci.Rep.,2025,15(1):27728-27728.
[6]Ye X M.Applications of Novel QuEChERS Protocols for Analysis of Pesticide Residues in Fruits and Vegetables.Hangzhou:Zhejiang University of Technology,2020.
叶学敏.新型QuEChERS方法在果蔬农残分析中的应用研究.杭州:浙江工业大学,2020.
[7]Tong L Y,Li G R,Gong Y K,Jin M Y,Xiao Z J,Zhou C X,Zhang J,Li M W.Chin.J.Anal.Lab.,2025,44(5):712-719.
童兰艳,李根容,龚迎昆,金梦瑶,肖昭竞,周朝旭,章健,李明伟.分析试验室,2025,44(5):712-719.
[8]JIANG J J,LIU L,JIANG J G,LUO Y,GAO S P.Chem.Reagents,2025,47(1):74-79.
蒋建军,刘丽,蒋家贵,罗宇,高帅鹏.化学试剂,2025,47(1):74-79.
[9]Tang Y,Wen S,Cao W C.Chin.J.Chromatogr.,2025,43(4):309-316.
唐艳,闻胜,曹文成.色谱,2025,43(4):309-316.
[10]Meng L,Ma W,Chen W.Polymer,2025,321:128145-128145.
[11]Xu R H,Xie Q W,Li X J.Chin.J.Chromatogr.,2022,40(5):469-476.
许芮菡,谢倩文,李旭军.色谱,2022,40(5):469-476.
[12]Li S Y,Liu J F,Li M.J.Zhejiang A F Univ.,2021,38(2):355-361.
李思艳,刘俊蕃,李梅.浙江农林大学学报,2021,38(2):355-361.
[13]Zhang S,Wang Y,Xie P F.Food Sci.,2025,46(19):281-289.
张帅,王钰,谢鹏飞.食品科学,2025,46(19):281-289.
[14]Guo C L,Wang Y,Lei Y T,Jia X Y,Liu H J,Chen L J,Han F,Song W.Phys.Test Chem.Anal.,Part B:Chem.Anal.,2025,61(1):10-21.
郭春丽,王钰,雷雨甜,贾学颖,刘会佳,陈莉君,韩芳,宋伟.理化检验-化学分册,2025,61(1):10-21.
[15]Zhang Y P.Phys.Test Chem.Anal.,Part B:Chem.Anal.,2025,61(3):287-293.
张延平.理化检验-化学分册,2025,61(3):287-293.
[16]Wu W,Wang Z,Ye S R,Zhao A P,Wang G X,Feng D J.China Meas.Test,2024,50(S2):84-93.
吴微,王智,叶善蓉,赵爱平,王顾希,冯德建.中国测试,2024,50(S2):84-93.
[17]Zhang J W.The Study on the Determination of Neonicotinoid Insecticides and Their Metabolites by UPLC-Q Exactive Orbitrap HRMS.Beijing:Chinese People′s Public Security University,2024.
张婧文.UPLC-Q Exactive Orbitrap HRMS检验新烟碱类杀虫剂及其代谢物的研究.北京:中国人民公安大学,2024.
[18]Yang S.Detection of Multiple Pesticide Residues in Complex Matrices by Dispersive Solid-Phase Extraction-UPLC-MS/MS Based on Modified New-Type Mesoporous Material.Taian:Shandong Agricultural University,2020.
杨松.改性新型介孔材料分散固相萃取-UPLC-MS/MS法检测复杂基质中农药多残留.泰安:山东农业大学,2020.
[19]Liu Y X,Li M M,Bian K,Guan E Q,Liu Y F.Food Sci.,2019,40(13):326-333.
刘远晓,李萌萌,卞科,关二旗,刘远方.食品科学,2019,40(13):326-333.
[20]He J L,Li Y H,Liu F.Ionics,2023,29(8):3407-3419.
[21]GB 2763—2021.National Food Safety Standard-Maximum Residue Limits for Pesticides in Food,2021.
GB 2763—2021.食品安全国家标准食品 中农药最大残留限量,2021.