近年来,光驱动的有机化学转化因其清洁、高效等特点受到了广泛关注。可见光不仅来源丰富、环境友好,而且能够显著降低反应的能耗[1]。该类反应通常在温和条件下进行,无需高温、高压或其他苛刻条件,表现出优良的官能团兼容性[2]。在光驱动的有机反应中,光催化剂作为能量传递与电子转移的关键载体,起到了不可或缺的作用。目前,铱(Ir)、钌(Ru)等金属的联吡啶配合物,如[Ir(ppy)3]2+、[Ru(bpy)3]2+,由于其独特的分子结构与优异的可见光吸收能力,成为有机光合成化学中最经典的光催化剂[3-5]。这类配合物在可见光照射下,发生金属-配体电荷转移(Metal-to-Ligand Charge Transfer,MLCT)作用,产生的激发态寿命较长;这种长寿命的激发态为催化剂与底物之间发生后续的电子转移或能量转移等慢步骤提供了充足的时间。此外,其激发态既可表现出强氧化性,也可表现出强还原性,具有足够的热力学驱动力与反应底物发生单电子转移(SET)。更重要的是,它们的结构在多次的电子得失过程中通常能保持稳定,不易分解,从而保证了催化循环能够持续进行。
MLCT过程通常发生于金属中心d轨道电子激发至配体π*反键轨道,常见于Ru(Ⅱ)、Ir(Ⅲ)等过渡金属配合物中(图1a)。与MLCT型催化剂相比,配体-金属电荷转移(Ligand-to-Metal Charge Transfer,LMCT)则涉及配体π轨道电子向金属d轨道的转移,或者金属-配体的σ轨道电子向金属d轨道(图1b)[6]。LMCT过程在氧化还原光反应中具有重要作用,例如,配体衍生的自由基物种,如氯自由基(Cl·)具有极高的反应活性,能够通过氢原子转移(HAT)机制实现C—H键活化,拓展了光催化在有机合成中的应用范围[7,8]。
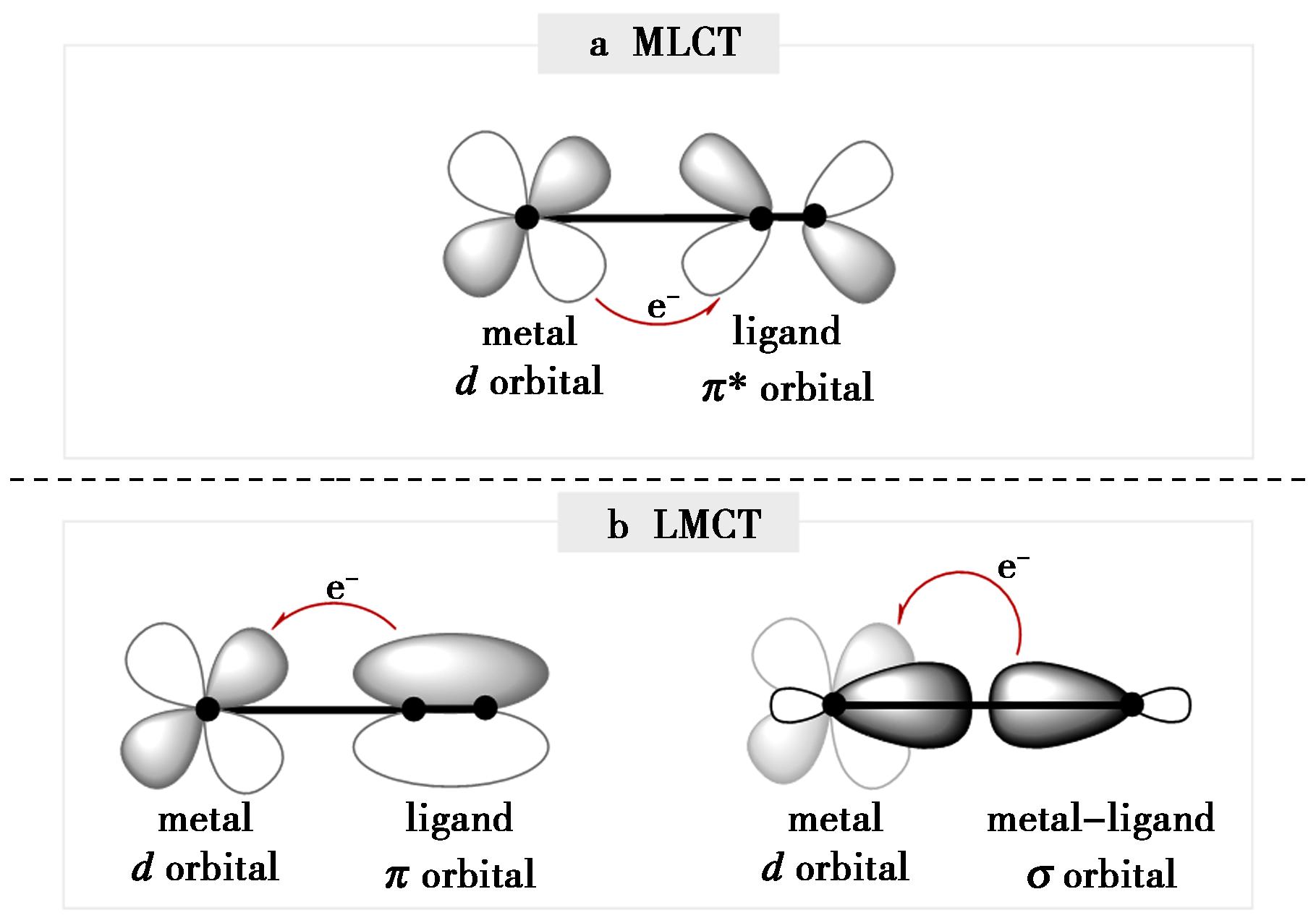
图1 典型的MLCT过程(a)与LMCT过程(b)[6]
Fig.1 Typical MLCT process (a) and LMCT process (b)[6]
LMCT型催化剂多以铁、铜、铈等丰产金属为核心,具有储量丰富、低毒无害等优点。其中,三氯化铈(CeCl3)是一种常见的铈盐,价格低廉、容易获得,毒性较低。近年来,CeCl3凭借其独特的光物理机制与多样的催化应用,已成为LMCT光催化研究中的重要体系[9]。
Ce元素之所以具有独特的LMCT性能,主要源于其独特的4f电子构型:Ce的电子构型为[Xe]4f15d16s2,其4f轨道仅有1个电子,且4f轨道位于内层,受到外层5s和5p轨道的屏蔽作用,使得4f电子具有较高的局域性。这种构型使得Ce3+/Ce4+氧化还原对具有相对容易的电子转移能力,为LMCT过程提供了理想的电子转移通道。本文综述了光诱导CeCl3催化构建碳-碳键的研究进展,主要包括:(1)C—H键官能团化反应;(2)醇的脱羟基转化反应;(3)脱羧偶联反应。
1 C—H键官能团化反应
含氮杂环广泛存在于自然界[10],是生物活性天然分子中的重要骨架,也是药物研发的关键结构单元[11-14]。含氮杂环化合物在医药、农药、生物成像、金属离子检测等领域具有广泛的应用。因此,发展含氮杂环化合物的直接官能团化为快速合成新型的氮杂环衍生物具有重要意义[15-17]。
1.1 含氮杂环化合物的烷基化反应
2021年,Liu等[18]报道了光驱动CeCl3催化的喹喔啉-2(1H)-酮的烷基化反应。利用空气中的氧气为氧化剂,四丁基氯化铵和三氟乙醇作为添加剂实现该反应(图2)。该反应中,氧气首先对Ce(Ⅲ)进行单电子氧化,生成的Ce(Ⅳ)中间体在光照下发生LMCT过程生成高活性的氯自由基(Cl·),同时再生Ce(Ⅲ)催化剂;Cl·通过HAT过程从烷烃中攫取氢原子生成相应的烷基自由基(R·);含氮杂环底物质子化之后,经过Minisci反应机制完成烷基化反应。该反应体系表现出优异的选择性和活性,对多种官能团具有良好的耐受性。
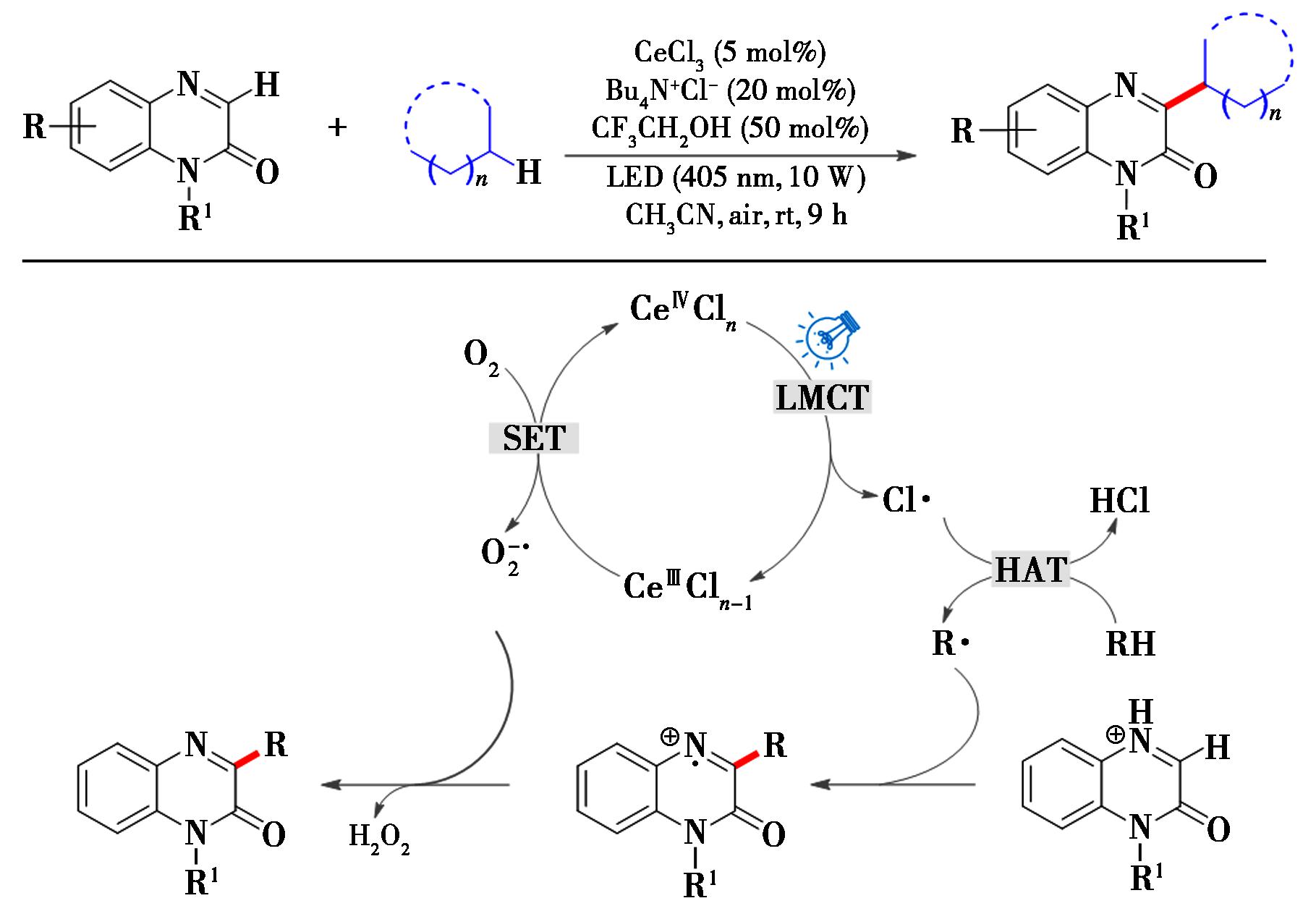
图2 喹喔啉-2(1H)-酮的烷基化反应[18]
Fig.2 Alkylation reaction of quinoxaline-2(1H)-ones[18]
对于异喹啉等相对惰性的底物,采用三氟乙酸(TFA)为添加剂,并延长反应时间至48 h,可以进一步提高反应收率。其中,喹啉、异喹啉、吡啶等杂环均能发生反应,以中等至良好的收率得到相应烷基化产物。该方法展现出良好的实用性,温和条件的高效烷基化反应为含氮杂环的结构修饰提供了高效合成路径,为后续生物活性方面研究奠定了基础。
2024年,Yi等[19]采用相似的CeCl3光催化策略,在空气和390 nm波长光照下,实现了N-磺酰基酮亚胺的烷基化反应(图3)。与上述反应不同的是,该反应体系无需外加质子源,不经历典型的Minisci反应历程。在该反应中,390 nm的紫外光直接激发反应底物N-磺酰基酮亚胺;该激发态与三线态氧(3O2)发生能量转移反应,生成活性单线态氧(1O2),为反应中提供氧化物种。底物拓展发现,反应底物N-磺酰基酮亚胺对各种官能团包括供电子基团(tBu)和吸电子基团(卤素、CF3)均能很好地兼容,合成相应的烷基化产物。
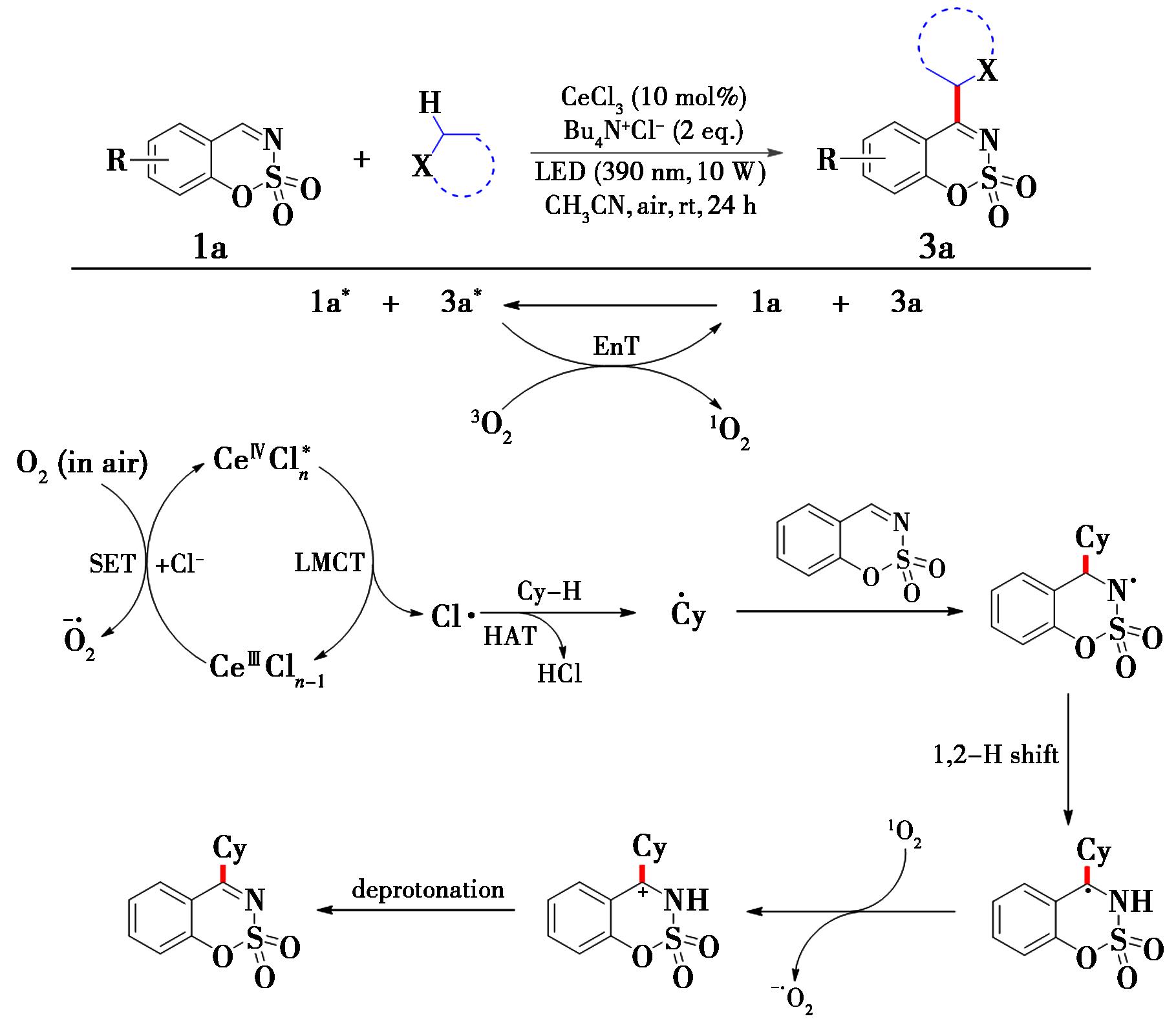
图3 N-磺酰基酮亚胺与环烷烃的烷基化反应[19]
Fig.3 Alkylation reaction of N-sulfonyl ketimine with cycloalkanes[19]
1.2 含氮芳杂环的交叉脱氢偶联反应
2023年,Shen等[20]在空气氛围和蓝光照射下,通过三氯化铈催化“一锅煮”的方法,实现了吲哚和喹喔啉-2(1H)-酮的交叉偶联反应(图4)。反应能够在构造氮杂环之间的碳-碳键的同时,利用安全的氟试剂N-氟代双苯磺酰亚胺(NFSI)成功将氟原子引入到吲哚环C-3位;同时,利用反应中产生的水,能够在C-2位置直接引入羰基,实现了碳-碳键、碳-氧双键和碳-氟键的构建。
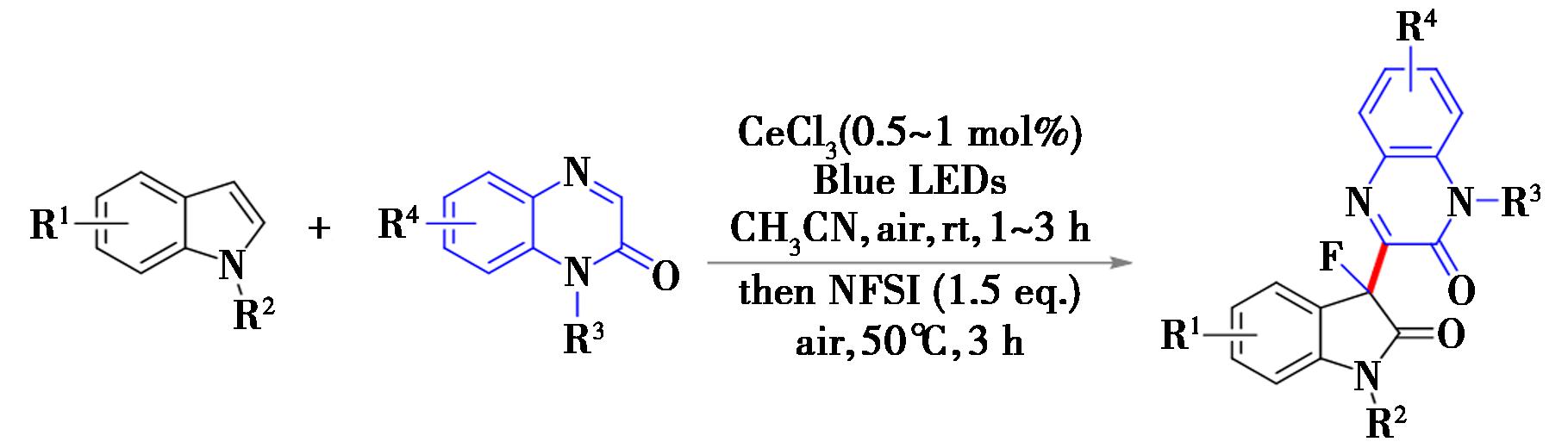
图4 吲哚衍生物与喹喔啉-2(1H)-酮衍生物的交叉脱氢氟化偶联反应[20]
Fig.4 Cross-dehydrogenative fluorination coupling reaction between indole derivatives and quinoxalin-2(1H)-one derivatives[20]
在反应过程中,吲哚C-2双键以及喹喔啉-2(1H)-酮羰基氧与铈中心配位后,通过光照下的LMCT作用,产生氯自由基(Cl·),进而引发后续HAT过程。总体而言,该方法在温和的条件下实现多个化学键的构建,并展现了良好的官能团兼容性。
1.3 C(sp3)—H键的酰基化反应
2023年,Scheidt等[21]利用三氯化铈催化,在空气氛围和390 nm波长光照下,采用稳定的2-酰基二唑试剂为酰基来源,实现未活化烷烃 C(sp3)—H键的酰化反应(图5)。类似地,该反应通过LMCT过程生成氯自由基作为HAT试剂,实现对C(sp3)—H的HAT,产生相应的烷基自由基。该反应对碱的碱性有一定要求,较弱的碱无法满足反应的需求;对氯离子添加剂进一步研究发现,KCl在该反应中表现出明显的抑制作用。
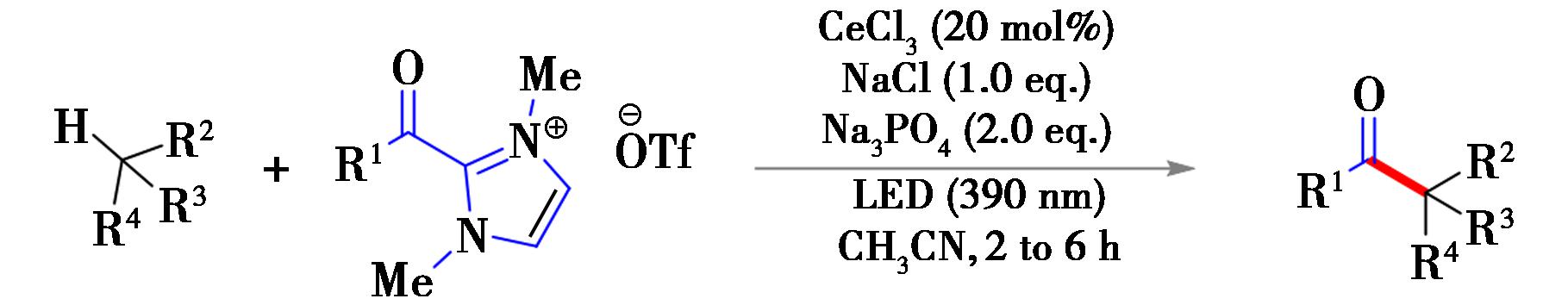
图5 酰基二唑与未活化烷烃C(sp3)—H键酰化反应[21]Fig.5 Acylation reaction of C(sp3)—H bonds in unactivated alkanes with acyl azoles[21]
基于该催化体系,加入手性的氮杂环卡宾(NHC),通过NHC-1和三氯化铈双催化,可以实现酰氟化合物与乙苯反应,生成不对称的酮羰基化合物(图6)。在反应过程中,[CeCl6]3-与酰基二唑试剂经过SET过程会产生寿命较长的阴离子自由基。随后通过由原位LMCT进程产生的氯自由基,经HAT过程产生烷基自由基与上述阴离子自由基反应,产生Breslow中间体,最终通过卡宾中间体释放羰基官能团化产物。
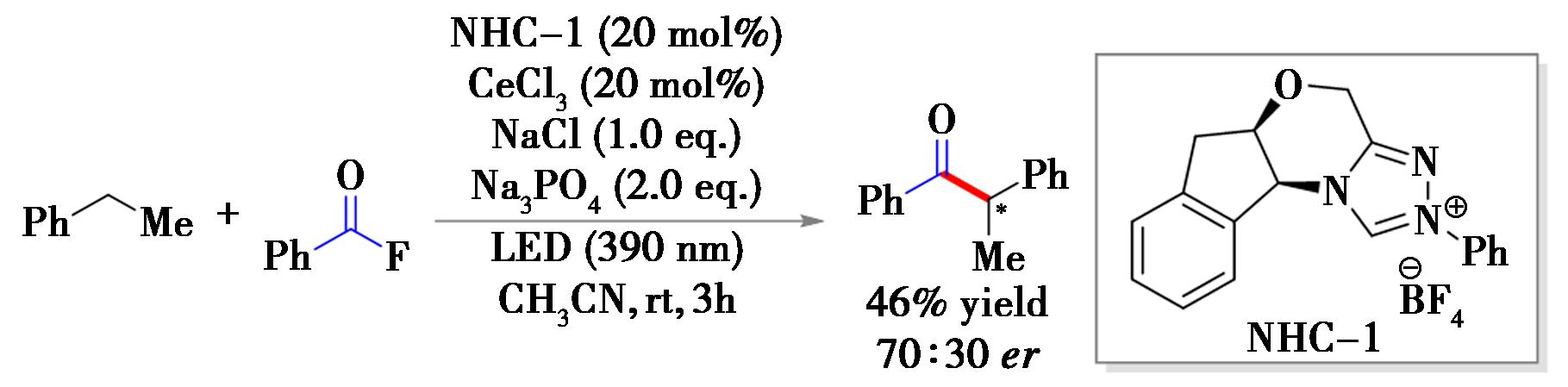
图6 乙苯的立体选择性酰基化反应[21]
Fig.6 Stereoselective acylation of ethylbenzene[21]
2 醇的脱羟基转化
醇类化合物在自然界中广泛存在,是一类易于获取的化学原料。在醇的脱羟基转化路径中,传统策略是添加质子酸对其进行质子化,通过失水之后产生相应的碳正离子,进而发生后续转化。这种经典的反应策略通常需要消耗一定量的质子化试剂。近年来,用醇作为反应原料,通过不同的催化策略实现其脱羟基转化合成更高附加值的有机化合物引起了广泛关注[22,23]。其中,三氯化铈光催化是一类非常重要的策略。
2018年,Zuo等[24]在空气氛围和395 nm波长的光照下,利用三氯化铈和9-,10-二苯基蒽(DPA)的协同催化作用,实现了环烷基醇7a与丁烯酸酯7b生成桥环内酯7c的反应(图7)。反应中,反应底物环烷基醇7a脱质子后,与铈中心配位,光照下经历LMCT历程,产生相应的烷氧自由基7d;随后经历β-断裂过程,产生相应的C-中心自由基7e;随后,与化合物7b进行自由基加成生成α-羰基自由基7f;中间体7f在光催化SET还原作用下生成相应的烯醇负离子7g,随后经历分子内的Aldol反应、分子内酯交换反应获得产物7c。该反应体系对于醚、酰胺和卤素原子在内的各种官能团都具有良好的耐受性;对于容易发生过渡金属插入的官能团,如环丙烷、氰芳烃和芳基溴化物,在该铈催化体系中也能很好地兼容。
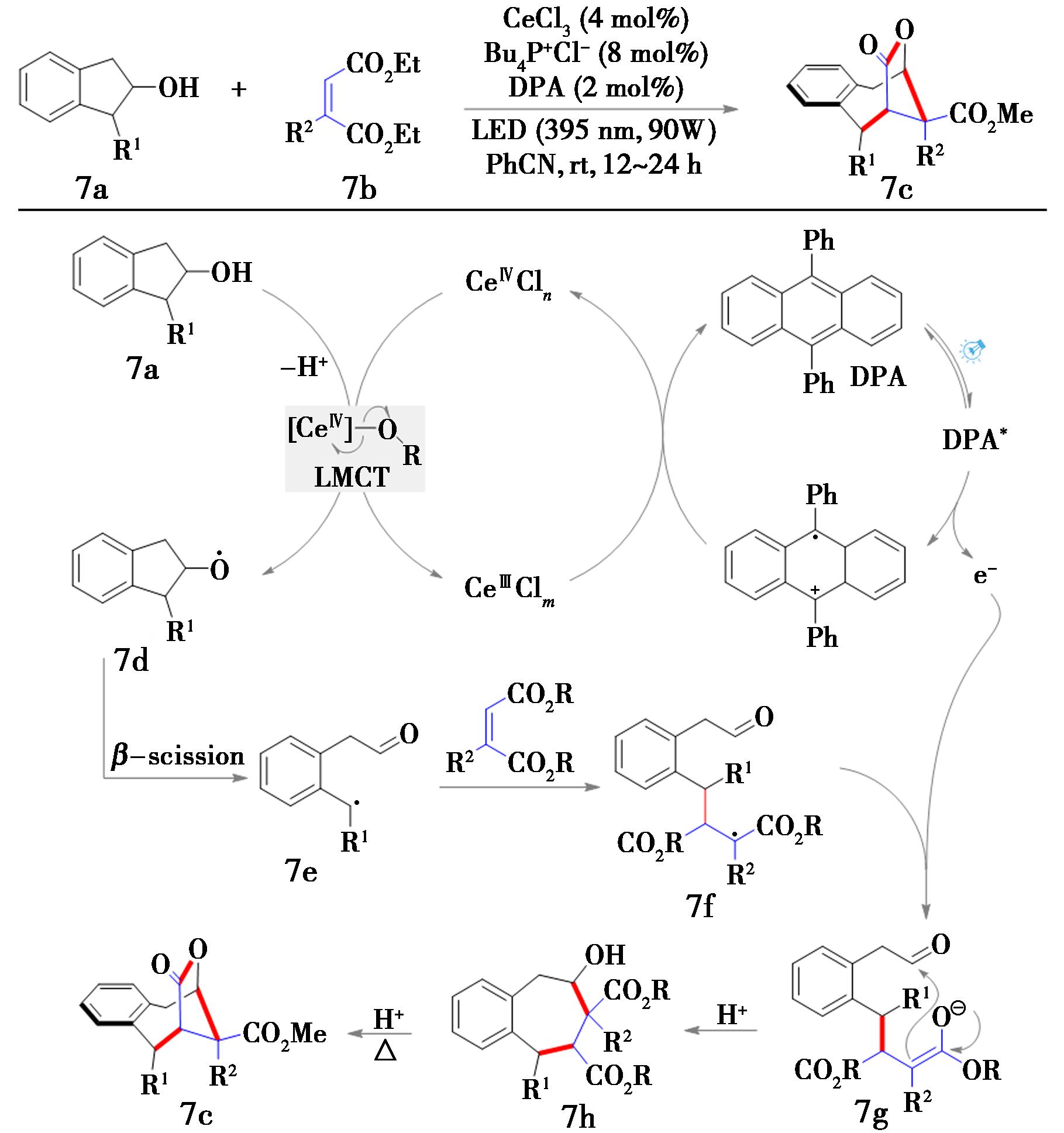
图7 环烷基-醇与丁烯酸脂的内酯化反应[24]
Fig.7 Lactonization reaction of naphthenic alcohol and crotonate[24]
按照上述反应机制,醇类底物在生成相应烷氧基自由基7d的过程中,容易发生β-切断反应(7d→7e)。如果该过程发生在链状的醇上,通过β-切断过程就可以实现羟甲基的切断。随后,在2019年,Zuo等[25]以烷基取代甲醇位,在385 nm光照下,使用三氯化铈催化,实现C—C键切断,实现脱羟甲基,并且与活化烯烃发生加成反应(图8)。反应通过使用四丁基溴化铵作为添加剂,避免了杂原子参与Michael加成的副反应。反应不仅能够完成醇类的脱羟甲基的酯基化,还可用于烷基化、氢化、胺化、烯基化和氧化转化反应,适用于多种醇类底物的片段偶联转化反应。
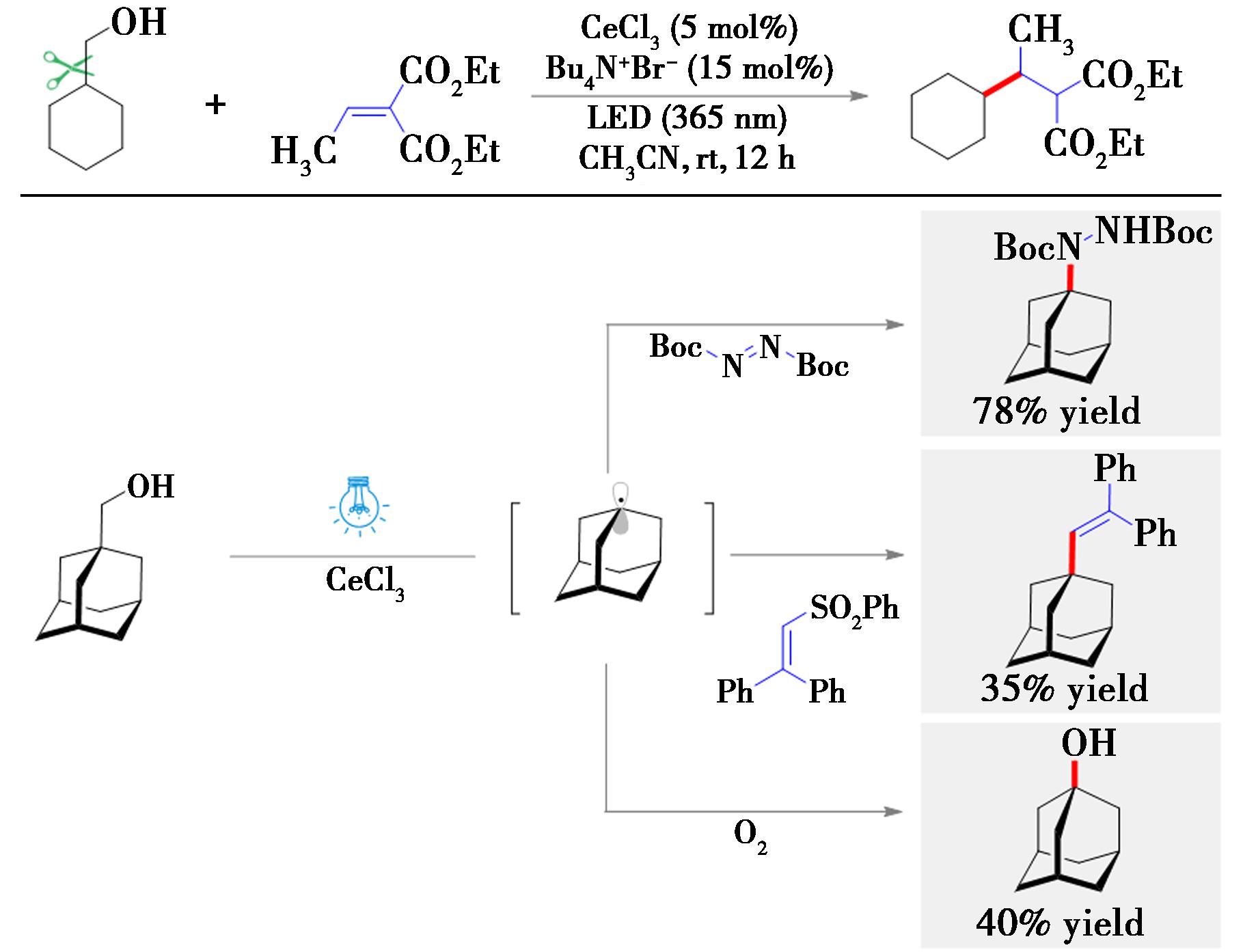
图8 烷基取代甲醇的脱羟甲基化反应[25]
Fig.8 Demethylolation reaction of alkyl-substituted methanol[25]
在实现上述“脱羟甲基反应”之后,Zuo等[26]进一步将脱羟甲基的步骤与镍催化的偶联反应结合:在蓝光照射下,以DPA作为光催化剂,通过三氯化铈与Ni的协同催化,实现伯醇脱羟甲基与芳基卤化物的交叉偶联构建C(sp3)—C(sp2)反应(图9)。反应使用Ni(dMebpy)(H2O)4Cl2作为催化剂,避免了单独使用镍与联吡啶配位时,游离的联吡啶对于LMCT进程的抑制作用。体系能够兼容各种具有含氮、氧原子的伯醇,并且对多种杂环也可作为底物,包括吲哚、噻吩、吡啶等。常见官能团,包括卤素、烷氧基、三氟甲基等,同样具有良好的耐受性。在反应的过程中,没有观察到α-C—H芳基化或C—O交叉偶联产物。
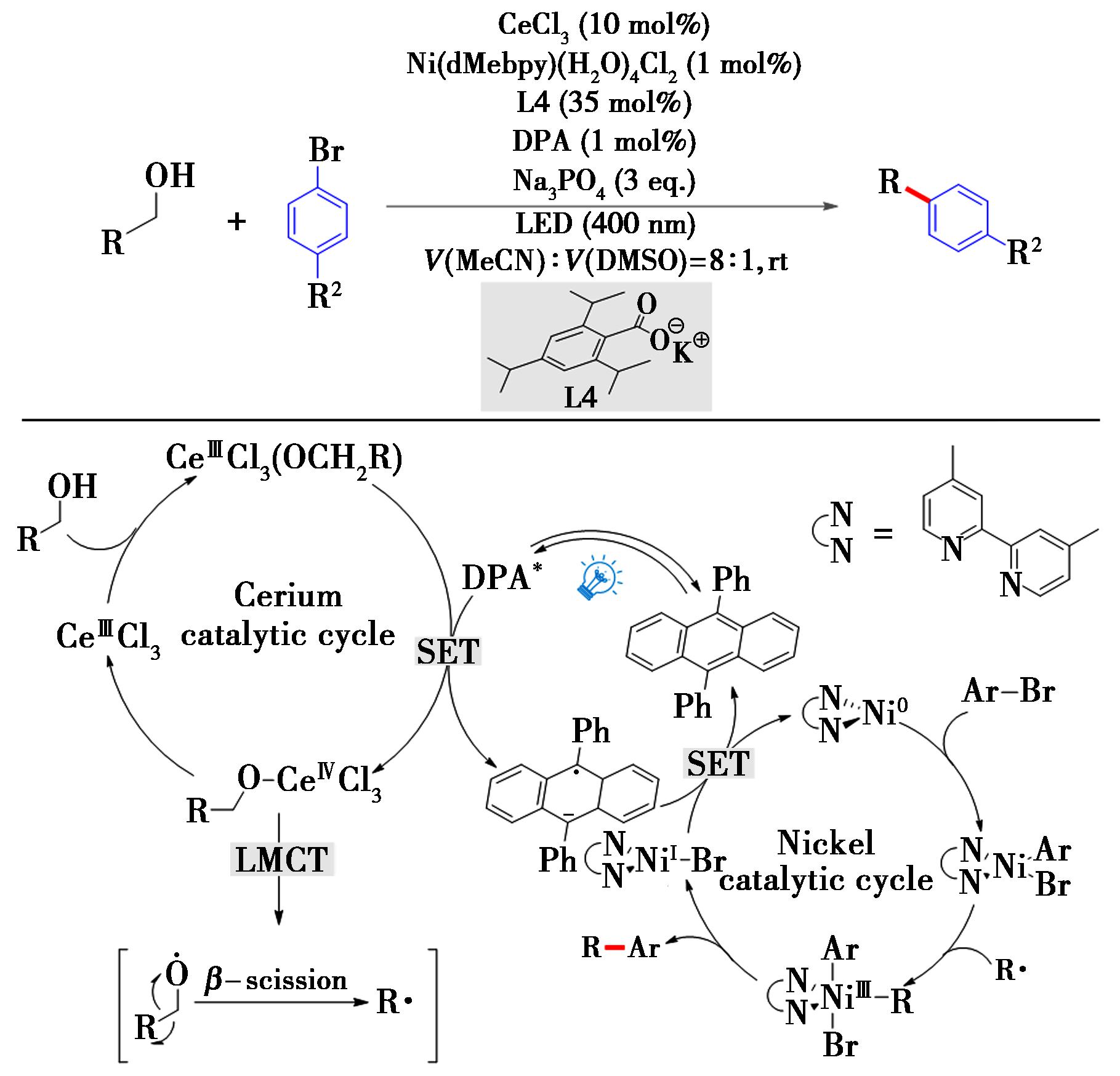
图9 伯醇脱羟甲基与芳基溴化物交叉偶联反应[26]
Fig.9 Cross-coupling reaction of primary alcohols dehydroxymethylative and aromatic bromides[26]
与“脱羟甲基反应”的不相同的是,Lei等[27]基于烷氧基自由基可以发生β-切断的特点,采用光电催化的策略,实现了环状烷基醇的开环官能团化反应。在2 mA恒电流和蓝光照射下,利用三氯化铈催化,实现了环醇的开环端位官能团化(图10),并且在反应中将羟基转化为羰基。光催化过程中实现了LMCT进程,利用电催化将芳基磺酰自由基转化为亚磺酸根,推动反应的进程。该光电催化体系不仅能够实现三至七元环等多种环醇的β-切断,选择性生成C—CN、C—S、C—Cl等,还能够兼容多种杂环,如四氢吡喃等。
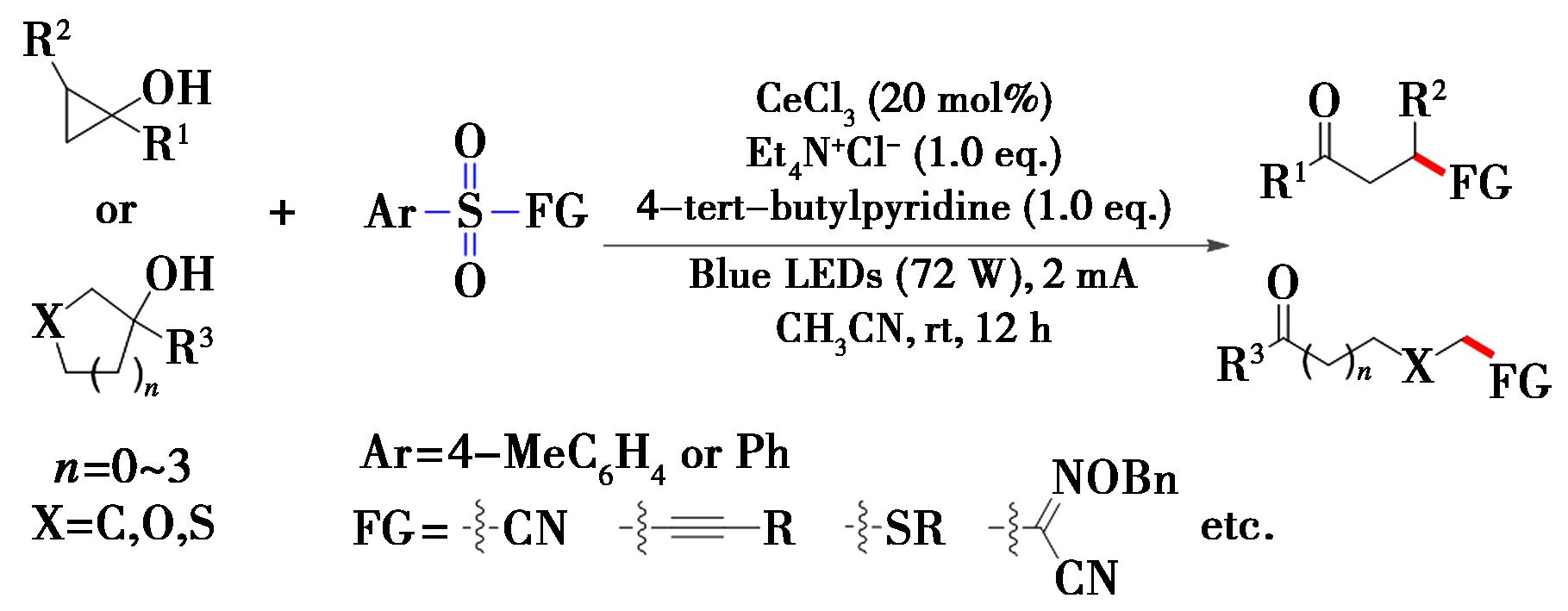
图10 环醇的开环端位官能团化反应[27]
Fig.10 Ring-opening terminal functionalization reaction of cyclic alcohols[27]
3 脱羧偶联反应
羧酸是大自然中广泛存在的一类化合物。此外,羧基具有丰富的官能团转化反应,在有机合成中得到广泛的应用[28]。在羧酸的转化路径中,通过脱羧反应生成自由基或其它活性中间体,进而实现后续偶联转化,是一种简便而高效的合成策略。近年来,以CeCl3为催化剂,通过配体到金属的电荷转移(LMCT)过程实现的脱羧官能团化反应取得了显著进展。
3.1 脱羧烷基化反应
2020年,Xu等[29]通过光电催化的策略,即在2 mA电流以及392 nm波长照射下,利用三氯化铈催化实现芳杂环11a与羧酸11b的脱羧烷基化(图11)。Ce(Ⅲ)在阳极被氧化为Ce(Ⅳ),与羧酸11b进行配位生成11d,通过LMCT进程,恢复到Ce(Ⅲ)并产生羧基自由基11f,随后经过脱羧,产生烷基自由基11g,随后化合物11g经过Minisci反应历程,加成到质子化的氮杂环11e上,产生中间体11h,随后经过脱质子、单电子氧化等步骤生成最终的烷基化杂环产物11c。该反应的区域选择性优异,避免了传统Minisci反应的多取代副产物的生成。
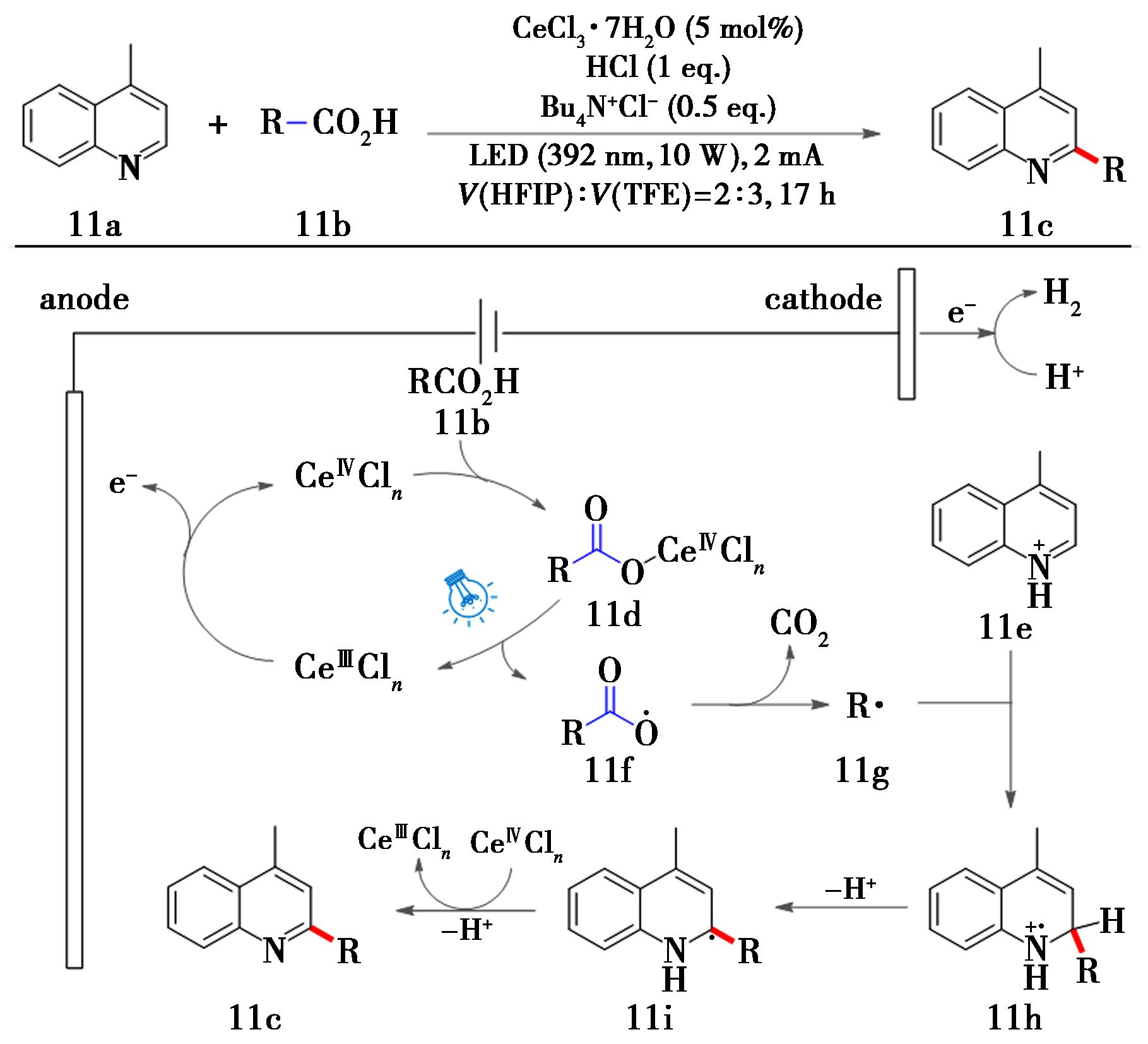
图11 4-甲基喹啉与羧酸的脱羧烷基化反应[29]
Fig.11 Decarboxylation alkylation reaction of 4-methylquinolines and carboxylic acids[29]
2022年,Roy等[30]在空气氛围中,427 nm的波长光照下,利用三氯化铈催化,实现了N-甲基喹喔啉-2(1H)-酮与羧酸的脱羧烷基化反应(图12)。该反应在碱性条件下进行,使用叔丁醇钾(tBuOK)作为碱,其发挥双重关键作用:一方面作为碱调控反应体系酸碱度,为反应提供适宜的碱性环境;另一方面,其解离产生的叔丁基氧阴离子(tBuO-)可作为配体与铈催化剂配位,参与光诱导的LMCT过程。多种羧酸均能良好地发生反应,生成相应的烷基化产物。同时,对于含有卤素、烷氧基的喹啉、喹啉酮、异喹啉等杂环底物,也具有良好的兼容性。
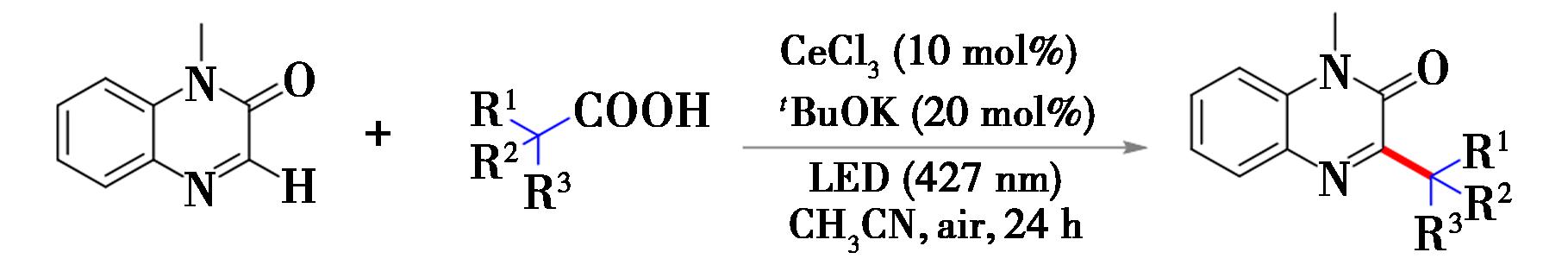
图12 N-甲基喹喔啉-2(1H)-酮与羧酸的脱羧烷基化反应[12]
Fig.12 Decarboxylative alkylation reaction between N-methylquinoxalin-2(1H)-ones and carboxylic acids[12]
同年,Roy等[31]采用类似的反应体系,以烷基羧酸为烷基化试剂,在空气中427 nm波长光照下,三氯化铈催化实现了香豆素双键的氢化/烷基化(图13)。其中,二级羧酸、二级α-氧代羧酸均有良好的反应;容易发生脱羧氧化的芳基乙酸类化合物,同样也能够产生良好收率。香豆素衍生物中,当苯环上连有供电子基团(甲基、甲氧基等)或者吸电子基团(卤素等),在该光催化条件下,均能顺利地发生反应。当香豆素3位上没有酯基或羰基取代基时,该脱羧烷基化反应无法发生;此外,当香豆素3位取代基为氰基时,烷基化反应也无法进行。这些结果表明香豆素底物中的3位取代羧基或酯基是非常关键的。
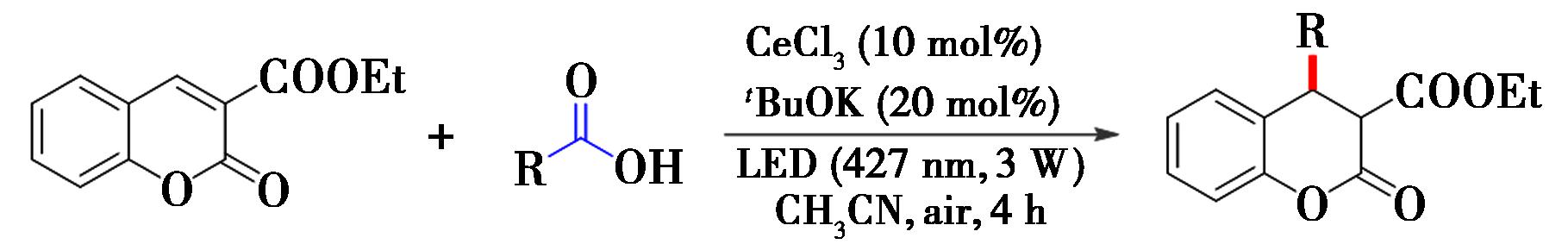
图13 香豆素衍生物的脱羧烷基化-氢化反应[31]
Fig.13 Decarboxylative alkylation-hydrogenation reaction of coumarins[31]
2022年,Shen等[32]同样以脂肪羧酸作为烷基自由基的前体,反应在空气氛围和蓝光照射下,利用三氯化铈催化实现了喹喔啉-2(1H)-酮的烷基化反应(图14)。当N原子上有烷基、烯基、苯基等取代基时以及苯环上连有卤素、硝基等取代基时均能顺利反应。在推测的反应机理中,二醋酸碘苯(PIDA)与反应体系中的羧酸发生配体交换生成高价碘中间体14d,在可见光照射下,发生I—O键异裂生成高价碘(Ⅲ)物种14e;化合物14e与Ce(Ⅲ)发生SET过程,生成化合物14i。另一方面,化合物14f与Ce(Ⅳ)配位,并通过LMCT进程产生羧基自由基14g,随后脱羧产生烷基自由基·R3。杂环底物14a与烷基自由基·R3加成,产生化合物14h;化合物14h与化合物14i经历SET过程生成相应的碳正离子中间体14j,随后经过去质子化生成产物14c,实现喹喔啉-2(1H)-酮分子中C-3位的烷基化修饰。
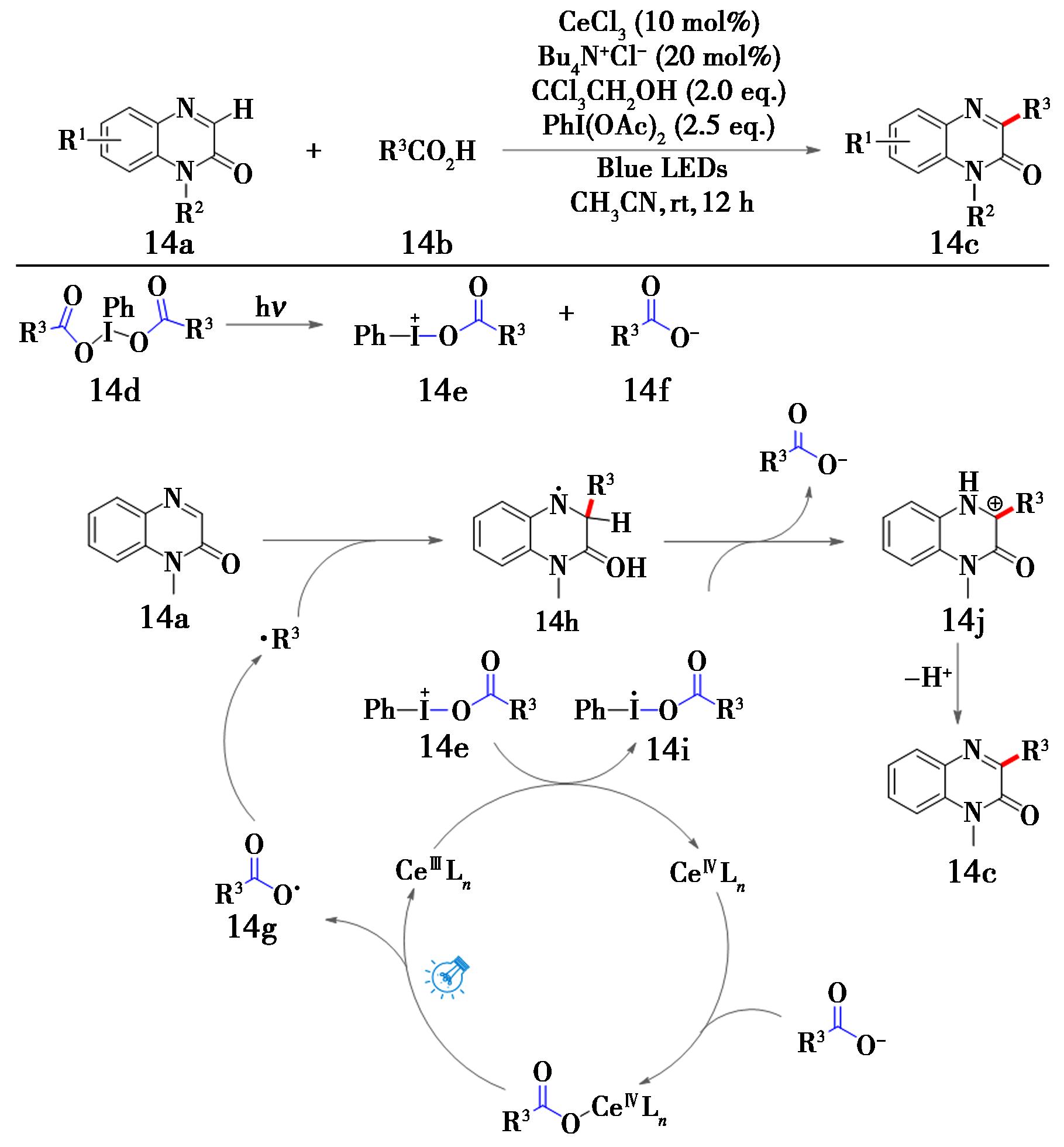
图14 喹喔啉-2(1H)-酮衍生物烷基化反应[32]
Fig.14 Alkylation reaction of quinoxalin-2(1H)-one derivatives[32]
3.2 脱羧官能团化反应
2022年,Yu等[33]在460 nm波长的光照下,通过铈催化“一锅煮”的方法,完成芳基异氰酸酯的烷基酰胺化反应(图15)。反应对于多种羧酸均有很好的兼容性,包括:一级羧酸、四元环到七元环的二级羧酸以及一些位阻较大的底物(1,4-苯并二噁烷)。反应对于多种吸电子基团(卤素、三氟甲基等)以及供电子基团(烷氧基、三氟甲氧基等)也有良好的兼容性。除此之外,当异氰酸酯上相连的取代基为芳基时,反应能够顺利进行;当取代基为烷基取代基时,几乎无反应产物生成。
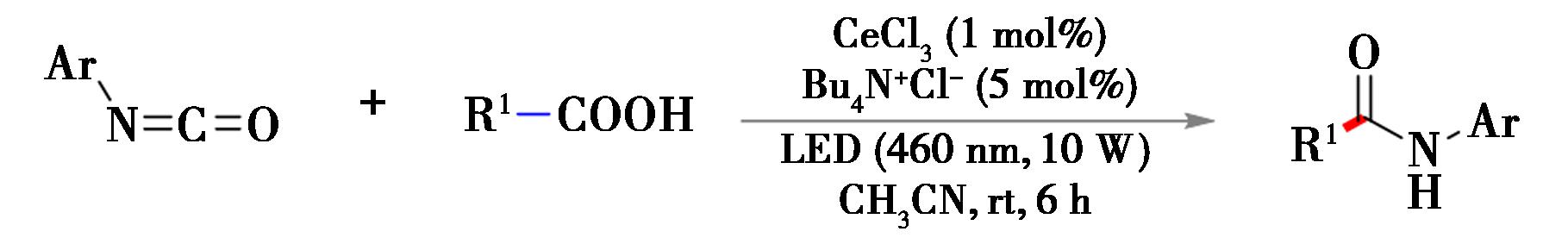
图15 羧酸与芳基异氰酸酯的脱羧酰胺化反应[33]
Fig.15 Decarboxylative amidation reaction of carboxylic acid with aryl isocyanate[33]
与前文所述环状烷基醇的开环端位官能团化反应类似[27],最近,Jin等[34]报道了在空气氛围和400 nm波长光照下,三氯化铈催化实现了环羧酸C(sp3)—C(sp3)键选择性断裂策略,实现了环状羧酸的脱羧开环官能团化反应(图16)。反应具有很好的兼容性,多种含有张力环和非张力环的环状羧酸以及含有吸电子基团(—CF3)或供电子基团(—tBu、—OMe)环状羧酸均有良好的兼容性。该反应直接利用空气作为氧化剂,合成了系列的端位官能化的羰基化合物。
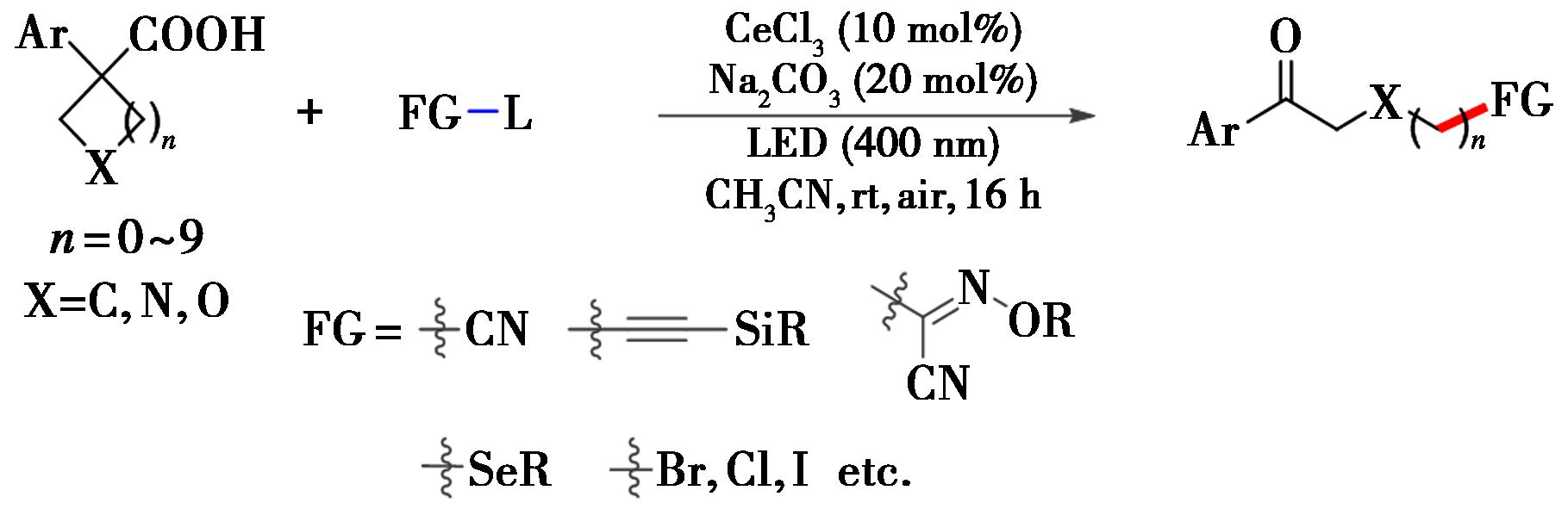
图16 环状羧酸的开环端位官能团化反应[34]
Fig.16 Ring-opening terminal functionalization reaction of cyclic carboxylic acids[34]
4 总结与展望
近年来,由于优异的光反应活性和LMCT催化性能,三氯化铈在光催化有机合成领域受到了广泛关注。本文综述了近年来光诱导三氯化铈催化构建碳-碳键的研究进展,主要包括:(1)C—H键官能团化反应;(2)醇的脱羟基转化反应;(3)脱羧偶联反应。
尽管可见光驱动三氯化铈催化的碳-碳键构建反应已取得显著进展,但该领域仍有广阔的发展潜力。未来的研究可着眼于探索更多新型的有机反应,尤其是具有特殊结构和功能的分子,如复杂天然产物类似物和新型功能材料单体等。此外,开发新的反应路径,如串联反应和多组分反应等,将有助于通过一步反应构建出更为复杂的碳骨架结构,极大地提升合成效率和分子多样性。
[1]Li S Q,Dong J.Curr.Org.Chem.,2023,27(12):1020-1035.
[2]Russo C,Brunelli F,Tron G C,Giustiniano M.J.Org.Chem.,2023,88(10):6284-6293.
[3]Victoria-miguel J,García-santos W H,Cordero-vargas A.J.Org.Chem.,2022,87(14):9088-9099.
[4]Wang Y,Wang J,Chen C,Song L H,Wang Z L,Wei W,Yi D.Chem.Commun.,2025,61(58):10812-10815.
[5]Zuo Z W,Macmillan D W C.J.Am.Chem.Soc.,2014,136(14):5257-5260.
[6]Zhang C C,Ding Q J,Lv Q Y,Ma C H,Jiang Y Q,Yu B.Chin.J.Org.Chem.,2025,45(10):3517.
[7]Hu A H,Guo J J,Pan H,Zuo Z W.Science,2018,361:668-672.
[8]Yuan X Y,Wang C C,Yu B.Chin.Chem.Lett.,2024,35(9):109517.
[9]Wadekar K,Aswale S,Yatham V R.Org.Biomol.Chem.,2020,18(5):983-987.
[10]Duan K H,Tang J L,Wu W Q.Chin.J.Org.Chem.,2023,43(3):826-854.
[11]Frank É,Szöllösi G.Molecules,2021,26(15):4617.
[12]Luo X Q,Huang Z H,He Y Q,Chen Q,Lin N.Chem.Reagents,2025,47(9):96-107.
罗小芹,黄桢惠,何依倩,陈清,林宁.化学试剂,2025,47(9):96-107.
[13]Tian J,Gao W C.Chem.Reagents,2025,47(7):10-17.
田俊,高文超.化学试剂,2025,47(7):10-17.
[14]Tong M N,Luo Y A,Guan X J,Wu Y L,Hu Y,Zhao Y F.Chem.Reagents,2024,46(9):66-80.
童梦楠,罗永安,管小军,吴翊乐,胡英,赵玉芬.化学试剂,2024,46(9):66-80.
[15]Lu Y H,Wu C,Hou J C,Wu Z L,Zhou M H,Huang X J,He W M.ACS Catal.,2023,13(19):13071-13076.
[16]Xiang P J,Yu B.Chin.J.Org.Chem.,2024,44(6):2057-2058.
[17]An J Z,Lv Q Y,Sun K,Chen X L,Qu L B,Yu B.Chin.J.Org.Chem.,2024,44(12):3747-3752.
[18]Xu J,Cai H,Shen J B,Shen C,Wu J,Zhang P F,Liu X G.J.Org.Chem.,2021,86(24):17816-17832.
[19]Zhou B,Dong M,Wang W,Yu S,Yue H L,Wei W,Yi D.J.Org.Chem.,2024,89(24):18337-18343.
[20]Zhang L T,He J J,Shen J B,Xu H,Zhu D C,Shen C.Org.Chem.Front.,2023,10(3):668-674.
[21]Cao J,Zhu J L,Scheidt K A.Chem.Sci.,2023,15(1):154-159.
[22]Cook A,Newman S G.Chem.Rev.,2024,124(9):6078-6144.
[23]Luo W,Chen Z,Yu B.Asian J.Org.Chem.,2025,14(3):e202400627.
[24]Hu A H,Chen Y L,Guo J J,Yu N,An Q,Zuo Z W.J.Am.Chem.Soc.,2018,140(42):13580-13585.
[25]Zhang K N,Chang L,An Q,Wang X,Zuo Z W.J.Am.Chem.Soc.,2019,141(26):10556-10564.
[26]Chen Y G,Wang X,He X,An Q,Zuo Z W.J.Am.Chem.Soc.,2021,143(13):4896-4902.
[27]Yang Z L,Yang D L,Zhang J Y,Tan C Y,Li J J,Wang S C,Zhang H,Huang Z L,Lei A W.J.Am.Chem.Soc.,2022,144(30):13895-13902.
[28]Tang S B,Zhao X B,Yang L D,Li B,Wang B Q.Angew.Chem.Int.Ed.,2022,61:e202212975.
[29]Lai X L,Shu X M,Song J S,Xu H C.Angew.Chem.Int.Ed.,2020,59(26):10626-10632.
[30]Singh S,Dagar N,Roy S R.Chem.Commun.,2022,58(23):3831-3834.
[31]Dagar N,Singh S,Roy S.J.Org.Chem.,2022,87(14):8970-8982.
[32]Zhang L X,He J W,Zhang P F,Zheng K,Shen C.Mol.Catal.,2022,519:112145.
[33]Li H C,Li G N,Sun K,Chen X L,Jiang M X,Qu L B,Yu B.Org.Lett.,2022,24(12):2431-2435.
[34]Xu Y,Wang J J,Zhang Q,Hu X Y,Lv C,Yang H,Sun B,Jin C.Angew.Chem.Int.Ed.,2025,64(19):e202500561.