大环化合物因其特殊的环状分子结构以及优良的功能特性,逐渐成为超分子化学研究的主要内容[1]。自1967年Pedersen[2]发现冠醚以来,其对碱金属、碱土金属的配位能力有助于生命过程中对离子(Na+、K+、Mg2+、Ca2+)的识别、运载等功能的理解,从而激励了人们对其研究[3]。历时50多年的研究和发展,大环化学的发展迅猛。早期对于冠醚、穴醚以及球醚的研究,科学家们逐渐揭示了超分子化学的基本概念,打破了传统化学的成键模式,以分子识别为基础、分子组装为手段、组装体功能为目标,奠定了超分子化学与大环化学的基础[4-9]。
鉴于大环化合物在气体吸附[10]、离子通道[11]、超分子两亲组装[12,13]、药物投递[14]以及超分子聚合物[15]等方面的广阔应用前景,对新型超分子大环的探索也从未停止。在最近的几十年的研究过程中,许多新颖的超分子大环化合物被报道出来,有很多具有非常独特的功能和性质[16]。新型大环化合物的合成与报道,足以见得人们对大环化合物的研究兴趣十分浓厚。
在这些被报道的新型大环化合物中,含蒽大环化合物因其结合了蒽的优异光物理性质和可调的大环空腔,已成为超分子化学和材料科学的前沿领域。通过精妙的分子设计,研究人员已经开发出多种合成策略,并探索了其在分子识别、刺激响应材料、光电器件和复杂组装体等方面的广泛应用。本文对2015~2025年报道的含蒽大环化合物进行了归纳。介绍了此类大环化合物的合成及其功能,旨在为今后含蒽大环化合物的合成与应用提供参考。
1 有机含蒽大环化合物
由有机官能团(酰胺键、醚氧键、脲键、硫脲键、席夫碱、炔键等)与蒽分子连接而成的大环化合物,其结构中不仅含有蒽分子较大的疏水刚性平面和较强的荧光特性,而且还具有有机官能团的性能。与其他的超分子主体相比,有机含蒽大环化合物可以为主体提供额外的分子间大π键,以增强其分子识别以及自组装等方面的特性[17,18]。
Smith等[19,20]一直从事含蒽大环化合物的特性研究。报道了此类由酰胺键大环化合物与方酸衍生物构建的轮烷,在红光照射条件下可以吸收空气中的氧气分子并形成新的内过氧化物的轮烷结构(图1)[16]。
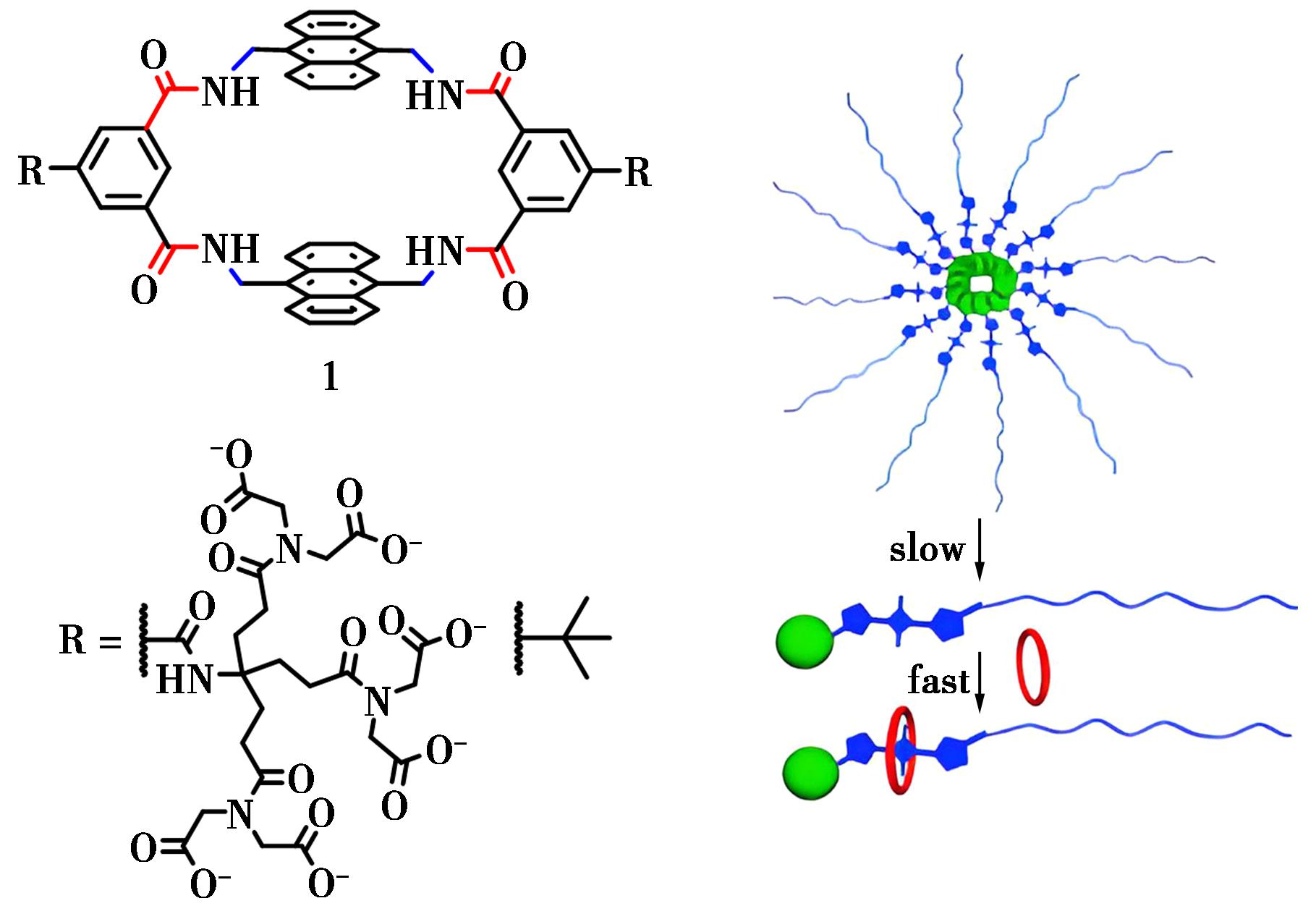
图1 含蒽大环化合物1的结构和分子识别行为[16]
Fig.1 Structure of the macrocycles 1 with anthracene and molecular recognition behavior[16]
同时,该课题组研究的含酰胺键构建的含蒽大环化合物1,不仅在不同的溶剂环境下实现了有机染料分子的识别,通过对大环结构的修饰,也在阴离子识别![]() 取得了一定进展[21,22]。
取得了一定进展[21,22]。
Yamaguchi等[23]报道了基于炔键连接的双蒽大环化合物2并详细研究了其晶体结构。通过改变大环分子左右两侧的烷基侧链的长度,分子间可以通过蒽结构单元的π-π堆积作用形成结构不同的晶型。当左右两侧的烷基侧链的长度均为7个碳原子时,大环分子间可以形成一种高度弯曲的晶型结构(图2)。
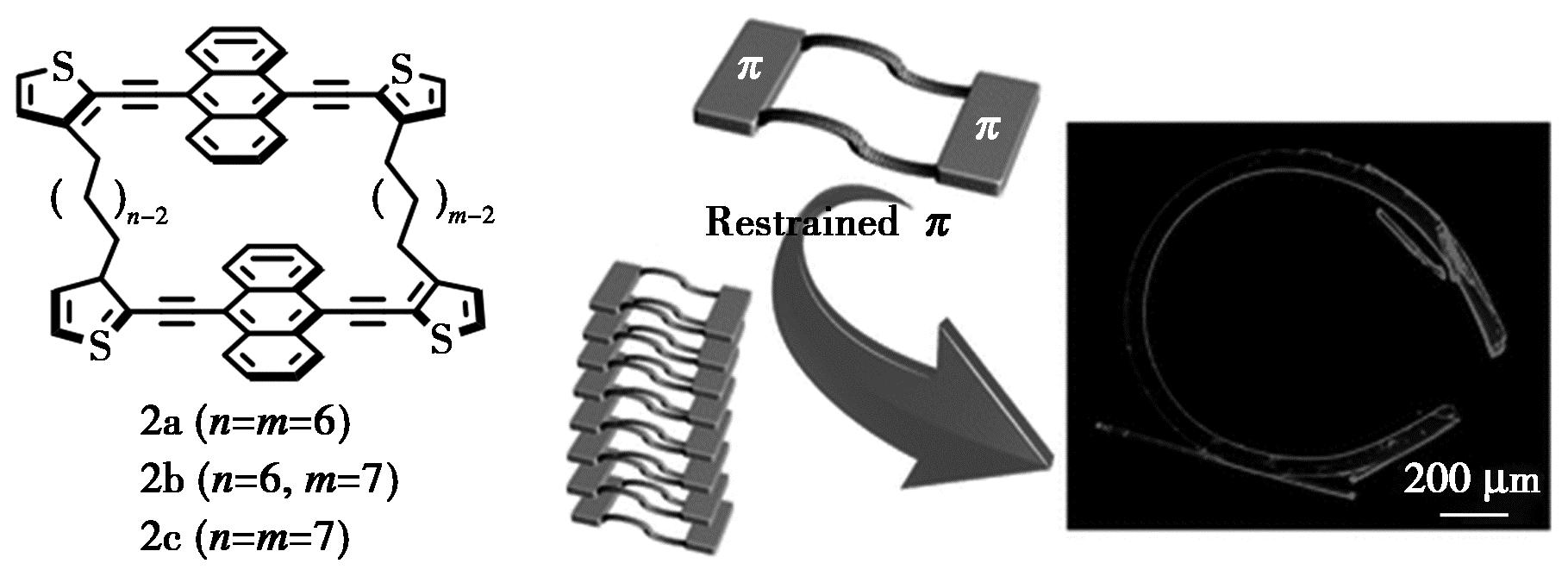
图2 基于炔基构建的含蒽大环化合物2a~2c[23]
Fig.2 Macrocycles 2a~2c connected via various combinations of alkylene linkers with anthracene[23]
Farr na等[24]运用10-己基-8-羟基异咯嗪与 1,5-双溴取代蒽作为反应原料,在一定条件下制备出两种含蒽大环分子3a、3b,产率均达到10%,大环分子的结构通过核磁共振谱以及X-单晶衍射得到了证实。在此基础上,该小组研究了两种大环分子因烷基链长的改变导致光诱导电子转移效应(PET)的差别。同时,在室温与77 K温度下,运用连续光波诱导吸收法(cw-PIA)等物理方法研究了因蒽结构单元引起的π-π堆积作用是导致的大环分子的光学性能改变的关键因素(图3)。
na等[24]运用10-己基-8-羟基异咯嗪与 1,5-双溴取代蒽作为反应原料,在一定条件下制备出两种含蒽大环分子3a、3b,产率均达到10%,大环分子的结构通过核磁共振谱以及X-单晶衍射得到了证实。在此基础上,该小组研究了两种大环分子因烷基链长的改变导致光诱导电子转移效应(PET)的差别。同时,在室温与77 K温度下,运用连续光波诱导吸收法(cw-PIA)等物理方法研究了因蒽结构单元引起的π-π堆积作用是导致的大环分子的光学性能改变的关键因素(图3)。
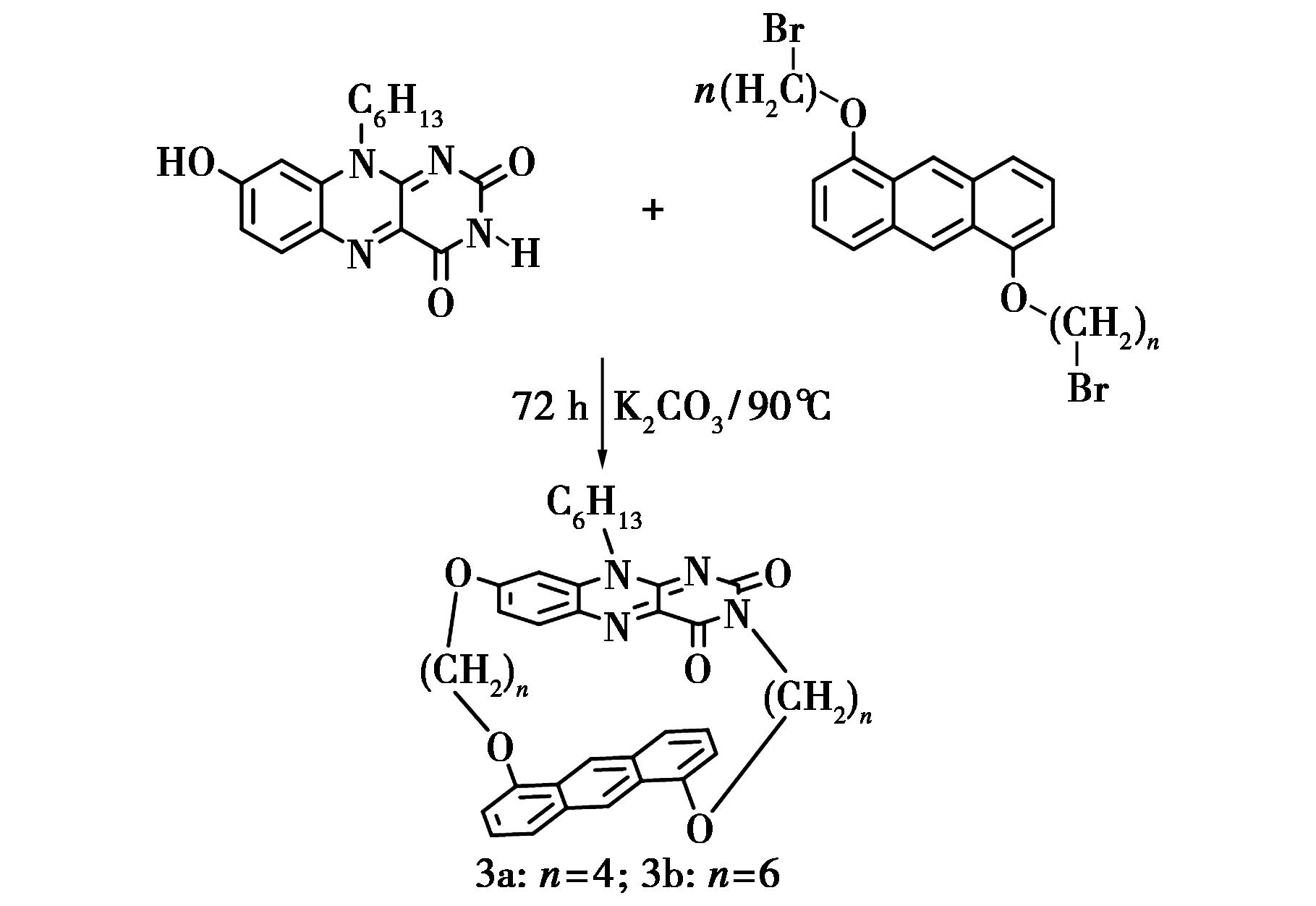
图3 含蒽大环化合物3a、3b的合成[24]
Fig.3 Synthesis of the anthracene-containing macrocycles 3a and 3b[24]
Yamaguchi等[25]以具有较强荧光吸收和发射的分子骨架化合物5作为结构基元,通过改变大环分子左右两侧的烷基侧链的长度,设计合成了3种不同的大环分子(4a~4c),详细研究了此类大环化合物的荧光寿命等性能。通过化合物4a与化合物5的紫外/荧光发现:相同条件下二者的紫外吸收光谱的变化不大;而荧光发射光谱却有较大的差别,并且具有较高的荧光量子产率(0.81)和较高的亮度(52400 mol/(L·cm)),而化合物5仅在波长503 nm处有荧光发射。而化合物4a的双重荧光发射光谱特性主要是由于自身分子内的基态原子发射所致。改变大环分子两侧的烷基侧链的长度(化合物4b、4c)以及连接方式(化合物6、7),证实烷基侧链的长度及连接方式直接决定该类大环分子的荧光特性(图4)。
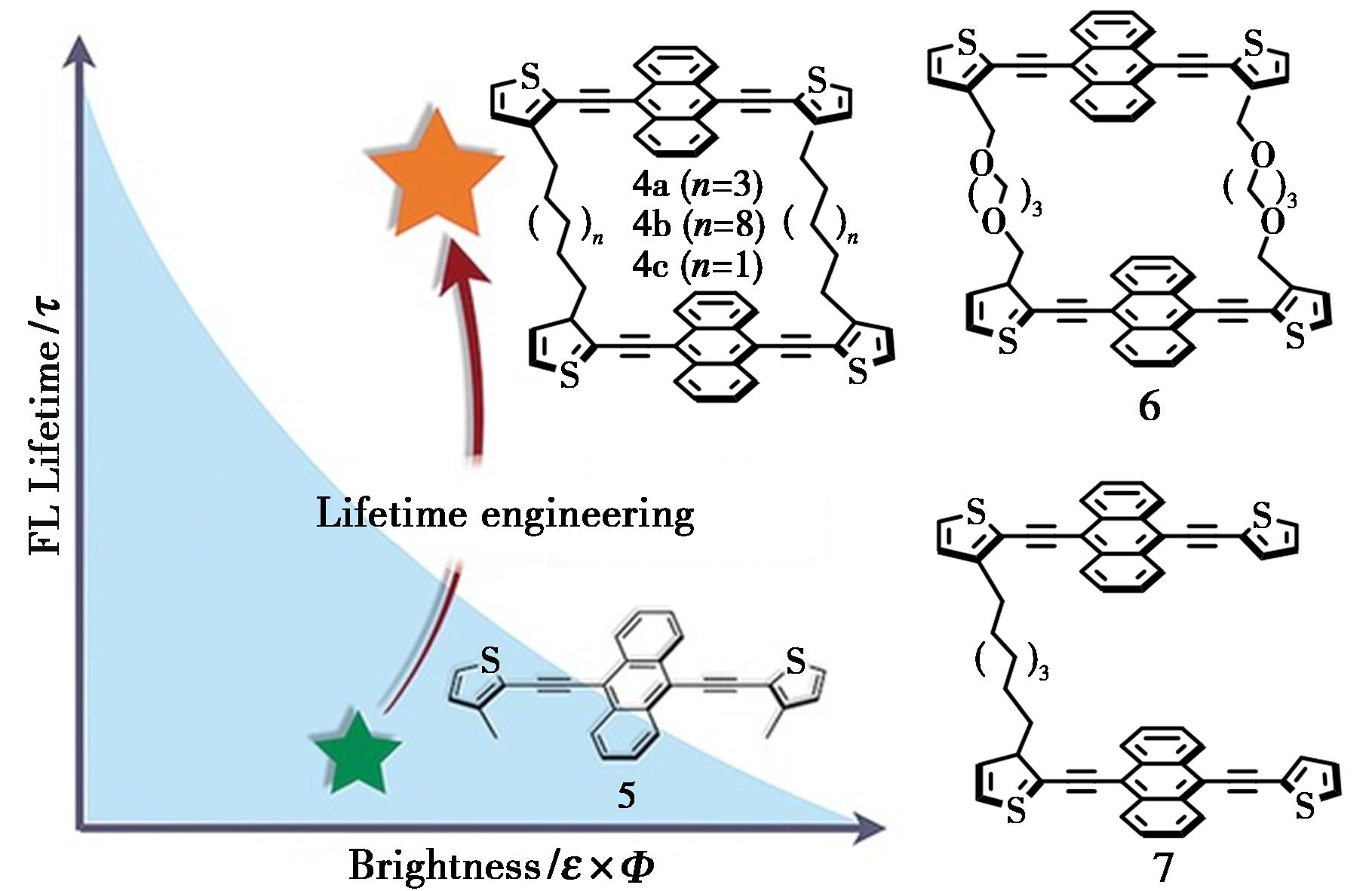
图4 不同的含蒽结构单元化合物[25]
Fig.4 Different anthracene-containing structural unit[25]
2016年,Kobayashi等[26]以2,7-取代蒽为反应原料,经过多步有机反应合成得到含蒽的大环化合物8,最终产率达到22%。运用分子模型进行密度泛函理论计算(DFT calculation)发现,该大环化合物具有1个C3对称轴,并且在结构上呈现出等边三角形的平面分子构型(图5)。该小组通过核磁共振氢谱详细研究了影响分子刚性平面构型的因素,浓度和溶解温度是至关重要的。在303 K的氘代氯仿环境中,大环化合物8有较强的分子间π-π堆积作用,缔合常数达到KE=6980 mol/L。粉末衍射(XRD),扫描电镜(SEM)以及切线入射-X射线衍射(GI-XRD)技术显示大环化合物8呈现一种螺旋形三维空间立体的晶型结构,通过分子内的3条关于C3轴对称的烷基链之间的范德华力自组装形成六边形的纳米纤维管。
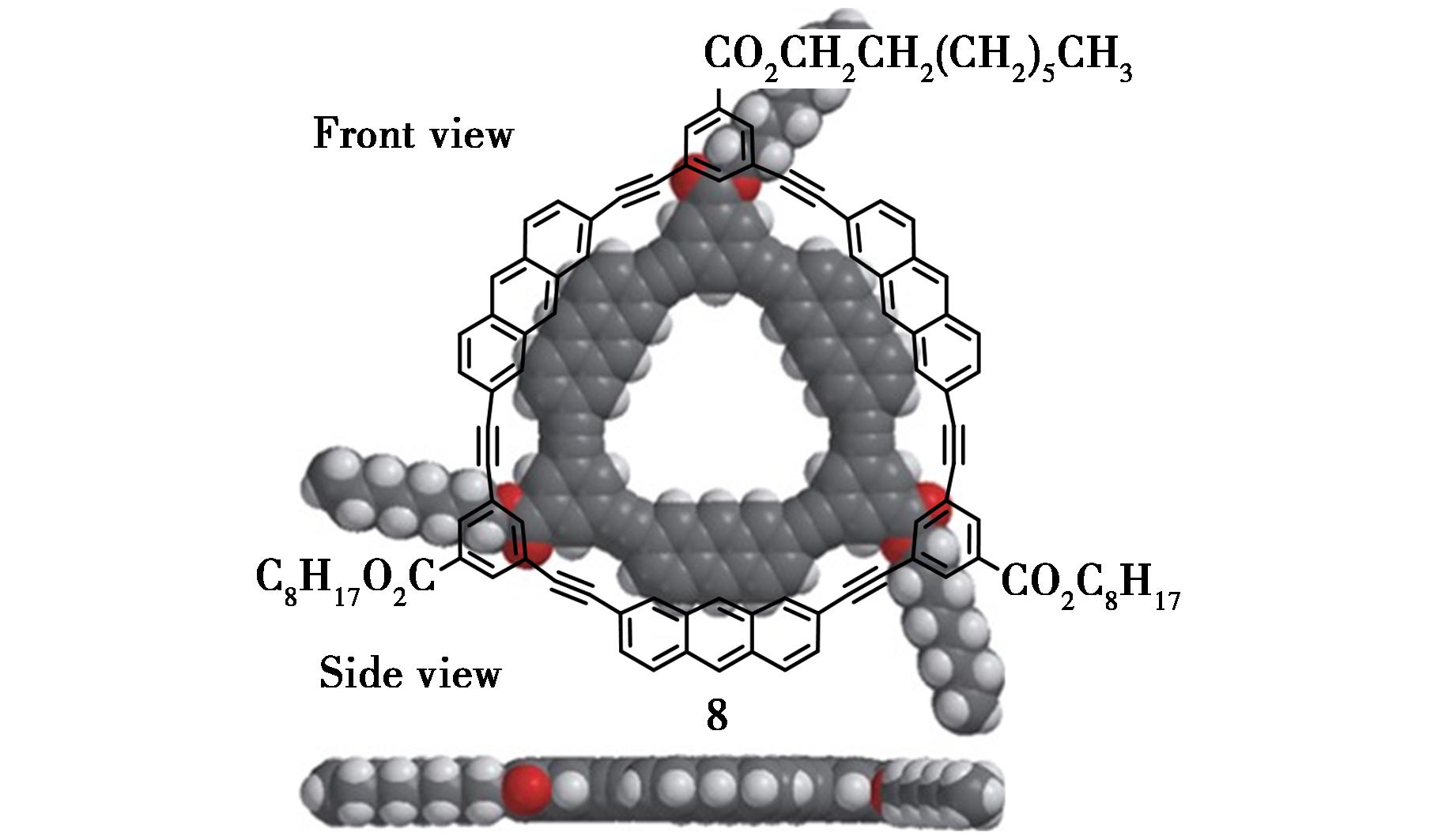
图5 含蒽大环化合物8的分子结构[26]
Fig.5 Structure of anthracene-containing macrocycle 8[26]
Toyota等[27]对基于蒽构建的含炔/烯大环化合物的研究持续火热。在1,8-取代蒽构建的含烯大环化合物的研究方面,该小组成功合成了具有(Z)-构型烯烃连接的大环化合物9,发现这类大环分子具有较为柔和的非平面结构。该课题组以1,8-二炔基蒽作为反应基元,运用不同的有机反应策略合成几种具有立体异构的大环化合物(如化合物10、11),详细介绍了该类大环化合物的结构合成,修饰以及主客体配合性质(图6)[28,29]。
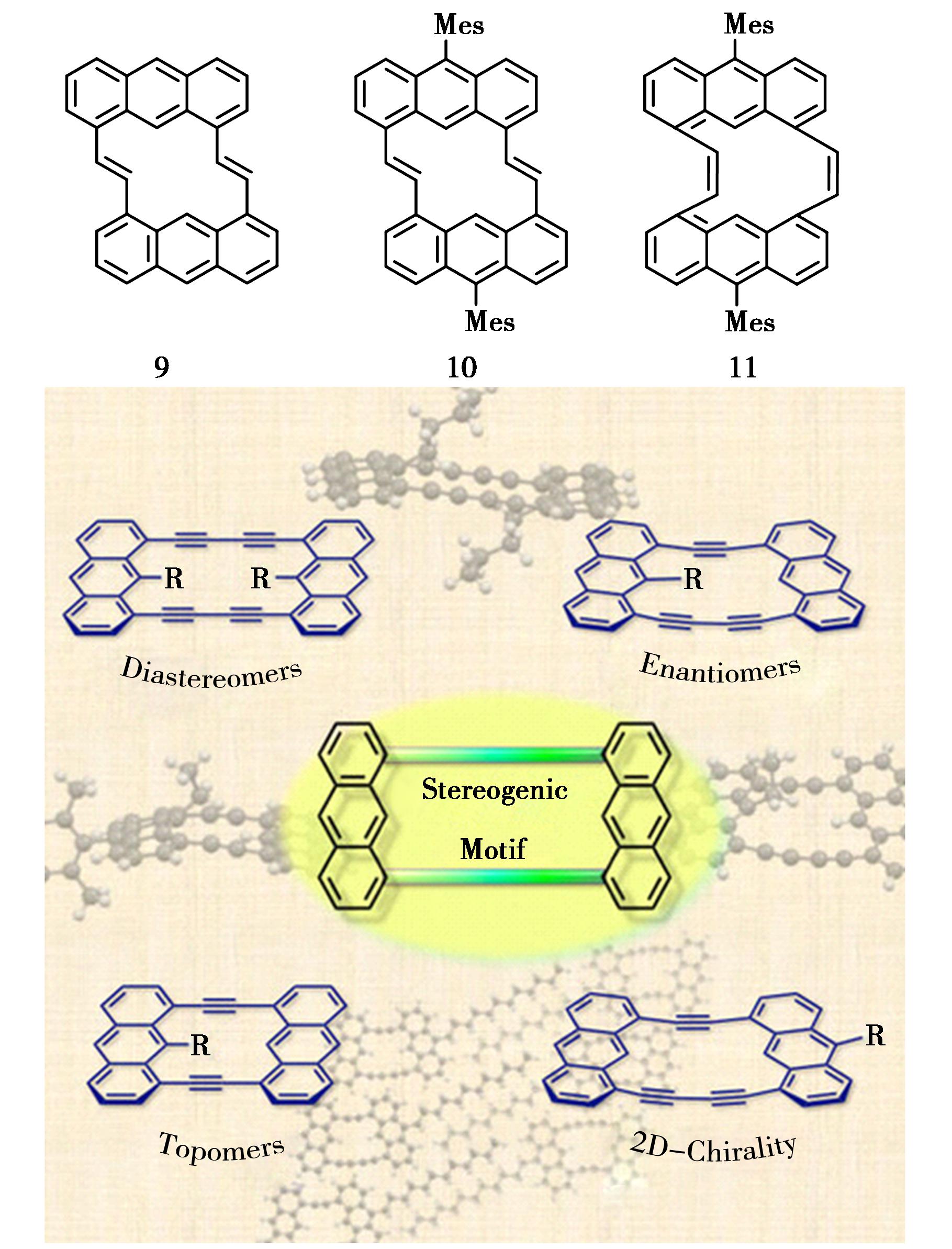
图6 含蒽大环化合物9、10、11的分子结构[27-29]
Fig.6 Structures of the anthracene-containing macrocycle 9,10 and 11[27-29]
由2,7-二取代蒽为结构单元构建的大环化合物的研究受到了广泛关注[30],然而其较大的分子结构和较强的刚性严重影响大环分子的稳定性和溶解性。Toyota等[31]结合之前的工作基础,以2,7-取代蒽的9,10-位引入芳烃取代基的衍生物为反应原料,在镍催化剂的作用下分别通过一步法,分步法均可以得到结构稳定性强,且在有机溶剂中溶解性较好的大环化合物12,产物通过核磁(NMR)、高分辨质谱(HRMS)得到表征。X-单晶衍射证实,该大环化合物含有6个蒽的结构单元,大环的外径达到2.0 nm,分子呈现出六边形的非平面空间结构(图7)。该小组还运用了核磁技术详细的研究了其分子结构转化的动力学过程。
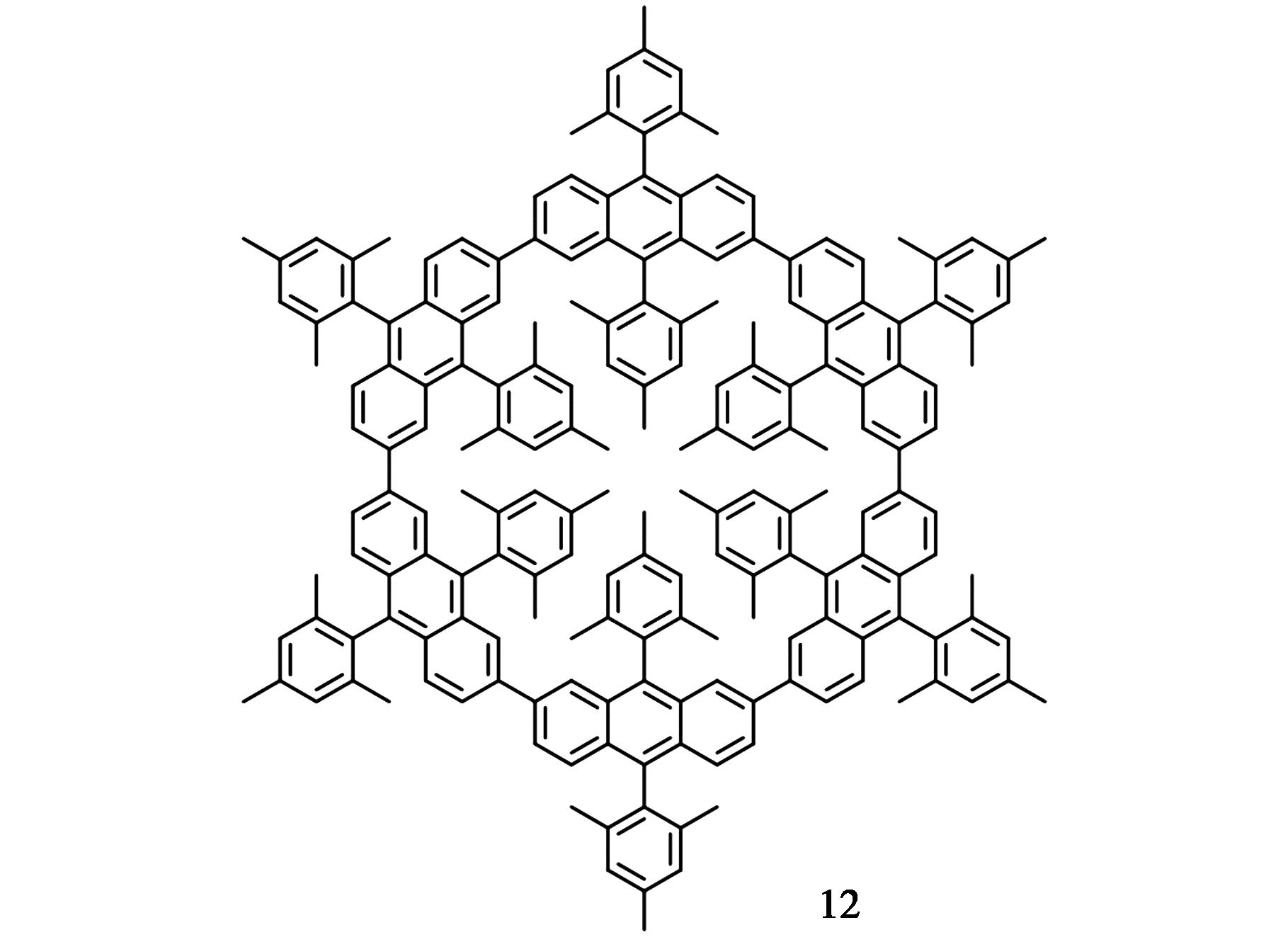
图7 含蒽大环化合物12的分子结构[31]
Fig.7 Structures of anthracene-containing macrocycle 12[31]
为了进一步探索由2,7-二取代蒽为结构单元构建的大环化合物的主客体识别性能,2018年,Toyota等[32]继续在大环化合物12的基础上做了修饰,更改侧链基团得到大环分子13,增加其溶解性能的同时,并没有改变其空腔的大小及结构。该小组发现大环化合物13可以与C60在甲苯作溶剂中形成较好的物质的量之比为1∶1的复合物。室温下,键合常数达到2.3×103 mol/L。X-单晶衍射也证实C60分子较好的进入主体分子的空腔内部,通过多重分子间的CH…π作用形成较好的配合作用(图8)。
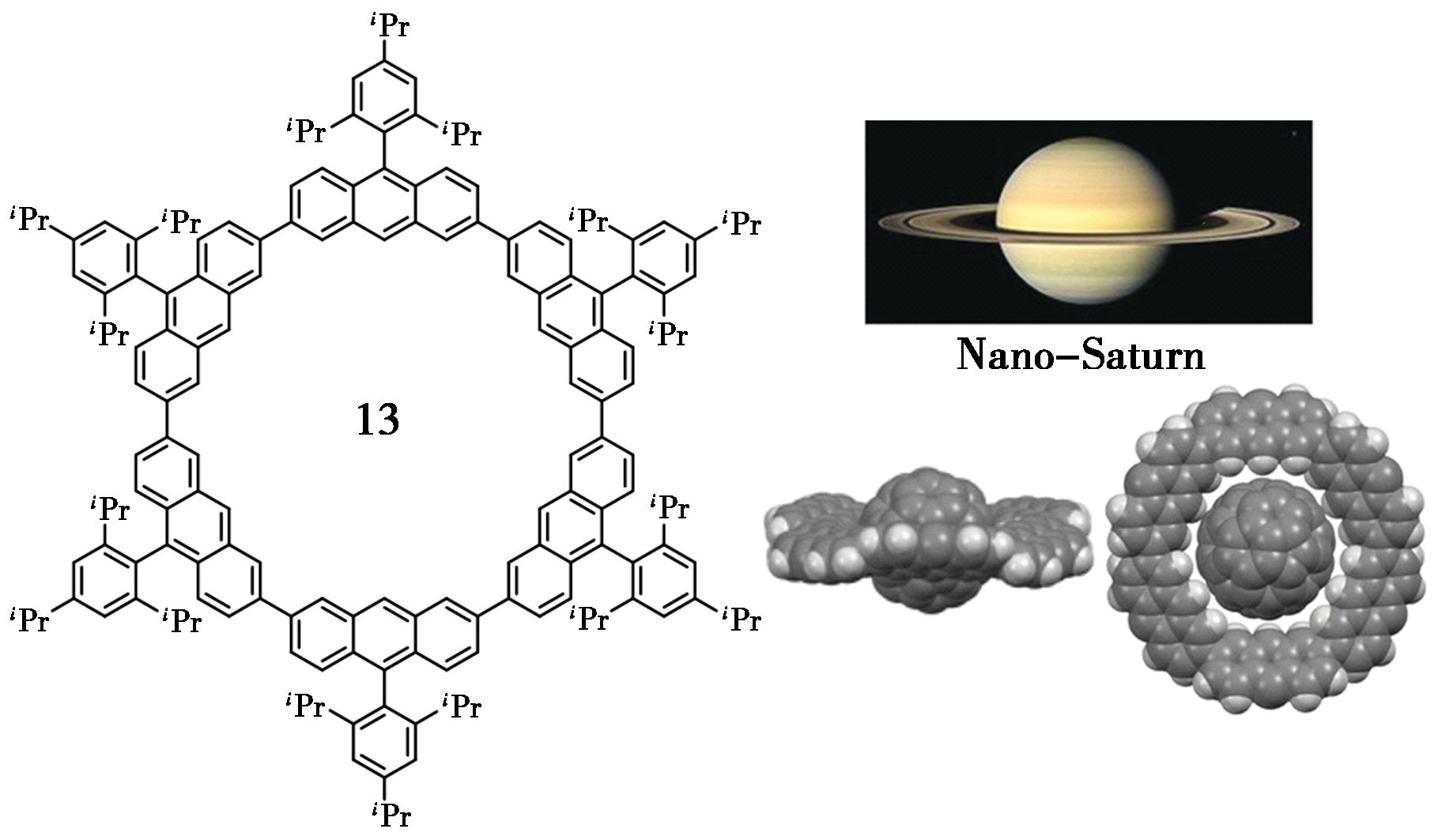
图8 含蒽大环化合物13的分子结构[32]
Fig.8 Structure of anthracene-containing macrocycle 13[32]
此外,Toyota通过Suzuki-Miyaura耦合和Yamamoto耦合两个耦合反应,合成了由Ant单元和Trip单元组成的3个大环笼(化合物14、15、16)。通过 1HNMR和荧光光谱证实,这些笼子与富勒烯客体形成物质的量之比为1∶1的包合物。由于非共价相互作用的增加,笼对C70客体相对于C60客体和功能化C60具有较高的亲和力(图9)[33-36]。
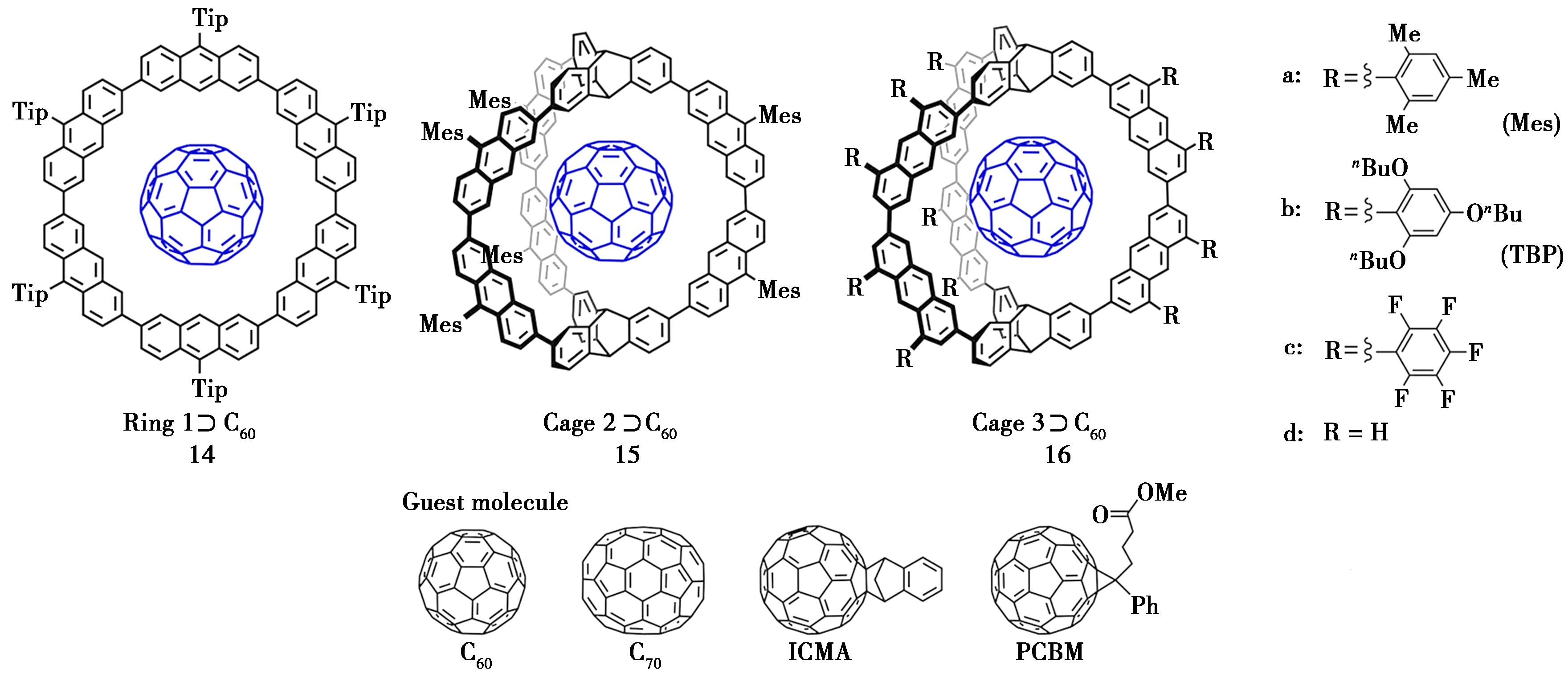
图9 含蒽大环化合物14、15、16分子结构[33-36]
Fig.9 Structures of anthracene-containing macrocycle 14,15 and 16[33-36]
Nakamura等[37]以4,4-二氨基二苯甲烷作为反应原料,经过6步合成反应得到含蒽的水溶性大环化合物17,产物经过核磁谱(1HNMR、13CNMR)和高分辨质谱验证。通过模拟计算发现,大环分子内部含有一个疏水的空腔,空腔的外部连接有4个铵基基团,可以较好的形成水溶性的大环分子,其水溶性达到了0.04 g/mL。该课题组还详细研究了该大环化合物与客体(化合物17a、17b)的分子识别行为,运用荧光滴定法测得大环化合物17与客体17b的配合常数达到了2.6×105 mol/L,二者以物质的量1∶1进行配合。当换成体积相对较小的客体17a时,主客体之间的配合常数只有3.6×103 mol/L,并且随着客体17a的加入,主体的荧光变化比较微弱(图10)。
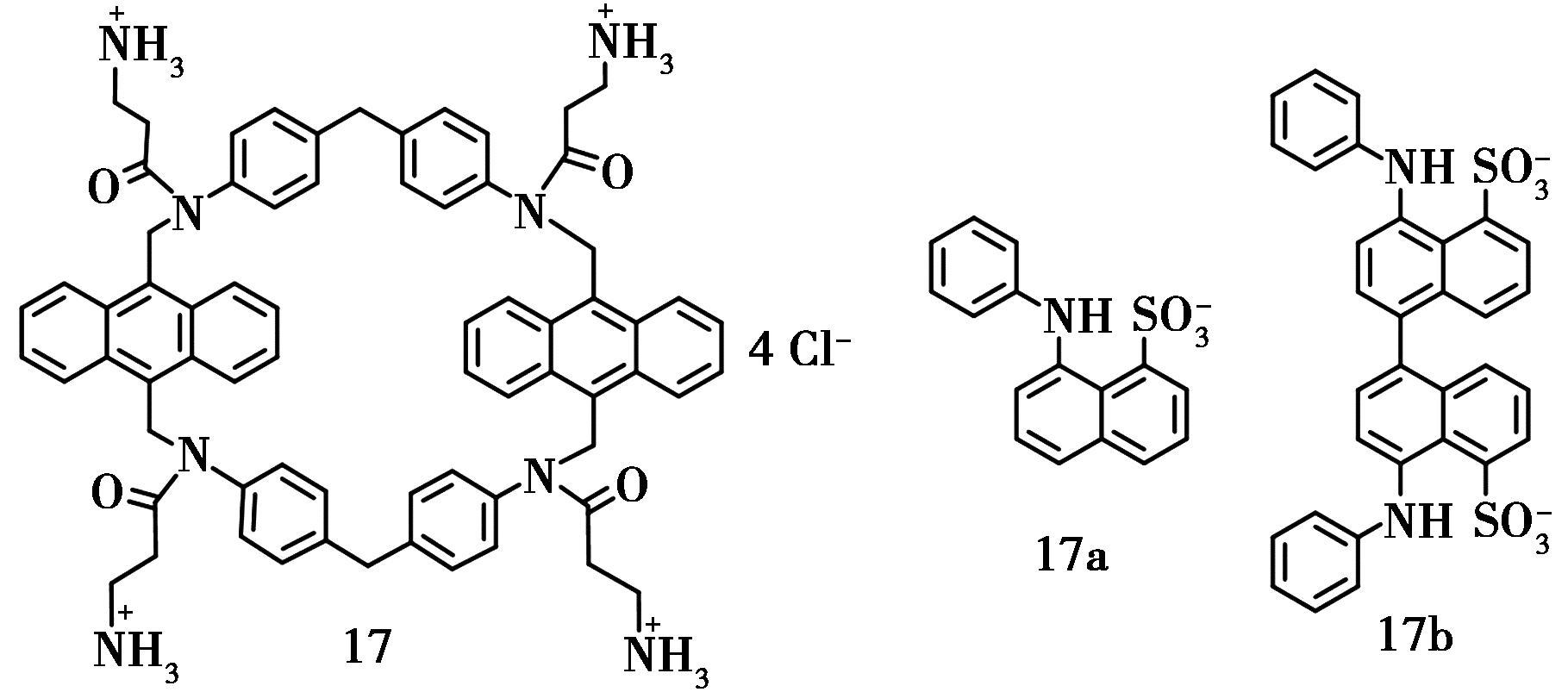
图10 含蒽大环化合物17及其客体17a、17b分子结构[37]
Fig.10 Structures of anthracene-containing macrocycle 17 and its guests 17a and 17b[37]
Zhou等[38]构建以DPP为分子轴的双蒽基束缚的类轮烷结构DPP-Cycle(18),该分子由1个中心DPP单元通过共价键与两条含蒽的侧链包封形成。外围的大环有效屏蔽了中心的DPPD核,化合物18及其对应二环聚合物DPP-Cycle呈现出双发射特征,这归因于大环的封装效果以及蒽单元向DPP单元之间的高效能量传递。可以实现在多种基材表面上的现场指纹成像,抑制ACQ效应(图11)。
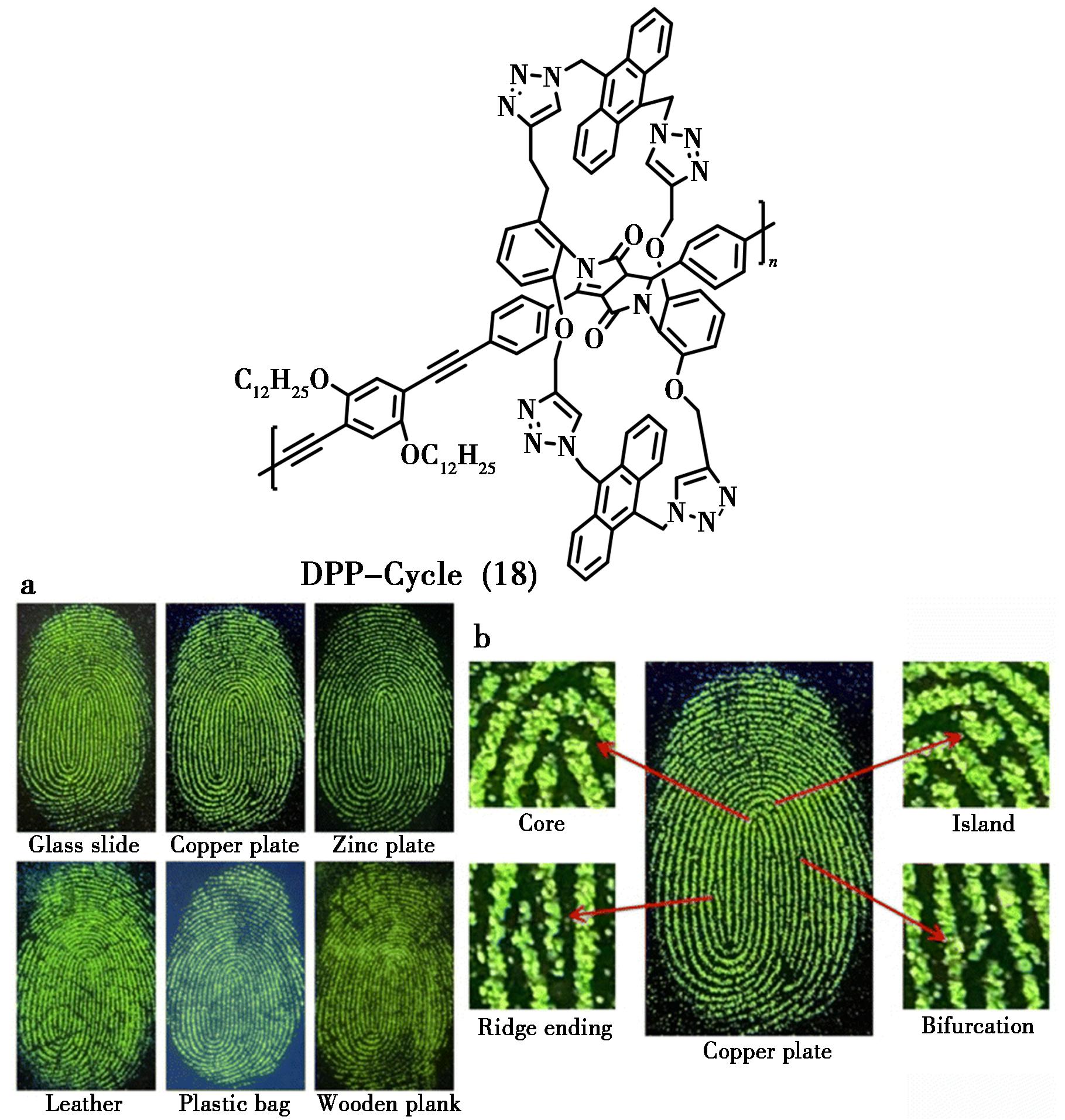
a.化合物18在不同材料表面上的现场指纹成像;b.化合物18在铜表面的指纹成像(抑制ACQ效应分析)
图11 含蒽大环化合物18分子结构及指纹成像[38]
Fig.11 Structures of anthracene-containing macrocycle 18 and fingerprint imaging[38]
Pang等[39]报道了一系列基于蒽的大环化合物。其在水溶性酰胺萘管被证明能够通过结合受限疏水腔的结合能力和屏蔽氢键,选择性地识别水中的高度亲水分子、药物分子、天然产物、聚乙二醇、光开关分子、极性有机污染物和其他有机分子,采用同步构建的合成策略,构建了一种具有蒽侧壁的新型仿生主体(19)。此外,该课题组通过一锅Suzuki-Miyaura交叉偶联反应,设计并合成了由3个蒽二聚体和3个2,6-二溴-4-甲氧基吡啶组成的六方蒽基纳米管,该纳米管能够从富含C60的富勒烯混合物中富集C70(图12)[40]。
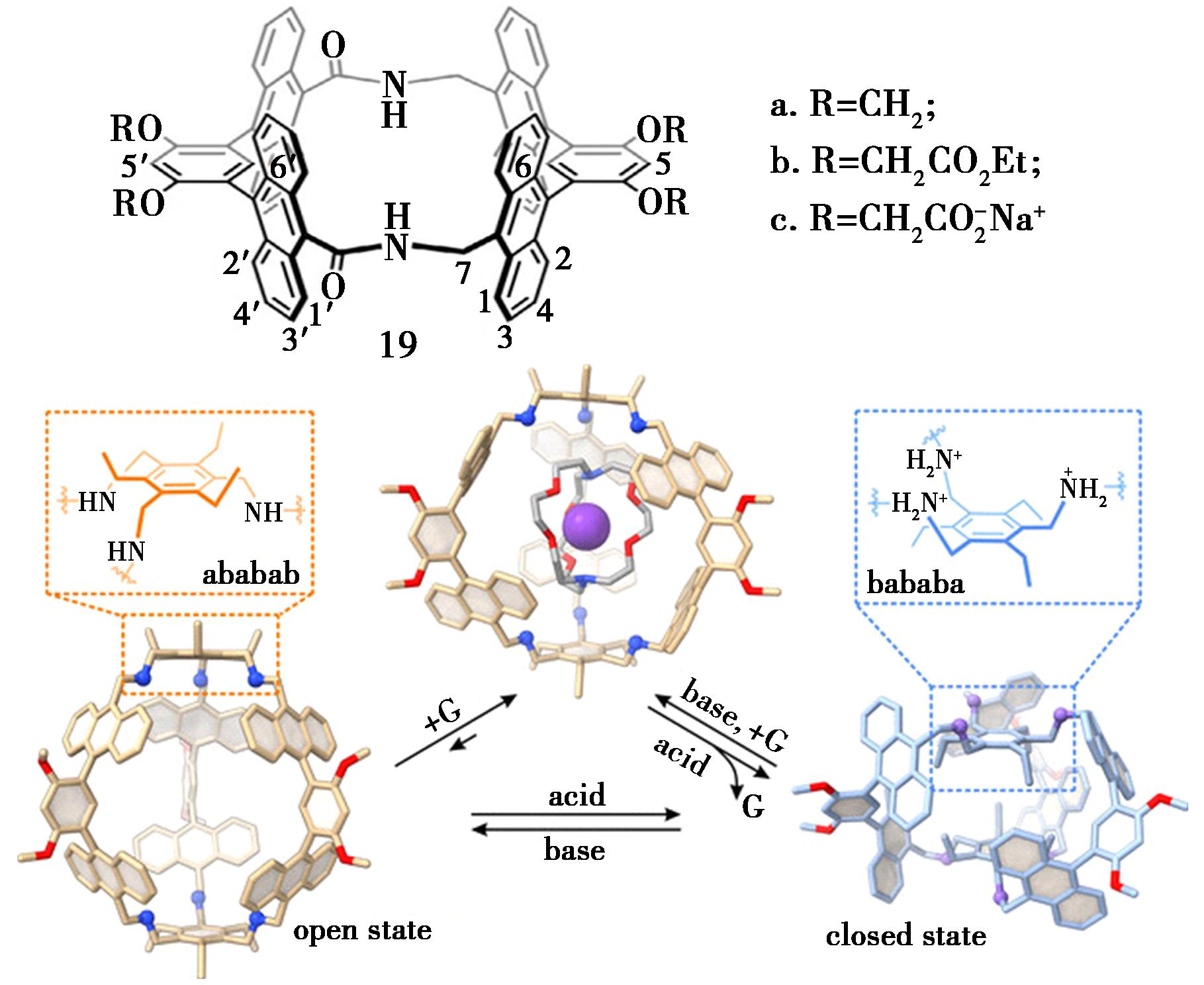
图12 含蒽大环化合物19分子结构[40]
Fig.12 Structure of anthracene-containing macrocycle 19[40]
曹迁永等[41]通过点击反应合成了一种以降冰片烯为骨架含蒽荧光团环状双三唑化合物20及其非环对应物21,并研究了二者对金属离子荧光识别能力。在V(CH3CN)∶V(H2O)=90∶10溶液中,大环分子20仅对Hg2+有很好的荧光淬灭响应。有意思的是,非环受体21对Zn2+、Hg2+与Cu2+都有荧光识别响应,其中滴加Zn2+使受体19荧光增强,而滴加Hg2+与Cu2+则导致其荧光淬灭(图13)。
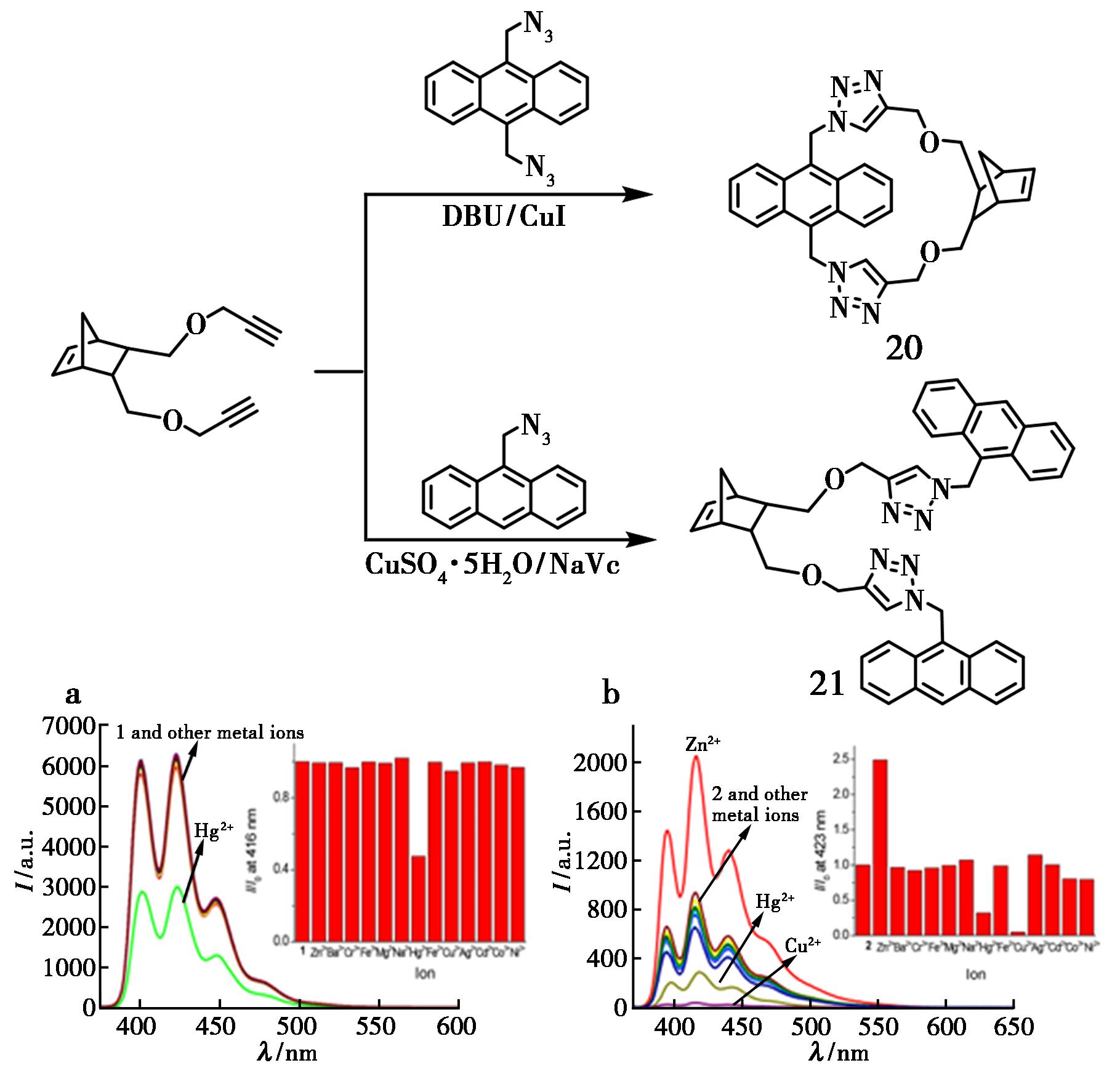
a、b分别为大环分子20、21与Hg2+荧光识别效应
图13 含蒽大环化合物20及其非环对应物21的合成路线及荧光识别[41]
Fig.13 Synthetic route of anthracene-containing macrocycle 20 and the acyclic counterpart 21 and fluorescence identification [41]
Li等[42]通过以1,4-二苄溴与9,10-二苄基醇作为反应原料,在强碱的作用下运用高度稀释法制备出含蒽大环化合物22,产率达到15%。研究发现,大环化合物22与缺电子的有机离子有强识别能力。在CD2Cl2溶液中,通过核磁滴定法证实大环分子22对客体BV、DBA、OTMA进行物质的量之比为1∶1键合,其中对客体BV的配合常数达到了2.2×107 mol/L,能使荧光猝灭(图14)。
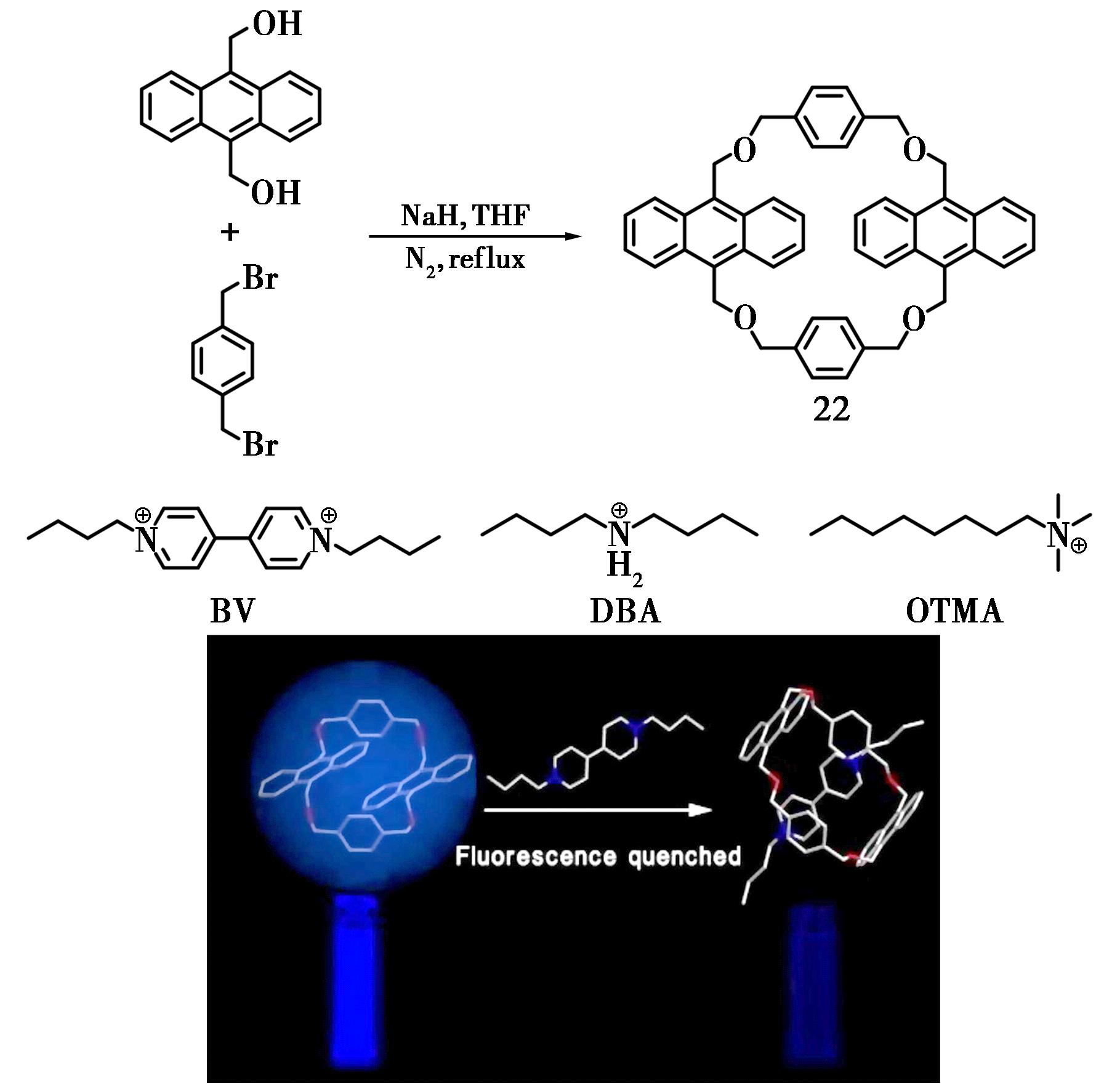
图14 含蒽大环化合物22的合成及其客体分子结构[42]
Fig.14 Synthesis of anthracene-containing macrocyclic 22 and the structures of the guests[42]
Francesconi等[43]研究了水溶性含蒽大环化合物的分子识别性能。以咔唑衍生物与9,10-二醛基蒽为反应原料,经过6步有机反应,高产率的得到了大环化合物23,总产率达到30%。大环分子含有4个亲水性的磷酸根基团,在水相环境中有一定的溶解性。通过核磁共振波谱、等温滴定量热法测试,化合物23与海藻糖等分子在生理性pH范围内有较好的分子识别性能(图15)。
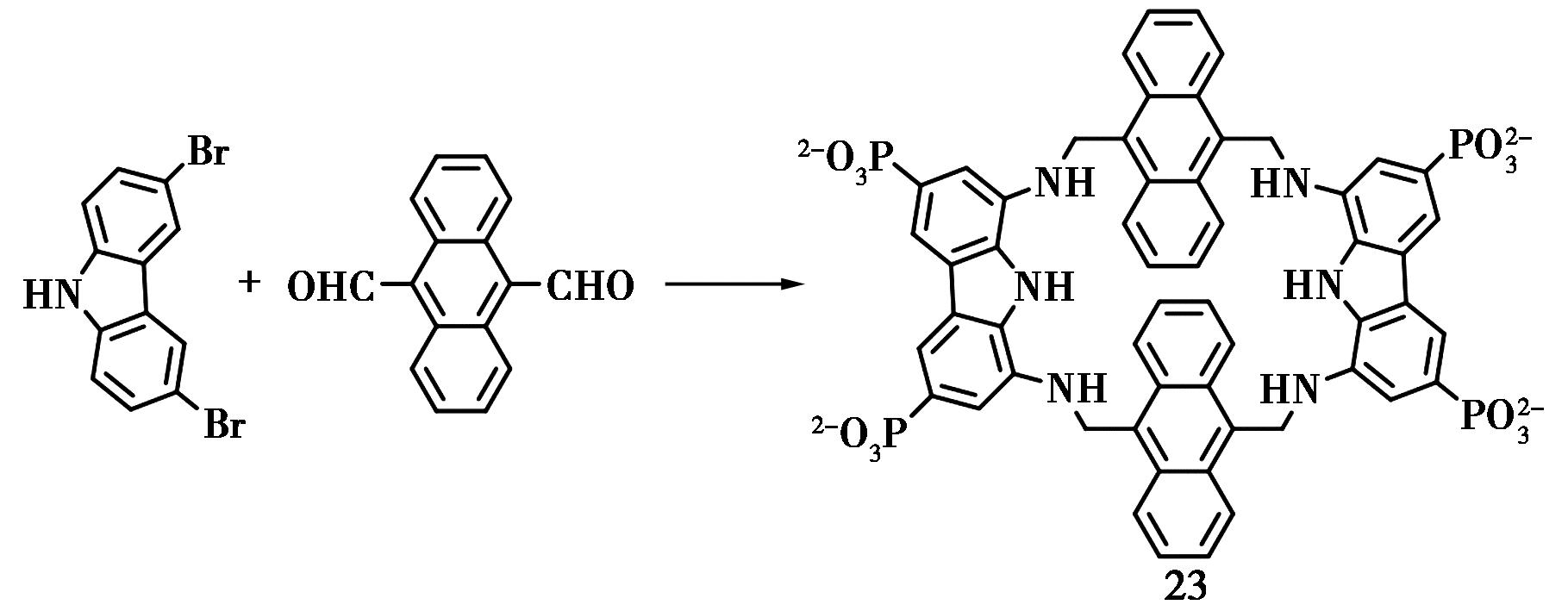
图15 含蒽大环化合物23的合成路线[43]
Fig.15 Synthetic route of anthracene-containing macrocycle 23[43]
2018年,Iyoda等[44]以1,8-二苯基蒽为建筑基元,合成出了含蒽大环化合物24,因为其大环具有较强的刚性,导致其在有机溶剂中的溶解度不好。在建筑基元1,8-二苯基蒽的10号位引入取代基R(2,4,6-三甲基苯),有效的增强了大环分子的溶解性。通过X-单晶衍射图可以清晰地发现,大环分子24与2个四氢呋喃分子形成了稳定的晶体结构,其结构中有1个C2对称轴,并且大环分子内部含有1个空腔,核磁共振氢谱证实该大环分子可以与三氟甲基磺酸亚铜(CuOTf)形成物质的量之比为1∶1的配合物(图16)。
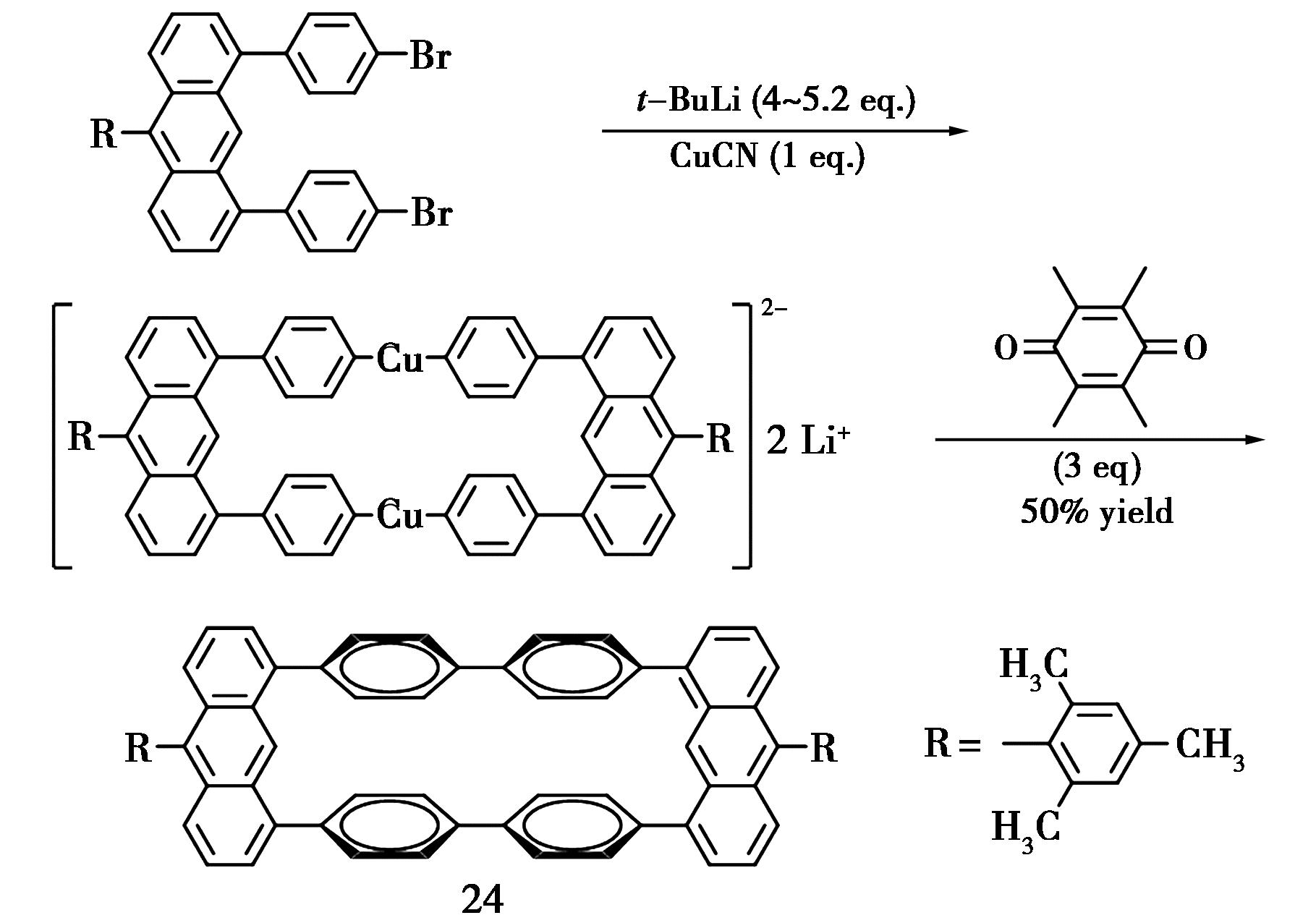
图16 含蒽大环化合物24的合成路线[44]
Fig.16 Synthetic route of anthracene-containing macrocycle 24[44]
Du等[45]研究了一系列由芳香环构建的大环化合物的纳米管的光电性能。2020年,该小组以2,6-二氨基蒽醌为反应原料,经过多步反应选择性的合成了成对的含蒽手性大环化合物25a、25b,它们都具有较强的荧光吸收和较大的光致发光红移现象(图17)。
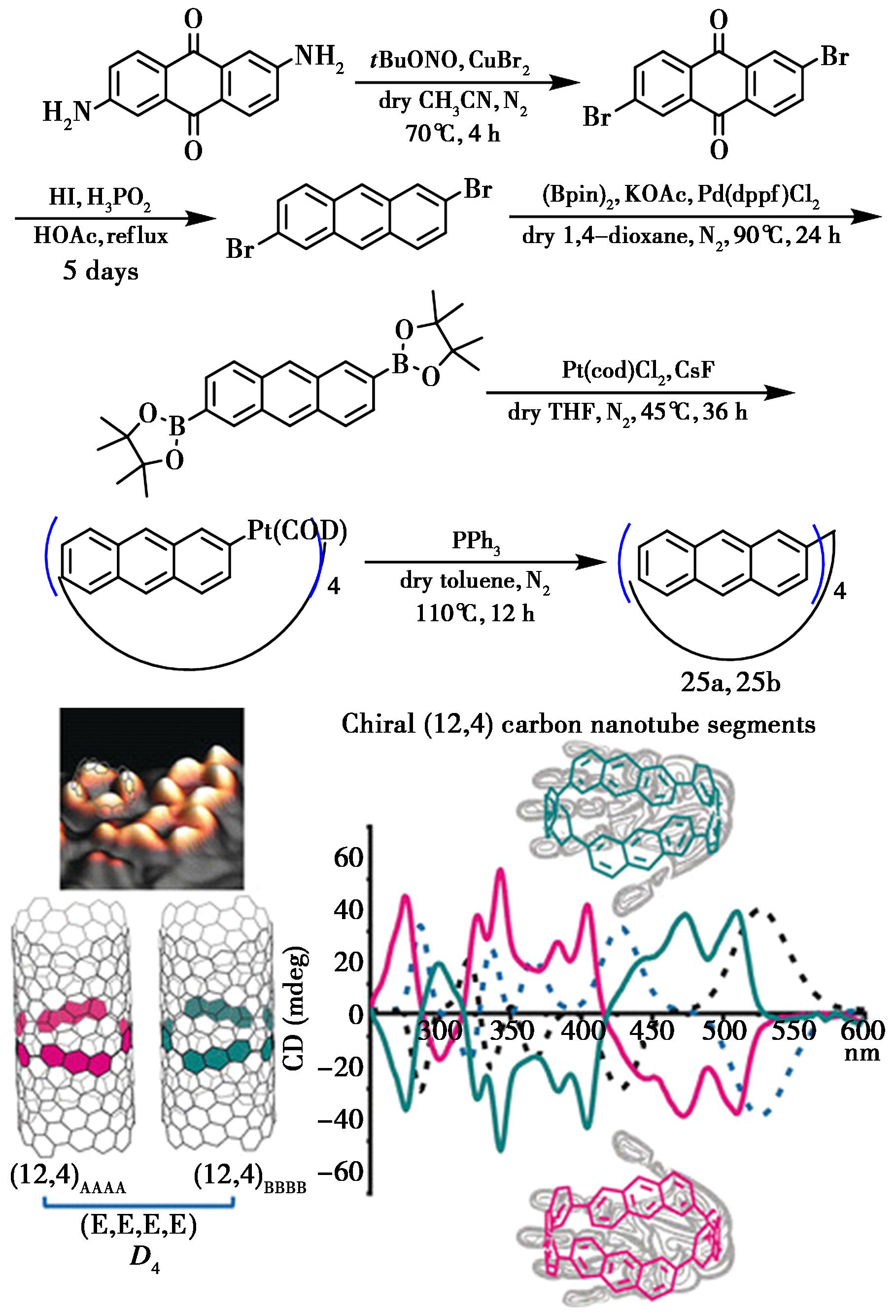
图17 含蒽大环化合物25a、25b的合成路线[45]
Fig.17 Synthetic route of anthracene-containing macrocycles 25a and 25b[45]
Davis课题组一直致力于含蒽大环化合物的合成及其分子识别性能,先后以蒽为建筑基元,合成了水溶性含双蒽的酰胺键大环分子,研究它们在水相中与葡萄糖[46]、麦芽糖糊精[47]的识别性能,并综述了此类大环化合物的合成策略及识别行为[48]。2020年,该小组以合成的大环化合物26为主体,在水相环境中完成了对嘌呤和嘧啶分子的识别研究[49]。大环分子26的结构中含有4个酰胺键,可以在分子识别行为过程中提供额外的分子间的氢键作用。通过核磁共振氢谱和荧光滴定法详细研究了其与尿酸的键合物质的量之比为1∶1。且与不同的客体分子有较强的分子识别性能,其中对次黄嘌呤的配合常数达到了8.7×106 mol/L(图18)。
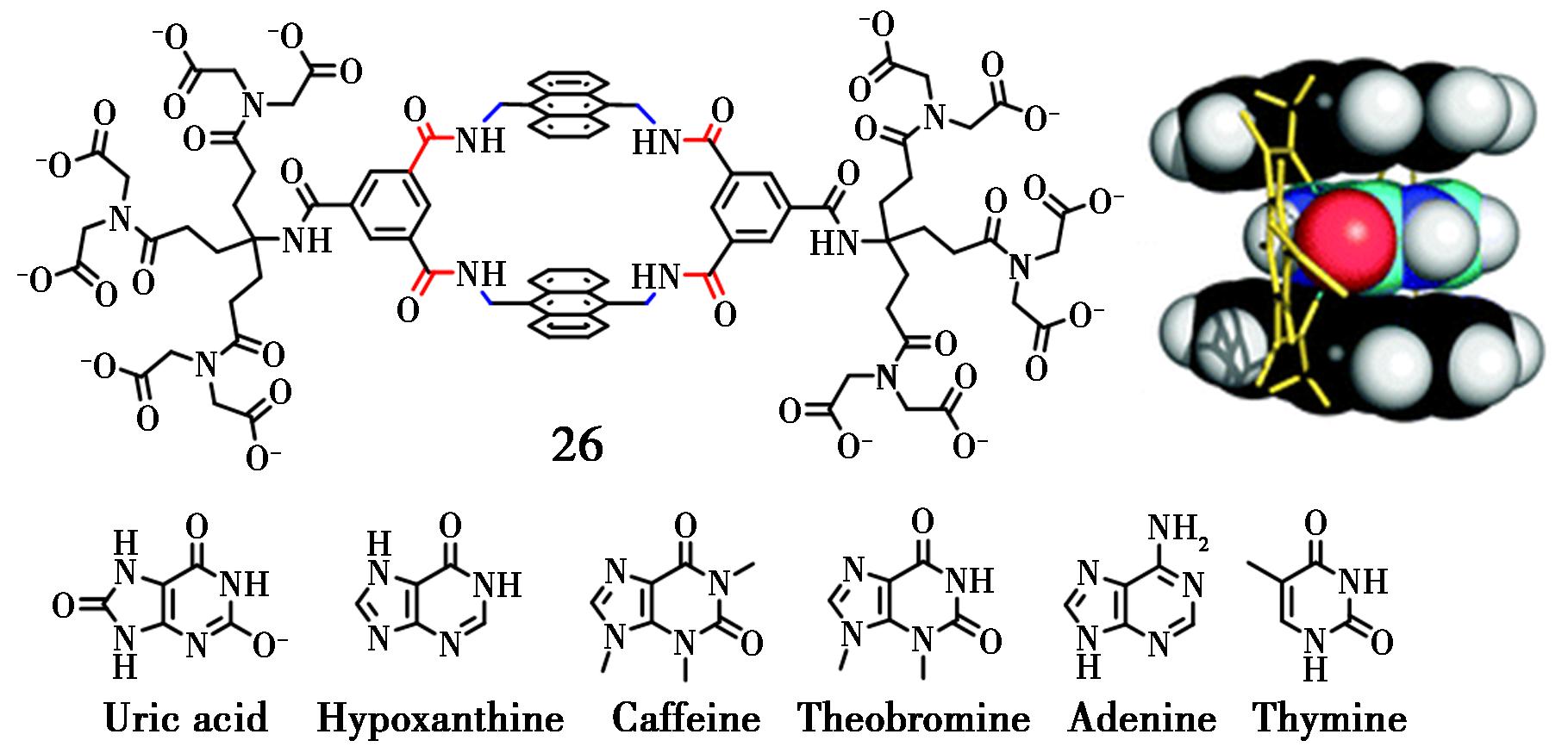
图18 蒽大环化合物26的结构及其客体分子结构[49]
Fig.18 Structures of anthracene-containing macrocycle 26 and the structures of the guests[49]
Xu等[50]对本体溶液中和2个[Pd6L4]12+超分子笼内Diels-Alder反应的机理、催化效率和区域选择性进行了详细的密度泛函理论研究,发现决定碗形笼27、28催化效率的根源在于过渡态的主客体稳定性和熵效应,碗形笼可通过非共价相互作用比预反应复合物更稳定相应的过渡态,从而降低了自由能垒(图19)。
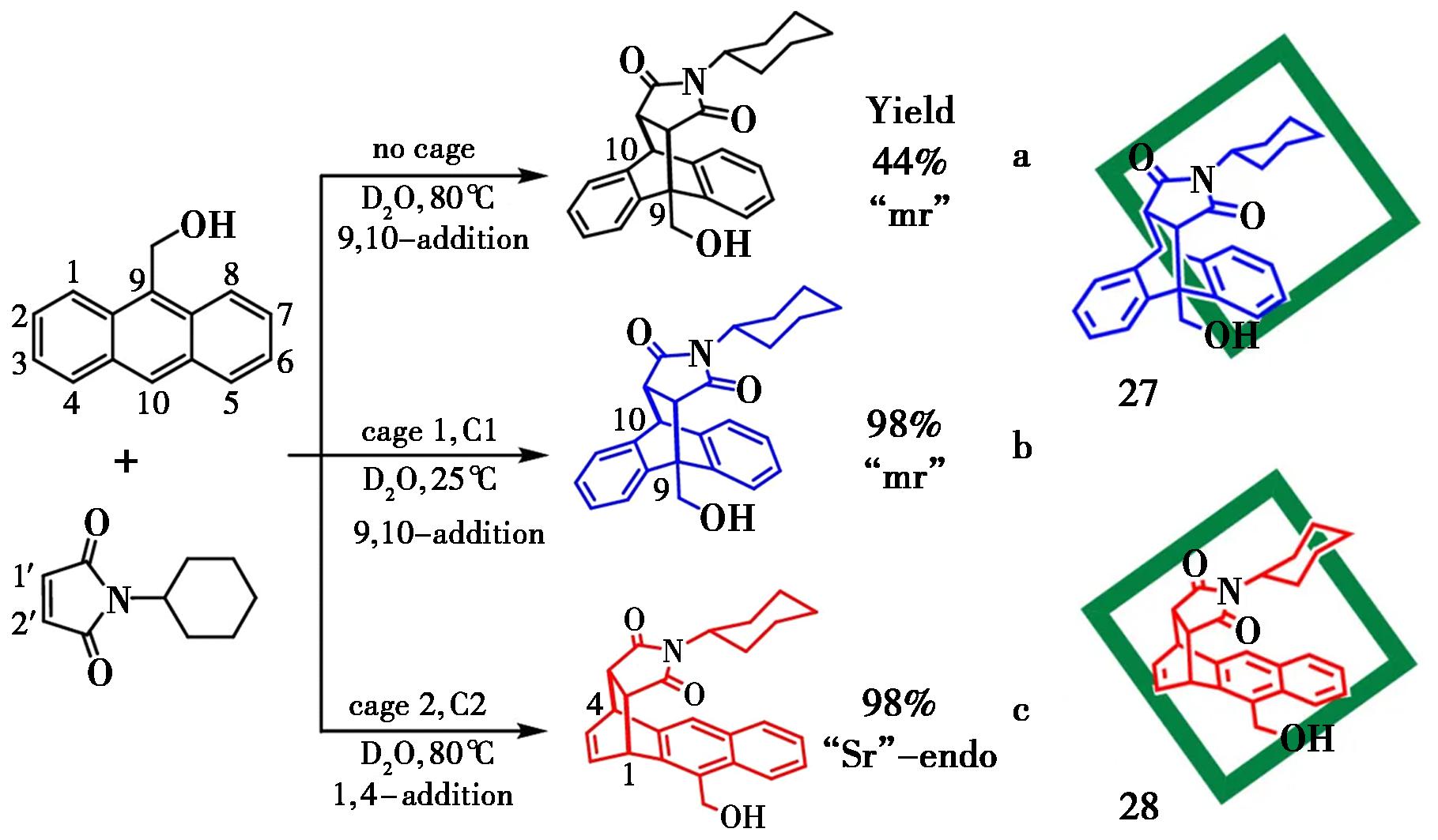
a、b、c分别为合成的大环主体
图19 含蒽大环化合物27、28的结构及其客体分子结构[50]
Fig.19 Structures of anthracene-containing macrocycle 27,28 and the structures of the guests[50]
2 金属-有机含蒽大环化合物
Shionoya小组在含金属-蒽大环化合物的合成及其识别性能方面有独特的研究。2014年,该小组报道了一种构建的基于双核金属银-蒽大环化合物[51]。该大环含有4个蒽分子结构单元,由2个邻二氮杂菲分子连接。2个银原子处于大环29的空腔内部,与空腔内部的N原子鳌合形成稳定的结构30。实验研究发现,即使在浓度为30 μmol/L的氘代氯仿溶剂中,二聚对二甲苯、二茂铁等客体分子可以很好的进入大环主体分子30的内部,在Ag-π的相互作用下主客体间依然有较好的识别行为(图20)。不仅如此,该小组还研究了金属-有机含蒽大环主体30与具有平面结构的蒽分子,非平面结构的三叠烯分子的识别性能[52,53]。
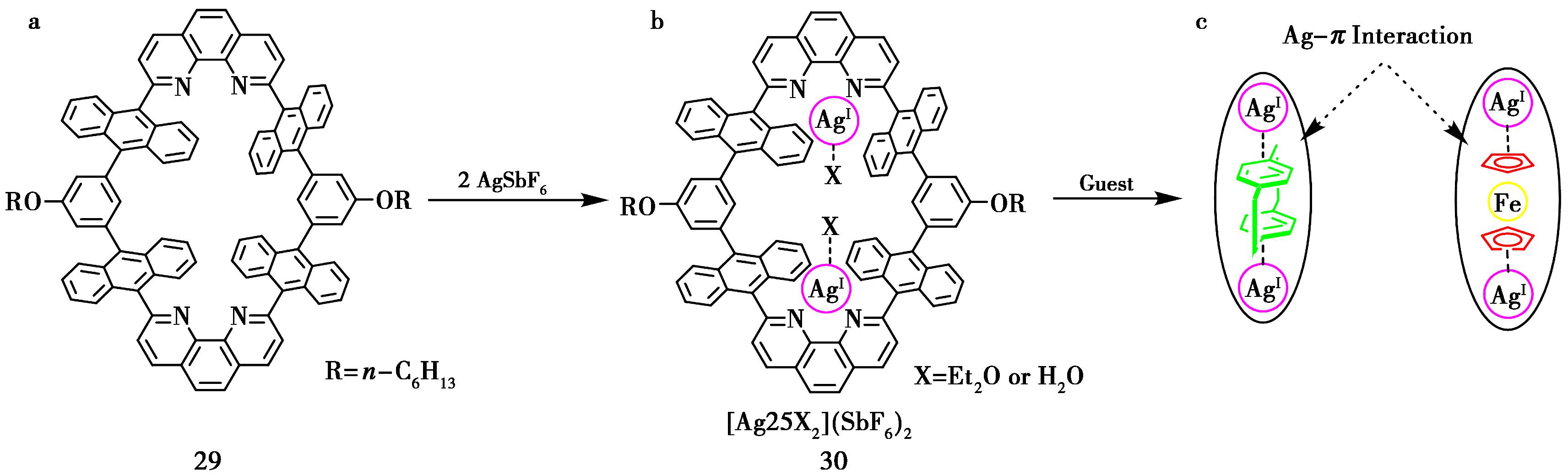
a.大环主体29的结构;b.大环主体分子30的结构;c.在Ag-π的相互作用下主客体的识别行为模式
图20 金属-有机大环化合物29、30的主客体识别[51]
Fig.20 Host-guest recognition of metal-organic macrocyclic compounds 29 and 30[51]
Jin等[54]以蒽的衍生物作为结构基元,在三氟甲基磺酸银的催化作用下,分别与铑配合物形成了金属铑-有机含蒽大环分子31a~31c。通过核磁共振谱以及紫外-可见光谱(UV/Vis)等技术手段详细的研究了铑-有机含蒽大环分子31a~31c在光照条件下可以与氧结合得到内过氧化物,铑-有机含蒽大环与内过氧化物之间在一定条件下可以相互转化(图21)。该小组运用核磁共振谱、红外光谱、元素分析以及单晶衍射技术详细研究了二者间的相互转化过程。此外,该课题组使用多环芳烃结构单元设计并获得了具有疏溶剂袋的盒状金属矩形结构[55-58]。
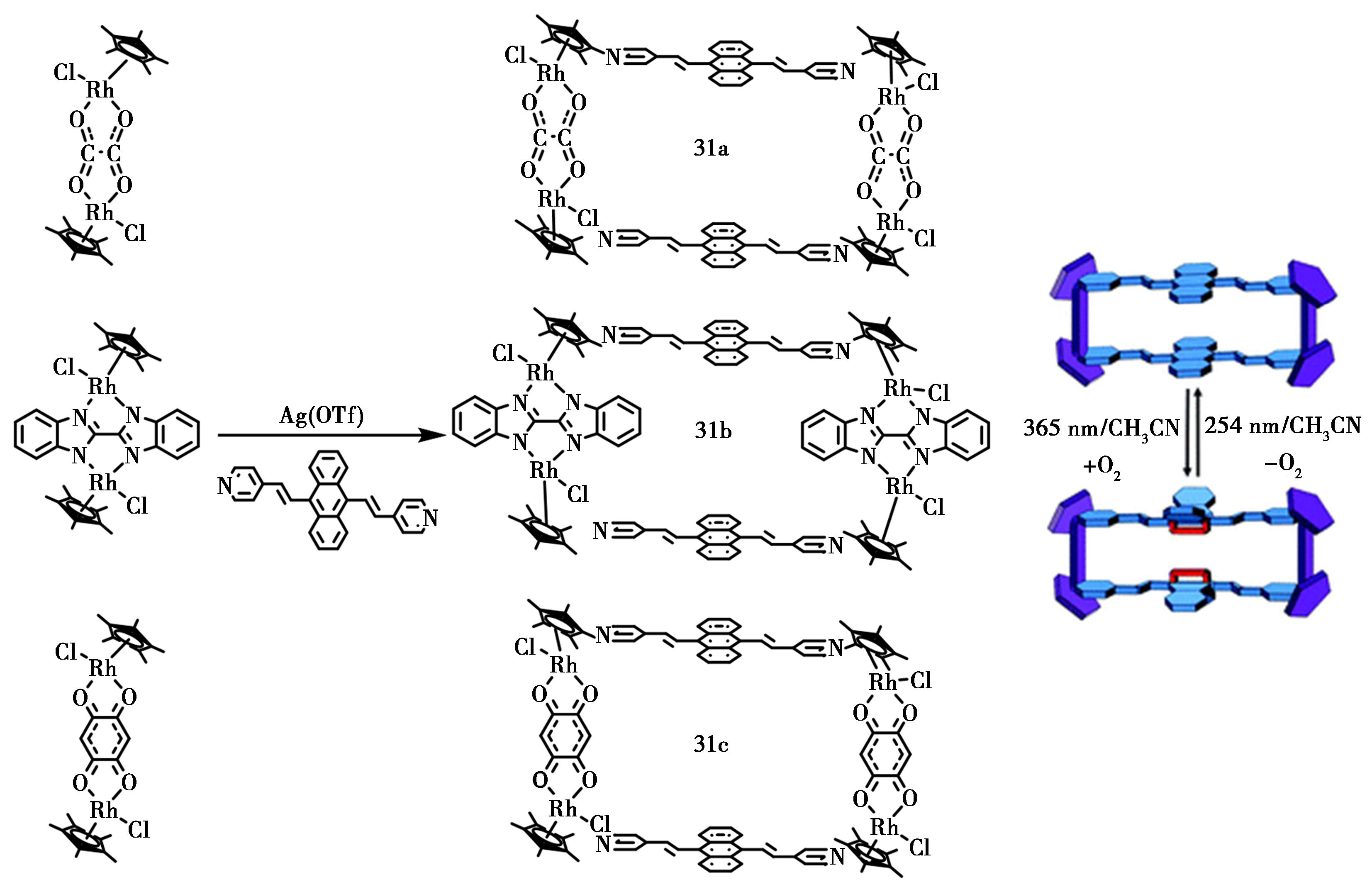
图21 金属-有机大环化合物31a~31c的合成[54]
Fig.21 Synthesis of metal-organic macrocycles 31a~31c[54]
Bibal等[59]以9,10-二溴蒽与2-甲硫基苯硼酸为反应原料,利用Suzuki-Miyaura偶联反应合成了具有顺式构型的有机配体32。变温核磁技术(VT-NMR)证实,该配体32在不同温度环境条件的构型均非常稳定。在此基础上向配体中加入一定量的不同银无机盐,可以高产率(77%~92%)的自组装成不同类型的金属银-含蒽有机大环分子(图22)。该小组还研究了此类大环化合物在均相环境下的催化炔烃的加成/环化异构化反应,在0.5~1 mol%的催化条件下可以较好得到目标产物。
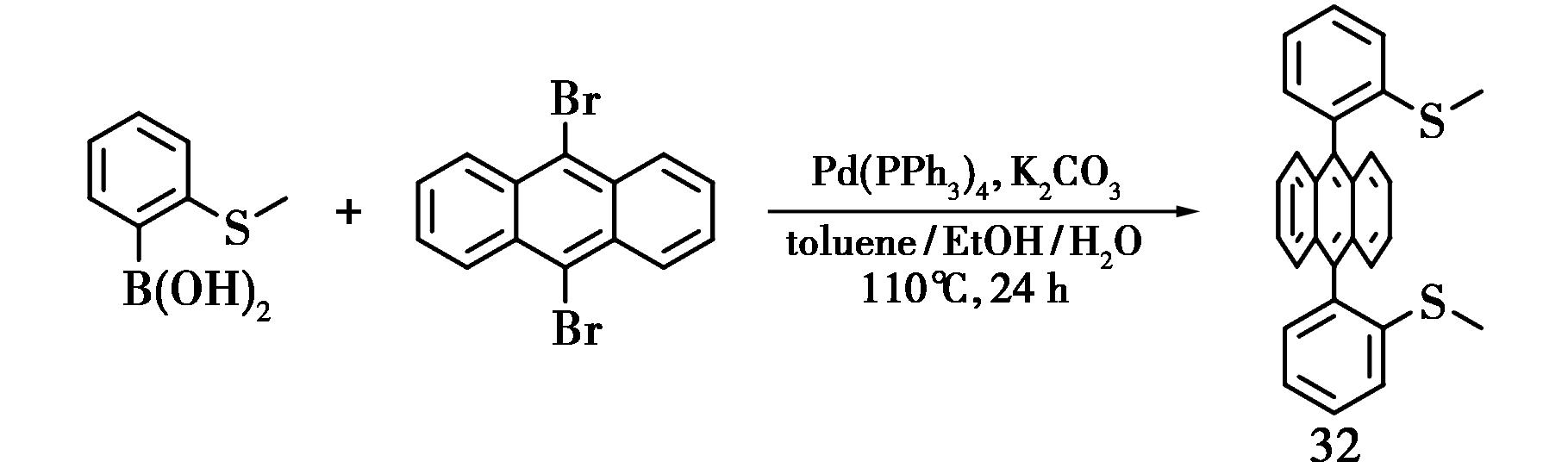
图22 有机配体32的合成[59]
Fig.22 Synthesis of the ligand 32[59]
Su等[60]以6,12-二溴代硼杂蒽嵌蒽为前体,通过中性卡宾配体(NHC/CAAC)配位与还原反应协同策略,成功构筑了卡宾稳定的6,12-二硼杂蒽嵌蒽分子33和34,并对其氧化还原性质进行了详细研究。结果发现,将传统多环芳烃的π电子离域特性与硼原子的缺电子特性相结合,形成具有特殊电子结构的芳烃体系(图23)。
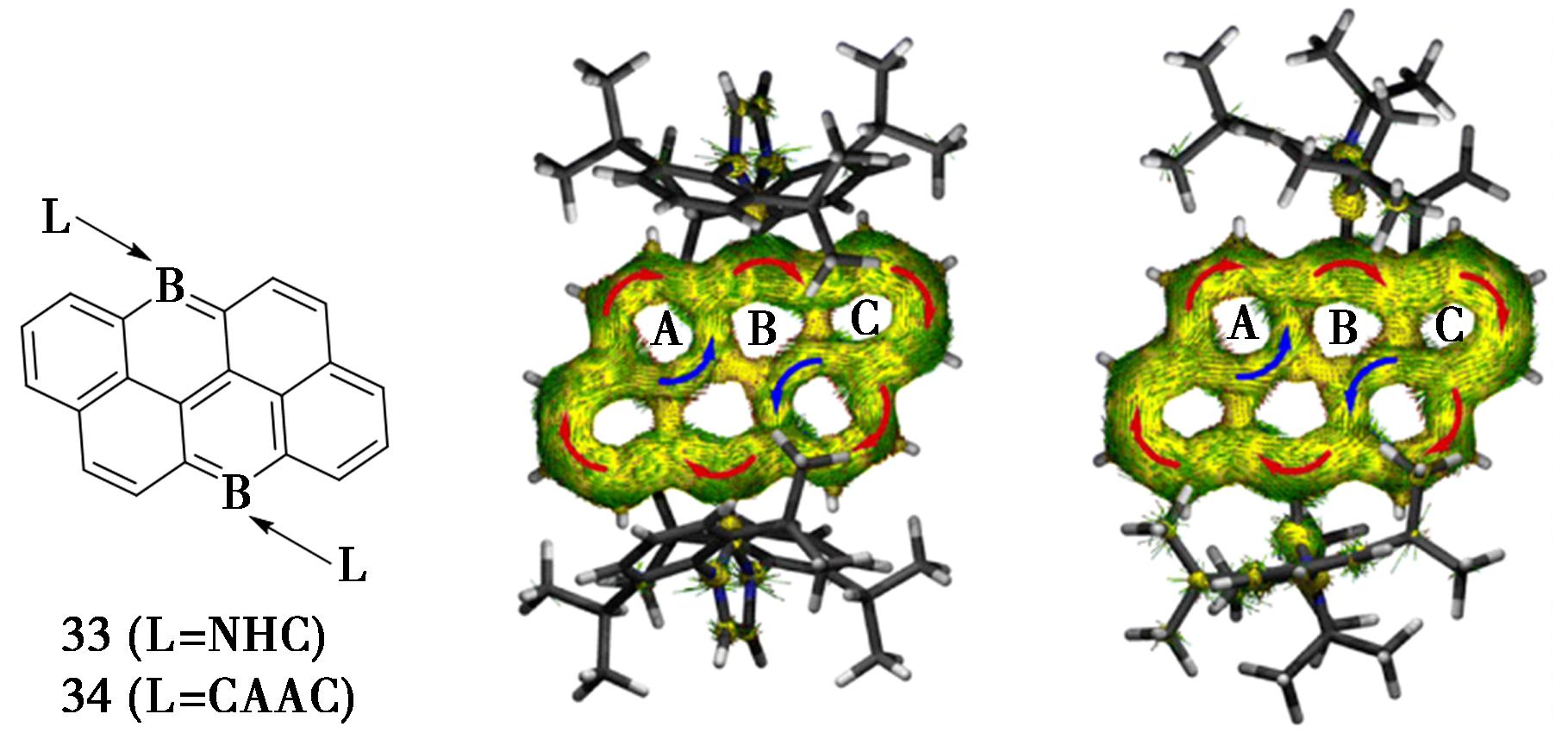
图23 6,12-二硼杂蒽嵌蒽分子33和34的结构及对应π电子感应电流密度各向异性(ACID)分布图[60]
Fig.23 Structures of 6,12-diborahexanthene-embedded anthracene molecules 33 and 34 and the corresponding anisotropy of the π-electron induced current density (ACID) maps[60]
3 结论与展望
尽管含蒽大环化合物的研究取得了显著进展,但仍面临一些挑战,未来发展方向:目前合成的含蒽的大环化合物结构复杂,合成步骤繁琐,产率偏低,且溶解性较差,如何高效构建水溶性的含蒽大环分子,通过改变有机合成路线提高产率以及增加溶解性将是此类大环化合物在合成研究中的核心任务;同时,如何在一个大环体系中集成多种功能(如识别、响应、传输),实现复杂的仿生功能和逻辑运算,是未来的重要方向;此外,需要更深入的理论计算和模拟来理解其构效关系,指导理性设计;目前大部分研究仍停留在实验室阶段,推动其在传感、生物成像、分子识别、能源转换等领域的实际应用是最终目标。
含蒽大环化合物因其结合了蒽的优异光物理性质和可调的大环空腔,已成为超分子化学和材料科学的前沿领域。通过精妙的分子设计,研究人员已经开发出多种合成策略,并探索了其在分子识别、刺激响应材料、光电器件和复杂组装体等方面的广泛应用。未来,随着合成方法的不断创新和对其性能的深入理解,含蒽大环化合物必将为创造新一代智能材料和器件提供更多可能。
[1]Liu Y,You C C,Zhang H Y.Supramolecular Chemistry——Molecular Recognition and Assembly of Synthetic Receptors.Tianjin:Nankai University Press,2003.
刘育,尤长城,张衡益.超分子化学—合成受体的分子识别与组装.天津:南开大学出版社,2003.
[2]Pedersen C J.J.Am.Chem.Soc.,1967,89(26):7017-7036.
[3]Luo Q H.Macrocyclic Chemistry:Host-guest Compounds and Supramolecular Systems.Beijing:Science Press,2009.
罗勤慧.大环化学:主-客体化合物和超分子.北京:科学出版社,2009.
[4]Huang G B,Jiang W.Prog.Chem.,2015,27(6):744-754.
黄国保,蒋伟.化学进展,2015,27(6):744-754.
[5]Huang G B,Chen Z L,Wei X S,Chen Y,Li X Y,Zhong H,Tan M X.Chin.J.Org.Chem.,2020,40(3):614-624.
黄国保,陈志林,韦贤生,陈钰,李秀英,仲辉,谭明雄.有机化学,2020,40(3):614-624.
[6]Ma W L,Li X Y,Hao A Y,Xing P Y.Sci.China Chem.,2024,67(10):3482-3492.
[7]Zheng B,Wang F,Dong S Y,Huang F H.Chem.Soc.Rev.,2012,41(5):1621-1636.
[8]Chen Y,Liu Y.Chem.Soc.Rev.,2010,39(2):495-505.
[9]Guo D S,Liu Y.Chem.Soc.Rev.,2012,41(18):5907.
[10]Tan L L,Li H W,Tao Y C,Zhang S X,Wang B,Yang Y W.Adv.Mater.,2014,26(41):7027-7031.
[11]Zhang L L,Liang Y,Xiao Z F,Meng Y X,Huang J Y,Lin X,Li J,Zhou H C,Fang Y.Sci.China Chem.,2024,67(5):1554-1560.
[12]He M M,Ma Z Y,Zhang Z W,Zhang L H,Zhang S Q,Wang R,Leng X F,Li Y,Fan J L,Sun W,Peng X J.Sci.China Chem.,2024,67(11):3875-3885.
[13]Guo C X,Su F,Su P R,Yu X J,Li X P.Sci.China Chem.,2023,66(7):1940-1962.
[14]Chang Y C,Yang K,Wei P,Huang S S,Pei Y X,Zhao W,Pei Z C.Angew.Chem.Int.Ed.,2014,53(48):13126-13130.
[15]Wang X Y,Han K,Li J,Jia X S,Li C J.Polym.Chem.,2013,4(14):3998.
[16]Wang S M,Nian H,Wang Y F,Zheng L S,Zheng Y T,Dong Y W,Huang L P,Wang X P,Jiang W,Yang L P.Sci.China Chem.,2025,68(1):369-376.
[17]Zhong Y M,Xuan J J,Qin X J,Xiao H,Xia Z J,Zhou L P,Guo X Q,Hu Y H,Zhang L,Li C S,Cai L X,Sun Q F.Sci.China Chem.,2025,68(2):561-569.
[18]Gassensmith J J,Arunkumar E,Barr L,Baumes J M,DiVittorio K M,Johnson J R,Noll B C,Smith B D.J.Am.Chem.Soc.,2007,129(48):15054-15059.
[19]Liu W Q,Johnson A,Smith B D.J.Am.Chem.Soc.,2018,140(9):3361-3370.
[20]Lau J Y,Shi K J,Oliver A G,Smith B D.Org.Lett.,2025,27(29):8083-8087.
[21]Liu W Q,Oliver A G,Smith B D.J.Am.Chem.Soc.,2018,140(22):6810-6813.
[22]Dharmarwardana M,Dempsey J M,Padilla-coley S,Jarvis T S,Shi K J,Atkinson K M,Smith B D.Chem.Commun.,2021,57(99):13518-13521.
[23]Chou C M,Nobusue S,Saito S,Inoue D,Hashizume D,Yamaguchi S.Chem.Sci.,2015,6(4):2354-2359.
[24]Farr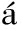 n M
n M 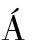 ,Listorti A,Roiati V,Accorsi G,Gigli G,Clarkson G J,Claramunt R M.J.Photochem.Photobiol.A Chem.,2016,314:189-197.
,Listorti A,Roiati V,Accorsi G,Gigli G,Clarkson G J,Claramunt R M.J.Photochem.Photobiol.A Chem.,2016,314:189-197.
[25]Osaki H,Chou C M,Taki M,Welke K,Yokogawa D,Irle S,Sato Y,Higashiyama T,Saito S,Fukazawa A,Yamaguchi S.Angew.Chem.Int.Ed.,2016,55(25):7131-7135.
[26]Takaki Y,Ozawa R,Kajitani T,Fukushima T,Mitsui M,Kobayashi K.Chem,2016,22(47):16760-16764.
[27]Inoue M,Iwanaga T,Toyota S.Bull.Chem.Soc.Jpn.,2015,88(11):1591-1602.
[28]Toyota S,Yoshikawa M,Saibara T,Yokoyama Y,Komori T,Iwanaga T.ChemPlusChem,2019,84(6):643-654.
[29]Toyota S,Ikeda H,Iwanaga T.ChemPlusChem,2017,82(7):957-966.
[30]May R,Jester S S,Höger S.J.Am.Chem.Soc.,2014,136(48):16732-16735.
[31]Yamamoto Y,Wakamatsu K,Iwanaga T,Sato H,Toyota S.Chem,2016,11(9):1370-1375.
[32]Yamamoto Y,Tsurumaki E,Wakamatsu K,Toyota S.Angew.Chem.Int.Ed.,2018,57(27):8199-8202.
[33]Fujise K,Tsurumaki E,Wakamatsu K,Toyota S.Chem,2021,27(14):4473.
[34]Yamamoto Y,Tsurumaki E,Wakamatsu K,Toyota S.Angew.Chem.Int.Ed.,2018,130(27):8331-8334.
[35]Toyota S,Yamamoto Y,Wakamatsu K,Tsurumaki E,Mu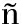 oz-castro A.Bull.Chem.Soc.Jpn.,2019,92(10):1721-1728.
oz-castro A.Bull.Chem.Soc.Jpn.,2019,92(10):1721-1728.
[36]Kajiyama K,Tsurumaki E,Wakamatsu K,Fukuhara G,Toyota S.ChemPlusChem,2021,86(5):716-722.
[37]Nakamura K,Kusano S,Hayashida O.J.Inclusion Phenom.Macrocycl.Chem.,2016,85(1/2):121-126.
[38]Zhou H,Zhang Y X,Zheng Z Y,Wan J H,Zhang H,Lin K H,Sessler J L,Wang H Y.Chem.Sci.,2025,16(2):910-919.
[39]Pang X Y,Zhou H,Xie X J,Jiang W,Yang Y H,Sessler J L,Gong H Y.Angew.Chem.Int.Ed.,2024,63(36):e202407805.
[40]Nian H,Wang S M,Wang Y F,Zheng Y T,Zheng L S,Wang X P,Yang L P,Jiang W,Cao L P.Chem.Sci.,2024,15(26):10214-10220.
[41]Zhu W B,Lv X L,Zhu J H,Cao Q Y.Chin.J.Org.Chem.,2017,37(3):624-629.
祝文斌,吕小兰,朱江华,曹迁永.有机化学,2017,37(3):624-629.
[42]Bao L P,Shu X Y,Yu M,Hou D B,Cui L,Li C J.Tetrahedron Lett.,2018,59(8):730-733.
[43]Francesconi O,Martinucci M,Badii L,Nativi C,Roelens S.Chem,2018,24(26):6828-6836.
[44]Shirai A,Sano H,Nakamura Y,Takashika M,Otani H,Hasegawa M,Kato S I,Iyoda M.J.Org.Chem.,2018,83(7):3857-3863.
[45]Wang J Y,Zhuang G L,Chen M Q,Lu D P,Li Z,Huang Q,Jia H X,Cui S S,Shao X,Yang S F,Du P W.Angew.Chem.Int.Ed.,2020,59(4):1619-1626.
[46]Destecroix H,Renney C M,Mooibroek T J,Carter T S,Stewart P F N,Crump M P,Davis A P.Angew.Chem.Int.Ed.,2015,54(7):2057-2061.
[47]Stewart P,Renney C M,Mooibroek T J,Ferheen S,Davis A P.Chem.Commun.,2018,54(62):8649-8652.
[48]Davis A P.Chem.Soc.Rev.,2020,49(9):2531-2545.
[49]Van E D,Samanta S K,Davis A P.Chem.Commun.,2020,56(65):9268-9271.
[50]Mao X R,Wang Q,Zhuo S P,Xu L P.Inorg.Chem.,2023,62(10):4330-4340.
[51]Omoto K,Tashiro S,Kuritani M,Shionoya M.J.Am.Chem.Soc.,2014,136(52):17946-17949.
[52]Omoto K,Tashiro S,Shionoya M.Chem.Sci.,2019,10(30):7172-7176.
[53]Omoto K,Tashiro S,Shionoya M.J.Am.Chem.Soc.,2021,143(14):5406-5412.
[54]Shan W L,Gao W X,Lin Y J,Jin G X.Dalton Trans.,2018,47(8):2769-2777.
[55]Liu D,Lin Y J,Jin G X.J.Organomet.Chem.,2022,967:122353.
[56]Liu D,Lu Y,Lin Y J,Jin G X.Chem.,2022,28(16):e202104617.
[57]Gao X,Cui Z,Shen Y R,Liu D,Lin Y J,Jin G X.J.Am.Chem.Soc.,2021,143(42):17833-17842.
[58]Hua P P,Bai J H,Feng H J,Wang J W,Zhang L F,Jin G X.J.Am.Chem.Soc.,2024,146(38):26427-26434.
[59]Cao Z,Lacoudre A,Rossy C,Bibal B.Beilstein J.Org.Chem.,2019,15:2465-2472.
[60]Wang Y Y,Shi T,Yue L,Zhou G J,Su B C.Chem.Sci.,2025,16(27):12510-12518.