氟喹诺酮类抗生素(Fluoroquinolones,FQs)是一类具有4-氧代喹啉-6-氟-3-羧基结构的合成抗菌药物,自20世纪80年代开发以来,因其抗菌谱广、杀菌能力强、体内分布广泛、半衰期长、价格低廉等优点,被广泛应用于人类医疗、畜禽养殖和水产养殖业中[1-3]。此类药物在治疗呼吸道、消化道、泌尿生殖系统等多种感染性疾病方面具有良好的效果,经过40余年的发展,目前已成为全球使用量最大的抗生素类药物之一[4,5]。然而,由于FQs的大量使用和不合理排放,这些化合物通过各种途径进入水环境,在地表水、地下水、污水处理厂出水甚至饮用水中频繁检出。研究表明,FQs在环境中的长期存在不仅会诱导产生耐药性菌株,破坏水生态系统平衡。还可能通过食物链在生物体内富集,对人类健康和生态环境造成潜在威胁[6,7]。
目前,氟喹诺酮类抗生素的检测方法包括高效液相色谱法(HPLC)、液相色谱-质谱法(LC-MS)及液相色谱-串联质谱法(LC-MS/MS)等[8-10]。其中,高效液相色谱-串联质谱法(HPLC-MS/MS)因其具有更强的分离能力、更高的样品通量和灵敏度而成为环境水样中痕量抗生素检测的首选方法[11]。固相萃取(SPE)作为一种高效的样品前处理技术,可以有效富集水样中的目标化合物,去除基质干扰,提高检测灵敏度,具有富集效率高、有机溶剂消耗少、操作简便等诸多优点[12,13]。近年来,国内外学者对HPLC-MS/MS检测水环境中氟喹诺酮类抗生素进行了大量研究。Wagil等[14]采用SPE-LC-MS/MS方法检测了波兰地表水中12种FQs,检出限为0.5~2.0 ng/L;Tong等[15]建立了QuEChERS结合UHPLC-MS/MS同时测定水样中15种抗生素的方法。王婷等[16]采用多反应监测模式下的超高效液相色谱-串联质谱法检测动物源性食品中19种FQs残留;廖杰等[17]建立了固相萃取-液相色谱-串联质谱法测定地表水中13种抗生素的方法,检出限为0.1~0.5 ng/L。然而,上述方法仍存在以下不足:一是针对饮用水基质的专门优化较少;二是缺乏系统的基质效应评价;三是与现行国家标准方法的比较验证不足。本研究建立了固相萃取-超高效液相色谱-三重四极杆质谱联用法,实现了对饮用水中马波沙星、氟罗沙星、氧氟沙星、培氟沙星等17种常见氟喹诺酮类抗生素的同时快速测定。系统评价了饮用水基质对17种FQs离子化效率的影响,与现行国家标准方法GB/T 5750.8—2023《生活饮用水标准检验方法 第8部分:有机物指标》进行了系统比较,构建了饮用水中FQs的风险评估框架。
1 实验部分
1.1 主要仪器与试剂
1290 Infinity Ⅱ型高效液相色谱-三重四极杆质谱联用系统(配备电喷雾离子源(ESI)和 ACQUITY UPLC BEH C18色谱柱(100 mm×2.1 mm,2.7 μm),美国Agilent科技公司);EXTRA型自动固相萃取系统(24位,北京普立泰科仪器有限公司);DC-24型防腐氮吹浓缩仪(24位,上海安谱实验科技股份有限公司);Milli-Q IQ 7000型超纯水系统(美国默克密理博公司);SECURA224-1S型分析天平(220 g×0.0001 g,德国赛多利斯公司);QL-901型涡旋混合器(0~2800 r/min可调,海门市其林贝尔仪器制造有限公司);FiveEasy Plus FP20型pH计(精度±0.01,梅特勒-托利多科技(中国)有限公司);5418R型高速离心机(艾本德中国有限公司)。
17种氟喹诺酮类混合标准溶液(100 μg/mL,0.1% NaOH,坛墨质检科技股份有限公司);甲醇(色谱纯,1.0 L)、甲酸(色谱纯,≥99%,50.0 mL)(国药集团化学试剂有限公司);甲酸铵(GR级,≥99%,上海阿拉丁生化科技股份有限公司);诺氟沙星-d5替代物(100 μg/mL,西格玛奥德里奇上海贸易有限公司);恩诺沙星-d5、环丙沙星-d8(均为100 μg/mL,加拿大多伦多研究化学品公司);13C3-氟甲喹内标(100 μg/mL,英国剑桥同位素实验室)。实验用水为超纯水系统制备的去离子水。
固相萃取柱采用HLB柱(500 mg/6 mL),填料为二乙烯苯和N-乙烯基吡咯烷酮共聚物。所有标准溶液在-18 ℃以下冷冻、密封、避光保存,使用前恢复至室温并充分混匀。
1.2 实验步骤
1.2.1 样品前处理
水样采集地点位于安徽省合肥市,涵盖城市供水管网末梢、居民小区二次供水设施、农村地下水井和水库取水口。使用2.5 L棕色玻璃采样瓶,按照HJ 494—2009《水质 采样技术指导》进行采集。水样采集后立即用甲酸调节至pH 2~4。使氟喹诺酮类化合物以质子化形式存在,提高其在反相固相萃取柱上的吸附效率[18]。样品于 4 ℃避光保存,24 h内完成分析。取1 L水样经0.45 μm玻璃纤维滤膜(Whatman GF/F,美国)过滤,去除悬浮颗粒。向滤液中加入10 μL替代物标准使用液(诺氟沙星-d5,0.5 mg/L)作为质量控制指标。
1.2.2 固相萃取富集
采用HLB固相萃取柱(500 mg/6 mL)进行样品富集。萃取柱依次用6 mL甲醇、6 mL水和 6 mL 1%甲酸溶液活化,活化过程保持柱填料始终湿润。将预处理后的水样以8~12 mL/min流速通过萃取柱,上样完毕后用6 mL甲醇溶液淋洗。抽真空干燥萃取柱20 min后,用10 mL V(甲酸)∶V(甲醇)=1∶1000溶液以1 mL/min流速洗脱,收集洗脱液。
1.2.3 浓缩定容
洗脱液在40 ℃下氮吹浓缩至近干,用V(甲酸铵/甲酸缓冲液)∶V(甲醇)=1∶1定容至 1.0 mL。加入10 μL内标使用液Ⅰ(恩诺沙星-d5和环丙沙星-d8,1.0 mg/L)和10 μL内标使用液Ⅱ(13C3-氟甲喹,0.2 mg/L),混匀后过0.22 μm滤膜,转移至进样瓶待测。
1.2.4 仪器分析
采用ACQUITY UPLC BEH C18色谱柱(100 mm×2.1 mm,1.7 μm)分离,流动相A为0.1%甲酸水溶液,流动相B为甲醇,梯度洗脱。质谱采用电喷雾正离子源(ESI+),多反应监测模式(MRM),根据保留时间和特征离子进行定性,内标法定量。每20个样品测定1个实验室空白和基质加标样品。
1.3 仪器工作条件
超高效液相色谱条件:流动相A为含0.1%甲酸的超纯水溶液,流动相B为色谱纯甲醇;柱温40 ℃,流速0.3 mL/min,进样体积5 μL。梯度洗脱程序见表1。
表1 梯度洗脱程序
Tab.1 Gradient elution program
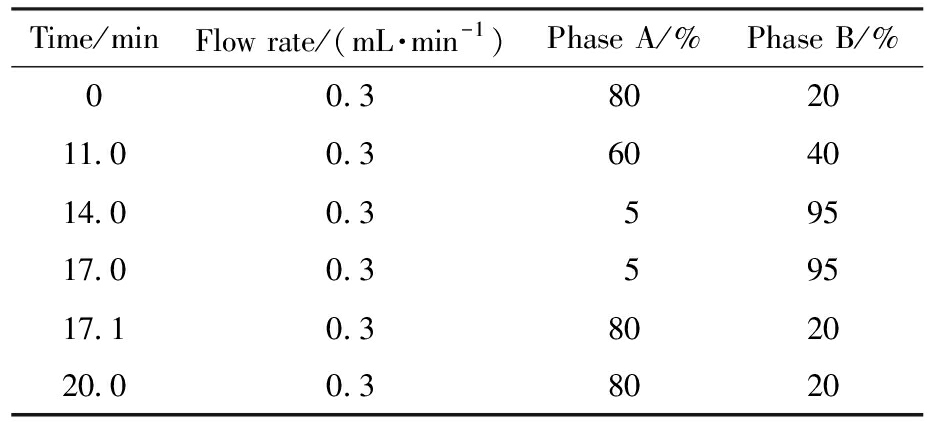
Time/minFlow rate/(mL·min-1)Phase A/%Phase B/%00.3802011.00.3604014.00.359517.00.359517.10.3802020.00.38020
质谱条件:电喷雾正离子源(ESI+)模式,毛细管电压2.0 kV,离子源温度150 ℃,脱溶剂温度500 ℃,锥孔气流量150 L/h,脱溶剂气流量800 L/h。采用多反应监测(MRM)模式。
2 结果与讨论
2.1 色谱条件优化
2.1.1 流动相组成的选择
采用2×4完全析因设计考察有机相(甲醇、乙腈)与水相添加剂(纯水、0.1%甲酸、0.1%乙酸、5 mmol/L甲酸铵)对17种氟喹诺酮类化合物检测响应的影响,以甲醇-水组为参照,结果见表2和图1。可以看出在相同水相添加剂条件下,甲醇组的相对响应强度均高于乙腈组,这与甲醇具有较强的质子给予能力、有利于正离子模式下电喷雾离子化有关[19]。添加0.1%甲酸后响应强度提升最为显著,甲醇组和乙腈组分别提高了35%和33%。甲酸使流动相维持在pH 2.8左右,促进氟喹诺酮类化合物羧基和哌嗪环的质子化,增强其在反相色谱柱上的保留和质谱响应;而0.1%乙酸和5 mmol/L甲酸铵虽也能提高响应,但效果不及甲酸且背景噪声较高。最终选择甲醇-0.1%甲酸作为流动相体系。
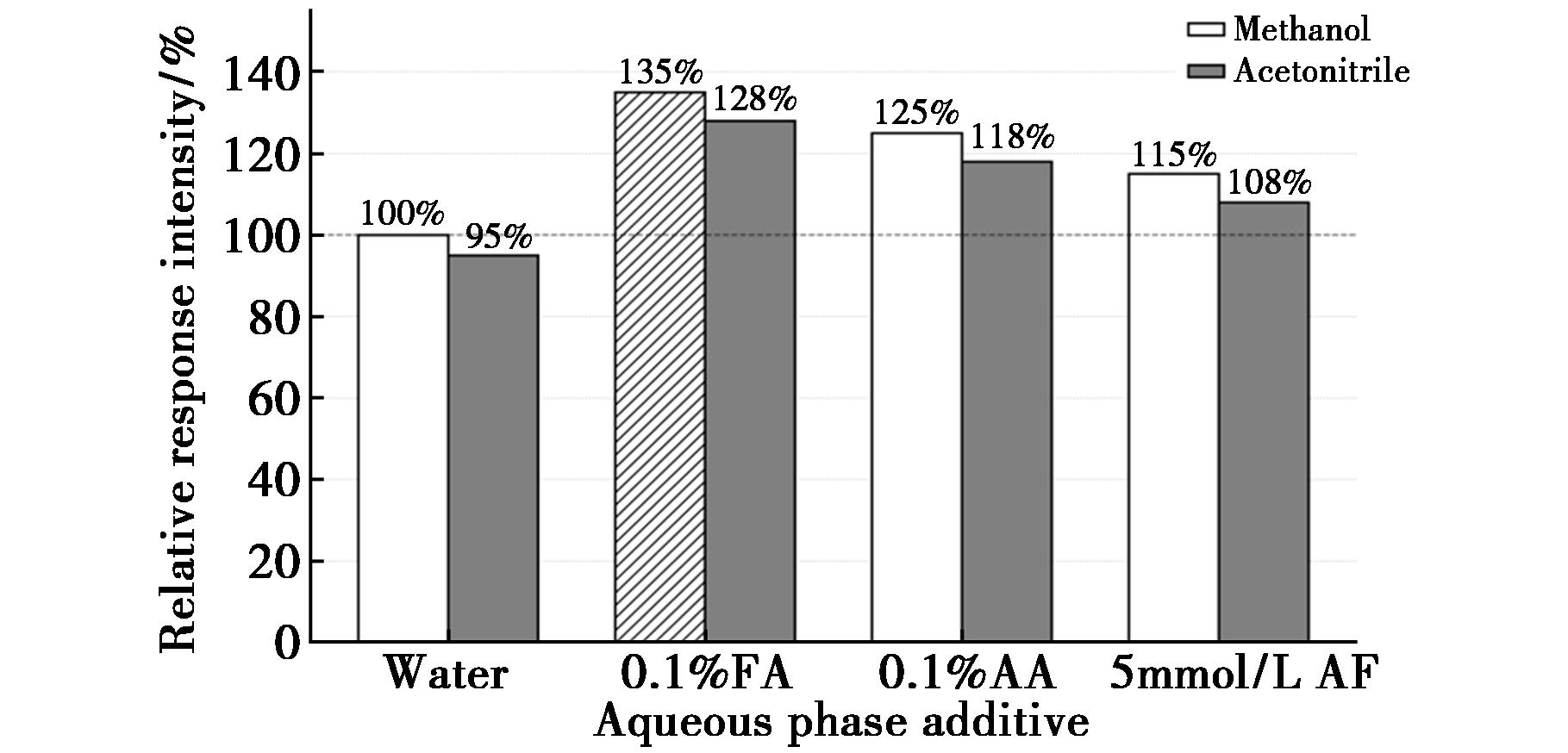
图1 流动相组成对相对响应强度的影响
Fig.1 Effect of mobile phase composition on relative response intensity
表2 不同流动相组成对分离效果的影响
Tab.2 Effect of different mobile phase compositions on chromatographic separation
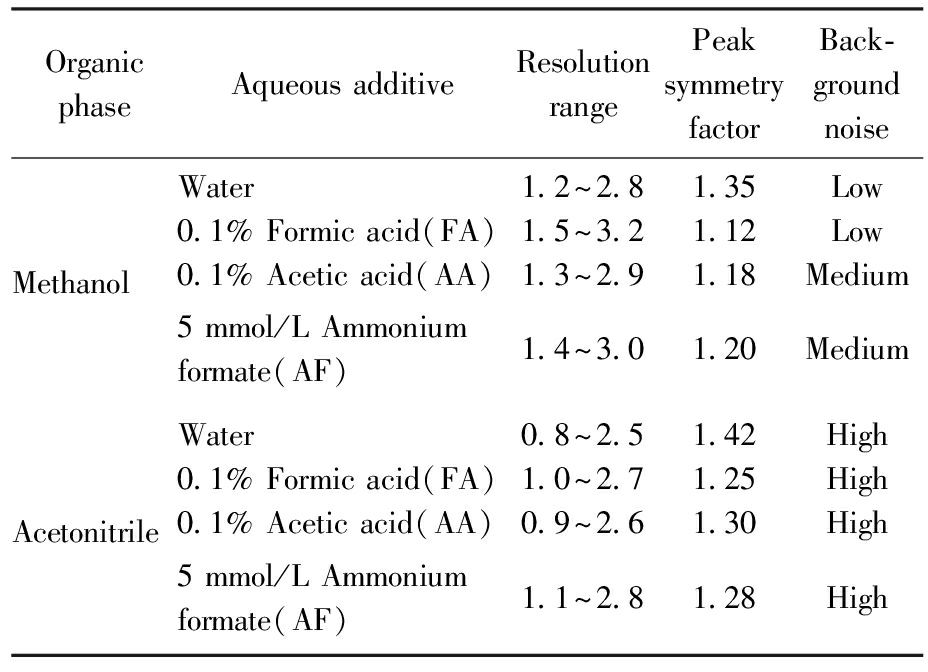
Organic phaseAqueous additiveResolution rangePeak symmetry factorBack-ground noiseMethanolWater0.1% Formic acid(FA)0.1% Acetic acid(AA)5 mmol/L Ammonium formate(AF)1.2~2.81.5~3.21.3~2.91.4~3.01.351.121.181.20LowLowMediumMediumAcetonitrileWater0.1% Formic acid(FA)0.1% Acetic acid(AA)5 mmol/L Ammonium formate(AF)0.8~2.51.0~2.70.9~2.61.1~2.81.421.251.301.28HighHighHighHigh
2.1.2 柱温和流速的优化
柱温和流速是影响色谱分离的重要参数。柱温优化实验在25~45 ℃范围内进行,实验结果见表3。结果显示40 ℃时各化合物的分离效果最佳。温度过低(25 ℃)时,峰形展宽,分析时间延长;温度过高(45 ℃)时,虽然保留时间缩短,但部分化合物的分离度下降。40 ℃时,柱压适中,各化合物的范德华力和氢键作用达到平衡,获得最优分离。流速优化在0.2~0.4 mL/min范围内进行,0.3 mL/min时综合效果最佳。流速过低会导致峰展宽和分析时间延长;流速过高则造成柱压升高(>35 MPa),影响色谱柱寿命,且部分化合物分离度下降。在优化条件下,方法的柱效达到15000理论塔板数/米。
表3 柱温和流速对分离效果的影响
Tab.3 Effect of column temperature and flow rate on chromatographic separation
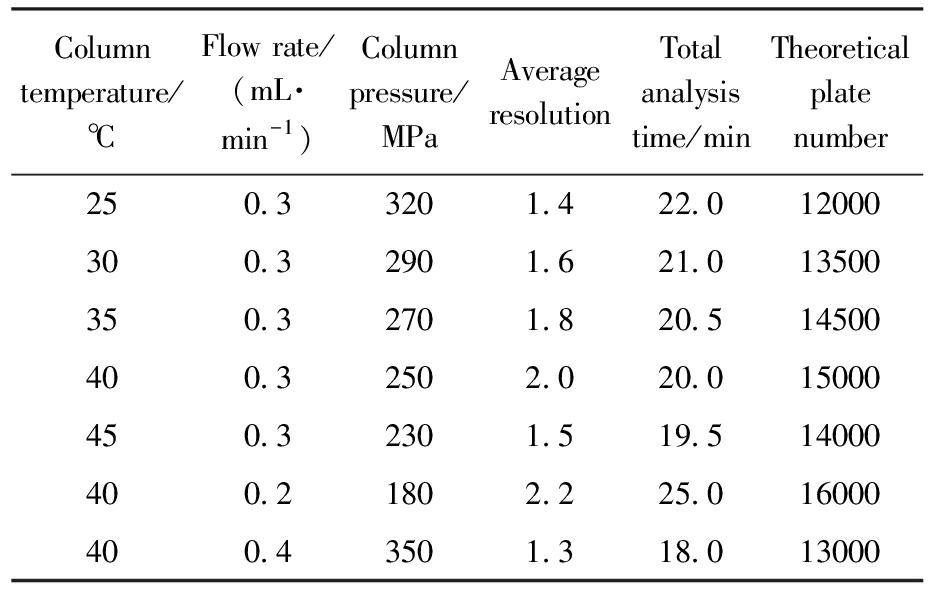
Column temperature/℃Flow rate/(mL·min-1)Column pressure/MPaAverage resolutionTotal analysis time/minTheoretical plate number250.33201.422.012000300.32901.621.013500350.32701.820.514500400.32502.020.015000450.32301.519.514000400.21802.225.016000400.43501.318.013000
2.2 质谱参数优化
2.2.1 脱溶剂温度优化
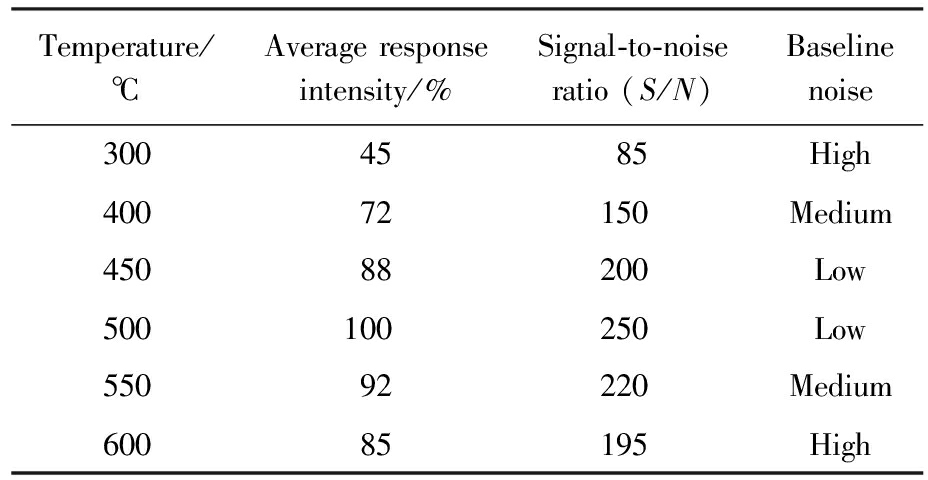
脱溶剂温度是影响离子化效率和检测灵敏度的关键参数。在300~600 ℃范围内对脱溶剂温度进行了系统优化。如表4所示,当温度过低(300~400 ℃)时,溶剂挥发不完全,导致离子源污染加重,基线噪音升高,信噪比降低;当温度升至500 ℃时,17种氟喹诺酮类化合物的响应强度达到最大值,平均信噪比提高了2.5倍。继续升高温度至600 ℃,由于部分热不稳定化合物开始出现热分解现象,导致了响应强度下降15%~20%。过高的脱溶剂温度还会加速离子源的老化,增加仪器维护频率。综合考虑灵敏度、稳定性和仪器寿命,确定500 ℃为最佳脱溶剂温度。
表4 脱溶剂温度对检测性能的影响
Tab.4 Effect of desolvation temperature on detection
Temperature/℃Average response intensity/%Signal-to-noise ratio (S/N)Baseline noise3004585High40072150Medium45088200Low500100250Low55092220Medium60085195High
2.2.2 毛细管电压的优化
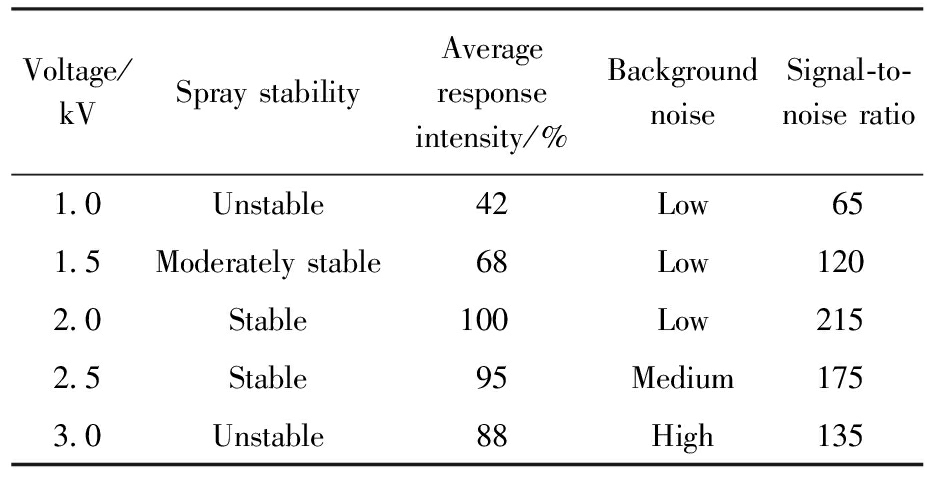
毛细管电压直接影响电喷雾的形成和离子化效率。在1.0~3.0 kV范围内优化毛细管电压,监测17种目标化合物的响应强度变化,结果如表5所示,当电压低于1.5 kV时,电喷雾不稳定,泰勒锥难以形成,导致离子化效率低下,各化合物响应强度仅为最优值的40%~60%。随着电压升高至2.0 kV,形成稳定的泰勒锥,液滴粒径减小,去溶剂化效率提高,所有化合物的响应强度达到最大值。继续增加电压至2.5~3.0 kV,虽然喷雾更加细密,但出现明显的电晕放电现象,导致背景噪音急剧增加,信噪比反而下降[14]。过高的电压还会产生大量的溶剂团簇离子,造成质谱图复杂化,影响定量准确性。因此,确定2.0 kV为最佳毛细管电压。
表5 毛细管电压优化结果
Tab.5 Optimization results of capillary voltage
Voltage/kVSpray stabilityAverage response intensity/%Background noiseSignal-to-noise ratio1.0Unstable42Low651.5Moderately stable68Low1202.0Stable100Low2152.5Stable95Medium1753.0Unstable88High135
2.2.3 锥孔电压的优化
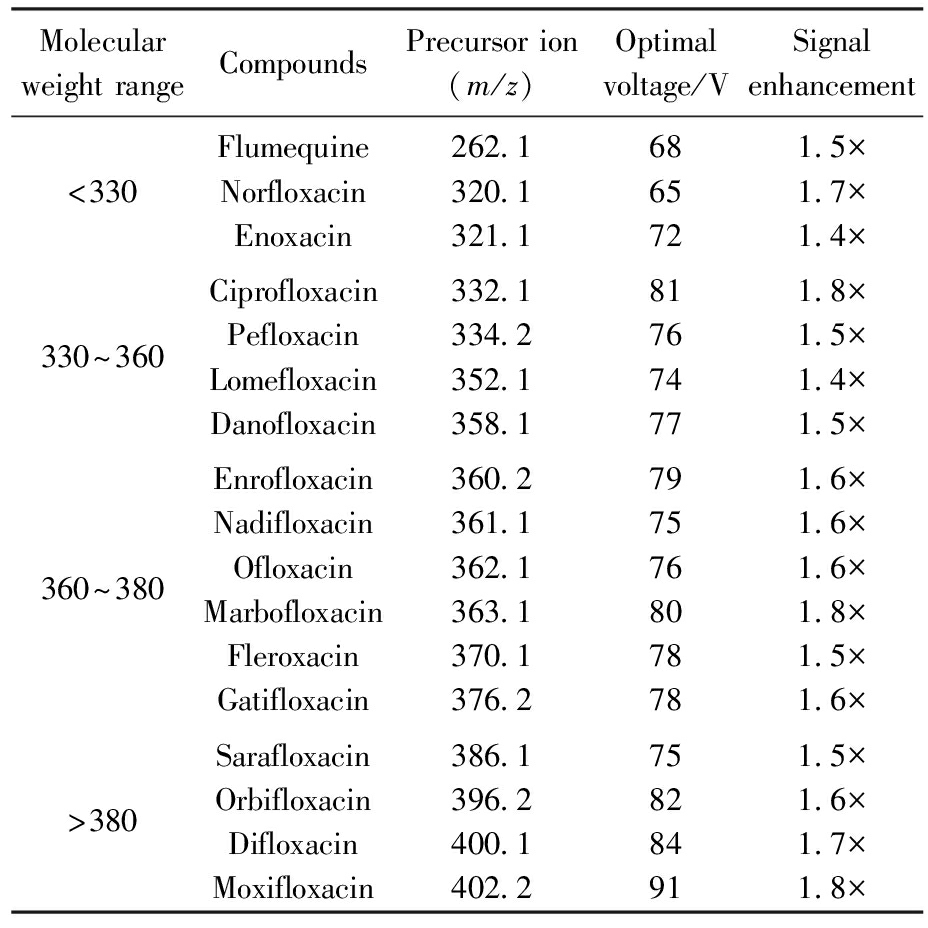
由于17种氟喹诺酮类化合物的分子结构和质量数存在差异,需要分别优化各自的锥孔电压。优化范围设定为20~100 V,以5 V为步长进行扫描。结果汇总于表6,诺氟沙星等分子量较小的化合物在较低电压(65~68 V)时响应最佳,而分子量较大的化合物(莫西沙星,m/z 402.2;二氟沙星,m/z 400.1)需要较高电压(84~91 V)才能获得最优传输效率。锥孔电压过低会导致离子传输效率不足,过高会引起源内裂解,影响母离子丰度[20]。通过优化,马波沙星在80 V、环丙沙星在81 V、氧氟沙星和培氟沙星在76 V时分别达到最佳响应。锥孔电压优化后,各化合物的平均检测灵敏度约为优化前的1.6倍。
表6 各化合物锥孔电压优化结果
Tab.6 Cone voltage optimization results for individual compounds
Molecular weight rangeCompoundsPrecursor ion (m/z)Optimal voltage/VSignal enhancement<330FlumequineNorfloxacinEnoxacin262.1320.1321.16865721.5×1.7×1.4×330~360CiprofloxacinPefloxacinLomefloxacinDanofloxacin332.1334.2352.1358.1817674771.8×1.5×1.4×1.5×360~380EnrofloxacinNadifloxacinOfloxacinMarbofloxacinFleroxacinGatifloxacin360.2361.1362.1363.1370.1376.27975768078781.6×1.6×1.6×1.8×1.5×1.6×>380SarafloxacinOrbifloxacinDifloxacinMoxifloxacin386.1396.2400.1402.2758284911.5×1.6×1.7×1.8×
2.3 方法性能评估
2.3.1 线性关系与相关系数
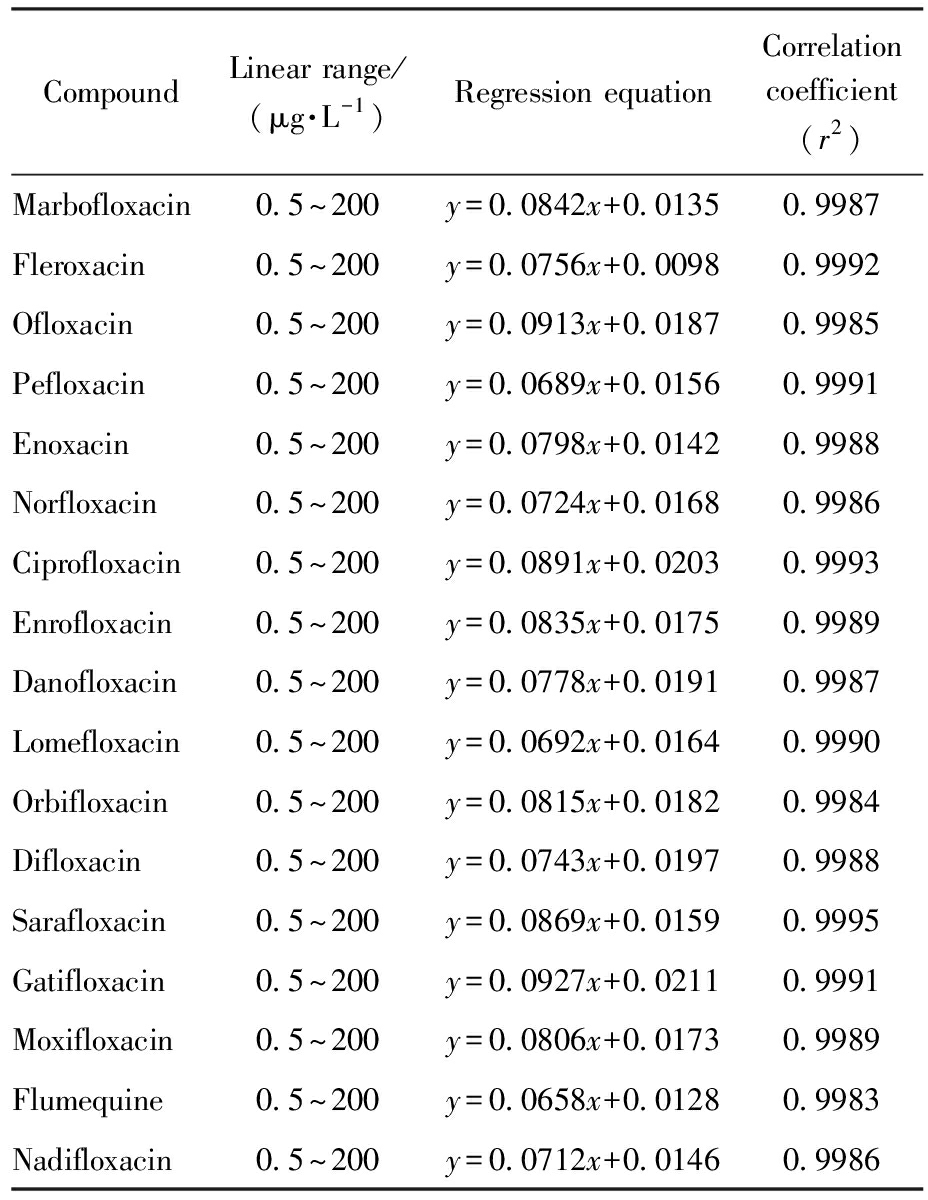
准确配制17种氟喹诺酮类抗生素的系列标准工作溶液,浓度范围为0.5~200 μg/L,共设置8个浓度点(0.5、1.0、5.0、10、20、50、100、200 μg/L)。每个浓度点加入相同浓度的内标物质(10 μg/L),按照优化后的仪器条件进行测定。以目标化合物与内标物的峰面积比值(y)对目标化合物浓度(x)进行线性回归分析,得到标准曲线方程。结果表明,17种氟喹诺酮类抗生素在0.5~200 μg/L浓度范围内均呈现良好的线性关系,相关系数(r2)均大于0.998,满足定量分析要求。各化合物的线性参数见表7。
表7 17种氟喹诺酮类抗生素的线性参数
Tab.7 Linear parameters of 17 fluoroquinolone antibiotics
CompoundLinear range/(μg·L-1)Regression equationCorrelation coefficient (r2)Marbofloxacin0.5~200y=0.0842x+0.01350.9987Fleroxacin0.5~200y=0.0756x+0.00980.9992Ofloxacin0.5~200y=0.0913x+0.01870.9985Pefloxacin0.5~200y=0.0689x+0.01560.9991Enoxacin0.5~200y=0.0798x+0.01420.9988Norfloxacin0.5~200y=0.0724x+0.01680.9986Ciprofloxacin0.5~200y=0.0891x+0.02030.9993Enrofloxacin0.5~200y=0.0835x+0.01750.9989Danofloxacin0.5~200y=0.0778x+0.01910.9987Lomefloxacin0.5~200y=0.0692x+0.01640.9990Orbifloxacin0.5~200y=0.0815x+0.01820.9984Difloxacin0.5~200y=0.0743x+0.01970.9988Sarafloxacin0.5~200y=0.0869x+0.01590.9995Gatifloxacin0.5~200y=0.0927x+0.02110.9991Moxifloxacin0.5~200y=0.0806x+0.01730.9989Flumequine0.5~200y=0.0658x+0.01280.9983Nadifloxacin0.5~200y=0.0712x+0.01460.9986
2.3.2 色谱分析结果
在优化的色谱条件下,17种氟喹诺酮类抗生素及内标物质在20 min内实现了良好的分离。各化合物色谱峰形对称、尖锐,无明显拖尾现象,分离度均大于1.5。采用梯度洗脱程序,充分利用了HPLC色谱柱的高效分离能力,在保证分离效果的同时缩短了分析时间,如图2所示。
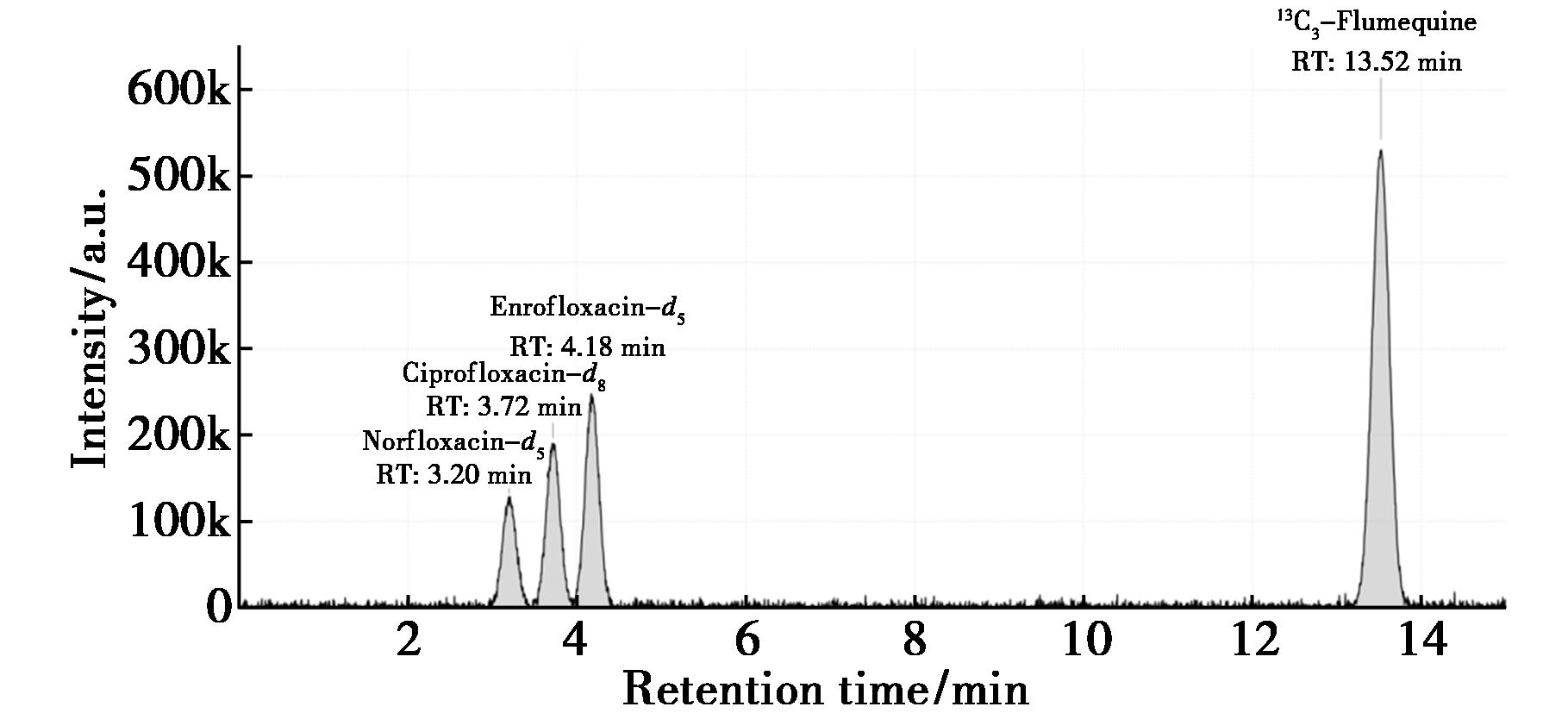
图2 空白样品HPLC-MS/MS总离子色谱图
Fig.2 HPLC-MS/MS total ion chromatogram of a blank
按照2.1、2.2优化后的仪器工作条件对已知浓度的质控样25AB024002进行检测,17种氟喹诺酮类抗生素HPLC-MS/MS谱图如图3所示。每种氟喹诺酮类抗生素的保留时间、母离子(m/z)、特征子离子(m/z)、碰撞能量(V)如表8所示。
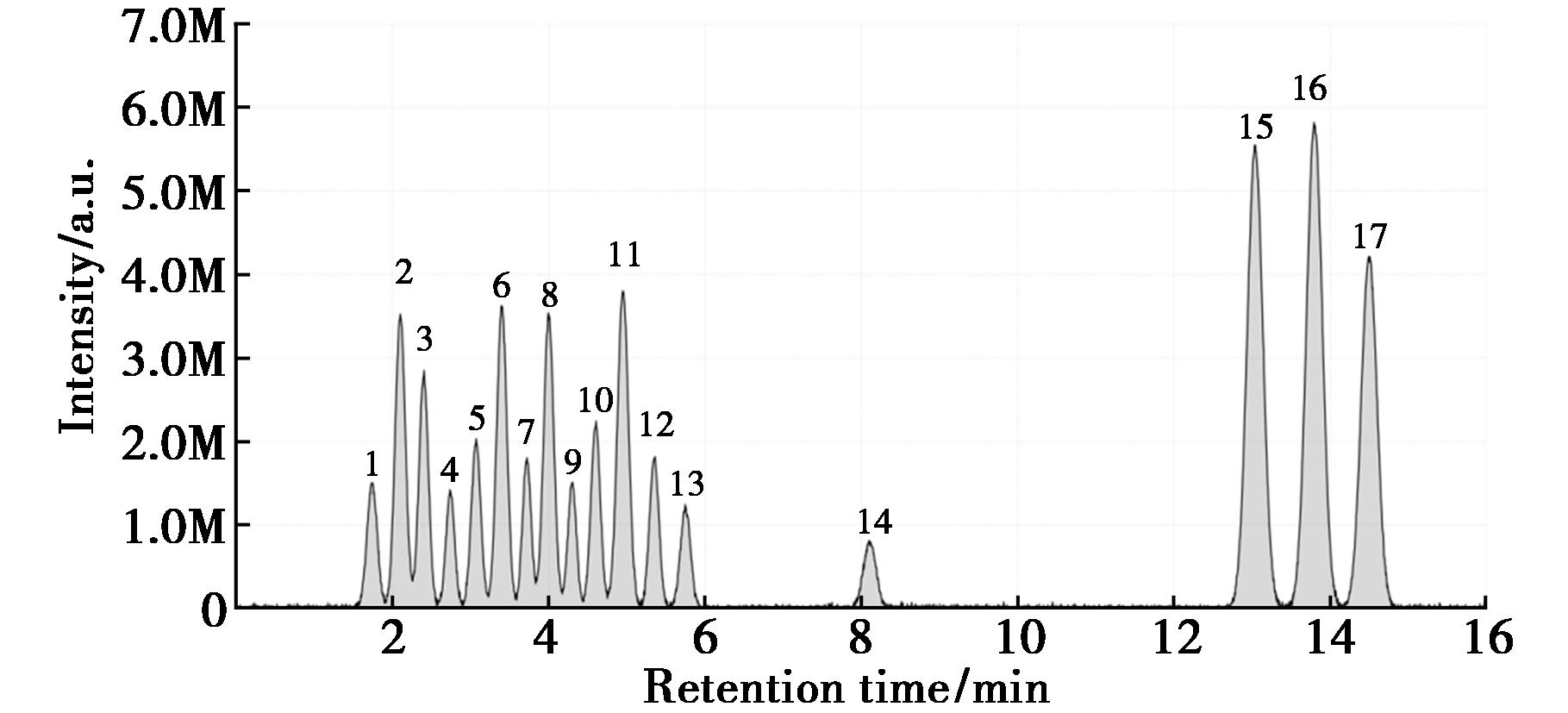
1~17对应抗生素见表11
图3 17种氟喹诺酮类抗生素HPLC-MS/MS色谱图
Fig.3 HPLC-MS/MS chromatogram of the 17 fluoroquinolone antibiotics
表8 17种氟喹诺酮类抗生素质谱多反应监测(MRM)参数
Tab.8 MS/MS multiple reaction monitoring (MRM) parameters for the 17 fluoroquinolone antibiotics
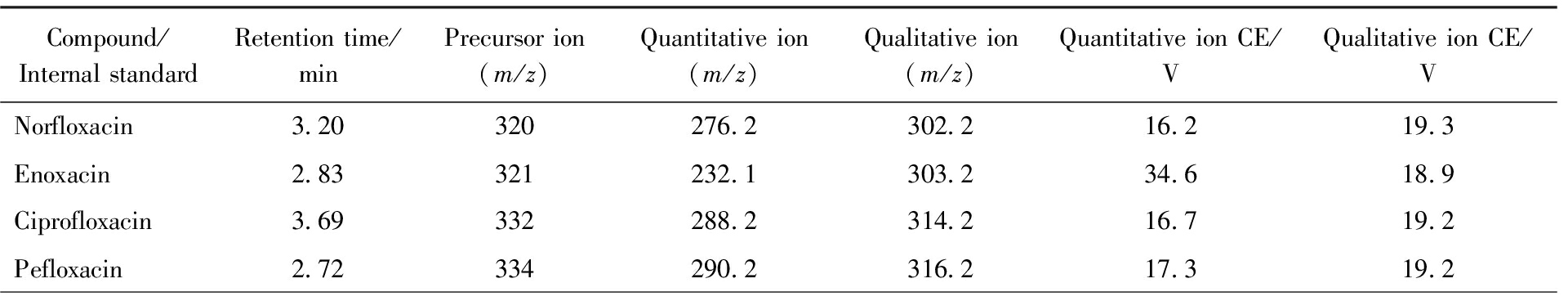
Compound/Internal standardRetention time/minPrecursor ion (m/z)Quantitative ion (m/z)Qualitative ion (m/z)Quantitative ion CE/VQualitative ion CE/VNorfloxacin3.20320276.2302.216.219.3Enoxacin2.83321232.1303.234.618.9Ciprofloxacin3.69332288.2314.216.719.2Pefloxacin2.72334290.2316.217.319.2
续表
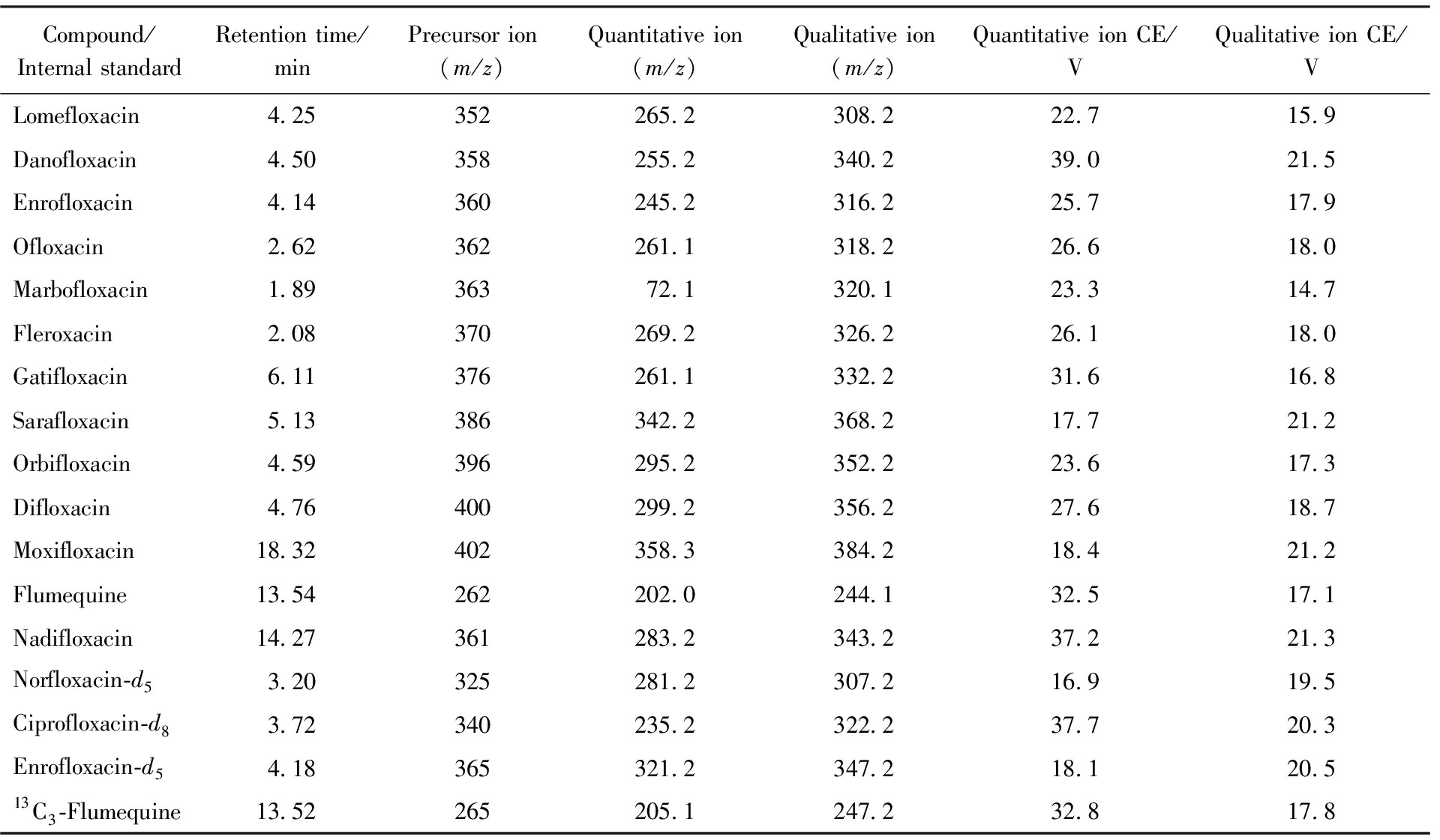
Compound/Internal standardRetention time/minPrecursor ion (m/z)Quantitative ion (m/z)Qualitative ion (m/z)Quantitative ion CE/VQualitative ion CE/VLomefloxacin4.25352265.2308.222.715.9Danofloxacin4.50358255.2340.239.021.5Enrofloxacin4.14360245.2316.225.717.9Ofloxacin2.62362261.1318.226.618.0Marbofloxacin1.8936372.1320.123.314.7Fleroxacin2.08370269.2326.226.118.0Gatifloxacin6.11376261.1332.231.616.8Sarafloxacin5.13386342.2368.217.721.2Orbifloxacin4.59396295.2352.223.617.3Difloxacin4.76400299.2356.227.618.7Moxifloxacin18.32402358.3384.218.421.2Flumequine13.54262202.0244.132.517.1Nadifloxacin14.27361283.2343.237.221.3Norfloxacin-d53.20325281.2307.216.919.5Ciprofloxacin-d83.72340235.2322.237.720.3Enrofloxacin-d54.18365321.2347.218.120.513C3-Flumequine13.52265205.1247.232.817.8
2.3.3 检出限与定量限
采用信噪比法结合逐级稀释法确定方法的检出限和定量限。将混合标准溶液逐级稀释,按照优化的前处理和仪器条件进行测定,以信噪比 S/N=3时的浓度作为检出限,S/N=10时的浓度作为定量限。为验证所得结果的可靠性,在计算得到的检出限和定量限浓度水平分别进行7次平行测定(表9),要求检出限浓度的检出率不低于95%,定量限浓度的相对标准偏差不超过20%,结果如表9所示。可以看出17种氟喹诺酮类抗生素的检出限范围为0.08~0.35 ng/L,定量限范围为0.25~1.15 ng/L。马波沙星的灵敏度最高,检出限为0.08 ng/L,得益于其在正离子模式下具有较高的离子化效率和特征碎片离子丰度。莫西沙星由于分子量较大且在该色谱条件下保留时间较长,基线噪音相对较高,检出限为0.35 ng/L。能满足饮用水中痕量氟喹诺酮类抗生素的检测需求。
表9 17种氟喹诺酮类抗生素的检出限和定量限
Tab.9 Detection limits and quantification limits of the 17 fluoroquinolone antibiotics
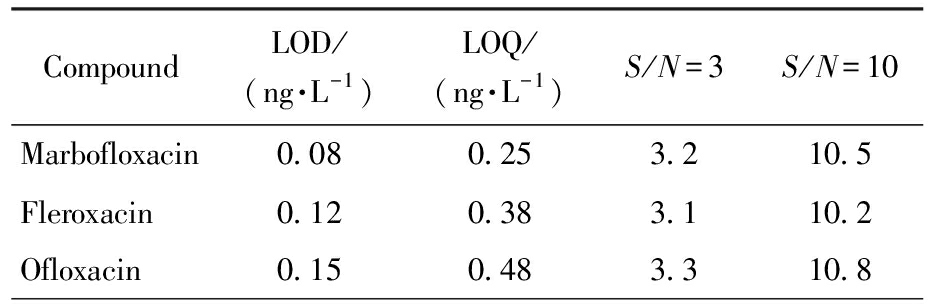
CompoundLOD/(ng·L-1)LOQ/(ng·L-1)S/N=3S/N=10Marbofloxacin0.080.253.210.5Fleroxacin0.120.383.110.2Ofloxacin0.150.483.310.8
续表
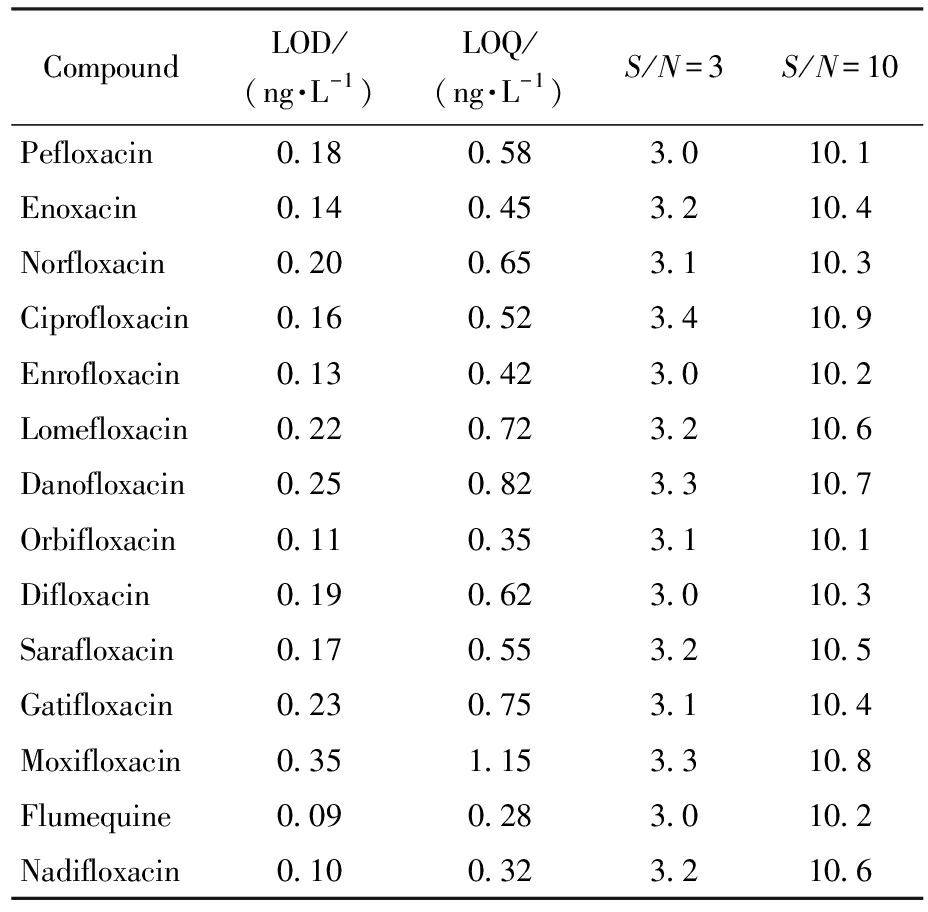
CompoundLOD/(ng·L-1)LOQ/(ng·L-1)S/N=3S/N=10Pefloxacin0.180.583.010.1Enoxacin0.140.453.210.4Norfloxacin0.200.653.110.3Ciprofloxacin0.160.523.410.9Enrofloxacin0.130.423.010.2Lomefloxacin0.220.723.210.6Danofloxacin0.250.823.310.7Orbifloxacin0.110.353.110.1Difloxacin0.190.623.010.3Sarafloxacin0.170.553.210.5Gatifloxacin0.230.753.110.4Moxifloxacin0.351.153.310.8Flumequine0.090.283.010.2Nadifloxacin0.100.323.210.6
2.3.4 精密度与准确度
方法的精密度和准确度通过加标回收实验进行评价。选取经检测不含目标化合物的空白水样,分别添加低(2.0 μg/L)、中(20.0 μg/L)、高(100.0 μg/L)3个浓度水平的混合标准溶液,每个浓度水平设置6个平行样品,按照建立的方法进行前处理和仪器分析。计算加标回收率和相对标准偏差(RSD),同时进行日内精密度(同一天内连续测定6次)和日间精密度(连续5天每天测定3次)实验。结果如表10所示,17种氟喹诺酮类抗生素在3个加标浓度水平的平均回收率范围为82.3%~108.5%,日内精密度RSD为 1.8%~5.8%,日间精密度RSD为3.5%~8.7%。其中,诺氟沙星、环丙沙星和恩诺沙星等常见化合物的回收率均在90%~105%之间,精密度RSD<5%,表现出优异的方法稳定性。加标回收率略低的化合物主要是莫西沙星(82.3%~87.6%),这可能与其分子结构中含有的二氟甲氧基和双环哌嗪基团在固相萃取过程中的吸附行为有关[19]。本方法的精密度和准确度均满足GB/T 5750—2023《生活饮用水标准检验方法》的技术要求,可用于饮用水中氟喹诺酮类抗生素的定量分析。
表10 方法的精密度和准确度实验结果
Tab.10 Experimental results for method precision and accuracy (n=6)
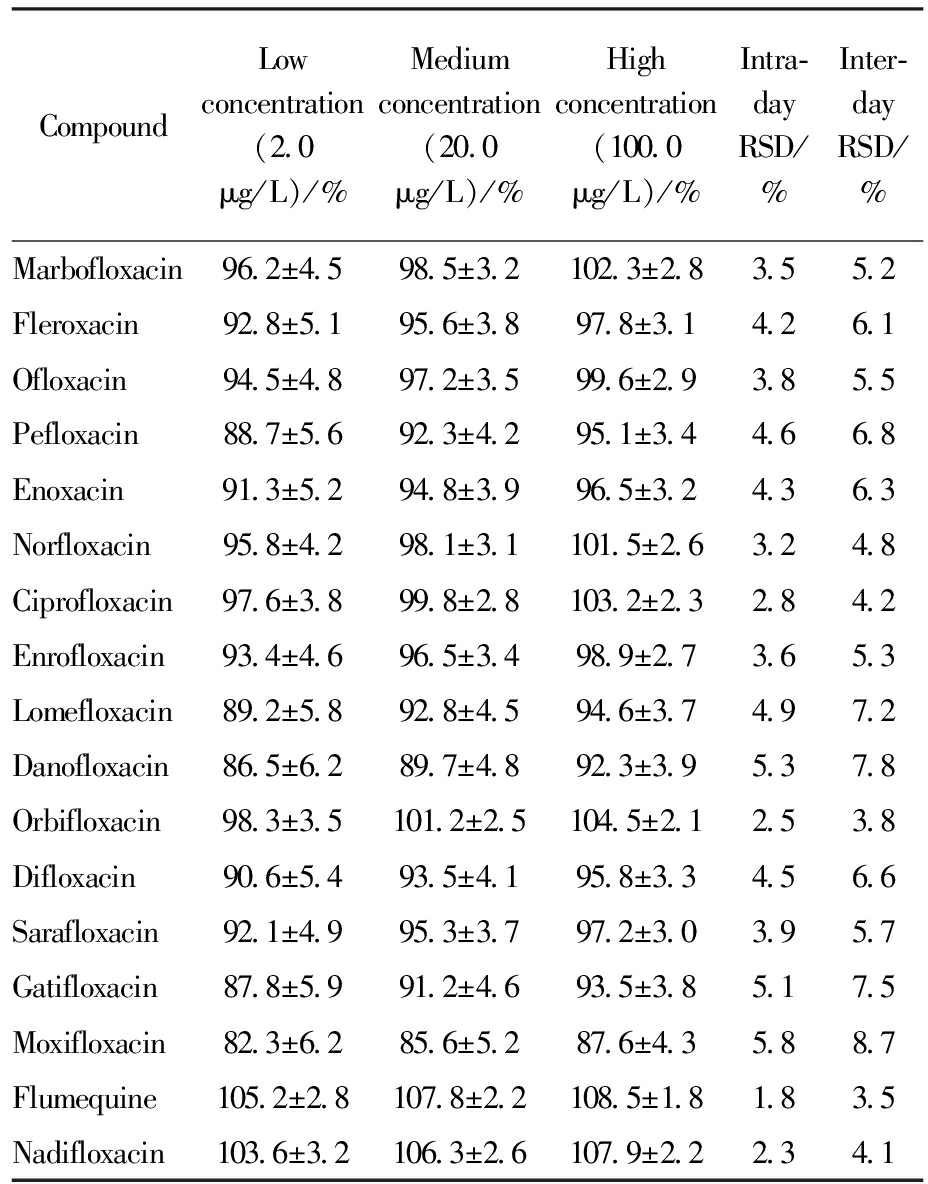
CompoundLow concentration (2.0 μg/L)/%Medium concentration (20.0 μg/L)/%High concentration (100.0 μg/L)/%Intra-day RSD/%Inter-day RSD/%Marbofloxacin96.2±4.598.5±3.2102.3±2.83.55.2Fleroxacin92.8±5.195.6±3.897.8±3.14.26.1Ofloxacin94.5±4.897.2±3.599.6±2.93.85.5Pefloxacin88.7±5.692.3±4.295.1±3.44.66.8Enoxacin91.3±5.294.8±3.996.5±3.24.36.3Norfloxacin95.8±4.298.1±3.1101.5±2.63.24.8Ciprofloxacin97.6±3.899.8±2.8103.2±2.32.84.2Enrofloxacin93.4±4.696.5±3.498.9±2.73.65.3Lomefloxacin89.2±5.892.8±4.594.6±3.74.97.2Danofloxacin86.5±6.289.7±4.892.3±3.95.37.8Orbifloxacin98.3±3.5101.2±2.5104.5±2.12.53.8Difloxacin90.6±5.493.5±4.195.8±3.34.56.6Sarafloxacin92.1±4.995.3±3.797.2±3.03.95.7Gatifloxacin87.8±5.991.2±4.693.5±3.85.17.5Moxifloxacin82.3±6.285.6±5.287.6±4.35.88.7Flumequine105.2±2.8107.8±2.2108.5±1.81.83.5Nadifloxacin103.6±3.2106.3±2.6107.9±2.22.34.1
2.3.5 基质效应评估
采用提取后添加法评估饮用水基质对17种氟喹诺酮类抗生素离子化效率的影响。分别制备纯溶剂标准溶液和基质匹配标准溶液(空白饮用水样经固相萃取处理后的提取液),在低(2.0 μg/L)、中(20.0 μg/L)、高(100.0 μg/L)3个浓度水平进行测定,每个浓度平行测定6次。按公式(1)计算基质效应(ME)。
ME(%)=(基质匹配标准溶液峰面积/
纯溶剂标准溶液峰面积)×100%
(1)
当ME值在80%~120%范围内时,表明基质效应可忽略;ME<80%表示存在离子抑制效应;ME>120%表示存在离子增强效应。结果见表11。可以看出,17种目标化合物的平均基质效应值范围为85.2%~112.6%,均在可接受范围内,表明饮用水基质对本方法的离子化效率影响较小。采用4种同位素内标进行校正可有效补偿基质效应引起的响应变化,使定量结果更加准确。
表11 17种氟喹诺酮类抗生素的基质效应评估结果
Tab.11 Evaluation of the matrix effect for the 17 fluoroquinolone antibiotics
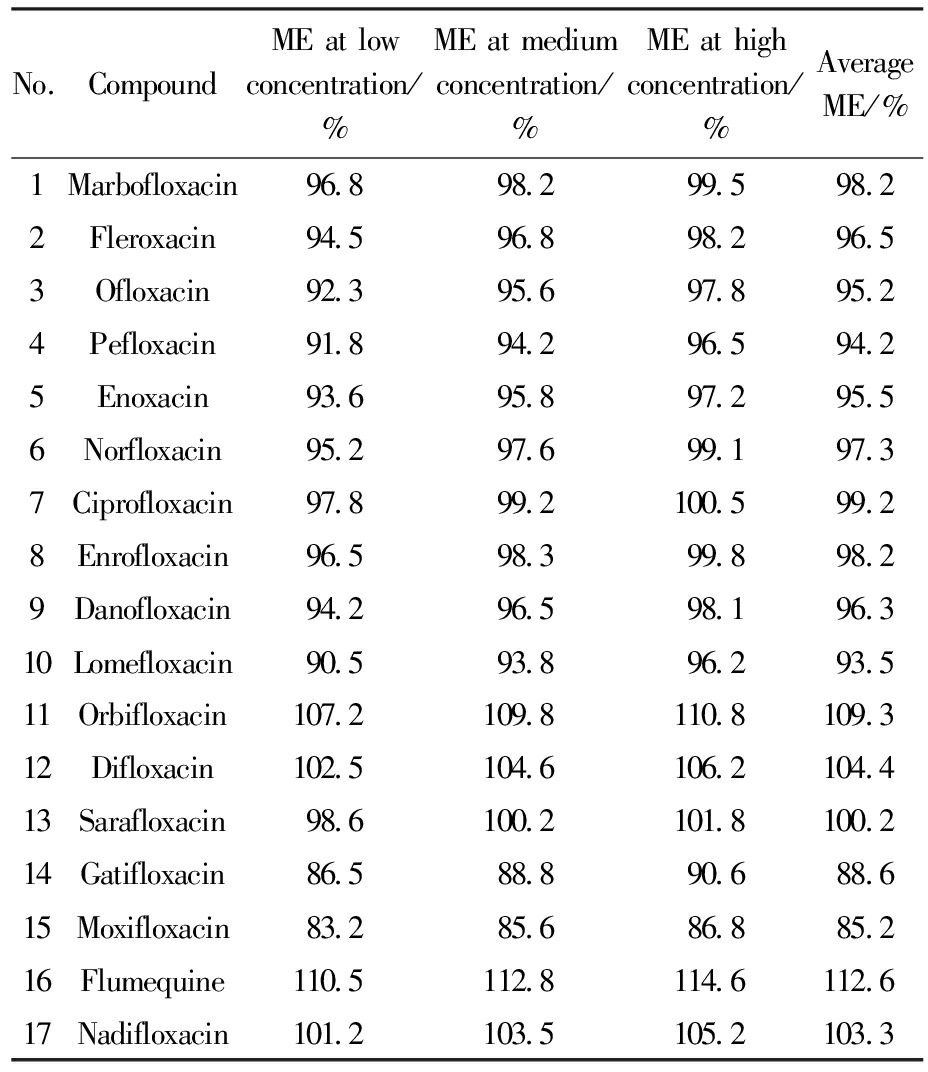
No.CompoundME at low concentration/%ME at medium concentration/%ME at high concentration/%Average ME/%1Marbofloxacin96.898.299.598.22Fleroxacin94.596.898.296.53Ofloxacin92.395.697.895.24Pefloxacin91.894.296.594.25Enoxacin93.695.897.295.56Norfloxacin95.297.699.197.37Ciprofloxacin97.899.2100.599.28Enrofloxacin96.598.399.898.29Danofloxacin94.296.598.196.310Lomefloxacin90.593.896.293.511Orbifloxacin107.2109.8110.8109.312Difloxacin102.5104.6106.2104.413Sarafloxacin98.6100.2101.8100.214Gatifloxacin86.588.890.688.615Moxifloxacin83.285.686.885.216Flumequine110.5112.8114.6112.617Nadifloxacin101.2103.5105.2103.3
2.3.6 与现行标准方法的比较
将本方法与现行国家标准方法进行比较(表12)。GB 31658.17—2021《食品安全国家标准 动物性食品中四环素类、磺胺类和喹诺酮类药物残留量的测定 液相色谱-串联质谱法》针对动物源性食品基质,喹诺酮类化合物检出限为1.0~2.0 μg/kg,定量限为2.0~5.0 μg/kg;GB 31656.3—2021《食品安全国家标准 水产品中诺氟沙星、环丙沙星、恩诺沙星、氧氟沙星、噁喹酸、氟甲喹残留量的测定 液相色谱-串联质谱法》针对水产品基质,检出限为0.5~1.0 μg/kg。本方法专门针对饮用水基质进行优化,通过改进固相萃取条件和质谱参数,将检出限降至0.08~0.35 ng/L,定量限降至0.25~1.15 ng/L,较现行标准降低了约3个数量级。本方法涵盖17种氟喹诺酮类抗生素,较国标(13种)更为全面;回收率为82.3%~108.5%,日内精密度为1.8%~5.8%,日间精密度为3.5%~8.7%,均有效满足GB/T 5750—2023《生活饮用水标准检验方法》的技术要求。
表12 本方法与现行标准方法的比较
Tab.12 Comparison between the developed method and the current standard methods
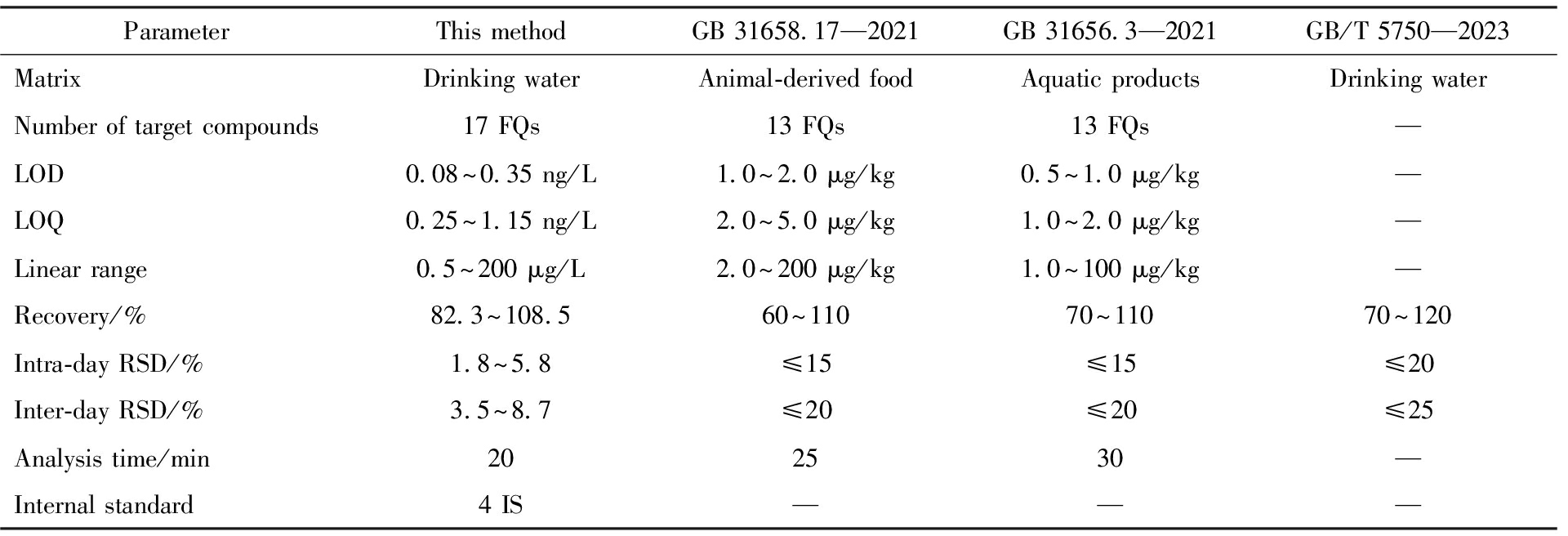
ParameterThis methodGB 31658.17—2021GB 31656.3—2021GB/T 5750—2023MatrixDrinking waterAnimal-derived foodAquatic productsDrinking waterNumber of target compounds17 FQs13 FQs13 FQs—LOD0.08~0.35 ng/L1.0~2.0 μg/kg0.5~1.0 μg/kg—LOQ0.25~1.15 ng/L2.0~5.0 μg/kg1.0~2.0 μg/kg—Linear range0.5~200 μg/L2.0~200 μg/kg1.0~100 μg/kg—Recovery/%82.3~108.560~11070~11070~120Intra-day RSD/%1.8~5.8≤15≤15≤20Inter-day RSD/%3.5~8.7≤20≤20≤25Analysis time/min202530—Internal standard4 IS———
2.4 在实际样品检测中的应用
为验证所建立方法的实用性,采集了安徽省合肥市不同类型的饮用水样品共50份进行检测。采样时间为2025年3~5月,采样地点包括:自来水15份(蜀山区、庐阳区、包河区供水管网末梢)、瓶装纯净水15份(市售主流品牌)、地下水10份(肥东县农村饮用水井,井深30~80 m)和水源地原水10份(大房郢水库取水口)。所有样品按照建立的方法进行前处理和仪器分析,检测结果如表13所示。
表13 实际饮用水样品中氟喹诺酮类抗生素的检出情况
Tab.13 Detection of fluoroquinolone antibiotics in real drinking water samples
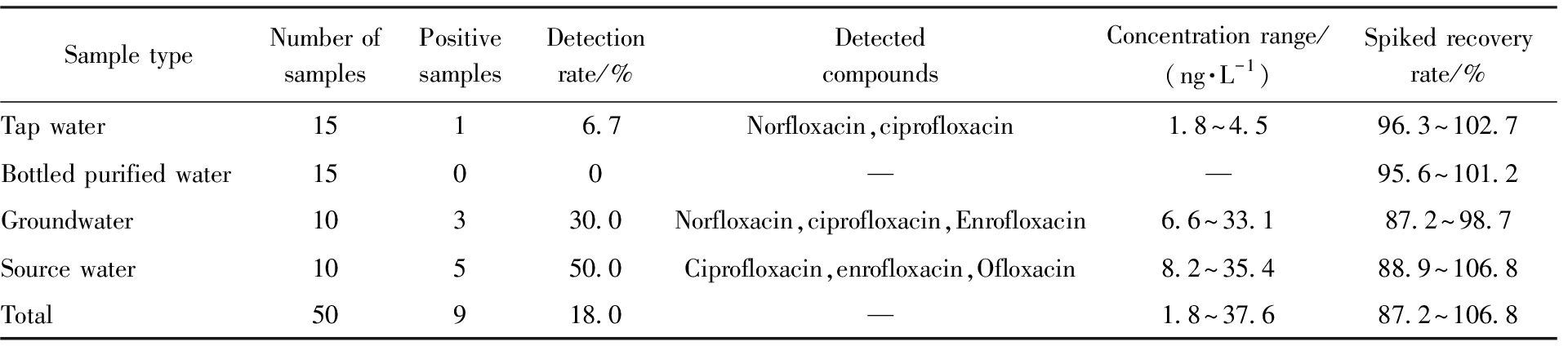
Sample typeNumber of samplesPositive samplesDetection rate/%Detected compoundsConcentration range/(ng·L-1)Spiked recovery rate/%Tap water1516.7Norfloxacin,ciprofloxacin1.8~4.596.3~102.7Bottled purified water1500——95.6~101.2Groundwater10330.0Norfloxacin,ciprofloxacin,Enrofloxacin6.6~33.187.2~98.7Source water10550.0Ciprofloxacin,enrofloxacin,Ofloxacin8.2~35.488.9~106.8Total50918.0—1.8~37.687.2~106.8
检测结果显示,在50份实际样品中,有9份检出氟喹诺酮类抗生素残留,检出率为18%。其中恩诺沙星、环丙沙星和诺氟沙星的检出频率最高,分别在7、6和4份样品中检出,浓度范围为1.8~37.6 ng/L。地下水和水源地原水中的检出浓度普遍高于自来水和瓶装水,这可能与地表径流和农业面源污染有关。值得注意的是,虽然检出浓度远低于相关限值标准,但多种抗生素的共存可能产生协同效应,其长期暴露的健康风险仍需关注。所有阳性样品的加标回收率在87.2%~106.8%之间,RSD<7.5%,表明该方法在实际样品检测中具有良好的准确性和重现性。
3 结论
本研究成功建立了固相萃取-高效液相色谱-串联质谱联用法同时测定饮用水中17种氟喹诺酮类抗生素的分析方法。通过系统优化前处理条件和仪器参数,实现了目标化合物的高效富集、完全分离和灵敏检测。方法学验证结果表明,该方法具有宽线性范围(0.5~200 μg/L)、低检出限(0.08~0.35 ng/L)、高回收率(82.3%~108.5%)和良好精密度等优点,各项技术指标均满足或优于现行国家标准要求。在实际样品应用中,该方法成功检测出多种氟喹诺酮类抗生素残留,证实了其在饮用水质量监测中的实用性和可靠性。与现有方法相比,本方法的主要优势在于:一次进样可同时检测17种目标化合物,分析效率高;检出限降低1~2个数量级,可满足痕量和超痕量分析需求;自动化程度高,减少了人为操作误差。该方法的建立为饮用水中氟喹诺酮类抗生素的常规监测提供了标准化的分析程序,也为评估抗生素污染的环境风险、制定相关水质标准和保障饮用水安全提供了重要的技术支撑。
[1]Xie J P,Huang Y,Song J.J.Sichuan Norm.Univ.Nat.Sci.,2023,46(6):719-730;708.
谢建平,黄煜,宋洁.四川师范大学学报(自然科学版),2023,46(6):719-730;708.
[2]Wu J.Removal of Moxifloxacin in Water by G-C3N4TiO2@MoS2 Composite.Hangzhou:Zhejiang University,2019.
吴俊.g-C3N4@TiO2@MoS2复合材料去除水中莫西沙星的研究.杭州:浙江大学,2019.
[3]Tang J,Cheng Q,Sun W X.World Notes Antibiot.,2016,37(5):198-203.
唐炯,程强,孙文霞.国外医药(抗生素分册),2016,37(5):198-203.
[4]Zhao X D,Lv C Z,Yu X Z,Liu H S,Liu S Q.Chin.J.Crit.Care Med.,2020,40(11):1047-1056.
赵晓东,吕传柱,于学忠,刘红升,刘双庆.中国急救医学,2020,40(11):1047-1056.
[5]Wei J P,Yang L,Yu F.Organo Fluor.Ind.,2012,(4):47-51.
韦锦萍,杨琳,于飞.有机氟工业,2012,(4):47-51.
[6]Meng S L,Li M X,Chen X,Qiu L P,Xu H M,Song C,Li D D,Fan L M.J.Agro-Environ.Sci.,2025,44(3):580-593.
孟顺龙,李鸣霄,陈曦,裘丽萍,徐慧敏,宋超,李丹丹,范立民.农业环境科学学报,2025,44(3):580-593.
[7]Li H M,Ouyang Z Y,Bai J M,Li B,Liang Z J,Xia Z H,Zhang L,Long D F,Li Y J.Asian J.Ecotoxicol.,2024,19(6):190-207.
李慧民,欧阳章燕,白珈鸣,李冰,梁祖金,夏智恒,张琳,龙丹凤,李拥军.生态毒理学报,2024,19(6):190-207.
[8]Li Y J,Chen Z R,Wang X P.Mod.Chem.Ind.,2018,38(9):237-241.
李玉静,陈志冉,王雪平.现代化工,2018,38(9):237-241.
[9]Hou M Y,Sun D N,Yan L X,Fu L W,Wang H D,Yu J L,Liu H T.Chin.J.Anal.Lab.,2025,44(1):148-158.
侯铭洋,孙大妮,闫李霞,付龙文,王虹丹,于佳洛,刘惠涛.分析试验室,2025,44(1):148-158.
[10]Jiang J,Wu Z Z,Ma S T,Zhang X B,Wu Y P,Zhang S L,Tong W Z,Liu F Y.Phy.Test.Chem.Anal.part B:Chem.Anal.,2025,61(8):960-970.
姜俊,吴珍珍,马苏婷,张秀博,吴银萍,张世林,童渭泽,刘方毅.理化检验-化学分册,2025,61(8):960-970.
[11]Guo W J,Cao Y Y,Li L,Zhu C,Zhang H,Wang C,Shi J H,Sun J L.Phy.Test.Chem.Anal.part B:Chem.Anal.,2025,61(5):577-586.
郭文建,曹燕燕,李琳,朱晨,张慧,王超,石敬华,孙俊玲.理化检验-化学分册,2025,61(5):577-586.
[12]Ding Z R,Li Y Q,Wang X,Yan Y N,Li Y X,Xu W J,Li X X,Chen M J,Jin M.Chin.J.Environ.Eng.,2022,16(2):674-683.
丁紫荣,黎玉清,王雄,闫雅楠,李彦希,许文杰,李香香,陈铭杰,金梦.环境工程学报,2022,16(2):674-683.
[13]Xie Y Q.Research on Clinical Mass Spectrometry Methods for Immunosuppressant Drugs.Beijing:Beijing University of Chinese Medicine,2023.
谢以清.免疫抑制剂类药物临床质谱检测方法研究.北京:北京中医药大学,2023.
[14]Wagil M,Kumirska J,Stolte S, ukaszewicz P,Stepnowski P,Bia
ukaszewicz P,Stepnowski P,Bia k-bielińska A.Sci.Total.Environ.,2014,493:1006-1013.
k-bielińska A.Sci.Total.Environ.,2014,493:1006-1013.
[15]Tong L,Li P,Wang Y X,Zhu K Z.Chemosphere,2009,74(8):1090-1097.
[16]Wang T,Chen M T.China Food Saf.Mag.,2020,(7):66-70.
王婷,陈明涛.食品安全导刊,2020,(7):66-70.
[17]Liao J,Li Q S.Environ.Chem.,2022,41(5):1538-1547.
廖杰,李青松.环境化学,2022,41(5):1538-1547.
[18]Ma L S,Xie W P,Yin Y,Shan Q,Liu S G,Li L C,Zhao C,Dai X X,Wei L T,Zheng G M.J.Chin.Mass Spectrom.Soc.,2021,42(6):1025-1032.
马丽莎,谢文平,尹怡,单奇,刘书贵,李丽春,赵成,戴晓欣,魏林婷,郑光明.质谱学报,2021,42(6):1025-1032.
[19]Jing Y.Three-Dimensional Composite Aerogels Decorated with MIL-88B(Fe) for Activation Persulfate Removal of Norfloxacin from Water.Changsha:Hunan University,2022.
景颖.MIL-88B(Fe)修饰的三维复合气凝胶活化过硫酸盐去除水中诺氟沙星的研究.长沙:湖南大学,2022.
[20]Ferrer I,Thurman E M.TrAC Trends Anal.Chem.,2012,32:63-81.