黄芪是山西十大道地药材之一[1],来自豆科植物膜荚黄芪Astragalus membranaceus(Fisch.) Bge.或蒙古黄芪Astragalus membranaceus(Fisch.) Bge.var.mongholicus(Bge.)的干燥根[2],其主要活性成分为黄芪多糖(Astragalus Polysaccharide,APS),研究表明不同分子量黄芪多糖具有不同生物活性[3],高分子量(1000 kDa以上)黄芪多糖可通过增强免疫细胞活性、特异性抗体滴度,提高机体免疫应答能力及疫苗效力[4,5];低中分子量(10~1000 kDa)黄芪多糖可通过调控免疫细胞、免疫器官、免疫因子发挥抗炎活性,目前低分子量(<10 kDa)范围中0.3、2、2.7、4.9、5.64、10 kDa分子量已得到均一多糖并进行结构分析[6-9],而3 kDa左右的均一APS未见报道。黄芪多糖作为疫苗佐剂可以增强免疫效果,提高抗体效价[10],且因结构明确、生物相容性好、易于化学修饰等特点,为其药物递送系统中的应用提供了可能[11]。因此,本文通过超滤截留法和离子、凝胶色谱分离法制备3 kDa左右均一分子量黄芪多糖,并确认其结构特征,为进一步探究小分子量APS作为免疫增强制剂的构效关系及开发提供理论依据。
1 实验部分
1.1 主要仪器与试剂
TU-1810型紫外-可见分光光度计(北京普析通用仪器有限公司);IRSpirit-X型傅里叶变换红外光谱仪(日本京都岛津制作所);AB-135S型十万分之一电子天平(瑞士METTLER公司);U3000型凝胶色谱-示差-多角度激光光散射系统、Thermo ICS 5000+型离子色谱系统(美国 Thermo Fisher Scientific公司);Optilab T-rEX型示差检测器、DAWN HELEOS Ⅱ型激光光散射检测器(美国Wyatt technology公司);HITACH SU8010型冷场发射扫描电子显微镜(日本株式会社日立制作所)。
黄芪饮片(批次:230402,山西元和堂中药有限公司);D101大孔树脂(山东科源生化有限公司);透析袋(3 kDa,上海源叶生物科技有限公司);DEAE-52离子纤维素(上海麦克林生化科技有限公司);Sephadex G-50(合肥博美生物科技有限公司);无水葡萄糖对照品(纯度>99%,批号:190106,上海融禾医药科技有限公司);苯酚(分析纯,天津市北联精细化学品开发有限公司);浓硫酸、无水乙醇(分析纯,天津市天力化学试剂有限公司)。单糖标准品:岩藻糖(Fuc,2438-80-4)、鼠李糖(Rha,10030-85-0)、阿拉伯糖(Ara,5328-37-0)、半乳糖(Gal,26566-61-0)、葡萄糖(Glc,50-99-7)、木糖(Xyl,58-86-6)、甘露糖(Man,3458-28-4)、果糖(Fru,57-48-7)、核糖(Rib,50-69-1)、半乳糖醛酸(Gal-UA,14982-50-4)、葡萄糖醛酸(Glc-UA,6556-12-3)、甘露糖醛酸(Man-UA,6814-36-4)、古罗糖醛酸(Gul-UA,15769-56-9)(美国Sigma公司)。
1.2 实验方法
1.2.1 黄芪多糖的制备
将黄芪饮片粉碎,过40目筛,精密称取50.00 g黄芪粉末,置于1000 mL圆底烧瓶,加150 mL 75%无水乙醇,解吸40 min,按照料液比 1∶12(g/mL)加入80 ℃蒸馏水,80 ℃减压蒸馏 6 min,抽滤,药渣同法提取2次,合并滤液,浓缩至250 mL,加无水乙醇至含醇量80%,静置过夜,抽滤,Sevage法除蛋白,大孔树脂除色素[12],浓缩冻干,得黄芪多糖,精密称定其质量备用。
1.2.2 透析法分离3 kDa及以下黄芪多糖
为获得分子量为3 kDa及以下的高纯度均一黄芪多糖,采用串联纯化方案,首先通过透析法基于分子尺寸截留初步分离低分子量组分;其次利用DEAE-52离子纤维柱依据电荷差异去除带电杂质;最后通过Sephadex G-50凝胶柱基于分子尺寸进一步纯化,以获得单体多糖组分。
1.2.2.1 透析袋的预处理
将截留分子量为3 kDa的透析袋剪成约 15 cm小段,依次用纯净水、1 mmol/L EDTA与2% NaHCO3混合溶液煮沸10 min,纯水漂洗后浸没于去离子水中,4 ℃保存备用。
1.2.2.2 3 kDa及以下黄芪多糖的透析过程
取一定量1.2.1干燥黄芪多糖粉末,加入适量蒸馏水,冰箱4 ℃下制备饱和溶液,离心后将上清液转移至留分子量为3 kDa透析袋中,多糖溶液约占透析袋体积的2/3,排出气泡,析袋用透析夹封口,放入盛有蒸馏水的大烧杯中,于4 ℃下透析。每12 h更换水溶液,直至透析袋不再透析出新物质,即烧杯中的溶液不再变色。将所得透析溶液回流浓缩,冻干,精密称定其质量,即得 3 kDa及以下分子量的黄芪多糖。
1.2.3 DEAE-52离子纤维柱纯化APS-3k
1.2.3.1 DEAE-52纤维素的预处理
DEAE-52纤维素经蒸馏水充分浸泡后,依次用0.5 mol/L的盐酸和0.5 mol/L的NaOH溶液处理,洗至中性,湿法装柱至纤维素层高度为225 mm[13]。
1.2.3.2 APS-3k溶液制备
称取0.2 g APS-3k,溶于10 mL离心管中,超声30 min,使其充分溶解,超声结束后以4000 r/min离心10 min,弃去不溶物,即得APS-3k溶液。
1.2.3.3 上样洗脱
将APS-3k溶液旋转上样,待液面完全进入填料中后,依次用纯化水、0.1和0.3 mol/L NaCl溶液作为流动相进行梯度洗脱,流速控制为 1 mL/min并用集液瓶收集洗脱液,每瓶收集 5 mL,每种流动相接收10瓶。
1.2.3.4 标准曲线的制备
葡萄糖对照品溶液的制备:精密称取14.1 mg无水葡萄糖对照品放入烧杯中,用蒸馏水溶解,转移至100 mL容量瓶中,定容至刻度,摇匀,得到浓度为0.141 mg/mL的无水葡萄糖对照品溶液。
制作标准曲线:精密移取对照品溶液0.00、0.25、0.30、0.35、0.45、0.60、0.70、0.90 mL于 10 mL比色管中,加入蒸馏水至1.0 mL,加入5%的苯酚溶液0.6 mL,缓慢连续滴入3.0 mL浓硫酸,放置2 min,摇匀,沸水浴显色20 min,冷却至室温。以相应试剂为空白,在490 nm处测定吸光度A,计算标准曲线。
1.2.3.5 绘制流出曲线
采用1.2.3.4方法对洗脱液中的糖类物质进行检测。将测得的A通过标准曲线计算出C,以管数为横坐标,C为纵坐标,绘制出流出曲线。
1.2.4 Sephadex G-50凝胶柱纯化APS-1
1.2.4.1 Sephadex G-50凝胶的预处理
称取25 g Sephadex G-50颗粒粉末,加入去离子水煮沸溶胀15 min,冷却后超声除去气泡。湿法装柱后柱高225 mm。用2~3倍柱体积的流动相平衡完成后备用[14]。
1.2.4.2 上样洗脱
精密称取一定体积APS-1,蒸馏水溶解后定容,胶头滴管吸取样品,沿柱壁缓慢旋转上样。设置流速为1 mL/min。待样品全部进入填料中后,用纯化水作为流动相进行洗脱,每瓶收集5 mL,共接收20瓶。按照1.2.3.5方法绘制流出曲线。
1.2.4.3 优化Sephadex G-50凝胶纯化APS-1条件
按照1.2.4.2上样方法,考察不同浓度(2、3、4、5、6 mg/mL)的黄芪多糖溶液,不同上样体积(6、8、10、12 mL)对洗脱曲线和分离效果的影响,优化Sephadex G-50凝胶过滤纯化条件,确定最佳上样参数,以提高目标组分的纯度。
1.2.5 APS-1a的纯度测定
精密称取5 mg APS-1a,用蒸馏水定容至 10 mL容量瓶,精密移取1.0 mL该溶液按照1.2.3.4方法检测A并计算APS-1a纯度。
1.2.6 APS-1a的分子量检测
色谱条件:凝胶排阻色谱柱Ohpak SB-805 HQ(300 mm×8 mm)和Ohpak SB-803 HQ(300 mm×8 mm)串联;柱温45 ℃,进样量100 μL,流动相A(0.02% NaN3,0.1 g/mL NaNO3),流速0.6 mL/min,洗脱梯度:等度,75 min。
样品溶液的制备:将APS-1a溶解在0.1 g/mL NaNO3水溶液(质量分数0.02% NaN3)中,终浓度为1 mg/mL,并通过孔径为0.45 μm的过滤器过滤后上机检测。
1.2.7 APS-1a的单糖组成检测
1.2.7.1 色谱条件
液相色谱柱:DionexTM CarboPacTM PA20(150 mm×3.0 mm,10 μm);进样量为5 μL。流动相A(H2O),流动相B(0.1 mol/L NaOH),流动相C(0.1 mol/L NaOH,0.2 mol/L NaAc),流速0.5 mL/min;柱温为30 ℃;洗脱梯度:0 min V(A相)∶V(B相)∶V(C相)=95∶5∶0;26 min V(A相)∶V(B相)∶V(C相)=85∶5∶10;42 min V(A相)∶V(B相)∶V(C相)=85∶5∶10;42.1 min V(A相)∶V(B相)∶V(C相)=60∶0∶40;52 min V(A相)∶V(B相)∶V(C相)=60∶40∶0;52.1 min V(A相)∶V(B相)∶V(C相)=95∶5∶0;60 min V(A相)∶V(B相)∶V(C相)=95∶5∶0。
1.2.7.2 对照品溶液的制备
精确称取本实验所用标准品后,加入水配成10 mg/mL标准溶液母液单标,然后取适量标准品母液单标混合配制成表1所示最高指标浓度为60、50或40 μg/mL的标准品混标。
表1 单糖混标梯度浓度信息
Tab.1 Gradient concentrations of monosaccharide standard
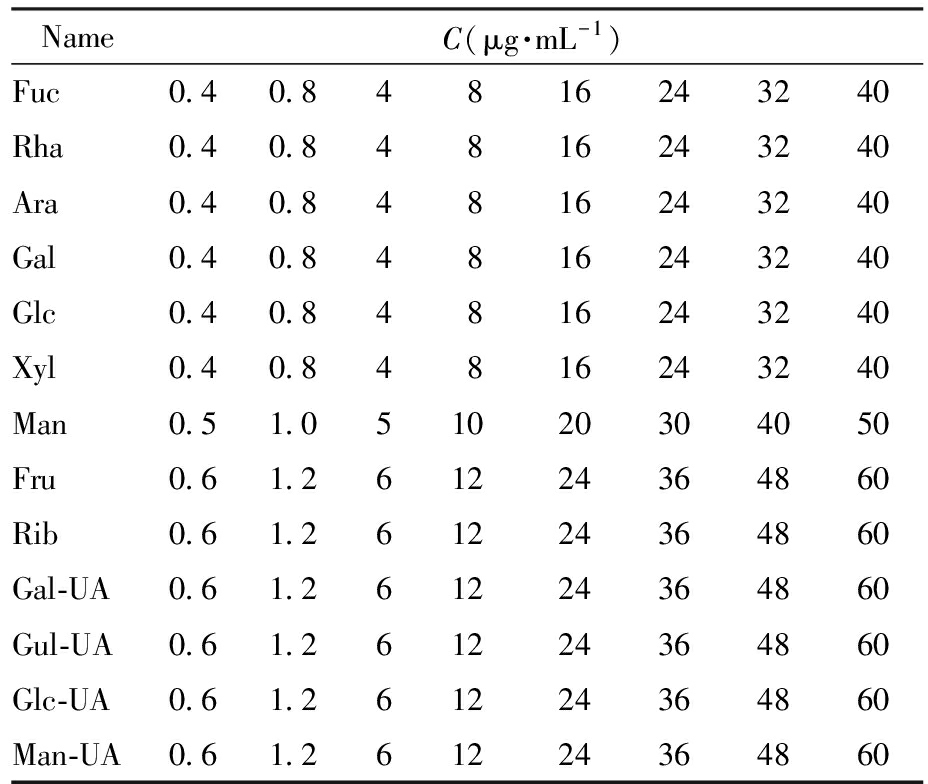
NameC(μg·mL-1)Fuc0.40.84816243240Rha0.40.84816243240Ara0.40.84816243240Gal0.40.84816243240Glc0.40.84816243240Xyl0.40.84816243240Man0.51.051020304050Fru0.61.261224364860Rib0.61.261224364860Gal-UA0.61.261224364860Gul-UA0.61.261224364860Glc-UA0.61.261224364860Man-UA0.61.261224364860
1.2.7.3 标准曲线的绘制
精密移取1.2.7.2混合对照品溶液按照以下梯度,在1.2.7.1色谱条件下分别测定峰面积,以峰面积为纵坐标,质量浓度为横坐标进行线性回归。
1.2.7.4 供试品溶液的制备
称取2.02 mg APS-1a样品,加入1 mL(2 mol/L) TFA酸溶液,121 ℃加热2 h。通入氮气,吹干。加入99.99%甲醇清洗再吹干,重复甲醇清洗2~3次。加入无菌水溶解,转入色谱瓶中待测。
1.2.8 扫描电镜分析
使用冷场发射扫描电子显微镜观察粉末状的APS-1a,将样品均匀分散在覆盖有双面粘合剂的样品台上,喷涂金粉。在不同放大倍率下观察样品。
1.2.9 红外光谱分析
取少量APS-1a粉末与在105 ℃下干燥后的200 mg溴化钾,均匀混合后压片,在400~4000 cm-1范围绘制红外光谱图[15]。
1.2.10 核磁波谱分析
采用德国布鲁克500MHz核磁共振波谱仪对目标物进行定量分析,扫描温度为25 ℃。液体探头QXI 1H/31P/13C/15N 5 mm四共振反向检测探头(Z-gradient,ATM Acc),技术参数:信噪比(1H):888;分辨率(Hz):0.32(rotating),BBFO 1H-19F,31P-15N,1H decoupling/observe多核正向检测探头(Z-gradient,ATM),技术参数:信噪比(1H):798;分辨率(Hz):0.26(rotating);信噪比(13C):328;分辨率(Hz):0.1。
供试品溶液的制备:取适量APS-1a充分溶解至D2O中,配制成浓度≥40 mg/mL溶液。转移0.5 mL至核磁管中。将核磁管放入核磁共振波谱仪中扫描一维 1H谱、13C谱图。
2 结果与讨论
2.1 APS透析结果
经透析法分离3 kDa及以下分子量的黄芪多糖。对分离产物进行检测分析,结果显示3 kDa及以下低分子量黄芪多糖(APS)占比达67%。
2.2 3 kDa及以下分子量APS柱层析纯化结果
2.2.1 无水葡萄糖标准曲线结果
无水葡萄糖浓度(C)与吸光度(A)的线性回归方程为A=0.051C-0.0099(r2=0.999),在4.41~15.86 μg/mL范围内呈现良好线性关系,符合定量分析要求。
2.2.2 DEAE-52离子纤维柱纯化APS-3k结果
使用DEAE-52离子交换柱纯化分子量在 3 kDa及以下的黄芪多糖,根据流脱曲线(图1)结果,0~8瓶溶液合并,浓缩,冻干,得到淡黄色絮状产物(APS-1)。
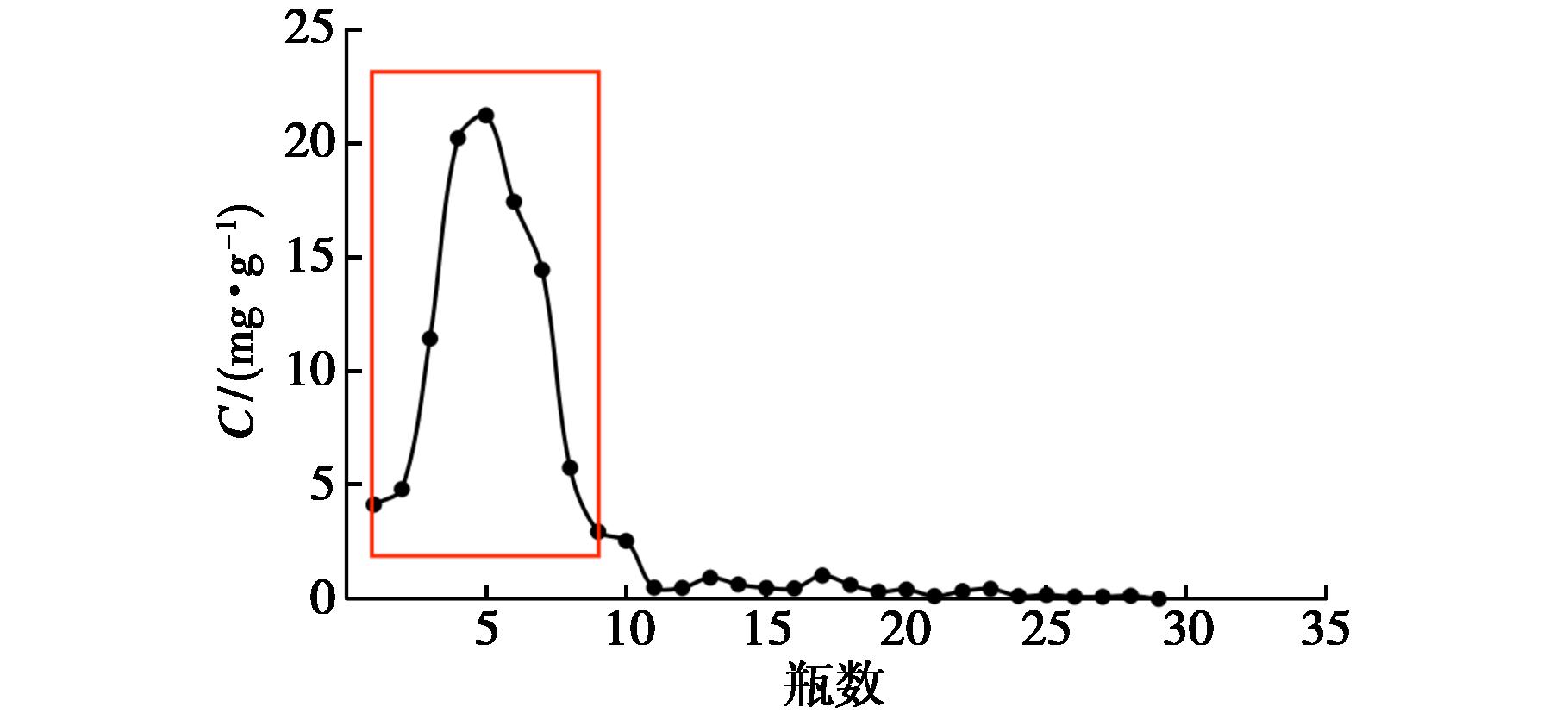
图1 DEAE-52纤维柱层析纯化APS-3k结果
Fig.1 Purification profile of APS-3k on a DEAE-52
cellulose column
2.2.3 Sephadex G-50凝胶柱纯化APS-1
根据单因素结果,当多糖浓度为2 mg/mL(图2)、上样体积为8 mL(图3)时,Sephadex G-50凝胶柱纯化APS-1效果更好。
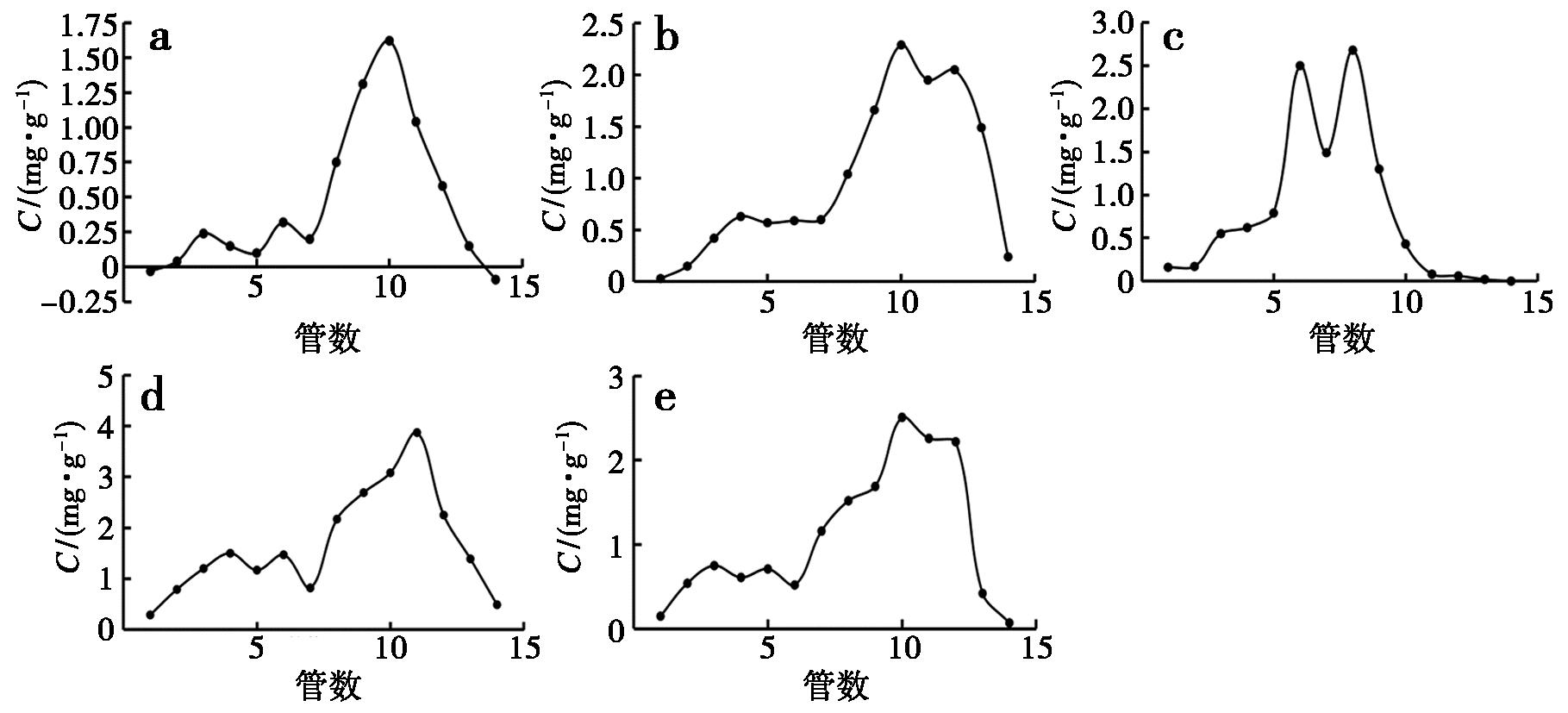
a~e多糖浓度分别为2、3、4、5、6 mg/mL
图2 多糖浓度的影响
Fig.2 Effect of polysaccharide concentration
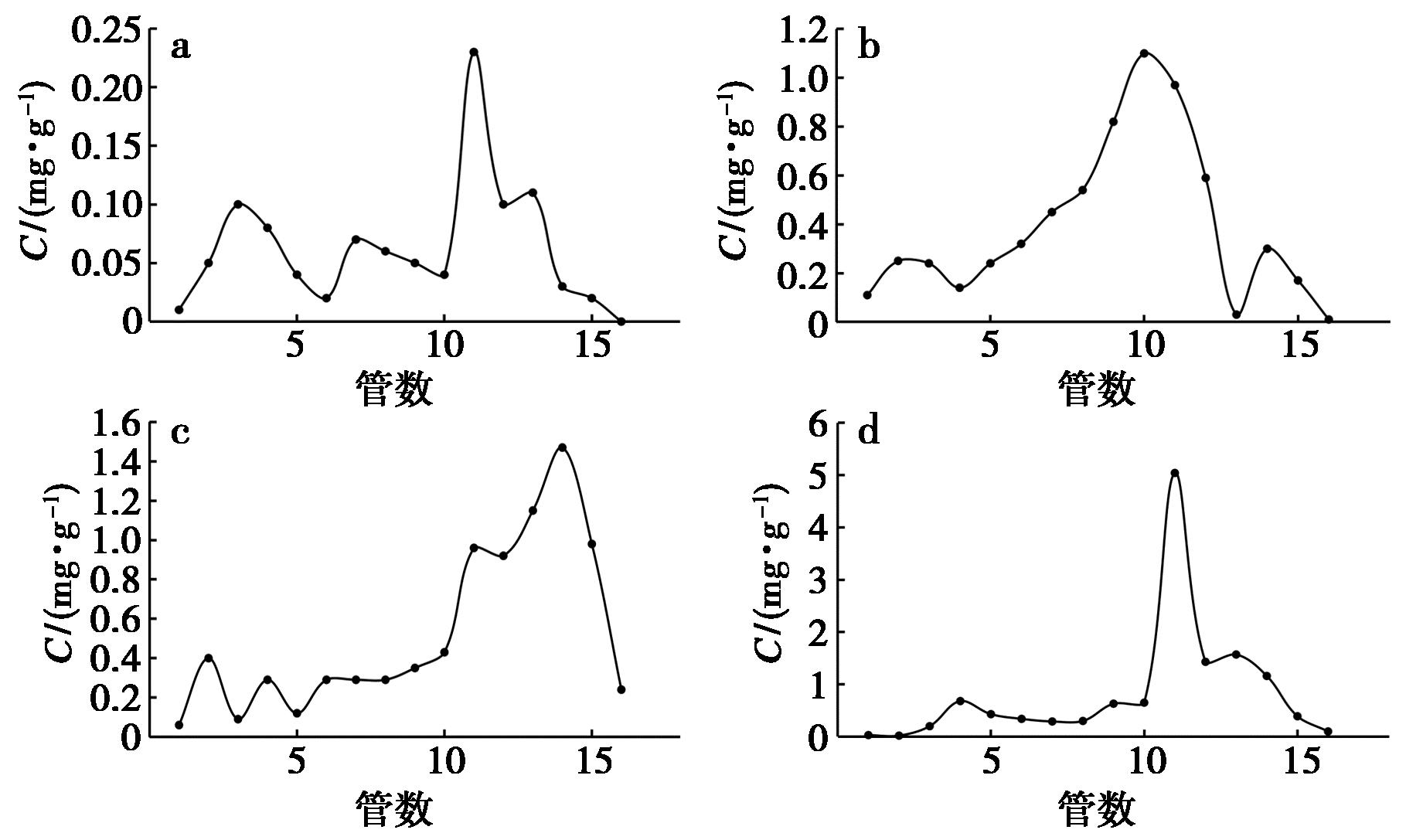
a~d上样量分别为6、8、10、12 mL
图3 上样量的影响
Fig.3 Effect of sample loading
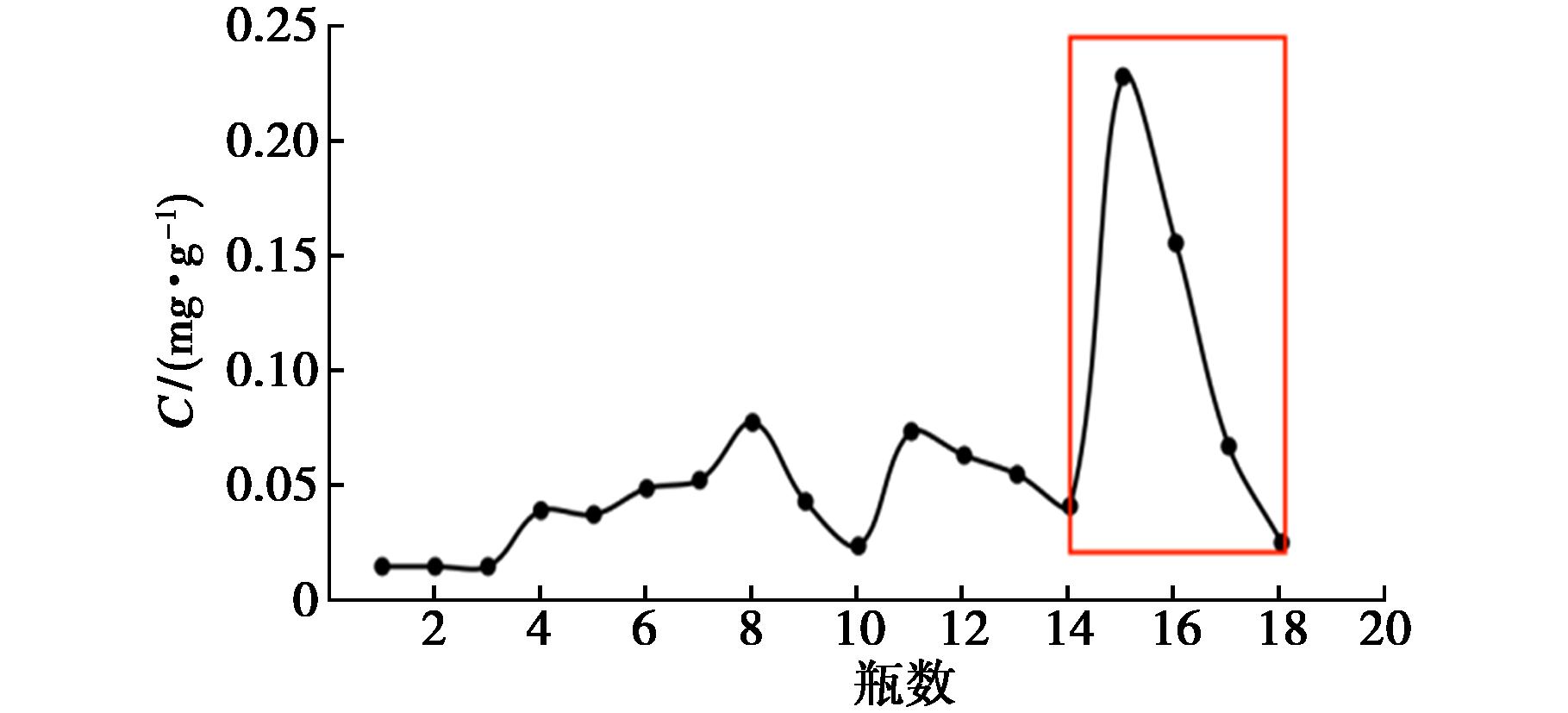
图4 APS-1柱层析纯化结果
Fig.4 Chromatography purification profiles of
APS-1 column
按照单因素结果纯化APS-1,根据洗脱曲线(图4)结果,将14~18溶液合并,浓缩,冻干,得到淡黄色絮状产物(APS-1a)。
2.3 APS-1a分子量检测结果
由表2可知,APS-1a的纯度为99.3%。聚合物分散性指数(Polymer Dispersity Index,PDI)为重均分子量(Weight-Average Molecular Weight,Mw=3381 Da)与数均分子量(Number-Average Molecular Weight,Mn=2865 Da)的比值,用于衡量多糖分子量分布的不均一程度。APS-1a的PDI为1.18,表明分子在水溶液中的不均一程度较低,不会形成大的聚合物。如图5所示,在 RT=34.15 min时出现信号强度峰值,且色谱图仅有一个对称峰,表明APS-1a为均一多糖,这种高度分子均一性和化学纯度确保了其在后续应用中的可靠性,这是保证剂量-效应关系准确的物质基础。
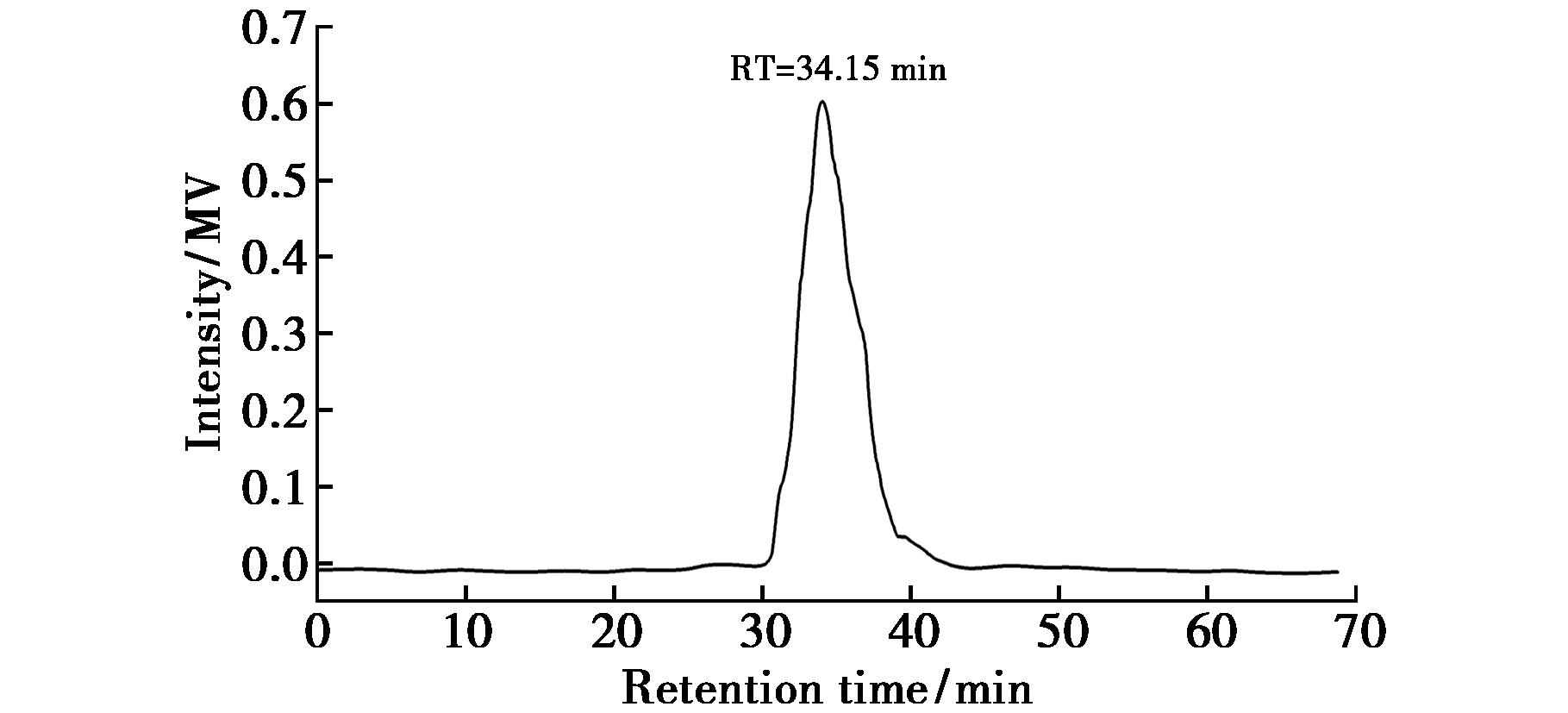
图5 APS-1a的分子量检测结果图
Fig.5 Determination profile of APS-1a molecular weight
表2 APS-1a分子量检测结果
Tab.2 Determination results of APS-1a molecular weight
ComponentPurityRT/minMw/DaMn/DaPDIAPS-1a99.3%34.15338128651.18
图6为多角度光散射测定的APS-1a构象图。横坐标是分子量,纵坐标是均方根(RMS)半径,用以分析大分子在溶液中的形状。图中的每一个点代表色谱峰在不同洗脱时间的一个片段,其对应的分子量和旋转半径被同时测定。斜率揭示其分子构象,分子量增加时,分子尺寸增大的速率。斜率值在0.5~0.6之间时,分子构象为柔性无规则团,APS-1a斜率值为0.55,说明APS-1a分子链具有较好的柔顺性和动态变化能力,从而拥有较大的流体动力学体积,更容易与免疫细胞表面的受体发生相互作用,是触发免疫响应的理想分析形态,为其潜在的免疫调节活性提供了有利的结构前提。
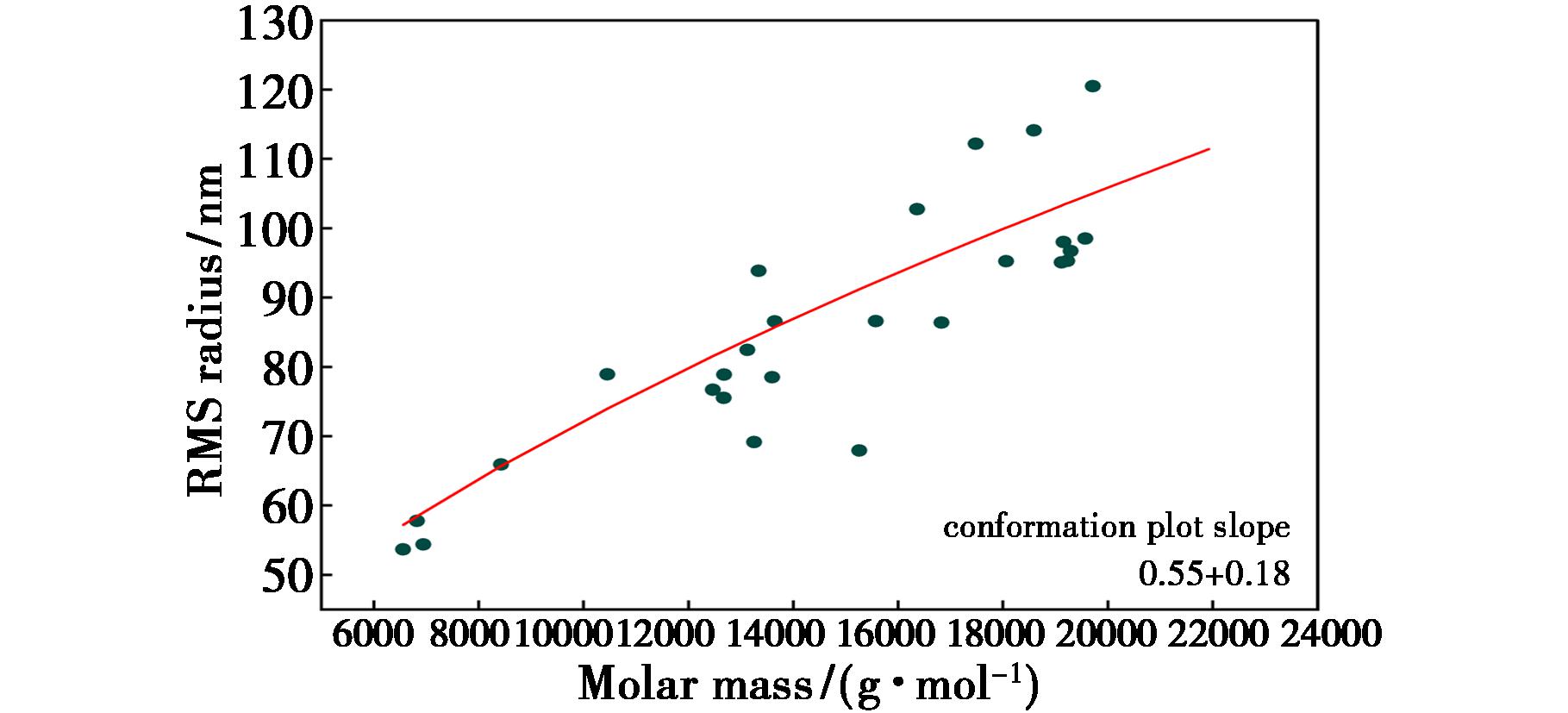
图6 APS-1a溶液构象图
Fig.6 Solution conformation of APS-1a
2.4 APS-1a单糖组成结果
APS-1a组分纯度较高,采用离子色谱法测定其单糖组成,单糖标准品和APS-1a的离子色谱图见图7、8,通过与单糖标准品图谱对比,根据出峰时间确定单糖种类,根据标准曲线结果(表3)结合峰面积确定各种单糖的物质的量比,APS-1a主要由葡糖糖和半乳糖组成,单糖组成物质的量比为n(gal)∶n(glc)=4.49∶95.71。结果表明,APS-1a为中性多糖,葡糖糖是APS-1a中的主要单糖。
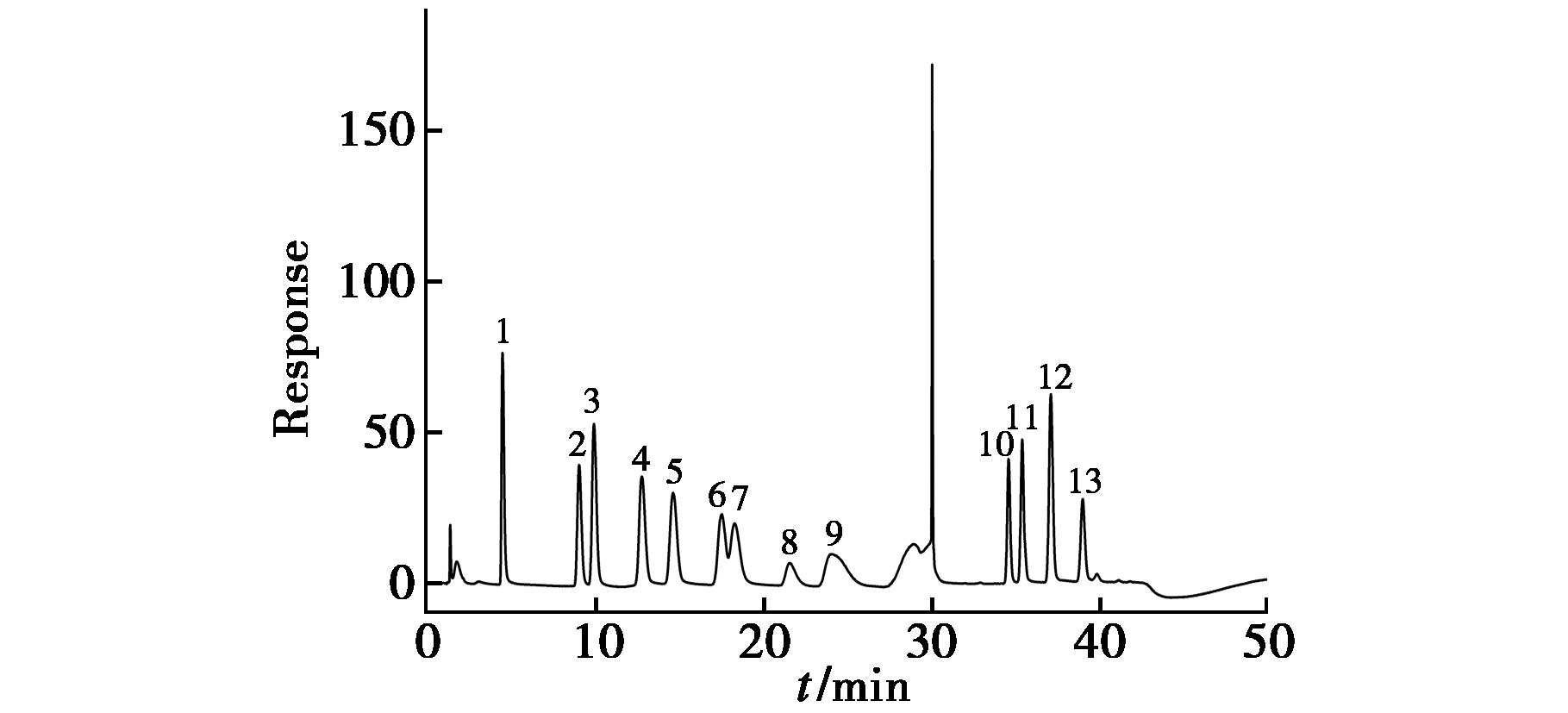
1.Fuc;2.Rha;3.Ara;4.Gal;5.Glc;6.Xyl;7.Man;8.Fru;9.Rib;10.Gal-UA;11.Gul-UA;12.Glc-UA;13.Man-UA
图7 单糖标准品色谱图
Fig.7 Chromatograms of monosaccharide standards
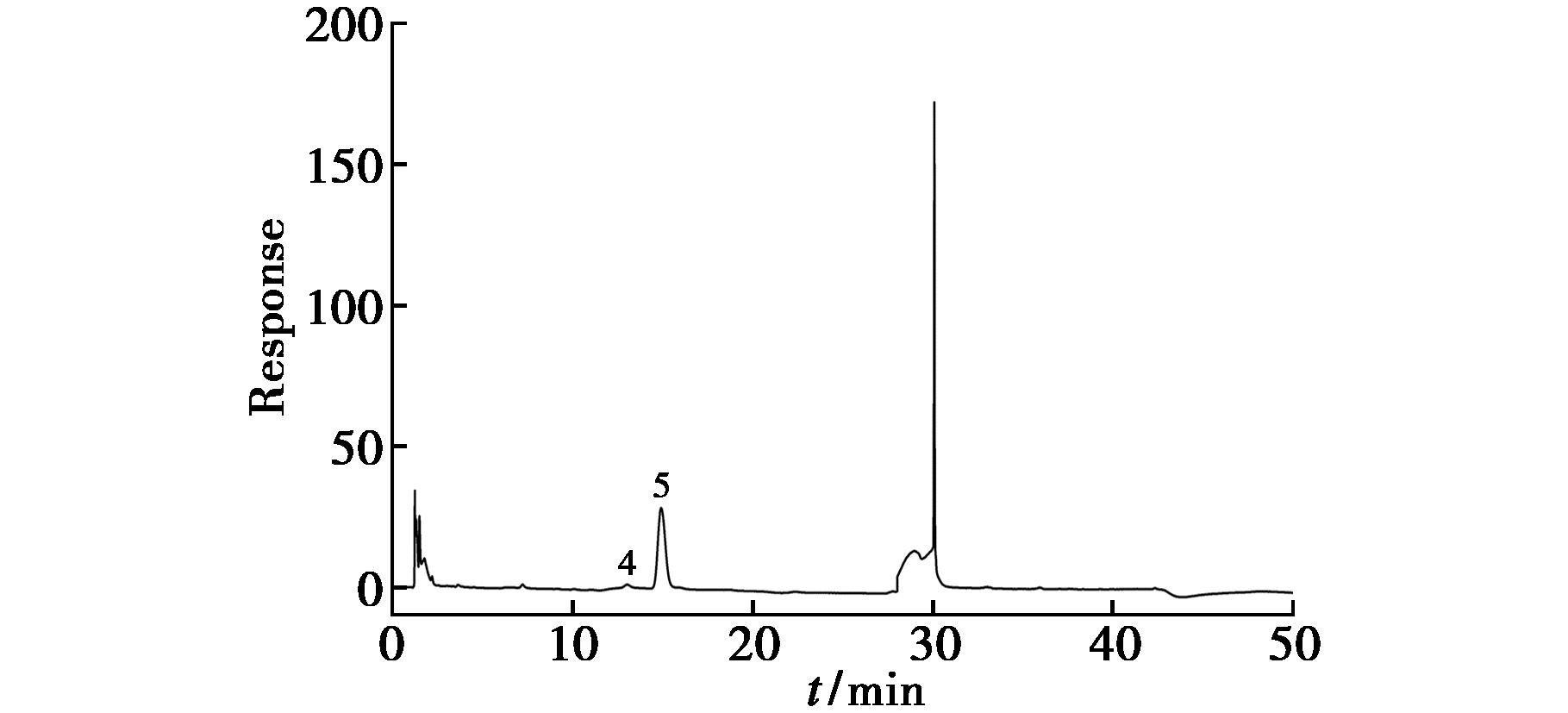
4.Gal;5.Glc
图8 APS-1a单糖组成色谱图
Fig.8 Chromatogram of the monosaccharide composition of APS-1a
表3 标准曲线结果
Tab.3 Standard curve results
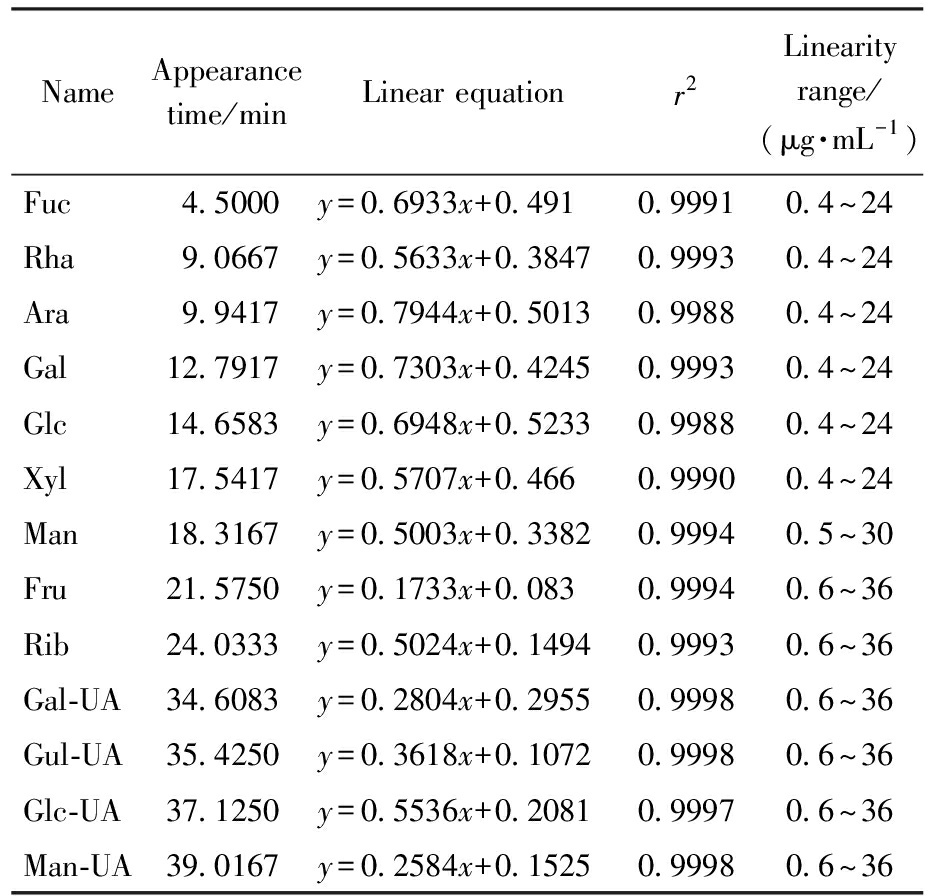
NameAppearance time/minLinear equationr2Linearity range/(μg·mL-1)Fuc4.5000y=0.6933x+0.4910.99910.4~24Rha9.0667y=0.5633x+0.38470.99930.4~24Ara9.9417y=0.7944x+0.50130.99880.4~24Gal12.7917y=0.7303x+0.42450.99930.4~24Glc14.6583y=0.6948x+0.52330.99880.4~24Xyl17.5417y=0.5707x+0.4660.99900.4~24Man18.3167y=0.5003x+0.33820.99940.5~30Fru21.5750y=0.1733x+0.0830.99940.6~36Rib24.0333y=0.5024x+0.14940.99930.6~36Gal-UA34.6083y=0.2804x+0.29550.99980.6~36Gul-UA35.4250y=0.3618x+0.10720.99980.6~36Glc-UA37.1250y=0.5536x+0.20810.99970.6~36Man-UA39.0167y=0.2584x+0.15250.99980.6~36
2.5 APS-1a扫描电镜结果
由电镜扫描图9显示,APS-1a多为表面粗糙的颗粒物或块状物,其中还存在链间氢键作用自组装形成的球状结构。在水溶液中,多糖分子被水合层包围,糖链运动自由,主要表现出动态的无规则线团构象[16]。当干燥脱水后,分子间作用力占据主导,同一多糖链的不同部分之间极易通过羟基发生分子间氢键结合,进而驱动其自组装形成颗粒状或球状超分子结构。这种“溶液柔性链”到“固态聚集体”的转变,为APS-1a在药物递送系统中的应用提供了可能。

a.200 μm;b.50 μm;c.5 μm
图9 APS-1a扫描电镜图
Fig.9 Scanning electron microscopy (SEM) image of APS-1a
2.6 APS-1a红外光谱分析
由图10可知,3371 cm-1处的强吸收峰是由于O—H的伸缩振动,2935、1425 cm-1附近的吸收峰为糖环上—CH2—或—CH3的—CH—伸缩振动和弯曲振动产生,1500~800 cm-1是鉴别糖类结构最重要的区域,1205、1130、1051 cm-1归属为C—O—C、C—O—H的伸缩振动,是吡喃多糖骨架的特征。866 cm-1处的吸收峰归属为糖环或C—H面外弯曲振动。由此可见APS-1a具有典型的多糖特征吸收峰。未发现明显羧基(C![]() O在1740 cm-1处)或氨基(—NH2在1650和1550 cm-1处)的强吸收,说明该多糖主要为中性糖链,不含明显糖醛酸或乙酰氨基。
O在1740 cm-1处)或氨基(—NH2在1650和1550 cm-1处)的强吸收,说明该多糖主要为中性糖链,不含明显糖醛酸或乙酰氨基。
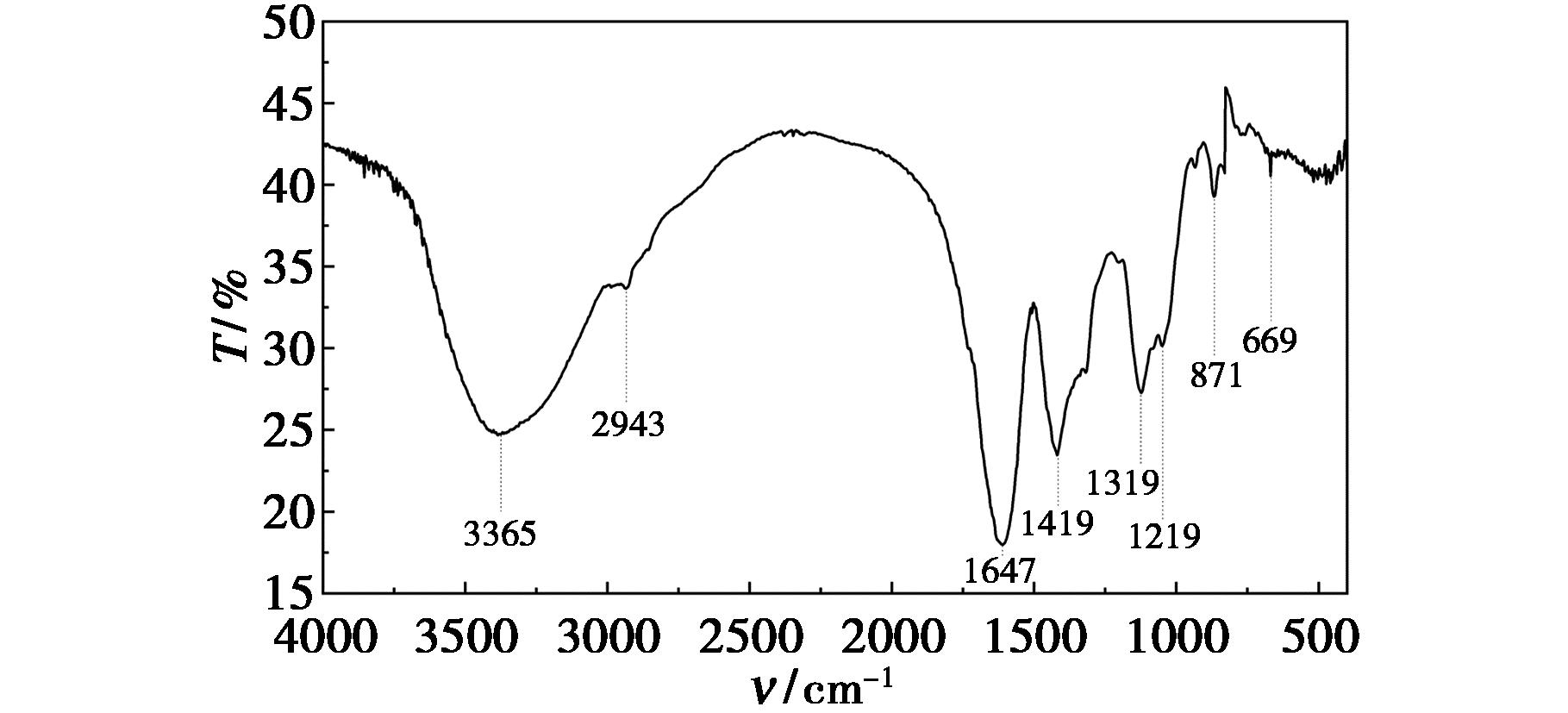
图10 APS-1a红外光谱图
Fig.10 FT-IR spectrum of APS-1a
2.7 核磁波谱解析结果
由图11可知,碳谱中异头碳δ 103.5与氢谱中异头质子信号在δ 4.1处,说明糖苷键类型是β-构型。α-构型的异头碳通常在δ 93~100之间,而β-构型在δ 103~105之间。碳谱中的δ 173为乙酰基的羰基碳,δ 21为乙酰基的甲基碳,与氢谱中 δ 2.0的乙酰基甲基质子信号相对应说明APS-1a是O-乙酰化多糖[17]。碳谱中δ 86~68为糖环上的C—2、C—3、C—4、C—5、C—6,与氢谱中 δ 3.50~4.00的密集信号区为吡喃糖环骨架的特征。δ 61~62为伯醇碳,这通常归属于未取代的C—6(—CH2OH)。
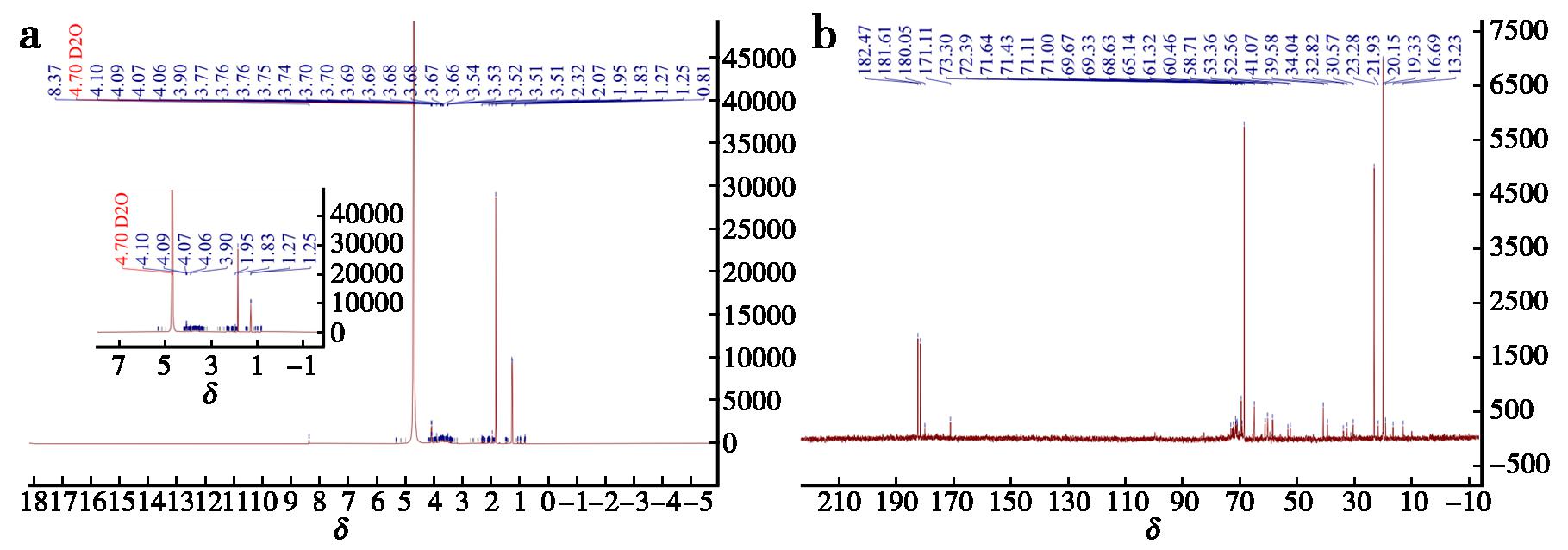
a.1HNMR;b.13CNMR
图11 APS-1a的 1H、13C核磁波谱图
Fig.11 1HNMR and 13CNMR spectra of APS-1a
NMR与FT-IR数据共同揭示,APS-1a以β-葡萄糖为主,葡萄糖通过β-(1→4)或β-(1→6)连接形成的骨架通常具有较高的构象稳定性和抗酶解能力,可能是APS-1a具有潜在免疫调节活性的关键分子基础。乙酰化修饰可能影响其水溶性、空间构象及其与免疫受体的亲和力,进而调节其生物活性[18]。陈广明[19]研究发现中性黄芪多糖比弱酸性黄芪多糖的免疫活性更强,结合本研究所得到的3 kDa左右黄芪多糖的结构特点,预测该分子量范围的黄芪多糖可能具有更强的潜在免疫调节活性,这为进一步开发APS新型免疫增强制剂提供了新的研究方向。
3 结论
本研究经分离纯化首次得到一种分子量为3.38 kDa,以葡萄糖为主的均一黄芪多糖APS-1a,测定结果明确揭示,APS-1a具有以β-糖苷键连接的葡萄糖-半乳糖吡喃环骨架及特有的O-乙酰基修饰,且其高度的结构均一性(PDI=1.18)与明确的溶液构象为其功能研究奠定了基础。是否可以通过调控其乙酰化修饰或分子组装行为来定向增强其免疫调节活性,这为黄芪多糖的靶向制备与结构优化提供了新的研究方向。同时本实验为深入解析黄芪多糖的构效关系及开发其作为新型免疫调节试剂或先导化合物奠定了坚实的物质与理论基础。
[1]Chen L,Yang H Y,Li T S,Xu S Q,He J L,Ji B Y,Hou Q F,Pei L X.Mod.Chin.Med.,2025,DOI:10.13313/j.issn.1673-4890.20241126001.
陈琳,杨昊源,李堂帅,许双全,何江龙,纪宝玉,侯庆峰,裴莉昕.中国现代中药,2025,DOI:10.13313/j.issn.1673-4890.20241126001.
[2]Wu Q,Zhao P,Wang M,Zhao C Q,Bai L G,Guo J H,Gao X F,Hou D Y,Geng Z G,Lu L,Liu J.Spectrosc.Spectral Anal.,2025,45(11):3066-3071.
吴强,赵鹏,王猛,赵彩权,白力格,郭嘉华,高雪峰,侯丁一,耿志刚,卢玲,刘杰.光谱学与光谱分析,2025,45(11):3066-3071.
[3]Zhao X L,Zhao W X,Duan C C,Zheng J,Sun N,Yang L Y,Zhao J,Duan X C.Chin.Arch.Tradit.Chin.Med.,2024,42(3):108-112.
赵雪莲,赵文晓,段晨晨,郑俊,孙娜,杨靓宇,赵军,段新成.中华中医药学刊,2024,42(3):108-112.
[4]Fan X H,Li K,Yang Y D,Li H F,Li X Q,Qin X M.J.Shanxi Univ.Chin.Med.,2022,23(3):260-267.
范信晖,李科,杨一丹,李虎峰,李雪琴,秦雪梅.山西中医药大学学报,2022,23(3):260-267.
[5]Rui W,Li C Y,Chen H Y.Tradit.Chin.Drug Res.Clin.Pharmacol.,2019,30(2):264-270.
芮雯,李婵艺,陈宏远.中药新药与临床药理,2019,30(2):264-270.
[6]Dai L L.The Isolation,Purification of Low Molecular Astragalus Polysaccharide and Its Immunomodulatory Activities.Changchun:Northeast Normal University,2008.
代丽莉.低分子量黄芪多糖的分离纯化及其免疫活性研究.长春:东北师范大学,2008.
[7]Cao Y X.Quality Comparison of Astragali Radix from Different Sources Based on Polysaccharide Molecular Weight Distribution and Immune Activity.Taiyuan:Shanxi University,2020.
曹宇欣.基于多糖分子量分布和免疫活性比较的黄芪质量研究.太原:山西大学,2020.
[8]Wang C N.Study on the Preparation of Astragalus Polysaccharide APS-IA and Its Anti-aging Activity by Regulating Gut Microbiota.Changchun:Changchun University of Chinese Medicine,2024.
王超楠.黄芪多糖APS-IA的制备及通过调节肠道菌群抗衰老活性的研究.长春:长春中医药大学,2024.
[9]Zhang H C.The Research on Antitumor Activity of Low Molecular Weight Polysaccharide from Astragalus Membranceus.Tianjin:Tianjin University of Science &Technology,2018.
张红翠.黄芪低分子量多糖抗肿瘤活性研究.天津:天津科技大学,2018.
[10]Chai D K.Study on Immune Activity of DEC-205-Targeting Astragalus Polysaccharide Long-Circulating Liposomes.Chongqing:Southwest University,2020.
柴东坤.DEC-205靶向的黄芪多糖长循环脂质体免疫活性研究.重庆:西南大学,2020.
[11]Li N.Application of a “Drug-Excipient Combined” Nanodelivery System Based on Plant-Derived Natural Polysaccharides in Tumor Immunology.Beijing:Peking Union Medical College,2023.
李楠.基于植物来源的天然多糖“药辅合一”纳米递送系统在肿瘤免疫中的应用.北京:北京协和医学院,2023.
[12]He H,Zhao S S,Zhang X R,Cui Z J,Shao J.J.Tradit.Chin.Vet.Med.,2022,41(5):1-6.
何海,赵沙沙,张小荣,崔治家,邵晶.中兽医医药杂志,2022,41(5):1-6.
[13]Ran S Q.Isolation,Purification,Structural Characterization of Polysaccharide APS-1a from Astragalus Membranaceus and Its Activity of Stimulating EPO Secretion in HepG2 Cells.Wuhan:Huazhong University of Science and Technology,2020.
冉思琪.黄芪多糖APS-1a的分离纯化、结构鉴定及促进肝细胞EPO分泌的研究.武汉:华中科技大学,2020.
[14]Mao T F,Lu L Y,Qian J F,Xu R,Yuan A J,Ni R.Phy.Test.Chem.Anal.part B:Chem.Anal.,2025,61(7):795-801.
毛亭枫,路凌怡,钱杰峰,徐睿,袁安杰,倪蓉.理化检验-化学分册,2025,61(7):795-801.
[15]Zhang B.Extraction,Purification and Anti-Aging Activity of Astragalus Polysaccharides.Hohhot:Inner Mongolia Agricultural University,2022.
张宝.黄芪多糖的分离纯化及其抗衰老活性研究.呼和浩特:内蒙古农业大学,2022.
[16]Yang Z Y,Wang Y F,Ayzklm Y,Wang Y L,Wei R J,Gu Y L,Rehebati N,Hulsidan I.Sci.Technol.Food Ind.,2025,DOI:10.13386/j.issn1002-0306.2025040212.
杨智艳,王宇帆,阿依左克拉木·牙森,王艳丽,魏瑞杰,顾雨露,热合巴提·努尔夏提,胡尔西丹·伊麻木.食品工业科技,2025,DOI:10.13386/j.issn1002-0306.2025040212.
[17]Zhao N,Han J,Jian Y L,Pang Z,Wang L,Di D L,Liu J F,Shao J.Chin.Tradit.Herb.Drugs,2024,55(21):7491-7506.
赵宁,韩著,简颖琳,庞哲,王露,邸多隆,刘建飞,邵晶.中草药,2024,55(21):7491-7506.
[18]Xia S B,Huang C Y.Curr.Biotechnol.,2025,15(5):854-864.
夏晟博,黄丛阳.生物技术进展,2025,15(5):854-864.
[19]Chen G M.Study on Isolation,Purification,Structural Characterization and Biological Activity of Polysaccharides from Astragalus membranaceus.Wuhan:Hubei University of Chinese Medicine,2023.
陈广明.黄芪多糖的分离纯化、结构表征及其生物活性研究.武汉:湖北中医药大学,2023.