胰腺癌作为全球癌症死亡相关的第七大原因,每年有超过30万人因胰腺癌死亡,其发病率和死亡率在预期20年内仍呈现上升阶段[1,2]。大部分胰腺癌晚期患者5年生存率低于13.3%。由于胰腺癌早期并没有明显症状,同时影像学诊断中难以观察到胰腺器官,使得患者进展到晚期才能被诊断,此时通常是局部不可切除或远程转移的阶段,这反过来又直接影响生存率[3]。由于胰腺癌发病较晚,发现和联合新的诊断和监测技术极其重要。中国临床肿瘤协会(CSCO)指出,需要对临床诊断和治疗胰腺癌患者的标准进行优化。包括利用正电子发射断层扫描(PET-CT)、磁共振胰胆管造影(MECP)和引入新型生物标志物糖类抗原24(CA242)进行联合诊断,提高诊断效率。
手术切除可以提高至20%的5年生存率,但手术死亡率和远处肿瘤复发,使得手术治疗胰腺癌的能力和范围有限。对于不同患病情况的患者,可以选择化疗或放射化疗等治疗手段。辅助化疗可以依据FDA批准的药物进行联合靶向治疗,根据患者的发病情况进行不同的药物组合方式。目前被批准治疗胰腺癌的一线药物主要包括:氟尿吡啶、厄洛替尼、吉西他滨以及丝裂霉素C,但这些药物对于患者治疗预后的总生存期改善情况仍不够显著[4]。对于已确诊胰腺癌的患者制定药物治疗时,需要发现新的靶向药物(例如:基因突变的分子靶向药物、胰腺癌基质的靶向药物)或免疫治疗药物(例如:免疫检查点抑制剂)。靶向治疗药物能够激活患者体内的免疫信号系统,从而增强对肿瘤细胞的识别和杀伤能力,实现患者的个性化治疗。
天然来源的活性成分已经广泛应用于癌症患者临床治疗以及潜在药物开发试验,这些活性成分可以通过调节上皮间充质转化(EMT)、亚细胞信号通路和基因突变驱动等来抑制胰腺癌肿瘤细胞的增殖、迁移和耐药等[5]。将天然活性小分子与肿瘤微环境的免疫细胞相联系,包括通过直接或间接作用于肿瘤细胞的免疫检测点PD-1/PD-L1或肿瘤浸润淋巴细胞等方式来改善肿瘤微环境,进而实现对患者的治疗[6]。但天然产物来源的活性小分子成分复杂,作用毒性和靶点需要研究者进行大量的体内和体外试验进行验证。基于计算建模、测序技术和靶向机制等研究方法来筛选出安全性高、作用靶点明确、生物利用度高的天然活性小分子是未来治疗胰腺癌药物开发的研究方向。
本文基于天然来源的活性小分子在体外试验和体内临床试验进行总结,阐明这些活性成分在胰腺癌发病早期、转移晚期和药物治疗预后的作用机制。
1 治疗胰腺癌的天然活性小分子的分类与来源
天然活性小分子由于其独特的有效性,已经在几个世纪以来广泛应用于各种癌症的辅助治疗[7]。治疗胰腺癌患者或肿瘤细胞的天然活性小分子来源广泛,包括中草药、微生物细菌真菌以及海洋药物等。
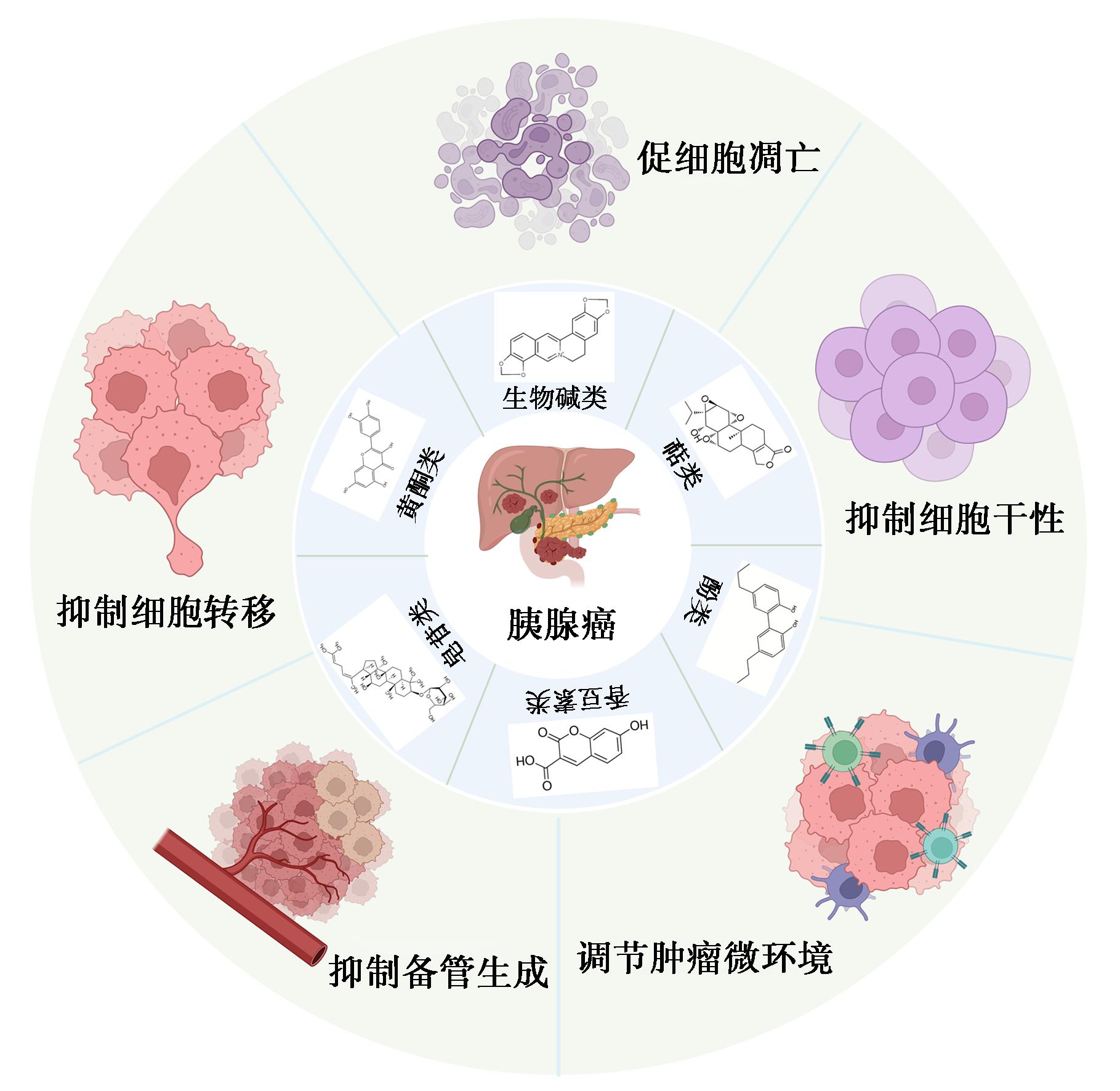
图1 天然活性小分子抗胰腺癌的研究进展
Fig.1 Research progress on natural active small molecules against pancreatic cancer
1.1 基于天然药用植物和中药草来源的天然活性小分子
药食同源是中国传统医学与营养学结合的核心理念。近几年玉米须茶的兴起重新让科研人员对玉米须的天然活性小分子进行研究。最新的研究发现玉米须黄酮类成分和粗多糖类成分S1会对胰腺癌细胞株表现多靶点和多途径的抑制作用。包括:(1)靶向免疫治疗:增强自然杀伤细胞(NK细胞)和T淋巴细胞的活性,提高机体对癌细胞的识别和清除能力;(2)靶向结合胰腺癌细胞表面的生长因子受体,阻断EGFR//PI3K/AKT/CREB信号通路来抑制胰腺癌细胞的增殖[8,9]。
对经典天然活性小分子进行结构修饰改造,是发现新的靶向药物的主要途径。通过对青蒿素进行结构改造,合成了一种新型含氰基青蒿素二聚体衍生物ZQJ29,利用蛋白质组学分析和功能分析发现ZQJ29能够抑制聚(ADP-核糖)聚合酶PARP1活性,从而引发胰腺癌细胞的铁死亡,并在体内外均表现出显著的抗胰腺癌活性[10]。
1.1.1 生物碱
在胰腺癌早期阶段,小檗碱可以通过抑制AMPK介导的TGF-β1/Smad信号传导和M2巨噬细胞极化抑制来减轻慢性胰腺炎和纤维化[11]。同时小檗碱可以通过靶向调节柠檬酸代谢来抑制胰腺癌细胞线粒体中特定的脂肪酸生物合成,从而造成胰腺癌细胞线粒体明显受损,抑制胰腺癌细胞的增殖和转移[12]。
联合吉西他滨等一线化疗药物,可以增强治疗效果并改善耐药性。小檗碱可以通过抑制EMT相关的信号通路来抑制胰腺癌干细胞的增殖和干细胞特性[13]。将小檗碱联合吉西他滨可以显著下调PANC-1细胞的干细胞基因:SOX2、POU5F1以及NANOG,同时减少侧群(SP)细胞比例,改善治疗过程的耐药性[14]。同时小檗碱可以通过逆转Rap1/PI3K-Akt信号通路来改善吉西他滨的治疗耐药性[15]。小檗碱可以通过产生ROS来增强吉西他滨诱导G1期停滞来抑制胰腺癌细胞增殖作用,将小檗碱联合吉西他滨对PANC-1和MIAPaCa-2进行给药后发现,PANC-1和 MIAPaCa-2的G1期相比于单独给予吉西他滨组增加了2%~10%[16]。
石蒜碱可以在诱导MIAPaCa-2、PANC-1的G2-M期周期阻滞的同时,通过抑制AKT的磷酸化从而下调AKT信号通路,以及促进胰腺癌细胞的凋亡[17]。生成的新生血管会利用血管生成的癌干细胞以及血管生成因子来加速胰腺癌的转移和侵袭。石蒜碱可以通过诱导与EMT转化以及新生血管生成相关的Notch1癌蛋白的降解、抑制Notch1下游NF-κB、HIF1α以及血管生成基因信号素4D(Sema4D)和血管生成素-2(Ang-2)的下调来抑制胰腺癌细胞的生长和新生血管[18]。
靶向肿瘤代谢以及重编程:石蒜碱通过调节参与营养吸收和代谢途径,抑制癌细胞生物合成和氧化还原反应。石蒜碱通过降低胰腺癌细胞对葡萄糖的吸收和乳酸的释放并下调糖酵解中关键激酶的表达来发挥抗癌作用。同时通过控制参与脂肪酸氧化的关键酶的表达,抑制ALDH3A1的表达和脂肪酸的氧化,从而抑制脂肪醛向脂肪酸的转化,导致脂质在细胞内积累,抑制细胞增殖[19]。
1.1.2 黄酮类
作为甘草中的一类查尔酮类成分,异甘草素在抑制胰腺癌进展中发挥重要作用,其可以通过下调EMT转化信号通路来抑制胰腺癌细胞PANC-1的迁移。
异甘草素可以显著提高化疗药物的临床治疗效果。其不仅可以通过提高ROS水平,还可以通过诱导p38磷酸化来靶向p38 MAPK信号通路来阻断自噬。与吉西他滨或5-FU联合使用可以缓解耐药性,提高化疗药的治疗效果[20]。异甘草素还通过减少抑制细胞(MDSC)的数量,同时增加T细胞的数量。在抑制M2巨噬细胞的极化的同时,通过Rac1-p38-CREB来抑制STAT1的激活,从而重新编程肿瘤免疫微环境,协同吉西他滨对胰腺癌细胞的生长抑制作用[21]。
槲皮素可以改善吉西他滨在治疗胰腺癌过程中的耐药性。基于网络药理学,发现槲皮素、吉西他滨以及胰腺癌三者的交集靶点:AKT、EGFR和HSP90AA1。OLA1作为Obg类的GTPase家族的一种内源性氧化应激负性调控因子,其在胰腺癌细胞中呈现过表达状态。通过构建OLA1顺转和稳转细胞系发现:槲皮素可以通过下调OLA1基因来抑制AKT信号通路,从而增强胰腺癌对吉西他滨的敏感性[22]。通过荧光激活细胞分选技术(FACS)从PANC-1分选出胰腺癌干细胞(PCSCs),发现槲皮素可以通过STAT3信号通路抑制脂肪酸氧化中的一类关键的限速酶——肉碱棕榈酰转移酶1B(CPT1B),从而调节PCSCs的脂质代谢,增强吉西他滨的耐药性[23]。此外槲皮素还通过抑制β-连环蛋白以及晚期糖基化终产物(RAGE)受体的RAGE/PI3K/AKT/mTOR轴来增强胰腺癌细胞在吉西他滨化疗的敏感性[24,25]。
由于槲皮素的生物相容性以及生物利用度有限,通过将槲皮素封装至表面结合透明质酸酶的脂质体中,增强其在肿瘤部位的通透性和留存性。在胰腺癌细胞系、3D细胞培养模型和胰腺癌衍生的类器官中显示出抑制细胞增殖、促进细胞凋亡和诱导G2/M细胞周期停滞的能力[26]。
1.1.3 萜类化合物
雷公藤甲素作为从雷公藤的根、花、叶和果实中提取的一类环氧二萜内酯化合物,从2005年起就报道了在胰腺癌中的多重治疗作用:包括抑制5-脂氧合酶(5-LOX)、HSP70蛋白的表达以及锌指转录因子Sp1的O-GlcNAc的糖基化修饰,从而抑制胰腺癌的增殖和诱导凋亡[27-29];通过在吉西他滨耐药的胰腺癌细胞中下调HSP27的表达,来提高对顺铂治疗的敏感性[30]。
最近基于网络药理学发现,雷公藤甲素可以在体外下调纤溶酶原激活剂尿激酶(PLAU)来抑制胰腺癌的增殖和迁移,并且在临床患者中PLAU过表达与淋巴结转移显著相关[31]。同时雷公藤甲素可以下调Pumilio RNA结合家族成员PUM1来诱导胰腺癌细胞的自噬,从而增强了对肿瘤坏死因子相关凋亡诱导配体(TRAIL)的敏感性[32]。此外雷公藤甲素可以抑制TLR4/NF-κB来增强胰腺癌细胞对吉西他滨的敏感性[33]。
对经典化合物进行结构修饰和纳米材料包装可以改善其临床应用前景。雷公藤甲素可以在缺氧诱导的高恶性胰腺癌上皮间充质转化和干细胞模型中,通过下调NF-κB信号通路来逆转EMT和CSC特征[34]。然而雷公藤甲素的溶解度以及体内毒性限制了其临床应用,通过利用C—C双键装饰C-19生成(E)-19-[(1′-苯甲酰氧基-1′-苯基)-甲基基]-雷公藤内酯,在与雷公藤甲素具有相似IC50的浓度下,改造后的雷公藤甲素仅在500 nmol/L下表现出毒性,并且通过抑制NF-κB通路来增加ROS的产生和诱导线粒体介导的胰腺癌细胞凋亡[35]。通过利用饱和长链脂肪酸酸化(S-LCFAylation)技术合成了雷公藤甲素衍生的长链循环脂质体偶联物,这种脂质体载体封装前药可以改善雷公藤甲素的水溶性差和爆发释放,减轻了毒素的体循环[36]。通过核蛋白特异性适配体(AS1411)介导的雷公藤甲素纳米载体,可以表现出更高的抗肿瘤活性以及胰腺癌细胞结合能力[37]。
1.1.4 皂苷类化合物
作为人参关键的甾醇皂苷类化合物,人参皂苷Rg3可以抑制多种肿瘤细胞的增殖和转移、逆转耐药性和前增强化疗敏感性[38]。人参皂苷Rg3通过下调E-钙粘蛋白、EphA2、MMP9和MMP2的表达,有效抑制胰腺癌血管生成[39]。同时在SW1990细胞通过抑制PI3K途径的活化,从而抑制上皮间充质转化以及血管生成拟态[40]。通过将一种金属基纳米酶(Fe@Fe3O4)与人参皂苷Rg3进行合成金属-有机纳米复合药物。人参皂苷Rg3的糖苷链在纳米药物的最外层形成亲水层,提高生物相容性和药代动力学的同时可以激活细胞死亡。而内部纳米酶进入TME可以有效地产生活性氧和氧气,从而促进胰腺癌细胞的凋亡[41]。
与化疗药物表现出协同治疗作用以及降低耐药性。EGFR抑制剂厄洛替尼可以显著抑制胰腺癌细胞的EGFR的磷酸化以及MAPK&JNK信号,但是由于EGFR非依赖性PI3K/Akt信号通路激活,限制了厄洛替尼的临床作用。人参皂苷Rg3可以通过下调EGFR/PI3K/Akt信号通路来在胰腺癌细胞BxPC-3和AsPC-1中增强厄洛替尼的抗增殖活性[42]。锌指蛋白91(ZFP91)可以诱导吉西他滨的耐药性,同时诱导睾丸特异性Y编码样蛋白2(TSPYL2)泛素化,促进蛋白酶体降解。而人参皂苷Rg3可以降低ZFP91介导的TSPYL2的泛素化和降解,从而逆转了在胰腺癌中吉西他滨的耐药性[43]。同时人参皂苷Rg3通过上调长链非编码RNA癌症易感候选者2(lncRNA-CASC2)水平和PTEN表达,通过参与CASC2/PTEN信号传导来促进吉西他滨耐药胰腺癌细胞生长抑制和凋亡[44]。
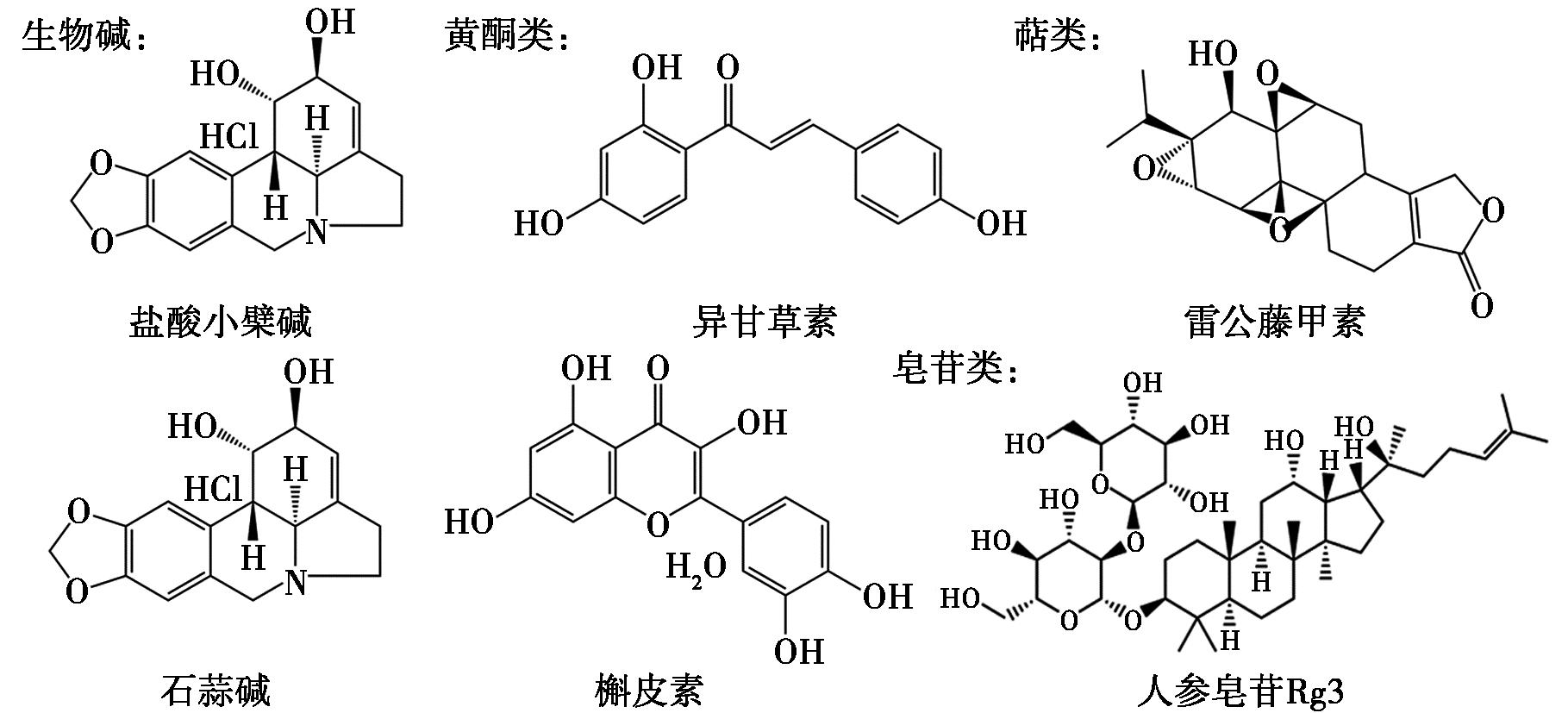
图2 代表性天然活性小分子化学结构式
Fig.2 Representative chemical structures of natural bioactive small molecules
1.1.5 其它
除了上述主要的活性小分子,其它来源皂苷、酚类以及香豆素类等天然活性小分子也有报道,但是研究较为单一。来源于重楼的巴黎皂苷 PSVII可以通过激活ROS/Bax相关的线粒体通路来导致Caspase-GSDME依赖性胰腺癌细胞焦亡[45]。
来源于厚朴的酚类活性小分子——四氢厚朴酚可以直接靶向YTH N6-甲基腺苷RNA结合蛋白F2(YTHDF2),阻断其对自噬相关基因ATG5和ATG7的m6A修饰的识别,从而诱导自噬性细胞死亡发挥抗胰腺癌作用。在调控自噬的同时,还通过改变PD-L1的表达影响肿瘤免疫微环境,促进T细胞的功能和浸润,从而激活具有抗肿瘤特性的免疫细胞,提高PD-L1免疫治疗的疗效[46]。
来源于的艾蒿中分离得到的倍半萜类香豆素——伞形花素可以通过阻断Akt信号通路来诱导人原位胰腺癌癌细胞的自噬和凋亡,同时通过降低Notch1受体胞内结合域(NICD1)的表达减少干细胞的亚群[47]。
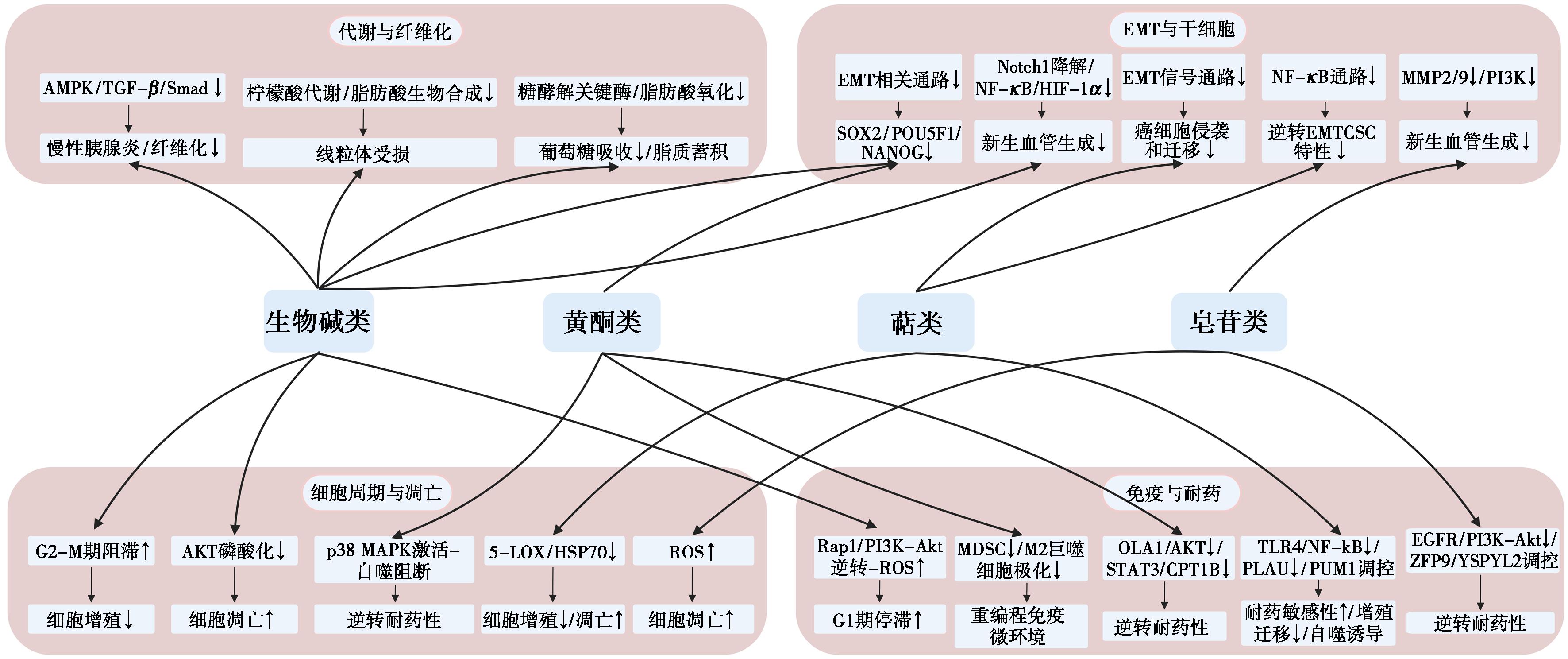
图3 天然活性小分子抗胰腺癌的机制
Fig.3 Mechanisms of natural active small molecules against pancreatic cancer
1.2 基于微生物来源的天然活性小分子
从真菌霉属科的嗜松青霉提取出的两种天然活性小分子——地卡纳林(Dicatenarin)以及斯凯林(Skyrin),可以通过激活细胞色素C以及半胱天冬酶-3来诱导细胞凋亡[48]。同样,从中国太白山苔藓土壤的一株放线菌中分离鉴定出的活性成分——三烯酶素A,可以通过显著抑制STAT3的705位点的酪氨酸磷酸化,来抑制人胰腺癌细胞PANC-1、MIAPaCa-2和胰腺癌异种移植小鼠模型的癌细胞增殖和迁移[49]。
最新的临床患者试验发现,日本大和药品工业株式会社对一种来自日本深山的特殊真菌进行生物转化分离,得到一种结构特殊的阿拉伯木聚糖复合物——大和米蕈(Biobran/MGN-3)[9]。通过创新性联合治疗方案:注射吉西他滨+白蛋白结合型紫杉醇+米蕈免疫调节。米蕈通过激活了蓄势待发的“杀手”NK细胞,增强NKG2D功能及其细胞毒性,最终联合治疗方案可以显著性激活胰腺癌患者体内的免疫杀伤系统。
表1 天然活性小分子抗胰腺癌的研究现状
Tab.1 Current research status of natural active small molecules against pancreatic cancer
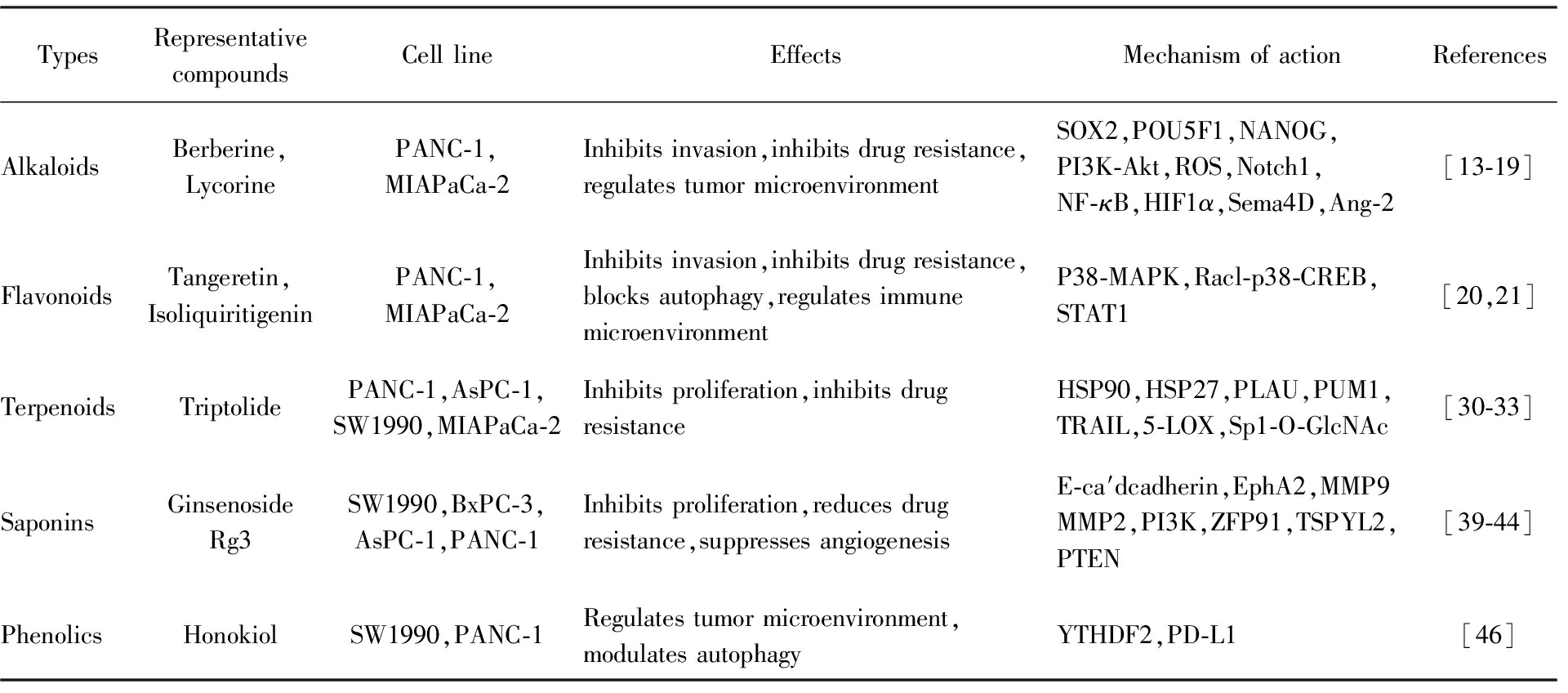
TypesRepresentative compoundsCell lineEffectsMechanism of actionReferencesAlkaloidsBerberine,LycorinePANC-1,MIAPaCa-2Inhibits invasion,inhibits drug resistance,regulates tumor microenvironmentSOX2,POU5F1,NANOG,PI3K-Akt,ROS,Notch1,NF-κB,HIF1α,Sema4D,Ang-2[13-19]FlavonoidsTangeretin,IsoliquiritigeninPANC-1,MIAPaCa-2Inhibits invasion,inhibits drug resistance,blocks autophagy,regulates immune microenvironmentP38-MAPK,Racl-p38-CREB,STAT1[20,21]TerpenoidsTriptolidePANC-1,AsPC-1,SW1990,MIAPaCa-2Inhibits proliferation,inhibits drug resistanceHSP90,HSP27,PLAU,PUM1,TRAIL,5-LOX,Sp1-O-GlcNAc[30-33]SaponinsGinsenoside Rg3SW1990,BxPC-3,AsPC-1,PANC-1Inhibits proliferation,reduces drug resistance,suppresses angiogenesisE-ca′dcadherin,EphA2,MMP9 MMP2,PI3K,ZFP91,TSPYL2,PTEN[39-44]PhenolicsHonokiolSW1990,PANC-1Regulates tumor microenvironment,modulates autophagyYTHDF2,PD-L1[46]
1.3 基于海洋药物来源的天然活性小分子
海洋生物资源是天然药物发现的重要来源,其所含的小分子活性物质具有结构多样性与独特的生物功能。研究显示,从红藻中分离出的劳林藻素和劳林醚能够诱导细胞内活性氧(ROS)过量积累,并激活p38 MAPK信号级联反应,从而触发胰腺癌细胞线粒体通路介导的程序性死亡。与此同时,来源于海绵的环肽天然产物松藻素A可与细胞膜甾醇组分特异结合,破坏膜稳定性,进而通过上调AMPK信号通路实现对胰腺癌细胞迁移与侵袭的抑制作用。此外,深海放线菌产生的海洋黄素被发现能阻断NF-κB与STAT3信号活化过程,显著削弱胰腺癌细胞的上皮-间质转化(EMT)及转移能力。综上,海洋来源的小分子天然产物凭借独特的化学骨架与多靶点作用机制,为胰腺癌抗转移药物及免疫联合治疗策略的开发提供了新的研究方向与理论依据。
2 天然活性小分子抗胰腺癌的作用机制
基于天然活性小分子治疗胰腺癌的作用机制主要包括:促进细胞凋亡、抗转移、抗耐药和抗血管生成。
2.1 抑制细胞增殖与诱导凋亡
从毛细蒿干燥地上部分提取的中药单体药物:东莨菪酮可以通过引起G0/G1期细胞周期停滞来诱导SW1990细胞和Capan-2细胞的凋亡。通过网路生物信息学和qRT-PCR技术确认了AKT1是东莨菪酮抑制胰腺癌细胞增强的关键基因,最终东莨菪酮可以通过抑制PI3K/AKT1信号通路来抑制癌细胞的增强和诱导凋亡[50]。
氧化应激产生的活性氧(ROS)在高浓度水平时会诱发多种类型的癌细胞死亡。作为天然黄酮类小分子——山奈酚被发现其可以通过增加ROS的产生促进PANC-1和MIAPaCa-2细胞凋亡,同时下调组织转谷氨酰胺酶TGM2的表达。山奈酚可以通过下调TGM2介导的Akt/mTOR信号传导诱导胰腺癌细胞中ROS依赖性胰腺癌细胞凋亡[51]。同样一种天然存在的含硫化合物:萝卜硫素也是通过增加ROS的水平来诱导胰腺癌细胞的凋亡[52]。
作为螺旋藻中提取出的一种天然活性小分子——藻蓝蛋白可以从多个靶点抑制胰腺癌细胞的增强。藻蓝蛋白通过作用MAPK信号通路相关的3个亚族:p38、JNK以及Erk,激活p38和JNK信号通路的同时抑制Erk通路来诱导PANC-1细胞的凋亡。同时藻蓝蛋白可以抑制PI3/Akt/mTOR信号通路促进自噬细胞死亡。此外,藻蓝蛋白促进NF-κB的激活和核易位来诱导胰腺癌细胞的自噬[53]。
2.2 抗转移与侵袭作用
EMT转化可以在降低胰腺癌细胞极性的同时,赋予更高的侵袭性,促进癌细胞向其他部位进行扩散与转移。从毛茛科植物芍药中提取的天然活性小分子芍药醇已经在多种癌症类型中产生抗癌效果。通过细胞划痕和Bodyen室侵袭实验发现,芍药醇可以对PANC-1和Capan-1细胞显示出显著的抗迁移和抗侵袭作用,并且芍药醇可以上调上皮相关的蛋白E-钙粘蛋白,并下调间充质相关的蛋白N-钙粘蛋白和波形蛋白的表达来抑制上皮间质转化。TGF-β1作为一种细胞因子,可以促进癌细胞的侵袭,免疫抑制以及EMT转化。最终发现芍药醇通过下调TGF-β1、p-Smad2/Smad2和p-Smad3/Smad3表达来抑制TGF-β1/Smad信号通路,从而抑制胰腺癌细胞的转移和侵袭[54]。
类黄酮类成分槲皮素3-O-葡糖苷可以通过阻断EGFR信号通路来抑制胰腺癌细胞的迁移。同时单独给予槲皮素3-O-葡糖苷或者联合吉西他滨都可以显著降低FAK和ERK1/2的磷酸化水平,所以槲皮素3-O葡糖苷可以通过阻断FAK和ERK1/2信号通路,在bFGF激活的人类胰腺癌细胞中诱导协同抗迁移作用[55]。
泛素-蛋白酶体在多种恶性肿瘤的发生发展中发挥关键作用,寻找可以靶向E2泛素结合酶的天然活性小分子是开发抗癌药物的新策略。通过从旋复花筛选到可以特异性结合E2泛素结合酶UbcH5c的抑制剂DHPO,从而抑制UbcH5c/cIAPs复合物的E2/E3相互作用,阻断IKK-β介导的IκBα降解和NF-κB的磷酸化激活,抑制胰腺癌细胞的转移[56]。
2.3 抑制肿瘤干细胞特性与耐药性
肿瘤干细胞(CSC)是一种CD24+CD44+ESA+的具有自我更新能力和分化能力的癌细胞,其能够表达耐药蛋白和抗凋亡蛋白,对DNA修复能力强,表现出对化疗药物耐药性。白藜芦醇作为广泛来源的天然多酚类小分子,发现可以显著抑制Kras基因突变的小鼠KrasG12D(胰腺癌模型小鼠)CSC相关的多能性维持因子:Nanog、Sox-2、c-Myc、Oct-4和耐药基因ABCG2,从而抑制胰腺CSC的自我更新能力和干细胞特征[57]。此外新的CSC研究靶点,敲低营养剥夺自噬因子NAF-1后,PACN-1和BxPC-3的CSC相关标志物:SOX2、NANOG和OCT4表达降低,而给予白藜芦醇可以显著抑制NAF-1的表达,从而抑制胰腺癌CSC的干细胞特性。
耐药性是胰腺癌临床治疗的主要挑战,间充质干细胞(ASC)等基质成分有助于形成化疗耐药肿瘤微环境(TME),奥沙利铂(OXP)和5-氟尿嘧啶(5-FU)可以降低胰腺癌细胞的活力,但对ASC表现出高耐药性,包括与DNA损伤反应、细胞周期调节和应激相关信号传导相关的途径,促进免疫逃避和驱动细胞外基质重塑显著影响肿瘤微环境[58]。汉防己甲素TET发现在对吉西他滨耐药PANC-1细胞中,可以通过抑制PI3K/Akt/mTOR信号通路并下调生存素的表达,从而增强胰腺癌细胞对吉西他滨的敏感性。同时TET通过上调AMPK-自噬轴增强细胞毒性和自噬依赖性细胞死亡[59]。
2.4 抗血管生成与免疫调节
浸润性肿瘤生长和远处转移会促进血管生成,加剧胰腺癌肿瘤细胞进入机体循环。胰腺癌表现出丰富的炎症浸润,含有更多的MC和免疫抑制型M2巨噬细胞,其表达血管生成分子,如VEGF-A、成纤维细胞生长因子-2、血小板衍生生长因子(PDGF)和MMP,促进肿瘤生长[60]。来自中药黄芪的天然多糖成分——黄芪多糖可以联合阿帕替尼在PANC-1和ASPC-1的VEGF/VEGFR信号通路,从而抑制血管生成,抑制癌细胞的增殖和迁移[61]。来自绿茶中的表没食子儿茶素-3-没食子酸酯EGCG可以随着浓度增加诱导抑制HIF-1的表达,同时EGCG会通过抑制在血管生成过程中的FOXOs的表达,最终EGCG会通过抑制PI3K/AKT和ERK通路与FKHRL1/FOXO3a激活相结合来抗血管生成[62]。
靶向肿瘤微环境或基质,包括CAF、胰腺星状细胞PSC、免疫细胞和巨噬细胞TAM是改善胰腺癌发展、转移和耐药的关键方向[63]。来自姜黄的天然成分姜黄素联合免疫点检查抑制剂PD-1/PD-L,可以直接抑制树突状细胞DC的STAT3对IL-6的激活,恢复癌细胞和免疫细胞靶向激活T细胞刺激活性来增强肿瘤抗原特异性T细胞的诱导[64]。Src同源性-2(SH2)结构域含有肌醇5′-磷酸酶-1(SHIP-1)是影响肿瘤免疫的髓系细胞发育和功能的主要调节因子,天然黄酮类小分子芹菜素可以在胰腺癌原位小鼠模型中增强SHIP-1表达,同时显著降低了免疫抑制TAM百分比,增强肿瘤的免疫反应[65]。
3 总结与展望
胰腺癌作为一种早期症状难以筛查,发病率较晚并预后较差的恶性癌症,需要发现和创新新的靶向药物,提高其治疗生存期。而来源于天然药物的活性小分子表现出巨大的潜力,本文综述了不同来源、不同作用机制以及不同结构代表的天然活性小分子的治疗作用和机制。未来研究应该将高通量筛选技术与网络药理学相结合、联合新用药策略(与吉西他滨/免疫检查点抑制剂等),降低耐药性、进行天然产物结构改造与药物递送系统,提高临床应用适用性,同时需要多学科合作推进其机制研究与临床转化。
基于天然活性成分发挥治疗胰腺癌的作用依赖于多组分对多个靶点的协同作用。基于单一的天然活性小分子的抗胰腺癌作用可能靶向多个途径:凋亡自噬、转移侵袭以及调节肿瘤微环境等,所以必须结合网络药理学智能研究手段,以系统的生物网络为研究对象,观察单个天然药物的多个活性分子对网络的影响,可以从多途径、多靶点的角度发现其关键的作用靶点。同时天然药物在体内发挥作用需要经过复杂的吸收,分布、代谢和排泄过程,而其作用可能依赖于多个组分或多种天然药物的相互作用,促进其在体内的吸收代谢过程。研究天然活性小分子会使得天然药物的内在系统联系割裂,协同作用消失,必须要基于代谢组学、药代动力学和药效动力学对活性成分进行研究。同时天然活性小分子的亲水性或亲脂性可能会影响在体内的渗透性、利用度以及后续的剂型开发,需要进一步的进行结构修饰和改造,提高临床可塑性。
对治疗胰腺癌的天然活性小分子的研究大多基于实验室体外或动物实验阶段,简单的靶向某个靶点的实验结果并不能直接代表其具有好的疗效,也不能代表其可以作为合格的药品上市。必须考虑其在复杂的胰腺癌患者体内残留的毒性、保留的半衰期以及其它药物的相互作用。未来需要结合纳米材料或结构修饰改造等,提高天然活性小分子在胰腺癌患者体内的靶向性和吸收利用,降低其毒性或副作用。
基于“药食同源”的中医理论,来源咖喱香料的姜黄素、玉米须的玉米须黄酮以及柑橘类水果的橙皮素的天然活性小分子都具有抗胰腺癌的药理作用。发现潜在的治疗胰腺癌的天然活性小分子需要重新了解和总结古代的经典药方名著,对生活中常见或者研究过的天然产物重新审视,挖掘其潜在的价值。同时靶向胰腺癌的天然活性小分子由于原料来源差异、缺乏标准化和高产量的提取工艺。同时由于其自身的理化性质、靶向性与选择性限制了其临床应用的剂型开发。未来应整合脂质体、外囊泡以及纳米材料等提高其生物相容性,实现智能递送,靶向晚期转移性或早期隐形胰腺癌。
[1]Ntukidem O L,Ogedegbe O J,Bai S.J.Clin.Oncol.,2025,43(4S):786.
[2]Hu J X,Zhao C F,Chen W B,Liu Q C,Li Q W,Lin Y Y,Gao F.World J.Gastroenterol.,2021,27(27):4298-4321.
[3]Huang J J,Lok V,Ngai C H,Zhang L,Yuan J Q,Lao X Q,Ng K,Chong C,Zheng Z J,Wong M C S.Gastroenterology,2021,160(3):744-754.
[4]Wang X,Hamann M T.Adv.Cancer Res.,2019,144:299-314.
[5]Sahu S K,Prabhakar P K,Vyas M.Mol.Biol.Rep.,2025,52(1):179.
[6]Izzo A A,Stefanska B.Br.J.Pharmacol.,2025,182(10):2069-2074.
[7]Triantafillidis J K,Triantafyllidi E,Sideris M,Pittaras T,Papalois A E.Nutrients,2022,14(3):619.
[8]Tao H,Chen X,Du Z Y,Ding K.Food Funct.,2020,11(8):6961-6970.
[9]Guo Z H,Zhou H L.Chin.J.Exp.Tradit.Med.Formulae,2015,21(8):222-225.
郭志红,周鸿立.中国实验方剂学杂志,2015,21(8):222-225.
[10]Chen J P,Yue L Y,Pan Y N,Jiang B Y,Wan J F,Lin H X,Guo F J,Li H Y,Li Y J,Zhao Q J.Adv.Sci.,2025,12(29):e01935.
[11]Bansod S,Doijad N,Godugu C.Toxicol.Appl.Pharmacol.,2020,403:115162.
[12]Liu J J,Luo X L,Guo R,Jing W H,Lu H T.J.Proteome Res.,2020,19(9):3825-3836.
[13]Liu M M,Pan Y,Tao X F,Kang W L,Liu Y J,Yang Y J,Xiao G.Biocell,2022,46(10):2257-2265.
[14]Park S H,Sung J H,Chung N.Mol.Cell.Biochem.,2014,394(1/2):209-215.
[15]Okuno K,Xu C M,Pascual S S,Tokunaga M,Han H Y,Fillat C,Kinugasa Y,Goel A.Pharmaceuticals,2022,15(10):1199.
[16]Park S H,Sung J H,Kim E J,Chung N.Braz.J.Med.Biol.Res.,2015,48(2):111-119.
[17]Guo G L,Yao G M,Zhan G Q,Hu Y F,Yue M,Cheng L,Liu Y P,Ye Q,Qing G L,Zhang Y H,Liu H D.Toxicol.Appl.Pharmacol.,2014,280(3):475-483.
[18]Qi J D,Meng M,Liu J T,Song X X,Chen Y,Liu Y X,Li X,Zhou Z,Huang X,Wang X H,Zhou Q S,Zhao Z.Biochem.Pharmacol.,2023,217:115833.
[19]Zhou X,Guo Z L,Liu S Z,Chen Z J,Wang Y,Yang R,Li X Z,Ma K T.Phytomedicine,2024,122:155128.
[20]Zhang Z,Chen W Q,Zhang S Q,Bai J X,Liu B,Yung K K,Ko J K.Phytomedicine,2022,106:154406.
[21]Ko J K.J.ImmunoTher.Cancer,2024,12:A8.
[22]Liu Y M,Xiao G S.J.Dalian Univ.Technol.,2025,65:243-248.
刘漪铭,肖桂山.大连理工大学学报,2025,65:243-248.
[23]Huang X S,Wen Z D,Cai H J,Yu D L.Biochem.Biophys.Res.Commun.,2025,772:152033.
[24]Cao C N,Sun L X,Mo W X,Sun L C,Luo J W,Yang Z H,Ran Y L.Pancreas,2015,44(8):1334-1339.
[25]Lan C Y,Chen S Y,Kuo C W,Lu C C,Yen G C.J.Food Drug Anal.,2019,27(4):887-896.
[26]Sun G,Wu Y,Li J K,Yang M J,Xu H,Li Y P,Tong P L,Shao R,Liu Y B,Kong X M.J.Control Release,2025,382:113642.
[27]Wu S B,Zhou G X,Zhang H,Huang J F,Wei Q,Ma P C,E Q.Chin.J.Clin.Oncol.,2005,32:4
吴深宝,周国雄,张弘,黄介飞,魏群,马鹏程,鄂群.中国肿瘤临床,2005,32:4.
[28]Phillips P A,Dudeja V,Mccarroll J A,Borja C D,Dawra R K,Grizzle W E,Vickers S M,Saluja A K.Cancer Res.,2007,67(19):9407-9416.
[29]Banerjee S,Sangwan V,Mcginn O,Chugh R,Dudeja V,Vickers S M,Saluja A K.J.Biol.Chem.,2013,288(47):33927-33938.
[30]Zhu W B,Li J J,Wu S H,Li S F,Le L,Su X W,Qiu P X,Hu H Y,Yan G M.Pancreas,2012,41(7):1029-1038.
[31]Zhao X,Liu Z,Ren Z Y,Wang H G,Wang Z S,Zhai J L,Cao D,Lyu S C,Li L X,Lang R,He Q.Eur.J.Pharmacol.,2020,880:173225.
[32]Dai H S,Jiang Y,Luo Y D,Bie P,Chen Z Y.Phytomedicine,2019,62:152953.
[33]Ma J X,Sun Y L,Yu Y,Zhang J,Wu H Y,Yu X F.Am.J.Transl.Res.,2019,11:3750-3760.
[34]Liu L,Salnikov A V,Bauer N,Aleksandrowicz E,Labsch S,Nwaeburu C,Mattern J,Gladkich J,Schemmer P,Werner J,Herr I.Int.J.Cancer,2014,134(10):2489-2503.
[35]Tian Q M,Zhang P,Wang Y H,Si Y H,Yin D P,Weber C R,Fishel M L,Pollok K E,Qiu B,Xiao F,Chong A S.eLife,2023,12:e85862.
[36]Chen H,Wang X Y,Liu M M,Yang J F,Kuang Y T,Wei R T,Tai Z G,Zhu Q G,Chen Z J,Chen J M,Wu X.Int.J.Pharm.,2023,648:123623.
[37]Wang C,Liu B,Xu X L,Zhuang B,Li H X,Yin J Q,Cong M Y,Xu W,Lu A P.Oncotarget,2016,7(7):8360-8372.
[38]Liu Y M,Li G C,Ning J Y,Zhao Y.Oncol.Lett.,2024,27(4):182.
[39]Guo J Q,Zheng Q H,Chen H,Chen L,Xu J B,Chen M Y,Lu D,Wang Z H,Tong H F,Lin S Z.Int.J.Oncol.,2014,45(3):1065-1072.
[40]Zhao T T,Wang Z H,Lin S Z.Chin.Tradit.Herb.Drugs,2024,55(18):6261-6268.
赵婷婷,王兆洪,林胜璋.中草药,2024,55(18):6261-6268.
[41]Zhao X X,Wu J C,Zhang K X,Guo D J,Hong L J,Chen X H,Wang B,Song Y J.Nanoscale Adv.,2021,4(1):190-199.
[42]Jiang J,Yuan Z G,Sun Y Q,Bu Y,Li W F,Fei Z H.Biomed.Pharmacother.,2017,96:619-625.
[43]Pan H X,Yang L H,Bai H S,Luo J,Deng Y.J.Ginseng Res.,2022,46(5):636-645.
[44]Zou J F,Su H F,Zou C L,Liang X D,Fei Z H.J.Biochem.Mol.Toxicol.,2020,34(6):e22480.
[45]Qian X Y,Liu Y,Chen W W,Zheng S X,Lu Y Y,Qiu P C,Ke X S,Tang H F,Zhang X.Chin.Herb.Med.,2025,17(1):94-107.
[46]Li G H,Wu Q B,Mou Y P,Qiao Y H,Jin L J,Shi Q,Zhang R N,Li J,Sun Y T,Zhang A L,Jiang H Y,Yang Z J,Zhu Z Y,Ma M M,Sun X Y,Sui X B.Theranostics,2025,15(15):7726-7746.
[47]Wang H C,Liu Y Z,Wang Y W,Xu T,Xia G G,Huang X Y.Cancer Med.,2023,12(14):15277-15288.
[48]Koul M,Meena S,Kumar A,Sharma P,Singamaneni V,Riyaz H S,Hamid A,Chaubey A,Prabhakar A,Gupta P,Singh S.Planta Med.,2016,82(4):344-355.
[49]He Q R,Tang J J,Liu Y,Chen Z F,Liu Y X,Chen H,Li D,Yi Z F,Gao J M.Br.J.Pharmacol.,2021,178(12):2496-2515.
[50]Li N,Yang F,Liu D Y,Guo J T,Ge N,Sun S Y.World J.Gastrointest.Oncol.,2021,13(9):1164-1183.
[51]Wang F J,Wang L,Qu C,Chen L Y,Geng Y W,Cheng C,Yu S L,Wang D,Yang L N,Meng Z Q,Chen Z.BMC Cancer,2021,21(1):396.
[52]Cho Y,Park M N,Choi M,Upadhyay T K,Kang H N,Oh J M,Min S,Yang J U,Kong M,Ko S G,Rahman M A,Harrath A H,Kim B.Front.Oncol.,2024,14:1442737.
[53]Liao G Y,Gao B,Gao Y N,Yang X G,Cheng X D,Ou Y.Sci.Rep.,2016,6(1):34564.
[54]Cheng C S,Chen J X,Tang J,Geng Y W,Zheng L,Lv L L,Chen L Y,Chen Z.Cancer Manag.Res.,2020,12:641-651.
[55]Lee J,Kim S J,Kim J H.Oncol.Rep.,2016,35(4):2473-2479.
[56]Qi S M,Guan X Q,Zhang J,Yu D H,Yu X F,Li Q L,Yin W J,Cheng X D,Zhang W D,Qin J J.Mol.Cancer,2022,21(1):70.
[57]Shankar S,Nall D,Tang S N,Meeker D,Passarini J,Sharma J,Srivastava R K.PLoS One,2011,6(1):e16530.
[58]Parvaneh V S,Miklós Z G,Páhi D,Szucs T,Monostori S,Póliska V,Venglovecz T,Pankotai L,Kemény Z V.Int J.Mol.Sci.,2025,26:390.
[59]Song J L,Xu J B,Guo J H,Shang Y,Wang J Y,Wang T M.Acta Histochem.,2021,123(6):151769.
[60]Zhang Z,Ji S R,Zhang B,Liu J,Qin Y,Xu J,Yu X J.Biomed.Pharmacother.,2018,108:1135-1140.
[61]Wu J,Wang J,Su Q,Ding W,Li T,Yu J X,Cao B W.OncoTargets Ther.,2018,11:2685-2698.
[62]Wan Q,Ren Q,Qiao S Y,Lyu A P,He X W,Li F F.Front.Nutr.,2024,11:1477140.
[63]Saadh M J,Mustafa M A,Malathi H,Ahluwalia G,Kaur S,Al A A,Alubiady M S,Zain S H,Shakier H G,Ali M S,Ahmad I,Abosaoda M K.Med.Oncol.,2024,41(8):201.
[64]Hayakawa T,Yaguchi T,Kawakami Y.Cancer Sci.,2020,111(12):4326-4335.
[65]Villalobos A K,Ortiz R I,Alvarez C,Husain K,Deloach D,Krystal G,Hibbs M L,Jiang K,Ghansah T.Cancers,2020,12(12):3631.