不对称Aldol反应作为一类重要的碳-碳键构建方法,在诸多天然产物和药物分子的合成中占据核心地位,尤其在精细调控多手性中心框架方面具有独特优势。该反应通常以烯醇或烯醇负离子对羰基化合物进行亲核加成为关键步骤,生成含一个或多个新手性中心的β-羟基羰基化合物[1]。该反应往往可以在极少量催化剂负载量下高效获得手性化合物,并为后续官能化提供 1,3-多官能团的反应平台[2]。
在过去几十年中,酶催化和过渡金属催化一直是不对称合成中的主流策略。然而,酶催化往往存在底物范围相对受限、制备与保存条件较苛刻等问题;金属催化则面临成本高、部分金属具有毒性、以及金属残留对环境和药物安全不利等挑战。随着绿色化学理念的深入人心,寻求兼具高效性与环境友好性的替代催化体系成为研究热点。随着Hajos等[3]和Eder等[4]相继报道了L-脯氨酸催化的分子内不对称Aldol反应,揭示了有机小分子在不对称催化中的巨大潜力,标志着有机小分子催化不对称Aldol反应研究的开端。此后,围绕氨基酸、有机胺、硫脲、磺酰胺以及多孔有机材料等不同骨架的有机催化剂不断涌现,不对称Aldol反应也从均相体系拓展到水相、多相、纳米和多孔框架等多种催化环境。
本文将重点综述近几年有机小分子催化不对称Aldol反应的代表性研究工作,按照催化剂结构类型分为3部分:氨基酸及其衍生物催化剂、含硫脲结构小分子催化剂以及其他类型有机小分子催化剂,并对其优势与不足进行归纳与展望。
1 有机小分子催化剂催化的不对称Aldol反应
1.1 氨基酸及其衍生物作为小分子催化剂催化的不对称Aldol反应
传统L-脯氨酸在有机溶剂中表现出优良的烯胺催化活性,但在水相中常因溶解度有限及氢键网络干扰而导致催化效率下降。针对这一瓶颈,Lataifeh等[5]于2022年设计了亲水性的二茂铁-氨基酸(Fc-amino acid)复合催化剂:利用Fc的刚性三维骨架提供额外手性诱导,同时以共价键锚定于氨基酸侧链,保留游离的α-氨基与α-羧基,形成兼具疏水骨架与亲水端基的分子结构,显著提高了水溶性与界面活性。在4-硝基苯甲醛(1)与丙酮(2)的水相不对称Aldol模型反应中,单取代Fc催化剂可实现90%的转化率和80% e.e.(图1),而双取代Fc催化剂表现不佳,作者推测与其过强亲水性削弱与底物的疏水相互作用有关。后续通过引入更刚性的骨架、精细调控Fc与氨基酸之间的连接基团,有望进一步优化亲水/疏水平衡与立体控制能力。
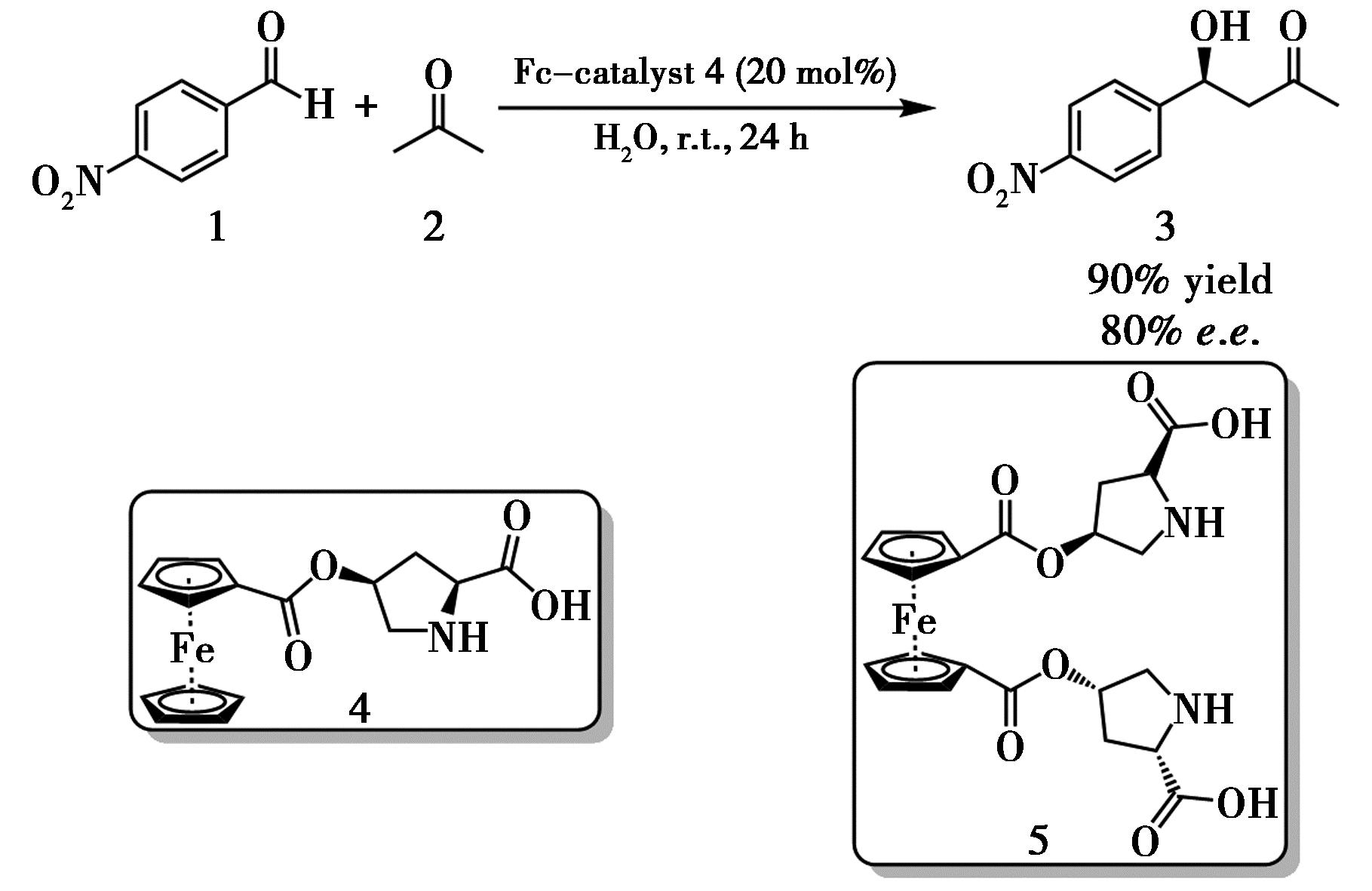
图1 二茂铁-氨基酸复合物催化的不对称Aldol反应[5]
Fig.1 Ferrocene-amino acid complex-catalyzed asymmetric Aldol reaction[5]
同年,Modi等[6]报道了一种无需保护步骤的L-脯氨酸硅基手性催化剂L-proline-(3° amine)-f-SiO2。该催化剂以10 mL丙酮(兼作反应物和溶剂)为介质,在无额外有机溶剂、室温条件下即可高效催化1 mmol 4-硝基苯甲醛与丙酮的直接不对称Aldol反应。催化剂循环使用6次后,转化率仍保持99%,产物S构型的对映选择性可以保持在97%以上(图2)。该工作充分展现了固载脯氨酸催化剂在绿色与可回收方面的优势,但目前的高活性数据主要集中于4-硝基苯甲醛体系,对其他醛类底物的普适性仍需系统考察。
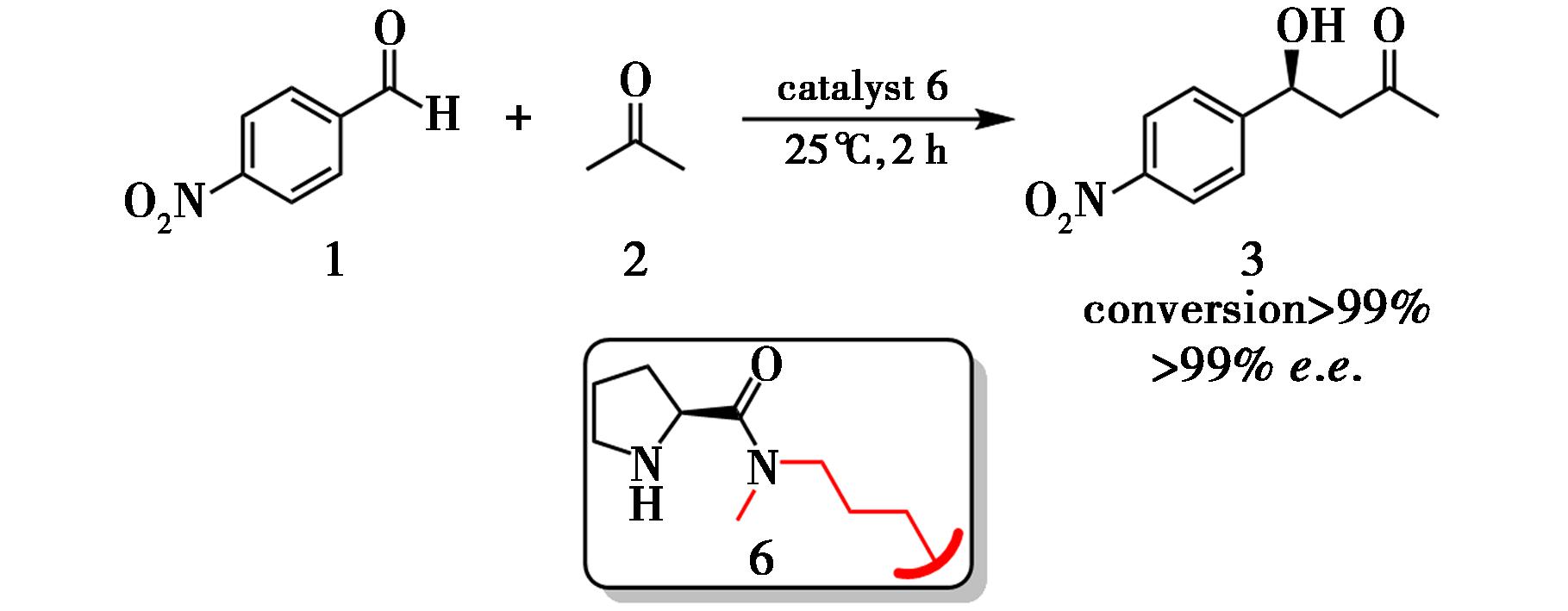
图2 L-proline-(3° amine)-f-SiO2催化的不对称Aldol反应[6]
Fig.2 L-proline-(3° amine)-f-SiO2-catalyzed asymmetric Aldol reaction[6]
针对经典L-脯氨酸在水相中催化效率低、对映选择性差等问题,Yimlaz等[7]于2022年合成了新型脯氨酸-THIQA衍生的手性二酰胺催化剂,并在水相、室温条件下实现了高效而绿色的不对称Aldol反应(图3)。通过助催化剂筛选,最终确定苯甲酸为最佳添加剂,在优化条件下以89%收率和84% e.e.获得目标产物。作者认为,吗啉环中的氮、氧原子通过吸电子诱导效应增强了酰胺N—H与甲酰基氧之间的氢键作用,从而更有效地活化底物。作者提供了一类绿色、高效、可水相操作的新型手性二酰胺催化剂并克服了L-脯氨酸在水相中催化结果欠佳、底物范围窄等问题。但是该催化体系对电子缺乏的芳香醛表现良好,而对弱吸电子或供电子取代的芳香醛(如4-溴苯甲醛)催化效果明显变差,提示其在底物电子性质方面具有一定局限性;同时,催化剂用量仍为10 mol%,催化剂回收和放大实验也有进一步优化空间。
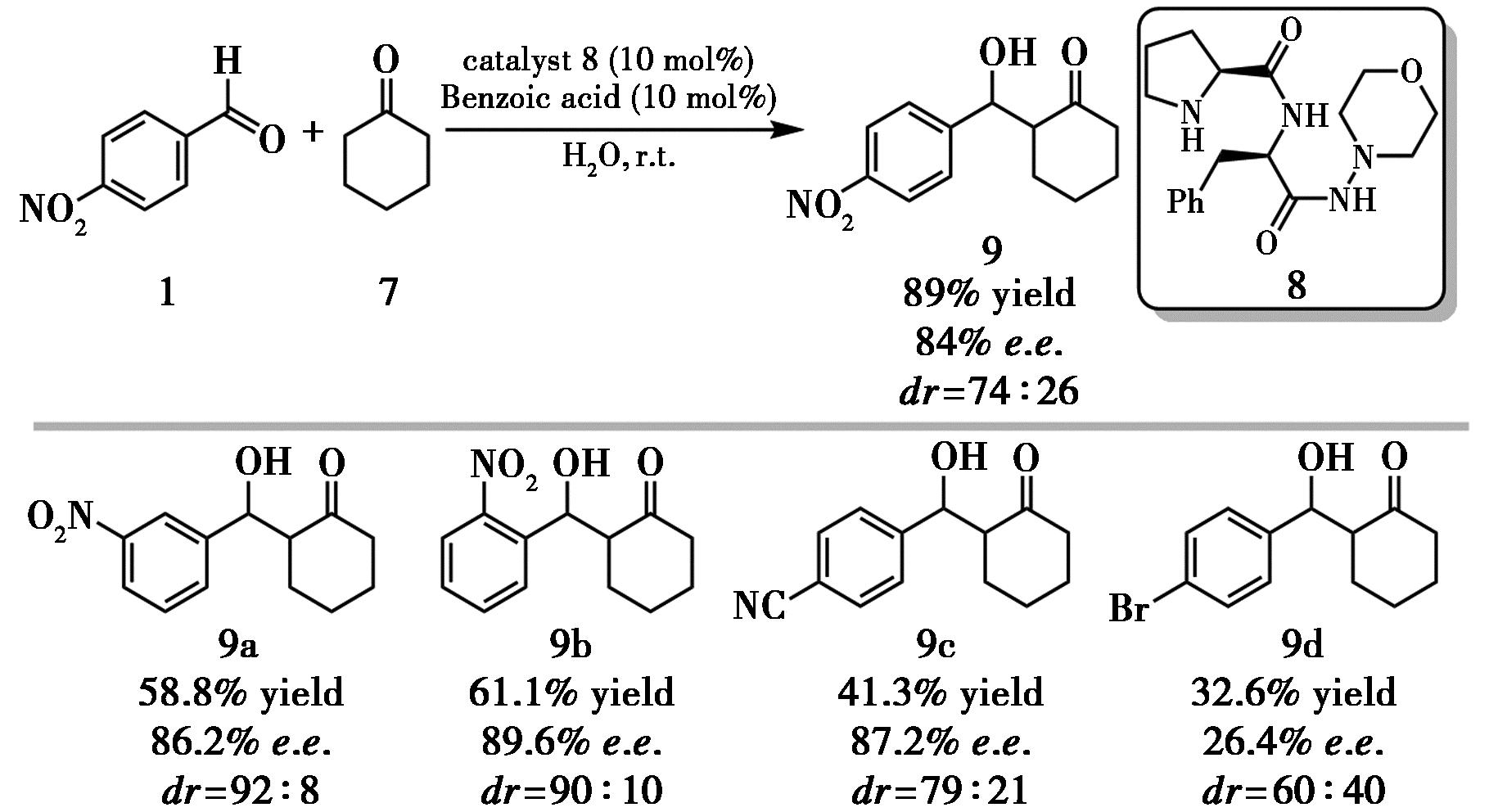
图3 催化剂8催化的不对称Aldol反应[7]
Fig.3 Asymmetric Aldol reaction catalyzed by catalyst 8[7]
Yilmaz等[8]随后继续围绕提高脯氨酸在水相中的催化效率开展研究,将L-脯氨酸引入杯芳烃骨架开发了兼具疏水空腔与烯胺亲核位点的新型有机催化剂。该类催化剂在水中对直接不对称Aldol反应表现出优良性能(收率94%,82% e.e.),当添加氯乙酸(CAA)时,e.e.值可进一步提升至88%(图4)。作者认为,CAA提供弱酸性环境有利于烯胺形成并稳定氢键网络,而杯[4]芳烃疏水空腔与水介质共同构筑的疏水效应及氢键协同作用是高对映选择性的关键。与前期工作相比,杯芳烃-脯氨酸杂化催化剂的催化结果优于早期“吗啉-脯氨酸”体系。尤其对4-溴苯甲醛底物收率达到了75%,e.e.值由26.4%升高至77%,而F、CN、CF3等取代基底物给出80%~94%收率、82%~88% e.e.。文章在低水量、单一溶剂条件下克服了前期工作中底物范围窄等局限,为在水相中有机催化提供了新的典范。
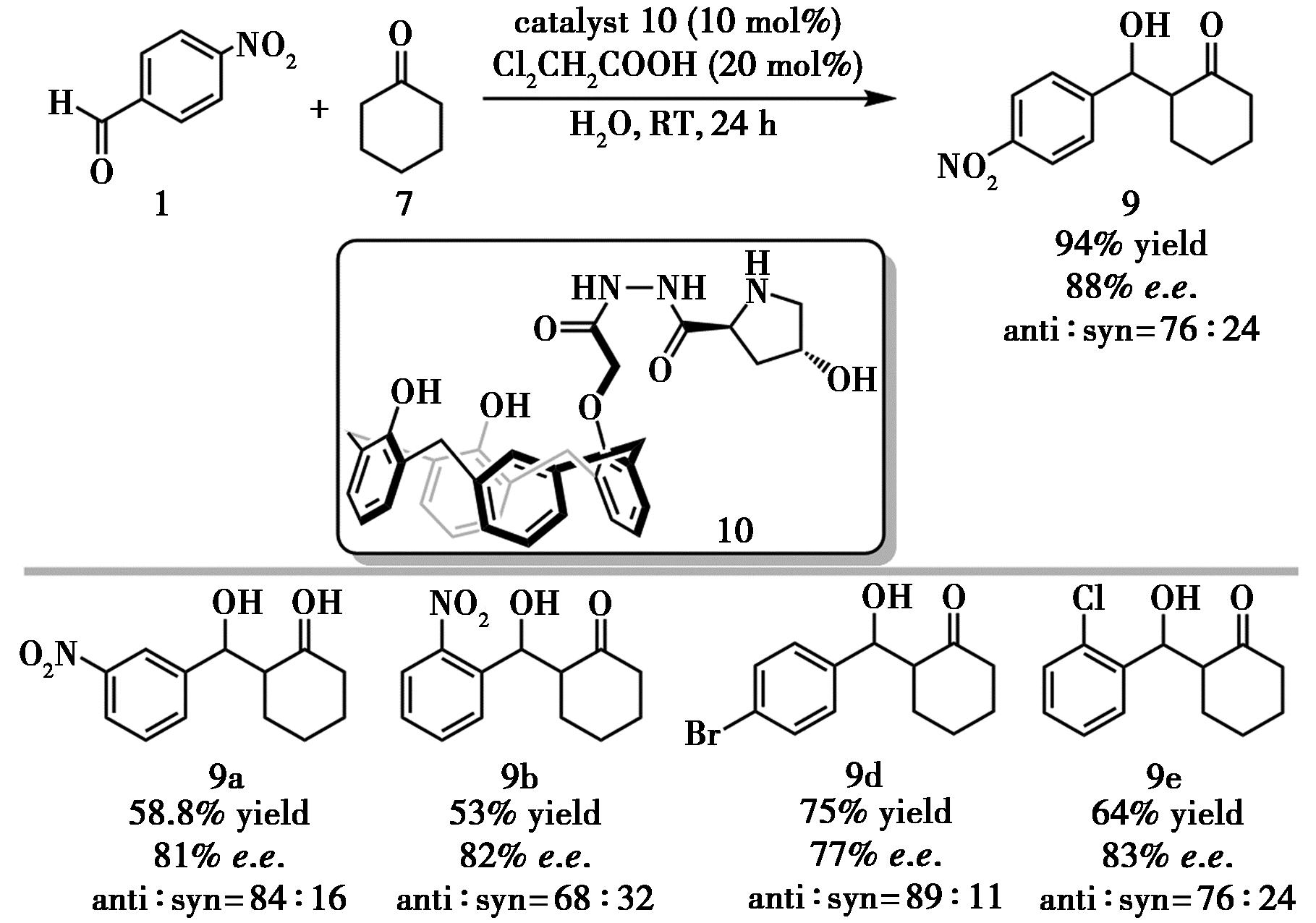
图4 催化剂10催化的不对称Aldol反应[8]
Fig.4 Asymmetric Aldol reaction catalyzed by catalyst 10[8]
同年,Salehi等[9]为克服传统L-脯氨酸催化下产物多为anti构型的局限,将(R)-四氢罂粟碱(THP)与L-脯氨酸进行肽杂化设计,构建了一类新型肽类催化剂,实现了syn选择性逆转的不对称Aldol反应(图5)。在THF/DMSO混合溶剂、-20 ℃条件下,二肽催化剂11可在30 mol%催化剂用量下获得高达90% e.e.的syn产物,而三肽催化剂的活性与选择性均有所下降,说明肽链长度并非越长越有利。作者提出,THP芳环与芳香醛芳环之间的π-π堆积有助于稳定过渡态,是立体选择性的关键因素。该工作为通过肽杂化策略发展新型手性催化剂提供了有益启示,后续可考虑引入更刚性或具有特定构象的连接链,以进一步提高立体控制能力并降低催化剂负载。
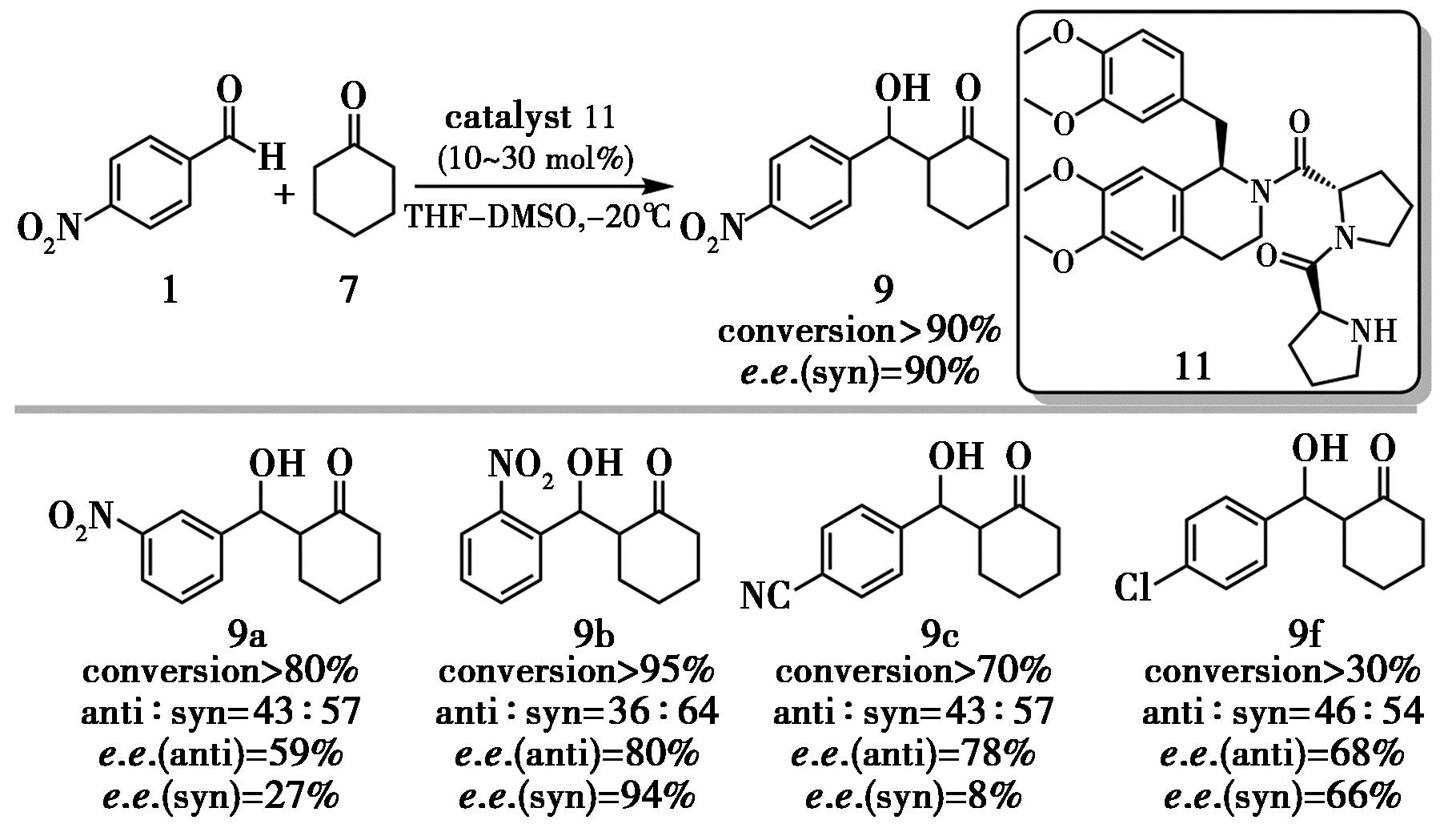
图5 催化剂11催化的不对称Aldol反应[9]
Fig.5 Asymmetric Aldol reaction catalyzed by catalyst 11[9]
2022年,Branco等[10]提出的手性离子液体(CILs)催化体系在兼具传统离子液体低挥发性、热稳定性和可设计性的基础上,引入L-半胱氨酸衍生物作为手性源,在不对称Aldol反应中表现出良好的催化性能。在10%~20%催化剂用量下可获得76%收率和96% e.e.的目标产物(图6)。尽管催化剂13在多次循环使用后仍能保持较高活性,但对映选择性由初始的96% e.e.降低至约53% e.e.,表明重复使用过程中手性微环境存在一定程度的衰减。通过在结构上引入更刚性的骨架或增强分子内氢键,有望提高该类催化剂的立体稳定性与循环利用性能。
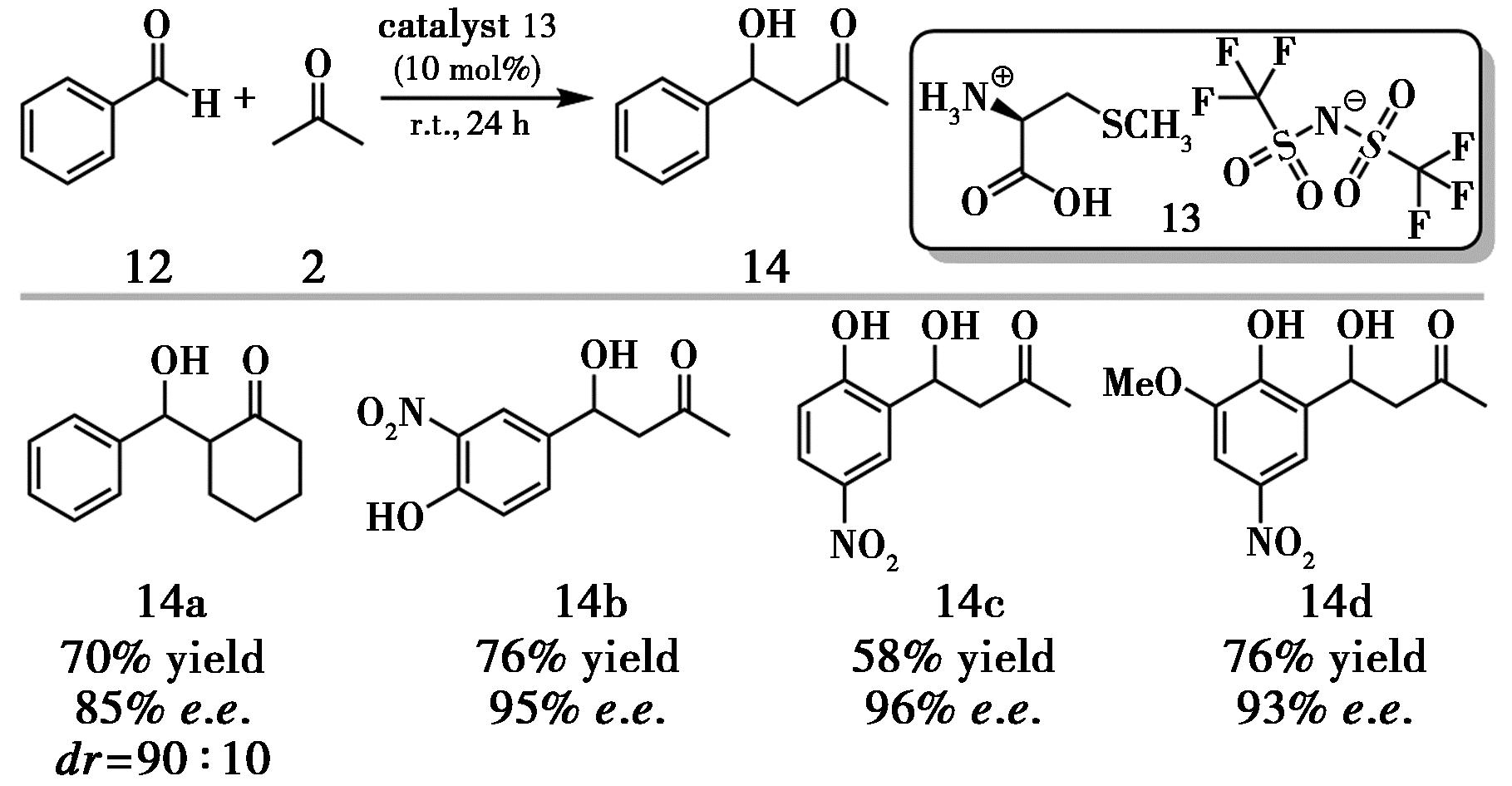
图6 催化剂13催化的不对称Aldol反应[10]
Fig.6 Asymmetric Aldol reaction catalyzed by catalyst 13[10]
多孔有机笼(Porous organic cages,POCs)是一类由有机分子自组装形成、具有内在空腔且可溶于有机溶剂的多孔材料。2022年,Xu等[11]首次将手性POCs引入不对称催化领域:通过将L-脯氨酸引入二胺配体,再与多醛单元C4RACHO经动态亚胺化学自组装,构建了[4+8]四聚体棱柱形和[6+12]六聚体八面体形手性POCs。以对硝基苯甲醛与环己酮为模型反应,可获得99%收率和92% e.e.的Aldol产物(图7)。底物拓展实验显示,大体积芳香醛底物反应效率明显下降,支持反应主要在笼内空腔中进行的推测。通过改变POCs的尺寸和构型可有效调控催化活性与选择性,为利用可溶性多孔有机笼构建新型不对称催化体系提供了思路。
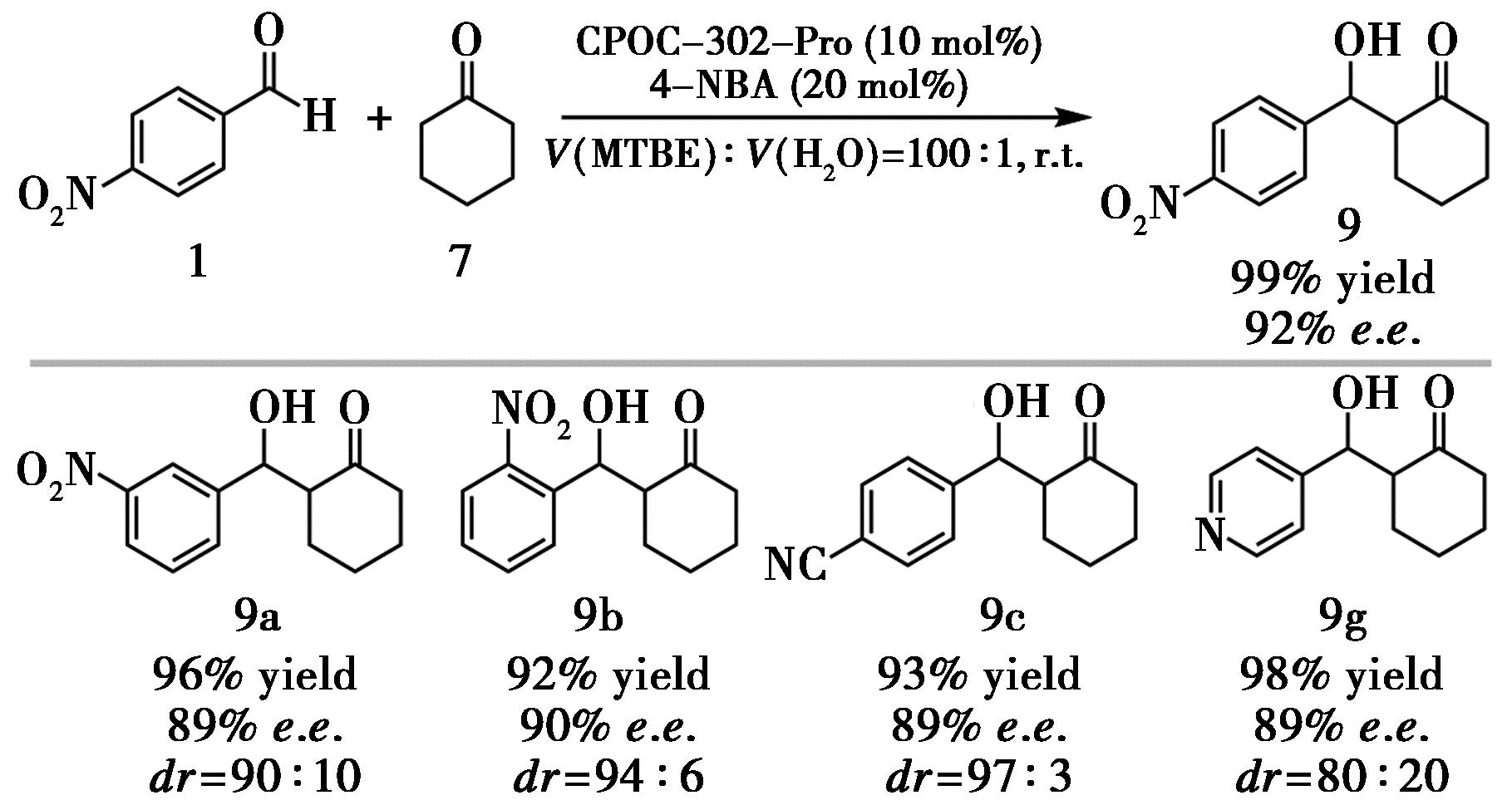
图7 POCs催化的不对称Aldol反应[11]
Fig.7 Asymmetric Aldol reaction catalyzed by catalyst POCs[11]
2023年,Lv等[12]针对3-羟基-2-吲哚酮这一广泛存在于天然产物与药物分子中的骨架,设计了以叔亮氨酸为核心的三功能中心手性催化剂,包含伯胺-酰胺-酚羟基3种功能单元。在优化条件下,该体系对靛红与芳香醛的Aldol反应可获得高达98%收率、99% e.e.及98∶2 dr的R构型产物(图8a),显示出优异的立体控制能力。该催化剂利用酚羟基与酰胺N—H构筑双氢键,实现对靛红底物的高效活化(图8b),并借助亲水基团增强水溶性与界面活性,使反应可在水相中进行。对于N-烷基取代或C-7溴取代的靛红底物,对映选择性有所下降,后续可通过调整氢键基团位置、增强催化剂整体刚性,有望进一步拓展底物范围。
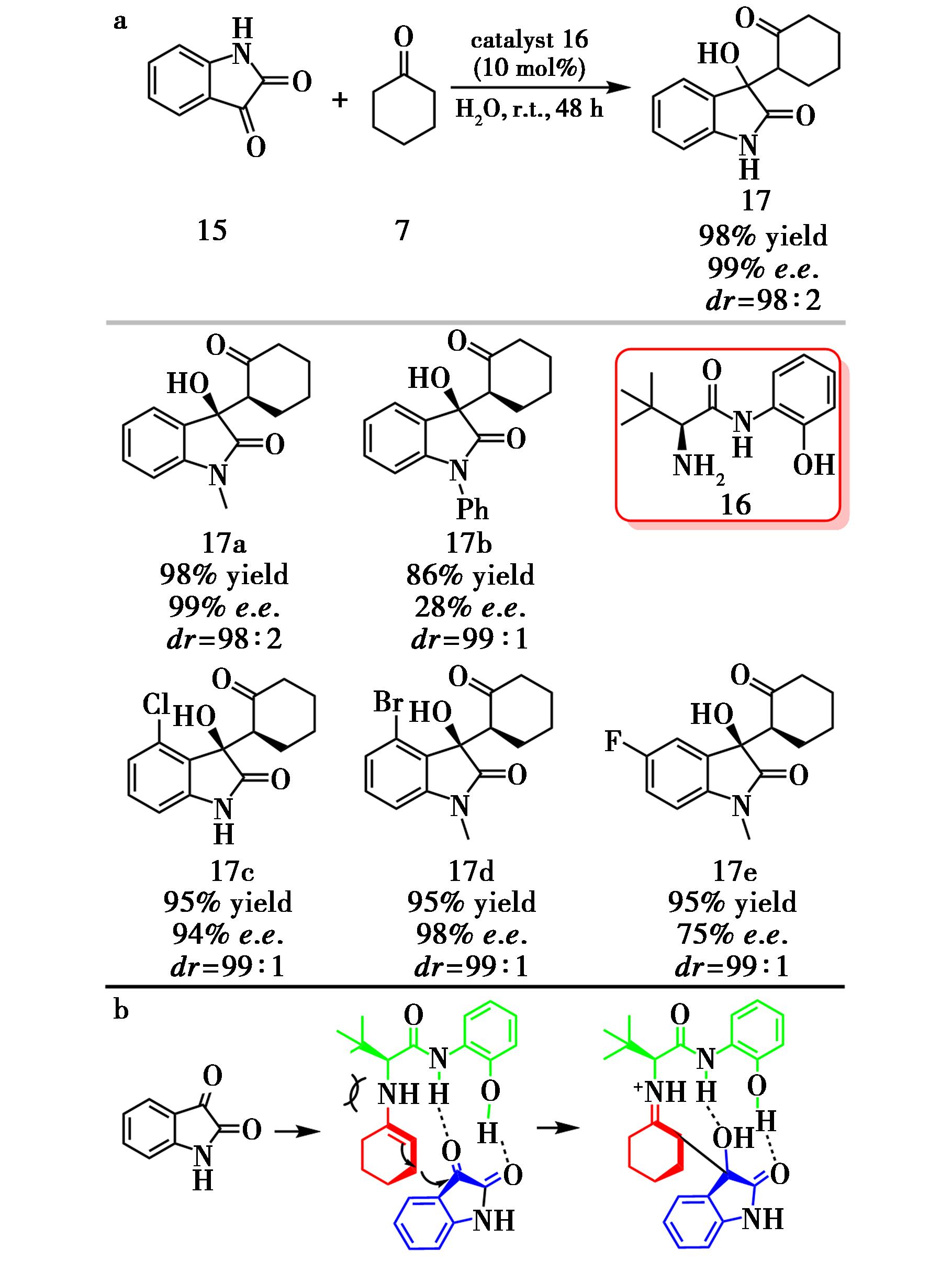
a.催化剂16催化的不对称Aldol反应;b.反应过渡态模型
图8 催化剂16催化的不对称Aldol反应[12]
Fig.8 Asymmetric Aldol reaction catalyzed by catalyst 16[12]
Nakano等[13]在市售氨基酸的基础上引入硼原子,构建了含硼-伯胺-酰胺三功能中心的新型有机催化剂,并应用于4-硝基苯甲醛(1)与环己酮(7)的不对称Aldol反应。在优化条件下,可获得82%收率和94% e.e.的产物(图9a)。值得注意的是,他们发现海水与自来水的混合体系可显著提高反应效率和e.e.值,推测与溶液的离子强度、pH以及界面张力等因素有关。在机理研究中,作者指出硼原子并非传统意义上的Lewis酸中心,而是通过与水分子配位及保持催化剂刚性构象,协同控制立体化学(图9b)。该催化体系具有绿色经济的优势,但仍存在催化剂失活问题,且需苯甲酸作为共催化剂,未来可通过进一步修饰结构以提高对脂肪醛和杂芳香醛底物的反应性与稳定性。
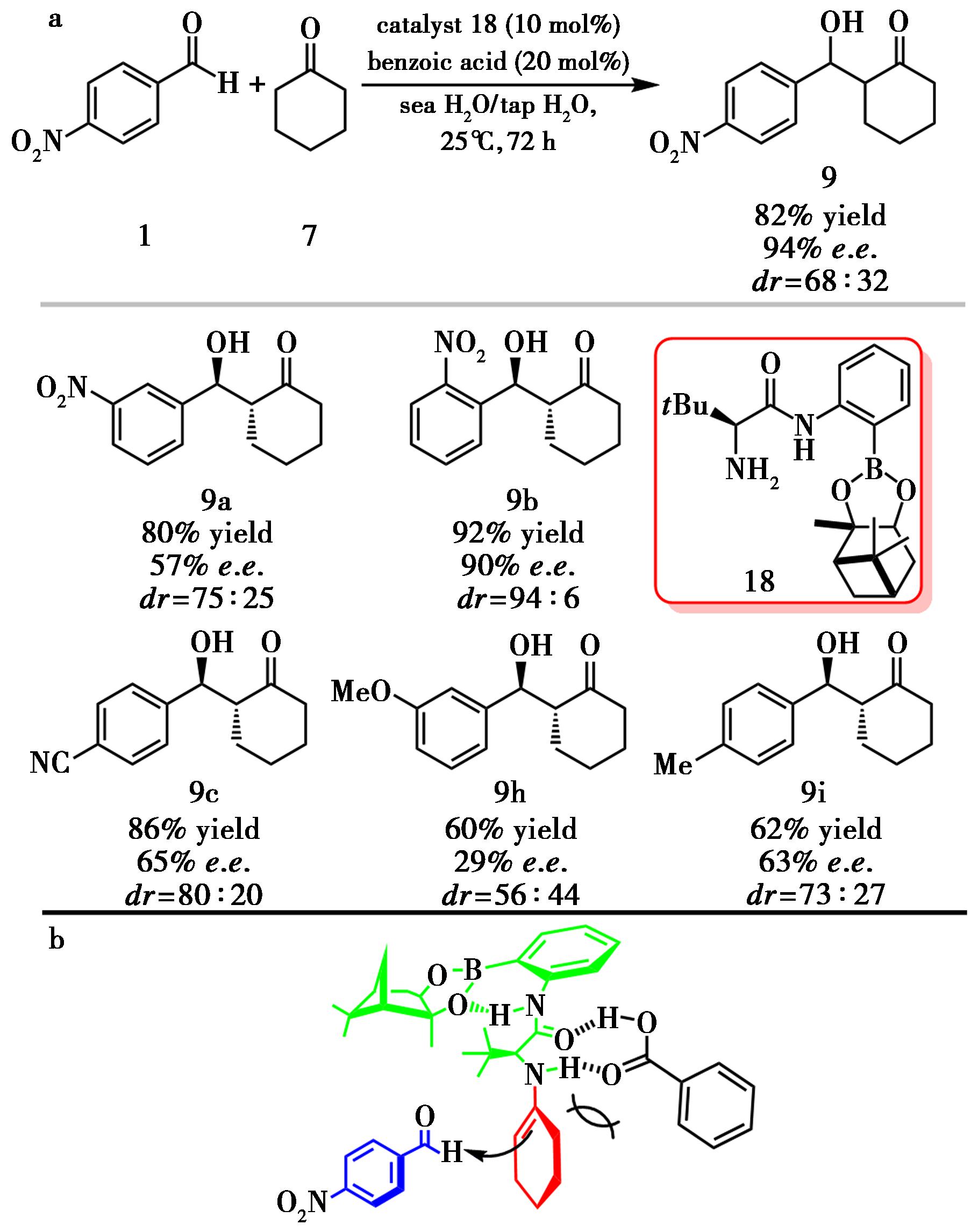
a.催化剂18催化的不对称Aldol反应;b.反应过渡态模型
图9 催化剂18催化的不对称Aldol反应[13]
Fig.9 Asymmetric Aldol reaction catalyzed by catalyst 18[13]
传统不对称Aldol反应大多只能生成两个相邻立体中心。2023年,Kano等[14]利用动态动力学拆分(Dynamic kinetic resolution,DKR)策略,在一次Aldol反应中构建3个连续立体中心。以α-硅氧基酮(19)为供体、易发生外消旋化的α-卤代醛(20)为受体,氨基酸为催化剂,叔丁醇为溶剂,简单一锅法即可合成三立体中心产物,表现出优异的收率和立体选择性(图10)。条件优化表明,催化剂侧链的TBS基团能显著提升溶解性与立体选择性,而叔丁醇作为质子溶剂有助于抑制背景反应,提高非对映选择性。同时,他们也指出含苯基的α-溴代醛易发生脱溴副反应、α-碘代醛易分解,无法得到目标产物,限定了底物范围。因此,后续可通过优化反应条件,明确卤原子对反应速率和选择性的影响以拓宽适用底物。
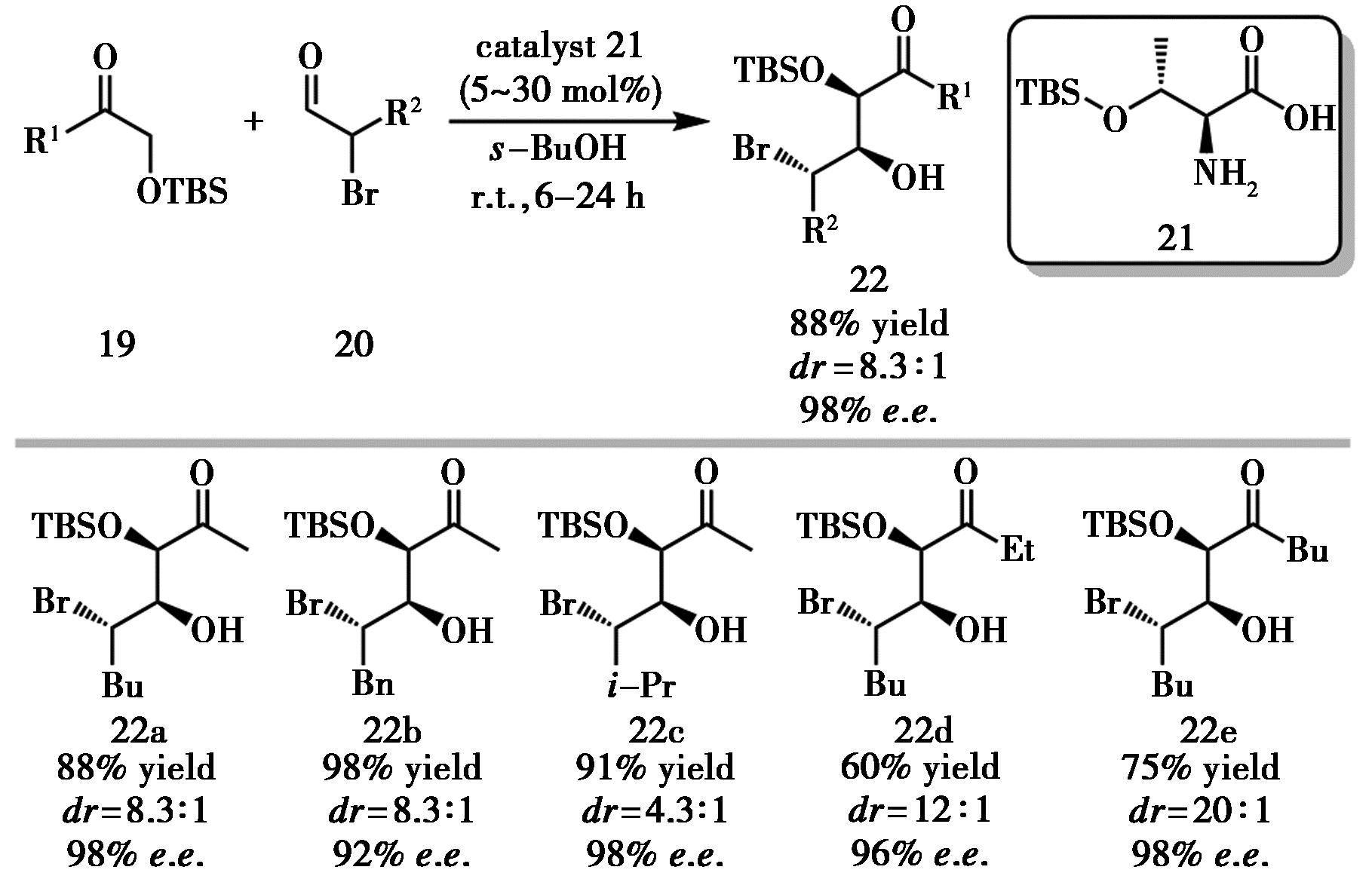
图10 催化剂21催化的不对称Aldol反应[14]
Fig.10 Asymmetric Aldol reaction catalyzed by catalyst 21[14]
手性聚合物纳米粒子(Chiral polymeric nanoparticles,CPPs)兼具不对称催化与材料可加工性的优势,但其在无溶剂Aldol反应中的应用报道较少且立体选择性有限。Mastai等[15]以保护氨基酸为单体,通过微乳液聚合和反向微乳液聚合分别制备了多种CPPs,并将其用于不对称Aldol反应。该体系在无溶剂条件下可获得最高72%收率和86% e.e.的目标产物(图11),催化剂可通过简单离心回收,循环4次后活性几乎保持不变。通过进一步降低粒径、构建交联梯度或引入多功能手性单元,有望进一步提升立体选择性与催化效率。
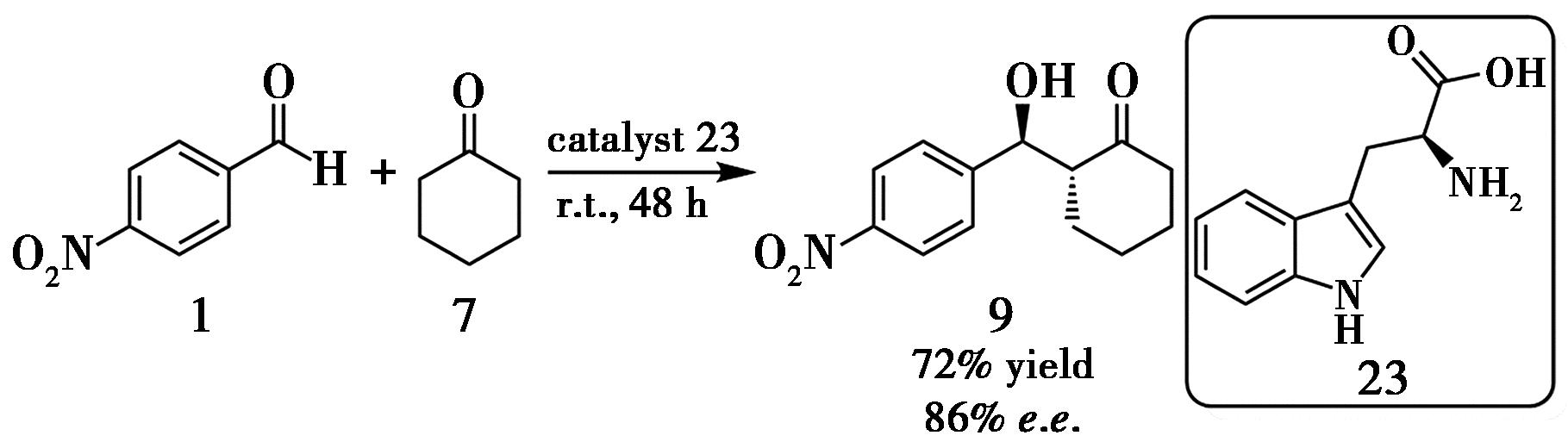
图11 催化剂23催化的不对称Aldol反应[15]
Fig.11 Asymmetric Aldol reaction catalyzed by catalyst 23[15]
针对在诸多天然产物和药物中存在的3-烷基-3-羟基吲哚-2-酮骨架,Singh等[16]通过将L-脯氨酰胺及其离子液体衍生物插入膨润土层间,构建了可回收的异相催化体系,用于不对称Aldol反应(图12)。在该体系中,从(S)-苯乙胺衍生的手性离子液体表现出最佳对映选择性,收率为72%~98%,e.e.值为37%~80%。作者认为疏水阴离子![]() 在反应过程中对过渡态具有包裹效应,从而抑制非手性反应路径。未来通过优化催化剂结构与反应条件,有望进一步提高对映选择性并扩展至更多醛、酮底物;同时,可结合同位素标记与动力学研究对机理进行更深入验证。
在反应过程中对过渡态具有包裹效应,从而抑制非手性反应路径。未来通过优化催化剂结构与反应条件,有望进一步提高对映选择性并扩展至更多醛、酮底物;同时,可结合同位素标记与动力学研究对机理进行更深入验证。
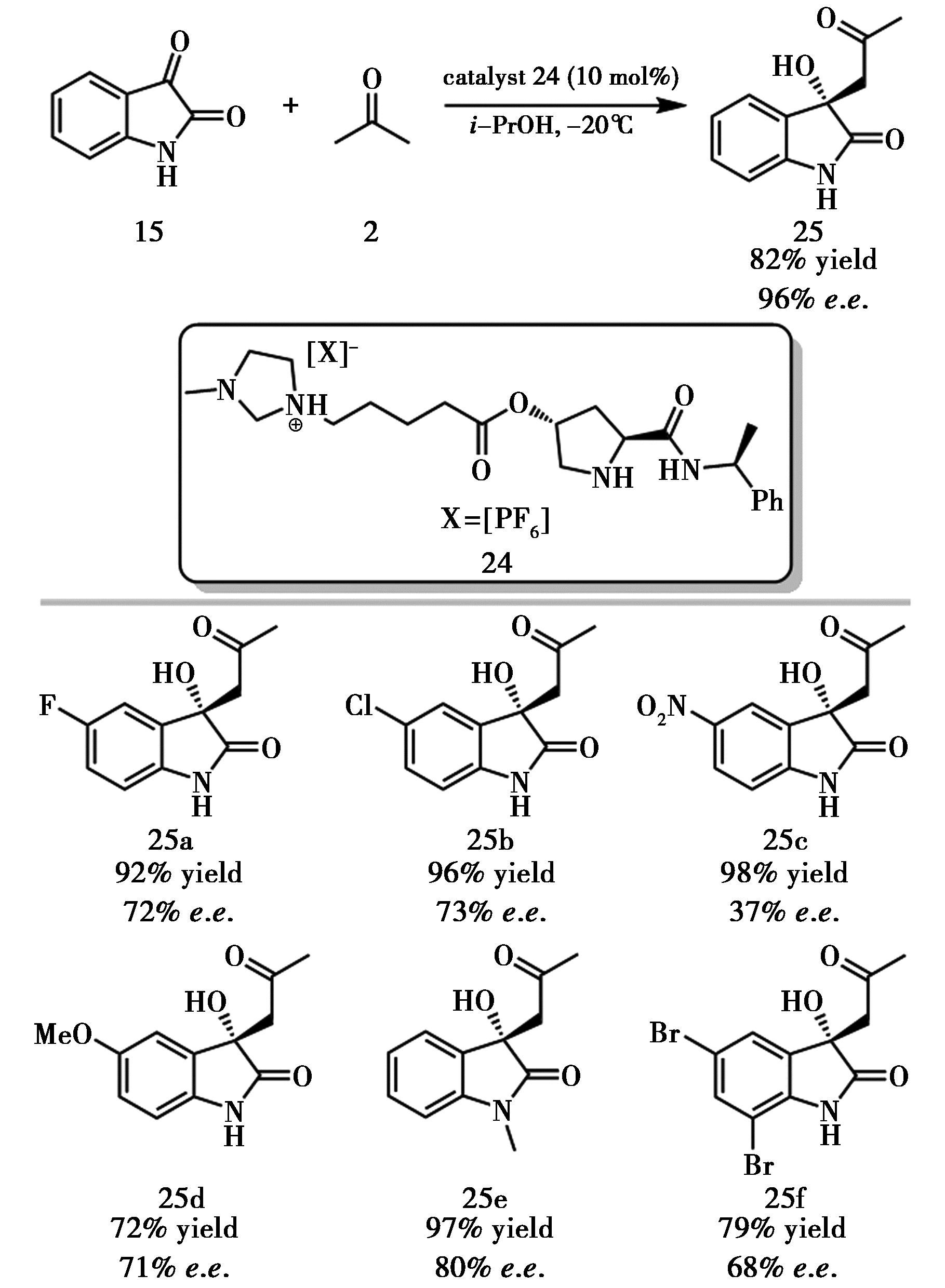
图12 催化剂24催化的不对称Aldol反应[16]
Fig.12 Asymmetric Aldol reaction catalyzed by catalyst 24[16]
Palkó等[17]设计合成了一系列β-氨基酸衍生物,系统考察其在异靛红(15)与丙酮(2)不对称Aldol反应中的催化活性与立体控制能力(图13)。结果表明,Boc保护的酰胺催化剂与LiOH共同催化体系在反应速率与立体选择性方面较为理想;而盐酸盐形式的催化剂因自带游离胺,可避免外加碱,在无碱条件下虽反应时间略长但更符合绿色化学要求。C-5位带有I、F、Me的e.e.值较低,而在带有Cl、Br取代基的异靛红通常可以获得更高的e.e.值。该工作还进行机械化学研究,高速球磨(HSBM)可将溶剂用量降低约99%,且对映选择性不逊于溶液相,展示了向绿色放大和连续化转化的潜力。
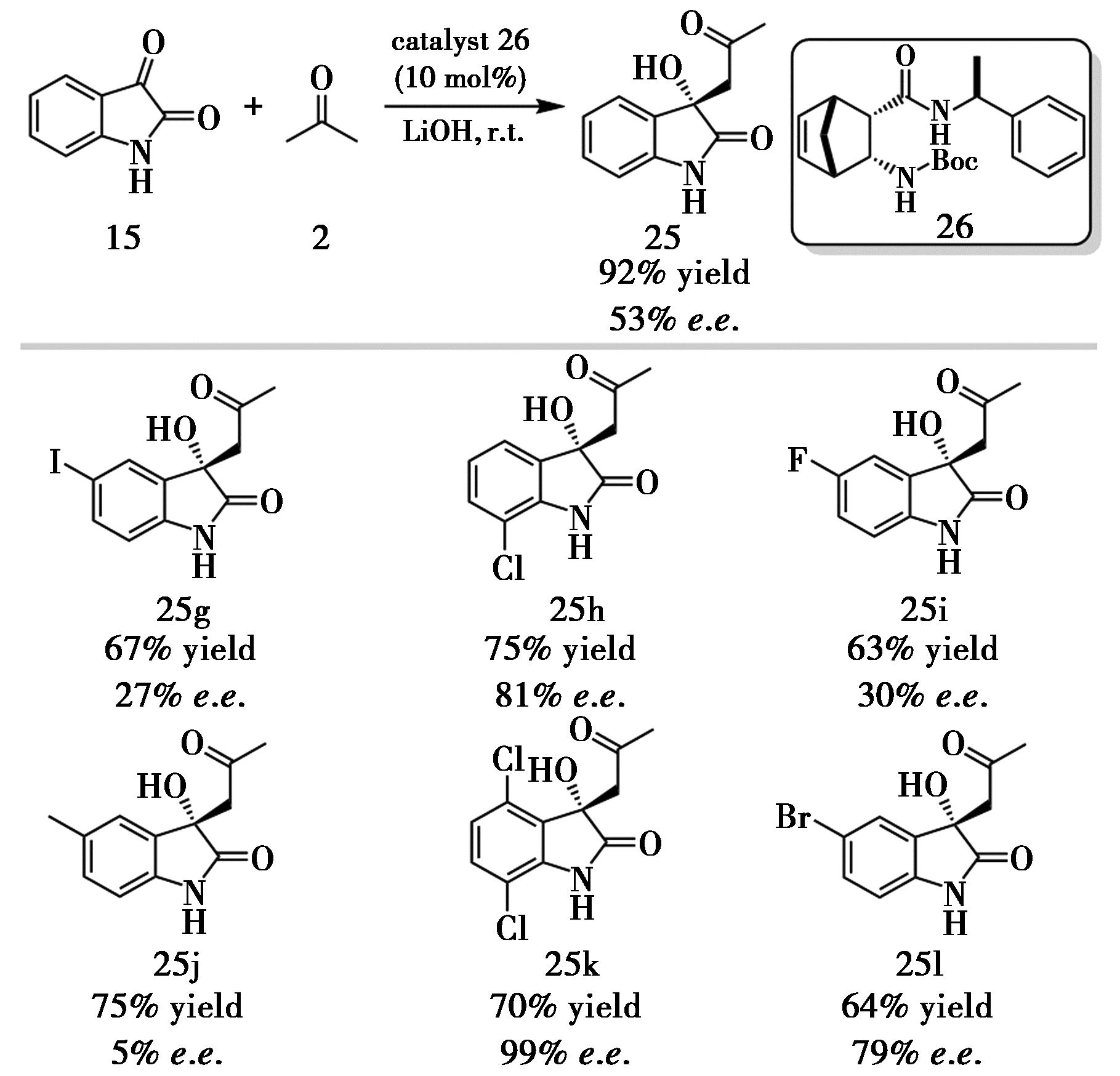
图13 催化剂26催化的不对称Aldol反应[17]
Fig.13 Asymmetric Aldol reaction catalyzed by catalyst 26[17]
Easwar等[18]首次将磺酰胺基团引入脯氨酸C4位,构建具有羧基与磺酰胺双功能的手性催化剂,在水相中催化对硝基苯甲醛(1)与环己酮(7)的不对称Aldol反应。该体系在水相中实现了71%~94%收率、98% e.e.以及98∶2 dr的高效转化(图14)。通过对同侧与对侧修饰羧基和磺酰胺两种结构的比较,发现同侧结构催化剂可通过分子内氢键协同作用更有效地稳定过渡态,从而提升收率和对映选择性,该结论也得到DFT计算支持。该工作突出了水作为绿色介质在降低反应活化能、促进协同氢键催化中的重要作用。
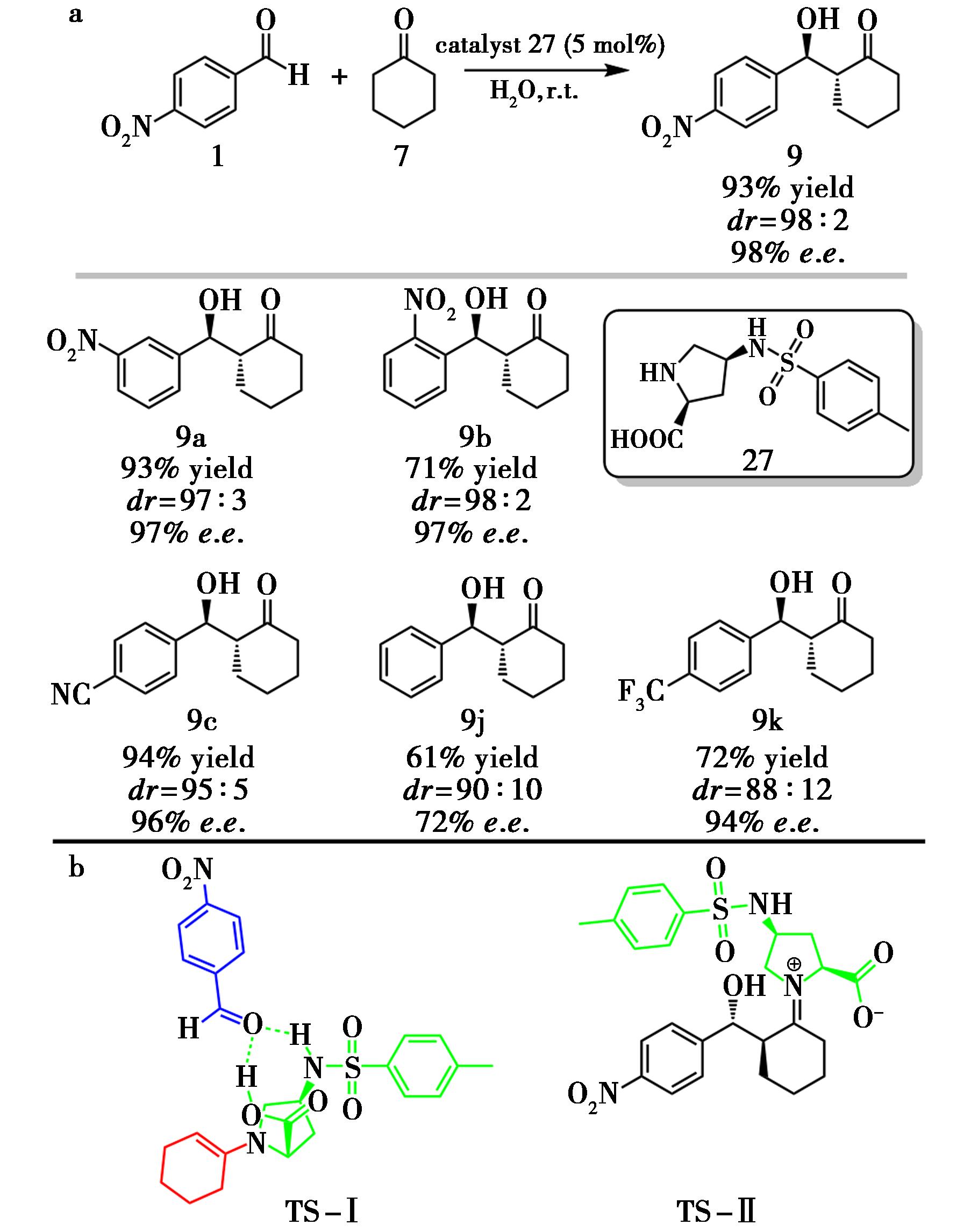
a.催化剂27催化的不对称Aldol反应;b.反应过渡态模型
图14 催化剂27催化的不对称Aldol反应[18]
Fig.14 Asymmetric Aldol reaction catalyzed by catalyst 27[18]
传统有机催化体系往往依赖较高催化剂负载,这在工业放大时会带来纯化和催化剂回收的难题。Makatini等[19]利用金纳米颗粒(AuNPs)易于合成与表面修饰的特点,将肽催化剂固定于AuNPs表面,构建了肽-AuNPs异相催化体系。该体系在对硝基苯甲醛(1)与环己酮(7)的不对称 Aldol反应中,可在较低催化剂用量下获得85%收率和94% e.e.(图15)。进一步研究表明,柠檬酸盐缓冲液有助于维持肽构象和AuNPs分散性,而粒径为12 nm的AuNPs兼具较大比表面积与良好稳定性,表现出最佳催化性能。粒径超过 15 nm时易聚集导致性能下降。该方法首次将肽与金纳米颗粒(AuNPs)相结合用于不对称催化,为该领域提供了一种绿色、可持续、低催化剂负载的催化策略。未来可围绕循环使用稳定性和结构-性能关系展开深入研究。

图15 肽-金纳米颗粒催化的不对称Aldol反应[19]
Fig.15 Asymmetric Aldol reaction catalyzed by peptide-gold nanoparticles[19]
手性1,3-二醇广泛存在于天然产物、药物、农药中,是合成手性配体、助剂、金属有机催化剂的关键中间体。但因其具有两个手性中心,合成难度较高,尤其是单一对映体的选择性构建方面仍是急需解决的难题。Hasdemir等[20]通过“两步串联策略”——脯氨酸衍生物催化的不对称Aldol反应与CBS不对称还原相结合,成功合成了具有单一构型的1,3-二醇骨架。以V(DMSO)∶V(H2O)=8∶2为混合溶剂、Cu(OTf)2为添加剂时,Aldol步骤可获得优异的99%收率、98% e.e.和97∶3 dr(图16a)。作者推测Cu2+与催化剂之间形成的刚性配合物有助于增强对映选择性(图16b)。该催化剂对含有供吸电子取代基的苯甲醛均有很好的耐受性。该工作为通过级联或串联策略从简单底物高效构建多立体中心1,3-二醇提供了有价值的范例。
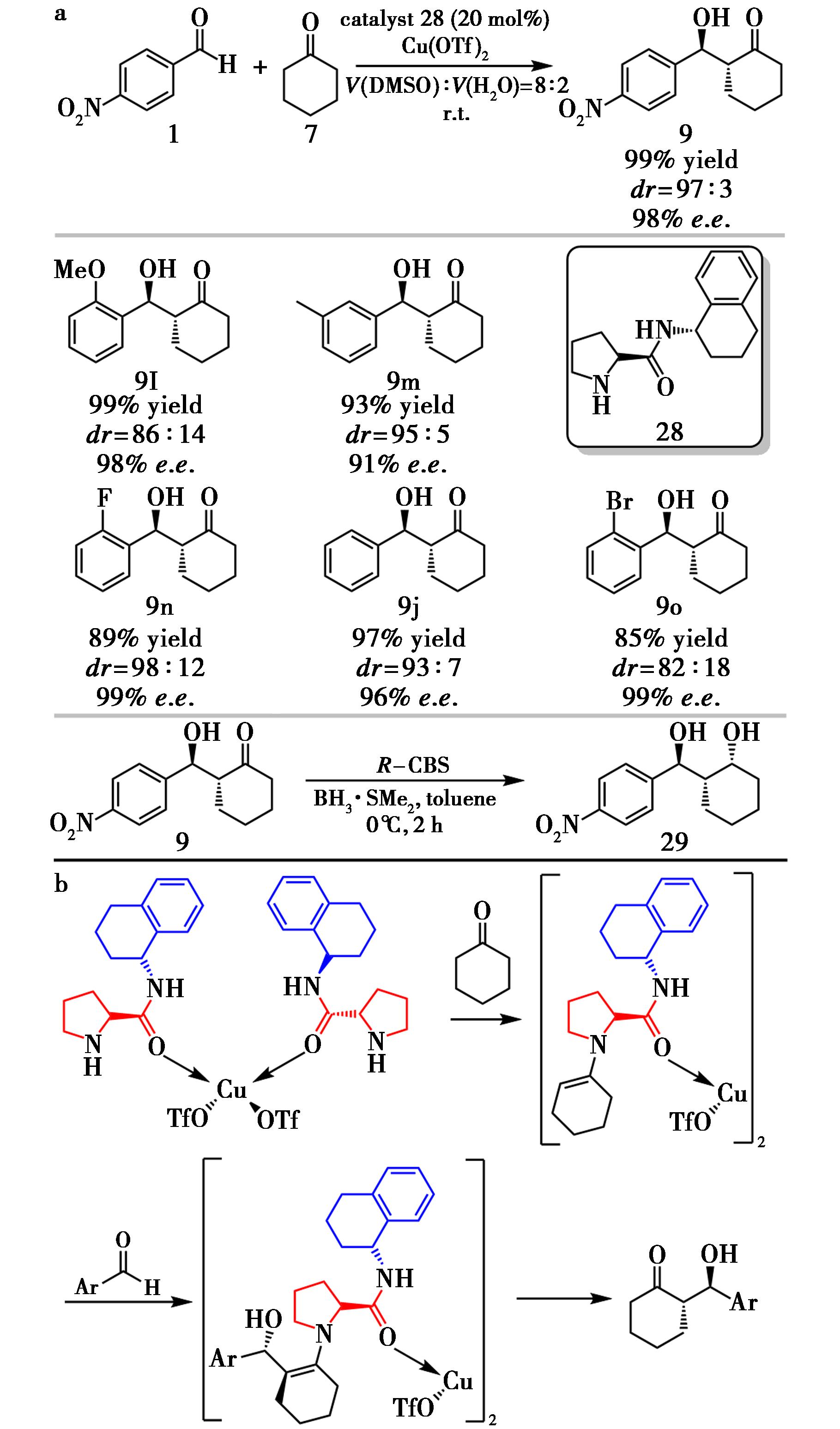
a.催化剂28催化的不对称Aldol反应及CBS还原;b.可能的反应机理
图16 催化剂28催化的不对称Aldol反应及CBS还原[20]
Fig.16 Asymmetric Aldol reaction catalyzed by catalyst 28 and CBS reduction[20]
2025年,Raglione等[21]报道了一类基于胆汁酸和氨基酸的有机催化剂,用于水相中的不对称Aldol反应。胆汁酸部分在水相中提供疏水微环境,氨基酸部分则主导立体选择性控制。在优化条件下,该体系可实现高达99%的收率和77∶23的anti/syn非对映比,但对映选择性仍仅为19% e.e.(图17)。反应后产物可通过乙酸乙酯萃取回收,而水相可直接重复使用5次,活性与选择性基本保持不变,契合绿色化与可持续发展的要求。该工作克服氨基酸催化剂在水中几乎完全失活的局限,让“绿色水相Aldol反应”从不能用变成了能用,但还不够“好用”。通过进一步优化催化剂结构与反应条件,有望提高对映选择性并拓展底物范围。
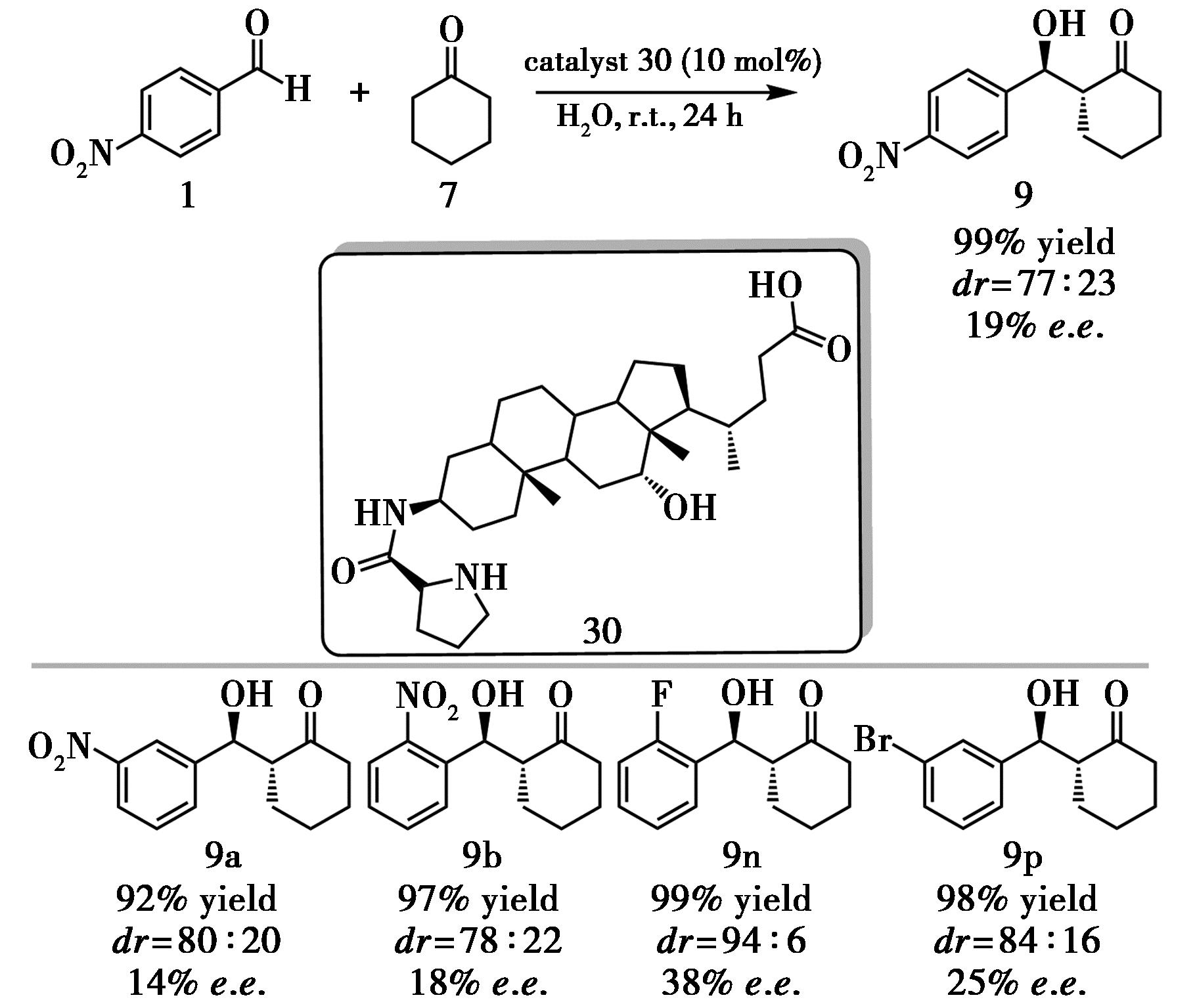
图17 催化剂30催化的不对称Aldol反应[21]
Fig.17 Asymmetric Aldol reaction catalyzed by catalyst 30[21]
Wieland-Miescher Ketone (WMK)是众多天然产物(尤其是萜类和甾体)的关键中间体[22]。2000年,Barbas等[23]实现了S-脯氨酸催化的分子内Aldol反应一锅法合成WMK,但仅能获得S构型产物。2022年,Inomata等[24]设计了新型三胺-吡咯烷手性催化剂,首次实现了R构型WMK的合成(图18a)。研究表明,在无酸条件下产物对映选择性较低(e.e.<25%),随着三氟乙酸(TFA)用量增加,收率与e.e.值先升后降,说明适度质子化是提高立体选择性的关键,而TFA过量则导致催化剂过度质子化而活性下降。作者提出的过渡态模型表明,手性三胺催化剂与三氟乙酸反应生成铵离子,TS-Ⅱ的铵离子上的H在立体结构中与底物羰基氧原子的空间位阻较小,可以形成稳定氢键作用,但由于TS-Ⅰ的立体位阻较大,所以S构型产物的对映选择性低于R构型产物(图18b)。仲胺经质子化形成的铵离子通过单点氢键精细调控立体化学,而叔胺因不能有效形成氢键导致立体选择性丢失。相比之前工作提出的烯胺-羧酸氢键相互作用的模式,文章首次利用侧链胺类型作为立体选择性的控制位点。该工作在构建R构型WMK方面具有开创性意义,但对映选择性中等、底物范围有限且催化剂用量偏高,后续仍需在骨架精修与底物拓展方面持续优化。
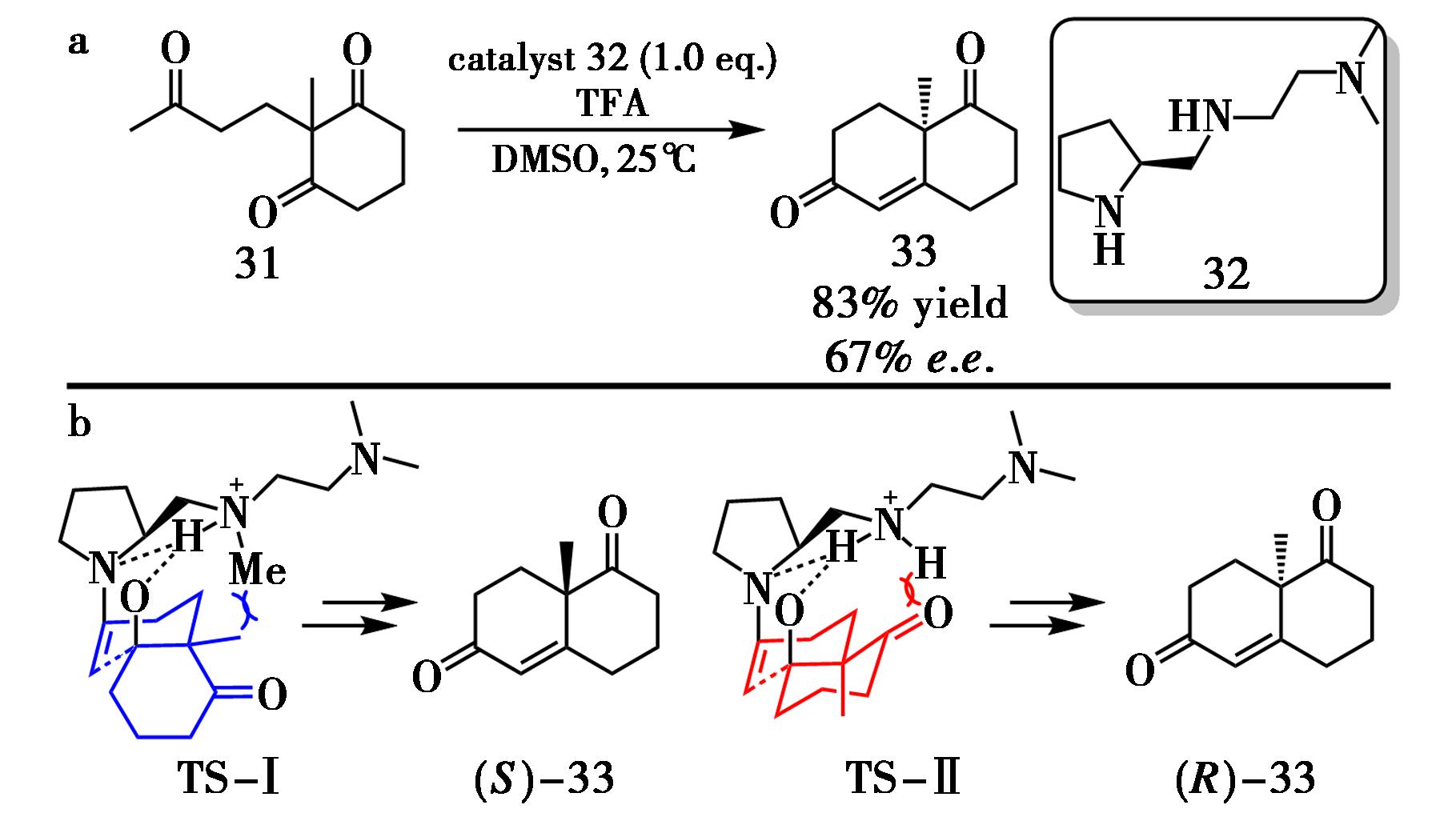
图18 催化剂32催化的不对称Aldol反应(a)及过渡态模型(b)[24]
Fig.18 Asymmetric Aldol reaction catalyzed by catalyst 32 (a) and its transition-state model (b)[24]
小分子手性环己二胺衍生物虽具有高活性与高选择性,但普遍存在用量大和回收困难等问题。Li等[25]于2024年将手性环己二胺引入具有手性放大效应的螺旋聚苯异腈(PPI)侧链,构建了新型可回收有机催化剂。该催化剂在甲醇/苯甲酸体系中对不对称Michael反应可实现97% e.e.,但在Aldol反应中的对映选择性仅为49% e.e.(图19a、19b)。随后,Li等[26]通过在侧链上进一步引入哌啶基团增强供电子能力,并通过溶剂筛选发现乙醇可显著提高反应立体选择性,特别是对邻位三氟甲基苯甲醛底物,e.e.值可提升至87.8%(图19c)。研究表明,邻位体积效应及质子溶剂的氢键作用均有利于提高对映选择性和非对映选择性。该系列工作展示了聚苯异腈骨架在手性信息放大与可回收不对称催化中的潜力,但在保持高e.e.值的同时拓展更广泛的底物范围仍是今后的重要课题。
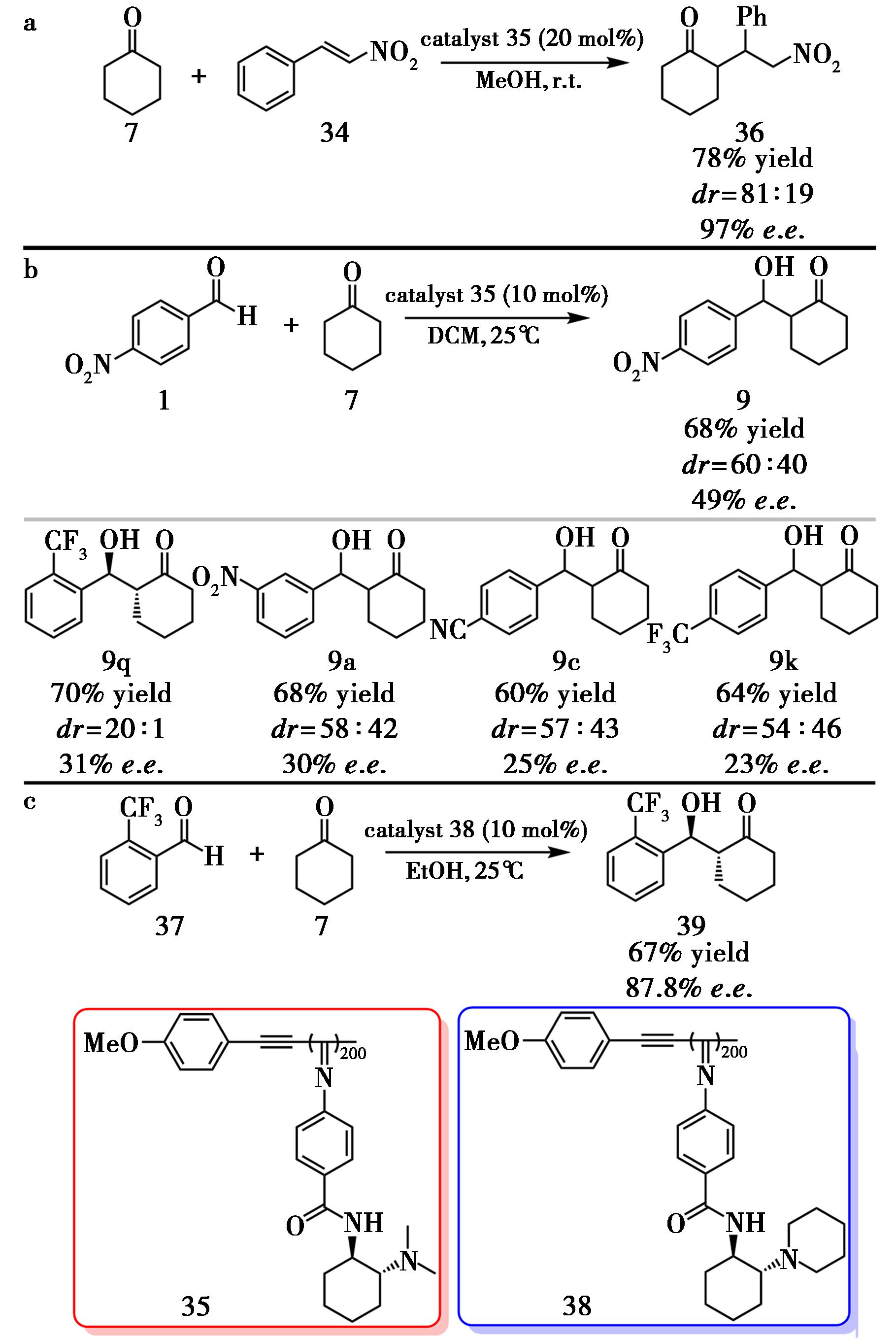
a.环己二胺聚合物35催化的不对称Michael反应;b.环己二胺聚合物35催化的不对称Aldol反应;c.环己二胺聚合物38催化的不对称Aldol反应
图19 环己二胺聚合物催化的不对称Aldol反应及其改进[25,26]
Fig.19 Asymmetric Aldol reaction catalyzed by cyclohexanediamine-based polymers and its improvement[25,26]
1.2 含硫脲结构的小分子催化剂催化的不对称Aldol反应
手性硫脲催化剂因其骨架上具有两个N—H氢键供体位点,能够与底物或中间体形成双重氢键,从而显著活化亲电试剂并通过调控取代基与空间构型实现高水平立体控制,已广泛用于多类不对称反应[27]。近年来,随着对硫脲催化机理认识的深化,其骨架及周边官能团不断被重新设计,从而实现更宽广的底物适用性与更复杂的转化类型。目前,硫脲催化剂大致可分为3类:具有手性环己二胺骨架的硫脲催化剂、具有天然生物碱(金鸡纳碱)骨架的硫脲催化剂,以及最新发展的双功能手性硫脲-胺催化剂。
2022年,Han等[28]报道了紫外光驱动的不对称Aldol反应,用于高效合成手性3-羟基吲哚骨架。该方法以手性胺衍生硫脲为有机催化剂,利用2-烷基苯乙酮(40)在365 nm UV光照下生成ortho-quinodimethane(o-QDM)中间体,随后在硫脲催化剂的氢键活化下与靛红发生vinylogous-Aldol反应,o-QDM从Re面进攻isatin的羰基然后释放催化剂,最终得到S构型3-羟基吲哚产物,在温和条件下即可实现95%收率和90% e.e.(图20)。该工作首次将光生o-QDM中间体引入不对称Aldol型反应,并在克级放大实验中仍保持优良选择性,展现出在天然产物全合成中的应用潜力。
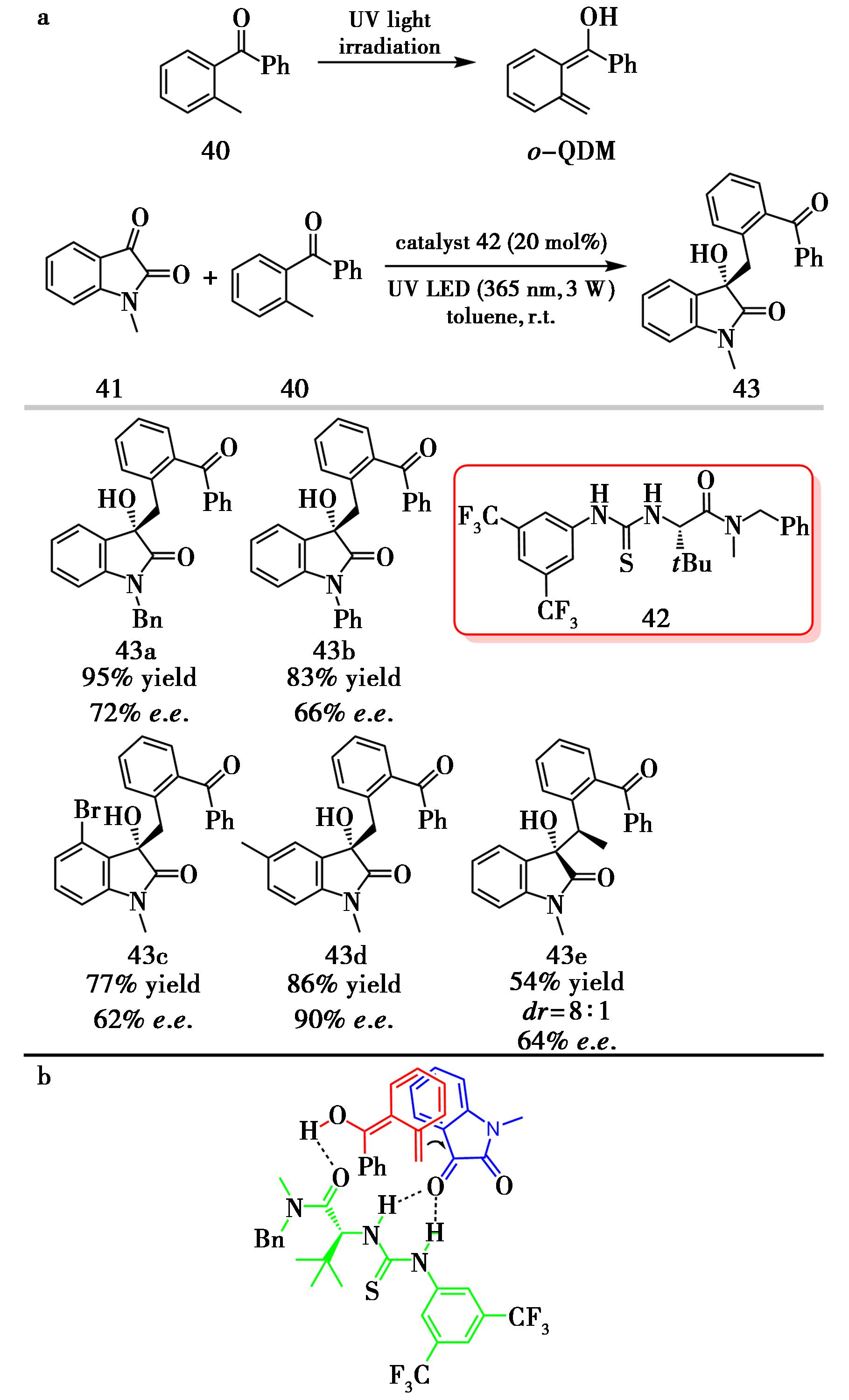
a.o-QDM的形成及催化剂42催化的不对称Aldol反应;b.反应的过渡态模型
图20 o-QDM的形成及催化剂42催化的不对称Aldol反应[28]
Fig.20 Formation of o-QDM and asymmetric Aldol reaction catalyzed by catalyst 42[28]
Mohanan等[29]则开发了Takemoto型硫脲催化的有机催化不对称亚硝基Aldol反应。以α-甲基丙二酰胺(44)为供体、亚硝基芳烃为受体,一步构建含季碳手性中心,并获得高达90% e.e.的N-选择性α-羟胺化产物(图21a)。机理研究表明,硫脲催化剂通过氢键活化亚硝基芳烃并稳定过渡态;丙二酰胺在叔胺碱作用下脱质子生成烯醇负离子,从Re面进攻亲电试剂,得到S构型产物(图22b)。后续在Zn/AcOH条件下还原N—O键,可得到相应的α-氨基酰胺,但e.e.值略有下降。值得注意的是,文章首次以丙二酰胺为供体、商品化Takemoto硫脲催化,实现无金属、高对映选择性构建含季碳的α-羟氨基丙二酸衍生物,但该体系在最优条件下仍需20 mol% Takemoto催化剂,且尚未开展回收与循环使用研究,降低催化剂负载量和解决可回收性仍是未来需要攻克的课题。
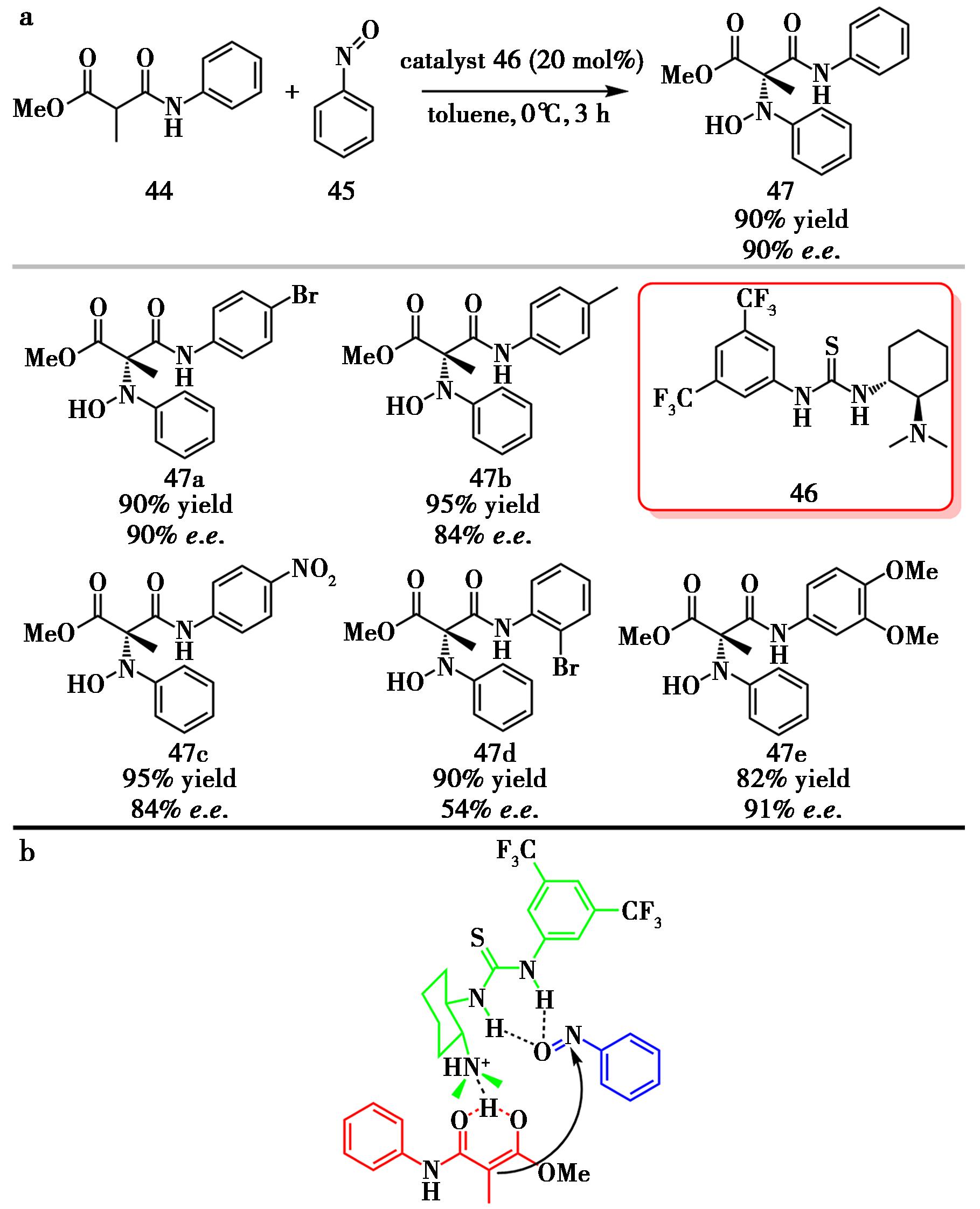
a.催化剂46催化的不对称Aldol反应;b.反应的过渡态模型
图21 催化剂46催化的不对称Aldol反应[29]
Fig.21 Asymmetric Aldol reaction catalyzed by catalyst 46[29]
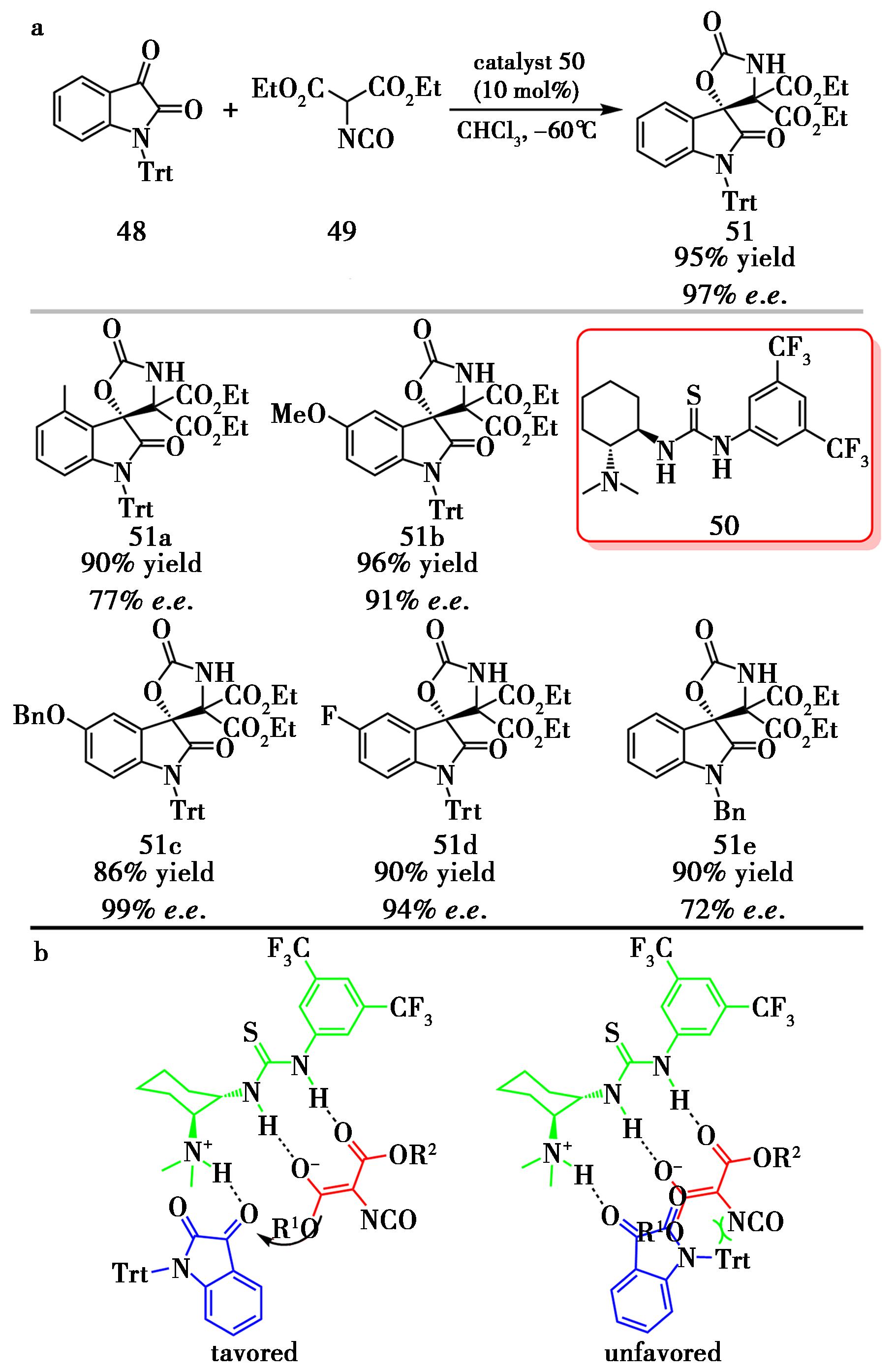
a.催化剂48催化的不对称Aldol反应;b.反应的过渡态模型
图22 催化剂48催化的不对称Aldol反应[30]
Fig.22 Asymmetric Aldol reaction catalyzed by catalyst 48[30]
Chen等[30]设计了一类双功能手性硫脲-叔胺催化剂,用于构建螺环噁唑啉酮-氧吲哚重要骨架。以靛红(48)与2-异氰酸酯丙二酸酯(49)为底物,在温和条件下该体系可通过Aldol/环化串联反应高效构建目标产物,收率达86%~96%、对映选择性72%~99% e.e.(图22a)。机理上,硫脲片段通过氢键活化2-异氰酸酯丙二酸酯生成烯醇中间体,叔胺片段经质子化后与靛红羰基形成氢键,增强其亲电性并控制进攻面,从而得到R构型产物(图22b)。该方法对多种取代靛红和2-异氰酸酯底物均具有良好兼容性,产物进一步官能化过程中对映纯度保持良好,显示出在药物化学与结构多样化方面的应用潜力。
Liu等[31]于2023年首次利用芳香族供体—受体(Donor-acceptor,D-A)相互作用自组装构建协同有机催化体系,并将其应用于水相不对称 Aldol反应。该体系由脯氨酰胺与芳香硫脲通过D-A相互作用自组装而成,相较单一催化剂体系可显著提高收率与对映选择性(96%转化率,92% e.e.,图23)。在添加4-硝基苯甲酸后,反应表现出更高立体选择性和反应速率,表明弱酸性环境通过增强硫脲的氢键供体能力在催化过程中起关键作用。质谱、UV-Vis等表征手段证实了D-A自组装体系的存在和稳定性,动力学研究也显示协同体系具有更高的催化效率,为构建非共价自组装有机催化体系提供了重要范例。
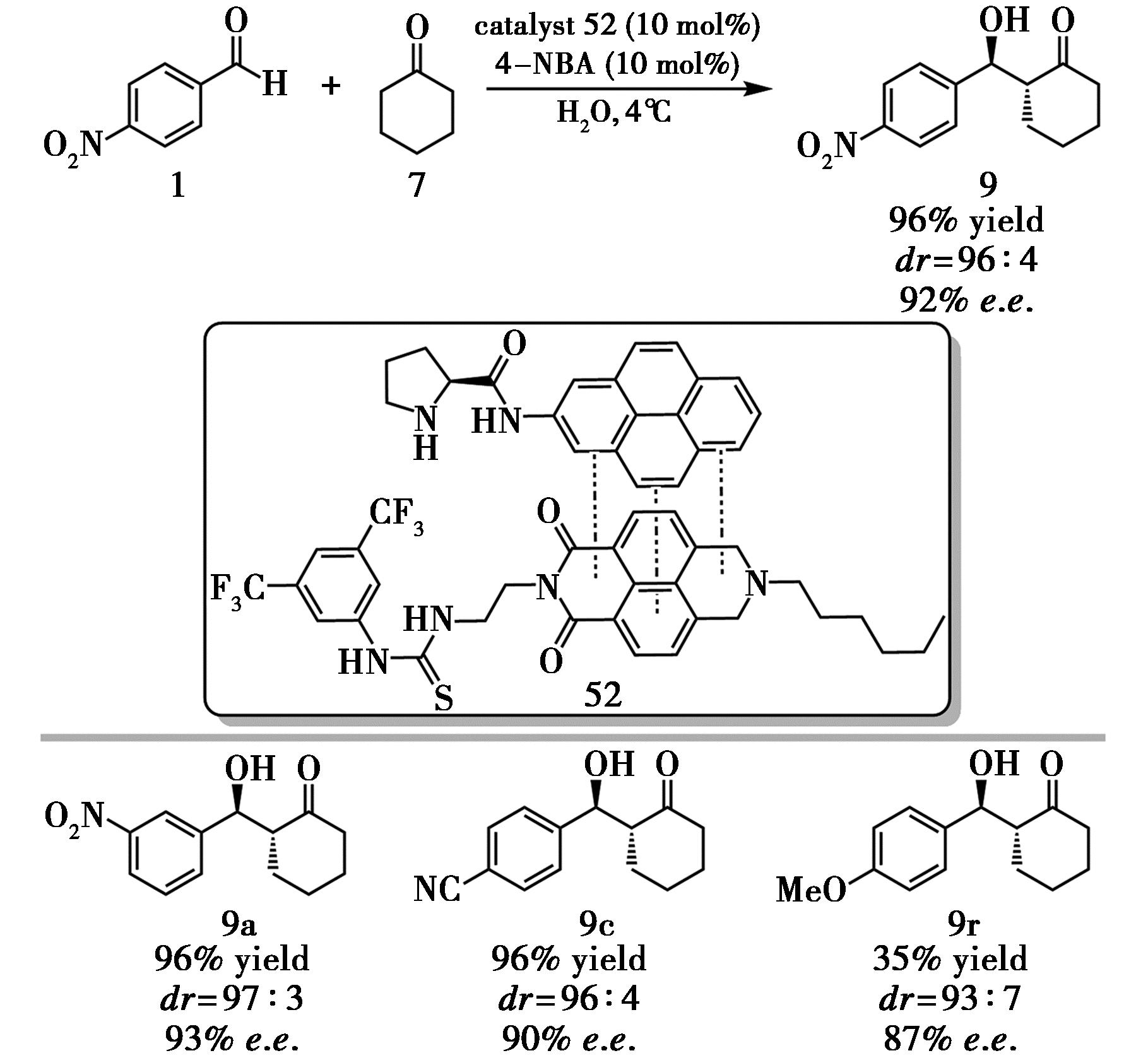
图23 催化剂52催化的不对称Aldol反应[31]
Fig.23 Asymmetric Aldol reaction catalyzed by catalyst 52[31]
1.3 其他有机小分子催化剂催化的不对称 Aldol反应
大环化合物因其刚性骨架与可调控的功能化空腔,在手性诱导和多位点协同催化方面具有独特优势。2024年,Ozgun等[32]首次将手性二氮二氧杂杯[2]芳烃[2]三嗪衍生物应用于不对称 Aldol反应。以对硝基苯甲醛(1)和丙酮(2)为模型反应,在室温、甲苯中该催化剂可实现高达92%收率和89% e.e.的转化(图24a)。低温条件下,虽然某些体系可进一步提升对映选择性,但反应时间明显延长且大环构象刚性过强不利于底物进入空腔。对比实验表明,大环催化剂的活性和选择性均明显优于相应的单体催化剂,进一步证明杯芳烃骨架在构筑手性微环境和调控立体选择性方面的关键作用(图24b)。
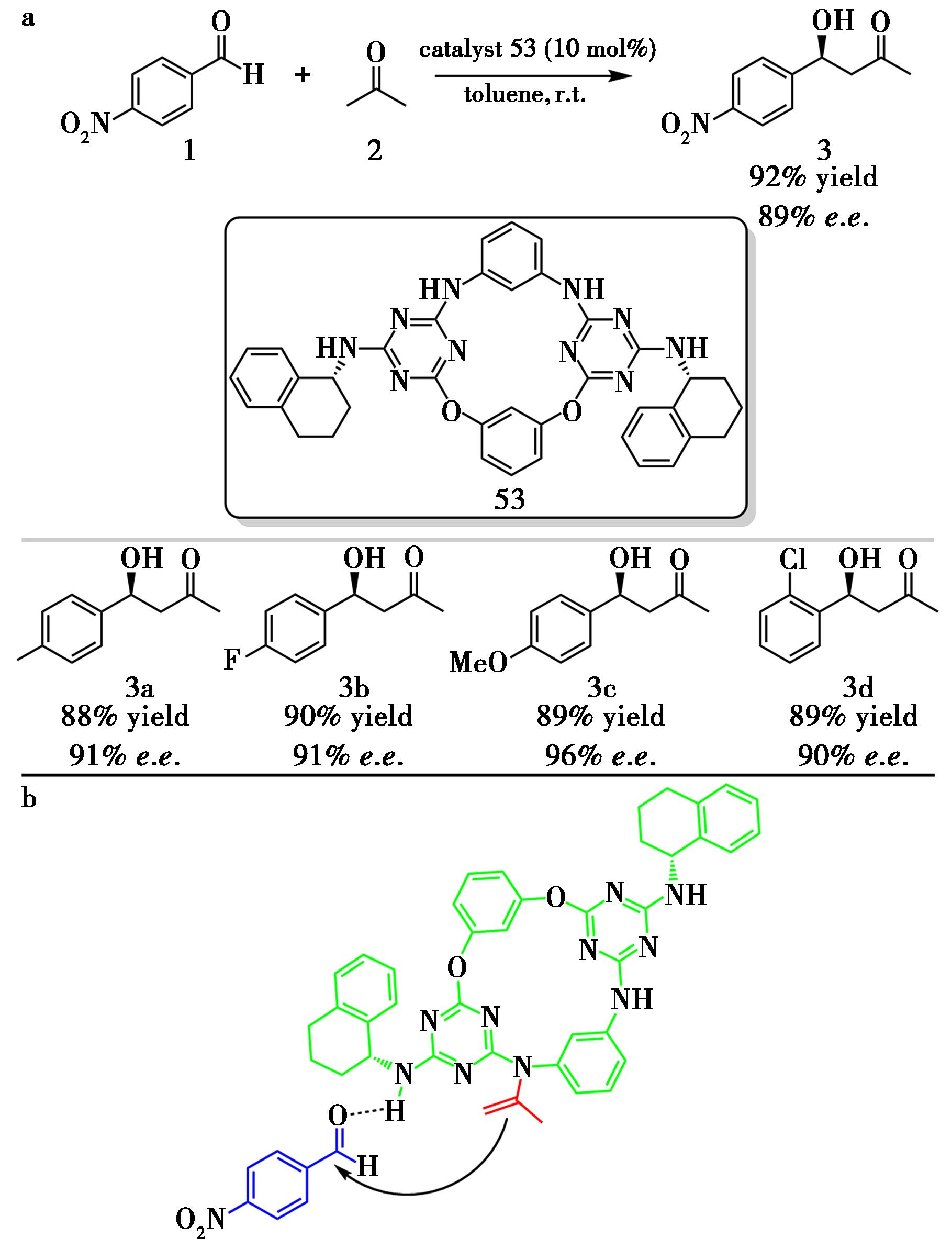
a.催化剂53催化的不对称Aldol反应;b.可能的反应机理
图24 催化剂53催化的不对称Aldol反应[32]
Fig.24 Asymmetric Aldol reaction catalyzed by catalyst 53[32]
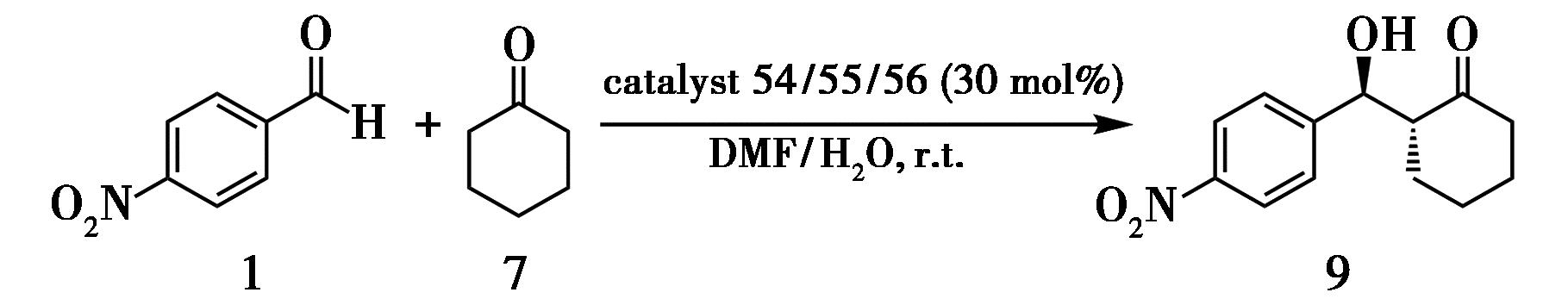
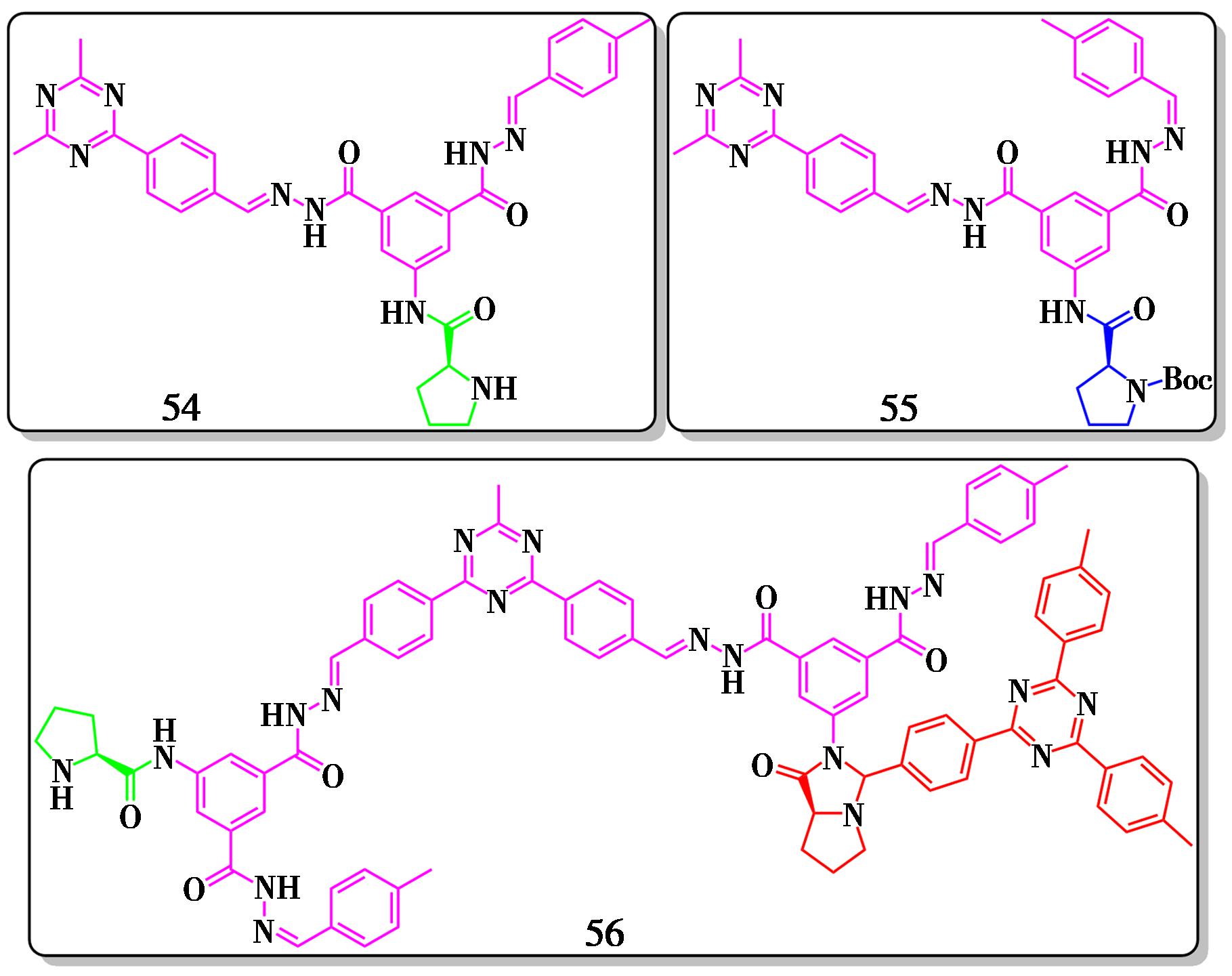
图25 3种不同手性COFs催化的不对称Aldol反应[33]
Fig.25 Asymmetric aldol reactions catalyzed by three different chiral COFs[33]
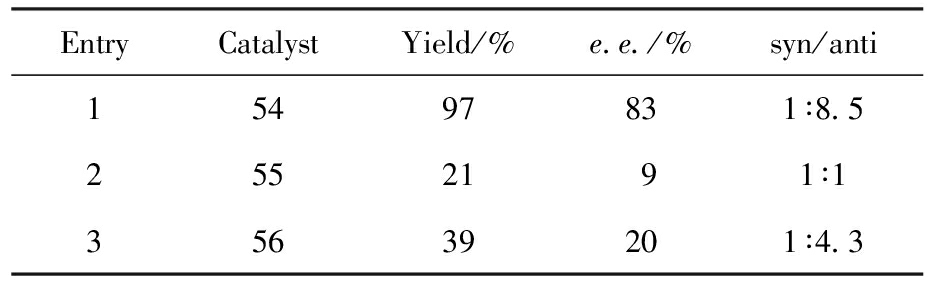
共价有机框架(Covalent organic frameworks,COFs)是一类具有高度有序孔道结构、大比表面积和优良化学稳定性的晶态多孔材料。2024年,Liu等[33]设计并合成了一系列三叶草型、肼键连接的手性COFs,将吡咯烷基团作为活性位点引入框架中。其中,孔道中几乎完全暴露吡咯烷NH位点的催化剂54在对硝基苯甲醛(1)与环己酮(7)的Aldol反应中表现最佳,可实现97%收率和83% e.e.;而在催化剂55和56中,孔道对NH位点完全或部分遮蔽,则收率和对映选择性显著下降(分别为21%/9% e.e.和39%/20% e.e.,表1)。该结果表明,活性位点暴露程度直接决定催化效率和立体控制能力。催化剂54在3次循环使用后仍保持较高结晶度与催化性能,体现了手性COFs在不对称Aldol反应中作为多相手性催化剂的应用潜力。
表1 COFs催化的不对称Aldol反应
Tab.1 Asymmetric Aldol reactions catalyzed by COFs
EntryCatalystYield/%e.e./%syn/anti15497831∶8.52552191∶135639201∶4.3
2 结论与展望
本文围绕近几年有机小分子催化不对称 Aldol反应的研究进展,重点讨论了氨基酸及其衍生物、含硫脲结构有机催化剂以及其他类型有机小分子催化剂在构建手性β-羟基羰基化合物及相关复杂骨架中的应用。总体来看,随着催化剂结构与反应体系设计的不断创新,不对称Aldol反应在催化效率、立体选择性、底物范围以及绿色化程度等方面均取得了显著进展。
在氨基酸及其衍生物催化体系中,脯氨酸骨架通过官能化、固载化、多孔材料化、多肽化以及聚合物化等策略,实现了在水相、无溶剂以及多相体系中的高效催化,显示出良好的可回收性和放大潜力。含硫脲结构的双功能有机催化剂,尤其是与胺功能团协同的体系,在复杂骨架构建(如螺环氧吲哚、季碳中心等)中展现出出色的立体控制能力。大环结构、POCs、COFs、金纳米颗粒以及聚合物纳米粒子等多孔或纳米材料,则为构建可控手性微环境提供了新平台,有助于实现高效、可循环的多相不对称催化。
尽管如此,现有工作仍存在一些共性挑战:1)部分催化体系在实现高对映选择性时需较高催化剂负载,工业化应用仍存在成本与纯化方面的压力;2)许多催化剂对底物电子性质与空间位阻较为敏感,普适性有待进一步提升;3)水相和无溶剂体系虽符合绿色化要求,但在底物溶解度、界面效应和微环境稳定性方面仍有许多基础问题需要深入阐明。
展望未来,有机小分子催化不对称Aldol反应的发展可从以下几个方面持续推进:其一,借助计算化学与机器学习等手段进行催化剂的理性设计和快速筛选,有望加速高性能手性催化剂的发现;其二,与连续流、机械化学、高通量实验等现代工艺手段结合,有助于将实验室方法学更顺畅地推向规模化应用;其三,进一步整合多功能协同催化策略(如氢键/离子对/疏水效应多重协同),在保持高对映选择性的同时兼顾绿色工艺与可回收性。可以预期,有机小分子催化不对称Aldol反应将在药物发现、天然产物全合成以及功能材料构筑中扮演愈发重要的角色。
[1]Koskinen A M P,Karisalmi K.Chem.Soc.Rev.,2005,34(8):677.
[2]Pousse G,Cavelier F,Humphreys L,Rouden J,Blanchet J.Org.Lett.,2010,12(16):3582-3585.
[3]Hajos Z G,Parrish D R.J.Org.Chem.,1974,39(12):1615-1621.
[4]Eder U,Sauer G,Wiechert R.Angew.Chem.Int.Ed.,1971,10(7):496-497.
[5]Al-momani L,Lataifeh A.Ind.Eng.Chem.Res.,2022,61(6):2417-2424.
[6]Lakhani P,Modi C K.Mol.Catal.,2022,525:112359.
[7]Yilmaz D G,Aydogan F,Yolacan C.J.Heterocycl.Chem.,2022,59(7):1169-1179.
[8]Uyanik A,Sahin O,Akceylan E,Eymur S,Uyanik I,Yilmaz M.Russ.J.Gen.Chem.,2022,92(11):2390-2399.
[9]Naeimi S S,Salehi P,Bararjanian M.J.Iran.Chem.Soc.,2022,19(8):3407-3416.
[10]Zalewska K,Zakrzewska M E,Branco L C.Catalysts,2022,12(1):47.
[11]Xu N,Su K Z,El-sayed E M,Ju Z F,Yuan D Q.Chem.Sci.,2022,13(12):3582-3588.
[12]Lv X X,Liu N,Chen F,Zhang H,Du Z H,Wang P,Yuan M,Da C S.Org.Biomol.Chem.,2023,21(43):8695-8701.
[13]Begum Z,Seki C,Okuyama Y,Kwon E,Uwai K,Tokiwa M,Tokiwa S,Takeshita M,Nakano H.RSC Adv.,2023,13(2):888-894.
[14]Hikawa R,Shimogaki M,Kano T.Chem.Commun.,2023,59(54):8424-8427.
[15]Mastai Y,Abuaf M,Das S.RSC Adv.,2023,13(3):1580-1586.
[16]Singh S,Deep A.Chem.Select,2023,8(1):e202202379.
[17]Faragó T,Remete A M,Szatm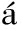 ri I,Ambrus R,Palkó M.RSC Adv.,2023,13(28):19356-19365.
ri I,Ambrus R,Palkó M.RSC Adv.,2023,13(28):19356-19365.
[18]Easwar S,Reddy S R,Kumari K,Bhati M,Madhukar R S,Khan A G H,Janjani P.New J.Chem.,2023,47(36):17042-17050.
[19]Peme T,Brady D,Shumbula N P,Machumele K,Moloto N,Adams T,Makatini M M.Catalysts,2024,14(11):826.
[20]Y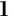 ld
ld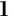 z T,Hasdemir B,Ya
z T,Hasdemir B,Ya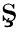 a H,Ba
a H,Ba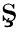 p
p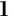 nar K H.ACS Omega,2024,9(8):8913-8921.
nar K H.ACS Omega,2024,9(8):8913-8921.
[21]Raglione V,Palmeri F,Vetica F,D′annibale A.Tetrahedron Green Chem.,2025,6:100086.
[22]Bonjoch J,Bradshaw B.Synlett,2012,3:337-356.
[23]Bui T,Barbas C F.Tetrahedron Lett.,2000,41(36):6951-6954.
[24]Inomata K,Akahane Y.Heterocycles,2022,105(1):566.
[25]Li C L,Zhan M R,Wang Z X,Gao H,Yang Y,Gou H Q.Catal.Lett.,2024,154(4):1420-1430.
[26]Li C L,Lai C Y,Zhan M R,Zhao X N,Dong W Y,Liu J Q,Wang P B.Russ.J.Org.Chem.,2025,61(2):338-345.
[27]Chao Y H,Jamwal P,Ananda R G,Gurubrahamam R,Chen K.Org.Lett.,2024,26(23):4938-4944.
[28]Cao S X,Li J T,Yan T S,Han J,He Z J.Org.Chem.Front.,2022,9(3):643-648.
[29]Gupta E,Vaishanv N K,Kumar S,Purshottam R K,Kant R,Mohanan K.Beilstein J.Org.Chem.,2022,18:217-224.
[30]Chen F E,Xiao Y C,Chen X P,Liu J X,Li H Y.Adv.Synth.Catal.,2022,364:2067-2071.
[31]Meso G,Gregorich D,Waite A J,Smith S,Liu L N,Cortez J,Harris E,Baluyut R D,Correa N,Liang J,Liu Y.ChemCatChem,2023,15(11):e202300012.
[32]Ozgun U,Sirit A,Genc H N.J.Inclusion Phenom.Macrocycl.Chem.,2024,104(11/12):623-632.
[33]Zhang K,Tang X H,Yang X,Wu J L,Guo B Y,Xiao R,Xie Y,Zheng S R,Jiang H W,Fan J,Zhang W G,Liu Y,Cai S L.ACS Appl.Mater.Interfaces,2024,16(8):10661-10670.