丙酮酸及其酯类衍生物作为重要的化工原料和反应中间体,广泛应用于营养剂[1]、化妆、医药[2]、农业、食品等领域[3-5]。目前,丙酮酸及其酯类衍生物的制备方法主要有酒石酸脱羧脱水法、微生物发酵法[6]、1,2-丙二醇氧化法[7]、乳酸氧化法[8]、乳酸乙酯氧化法等[9-11]。其中,乳酸乙酯氧化法中常用氧化剂为高锰酸钾、过氧化氢、氧气等,其中过氧化氢氧化乳酸乙酯生产丙酮酸乙酯,再经连续水解生产丙酮酸,生产效率高、污染小,具有较好的应用前景,现已工业化生产。在丙酮酸的连续生产过程中,需同时关注氧化工段与水解工段的参数变化,需关注中间体丙酮酸乙酯和产物丙酮酸的含量变化趋势,因此需建立一种能同时测定反应液中的丙酮酸和丙酮酸乙酯含量的分析方法。
目前,丙酮酸和丙酮酸乙酯常见的检测方法有紫外分光光度法[12]、气相色谱法[13]、柱前衍生-气相色谱法[14]、超高效液相色谱-串联质谱法[15]等。由于丙酮酸反应液中基质复杂,含有双氧水、丙酮酸、丙酮酸乙酯与乳酸乙酯等,紫外分光光度法、气相色谱法、柱前衍生-气相色谱法不适合丙酮酸与丙酮酸乙酯混合物的测定;超高效液相色谱-串联质谱法的灵敏度高,进样浓度低,反应液的稀释误差较大,且反应液中组分较多,可能会污染质谱检测器。
本研究建立了衍生-HPLC法测定丙酮酸反应液中丙酮酸和丙酮酸乙酯含量。选用抗坏血酸为淬灭剂,在衍生过程中,能够有效防止双氧水破坏丙酮酸与DNPH,无空白干扰;优化衍生温度与时间等因素,选用DNPH为衍生剂,丙酮酸与丙酮酸乙酯衍生产物稳定好,检测灵敏度高;经过色谱条件优化,选用0.1%磷酸溶液+乙腈为流动相,C18柱为洗脱色谱柱,更具有可操作性。经过方法验证,该方法的精密度、准确度与溶液稳定性均良好,可用于工艺开发和生产过程中反应液中常量丙酮酸与丙酮酸乙酯的含量测定。
1 实验部分
1.1 主要仪器与试剂
LC-20AD型高效液相色谱仪(配置紫外可见光检测器,日本岛津公司);HH-4型水浴锅(常州金坛良友仪器有限公司);PRACTUM124-1CNSQP型电子天平(感量0.01 mg,赛多利斯科学仪器(北京)有限公司)。
丙酮酸标准品、丙酮酸乙酯(分析纯,99.0%,上海麦克林生化科技有限公司);2,4-二硝基苯肼(分析纯,98.0%)、L(+)-抗坏血酸(分析纯,99.7%)、磷酸(分析纯,85%)、盐酸(分析纯,36%)(国药集团化学试剂有限公司);乙腈(色谱纯,99.9%,Thermo Fisher(中国)公司);丙酮酸产品过程中的自制反应液样品为实验室合成;溶剂为 V(乙腈)∶V(水)=80∶20。
1.2 实验方法
1.2.1 溶液配制
盐酸溶液的配制:移取50 mL盐酸至100 mL容量瓶中,加水稀释至刻度,摇匀,配制成5.8 mol/L的盐酸溶液。
淬灭剂溶液的制备:称取适量抗坏血酸,加溶剂溶解,配制成10 g/L的VC溶液。
衍生剂溶液的制备:称取DNPH,加乙腈溶解,配制成5 g/L的衍生剂溶液。
混合标准品溶液的制备:称取1.5 g丙酮酸标准品和1.5 g丙酮酸乙酯标准品置于100 mL容量瓶中,加入溶剂溶解,配制成含1.5 g/L丙酮酸与1.5 g/L丙酮酸乙酯的混合标准品储备液;移取1 mL上述配制溶液,置于50 mL容量瓶中,依次加入2 mL淬灭剂溶液、1 mL盐酸溶液与 2.0 mL衍生剂溶液,置于40 ℃水浴中衍生20 min,冷却至室温,再用溶剂稀释至刻度,摇匀,作为丙酮酸和丙酮酸乙酯混合标准品溶液。
混合模拟液的制备:称取丙酮酸和丙酮酸乙酯标准品适量,加入溶剂溶解,配制成丙酮酸含量为20%与丙酮酸乙酯含量为20%的混合模拟液。
空白溶液的制备:量取2 mL淬灭剂溶液、1 mL盐酸溶液与2.0 mL衍生剂溶液,置于 50 mL量瓶中,于40 ℃水浴中衍生20 min,冷却至室温,再用溶剂稀释至刻度,摇匀,作为空白溶液。
1.2.2 色谱分析条件
中谱红RD C18色谱柱(250 mm×4.6 mm×5 μm);柱温35 ℃;检测波长360 nm;进样量 10 μL;流速1.0 mL/min;流动相A为乙腈,流动相B为0.1%磷酸水溶液;梯度洗脱程序:0~12 min,40% A+60% B→85% A+15% B;12~18 min,85% A+15% B→85% A+15% B;18~18.01 min,85% A+15% B→40% A+60% B,18.01~27 min,40% A+60% B。
1.2.3 样品衍生化处理
精确称取0.4 g反应液,置于50 mL容量瓶中,加入溶剂溶解并稀释至刻度;移取1 mL上述溶液,置于50 mL容量瓶中,依次加入2 mL淬灭剂溶液、1 mL盐酸溶液与2.0 mL衍生剂溶液,于40 ℃水浴中衍生20 min,冷却至室温,再用溶剂稀释至刻度,摇匀,作为样品溶液。
2 结果与讨论
2.1 前处理条件的考察
2.1.1 衍生剂的选择与VC的添加
丙酮酸的分子小,极性较大,紫外吸收较弱,直接检测时灵敏度不足,且丙酮酸乙酯在检测时,出现了严重的峰展宽现象,存在包含其他杂质色谱峰的可能性,且与反应原料乳酸乙酯的色谱峰分离度不符合要求(图1)。尝试采用衍生法,采用DNPH作为衍生剂对丙酮酸与丙酮酸乙酯进行衍生,引入强发光基团,提高检测的灵敏度与稳定性。
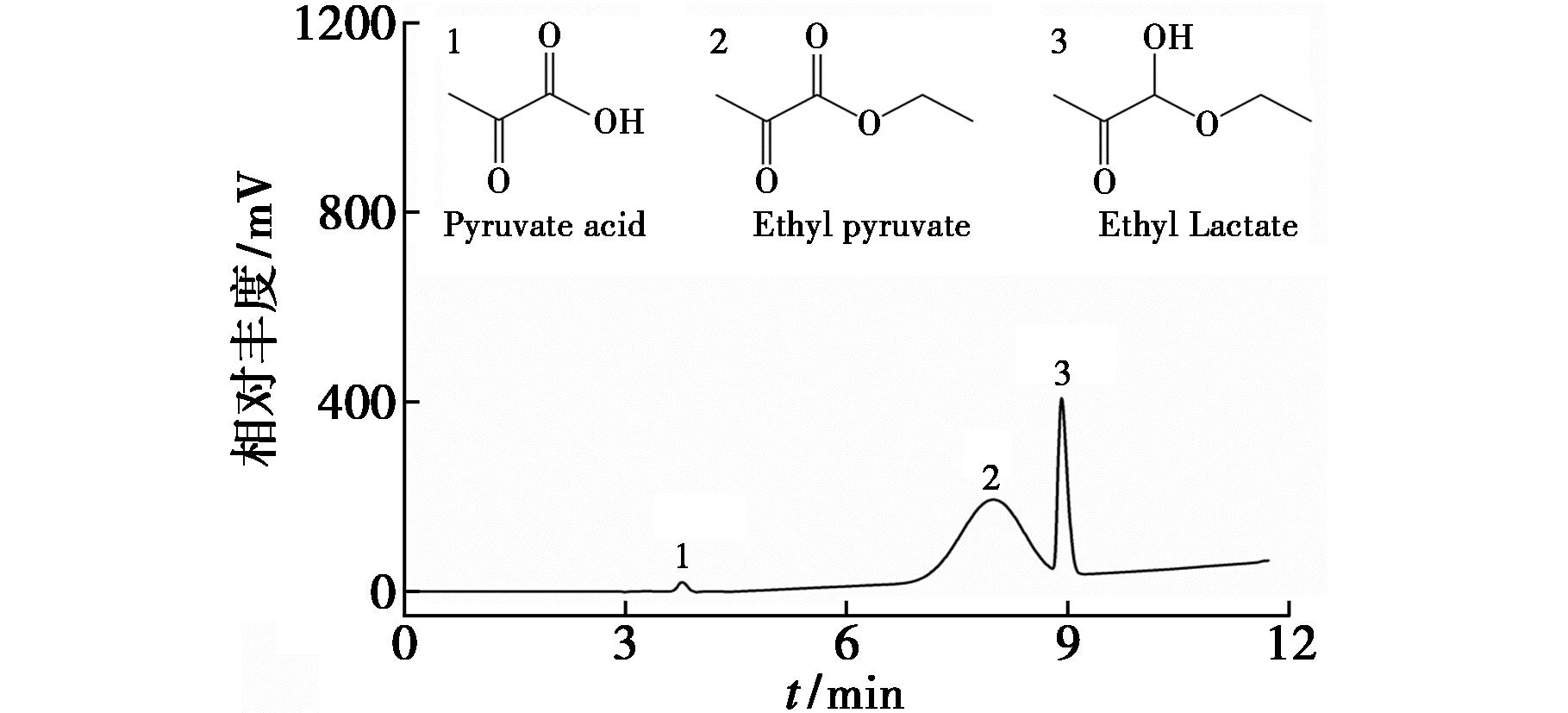
1.丙酮酸;2.丙酮酸乙酯;3.乳酸乙酯
图1 丙酮酸、丙酮酸乙酯和乳酸乙酯混合溶液直接检测色谱图(205 nm)
Fig.1 Chromatogram of a mixed solution of pyruvate,ethyl pyruvate,and ethyl lactate directly detected at 205 nm
在实验过程中,丙酮酸与丙酮酸乙酯的含量测定重现性较差,且色谱峰杂质较多。经过分析发现,丙酮酸生产过程中使用过氧化氢为氧化剂,样品溶液中残留过氧化氢。在丙酮酸与丙酮酸乙酯衍生过程中,过氧化氢会氧化丙酮酸与DNPH,消耗衍生剂产生大量杂质影响测定(图2a)。尝试添加适量还原剂将过氧化氢淬灭以消除影响,考察了10 g/L硫代硫酸钠溶液、10 g/L盐酸羟胺溶液与10 g/L VC溶液,硫代硫酸钠溶液在高比例乙腈溶液中易分层,不能充分混合;盐酸羟胺会与丙酮酸和丙酮酸乙酯发生反应,导致检验结果偏低;用VC溶液做抗氧剂时,丙酮酸和丙酮酸乙酯衍生物的检验结果准确度高且杂质峰干扰少(图2b),空白溶剂无干扰,实验选择10 g/L VC溶液。
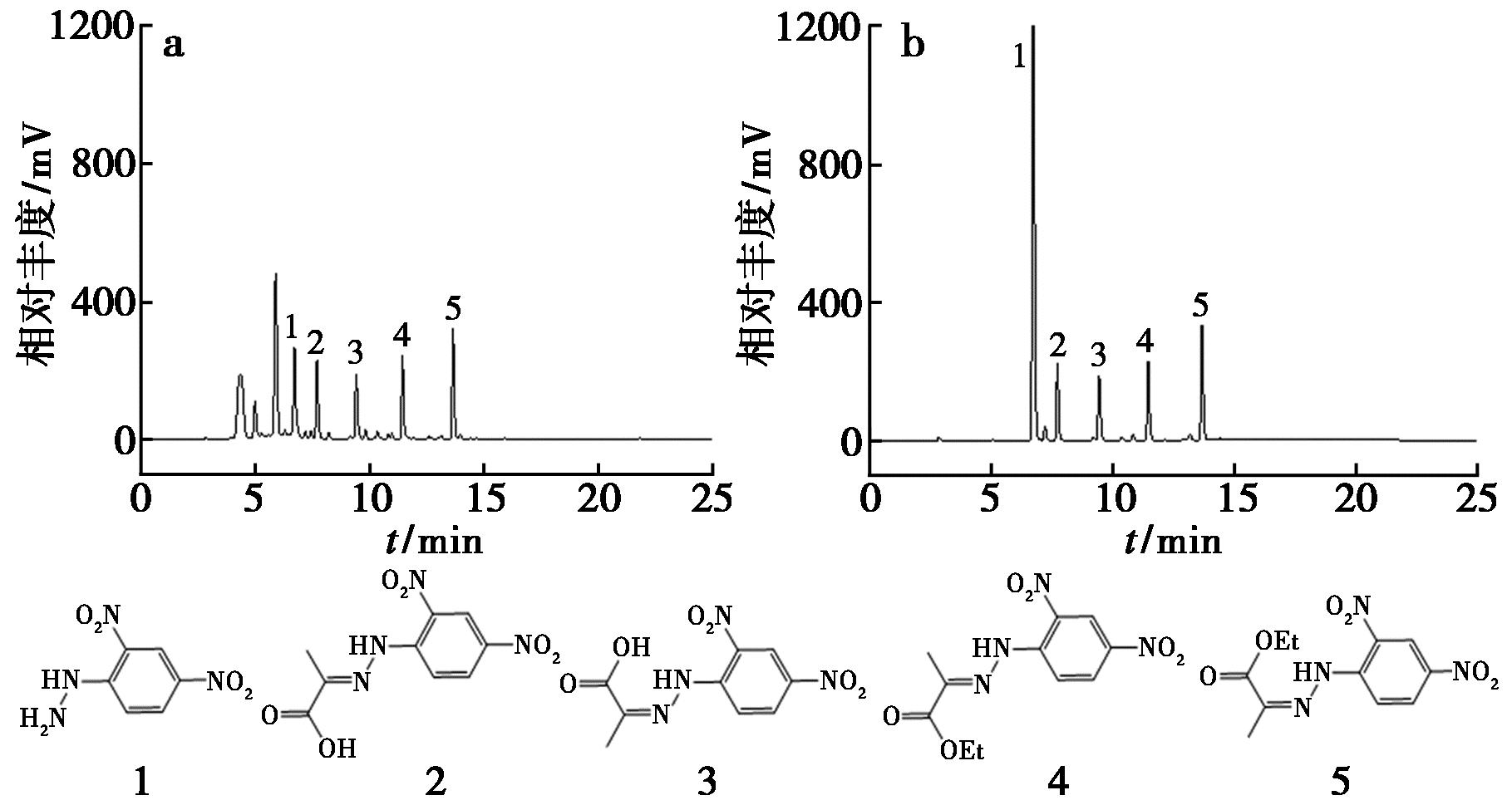
1.DNPH;2与3.丙酮酸衍生物;4与5.丙酮酸乙酯衍生物
a.不添加VC溶液衍生;b.添加VC溶液衍生
图2 样品溶液衍生时VC溶液添加/不添加的对比色谱图
Fig.2 Comparative chromatograms of the sample solution derivatized with or without the addition of VC
2.1.2 淬灭剂、盐酸与衍生剂加入量
2.1.2.1 淬灭剂加入量
推算VC与过氧化氢反应的物质的量比为 1∶1,为保证淬灭效果,前处理时淬灭剂加入量应高于反应液样品中过氧化氢的量。经考察,在现有分析方法条件下,需加入1.5 mL淬灭剂溶液,实验中加入2 mL。
2.1.2.2 盐酸溶液加入量
考察了在碱性、中性和酸性条件下,丙酮酸和丙酮酸乙酯衍生情况。发现碱性和中性环境下,丙酮酸和丙酮酸乙酯几乎未与DNPH反应,丙酮酸回收率低于10%,丙酮酸乙酯回收率低于1%。在酸性条件下,丙酮酸与丙酮酸乙酯的回收率变高,且与酸的种类相关。
酸性条件下,考察了乙酸、盐酸和高氯酸对丙酮酸和丙酮酸乙酯的回收率情况:相同酸量添加下,乙酸条件下丙酮酸回收率约为56%,丙酮酸乙酯回收率仅约为5%,盐酸和高氯酸条件下丙酮酸和丙酮酸乙酯的回收率均在98%~101%之间;可能是乙酸酸性较弱,添加的量未能将羰基完全活化;高氯酸与盐酸的酸性均较强,但高氯酸还具有氧化性,故试验选用盐酸溶液。
试验考察添加不同体积(0、0.2、0.5、1.0、1.5、2.0 mL)盐酸溶液对模拟液中丙酮酸和丙酮酸乙酯的回收率影响,试验结果见图3。当添加盐酸溶液体积低于0.5 mL时,丙酮酸和丙酮酸乙酯的回收率均较低;添加0.5 mL以上盐酸溶液时,目标物组分回收率均大于99.0%;当超过 1.5 mL盐酸溶液时,由于样品溶液酸度过高,导致色谱峰分叉,且衍生完成后需进行pH调节,增加实验步骤,故试验选择加入1.0 mL盐酸溶液。
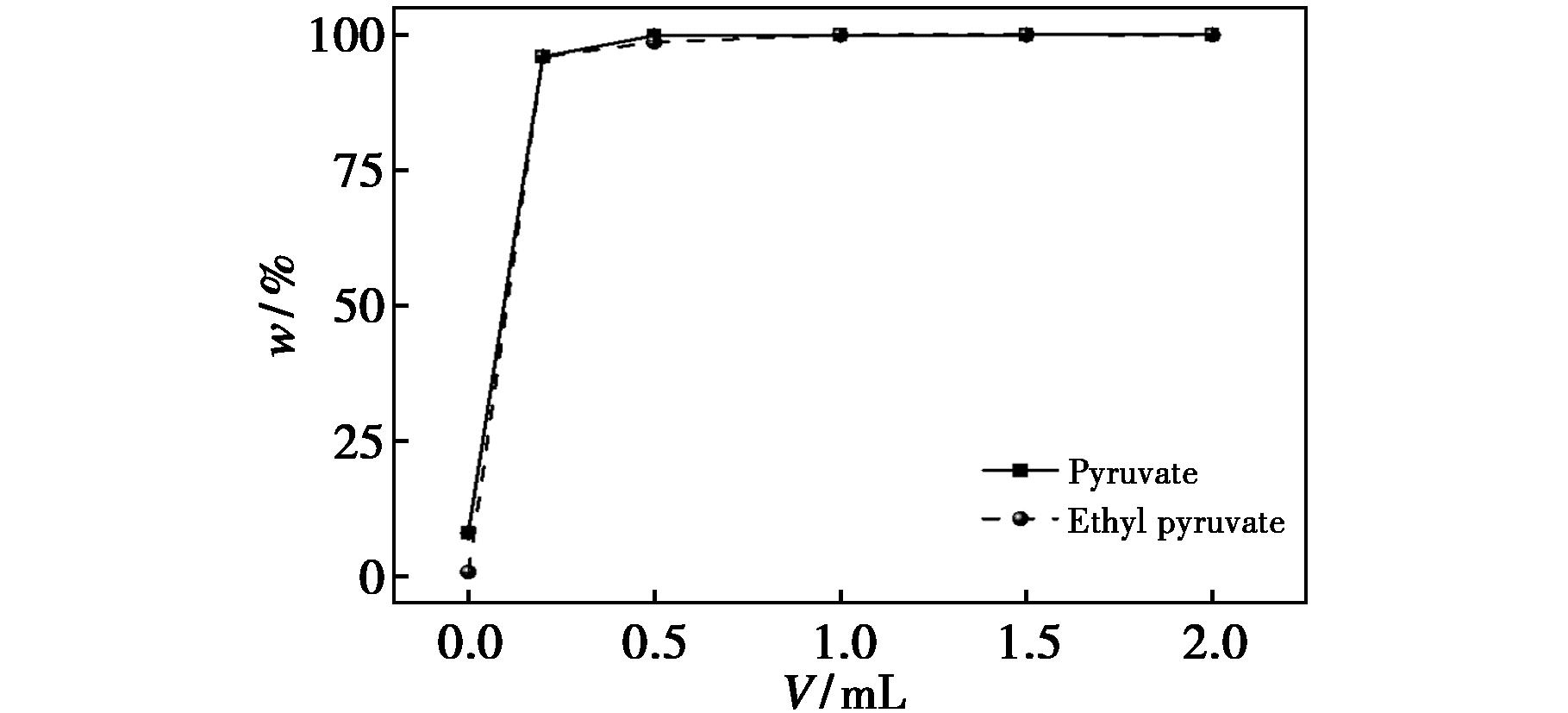
图3 盐酸溶液添加体积与两种组分回收率的关系
Fig.3 Effect of the volume of added hydrochloric acid solution on the recovery rates of the two components
2.1.2.3 衍生剂溶液加入量
在衍生反应过程中,n(DNPH)∶n(丙酮酸与丙酮酸乙酯)=1∶1。考察了衍生剂加入物质的量比对检测结果的影响,分别加入n(DNPH)∶n(丙酮酸与丙酮酸乙酯)=0.4、0.8、1.0、1.2、1.6、2.0的衍生剂溶液时,进行模拟液样品测定,计算丙酮酸与丙酮酸乙酯的回收率。当衍生剂加入物质的量比低于1.0时,由于衍生剂的量不足,导致检验结果偏低;当加入物质的量比>1.2时,衍生剂溶液过量,丙酮酸与丙酮酸乙酯的回收率均高于99.0%,结果见图4,试验选择物质的量比为1.6,即加入2 mL的衍生剂溶液。
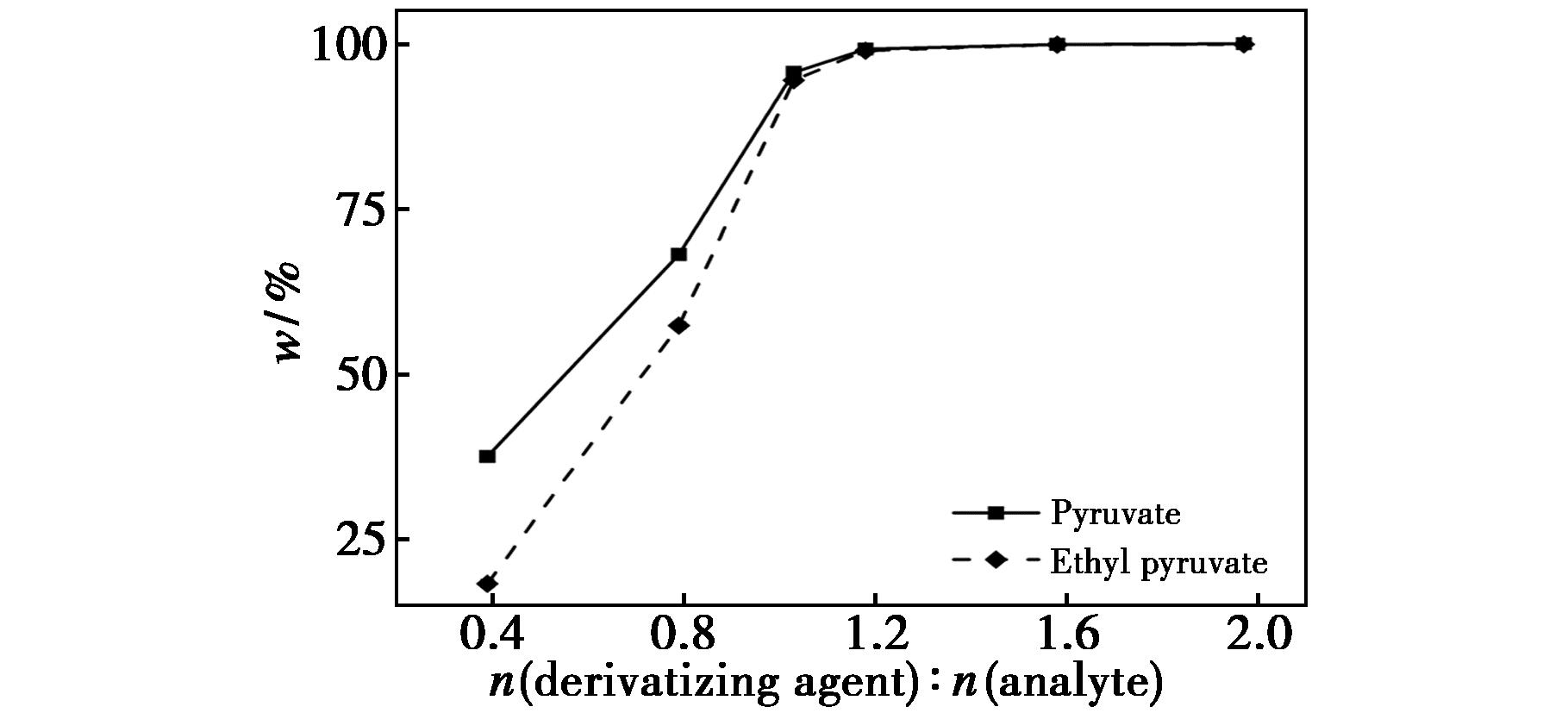
图4 DNPH添加量与两种组分回收率的关系
Fig.4 Effect of the amount of DNPH added on the recovery rates of the two components
2.1.3 衍生温度和时间
试验考察衍生温度对模拟液样品中丙酮酸与丙酮酸乙酯的测定的影响。当衍生时间为20 min时,衍生温度分别为20、25、30、35、40、45、50、55与60 ℃时,丙酮酸与丙酮酸乙酯的回收率测定结果见图5。
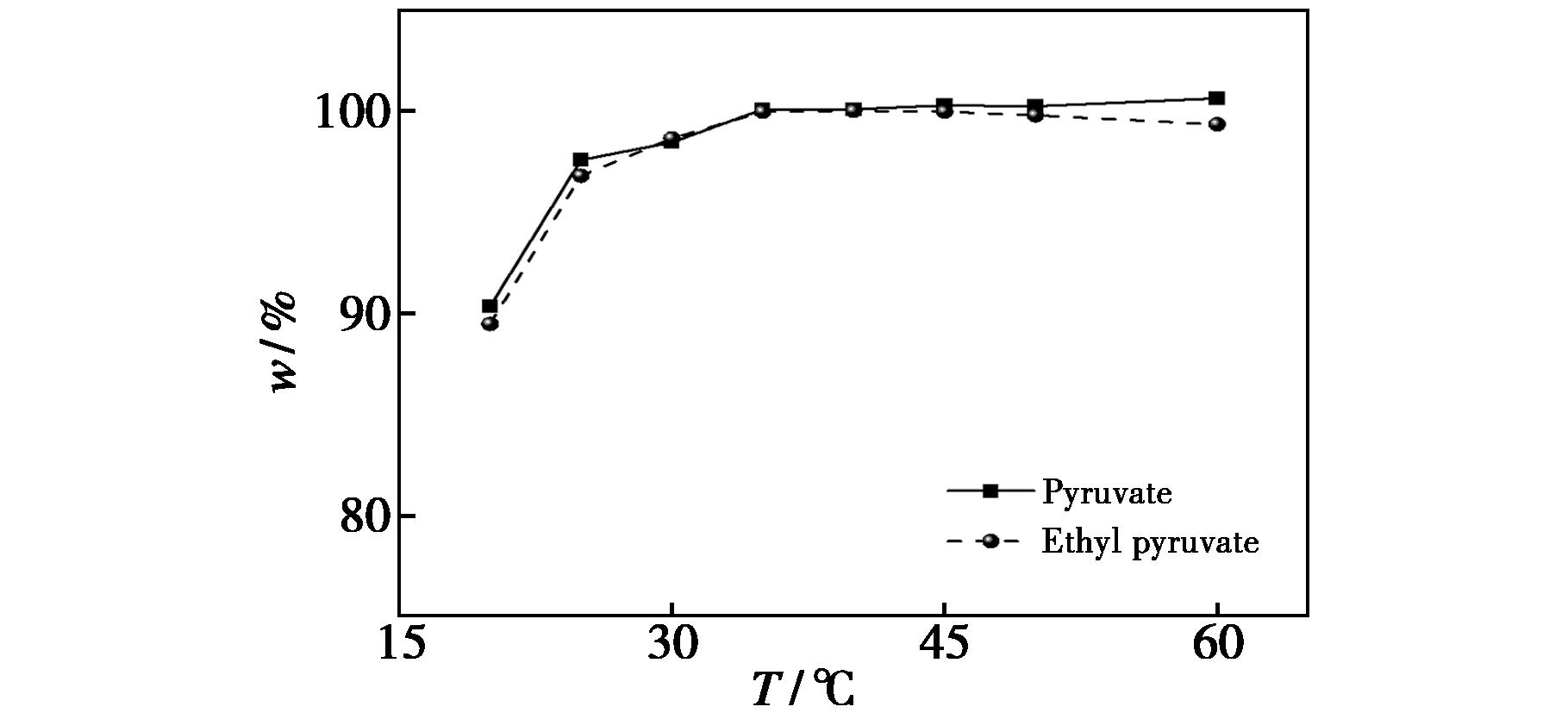
图5 衍生温度与两种组分回收率的关系
Fig.5 Effect of derivatization temperature on the recovery rates of the two components
试验考察衍生时间对模拟液中丙酮酸与丙酮酸乙酯测定的影响。当衍生温度为40 ℃时,衍生时间分别5、10、20、30与40 min,丙酮酸与丙酮酸乙酯回收率结果见图6。
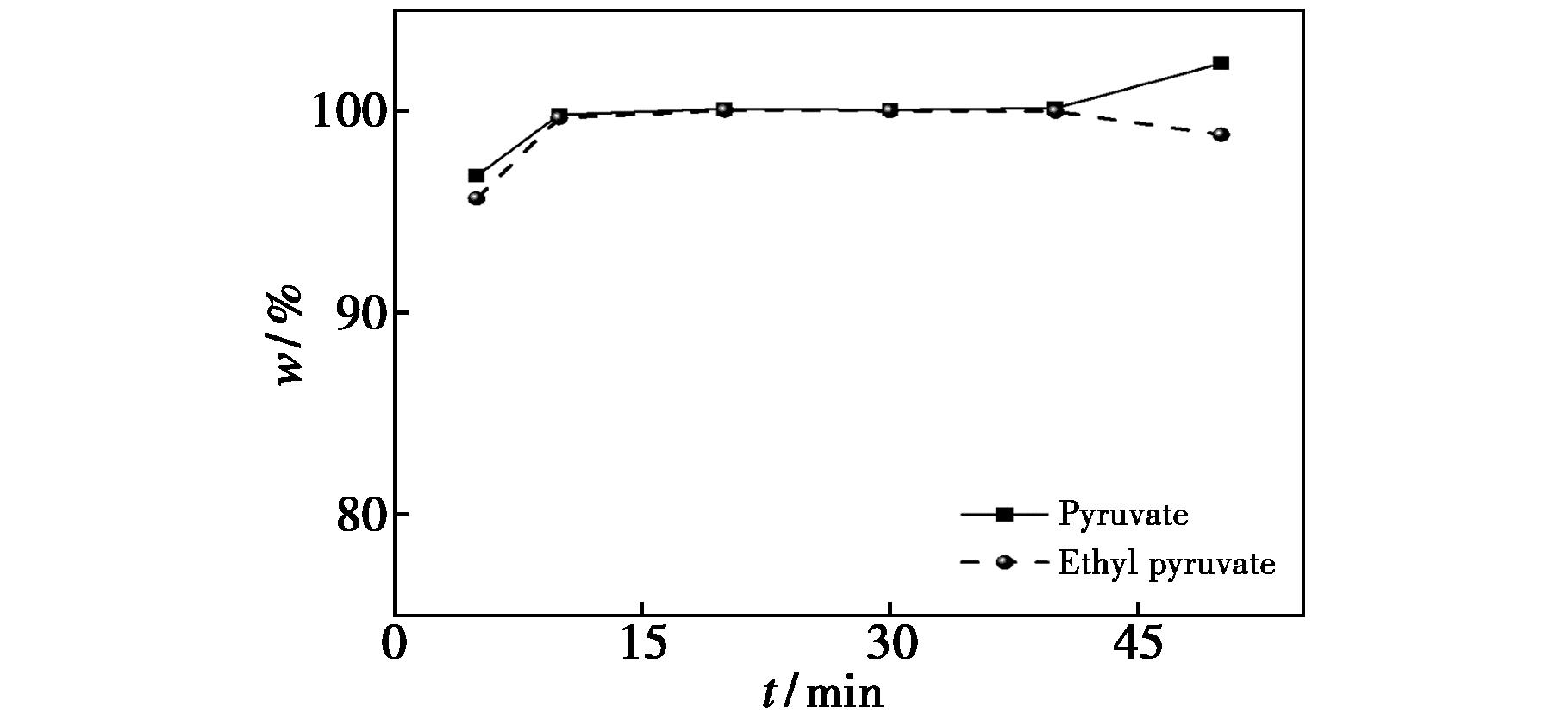
图6 衍生时间与两种组分回收率的关系
Fig.6 Effect of derivatization time on the recovery rates of the two components
由图5、图6可知,当衍生温度低于30 ℃或衍生时间少于5 min时,丙酮酸和丙酮酸乙酯的衍生结果的回收率低于99.0%。在相同的衍生温度下,随着衍生时间的延长,丙酮酸和丙酮酸乙酯的含量测定,与理论值之间的偏差越小,但时间超过45 min时,丙酮酸乙酯会部分水解变成丙酮酸,导致丙酮酸结果偏高;在相同的衍生时间下,随着衍生温度的提高,丙酮酸和丙酮酸乙酯的含量测定,与理论值之间的偏差越小,温度为50 ℃时,丙酮酸乙酯会部分水解变成丙酮酸,导致丙酮酸乙酯测定结果偏低而丙酮酸结果偏高,测定结果偏离真实值;为确保衍生完全,本实验选择衍生时间为20 min与衍生温度为40 ℃。
2.2 色谱条件的优化
2.2.1 检测波长的选择
根据DNPH性质,以及丙酮酸与丙酮酸乙酯衍生物的化合物性质,选择360 nm作为检测波长,有效避开试样中杂质与空白溶剂峰干扰。
2.2.2 流动相和检测条件选择
丙酮酸和丙酮酸乙酯衍生物为两性化合物,其电离形式随着溶液pH变化而变化,因此,考察了不同pH值流动相对丙酮酸和丙酮酸乙酯分离效果的影响。采用水+乙腈作为洗脱体系时,在C18上进行洗脱,丙酮酸乙酯分为两个色谱峰,峰型均较好,而丙酮酸衍生物的色谱峰峰形较差(图7a);采用0.1%磷酸溶液+乙腈作为洗脱体系时,丙酮酸乙酯分为两个色谱峰,丙酮酸为两个色谱峰,且各色谱峰峰形较好、分离度均大于2.0(图7b)。试验0.1%磷酸溶液+乙腈为流动相,C18柱为色谱柱。
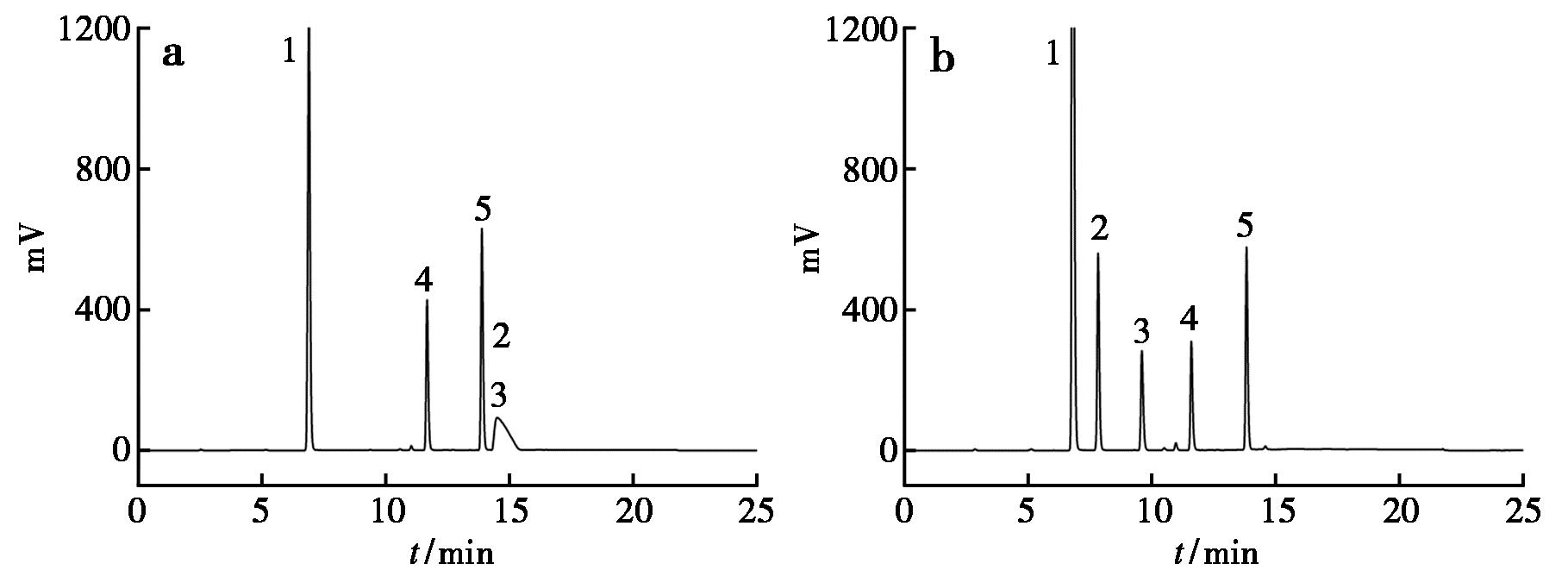
1.DNPH;2与3.丙酮酸衍生物;4与5.丙酮酸乙酯衍生物
a.水-乙腈;b.0.1%磷酸溶液-乙腈
图7 流动相体系的选择
Fig.7 Selection of the mobile phase
2.3 色谱行为
分别量取空白衍生溶液、丙酮酸标准品溶液、丙酮酸乙酯标准品溶液、样品溶液,按照1.2.2色谱分析条件进行测定,试验结果见图8。由于丙酮酸和丙酮酸乙酯与DNPH生成的腙类衍生物存在顺反异构体,在检测时会分别产生两个邻近的色谱峰,反应机理见图9。在定量分析时,需要将这两个峰的面积相加来代表丙酮酸或丙酮酸乙酯的总浓度。由图可知,衍生剂、丙酮酸和丙酮酸乙酯与相邻色谱峰的分离度均大于2.0,达到基线分离,衍生剂和杂质不干扰目标物测定。
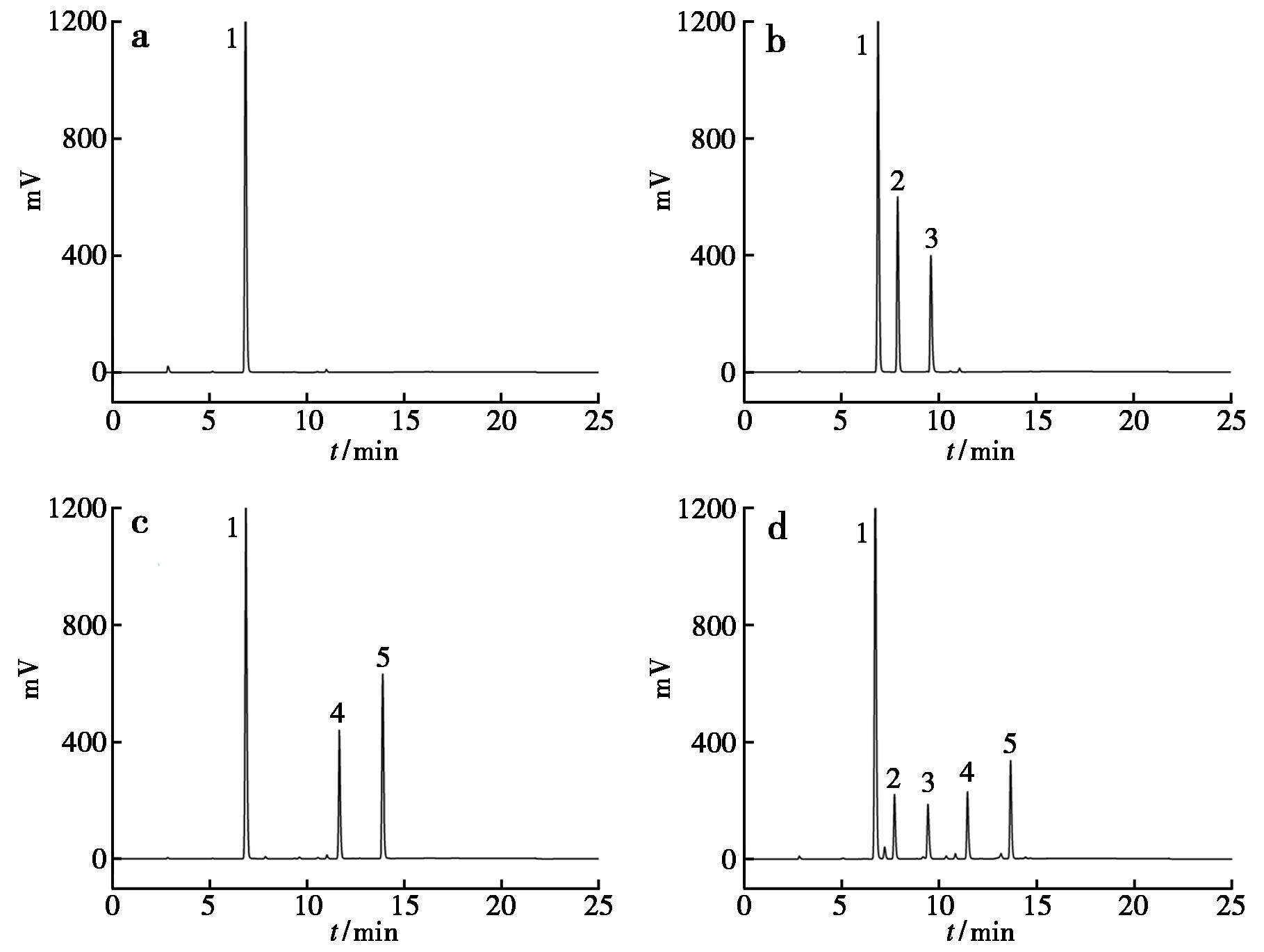
1.DNPH;2与3.丙酮酸衍生物;4与5.丙酮酸乙酯衍生物
a.空白衍生溶液;b.丙酮酸标准品溶液;c.丙酮酸乙酯标准品溶液;d.样品溶液
图8 不同样品衍生后的色谱图
Fig.8 Chromatograms of different samples after derivatization
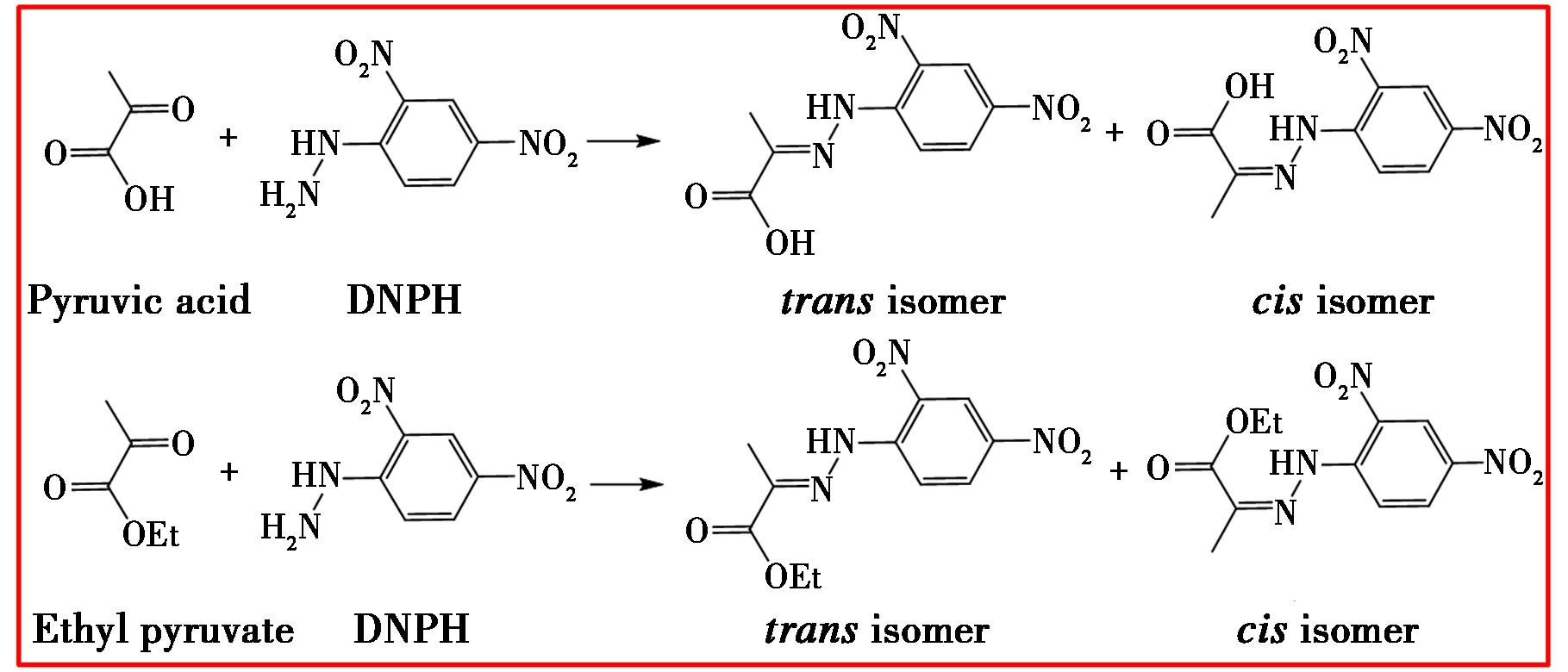
图9 丙酮酸和丙酮酸乙酯与NDPH的反应机理
Fig.9 Mechanism of the reaction between DNPH and pyruvate or ethyl pyruvate
2.4 方法学考察
2.4.1 标准曲线、检出限和定量限
分别移取0.15、0.3、0.6、0.8、1.0、1.2、1.5 mL的混合标准品储备液,置于50 mL容量瓶中,依次加入2 mL淬灭剂溶液、1 mL盐酸溶液与2.0 mL衍生剂溶液,置于40 ℃水浴中衍生20 min,冷却至室温,再用溶剂稀释至刻度,摇匀,作为线性关系溶液。
按照1.2.2色谱分析条件对标准溶液系列进行测定,以各目标物的质量浓度为横坐标,其对应的两个峰面积之和为纵坐标绘制标准曲线,试验结果见表1。结果表明:两种化合物标准曲线的线性相关系数均大于等于0.9998。
表1 两种组分的线性方程、相关系数、线性范围、检出限和定量限
Tab.1 Linear equations,correlation coefficients,linear range,limits of detection and limits of quantification of two analytes

AnalyteLinear equationsR2Linear range/(mg·L-1)LOD/(mg·L-1)LOQ/(mg·L-1)Pyruvatey=130915.9170x+192444.10.99984.50~45.000.003360.0112Ethyl pyruvatey=133585.8896x+4856.81.00004.50~45.000.003870.0129
取最低浓度的标准溶液进行稀释,测定各目标物的检出限与定量限。以3倍信噪比(S/N)和10倍信噪比计算检出限(LOD)和定量限(LOQ),试验结果见表1。
2.4.2 精密度试验
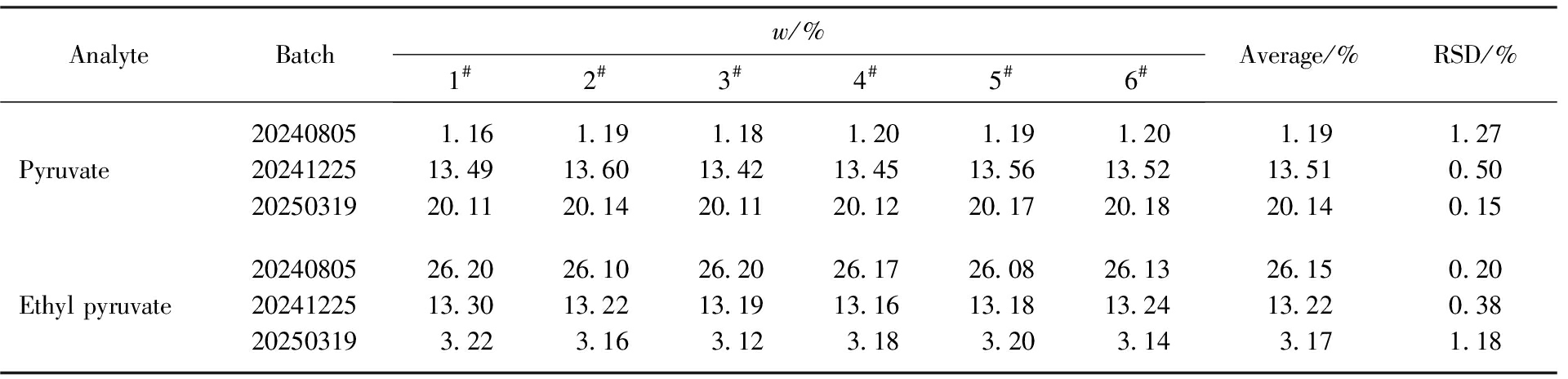
精密移取0.4 g 3批反应液(20240805、20241225和20240319),置于50 mL容量瓶中,加入溶剂溶解并稀释至刻度;移取1 mL反应液,置于50 mL容量瓶中,依次加入2 mL淬灭剂溶液、1 mL盐酸溶液与2.0 mL衍生剂溶液,置于40 ℃水浴中衍生20 min,冷却至室温,再用溶剂稀释至刻度,摇匀,作为样品溶液。按1.2.2色谱分析条件对精密度试验样品溶液进行测定,每批样品平行测定6次,计算各样品的RSD,见表2。
表2 精密度测定结果
Tab.2 Precision results (n=6)
AnalyteBatchw/%1#2#3#4#5#6#Average/%RSD/%Pyruvate2024080520241225202503191.1613.4920.111.1913.6020.141.1813.4220.111.2013.4520.121.1913.5620.171.2013.5220.181.1913.5120.141.270.500.15Ethyl pyruvate20240805202412252025031926.2013.303.2226.1013.223.1626.2013.193.1226.1713.163.1826.0813.183.2026.1313.243.1426.1513.223.170.200.381.18
2.4.3 准确度试验
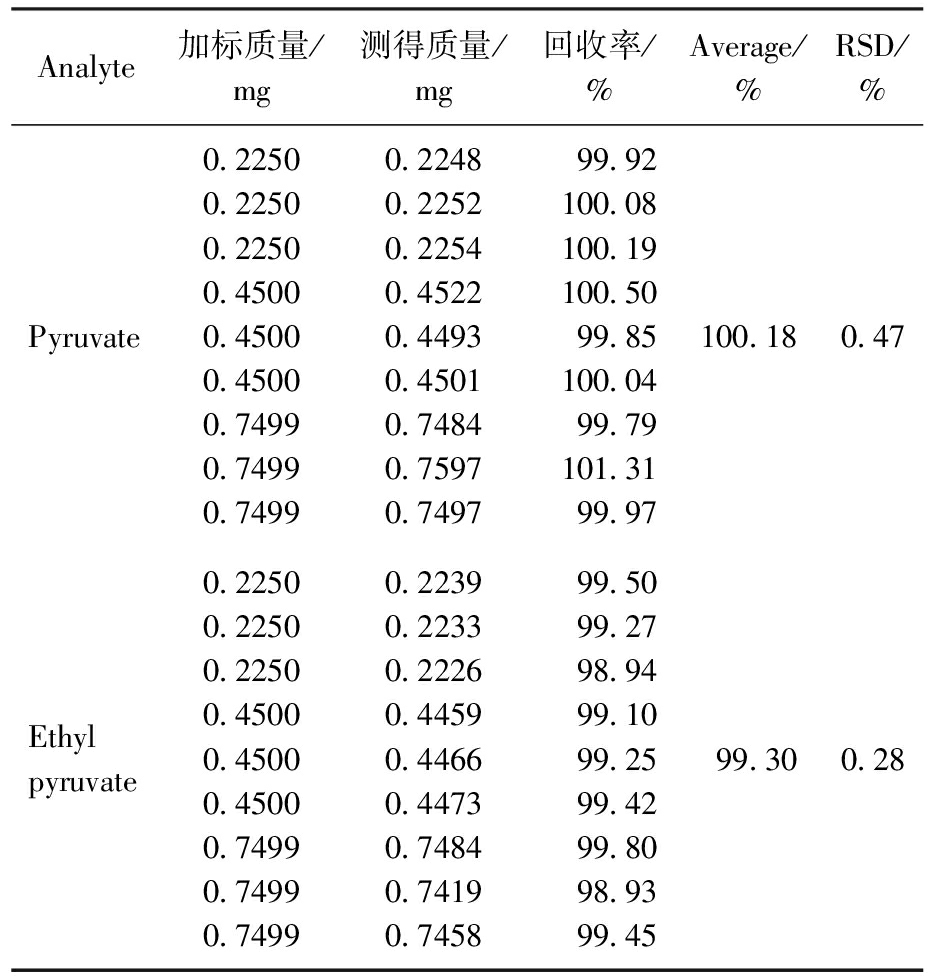
移取0.2 g反应液(20241225,丙酮酸含量13.51%与丙酮酸乙酯13.22%),置于50 mL容量瓶中,加入溶剂溶解并稀释至刻度;移取1 mL反应液,置于50 mL容量瓶中,分别加入0.15、0.3、0.5 mL的混合标准储备液溶液,考察低、中、高3个浓度水平,每个浓度平行测定3次,按试样方法进行衍生,按1.2.2色谱分析条件进行检测,对回收率试验样品溶液进行测定,每个浓度水平平均测定3次,计算回收率平均值和RSD,见表3。
表3 回收率测定结果
Tab.3 Recovery results (n=9)
Analyte加标质量/mg测得质量/mg回收率/%Average/%RSD/%Pyruvate0.22500.22500.22500.45000.45000.45000.74990.74990.74990.22480.22520.22540.45220.44930.45010.74840.75970.749799.92100.08100.19100.5099.85100.0499.79101.3199.97100.180.47Ethyl pyruvate0.22500.22500.22500.45000.45000.45000.74990.74990.74990.22390.22330.22260.44590.44660.44730.74840.74190.745899.5099.2798.9499.1099.2599.4299.8098.9399.4599.300.28
由表2可知,丙酮酸和丙酮酸乙酯的精密度测定结果的RSD均小于1.5%;由表3可知,丙酮酸和丙酮酸乙酯的加标回收率范围分别为99.79%~101.31%、98.93%~99.80%,相对标准偏差RSD均小于0.5%,表明方法的精密度和准确度高,可满足同时检测反应液中丙酮酸和丙酮酸乙酯含量的要求。
2.4.4 溶液稳定性试验
取样品溶液,分别于2、6、12、24、36和48 h时进样检测。按1.2.2条件进行测定,记录丙酮酸和丙酮酸乙酯峰面积的变化情况。
考察了48 h内,样品溶液的稳定性,丙酮酸与丙酮酸乙酯衍生物的峰面积的RSD<1.0%,表明48 h内丙酮酸与丙酮酸乙酯衍生物的溶液稳定性良好,满足测试要求。
2.4.5 样品测定
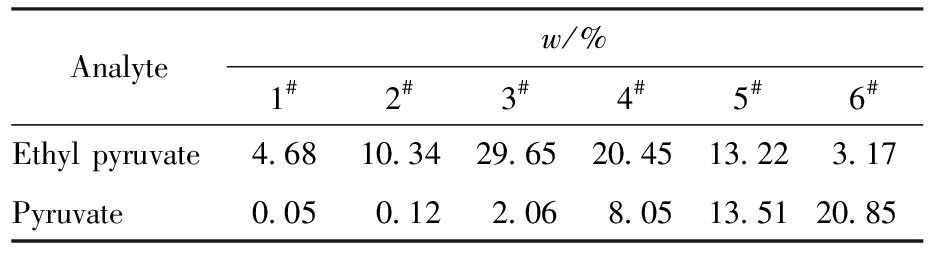
选取一次试验中,不同取样点的反应液,按照1.2实验方法测定丙酮酸和丙酮酸乙酯,结果见表4。由试验结果可知,随着反应的进行,丙酮酸乙酯逐渐增加,同时丙酮酸缓慢增加,丙酮酸乙酯达到峰值;反应逐渐进行,丙酮酸乙酯逐渐降低,丙酮酸逐渐增加,表明丙酮酸乙酯水解后生成丙酮酸。表明该方法能够有效检测反应进程。
表4 样品测定结果
Tab.4 Analytical results of samples
Analytew/%1#2#3#4#5#6#Ethyl pyruvate4.6810.3429.6520.4513.223.17Pyruvate0.050.122.068.0513.5120.85
3 结论
本研究建立了衍生-HPLC相结合同时测定反应液中丙酮酸与丙酮酸乙酯的分析方法。通过优化前处理条件与色谱条件,以DNPH为衍生剂,以VC为淬灭剂,考察衍生温度与衍生时间等因素及检测波长与流动相的pH值等因素,确认了丙酮酸与丙酮酸乙酯检测的分析方法。丙酮酸与丙酮酸乙酯衍生物的线性关系、精密度、准确度与溶液稳定性均符合要求,表明该方法专属性强、灵敏度高、操作简便,方法适用性强,可应用于乳酸乙酯制备丙酮酸反应过程中的反应监控,并为各工段丙酮酸和丙酮酸乙酯产率和转化率的评估提供数据支持,对丙酮酸制备工艺的反应监控和产率情况评估具有指导意义。
[1]Zhou B,Wei Y.Yinshan Acad.J.Nat.Sci.Ed.,2006,20(2):55-57.
周波,魏毅.阴山学刊(自然科学版),2006,20(2):55-57.
[2]Hong H S,Zhou H Y,Zhang Q W,Wang Y L.China Brew.,2008,27(12):10-13.
洪厚胜,周海燕,张庆文,王亚利.中国酿造,2008,27(12):10-13.
[3]Xue J X,Huang K H,Zhang K C.J.Dairy Sci.Technol.,2010,33(3):142-145.
薛俊欣,黄克和,张克春.乳业科学与技术,2010,33(3):142-145.
[4]Shi X R,Zhao H,Zhang H,Li Q F,Lou F M.Chin.J.Anal.Lab.,2024,43(3):314-321.
石晓冉,赵慧,张涵,李群芳,娄方明.分析试验室,2024,43(3):314-321.
[5]Wang W J,Zheng J X.Food Mach.,2005,22(4):69-71,75.
王伟江,郑建仙.食品与机械,2005,22(4):69-71,75.
[6]Qian L L,Na D L,Lan Y F,Hai Z Q,Yu F,Yan L H.Molecules,2023,28(3):1418-1418.
[7]Jin H X,Bai Z L,Zhang Y.Chem.React.Eng.Technol.,2008,24(2):163-167.
金宏轩,柏子龙,张艺.化学反应工程与工艺,2008,24(2):163-167.
[8]Li J,Wang X M,Li C,Zhang W Y.Chem.Reagents,2023,45(10):61-69.
李江,王溪梦,李晨,张文燕.化学试剂,2023,45(10):61-69.
[9]CN201910444802.4.Zhang E F,Wang B C,Wang X B,Li J.2019-07-26.
CN201910444802.4.张恩锋,王炳春,王贤彬,李进,2019-07-26.
[10]Zhang W,Giada I,Marilena F,Enrique V R F,Antonio S E,Wu H H,Fabrizio C,Gadi R,Raveendran S N.Catal.Sci.Technol.,2018,8(15):3737-3747.
[11]Lu P B,Mo F Z.Chem.Ind.Times,2002,(4):48-49.
陆平波,莫芬珠.化工时刊,2002,(4):48-49.
[12]Lou L W,Gao N F.Chin.J.Anal.Lab.,2005,24(4):11-13.
楼良旺,高年发.分析试验室,2005,24(4):11-13.
[13]Tao G Z,Guo Y,Lu G Z,Wang Y Q,Guo Y L,Zhang Z G,Wang Y S,Liu X H.Chin.J.Anal.Chem.,2007,35(3):447-450.
陶国忠,郭耘,卢冠忠,王艳芹,郭杨龙,张志刚,王筠松,刘晓晖.分析化学,2007,35(3):447-450.
[14]Zhang H Y.Derivatization Gas Chromatography Methods for the Detection of Lactic Acid and Pyruvic Acid in Biological Samples.Shijiazhuang:Hebei Medical University,2019.
张铧尹.衍生气相色谱法检测生物样本中乳酸丙酮酸的新方法研究.石家庄:河北医科大学,2019.
[15]Jin S M,Wang Y N,Liang R Q,Liu T T,Cao J.J.Food Saf.Qual.,2024,15(24):139-144.
金绍明,王耀楠,梁瑞强,刘彤彤,曹进.食品安全质量检测学报,2024,15(24):139-144.