微塑料(Microplastics)是一种新型全球环境污染物,其粒径通常<5 mm,形态包括塑料微粒、纤维或碎屑等。根据来源,微塑料可分为初生微塑料(生产过程中直接排放)和次生微塑料(由塑料制品经物理化学作用分解形成)[1,2]。这类污染物在水体环境中分布广泛,我国长江流域、东海沿岸、南海及渤海滨海区域等多个水域均存在显著的微塑料污染[3]。研究表明,长江流域原水中微塑料含量可达(6614±1132)个/L[4,5],三峡库区地表水中微塑料丰度在(1597~12611)个/m3之间[6,7],充分反映了当前水环境中微塑料污染的严峻形势。
微塑料因其特殊的理化特性,在自然环境中难以降解,其潜在生态风险主要体现在以下几个方面:首先,微塑料表面粗糙且富含官能团,能吸附重金属离子、抗生素及持久性有机污染物等有毒物质,成为这些污染物的迁移载体[8];其次,微塑料可通过水生生物(如浮游动物、鱼类)误食等途径进入食物链,在生物体内积累并通过营养级传递产生生物放大效应,最终对生态系统稳定性和人类健康构成长期威胁[9];此外,微塑料制造过程中添加的双酚A、邻苯二甲酸酯类等内分泌干扰物,在老化过程中会逐渐溶解释放,可能破坏生物体的正常内分泌功能,从而增加其环境风险[10-12]。因此,研究对水体中微塑料的去除具有重要的意义。
生物炭是由生物质(如农作物秸秆、木屑、城市污泥等)在厌氧或限氧条件下经热解转化制备的一种富碳材料[13,14]。其独特的孔隙结构和丰富的表面官能团,使其在环境污染治理领域表现出优异的吸附性能和应用前景[14]。生物炭能够通过多孔结构的物理截留和表面官能团的化学作用富集污染物,同时具有成本低廉、环境相容性好等优点,有作为高效吸附剂的潜力[15]。然而,未经改性的原状生物炭在吸附微塑料方面存在明显不足:孔隙结构单一、比表面积有限,难以有效截留不同粒径的微塑料颗粒;同时,其表面活性位点种类单一,与微塑料之间的相互作用力较弱,导致吸附效率低下且选择性不足[16]。
为克服原状生物炭的性能缺陷,研究者们探索了多种改性策略。主要是通过化学或物理方法对生物炭进行改性,可以优化其孔隙结构、调控表面电荷、引入特异性官能团,从而显著增强对微塑料的吸附效能[17]。例如,金属离子改性可调节生物炭表面电荷,增强对带电微塑料的静电吸引[18];磁性改性则使生物炭能够借助外部磁场实现快速分离,提高了材料的回收利用率[19]。因此,对改性生物炭的研究具有重要的科学与应用价值,可有力推动水环境中微塑料的污染治理技术发展。
本文旨在系统梳理改性生物炭去除水体中微塑料的研究进展,重点阐述其功能化改性方法,深入分析吸附机制,探讨关键影响因素,并对其再生技术及实际应用挑战进行展望,以期为该领域的深入研究与工程实践提供理论支撑。
1 生物炭去除微塑料的改性方法
原状生物炭对微塑料的去除效果常受限于其单一的孔隙结构和不足的表面活性位点。通过物理和化学改性手段,可显著优化生物炭的比表面积、孔隙结构、表面官能团及电荷特性等理化性质,从而提升其对水体中微塑料的吸附能力。改性方法主要分为化学改性和物理改性两大类。
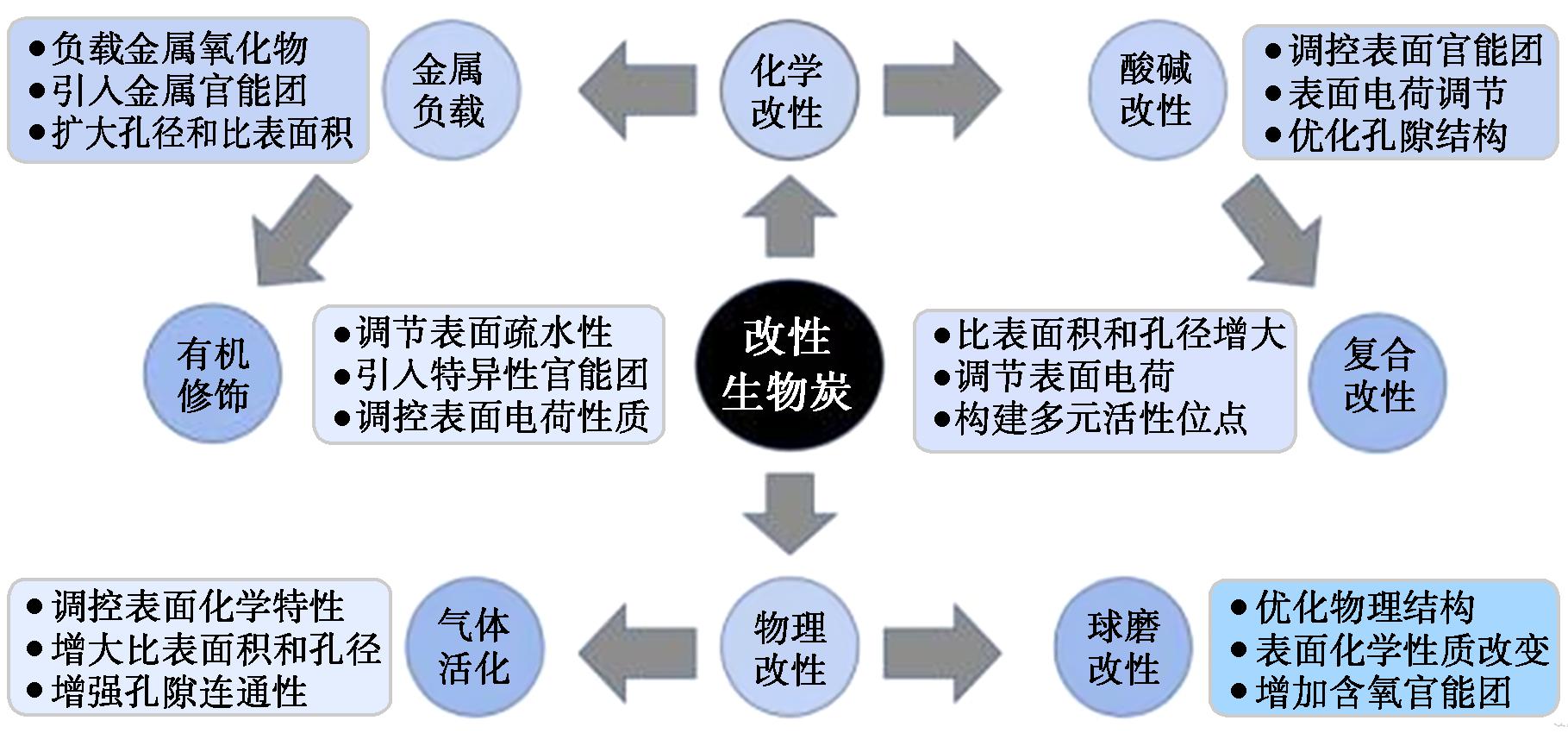
图1 生物炭改性方法
Fig.1 Modification methods of biochar
1.1 化学改性
化学改性是通过引入外来物质或与化学试剂反应,改变生物炭表面化学组成的有效方法。
1.1.1 金属负载
金属负载改性是通过在生物炭表面负载金属或其氧化物(如铁、镁、锌等),利用金属离子与微塑料表面的含氧官能团形成配位键,以及金属氧化物的表面活性来提升吸附效率。
有研究通过Fe3O4负载制备磁性生物炭,发现对1 μm粒径的聚苯乙烯(PS)微球的去除效率达到94.81%。该材料的高效吸附性能主要归因于:Fe—O活性位点与微塑料表面基团之间的静电相互作用;Fe3O4与聚合物分子间的络合效应[18]。此外,经磁化改性的生物炭能够在外加磁场作用下,实现快速分离与回收,解决了传统生物炭回收困难的问题[20]。
也有研究采用Fe3O4改性丝状藻类生物炭,发现改性可以负载磁性纳米颗粒Fe3O4,并通过水热法显著提升比表面积(47.95 m2/g,较原状生物炭增加206%)和孔隙体积(0.0359 cm3/g),对1 μm PS微球的吸附容量达215.58 mg/g,其表面羟基(—OH)数量增加,并通过氢键作用强化对微塑料的捕获,同时还通过络合和静电相互作用进一步提升吸附性能[21]。
还有研究采用Fe/Ni改性生物炭,发现改性可以负载金属,并提高比表面积(较未改性生物炭增加139%,达到45.94 m2/g)和改善孔隙结构。改性生物炭对PS微塑料的最大吸附量为8974.40 mg/g,是单金属Fe改性生物炭的3.43倍[19]。Wang等[18]也研究发现Fe/Mg和Fe/Zn改性生物炭对PS的吸附率分别达到98.75%和99.46%,优于单一Fe改性,其中Mg、Zn的引入使生物炭表面形成更多的金属氧化物(如Mg(OH)2、ZnO),以及金属离子的负载减少了对生物炭微孔的堵塞,提高了比表面积,有利于微塑料颗粒的扩散与截留,而单一Fe改性可能因Fe3O4颗粒部分阻塞孔隙。
1.1.2 酸碱改性
酸碱处理可引入含氧官能团并优化孔隙结构,从而提升吸附性能。酸处理通过质子化作用引入大量羧基、羟基等酸性官能团,增强生物炭表面的亲水性和电荷密度;碱处理则通过脱除生物炭表面的杂质和部分无定形碳,扩大孔径并增加孔隙体积[22-24]。
有研究用盐酸、磷酸等酸对生物炭进行改性处理,能明显提升其吸附微塑料的能力。酸改性的作用在于,它能增加生物炭表面的官能团数量,如羧基、羟基,同时还能优化其孔隙结构,增强生物炭与微塑料之间的静电相互作用,物理截留效果也会提高。比如,经过酸改性的氧化玉米芯生物炭,因为引入了更多的羟基官能团,对PS微塑料的去除率能达到90%以上,明显优于未改性的生物炭。另外,酸改性还能让生物炭的比表面积变大,从而进一步增加对微塑料的吸附[25]。
也有研究结合高温(700 ℃)热活化,对松树皮生物炭进行NaOH碱改性,发现在改性过程中,生物炭表面的氧含量从11.7%上升到17.2%,并且成功负载了Na元素[26],同时相关表征分析显示,改性后的生物炭比表面积从368增加到 550 m2/g,还形成了更为丰富的孔隙结构。Bashir等[27]研究表明,碱改性生物炭对水溶液中的聚氯乙烯微塑料有着出色的吸附效果,最大吸附量达到156.08 mg/g,去除率高达78%,相比未改性的生物炭(吸附量131.5 mg/g,去除率65%)有明显提高。
1.1.3 有机修饰
有机改性通过引入有机分子(如表面活性剂、聚合物)来调控生物炭表面疏水性或电荷特性,从而增强疏水作用或实现特异性结合。
有研究采用十六烷基三甲基溴化铵(CTAB)改性棕榈仁壳生物炭,发现改性使生物炭表面Zeta电位从-18.3转变为+12.9 mV,同时接触角从112.6°提升至120.2°,表面正电荷和疏水性得到显著增强。CTAB改性生物炭通过疏水相互作用和静电吸引有效截留微塑料,且不规则形状的微塑料因表面粗糙更易被去除,对聚乙烯微塑料(PE,2~4 μm)的去除率从未改性时的83.54%提升至95.71%,对较大尺寸PE微塑料(40~48 μm)的去除率更是达到了99.61%[28]。也有研究采用壳聚糖改性磁性榴莲壳生物炭,发现壳聚糖分子中的氨基使生物炭表面Zeta电位从 -15.6升至+8.3 mV,同时亲水性羟基虽小幅降低接触角(从118.5°降至112.3°),但通过氨基与微塑料表面羧基的静电吸引,以及羟基与微塑料间的氢键作用,在保持适度疏水性的基础上,协同提升了对PS微塑料的吸附能力,对1 μm PS微塑料的去除效率达到97.22%,吸附容量为15.56 mg/g[29]。
1.1.4 复合改性
复合改性结合多种功能化改性手段,实现对材料性能的系统性优化,发挥不同改性方法的协同效应和优势互补,从而提升对微塑料的去除性能。
有研究采用FeCl3和CTAB共改性生物炭,发现Fe改性引入的Fe3O4和Fe2O3磁性组分,其表面羟基通过氢键进一步促进对微塑料的捕获。同时CTAB改性显著提升了生物炭的疏水性和表面正电荷密度,作为阳离子表面活性剂,其带正电的季铵基团通过静电作用,高效吸附带负电的PS微球,是增强吸附效果的关键。实验表明,共改性生物炭对1 μm微塑料的去除率可达98%,最大吸附容量达247.52 mg/g;而未改性生物炭的去除率不足60%[30]。
1.2 物理改性
物理改性主要通过物理手段改变生物炭的宏观结构,一般不引入新的化学物质。
1.2.1 气体活化
气体活化是通过CO2、H2O等气体在高温或缺氧环境中,利用活化气体对生物炭表面进行刻蚀与扩孔的物理改性技术。在这一过程中,活化气体与生物炭中的部分碳发生反应(如CO2与碳反应生成CO),选择性去除表面无序碳和杂质,同时在生物炭内部形成大量相互连通的微孔和介孔,从而提升比表面积和孔隙体积[31-35]。
有研究采用气体活化法改性云杉树皮生物炭,发现可显著提升对微塑料的去除效果,其中,活化过程中优化的孔隙结构(特别是中孔和大孔的发育)为微塑料的物理截留提供了更多通道。实验表明,改性后的生物炭对较大尺寸微塑料颗粒的去除率接近100%,同时对较小颗粒也展现出良好去除潜力,且中孔和大孔含量更高的样品表现更优,其去除机制可能以物理截留为主,并伴随表面粗糙度增加带来的附着作用,气体活化生物炭的整体性能优于未活化样品[32]。
也有研究采用气体活化改性生物炭,发现气体活化能显著增加生物炭的表面积和孔隙体积,形成高度多孔的结构,为微塑料提供更多的吸附位点,这是提升微塑料去除效果的重要原因,其去除机制涉及物理和化学作用,如范德华力、氢键等。研究还表明,较高的活化温度通常能促进孔隙发育和表面积增加,使生物炭具备更优的微塑料截留能力[35]。
1.2.2 球磨改性
球磨改性是一种常见的物理改性方法,通过机械力调控生物炭的粒径分布、比表面积大小以及表面粗糙度,从而显著提升其对微塑料的截留效果。相较于化学改性方法,球磨改性无需添加任何化学试剂,避免了可能产生的二次污染问题。并且通过调节研磨时长、转速强度等参数,可以实现对生物炭微观形貌的精细调控,使其能够适配不同类型微塑料的去除要求,满足多样化的污染治理需求[36-38]。
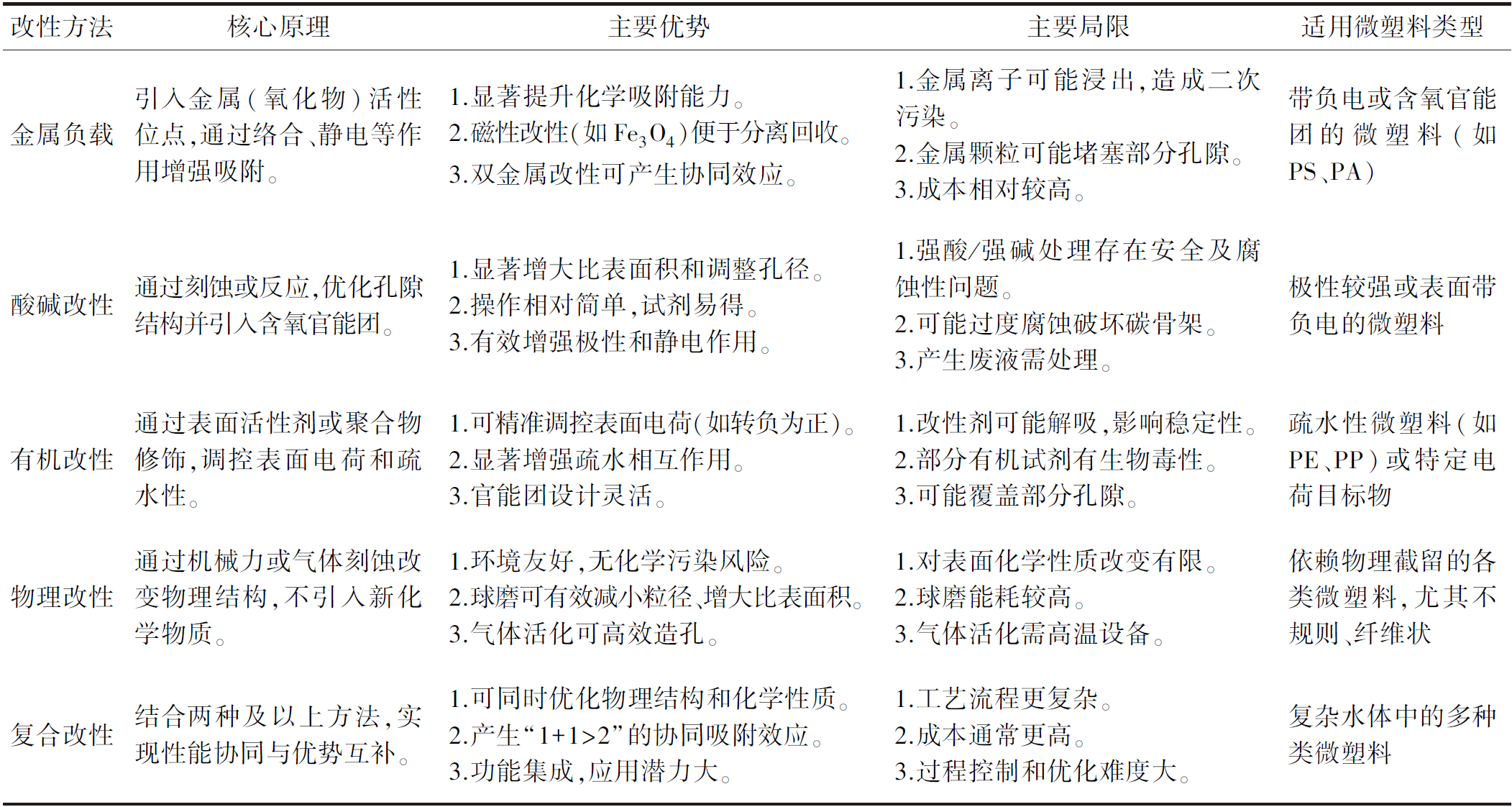
有研究表明,球磨后的生物炭具有更高的比表面积和丰富的孔隙结构,为微塑料提供了更多的吸附位点;同时,球磨过程还增加了表面含氧官能团(如羧基和酚羟基),通过疏水作用和π-π相互作用增强了对疏水性微塑料的捕获能力[38]。Siipola等[32]发现球磨改性后的松木生物炭在固定床柱试验中,对PE微球(10 μm)的去除效率达到85.4%~100%。Tong等[39]也发现球磨与Fe3O4纳米颗粒复合制备的磁性生物炭,对微塑料的去除效率可进一步提升至92.5%。这些结果表明,球磨改性通过优化生物炭的物理结构和表面化学性质,有效提高了其对微塑料的去除性能。表1总结了生物炭不同改性方法的优缺点以及适用去除的微塑料类型。
表1 生物质改性方法优缺点对比
Tab.1 Advantages and disadvantages of biochar modification methods
2 吸附机制
改性生物炭对水体微塑料的吸附是物理与化学作用协同的结果[40]。不同改性方法通过调控生物炭的结构与表面特性,强化了特定的吸附路径,主要涉及静电作用、氢键作用、疏水作用、物理截留、络合和π-π作用,见图2。
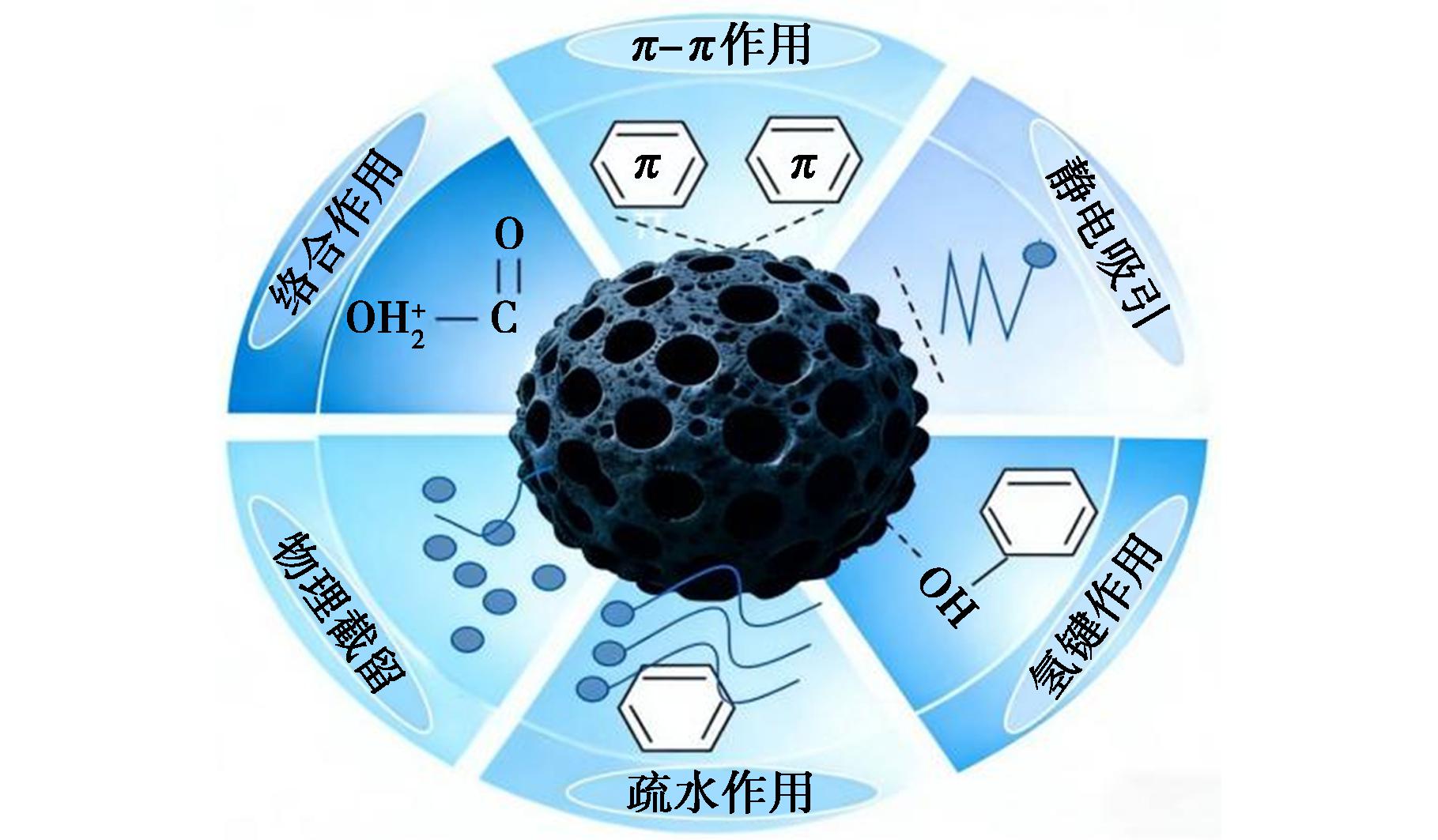
图2 生物炭吸附微塑料的机制
Fig.2 Adsorption mechanisms of microplastics by biochar
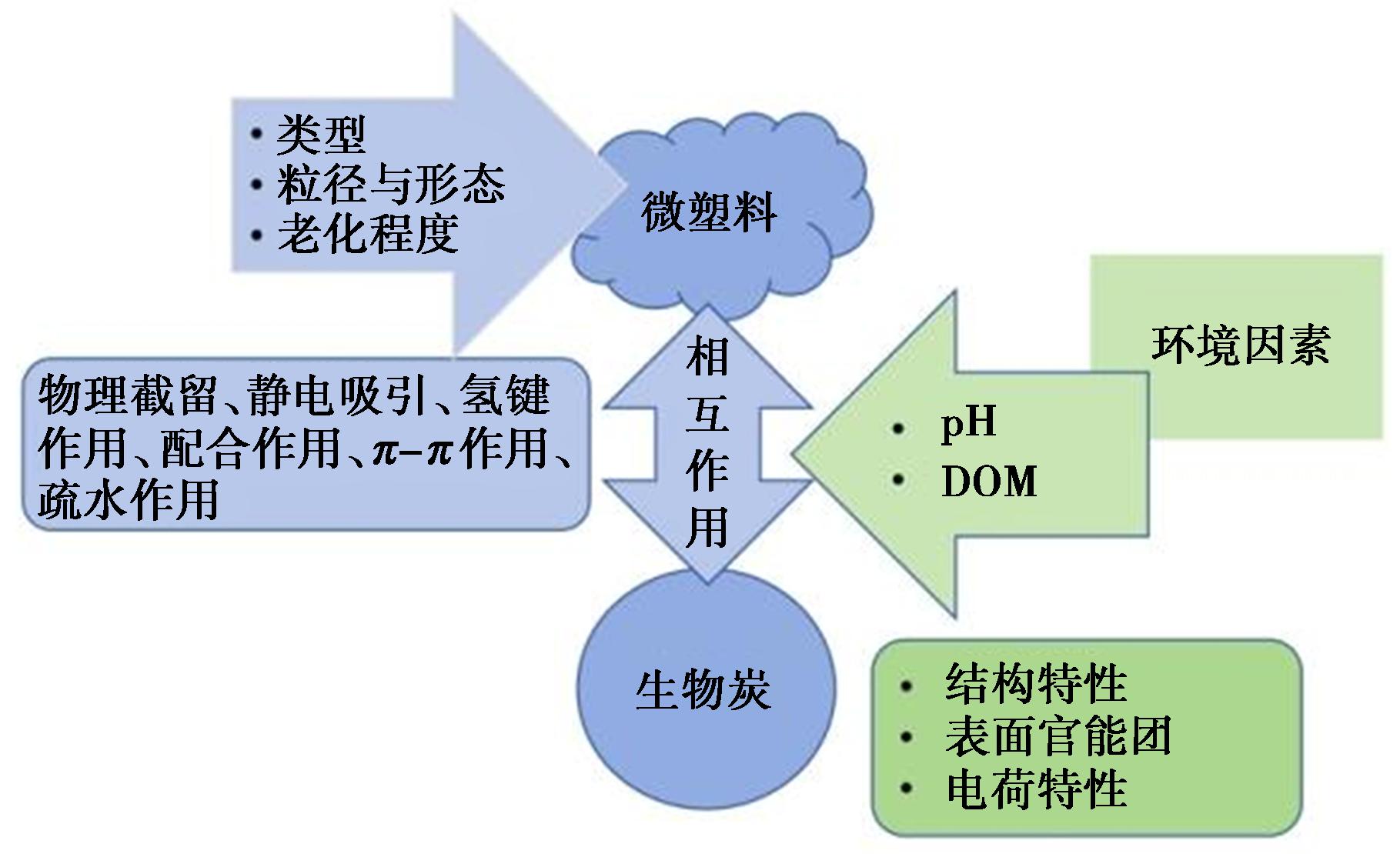
图3 生物炭吸附微塑料的影响因素
Fig.3 Influencing factors affecting the adsorption of microplastics by biochar
2.1 物理截留
改性生物炭的比表面积与孔径结构是实现微塑料物理截留的核心。丰富的孔隙结构可截留和吸附微塑料,更大的比表面积则提供了更多的接触位点[41]。
Parashar等[30]以稻壳为原料制备磁性生物炭,发现改性过程显著影响生物炭的孔隙结构。原状稻壳生物炭的比表面积为109.56~123.10 m2/g,经FeCl3磁化后,由于铁氧化物清除了生物炭表面孔隙堵塞物,使比表面积提高49%,孔体积增至0.114 cm3/g,进一步CTAB改性后,表面活性剂颗粒填充部分孔隙,FESEM分析显示,PS微塑料颗粒主要被吸附在孔隙内部,在优化条件下,去除效率达98%,孔隙填充和物理截留是主要作用机制。Jiao等[42]采用FeCl3·6H2O改性木质素生物炭,发现当木质素/Fe盐质量比为1∶1时,孔隙结构最优,比表面积为417.81 m2/g,微孔面积占比90.89%,分别是未改性木质素生物炭的7.4倍和6.8倍。SEM观察表明,100 nm PS微塑料颗粒可牢固附着于改性生物炭孔隙中,其吸附容量(68.57 mg/g)远超未改性。Fe3O4晶体的形成不仅赋予材料磁性,还优化了微孔-介孔分布,显著提升物理截留能力。Siipola等[32]对比了松树和云杉树皮生物炭的孔隙特性,松树生物炭在30%气体活化下比表面积达454~615 m2/g,以微孔为主(79.6%~86.9%);而云杉生物炭在40%气体活化下中孔比例更高(4.2%~5.6%),两者对2~3 mm PE微塑料碎片截留率均为100%,但对10 μm PE微球的吸附量存在差异,云杉生物炭((0.293±0.046) g)优于松树生物炭(0.130~0.165 g),说明中-大孔结构对大尺寸微塑料的截留更具优势。改性生物炭对微塑料的物理截留效果高度依赖比表面积和孔径结构。
2.2 静电吸引
改性生物炭去除微塑料的静电吸引机制主要可能依赖于表面电荷调控。化学修饰(如金属氧化物负载等)可在生物炭表面引入正电荷,与通常带负电的微塑料颗粒形成定向静电吸附,这种作用力能有效克服微塑料的疏水性和空间位阻,促进其向吸附剂表面迁移并固定,吸附强度受表面电位、离子强度等因素调控。
Hanif等[28]用CTAB改性棕榈仁壳生物炭,发现其表面Zeta电位从负值转变为正值(-18.3~+14.1 mV),与本身带负电的微塑料之间产生强烈静电吸引力,这种吸引力有效克服了未改性生物炭与微塑料间的静电排斥,增强了捕获能力。在最佳CTAB浓度下,该改性生物炭对2~4 μm PE微塑料的去除率可达95.71%(浊度法)和96.12%(重量法),且对不同尺寸(2~48 μm)、形状(不规则、球形、纤维状)和聚合物类型(PE、PA)的微塑料均表现出优异去除效果,反应了静电吸引是该改性生物炭高效去除微塑料的关键机制之一。Wang等[18]研究发现,Mg/Zn改性磁性生物炭在对1 μm PS微塑料的吸附过程中,静电吸引作用受体系pH调控显著:当溶液pH低于生物炭零电荷点时,其表面带正电,与带负电的PS微塑料产生强烈静电吸引,其中锌改性生物炭的去除效率可达99.46%,高于未改性生物炭(94.81%)。Tong等[39]研究表明,Fe3O4改性生物炭在对0.2~2 μm微塑料的吸附中,低离子强度条件下,静电斥力减弱使生物炭与微塑料表面电荷相互作用增强,进而抑制微塑料迁移。Li等[20]研究发现,磁性玉米芯生物炭对75 μm老化聚酰胺(PA)微塑料的高效去除(97%)与静电引力密切相关:老化过程使PA表面氧官能团增加,负电荷密度提高,与带正电的磁性玉米芯生物炭之间的静电吸引作用显著增强;而在高离子强度环境中,溶液中的阳离子会压缩双电层,削弱这种静电相互作用,导致吸附效率下降。此外,pH偏离最佳范围时,静电吸引作用会减弱:pH过高时,生物炭表面负电荷增加,与带负电的微塑料产生斥力;pH过低则可能因H+占据吸附位点,竞争静电结合位点,从而降低吸附效能[35,43]。
2.3 氢键作用
改性生物炭的氢键作用主要依赖表面含氧/含氮官能团与微塑料的极性基团(如酰胺基、羧基)结合,通过氢原子与电负性原子(氧、氮)之间的静电吸引实现。其效率受pH、微塑料类型及共存物质影响,通常作为辅助机制与静电作用、疏水作用协同提升去除效果。
Ganie等[36]研究氧化改性玉米芯生物炭,发现经HNO3/H2SO4处理后,生物炭表面羟基数量明显增加,与PS微塑料表面的氢原子形成氢键,苯环上的氢原子与生物炭羟基的氧原子通过氢键结合,在pH 5时,这种作用对PS微塑料的吸附作用占比约12%,辅助提升去除效率至90%以上。Hanif等[28]研究了CTAB改性棕榈仁壳生物炭,发现其表面丰富的羟基和羰基可作为氢键供体或受体,与PA微塑料中的酰胺基形成氢键,改性棕榈仁壳生物炭的羟基氢可与PA微塑料中酰胺基的氧原子结合,羰基氧则可与酰胺基的氢原子形成氢键,在pH 7时,氢键作用效果最佳,对PA微塑料的去除率较未改性生物炭提升约9%。研究Mg/Zn改性松木生物炭发现表面金属羟基可与PA微塑料的酰胺基形成氢键,金属离子的电负性增强了羟基的极性,使其氢原子更易与酰胺基的氧原子结合,在pH 6时,这种作用使PA微塑料的吸附稳定性增强,解吸率降低约8%[18]。也有研究发现生物炭的羟基可与胺基修饰PS微塑料的胺基形成氢键。生物炭羟基的氧原子与胺基PS中胺基的氢原子通过氢键相互作用,在pH 4~7范围内,该氢键作用占总吸附量的10%~15%,且不受低浓度离子强度影响[44]。
2.4 络合作用
改性生物炭通过表面功能化修饰引入的特定官能团可与微塑料表面的极性基团发生络合作用。这种作用依赖于生物炭表面的活性位点与微塑料分子中的供电子基团(如羟基、羰基等)形成稳定的配位键或螯合结构。通过增强表面络合能力,有效捕获微塑料颗粒,并在其表面形成稳定的有机-无机复合物,从而抑制微塑料的迁移和释放。此外,生物炭的孔隙结构可进一步束缚已络合的微塑料,提高去除效率。
Siipola等[32]研究气体活化的松木和云杉树皮生物炭发现,生物炭表面的官能团可与2~3 mm圆柱形PE微塑料形成络合作用。在络合时,改性生物炭表面的含有孤对电子的基团,与PE微塑料表面具有空轨道的原子之间,发生电子对的给予和接受,从而以配位键结合。这种络合作用使得改性生物炭对这类微塑料的去除率近乎100%,表明络合作用在生物炭去除微塑料过程中起着重要作用。Shrivastava等[35]研究酸改性玉米芯生物炭发现,经5% HNO3-H2SO4处理后,生物炭表面羧基和羟基含量显著增加。在络合过程中,这些增加的含氧官能团充当电子对给予体,PS微塑料表面的极性基团作为电子接受体,二者通过配位作用相互结合,形成稳定的络合物。这种络合作用使得10 μm PS微塑料的吸附效果大幅提升,去除效率超过90%,充分体现了酸改性通过增强表面络合作用,增强对生物炭去除微塑料能力的积极影响。Wang等[45]研究玉米秸秆和硬木生物炭发现,生物炭可通过孔隙捕获和表面络合作用去除微塑料。其表面络合作用的原理为:生物炭表面存在着各类含孤对电子的官能团,这些官能团能与10 μm PS微球表面原子形成配位键,在这个过程中,微塑料表面原子接受生物炭表面官能团提供的电子对,二者紧密结合,使微塑料“被困”“纠缠”在生物炭孔隙中,最终对PS微球的去除效率超过95%。
2.5 π-π作用
改性生物炭通过π-π作用去除微塑料的机制主要依赖于其表面修饰后增强的芳香性结构。生物炭经过化学或物理改性后,其碳层结构更加有序,表面富含共轭π电子体系或多环芳烃结构。这些官能团与微塑料分子中的苯环或疏水聚合物链之间产生π-π共轭效应。改性后的生物炭不仅表面π电子密度增加,其孔隙结构和比表面积的优化也提供了更多吸附位点,从而显著提升了材料对微塑料的捕获能力。
Bashir等[27]研究松木树皮衍生的改性生物炭时发现,其表面存在芳香族基团,XRD分析显示改性后的生物炭峰强度增加,表明石墨化程度更高,这种芳香结构可通过π-π作用与聚氯乙烯微塑料发生相互作用,且改性生物炭对聚氯乙烯微塑料的吸附容量(156.08 mg/g)明显高于未改性生物炭(131.5 mg/g),与芳香性增强的趋势一致。Li等[20]在研究磁性玉米芯生物炭去除老化PA微塑料时发现,老化PA微塑料经氧化后表面暴露芳香结构,而磁性玉米芯生物炭因热解形成芳香环结构,二者通过π-π堆积作用增强吸附亲和力,该作用与疏水作用、静电吸引协同,使老化PA微塑料去除率达97%,显著高于原状PA微塑料(25%)。有研究表明,Mg/Zn改性磁性生物炭保留芳香环结构,其与PS微塑料的苯环间存在π-π键作用,实验数据显示,锌改性生物炭对PS微塑料的去除率达99.46%,且生物炭石墨化程度与吸附效率正相关,表明π-π作用随芳香共轭体系稳定性增强而增强。同时,石墨烯基改性生物炭的石墨层具有大π键体系,通过吸附实验证实其与PS微塑料的苯环通过π-π堆叠作用结合,吸附效率达89.04%,且该作用不受溶液pH显著影响[35]。
2.6 疏水作用
生物炭表面的疏水区域与疏水性微塑料之间通过范德华力产生吸引,可能是吸附疏水性微塑料(如PS、PE)的主要机制之一[46]。Parashar等[30]的研究表明,CTAB修饰的磁性稻壳生物炭通过表面疏水性的增强有效去除微塑料,其长链烷基结构形成疏水性区域促进微塑料吸附。实验证实,当腐殖酸浓度升高时,微塑料去除率从75%降至45%,间接验证了疏水相互作用在吸附过程中的重要作用。铁改性磁性生物炭通过疏水作用有效吸附水中微塑料,FT-IR分析表明吸附后生物炭表面疏水性C—O基团减少,证实了疏水相互作用在吸附过程中的关键作用。此外,生物炭的疏水表面与PS微塑料的疏水特性相匹配,进一步增强了吸附效率[42]。表2总结了不同改性策略的改性思路以及使用场景。
表2 改性目的汇总
Tab.2 Summary of modification objectives

改性策略改性思路应用场景增强物理截留采用气体活化、球磨或模板法,重点扩增介孔和宏孔的体积和连通性。去除粒径较大、形状不规则的微塑料。强化静电吸引通过金属阳离子负载(如Fe3+、Mg2+)、有机阳离子修饰(如CTAB)或胺基化,提高生物炭表面正电性,使其零电荷点(pHPZC)高于水体pH。处理带负电的微塑料(大多数微塑料在中性水中带负电),或在酸性至中性水体中应用。利用疏水作用通过热解提高碳化程度、减少表面含氧官能团或负载疏水聚合物,增强生物炭表面的疏水性。去除PE、PP等强疏水性微塑料。构筑π-π作用通过高温热解、石墨化处理或引入石墨烯/碳纳米管,提升生物炭的芳香性和π电子云密度。特异性高效去除PS微塑料。多机制协同采用复合改性。例如,Fe3O4/CTAB共改性生物炭,同时具备磁性分离(便利性)、正电性(静电吸引)和长链烷基(疏水作用),实现了多种机制的优势互补与协同增效。复杂实际水体中多种类、多形态微塑料的共去除。
3 关键影响因素
改性生物炭对水体微塑料的吸附效果受到多种因素的综合影响。这些因素既包括生物炭自身的性质,如结构特性、表面官能团和电荷特性等,也涉及微塑料的类型、粒径、形态及老化程度等自身特性,同时还与水体环境中的pH值、溶解性有机质(DOM)和温度等环境因素密切相关。
3.1 生物炭性质
3.1.1 结构特性
改性生物炭的高比表面积和发达的孔体积是提高生物炭吸附微塑料效果的关键因素之一。比表面积增大可增加吸附位点,增强生物炭与微塑料之间的物理和化学相互作用(如π-π堆积、静电作用等),介孔(2~50 nm)和宏孔(>50 nm)则通过物理截留捕获微塑料[47],孔体积的增大还促进了微塑料与生物炭表面的接触面积,从而提升吸附容量。改性生物炭需平衡这些结构特性以优化吸附性能[48]。
3.1.2 表面官能团
改性生物炭表面的官能团种类和数量是影响其与微塑料之间相互作用的核心因素之一,决定了化学吸附强弱。特性改性之后官能团的类型更加丰富。例如,Fe3O4改性生物炭表面的Fe—O活性位点可与微塑料表面的含氧官能团形成稳定的配位键,提升吸附效率[18]。酸处理能使生物炭表面生成大量的羧基、羟基等酸性官能团,这些官能团可增强生物炭与微塑料之间的静电相互作用和氢键作用,如酸改性的氧化玉米芯生物炭因羟基官能团数量增加,对PS微塑料的去除率显著提高[25];有机改性会为生物炭表面带来新的官能团。如CTAB改性使生物炭表面带有季铵基团,增强了表面正电荷,通过静电吸引作用吸附带负电的微塑料[28]。
3.1.3 电荷特性
改性生物炭的表面电荷特性在去除微塑料过程中发挥重要作用,多数微塑料表面带负电,通过金属改性或表面功能化可使生物炭表面带正电,借助静电引力增强对负电微塑料的吸附,而未改性生物炭表面通常带负电,会与负电微塑料产生静电排斥,从而降低吸附效率[49]。此外,溶液pH会改变生物炭和微塑料的表面电荷,低pH条件下,生物炭表面负电荷减少,与微塑料的静电排斥作用减弱,吸附效率提升,高pH则会增强生物炭负电荷,导致静电排斥加剧,吸附效率下降[36];而高离子强度(如Ca2+、Na+)可压缩双电层,削弱生物炭与微塑料间的静电排斥,促进两者聚集,间接增强吸附。例如,Ca2+通过阳离子桥接作用增强负电生物炭与微塑料的结合[20]。
3.2 微塑料特性
3.2.1 微塑料类型
不同类型的微塑料因化学组成和表面性质不同,与改性生物炭的相互作用存在差异。有研究使用微塑料为1 μm羧基化PS微球,其带负电且疏水的表面特性是吸附的关键,经CTAB改性后的磁性生物炭表面呈强正电性(+63.7 mV),通过静电吸引、疏水相互作用、氢键和孔隙填充等多重机制实现对微塑料的高效去除。在最优条件下,该吸附剂对PS微球的去除率超过97%,最大吸附容量达247 mg/g[30]。PS微塑料表面含有苯环结构,易与改性生物炭表面的芳香性官能团发生π-π作用,从而提高吸附效率;而PS微塑料表面可能存在更多的氯原子,与改性生物炭表面的官能团相互作用方式不同,吸附效果也会有所差异。Bashir等[27]研究发现,松木树皮衍生的改性生物炭对PS微塑料的吸附容量为156.08 mg/g,而对其他类型微塑料的吸附容量则有不同表现。
3.2.2 粒径与形态
微塑料的物理特性,尤其是其粒径和形态,是决定改性生物炭对其吸附去除效果和机制的关键因素。其中,粒径虽会影响去除机制,但对吸附效果影响不显著,微米级颗粒(如10 μm)主要依靠生物炭的物理截留和缠绕被高效去除,去除率可超过95%[45]。有研究表明,木屑生物炭对1 μm PS微塑料的去除率可达100%[50],也有研究表明,气体活化松树皮与云杉皮生物炭对粒径为2~3 mm的PE颗粒及纤维状微塑料的去除率接近100%,以物理截留作用为主,化学吸附为辅。值得注意的是,尽管云杉皮生物炭比表面积(187 m2/g)较低,但其对10 μm微球的永久保留量((0.293±0.046) g)更高,此现象归因于其更发达的介孔与宏孔结构[32],因此,针对微米级微塑料的去除,生物炭吸附剂的孔结构设计比单纯追求高比表面积更具实际意义。总体而言,生物炭对微米级微塑料表现出极高且稳定的吸附效率(通常>90%),且其吸附效果受微塑料粒径变化的影响不明显,这主要归因于物理拦截、孔填充和缠结等主导机制[51]。而形态则显著影响其与生物炭结构的机械互锁效率,其中,不规则形态的微塑料(如碎片、纤维)比球形颗粒更具吸附优势,因为它们更易发生物理缠绕[45]。同时,也因其形状易于被“卡住”而比球形颗粒更易被捕获。纤维状微塑料易被生物炭的复杂孔隙网络缠绕而实现高效去除[52],相比之下,球形微塑料(如化妆品微球)更依赖范德华力等表面吸附作用,其去除效率因而更依赖于生物炭的表面化学性质,根据环境扫描电子显微镜(ESEM)分析证实,微塑料颗粒被固定在其表面、孔隙内部及薄片结构之下[45],说明微塑料的物理形态是影响其与生物炭相互作用的关键因素,不规则形状的颗粒更易被生物炭的片状结构“缠结”并通过机械作用被“卡住”和“困住”[51]。
3.2.3 老化程度
微塑料在环境迁移过程中因碰撞、撕裂等物理作用导致其表面形态变得粗糙多孔[53],同时受紫外线照射及环境影响发生表面氧化,富集多种含氧官能团[54]。这些物化特性的改变显著增强了其与生物炭的相互作用:粗糙表面更易被生物炭捕捉固定,而表面官能团可与生物炭形成氢键等化学键合,Li等[20]实验发现,改性玉米芯生物炭对老化PA微塑料的去除率(97%)显著高于原状微塑料(25%),证实了微塑料老化程度对吸附效果的增强。
3.3 环境因素
3.3.1 pH
环境pH是影响改性生物炭对微塑料吸附效果的重要因素,主要可能通过调控静电相互作用发挥作用[55]。在较低pH水平下,改性生物炭表面官能团发生质子化,可增强其与带相反电荷微塑料之间的静电吸引力,从而提高吸附保留效率;当pH较高时,改性生物炭表面官能团可能发生去质子化,这会减弱其与微塑料之间的静电相互作用,进而降低吸附效率[56]。有研究表明,高pH条件下会增加生物炭和微塑料颗粒的负电动电位,导致静电斥力增强,从而降低微塑料在改性生物炭上的吸附效率,例如,氧化玉米芯生物炭对PS微塑料的吸附便呈现此规律[57]。pH还会影响微塑料的电荷状态,通过改变微塑料自身带电性质,间接作用于其与改性生物炭之间的静电吸引力[58]。Parashar等[30]发现,溶液pH对CTAB改性磁性生物炭吸附微塑料效果影响显著,在pH 2~4范围内,微塑料吸附量随pH升高而增加,并在pH 4时,对微塑料吸附能力最强,吸附容量达83.46 mg/g,此时吸附剂表面带最高正电荷(+54.2 mV),与带负电的微塑料间静电吸引力最强,微塑料去除率较高;但当pH超过4后,吸附剂吸附能力随pH升高显著降低,溶液从酸性变为碱性时,吸附容量从82.62降至14.35 mg/g,微塑料去除效率从96.4%骤降至16.7%。这是因为改性生物炭的零电荷点(pHPZC)为5.2,当pH高于5.2时,吸附剂表面电负性逐渐增加,与带负电的微塑料间静电相互作用减弱,导致吸附能力下降。总体而言,pH主要通过影响改性生物炭和微塑料的表面电荷性质,改变两者间的静电相互作用,进而影响吸附效果。
3.3.2 DOM
DOM对改性生物炭去除微塑料的吸附效果存在双重影响,具体表现为抑制或促进作用,其作用方向与环境条件、DOM种类及微塑料特性相关。DOM的抑制作用主要通过与微塑料竞争改性生物炭表面的吸附位点实现,进而降低生物炭对微塑料的吸附容量。特定条件下,DOM可通过桥连作用促进微塑料在改性生物炭上的吸附[35]。DOM对改性生物炭吸附微塑料的影响程度会因DOM的种类和性质差异而有所不同。有研究表明,DOM与改性生物炭及微塑料的相互作用会影响改性生物炭对微塑料的吸附效果[59]。也有研究表明,DOM可能阻塞生物炭的孔隙,从而降低改性生物炭对微塑料的吸附能力,还可能与微塑料等有机污染物竞争生物炭表面的吸附位点,进一步削弱改性生物炭的吸附效率[60]。紫外线老化也可能改变生物炭释放的DOM的浓度和分子组成[61]。
4 实际应用挑战
4.1 再生技术
改性生物炭的再生性能是决定其可持续性的关键因素,目前针对吸附微塑料后的改性生物炭,主要再生方法包括热再生和溶剂再生。
热解再生通过高温处理使微塑料分解,同时恢复生物炭的孔隙结构和表面活性,例如,经过5次热再生循环后,锌磁性生物炭和镁磁性生物炭对微塑料的去除效率仍分别达到95%和95.8%,显示出热再生后改性生物炭仍保持较高的吸附性能[18];也有Fe3O4改性生物炭经3次热解循环后,对PS微塑料的去除率仍保持在85%以上,但多次循环可能导致生物炭骨架坍塌,降低吸附容量[20]。
溶剂再生是借助酸、碱等化学解吸剂破坏改性生物炭与吸附的微塑料之间的相互作用,使微塑料从生物炭表面解吸,从而恢复生物炭的吸附能力。但技术的效果受多种因素影响,包括所使用的解吸剂类型及浓度、处理的时间和温度,以及生物炭基质本身的性质等,需要对这些参数进行优化,以提高解吸效率[35]。
尽管再生技术可恢复吸附性能,但生物炭市场价格低廉,其经济可行性仍需进一步评估。鉴于部分水域或高附加值场景对即时再生-循环使用需求迫切,再生技术仍然有一定应用前景。
4.2 未来研究方向
目前的研究大多仅限于实验室的静态实验结果,缺乏动态水流条件下的长期运行数据,该技术在污水处理厂、地表水体等真实环境中的实际实用性与稳定性仍需进一步验证。结合当前研究现状与实际应用需求,未来工作宜进一步聚焦以下方面:针对高DOM河水、高盐度海水或复杂工业废水等基质,精准调控生物炭孔隙、电荷与官能团,开发抗干扰的靶向改性技术;在PS、PE、PA多种微塑料共存及微塑料-重金属/抗生素复合污染场景下,阐明竞争-协同吸附机制,为多功能分子设计提供量化依据[62];基于实际流速、pH、温度等动态参数,构建多因素数学模型,为设备工艺优化提供数据支撑;同时开展从原料制备、改性、运输、再生到废弃的全生命周期评估,重点关注改性剂残留及老化二次污染风险,实现低能耗、低足迹的绿色升级[63]。可以预见,抗干扰能力强、低成本且环境友好的改性技术,是未来建立从实验室到工程应用转化体系的关键。
5 结论
通过化学和物理方法改性的生物炭,可显著提高对水体中微塑料的吸附性能,其吸附过程是物理截留、静电吸引、氢键作用、络合作用、π-π相互作用及疏水效应等多种机制协同作用的结果。吸附效果受生物炭特性、微塑料特性及环境因素(如pH、DOM)的综合影响。目前,热再生等技术为改性生物炭的循环利用提供了可能,但多次再生可能导致性能衰减,需进一步探索和优化再生工艺,以提升再生效率并减少对材料结构的破坏。此外,针对特定应用场景定制改性与再生技术至关重要。该技术在实际环境中的应用仍面临挑战,未来研究应侧重于在实际水体中的长期性能评估、环境风险分析以及低成本绿色改性技术的开发,以推动其从实验室走向工程实践。
[1]Li H D,Feng D S,Yi J M,Liu P Z,Cui K,Guo J.Technol.Water Treat.,2025,51(5):8-15.李会东,丰东昇,伊俊铭,刘佩祖,崔凯,郭静.水处理技术,2025,51(5):8-15.
[2]Maria S,Loris P,Francesca L,Valentina I,Mauro F,Lucia C,Stefania D,Simone N,Giorgio Z.Environ.Pollut.,2018,236:645-646.
[3]Chen X,Zhang J E,Xiang H M,Wei H.Ecol.Environ.Sci.,2020,29(6):1198-1204.陈璇,章家恩,向慧敏,危晖.生态环境学报,2020,29(6):1198-1204.
[4]Yu Y,Zhao Y J,Dong Z Q,Sun D X,Qiu Y P.Water Purif.Technol.,2023,42(6):45-56.于颖,赵奕锦,董志强,孙东晓,邱宇平.净水技术,2023,42(6):45-56.
[5]Wang Z F,Lin T,Chen W.Sci.Total Environ.,2020,700:134520.
[6]Sun X C,Yi L Y,Wang N,Liu Z Z,Jiang W,Chen Z L.Environ.Sci.Technol.,2021,44(6):211-218.孙晓晨,易琳雅,汪楠,刘振中,江文,陈战利.环境科学与技术,2021,44(6):211-218.
[7]Di M X,Wang J.Sci.Total Environ.,2018,616/617:1620-1627.
[8]Okoffo E D,Rauert C,Thomas K V.Sci.Total Environ.,2023,856:159251.
[9]Zhu G J,Chen L D,Duan S,Wu W B,Dai H Q,Bian H Y.Acta Materiae Compositae Sinica,2023,40(2):637-648.朱高坚,陈李栋,段晟,吴伟兵,戴红旗,卞辉洋.复合材料学报,2023,40(2):637-648.
[10]Guo W,Luo Y D,Li C G,Chen L,Yang Y H,Yang X H,Li F M.Asian J.Ecotoxicol.,2022,17(4):33-46.郭威,罗雅丹,李晨光,陈琳,杨宇航,杨翔昊,李锋民.生态毒理学报,2022,17(4):33-46.
[11]Su J Z,Zhan J.Chem.Ind.Eng.Prog.,2023,42(10):5445-5458.苏景振,詹健.化工进展,2023,42(10):5445-5458.
[12]Lai L H,Tian F,Xiong Q,Wang X F,Ye G L,Chen H G.J.Agro Environ.Sci.,2023,42(7):1616-1623.赖丽华,田斐,熊倩,王学锋,叶国玲,陈海刚.农业环境科学学报,2023,42(7):1616-1623.
[13]Wang S,Wang Y R,Yin T,Liu H,Fan Z H,Fan S S.Chem.Reagents,2023,45(7):119-127.王硕,汪雅茹,尹通,刘慧,范子涵,范世锁.化学试剂,2023,45(7):119-127.
[14]Xiao X,Chen B L,Chen Z M,Zhu L Z,Schnoor J L.Environ.Sci.Technol.,2018,52(9):5027-5047.
[15]Zhang Y B,Yang H G,Ma L P,Hua Q X.Appl.Chem.Ind.,2023,52(11):3101-3106.张彦彬,杨会国,马丽萍,化全县.应用化工,2023,52(11):3101-3106.
[16]Wang Y,Wang H,Xing Y R,Ren Y F,Liu Z Y,Zhang T Y,Kang J J,Li X H.J.Contam.Hydrol.,2025,1:104810.
[17]Liu L,Fan S S,Mei Y L.Chem.Reagents,2023,45(5):66-76.刘丽,范世锁,梅杨璐.化学试剂,2023,45(5):66-76.
[18]Wang J,Sun C,Huang Q X,Chi Y,Yan J H.J.Hazard.Mater.,2021,419:126486.
[19]Qin H,Wu J J,Li Q Y,Li P F,Qi W B,Song F M.J.Agro-Environ.Sci.,2025,44(5):1387-1398.秦华,吴娟娟,李巧云,李鹏飞,齐文博,宋凤敏.农业环境科学学报,2025,44(5):1387-1398.
[20]Li J,Chen X H,Yu S G,Cui M.Sci.Total Environ.,2023,875:162647.
[21]Li X Y,Liu W J,Zhang J S,Wang Z B,Guo Z W,Ali J F,Wang L,Yu Z S,Zhang X R,Sun Y Z.Chemosphere,2024,358:142152.
[22]Demiral ![]() C,Demiral H.Surf.Interfaces,2021,22:100873.
C,Demiral H.Surf.Interfaces,2021,22:100873.
[23]Lee S H,Han S J,Wee J H.J.Contam.Hydrol.,2025,269:104485.
[24]Inyang M I,Gao B,Yao Y,Xue Y W,Zimmerman A,Mosa A,Pullammanappallil P,Ok Y S,Cao X D.Crit.Rev.Environ.Sci.Technol.,2016,46(4):406-433.
[25]Obadimu C O,Shaibu S E,Ekwere I O.Isotopes Environ.Health Stud.,2025,61(2):1-11.
[26]Liu Z X,Xu Z Y,Xu L F,Buyong F,Chay T C,Li Z,Cai Y W,Hu B W,Zhu Y L,Wang X K.Carbon Res.,2022,1(1):8.
[27]Bashir M,Ahmad A M,Gani K M.Envir on.Sci.Pollut.Res.,2024,31(49):59416-59429.
[28]Hanif M A,Ibrahim N,Hayazi N A,Dahalan F A,Ali U F,Abdul J A,Syafiuddin A.Sep.Purif.Technol.,2025,360:130596.
[29]Wang S,Qiang T,Shen L H,Xv B,Lan Y L,Zhang J H,Wu Q,Su Y N,Song N N.Int.J.Biol.Macromol.,2025,307:141401.
[30]Parashar N,Hait S.J.Clean.Prod.,2024,474:143606.
[31]Mohanty S K,Valenca R,Berger A W,Yu I K M,Xiong X N,Saunders T M,Tsang D C W.Sci.Total Environ.,2018,625:1644-1658.
[32]Siipola V,Pflugmacher S,Romar H,Wendling L,Koukkari P.Appl.Sci.,2020,10(3):788.
[33]Sommer F,Dietze V,Baum A,Sauer J,Gilge S,Maschowski C,Gieré R.Aerosol Air Qual.Res.,2018,18(8):2014-2028.
[34]Mota L S O,Oliveira P C O,Peixoto B S,Bezerra E S,Moraes M C.Environ.Sci.:Water Res.Technol.,2025,11(2):222-241.
[35]Shrivastava A,Abhishek K,Gupta A K,Jain H,Kumari M,Patel M,Sharma P.J.Hazard.Mater.Adv.,2024,16:100518.
[36]Ganie Z,Khandelwal N,Tiwari E,Singh N,Darbha G K.J.Hazard.Mater.,2021,417:126096.
[37]Kumar M,Xiong X N,Wan Z H,Sun Y Q,Tsang D C W,Gupta J,Gao B,Cao X D,Tang J C,Ok Y S.Bioresour.Technol.,2020,312:123613.
[38]Lyu H H,Gao B,He F,Zimmerman A R,Ding C,Huang H,Tang J C.Environ.Pollut.,2018,233:54-63.
[39]Tong M P,He L,Rong H F,Li M,Kim H J.Water Res.,2020,169:115284.
[40]Hua C S,Wang J M,Gu Z R,Xiong J.Chem.Reagents,2025,47(11):66-74.华成硕,王菊梅,古增瑞,熊健.化学试剂,2025,47(11):66-74.
[41]Yalikunjiang T,Zhang K Y,Gao Z W,Wang K,Zhong M,Dai Z H,Li J,Liu Y.Chem.Reagents,2024,46(5):39-46.亚力昆江·吐尔逊,张凯悦,高志伟,王珂,钟梅,代正华,李建,刘洋.化学试剂,2024,46(5):39-46.
[42]Jiao Y,Wang S Q,Sun B Y,Han Y,Zhang Z L,Shen X L,Li Z H.Sep.Purif.Technol.,2025,353:128468.
[43]Abuwatfa W H,Al-muqbel D,Al-othman A,Halalsheh N,Tawalbeh M.Case Stud.Chem.Environ.Eng.,2021,4:100151.
[44]Yen P L,Hsu C H,Huang M L,Liao V H.Chemosphere,2022,286:131863.
[45]Wang Z H,Sedighi M,Lea-langton A.Water Res.,2020,184:116165.
[46]Duan X T,Chen X,Shi L L,Cao Y R,Liang Y C,Wang T Y,Huang C,Cao Y X.J.Environ.Chem.Eng.,2025,13(2):115509.
[47]Li H B,Dong X L,Silva E B,Oliveira L M,Chen Y S,Ma L Q.Chemosphere,2017,178:466-478.
[48]Subair A,Krishnamoorthy L P,Chellappan S,Chinghakham C.Environ.Sci.Pollut.Res.,2024,31(9):13753-13765.
[49]Kumar R,Verma A,Rakib M R J,Gupta P K,Sharma P,Garg A,Girard P,Aminabhavi T M.Sci.Total Environ.,2023,856:159097.
[50]Hsieh L,He L,Zhang M Y,Lv W Z,Yang K,Tong M P.Water Res.,2022,221:118783.
[51]Ahmad M,Lubis N M A,Usama M,Ahmad J,Al-wabel M I,Al-swadi H A,Rafique M I,Al-farraj A S F.Environ.Pollut.,2023,335:122319.
[52]Hernandez E,Nowack B,Mitrano D M.Environ.Sci.Technol.,2017,51(12):7036-7046.
[53]Sun Y R,Yuan J H,Zhou T,Zhao Y C,Yu F,Ma J.Environ.Pollut.,2020,265:114864.
[54]Liu P,Qian L,Wang H Y,Zhan X,Lu K,Gu C,Gao S X.Environ.Sci.Technol.,2019,53(7):3579-3588.
[55]Tan X F,Zhu S S,Wang R P,Chen Y D,Show P L,Zhang F F,Ho S H.Chin.Chem.Lett.,2021,32(10):2939-2946.
[56]Wang T T,Zhang D,Fang K K,Zhu W,Peng Q,Xie Z G.J.Environ.Chem.Eng.,2021,9(4):105184.
[57]Abdoul-magid A S I,Islam M S,Chen Y L,Weng L P,Li J B,Ma J,Li Y T.Sci.Total Environ.,2021,784:147115.
[58]Shaibu S,Inam E,Moses E,Ofon U,Fatunla O,Obadimu C,Ibuotenang N,Offiong N A,Ekpo V,Adeoye T,Udokang E,Fapojuwo D.J.Nig.Soc.Phys.Sci.,2023,1:1043.
[59]Yang L Y,Liang H Y,Wu Q,Shen P.J.Sci.Food Agric.,2024,104(5):2990-3001.
[60]Wu L,Yang N W,Li B H,Bi E P.Environ.Sci.Pollut.Res.,2018,25(31):31486-31496.
[61]Yang H R,Yan Y M,Yu Y K,He Y L,Fu B,Wang J.Ecotoxicol.Environ.Saf.,2022,243:114009.
[62]Mohsenzadeh A,Persson M,Pettersson A,Frandsen F J.Microplastics,2025,4(4):99.
[63]Goel R,Sharma A,James A,Kumar D,Dhir Y,Dhir S,Kaushal A,Gupta S,Kala D,Kaushik N K,Noorani M S,Nagraik R.Water Air Soil Pollut.,2025,236(10):680.