簕欓花椒(Zanthoxylum avicennae (Lam.) DC.)为芸香科花椒属植物,又名鹰不泊(广东、广西)、花椒簕、鸡咀簕、画眉簕、雀笼踏、搜山虎等,是一种落叶乔木,高可达15 m。常见于北纬约25°以南地区,如台湾、福建、广东、海南、广西、云南等地,菲律宾、越南北部也有分布[1]。
文献报道芸香科簕欓花椒中主要含有香豆素类、生物碱、甾体、三萜、挥发油等成分。簕欓花椒在民间用作草药,有祛风化湿、消肿通络的作用,用于黄疸、咽喉肿痛、疟疾、风湿骨痛、跌打挫伤等症状[2]。其中《本草求原》中记载簕欓花椒根有理痰火、酒痰,开喉咽肿痛的功效[3]。《岭南草药志》中记载其有化湿、祛风、消肿、退黄、理臌、治疟退热等作用[4]。目前与簕欓花椒有关的综合文献报道比较少,本文就簕欓花椒的药理作用和化学成分的相关研究做整理,为簕欓花椒的进一步研究提供理论支持。
1 簕欓花椒的化学成分研究概况
目前对簕欓花椒共分离发现得到了68个化合物,包括香豆素类、生物碱类、木脂素类、三萜类、黄酮类、甾体类、芳香类以及其他类化合物,其中香豆素类和生物碱类化合物是簕欓花椒中发现数量最多的化合物,下面对簕欓花椒中已经分离得到的化合物进行总结叙述。
1.1 香豆素类
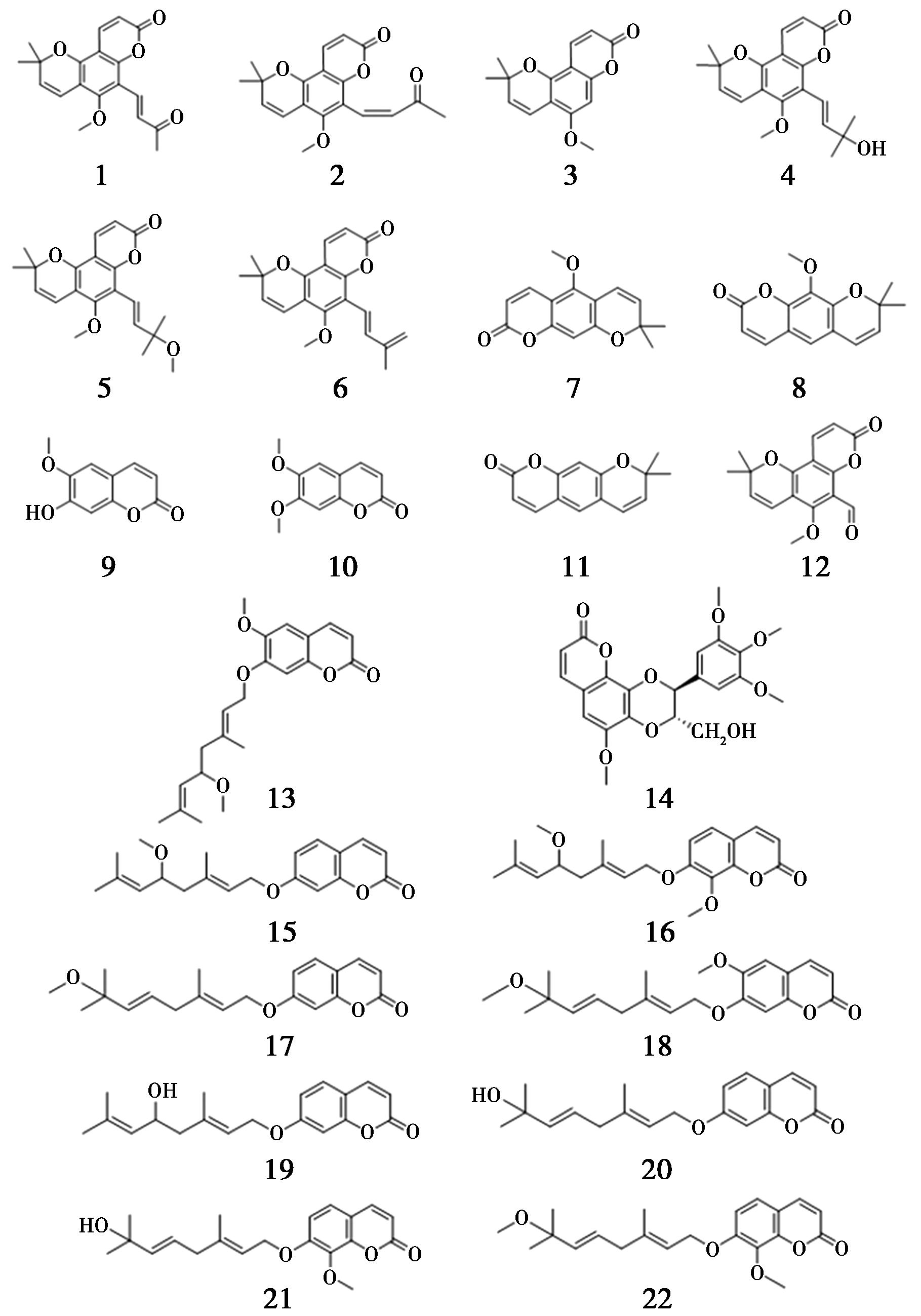
图1 簕欓花椒中的香豆素类化合物
Fig.1 Coumarins from Z.avicennae (Lam.) DC.
香豆素类化合物是存在于自然界中的一类非常重要的化合物,其被发现具有抗肿瘤、抗菌等多种生物活性,在很多领域具有一定的应用价值[5]。根据文献的整理,发现簕欓花椒中富含香豆素类化合物,因此推测香豆素类化合物是簕欓花椒中的主要成分之一。截至2023年9月,文献中共报道了22个从簕欓花椒的树皮、树叶和茎中分离得到的香豆素类成分,分别为avicennone(1)、(Z)-avicennone(2)、alloxanthoxyletin(3)、avicennol(4)、avicennol methyl ether(5)、簕素(avicennin,6)、xanthoxyletin(7)、luvangetin(8)、scopoletin(9)、滨蒿内酯(scoparone,10)、美洲花椒素(xanthyletin,11)、8-formylalloxanthoxyletin(12)、6,5′-dimethoxyauraptene(13)、(7′s,8′s)-4′-omethylcleomiscosin d(14)、5′-甲氧基金合欢烯(5′-methoxyauraptene,15)、5′-methoxycollin(16)、7-((2′e,5′e)-7′-methoxy-3′,7′-dimethylocta-2′,5′-dienyloxy) coumarin(17)、6-methoxy-7-((2′e,5′e)-70methoxy-3′,7′-dimethylocta-2′,5′-dienyloxy) coumarin(18)、5′-hydroxyaurapten(19)、7-((2′e,5′e)-7′-hydroxy-3′,7′-dimethylocta-2′5′-dienyloxy) coumarin(20)、schinilenol(21)、methylschinilenol(22),簕欓花椒中的香豆素类化合物的结构如 图1所示[6-9]。
1.2 生物碱类
截至2023年10月,文献中共报道了20个从簕欓花椒的果实、叶和根茎中分离得到的生物碱类成分,分别为白屈菜季铵碱(chelerythrine,1)、白鲜碱(dictamine,2)、前茵芋碱(preskimmianine,3)、3-吲哚甲酸(1H-indole-3-carboxylicacid,4)、γ-崖椒碱(γ-fagarine,5)、茵芋碱(skimmianine,6)、norchelerythrine(7)、arnottianamide(8)、1-methyl-2-pentylquinolin-4(1H)-one(9)、indole-3-carboxylic acid(10)、avicenine A(11)、avicenine B(12)、avicenine C(13)、avicenine D(14)、avicenine E(15)、avicenine F(16)、(+)-myrtopsine(17)、(-)-edulinine(18)、4-methoxy-3-(3-methylbut-2-en-1-yl) quinolin-2(1H)-one(19)、(E)-4-methoxy-3-(3-methylbuta-1,3-dien-1-yl)quinolin-2(1H)-one(20),如图2所示[7,8,10-13]。
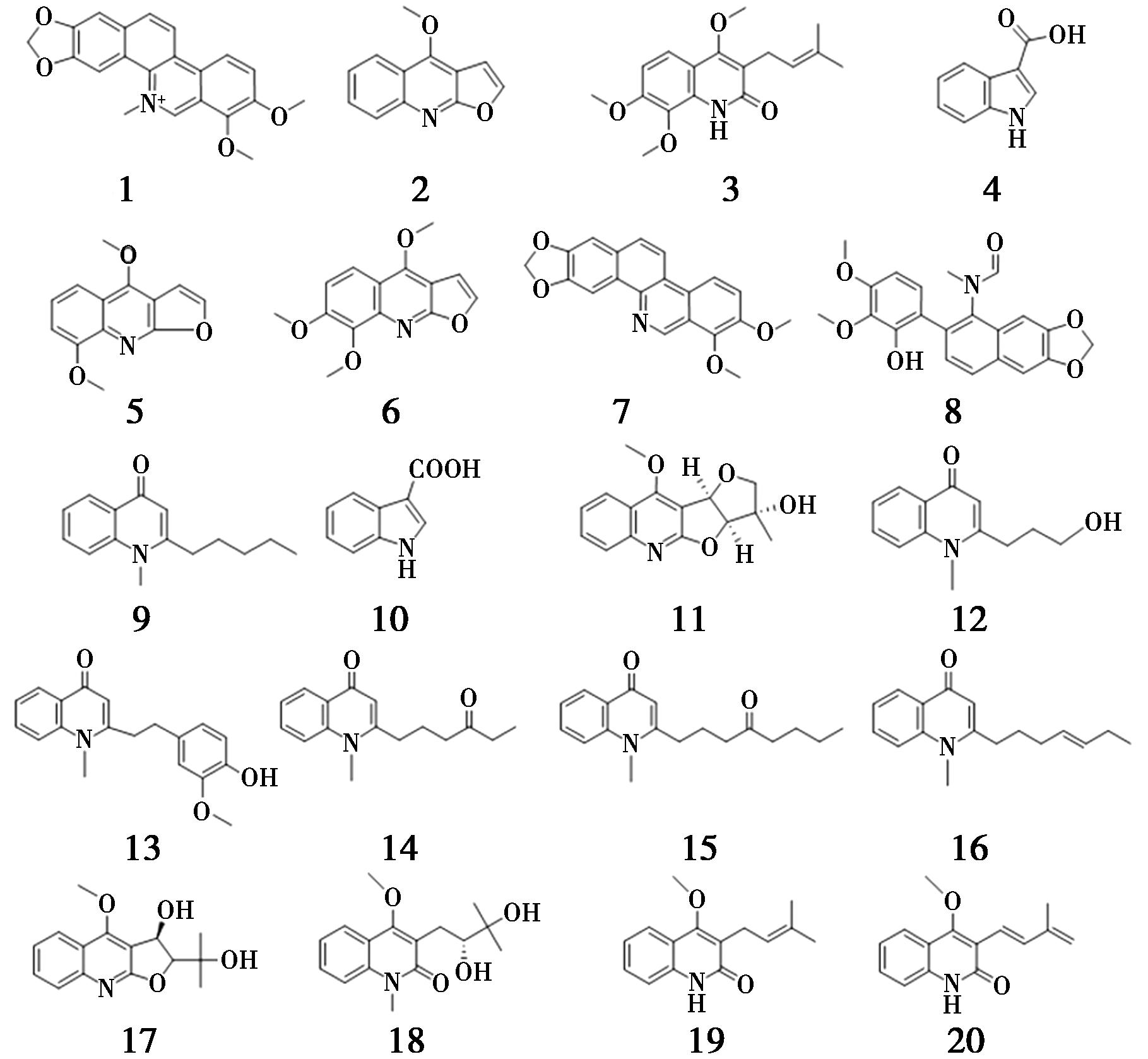
图2 簕欓花椒中的生物碱类化合物
Fig.2 Alkaloids from Z.avicennae (Lam.) DC.
1.3 木脂素类
截至2023年9月,文献中共报道了9个从簕欓花椒的根茎中分离得到的木脂素类成分,分别为丁香脂素(syringaresinol,1)、芝麻素(sesamin,2)、(7′S,8′S)-bilagrewin(3)、(7′S,8′S)-5-demethoxybilagrewin(4)、(7′S,8′S)-5-O-demethyl-4′-O-methylbilagrewin(5)、(7′S,8′S)-nocomtal(6)、(+)-9′-O-(Z)-feruloyl-5,5′-dimethoxylariciresinol(7)、(+)9′-O-(E)-feruloyl-5,5′-dimethoxylariciresinol(8)、(E)-3-(2,2-dimethyl-2H-chromen-6-yl)prop-2enal(9),如图3所示[9,12]。
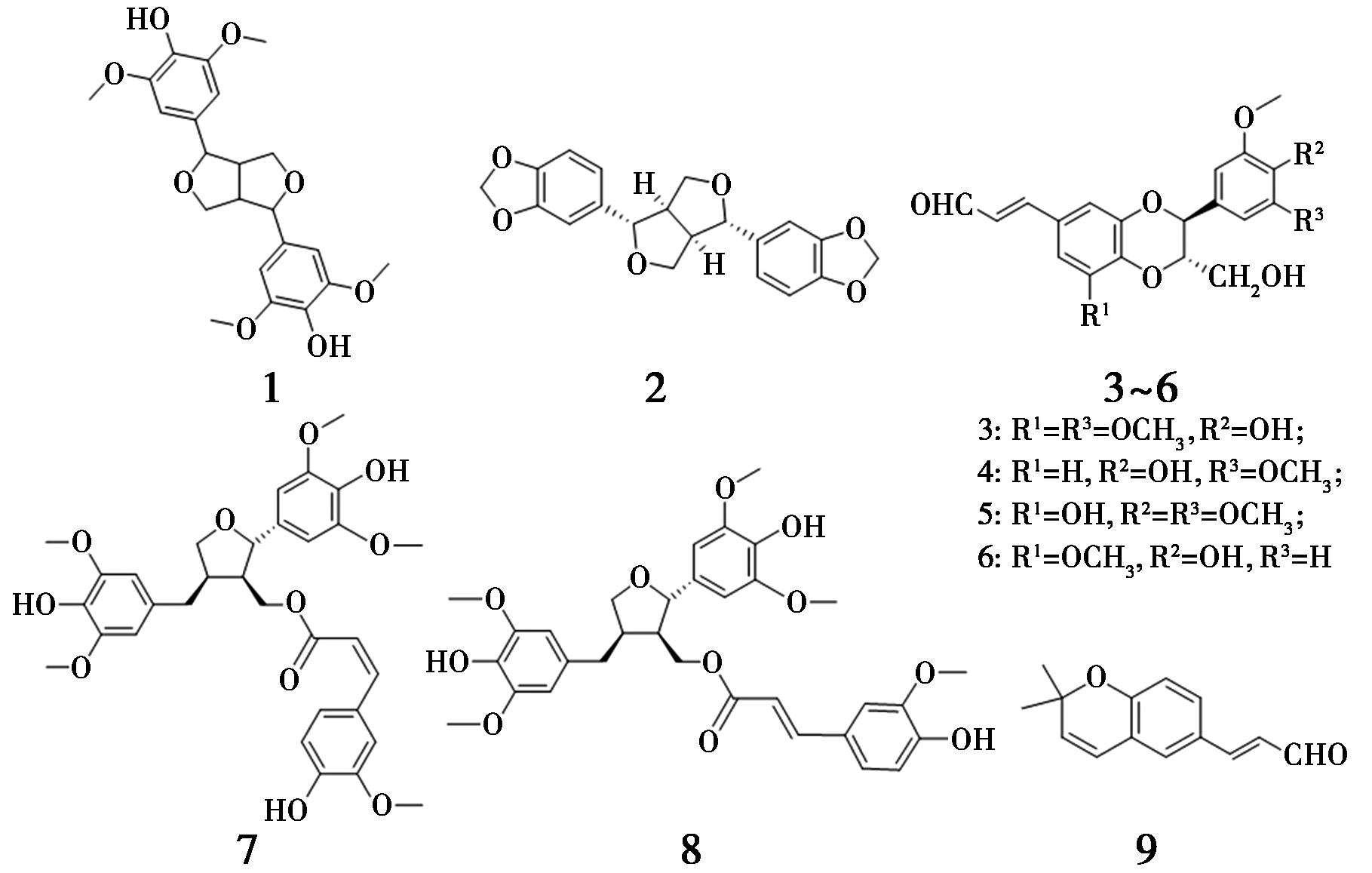
图3 簕欓花椒中的木脂素类化合物
Fig.3 Lignans from Z.avicennae (Lam.) DC.
1.4 三萜类
文献中共报道了3个从簕欓花椒的根茎中分离得到的三萜类成分,分别为α-香树脂醇(α-amyrin,1)、β-香树脂醇(β-amyrin,2)、羽扇豆醇(lupol,3),如图4所示[12,13]。
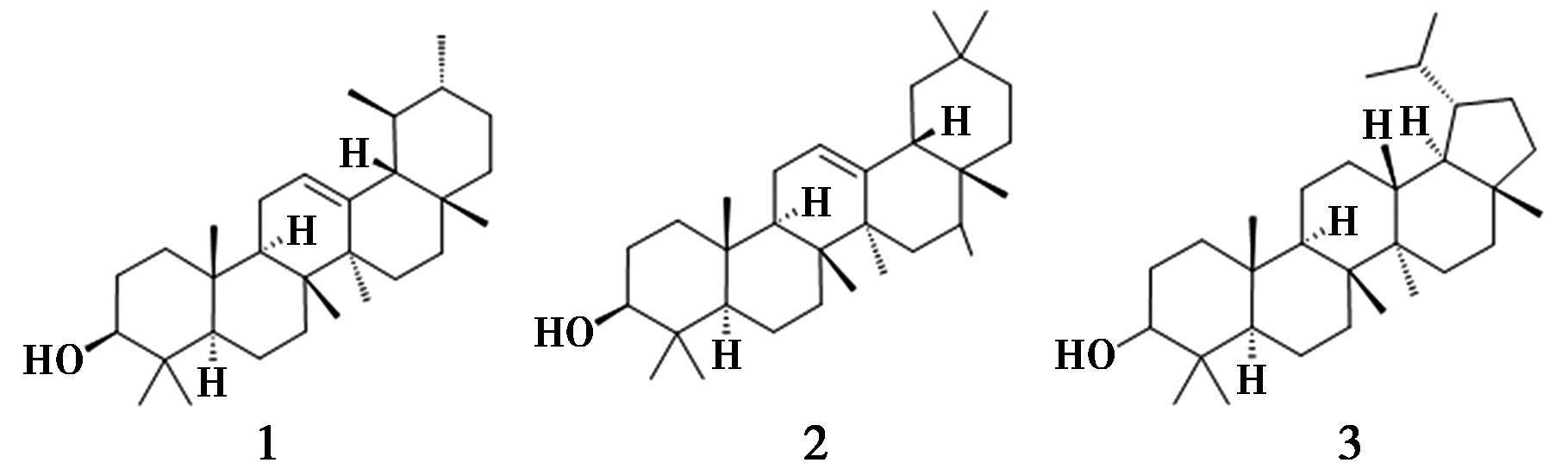
图4 簕欓花椒中的三萜类化合物
Fig.4 Triterpenes from Z.avicennae (Lam.) DC.
1.5 黄酮类
文献中共报道了4个从簕欓花椒的根茎中分离得到的黄酮类成分,分别为diosmetin(1)、apigenin(2)、香叶木苷(diosmin,3)、二氢山柰素(dihydrokaempferide,4),如图5所示[9,10,14]。
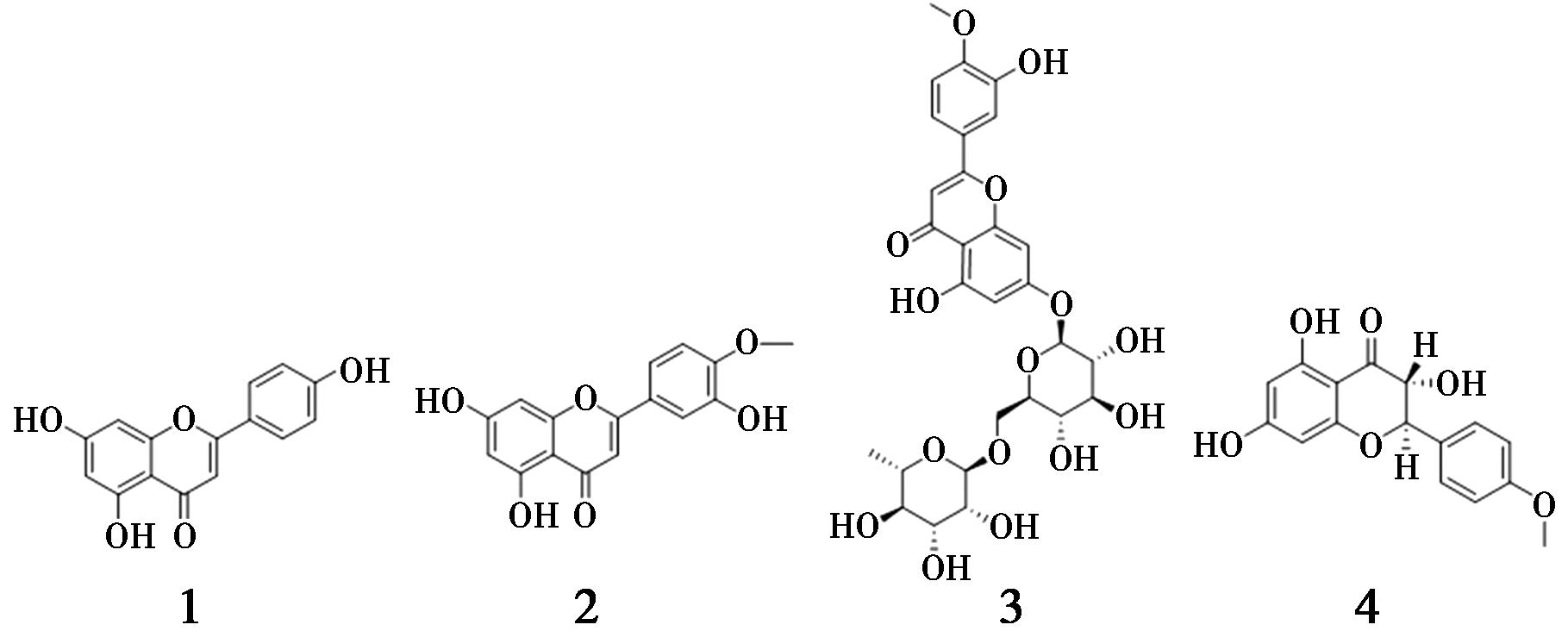
图5 簕欓花椒中的黄酮类化合物
Fig.5 Flavonoids from Z.avicennae (Lam.) DC.
1.6 甾体类
文献中共报道了2个从簕欓花椒中分离得到的甾体类成分,分别为β-谷甾醇(β-sitosterol,1)、stigmasterol(2),如图6所示[8,10]。
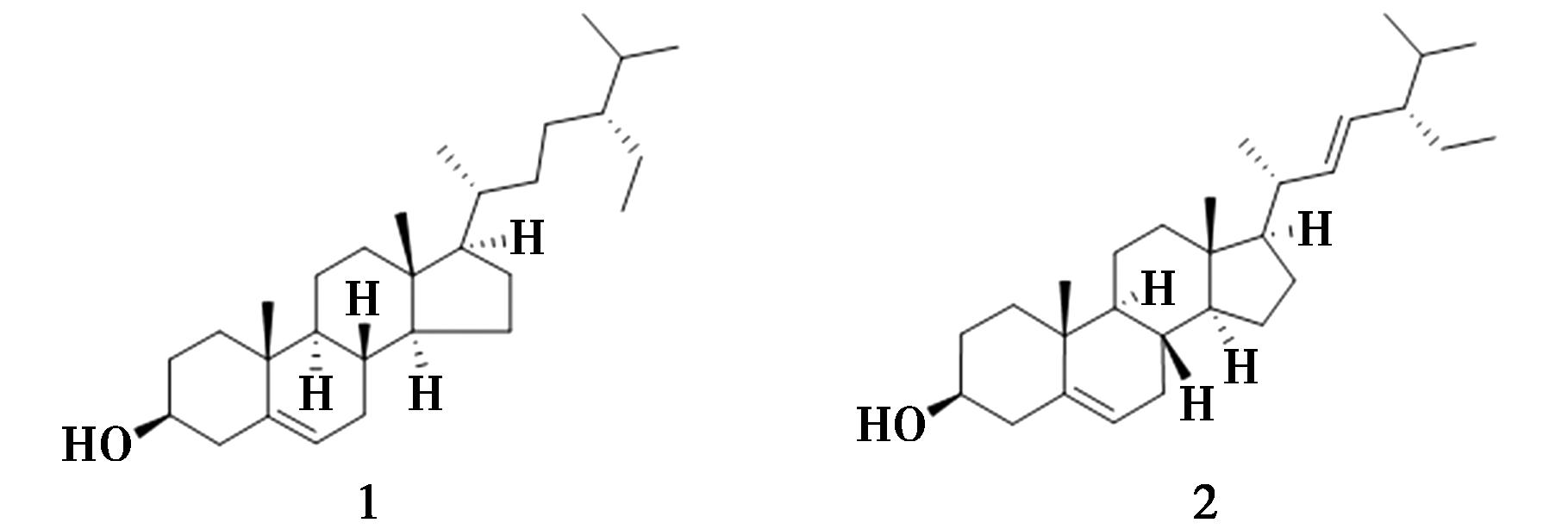
图6 簕欓花椒中的甾体类化合物
Fig.6 Steroids from Z.avicennae (Lam.) DC.
1.7 芳香类化合物
文献中共报道了6个从簕欓花椒的根茎中分离得到的芳香类成分,分别为benzoic acid(1)、邻苯二甲酸二异丁酯(diisobutyl phthalate,2)、methyl syringate(3)、对羟基苯甲酸(p-hydroxybenzoic acid,4)、methyl 4-hydroxybenzoate(5)、methyl(E)-p-hydroxycinnamate(6),如图7所示[9,10,12,13]。
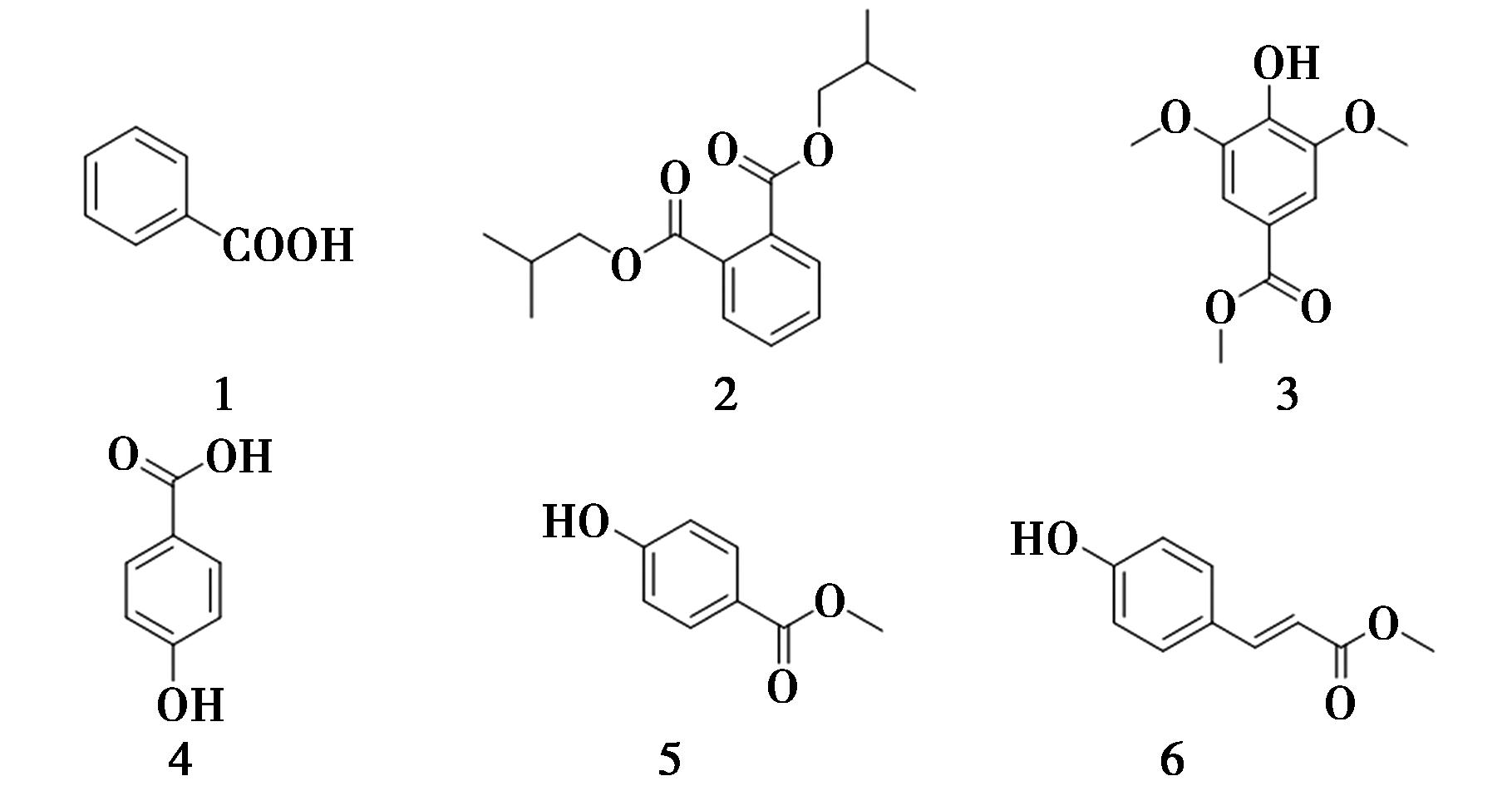
图7 簕欓花椒中的芳香类化合物
Fig.7 Aromatic compounds from Z.avicennae (Lam.) DC.
1.8 其他
除上述的化合物以外,还有2个从簕欓花椒的茎中分离得到的其他成分,分别为辛二酸(subericacid,1)和(loliolide,2),如图8所示[9,10]。
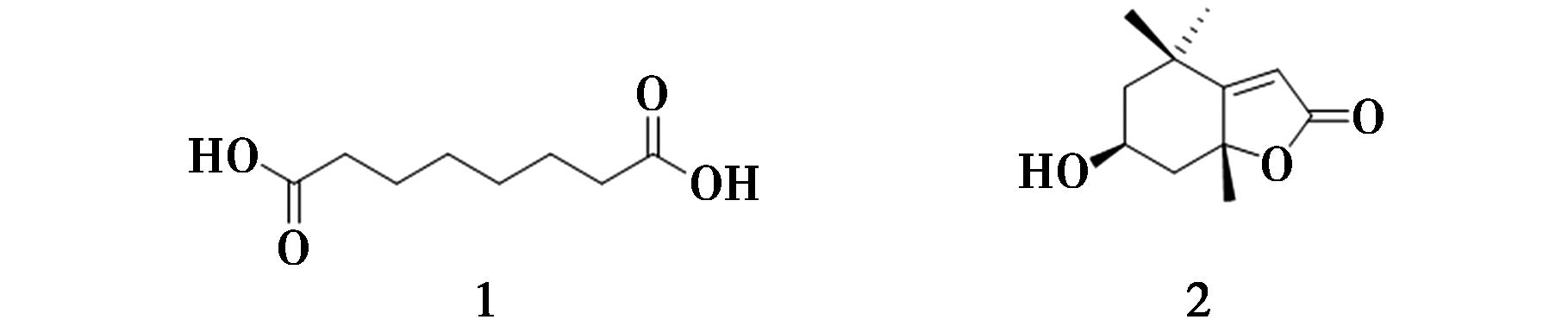
图8 簕欓花椒中的其他类化合物
Fig.8 Other compounds from Z.avicennae (Lam.) DC.
2 簕欓花椒的药理作用研究概况
据文献报道,簕欓花椒的药理学作用主要包括抗氧化、抑菌、抗肿瘤、镇痛抗炎以及保肝等作用,以下对簕欓花椒的药理作用研究情况进行概述。
2.1 抗氧化作用
牟振鑫等[15]采用清除DPPH自由基测定法,对鹰不泊的丙酮提取物、乙醇提取物和水提物抗氧化活性进行评价。结果发现鹰不泊的丙酮提取物、乙醇提取物和水提物清除DPPH自由基的能力均弱于阳性对照组维生素C。3种提取物中,丙酮提取物的清除率最高,其次为乙醇提取物和水提取物,说明鹰不泊的提取溶剂极性越小,提取物抗氧化活性越强。
郑楠楠等[16,17]将簕欓花椒用70%乙醇冷浸提取,浓缩得浸膏,再用石油醚、乙酸乙酯和正丁醇依次萃取,其中正丁醇萃取部位分别用不同浓度的甲醇进行梯度洗脱,分别得到正丁醇的20%、40%和60%甲醇洗脱部位。通过实验发现簕欓花椒正丁醇萃取部位的40%甲醇洗脱部位总黄酮的含量最高,通过DPPH评价体系比较发现40%甲醇洗脱部位对DPPH的清除能力最好,在ABTS评价体系中,通过比较发现40%甲醇洗脱部位ABTS自由基的清除作用最为明显,在FRAP的评价体系中,各部位提取物对Fe3+的还原力存在差异,其中还原力最强的是40%甲醇洗脱部位。簕欓花椒提取物中存在一定的抗氧化活性,但发挥作用的具体化学成分或有效部位还不清楚,日后有待开展进一步的工作研究,发现其具有抗氧化活性的单体或有效部位,开发其药用价值。
2.2 抑菌作用
张大帅等[18]用水蒸气蒸馏法从簕欓花椒叶中提取挥发油,并且用气相色谱-质谱联用技术对其挥发油成分进行分析。最终从挥发油中分析鉴定出72个物质,其中含量较高的组分为芳樟醇、β-榄香烯、(E)-2-己烯-1醇、石竹烯氧化物等,且发现簕欓花椒叶挥发油对供试菌种均有不同程度的抑制作用,且随挥发油剂量的增加而增强。
郑楠楠[17]对簕欓花椒的乙醇提取物、乙酸乙酯萃取部位、正丁醇萃取部位、正丁醇萃取部位的20%、40%和60%甲醇洗脱部位进行了抑菌活性测定,研究发现簕欓花椒正丁醇萃取部位的40%甲醇洗脱部位的抑菌活性最好,特别是对镰刀菌、小麦赤霉病菌和禾谷镰刀菌有很好的抑菌活性;而簕欓花椒乙酸乙酯部分的抑菌效果整体稍低于40%甲醇洗脱部位,而其余部位也有抑菌效果,但抑菌活性相对正丁醇萃取部位的40%甲醇洗脱部位和乙酸乙酯萃取部位比较低。除此以外,郑楠楠等[10]用斜面试管法测定了从簕欓花椒中提取的3个单体化合物二氢山柰素、滨蒿内酯、3-吲哚甲酸对7种植物病原真菌的抗菌活性。实验结果表明化合物滨蒿内酯的抑菌活性最好,特别是对玉米大斑病菌、大麦赤霉病菌,由此表明簕欓花椒有一定的抑菌作用。
Xiong等[6]研究发现,簕欓花椒树皮中含有抗真菌的活性物质,并分离鉴定出3个抗真菌单体化合物,分别为美洲花椒素(xanthyletin,11)、鲁望橘内酯(luvangetin,8)和簕素(avicennin,6),对禾谷镰刀菌、水稻纹枯病菌和稻瘟病菌均具有较好的抑菌活性,因此这3个单体化合物可作为杀菌剂的先导化合物,具有较好的开发价值和应用前景。
2.3 抗肿瘤作用
张大帅等[18]从簕欓花椒叶提取出挥发油,发现其对4种细胞均有一定抑制活性;其中对白血病细胞K-562的抑制活性最强,表明簕欓花椒叶挥发油具有一定的抗肿瘤活性。
郑楠楠[17]分别测定了簕欓花椒70%乙醇粗提物部位,乙酸乙酯萃取部位,正丁醇萃取部位,正丁醇萃取部位的10%、20%、40%和60%甲醇洗脱部位对海虾幼虫的半数致死率,实验表明不同提取部位均具有很强的细胞毒活性。进一步采用簕欓花椒70%乙醇粗提物进行抗肿瘤活性的测定,从整体的角度观察簕欓花椒乙醇提取物对移植性H22实体瘤模型小鼠的肿瘤生长、H22腹水瘤小鼠生存时间和免疫缺陷小鼠免疫器官指数的影响,结果表明簕欓花椒乙醇提取物组对移植性H22实体瘤小鼠均表现出抑制肿瘤生长、延长H22腹水瘤小鼠的生存时间和提高免疫缺陷小鼠免疫器官指数的作用,说明簕欓花椒醇提物具有很强的抗肿瘤活性。
Cui等[19]发现簕欓花椒的正丁醇提取物可通过改善荷瘤小鼠的炎症因子,提高H22荷瘤小鼠的生存质量,增强其免疫能力,表现出非常优异的抗肿瘤活性。其机制可能是通过提高荷瘤小鼠免疫器官质量而发挥抗肿瘤作用,同时增加肿瘤坏死因子-α(TNF-α)、白细胞介素-2(IL-2)等细胞炎症因子的分泌。簕欓花椒的正丁醇部位能帮助改善H22荷瘤小鼠的生存质量和体内的脂质过氧化,具有明显的抗肿瘤和免疫调节作用,且无明显的肝损伤。
Huang[20]研究了鹰不泊提取物(YBBEs)在体外和体内小鼠移植瘤模型中对HA22T人肝癌细胞的影响。YBBEs通过PP2A显著促进HA22T细胞凋亡,并以剂量依赖的方式降低裸鼠移植瘤的肿瘤大小。
Dung等[21]发现通过簕欓花椒提取物处理的HA22T细胞中,包括uPA和tPA以及下游MMP-2/-9蛋白在内的ECM降解相关通路被显著抑制,HA22T细胞中的内源性抑制因子TIMP-1/-2和PAI-1表达增强,MMP-2/-9的mRNA水平和酶活性均下调。PP2A siRNA或PP2A抑制剂完全逆转了YBBE的作用,证实了PP2A在YBBE抑制HA22T细胞迁移和侵袭效应中的重要作用。裸鼠异种移植动物实验显示了与体外系统相似的结果,体外和体内模型均清楚地表明,YBBEs通过激活PP2A抑制高转移性HA22T肝癌细胞的迁移和侵袭作用,表明YBBEs具有一定的抗肿瘤活性。
Wu等[14]的研究进一步表明,在体外和体内模型中,YBBEs通过激活PP2A抑制人肝癌细胞的细胞转移信号,并呈剂量依赖性,且与β-catenin信号通路的失活有关,因此表明YBBEs可能是一种很有开发前景的抗癌剂,日后有望能够对抗晚期或转移性肝癌。
从以上的研究来看,有不少都是簕欓花椒提取物对肝癌的研究,说明簕欓花椒有潜在的抗肝癌作用,日后可在抗肝癌活性方面做更深一步的研究,寻找抗肝癌的活性部位或者单体化合物。
2.4 抗炎作用
吴晓华等[22]将簕欓根用90%乙醇加热回流提取,浓缩得浸膏,以蒸馏水分散,得到水混悬液,依次加入石油醚、乙酸乙酯和正丁醇萃取得到各部位。发现簕欓根水混悬液和正丁醇萃取部位在口服给药后能明显减轻蛋清所致小鼠足跖的肿胀和腹腔毛细血管的炎性渗出,对抑制急性炎症有较好的作用;并且能显著抑制大鼠肉芽肿增生,对慢性炎症也有不错的抑制效果,有较好的抑制炎性疼痛的作用。且提取物镇痛抗炎的活性从高到低依次为水混悬液或正丁醇萃取部位,其次为乙酸乙酯萃取部位,最后是石油醚萃取部位。
Ji等[11]从簕欓花椒的果实中分离得到10个喹啉类生物碱,包括6个新的喹啉类生物碱,其中一个化合物对巨噬细胞中促炎细胞因子IL-1β和IL-6的基因表达和分泌起到了抑制作用。
Cho等[7]从簕欓花椒叶的甲醇提取物中分离得到20个化合物,其中包括5个新香豆素类化合物,其中9个化合物能显著抑制fMLP诱导的超氧阴离子的产生和弹性蛋白酶的释放。因此簕欓花椒可进一步开发,用于治疗或预防各种炎症性疾病。
Chen等[8]从簕欓花椒茎皮的甲醇提取物分离出了18个化合物,其中化合物(7′S,8′S)-4′-O-methylcleomiscosin D、cleomiscosin D、skimmianine、robustine和integrifoliolin对人中性粒细胞产生超氧阴离子和释放弹性蛋白酶均有较强的抑制作用,说明簕欓花椒有一定的生物医药价值,有望开发成为预防或治疗各种炎症性疾病的药物。
2.5 其他作用
除了上述药理作用外,簕欓花椒还有免疫调节、肝保护、降酶退黄等作用。胡松[23]发现复方鹰不泊能上调环磷酞胺免疫抑制小鼠血清IFN-γ、IL-2的表达,因此进一步表明复方鹰不泊治疗慢性丙型肝炎可能通过调节细胞因子而发挥抗感染的作用。另外,也有专利表明含鹰不泊的中药组合物对治疗肝硬化有一定的作用[24]。吴晓华等[25]研究了簕欓花椒根的不同溶剂提取物的降酶退黄作用,将簕欓花椒根用90%乙醇提取和浓缩得到浸膏,与模型组相比,浸膏的水混悬液组和正丁醇萃取部位组的丙氨酸氨基转移酶(ALT)、天门冬酸氨基转移酶(AST)、碱性磷酸酶(ALP)、γ-谷氨酰基转移酶(GGT)肝脏指数均显著下降(P<0.01或P<0.05),且组间无显著性差异(P>0.05),由此判断簕欓花椒根有较好的降酶退黄作用。
3 结论与展望
簕欓花椒是芸香科花椒属植物,民间记载其存在一定的药用价值,但其研究和开发利用还在起步阶段,与之相关的应用产品也基本在空白阶段,簕欓花椒的潜在应用价值还有待被进一步发现。
鉴于目前的研究现状,仍需要对簕欓花椒的化学成分进行系统的研究,了解其具体组成成分,发现簕欓花椒中可能存在的新化合物。除此以外,还需要对其中的单体化合物和部位进行活性研究,直到目前,香豆素和生物碱类化合物也是簕欓花椒中被发现种类最多的两类成分,因此后续也有望加强对簕欓花椒中香豆素和生物碱类化合物的研究,发掘簕欓花椒中香豆素和生物碱类化合物的药用价值。
由于合成的化学药物价格比较昂贵且存在不少的副作用,天然植物被认为是筛选研发镇痛药物的不错来源。当前对于疼痛的临床治疗主要通过使用阿片类药物或是采用非甾体抗炎药,但是阿片类药物会产生严重的依赖性和成瘾性,目前镇痛剂滥用和药物依赖的问题愈发严重,而非甾体抗炎药只能用于轻度的疼痛,还会引发胃肠道、皮肤等诸多不良反应,因此开发研究出依赖性小、成瘾性低和不良反应少的镇痛药物是一个亟待解决的问题[26-28]。在前文中提到簕欓花椒根对小鼠起到了抑制炎性疼痛的作用,因此有望能从簕欓花椒中发现发挥镇痛作用的活性成分,开发出新的镇痛药物。
簕欓花椒是我国传统的中药材,民间也有不少关于簕欓花椒的药用记载,说明了簕欓花椒存在的药用价值,期望能对簕欓花椒成分进行系统的研究,从中发现具有良好的抗氧化、抗菌、抗肿瘤、镇痛抗炎和保肝等活性的先导化合物或有效部位,以及挖掘可能存在的其他活性作用。除此以外,明确其化学成分与药理活性之间的联系,探索其发挥作用的机制,不仅为后续簕欓花椒的开发和利用提供理论基础,而且对于簕欓花椒下一阶段的研究具有重要的意义。
[1]中国科学院中国植物志编辑委员会.中国植物志[M].北京:科学出版社,1977.
[2]莫少红,唐弟光,粟华生,等.HPLC法测定鹰不泊药材中橙皮苷的含量[J].中药新药与临床药理,2012,23(3):316-318.
[3]赵其光.本草求原[M].广东:广东科技出版社,2009.
[4]广东省中医药研究所.岭南草药志[M].上海:上海科学技术出版社,1961.
[5]王荣香,宋佳,孙博,等.香豆素类化合物功能及生物合成研究进展[J].中国生物工程杂志,2022,42(12):79-90.
[6]XIONG Y T,HUANG G,YAO Z L,et al.Screening effective antifungal substances from the bark and leaves of Zanthoxylum avicennae by the bioactivity-guided isolation method[J].Molecules,2019,24(23):4 207.
[7]CHO J Y,HWANG T L,CHANG T H,et al.New coumarins and anti-inflammatory constituents from Zanthoxylum avicennae[J].Food Chem.,2012,135(1):17-23.
[8]CHEN J J,YANG C K,KUO Y H,et al.New coumarin derivatives and other constituents from the stem bark of zanthoxylum avicennae:Effects on neutrophil pro-inflammatory responses[J].Int.J.Mol.Sci.,2015,16(12):9 719-9 731.
[9]CHEN J J,WANG T Y,HWANG T L.Neolignans,a coumarinolignan,lignan derivatives,and a chromene:Anti-inflammatory constituents from Zanthoxylum avicennae[J].J.Nat.Prod.,2008,71(2):212-217.
[10]郑楠楠,杨胜祥,周慧,等.簕欓花椒的化学成分及生物活性研究[J].中草药,2015,46(2):189-193.
[11]JI K L,LIU W,YIN W H,et al.Quinoline alkaloids with anti-inflammatory activity from Zanthoxylum avicennae[J].Org.Biomol.Chem,2022,20(20):4 176-4 182.
[12]GUO T,TANG X F,ZHANG J B,et al.Chemical constituents from the root and stem of Zanthoxylum avicennae[J].Appl.Mech.Mater.,2014,618:426-430.
[13]郭涛.竹叶椒(Zanthoxylum armatum DC.)和簕欓(Z.avicenna (Lam.) DC.)的化学成分及竹叶椒镇痛抗炎活性研究[D].上海:上海复旦大学,2011.
[14]WU H C,LAY I S,SHIBU M A,et al.Zanthoxylum avicennae extract enhances GSK-3β to attenuate β-catenin via phosphatase 2A to block metastatic effects of HA22T cells and hepatocellular carcinoma xenografted nude mice[J].Environ.Toxicol.,2017,32(9):2 133-2 143.
[15]牟振鑫,李洪娟,王雪,等.两种中药的体外抗氧化活性研究[J].时珍国医国药,2014,25(4):809-810.
[16]LI X F,ZHENG N N,TANG L,et al.Antioxidant activities of ethanol extracts from Zanthoxylum avicennae[J].Appl.Mech.Mater.,2014,472:801-804.
[17]郑楠楠.簕欓花椒的生物学评价研究[D].郑州:河南中医学院,2014.
[18]张大帅,钟琼芯,宋鑫明,等.簕欓花椒叶挥发油的GC-MS分析及抗菌抗肿瘤活性研究[J].中药材,2012,35(8):1 263-1 267.
[19]CUI H X,CHENG F R,ZHENG N N,et al.Antitumor and immunoregulation effects and mechanism of n-butanol fraction from Zanthoxylum avicennae in H22 mice[J].Pharmacogn.Mag.,2019,15(63):443.
[20]HUANG C Y.Zanthoxylum avicennae extracts induce cell apoptosis through protein phosphatase 2A activation in HA22T human hepatocellular carcinoma cells and block tumor growth in xenografted nude mice[J].Int.J.Mol.Med.,2011,28(6):927-936.
[21]DUNG T D,FENG C C,KUO W W,et al.Suppression of plasminogen activators and the MMP-2/-9 pathway by a Zanthoxylum avicennae extract to inhibit the HA22T human hepatocellular carcinoma cell migration and invasion effects in vitro and in vivo via phosphatase 2A activation[J].Biosci.Biotechnol.Biochem.,2013,77(9):1 814-1 821.
[22]吴晓华,田素英,梁爱华.簕欓根不同提取物镇痛抗炎作用的研究[J].今日药学,2017,27(7):441-443;450.
[23]胡松.复方鹰不泊对环磷酰胺免疫抑制小鼠血清IFN-γ、IL-2及血T淋巴细胞亚群影响的研究[D].长沙:湖南中医学院,2004.
[24]何欣怡,何浩.一种用于治疗肝硬化的中药组合物:CN111 759 968A[P].2020-10-13.
[25]吴晓华,田素英,郭巧玲.簕欓根不同提取物降酶退黄作用研究[J].中国药业,2017,26(21):18-20.
[26]李龙飞,黄芝瑛,张颖丽,等.镇痛药潜在依赖性及其非临床安全性评价研究进展[J].药物评价研究,2023,46(12):2 717-2 723.
[27]郑东森,季晖,胡庆华.中药止痛作用的研究进展[J].中国新药杂志,2017,26(7):782-786.
[28]BOUYAHYA A,GUAOUGUAOU F E,EL-OMARI N,et al.Anti-inflammatory and analgesic properties of moroccan medicinal plants:Phytochemistry,in vitro and in vivo investigations,mechanism insights,clinical evidences and perspectives[J].J.Pharm.Anal.,2022,12(1):35-57.