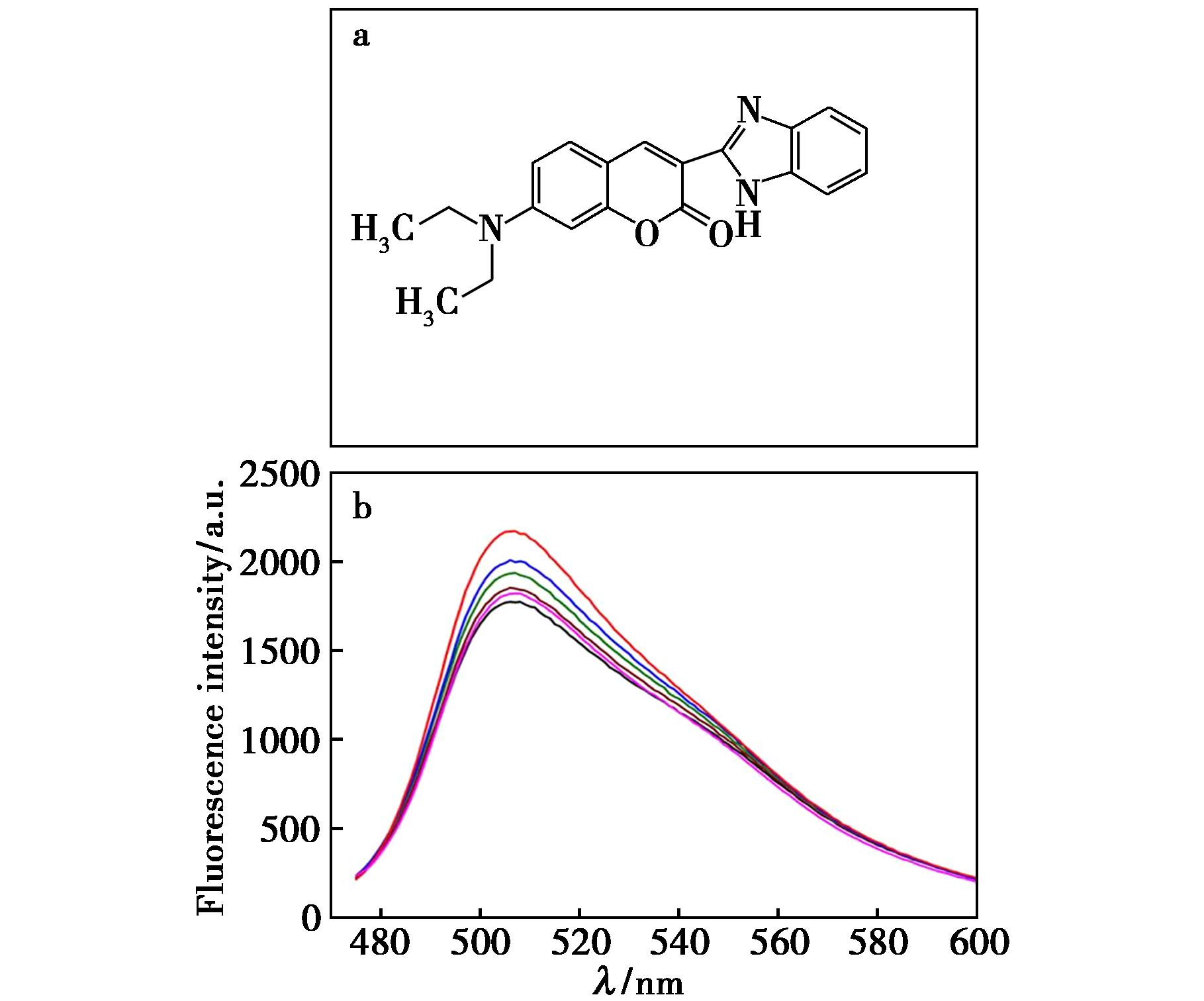
图1 a.BDC探针分子结构;b.BDC在不同激发波长下的发射光谱,曲线的激发波长分别为435、440、445、450、455、465 nm
Fig.1 a.Molecular structure of the probe BDC;b.Emission spectrum of BDC under different excitation wavelengths
Zn2+作为生命体必需的过渡金属离子,在酶催化[1,2]、基因表达调控及细胞信号传导[3,4]中起关键作用。人体血清中Zn2+浓度需维持在70~110 μg/dL,其失衡与糖尿病、神经退行性疾病等密切相关;工业废水中过量Zn2+则会破坏生态系统并通过生物富集威胁健康。因此,开发高灵敏、高选择性的Zn2+检测技术具有重要意义。传统检测方法(如原子吸收光谱、电感耦合等离子体质谱)虽精度高,但存在前处理复杂、无法实时原位监测等局限。荧光传感技术具有高时空分辨率和可视化检测等显著优势,现已成为金属离子检测研究热点。基于香豆素衍生物的荧光探针,其结构中的内酯环和共轭体系赋予其卓越的光稳定性,通过引入不同的官能团,可以灵活调控探针的选择性和响应性,被广泛应用于金属离子的检测[5-7]。
王晔等[8]报道了一种基于香豆素和四氮唑的荧光探针ASZ,该探针通过“OFF-ON”荧光增强机制,实现了对Zn2+的高选择性检测,检测限低至9.94 nmol/L,并成功应用于细胞和小鼠体内的Zn2+成像。肖嘉扬等[9]则设计了一种香豆素-呋喃肟衍生物探针AFY,通过荧光整合增强效应(CHEF),实现对Fe3+的红色荧光检测,为多价金属离子的区分提供了新思路。此外,陈义豪等[10]和盛筱等[11]分别利用香豆素骨架开发了针对次氯酸(ClO-)和肼(N2H4)的荧光探针,进一步拓展了香豆素探针在活性小分子检测中的应用。
尽管这些研究取得了显著进展,但针对Zn2+的香豆素荧光探针仍存在一些限制,如易受其他金属离子(如Cd2+、Cu2+)的干扰,部分探针的水溶性较差,限制了其在生物体系中的应用。本文通过筛选,成功寻找到能与Zn2+特异性结合的香豆素衍生物:3-(1H-苯并[d]咪唑-2-基)-7-(二乙氨基)-2H-苯并吡喃-2-酮(BDC)荧光探针(图1a)。该探针在乙醇-水体系中表现出对Zn2+的高选择性、优异的抗干扰能力和低检测限,为Zn2+的检测提供了新工具,也为香豆素荧光探针的设计和优化提供了理论参考。

图1 a.BDC探针分子结构;b.BDC在不同激发波长下的发射光谱,曲线的激发波长分别为435、440、445、450、455、465 nm
Fig.1 a.Molecular structure of the probe BDC;b.Emission spectrum of BDC under different excitation wavelengths
APEXII型X-射线单晶衍射仪(美国Rigaku公司);F-7000型荧光分光光度计(日本日立公司)。
3-(1H-苯并[d]咪唑-2-基)-7-(二乙氨基)-2H-苯并吡喃-2-酮(BDC,纯度≥98%,上海毕得医药科技股份有限公司);所用有机试剂和无机盐均为分析纯,使用前未进行进一步纯化。
1.2.1 荧光光谱测定
确定最佳激发波长实验:探针BDC用无水乙醇配成1×10-3 mol/L的母液,取100 μL母液,用乙醇-水(V(乙醇)∶V(水)=1∶1)补足3.0 mL,激发狭缝和发射狭缝为5 nm,电压为450 V,在不同的激发波长下测其发射光谱。
1.2.1.1 金属离子识别实验
取100 μL探针母液,用乙醇-水(V(乙醇)∶V(水)=1∶1)补足3.0 mL,分别加入20 μL(2.0×10-3 mol/L)的14种金属离子溶液(Na+、K+、Ag+、Ca2+、Ba2+、Mg2+、Fe2+、Co2+、Ni2+、Cu2+、Zn2+、Mn2+、Pb2+、Cd2+),混合均匀,测其荧光发射光谱。
1.2.1.2 离子干扰实验
取100 μL探针母液,加入40 μL(2.0×10-3 mol/L)的干扰离子和2 860 μL乙醇-水溶剂,混合均匀,在455 nm的激发波长下测其荧光光谱;随后继续加入20 μL(2.0×10-3 mol/L)的Zn2+,混合均匀后测荧光光谱。
1.2.1.3 荧光滴定实验
在探针溶液中,逐渐增加Zn2+的浓度,测体系的荧光光谱变化情况。Zn2+的检出限(LOD)的计算公式为:LOD=3σ/k,其中,σ为空白样品的标准偏差,k为荧光强度与探针浓度的斜率[12,13]。
1.2.1.4 Job′s Plot实验
在等物质的量连续变化实验(Job′s Plot实验)中,保持探针BDC与Zn2+的总浓度不变,通过不断调节两者的比例x=[Zn2+]/([Zn2+]+[BDC]),测不同比例下的荧光强度,推测探针与Zn2+的结合比[14,15]。
1.2.1.5 水样中Zn2+的测定
实验选取的是自来水和百色右江河水,其中右江河水在百色市区东合大桥下岸边随机取样,经过0.22 μm滤膜过滤掉悬浮物再进行检测;自来水取自化学实验室,使用前未经过任何处理。对水样中Zn2+进行加标回收实验时,测试条件与金属离子识别实验条件相同。
1.2.2 配合物BDC-Zn的合成
称取0.016 6 g探针BDC与0.018 6 g的高氯酸锌置于耐压管中,用无水乙醇-水作溶剂,于80 ℃烘箱中反应3 d后梯度降温,静置1 d,瓶内析出橙色棒状晶体(BDC-Zn),产率约为49%,挑出合适晶体进行X-射线单晶衍射分析。
测试了不同的激发波长(435、440、445、450、455、460 nm)下探针BDC的荧光发射光谱,如图1b所示。在不同的激发波长下,探针在506 nm处有最强发射光谱,随着激发波长的增加,探针发射光谱先升高后降低,但发射光谱图形未有明显变化,在455 nm的激发下,探针的发射光谱最强,可用于探针的最佳激发波长。
为了探究探针BDC对不同金属离子的选择识别性,分别加入Na+、K+、Ag+、Ca2+、Ba2+、Mg2+、Fe2+、Co2+、Ni2+、Cu2+、Zn2+、Mn2+、Pb2+、Cd2+等离子后,测试探针BDC溶液的荧光光谱变化,结果如图2a所示。加入Zn2+后,在506 nm处BDC的荧光强度由1 998增加到5 536,荧光增强2.8倍;加入Ag+后,BDC的荧光强度下降到1 480,下降了25.9%,而其他受试金属离子的加入,体系的荧光光谱变化很小或几乎没有变化,表明探针分子BDC可以实现对Zn2+的荧光选择性识别。
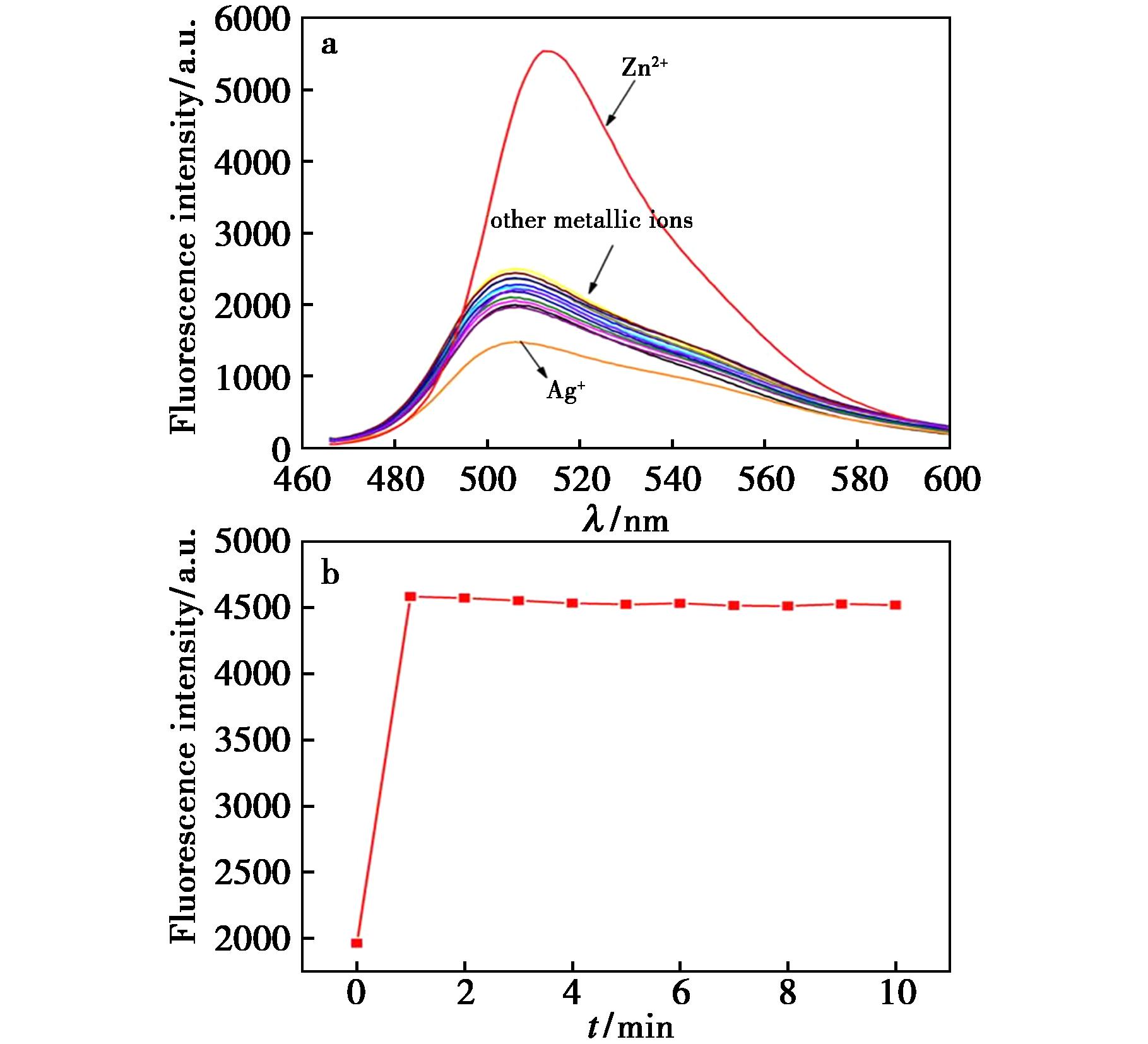
图2 a.不同金属离子对探针BDC荧光光谱的影响;b.探针BDC识别Zn2+的响应时间测定
Fig.2 a.Effect of different metal ions on the fluorescence spectrum of probe BDC;b.Response time determination of probe BDC to Zn2+
对于离子探针来说,响应时间是检测方法中尤为关键的一步,向BDC探针中加入Zn2+,测定在0~10 min内体系荧光强度变化,如图2b所示。可见,BDC与Zn2+的混合后,体系的荧光在极短的时间(0.5 min)迅速升高达到稳定,在10 min内监测,体系的荧光强度几乎不再发生变化,可见,探针BDC在检测Zn2+中具有快速响应和稳定的优势,后续的荧光实验反应时间建立在此基础上进行。
为了进一步考察探针BDC对Zn2+的识别灵敏性,进行了Zn2+的荧光光谱滴定实验,结果如图3a所示。在BDC体系中,随着Zn2+浓度的增加,荧光光谱不断增强,当Zn2+浓度由0~13.5 μmol/L时,BDC在506 nm处的荧光值由1 957增加到 5 489,荧光值增强2.8倍,最大发射波长移到512 nm处。探针BDC对Zn2+的检出限(LOD)根据公式LOD=3σ/k进行计算,其中,σ代表10次探针BDC的荧光值标准偏差(10.79),k代表BDC荧光强度与Zn2+浓度线性曲线斜率。计算得出探针BDC对Zn2+的检出限结果为0.117 μmol/L,远低于国家标准《生活饮用水卫生标准》(GB 5749—2006)规定的饮水中Zn2+含量的限量值1.0 mg/L(约15 μmol/L)[16],比文献[17]报道的雌二醇喹啉缀合物荧光探针对Zn2+的检出限(2.18 μmol/L)低,与文献[18]报道的基于芘的双席夫碱荧光探针对Zn2+的检出限(0.074 μmol/L)相当,但比文献[8,19]报道的探针检测Zn2+的检出限(9.94、5.5nmol/L)高。
表1 BDC-Zn晶体数据及结构参数
Tab.1 Crystal data and structure parameters of BDC-Zn
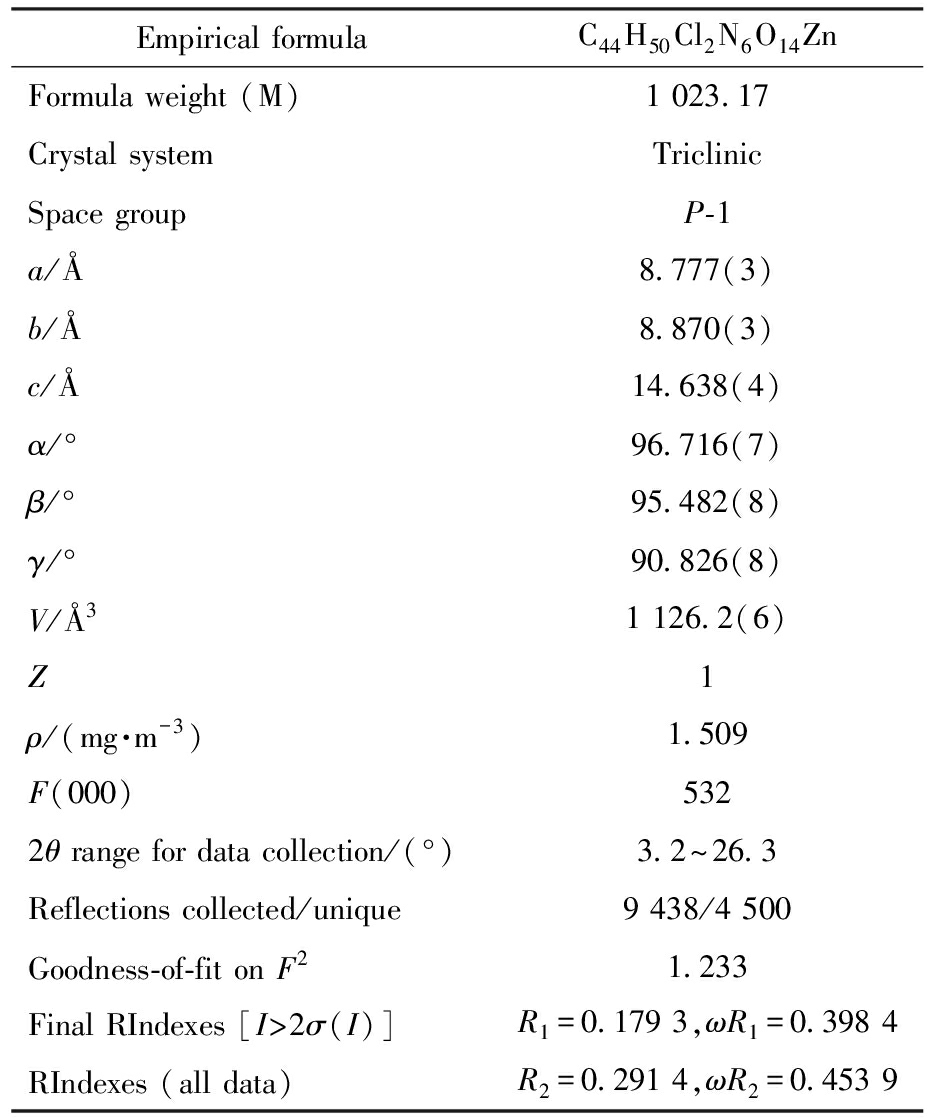
Empirical formulaC44H50Cl2N6O14ZnFormula weight (M)1 023.17Crystal systemTriclinicSpace groupP-1a/Å8.777(3)b/Å8.870(3)c/Å14.638(4)α/°96.716(7)β/°95.482(8)γ/°90.826(8)V/Å31 126.2(6)Z1ρ/(mg·m-3)1.509F(000)5322θ range for data collection/(°)3.2~26.3Reflections collected/unique9 438/4 500Goodness-of-fit on F21.233Final RIndexes [I>2σ(I)]R1=0.179 3,ωR1=0.398 4RIndexes (all data)R2=0.291 4,ωR2=0.453 9
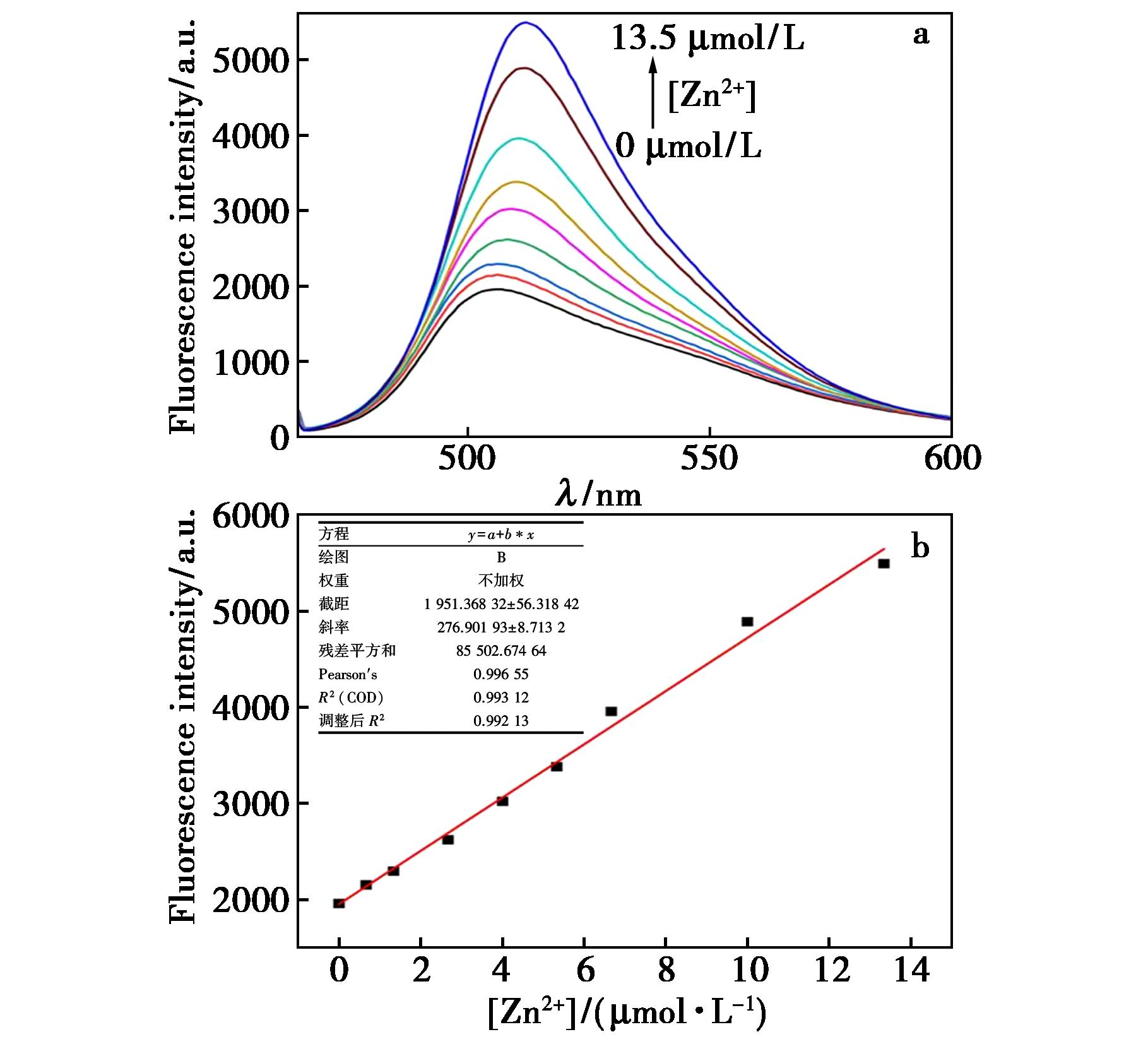
图3 a.不同Zn2+浓度(0~13.5 μmol/L)对BDC荧光光谱的影响;b.BDC在λ=506 nm处荧光强度与Zn2+浓度的线性关系
Fig.3 a.Effect of different Zn2+ concentrations(0~13.5 μmol/L) on fluorescence spectra of probe BDC;b.Linear relationship of the fluorescence intensity of probe BDC at λ=506 nm versus Zn2+ concentration
可见,BDC的荧光强度与Zn2+浓度在0.117~13.5 μmol/L范围内线性关系良好,回归方程y=1 951.37+276.90x,相关系数R2=0.992 1,探针BDC可用于Zn2+的高效定量检测。
为考察探针BDC的抗干扰能力,研究了探针在有其他离子存在时对Zn2+的检测识别能力。在35 μmol/L的探针溶液中分别加入干扰离子(K+、Na+、Ag+、Ca2+、Mg2+、Ba2+、Fe2+、Co2+、Cu2+、Ni2+、Mn2+、Pb2+、Cd2+),再加入Zn2+溶液,混合均匀后测定体系的荧光强度,结果如图4所示。BDC体系中仅加入干扰离子时,除了Ag+有一定的干扰外(体系荧光减弱24.3%),其他受试离子对BDC的荧光值影响不大,当加入Zn2+时,体系的荧光值显著升高,506 nm处的荧光值是原来荧光强度的2.1~2.4倍,这说明BDC具有较强的坑干扰能力,具有检测复杂环境中Zn2+的潜力。
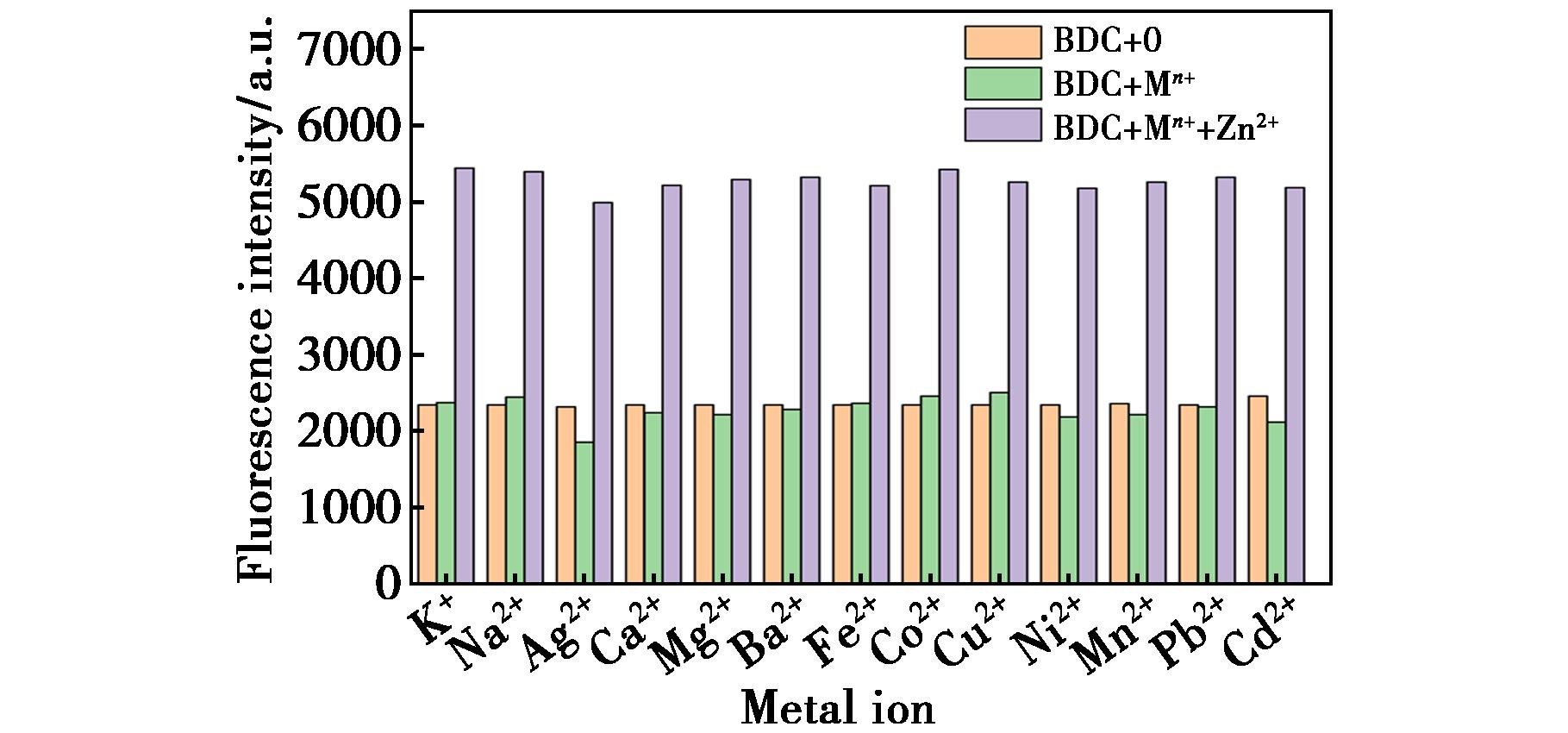
图4 不同金属离子对BDC+Zn2+荧光强度的影响
Fig.4 Effects of different metal ions on the fluorescence intensities of probe BDC+Zn2+
采用Job′s Plot实验(等物质的量连续变化法)探讨BDC与Zn2+的化学计量结合比[20]。首先保持BDC和Zn2+的总浓度不变,通过不断调整[Zn2+]/([Zn2+]+[BDC])的浓度比例,测定不同浓度比例下,体系在λ=506 nm处的荧光强度,绘制Job′s Plot曲线图(图5)。当Zn2+的物质的量分数占比约在0.35时,体系的荧光值达到最大,表明BDC与Zn2+结合比为2∶1[16]。
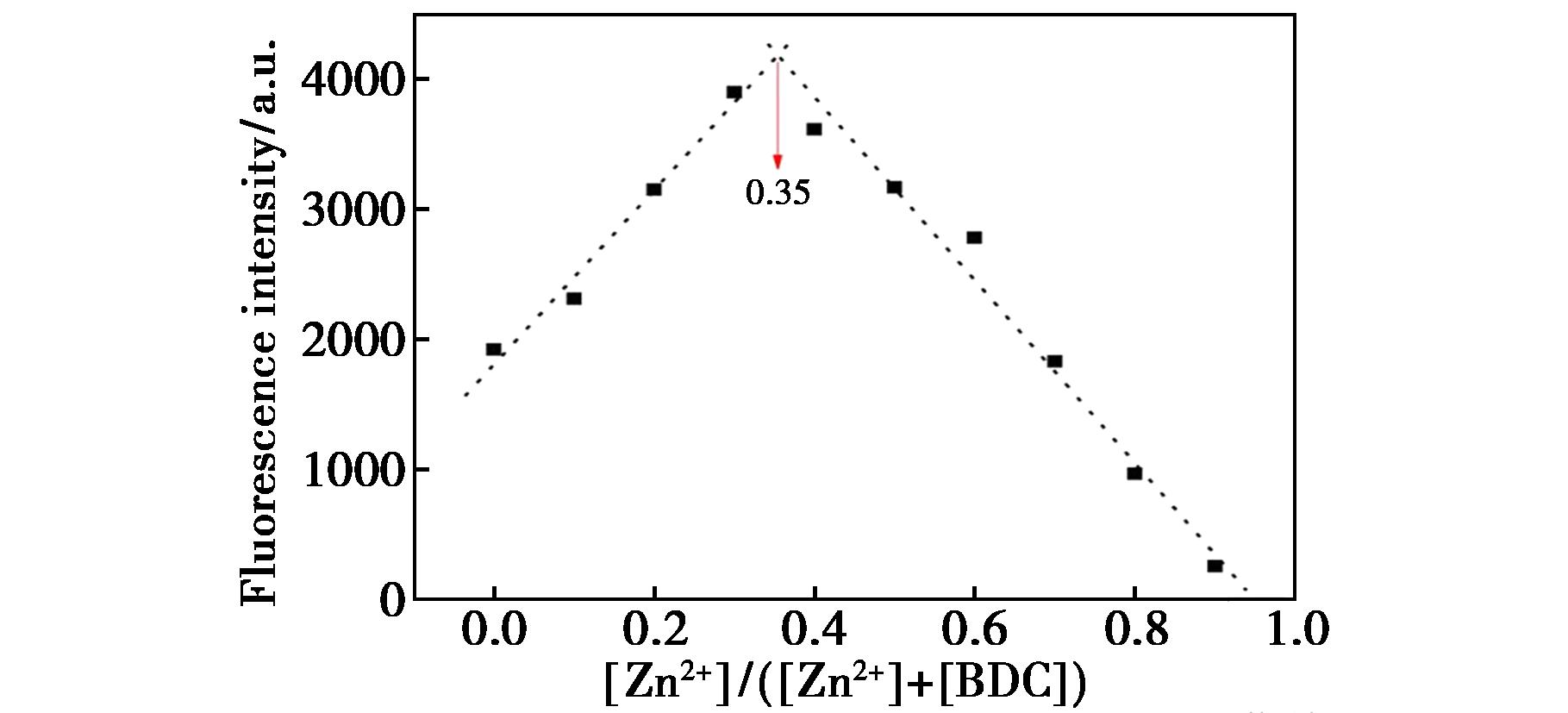
图5 BDC与Zn2+结合的Job′s Plot曲线
Fig.5 Job′s plot of the binding between of BDC and Zn2+
为了进一步研究探针与Zn2+的配位结合关系,在无水乙醇-水体系中培养获得BDC-Zn配合物晶体,通过X-射线单晶衍射获得配合物的晶体结构(图6)。X-射线单晶衍射分析表明,BDC-Zn属于三斜晶系,P-1空间群。不对称单元中含有1个Zn2+离子、1个BDC配体、1个端基配位的乙醇分子以及1个游离的![]() 离子。其中Zn2+离子位于对称点上。Zn2+离子采取扭曲的cis-N2O4八面体构型,与来自于2个BDC配体上的2个O原子(O12,O12A A:-x,-y+1,-z.)和2个N原子(N5,N5A)以及2个乙醇分子(O3,O3A)配位,形成1个中心对称的单核[Zn(BDC)2(EtOH)2]2+配位单元,外围游离的
离子。其中Zn2+离子位于对称点上。Zn2+离子采取扭曲的cis-N2O4八面体构型,与来自于2个BDC配体上的2个O原子(O12,O12A A:-x,-y+1,-z.)和2个N原子(N5,N5A)以及2个乙醇分子(O3,O3A)配位,形成1个中心对称的单核[Zn(BDC)2(EtOH)2]2+配位单元,外围游离的![]() 离子起到平衡电荷的作用。相邻的[Zn(BDC)2(EtOH)2]2+配位单元通过π-π堆积以及与
离子起到平衡电荷的作用。相邻的[Zn(BDC)2(EtOH)2]2+配位单元通过π-π堆积以及与![]() 离子之间的氢键、静电作用相互堆积,形成三维超分子结构。相关晶体数据见表1,配位作用相关的键长键角见表2。
离子之间的氢键、静电作用相互堆积,形成三维超分子结构。相关晶体数据见表1,配位作用相关的键长键角见表2。
表2 BDC-Zn的部分键长(Å)和键角(°)
Tab.2 Selected bond lengths (Å) and bond angles (°) of BDC-Zn
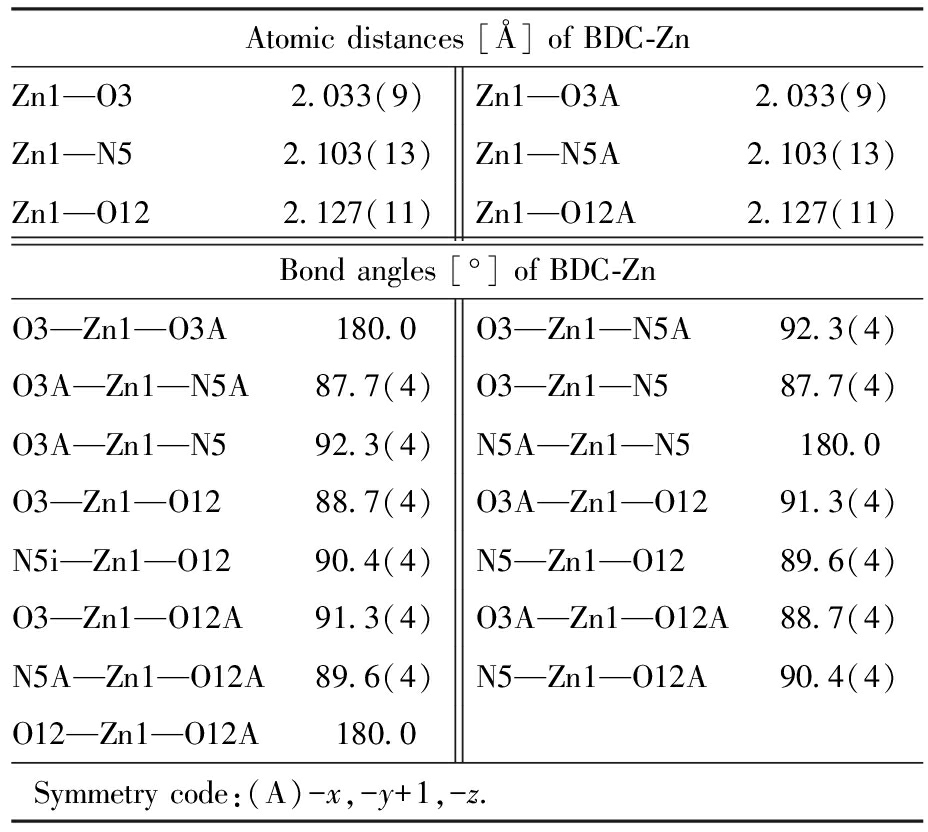
Atomic distances [Å] of BDC-ZnZn1—O32.033(9)Zn1—O3A2.033(9)Zn1—N52.103(13)Zn1—N5A2.103(13)Zn1—O122.127(11)Zn1—O12A2.127(11)Bond angles [°] of BDC-ZnO3—Zn1—O3A180.0O3—Zn1—N5A92.3(4)O3A—Zn1—N5A87.7(4)O3—Zn1—N587.7(4)O3A—Zn1—N592.3(4)N5A—Zn1—N5180.0O3—Zn1—O1288.7(4)O3A—Zn1—O1291.3(4)N5i—Zn1—O1290.4(4)N5—Zn1—O1289.6(4)O3—Zn1—O12A91.3(4)O3A—Zn1—O12A88.7(4)N5A—Zn1—O12A89.6(4)N5—Zn1—O12A90.4(4)O12—Zn1—O12A180.0 Symmetry code:(A)-x,-y+1,-z.
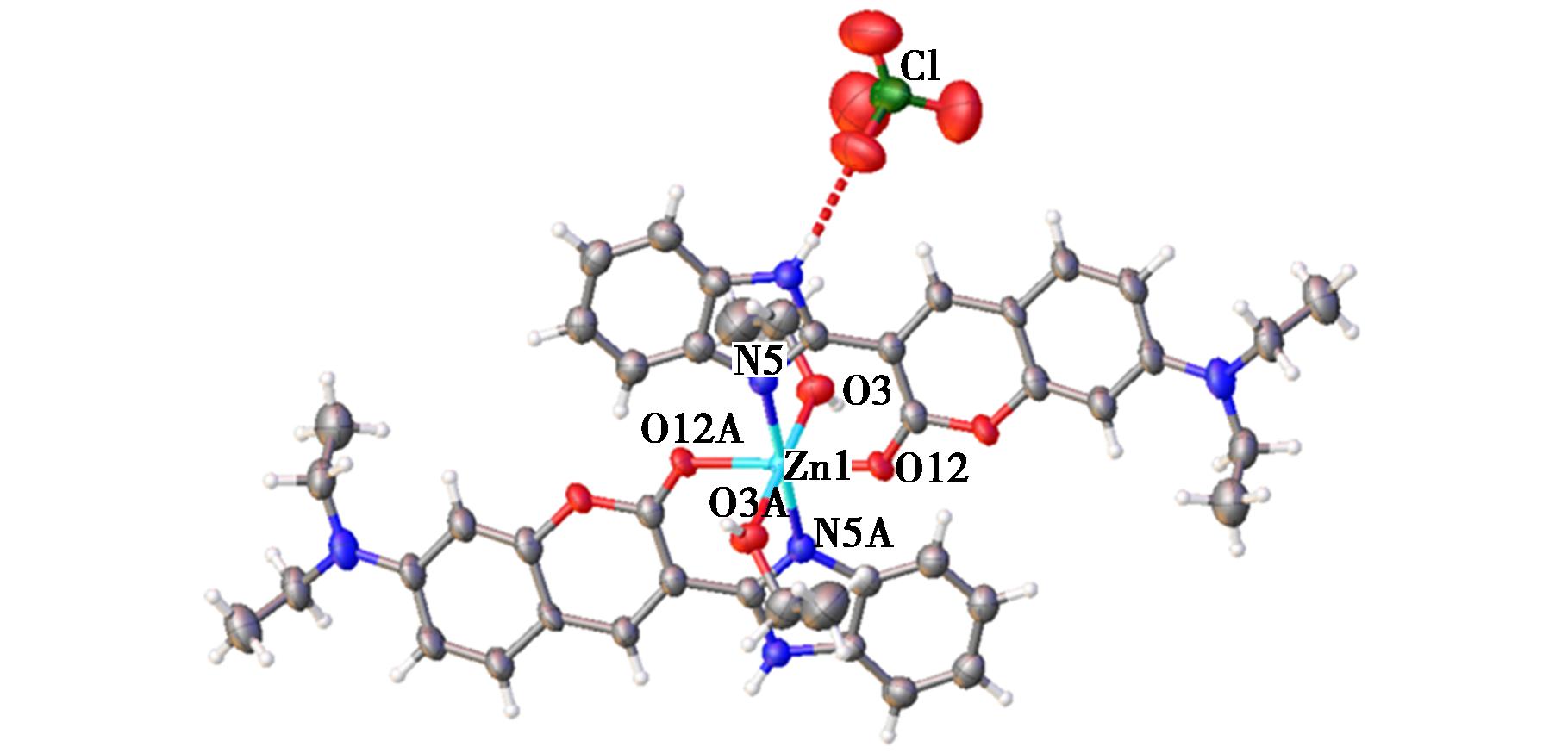
图6 配合物BDC-Zn的单晶结构图
Fig.6 Single crystal structure of compound BDC-Zn
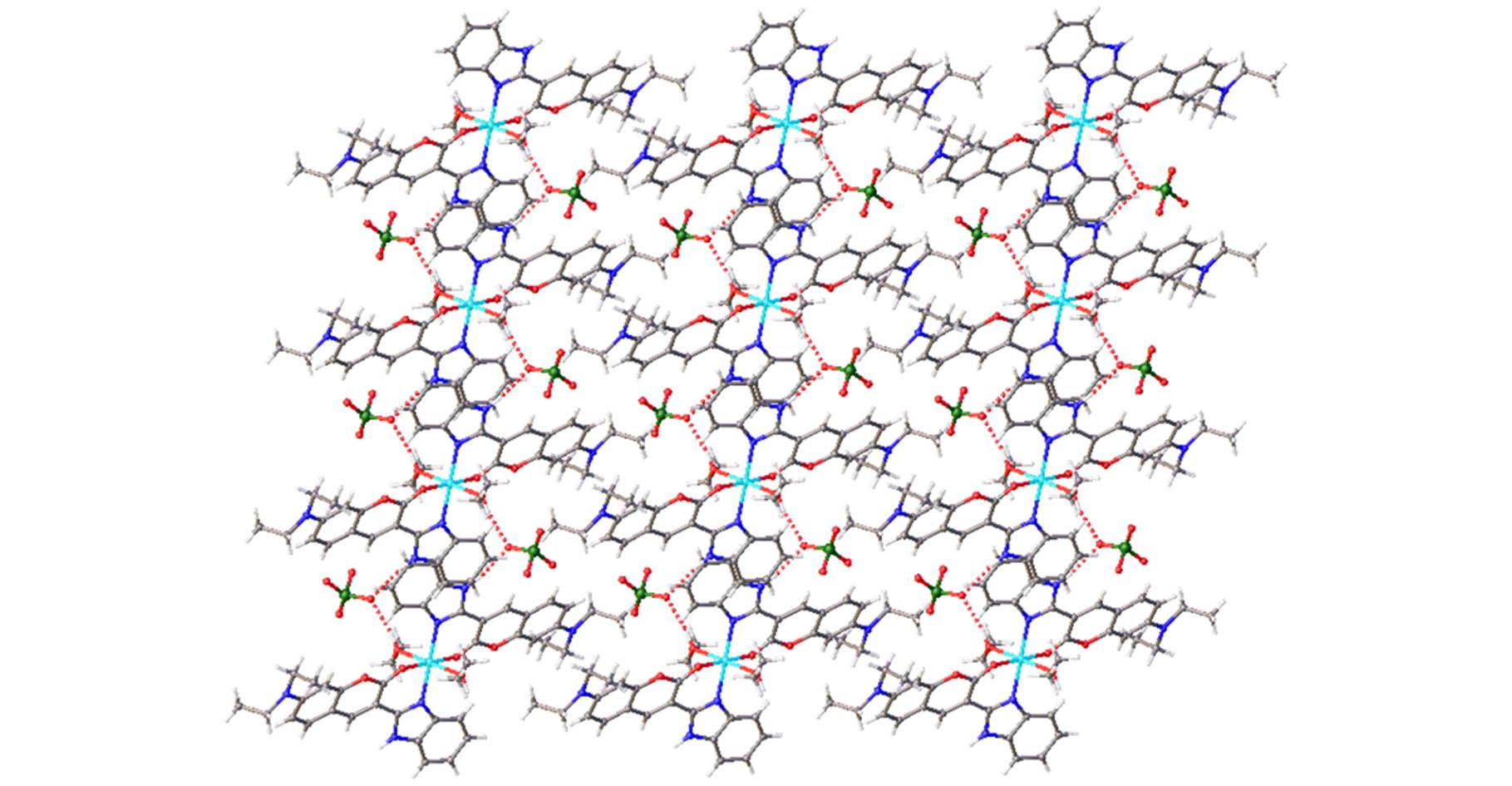
图7 BDC-Zn的晶体堆积图
Fig.7 Crystal packing structure of BDC-Zn
结合Job′s曲线(结合比验证)与X-射线单晶衍射结果可知,探针BDC对Zn2+的识别机理应该是配位抑制探针分子的分子内质子转移(ESIPT)过程,触发螯合荧光增强(CHEF)效应[21,22]。自由态BDC分子中,咪唑环上的N—H键与相邻酮羰基的C![]() O键形成分子内氢键(N—H…O
O键形成分子内氢键(N—H…O![]() C);在光激发下,BDC进入激发态后,分子内质子会从咪唑N原子转移至酮羰基O原子,发生 ESIPT过程,该过程会导致激发态能量通过“非辐射跃迁”耗散,因此,自由态BDC的荧光强度低。当BDC的咪唑N原子和酮羰基O原子与Zn2+配位后限制了BDC配体的旋转和振动,抑制ESIPT的非辐射跃迁耗散。而Zn2+的正电荷会吸引BDC的电子云向配位中心偏移,优化其前线分子轨道能级差,使荧光发射更易发生,构成螯合荧光增强(CHEF)效应[23]。
C);在光激发下,BDC进入激发态后,分子内质子会从咪唑N原子转移至酮羰基O原子,发生 ESIPT过程,该过程会导致激发态能量通过“非辐射跃迁”耗散,因此,自由态BDC的荧光强度低。当BDC的咪唑N原子和酮羰基O原子与Zn2+配位后限制了BDC配体的旋转和振动,抑制ESIPT的非辐射跃迁耗散。而Zn2+的正电荷会吸引BDC的电子云向配位中心偏移,优化其前线分子轨道能级差,使荧光发射更易发生,构成螯合荧光增强(CHEF)效应[23]。
为验证探针BDC在实际样品基质中对Zn2+的检测适用性,采用标准加入回收法开展实验,选择实验室自来水、百色右江河河水2种水样作为检测对象,考察不同基质条件下BDC对Zn2+的定量准确性与精密度,实验结果如表3所示。由表3数据可知,在2种水样基质中,向体系中加入不同浓度水平的外源Zn2+标准溶液后,Zn2+的回收率均稳定在90%~110%范围内,相对标准偏差(RSD)在3.7%~5.1%之间(大部分低于5%),说明探针DBC能对实际水样中的Zn2+有高选择性,可进行荧光定量检测。
表3 不同水样中测定Zn2+
Tab.3 Detection of Zn2+ in various water samples
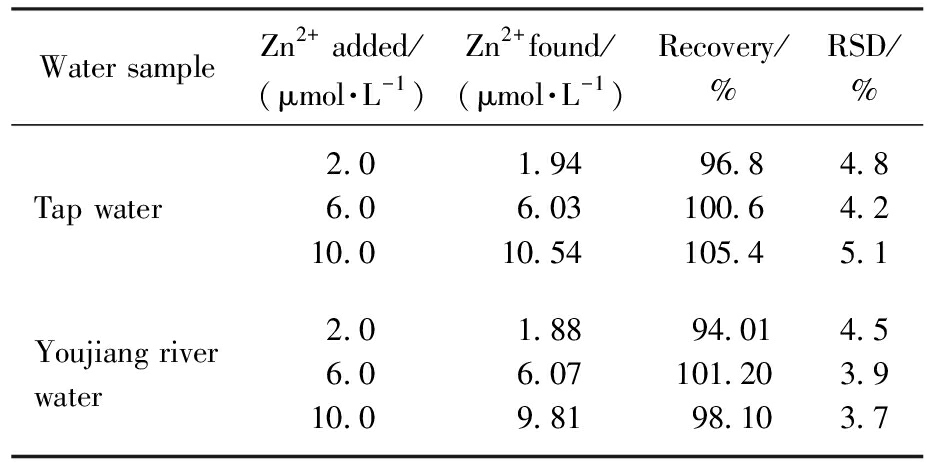
Water sampleZn2+ added/(μmol·L-1)Zn2+found/(μmol·L-1)Recovery/%RSD/%Tap water2.06.010.01.946.0310.5496.8100.6105.44.84.25.1Youjiang river water2.06.010.01.886.079.8194.01101.2098.104.53.93.7
本研究发现香豆素7荧光探针对Zn2+表现出优异的选择性和灵敏性,Zn2+的加入可显著增强BDC的荧光强度,响应迅速,且对多种共存离子表现出较强的抗干扰能力。探针BDC识别Zn2+的检出限为0.117 μmol/L,可测实际水样中Zn2+含量,其作用机制源于探针与Zn2+之间发生配位反应,产生的荧光螯合增强作用(CHEF)。在乙醇-水体系中培养获得BDC-Zn晶体,单晶结构分析证实了BDC与Zn2+之间的结合比(2∶1)。本研究不仅拓展了香豆素类探针在金属离子检测中的应用,也为开发新型高效Zn2+识别材料奠定了实验与理论基础。
[1]Qin J J,Qiang J F,Liu C X.J.South-Central Univ.Natl(Nat.Sci.Edition),2007,26(1):7-9.
覃建军,蒋剑飞,柳畅先.中南民族大学学报(自然科学版),2007,26(1):7-9.
[2]Tuo X,Yang W Y,Liu C X.Chem.Res.Appl.,2006,18(7):884-885.
庹浔,杨雯雁,柳畅先.化学研究与应用,2006,18(7):884-885.
[3]Zhao Y J,Zhao L,Su Y.Chin.J.Cell Biol.,2020,42(9):1 631-1 641.
赵又佼,赵龙,苏颖.中国细胞生物学学报,2020,42(9):1 631-1 641.
[4]Christos T C,Panagoula-stamatina A N,Chara A S,Maria E.S.Arch.Toxicol.,2020,94(5):1 443-1 460.
[5]Gosi M,Kumar A C,Sunandamma Y.J.Fluoresc.,2022,32(6):2 379-2 393.
[6]Isaad J,Achari A E L.Opt.Mater.,2022,127:112 275.
[7]Wang X Y,Meng Z Y,Tian X C,Kou J L,Xu K,Wang Z L,Yang Y Q.Spectrochim.Acta Part A:Mol.Biomol.Spectrosc.,2023,292:122 378.
[8]Wang Y,Zhu X Y,Huai Y,Cui T,Li C,Liu Y,Gao Y.Chin.J.Lumin.2025,46(1):185-193.
王晔,朱鑫玥,怀玉,崔彤,李超,刘洋,高云.发光学报,2025,46(1):185-193.
[9]Xiao J Y,Zhu X Y,Xu Y,Sun H Y,Huang L F,Li C,Gao Y,Gao Y,Zhong S.Acta Optica Sinica,2025,45(3):270-280.
肖嘉扬,朱鑫玥,徐艺,孙宏阳,黄丽帆,李超,高妍,高云,钟声.光学学报,2025,45(3):270-280.
[10]Chen Y H,Feng Y Q,Yan K X,Yuan M Y,Xu K X.Chem.Res.,2025,36(2):134-139.
陈义豪,冯怡强,燕凯翔,袁梦瑶,徐括喜.化学研究,2025,36(2):134-139.
[11]Sheng X,Yan W H,Xie D,Zhang Y W,Zhang C L,Wang S X.Chin.J.Anal.Lab.,2023,42(2):235-240.
盛筱,晏文慧,谢丹,张艺雯,张传蕾,王守信.分析试验室,2023,42(2):235-240.
[12]Shun X F,Zhu Y Y,Xie X H,Sheng X,Wang S X.Chem.Reagents,2024,46(10):52-57.
孙新峰,朱奕妍,解晓华,盛筱,王守信.化学试剂,2024,46(10):52-57.
[13]Gao H,Hu Z W,Ma Z Y,Zu H Q,Cai X H,Bao D M,Zhang Y P.Chem.Reagents,2024,46(10):44-51.
高桓,胡紫雯,马振宇,祖红桥,蔡小华,宝冬梅,张玉鹏.化学试剂,2024,46(10):44-51.
[14]Zhou W,Pan Y J,Cao Y,Wu A B,Shu W M,Yu W C.Chem.Res.Appl.,2023,35(12):2 908-2 914.
周五,潘远江,曹语,吴爱斌,舒文明,余维初.化学研究与应用,2023,35(12):2 908-2 914.
[15]Xu Y,Zhang Y,Zeng J Z,Wang X,Xue L,Wang H B.Chem.Res.Appl.,2023,35(9):2 092-2 098.
徐阳,张杨,曾俊柱,王欣,薛蕾,王海滨.化学研究与应用,2023,35(9):2 092-2 098.
[16]Li Z Y,Qin H P,Zhu H Y,Fan X,Yuan L.Chin.J.Inorg.Chem.,2022,38(7):1 291-1 298.
李中燕,覃海波,朱洪宇,樊旭,袁霖.无机化学学报,2022,38(7):1 291-1 298.
[17]Zhan J Y,Zhao J,Gan C F,Huang Y M.Chem.Reagents,2025,47(2):33-38.
展军颜,赵杰,甘春芳,黄燕敏.化学试剂,2025,47(2):33-38.
[18]Hou X Q,Wang Y J,Shang G F,Wang H J,He S H.Mater.Rep.,2025,39(5):267-272.
侯学清,王燚婧,尚光富,王环江,何淑花.材料导报,2025,39(5):267-272.
[19]Zhang L,Liu Q,Zhang Y T,Xu Q G,Gu P C,Gan Y J.Chem.Res.Appl.,2022,34(11):2 671-2 679.
张量,刘倩,张艳涛,徐启贵,辜鹏程,甘勇军.化学研究与应用,2022,34(11):2 671-2 679.
[20]Li N,Li Z,Wang S J,Chen Y,Xiao L W.Chin.J.Anal.Lab.,2023,42(10):1 311-1 316.
李娜,李政,王树军,陈钰,肖立伟.分析试验室,2023,42(10):1 311-1 316.
[21]Zhang Y G,Zhang H Y,Zhao F R,Rao H H,Xie Y J,Liu W S.Chin.J.Anal.Lab.,2025,44(9):1 365-1 368.
张艳阁,张红月,赵付荣,饶欢欢,谢勇捷,刘伟生.分析试验室,2025,44(9):1 365-1 368.
[22]Rabiul A,Tarun M,Rahul B,Atul K,Keya C H,Mahammad A.RSC Adv.,2016,6:1 268-1 278.
[23]Ni L,Zhang S T,Zou F,Li Z Y,Yuan L.Mod.Chem.Ind.,2023,43(12):242-245.
倪赖,张胜婷,邹菲,李中燕,袁霖.现代化工,2023,43(12):242-245.