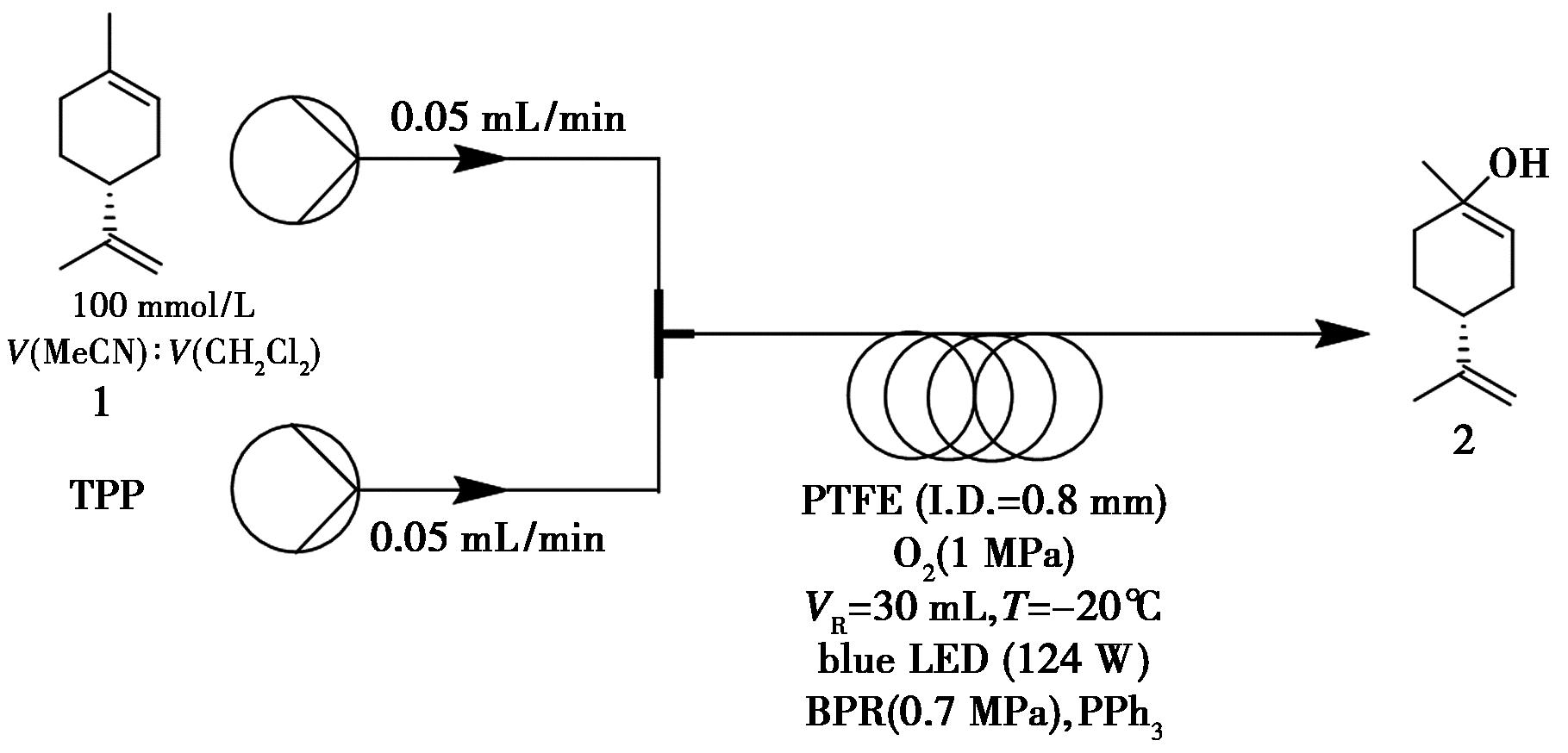
图1 大麻素中间体2的连续流合成路线
Fig.1 Continuous flow synthetic route of cannabidiol intermediate 2
传统反应釜受其结构限制,在反应过程中常存在多项安全隐患与技术瓶颈。例如,剧烈放热反应或气态产物的生成容易造成系统内外压力失衡,增加操作风险;搅拌浆的类型、浆叶尺寸与搅拌幅度若设计不当,则可能导致反应物料混合不均,降低目标产物选择性;此外,长时间的反应停留易使产物发生分解或变质,影响最终产率。在大规模生产过程中,反应釜占用空间大、废物产生量多,也显著推高了生产成本。相比之下,连续流技术凭借其模块化与可精密调控的结构特点,能够有效缓解上述问题。同时,结合光催化与电催化协同作用的反应体系,可减少传统催化剂的使用量与污染,推动绿色合成工艺的发展。
连续流合成技术是一种区别于传统间歇式反应的新型合成方法,其核心特征在于反应物料以连续流动的方式通过反应器完成化学反应[1,2]。该技术在化工与制药等领域表现出显著优势。在连续流体系中,物料的流动状态(如层流或湍流)对反应物混合效率、传热行为及产物分布具有决定性影响;通过调节反应器结构参数(如管径与长度)及流速,可实现对物料停留时间的精确控制[3],从而有效避免传统间歇工艺中因局部滞留引发的副反应。此外,较高的传质效率能够促进反应动力学过程,缩短体系达到平衡所需时间。
连续流技术安全性高。连续流技术属于本质安全型工艺,符合国家危化品安全生产规划及安全生产的政策导向。尤其适用于硝化、氯化、磺化、胺基化、重氮化、加氢、烷基化、氧化等18类国家重点监管的危险工艺。该技术可显著提升过程安全性,为高危反应的规模化实施提供了可行路径。
绿色化学特性突出。通过精确调控反应参数,连续流工艺能够显著减少溶剂消耗与副产物的生成,符合绿色化学原则,助力清洁生产。
高效性显著。在医药中间体合成中,连续流技术可将传统间歇反应耗时从数小时压缩至分钟级别,并提高反应产率10%~30%。以吉利德科学的HIV药物合成为例,采用连续流硝化工艺替代原有批次方式,生产效率获得大幅提升。
连续流技术产业化应用优势明显。该技术能够大幅缩短从项目设计到投产的建设周期,节约能耗并提高经济效益;同时减少场地占用,提升土地利用率,加快工艺放大进程,推动自动化与智能化制造。连续流技术符合国家“创新、协调、绿色、开放、共享”的新发展理念,并与多项产业升级政策高度契合。
在液-液、气-液等多相反应体系中,常面临相界面传质限制所带来的相分离问题。可通过优化反应器结构(如内置静态混合单元)或采用新型微结构反应器以增强界面接触,提高传质效率。
对于连续流中的催化反应,催化剂稳定性与循环使用性能仍是当前面临的挑战,尤其在长时间运行过程中易发生失活,且其分离与回收工艺尚需进一步的技术突破。
反应过程中残留试剂或副产物的连续积累可能造成交叉污染,进而引起催化剂中毒或最终产物纯度降低。
随着光电催化技术的迅速发展,光催化与电化学方法同连续流反应相结合的应用日益增多。该类集成策略不仅可缓解催化剂的失活问题、简化分离流程,还能通过对反应过程进行精准调控,显著强化反应速率与整体效率。
大麻及其活性成分的医疗价值近年来在基础研究与药物研发领域受到广泛关注[4,5]。Aguillón等[6]将光催化与连续流技术相结合,开发出一种高效合成大麻素关键中间体的新方法。在已有实验条件的基础上,研究发现采用氯化溶剂体系可显著提高光氧化反应的转化效率,选用二氯甲烷与乙腈的混合溶剂(CH2Cl2:MeCN)。具体反应条件为:以100 mmol/L(R)-柠檬烯作为底物1,0.1 mmol/L TPP为光敏剂,氧气作为氧化剂,溶剂比例为V(CH3CN)∶V(CH2Cl2)=3∶1,在-20 ℃恒温条件下,采用100 W蓝色LED光源进行催化,反应物料以0.05 mL/min的流速通过反应器,最终实现99%的底物转化率(对应化合物2)。该体系经放大实验验证具有良好的稳定性,时空产率达到580.8 μmol/min(图1)[6]。

图1 大麻素中间体2的连续流合成路线
Fig.1 Continuous flow synthetic route of cannabidiol intermediate 2
大麻素中间体用于各种罕见儿童疾病和其他疾病的治疗展现出极高的商业价值,预计2025年的销售额将超过240亿美元,可推动创造30万个工作岗位[6]。
在化学研究与工业应用中,氧化反应一直受到广泛重视[7]。传统氧化方法常采用二氧化锰(MnO2)作为氧化剂[8-10],但该方法往往伴随大量副产物的生成,环境负担较重。相比之下,使用氧气作为氧化剂更符合绿色化学原则。特别是直接利用空气而非高纯氧气,不仅可显著降低成本,还能有效缓解纯氧体系的安全风险[11]。Bannon等[12]发展了一种基于有氧光氧化策略,成功将苯并类底物转化为相应的酮或醛。经过系统条件优化,最终确定反应体系如下:将二苯基甲烷(3)溶于乙腈与水的混合溶剂(V(MeCN)∶V(H2O)=3∶1)中,以1 mL/min的流速进样,空气流速设定为24.8 mL/min,以确保反应体系中存在2.2 eq.的氧气。在50 ℃反应温度及蓝色LED光照条件下,总停留时间为54.4 s,最终通过 1HNMR分析测得二苯基甲烷转化为二苯基甲酮(4)的转化率达到92%(图2)。
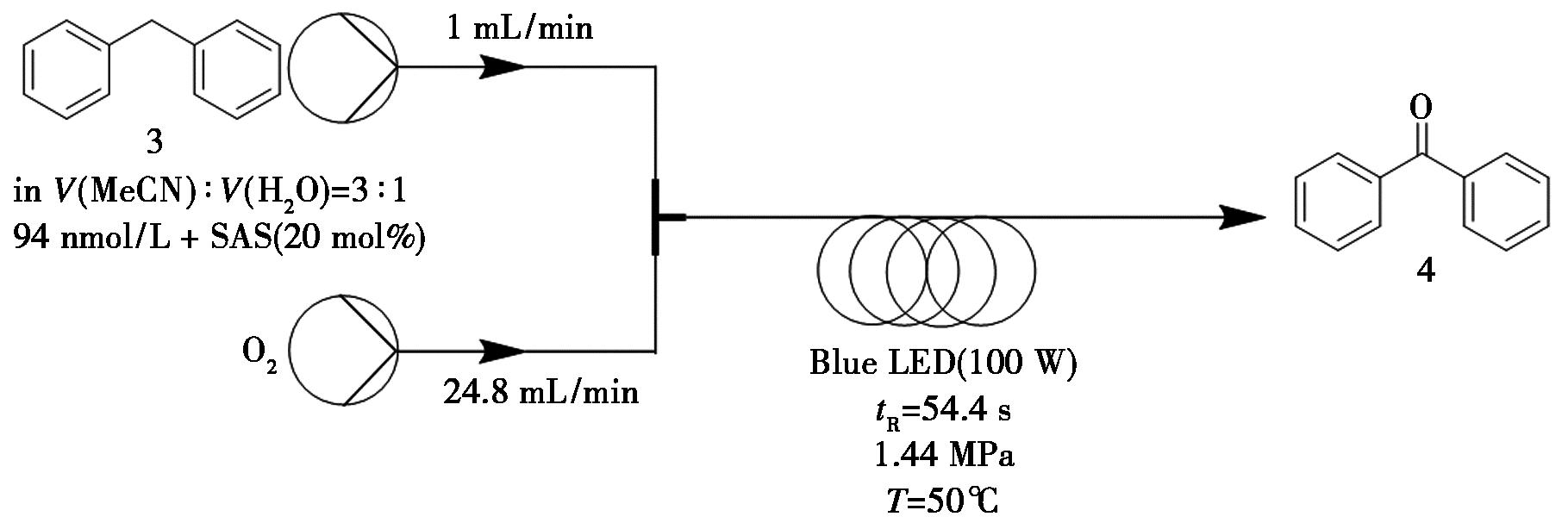
图2 以二苯基甲烷为原料的二苯基甲酮4的连续流合成路线
Fig.2 Continuous flow synthetic route of benzophenone 4 for diphenylmethane as starting material
烯烃氧化裂解是合成羰基化合物的重要反应路径,传统方法多依赖臭氧或贵金属催化剂,存在显著的安全隐患和环境负担[13-15]。Xiao等[16]开发了一种高效、简便的可见光催化烯烃氧化裂解新策略,采用氰基修饰的石墨相氮化碳催化膜(g-NCNCN)与CF3SO2Na组合,在氧气氛围中实现温和条件下的烯烃断裂。氰基修饰有效促进了单线态氧(1O2)及其他活性氧物种(ROS)的生成,相较于原始g-CN材料,其光催化氧化活性显著提升。在催化膜负载面积为9 cm2的反应器中,该体系相比常规液相催化反应,转化率提高了 7倍(达8.8 mmol/(g·h)),时空产率提升3倍(至2.5 g/h),并以85%的单程转化率高效生成二苯基甲酮(4,图3)。该方法不仅突破了现有烯烃氧化裂解反应的产能限制,也为绿色合成提供了新途径。
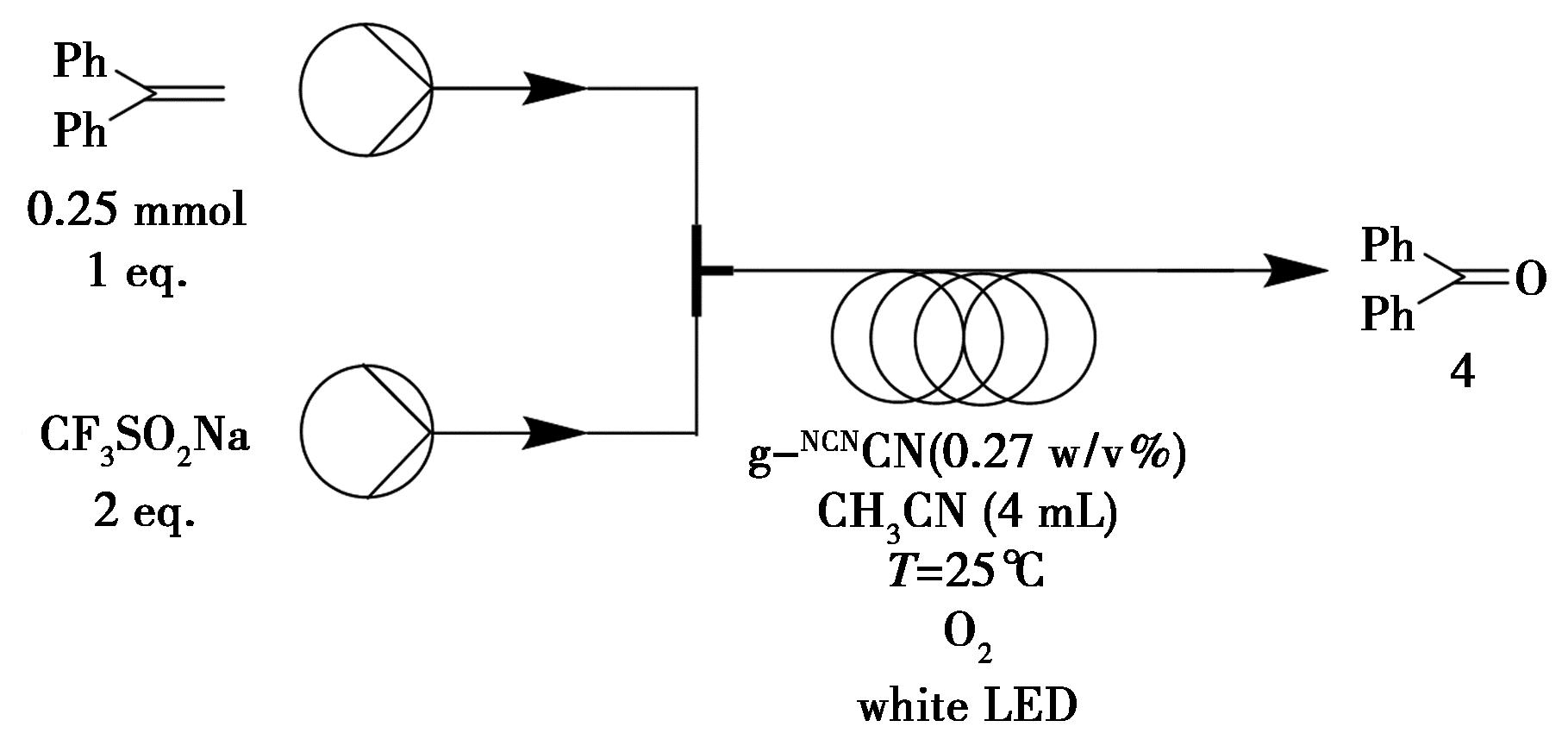
图3 以1,1-二苯基乙烯为起始原料的二苯基甲酮4的连续流合成路线
Fig.3 Continuous flow synthetic route of benzophenone 4 for 1,1-diphenylethylene as starting material
二苯基甲酮不仅可以用于紫外光固化体系中,还是多种药物活性成分的关键起始原料。
有机磷化合物作为重要的合成砌块,在药物分子设计、农用化学品中发挥着不可替代的作用[17]。Lapierre等[18]报道了一种可见光诱导的连续流磷酰化反应体系。该反应以碘苯甲醚(5,1.0 eq.)为底物,三乙胺(Et3N,2.0 eq.)作碱,亚磷酸三乙酯(P(OEt)3,2.0 eq.)作磷源,在 365 nm光源照射下,于30 ℃以0.1 mL/min的流速通过反应器,停留时间为200 min,最终以70%的产率得到目标磷酰化产物(6,图4)。
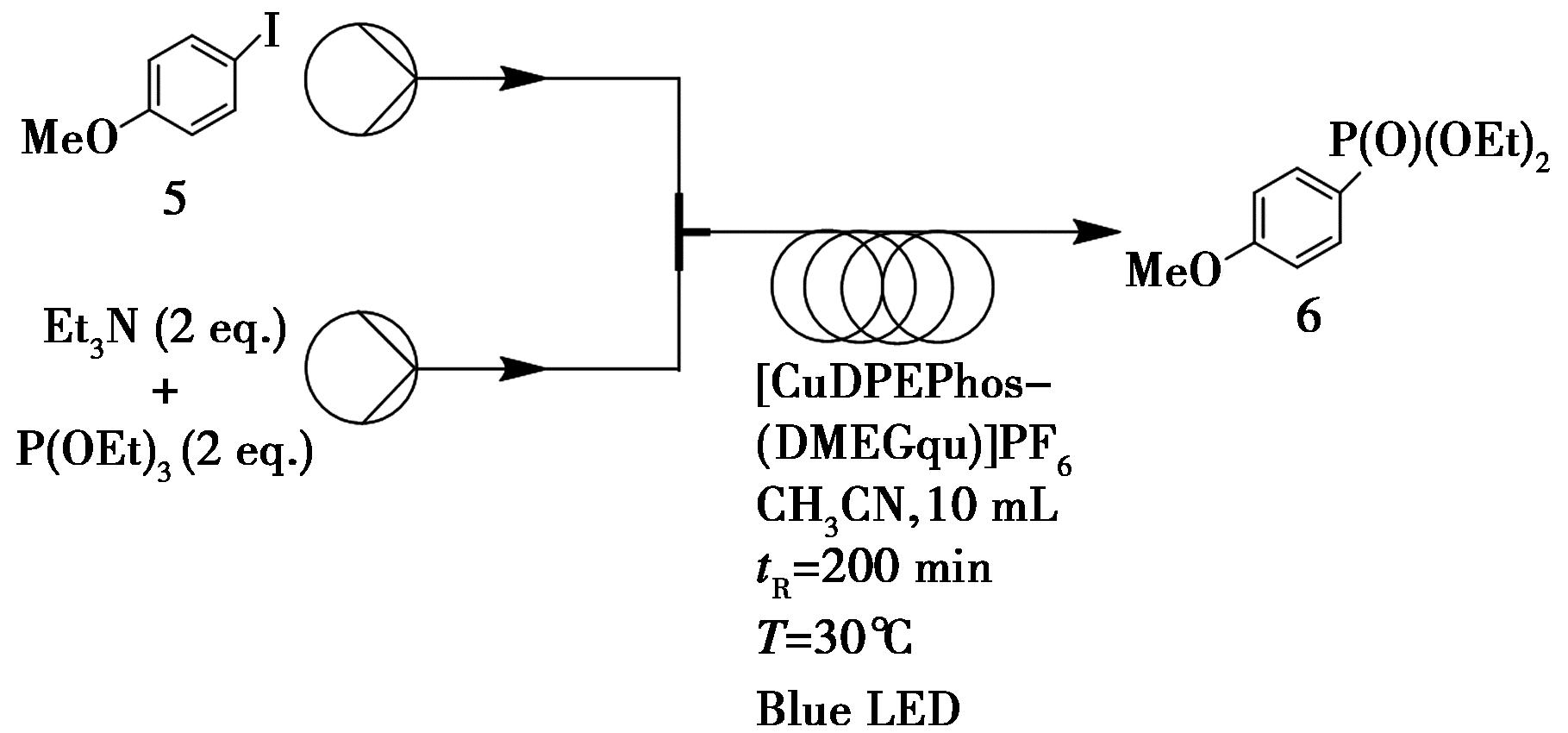
图4 磷化物6的连续流合成路线
Fig.4 Continuous flow synthetic route of phosphides 6
硫代吗啉是一类重要的药效团单元,因其表现出包括抗疟疾、抗菌、抗氧化及降血脂在内的多种生物活性,被广泛用于活性药物分子的构建。其典型代表药物Sutezolid(一种噁唑烷酮类抗生素)目前正处于治疗耐多药结核病的II期临床试验阶段[19]。然而,该化合物的现有合成路线在放大过程中存在显著安全隐患。针对这一问题,Steiner等[20]开发了一种两步连续流合成硫代吗啉的新工艺。该方法以廉价易得的半胱胺盐酸盐为起始原料,首先通过光催化硫醇-烯反应,在高浓度(4 mol/L)条件下仅使用微量(0.1~0.5 mol%)光催化剂9-芴酮(9-FL),即可定量获得中间体化合物7;随后经碱介导的环化反应高效合成硫代吗啉(8)。该流程经连续运行 7 h(总停留时间40 min),并结合蒸馏分离最终产物,验证了工艺的稳定性和可放大性(图5)。
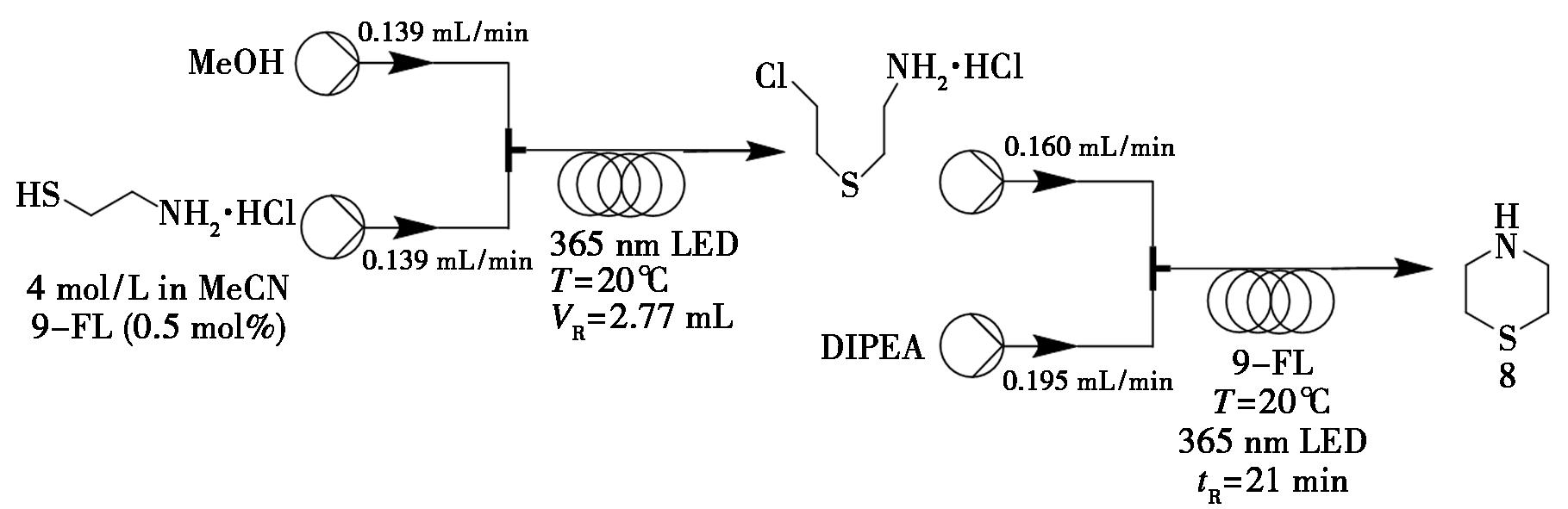
图5 硫代吗啉8的连续流合成路线
Fig.5 Continuous flow synthetic route of thiomorpholine 8
药物Sutezolid被认为是第一代治疗耐多药结核病利奈唑胺的理想替代药物,而硫代吗啉是合成过程中重要的成本因素。连续流合成硫代吗啉可以极大的降低用药成本,达到全民用药[20]。
喹啉衍生物广泛存在于天然产物及药理活性分子中,并表现出多样化的生物活性谱。尽管已有多种成熟合成策略(如Skraup反应、Doebner-von Miller反应和Friedlander反应),这些方法往往面临反应条件剧烈、区域选择性不理想或起始原料获取困难等问题,限制了其实际应用价值[21]。
针对上述挑战,Moln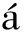 r等[22]开发了一种新型连续流合成策略,可用于多种3-取代喹啉的高效构建。经过系统条件优化,最终确定反应体系如下:将NBS(10)与HBr(5%)共同溶于二氯甲烷(DCM)中配制饱和溶液(0.165 mol/L),化合物9单独溶于0.047 mol/L DCM中,两股物料以2.05 mL/min的流速进样,停留时间为 2 min,反应在绿色LED光照下进行。在此条件下,3-氰基喹啉(11)的转化率达到77%。该体系在连续流动运行50 min后仍保持稳定,底物可实现完全转化,且目标产物的选择性维持在74%~78%之间(图6)。研究还进一步拓展了其他3-取代喹啉的合成,均取得良好效果,为该类化合物的高效合成提供了新途径。
r等[22]开发了一种新型连续流合成策略,可用于多种3-取代喹啉的高效构建。经过系统条件优化,最终确定反应体系如下:将NBS(10)与HBr(5%)共同溶于二氯甲烷(DCM)中配制饱和溶液(0.165 mol/L),化合物9单独溶于0.047 mol/L DCM中,两股物料以2.05 mL/min的流速进样,停留时间为 2 min,反应在绿色LED光照下进行。在此条件下,3-氰基喹啉(11)的转化率达到77%。该体系在连续流动运行50 min后仍保持稳定,底物可实现完全转化,且目标产物的选择性维持在74%~78%之间(图6)。研究还进一步拓展了其他3-取代喹啉的合成,均取得良好效果,为该类化合物的高效合成提供了新途径。
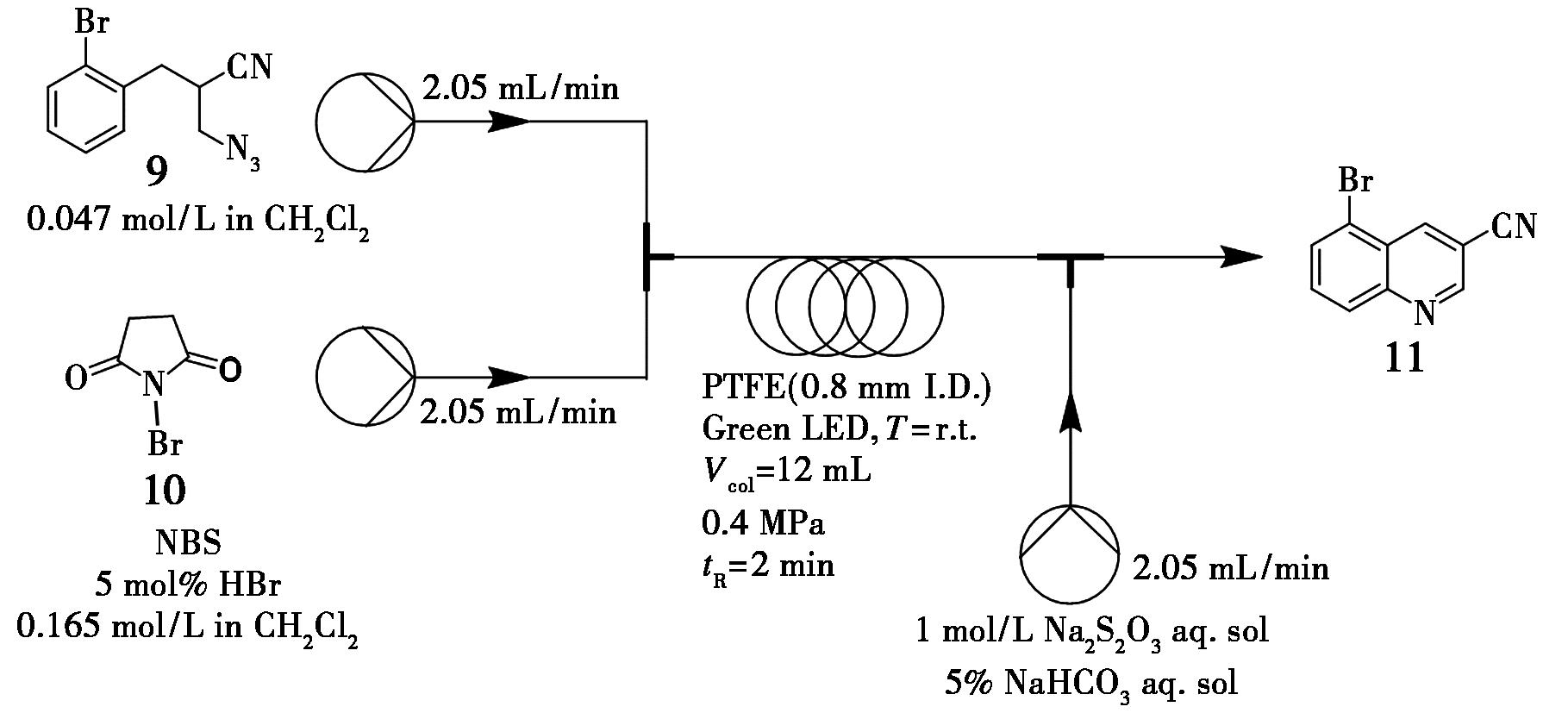
图6 3-氰基喹啉11的连续流合成路线
Fig.6 Continuous flow synthetic route of 3-cyanoquinoline 11
1,2-二氟苯是药物分子和农用化学品中重要结构单元,也是合成3,4-二氟硝基苯的关键前体,后者被广泛用于利奈唑胺、舒替唑胺和阿比维替尼等原料药的制备[23]。Simon等[24]开发了一种基于Balz-Schiemann反应的创新合成路径,以2-氟苯胺(12)为原料、HF/吡啶体系作为氟化试剂,通过连续流光催化诱导氟代脱氮反应高效合成1,2-二氟苯。该方法的核心优势在于采用高功率照明系统替代传统中压汞灯,在放大生产中表现出更优异的稳定性和反应效率,仅需10 min停留时间即可实现底物完全转化。与现有方法相比,该工艺在反应时间(10 min∶6~18 h)和转化率(>99%∶82%)方面均有显著提升,在最优条件下连续运行45 min,化合物14的产率可达1.9 g/h(图7)。
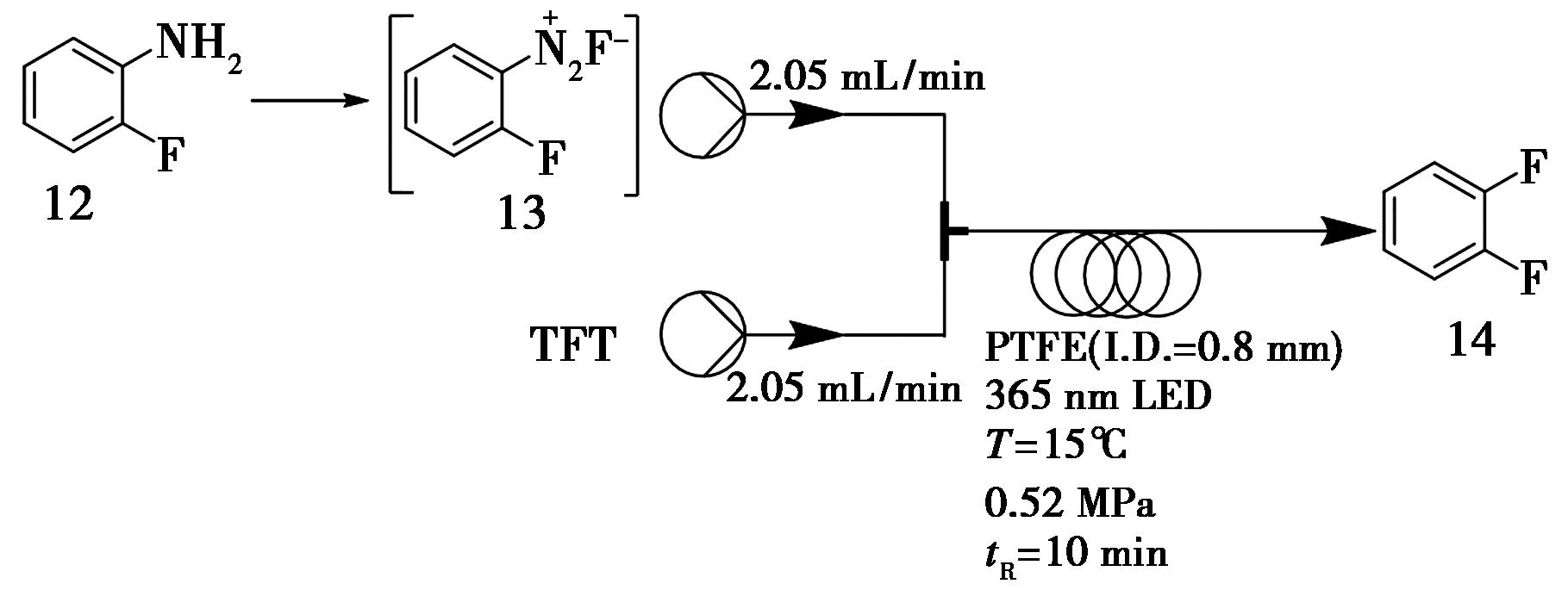
图7 1,2-二氟苯14的两步连续流合成路线
Fig.7 Continuous flow synthetic route of 1,2-difluorobenzene 14
传统合成1,2-二氟苯的过程中包含高温及重氮分解等危险工艺过程,存在巨大安全风险,连续流合成可大大降低生产过程中的安全隐患[24]。
羧基多环杂芳烃(以苯并吡喃和喹啉为代表)不仅表现出包括多巴胺激动剂特性、抗炎与抗癌活性在内的多种生物活性,还在材料科学中具有广泛应用前景。然而,现有合成方法通常依赖苛刻的反应条件和昂贵的过渡金属催化剂,限制了其进一步发展与应用[25]。针对这一挑战,Zhu等[26]开发了一种光催化自由基级联三环化策略,用于高效合成一系列结构新颖的磺化喹啉类化合物,并在连续流操作中实现了优异产率。该研究首先以苯并吡喃喹啉的合成为模型体系,采用化合物15作为自由基受体,DABCO·(SO2)2作为SO2源,烷基硫盐(16)或环丁酮试剂(17)作为自由基前体,在蓝色LED光照及连续流条件下,高效合成了化合物18和19(图8)。
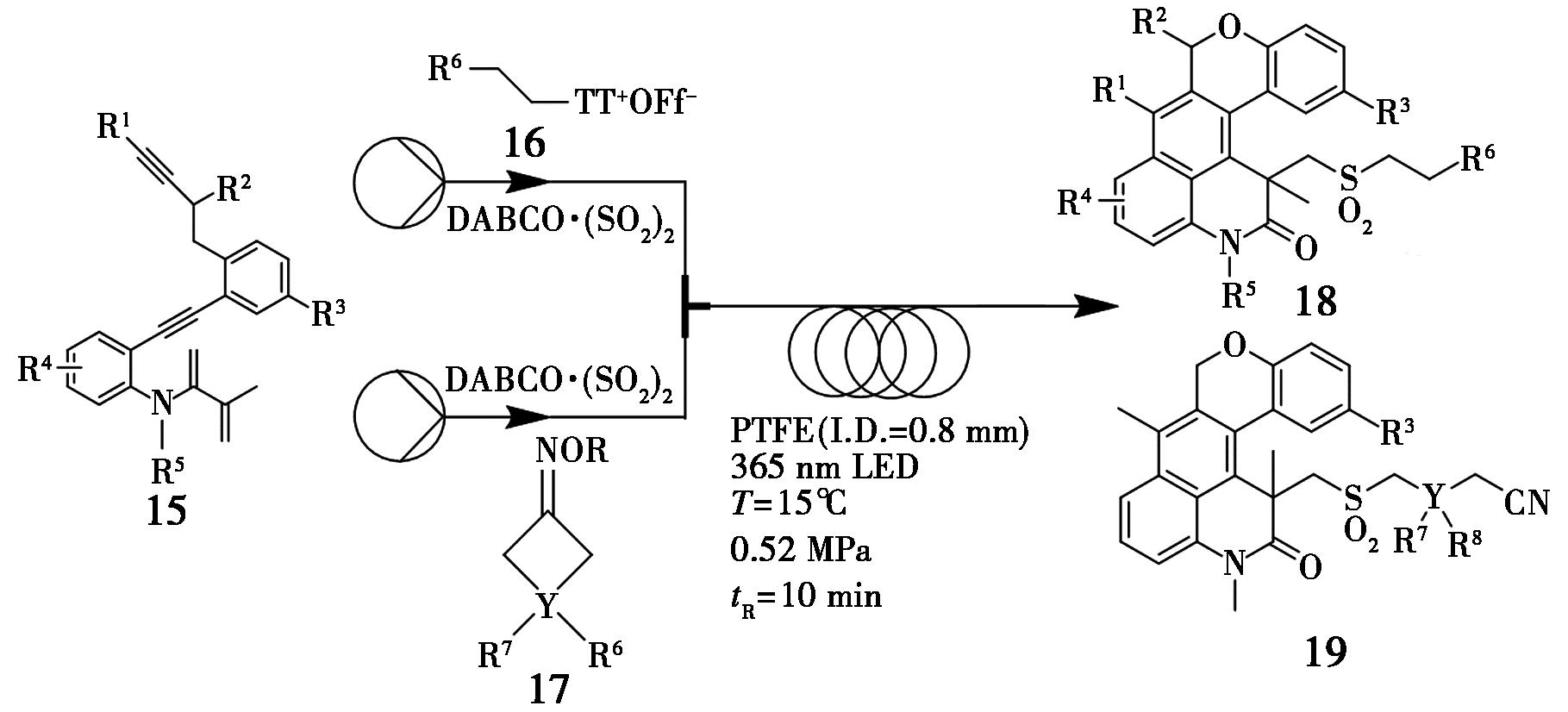
图8 磺化苯并吡喃喹啉17和18的连续流合成路线
Fig.8 Continuous flow synthetic route of chromenoquinolines 17 and 18
Zhu等[27]开发了一种基于光氧化还原催化的烷氧羰基化/三环化反应策略,以易得的烯二炔和烷基草酰氯为原料,在温和条件下通过自由基介导过程,高效构建了酯取代的多环N-杂芳烃骨架。该光催化方法在官能团兼容性、反应可扩展性以及环化/成键效率方面均表现出显著优势。通过引入连续流光催化技术,反应时间从传统批式工艺的12 h大幅缩短至40 min,合成效率显著提升。该研究使用物质的量分数为2% fac-Ir(ppy)3作为光催化剂,2.0 eq. 2,6-二甲基吡啶和烷基草酰氯(21,2.3 eq.)分别溶于DMF中。反应在容积为4.0 mL、内径0.6 mm的微通道反应器中进行,采用20 W蓝色LED(455 nm)为光源,室温下两股物料分别以50 μL/min的流速经Y型混合器进入光反应器,总流速为 100 μL/min,停留时间40 min。在该条件下,化合物22的产率达73%,显著优于批式反应的结果(12 h,产率65%)(图9)。
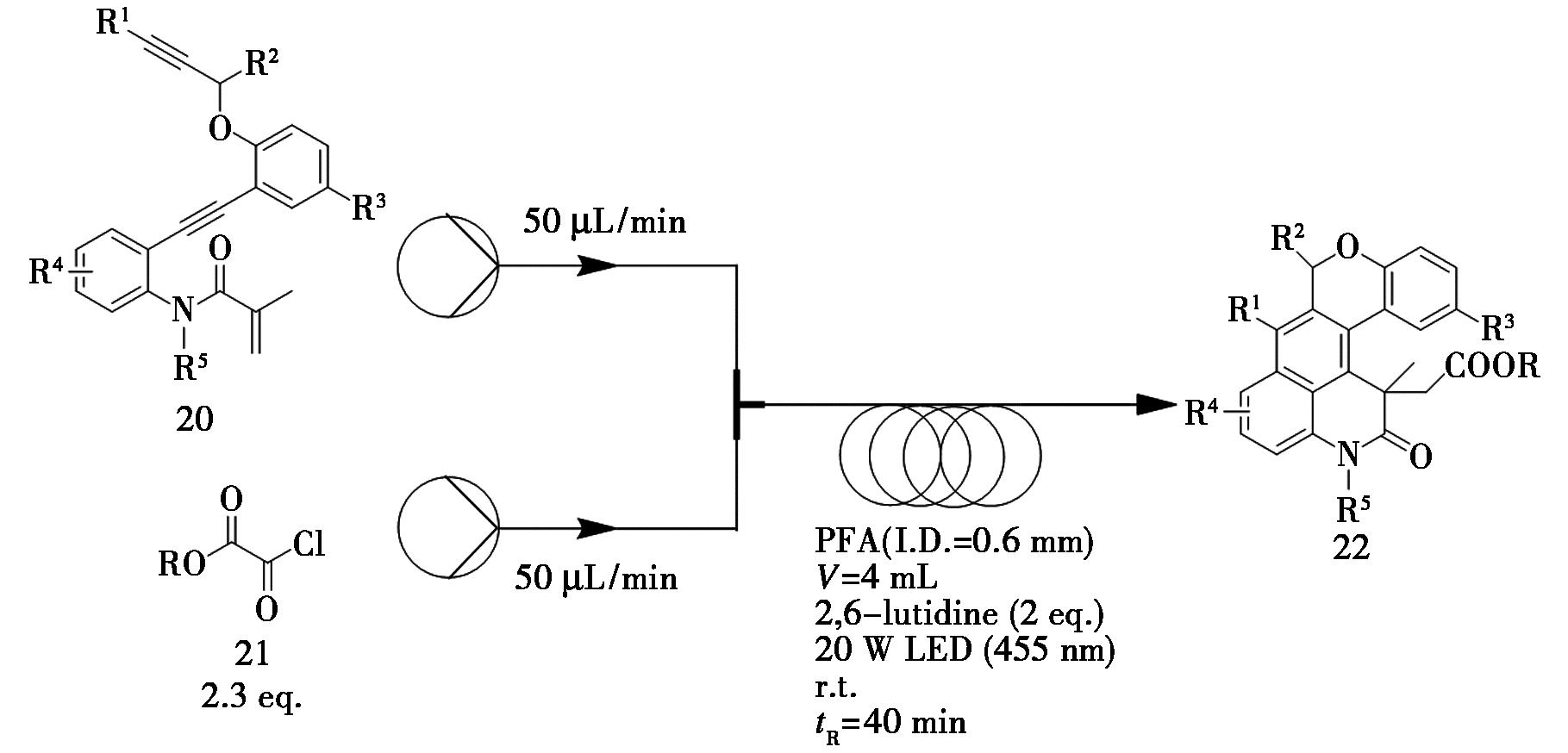
图9 N杂芳烃22连续流合成路线
Fig.9 Continuous flow synthetic route of N-heteroaromatic 22
氟化氨基酸因其独特的生物活性与药用潜力而受到广泛关注,常被用作生物示踪剂和分子探针等研究工具[28]。引入氟原子可增强分子的疏水性,因此在多肽类药物中引入含氟氨基酸有助于改善其热稳定性与化学稳定性,进而提升生物利用度和药理活性[29]。Liu等[30]报道了一种光催化合成三氟甲基化氨基酸的新方法。该方法以化合物23(0.1 mmol,1.0 eq.)和化合物24(0.1 mmol,1.0 eq.)为反应底物,乙腈(MeCN)作为溶剂,在微流反应器中于光催化条件下反应 2 h,可以90%的产率获得目标产物化合物25(图10)。
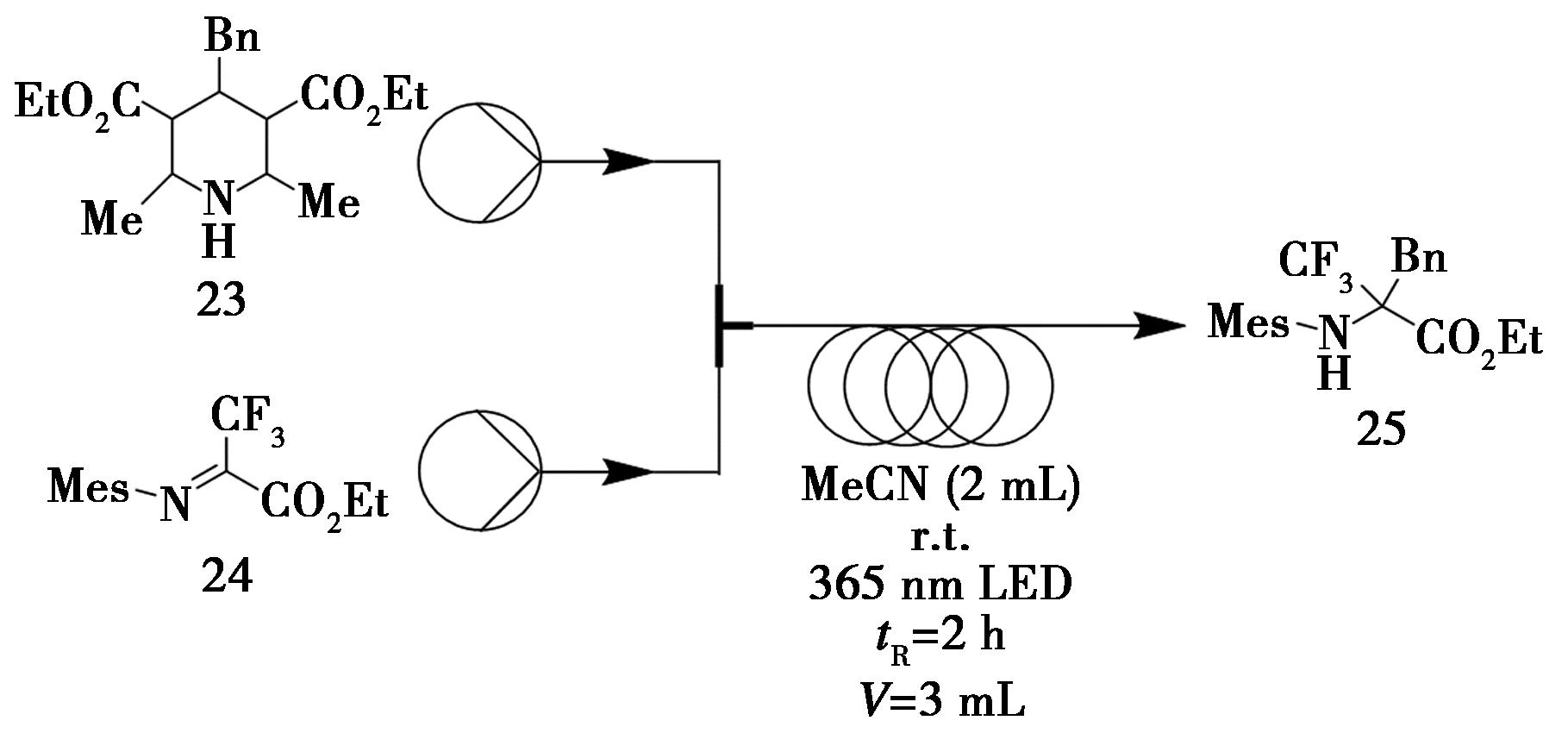
图10 三氟甲基氨基酸25的连续流合成路线
Fig.10 Continuous flow synthetic route of trifluoromethyl amino acid 25
羧酸因其商业性高、稳定性优异且易于合成等特点,常作为构建复杂分子骨架的起始原料[31,32]。Qin等[33]开发了一种绿色、高效的光氧化还原催化连续流策略,实现了羧酸与炔基溴的高效脱羧炔基化反应。该反应以化合物26(0.2 mmol,1.0 eq.)和化合物27(0.4 mmol,2.0 eq.)为反应物,碳酸钾(K2CO3,1.5 eq.)作碱,物质的量分数为2% 4CzIPN作光催化剂,二甲基亚砜(DMSO,2.0 mL)为溶剂。在室温条件下,采用蓝色LED(455 nm,50 W)作为光源,于内径为 600 μm的PFA材质微流反应管路中进行反应,流速设定为100 μL/min,最终以96%的产率获得化合物28(图11)。
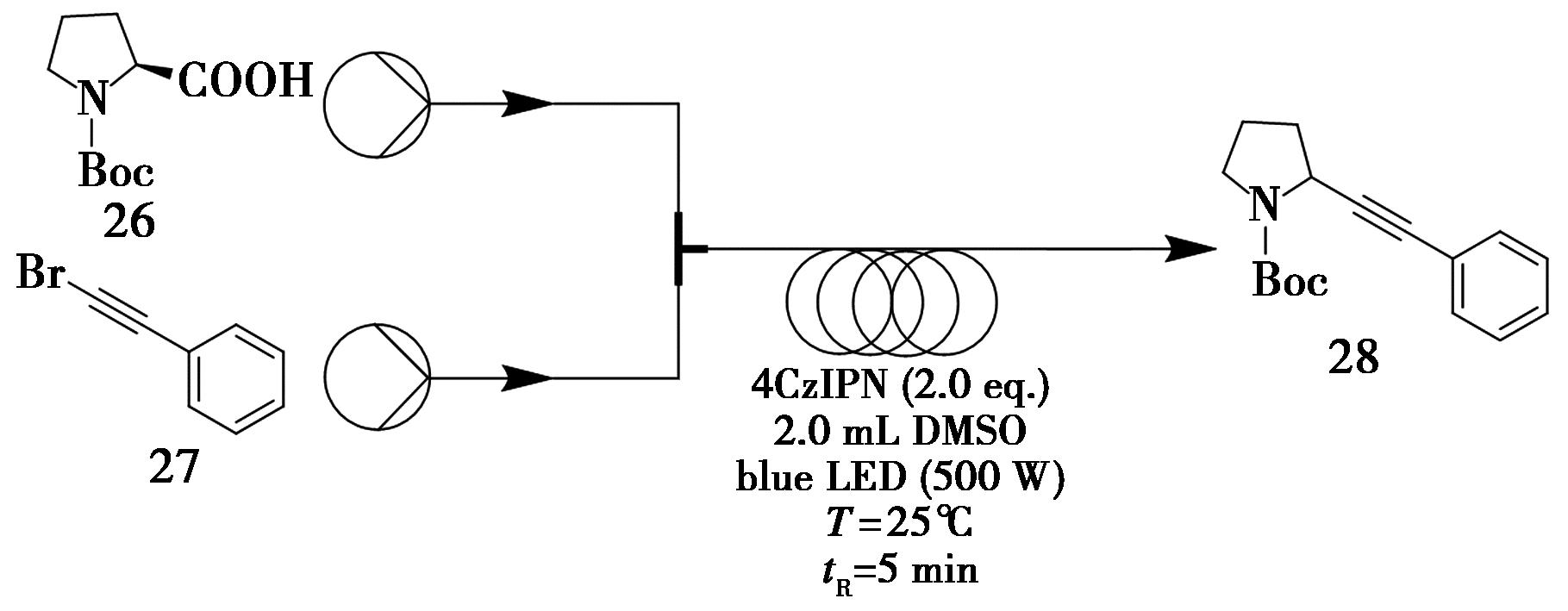
图11 脱羧炔基化合物28连续流合成路线
Fig.11 Continuous flow synthetic route of decarboxylative alkynylation 28
2-吡咯烷酮是多种生物活性分子中的重要结构单元,例如抗癫痫药物布立西坦和左乙拉西坦,以及用于治疗年龄相关记忆障碍的药物吡拉西坦和普拉西坦。Quertenmont等[34]将有机电合成与连续流技术相结合,开发出一种高效合成2-吡咯烷酮的新策略。研究采用3因素3水平实验设计,考察了底物浓度(33、66、99 mmol/L)、电流密度(41.66、62.50、83.33 mA/cm2)和流速(2、3、4 mL/min)对反应的影响。实验结果表明,在电流密度为41.66 mA/cm2、流速为4 mL/min、底物浓度为33 mmol/L的条件下,化合物31的产率达到73%,时空产率为0.13 g/h(图12)。
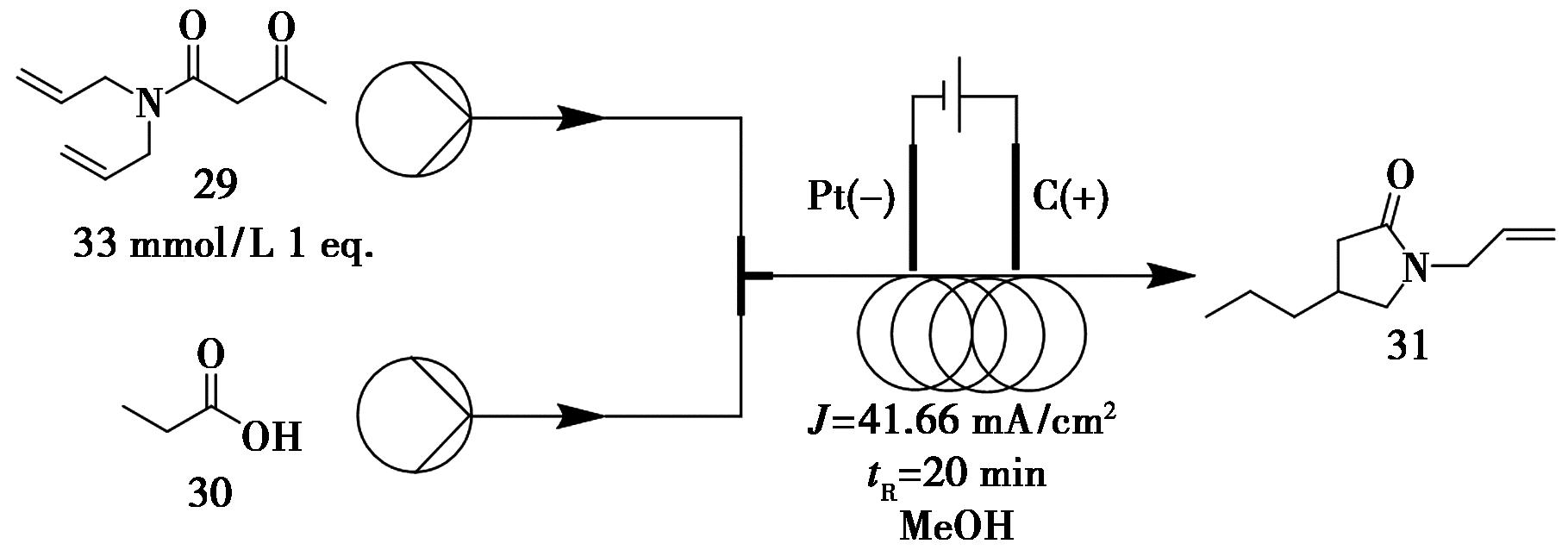
图12 2-吡咯烷酮31的连续流合成路线
Fig.12 Continuous flow synthetic route of 2-pyrrolidinones 31
三氟甲基化合物的高效合成一直是有机化学研究中的一个重要目标,这是由于该类结构在农用化学品与药物分子中具有广泛的应用价值。引入三氟甲基等氟化基团能够增强化合物的酸性、亲脂性及代谢稳定性,从而优化其生物活性与药代动力学性质[35-38]。
3.2.1 连续流技术偶联电化学实现三氟甲基化反应
Anna等[39]开发了一种环境友好的电化学三氟甲基化方法,该方法以Langlois试剂(CF3SO2Na)作为三氟甲基自由基来源,且无需额外添加电解质。研究团队以化合物32与Langlois试剂的反应为模型体系,通过一系列平行实验系统优化了反应条件,包括电极材料、电流密度、流速、溶剂、物料当量及电荷量等参数。在确定最优反应条件后,团队进行了放大实验。尽管在连续运行过程中观察到电极表面存在结垢现象,但最终仍以82%的产率获得目标产物33,突显该方法在绿色可持续合成方面的优势(图13)。
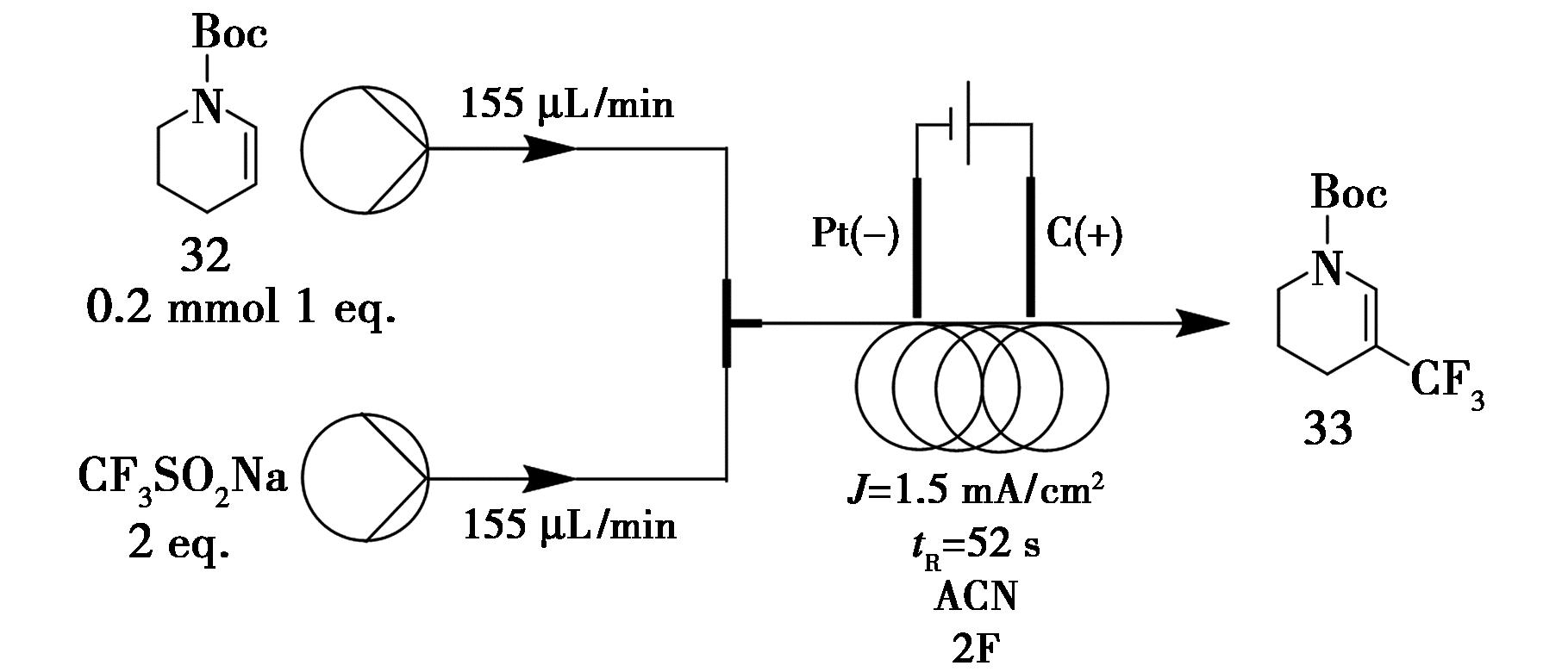
图13 三氟甲基胺33的连续流合成路线
Fig.13 Continuous flow synthetic route of trifluoromethylamide 33
3.2.2 5-三氟甲基尿嘧啶的电化学连续流合成
5-三氟甲基尿嘧啶是一种重要的医药与农用化学品中间体,具有广泛的应用前景[40]。其衍生物2,4-二氯-5-三氟甲基尿嘧啶可作为合成抗癌药物的关键前体。Gong等[41]通过电化学三氟甲基化策略,成功实现了尿嘧啶类化合物的高效转化。在进行一系列平行实验之后,团队确定了最优反应条件:以1.7 g(5 mmol)化合物34和CF3SO2Na(15 mmol,3.0 eq.)为反应物,采用石墨电极,电流设定为180 mA(19 F/mol),以硫酸铵((NH4)2SO4)水溶液作为电解质,在80 ℃条件下于内径0.3 mm的反应管路中反应7 min。在标准放大实验中,以50%的产率获得1.5 g化合物35(图14),时空产率达到39.8 g/(L·h)。团队进一步考察了其他取代尿嘧啶在该水电化学体系中的适用性,发现若化合物在水中溶解度较差,则反应活性显著下降。尽管在连续流条件下的产率较间歇反应器略低,该电化学方法仍表现出良好的综合性能,并具备进一步优化与推广的潜力。
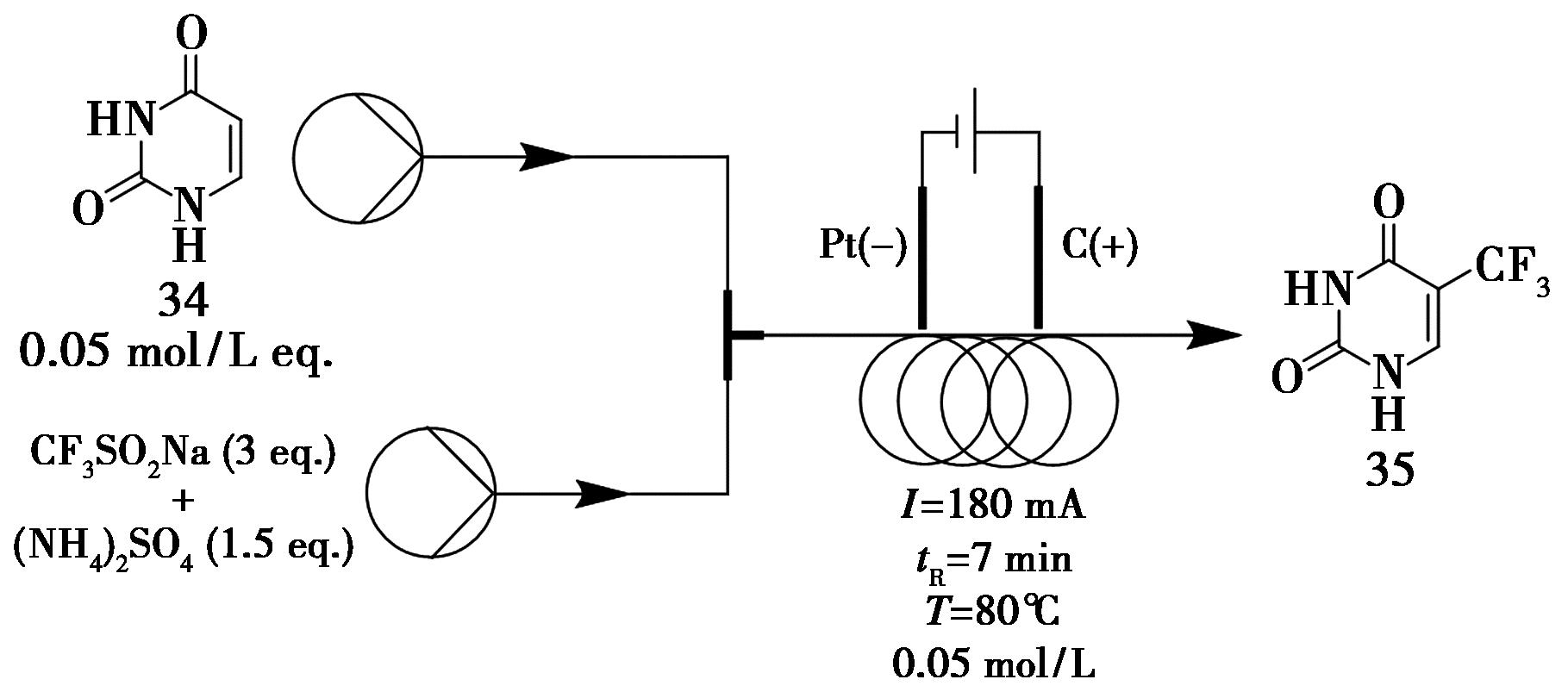
图14 5-三氟甲基尿嘧啶35的连续流合成路线
Fig.14 Continuous flow synthetic route of 5-trifluoromethyluracil 35
苯并噻吩及其衍生物是一类重要的杂环化合物。其卤代产物具有较高的实用价值,不仅广泛存在于药物及天然分子中作为关键结构单元,也是通过过渡金属催化氧化/还原交叉偶联反应制备精细化学品的重要合成砌块[42]。Zhang等[43]开发了一种在无过渡金属和氧化剂条件下,利用电化学连续流偶联系统实现化合物36与卤化钾反应合成C-3卤代苯并噻吩的绿色高效方法。最优反应条件为:分别以碳板和铂板作为阳极与阴极,V(乙腈)∶V(水)=5∶1为溶剂,流速50 μL/min,停留时间4.5 min。在恒电流条件下,C-3卤代苯并噻吩衍生物的转化率可达92%(图15)。
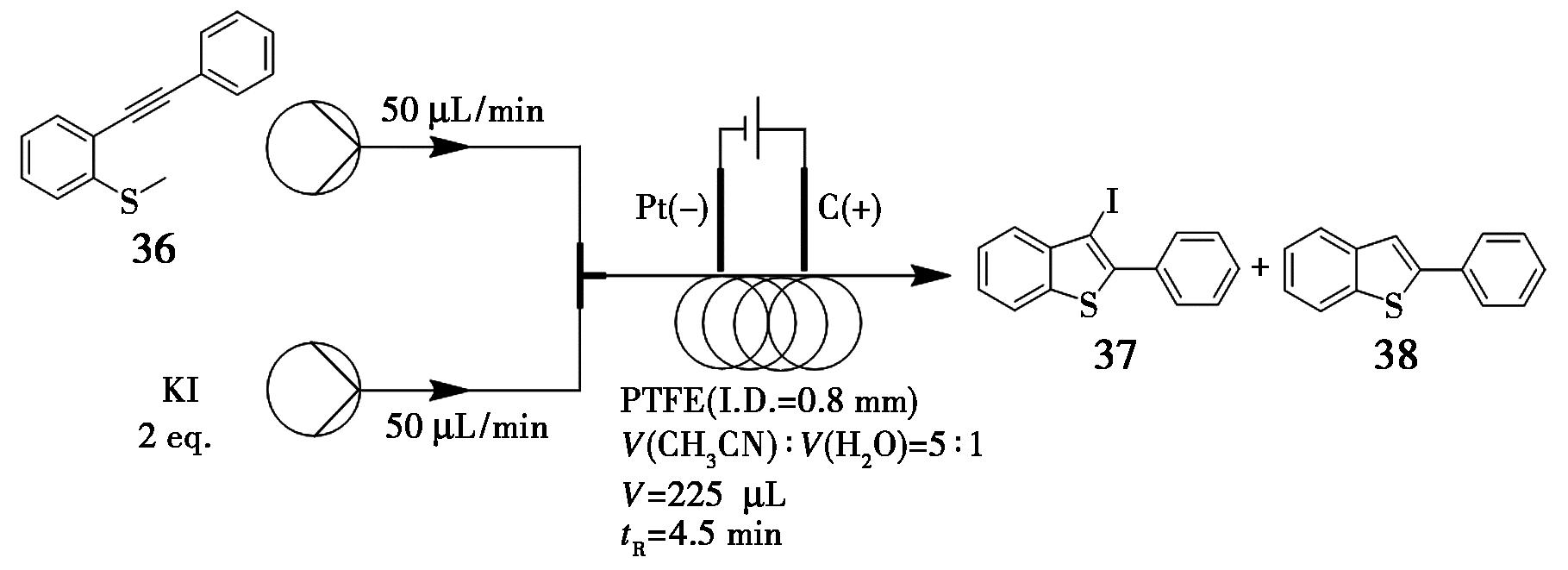
图15 苯并噻吩类化合物37和38的连续流合成路线
Fig.15 Continuous flow synthetic route of benzothiophenes 37 and 38
异噁唑啉是一类重要的杂环结构,其衍生物广泛存在于天然产物、生物活性分子以及农用化学品中,并可作为有机合成中的多功能中间体[44]。Kale等[45]开发了一种电化学合成异噁唑啉的方法,该方法在常温常压下进行,对空气和湿气具有良好的耐受性。最优反应条件包括:采用石墨阳极和SS316不锈钢阴极,在恒流模式下控制电流密度为100 mA/cm2;将化合物39(0.02 mmol,1.0 eq.)溶于V(DMSO)∶V(KBr)=1∶1混合溶液中,同时将NaOAc·3H2O溶于V(DMSO)∶V(水)=1∶1中;在20 ℃条件下,以200 μL/min流速通过反应器,最终以86%的产率获得目标产物异噁唑啉(化合物40,图16)。该策略以溴化钾同时作为电解质和溴源,无需使用有毒、对空气敏感的无机氧化剂或过渡金属催化剂,体现出良好的绿色合成特性。
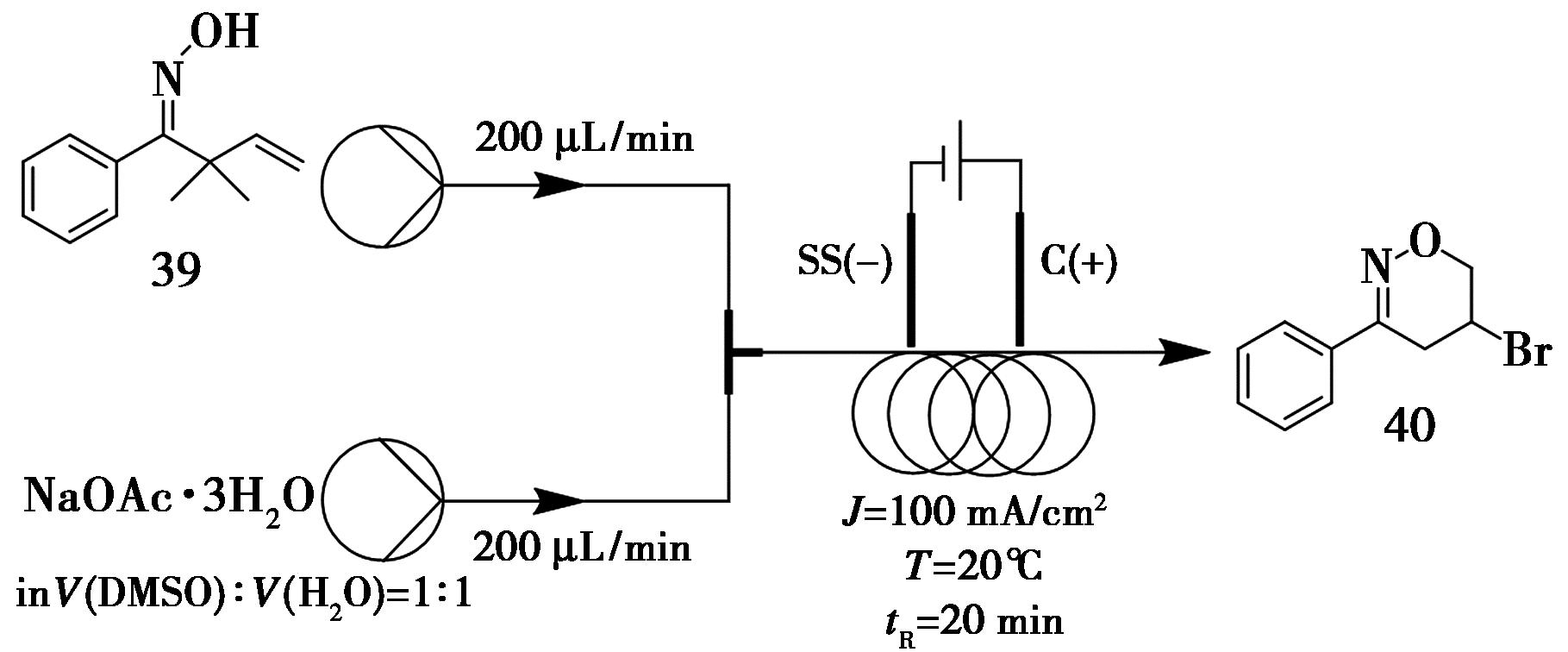
图16 异噁唑啉化合物40的连续流合成路线
Fig.16 Continuous flow synthetic route of isoxazoline 40
取代苯并咪唑类化合物不仅是多种天然产物的核心结构单元,也在有机合成与药物研发中具有广泛应用,其在抗寄生虫、抗过敏、镇痛、抗炎、抗抑郁及抗肿瘤等方面表现出显著生物活性。然而,传统合成方法通常伴随大量废弃物产生及安全隐患[46]。Shi等[47]开发了一种基于芳香醇与邻苯二胺的酶促电化学级联反应策略。该过程分为两步:第一步反应条件为:以0.1 mol/L化合物41为底物,700 UAO、6 μmol FAD及4 mg(0.02 μmol)过氧化氢酶作为酶催化剂,10 mL H2O2作为辅助试剂,反应液流速为56.25 μL/min,空气流速168.75 μL/min,停留时间25 min,获得中间体化合物42;第二步反应以等物质的量比(0.1 mol/L,1.0 eq.)的化合物42与化合物43为原料,乙腈为溶剂,流速56.25 μL/min,电解质为0.1 mol/L Et4NI,最终以79%的产率得到目标产物44(图17)。该反应在温和条件下进行,以空气为绿色氧化剂,氧化酶作为生物催化剂,成功将醇氧化与苯并咪唑构建这两个通常分步进行的反应整合于同一流程。该连续流系统已完成放大实验,展现出良好的工业应用潜力与实用价值。
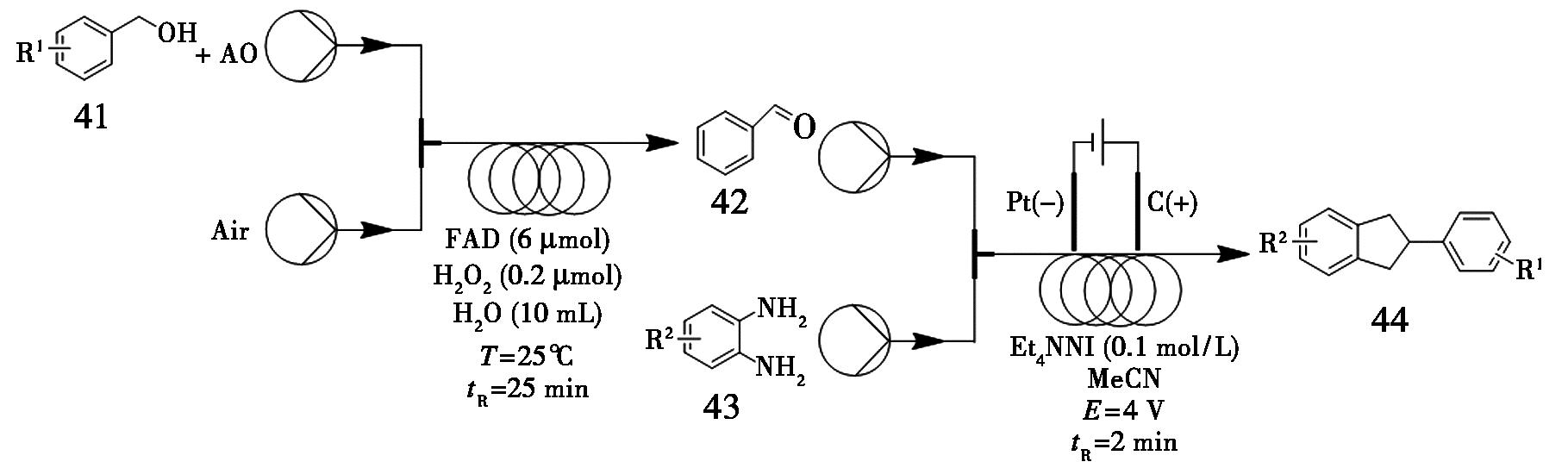
图17 苯并咪唑化合物44的连续流合成路线
Fig.17 Continuous flow synthetic route of benzimidazole 44
α-氨基膦酸盐是多种生物活性分子中的关键结构单元,其经典合成方法是通过Kabachnik-Fields三组分偶联反应实现,该反应涉及羰基化合物、胺和磷酰衍生物。近年来,以α组氨基酸为原料通过脱羧磷酸化制备α基氨基膦酸盐的路线因其底物来源广泛、稳定性高、环境友好等特点,展现出显著的发展潜力[48-50]。Xu等[51]提出了一种创新的电化学策略,实现了α-氨基酸的直接脱羧磷酸化转化。该反应以石墨为阳极、铂为阴极,电极间距0.15 mm;反应体系包括0.3 mmol(0.05 mol/L)化合物45、亚磷酸三甲酯(P(OMe)3,3.2 eq.)和甲酸(HCOOH,1.5 eq.);溶剂为V(MeCN)∶V(HFIP)=7∶1,电流密度 55 mA/cm2,流速0.2 mL/min,在氮气氛下总停留时间75 s,最终实现74%的转化率(图18)。该方法充分利用连续流电化学技术的优势,不仅避免了化学氧化剂的使用,还表现出优异的可扩展性,为α-氨基膦酸盐的绿色合成提供了新途径。
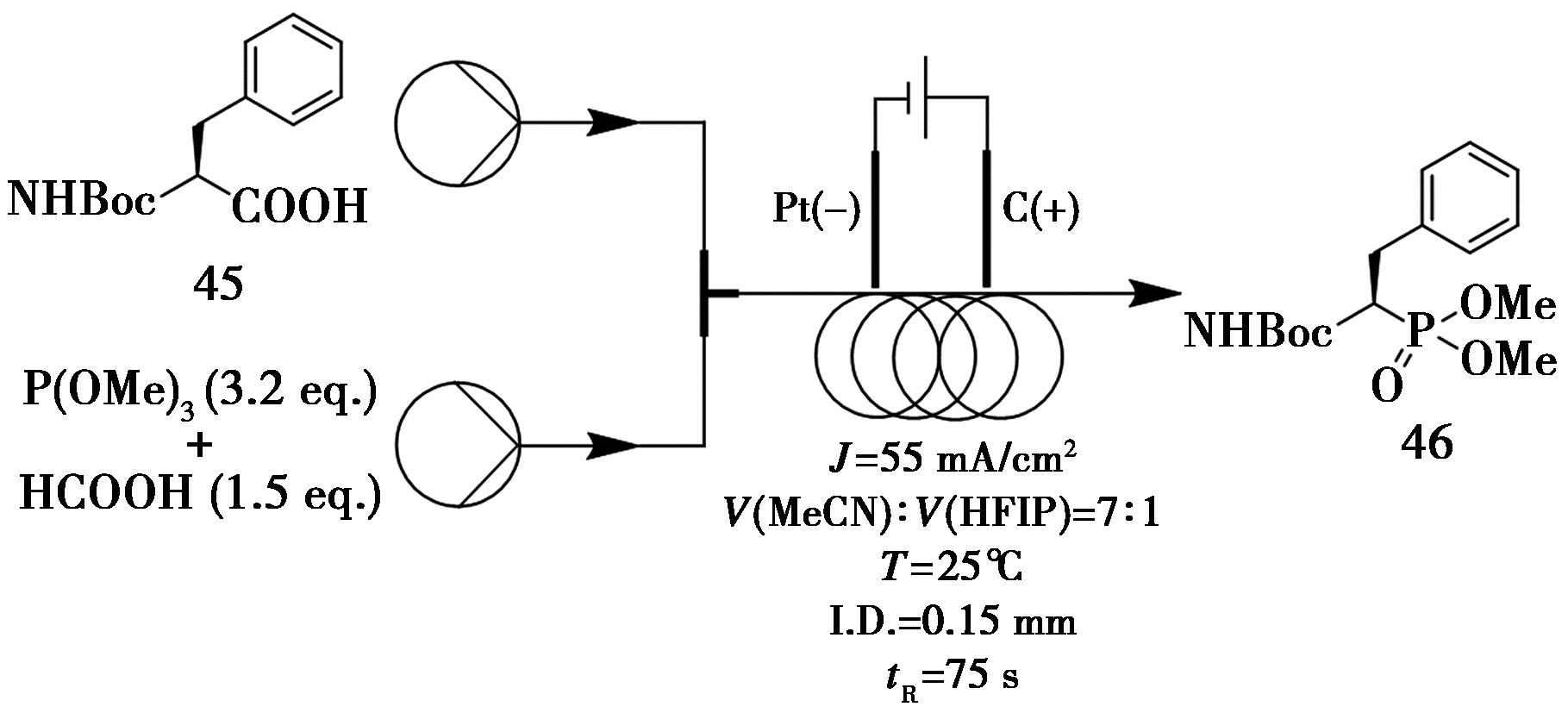
图18 α-氨基膦酸盐46的连续流合成路线
Fig.18 Continuous flow synthetic route of α-amino acids 46
异喹啉-1,3(2H,4H)-二酮是一类重要的含氮杂环结构,广泛存在于多种天然产物及药物分子中,并在抗病毒(如HIV-1整合酶抑制)和抗肿瘤(如胰腺癌抑制)药物研发中具有重要应用价值[52]。Guo等[53]开发了一种绿色高效的电化学连续流合成方法,通过烯烃与磺酰肼的磺酰基化反应,成功构建了4-(磺酰甲基)异喹啉-1,3(2H,4H)-二酮类衍生物。该反应体系包括化合物47(0.5 mmol,1.0 eq.)和化合物48(1.0 mmol,2.0 eq.)作为反应物,以乙腈/水混合溶剂(V(MeCN)∶V(H2O)=3∶1)为反应介质,六氟磷酸四丁基铵(Bu4NPF6)作为电解质。采用石墨板为阳极、铂板为阴极,在室温条件下于连续流电解槽中反应,停留时间仅为1 min,总转化率达79%(图19)。该方法无需金属催化剂和化学氧化剂,符合绿色合成原则。一系列活性烯烃底物均适用于该体系,以中等至良好产率获得相应产物。此外,该电化学连续流系统具有良好的可放大性,可在不改变反应条件的前提下实现规模制备。
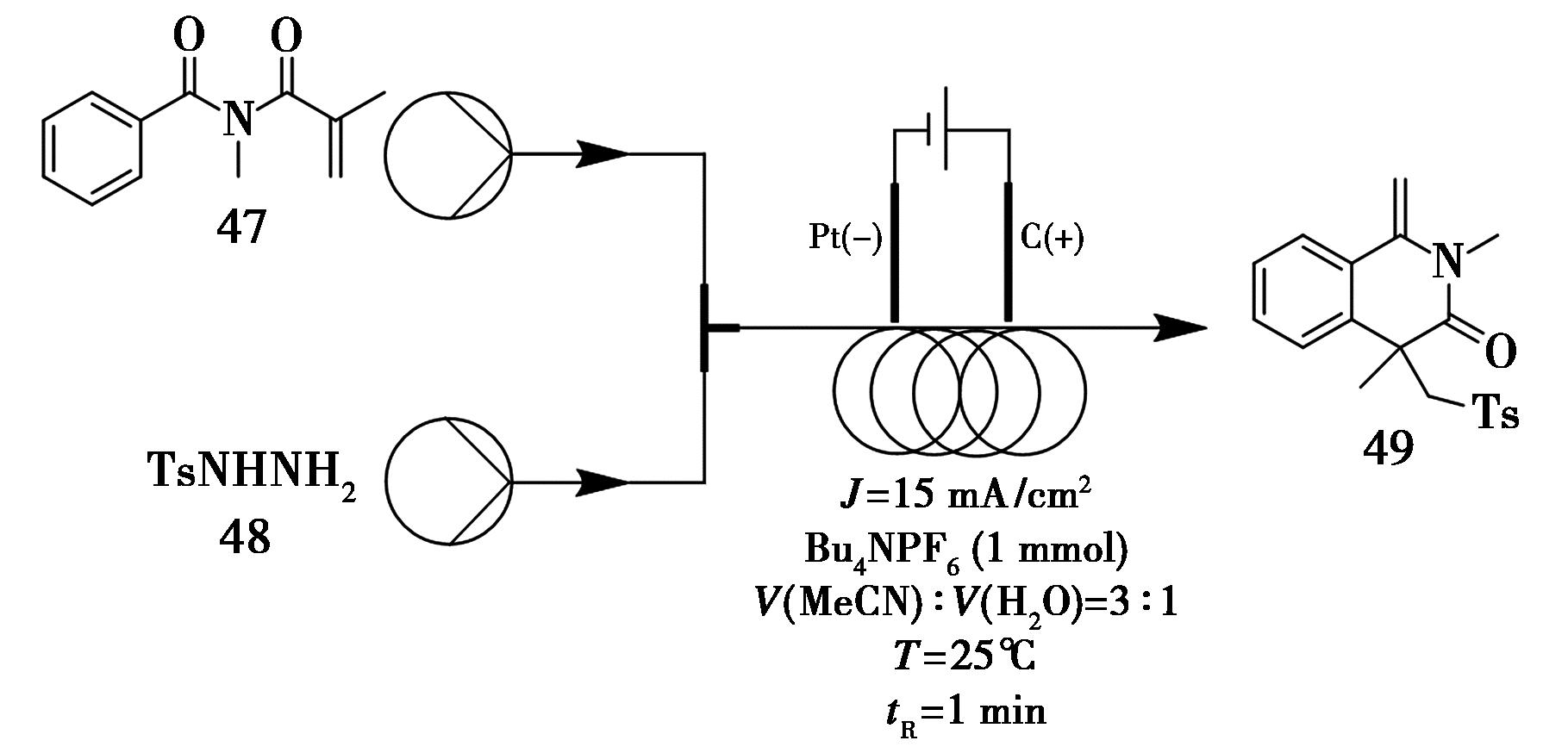
图19 异喹啉化合物49的连续流合成路线
Fig.19 Continuous flow synthetic route of isoquinoline compound 49
亚氨基膦烷(又称膦亚胺)是一类重要的有机合成中间体,在合成化学中具有广泛的应用潜力。由于其与磷酰化物为等电子体,两者在化学反应中表现出高度相似的特性。Morgan等[54]开发了一种在连续流电化学系统中由硝基(杂)芳烃合成芳基亚磷烷的创新方法。该连续流技术无需添加电解质,并具有良好的可扩展性。以4-硝基苯基异氰(0.05 mol/L,1.0 eq.)和三苯基膦(Ph3P,3.5 eq.)为反应底物,在优化后的连续流电化学条件下,化合物51的产率达到95%(图20)。
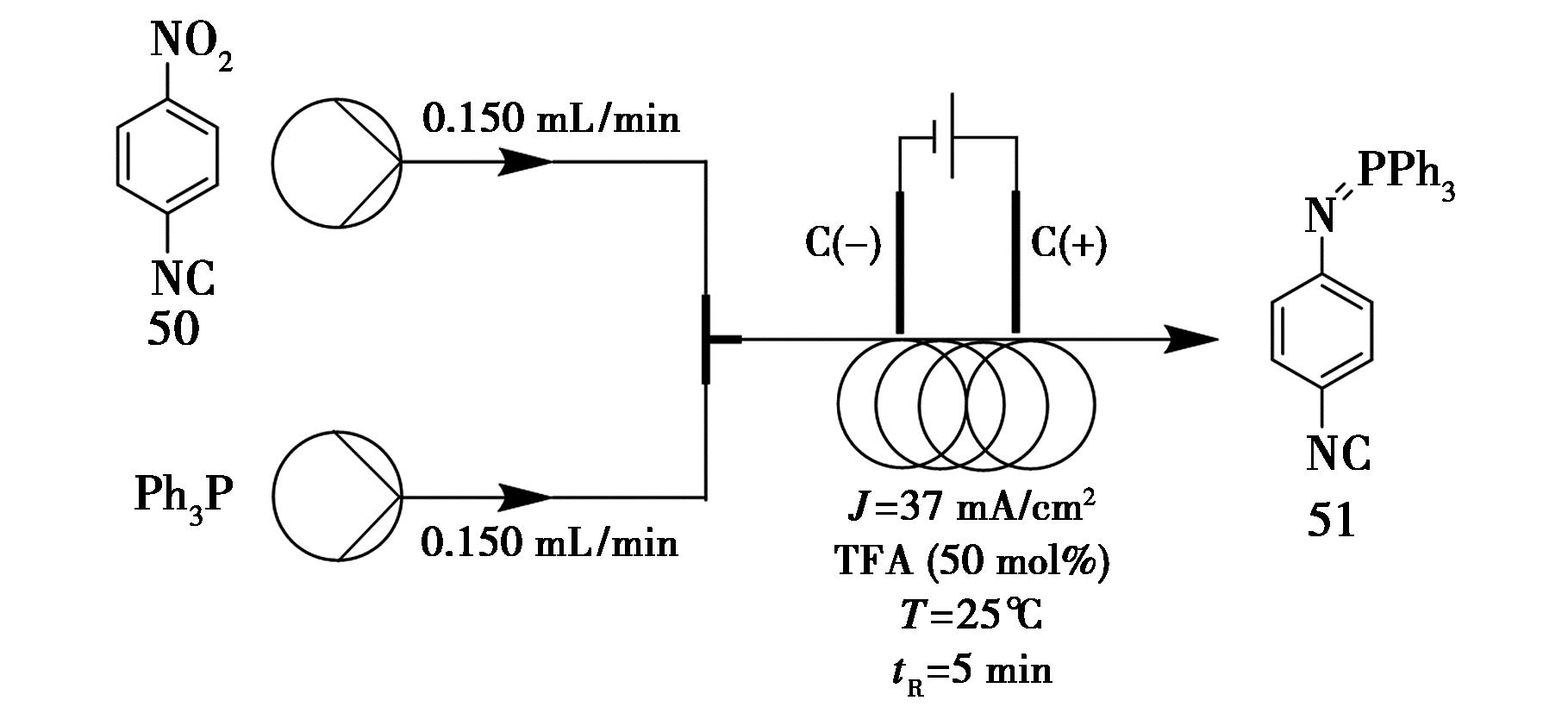
图20 亚氨基膦烷51的连续流合成路线
Fig.20 Continuous flow synthetic route of aryliminophosphoranes 51
以CO2作为羧基化反应的碳源具有显著潜力,近年来研究者已开发出多种光催化与电化学活化策略。Jonas等[55]报道了一种高效的单程通过式连续流合成羧酸的新方法。该体系采用镁和石墨分别作为阳极和阴极,电解液为0.1 mol/L Bu4NBF4,DMF为溶剂,水作为氢源,苯乙烯(化合物52,0.05 mol/L)作为反应底物。反应设定流速为0.208 μL/min,CO2流速为1.02 mL/min(4.4 eq.),电流50 mA,停留时间25 s,背压阀压力0.1 MPa。该连续流策略实现了高效、可控的羧基化过程,能够精确控制CO2输入、避免浪费,在提高反应效率的同时保持了优异的选择性与转化率,充分体现了连续流电化学技术在绿色合成中的广阔应用前景(图21)。
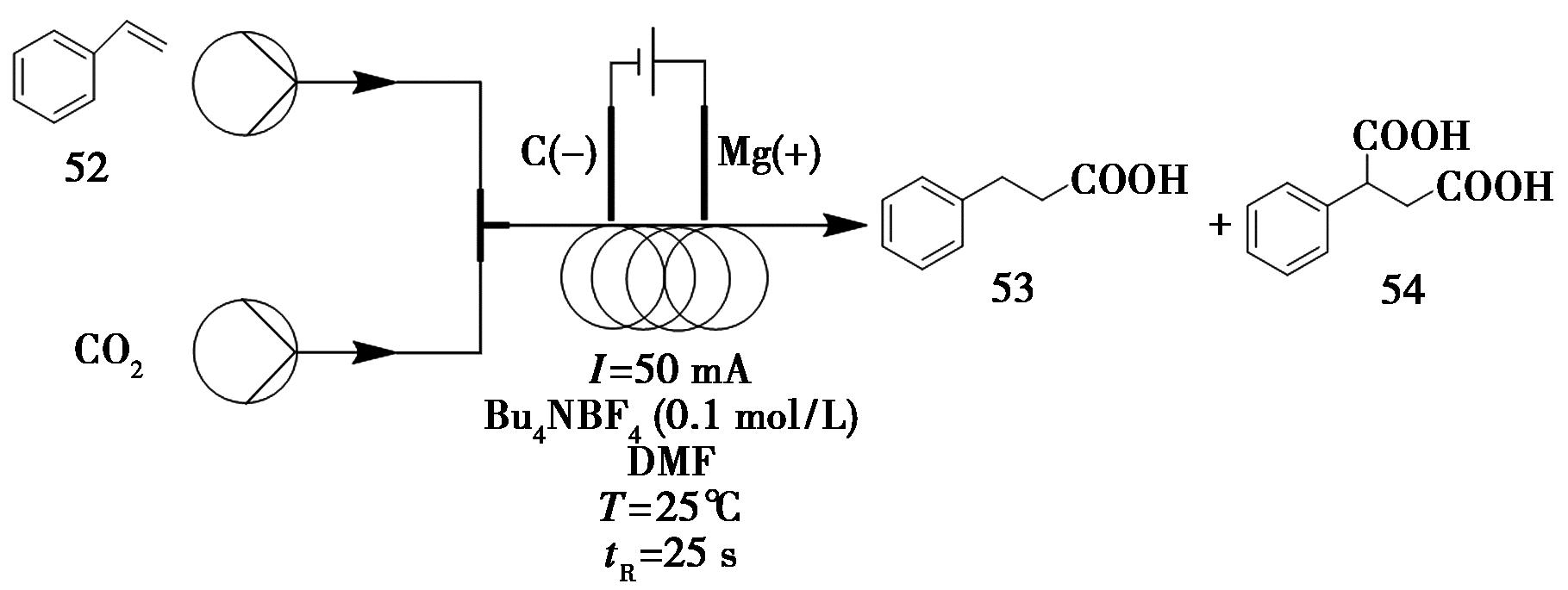
图21 羧酸53和54的连续流合成路线
Fig.21 Continuous flow synthetic route of carboxylic acid 53 and 54
Jiri等[56]提出了一种新型光电催化(Electrophotocatalysi,EPC)反应器概念,该反应器通过同时利用光子与电子协同驱动反应,实现了 C(sp3)—H键的高效杂芳基化。研究团队将光催化、电化学与连续流技术有机结合,构建了一套高效集成的反应体系。具体以化合物55(0.3 mmol,1.0 eq.)和化合物56(6.0 eq.)为反应底物,在紫色LED光照及石墨/铂电极电化学系统的协同催化作用下,最终以88%的产率获得目标产物57(图22)。该光电催化-连续流协同策略有效弥补了单一催化模式的局限性,在提升反应效率的同时体现了良好的原子经济性与过程绿色性,展现出广阔的应用前景。
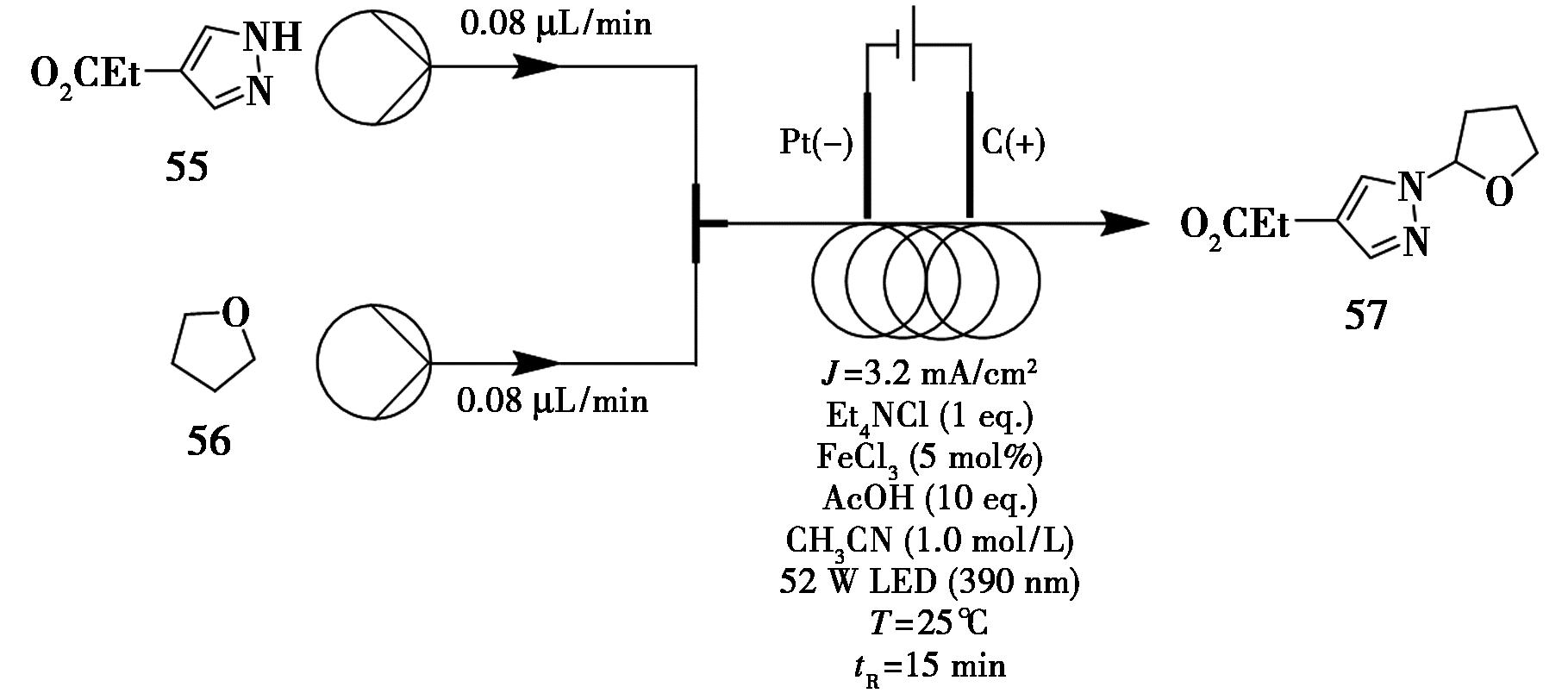
图22 EPC反应器中光电共同催化的化合物57连续流合成路线
Fig.22 Continuous flow synthetic route of compound 57 with photoelectrochemical co catalysis in EPC reactor
连续流技术与光电催化技术的融合是化学工程领域的一项重要进展,为多个行业带来了新的发展机遇。在能源短缺和环境污染问题日益突出的背景下,这一复合技术显示出显著的应用潜力。连续流系统为光催化和电化学体系提供了稳定的动态反应环境;光催化和电化学则为连续流过程提供了新的绿色催化方式,减少了对有害催化剂的依赖。两者融合强化了反应的传质传热效率与界面反应过程,有助于提高选择性与产率,减少污染物的生成。然而,该技术体系仍面临诸多挑战,如催化材料稳定性、反应器设计优化、系统长期运行可靠性等问题,亟需进一步深入研究。近年来,机器学习作为人工智能的核心分支,在从大量数据中识别、进行分类、预测与优化方面展现出强大能力。连续流工艺可实时产生包括反应参数、物料状态与产物品质在内的高维数据,机器学习方法可对这些数据进行建模与分析,辅助快速筛选最优工艺条件,显著缩短研发周期。从更宏观的视角看,连续流技术本身具备过程强化与废物减排的绿色属性,而机器学习的引入进一步提升了资源利用效率和系统智能化水平。两者协同可在提高生产效率的同时降低环境负荷,符合绿色化学与可持续发展方向。随着跨学科合作的深入推进和技术本身的不断成熟,这一融合策略有望在更多化工生产与能源转化场景中发挥重要价值。
[1]Gao F,Dai J W,Wang J F.Chin.J.Pharm.,2023,54(7):1 060-1 064.
高锋,戴佳炜,王俊峰.中国医药工业杂志,2023,54(7):1 060-1 064.
[2]Zhang Z,Xiao W T,Guo Y L.Chin.J.Pharm,2023,54(10):1 433-1 435.
张振,肖雯婷,郭艳丽.中国医药工业杂志,2023,54(10):1 433-1 435.
[3]Zhang M M.China.Rubber,2024,40(4):34-36.
张敏敏.中国橡胶,2024,40(4):34-36.
[4]Hanus L O.Med.Res.Rev.,2009,29(2):213-271.
[5]Bisogno T,Hanu L,Petrocellis L,Tchilibon S,Pondé D E,Brandi I,Moriello A S,Davis J B,Mechoulam R,Di M V.Br.J.Pharmacol.,2001,134(4):845-852.
L,Petrocellis L,Tchilibon S,Pondé D E,Brandi I,Moriello A S,Davis J B,Mechoulam R,Di M V.Br.J.Pharmacol.,2001,134(4):845-852.
[6]Aguillón A R,Leão R A C,Oliveira K T,Brocksom T J,Miranda L S M,Souza R O M.A.Org.Process Res.Dev.,2020,24(10):2 017-2 024.
[7]Sterckx H,Morel B,Maes B.Angew.Chem.,Int.Ed.,2019,58(24):7 946-7 970.
[8]Yun L,Zhao J N,Tang X F,Ma C F,Yu Z Y,Meng Q W.Org.Process Res.Dev.,2021,25(7):1 612-1 618.
[9]Fatiadi A J.Synthesis,1976,2:65-104.
[10]Dess D B,Martin J C.J.Org.Chem.,1983,48(24):4 155-4 156.
[11]Li G X,Morales-rivera C,Gao F,Wang Y,He G,Liu P,Chen G.Chem.Sci.,2017,8(10):7 180-7 185.
[12]Bannon R,Morrison G,Smyth M,Moody T S,Wharry S,Roth P M C,Gauron G,Baumann M.Org.Process Res.Dev.,2024,28(8):3 307-3 312.
[13]Caron S,Dugger R W,Ruggeri S G,Ragan J A,Ripin D H B.Chem.Rev.,2006,106(7):2 943-2 989.
[14]Ornum S G V,Champeau R M,Pariza R.Chem.Rev.,2006,106(7):2 990-3 001.
[15]Urgoitia G,Sanmartin R,Herrero M T,Domínguez E.ACS Catal.,2017,7(4):3 050-3 060.
[16]Xiao Y L,Lu C Y,Huang Y C,Zhang Y C,Qiu Y Q,You Z R,Fang L P,Wei Z Z,Xiong J J,Chi X,Rusydi A,Tu W G,Chen Z X,Shu T,Zou Z G.Chem.Eng.J.,2025,512:162 527.
[17]Wiemer A J,Wiemer D F.Top.Curr.Chem.,2015,360:115-160.
[18]Lapierre R,Le T M T,Schiavi B,Thevenet D,Bazin M,Buzdygon R,Jubault P,Poisson T.Org.Process Res.Dev.,2024,28(5):1 436-1 446.
[19]Foti C,Piperno A,Scala A,Giuffrè O.Molecules,2021,26(14):4 280.
[20]Steiner A,Nelson R C,Dallinger D,Kappe C O.Org.Process Res.Dev.,2022,26(8):2 532-2 539.
[21]Prajapati S M,Patel K D,Vekariya R H,Panchal S N,Patel H D.RSC Adv.,2014.4(47):24 463-24 476.
[22]Moln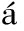 r M,Födi T,Tatai J,Kun V,Bal
r M,Födi T,Tatai J,Kun V,Bal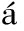 zs B,G
zs B,G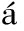 ti T,Dargó G,Nyerges M.Org.Process Res.Dev.,2025,29(5):1 237-1 247.
ti T,Dargó G,Nyerges M.Org.Process Res.Dev.,2025,29(5):1 237-1 247.
[23]Xia Z Q,Huang R D,Zhou X L,Chai Y Y,Chen H,Ma L L,Yu Q W,Li Y,Li W M,He Y.Eur.J.Med.Chem.,2021,224:113 711.
[24]Simon K,Zindar D,Boutet J,Guillamot G,Lenoir J Y,Dallinger D,Kappe C O.Org.Process Res.Dev.,2023,27(2):322-330.
[25]Xue Y,Gan J,Luo N,Wang C J.Org.Chem.,2022,87(15):10 422-10 429.
[26]Zhu S S,Lv H,Yuan X,Guo K.Org.Lett.,2024,26(41):8 910-8 915.
[27]Zhu S S,Chen Z W,Fan D D,Lv H,Yuan X,Guo K.J.Org.Chem.,2025,90(12):4 232-4 243.
[28]Moschner J,Stulberg V,Fernandes R,Huhmann S,Leppkes J,Koksch B.Chem.Rev.,2019,119(18):10 718-10 801.
[29]Berger A A,Völler J S,Budisa N,Koksch B.Acc.Chem.Res.,2017,50(9):2 093-2 103.
[30]Liu J Y,Zhang W G,Tao X Z,Wang Q,Wang X C,Pan Y,Ma J Z,Yan L,Wang Y.Org.Lett.,2023,25(17):3 083-3 088.
[31]Liu J,Zhao W,Lu L Q,Liu Y Y,Cheng Y.Synth.Catal.,2021,2(4):389-392.
[32]Dzik W I,Lange P P,Goossen L J.Chem.Sci.,2012,3(9):2 671-2 678.
[33]Qin L Z,Zhang X P,Sun H,Duan X,Liu J,Wu M Y,Yuan X,Qiu J K,Guo K.Green Synth.Catal.,2024,5(1):20-24.
[34]Quertenmont M,Toussaint F C,Defrance T,Lam K,Markó I E,Riant O.Org.Process Res.Dev.,2021,25(12):2 631-2 638.
[35]Cantillo D,Kappe C O.React.Chem.Eng.,2017,2(1):7-19.
[36]Champagne P A,Desroches J,Hamel J D,Vandamme M,Paquin J F.Chem.Rev.,2015,115(17):9 073-9 174.
[37]Atobe M,Tateno H,Matsumura Y.Chem.Rev.,2018,118(9):4 541-4 572.
[38]Plosker G L,Figgitt D P.Drugs,2003,63(15):1 611-1 618.
[39]Anna V,Tomas H,Eli B,Stevens C V.Org.Process Res.Dev.,2024,28(11):4 018-4 023.
[40]Salvetti R,Marchand A,Pregnolato M,Verri A,Spadari S,Focher F,Briant M,Sommadossi J P,Mathé C,Gosselin G.Bioorg.Med.Chem.,2001,9(7):1 731-1 738.
[41]Gong R Q,Zhou Y C,Su D D,Chen Y,Chen W B.Org.Process Res.Dev.,2024,28(5):1 430-1 435.
[42]Yue H F,Zhu C,Rueping M.Angew.Chem.,Int.Ed.,2018,57(5):1 371-1 375.
[43]Zhang D,Cai J L,Fang Z,Du J Z,Lin X X,Liu C K,He W,Yang Z,Guo K.ACS Sustainable Chem.Eng.,2020,8(35):13 302-13 309.
[44]Minter A R,Fuller A A,Mapp A K.J.Am.Chem.Soc.,2003,125(23):6 846-6 847.
[45]Kale A P,Nikolayenko P,Smirnova K.Eur.J.Org.Chem.,2021,24:3 496-3 500.
[46]Dandia A,Mahawar D K,Sharma R,Badgoti R S,Rathore K S,Parewa V.Appl.Organomet.Chem.,2019,33(11):5 232.
[47]Shi T T,Wang S Z,Yang Z,Wang Y L,Liu C K,He W,Fang Z,Guo L.React.Chem.Eng.,2021,6(5):937-943.
[48]Corcoran R C,Green J M.Tetrahedron Lett.,1990,31(47):6 827-6 830.
[49]Boto A,Gallardo J A,Hern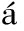 ndez R,Saavedra C J.Tetrahedron Lett.,2005, 46(45):7 807-7 811.
ndez R,Saavedra C J.Tetrahedron Lett.,2005, 46(45):7 807-7 811.
[50]Moeller K D.Chem.Rev.,2018, 118(9):4 817-4 833.
[51]Zhao Y L,Chen N,Xu H C.Chin.J.Chem.,2025,43(10):1 167-1 172.
[52]Billamboz M,Bailly F,Lion C,Touati N,Vezin H,Calmels C,Andreola M L,Christ F,Debyser Z,Cotelle P.J.Med.Chem.,2011,54(6):1 812-1 824.
[53]Xu J,Yang Z,Hua J W,Lin Y,Bian M X,Li Y G,Liu C K,He W,Fang Z,Guo K.Org.Chem.Front.,2020,7(20):3 223.
[54]Rodrigo C E S,Clara V,Morgan R.Adv.Synth.Catal.,2024,366(4):955-960.
[55]Jonas M,Christian S.React.Chem.Eng.,2025,10(7):1 455.
[56]Dimitris I I,Luca C,Jiri S.Chem.Int.Ed.,2023,62(52):1 433-7 851.