次氯酸及其盐(HClO/ClO-)作为一种重要的活性氧,在人体免疫防御中发挥关键作用[1,2]。生理浓度下,次氯酸可选择性修饰生物大分子,调控细胞信号转导、基因表达及免疫应答等生理功能[3,4]。然而,其过量产生会导致氧化应激,与炎症反应、免疫紊乱及神经退行性疾病的发生发展密切相关[5]。基于强氧化特性,次氯酸盐已广泛应用于食品工业的消毒保鲜环节[6],但其化学不稳定性、毒副产物风险及体内瞬时存在特性[7],亟需发展高灵敏、高选择性的实时检测方法,以应对环境监测与生命科学研究的精准化需求。
小分子荧光探针因其结构可设计性强、响应机制多样、检测灵敏度高等优势,在生物分析和环境检测领域具有重要应用价值[8-11]。吩噻嗪衍生物凭借其独特的电子供体性质、显著的斯托克斯位移以及近红外发射特性,成为构建高性能ClO-响应探针的理想平台[12,13]。基于吩噻嗪骨架的探针设计主要采用3种策略:1)利用其易被氧化的硫原子和富电子芳环构建氧化响应型探针;2)作为荧光发色团开发比率型检测体系;3)通过引入吸电子基团形成D-π-A结构,实现近红外发射。这些策略显著提升了探针对ClO-的识别性能和检测灵敏度,为活体成像和环境实时监测提供了新的技术手段。
本文利用ClO-对席夫碱(C![]() N)氧化断裂的机制,合成了一种结构简洁、水溶性良好的吩噻嗪席夫碱衍生物PTZCN,旨在开发具有高选择性和灵敏度的次氯酸检测探针分子。该探针在40%乙醇溶液中与ClO-反应后形成电荷转移复合物,最大吸收峰从445 nm显著红移至627 nm。探针C
N)氧化断裂的机制,合成了一种结构简洁、水溶性良好的吩噻嗪席夫碱衍生物PTZCN,旨在开发具有高选择性和灵敏度的次氯酸检测探针分子。该探针在40%乙醇溶液中与ClO-反应后形成电荷转移复合物,最大吸收峰从445 nm显著红移至627 nm。探针C![]() N键在ClO-作用下发生断裂-水解,分子内电荷转移(ICT)效应减弱,在470和500 nm处呈现显著的荧光发射。PTZCN不仅具有优异的线性响应关系和宽pH适应性,更在HeLa细胞和斑马鱼模型中展现出良好的生物相容性与成像性能。
N键在ClO-作用下发生断裂-水解,分子内电荷转移(ICT)效应减弱,在470和500 nm处呈现显著的荧光发射。PTZCN不仅具有优异的线性响应关系和宽pH适应性,更在HeLa细胞和斑马鱼模型中展现出良好的生物相容性与成像性能。
1.1 主要仪器与试剂
BRUKER AV-500M型核磁共振波谱仪(德国布鲁克公司);SHIMADZU FT-IRTracer-100型红外光谱仪(日本岛津公司);Thermo Q Exactive Orbitrap型LC-MS系统(美国赛默飞世尔科技公司);JASCO FP-6500型荧光光谱仪(日本佳斯科公司);TU-1901型紫外-可见分光光度计(北京普析通用仪器有限责任公司);Leica MDG41型荧光立体显微镜(德国徕卡显微系统公司);Olympus IX73DP80型荧光倒置显微镜(日本奥林巴斯有限公司)。
吩噻嗪(C12H9NS)、三氯氧磷(POCl3)、二氨基马来腈(C4H4N4)、N,N-二甲基甲酰胺(DMF)、10%次氯酸钠溶液(NaClO)(安徽泽升科技股份有限公司);石油醚(PE)、乙酸乙酯(C4H8O2)、二氯甲烷(CH2Cl2)、乙醇(C2H5OH)、冰醋酸(CH3COOH)、氢氧化钠(NaOH)、无水硫酸钠(Na2SO4)以及待测阴离子的钠盐(天津大茂化学试剂厂)。所用试剂均为分析纯,实验用水为超纯水。
1.2 实验方法
1.2.1 探针PTZCN的制备
10-H-吩噻嗪-3-甲醛(PTZCHO)的按照文献[14]报道的方法制备。将1.135 g (5 mmol) PTZCHO和0.541 g (5 mmol)二氨基马来腈溶解于30 mL乙醇溶液中,滴加2滴冰醋酸,搅拌回流 12 h。反应完毕后将反应液倾倒入200 mL饱和食盐水中,用二氯甲烷萃取、无水Na2SO4干燥、减压浓缩后得粗产物。粗产物经硅胶柱层析(V(石油醚)∶V(乙酸乙酯)=5∶1)纯化得到棕色固体0.51 g,产率为32%。
1HNMR(DMSO-d6,500 MHz),δ:9.04(s,1H);8.02(s,1H);7.72(d,3H,J=20.7 Hz);7.52(dd,1H,J=8.3,1.5 Hz);6.99(dd,1H,J=10.9,4.3 Hz);6.91(d,1H,J=7.5 Hz);6.77(t,1H,J=7.5 Hz);6.67(t,2H,J=7.5 Hz)。13CNMR(DMSO-d6,125 MHz),δ:154.18,145.00,140.58,130.72,129.87,128.19,126.71,126.36,125.99,123.01,117.46,116.36,115.33,115.17,114.35,106.57,103.69。IR(KBr),ν,cm-1:3 348,2 924,2 104,1 604,1 473,1 365,1 307。ESI-MS,m/z(%):317.072 0[M+H]+。
1.2.2 溶液配制/测试方法
探针溶液及待测离子的配制:称取0.003 2 g PTZCN用无水乙醇溶解并配制成1.0×10-4 mol/L的贮备液;测试前用40%乙醇稀释成2.0×10-5 mol/L。测试用待测物种溶液![]()
![]()
![]() 分别配制成10-2 mol/L的水溶液。·OH和ONOO-按照文献[15]报道的方法进行制备。
分别配制成10-2 mol/L的水溶液。·OH和ONOO-按照文献[15]报道的方法进行制备。
光谱测试:移取3.0 mL(2.0×10-5 mol/L)的PTZCN溶液(40%乙醇)于1 cm光程的石英比色皿中,加入30 μL(10-2 mol/L)的待测离子溶液,混合均匀后,立即进行紫外-可见吸收光谱和荧光发射光谱选择性测试。在选择性测试的样品中,再分别加入30 μL(10-2 mol/L)的ClO-溶液,进行光谱竞争测试。在探针溶液中,分别加入0~60 μL的ClO-溶液,进行光谱滴定测试。荧光光谱测定的激发波长为365 nm,灵敏度为中等,激发狭缝宽度为5 nm,发射狭缝宽度为3 nm。
2.1 探针PTZCN对ClO-的光谱识别
为了测试探针PTZCN对不同阴离子的特异性识别能力,在空白探针溶液(Free)中分别加入30 μL的待测离子或其他氧化性物种的溶液进行测试。如图1所示,大部分的待测物加入后,探针在293、344和445 nm处的吸收峰变化微弱;ONOO-加入后导致445 nm处的吸收峰出现了轻微的蓝移和减弱,紫外区的吸收出现了明显的增强(绿色线);而当向探针溶液中加入30 μL的ClO-后,627 nm处出现了新的吸收峰(红色线),293、344和445 nm处的吸收峰均出现了明显的降低,此时溶液的颜色由黄色迅速变为墨绿色。这可能是由于ClO-加入后,C![]() N和吩噻嗪环上电子的π→π*跃迁过程被破坏,吩噻嗪的硫原子或芳香环向ClO-氧化生成的中间体转移电子,生成了电荷转移复合物。
N和吩噻嗪环上电子的π→π*跃迁过程被破坏,吩噻嗪的硫原子或芳香环向ClO-氧化生成的中间体转移电子,生成了电荷转移复合物。
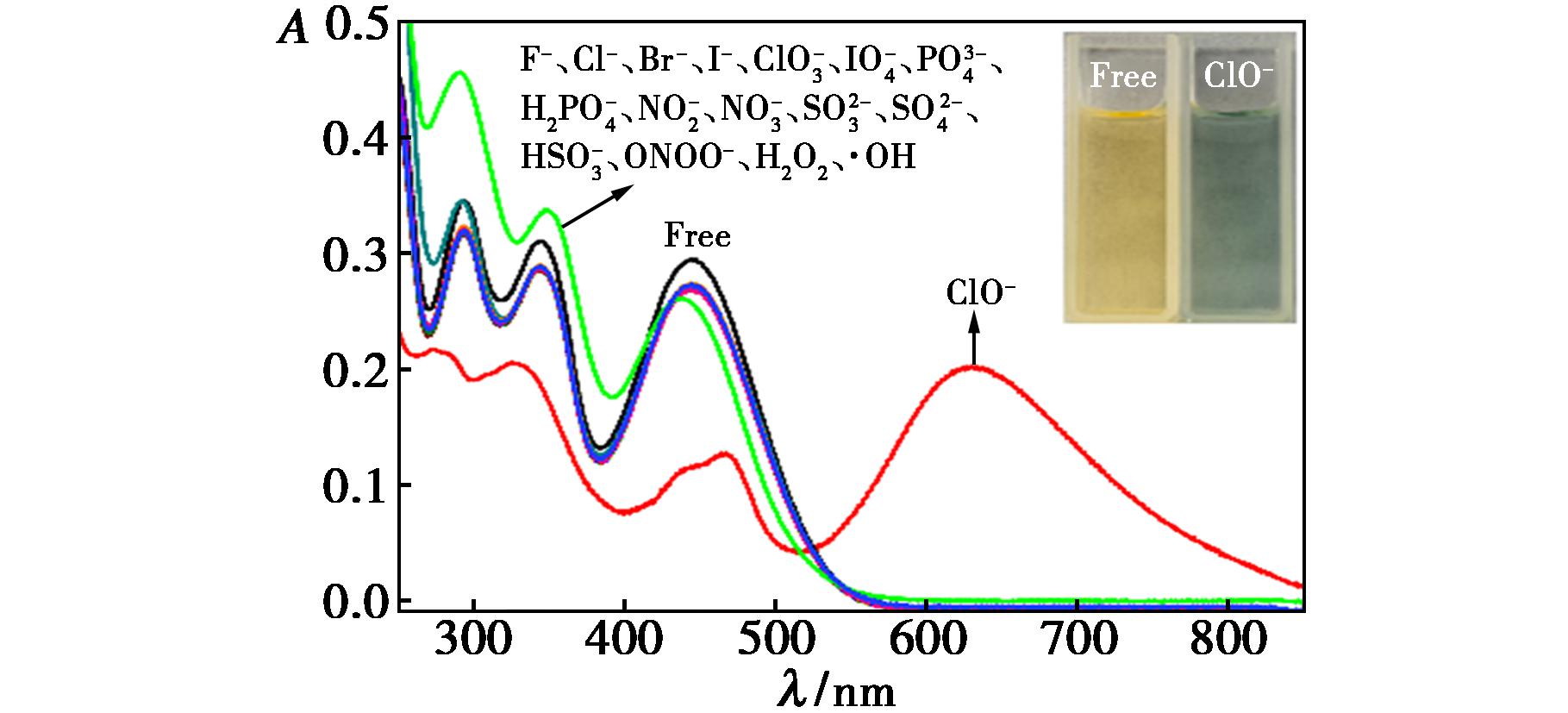
图1 PTZCN加入各种分析物后的紫外-可见吸收光谱
Fig.1 UV-Vis absorption spectra of PTZCN in the presence of various analytes
对探针分子进行荧光光谱选择性测试时(图2),发现加入的大部分阴离子和氧化性物种对PTZCN溶液的无明显荧光开启变化;而加入ClO-后,探针溶液在474和500 nm处出现明显的蓝色荧光发射,且强度为初始值的10倍以上。该结果表明,探针PTZCN对ClO-具有较好的荧光选择性。
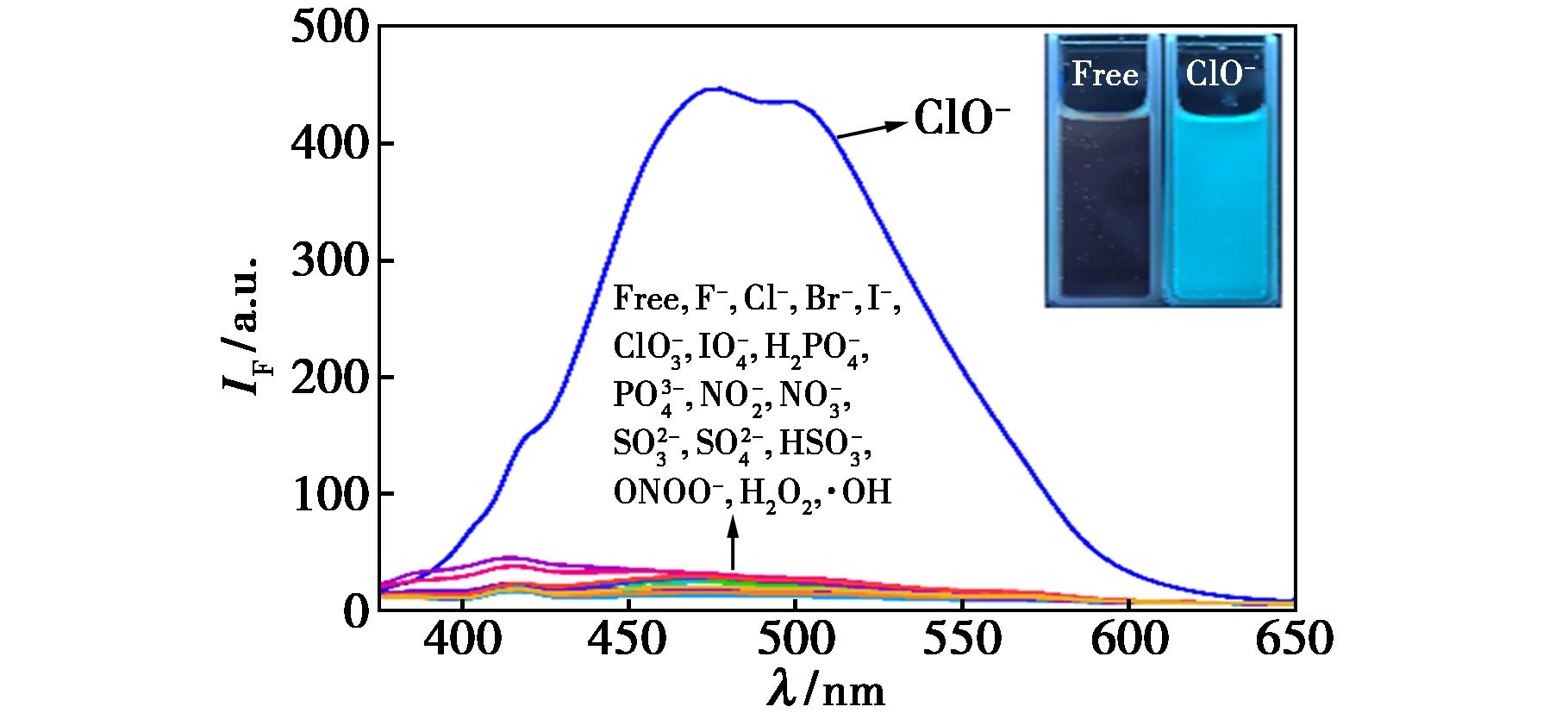
图2 PTZCN加入各种分析物后的荧光发射光谱
Fig.2 Fluorescence emission spectra of PTZCN in the presence of various analytes
2.2 探针PTZCN对ClO-的竞争实验
为了验证探针在复杂体系中对ClO-的识别能力,在两种离子共存的条件下,对其进行了竞争测试。从图3a可知,当待测液中无ClO-时,探针PTZCN在627 nm处的吸光度几乎为0;当向共存离子中加入ClO-后,除了活性较强的·OH和ONOO-外,大部分共存溶液的吸收强度均能出现大幅度上升,这可能是由于二者与ClO-在溶液中发生氧化还原反应,消耗了大部分的ClO-所致。当干扰分析物存在时,探针PTZCN的荧光强度均小于50;当ClO-加入后,共存溶液的荧光强度均迅速升高(图3b)。尽管活性较强的·OH和ONOO-消耗了加入的大部分ClO-,PTZCN仍能产生显著荧光增强,说明其对ClO-的反应能力优于其他活性物种。尽管在较高浓度的多种共存体系中观察到上述干扰现象,但在实际的生物环境中,由于上述干扰物的内源性浓度极低,潜在干扰通常不会发生。
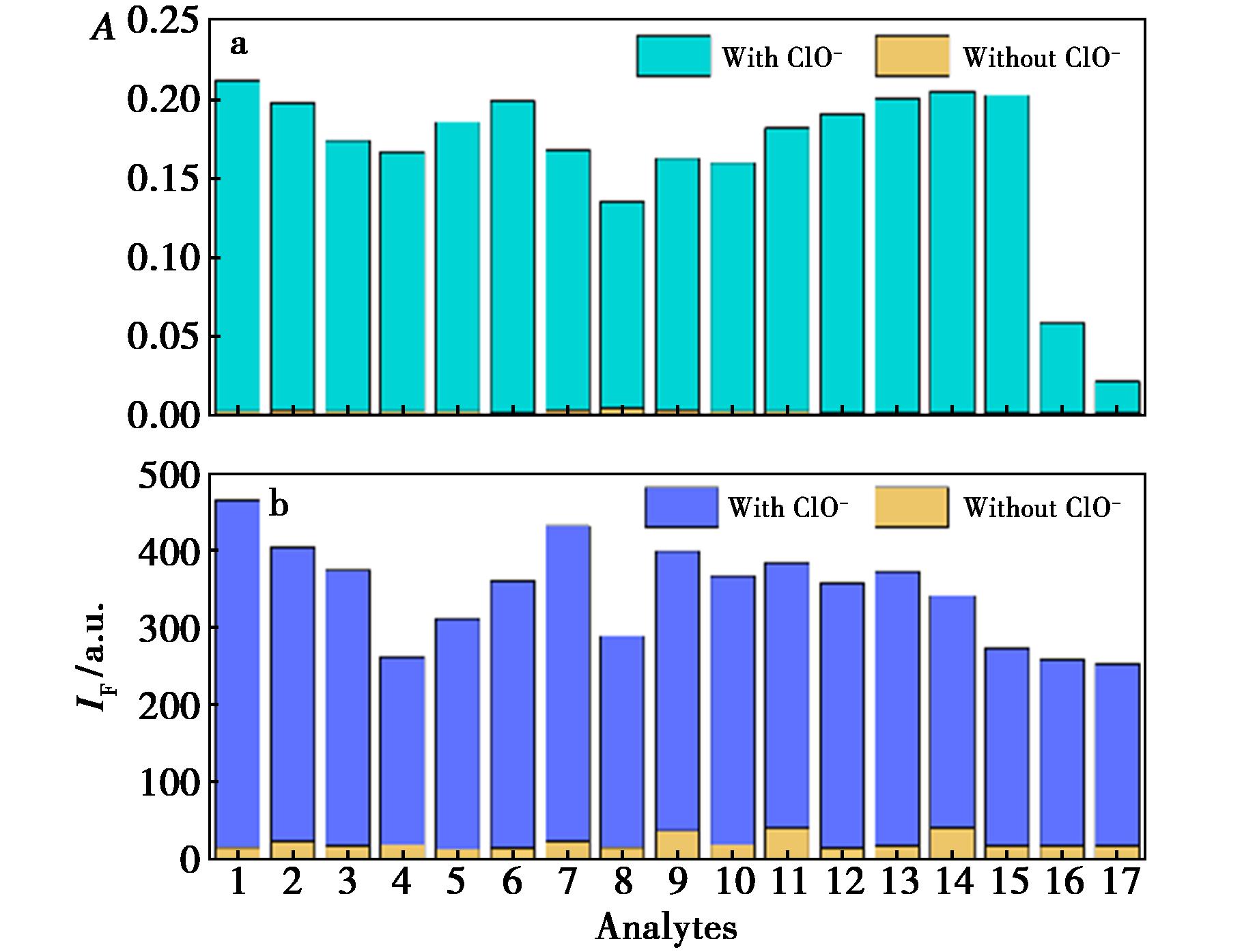
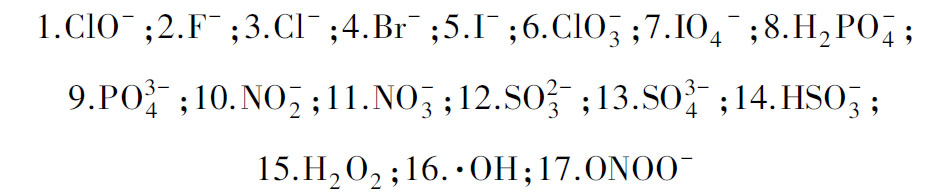
图3 探针PTZCN加入各种分析物的吸收(a)和荧光(b)光谱竞争实验
Fig.3 Absorption (a) and fluorescence (b) competition experiments of probe PTZCN with various competing analytes
2.3 探针PTZCN的光谱滴定实验
为了了解ClO-与探针之间反应的动力学过程,进行了吸收和荧光光谱滴定实验。由图4可知,随着ClO-加入量的逐渐增大(0~200 μmol/L),PTZCN溶液在465 nm处的吸光度和627 nm处的电荷转移复合物的吸光度也随之下降,当滴加200 μmol/L ClO-后,627 nm处的吸收强度下降至0.05,其吸收值和ClO-的加入量呈现较好的线性关系(R2=0.995 0)。
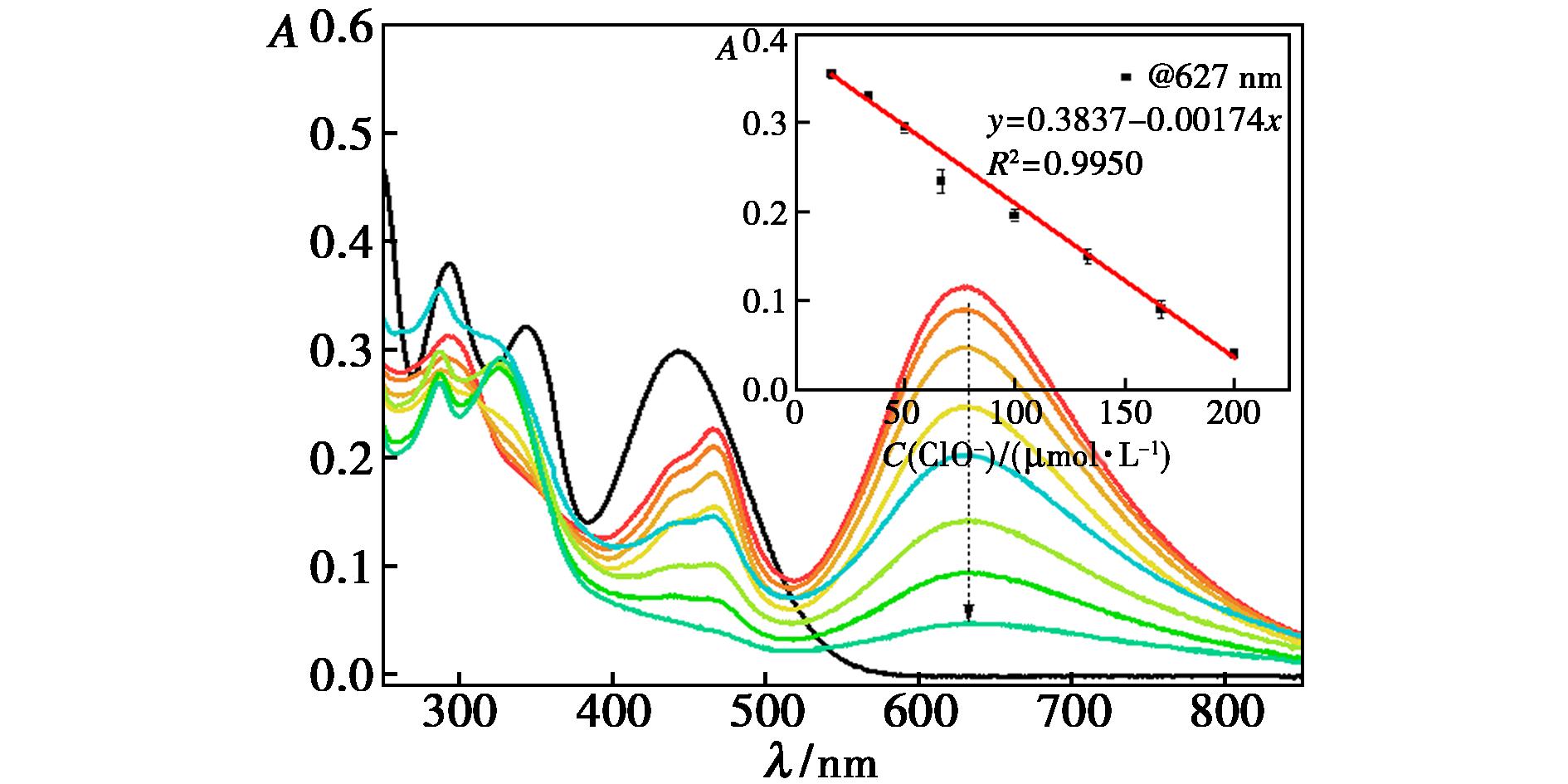
插图为I627处的吸光度值与ClO-加入量之间的线性关系
图4 PTZCN(20 μmol/L)在不同浓度ClO-作用下的吸收光谱变化
Fig.4 Absorption changes of PTZCN (20 μmol/L) with increasing ClO-
在荧光滴定中,实验发现随着ClO-加入量的不断增大,探针PTZCN溶液的发射峰值从 474 nm轻微蓝移至470 nm处,荧光强度也逐渐增强。当滴加200 μmol/L ClO-后,470 nm处的荧光强度上升至533,500 nm处的荧光强度上升至468。470 nm处的荧光强度与ClO-的浓度呈现出良好的线性关系R2=0.997 1(图5)。根据检测限公式LOD=3σ/S(σ为空白样品的标准偏差;S为标准曲线斜率),该探针的检测限为7.5×10-6 mol/L。
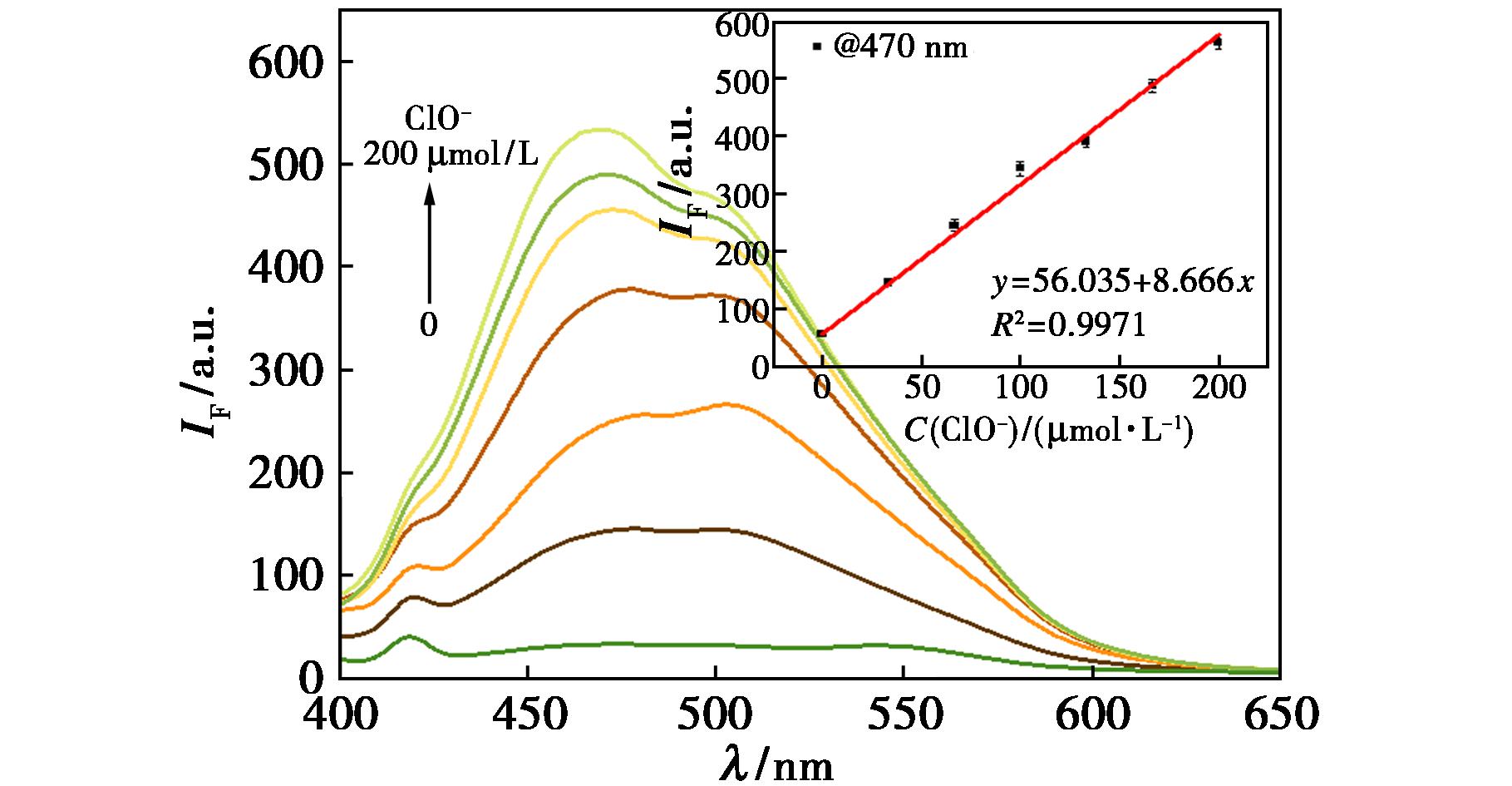
插图为I470处的荧光强度与ClO-加入量之间的线性关系
图5 PTZCN(20 μmol/L)在不同浓度ClO-作用下的荧光光谱变化
Fig.5 Fluorescence changes of PTZCN (20 μmol/L) with increasing ClO-
2.4 PTZCN在不同pH下对ClO-的响应
为了验证PTZCN的实际应用性能,在不同pH值条件下测试了探针响应的ClO-能力。从图6a可知,该探针本身在627 nm处的几乎无吸收,表明PTZCN在宽pH范围内具有稳定性。但当加入ClO-时,探针在pH 2~9的范围内的呈现逐渐上升并稳定在0.2附近;碱性增加,吸光度逐渐下降。在相同条件下,由图6b荧光测试可知,PTZCN本身的荧光对酸碱耐受性良好;当加入ClO-后,447 nm处的荧光强度逐渐上升,并且在pH 3~9的范围内稳定在450附近。当pH>9时,荧光强度出现轻微下降。这可能是由于碱性条件下ClO-的氧化性较酸性环境有所减弱所致。结果表明PTZCN能在酸性至碱性环境(特别是弱碱性的生理pH范围)中对ClO-实现精准监测。
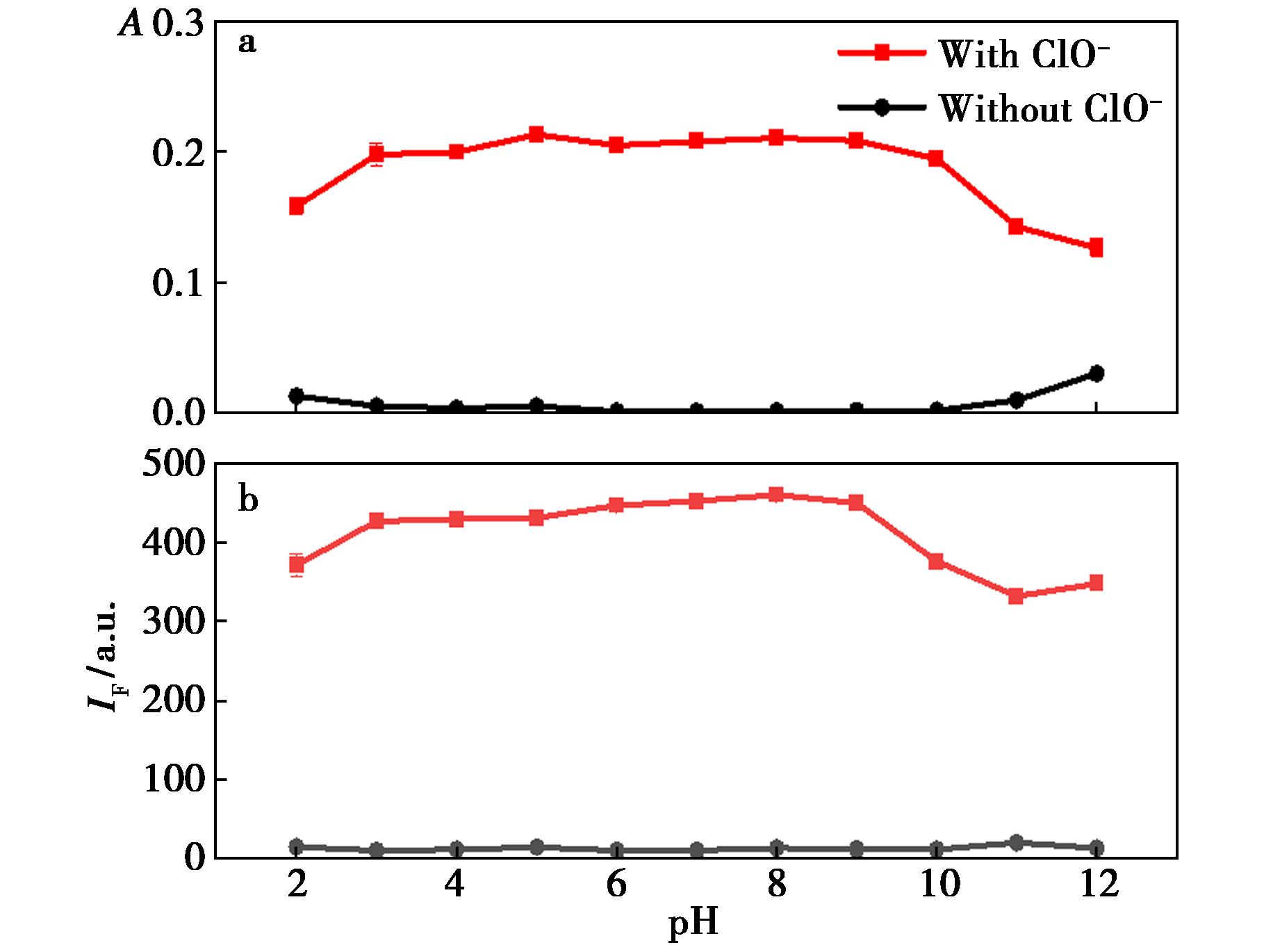
图6 pH值对PTZCN检测ClO-的吸收(a)和荧光(b)光谱
Fig.6 Asorption (a) and fluorescence (b) spectrums of pH on ClO- detection by PTZCN
2.5 PTZCN识别ClO-的机理
为了深入了解探针识别ClO-的过程,对探针进行了密度泛函理论(DFT)计算和ESI-MS测试。DFT计算显示,PTZCN的HOMO上的电子云主要分布在吩噻嗪分子上,而LUMO上的电子则都位于二氨基马来腈和C![]() N键附近。这说明探针分子本身具有明显的电荷转移效应(ICT),激发态电子会从吩噻嗪向二氨基马来腈转移(图7)。当HClO氧化C
N键附近。这说明探针分子本身具有明显的电荷转移效应(ICT),激发态电子会从吩噻嗪向二氨基马来腈转移(图7)。当HClO氧化C![]() N后,尽管LUMO依然位于吩噻嗪区域,但HOMO的电子云扩展范围受限,ICT过程被削弱。这种从PTZCN到PTZCHO的能级变化表明非辐射跃迁被抑制,荧光发射增强。ESI-MS测试发现,PTZCN的分子碎片峰m/z=317.073 5;与ClO-发生反应后,溶液中出现了新的碎片峰m/z=227.040 5,该峰与吩噻嗪醛PTZ-CHO相吻合。
N后,尽管LUMO依然位于吩噻嗪区域,但HOMO的电子云扩展范围受限,ICT过程被削弱。这种从PTZCN到PTZCHO的能级变化表明非辐射跃迁被抑制,荧光发射增强。ESI-MS测试发现,PTZCN的分子碎片峰m/z=317.073 5;与ClO-发生反应后,溶液中出现了新的碎片峰m/z=227.040 5,该峰与吩噻嗪醛PTZ-CHO相吻合。
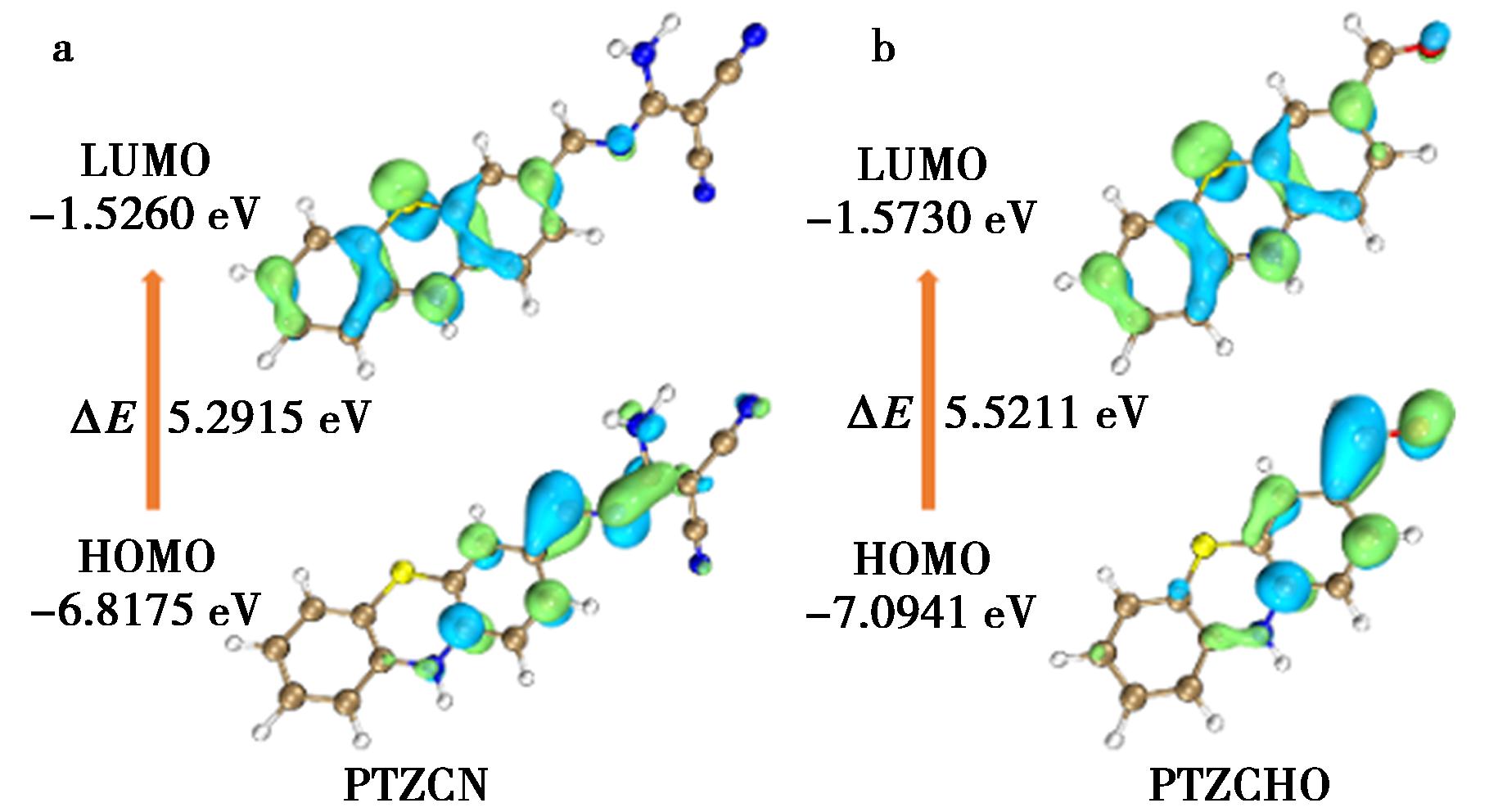
图7 探针PTZCN和PTZCHO的HOMO/LUMO理论计算能级和能隙
Fig.7 Theoretical calculation of HOMO/LUMO energy levels and energy gaps for PTZCN and PTZCHO
根据文献报道的反应机制[16,17],PTZCN识别ClO-的机理可能为:在水溶液中,探针分子C![]() N键上的碳原子首先受到ClO-的亲核进攻,然后N原子接受H+质子,形成中间体I;随后I发生水解反应,生成不稳定的中间产物II;最终进一步重排形成吩噻嗪醛PTZCHO(图8)。
N键上的碳原子首先受到ClO-的亲核进攻,然后N原子接受H+质子,形成中间体I;随后I发生水解反应,生成不稳定的中间产物II;最终进一步重排形成吩噻嗪醛PTZCHO(图8)。
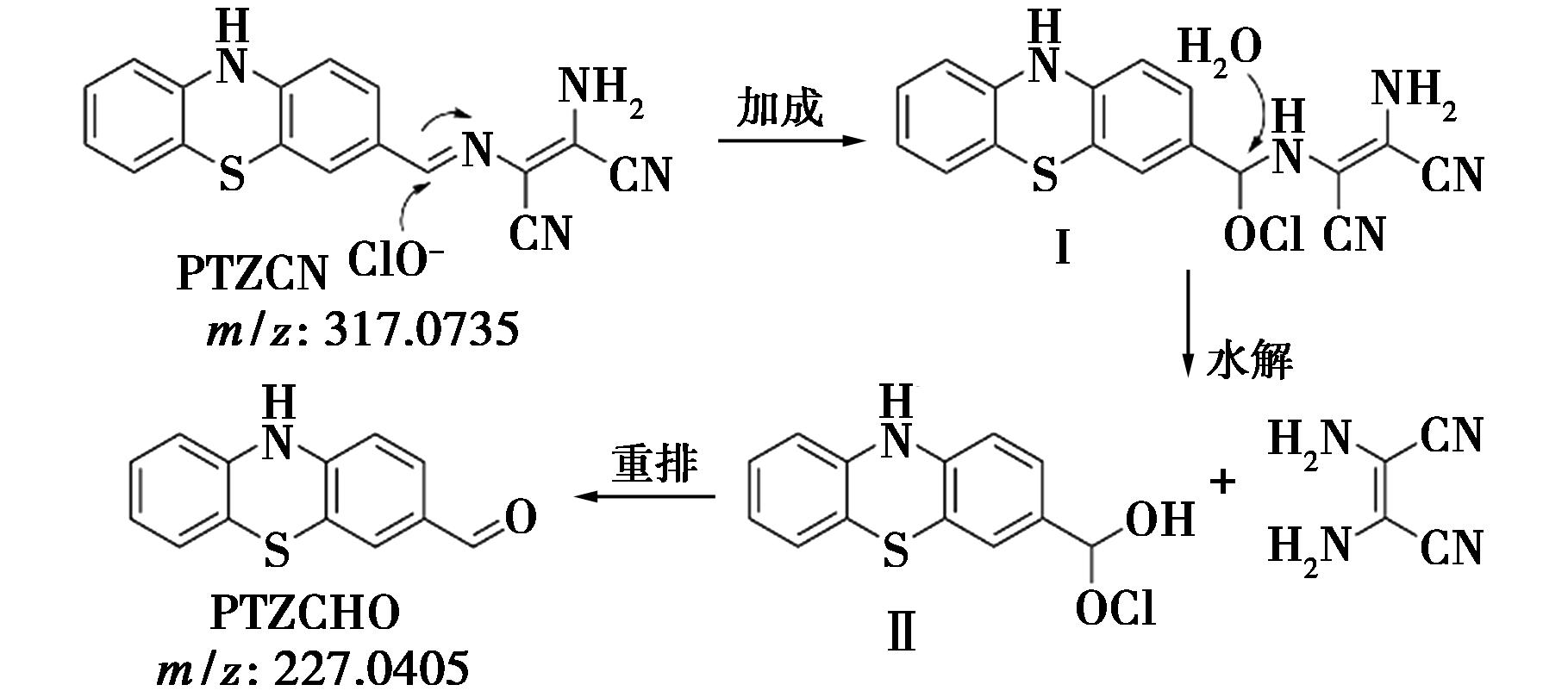
图8 探针PTZCN识别ClO-的可能机理
Fig.8 Proposed mechanism of ClO- detection by PTZCN
2.6 PTZCN在荧光成像中的应用
基于PTZCN对ClO-优异的传感性能,进一步评估了其在HeLa细胞中外源性ClO-成像的实际效果。如图9所示,仅与PTZCN(10.0 μmol/L)共孵育的HeLa细胞几乎未显示荧光信号(A1);相反,当细胞与探针PTZCN(10.0 μmol/L)及ClO-(100.0 μmol/L)共孵育后,则表现出强烈的蓝色荧光(B1);将明场和蓝光通道下的图片叠加,发现蓝色荧光主要分布在HeLa细胞的细胞核区域,而细胞质区无明显荧光变化。这表明探针PTZCN的特异性较高,可以用于荧光标记细胞核及对活细胞外源性的ClO-进行成像。
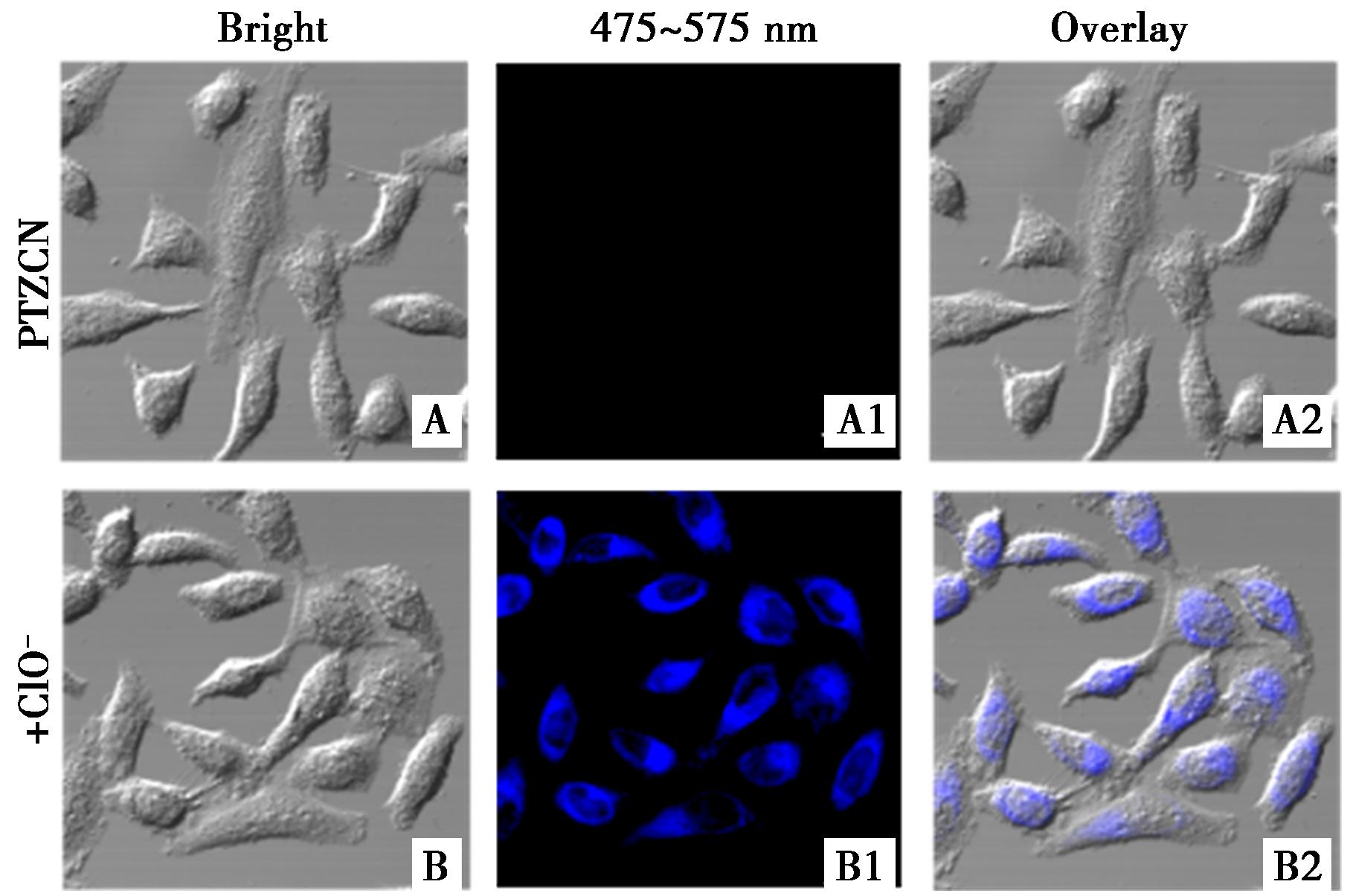
图9 PTZCN对Hela细胞中ClO-的共聚焦荧光成像
Fig.9 Confocal fluorescence microscopy images of ClO- in HeLa cells by PTZCN
为了进一步验证探针在活体斑马鱼中监测ClO-的可行性,将不同胚胎发育阶段的斑马鱼与探针进行了孵育和成像。当用ClO-刺激探针孵育6 h的斑马鱼卵后(图10a),蓝色荧光主要分布于卵黄囊部位,胚胎体部信号较弱;当斑马鱼卵发育到48 h时进入体节期(图10b),胚体开始明显形成,但卵黄囊仍主导次氯酸反应信号的部位;当斑马鱼胚胎孵化72 h后(图10c),蓝色荧光仍主要集中在卵黄囊区域,但在头部或体部的局部也出现了微弱信号。胚胎发育过程中蓝色荧光主要集中于卵黄囊,一方面次氯酸的产生主要发生在该区域,另外由于卵黄的含脂量高探针易富集于此,因而出现荧光增强响应。该实验表明PTZCN具有良好的成像能力,可用于斑马鱼体内ClO-的检测。
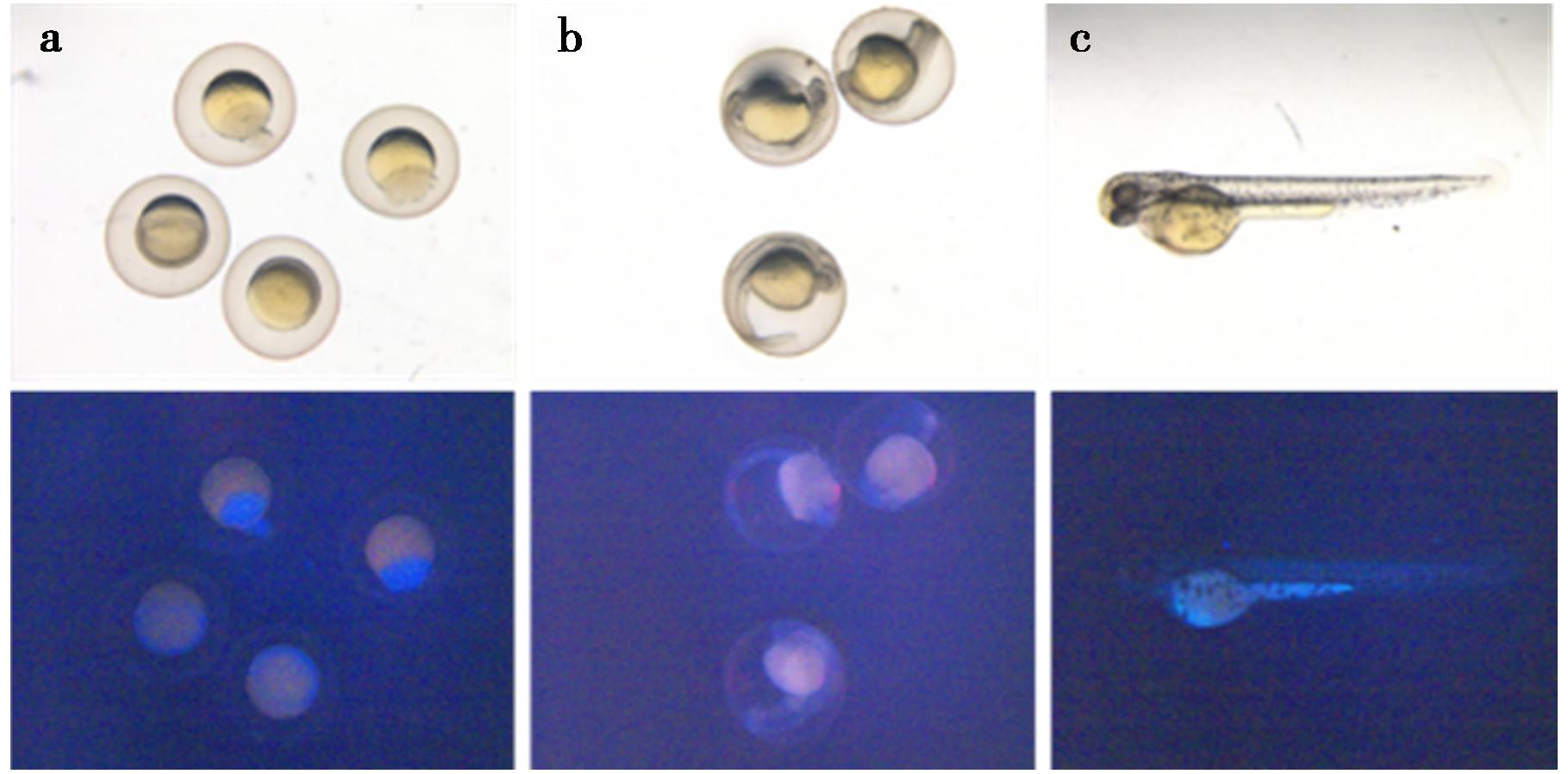
a~c孵育时间分别为6、48、72 h
图10 PTZCN对斑马鱼不同发育形态的荧光成像
Fig.10 Fluorescence imaging of PTZCN in zebrafish at different developmental stages
本文将吩噻嗪作为荧光团与二氨基马来腈通过缩合反应,制备了一种席夫碱类荧光探针分子PTZCN。
3.1 该探针在40%乙醇溶液中与ClO-反应形成电荷转移复合物,导致吸收峰红移(445→627 nm),并在470和500 nm处出现特征荧光发射。与文献报道的同类探针相比,其检测限已经达到微摩尔水平(7.5×10-6 mol/L),且在较宽的pH范围内对ClO-进行快速检测。
3.2 探针PTZCN在HeLa细胞中可实现外源性ClO-的特异性核定位成像,并在斑马鱼胚胎发育过程中呈现卵黄囊富集及72 h后头体部弱荧光分布的时空特征。
3.3 研究证实—CN和C![]() N键作为ClO-特异性反应位点可显著提升探针氧化敏感性,为开发用于生物活体内次氯酸及其盐的生物成像材料提供可参考的策略。
N键作为ClO-特异性反应位点可显著提升探针氧化敏感性,为开发用于生物活体内次氯酸及其盐的生物成像材料提供可参考的策略。
[1]Cao Y Z,Zhao Z H,Lu J H,Liu R L,Liu Y,Bai Y L.Chem.Reagents,2025,47(4):1-15.
曹艳珍,赵志豪,鲁谨菡,刘润乐,刘雨,白燕玲.化学试剂,2025,47(4):1-15.
[2]Winterbourn C C,Kettle A J.Antioxid.Redox Signal.,2013,18(6):642-660.
[3]Dickinson B C,Chang C J.Nat.Chemi.Bio.,2011,7:504-511.
[4]Hartsema E A,Hallberg L A E,Barlous K,Hawkins C L.Redox Biochem.Chem.,2023,5:100 010.
[5]Sabharwal S S,Schumacker P T.Nat.Rev.Cancer,2014,14(11):709-721.
[6]Kim J M,Zhang B Z,Park J M.Food Control,2023,152:109 865.
[7]Slaughter R J,Watts M,Vale J A,Grieve J R,Schep L J.Clin.Toxicol.,2019,57(5):303-311.
[8]Ma Z W,Zhou S J,Wang C C,Chen X P,Wang J L,Li A Q.Chem.Reagents,2021,43(8):1 130-1 135.
马志伟,周诗瑾,王川川,陈晓培,王建玲,李爱勤.化学试剂,2021,43(8):1 130-1 135.
[9]Geng Y,Wang Z,Zhou J,Zhu M,Liu J,James T D.Chem.Soc.Rev.,2023,52(11):3 873-3 926.
[10]Li D L,Zhou P F,Liu L Y,Zhang X B,Liang H,Chen L L.Phys.Test.Chem.Anal.B,2023,59(5):506-511.
李丹靓,周朴帆,刘璐瑶,张雪冰,梁好,陈丽丽.理化检验-化学分册,2023,59(5):506-511.
[11]Li L K,Xu J H,Ma Q J,Zhu N N,Liu S Z.Chem.Reagents,2023,45(7):25-33.
李林柯,徐俊红,麻秋娟,朱楠楠,刘淑珍.化学试剂,2023,45(7):25-33.
[12]Lu X,Zhan Y,He W.J.Photoch.Photobio.B,2022,234:112 528.
[13]Shen S,Yuan Y,Song J.Food Chem.,2025,485:144 547.
[14]Dua A,Selvam P,Majeed S A,Kumar S K A,Sharma H K,Ramasamy S K.J.Photoch.Photobio.A,2024,447:115 219.
[15]Zhang W,Sheng Y,Zhang M,Wang Q,Wang X,Wang H,Zhang W,Li P,Tang B.Chem.Commun.,2025,61:13 924-13 927.
[16]Zhang X,Zhang F,Chai J,Yang B,Liu B.Spectrochim.Acta A,2021,256:119 735.
[17]Xia W,Yuan Y,Shen S,Zhu Y,Wang Y,Hou Y,Huang B,Tian M,Feng F.J.Food Compos.Anal.,2024,128:106 053.