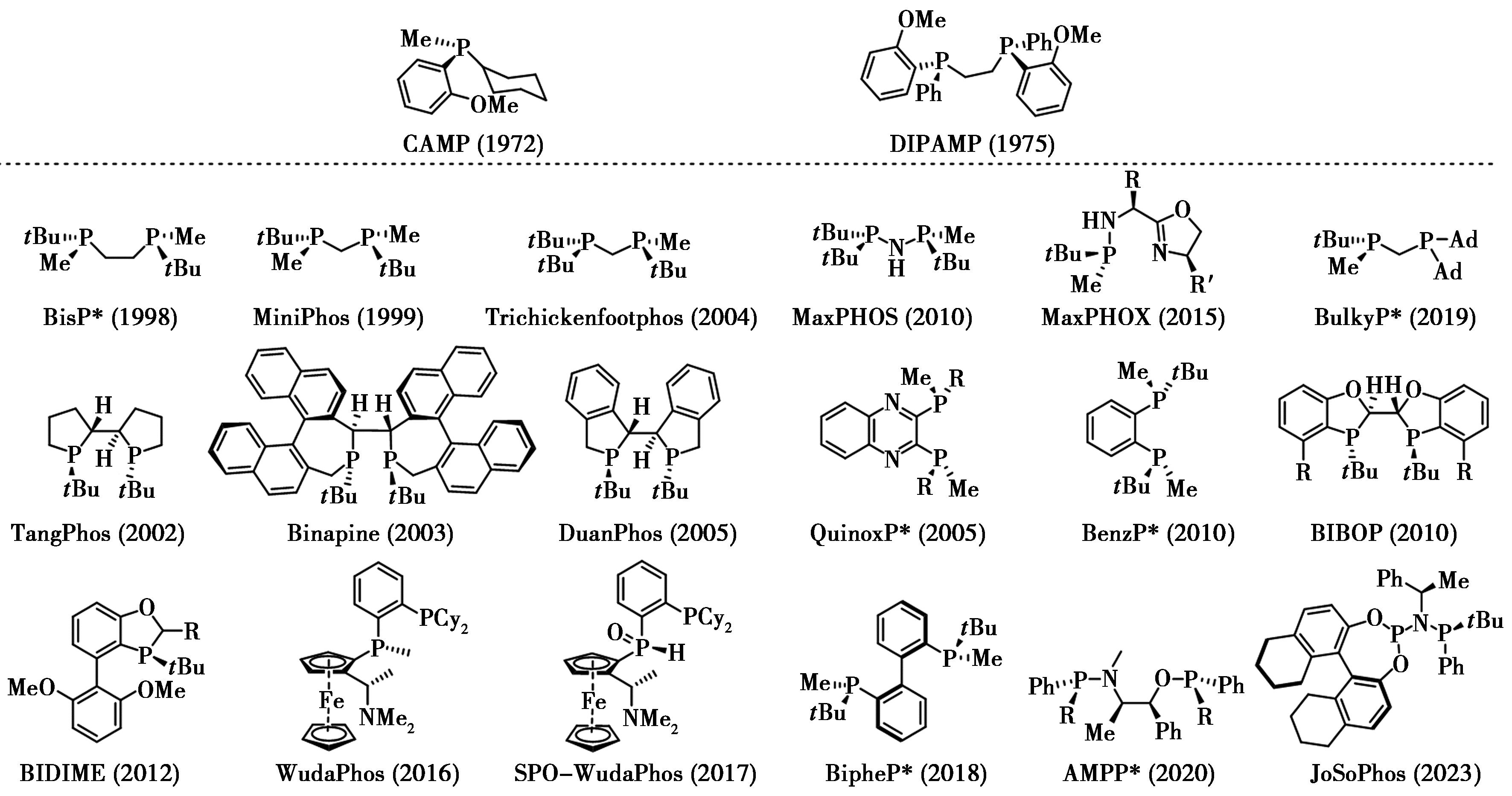
图1 代表性磷手性配体
Fig.1 Representative P-chiral phosphorus ligands
特约专题
膦配体因其在过渡金属催化中卓越的电子和空间位阻可调性已成为该领域最重要的配体类型之一。通过对金属中心电子云密度和空间环境的精准调控,这类配体可以为多种转化和反应提供优异的反应活性和选择性。膦配体的发展促进了近代工业催化的发展,而手性膦配体的发展则显著推进了不对称催化领域。手性膦配体根据磷中心手性特征可分为两类:骨架手性膦配体和磷手性配体。虽然两类配体均适用于多种催化反应,磷手性配体因其手性环境更接近作为反应中心的过渡金属在手性控制方面往往具有更显著的优势。
自上个世纪七十年代Knowles等[1]发展第一代磷手性配体CAMP及DIPAMP并在铑催化不对称氢化实现帕金森治疗药物L-DOPA的高对映选择性合成中取得开创性成功以来,磷手性配体的发展在不对称催化领域愈发受到广泛的关注。根据膦配体与金属配位后的四象限分析理论,化学家有意识地在磷原子上引入叔丁基和金刚烷基等大位阻基团有利于固定其构象,以期获得更加精准的手性控制。因此,以 BisP*、TangPhos、DuanPhos、QuinoxP*及BIBOP为代表的第二代磷手性配体被接连设计合成并成功应用于不对称氢化反应,展现了优异的催化活性和对映选择性[2,3]。图1列举了20年来报道的具有代表性的磷手性配体。目前大多数磷手性配体已实现商业化且在多种工业催化反应中实现规模化应用。

图1 代表性磷手性配体
Fig.1 Representative P-chiral phosphorus ligands
近10年来,基于二氢苯并氧杂膦烷骨架的磷手性配体取得了长足的发展,目前已报道超过百个配体并应用于各类有机化学转化中[4,5]。该骨架配体主要包括以下5类:二氢苯并氧杂膦配体(BOP)、2位膦酰基取代的二氢苯并氧杂膦配体(BOPPO)、2位膦基取代的二氢苯并氧杂膦配体(POP)、双二氢苯并氧杂膦配体(BIBOP)以及联芳基双二氢苯并氧杂膦配体(BABIBOP)(图2)。这些大位阻富电子配体在多种转化中展现出优异的反应活性和选择性,其主要特征包括:1)结构刚性且富电子,尤其有利于促进交叉偶联反应中的氧化加成与还原消除步骤;2)构型明确,能够构建清晰的手性环境,用于不对称催化;3)通过在二氢苯并氧杂膦烷骨架不同位点引入取代基,可系统调控配体的电子效应和空间位阻特性,例如在靠近磷原子的芳基位置引入取代基可显著影响手性口袋的形状、深度及电子性质;4)多数配体为固体且空气条件下稳定,操作简便,适用于工业化生产;5)大多数已实现公斤级规模量产,其中一些实现百公斤制备,满足工业应用需求。这类成本可控的磷手性二氢苯并氧杂膦烷配体正积极推动不对称催化反应的工业化应用。
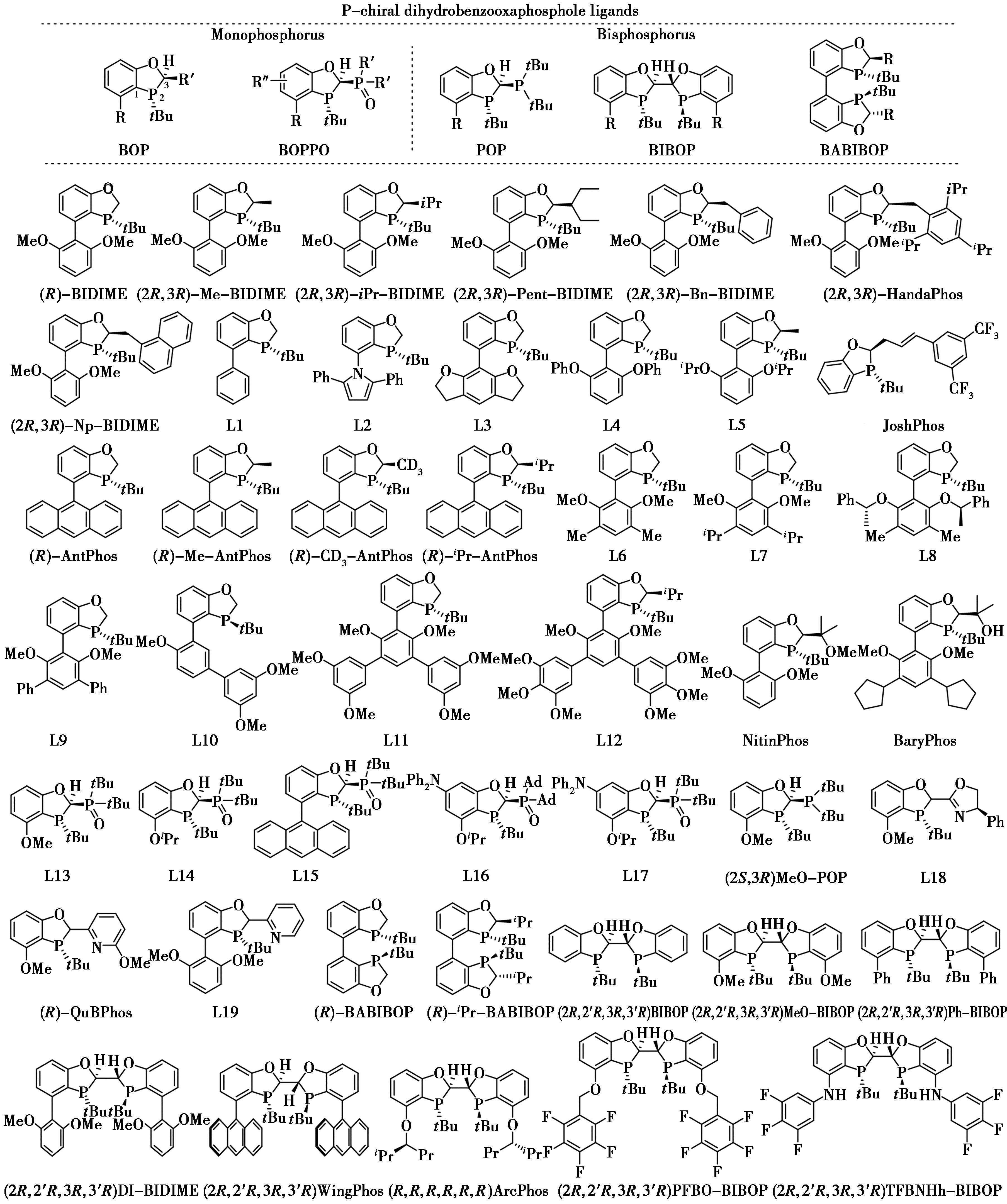
图2 该综述中涉及的磷手性二氢苯并氧杂膦烷配体
Fig.2 P-chiral dihydrobenzooxaphosphole ligands involved in this review
2019年,Tang等[4]以个人评形述式总结了基于二氢苯并氧杂膦烷骨架的磷手性配体在不对称催化中的应用,例如双膦配体(BIBOP)在多种不对称氢化中展现超高的催化转化数,为手性胺、醇、羧酸及α/β-氨基酸的合成提供高效实用的解决方案,促进多个手性天然产物和治疗药物的简洁高效合成。2024年,Tang等[5]对该类配体在催化与合成中的应用做了更加全面的总结,详细阐述了其在交叉偶联反应、不对称偶联、不对称环化反应、不对称加成反应以及不对称氢化反应中的应用,展现了其广泛且优异的催化特性。
近期,化学家们又发现了该类配体在不对称催化领域的诸多独特催化特性,取得了众多重要的研究进展,包含杂环类化合物在内的更加普适的不对称Suzuki-Miyaura偶联、分子内和分子间的不对称碳氢键活化、构型保持的不对称偶联以及不对称还原Heck偶联等。本文将延用2024年总结的叙述结构,内容分为4个主要部分,包含磷手性二氢苯并氧杂膦烷配体在偶联反应包含不对称偶联、不对称加成反应、不对称环化反应以及不对称氢化反应中的应用,并就部分案例详细阐述其反应机理。旨在更新该类磷手性二氢苯并氧杂膦烷配体在不对称催化与合成中的应用进展,期望给从事不对称催化领域的化学工作者带来启发,不涉及配体的详细合成方法。
交叉偶联反应已成为构建碳碳键、碳杂键最有效的策略之一,在有机合成化学、药物化学和材料科学领域的应用日益广泛。基于二氢苯并氧杂膦烷骨架的磷手性单膦配体已被证实是多种交叉偶联反应的高效催化剂,尤其是不对称偶联在轴手性药物合成发挥着至关重要的作用。本节重点阐述了其在以下领域的进展:包含高效大位阻碳碳键偶联、不对称Suzuki-Miyaura偶联、不对称Heck类型反应、不对称碳氢键芳基化、不饱和碳碳键的不对称官能团化、烯丙位的不对称官能团化以及其他偶联反应。
过去数十年间,关于大位阻Suzuki-Miyaura交叉偶联反应的研究成果较为有限。Buchwald团队曾报道使用菲罗啉单膦配体通过Suzuki-Miyaura交叉偶联构建四邻甲基取代联芳烃的方法,但该策略中两个邻位取代基仅限于甲基。2010年,Tang等[6]利用二氢苯并氧杂膦烷配体BIDIME或AntPhos,在低催化剂负载量下成功实现了邻位四取代联芳烃的合成(图3a)。值得注意的是,该方法可兼容异丙基、异丙氧基等大位阻取代基,收率最高达99%。随后,通过使用相同催化剂体系,进一步实现了邻位双取代卤代芳烃与仲烷基硼酸之间的大位阻芳基-烷基Suzuki-Miyaura偶联。该方法的高效性在分子齿轮化合物的合成中得到充分验证,以优异收率获得目标产物(图3b)[7,8]。
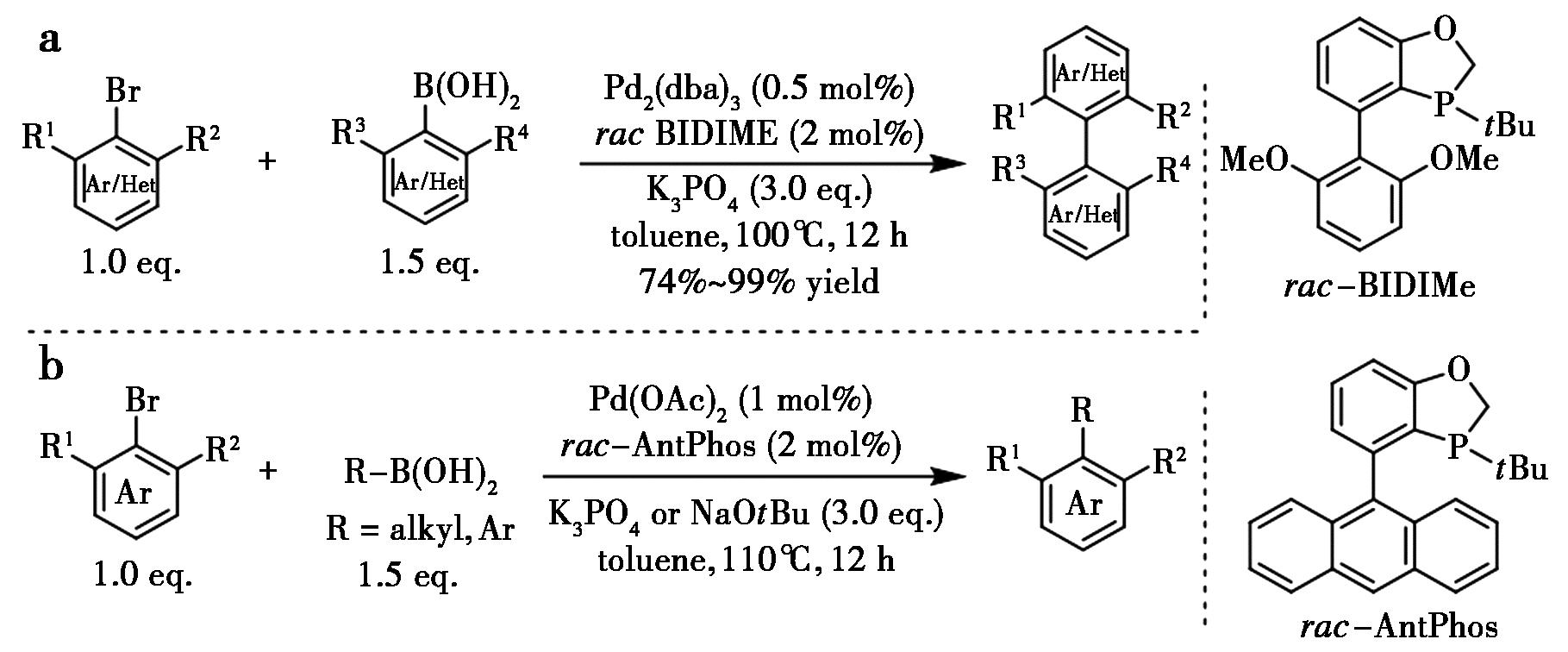
a.文献[6];b.文献[7,8]
图3 钯催化的大位阻芳基-芳基及芳基-烷基Suzuki-Miyaura交叉偶联反应[6-8]
Fig.3 Pd-catalyzed steric hindered aryl-aryl and aryl-alkyl Suzuki-Miyaura cross-coupling reactions[6-8]
芳基-烷基Suzuki-Miyaura交叉偶联通常因固有的β-氢消除问题,易产生还原副产物和异构化副产物,导致反应体系复杂。Tang等[9-11]利用具有弱配位作用的BOPPO配体可有效抑制β-氢消除现象。该类配体不仅能高效抑制异构化与还原副反应,更首次实现了邻位双取代卤代芳烃与异丙基硼酸的高收率交叉偶联(图4),其合成实用性已在雌酮的后期修饰和棉酚的高效合成中得到成功验证。
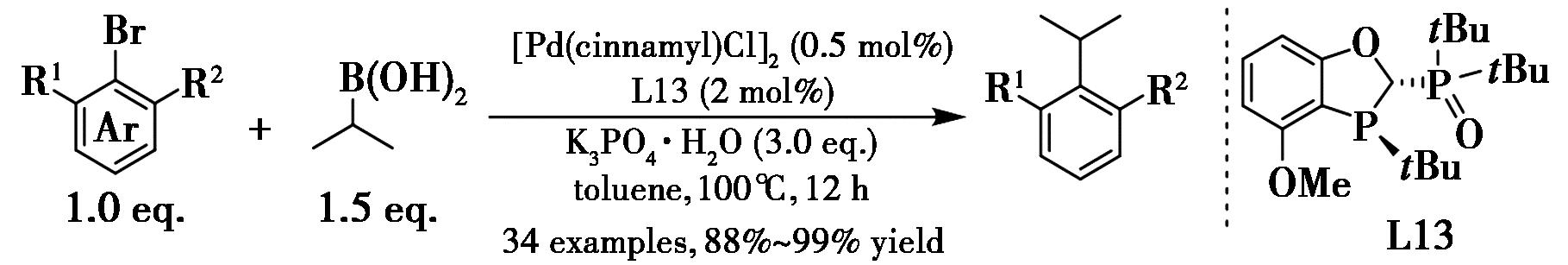
图4 钯-BOPPO配体催化的大位阻芳基-烷基Suzuki-Miyaura交叉偶联反应[9-11]
Fig.4 Pd-catalyzed sterically hindered aryl-alkyl Suzuki-Miyaura cross-coupling with BOPPO ligand[9-11]
为了进一步方便该类配体在化学工艺开发中的使用,Sieber等[12]和Denmark等[13]合成了 BIDIME和AntPhos的第3代钯配合物预催化剂(图5),在包含杂环的Suzuki-Miyaura偶联反应中展现了高效的催化效率,仅在30 min内反应即完成,并且成功应用于连续流反应。
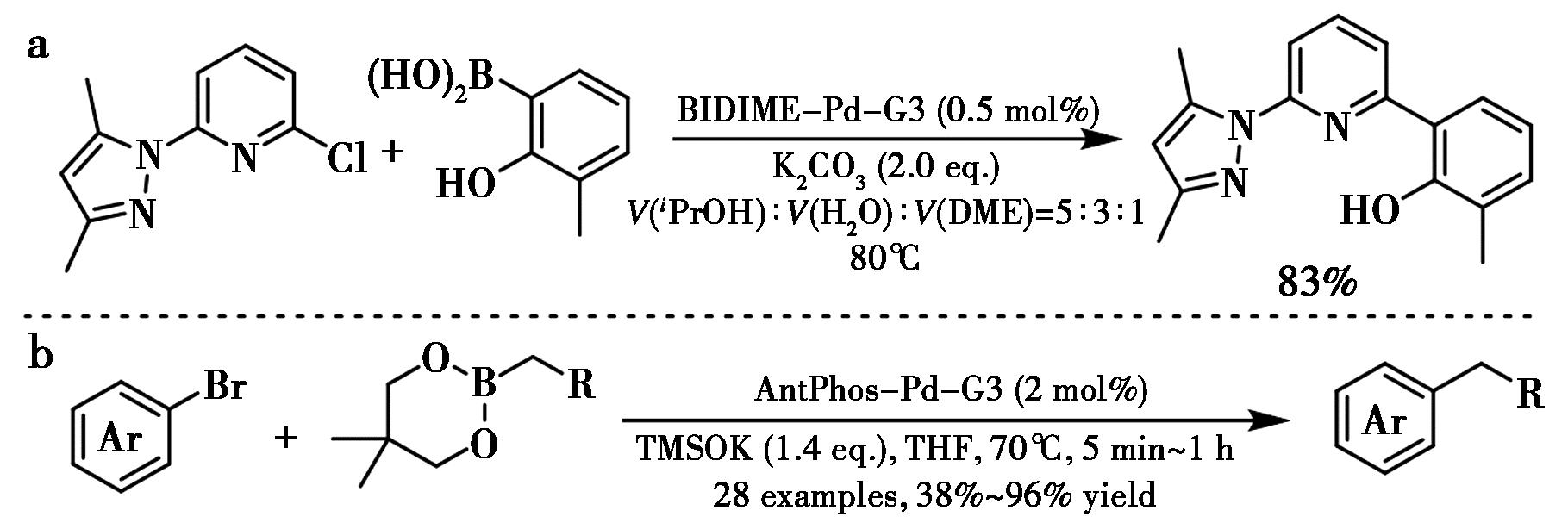
a.文献[12];b.文献[13]
图5 第三代钯配合物催化的Suzuki-Miyaura交叉偶联反应[12,13]
Fig.5 Pd-catalyzed Suzuki-Miyaura cross-coupling reactions using Pd-G3 complex[12,13]
2017年,Patel等[14]报道了采用BIDIME为配体,在非离子表面活性剂Triton X-100存在下,于水相中实现超低剂量钯催化的Suzuki-Miyaura交叉偶联反应(图6),该方法适用于多种联芳烃的高效合成,收率优异(84%~98%)。值得关注的是,该方法在10 g规模上成功合成11β-HSD-1抑制剂,收率接近定量且纯度优异。
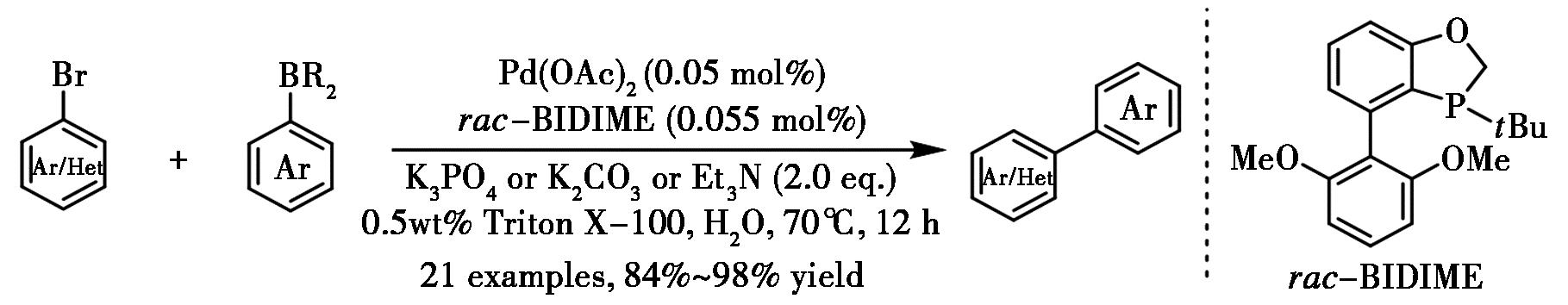
图6 钯-BIDIME催化水相芳基-芳基Suzuki-Miyaura交叉偶联反应[14]
Fig.6 Pd-BIDIME catalyzed Suzuki-Miyaura cross-coupling between two aryls in water[14]
Lipshutz等[15-17]报道了以HandaPhos钯环化合物作为前体催化剂,在水相中实现Suzuki-Miyaura交叉偶联的方法,催化剂负载量可低至25 mg/L(图7)。研究表明,钯环联苯骨架上的取代基对反应活性具有显著影响(叔丁基取代的收率为20%,二异丙基取代的收率为99%)。该技术已成功应用于医药、农业和材料领域多个目标分子的合成。尤为突出的是,水相催化剂可循环使用4次仍保持活性。
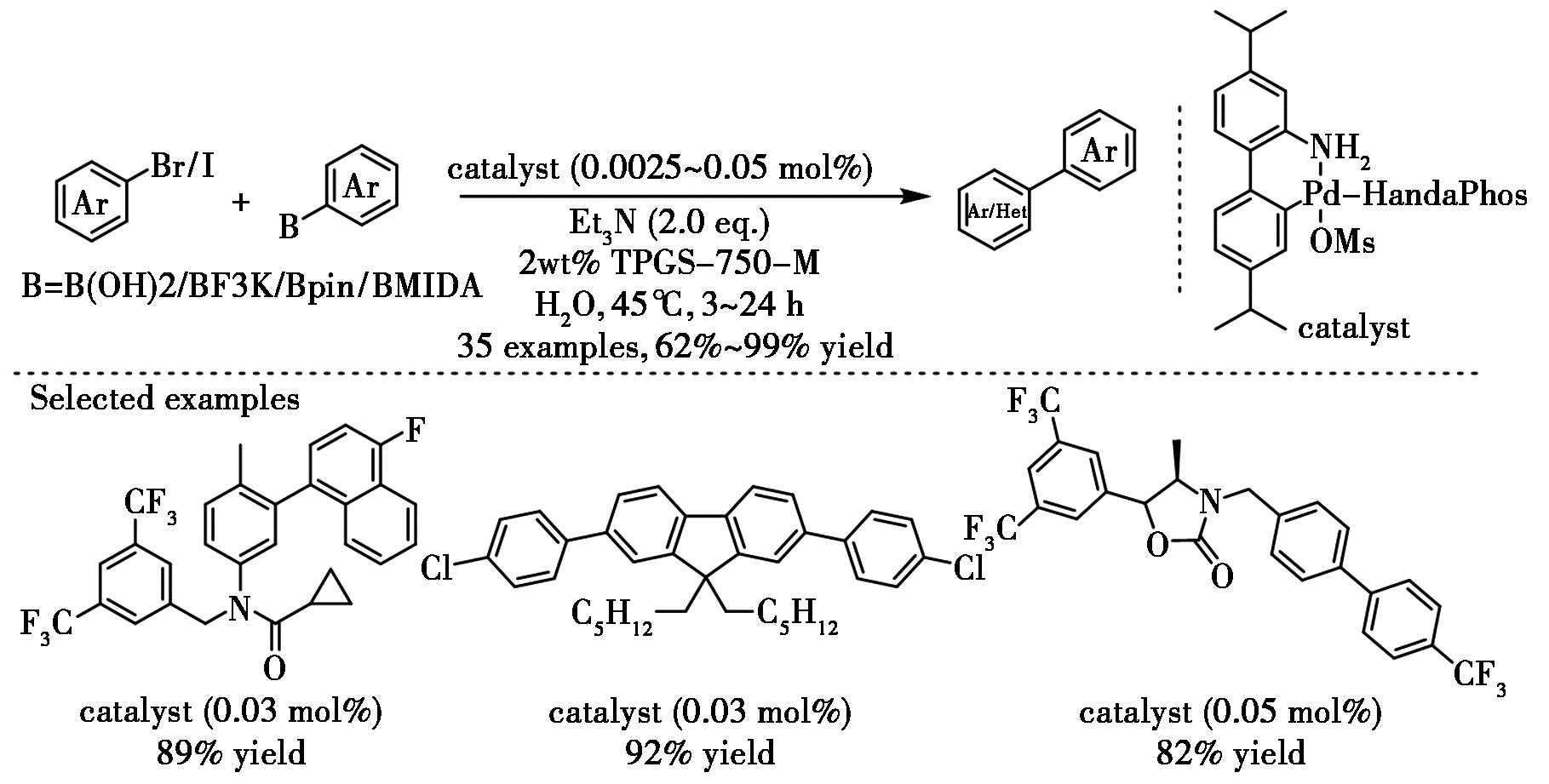
图7 钯-HandaPhos催化水相芳基-芳基Suzuki-Miyaura交叉偶联反应[15-17]
Fig.7 Pd-HandaPhos catalyzed Suzuki-Miyaura cross-coupling between two aryls in water[15-17]
除了通过补加表面活性剂实现水相偶联反应,Shada等[18]在BIDIME配体上引入磺酸钠基团,合成了水溶性的配体CSPhos,在相转移催化剂存在条件下成功实现了芳基-芳基Suzuki-Miyaura偶联(图8),催化剂量低至0.1 mol%。
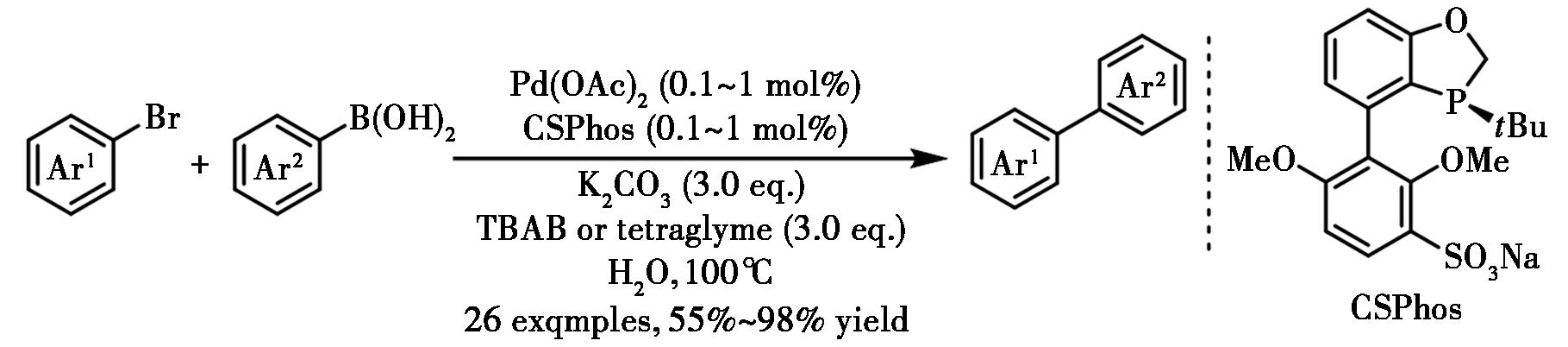
图8 钯-CSPhos催化水相芳基-芳基Suzuki-Miyaura交叉偶联反应[18]
Fig.8 Pd-CSPhos catalyzed Suzuki-Miyaura cross-coupling in water[18]
Lipshutz与Handa合作开发了BIDIME的衍生配体HandaPhos[19],该配体在无铜盐条件下,以纯水为溶剂即可高效催化Sonogashira偶联反应(图9),在1 000 mg/L钯催化剂负载量下,多种杂芳基/芳基卤代物与取代炔烃均可顺利反应,以70%~95%的收率获得目标产物[19]。值得注意的是,带有2,4,6-三异丙基苄基取代基的HandaPhos配体对该转化展现出独特催化效果,而XPhos和BIDIME配体在此体系中均无效。
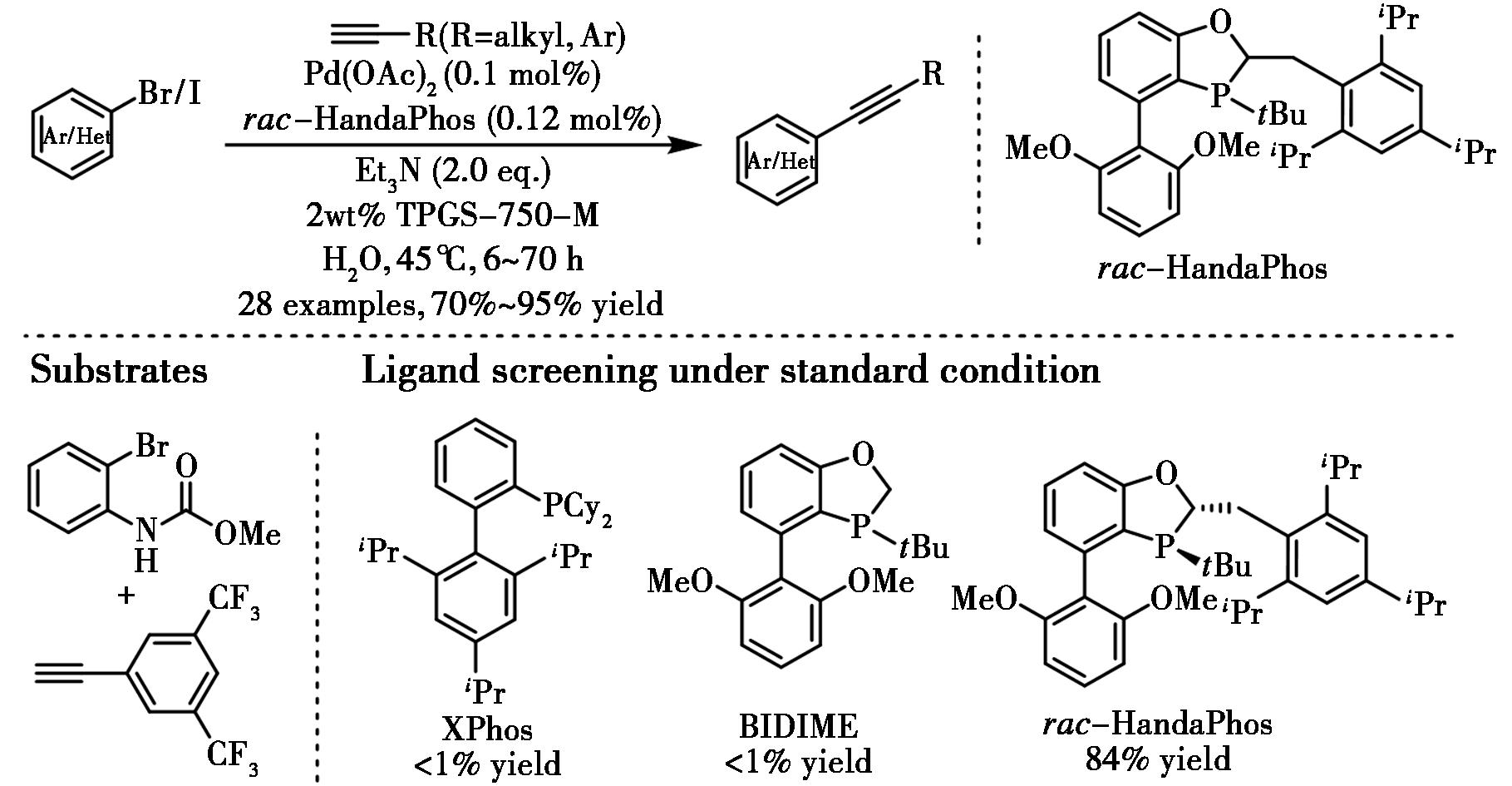
图9 钯-HandaPhos催化水相Sonogashira交叉偶联反[19]
Fig.9 Pd-HandaPhos catalyzed Sonogashira cross-coupling in water[19]
轴手性联芳烃结构广泛存在于多种生物活性天然产物和药物活性成分中[20,21]。不对称Suzuki-Miyaura交叉偶联仍是构建多样化轴手性联芳烃最直接、通用且经济高效的方法[22]。2012年,Tang等[23]报道了采用2-取代BIDIME手性配体,通过钯催化不对称Suzuki-Miyaura偶联反应高效构建系列功能化手性联芳烃的新方法(图10),该反应兼具高收率与优异对映选择性(e.e.值高达96%)。
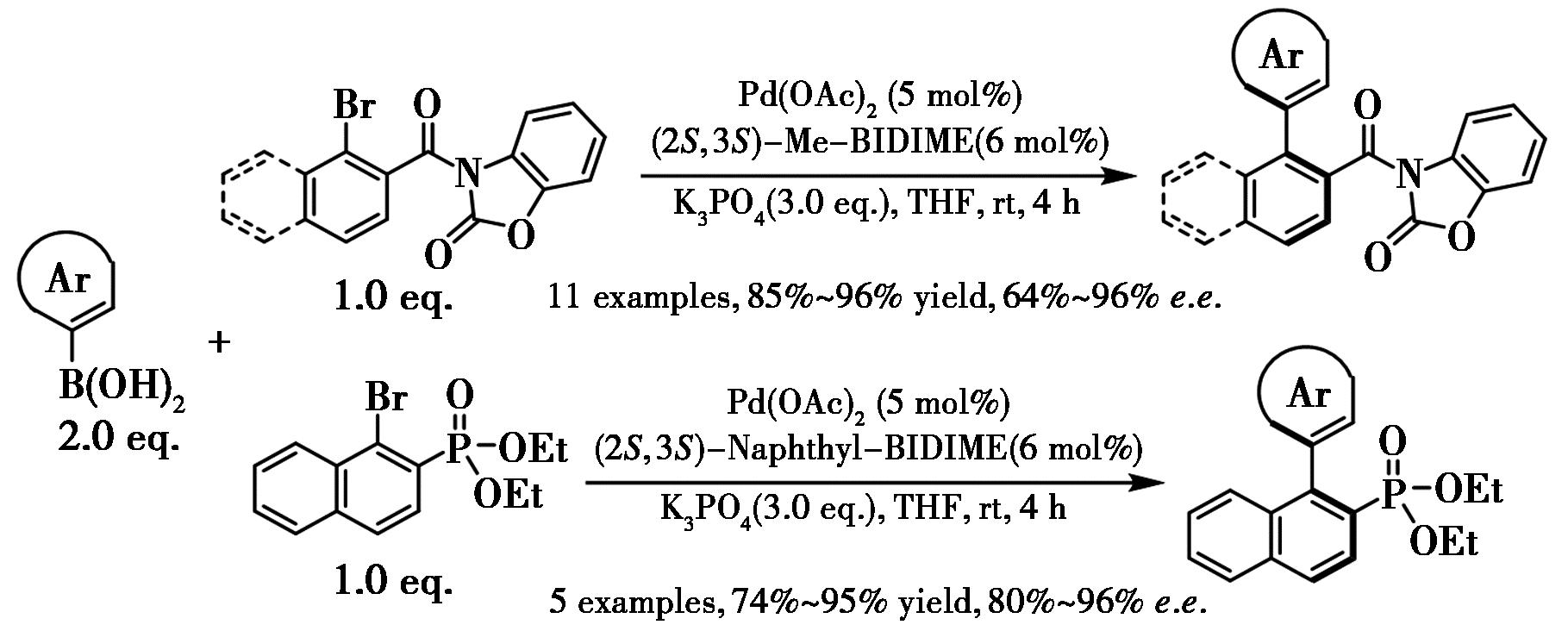
图10 钯-BIDIME催化的不对称Suzuki-Miyaura交叉偶联反应[23]
Fig.10 Pd-BIDIME catalyzed asymmetric Suzuki-Miyaura cross-coupling reaction[23]
2014年,Tang等[24]发展了高效不对称Suzuki-Miyaura偶联完成了手性联芳烃天然产物Korupensamine A和B的全合成,并结合非对映选择性氢化反应实现了Michellamine B的简洁立体选择性合成(图11)。研究发现,高极性苯并噁唑烷酮基团与芳基硼酸偶联底物扩展π体系之间的极性-π相互作用对高对映选择性至关重要。
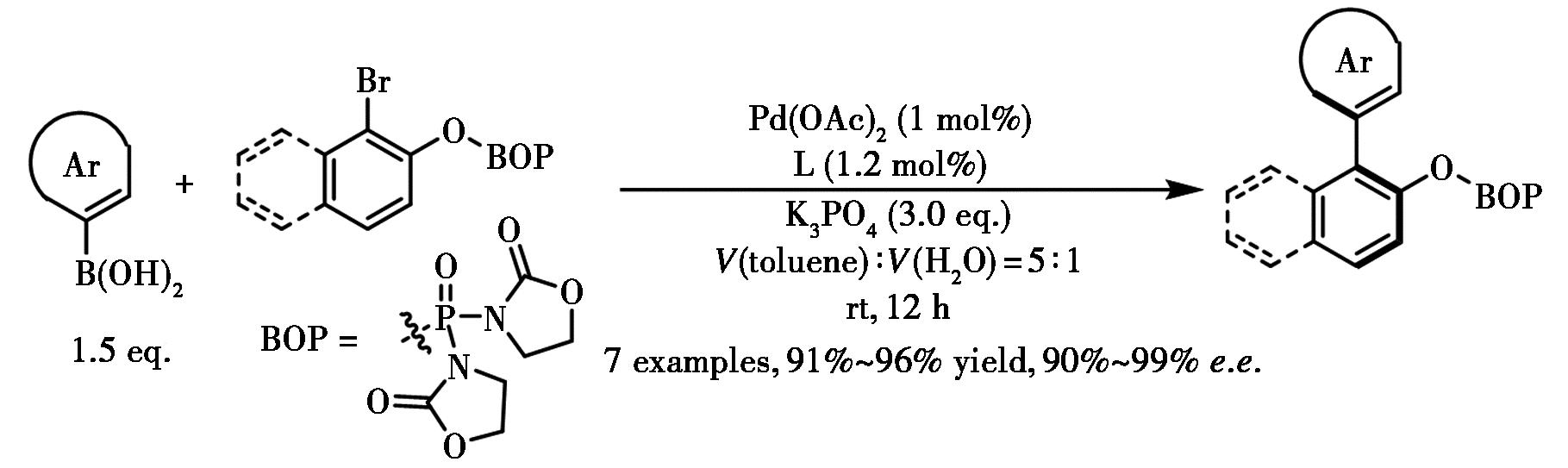
图11 钯-BIDIME催化的不对称Suzuki-Miyaura交叉偶联反应及在天然产物合成的应用[24]
Fig.11 Pd-BIDIME catalyzed asymmetric Suzuki-Miyaura cross-coupling in the synthesis of natural products[24]
2015年,Fandrick等[25]发现底物中存在苄位手性官能团时,其不对称偶联反应也能兼容,该团队报道了采用手性BIDIME配体通过不对称 Suzuki-Miyaura交叉偶联高效合成复杂阻转异构HIV整合酶抑制剂的方法(图12)。
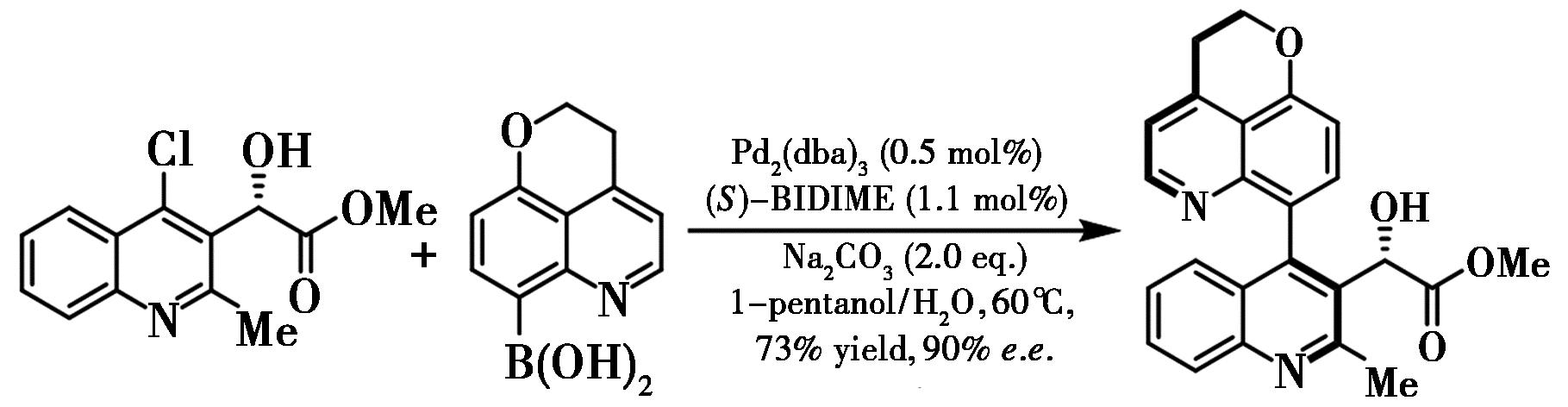
图12 钯-BIDIME催化的不对称Suzuki-Miyaura交叉偶联反应[25]
Fig.12 Pd-BIDIME catalyzed asymmetric Suzuki-Miyaura cross-coupling reaction[25]
2020年,Tang等[26]开发了BaryPhos配体用于对映选择性Suzuki-Miyaura交叉偶联,成功合成系列具有重要合成价值的手性四邻位取代联芳烃,且兼具优异对映选择性和收率(图13a)。BaryPhos的巧妙设计代表了一种新的不对称交叉偶联催化模式,通过配体与两个偶联底物之间的非共价相互作用实现高效立体诱导。该方法稳健、实用且普适,实现了具有治疗价值的男性避孕药和抗肿瘤药物棉酚的对映选择性全合成。紧接着,Tang等[27]利用钯-BaryPhos体系能有效实现含邻位磺酰基或邻位硝基底物的不对称Suzuki-Miyaura交叉偶联,以优异收率和对映选择性获得多种功能化联芳烃(图13b),进一步表明了其普适性。该方法成功用于isoplagiochin D的十步简洁不对称合成,并构建了具有圆偏振发光特性的手性光学分子。
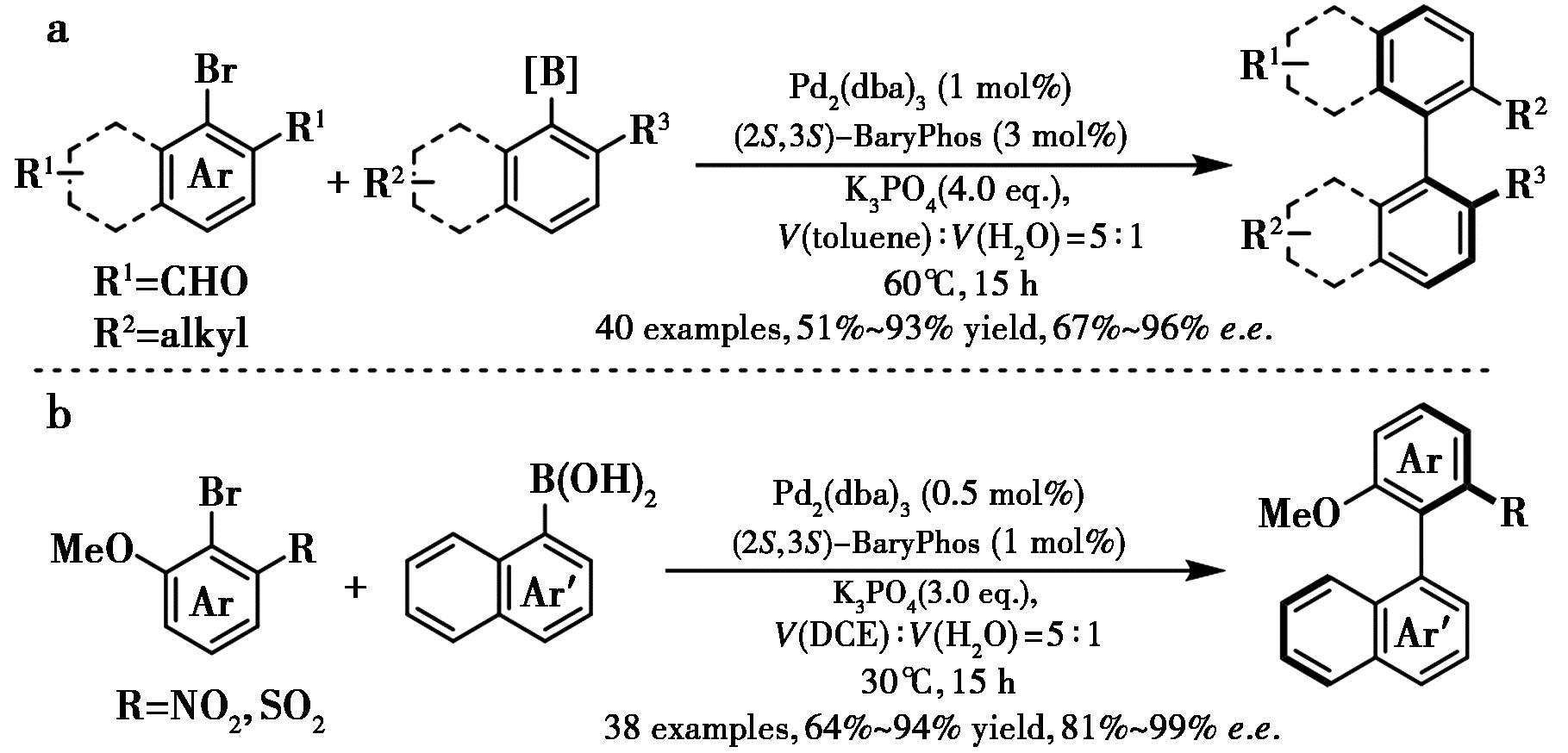
a.文献[26];b.文献[27]
图13 钯-BaryPhos催化邻位含各种官能团芳基底物的不对称Suzuki-Miyaura交叉偶联反应[26,27]
Fig.13 Pd-BaryPhos catalyzed asymmetric Suzuki-Miyaura cross-coupling for aryl substrates with various functionalities[26,27]
近年来,含轴手性的KRAS药物受到药物化学家的广泛关注,但构建复杂杂环的轴手性极具挑战性。2022年,强生公司的Jouffroy等[28]报道了采用BIDIME型配体ent-L7实现吡唑和吲哚化合物间的高效不对称Suzuki-Miyaura交叉偶联,以96%收率和52% e.e.值获得四邻位取代杂芳基产物(图14a)。最近,阿斯利康公司研究团队Howell等[29]系统筛选研究了复杂轴手性大环结构的抗肿瘤药物分子AZD5991的合成路线,其中,关键杂环轴手性的构建可以顺利在钯-BaryPhos催化体系下实现,以73%收率和97% e.e.实现吡唑和吲哚底物间的高效不对称Suzuki-Miyaura交叉偶联(图14b)。
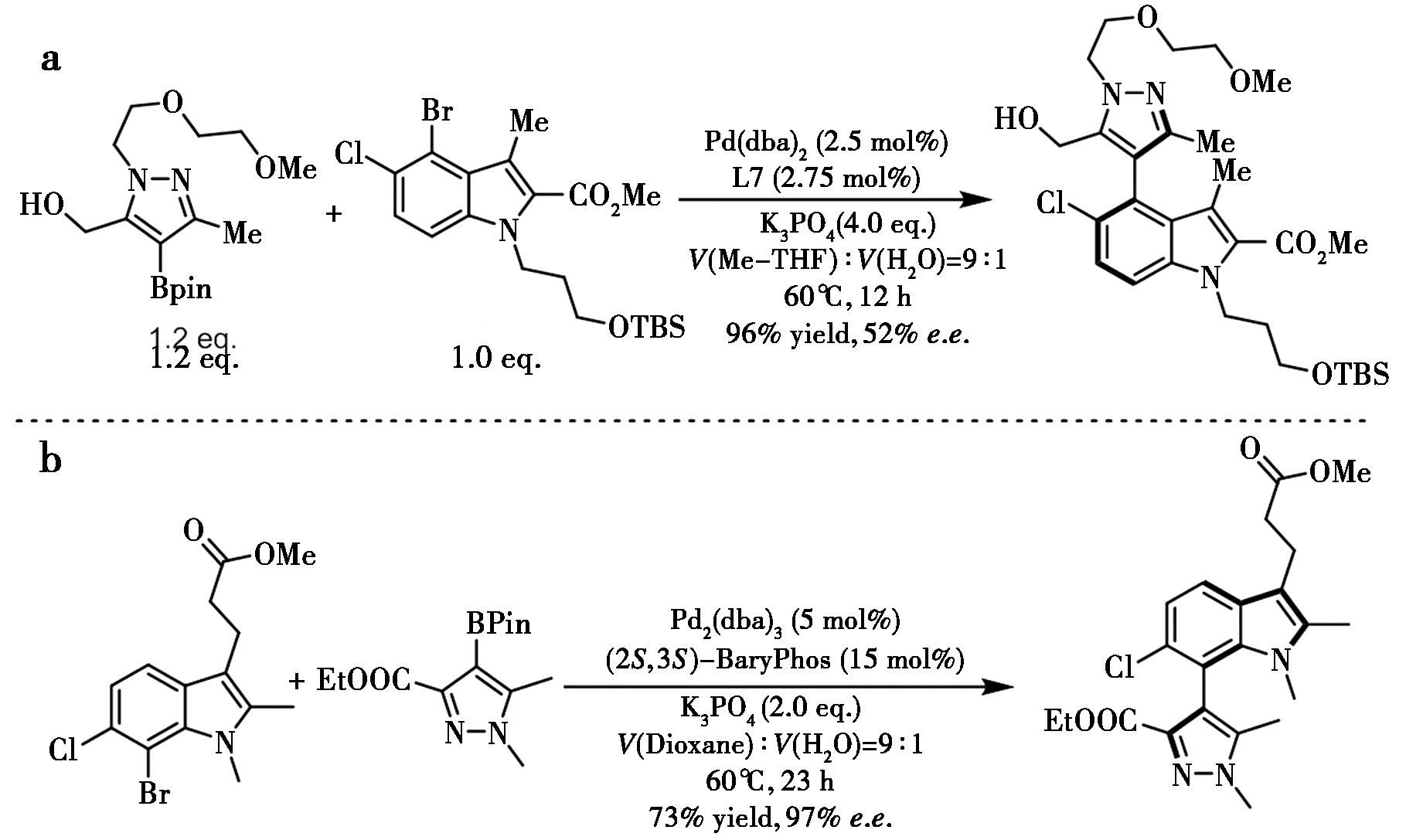
a.文献[28];b.文献[29]
图14 钯催化杂芳基底物的不对称Suzuki-Miyaura交叉偶联反应[28,29]
Fig.14 Pd-catalyzed asymmetric Suzuki-Miyaura cross-coupling between two heteroaryl substrates[28,29]
在缺少底物与催化剂相互作用的情况下,在配体BIDIME的氧磷之间引入带有二甲氧基(DMM)取代基,可高效合成二甲基取代四邻位取代联萘(收率97%,89% e.e.)(图15),但该催化体系存在底物适用范围有限且硼酸酯用量较高等局限性。使用手性BIDIME配体的不对称Negishi交叉偶联反应仅获得70% e.e.[30]。
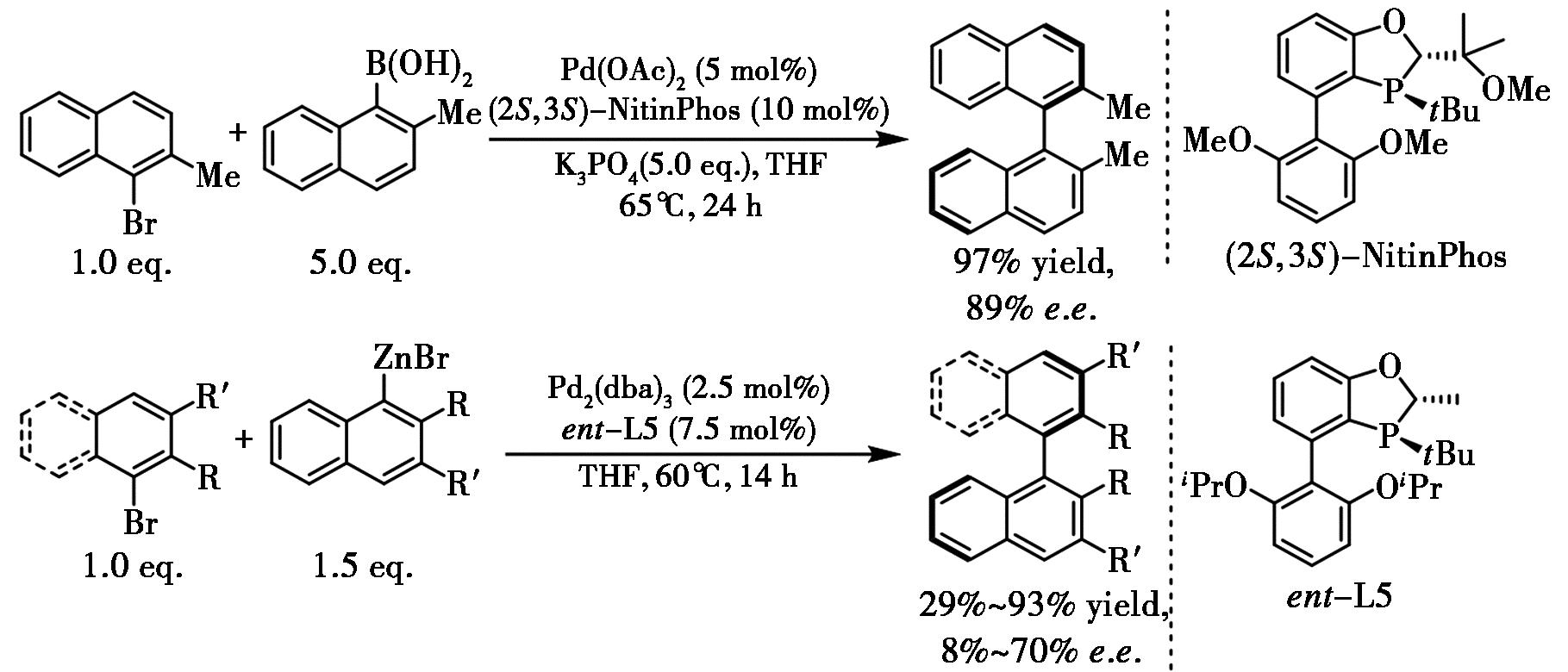
图15 钯-BIDIME催化不对称芳基-芳基交叉偶联[30]
Fig.15 Pd-BIDIME catalyzed asymmetric aryl-aryl cross-coupling[30]
2024年,Dou等[31]首次报道利用钯-AntPhos实现了联芳半硼酸酯的不对称Suzuki-Miyaura交叉偶联反应(图16),该动态动力学阻转选择性偶联反应具有高对映选择性、良好官能团耐受性和宽泛的底物适用范围。初步机理研究表明,反应通过对映体决定性的动态动力学阻转选择性转金属化步骤进行。

图16 钯-AntPhos催化的不对称Suzuki-Miyaura交叉偶联反应[31]
Fig.16 Pd-AntPhos catalyzed asymmetric Suzuki-Miyaura cross-coupling[31]
由于芳基烷基偶联中容易发生β-氢消除的副反应,不对称芳基-烷基Suzuki-Miyaura交叉偶联极具挑战[10]。Fu等[32,33]在镍催化不对称 Suzuki-Miyaura偶联方面取得重要进展。相比之下,钯催化不对称芳基-烷基Suzuki交叉偶联研究仍不充分。Tang等[34]报道了α-溴代羧酰胺与芳基硼酸的高效不对称交叉偶联,以良好收率和优异对映选择性生成系列手性α-芳基羧酰胺(图17)。通过采用具有弱配位的BOPPO手性配体,成功克服了关键的二次转金属化难题。该方法已应用于布洛芬和氟比洛芬的合成,并通过具有弱配位的磷手性配体实现了手性α,α-二芳基羧酰胺的通用合成[35]。
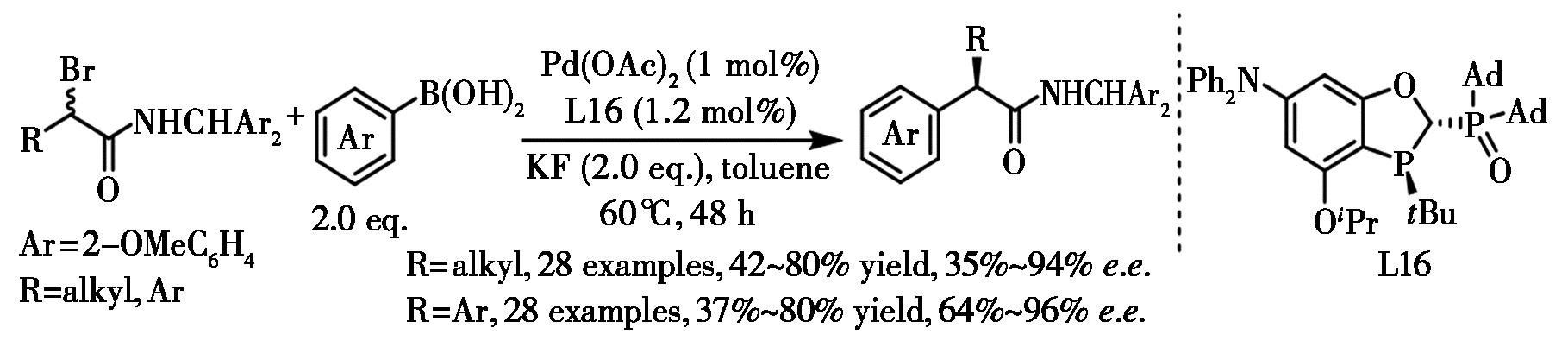
图17 钯-BOPPO催化的不对称芳基-烷基Suzuki-Miyaura交叉偶联[34,35]
Fig.17 Pd-BOPPO catalyzed asymmetric aryl-alkyl Suzuki-Miyaura cross-coupling[34,35]
Heck反应已成为合成化学中最重要的反应之一[36]。Tang等[37]报道了通过钯催化硅基烯酮缩醛的α-杂芳基化反应高效合成α-杂芳基丙酸酯的实用方法(图18a),该反应在大位阻BOPPO配体是实现高效转化的关键。同样,利用BOPPO催化体系,高产率实现了N-杂芳基卤化物与杂环烯烃的Heck反应(图18b)[38]。遗憾的是,当使用手性配体L15时未观察到对映选择性,而 DTBM-SegPhos配体则呈现更好的手性控制。
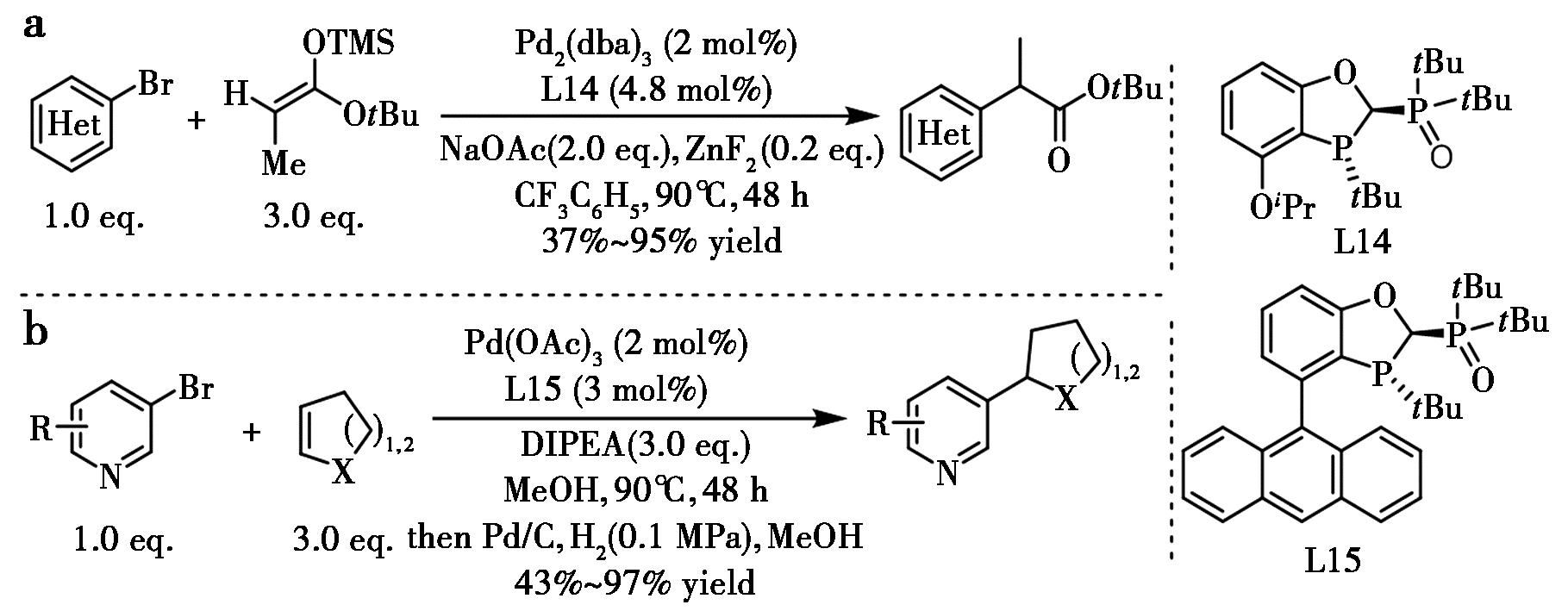
a.文献[37];b.文献[38]
图18 钯催化的Heck类型的偶联反应[37,38]
Fig.18 Pd-catalyzed Heck-type coupling reactions[37,38]
Chen等[39]报道了钯催化环内1-氮杂烯丙基阴离子的α-芳基化反应,以良好收率制备系列顺式-2,3-二芳基哌啶(图19),其不对称偶联采用异丙基取代的BIDIME作为配体,获得中等至良好的收率和对映选择性。机理研究表明环内1-氮杂烯丙基阴离子在碱性条件下原位生成。
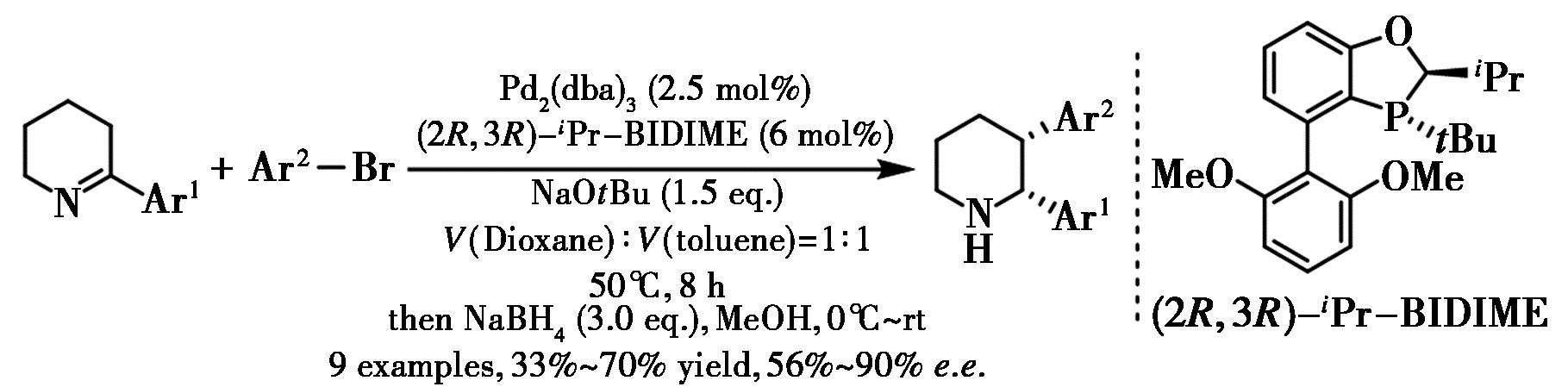
图19 钯催化的Heck类型的偶联反应[39]
Fig.19 Pd-catalyzed Heck-type coupling reactions[39]
通过远程控制去对称化策略引入轴手性是一类具有挑战的课题。2024年,Tan等[40]报道了钯催化具有双取代基的蒽环外双键进行对映选择性Heck芳基化反应,成功构建了结构多样化的蒽亚甲基骨架化合物(图20),并实现从中等到良好的对映选择性控制。
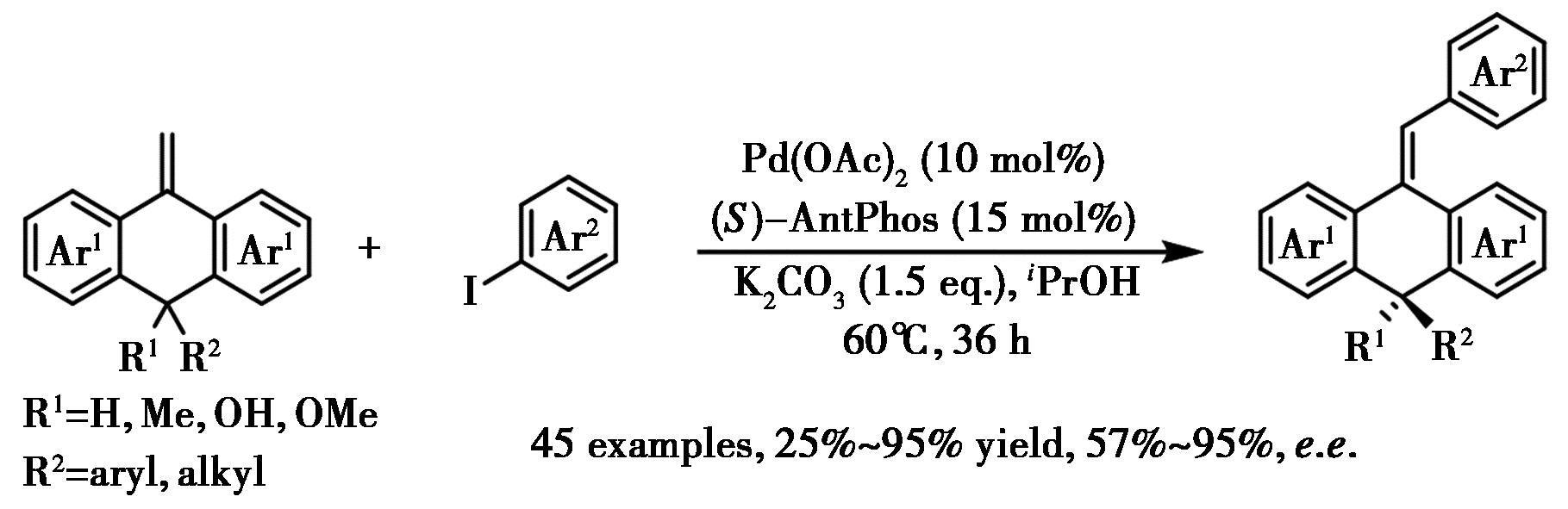
图20 钯-AntPhos催化的不对称Heck反应[40]
Fig.20 Pd-AntPhos catalyzed asymmetric Heck reaction[40]
脂肪族张力环因其优异的理化性质和药代动力学特性,在药物化学中的应用日益广泛。实现具有多样结构模式的对映体富集环丁烷衍生物的合成仍是一个重大挑战。陆平和王敏燕等报道了钯催化的环丁烯对映选择性去对称化反应,发生类似还原Heck类型的偶联反应,成功获得了一系列氢芳基化及1,2-与1,3-双芳基化产物(图21)[41]。该方法的合成实用性在贝拉哌酮骨架和曲辛酸类衍生物的合成中得到验证。
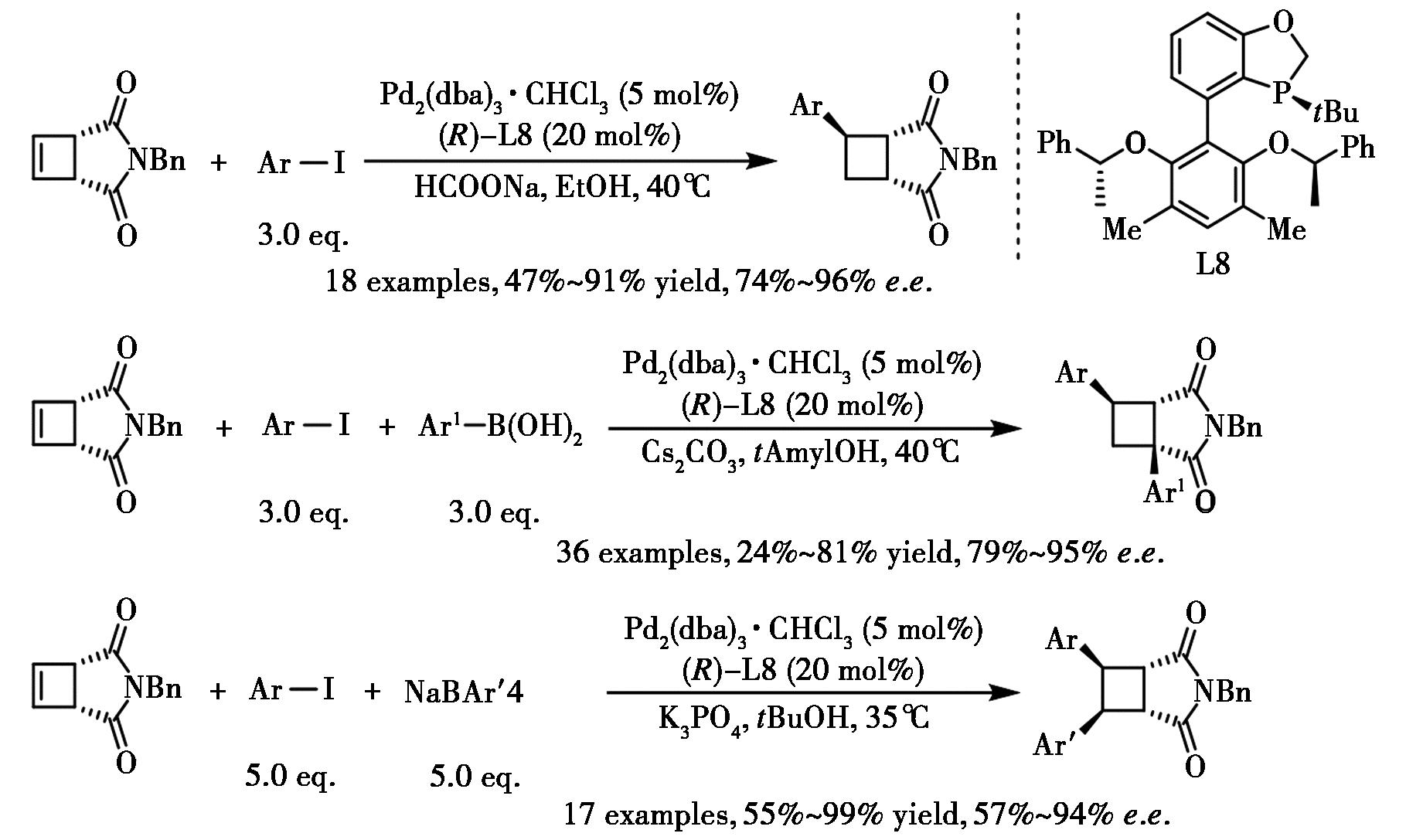
图21 钯催化的不对称还原Heck反应[41]
Fig.21 Pd catalyzed asymmetric reductive Heck reaction[41]
构建具有较低稳定性的轴手性烯烃具有重大挑战。通过对催化体系的理性设计,Lin等[42]报道了钯催化芳基卤化物与炔烃的不对称烯化反应,以高产率高选择性实现了轴手性的构建(图22)。对于1,6-二炔底物,发生还原Heck反应,而对于1-炔基环丁醇底物,发生环张力驱动的碳碳键偶联/烯化反应。在这两种偶联体系中,反应均展现出高效的区域选择性、Z/E选择性和优异对映选择性。
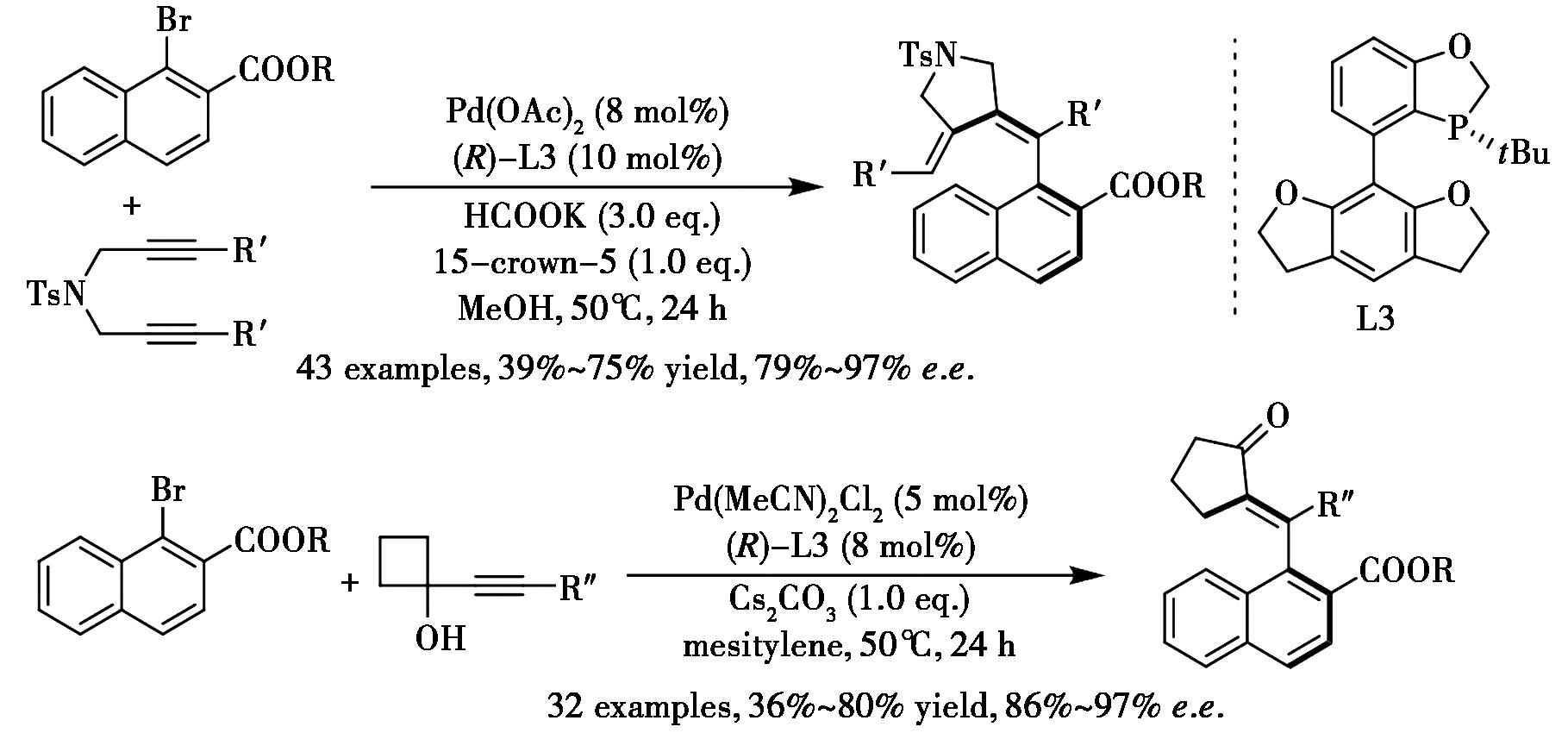
图22 钯催化的不对称还原Heck反应合成轴手性二烯化合物[42]
Fig.22 Pd-catalyzed asymmetric reductive Heck reaction for the synthesis of axially dienes[42]
钯催化不对称α-芳基化是构建含全碳季位手性中心分子骨架的有效方法[43],该类结构广泛存在于天然产物和治疗药物中。Senanayake等[44]报道了采用钯-BIDIME催化体系实现吲哚酮的3-芳基化反应(图23),收率优异。通过使用改进型BIDIME配体,该不对称芳基化反应实现了86%的对映选择性。
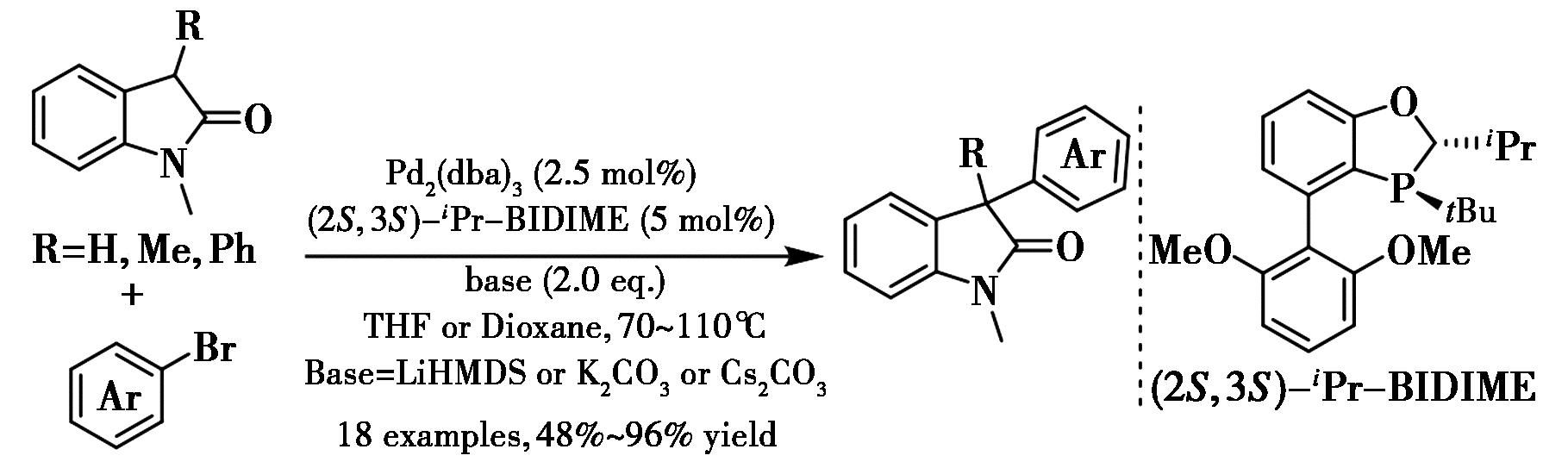
图23 钯-BIDIME催化吲哚酮α位的不对称芳基化[44]
Fig.23 Pd-BIDIME catalyzed enantioselective α-arylation of oxindoles[44]
Tang等[45]开发了2-取代环酮的高效空间位阻不对称芳基化反应(图24a),在Pd-BIDIME催化剂作用下获得优异收率和对映选择性,该方法学已成功应用于多种天然产物的简洁合成。随后Tang等[46]又报道了钯-BIDIDME催化分子内α-芳基化反应以高收率与优异对映选择性实现手性[4.4]、[4.5]和[4.6]-螺环的构建(图24b)。研究观察到显著的水效应,推测水的加入可与底物羰基形成氢键作用。2025年,Tang等[47]又设计合成了更大位阻的3-Pent-BIDIME磷手性单膦配体,实现了钯催化α,α-二取代酯与芳基溴化物的对映选择性α-芳基化反应,以中等至良好收率及高对映选择性合成了一系列具有季碳手性中心的对映体富集α,α-二芳基酯(图24c)。该方法底物适用范围广、反应条件温和官能团兼容性优。理论计算揭示了非共价相互作用在控制对映选择性中的关键作用。
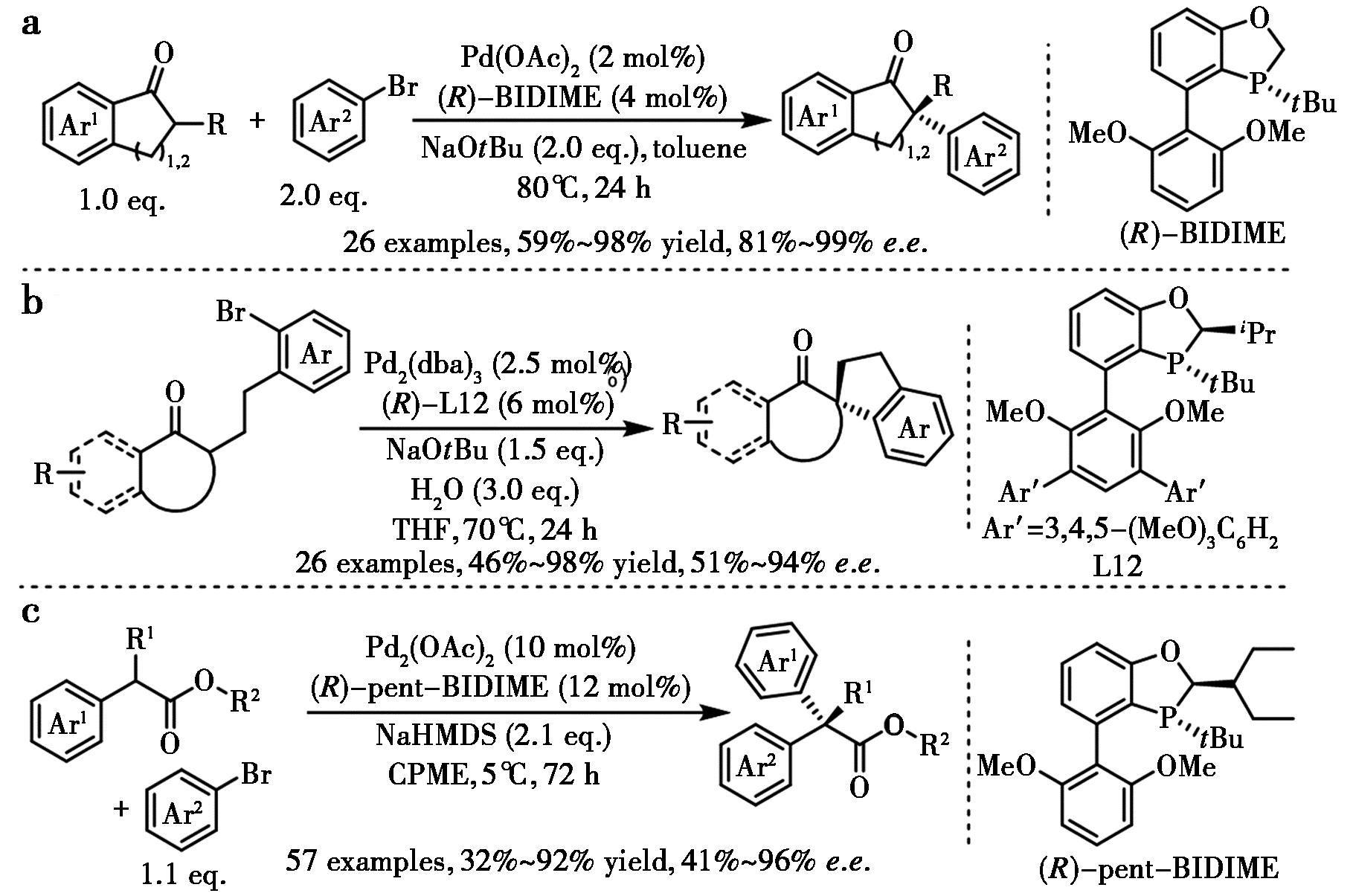
a.文献[45];b.文献[46];c.文献[47]
图24 钯-BIDIME催化环状酮或酯α位碳氢键的不对称芳基化[45-47]
Fig.24 Pd-BIDIME catalyzed enantioselective α-arylation of cyclic ketones or esters[45-47]
2022年,Zhang等[48]报道了Pd-AntPhos催化的β,γ-不饱和丁烯内酯的高效对映选择性γ-芳基化反应(图25),该方法可获得系列γ-丁烯内酯和γ-丁内酯骨架,具有高γ-选择性、良好官能团耐受性和优异对映选择性。通过该方法实现(R)-boivinianin A的简洁合成验证了其实用性。
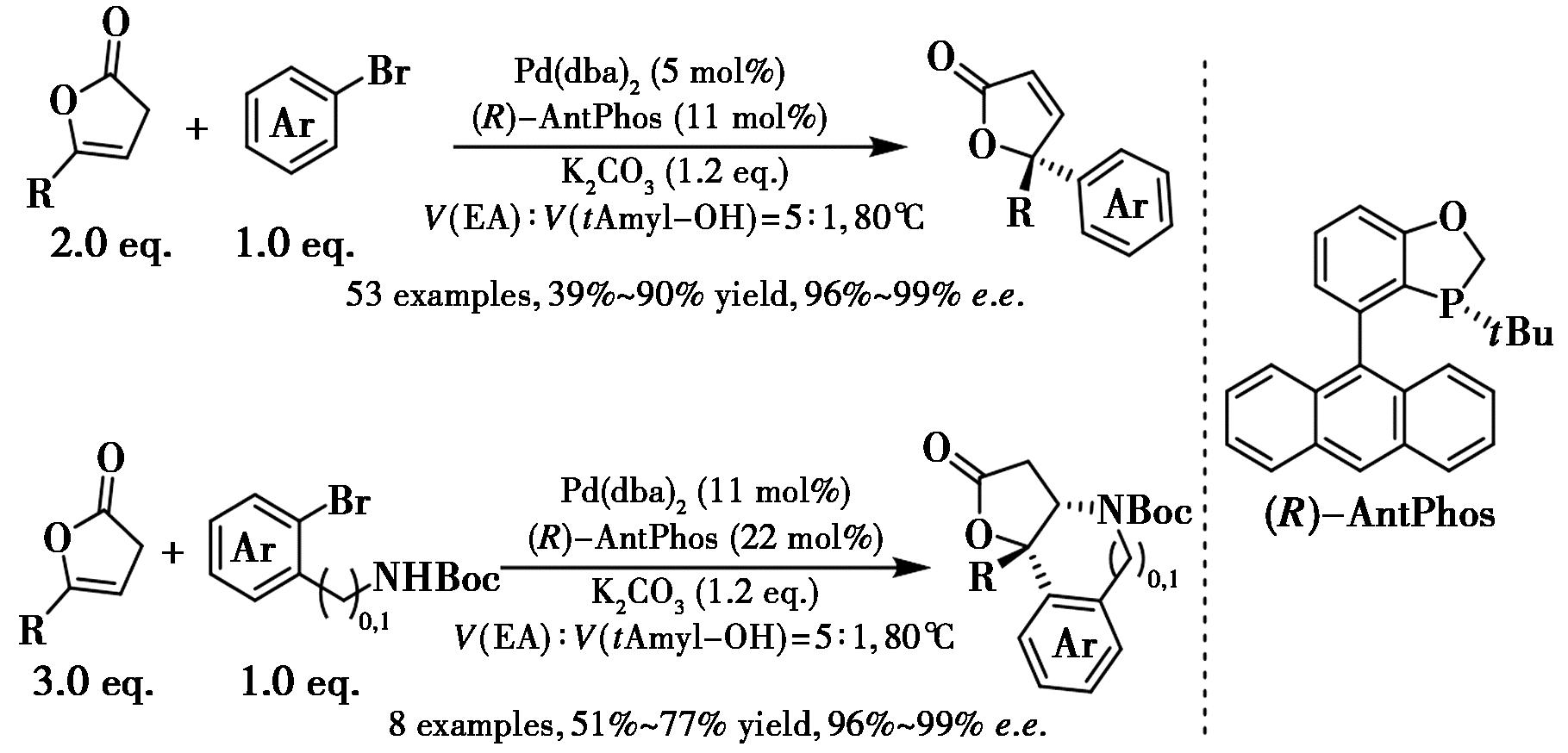
图25 钯-AntPhos催化环状内酯γ位碳氢键的不对称芳基化[48]
Fig.25 Pd-AntPhos catalyzed enantioselective γ-arylation of cyclic lactones[48]
碳氢键活化是一种原子经济性的高效的构建碳碳键的方法,通过不对称碳氢键活化构建杂原子手性中心是更具挑战的课题。2015年,Tang等[49]发展了钯催化立体选择性分子内环化反应,成功从二芳基-2-溴代芳基膦酸酯高效合成系列磷手性联芳基膦酸酯(图26),收率最高达92%,对映选择性高达88% e.e.。该方法为获取多种磷手性联芳基单膦化合物提供了便捷途径。
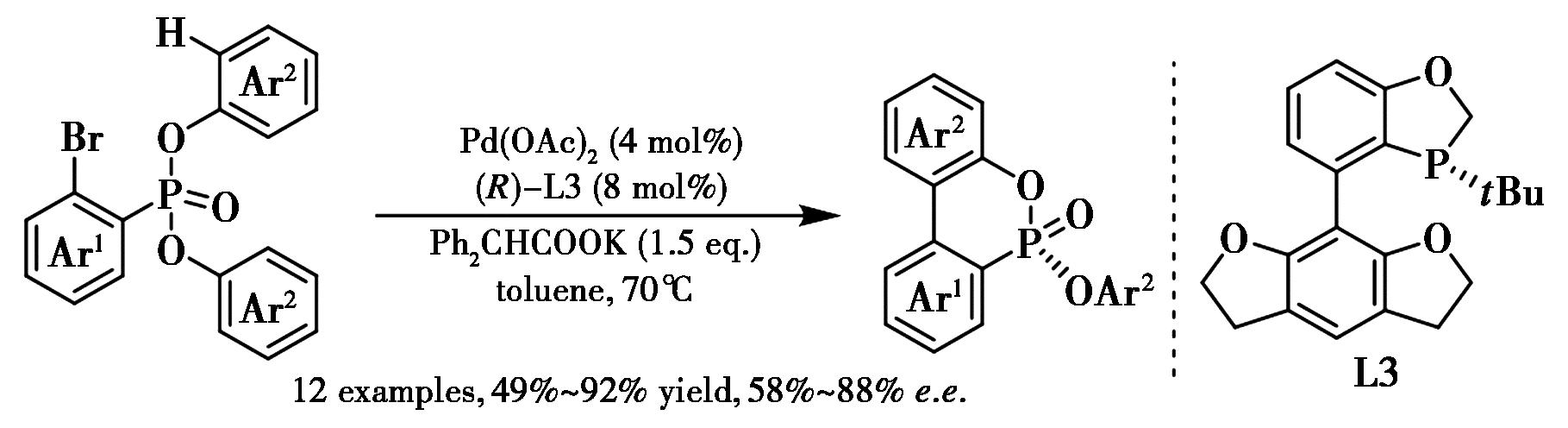
图26 钯催化的分子内碳氢键不对称芳基化构建手性膦酸酯[49]
Fig.26 Pd-catalyzed intramolecular asymmetric C—H arylation for construction of chiral phosphonates[49]
不对称碳氢键活化在杂原子掺杂多环芳烃的合成中也展现了其实用性。2025年,Jiang等[50]利用钯-BIBOP催化体系实现了二芳基硫氧亚胺与磺酰二亚胺的对映选择性去对称化反应,以高产率和高对映选择性制备出手性硫(Ⅵ)掺杂杂环化合物(图27)。值得注意的是,添加剂甲氰菊酸(TMCPA)对产物对映选择性的影响显著,底物为分离式芳环和稠合芳环时,呈现相反的对映选择性。

图27 钯-BIBOP催化的分子内碳氢键不对称芳基化构建手性亚砜亚胺[50]
Fig.27 Pd-BIBOP catalyzed intramolecular asymmetric C—H arylation for construction of chiral sulfoximines[50]
利用不对称碳氢键芳基化,也能方便实现面手性和笼手性的构建。Xie等[51]报道了通过Pd-BIDIME催化的分子内硼氢键不对称芳基化反应(图28a),高对映选择性和区域选择性地合成光学活性碳硼烷,为构建笼手性化合物提供新途径。Liu等[52]发表了钯催化二茂铁碳氢键的不对称芳基化反应(图28b),以高收率和高对映选择性生成多种平面手性异喹啉酮并二茂铁,该类化合物在配体开发中具有重要价值。
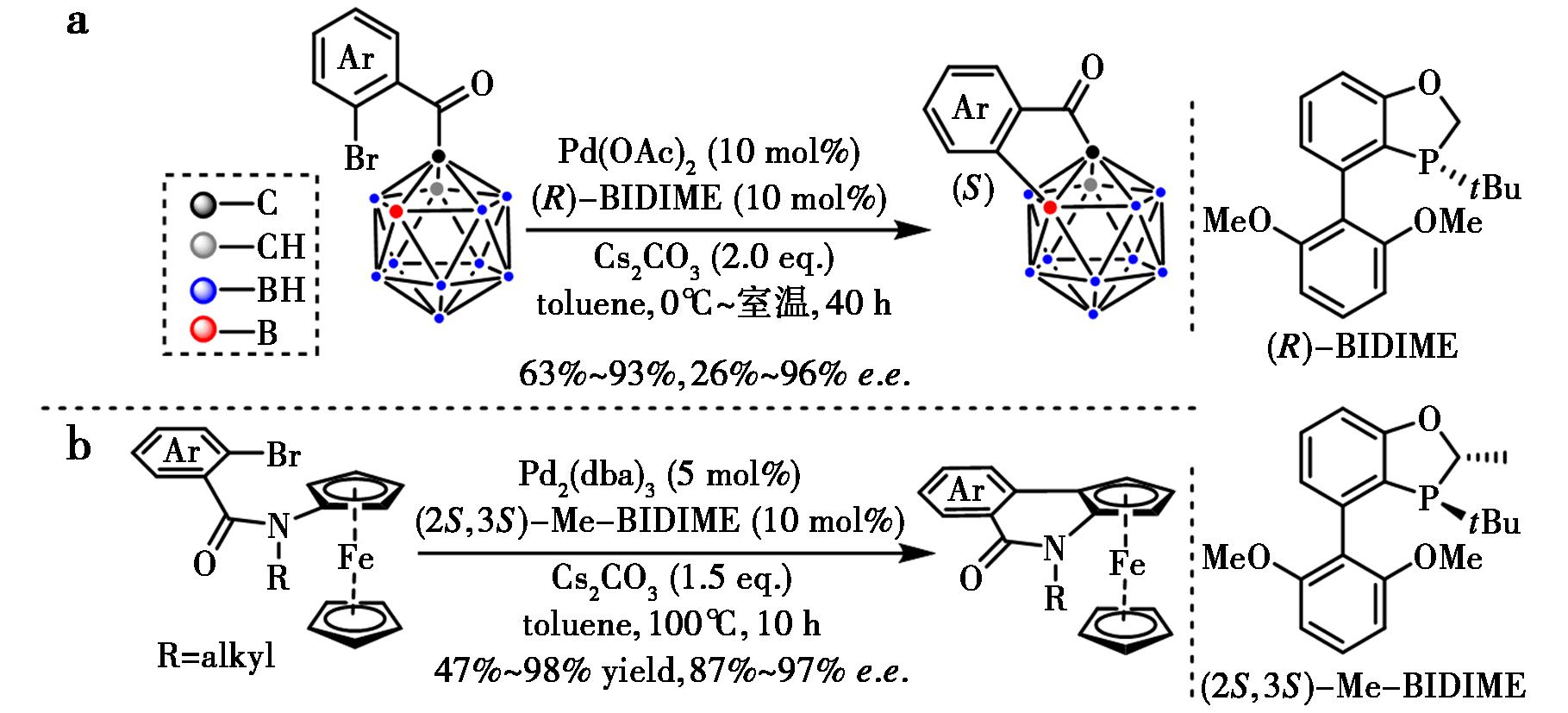
a.文献[51];b.文献[52]
图28 钯-BIDIME催化的分子内硼氢键和碳氢键的不对称芳基化[51,52]Fig.28 Pd-BIDIME catalyzed asymmetric B—H or C—H arylation[51,52]
分子间的对映选择性碳氢键官能团化是构建手性骨架最高效的方法,但也极具挑战[53,54]。Tang等[55]报道了钯-AntPhos催化体系可实现咪唑或三氮唑碳氢键的不对称芳基化反应(图29),在温和反应条件下以优异对映选择性和良好收率制备多种杂联芳烃。值得关注的是,为提高对映选择性控制,该研究采用了氘代CD3-AntPhos配体,推测配体和底物之间存在关键的C—H/π作用。
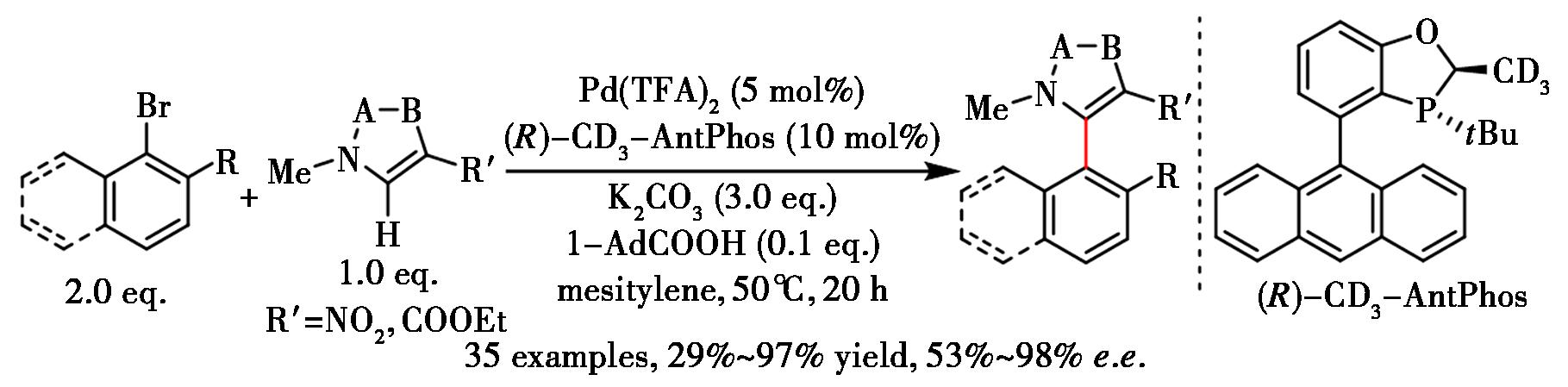
图29 钯-AntPhos催化的分子间的碳氢键不对称芳基化[55]
Fig.29 Pd-AntPhos intermolecular enantioselective C—H arylation[55]
2010年,Fandrick等[56]报道了使用MeO-BIBOP作为配体,铜催化醛与丙炔基硼烷试剂的高效不对称丙炔基化,以优异收率和对映选择性(90%~99% e.e.)提供了一系列手性高炔丙醇(图30)。该方法显示出广泛的底物范围,包括芳基、杂芳基、烯基和烷基醛。Trost及其合作者进一步将该方法应用于bryostatin 3的全合成,对烯醛进行丙炔基化,收率和对映选择性优异(86%,98% e.e.)[57]。
图30 铜-BIBOP催化醛类化合物的不对称炔丙基化[56,57]
Fig.30 Cu-BIBOP catalyzed asymmetric propargylation of aldehydes[56,57]
2013年,Tang等[58]合成了BIDIME配体的变体,并实现了钌催化芳基硼酸与芳醛的不对称加成,以优异收率和对映选择性(高达92% e.e.)得到了一系列手性二芳基甲醇(图31a)。机理涉及芳基硼酸的转金属化,随后羰基插入和转金属化再生活性Ru配合物。2022年,Luo等[59]使用 BIDIME作为配体,以高收率和对映选择性实现了钌催化芳基硼酸对烷基醛的不对称加成(图31b)。该反应底物适用范围广,合成了系列芳基烷基手性醇。
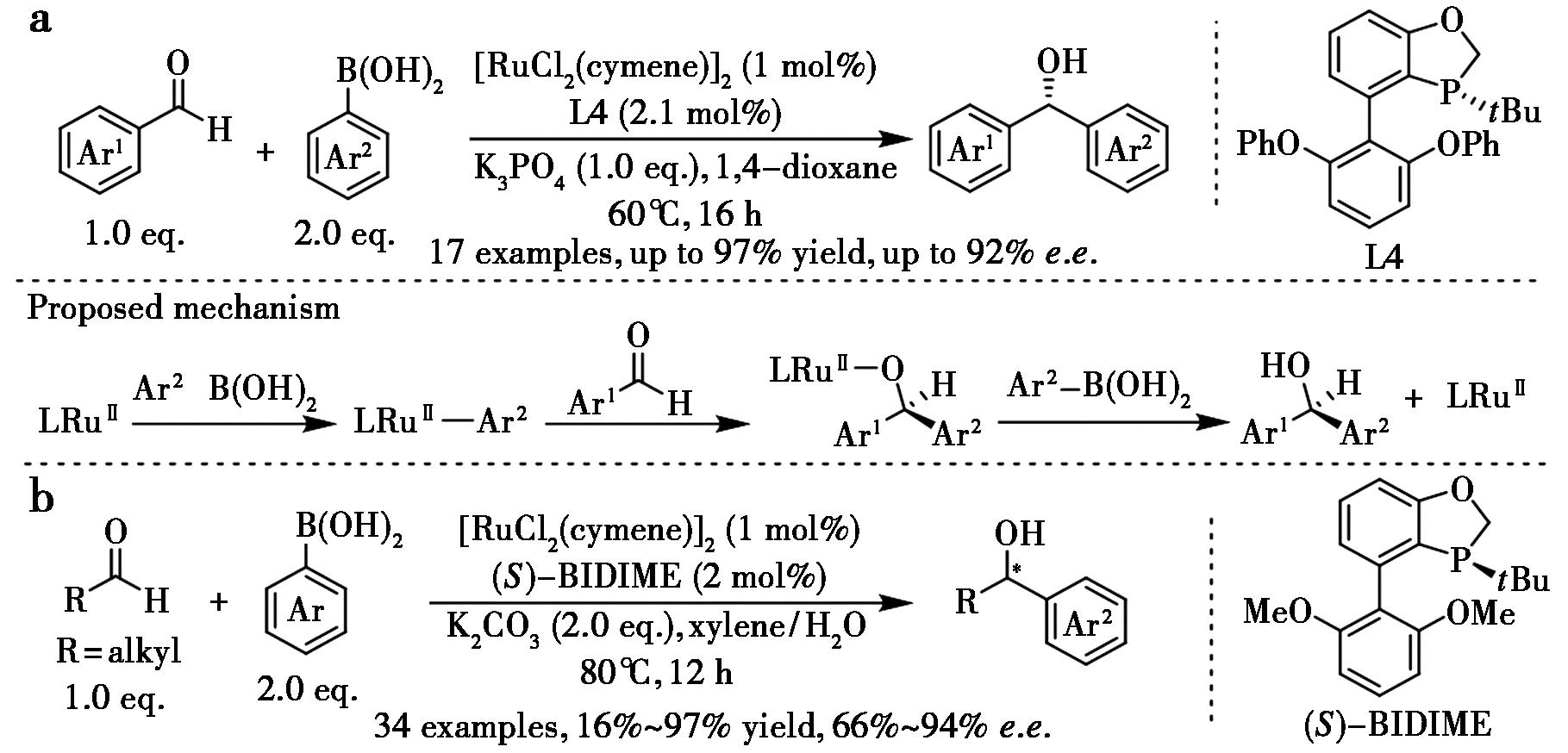
a.文献[58];b.文献[59]
图31 钌-BIDIME催化芳基硼酸对芳基醛的不对称加成[58,59]
Fig.31 Ru-BIDIME catalyzed asymmetric addition of arylboronic acids to aryl aldehydes[58,59]
2013年,Tang等[60]报道了铑催化芳基硼酸与三氟甲基酮的亲核加成,使用DI-BIDIME作为配体,以高收率(高达93%)和优异对映选择性(高达99%)形成了一系列手性三氟甲基取代叔醇(图32a)。其机理与钌催化芳基硼酸与芳醛的不对称加成过程类似[58]。随后,Tang等[61]采用Rh-WingPhos催化剂首次实现了芳基硼氧烷与简单芳酮的高对映选择性加成反应,以优异对映选择性和收率合成了一系列手性二芳基烷基甲醇(图32b)。WingPhos配体被证明对实现高反应活性和对映选择性起决定性作用。该方法为抗抑郁药物艾司西酞普兰提供了一种全新、简洁且对映选择性的合成路线。最近,Zhu等[62]报道了一种高对映选择性的铑催化芳基硼酸与N-杂芳基酮的加成,使用WingPhos作为配体,以优异的收率和对映选择性便捷地获得一系列手性苯并噁唑基取代叔醇(图32c)。该温和反应具有广泛的官能团兼容性,铑负载量低至0.3 mol%,使用WingPhos对于对映选择性和反应活性都至关重要。
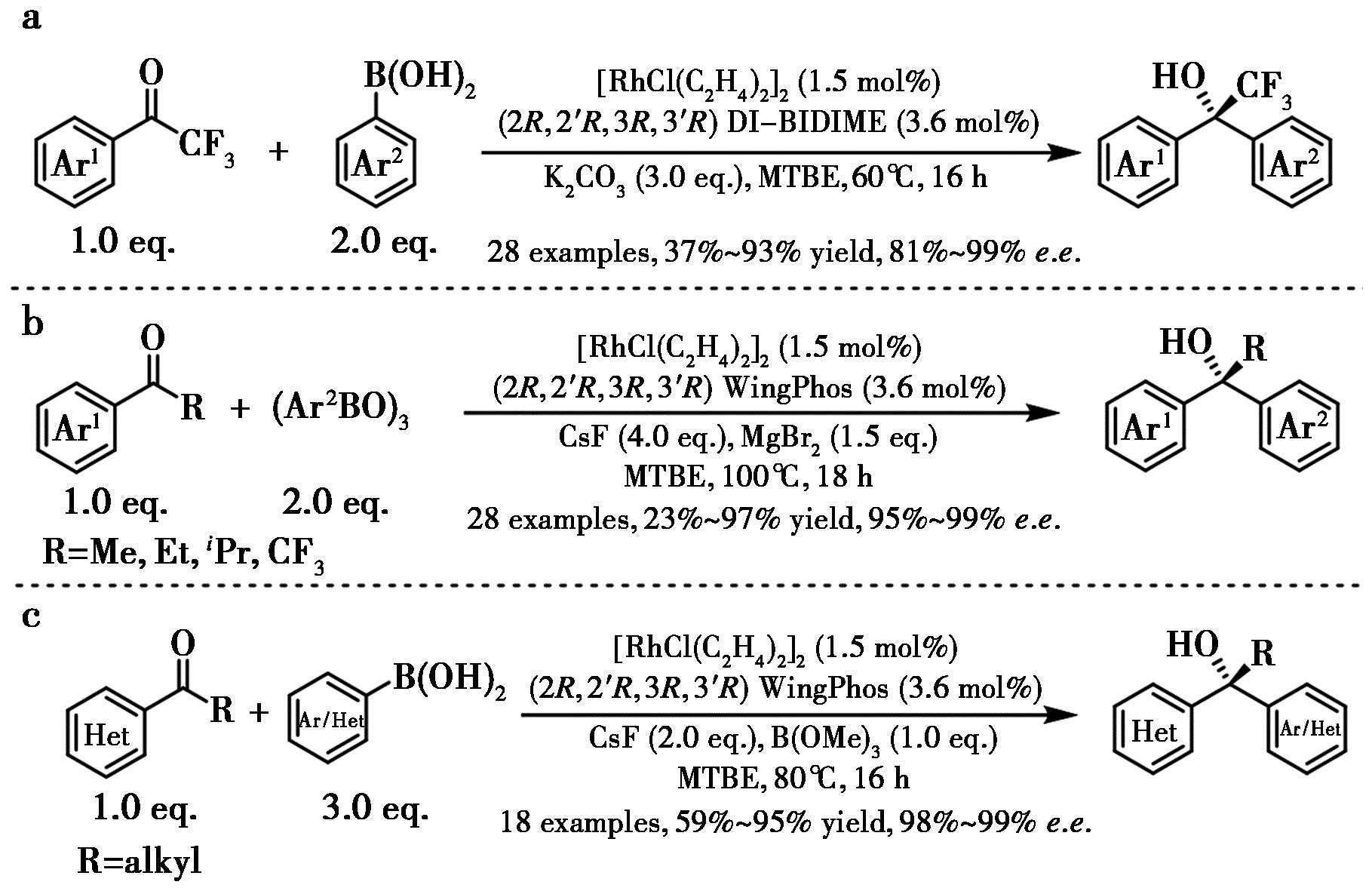
a.文献[60];b.文献[61];c.文献[62]
图32 铑催化芳基或杂芳基硼酸对芳基酮或杂芳基酮的不对称加成[60-62]
Fig.32 Rh-BIBOP catalyzed asymmetric addition of arylboronic acids to aryl ketones[60-62]
2014年,Sieber等[63]开发了一种新型的p,π-二氢苯并氧杂膦烷杂化配体,并应用于铑催化芳基硼酸与亚胺亲电试剂的不对称加成,以优异的对映选择性合成多种手性叔胺(图33)。推测机理可能涉及形成Rh-p,π二聚体配合物,这与碱性条件下的XRD结构一致。立体化学模型表明是Si面进攻生成所需产物。
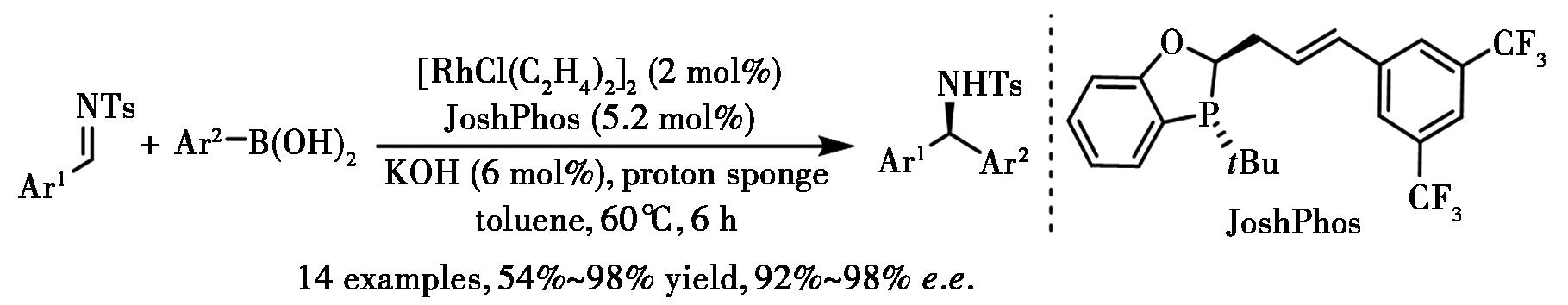
图33 铑催化芳基硼酸对醛亚胺类化合物的不对称加成[63]
Fig.33 Rh-catalyzed asymmetric addition of arylboronic acids to imines[63]
2019年,Tang等[64]报道了使用WingPhos或PFBO-BIBOP作为配体,铑催化芳基硼氧烷与N-无保护酮亚胺的高对映选择性加成,以优异e.e.值和收率得到一系列手性α-三氟甲基 α,α-二芳基α-叔胺或3-氨基-3-芳基氧化吲哚(图34)。该方法能够实现高效对映选择性合成西帕格雷明。

图34 铑催化芳基硼酸酯对无保护酮亚胺类化合物的不对称加成[64]
Fig.34 Rh-BIBOP catalyzed asymmetric addition of arylboroxines to unprotected ketimines[64]
二烯羧酸作为不常见的亲核试剂和阴离子替代物,Chen等[65]报道了钯催化(E,E)-2,4-二烯酸与亚胺的Friedel-Crafts类型的加成反应,以优异收率和对映选择性及专属的α-区域选择性得到形式上的二烯化加合物(图35)。该反应底物范围广,收率和对映选择性优异。有趣的是,通过配体控制(使用BIDIME得到Z选择性,使用MeO-BIBOP得到E选择性),可以非对映发散性地很好地制备可切换的(E,E)-和(Z,E)-构型产物,并具有高对映选择性。使用单膦P-手性配体L9与双膦配体MeO-BIBOP得到相同的Z选择性二烯化产物,表明配体控制的形式二烯化反应可能涉及不同的机理。提出了一个合理的机理,涉及与二烯酸形成η2-配合物,随后亚胺插入和脱羧生成产物并再生催化剂,同时提出了双膦配体的外球模式和单膦配体的内球模式用于亚胺插入步骤。
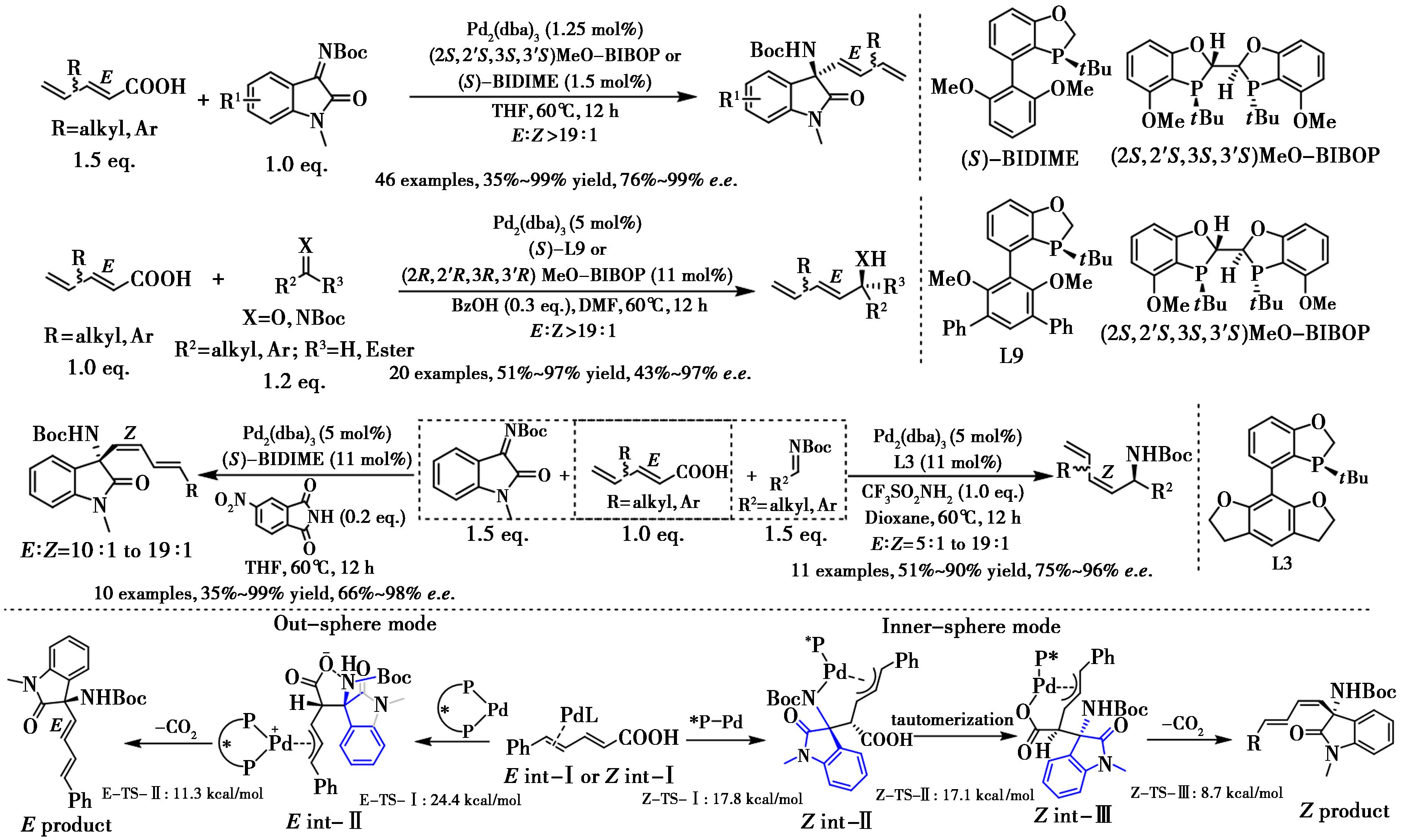
图35 钯催化酮亚胺立体选择性脱羧双烯化反应[65]
Fig.35 Pd-catalyzed stereoselective decarboxylative dienylation of imines[65]
过渡金属催化的不饱和碳碳键的不对称氢官能团化近几十年来备受关注并取得重大进展[66-69]。其中过渡金属催化的不对称氢硼化已成为合成手性有机硼酸酯的有效方法。Tang等[70]报道了铑催化的α-芳基烯酰胺的不对称氢硼化,使用BIDIME作为手性配体,以良好收率和优异对映选择性形成了一系列α-氨基叔硼酸酯(图36)。引入作为导向基团的酰胺基团对于反应活性和对映选择性都至关重要。
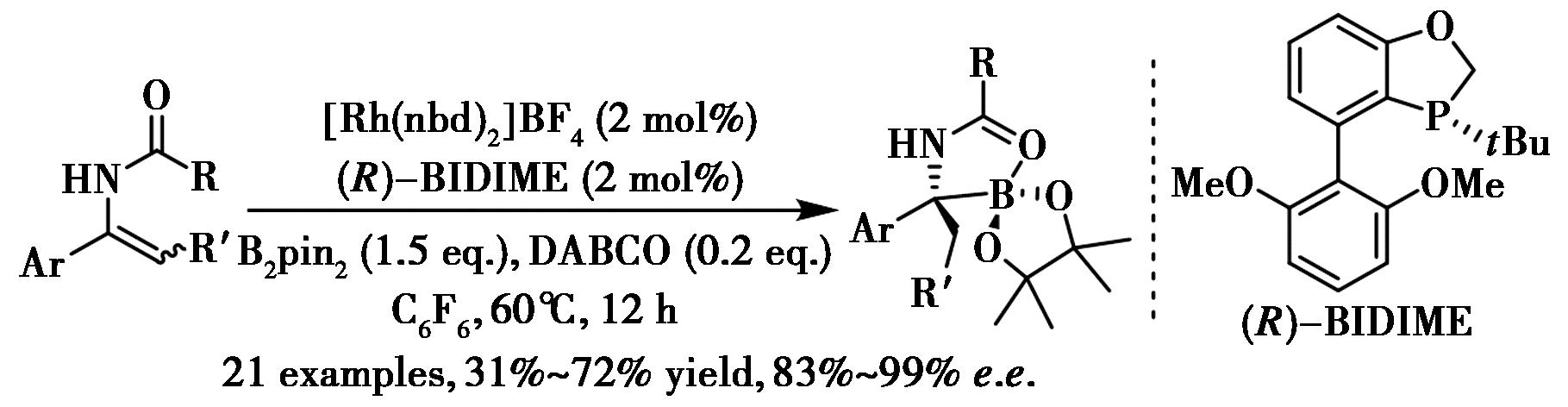
图36 铑-BIDIME催化烯酰胺的硼氢化反应[70]
Fig.36 Rh-BIDIME catalyzed enantioselective hydroboration of enamides[70]
随后,Ding等[71]报道了使用钯-BIDIME催化体系成功实现的1,1-二取代联烯的对映选择性双硼化反应,以高收率和高选择性得到了多种手性双硼酸酯(图37a)。DFT计算支持了联硼酸频哪醇酯氧化加成和丙二烯插入的协同机理。通过brasinazole的简洁合成验证了其实用性。除了贵金属催化的不对称氢硼化,使用含氮手性配体的非贵金属催化剂(包括Cu、Fe、Co)催化的不对称氢硼化也取得了显著进展[72]。Rajanbabu等[73]报道了钴催化的1,3-二烯的区域和对映选择性氢硼化,使用MeO-BIBOP作为手性配体,以优异收率和对映选择性(高达96% e.e.,>98∶2 dr)提供多种烯丙基仲硼酸酯类化合物(图37b)。高对映选择性控制推测是得益于钴和MeO-BIBOP配体之间相对较小的咬合角。DFT计算表明,非对映异构二烯结合复合物的相对稳定性导致了初始的非对映面选择性,这种选择性在后续步骤中得到进一步保持,从而产生了优异的e.e.值。手性氟化环丁烷衍生物的多样化合成一直是合成化学中的难题。近来,Xia等[74]开发了铑催化偕二氟环丁烯的不对称氢硼化反应,以优异的区域选择性和对映选择性制备出手性偕二氟α-硼基环丁烷(图37c)。反应成功关键在于采用铑-BIDIME类型的催化剂,使用BINAP等其他类型的配体几乎没有反应活性。另外,通过在钯和碱存在情况下,可生成脱氟环丁烯产物。
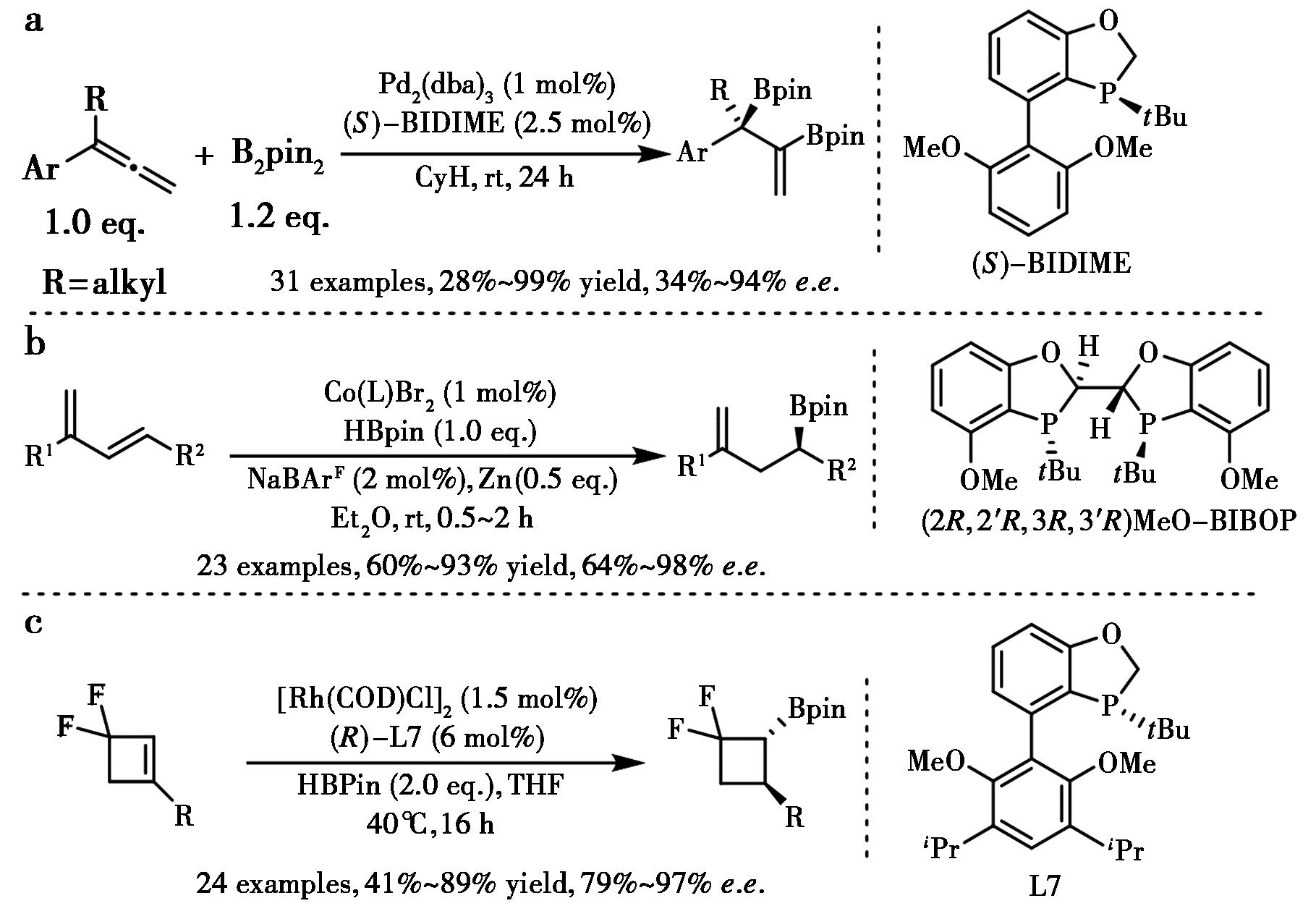
a.文献[71];b.文献[73];c.文献[74]
图37 过渡金属催化的不饱和碳碳键的硼氢化反应[71,73,74]
Fig.37 Transition metal catalyzed asymmetric hydroboration of unsaturated C—C bond[71,73,74]
与导向基团辅助的氢硼化不同,Zhao等[75]设计合成了取代的BIDIME配体,对烯醇硅醚进行对映选择性铑催化氢硼化(图38a)。该方法底物范围广,以优异收率和对映选择性提供了一系列具有合成价值的硼醚。值得注意的是,配体芳环的3位3,5-二甲氧基苯基取代基具有合适的空间位阻,对于实现高对映选择性至关重要。类似的,不对称芳基化[46]和不对称Suzuki-Miyaura交叉偶联[26]案例中也存在显著间位取代效应。通过该方法实现了抑制剂索利氨醇的简洁合成。令人意外的是,当采用端烯的烯醇硅醚底物时,双膦配体展现出优异的对映选择性控制(图38b)[76]。
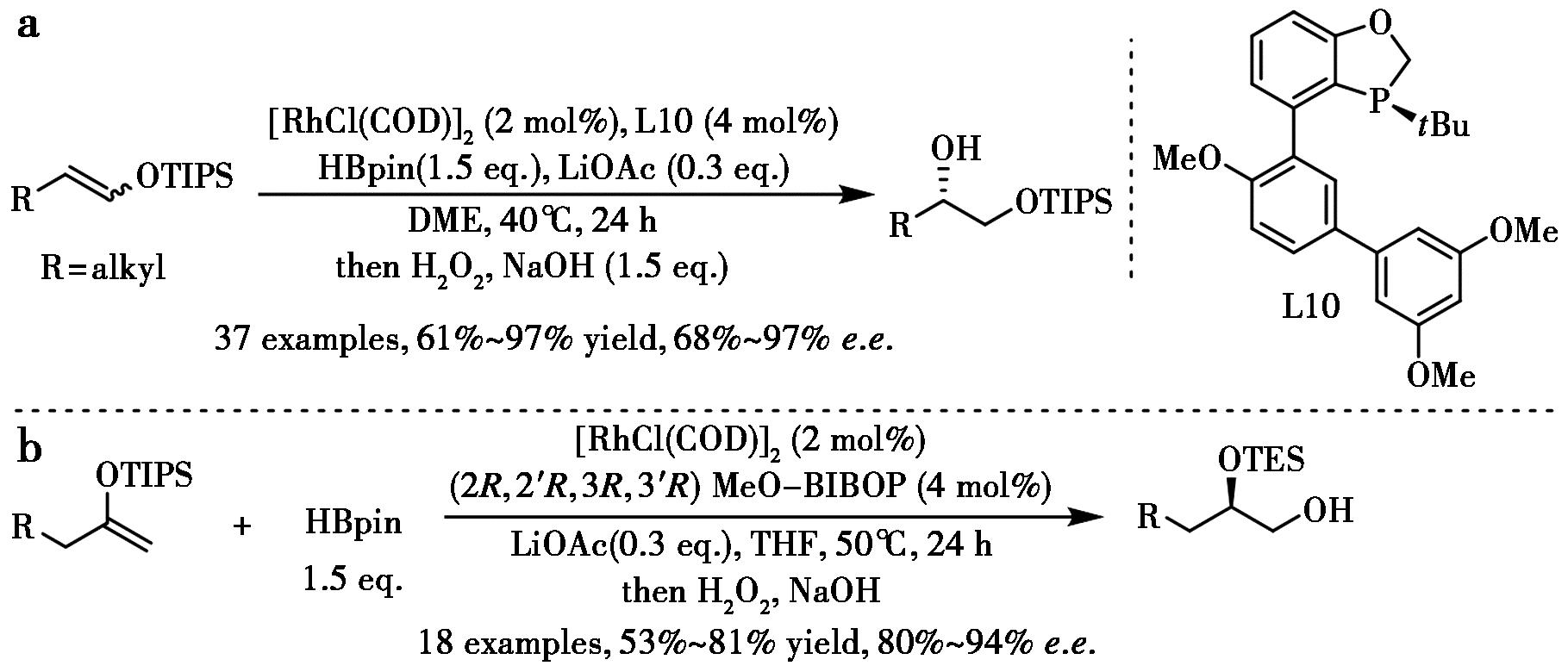
a.文献[75];b.文献[76]
图38 铑催化烯醇硅醚的不对称硼氢化反应[75,76]
Fig.38 Rh-BIDIME catalyzed enantioselective hydroboration of silyl enol ethers[75,76]
受镍氧化环金属化生成镍环的启发,Shi等[77]开发了镍催化的易得N-磺酰胺与炔烃的对映选择性α-烯基化,使用改进的BIDIME配体,以优异收率和对映选择性获得了多种手性α-支链胺(图39a)。手性α-支链胺的可进一步转化合成α-氨基酸酰胺和β-氨基醇。使用类似策略,该团队还使用BIDIME作为配体,实现了镍催化的烯烃与易得N-磺酰胺的氢烷基化(图39b)[78]。该方法底物范围广,可构建一系列手性α-支链胺,收率和对映选择性优异。
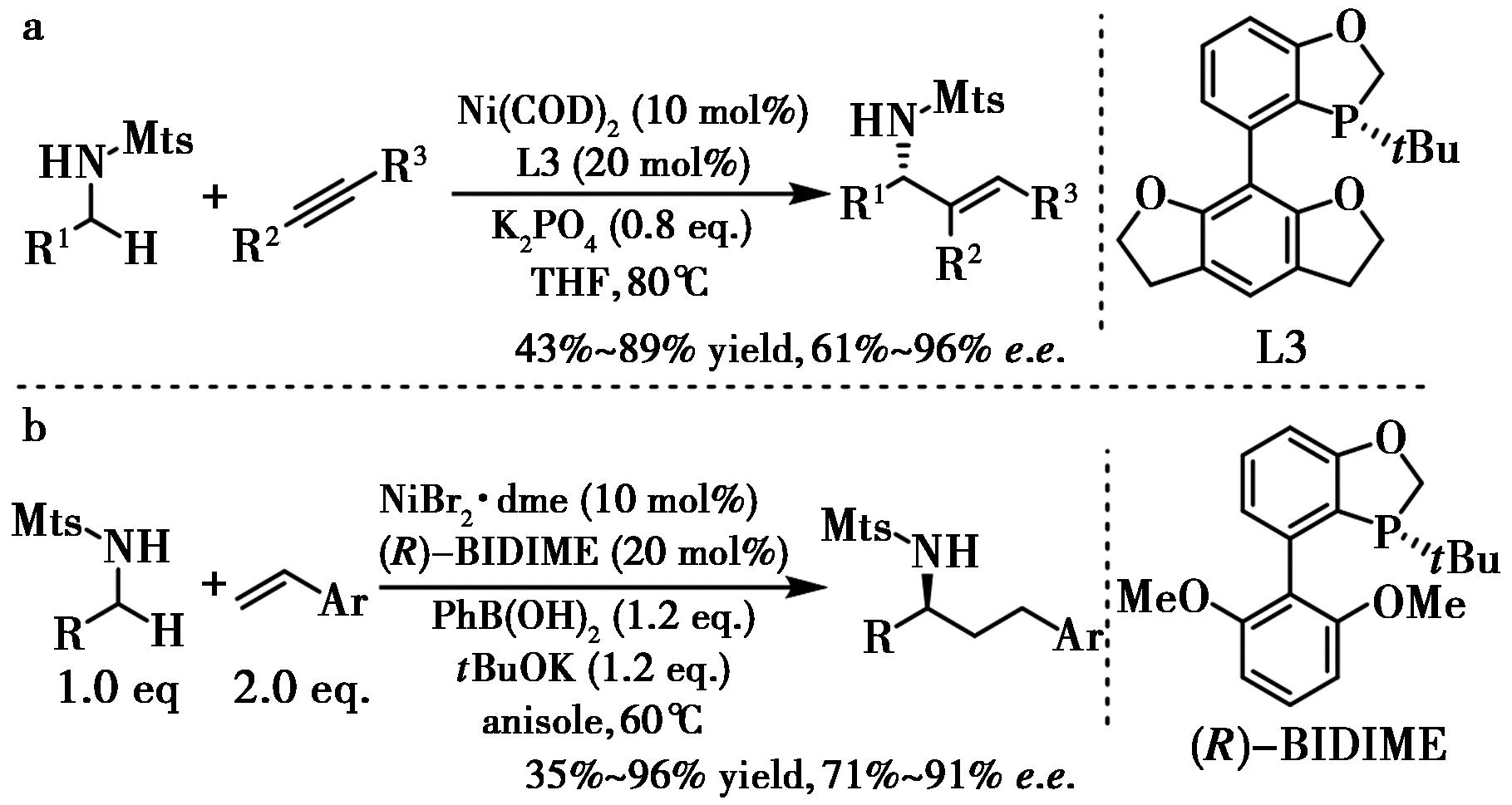
a.文献[77];b.文献[78]
图39 镍催化不饱和碳碳键的不对称氢胺化[77,78]
Fig.39 Ni-BIDIME catalyzed enantioselective hydroamination of unsaturated C—C bond[77,78]
催化不对称环化是构建复杂多环骨架的强大工具[79,80]。磷手性二氢苯并氧杂膦烷配体被证明对多种类型的催化不对称环化反应非常有效,为天然产物合成提供了高效的合成方法。
2015年,Tang等[81]开发了一种对映选择性钯催化带有取代酚部分的芳基卤化物的脱芳构环化,以优异对映选择性和中等至良好收率提供了一系列带有全碳季碳中心的手性菲酮衍生物(图40)。该方法能够以优异的对映选择性(高达99% e.e.)和产率实现系列含杂芳基或七元环的多环产物。提出的立体化学模型显示,配体L2的吡咯环上的苯基基团与配体磷中心的叔丁基的大位阻是高对映选择性关键。该方法在萜烯和甾体合成中的有效性通过高效合成贝壳杉烯(Kaurene)中间体、轻松构建合成代谢类固醇勃地酮(Boldenone)的骨架以及对抗菌二萜(-)-totaradiol的对映选择性全合成得到证明。本课题组随后通过钯催化脱芳构化策略完成了triptoquinone H及其差向异构体的合成[82]。
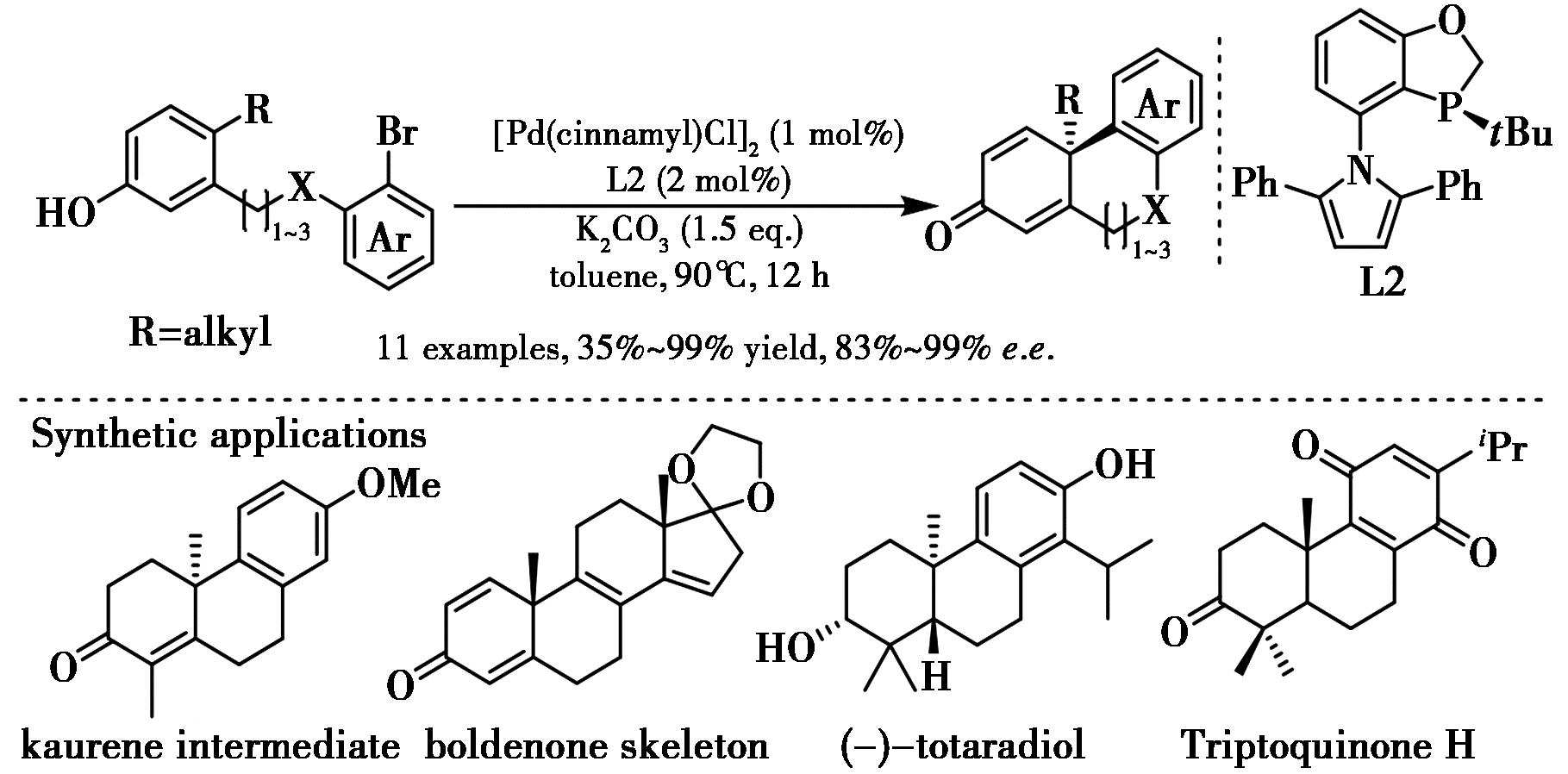
图40 钯催化不对称去芳构环化用于合成手性萜烯和甾体分子[81,82]
Fig.40 Pd-catalyzed enantioselective dearomative cyclization for the synthesis of terpenes and steroids[81,82]
利用相似的策略,Tang等[83]报道了钯-AntPhos催化的分子内不对称去芳构环化反应(图41),并成功实现高氧化强心甾体19-hydroxysarmentagenin和Ouabagenin的全合成。
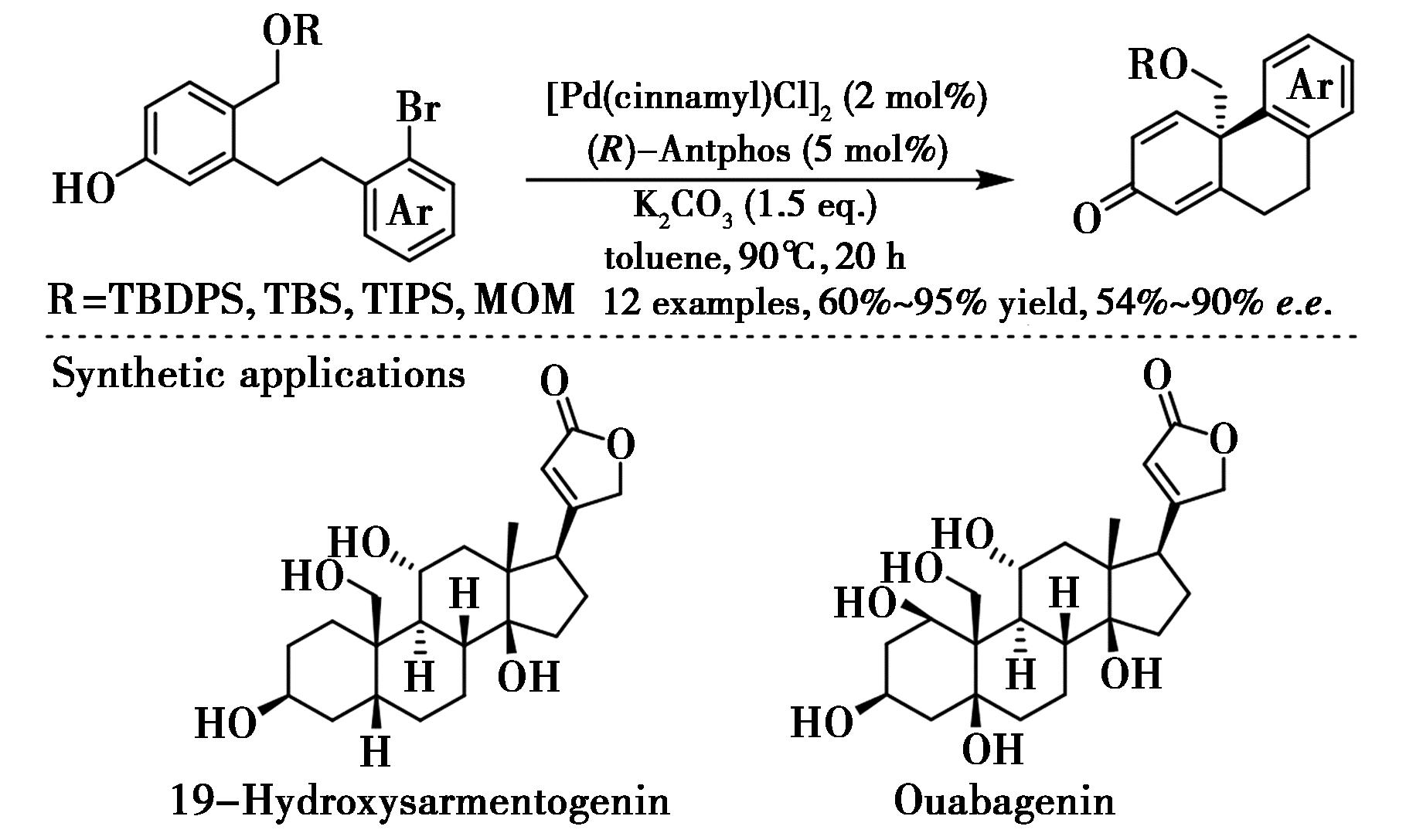
图41 钯催化不对称去芳构环化用于合成甾体分子[83]
Fig.41 Pd-catalyzed enantioselective dearomative cyclization for the synthesis of steroids[83]
为了解决具有挑战性的多环生物碱的合成,Tang等[84]开发了一种高效的钯催化对映选择性脱芳构环化方法,能够合成含氮三环骨架,如带有全碳季碳中心的手性二氢菲啶酮和二氢咔唑酮衍生物,收率和对映选择性优异(图42a)。磷手性配体AntPhos对反应活性和对映选择性至关重要,而N-膦酰胺保护基的选择对于化学选择性至关重要。该方法实现了3种独特且具有挑战性的重要生物活性多环生物碱的对映选择性全合成,提供了(-)-文殊兰碱的简洁克级规模合成、吲哚生物碱(-)-白坚木米定的高效合成以及(-)-minfiesine的形式全合成。在手性AntPhos(96% e.e.)存在下,通过高效的对映选择性钯催化去芳构环化,简洁地完成了免疫抑制剂(+)-dalesconol A和B的对映选择性合成(图42b)[85]。
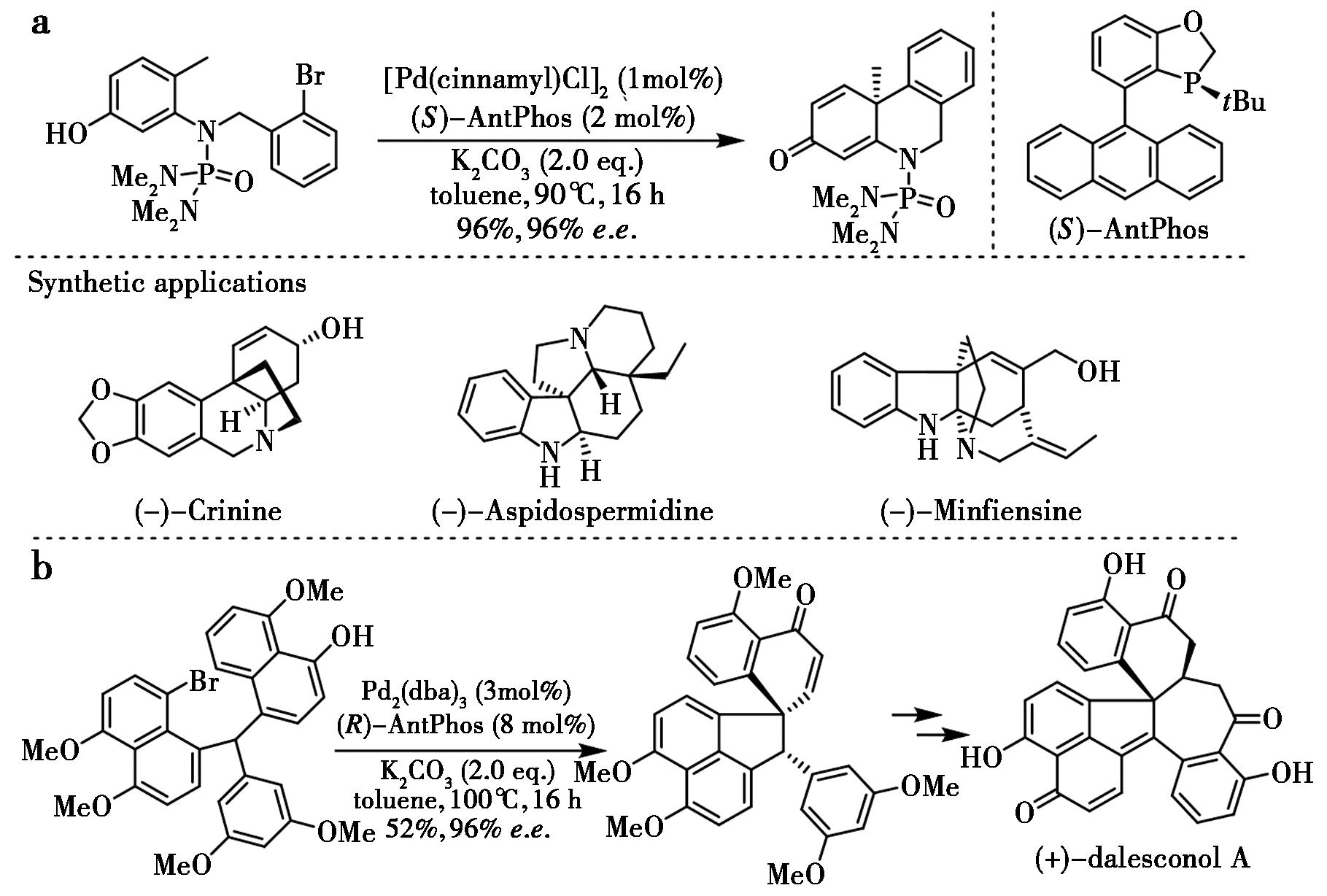
a.文献[84];b.文献[85]
图42 钯-AntPhos催化不对称去芳构环化合成生物碱和多酮天然产物分子[84,85]
Fig.42 Pd-AntPhos catalyzed asymmetric dearomative cyclization for the synthesis of alkaloids and polyketal[84,85]
最近,Li等[86]报道了一种钯催化酚及萘酚的对映选择性芳基化脱芳构化反应,该反应具有广泛的底物适用性和优异的官能团耐受性(图43)。该方法能高效构建包含对映体富集三维分子结构的喹唑啉螺环化合物库。进一步验证了所开发方法能够成功将平面芳香前体转化为复杂三维分子结构。
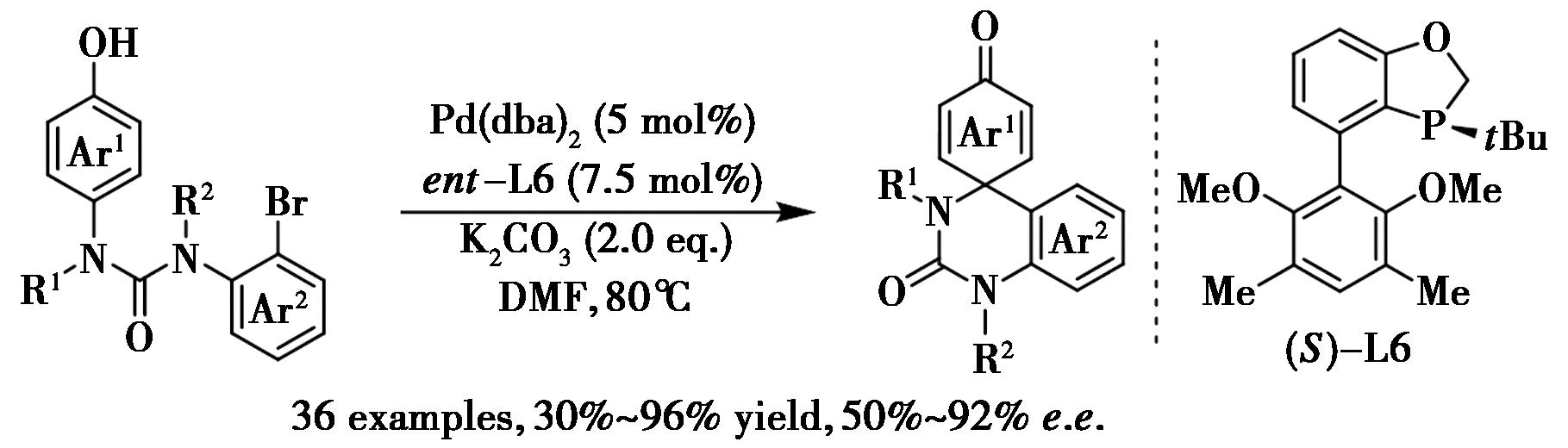
图43 钯催化酚类化合物的不对称去芳构环化合成螺环类化合物[86]
Fig.43 Pd-catalyzed enantioselective dearomative cyclization of phenols for the synthesis of spirocycles[86]
Deng等[87]报道了使用BIDIME作为配体,钯催化4-乙烯基苯并噁嗪酮与羧酸的选择性脱羧[4+2]环加成,以中等至良好收率和良好至优异的立体选择性提供了一系列结构多样的带有两个连续手性中心的3,4-二氢喹啉-2-酮(图44)。

图44 钯催化立体选择性脱羧[4+2]环加成[87]
Fig.44 Pd-catalyzed stereoselective decarboxylative [4+2] cycloaddition[87]
Huang等[88]报道了通过钯催化乙烯基苯并噁嗪酮和七元环状N-磺酰醛亚胺的[4+2]成环反应,以中等收率和高对映选择性及非对映选择性获得带有1,3-非相邻手性中心的[6.7]-稠合N-杂环(图45)。Pd-WingPhos催化剂是实现对映选择性环化的关键。
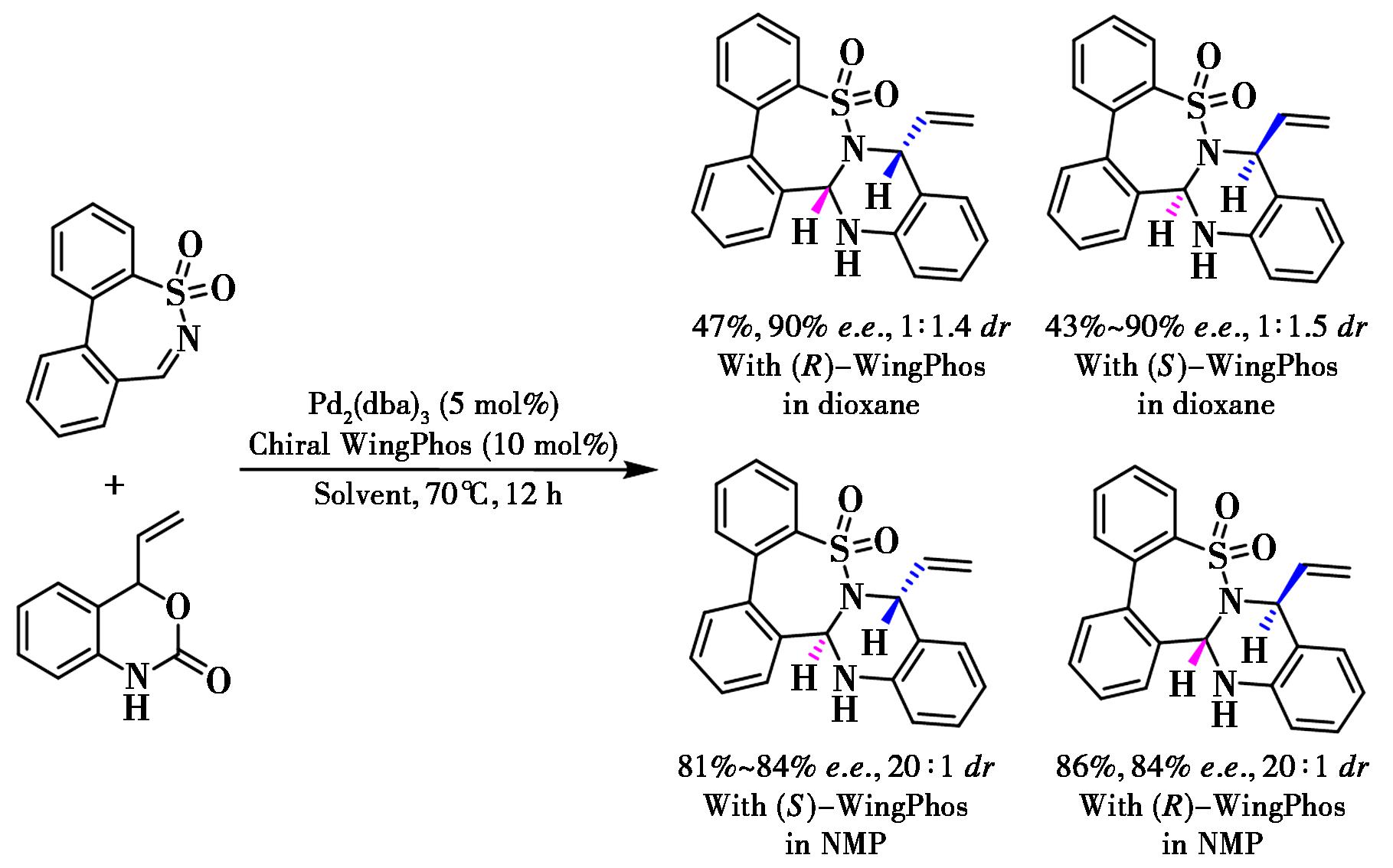
图45 钯-WingPhos催化不对称[4+2]成环反应[88]
Fig.45 Pd-WingPhos catalyzed enantioselective [4+2] annulations[88]
Shao等[89]报道了钯-WingPhos催化的1,3-烯炔与杂环和碳环亲核试剂的对映选择性环加成,用于合成多种具有重要药学价值的螺环化合物,收率和对映选择性优异(图46)。该反应条件温和,底物范围广。使用WingPhos可以抑制双烯丙基副产物的形成并控制立体选择性。有趣的是,具有末端三键或末端双键的1,3-烯炔提供了相反的立体选择性。由于配体的叔丁基基团与烯炔上取代基之间的空间相互作用,如提出的立体化学模型所示,即氢钯化物种进行立体选择性亲核取代。
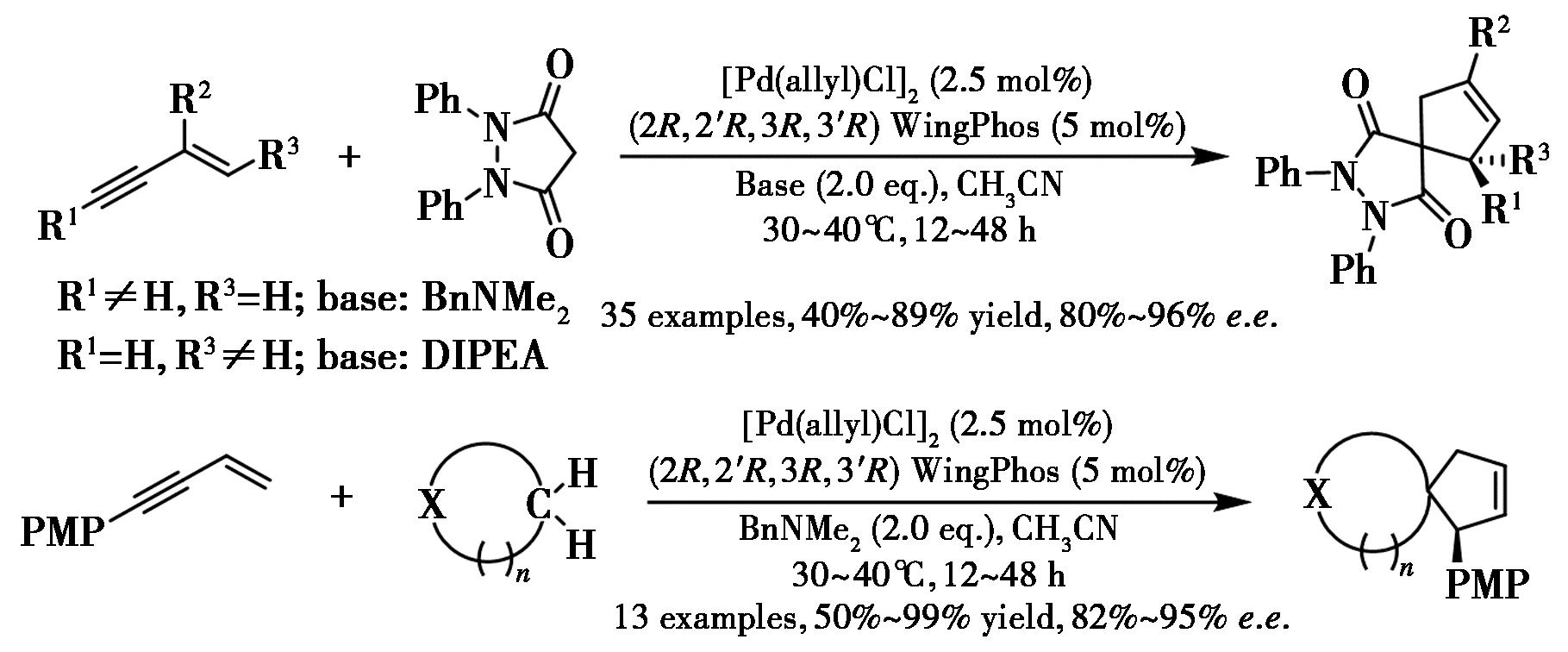
图46 钯-WingPhos催化1,3-炔烯与吡唑烷酮不对称环加成反应合成手性螺环[89]
Fig.46 Pd-WingPhos catalyzed enantioselective cycloaddition of 1,3-enynes and pyrazolidinone[89]
2025年,Liu等[90]报道了钯催化1,3-二炔取代丙二腈与异氰酸酯的[2+2+2]环加成反应,构建多取代嘧啶-2-酮骨架(图47)。该反应具有广泛的底物适用范围和中等至优良的收率。共轭的嘧啶-2-酮分子展现出作为三价铁离子荧光化学传感器的应用潜力。
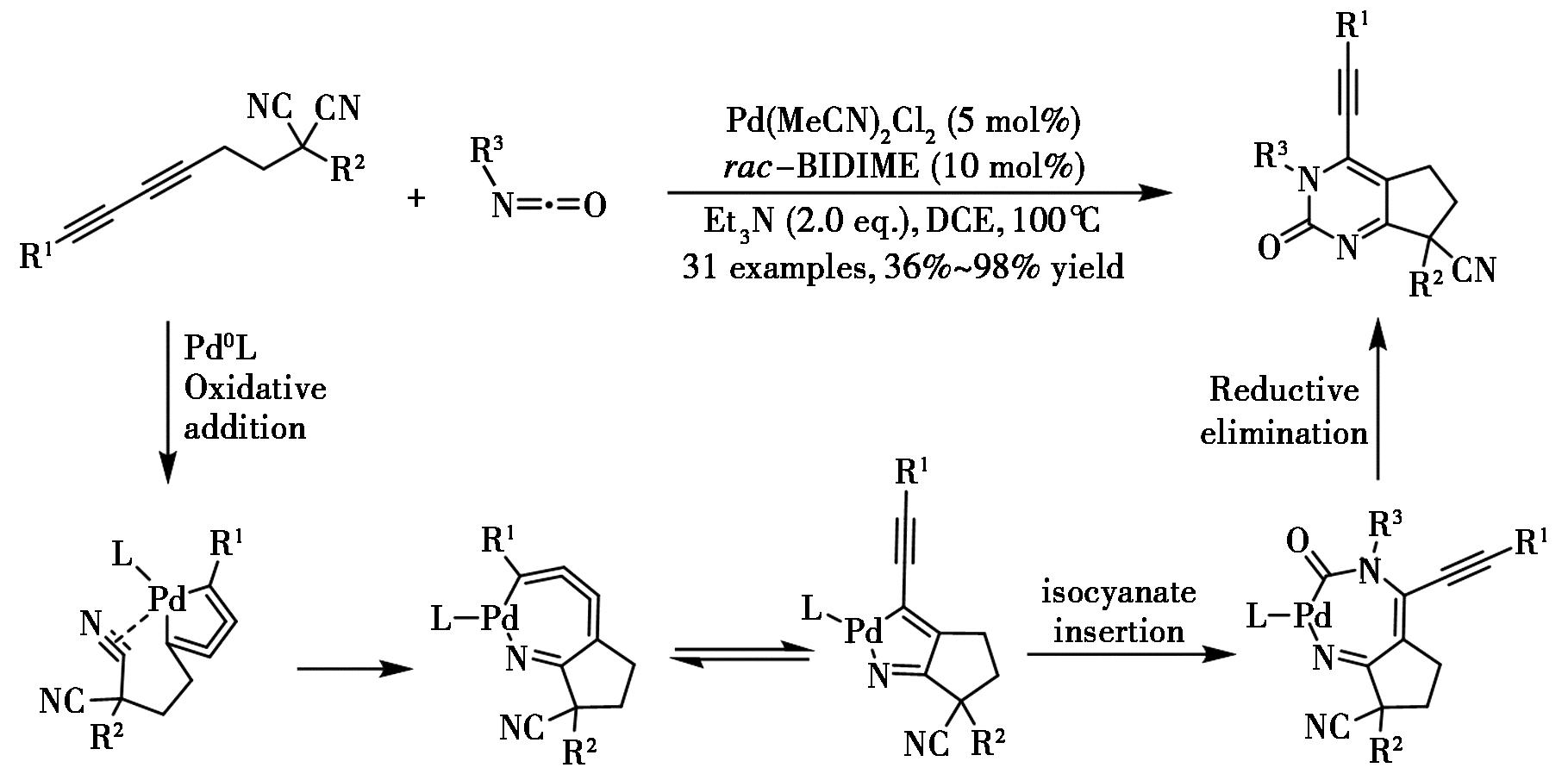
图47 钯催化炔基二腈化合物与异氰酸类化合物的[2+2+2]环加成反应[90]
Fig.47 Pd-catalyzed [2+2+2] cycloaddition of alkyne-tethered malononitriles and isocyanates[90]
Chen等[91]报道了一种钯催化1,3-二烯与2-甲酰芳基硼酸的不对称[3+2]环化反应,该反应通过插烯加成与Suzuki偶联的串联过程实现(图48)。在相同催化条件下,电子中性与缺电子1,3-二烯均能良好兼容,且通过对1,3-二烯底物的官能团调控可观察到显著的区域选择性差异。该方法可立体选择性构建一系列具有多官能团的1-茚满醇类化合物。

图48 钯-AntPhos催化官能团导向的1,3-二烯与芳基硼酸区域选择性[3+2]环合反应[91]
Fig.48 Pd-AntPhos catalyzed functional-group-directed regiodivergent [3+2] annulations of 1,3-dienes and arylboronic acids[91]
双膦配体WingPhos具有很深手性口袋往往展现出独特的催化性质。Tang等[92]报道了钯-WingPhos催化串联烯丙位取代,以优异对映选择性、区域选择性和收率合成系列手性乙烯基取代杂环,包括四氢喹喔啉、哌嗪、二氢苯并噁嗪和吗啉等化合物(图49a)。该反应条件温和、底物范围宽和钯负载量低(0.1 mol%)。机理研究支持串联烯丙位取代过程。进一步的研究表明,该催化体系对邻苯二胺和邻氨基酚的无保护基对映选择性串联烯丙位取代同样有效,收率和对映选择性优异(图49b)[93]。
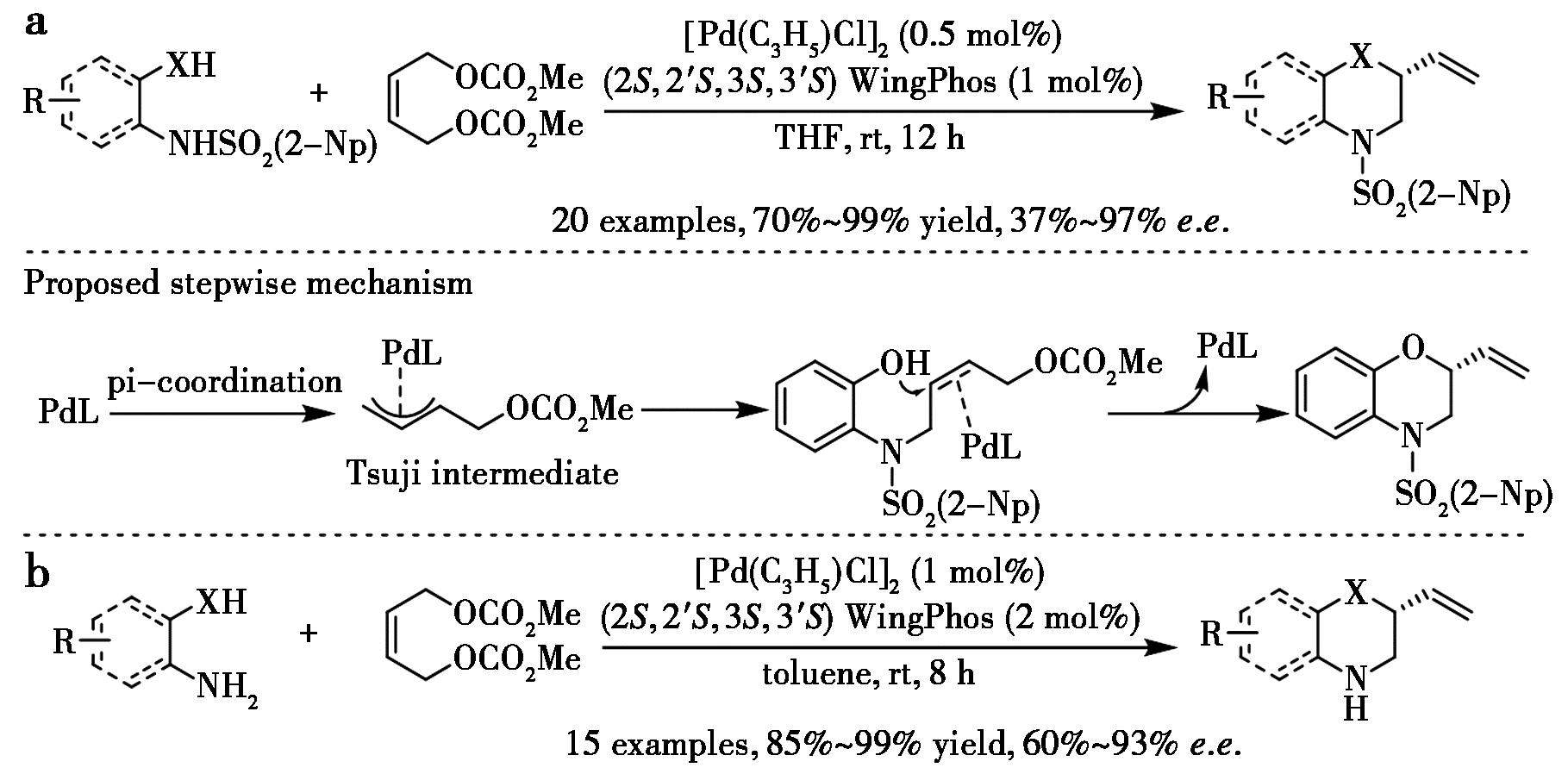
a.文献[92];b.文献[93]
图49 钯-WingPhos催化区域选择性和对映选择性串联烯丙位取代[92,93]
Fig.49 Pd-WingPhos catalyzed regio- and enantioselective tandem allylic substitution[92,93]
手性双膦配体是目前最成功和高效的配体,常用于不对称氢化。其中,磷手性双膦配体在不对称氢化中发挥了重要作用,能兼顾高立体选择性控制和高转化数(TONs)。
2010年,Tang等[94]开发了手性POP配体成功应用于铑催化α-(酰氨基)丙烯酸酯和β-(酰氨基)丙烯酸酯的不对称氢化反应中,对映选择性高达>99% e.e.,反应活性达10 000 TON(图50a)。同年,Tang等[95]又设计合成了空气稳定且结构可调控的手性双膦配体BIBOP,成功应用于铑催化多官能团化烯烃的不对称氢化反应,对映选择性达99% e.e.,反应活性达2 000 TON(图50b)。2013年,Tang等[96]实现了MeO-BIBOP公斤级合成,并将其铑配合物应用于N-乙酰基烯酰胺的不对称氢化中,反应转化数达200 000 TON(图50c)。2014年,Reeves等[97]开发了利用铑-BIBOP催化烯酰胺的高对映选择性氢化,值得强调的是,在0.01 mol%催化剂负载量下以高达99.9% e.e.得到所需的手性氢化产物,并最终实现手性取代的吡啶药物中间体的制备(图50d)。
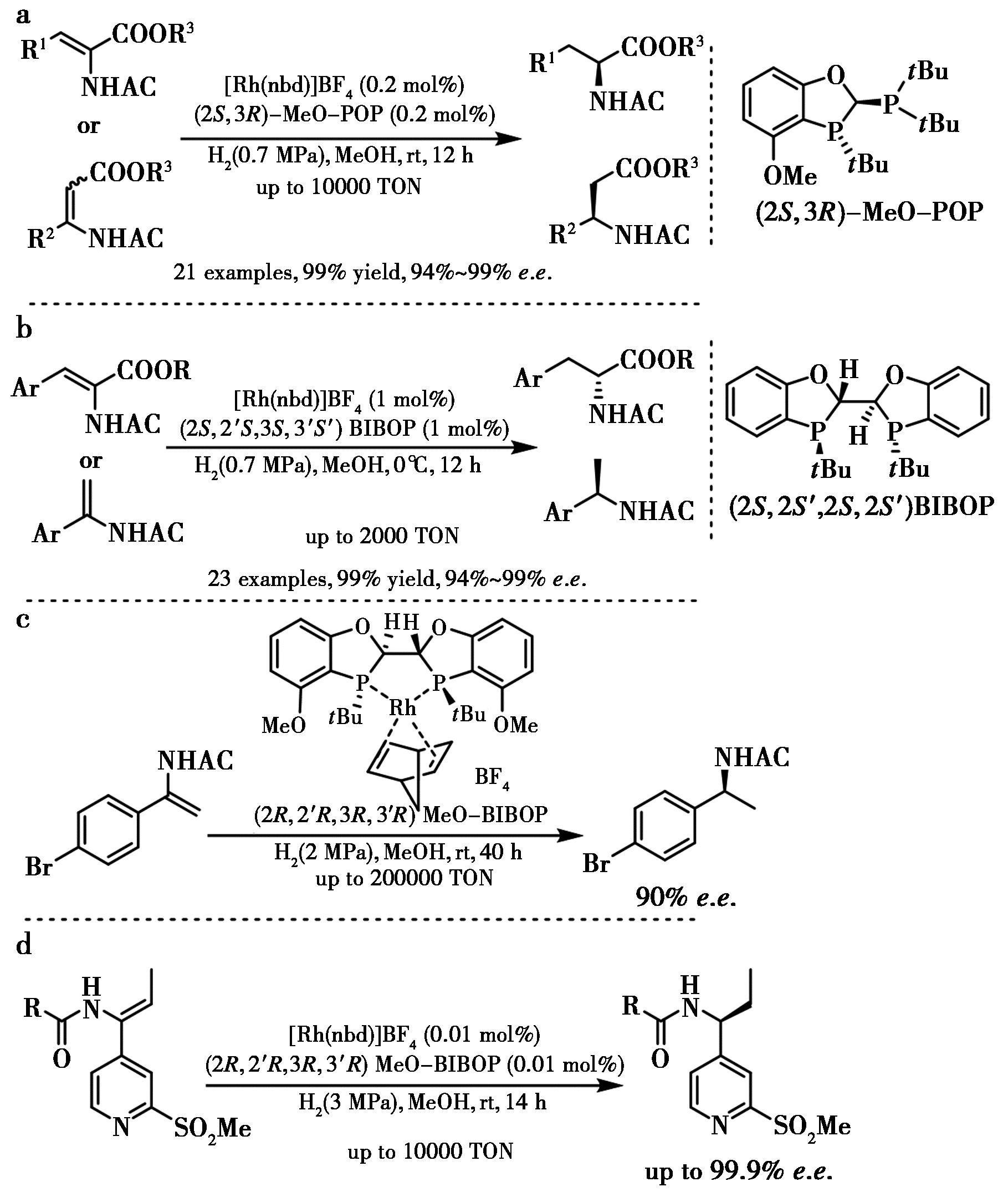
a.文献[94];b.文献[95];c.文献[96];d.文献[97]
图50 铑催化烯酰胺的不对称氢化反应[94-97]
Fig.50 Rh-catalyzed asymmetric hydrogenation of enamides[94-97]
2013年,Tang等[98]报道合成了深手性口袋属性的配体WingPhos,并应用于铑催化三取代β-芳基烯酰胺的不对称氢化,以优异对映选择性(92%~99% e.e.)形成了一系列手性β-芳基胺(图51a)。随后,Tang等[99]设计合成了ArcPhos发现在铑催化剂以优异的对映选择性和高转化数实现了脂肪族环状四取代烯酰胺的对映选择性氢化。该方法为便捷获得一系列手性顺式-2-烷基取代碳环和杂环胺衍生物提供了新的合成方法(图51b)。通过托法替尼((R)-tofacitinib)的不对称简洁合成展示了该方法的实用性。2021年,Tang等[100]利用Rh-ArcPhos催化剂成功实现了环状四取代烯烃型脱氢氨基酸衍生物的高效不对称氢化反应,以高达96%的对映选择性和1 000的转化数(TON),合成了一系列具有两个连续手性中心的α-酰氨基-β-烷基四氢吡喃酮类化合物(图51c)。
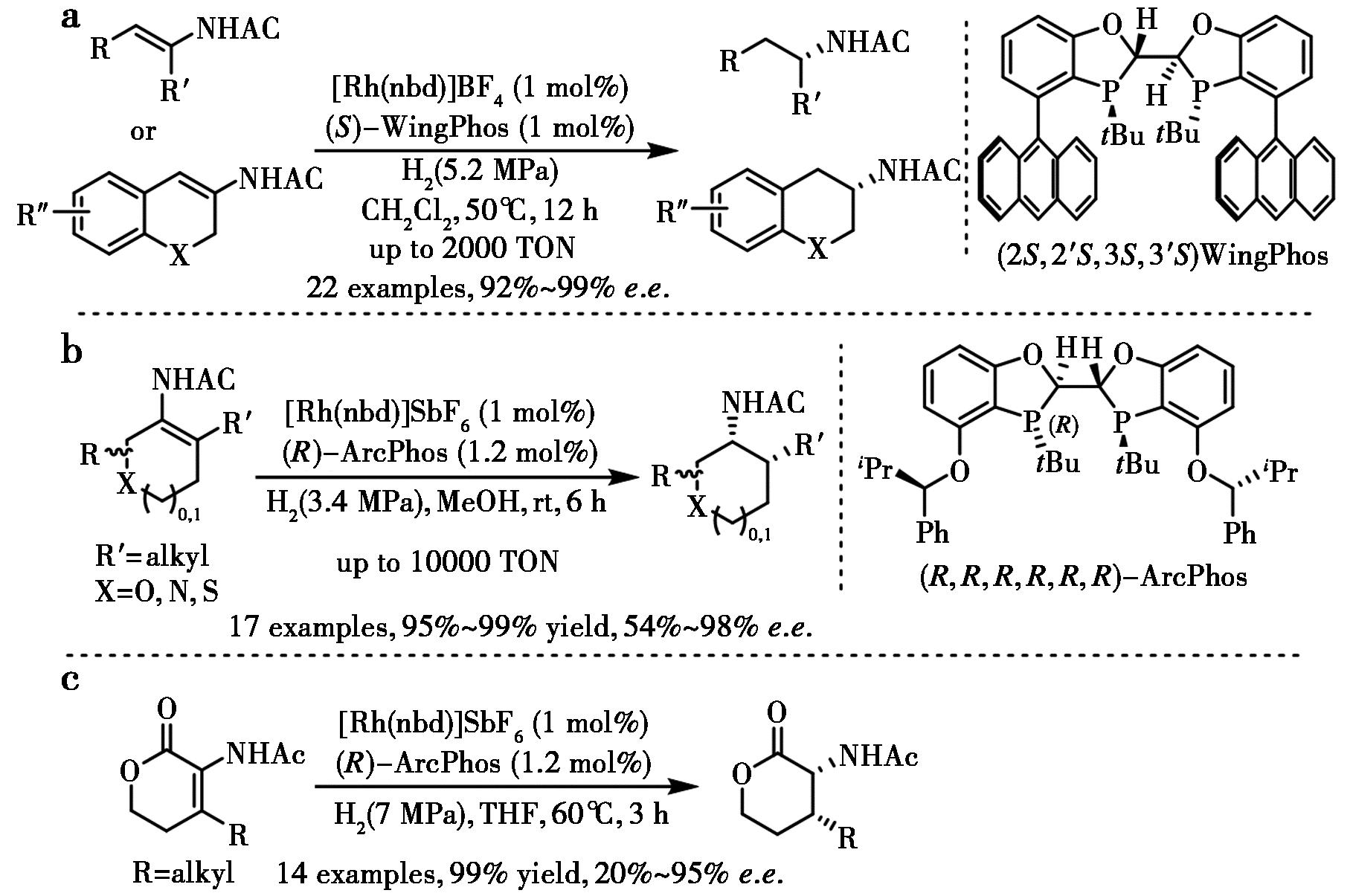
a.文献[98];b.文献[99];c.文献[100]
图51 铑催化四取代环状烯酰胺化合物的不对称氢化[98-100]
Fig.51 Rh-catalyzed asymmetric hydrogenation of aliphatic cyclic tetrasubstituted enamides[98-100]
BIBOP配体对复杂杂芳基酮的不对称氢化也有效。Rodríguez等[101,102]报道了Ru-BIBOP双胺催化杂芳基环酮的不对称氢化,合成了抑制蛋白转移药物的关键手性药物中间体。该方法的催化载量低、收率高和对映选择性高(图52a)。其中双胺作为催化剂的一部分也对反应活性起着关键作用,产物的手性由BIBOP配体决定。2018年,Tang等[103]开发了钯催化β-芳基和β-烷基取代β-酮酯的不对称氢化,使用iPr-BABIBOP作为配体,在低至0.01 mol%的催化剂负载量下,以优异对映选择性(高达>99% e.e.)和收率提供了一系列手性β-羟基羧酸酯(图52b)。
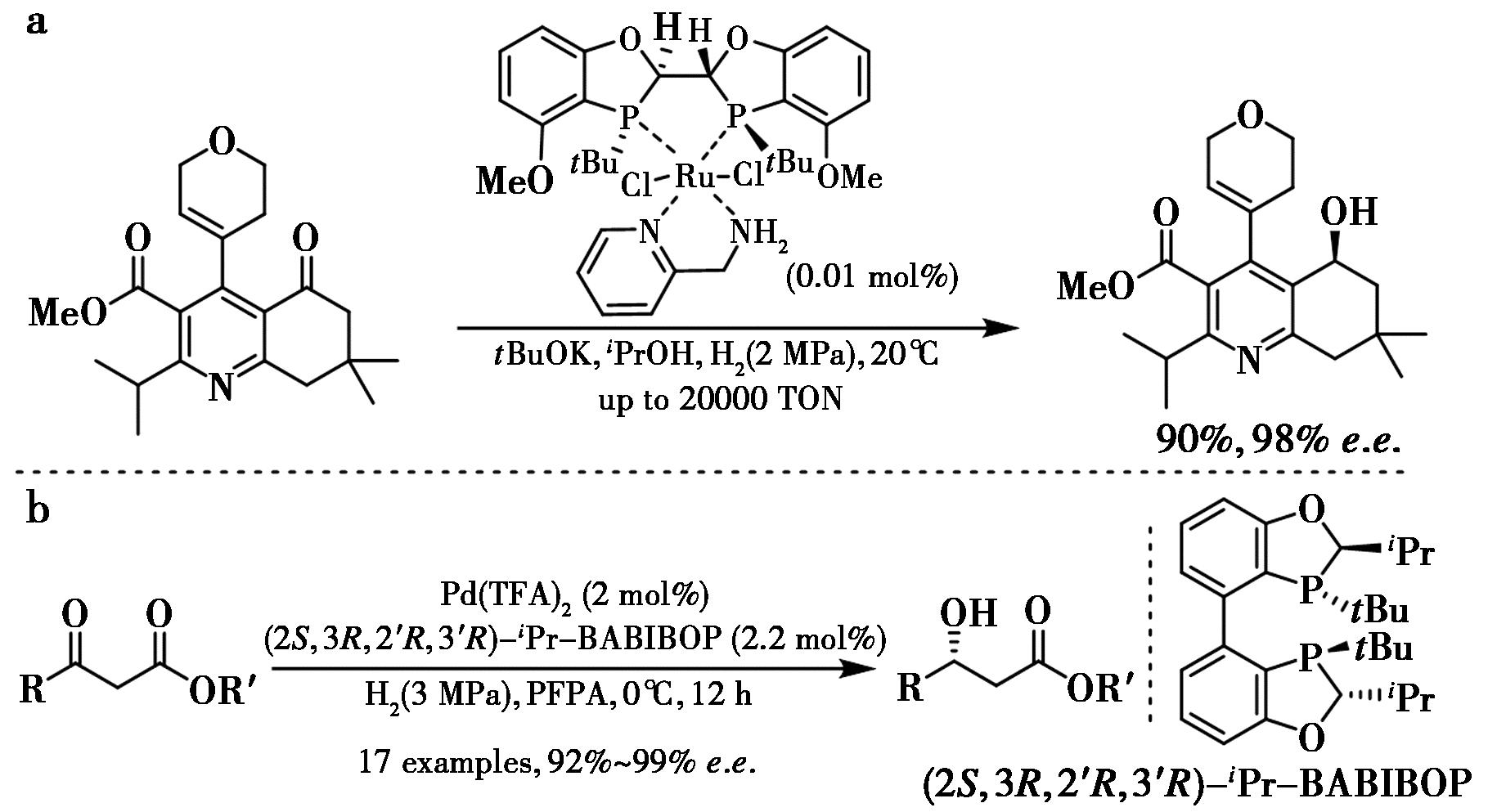
a.文献[101,102];b.文献[103]
图52 钌或钯催化酮的不对称氢化[101-103]
Fig.52 Ru or Pd-catalyzed asymmetric hydrogenation of ketones[101-103]
2014年,Qu等[104]设计合成了一类空气稳定的磷手性二氢苯并氧杂膦烷噁唑啉配体,成功应用于铱催化非官能化1-芳基-3,4-二氢萘的不对称氢化反应,可获得高达99% e.e.(图53a)。同年,Qu等[105]又报道了酰基吡啶进行非对映选择性亲核芳香取代反应,设计并合成了一系列空气稳定、可调控的磷手性二氢苯并氧杂膦烷吡啶配体,该配体在铱催化非官能化烯烃的不对称氢化反应中成功应用,展现出良好的对映选择性(图53b)。2017年,Li等[106]报道了铑催化的四取代茚双键的不对称氢化反应,能以95% e.e.得到手性茚化合物(图53c),最终合成了异喹啉生物碱Delavatine A。随后,Li等[107]报道了使用BABIBOP配体,实现了铑催化二取代和三取代烯酰胺的对映选择性氢化(图53d)。接着,Qu等[108]报道了Ir-DI-BIDIME催化1,4-苯并二噁英的不对称氢化,以高对映选择性得到2-取代1,4-苯并二噁烷(图53e)。最近,Lu等[109]报道了铑催化的取代己二烯酮的不对称氢化,以99% e.e.,99% dr得到双甲基手性中心己二酮(图53f),最终合成了倍半萜环奥烯酮和迪西萜醇。
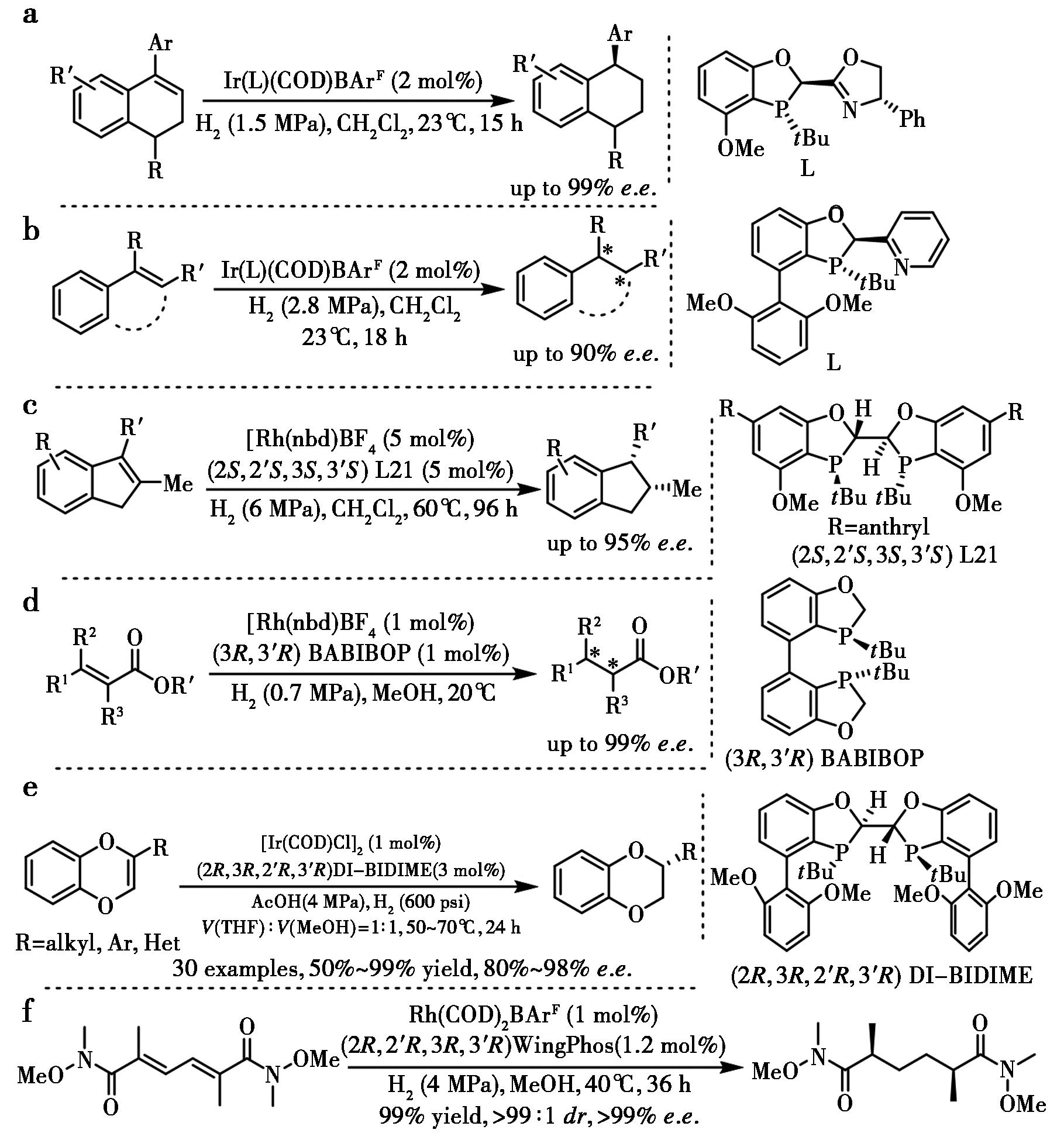
a.文献[104];b.文献[105];c.文献[106];d.文献[107];e.文献[108];f.文献[109]
图53 铱或铑催化多取代烯烃类化合物的不对称氢化[104-109]
Fig.53 Ir- or Rh-catalyzed asymmetric hydrogenation of multi-substituted olefinic substrates[104-109]
2018年,Qu等[110]报道了α-芳基与α-杂芳基哌啶的对映选择性合成方法。其关键步骤在于铱催化取代N-苄基吡啶鎓盐的不对称氢化反应(图54a)。该反应对多种α-杂芳基哌啶衍生物均表现出优异对映选择性。值得注意的是,最终烯胺中间体的初始质子化过程决定了转化的立体化学结果,而非后续亚胺中间体的氢化物还原。2022年,Qu等[111]利用铱-MeO-BoQPhos催化体系实现稠合三环茚并吡啶鎓盐的不对称氢化反应,合成系列手性富集的茚并哌啶产物(图54b)。值得强调的是,该反应催化剂负载量可低至1 000 mg/L。
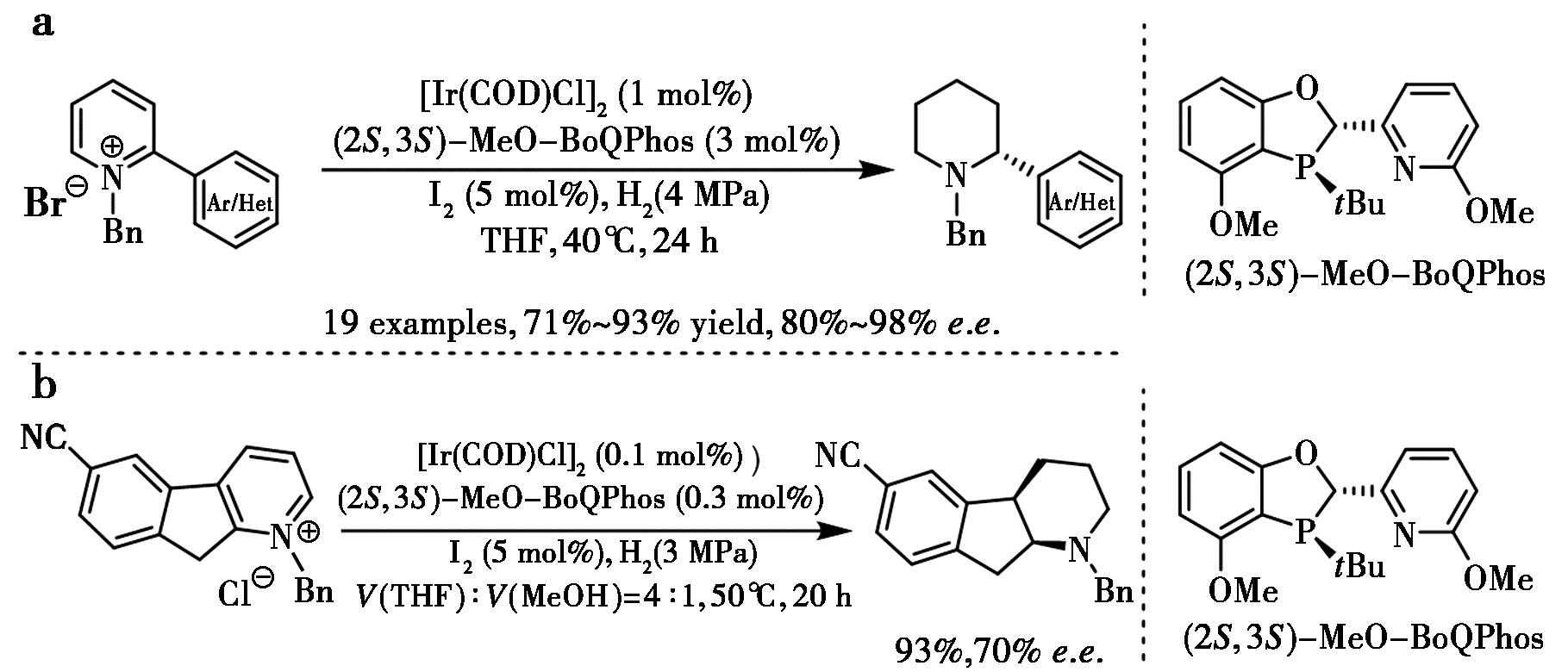
a.文献[110];b.文献[111]
图54 铱催化吡啶盐的不对称氢化反应[110,111]
Fig.54 Ir-catalyzed asymmetric hydrogenation of pyridinium salts[110,111]
与杂芳烃相比,由于强芳香性和对映选择性控制的困难,全碳芳香环的均相不对称氢化仍然是有机合成中的一个重大挑战。Zhou等[112]利用铑-WingPhos催化实现了全碳芳香环不对称氢化,通过去对称化或动力学拆分,以高对映选择性提供了一系列轴手性环状化合物(图55a)。WingPhos的独特结构和富电子特性对于实现高对映选择性以及反应活性至关重要。2022年,Zhou等[113]又报道了钯催化未保护3-取代吲哚的不对称氢化,以优异收率和高对映选择性合成了一系列3-取代二氢吲哚(图55b)。大位阻双膦配体在该反应的对映选择性控制中起关键作用。此外,成功完成了克级规模的氢化实验及产物衍生化研究。
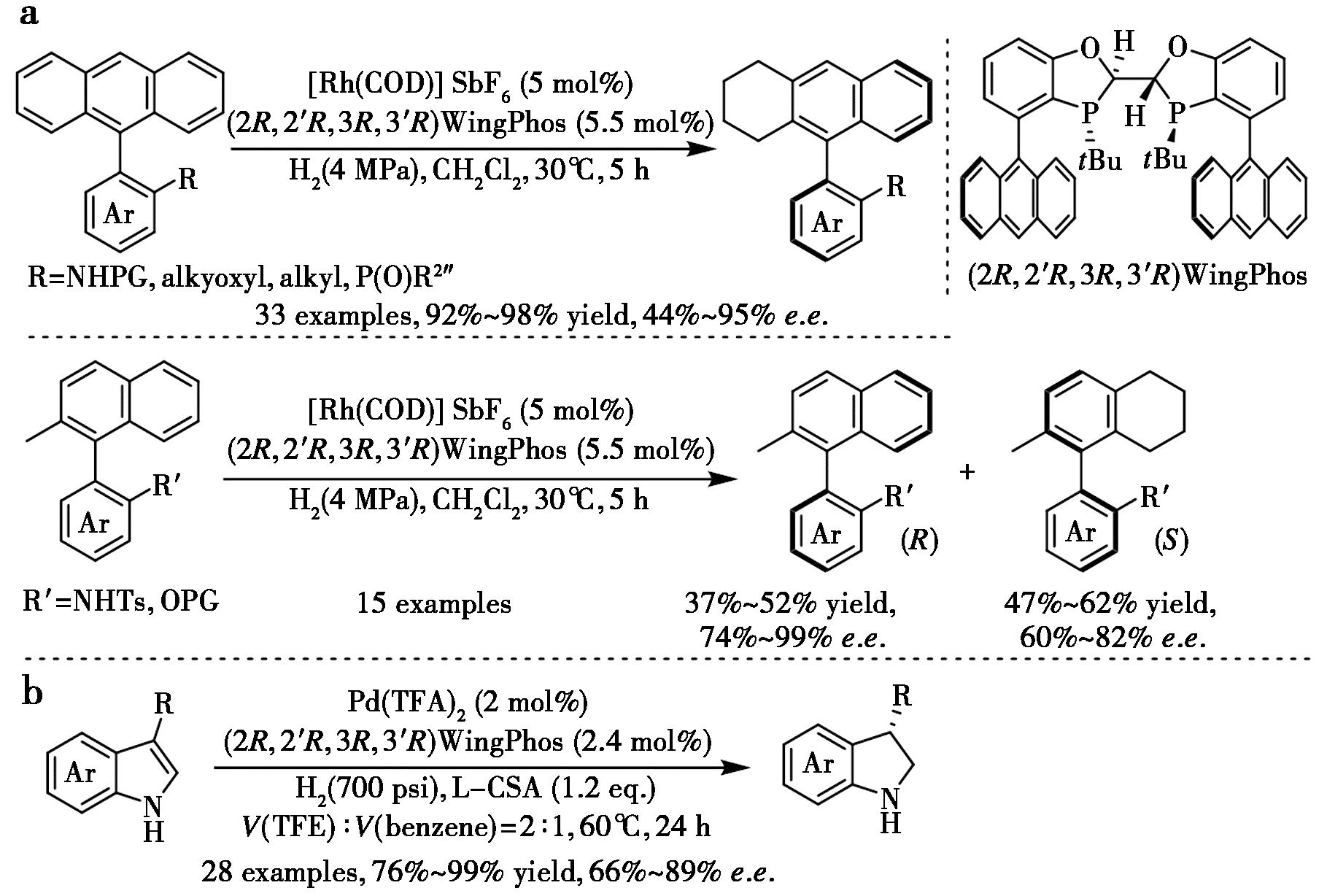
a.文献[112];b.文献[113]
图55 铑-WingPhos催化全碳芳环的不对称氢化[112,113]
Fig.55 Rh-WingPhos catalyzed asymmetric hydrogenation of all-carbon aromatic rings[112,113]
自2010年首次报道以来,基于磷手性二氢苯并氧杂膦烷骨架的配体已超过百种被报道并成功应用于各种有机化学转化,在不对称催化和合成领域取得了显著的成就。磷手性二氢苯并氧杂膦烷配体是一类大位阻、富电子特性、性质稳定和结构易于修饰的膦配体。利用这些配体,已经开发出各种高效的金属催化不对称转化,包括不对称交叉偶联、不对称环化、不对称加成和不对称氢化,具有优异的反应活性、对映选择性和TONs,为复杂天然产物、手性药物及其中间体的合成提供了新的有效方法。特别是,由配体驱动的不对称交叉偶联和不对称氢化已频繁用于工业上的公斤级规模的药物发现和开发。毫无疑问,未来将会发现更多由磷手性二氢苯并氧杂膦烷配体主导的高效催化和合成,将在药物绿色工艺开发及工业化生产中发挥着更加突出的作用。
新的配体结构有利于发现新的反应活性和选择性,实现新的高效催化剂和反应。例如二氢苯并氧杂膦烷结构的发现促进了结构独特的双膦配体的开发,如WingPhos和MeO-BIBOP等;以及一系列不可替代的单膦配体,如BIDIME、AntPhos、BaryPhos以及手性BOPPO配体,这些配体在学术界和工业界的应用日益增多。配体的发展将会极大地促进更多有趣和有用反应的发现,如不对称碳氢键活化及不对称去芳构环化反应等。因此,继续开发具有新颖结构母核的配体以解决催化与合成中未解决的问题及挑战极为重要。希望本综述能鼓励读者继续从事配体的开发研究,以创造力和想象力在催化与合成中创造更多奇迹。
[1]Knowles W S,Sabacky M J,Vineyard B D,Weinkauff D J.J.Am.Chem.Soc.,1975,97(9):2 567-2 568.
[2]Rojo P,Riera A,Verdaguer X.Coord.Chem.Rev.,2023,489:215 192.
[3]Imamoto T.Chem.Rev.,2024,124(14):8 657-8 739.
[4]Xu G Q,Senanayake C H,Tang W J.Acc.Chem.Res.,2019,52(4):1 101-1 112.
[5]Cao Z,He D,Tang W.Org.Process Res.Dev.,2024,28(4):949-977.
[6]Tang W J,Capacci A G,Wei X,Li W,White A,Patel N D,Savoie J,Gao J J,Rodríguez S,Qu B,Haddad N,Lu B Z,Krishnamurthy D,Yee N K,Senanayake C H.Angew.Chem.,Int.Ed.,2010,49(34):5 879-5 883.
[7]Zhao Q,Li C,Senanayake C H,Tang W J.Chem.Eur.J.,2013,19(7):2 261-2 265.
[8]Li C,Xiao G,Zhao Q,Liu H,Wang T,Tang W J.Org.Chem.Front.,2014,1(3):225-229.
[9]Li C,Chen T,Li B,Xiao G,Tang W J.Angew.Chem.,Int.Ed.,2015,54(12):3 792-3 796.
[10]Li C,Chen D,Tang W J.Synlett,2016,27(15):2 183-2 200.
[11]Si T,Li B,Xiong W,Xu B,Tang W J.Org.Biomol.Chem.,2017,15(46):9 903-9 909.
[12]Sieber J D,Buono F,Brusoe A,Desrosiers J N,Haddad N,Lorenz J C,Xu Y,Wu H,Zhang L,Han Z S,Roschangar F,Song J J,Yee N K,Senanayake C H.J.Org.Chem.,2019,84(8):4 926-4 931.
[13]Bock M J,Denmark S E.J.Org.Chem.,2024,89(22):16 195-16 202.
[14]Patel N D,Rivalti D,Buono F G,Chatterjee A,Qu B,Braith S,Desrosiers J N,Rodríguez S,Sieber J D,Haddad N,Fandrick K R,Lee H,Yee N K,Busacca C A,Senanayake C H.Asian J.Org.Chem.,2017,6(9):1 285-1 291.
[15]Thakore R R,Takale B S,Hu Y,Ramer S,Kostal J,Gallou F,Lipshutz B H.Tetrahedron,2021,87:132 090.
[16]Thakore R R,Takale B S,Casotti G,Gao E S,Jin H S,Lipshutz B H.Org.Lett.,2020,22(16):6 324-6 329.
[17]Takale B S,Thakore R R,Handa S,Gallou F,Reilly J,Lipshutz B H.Chem.Sci.,2019,10(38):8 825-8 831.
[18]Shada A D R,Mangunuru H P R,Terrab L,Tenneti S,Kalikinidi N R,Naini S R,Gajula P,Crull E B,Janganati V,Kovvuri R,Natarajan V,Lee D,Yin J,Samankumara L,Mahar R,Zhang X,Chen A,Hewa-rahinduwage C C,Wang Z,Mamunooru M,Rana J,Wannere C S,Armstrong J D,III,Williamson R T,Sirasani G,Qu B,Senanayake C H.Org.Lett.,2024,26(14):2 751-2 757.
[19]Handa S,Smith J D,Zhang Y,Takale B S,Gallou F,Lipshutz B H.Org.Lett.,2018,20(3):542-545.
[20]Bringmann G,Mortimer A J P,Keller P A,Gresser M J,Garner J,Breuning M.Angew.Chem.,Int.Ed.,2005,44(34):5 384-5 427.
[21]Bringmann G,Gulder T,Gulder T A M,Breuning M.Chem.Rev.(Washington,DC,U.S.),2011,111(2):563-639.
[22]Baudoin O.Eur.J.Org.Chem.,2005,(20):4 223-4 229.
[23]Tang W J,Patel N D,Xu G Q,Xu X,Savoie J,Ma S,Hao M H,Keshipeddy S,Capacci A G,Wei X,Zhang Y,Gao J J,Li W,Rodríguez S,Lu B Z,Yee N K,Senanayake C H.Org.Lett.,2012,14(9):2 258-2 261.
[24]Xu G Q,Fu W,Liu G,Senanayake C H,Tang W J.J.Am.Chem.Soc.,2014,136(2):570-573.
[25]Fandrick K R,Li W,Zhang Y,Tang W J,Gao J,Rodríguez S,Patel N D,Reeves D C,Wu J,Sanyal S,Gonnella N,Qu B,Haddad N,Lorenz J C,Sidhu K,Wang J,Ma S,Grinberg N,Lee H,Tsantrizos Y,Poupart M A,Busacca C A,Yee N K,Lu B Z,Senanayake C H.Angew.Chem.,Int.Ed.,2015,54(24):7 144-7 148.
[26]Yang H,Sun J,Gu W,Tang W J.J.Am.Chem.Soc.,2020,142(17):8 036-8 043.
[27]Yang H,Tang W J.Nat.Commun.,2022,13(1):4 577.
[28]Jouffroy M,Neufeld K.ACS Catal.,2022,12(14):8 380-8 385.
[29]Howell G P,Agnew L R,Bauer C,Bell F J,Campbell A D,Dai K,Dave D,Ellis S R,Foulkes M J,Gall M A Y,Garrec K,Ge H,Hayter B R,Jones M F,Karageorgis G,Littleson M,Lloyd-hughes T W,Mcnicholl H C,Mooney D T,Moore B J,Munday R H,Noone E,Perkins D,Powell L,Putra O D,Tomasi S,Turner M,Wang H,Zhao H,Ring O T.Org.Process Res.Dev.,2025,29(3):804-827.
[30]Patel N D,Sieber J D,Tcyrulnikov S,Simmons B J,Rivalti D,Duvvuri K,Zhang Y,Gao D A,Fandrick K R,Haddad N,Lao K S,Mangunuru H P R,Biswas S,Qu B,Grinberg N,Pennino S,Lee H,Song J J,Gupton B F,Garg N K,Kozlowski M C,Senanayake C H.ACS Catal.,2018,8(11):10 190-10 209.
[31]Yang Y,Wu C,Xing J,Dou X.J.Am.Chem.Soc.,2024,146(9):6 283-6 293.
[32]Dai X,Strotman N A,Fu G C.J.Am.Chem.Soc.,2008,130(11):3 302-3 303.
[33]Lundin P M,Fu G C.J.Am.Chem.Soc.,2010,132(32):11 027-11 029.
[34]Li B,Li T,Aliyu M A,Li Z H,Tang W J.Angew.Chem.,Int.Ed.,2019,58(33):11 355-11 359.
[35]Li B,Aliyu M A,Gao Z,Li T,Dong W,Li J,Shi E,Tang W J.Org.Lett.,2020,22(13):4 974-4 978.
[36]Farina V.Adv.Synth.Catal.,2004,346(13/15):1 553-1 582.
[37]Li B,Luo B,Blakemore C A,Smith A C,Widlicka D W,Berritt S,Tang W J.Org.Lett.,2021,23(16):6 439-6 443.
[38]Li B,Luo B,Yang H,Tang W J.Angew.Chem.,Int.Ed.,2022,61(38):e202 209 087.
[39]Zhang B,Ruan J,Seidel D,Chen W.Angew.Chem.,Int.Ed.,2023,62(36):e202 307 638.
[40]He S,Shen B,Zuo L,Xiang S,Liu H,Yu P,Tan B.J.Am.Chem.Soc.,2024,146(28):19 137-19 145.
[41]Wang Z,Zhu J,Wang M,Lu P.J.Am.Chem.Soc.,2024,146(18):12 691-12 701.
[42]Lin Z,Jiang Y,Wang F,Huang G,Li J,Li X W.Chem.Sci.,2025,16(31):14 252-14 261.
[43]Long R,Huang J,Gong J,Yang Z.Nat.Prod.Rep.,2015,32(11):1 584-1 601.
[44]Mangunuru H P R,Malapit C A,Haddad N,Reeves J T,Qu B,Rodríguez S,Lee H,Yee N K,Song J J,Busacca C A,Senanayake C H.Synthesis,2018,50(22):4 435-4 443.
[45]Rao X,Li N,Bai H,Dai C,Wang Z,Tang W J.Angew.Chem.,Int.Ed.,2018,57(38):12 328-12 332.
[46]Wu T,Kang X,Bai H,Xiong W,Xu G,Tang W J.Org.Lett.,2020,22(12):4 602-4 607.
[47]Huang J,Pei C,Yang H,Wu B,Tang W J.Angew.Chem.,Int.Ed.,2025,64(28):e202 505 458.
[48]Li S,Chen Q,Yang J,Zhang J.Angew.Chem.,Int.Ed.,2022,61(23):e202 202 046.
[49]Xu G,Li M,Wang S,Tang W J.Org.Chem.Front.,2015,2(10):13 42-1 345.
[50]Zeng D,Zhang X,Wang M,Jiang X.Nat.Commun.,2025,16(1):3 046.
[51]Cheng R,Li B,Wu J,Zhang J,Qiu Z Z,Tang W J,You S L,Tang Y,Xie Z W.J.Am.Chem.Soc.,2018,140(13):4 508-4 511.
[52]Liu L T,Liu H,Zuo Z,Zhang A,Li Z,Meng T,Wu W,Hua Y,Mao G L.Chin.Chem.Lett.,2021,32(1):239-242.
[53]Diesel J,Cramer N.ACS Catal.,2019,9(10):9 164-9 177.
[54]Liao G,Zhang T,Lin Z K,Shi B F.Angew.Chem.,Int.Ed.,2020,59(45):19 773-19 786.
[55]Liu Z,Gao B,Chernichenko K,Yang H,Lemaire S,Tang W J.Org.Lett.,2023,25(38):7 004-7 008.
[56]Fandrick D R,Fandrick K R,Reeves J T,Tan Z,Tang W J,Capacci A G,Rodríguez S,Song J J,Lee H,Yee N K,Senanayake C H.J.Am.Chem.Soc.,2010,132(22):7 600-7 601.
[57]Trost B M,Wang Y,Buckl A K,Huang Z,Nguyen M H,Kuzmina O.Science,2020,368(6 494):1 007-1 011.
[58]Li K,Hu N,Luo R,Yuan W,Tang W J.J.Org.Chem.,2013,78(12):6 350-6 355.
[59]Miao R,Xia Y,Wei Y,Ouyang L,Luo R.Molecules,2022,27(12):3 898.
[60]Luo R,Li K,Hu Y,Tang W J.Adv.Synth.Catal.,2013,355(7):1 297-1 302.
[61]Huang L,Zhu J,Jiao G,Wang Z,Yu X,Deng W P,Tang W J.Angew.Chem.,Int.Ed.,2016,55(14):4 527-4 531.
[62]Zhu J,Li Z,Li J,Tian D,Xu R,Tan Z,Chen Z,Tang W J.Chem.Sci.,2023,14(6):1 606-1 612.
[63]Sieber J D,Chennamadhavuni D,Fandrick K R,Qu B,Han Z S,Savoie J,Ma S,Samankumara L P,Grinberg N,Lee H,Song J J,Senanayake C H.Org.Lett.,2014,16(20):5 494-5 497.
[64]Zhu J,Huang L,Dong W,Li N,Yu X,Deng W P,Tang W J.Angew.Chem.,Int.Ed.,2019,58(45):16 119-16 123.
[65]Tan S,Chen P,Zhu L,Gan M Q,Ouyang Q,Du W,Chen Y C.J.Am.Chem.Soc.,2022,144(49):22 689-22 697.
[66]Crossley S W M,Obradors C,Martinez R M,Shenvi R A.Chem.Rev.(Washington,DC,U.S.),2016,116(15):8 912-9 000.
[67]Blieck R,Taillefer M,Monnier F.Chem.Rev.,2020,120(24):13 545-13 598.
[68]Kennemur J L,Maji R,Scharf M J,List B.Chem.Rev.,2021,121(24):14 649-14 681.
[69]Sun X Y,Yao B Y,Xuan B,Xiao L J,Zhou Q L.Chem Catal.,2022,2(11):3 140-3 162.
[70]Hu N,Zhao G,Zhang Y,Liu X,Li G,Tang W J.J.Am.Chem.Soc.,2015,137(21):6 746-6 749.
[71]Liu J,Nie M,Zhou Q,Gao S,Jiang W,Chung L W,Tang W J,Ding K.Chem.Sci.,2017,8(7):5 161-5 165.
[72]Guo J,Cheng Z,Chen J,Chen X,Lu Z.Acc.Chem.Res.,2021,54(11):2 701-2 716.
[73]Parsutkar M M,Bhunia S,Majumder M,Lalisse R F,Hadad C M,Rajanbabu T V.J.Am.Chem.Soc.,2023,145(13):7 462-7 481.
[74]Yuan F,Qi X,Zhao Y,Jia J,Yan X,Hu F,Xia Y.Angew.Chem.,Int.Ed.,2024,63(23):e202 401 451.
[75]Dong W,Xu X,Ma H,Lei Y,Lin Z,Zhao W.J.Am.Chem.Soc.,2021,143(29):10 902-10 909.
[76]Liu L,Zhao J,Dong W,Zhao W.ChemCatChem,2024,16(20):e202 400 862.
[77]Li L,Liu Y C,Shi H.J.Am.Chem.Soc.,2021,143(11):4 154-4 161.
[78]Yan X,Li L,Wu W,Xu L,Li K,Liu Y,Shi H.Nat.Commun.,2021,12(1):5 881-5 890.
[79]Liu X,Zheng H,Xia Y,Lin L,Feng X.Acc.Chem.Res.,2017,50(10):2 621-2 631.
[80]Zheng C,You S L.Acc.Chem.Res.,2020,53(4):974-987.
[81]Du K,Guo P,Chen Y,Cao Z,Wang Z,Tang W J.Angew.Chem.,Int.Ed.,2015,54(10):3 033-3 037.
[82]Cao Z,Du K,Liu J,Tang W J.Tetrahedron,2016,72(14):1 782-1 786.
[83]Sun J,Chen Y,Ragab S S,Gu W,Tang Z,Tang Y,Tang W J.Angew.Chem.,Int.Ed.,2023,62(24):e202 303 639.
[84]Du K,Yang H,Guo P,Feng L,Xu G Q,Zhou Q,Chung L W,Tang W J.Chem.Sci.,2017,8(9):6 247-6 256.
[85]Zhao G,Xu G,Qian C,Tang W J.J.Am.Chem.Soc.,2017,139(9):3 360-3 363.
[86]Zhang C,Xu G Q,Zhao W,Li X,Zheng M,Zhou Y,Li J,Li Q.Angew.Chem.,Int.Ed.,2025,64(27):e202 503 359.
[87]Jin J H,Wang H,Yang Z T,Yang W L,Tang W J,Deng W P.Org.Lett.,2018,20(1):104-107.
[88]Ma Z C,Wei L W,Huang Y.Org.Lett.,2023,25(10):1 661-1 666.
[89]Li L,Wang S,Luo P,Wang R,Wang Z,Li X,Deng Y,Peng F,Shao Z.Nat.Commun.,2021,12(1):5 667-5 677.
[90]Wang X Z,Hu X D,Liu W B.Org.Lett.,2025,27(19):5 020-5 026.
[91]Liang S Y,Zhang T Y,Chen Z C,Du W,Chen Y C.Org.Lett.,2024,26(7):1 483-1 488.
[92]Qian C,Tang W J.Org.Lett.,2020,22(11):4 483-4 488.
[93]Kang X,Qian C,Yang H,Shi J,Claverie J,Tang W J.Green Synth.Catal.,2022,3(2):185-189.
[94]Tang W J,Capacci A G,White A,Ma S,Rodríguez S,Qu B,Savoie J,Patel N D,Wei X,Haddad N,Grinberg N,Yee N K,Krishnamurthy D,Senanayake C H.Org.Lett.,2010,12(5):1 104-1 107.
[95]Tang W J,Qu B,Capacci A G,Rodríguez S,Wei X,Haddad N,Narayanan B,Ma S,Grinberg N,Yee N K,Krishnamurthy D,Senanayake C H.Org.Lett.,2010,12(1):176-179.
[96]Li W J,Rodriguez S,Duran A,Sun X,Tang W J,Premasiri A,Wang J,Sidhu K,Patel N D,Savoie J,Qu B,Lee H,Haddad N,Lorenz J C,Nummy L,Hossain A,Yee N,Lu B,Senanayake C H.Org.Process Res.Dev.,2013,17(8):1 061-1 065.
[97]Reeves J T,Tan Z,Reeves D C,Song J J,Han Z S,Xu Y,Tang W J,Yang B S,Razavi H,Harcken C,Kuzmich D,Mahaney P E,Lee H,Busacca C A,Senanayake C H.Org.Process Res.Dev.,2014,18(7):904-911.
[98]Liu G,Liu X,Cai Z,Jiao G,Xu G,Tang W J.Angew.Chem.,Int.Ed.,2013,52(15):4 235-4 238.
[99]Li C,Wan F,Chen Y,Peng H,Tang W J,Yu S,Mcwilliams J C,Mustakis J,Samp L,Maguire R J.Angew.Chem.,Int.Ed.,2019,58(38):13 573-13 583.
[100]Wan F,Wang N,Zhu Y,Tang C,Claverie J,Tang W J.Chem.Commun.,2021,57(45):5 546-5 549.
[101]Han Z S,Xu Y,Fandrick D R,Rodríguez S,Li Z,Qu B,Gonnella N C,Sanyal S,Reeves J T,Ma S,Grinberg N,Haddad N,Krishnamurthy D,Song J J,Yee N K,Pfrengle W,Ostermeier M,Schnaubelt J,Leuter Z,Steigmiller S,Däubler J,Stehle E,Neumann L,Trieselmann T,Tielmann P,Buba A,Hamm R,Koch G,Renner S,Dehli J R,Schmelcher F,Stange C,Mack J,Soyka R,Senanayake C H.Org.Lett.,2014,16(16):4 142-4 145.
[102]Rodríguez S,Qu B,Fandrick K R,Buono F,Haddad N,Xu Y,Herbage M A,Zeng X,Ma S,Grinberg N,Lee H,Han Z S,Yee N K,Senanayake C H.Adv.Synth.Catal.,2014,356(2/3):301-307.
[103]Jiang W,Zhao Q,Tang W J.Chin.J.Chem,2018,36(2):153-156.
[104]Qu B,Samankumara L P,Ma S,Fandrick K R,Desrosiers J N,Rodríguez S,Li Z,Haddad N,Han Z S,Mckellop K,Pennino S,Grinberg N,Gonnella N C,Song J J,Senanayake C H.Angew.Chem.,Int.Ed.,2014,53(52):14 428-14 432.
[105]Qu B,Samankumara L P,Savoie J,Fandrick D R,Haddad N,Wei X,Ma S,Lee H,Rodríguez S,Busacca C A,Yee N K,Song J J,Senanayake C H.J.Org.Chem.,2014,79(3):993-1 000.
[106]Zhang Z,Wang J,Li J,Yang F,Liu G,Tang W J,He W,Fu J J,Shen Y H,Li A,Zhang W D.J.Am.Chem.Soc.,2017,139(15):5 558-5 567.
[107]Li G,Zatolochnaya O V,Wang X J,Rodríguez S,Qu B,Desrosiers J N,Mangunuru H P R,Biswas S,Rivalti D,Karyakarte S D,Sieber J D,Grinberg N,Wu L,Lee H,Haddad N,Fandrick D R,Yee N K,Song J J,Senanayake C H.Org.Lett.,2018,20(7):1 725-1 729.
[108]Chong E,Qu B,Zhang Y,Cannone Z P,Leung J C,Tcyrulnikov S,Nguyen K D,Haddad N,Biswas S,Hou X,Kaczanowska K,Chwalba M,Tracz A,Czarnocki S,Song J J,Kozlowski M C,Senanayake C H.Chem.Sci.,2019,10(15):4 339-4 345.
[109]Huang Y H,Gu Q X,Chao Q C,Xiao H Z,Lu H H.Angew.Chem.,Int.Ed.,2025,64(30):e202 507 638.
[110]Qu B,Mangunuru H P R,Tcyrulnikov S,Rivalti D,Zatolochnaya O V,Kurouski D,Radomkit S,Biswas S,Karyakarte S,Fandrick K R,Sieber J D,Rodríguez S,Desrosiers J N,Haddad N,McKellop K,Pennino S,Lee H,Yee N K,Song J J,Kozlowski M C,Senanayake C H.Org.Lett.,2018,20(5):1 333-1 337.
[111]Qu B,Wei X,Zeng X,Yang B S,Desrosiers J N,Savoie J,Wang J,Marsini M A,Li Z,Haddad N,Lorenz J C,Tielmann P,Maier N,Song J J,Senanayake C H.Org.Process Res.Dev.,2022,26(3):963-975.
[112]Ding Y X,Zhu Z H,Chen M W,Yu C B,Zhou Y G.Angew.Chem.,Int.Ed.,2022, 61(34):e202 205 623.
[113]Wang K,Yu Y J,Wang X Q,Bai Y Q,Chen M W,Zhou Y G.J.Org.Chem.,2022,87(15):10 398-10 407.