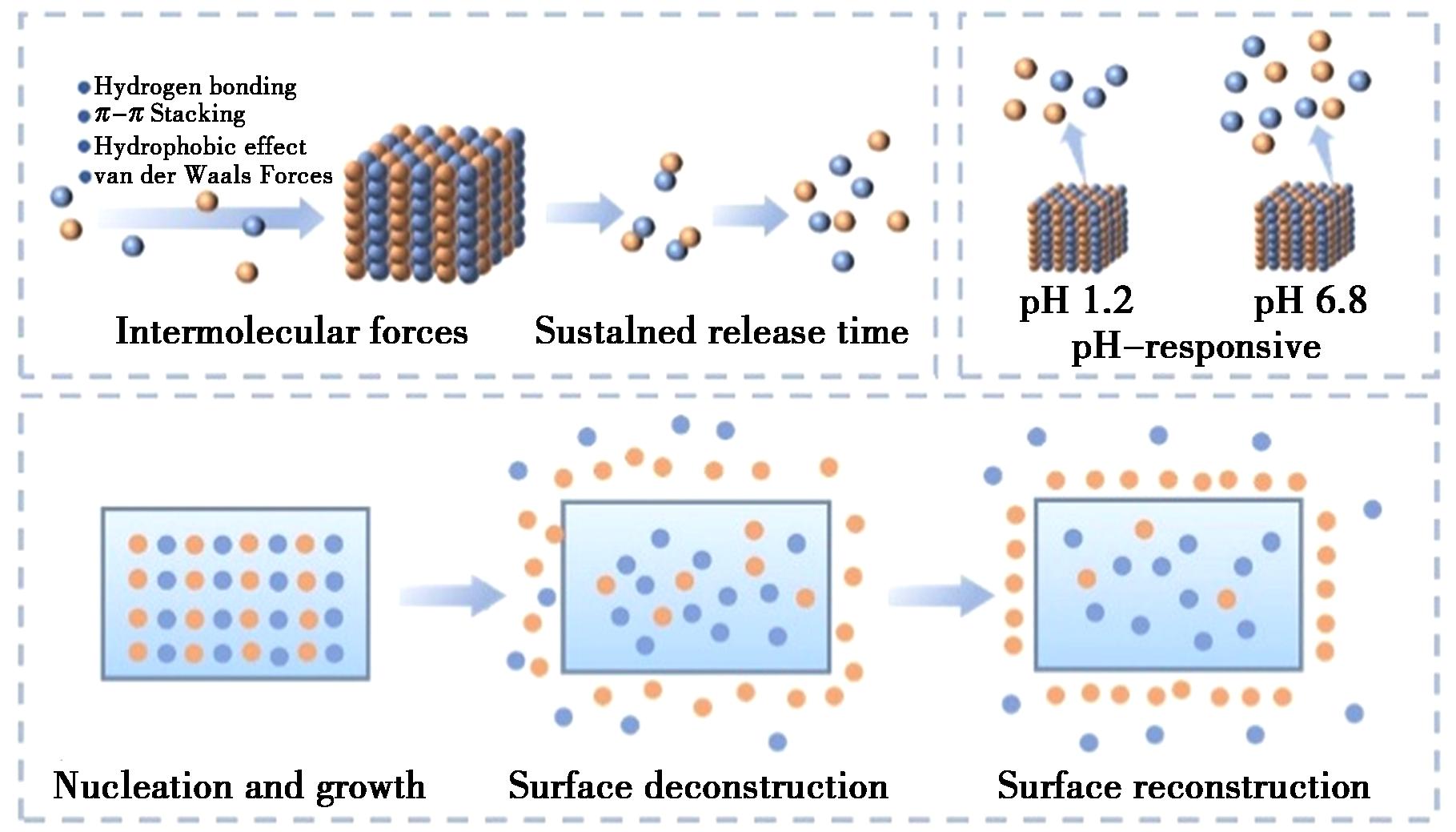
图1 共晶体系缓释机制示意图
Fig.1 Schematic diagram of slow release mechanism of cocrystal system
生化与药用试剂
缓释制剂的设计旨在通过精确控制药物释放速率,使血药浓度在较长时间内维持在治疗窗范围内[1]。这一特性不仅能显著减少给药频率、改善患者用药依从性,还能通过平稳的血药浓度-时间曲线,有效降低因浓度波动引发的局部及全身不良反应[2]。目前实现稳定释药的制剂策略主要包括聚合物基质系统、膜控释系统和渗透泵系统等[3-6]。上述传统技术往往存在载药量低、载体系统稳定性不足等局限性。针对高水溶性药物而言,在避免引入聚合物材料的前提下开发高效缓释剂型,其技术难度显著增加。共结晶技术因其能够通过分子间相互作用精确调控药物的溶解度和溶出性能[7,8],为解决这一难题提供了新思路。
近年来,晶体工程技术作为调控活性药物成分(Active Pharmaceutical Ingredient,API)理化性质的重要手段,可通过改变晶格结构和原子堆积方式,显著改善药物的稳定性、溶解性、吸湿性等关键性质,进而影响固体剂型的治疗效果和制备工艺[9,10]。目前,盐型[11]、多晶型[12]、水合物[13]、溶剂化物[14]和共晶[15]等多种固态修饰策略已被广泛应用于API性质的优化,其中药物共晶技术作为一种重要的缓释策略,在药物研究中得到广泛应用。本文基于晶体工程技术,系统总结了近十年来缓释药物共晶的研究进展,以期为该领域的后续开发提供理论参考和实践指导。
药物共晶是由两种或多种中性分子(其中至少一种为活性药物成分API)通过非共价键相互作用(例如,氢键、范德华和π-π堆积相互作用)以特定化学计量比结合形成的晶态形式[16]。在共晶设计中,超分子合成子(Supramolecular Synthons)发挥着关键作用,其中如羧酸、酰胺和醇等官能团因其优异的分子识别能力,常被用于构建稳定的共晶结构[17,18]。根据分子间作用模式,超分子合成子可分为同合成子(Homosynthons,相同官能团间作用)和异合成子(Heterosynthons,不同官能团间作用)两类[19]。药物共晶技术因其在改善API理化性质方面的独特优势,已成为医药领域和制药工业的研究热点[20-26]。多个共晶药物已获批上市,如用于Ⅱ型糖尿病治疗的Steglatro®(依帕列净-二甲双胍共晶)和心力衰竭治疗药物Entresto®(沙库巴曲-缬沙坦共晶)[27,28]。目前,更多共晶候选药物正处于临床开发阶段,展现出广阔的应用前景。
共晶技术通过分子设计,可构建具有特定释放特性的新型药物固体形式。其缓释性能源于多层次的协同作用机制,主要包括晶体结构调控、溶解平衡调控、释放路径优化及环境响应触发等[29-31]。
在晶体结构调控层面,共晶通过分子间氢键、π-π堆积等非共价相互作用重构晶体结构,形成具有更高稳定性的晶格网络,有效延缓药物分子解离速率,同时共晶配体产生的空间位阻效应可限制药物分子的自由扩散,构建物理缓释屏障。其次,在溶解平衡调控方面,共晶通过优化药物与配体的溶解度匹配性,既抑制高溶解度药物的过饱和倾向,又改善低溶解度药物的溶出性能,可实现协同缓释效果。在动态溶解-再结晶过程中,共晶表面形成的扩散层通过溶出动力学机制精细调控释放速率。在释放路径协同方面,共晶组分在溶出介质中逐步解离形成浓度梯度,实现扩散控制释放。部分共晶还能在体液中发生原位相变,生成低溶解度中间态物质,从而显著延长释放周期。此外,环境响应型共晶可依据生理环境变化智能调节释放行为,如pH敏感型共晶通过配体电离状态改变(如羧酸类配体在肠道pH下的离子化)调控释放特性。
药物共晶通过“结构稳定性增强-溶解动力学调控-扩散路径延长-环境响应触发”的多级联机制,实现对药物释放速率和时间的控制,为开发新型缓释制剂提供理论依据。

图1 共晶体系缓释机制示意图
Fig.1 Schematic diagram of slow release mechanism of cocrystal system
洛铂(Lobaplatin,LBP)是第三代铂类抗肿瘤药物,临床上主要用于治疗慢性转移性乳腺癌、骨髓性白血病和小细胞肺癌。虽然其良好的水溶性使其适合静脉注射给药,但药物在体内的快速水解导致的胃肠道毒性、肾毒性、骨髓抑制和血小板减少等副作用严重限制了其临床应用。共晶溶解度降低至原料药的20%,呈现显著缓释特性(8 h内累积释放率达72%,原料药在2 h完全释放),水解半衰期延长至原药2.3倍,同时黄酮成分的溶解度和生物利用度提升4~6倍。研究发现,LBP与黄酮类化合物形成共晶后,共晶体结构中形成了新的强的异合成子氢键N—H…O/O—H…O,稳定的晶体结构能减缓LBP释放速以及提高药物在溶液中的稳定性。该共晶技术不仅增强了药物胃肠稳定性,还通过缓释作用降低毒性,为开发口服铂类抗癌新剂型提供了新方案[32]。
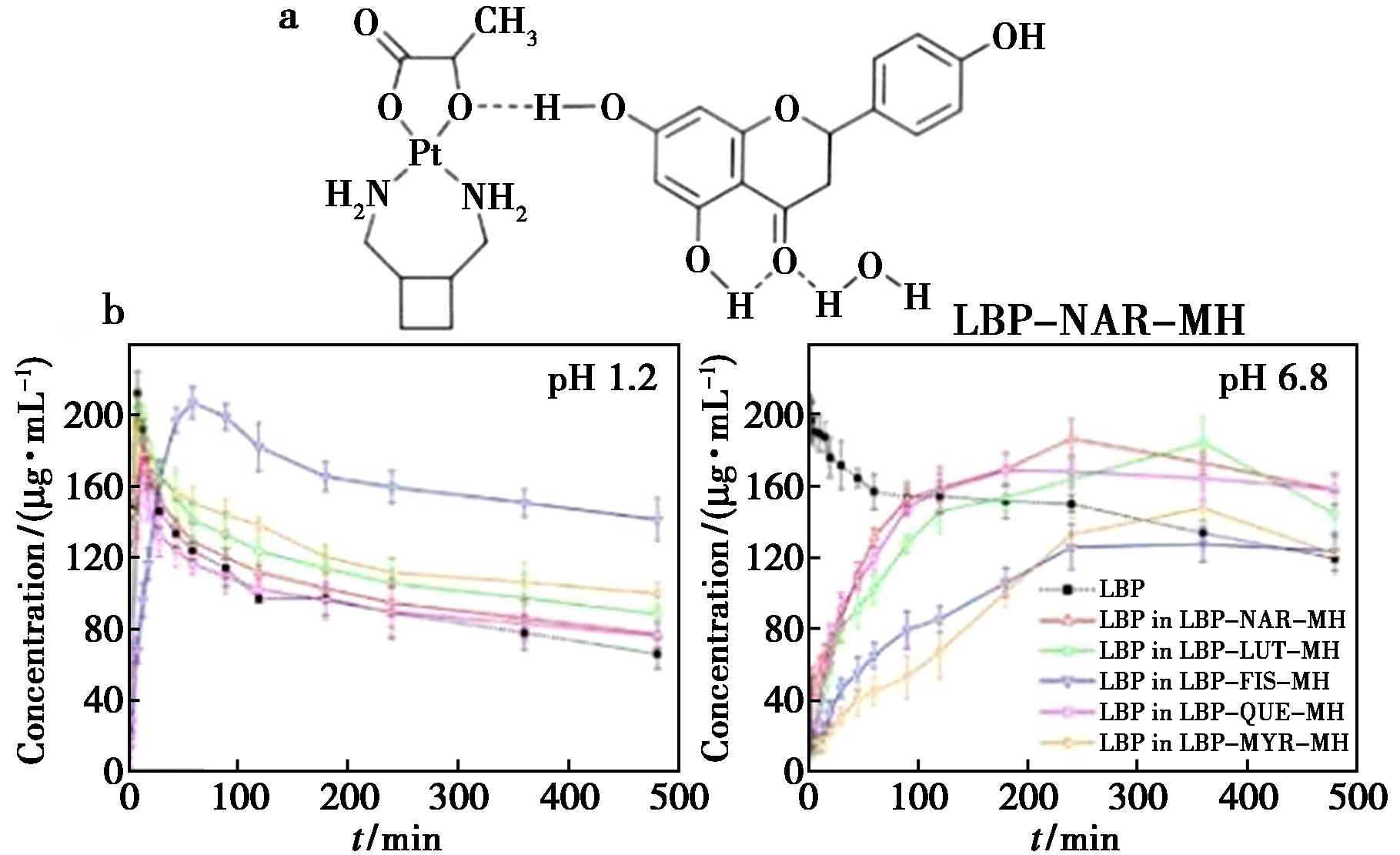
图2 LBP-NAR-MH分子结构(a)和不同pH下LBP溶出曲线(b)
Fig.2 LBP-NAR-MH molecular structure (a) and LBP dissolution curves at different pH values (b)
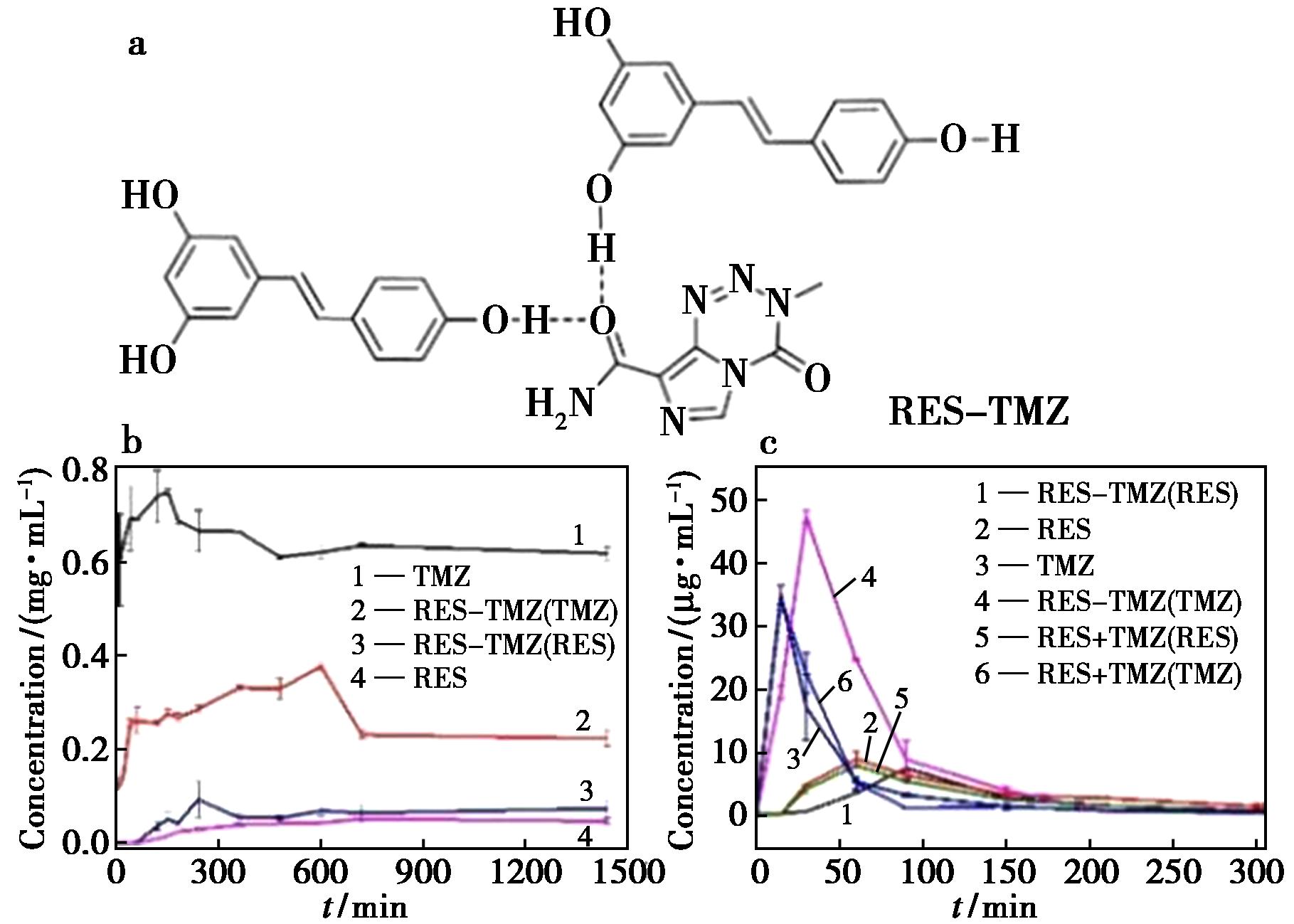
图3 RES-TMZ分子结构(a)、药物溶出(b)和血药浓度-时间曲线(c)
Fig.3 RES-TMZ molecular structure (a) and drug dissolution (b) and blood concentration-time curve (c)
替莫唑胺(Temozolomide,TMZ)是一种脂溶性烷基化抗肿瘤药物,但其临床应用受限于快速消除、稳定性差和口服生物利用度低等问题。通过构建替莫唑胺-白藜芦醇(RES-TMZ)共晶,体外溶出实验显示,RES-TMZ在模拟胃液(pH 1.2缓冲介质)中TMZ呈现缓释特性,大鼠体内生物利用度实验表明共晶中TMZ生物利用度提升1.9倍。RES-TMZ共晶中RES的引入,在结构中形成多重强氢键O—H…O,使得共晶中TMZ释放减缓。更为重要的是,RES的抗氧化和促凋亡特性与TMZ的烷基化作用产生协同增效,增强了对胶质瘤细胞的抑制作用,为TMZ剂型改良提供新策略[33]。
地尔硫卓(Diltiazem,DIL)是一种临床常用的钙离子通道拮抗剂,用于治疗高血压、心绞痛和某些心律失常。目前上市制剂采用其盐酸盐形式(DIL-HCl),易溶于水(565 mg/mL),但存在半衰期短((3.2±1.3)h)的缺陷。研究通过将DIL游离碱与琥珀酸(SUG)、草酸(OXA)和富马酸(FUM)共结晶,成功制备了DIL的3种多组分离子共晶。与DIL-HCl相比,DIL-FUM-H2FUM中DIL的溶解度降低16.5倍,溶出速率减缓13.7倍,展现出显著的缓释特性。DIL-FUM-H2FUM共晶结构中,分子的极性结构域较少暴露在晶体中,这进一步抑制DIL在溶剂中的扩散行为,改变溶解过程中的溶剂化程度,实现DIL的缓释。该共晶不仅证实了通过晶体工程调控药物释放速率的可行性,更为开发长效降压制剂提供了新思路,有望改善需长期用药高血压患者的治疗方案[34]。
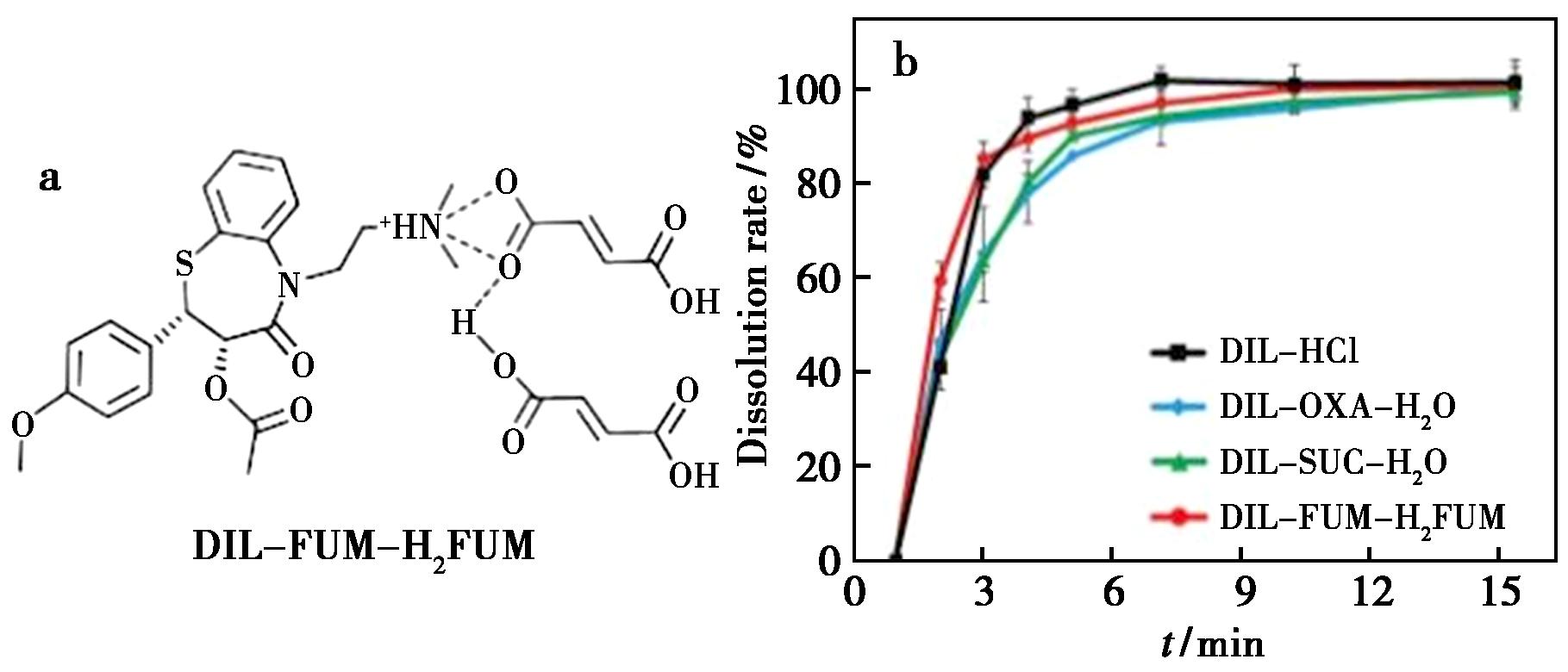
图4 DIL-FUM-H2FUM分子结构(a)和药物DIL溶出曲线(b)
Fig.4 DIL-FUM-H2FUM molecular structure (a) and DIL dissolution curves (b)
尼可地尔(Nicorandil,NCD)作为治疗心绞痛等心血管疾病的钾通道激活剂,其化学性质不稳定(消除半衰期仅50 min),且属于BCS I类药物,易导致血药浓度波动和毒性风险,临床应用面临重大挑战。研究创新性的采用1-羟基-2-萘甲酸(HNA)和水杨酸(SA)分别作为共晶形成物,与NCD成功构建了具有缓释特性的共晶NCD-HNA和NCD-SA。实验表明,NCD-HNA共晶在pH 2.0、4.6和6.8缓冲液中的溶出速率较原料药分别降低22.7、21.6和7.4倍,显著延长了药物作用时间。这是由于NCD共晶的形成重新调整了NCD的堆积方式,改变了原料药NCD的溶解过程,减缓药物的解离释放速率。共晶通过超分子相互作用机制,为同时改善BCS I类药物的稳定性和释放动力学提供了科学依据,对需要长期用药的心血管疾病患者具有重要临床价值[35]。
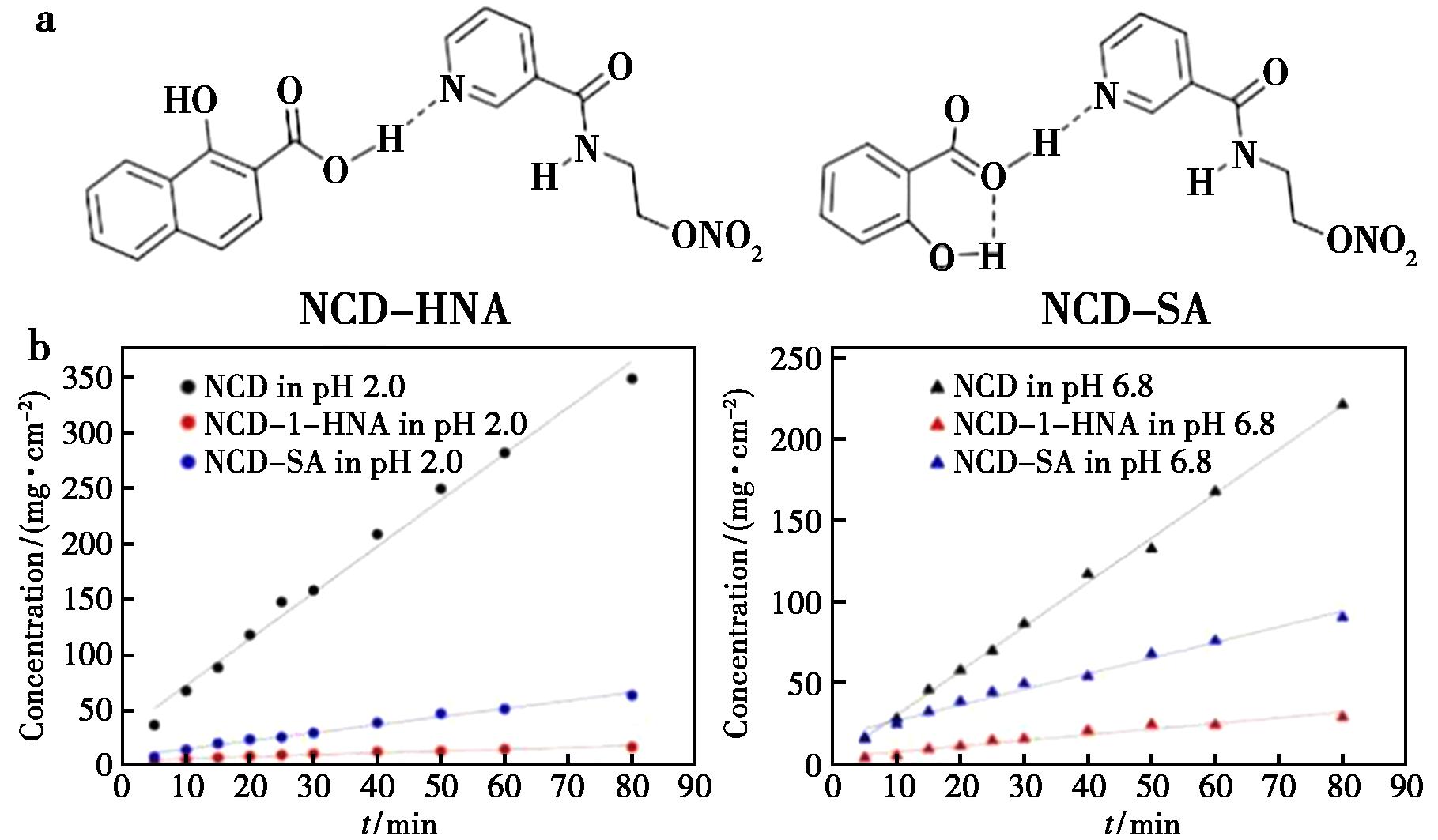
图5 NCD共晶分子结构(a)和不同pH下的NCD溶出曲线(b)
Fig.5 NCD cocrystal molecular structures (a) and NCD dissolution curves at different pH values (b)
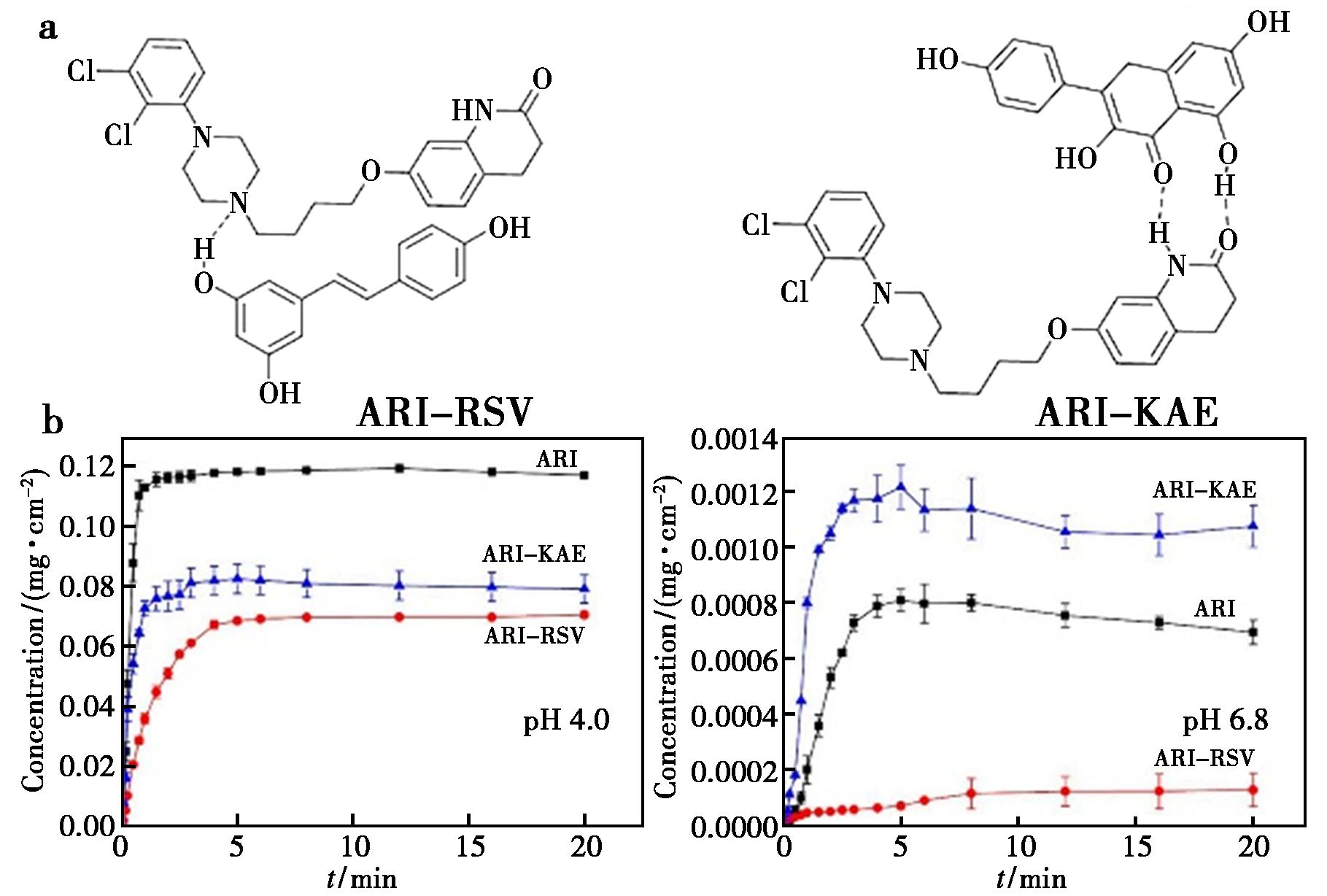
图6 ARI共晶分子结构(a)和不同pH下的ARI溶出曲线(b)
Fig.6 ARI cocrystal molecular structures (a) and ARI dissolution curves at different pH values (b)
阿立哌唑(Aripiprazole,ARI)是第三代非典型抗精神病药物,其长效注射剂存在明显的肌肉刺激性问题。阿立哌唑分别与具有抗炎作用的白藜芦醇(RSV)和山奈酚(KAE)形成ARI-RSV和ARI-KAE共晶,在pH 4.0醋酸盐缓冲液中,ARI-RSV和ARI-KAE共晶使ARI的溶出速显著降低,由于共晶抑制了ARI的过饱和倾向。ARI的溶出度具有pH值依赖性,在pH 6.8的磷酸盐缓冲液中,ARI溶出度减小,由于ARI和RSV在磷酸盐缓冲液中相互溶解抑制作用,RSV在ARI-RSV中的溶解也受到了明显的抑制。更有意义的是,RSV和KAE固有的抗炎特性与共晶技术协同作用,不仅有效缓解了注射部位刺激反应,还通过晶体工程精确调控了药物释放行为。该研究为开发兼具良好耐受性和可控释放特性的长效抗精神病制剂提供了创新解决方案[36]。
唑尼沙胺(Zonisamide,ZNS)作为磺酰胺类抗癫痫药物,口服后约2~4 h完全吸收,其临床应用面临半衰期波动(63~69 h)的挑战。研究通过构建ZNS-咖啡因(CAF)和ZNS-L-脯氨酸(LP)共晶体系,成功实现了药物释放特性的调控。实验结果显示,两种共晶均表现出比原料药更低的溶解度和溶出速率,这主要归因于ZNS分子与共形成物CAF和LP形成强的分子间相互作用。CAF和LP对溶剂化位点的阻断,ZNS和共形成物之间的分子间相互作用可能超过溶剂化效应,导致溶解速率较慢。该发现为开发具有稳定半衰期的ZNS缓释制剂提供了新思路,有望改善抗癫痫治疗稳定性和可靠性[37]。
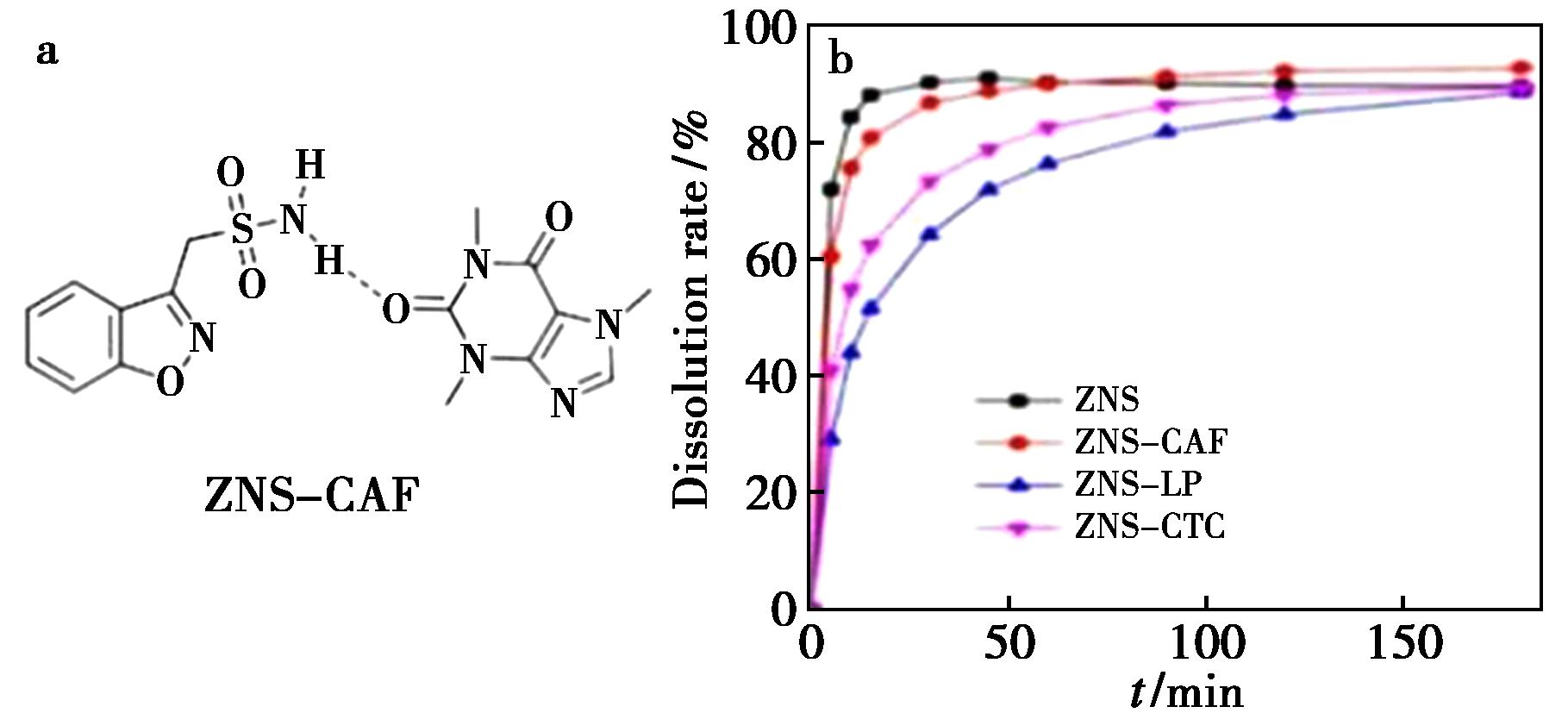
图7 ZNS-CAF分子结构(a)和不同ZNS共晶的药物溶出曲线(b)
Fig.7 ZNS-CAF Molecular structure (a) and dissolution curves of different ZNS cocrystals (b)
异烟肼(Isoniazid,INH)作为结核病一线治疗药物,长期大剂量使用会导致的肝毒性、耐药性及患者依从性差等问题。研究通过构建异烟肼-姜黄素INH-CUR共晶体系。在模拟胃液环境(pH 1.2)中,该共晶表现出显著的缓释效果:15 min内仅释放28%,而物理混合物同期已完全释放。这是由于难溶性CUR的沉淀可能包覆了未溶解的INH-CUR共晶体颗粒表面。此外由于CUR在pH 1.2环境下更稳定,该包覆层延长了INH的释放周期,实现INH的缓释。INH-CUR共晶显著降低INH的药物溶出速率,不仅可降低给药频率、提高用药灵活性,更重要的是通过维持稳定的血药浓度,有望同时解决毒性、耐药和依从性问题。该研究为结核病的长效治疗方案开发提供了新思路[38]。
研究发现阿魏酸哌嗪(Piperazine Ferulate,PRZ-FLA)的血浆半衰期较短(仅27 min),因此必须每日3次口服给药才能维持治疗性血药浓度,导致血药浓度波动显著并影响患者依从性。阿魏酸哌嗪-吡嗪酰胺双药三元共晶PRZ-FLA-PRA,展现出两大优势,通过降低45%溶解度和1.8倍溶出速率,有效延长药物作用时间并实现抗结核与肾脏保护的双重药理协同。缓释的机制是由于共晶中的紧密堆积,这在其溶解度降低中起到了作用,而且紧密的网络结构使得PRZ-FLA的溶剂化位点在很大程度上减少,控制释放的速率。该共晶体系不仅解决了PRZ-FLA的药代动力学缺陷,更开创了结核病合并肾损伤的联合治疗新方案[39]。
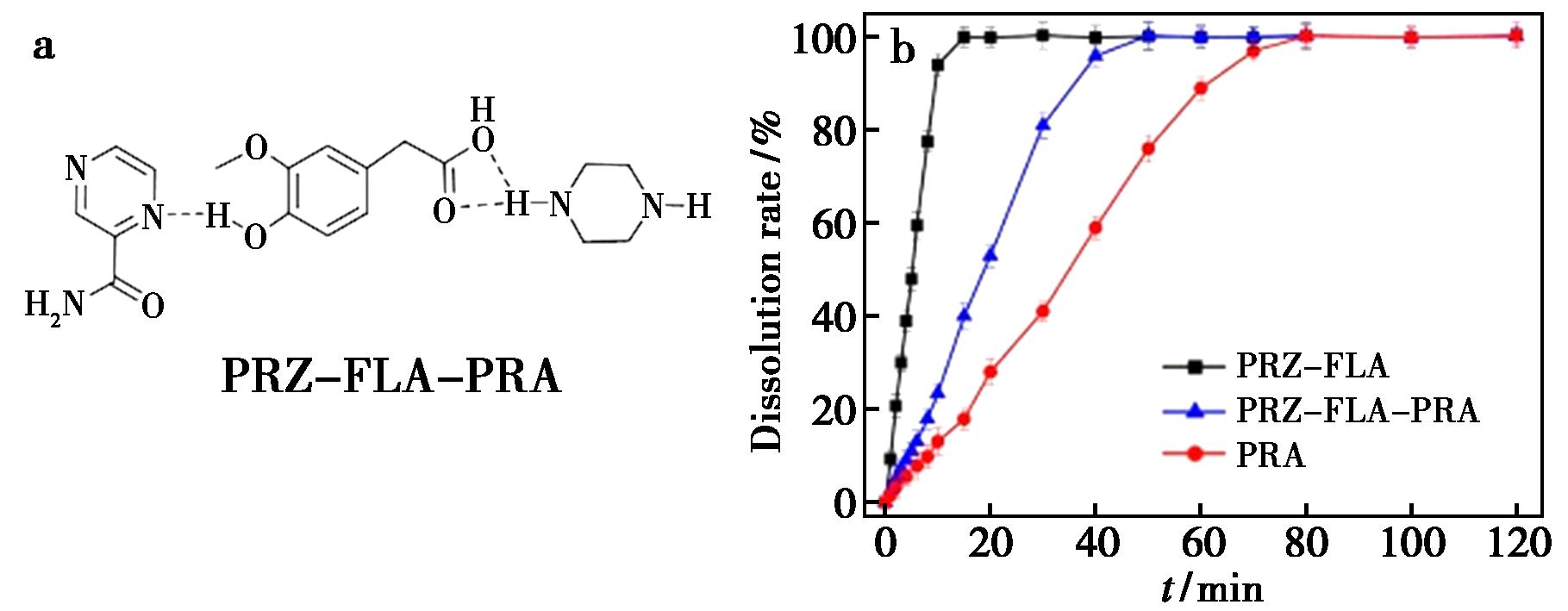
图8 PRZ-FLA-PRA分子结构(a)和药物溶出曲线(b)
Fig.8 PRZ-FLA-PRA molecular structure (a) and PRA dissolution curves (b)
吡非尼酮(Pirfenidone,PFD)是一种用于治疗特发性肺纤维化的口服药物,其快速吸收和短半衰期导致生物利用度低且需高剂量给药,引发严重副作用。PFD分别通过与橙皮素(HES)和染料木黄酮(GEN)共结晶,得到PFD-HES和PFD-GEN共晶,具有显著降低的PFD溶解度和溶出速率。在pH 1.2介质中,两种共晶中PFD的释放速率分别降低了93%和98%,且在pH 6.8介质中同样保持优异缓释特性。溶解度的降低和缓释作用源于共晶中引入了难溶性的类黄酮分子,有增强分子间相互作用的共晶结构,共同实现PFD的缓释。该研究成果不仅解决了高溶解度药物的快速释放难题,更通过延长药物作用时间,有望将给药剂量降低40%~60%,从而显著改善患者耐受性,为肺纤维化治疗提供了更优的用药选择[40]。
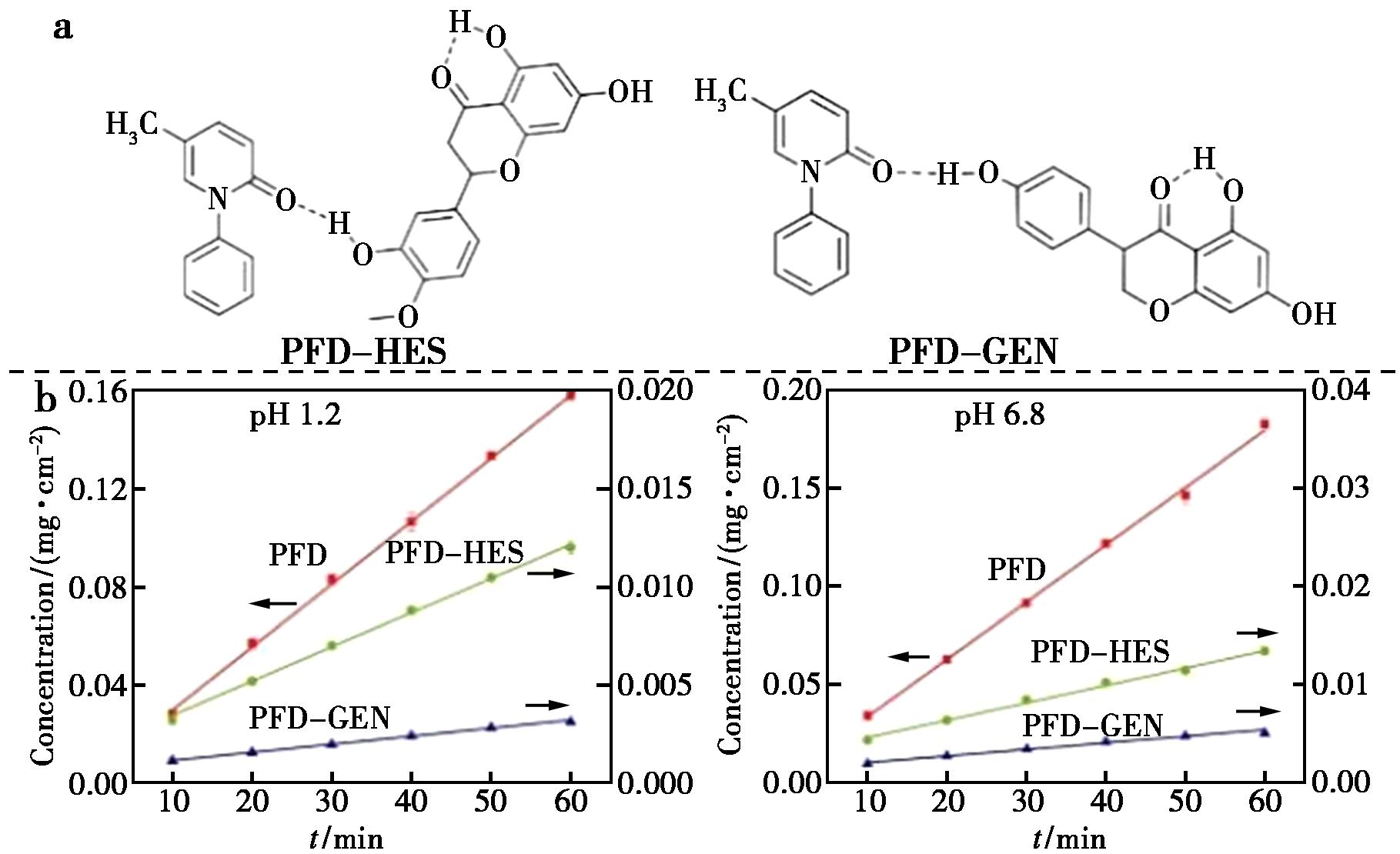
图9 PFD共晶分子结构(a)和不同pH下的PFD溶出曲线(b)
Fig.9 PFD cocrystal molecular structures (a) and PFD dissolution curves at different pH values (b)
利巴韦林(Ribavirin,RBV)是一种水溶性的广谱抗病毒药物,但其血药浓度的峰谷波动和一些不良反应严重限制了其应用。研究成功制备了RBV与3,5-二羟基苯甲酸(DHBA)、没食子酸(GA)和巴比妥酸(BA)共晶。体外溶出实验表明,在模拟肠道pH 6.8的缓冲溶液中,与RBV相比,共晶中药物的释放速率降低,且释放行为可通过不同共晶配方的选择实现精准调控。缓释的机制是由于在共晶体晶格中加入溶解度较小的共形成物,水合物的形成会降低其水溶性,晶体堆积排列延长溶出过程,也将有助于其降低的释放速率。共晶技术为优化RBV的药代动力学特性提供了新思路,有望通过维持稳定的血药浓度来降低不良反应发生率,从而改善抗病毒治疗的临床效果[41]。
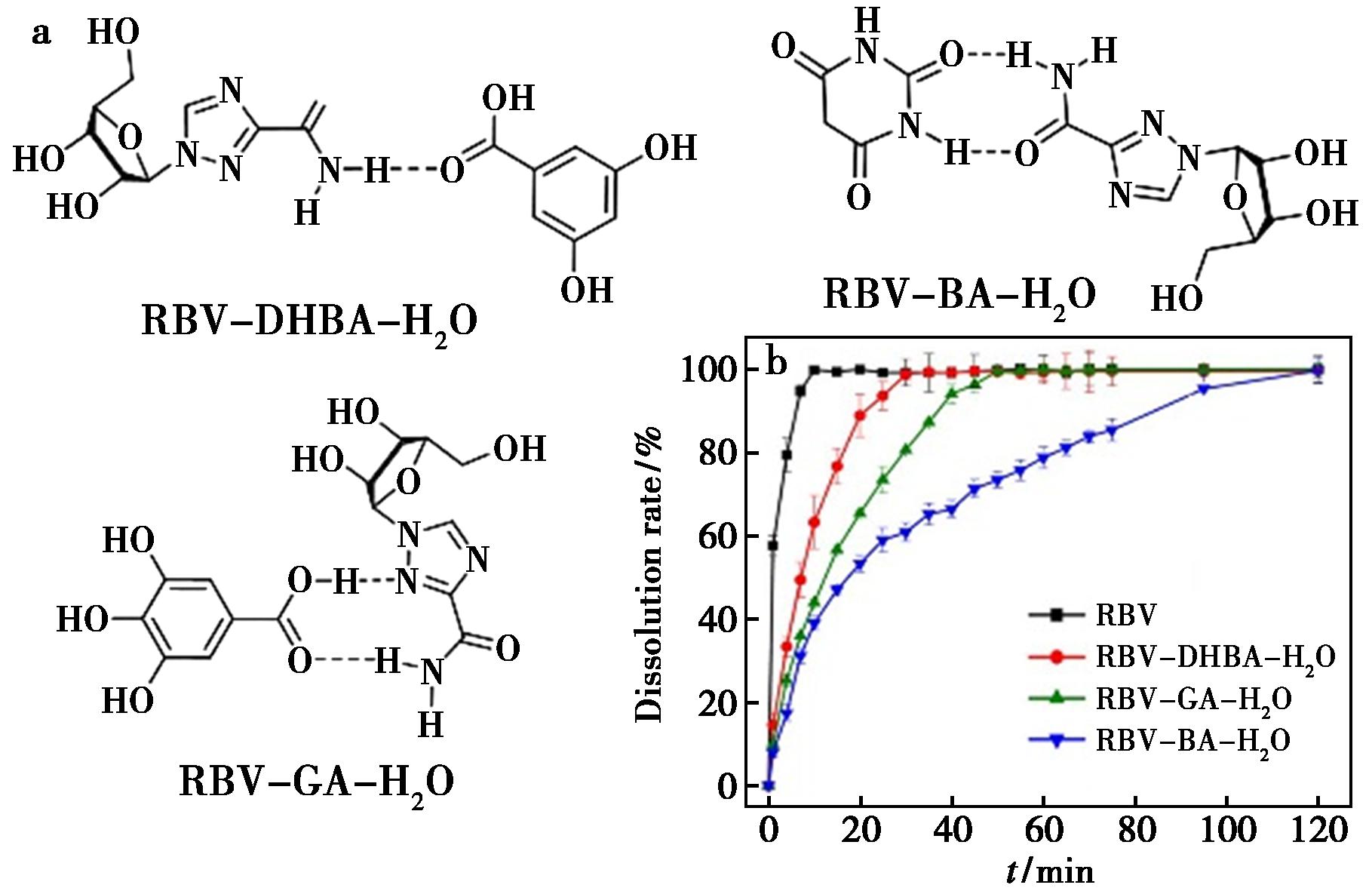
图10 RBV共晶分子结构(a)和药物溶出曲线(b)
Fig.10 RBV cocrystal molecular structures (a) and RBV dissolution curves (b)
丙基硫氧嘧啶(Propylthiouracil,PTU)作为甲亢一线药物,其快速释放导致的肝毒性问题亟待解决。研究发现了4种新的PTU分别与肉桂酸(CA)、龙胆酸(GA)、鞣花酸(EA)和山奈酚(KA)构建共晶体。所有共晶在加速储存条件(40 ℃和75% RH)下在12周内显示出优异的稳定性。此外,共晶均表现出溶解度降低和固有溶出速率(IDR)减慢。其中,PTU-KA共晶显示出最好的性能。在pH 1.2和6.8缓冲液中,PTU的溶解度分别下降了77.3%和85.2%。缓释效果可以归因于通过共结晶引入适当的CCF,使得晶格能和分子相互作用的增强,延长释放过程。共晶技术通过显著延缓药物释放,有效降低了肝毒性风险,为PTU的安全应用提供了创新解决方案[42]。
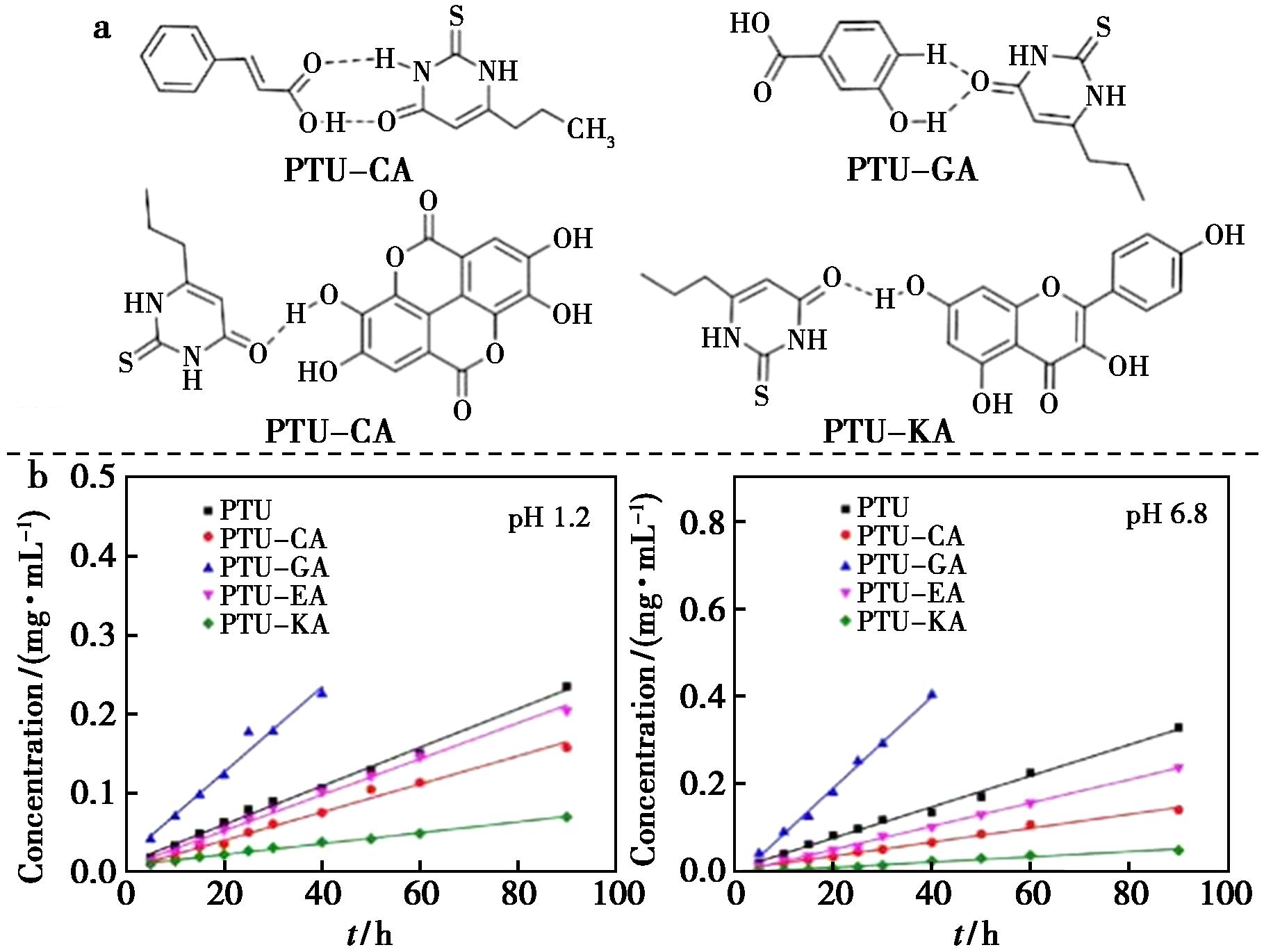
图11 PTU共晶分子结构(a)和不同pH下的PTU溶出曲线(b)
Fig.11 PTU cocrystal molecular structures (a) and PTU dissolution curves at different pH values (b)
烟酰胺单核苷酸(Nicotinamide Mononucleotide,NMN)作为具有抗衰老作用的辅酶I(NAD+)前体,其应用受限于体内快速释放、在胃环境下易降解及低生物利用度。通过构建烟酰胺单核苷酸-没食子酸(NMN-GA)共晶,该共晶体系在pH 1.2的介质中,展现出良好的缓释特性,缓释的机制是由于水合物的形成和晶体堆积产生氢键网络减缓NMN的释放速率。该共晶体系通过没食子酸的抗氧化作用与NMN的NAD+合成功能产生协同增效。这一发现为开发具有多靶点协同作用的抗衰老制剂提供了新思路,同时证实共晶技术可有效调控水溶性差异药物的协同递送[43]。
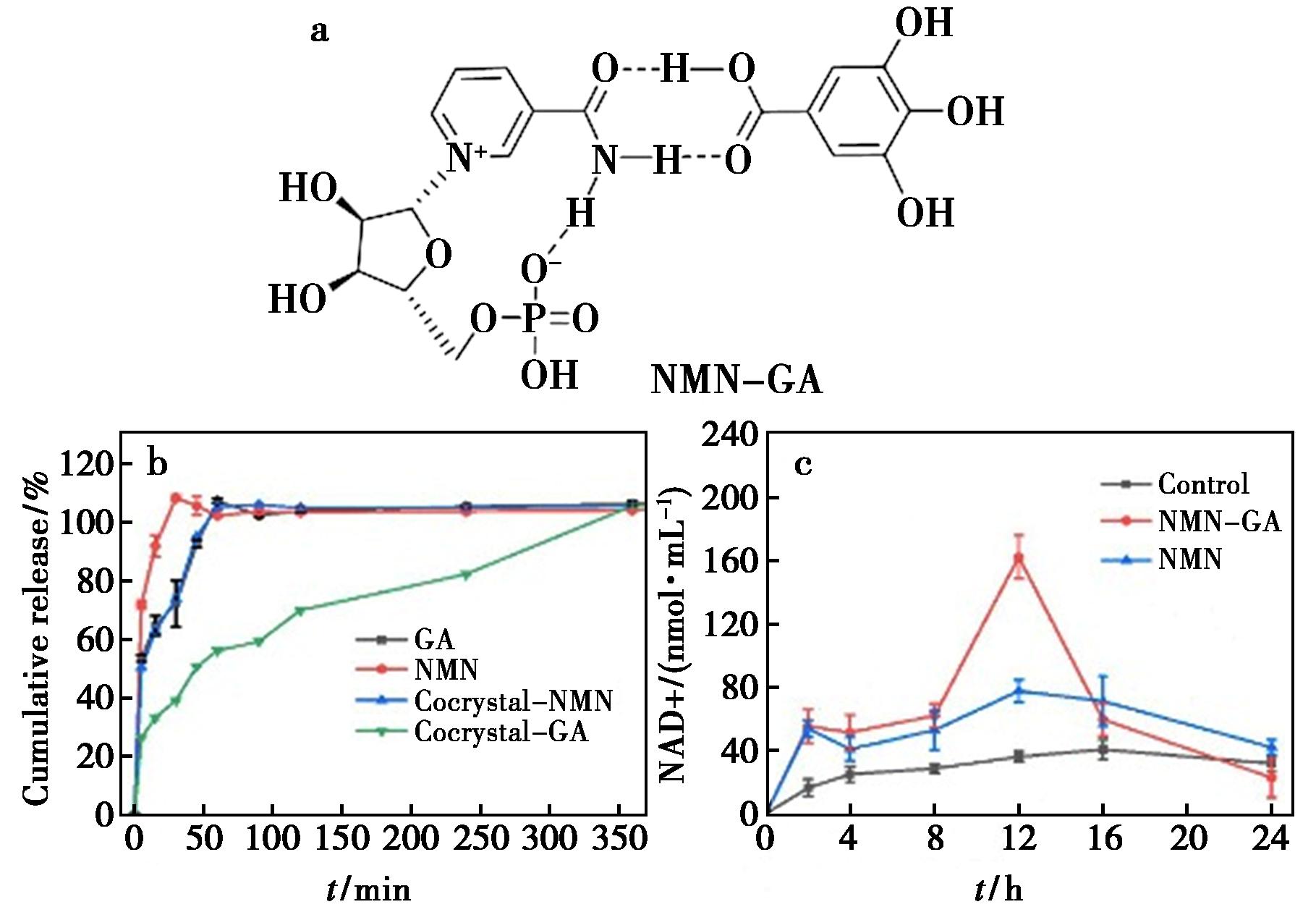
图12 NMN-GA分子结构(a)、药物溶出曲线(b)和NAD+浓度-时间曲线(c)
Fig.12 NMN-GA molecular structure (a),drug dissolution curve (b) and NAD+ concentration time curve (c)
盐酸巴马汀(Palmatine Hydrochloride,PCl)是一种天然异喹啉生物碱,具有多种药理作用,如抗氧化、抗癌、广谱抗菌和抗病毒。目前,该化合物已被开发为可溶性抗菌药物,但其氯化物形式的药物研究应用仍较为有限。研究成功获得了盐酸巴马汀与橙皮素(HES)形成的两种不同的共晶晶型,实验表明,PCl·3H2O在5 min内几乎完全溶解。相比之下,30 min时晶型Ⅰ和晶型Ⅱ分别仅释放出32%和47%的PCl,共晶的溶出均在12 h后达平台期。研究表明,显著降低了PCl溶解度,但HES的溶解性能却得到改善。PCl从两种共晶中的持续释放可能归因于两组分在晶格中的强相互作用,形成稳定晶体结构。在纯水体系中,两种共晶多晶型物均能实现盐酸巴马汀的缓释效应和橙皮素的增溶效果[44]。
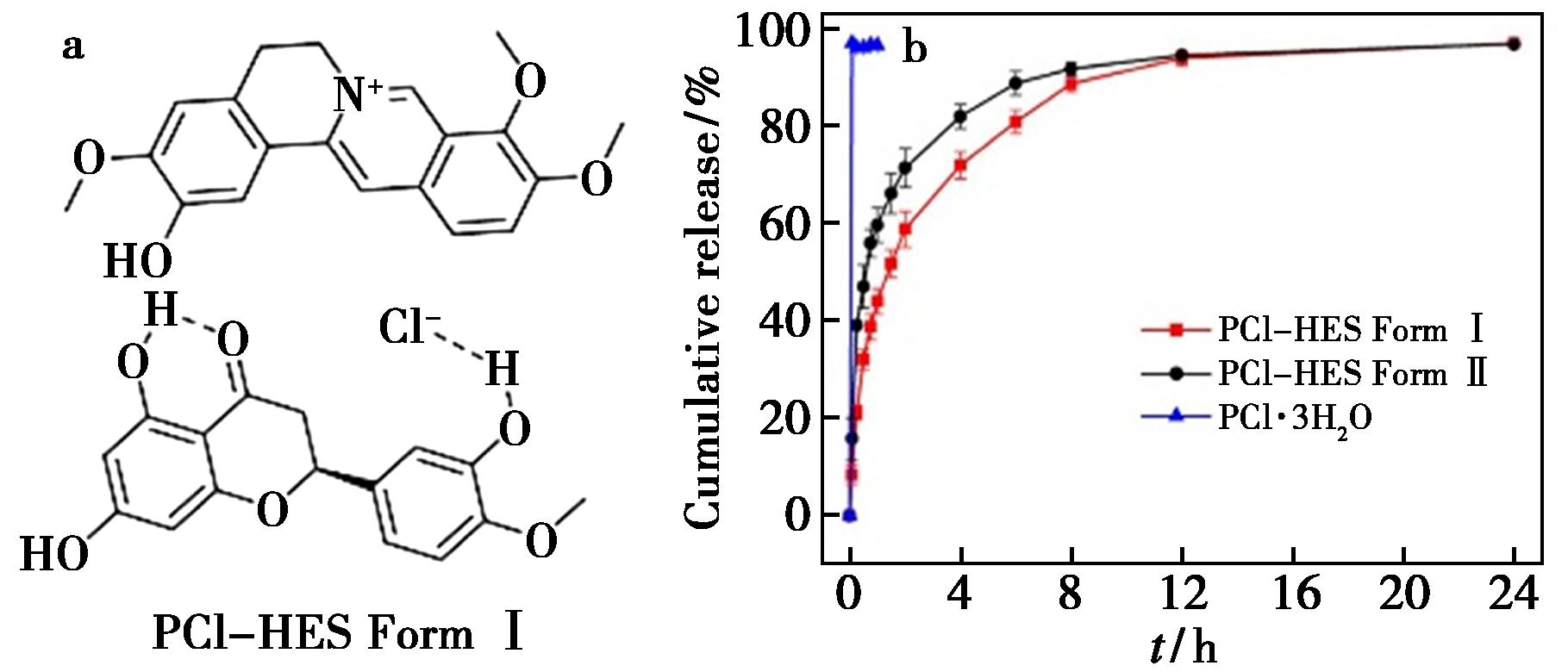
图13 PCl-HES共晶分子结构(a)和PCl的溶出曲线(b)
Fig.13 PCl-HES cocrystal molecular structure (a) and PCl drug dissolution curves (c)
二氢杨梅素(Dihydromyricetin,DMY)可通过共晶策略增强化疗药物的抗肿瘤活性。己酮可可碱(Pentoxifylline,PTX)由于其本身具有高水溶性和快速吸收特性,PTX通常被制成缓释片剂。在溶出实验中,DMY和PTX在纯水和HCl溶液中均能迅速溶解。在形成共晶后,实现了长达12 h的DMY和PTX的持续且同步的释放,己酮可可碱的平衡溶解度显著下降,而二氢杨梅素的溶解度则略有提升,两种原料药几乎同时释放,该机制通过优化药物与CCF的溶解度匹配性,既抑制高溶解度药物的过饱和倾向,又改善低溶解度药物的溶出性能,可实现协同缓释效果。这是由于研究结果表明,共晶技术可调控多组分药物的释放动力学,实现疗效与药代特性的同步优化,为开发具有协同抗肿瘤作用的复合缓释制剂提供了创新解决方案[45]。
苯草隆(Metamitron,MET)是一种用于控制甜菜田禾本科杂草和阔叶杂草的高水溶性除草剂,其环境迁移性对水生生态系统构成严重威胁。研究通过构建MET-柚皮素(NA)和MET-黄芩素(BA)共晶体系,实现了突破性的缓释效果:两种共晶分别使MET的溶出率降低98.3%和96.3%,溶解度下降95.5%和96.2%。缓释效果可以归因于通过共结晶由适当的CCF引入的增强的晶格能和分子相互作用。共晶技术通过黄酮类化合物的分子调控作用,在不影响除草活性的前提下,将MET的环境风险降低近20倍,为开发高效环保的新型农用化学品提供了创新解决方案[46]。
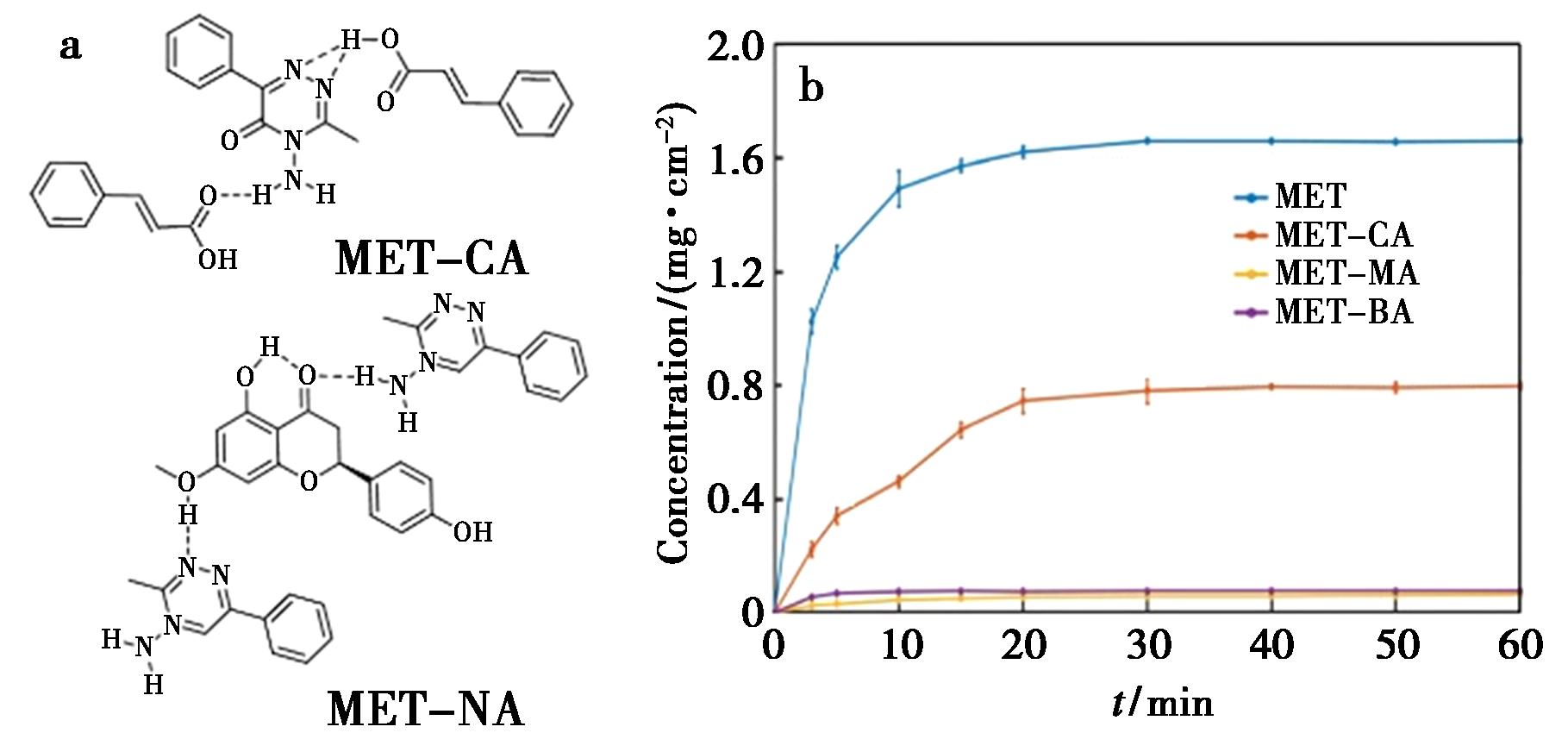
图14 MET共晶分子结构(a)和药物溶出曲线(b)
Fig.14 MET cocrystal molecular structures (a) and drug dissolution curves (b)
药物共晶技术作为一种创新的缓释制剂策略,通过独特的晶体工程学设计,在不依赖高分子聚合物的条件下即可实现药物的长效释放。该技术在减少给药频率、提高患者依从性以及血浆波动较小而达到稳态血药浓度而减轻副作用方面展现出显著优势,尤其适用于需要长期维持最佳血药浓度的治疗需求。未来该领域的研究应聚焦于共晶微观结构与释放性能的构效关系解析、新型功能化共晶材料开发、体外释放评价方法标准化、以及规模化制备工艺优化与质量控制体系建立。随着晶体工程学与现代药剂学的交叉融合,药物共晶技术有望突破传统缓释制剂的局限,为新型给药系统开发提供创新思路。后续研究应当聚焦于共晶材料的理性分子设计、制备工艺的标准化以及质量评价体系的建立,以加速该技术的产业化进程和临床应用转化。
[1]Wang S,Liu R H,Fu Y,John K W.Expert Opinion Drug Delivery,2020,17(9):1 289-1 304.
[2]Addanki A,Krishnaphanisri P,Swapna L,Mabrur H M,Siddhardha A.World J.Biol.Pharm.Health Sci.,2023,3(3):221-233.
[3]Li X M,Tang J H,Guo W W,Dong X,Gao K S,Tang F S.Gels,2025,11(3):190.
[4]Tran T,Tran P.Pharmaceutics,2019,11(6):290.
[5]Wang J J,Ni Q K,Wang Y F,Zhang Y X,He H Y,Gao D W,Ma X W,Liang X J.J.Control.Release.,2021,331(10):282-295.
[6]Maincent J,Williams R O.Drug Deliv.Transl.Res.,2018,15(16):1 714-1 725.
[7]Guo M S,Sun X J,Chen J H,Cai T.Acta Pharm.Sin.B,2021,11(8):2 537-2 564.
[8]Cerreia V P,Chierotti M R,Gobetto R G.Adv.Drug Deliver.Rev.,2017,117:86-110.
[9]Wang X J,Du S Z,Zhang R,Jia X D.Asian.J.Pharm.Sci.,2021,16(3):307-317.
[10]Li J H,Wang X H,Yu D H,Zhoujin Y P,Wang K L.Int.J.Pharm.,2023,648:123 555.
[11]Masataka I,Yuriko I,Hiroyasu I,Kyu H,Taku M,Hidemasa H,Isao A,Hironori S,Shuji N.Cryst.Growth Des.,2023,23(9):6 298-6 307.
[12]Ma K,Wang N N,Cheng L F,Wei Y F,Zhang J J,Gao Y,Qian S.Int.J.Pharm.,2019,566:361-370.
[13]Rai S K,Baidya D,Nangia A K.Cryst.Eng.Comm.,2021,35(23):5 994-6 011.
[14]Shota T,Chie U I,Kyu H,Hironori S,Masataka I,Shuji N.Chem.Pharm.Bull.,2023,71(8):633-640.
[15]Xu J,Shi Q,Wang Y N,Wang Y,Xin J B,Cheng J,Li F.Molecules,2023,28(2):613.
[16]Geetha B,Bipul S,Ashwini K.Chem.Rev.,2022,122(13):11 514-11 603.
[17]Roshni J,Karthick T.J.Mol.Struct.,2025,1 321(2):139 868.
[18]Anisha C,Ankita S,Govind P S,Partha P B.J.Pharm.Pharmacol,2024,76(1):1-12.
[19]Guan D,Xuan B,Wang C,Long R T,Jiang Y Q,Map L N,Kang J B,Wang J W,Chow S F,Zhou Q.Pharmaceutics,2021,13(12):2160.
[20]Khushi R,Indrani M,Srushtiti M,Pankaj K S.Rug.Discov.Today,2024,29(7):104 050.
[21]Iashia T R,Ayesha K,Hafiza F R,Abbeha M,Muhammad A,Muhammad S K,Ali R,Sumera S,Zureesha S,Muhammad F K,Rana A T,Sheikh A S.Recent Pat.Anti-Canc,2023,18(3):e130 922 208 782.
[22]Utsav G,Yasser A.RSC Med.Chem.,2021,12(5):705-721.
[23]Srinivasulu A,Geetha B.Mol.Pharmaceutics,2024,21(7):3 121-3 143.
[24]Wang Z M,Shang H Z,Gao L H,Oiao N.Curr.Drug.Deliv.,2023,20(10):6 399-6 408.
[25]Jidnyasa P,Niraj K,Sopan N,Swati P,Shweta P,Namdeo J.J.Drug Deliv.Sci.Tec.,2025,104:106-112.
[26]André L C S N,Richard P F,Maxime D C,Joop H H,Fl vio J C,Marlus C.Particuology,2021,58:227-241.
vio J C,Marlus C.Particuology,2021,58:227-241.
[27]Fala L.Am.Health.Drug Benefits,2015,8(6):78-82.
[28]Cavanagh K L,Kuminek G,Rodríguez-hornedo N.Mol.Pharmaceutics.,2020,17(11):4 286-4 301.
[29]Tatiane C M,Gislaine K,Simone G C,Naír R H.Eur.J.Pharm.Sci.,2020,152:105 422.
[30]Shi K,Li M.Pharm.Res.,2023,40:2 051-2 069.
[31]Cao Y X,Qu H B,Wan X X,Guo S Z,Li K L,Wu S G,Gong J B.Chem.Eng.J.,2025,506:160 288.
[32]Yin H M,Xie J Y,Jiang J Y,Hong M H,Zhu B,Ren G B,Qi M H.Cryst.Growth Des.,2022,22(4):2 602-2 610.
[33]CN111423444B.Chen Q,Lin N,Ma X Q,Liu S L.2024-05-28.
CN111423444B.陈清,林宁,马晓琴,刘水丽.2024-05-28.
[34]Luan F D,Chris H J,Franco D F,Larissa S M,Paulo S C,Mateus A C S,Naialy F A R.Int.J.Pharm.,2021,605(10):120 790.
[35]Guo C Y,Zhang Q,Zhu B Q,Zhang Z Y,Bao J J,Ding Q C,Ren G B,Mei X F.Cryst.Growth Des.,2020,20(10):6 995-7 005.
[36]Liu W,Ma R,Liang F,Duan C X,Zhang G S,Chen Y,Hao C.Molecules,2021,26(9):2 414.
[37]Srinivasulu A,Joseph C,Chow P S.Cryst.Eng.Comm.,2018,20(21):2 923-2 931.
[38]Xuan B F,Wong S N,Zhang Y J,Weng Z W,Tong H L,Wang C G,Sun C Q,Chow S F.Cryst.Growth Des.,2020,20(3):1 951-1 960.
[39]Yu X Z,Wang L Y,Liu F,Li Y T,Wu Z Y,Yang C W.Cryst.Growth Des.,2020,20(3):2 064-2 073.
[40]Meng L S,Li D X,Zhu Y J,Wang J M,Deng J W,Zhang H L.Cryst.Eng.Comm.,2023,25(36):5 133-5 140.
[41]Chen J M,Li S,Lu T B.Cryst.Growth Des.,2014,14(12):6 299-6 408.
[42]Xiao Y T,Zhong L,Hao H X.Cryst.Growth Des.,2021,21(2):1 202-1 217.
[43]CN119823203A.Chen Q,Lin N,Zhang S,Chen L.2025-04-15.
CN119823203A.陈清,林宁,张顺,陈玲.2025-04-15.
[44]Zhang Y J,Li Y G,Liu L,Guo Q H,Sa R J,Zhang M,Lou B Y.Cryst.Growth Des.,2022,22(2):1 073-1 082.
[45]Liu L,Li Y G,Zhang M,Zhang Y J,Lou B Y.J.Pharm.Sci.,2021,111(1):82-87.
[46]Xiao Y T,Wu C H,Zhou L,Yin Q X,Yang J X.Green Chem.,2022,24(20):8 088-8 099.