图1 Cd-CPs对各类抗生素的检测
Fig.1 Detection of various antibiotics by Cd-CPs
功能材料
编者按:荧光检测技术因具有操作简便、响应快速、灵敏度高和时空分辨率出色等优势,在环境监测、食品安全、医学诊断及生物成像等领域展现出巨大的应用潜力,已成为前沿交叉研究的热点。
为集中展示该领域的最新进展,本期策划了荧光检测专题,收录的4篇研究论文从不同维度展现了本技术的广度与深度,内容涵盖镉配合物荧光传感检测抗生素的研究进展、苯并吡喃酮荧光探针检测Zn2+、Zn/U异核铀酰MOF的构筑与荧光传感性能,以及吩噻嗪席夫碱荧光探针的合成与其在ClO-生物成像中的应用。
近年来,国内外各类水体中频繁检出的新污染物(例如抗生素、氨基酸等)引起了公众的担忧。这些污染物具有环境持久性或潜在的健康风险,极有可能成为未来的污染管控对象,因此探究这些污染物的检测方法是目前的紧迫任务[1,2]。《中华人民共和国水污染防治法》鼓励大家保护和改善环境,防治水污染,保护水生态,保障饮用水安全,维护公众健康,推进生态文明建设,促进经济社会可持续发展[3]。抗生素是与人类活动密切相关的典型的新污染物,它们被频繁使用并进入环境,导致其对生态环境和人体健康造成潜在危害[4-6]。因此,开发具备卓越稳定性与高检测灵敏度的材料,将其应用于水溶液中抗生素的分析工作,已成为一项刻不容缓且充满巨大挑战的课题。目前检测抗生素的方法包括酶免疫分析法[7,8]、色谱-串联质谱法[9,10]、离子迁移谱法[11,12]和表面增强拉曼光谱法等[13,14]。然而,这些方法需要复杂的样品预处理和昂贵的检测设备。相比之下,荧光传感技术由于其低成本、实时观测、高灵敏度和操作简单而引起了人们的极大兴趣[15-20]。
抗生素(Antibiotics)是一类天然或人工合成的化学物质,具有抑制或杀灭其他微生物、治疗人类和动植物病害的功能。目前已经发现或合成了上万种抗生素,按照用途可以分为青霉素类、四环素类、头孢菌类、喹诺酮类、大环内酯类等[21,22]。
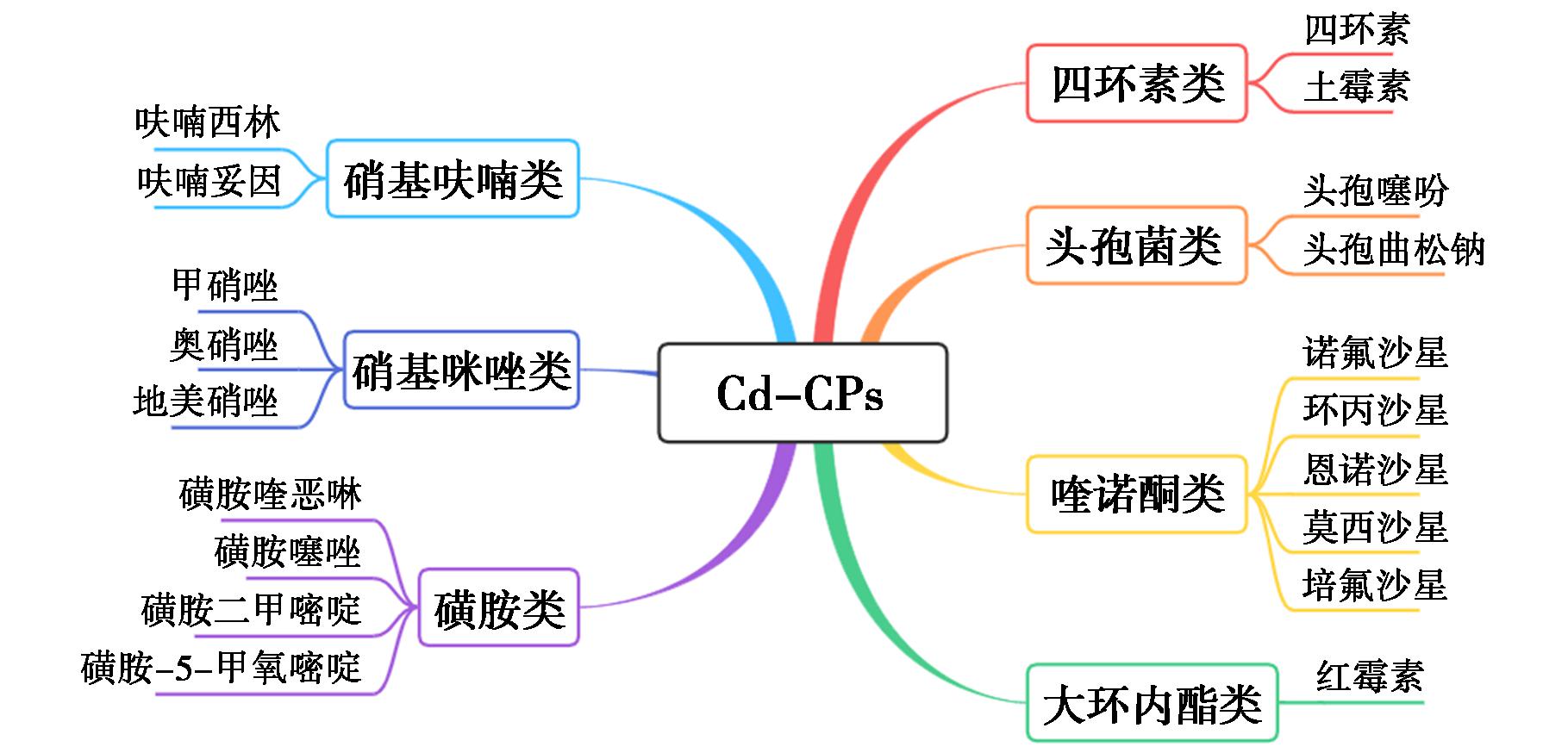
在公众健康与环境保护意识不断增强的今天,对污水中抗生素、农药、有机物、离子等痕量污染物进行快速、准确的分析,对于我国生态文明建设与可持续发展有着重大意义。因此,本文简述了近几年镉配合物(Cd-CPs)对各类抗生素的检测研究进展(图1)。

图1 Cd-CPs对各类抗生素的检测
Fig.1 Detection of various antibiotics by Cd-CPs
镉离子(Cd2+)的配位数通常为4、5、6、7,甚至更高,几何构型具体取决于配体的空间位阻和电子效应。常见的配位数和几何构型包括:1)四面体构型(4配位):配体排斥最小,常见于空间位阻较大的配体或阴离子环境(例如:[CdCl4]2-、[Cd(CN)4]2-、[Cd(NH3)4]2+)[23];2)八面体(6配位):最稳定的配位数之一,Cd2+离子半径(97 pm)与6配位环境的“离子半径比”(0.414~0.732)匹配(例如:[Cd(NH3)6]2+、[Cd(H2O)6]2+)[24];3)更高配位数(7/8配位):需大体积、低电荷配体(如冠醚、羧酸根),或溶剂分子辅助,减少配体间空间排斥;常见于“高配位需求”的组装反应、多齿配体(如EDTA、大环席夫碱)或MOFs(金属-有机框架)中[25]。
镉配合物的设计需结合镉离子的化学性质(如价态、配位偏好等)及目标功能需求,以下是核心设计策略。
1.2.1 配体选择
1.2.1.1 配位原子类型
合成镉配合物的配位原子主要来自配体中的电负性较强、易提供孤对电子的非金属元素,常用的配位原子有O、N、S,可根据需求选择含这些原子的配体(如羧酸类、胺类、硫醚类)。
1.2.1.2 配体结构
单齿配体主要起封端作用或辅助配位,较少单独用于构筑扩展结构。多齿配体(如EDTA、联吡啶)可增强配合物稳定性,减少解离。柔性配体(如长链羧酸)利于形成多变结构,刚性配体(如芳香族配体)可构建规整框架(如MOFs)。
1.2.1.3 功能化配体
引入荧光基团(Cd2+为d10电子构型,本身无d-d跃迁发光,但通过引入含共轭π体系或杂原子(N、O、S)发光基团的配体);引入活性位点前体(Cd配合物的催化活性需通过配体引入活性位点前体(如羟基、氨基、吡啶环)或协同作用基团(如羧基、膦酸基),利用Cd2+ Lewis酸性(接受电子对)与配体功能基团的协同作用,实现对特定反应的催化;引入其他配体,赋予配合物特定功能如吸附功能、生物功能等(图2)。
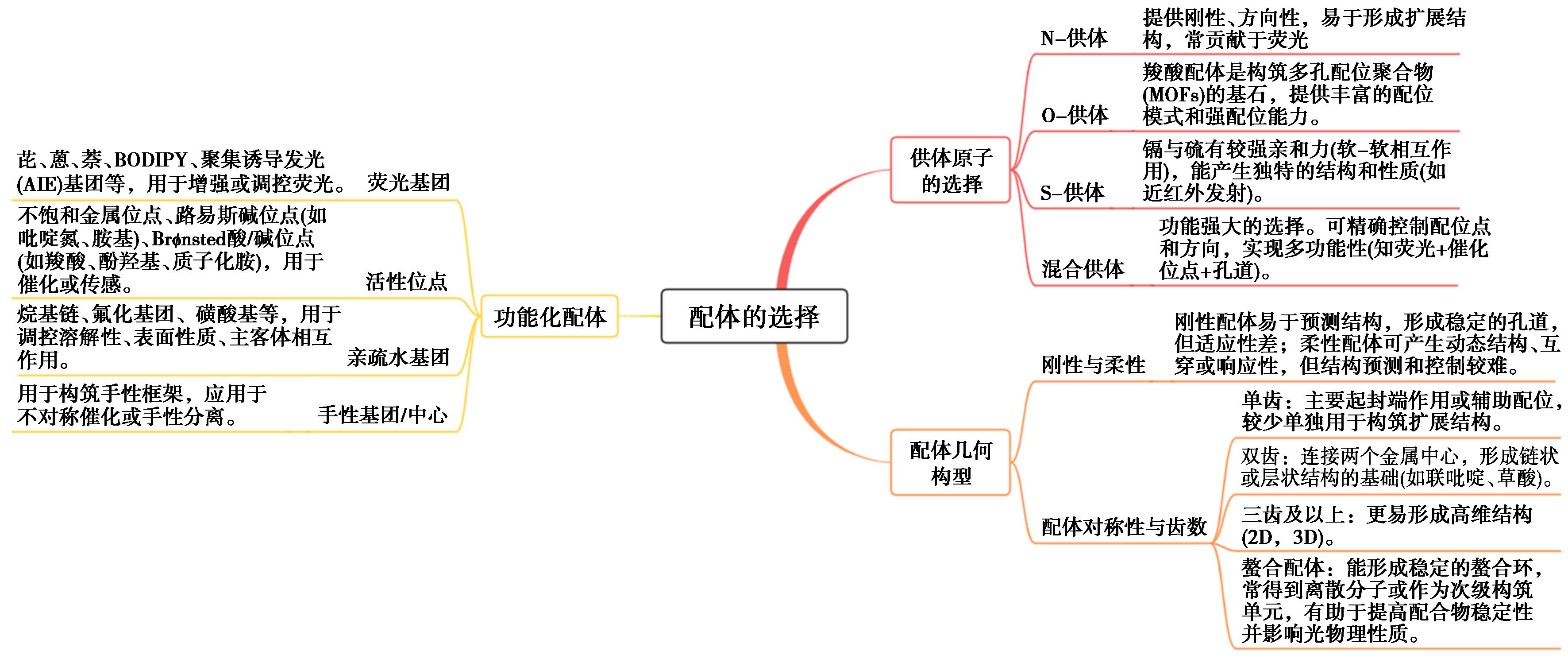
图2 设计合成镉配合物的配体选择
Fig.2 Ligand selection for designing and synthesizing cadmium coordination polymers
1.2.2 反应条件调控
1.2.2.1 pH
pH影响配体解离度和镉离子存在形态(如碱性条件可能生成氢氧化物沉淀)。
1.2.2.2 温度
低温(室温-60 ℃):反应速率慢,易形成动力学稳定的产物(如低结晶度的配合物、简单单核配合物);高温(80~180 ℃,水热/溶剂热条件):提高反应活性,促进配体与Cd2+的充分配位,易形成热力学稳定的产物(如高结晶度的MOFs、多维聚合结构);极端高温(>200 ℃):可能导致配体分解或配合物框架坍塌,需根据配体热稳定性(如羧酸配体耐温性高于席夫碱配体)选择温度。
1.2.2.3 模板剂使用
加入离子或分子模板,诱导特定结构(如多孔框架)形成。例如:阳离子型模板试剂![]() [Co(en)3]3+);阴离子型模板试剂
[Co(en)3]3+);阴离子型模板试剂![]() 中性分子模板试剂(H2O、吡啶、CO2)。
中性分子模板试剂(H2O、吡啶、CO2)。
四环素类抗生素(Tetracyclines)在医疗、农业和食品生产中的广泛应用,对人类社会和生态环境产生了多方面的深远影响,既有积极作用,也存在潜在风险。常见的四环素类抗生素有:四环素(Tetracycline,TC)、多西环素(Doxycycline,DOX)、米诺环素(Minocycline,MINO)、土霉素(Oxytetracycline,OTC)、金霉素(Chlortetracycline,CTC)等。大量研究数据显示,镉配合物在识别四环素类的相关报道数量最多。
2024年,Kang等[26]成功合成一种利用吡唑功能化的四苯基乙烯配体(Py-TPE)和Cd2+组成的新型镉基金属-有机框架[Cd3(Py-TPE)2(H2O)2(NO3)2]n(化合物1),具有一个新的(3,3,3,6,6,8)连接的拓扑网络,该配合物在水溶液中对TC具有极高的灵敏性和专一的选择性(图3)。
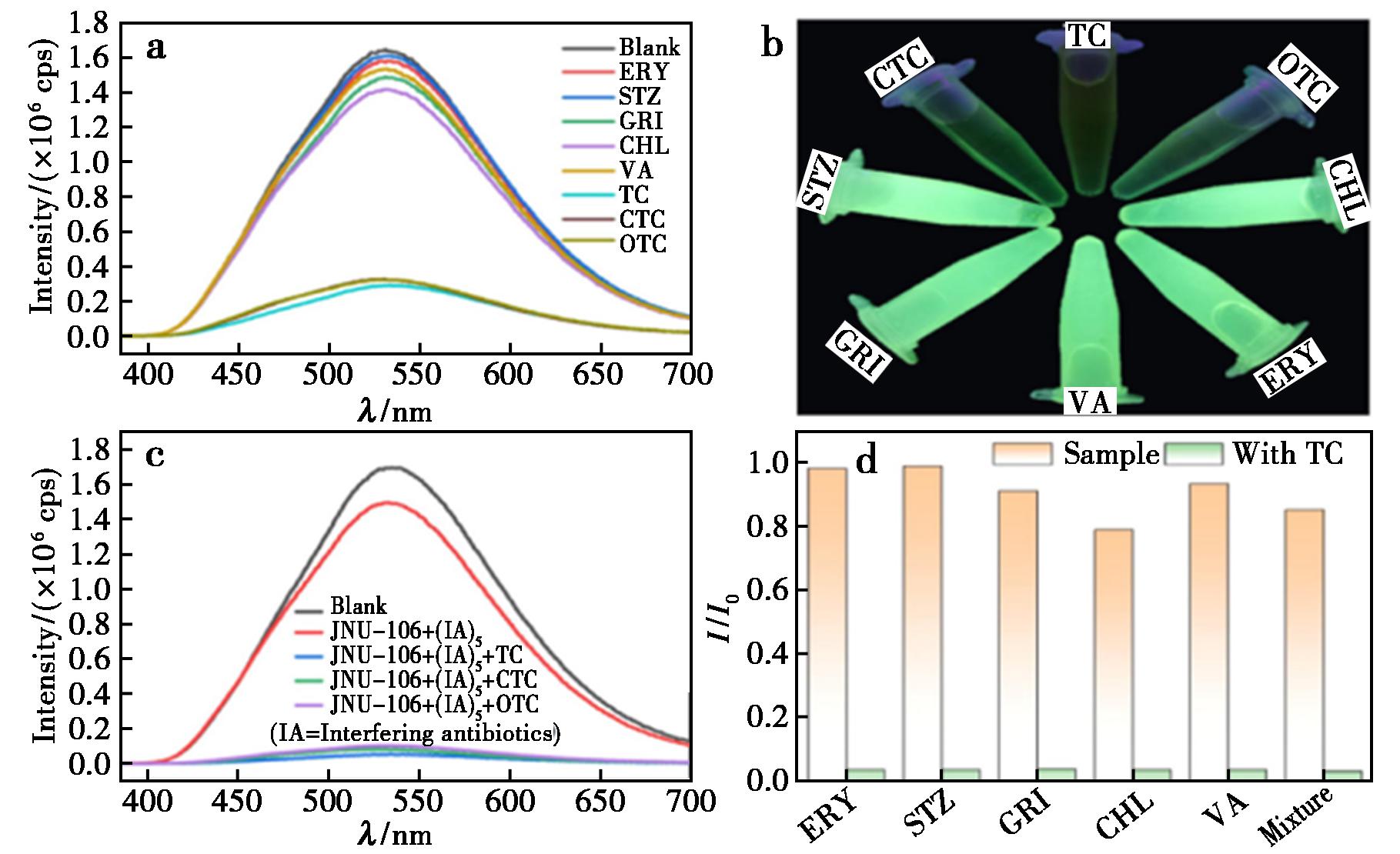
a.化合物1在不同抗生素中的荧光光谱;b.化合物1在紫外光下,对不同抗生素水悬浮液的发光程度照片;c.化合物1在干扰抗生素存在下的荧光强度以及进一步加入TC、CTC或OTC后的荧光强度;d.加入干扰抗生素和TC后化合物1的发光强度对比
图3 化合物1对TC的传感选择性[26]
Fig.3 Sensing selectivity of compound 1 for TC[26]
2023年,Sun等[27]在溶剂热条件下,合成了一种新型Cd配位聚合物[Cd(bbimc)(ata)]n(化合物2)。单晶结构测定表明化合物2具有sql拓扑的二维(2D)结构。化合物2表现出良好的热稳定性(413 ℃开始分解)和优异的酸碱稳定性(pH 1~13,水溶液)。此外,化合物2可以通过关断效应高选择性和高灵敏度地检测水溶液中的四环素和金霉素。2025年,Wu等[28]在溶剂热条件下,利用两个官能团(羧基和咪唑基)的组合优势,合成了一个新的镉基配位聚合物[CdL·3H2O]n(化合物3)。研究表明,化合物3可以通过“turn-off”效应在水溶液中高选择性和高灵敏度地检测TC和CTC,并且在荧光检测中也表现出较高的效率。2024年,Li等[29]利用Cd2+离子与刚性配体1-(3,4-二羧基苯基)-4-羟基吡啶(H2L)成功合成了一个二维配位聚合物,即[Cd(L)]n(化合物4)。在该配合物中,每个镉离子呈现六配位模式,并形成具有(6,3)Ia型拓扑结构的二维网状结构。此外,配合物良好的稳定性和优异的荧光性能使其成为水溶液中识别环丙沙星和土霉素的优异荧光传感器,具有较低的检测限(环丙沙星0.28 μmol/L,土霉素36.5 μmol/L)。
头孢菌素类抗生素(Cephalosporins)是临床上广泛使用的β-内酰胺类抗生素,对人类健康的影响既有重要的治疗作用,也可能伴随一些副作用和潜在风险。常见的头孢菌素类抗生素有:头孢唑林(Cefazolin,CZO)、头孢呋辛(Cefuroxime,CXM)、头孢曲松钠(Ceftriaxone Sodium,CRO)、头孢噻吩(Cefalotin,CET)等。
2024年,Zhang等[30]采用溶剂热法合成了两种新型的Cd-MOFs,即Cd2(pycz)4(H2O)2(HCl)2(化合物5)和[Cd(dpycz)3H2O]·H2O(化合物6)。荧光传感研究表明,化合物5可以灵敏地检测较低浓度的CRO,化合物6对TC表现出荧光猝灭。化合物5和化合物6作为荧光探针为检测水溶液中的有害物质提供了一种新的策略。
2024年,Wang等[31]用1-(4-羧基苯基)-1H-吡唑-3-羧酸(H2L)作配体,制备了一种发光的二维(2D)金属有机框架CdLH2O(化合物7)。化合物7可以通过荧光增强响应特异性识别水环境中的头孢噻吩(CET),其荧光强度与CET的浓度之间(0~50 μmol/L)具有良好的线性关系,线性荧光增强斜率KEC值为5.475 0×104 M-1,检测限(LOD)为165 nmol/L。并验证了其对CET识别的快速响应、良好的选择性、抗干扰能力和可重复使用性。
喹诺酮类抗生素(Quinolones)是一类人工合成的广谱抗菌药,广泛用于治疗多种细菌感染。常见的喹诺酮类抗生素有:诺氟沙星(Norfloxacin,NOR)、环丙沙星(Ciprofloxacin,CIP)、恩诺沙星(Enrofloxacin,ENR)、莫西沙星(Moxifloxacin,MXF)、培氟沙星(Pefloxacin,PEF)等。
2024年,Zhao等[32]成功得到了一个新型镉基金属-有机框架,即[Cd0.5L0.5(BA)(H2O)]n(化合物8)。该化合物可作为多功能荧光探针对恩诺沙星和环丙沙星进行高选择性和高灵敏度的检测。2022年,Wu等[33]采用水热法合成了2个 Cd(Ⅱ)配位聚合物[Cd(TDC)(L)]n(化合物9)和{[Cd(TCPA)(L)]·H2O}n(化合物10)。化合物9和化合物10在较宽的pH范围(2~13)内具有良好的化学稳定性。两种Cd(Ⅱ)-CP均可作为高效的发光探针,用于检测水体中的NOR。2024年,Fan等[34]成功合成了3个新的Cd(Ⅱ)配位聚合物,即[Cd(DCTP)(L)(OH)]n(化合物11)、[Cd(TBTA)(L)(OH)]n(化合物12)和[Cd(NPHT)(L)(H2O)]n(化合物13)。3种CPs对培氟沙星(PEF)的传感具有高灵敏度、高选择性和良好的抗干扰性等优点,具有较高的稳定性和优异的发光性能。
大环内酯类抗生素(Macrolides)是一类广泛应用于医疗领域的抗生素,常见的大环内酯类抗生素有红霉素(Erythromycin,ERY)、阿奇霉素(Azithromycin,AZM)、克拉霉素(Clarithromycin,CLR)等,它们对人类生活的影响既有积极的治疗作用,也存在潜在的挑战。目前,对大环内酯类抗生素检测被报道相对较少。
2024年,Liu等[35]采用水热法合成了3个Cd(Ⅱ)配合物[Cd(dbim)(p-phda)]n(化合物14)、[Cd(dbim)1.5(suc)]n(化合物15)、[Cd(dbim)0.5(m-bdc)(2H2O)]n(化合物16)。其中配合物16呈现链状结构,链上有未配位的Lewis碱性O供体。研究表明,化合物16能在水溶液中高选择性和高灵敏度地检测ERY。
硝基呋喃类(Nitrofurans)是一类人工合成的抗菌药物,常见的有呋喃妥因(Nitrofurantoin,NFT)、呋喃唑酮(Furazolidone,FZD)、呋喃西林(Nitrofurazone,NFZ)等。它们曾广泛用于人类医疗、畜牧业和水产养殖,但由于潜在的致癌性和耐药性问题,许多国家已严格限制其使用。
2024年,Wu等[36]合成了一种新的基于d10构型的Cd(Ⅱ)配位聚合物[Cd2(CH3-COO)2(bimb)2]·2ClO4(化合物17),用于光降解抗生素,特别是对NFT具有较低的检测限和较高的降解效率。传感实验表明,化合物17可选择性检测硝基呋喃妥因,检测限为0.025 μmol/L,而CP化合物17作为光催化剂时,在20 min的时间跨度内可将NFT光降解高达91.83%。
2023年,Meng等[37]合成了一种新型的基于邻菲罗啉的金属-有机笼[Cd3L3·6MeOH·6H2O](化合物18)。根据单晶X-射线衍射,笼子化合物18表现出罕见的三叶形结构。同时,离散的MOC通过丰富的分子间C—H…O相互作用进一步堆叠成3D多孔超分子结构。此外,通过对水溶液中抗生素的荧光传感探索,实验结果表明,化合物18对硝基呋喃和硝基咪唑类抗生素具有优异的荧光传感能力。化合物18对分析物的传感能力在5个循环中保持不变(图4)。
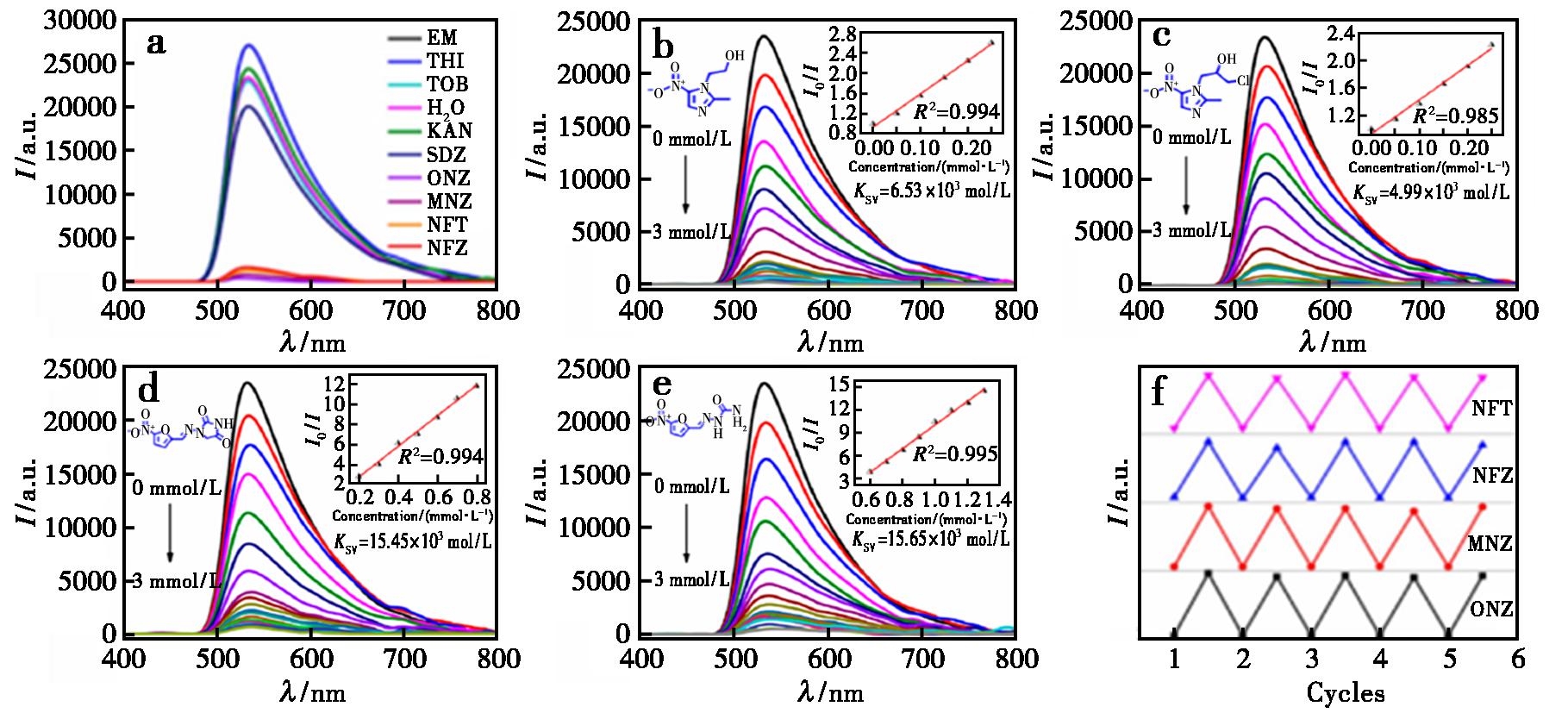
a.化合物18对不同抗生素的荧光光谱;b.化合物18对MNZ的荧光滴定实验;c.化合物18对ONZ的荧光滴定光谱;d.化合物18对NFT的荧光滴定光谱;e.化合物18对NFZ的荧光滴定光谱;f.加入NFT、NFZ、MNZ和ONZ后化合物18的循环稳定性
图4 化合物18对对硝基呋喃和硝基咪唑类抗生素的传感选择性、滴定实验和循环测试[37]
Fig.4 Sensing selectivity,titration experiment and cycle test of compound 18 towards p-nitrofuran and nitroimidazole antibiotics[37]
2020年,Feng等[38]合成了一个新的二维(2D)镉基金属有机框架[Cd2(HDDB)(bimpy)(NMP)(H2O)]·3H2O(化合物19),该框架具有良好的水稳定性、pH稳定性和优异的光致发光性能。由于光诱导电子转移(PET)和荧光共振能量转移(FRET),配合物19对硝基呋喃/硝基咪唑类抗生素和DCN农药表现出荧光猝灭行为。2025年,Fang等[39]合成了3个新型的Cd基MOFs荧光传感器[Cd1.5(TPT)0.5(BTC)H2O·DMF](化合物20)、[Cd(TPT)(5-NTPA)·H2O](化合物21)和[Cd1.5(TPTZ)1.5(BTC)H2O·H2O](化合物22)。发现化合物21对NFT具有非常低的LOD。此外,该方法还具有检测限低、响应时间快、线性范围宽、发光灵敏度可重复等特点。
硝基咪唑类抗生素是一类重要的抗菌药物,常见的有甲硝唑(Metronidazole,MDZ)、奥硝唑(Ornidazole,ODZ)、地美硝唑(Dimetridazole,DTZ)等,对人类生活产生了广泛影响。近年来镉配合物检测硝基咪唑类的抗生素相对较多。
2025年,Zhao等[40]成功地合成了{[Cd(Hade)(btc)0.5(DMF)]·DMF}n(化合物23)。研究发现,即使存在其他类型的抗生素干扰,配合物23也可以选择性区分甲硝唑(MDZ)或地美硝唑(DTZ)。
2025年,Song等[41]在不同的水热合成条件下合成了3个MOFs,[Zn(CIP)(pyterpy)]·2H2O(化合物24)、[Zn3(CIP)3(pyterpy)2]·1.5H2O(化合物25)和[Cd3(CIP)3(pyterpy)2]n(化合物26)。化合物24在水溶液中选择性检测甲硝唑(MDZ),化合物25在水溶液中选择性检测奥硝唑(ORN)。化合物26与MET或ORN发生明显的荧光猝灭。这些MOFs还可以以不同的猝灭率检测水溶液中的硝基苯(图5)。
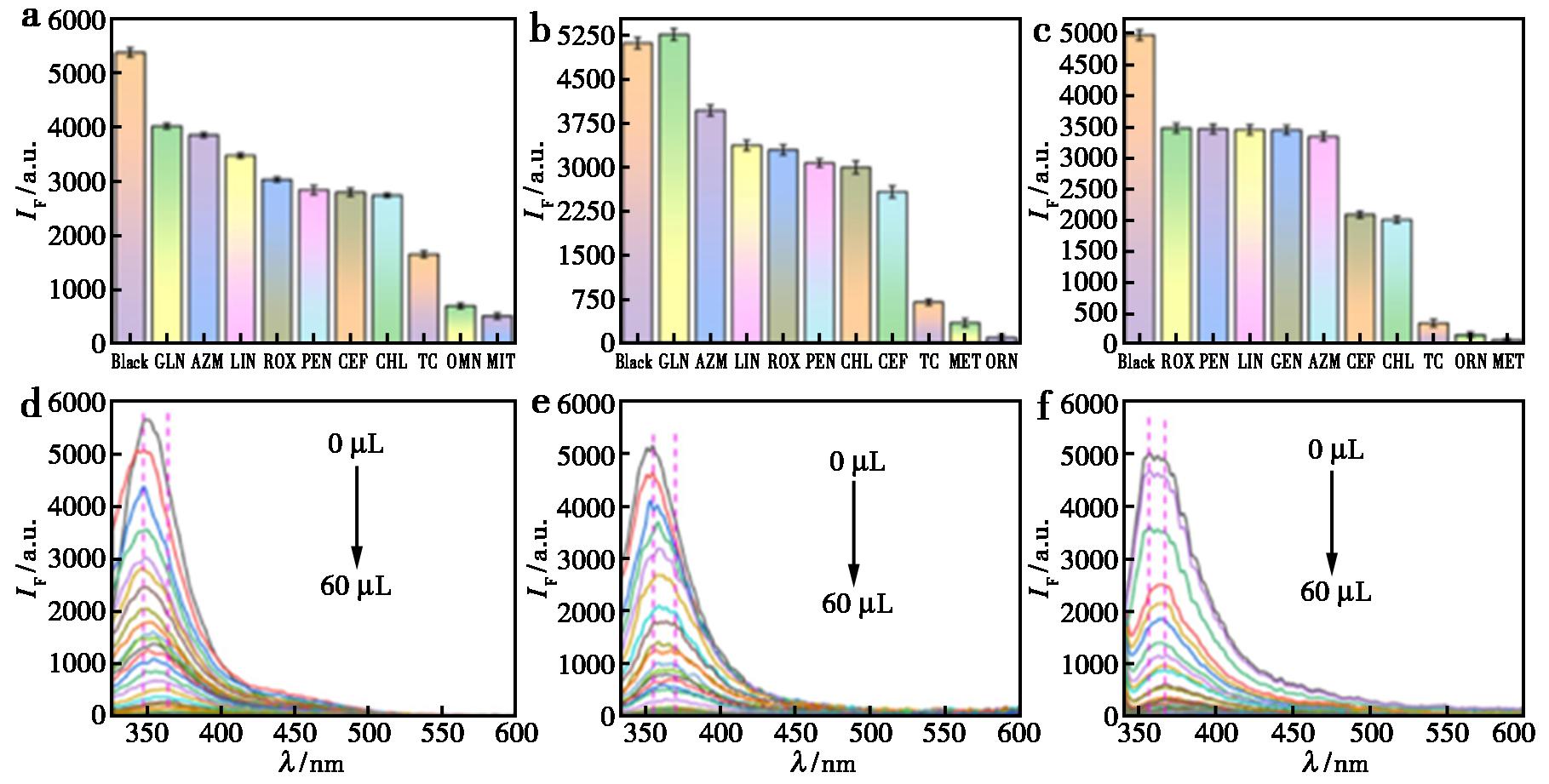
a.化合物24在不同抗生素存在下的荧光强度;b.化合物25在不同抗生素存在下的荧光强度;c.化合物26在不同抗生素存在下的荧光强度;d.化合物24对MET的荧光滴定光谱;e.化合物25对ORN的荧光滴定光谱;f.化合物26对MET的荧光滴定光谱
图5 化合物24~26对MET和ORN的传感选择性和滴定实验[41]
Fig.5 Sensing selectivity and titration experiments of compounds 24~26 for MET and ORN[41]
2025年,Zhong等[42]采用溶剂热法合成了一个新的配位聚合物(CPs),即[Cd2(bbpy)(L)2(DMF)2]n(化合物27)。该化合物在紫外光下对多种抗生素污染物的降解均表现出较强的光催化活性。2024年,Yin等[43]合成了1个新的配合物,即{[Cd(HPA)(LBTX)]·H2O}n(化合物28)。对ODZ/NFZ抗生素表现出不同程度的识别。在各种干扰物质如抗生素的存在下,它对底物表现出良好的灵敏度和高选择性。此外,拟合曲线直观地显示了化合物28对ODZ/NFZ的选择性检测效果。
磺胺类抗生素(Sulfonamides)是一类人工合成的抗菌药物,通过干扰细菌的叶酸代谢发挥抑菌作用。常见的磺胺类抗生素有:磺胺嘧啶(Sulfadiazine,SD)等。目前,对水中磺胺类抗生素的检测被报道较少。
2024年,Das等[44]合成了一种新的基于Cd(Ⅱ)的二维配位聚合物[Cd(L)(NA)(H2O)](化合物29),含有2个由N-烟酰甘氨酸产生的连接子。在水介质中,化合物29在260 nm激发下,在420 nm处显示出强的荧光发射。该化合物的发射行为被用于检测各种磺胺类抗生素,磺胺嘧啶、磺胺二甲基嘧啶、磺胺氯哒嗪、磺胺-5-甲氧嘧啶、磺胺喹恶啉和磺胺噻唑,在常见的水污染物存在下。化合物29对磺胺类抗生素的发光猝灭响应显著,范围为81%~94%,检测灵敏度达到μg/L级别(226~726 μg/L)。
表1 不同镉配合物的材料组成和优缺点
Tab.1 Material composition,advantages and disadvantages of different cadmium coordination polymers
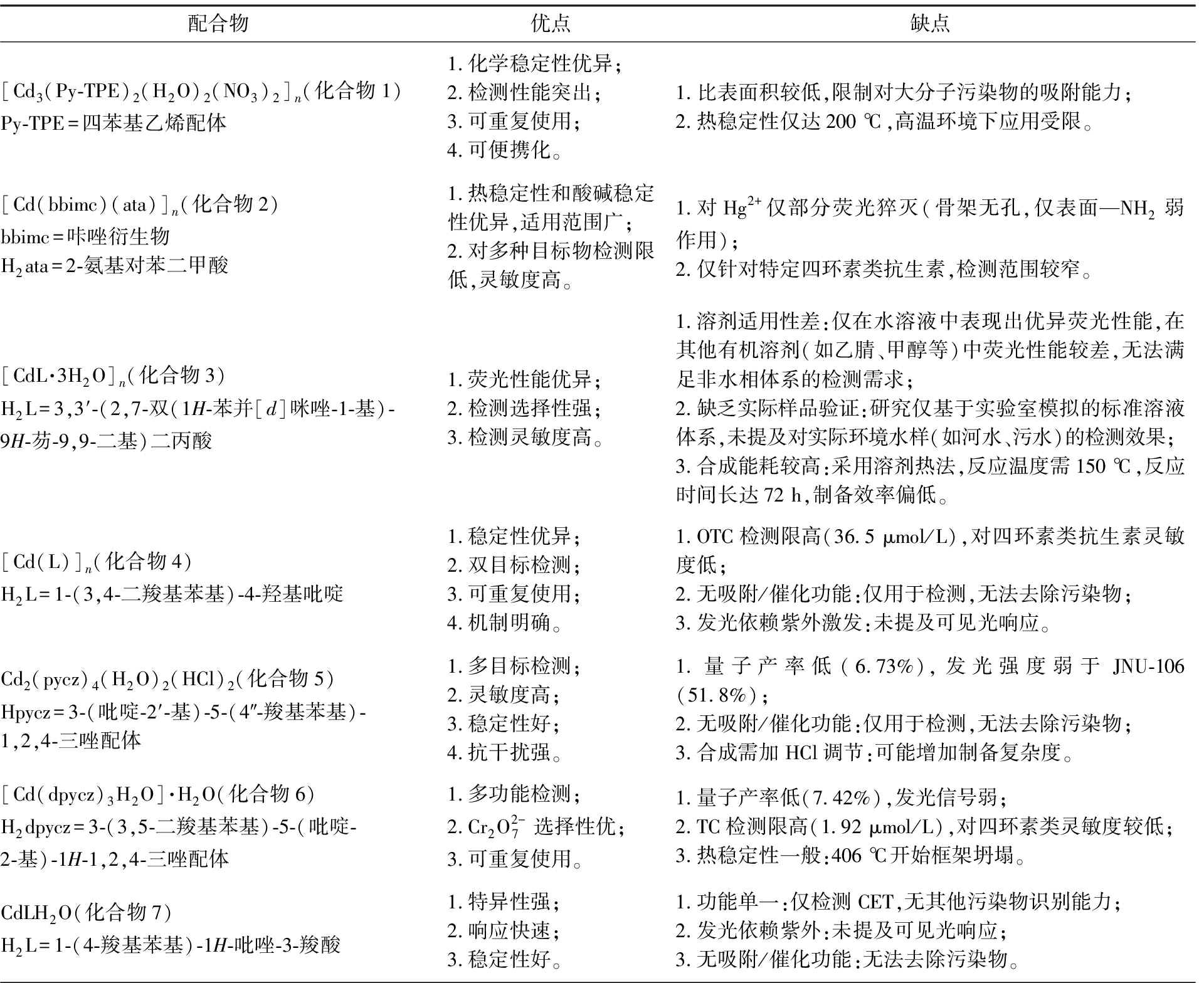
配合物优点缺点[Cd3(Py-TPE)2(H2O)2(NO3)2]n(化合物1)Py-TPE=四苯基乙烯配体1.化学稳定性优异;2.检测性能突出;3.可重复使用;4.可便携化。1.比表面积较低,限制对大分子污染物的吸附能力;2.热稳定性仅达200 ℃,高温环境下应用受限。[Cd(bbimc)(ata)]n(化合物2)bbimc=咔唑衍生物H2ata=2-氨基对苯二甲酸1.热稳定性和酸碱稳定性优异,适用范围广;2.对多种目标物检测限低,灵敏度高。1.对Hg2+仅部分荧光猝灭(骨架无孔,仅表面—NH2弱作用);2.仅针对特定四环素类抗生素,检测范围较窄。[CdL·3H2O]n(化合物3)H2L=3,3′-(2,7-双(1H-苯并[d]咪唑-1-基)-9H-芴-9,9-二基)二丙酸1.荧光性能优异;2.检测选择性强;3.检测灵敏度高。1.溶剂适用性差:仅在水溶液中表现出优异荧光性能,在其他有机溶剂(如乙腈、甲醇等)中荧光性能较差,无法满足非水相体系的检测需求;2.缺乏实际样品验证:研究仅基于实验室模拟的标准溶液体系,未提及对实际环境水样(如河水、污水)的检测效果;3.合成能耗较高:采用溶剂热法,反应温度需150 ℃,反应时间长达72 h,制备效率偏低。[Cd(L)]n(化合物4)H2L=1-(3,4-二羧基苯基)-4-羟基吡啶1.稳定性优异;2.双目标检测;3.可重复使用;4.机制明确。1.OTC检测限高(36.5 μmol/L),对四环素类抗生素灵敏度低;2.无吸附/催化功能:仅用于检测,无法去除污染物;3.发光依赖紫外激发:未提及可见光响应。Cd2(pycz)4(H2O)2(HCl)2(化合物5)Hpycz=3-(吡啶-2′-基)-5-(4″-羧基苯基)-1,2,4-三唑配体1.多目标检测;2.灵敏度高;3.稳定性好;4.抗干扰强。1.量子产率低(6.73%),发光强度弱于JNU-106(51.8%);2.无吸附/催化功能:仅用于检测,无法去除污染物;3.合成需加HCl调节:可能增加制备复杂度。[Cd(dpycz)3H2O]·H2O(化合物6)H2dpycz=3-(3,5-二羧基苯基)-5-(吡啶-2-基)-1H-1,2,4-三唑配体1.多功能检测;2.Cr2O2-7选择性优;3.可重复使用。1.量子产率低(7.42%),发光信号弱;2.TC检测限高(1.92 μmol/L),对四环素类灵敏度较低;3.热稳定性一般:406 ℃开始框架坍塌。CdLH2O(化合物7)H2L=1-(4-羧基苯基)-1H-吡唑-3-羧酸1.特异性强;2.响应快速;3.稳定性好。1.功能单一:仅检测CET,无其他污染物识别能力;2.发光依赖紫外:未提及可见光响应;3.无吸附/催化功能:无法去除污染物。
续表

配合物优点缺点[Cd0.5L0.5(BA)(H2O)]n(化合物8)L=1,4-双(咪唑-1-基甲基)苯BA=苯甲酸1.双目标检测;2.灵敏度高;3.稳定性好。1.结构维度低(1D链):可能影响吸附能力;2.无重金属检测能力:功能覆盖范围窄;3.热稳定性一般:未提及高温稳定性数据。[Cd(TDC)(L)]n(化合物9){[Cd(TCPA)(L)]·H2O}n(化合物10)L=1,4-双(噻苯达唑-1-基)-2-丁烯H2TDC=2,5-噻吩二甲酸H2TCPA=2,3,5,6-四溴对苯二甲酸1.NOR检测限极低,灵敏度突出;2.兼具光催化性能;3.稳定性好。1.仅针对特定抗生素(NOR)和小分子(acac),检测范围有限;2.光催化需UV照射,能耗较高。[Cd(DCTP)(L)(OH)]n(化合物11)[Cd(TBTA)(L)(OH)]n(化合物12)[Cd(NPHT)(L)(H2O)]n(化合物13)L=2-((1H-咪唑-1-基)甲基)-5,6-二甲基-1H-苯并[d]咪唑H2DCTP=2,5-二氯对苯二甲酸H2TBTA=四溴对苯二甲酸H2NPHT=3-硝基邻苯二甲酸1.超高灵敏度;2.双功能检测;3.宽pH稳定。1.配体制备复杂:L为新型配体,合成难度较高;2.量子产率未明确:发光强度数据不足;3.无吸附/催化功能:仅用于检测。[Cd(dbim)(p-phda)]n(化合物14)[Cd(dbim)1.5(suc)]n(化合物15)[Cd(dbim)0.5(m-bdc)(2H2O)]n(化合物16)dbim=1-(4-((2,5-二甲基-3aH-苯并[d]咪唑-1(7aH)-基)甲基)苄基)-3a,7a-二氢-2,5-二甲基-1H-苯并[d]咪唑p-H2phda=对苯二乙酸H2suc=丁二酸m-H2bdc=间苯二甲酸1.拓扑结构规整;2.合成简便;3.化学稳定性较好。1.功能单一:无特定污染物检测能力,仅对溶剂有响应;2.发光性能数据不足:未明确量子产率、发射峰等关键参数;3.无吸附/催化功能:仅可作为基础荧光材料。1.结构含独特26元环;2.热稳定性较好;3.配位模式多样。1.功能单一:无靶向检测能力;2.发光性能未优化:无量子产率、响应时间等数据;3.抗干扰性未验证:未测试复杂体系中稳定性。1.多目标检测;2.响应快速;3.机制明确。1.检测限高:p-NP LOD=1.792×10-4 mol/L,远高于同类材料(如CUST-781对TNP LOD=0.14 μmol/L);2.量子产率未明确:发光强度可能较弱;3.无循环性能数据:未验证重复使用稳定性。[Cd2(CH3-COO)2(bimb)2]·2ClO4(化合物17)bimb=4,4′-双(咪唑基)联苯1.双功能特性;2.检测灵敏度极高;3.光催化效率高;4.结构稳定。1.检测范围窄:仅对NFT有选择性响应,无其他污染物识别能力;2.光响应依赖UV:未提及可见光催化性能,太阳能利用率低;3.合成需特定溶剂:需CH3CN与CH3COOH混合溶剂,成本较高。[Cd3L3·6MeOH·6H2O](化合物18)H2L=3,3′-[(1E,1′E)-(1,10-菲咯啉-2,9-二基)双(乙烯-2,1-二基)]二苯甲酸1.结构新颖;2.多目标检测;3.检测性能优异;4.稳定性极佳;5.可重复使用。1.合成复杂:配体H2L需经Knoevenagel偶联与水解两步合成,步骤较多;2.Fe3+/Cr2O2-7灵敏度一般:Ksv仅103量级,低于CCSFU-1(Cr2O2-7 Ksv=4.82×105 M-1);3.无吸附/催化功能:仅用于检测,无法去除污染物。[Cd2(HDDB)(bimpy)(NMP)(H2O)]·3H2O(化合物19)H5DDB=3,5-二(2′,4′-二羧基苯基)苯甲酸bimpy=3,5-双(1-咪唑基)吡啶1.实现“on-off-on”检测,功能多样;2.可同时检测抗生素、农药、金属离子和小分子,适用场景广;3.水稳定性和pH稳定性优异。1.对AA检测限较高,灵敏度相对较低;2.检测农药仅针对DCN,范围较窄。[Cd1.5(TPT)0.5(BTC)H2O·DMF](化合物20)[Cd(TPT)(5-NTPA)·H2O](化合物21)[Cd1.5(TPTZ)1.5(BTC)H2O·H2O](化合物22)TPT=2,4,6-三(4-吡啶基)-1,3,5-三嗪H3BTC=苯三甲酸NTPA=5-硝基间苯二甲酸TPTZ=2,4,6-三(2-吡啶基)-1,3,5-三嗪1.水稳定性优异;2.抗干扰能力强;3.可重复使用。1.检测灵敏度有限:MDZ、Ag+及[Fe(CN)6]4-的LOD高;2.热稳定性一般:106 ℃开始失去客体DMF分子,384 ℃以上框架发生坍塌;3.对阴离子检测性能弱:[Fe(CN)6]4-的Ksv仅为102量级,检测选择性与灵敏度均较低。1.NFT检测灵敏度高;2.结构稳定;3.抗干扰强。1.Fe3+检测限高(13.9 μmol/L),灵敏度不足;2.无多目标检测能力:仅对NFT响应最优,其他污染物灵敏度一般;3.合成需DMF溶剂:可能增加环境风险。1.Cu2+检测性能优异;2.结构稳定性好;3.可重复使用。1.FBC检测限较高(0.7 μmol/L),低于金属离子检测水平;2.无发光增强功能:仅依赖荧光猝灭,适用场景受限;3.无催化功能:无法去除污染物。
续表
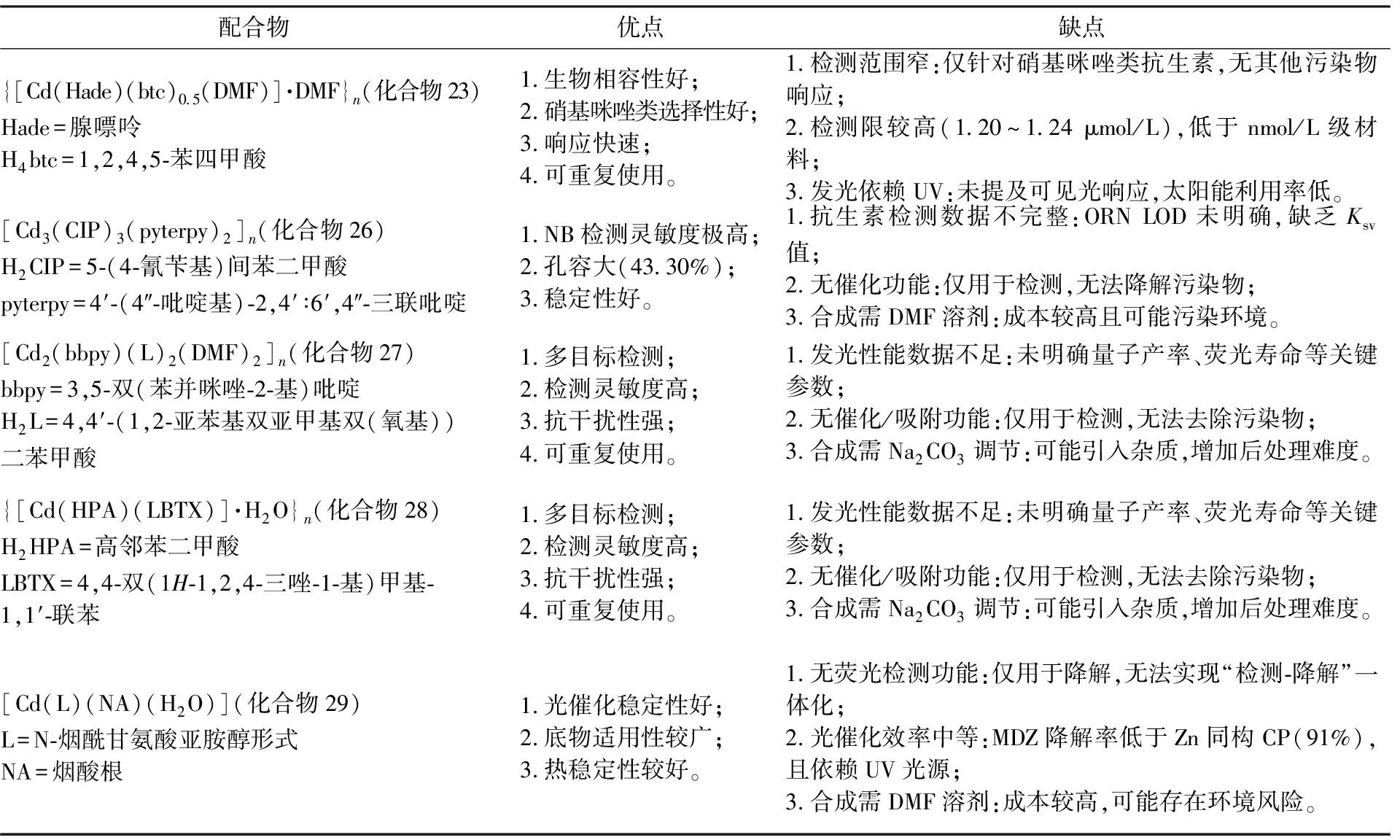
配合物优点缺点{[Cd(Hade)(btc)0.5(DMF)]·DMF}n(化合物23)Hade=腺嘌呤H4btc=1,2,4,5-苯四甲酸1.生物相容性好;2.硝基咪唑类选择性好;3.响应快速;4.可重复使用。1.检测范围窄:仅针对硝基咪唑类抗生素,无其他污染物响应;2.检测限较高(1.20~1.24 μmol/L),低于nmol/L级材料;3.发光依赖UV:未提及可见光响应,太阳能利用率低。[Cd3(CIP)3(pyterpy)2]n(化合物26)H2CIP=5-(4-氰苄基)间苯二甲酸pyterpy=4′-(4″-吡啶基)-2,4′∶6′,4″-三联吡啶1.NB检测灵敏度极高;2.孔容大(43.30%);3.稳定性好。1.抗生素检测数据不完整:ORN LOD未明确,缺乏Ksv值;2.无催化功能:仅用于检测,无法降解污染物;3.合成需DMF溶剂:成本较高且可能污染环境。[Cd2(bbpy)(L)2(DMF)2]n(化合物27)bbpy=3,5-双(苯并咪唑-2-基)吡啶H2L=4,4′-(1,2-亚苯基双亚甲基双(氧基))二苯甲酸1.多目标检测;2.检测灵敏度高;3.抗干扰性强;4.可重复使用。1.发光性能数据不足:未明确量子产率、荧光寿命等关键参数;2.无催化/吸附功能:仅用于检测,无法去除污染物;3.合成需Na2CO3调节:可能引入杂质,增加后处理难度。{[Cd(HPA)(LBTX)]·H2O}n(化合物28)H2HPA=高邻苯二甲酸LBTX=4,4-双(1H-1,2,4-三唑-1-基)甲基-1,1′-联苯1.多目标检测;2.检测灵敏度高;3.抗干扰性强;4.可重复使用。1.发光性能数据不足:未明确量子产率、荧光寿命等关键参数;2.无催化/吸附功能:仅用于检测,无法去除污染物;3.合成需Na2CO3调节:可能引入杂质,增加后处理难度。[Cd(L)(NA)(H2O)](化合物29)L=N-烟酰甘氨酸亚胺醇形式NA=烟酸根1.光催化稳定性好;2.底物适用性较广;3.热稳定性较好。1.无荧光检测功能:仅用于降解,无法实现“检测-降解”一体化;2.光催化效率中等:MDZ降解率低于Zn同构CP(91%),且依赖UV光源;3.合成需DMF溶剂:成本较高,可能存在环境风险。
镉配合物检测抗生素的机理主要基于分子识别引发的光物理信号变化,其核心是抗生素与镉配合物之间的相互作用(如配位、能量转移、电子转移等)改变配合物的荧光特性(增强或猝灭)。常见的机理有:
1)光诱导电子转移(PET)[45]:抗生素作为电子供体/受体,与配合物结合后引发电子传递,导致配合物的荧光猝灭或增强;2)荧光共振能量转移(FRET)[46]:配合物(供体)与抗生素(受体)的发射/吸收光谱重叠,发生能量转移,导致荧光强度或波长变化;3)静态猝灭与动态猝灭[47]:抗生素与配合物基态结合形成非荧光复合物(例如氢键或配位作用);4)聚集诱导发光(AIE)[48]:抗生素诱导配合物聚集或解聚,改变荧光行为;5)内滤效应(IFE)[49]:抗生素吸收配合物的激发或发射光,导致表观荧光减弱;6)协同作用(多重机理结合)[50],例如抗生素同时通过PET和FRET猝灭配合物荧光(图6)。
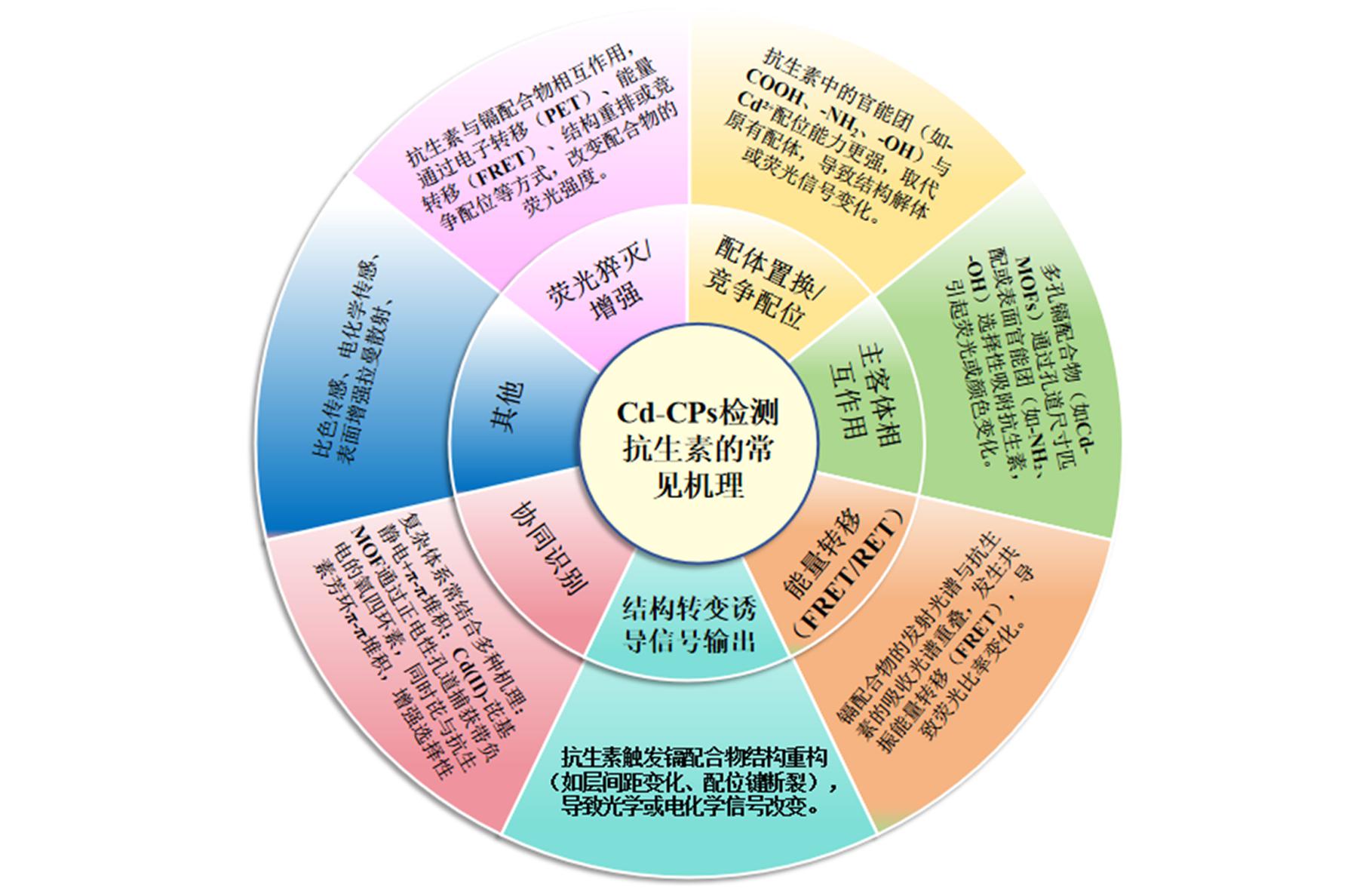
图6 Cd-CPs检测各类抗生素的常见机理
Fig.6 Common mechanism of Cd-CPs for the detection of various antibiotics
本文综述了镉配合物对各类抗生素检测研究进展。到目前为止,镉配合物对各类抗生素检测研究已经取得了重大进展,但仍面临一些挑战。
首先,对于荧光传感技术测定水中抗生素,其优点是低成本、实时观测、高灵敏度和操作简单;其缺点是镉配合物在生活应用方面检测抗生素还不够灵活,限制了应用范围。因此,有必要进一步探索具有广泛应用价值的镉配合物。首要的挑战的是研究一种低成本,不限定空间,灵敏度高的镉配合物加工品,这种方便携带的加工品才有利于人们在日常生活中应用。为了未来能实现更加便捷的检测,可以采用光信号、颜色信号采集系统,结合其他领域的信号处理手段,实现荧光信号与手机实时互通,真正实现利用上述镉配合物加工品的实时检测。
其次,对于一些常见的抗生素,例如青霉素类,目前能检测青霉素类的镉配合物相对较少。因此,有必要进一步探索可以检测各种抗生素的镉配合物。需结合镉离子的配位特性、荧光基团的选择及对某类抗生素的特异性识别能力,主要是构建能通过配位作用或化学反应与某类结合并产生荧光信号变化的镉配合物。
除此之外,还要考虑水中或食品中其他物质和酸碱度的影响,现有的许多研究都没有将上述因素纳入到探针的设计中,从而造成探针容易受外界影响。在此基础上,还可以进一步开发出一种新型的、能够特异性识别特定抗生素的荧光探针,并将其应用于河流水体中,以检验该方法在实际水体中的应用。
综上所述,研究一种更稳定、更便利、应用场景更多、灵敏度更高的并且可进行实时检测的镉配合物是一项需长期探索的项目。
[1]Tao H.Construction of Zinc and Cadmium Pyridinecarboxylate Complexes and Antibiotic Fluorescence Dection Performance.Harbin:Harbin Institute of Technology,2023.
陶贺.吡啶羧酸锌镉配合物的构筑及抗生素荧光检测性能研究.哈尔滨:哈尔滨工业大学,2023.
[2]Dong G G.Research on the Occurrence,Risk Assessments and Removal of Typical Antibiotics and Pesticides in Biliuhe Reservoir Basin.Dalian:Dalian University of Technology,2022.
董莞莞.碧流河水库流域典型抗生素和农药的环境赋存、风险评价和去除研究.大连:大连理工大学,2022.
[3]Li Z S.J.Renmin Univ.China,2019,(19):23-29.
栗战书.中国人大,2019,(19):23-29.
[4]Xie J H.Occurrence Characteristics and Risk Assessment of Antibiotics and Antibiotic Resistance Genes at Urban Water Sources in Plain River Network Area.Yancheng:Yancheng Institute of Technology,2023.
谢加豪.平原河网区城市水源中抗生素与抗性基因赋存特征研究及风险评估.盐城:盐城工学院,2023.
[5]Li S M,Wu H S,Cheng Y P,Meng X,Hao J Y,Yang J R,Zhang H Z.Acta Scientiae Circum.,2025,45(5):232-245.
李思敏,吴会双,程远鹏,孟鑫,郝婧延,杨敬茹,张洪正.环境科学学报,2025,45(5):232-245.
[6]Zhang R L.Characteristics of Antibiotic Contamination and Contamination Risk of Seafood in Typical Culture Areas of The Beibu Gulf Abstract.Nanning:Guangxi University,2018.
张瑞玲.北部湾典型养殖区抗生素污染特征及海产品食用风险.南宁:广西大学,2018.
[7]Ahmed S,Ning J N,Peng D P,Chen T,Ahmad L,Ali A,Lei Z X,Abubakr S M,Chen G Y,Yuan Z H.Food Agr.Immunol.,2020,31(1):268-290.
[8]Grubelnik A,Padeste C,Tiefenauer L.Food Agr.Immunol.,2001,13(3):161-169.
[9]Wang N,Su Y Z,Lei H Q,Li Y M,Li F,Wang X L.Phys.Test.Chem.Anal.B,2024,60(8):802-809.
王宁,粟有志,雷红琴,李艳美,李芳,王兴磊.理化检验-化学分册,2024,60(8):802-809.
[10]Zou J J,Liu A,Qin C,Yang Z,Li R,Liu J M.Phys.Test.Chem.Anal.B,2024,60(6):598-605.
邹佳洁,刘安,秦冲,央珠,李然,刘俊妙.理化检验-化学分册,2024,60(6):598-605.
[11]Li S,Jia J,Gao X G,He X L,Li J P.Anal.Chim.Acta,2012,720:97-103.
[12]Armenta S,Guardia M,Abad-fuentes A,Abad-somovilla A,Esteve-turrillas A.Anal.Bioanal.Chem.,2016,408(29):8 559-8 567.
[13]Huang Y H,Wei H,Santiago P J,Thrift W J,Ragan R,Jiang S.Environ.Sci.Technol.,2023,57(12):4 880-4 891.
[14]Wang X Q,Zeng J Y,Sun Q,Yang J L,Xiao Y L,Zhu Z,Yan B D,Li Y.Sens.Actuat.B-Chem.,2021,343:130 084.
[15]Liu J H,Li Y,Liu L,Gao Y Y,Zhang Y Y,Yin Z Y,Pi F W,Sun X L.Bull.Environ.Contam.Toxicol.,2020,107(2):176-184.
[16]Singh H,Thakur B,Bhardwaj S K,Khatri M,Kim K,Bhardwaj N.Food Chem.,2023,426:136 657.
[17]Liu Q,Ning D,Li W J,Du X M,Wang Q,Li Y,Ruan W J.Analyst,2019,144(6):1 916-1 922.
[18]Wang G D,Li Y Z,Shi W J,Zhang B,Hou L,Wang Y Y.Sens.Actuat.B-Chem.,2021,331:129 377.
[19]Wei X J,Tao T,Ye Z W,Li Q J,Li Z,Mao S.Sens.Actuat.B-Chem.,2025,430:137 384.
[20]Zhu G S,Cheng S L,Zhou Z D,Du B,Shen Y Y,Yu B Y.Polyhedron,2022,217:115 759.
[21]Wei X,Chen Y Y,Zhong J Q,Zhu X P,Ren W,Zhao P.Chin.J.Anal.Lab.,2024,43(5):627-632.
魏霄,陈雨莹,钟佳祺,朱霞萍,任维,赵平.分析试验室,2024,43(5):627-632.
[22]Wei L l,Cheng Z,Ding Y,Lu L X,Wu C X,Wang J,Xue X,Liu Y M.Chin.J.Anal.Lab.,2024,43(7):1 017-1 023.
魏莉莉,程志,丁一,卢兰香,武传香,王骏,薛霞,刘艳明.分析试验室,2024,43(7):1 017-1 023.
[23]Huang Y,Liu W L,Zhong A G,Liu S B.J.Nat.Sci.,Hunan Norm.Univ.,2010,33(4):69-74.
黄莺,刘文龙,钟爱国,刘述斌.湖南师范大学自然科学学报,2010,33(4):69-74.
[24]Dong L L,Liu J,Yang H,Fu Y P,Liu H L,Chen X L,Cui H L,Liu L,Wang J J.Chinese J.Inorg.Chem.,2025,41(4):809-820.
董璐璐,刘洁,杨华,符钰培,刘红丽,陈小莉,崔华莉,刘琳,王记江.无机化学学报,2025,41(4):809-820.
[25]Xu H,Yin T.J.Univ.South China(Sci.Technol.),2023,37(1):95-100.
徐涵,尹婷.南华大学学报(自然科学版),2023,37(1):95-100.
[26]Kang S H,Luo F L,Huang Y L,Luo D,Hang G Q,Wu Y,Liu M L,Xu S H,Lu W G,Li D.Inorg.Chem.,2024,63(6):3 075-3 082.
[27]Sun X C,Li C X,Meng X G,Wang D J,Zheng C Y.CrystEngComm,2023,25(32):4 531-4 538.
[28]Wu G L,Dong C Z,Liu P Z,Zheng C Y.CrystEngComm,2025,27(11):1 560-1 567.
[29]Li X Q,Yang P Y,Zhao Y X,Li Y,Li M G,Li X Y,Wu J H,Shen J X,Wang X L,Han H,Lin Z G,Zhang X L,Ma S.Polyhedron,2024,250:116 818.
[30]Zhang W T,He C C,Zhang W X,Sun J,Peng D X,Li X,Su Z M.Cryst.Growth Des.,2024,24(8):3 441-3 448.
[31]Wang Q C,Zhu S,Tan Z Q,Quan Y,Li Y F,Yang T,Zhou X H,You Y J,Wang R.Appl.Organomet.Chem.,2024,38(7):e7 557.
[32]Zhao L,Zhang D,Wang F.Inorg.Chim.Acta,2024,565:121 994.
[33]Wu Y B,Ren L,Dong G Y.Inorg.Chim.Acta,2022,530:120 703.
[34]Fan X F,Fu L,Cui G H.Dalton Trans.,2024,53(11):5 051-5 063.
[35]Liu L,Wang H J,Qu L B,Li C X,Li Y,Cui C X.J.Mol.Struct.,2024,1 310:138 278.
[36]Wu Y,Li J L,Xu J,Muddassir M,Kushwaha A,Daniel O,Kumar A,Zou L.CrystEngComm,2024,26(23):3 113-3 122.
[37]Meng Z X,Yang F N,Wang X J,Shan W L,Liu D D,Zhang L Y,Yuan G Z.Inorg.Chem.,2023,62(4):1 297-1 305.
[38]Feng D D,Tang J,Yang J,Ma X H,Fan C Z,Wang X Q.J.Mol.Struct.,2020,1 221:128 841.
[39]Fang M,Wang Y M,Wang Y Y,Wang J W,Hu X L,Su Z M.J.Mol.Struct.,2025,1 320:139 625.
[40]Zhao H K,Wang Q,Yang H W,Wang X G,Liu Z Y.J.Mol.Struct.,2025,1 328:141 337.
[41]Song X M,Zhao Q X,Hou X F,Liu S,Luo L X,Ren Y X.J.Mol.Struct.,2025,1 324:140 813.
[42]Zhong X,Ghosh M K,Ayue Y,Liang J Y,Wang J,Afzal M,Alarifi A,Ghorai T K.Polyhedron,2025,267:117 365.
[43]Yin B B,Cao Y,Yuan K X,Wang Y.Inorg.Chem.Commun.,2024,169:112 981.
[44]Das C,Patel V D,Gupta D,Mahata P.Inorg.Chem.,2024,63(8):3 656-3 666.
[45]Chen X,Hao X Y,Zhai L J,Fan L M,Niu Y L.J.Cluster Sci.,2022,33(1):293-300.
[46]Wang K M,Zhao X,Bai X L,Dong Y Q,Fan R F,Yu H M,Tang H J,Ma Y L.Chin.J.Inorg.Chem.,2023,39(8):1 587-1 596.
王凯民,赵雄,白旭玲,董艳秋,樊瑞峰,于红梅,唐怀军,马钰璐.无机化学学报,2023,39(8):1 587-1 596.
[47]Zhao Y Y,Zhou Y,Li R,Li B.J.Cluster Sci.,2023,34(6):2 791-2 797.
[48]Gao Z H,Deng X C,Cui G H,Fu L S.J.Solid State Chem.,2024,330:124 450.
[49]Qiu H M,Yang H,Gao X,Nie C,Gu Y,Shen Y Z.Coord.Chem.Rev.,2023,493:215 305.
[50]Cao Y,Yuan K X,Wang Y.Dyes Pigments,2025,242:112 999.