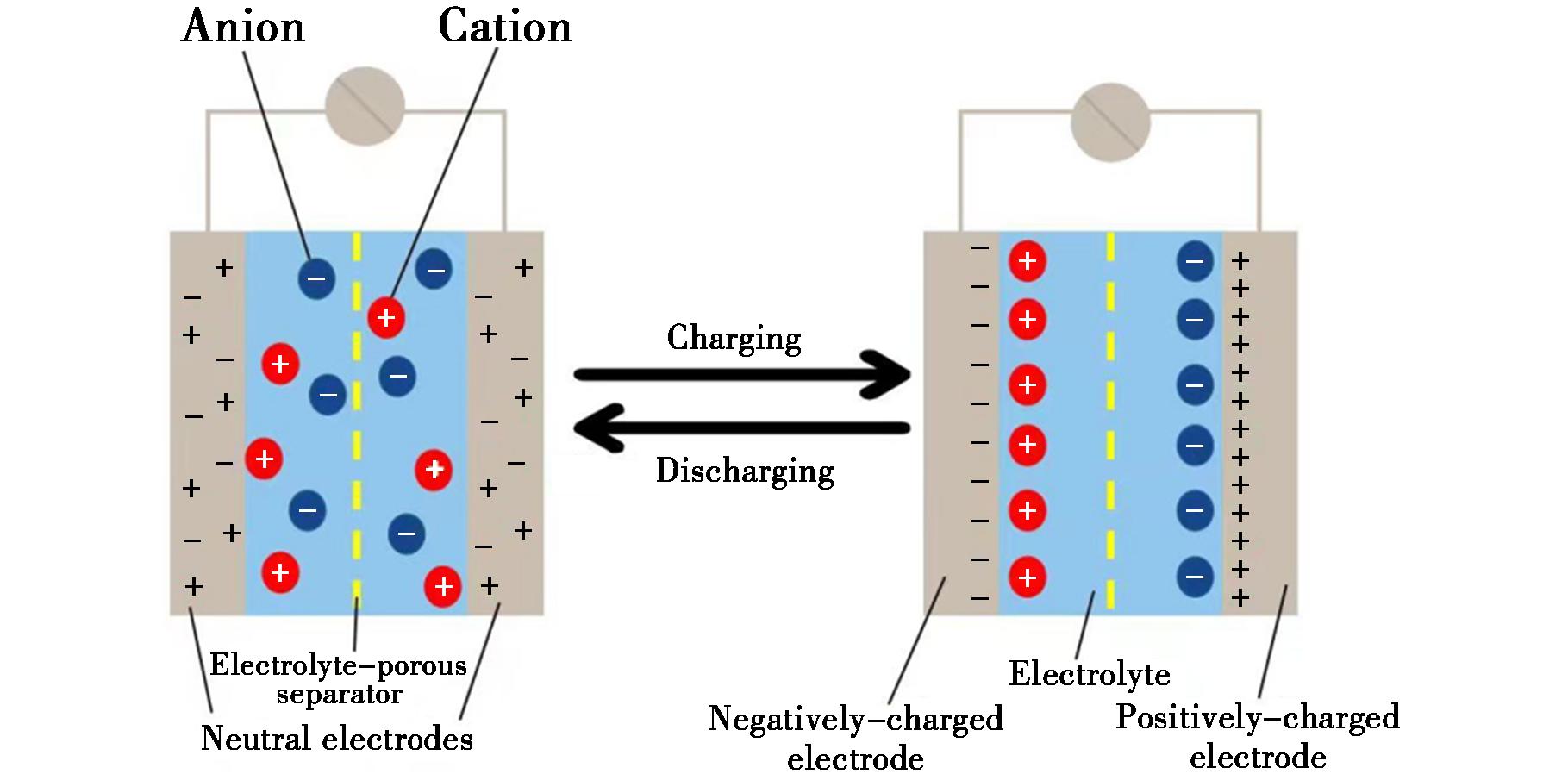
图1 超级电容器的工作原理图
Fig.1 Working principle diagram of supercapacitor
近年来,国际形势的持续发展对新能源的高质量改革提出了更深层次的要求,能源需求愈演愈烈,导致世界化学能源的储量急剧下降,而由此产生的温室气体过度排放到大气中引起了一系列环境污染危机。因此,在我国“双碳”的政策下,清洁能源的发展将会持续加快[1-3]。超级电容器作为一种新型电化学储能原件,具有比普通电池更大的导电率、稳定性以及较低成本等优势[4,5]。超级电容器作为高效的储能装置在混合动力电动汽车、便携式电子产品和通信设备领域的能量存储越来越受到关注[6]。我国超级电容器起步较晚,因此还具有很大的发展空间[7]。对于新能源产业的开发,习近平总书记在二十大会议中提出“推动战略性新兴产业集群融合发展,构建新一代信息技术、生物技术、人工智能、新能源、新材料、绿色环保等新兴产业的增长引擎”。由此可见我国政府非常重视新能源产业的开发。
随着国内外对过渡金属氧化物研究的不断深入,以锰(Mn)、镍(Ni)、钴(Co)等为主要元素的二元过渡金属作为超级电容器的主要原料受到广泛关注[8,9]。镍钴离子因其在自然界中有多种价态而具有较强的氧化还原性,且镍钴离子之间存在一种协同效应使得镍钴基电极材料显现出优于其他单一金属电极材料的电化学储能效果。而在NiCoO2@N-C表面形成的核壳结构除了可以作为稳定其结构的骨架外,还可以为电荷的储存与转移提供平台与通道,加大了它与电解质之间的接触面积,为工作电极中的电荷与电解液中的OH-之间的快速结合提供了更多的活性位点。这个特性对于提高电极材料在工作电极上的储能效果、改善电极材料的导电性能、保持NiCoO2晶体结构的稳定性等方面都起着至关重要的作用。
安露露等[10]利用共沉淀法,以六水合硝酸镍和六水合硝酸钴为主要原料制备样品,表征、测试手段表明产物为表面粗糙的片状结构,X射线衍射(XRD)的出峰位置分析发现其衍射峰强度随镍钴比例的增大而逐渐增强,因此得出产物具有更好的结晶度。不同电流密度下的恒流充放电(GCD)曲线表明在电流密度增大20倍的情况下产物具有良好的倍率性能。但于掺杂技术而言,尽管氮碳掺杂已被证实对提升电化学性能具有积极作用,但实现掺杂元素在材料中的精确含量调控与均匀分布仍面临巨大挑战。当前的制备方法难以确保掺杂原子在微观层面均匀嵌入镍钴晶格,致使材料内部形成局部性能差异显著的区域,严重影响电极整体性能的稳定性与一致性,增加了性能波动风险,不利于在实际应用中稳定发挥电极功能,故在掺杂工艺优化方面,通过借助先进的材料合成技术,如原子层沉积、分子束外延等手段,实现对掺杂元素在原子尺度的精确调控,确保其均匀分散于镍钴基材料中,提升材料性能的均一性。
在制备电极材料时,水热法因其具有简单、高效、易控且成本低廉等优势被应用于纳米结构材料的形貌控制合成[11]。毛振东等[12]用水热法以六水合硝酸镍和六水合硝酸钴为主要原料制备出了NiCo-LDHs,用同样的制备方法分别对样品进行Fe、Al掺杂。XRD表征发现其衍射峰比较高,因此得出3种样品都是相同的NiCo-LDHs。以NaOH溶液为电解液对这3种样品进行电化学测试。分别绘测不同材料在相同电流密度下的GCD曲线可以观察到NiCoAl-LDHs与NiCoFe-LDHs具有更高的催化活性。通过绘测相同测试电压下不同样品的安培时间曲线观察到NiCoAl-LDHs与NiCoFe-LDHs具有更高的电流密度,进而推测出金属掺杂后的NiCoAl-LDHs与NiCoFe-LDHs比未掺杂的NiCo-LDHs具有更好的催化性能。李傲等[13]从分子层面设计和合成新型的有机配体与筛选合适的多金属协同中心以构建高性能的MOF基材料应用于电池中,发现其具有比表面积大、孔隙率高、催化效率强、稳定性好等优点。
单一的过渡金属氧化物也有其自身的局限性[14],例如在长期的氧化还原过程中可能会存在外界环境的热胀冷缩导致电极材料塌陷或脱落,电阻的增大易造成电极材料循环性能以及电流密度的显著下降[15,16]。而元素掺杂又是通过修饰,调控电极材料的内部结构并增加其活性位点、提高其电化学活性的一种有效策略[17-19]。从毛振东等[12]的研究中得出对电极材料进行金属掺杂可以有效提高其电化学性能,而非金属对电极材料的电化学性能影响则由翟好英等[20]采用水热法合成了硼、磷共掺杂材料Fe-Co-B-P了解。运用SEM、TEM的表征手段发现它是由纳米颗粒堆积而成、表面疏松且有许多空隙。浸泡在KOH中进行电化学测试得出,掺杂后样品的电位随着电流密度的增大而增大,说明该电极材料具有较优的导电性能。将电极材料连续进行10 h计时电位测试以后发现,掺杂后的样品电势能够保持在1.55 V左右,表明共掺杂后的样品具备良好的电化学稳定性。这是由于双金属材料与非金属之间出现协同作用促进了电子的有效传递。
非金属元素的掺杂也是提高电化学性能的有效手段[21]。将过渡金属氧化物与非金属材料相结合所形成的电极材料既吸收了各组分的优点、有效改善了电极材料的导电性和超级电容器的电化学性能,又极大弥补了单一组分性能的不足[22,23]。可见非金属元素的掺杂对于电极材料的发展起到了至关重要的作用。
选用六水合硝酸钴、六水合硝酸镍作为主要实验原料,以尿素为结构导向剂,高温烘干粉碎的黄豆作为相应氮源展开本次实验设计。采用水热法及退火处理技术分别制备参与掺杂的二氧化钴镍@氮碳X(NiCoO2@N-C-X)以及未参与掺杂的二氧化钴镍(NiCoO2),利用多种表征手段对样品的微观结构进行分析,利用三电极体系将电极材料附着在泡沫镍上进行电化学性能测试以深入探究非金属掺杂对电极材料导电及储能效果的影响。
如图1所示,超级电容器主要是通过电极与电解质的表面对离子产生物理吸附来储存电荷。

图1 超级电容器的工作原理图
Fig.1 Working principle diagram of supercapacitor
充电时,在外电场作用下,正负电荷移动到电极板表面使两个电极板分别带有正、负两种电荷,电容可用公式(1)表达。
C=(εs)/(4πkd)
(1)
式中,ε为电解质的介电常数,s为电极材料的表面积,d为电极的有效厚度。
放电时电极表面的电荷又重新转移至电解液中,使外加电路产生了放电电流。又因为超级电容器储能过程为物理过程,并不存在化学反应,且电荷的吸脱附速率非常快,因此,超级电容器充放电速度快、循环性能好且功率密度大。由公式(1)可知,超级电容器的储电性能也极大程度取决于所选电极材料的比表面积。
在三电极体系中,可在充放电曲线下根据公式(2)计算得到工作电极在某电流密度下的比电容。
C=(IΔt)/(mΔV)
(2)
式中,I为电流密度,A/g;Δt为放电时间,s;ΔV为工作电压窗口,V。
1.1 主要仪器与试剂
85-2型磁力搅拌器(上海国华有限公司);DHG-9053A型电热鼓风干燥箱、Nicolet is5型傅里叶红外光谱仪(上海一恒有限公司);Miniflex600型台式X射线衍射仪(日本Rigaku有限公司);DG120C型粉碎机(浙江瑞安有限公司);NL20S型压片机(天津恒创有限公司);CHI660E型电化学工作站(上海辰华有限公司);15-1729型超声波清洗机(宁波新芝有限公司);H/T18MM型台式高速离心机(湖南赫西仪器有限公司);100 mL不锈钢高压反应釜(上海岩征有限公司);JEM2100F型透射电子显微镜(日本电子有限公司);Hitachi S4800型扫描电子显微镜、Thermo escalab 250Xi型X射线光电子能谱仪(美国赛默飞世尔科技公司);ASAP2020M+C型全自动物理化学吸附仪(美国Micromeritics有限公司)
六水合硝酸钴(Co(NO3)2·6H2O)、六水合硝酸镍(Ni(NO3)2·6H2O)(分析纯,北京百灵威科技有限公司);尿素(CH4N2O,分析纯,辽宁泉瑞试剂有限公司);无水乙醇(C2H5OH,分析纯,天津市恒兴化学试剂制造有限公司);氢氧化钾(KOH,分析纯,天津市登科化学试剂有限公司);泡沫镍(Ni,1.0 cm×1.5 cm×1.0 mm,天津安诺合新能源科技有限公司);导电炭黑(C,XC-72R,苏州晟尔诺科技有限公司);三羟甲基氨基甲烷(C4H11NO3,生化试剂,国药集团化学试剂有限公司);聚四氟乙烯溶液((C2F4)n,70 wt%,东莞市兴旺涂料科技有限公司)。
1.2 实验步骤
1.2.1 电极材料制备
1.2.1.1 Ni-Co前驱体的合成步骤
分别称取1.536 2 g(0.005 3 mol)Co(NO3)2·6H2O、1.523 5 g(0.005 3 mol)Ni(NO3)2·6H2O与1.814 8 g(0.03 mol)尿素溶于8 mL无水乙醇和40 mL去离子水中,打开磁力搅拌器,在室温下搅拌30 min,使药品溶解并混合均匀。将混合溶液转移至100 mL不锈钢高压反应器中,在120 ℃恒温下反应9 h。反应结束后,将其冷却至室温并取出。分别在离心机中用去离子水和无水乙醇离心洗涤3次,转移至坩埚并将其放入鼓风干燥箱中以80 ℃烘干9 h即可得到紫色Ni-Co前驱体粉末。
1.2.1.2 NiCoO2@N-C-X与NiCoO2的合成
称取约0.3 g烘干并粉碎的黄豆粉末,使其均匀分散在100 mL pH 8.0的Tris-HCl缓冲溶液中,利用磁力搅拌器在室温下搅拌10 min尽可能使更多固体粉末分散于该缓冲溶液中。随后称取约0.6 g Ni-Co前驱体,加入到上述混合溶液中磁力搅拌12 h使其充分混合。接着用去离子水、无水乙醇在离心机中分别离心洗涤3次以去除附着在固体表面的杂质,洗涤完成后将其放入干燥箱中80 ℃烘干9 h即可得到灰黑色粉末,待其冷却至室温后将坩埚放入鼓风干燥箱中以200 ℃恒温反应12 h,随后降至室温即可得到NiCoO2@N-C-X(X=1)。同时称取0.6、1.2 g黄豆粉末按照相同的制备方法分别制备NiCoO2@N-C-X(X=2、3)。为了后续的对比测试工作,在其他反应条件相同的条件下不添加粉碎的黄豆粉末制备NiCoO2。
1.2.2 工作电极的制备
超级电容器的工作电极由电极、电解液、集流体、隔膜这4部分组成,如图2所示。其中电极上所附着的活性材料对于电容器的电化学性能起着决定性的作用。
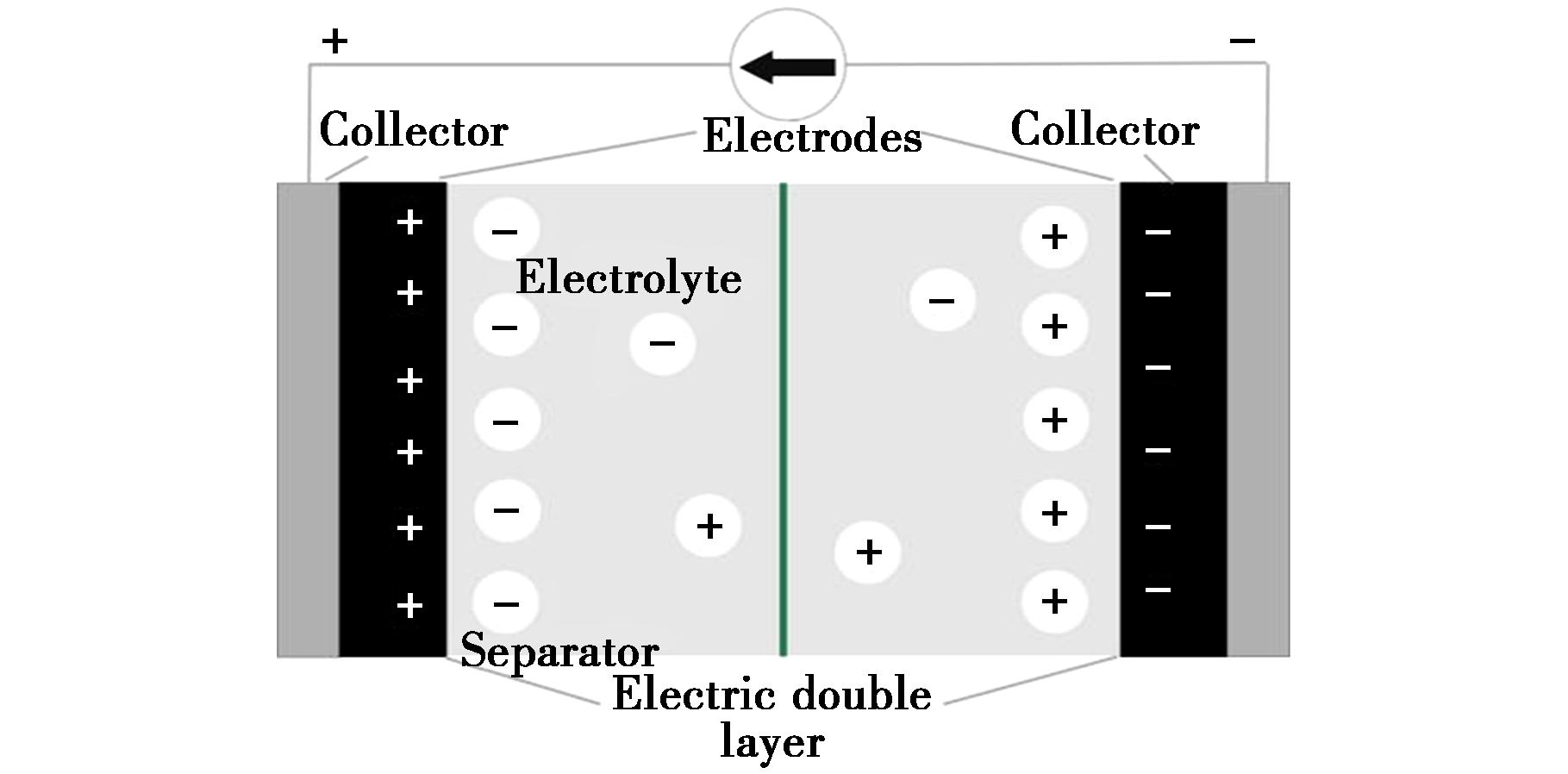
图2 超级电容器工作电极内部构造图
Fig.2 Internal structure diagram of working electrode of supercapacitor
泡沫镍因其具有特殊的3D网状结构。有较高孔径率与较大的比表面积,这种特点不仅为电荷的运动提供了通路、为电解质的扩散提供更多可接触区域,还为电极材料提供了更好的附着平台。除此之外,泡沫镍又具有售价较低、制作过程简单、原料易得等特点。因此,在本实验中最终选用泡沫镍作为集流体。
为了防止原附着在泡沫镍上的杂质干扰最终实验结果,泡沫镍在被用作集流体进行实验之前必须要先进行预处理:选用几块厚0.1 mm的泡沫镍均将其裁剪成1 cm×1.5 cm的长方形,将其放入烧杯中一并放进超声波清洗器中,利用无水乙醇溶液清洗10 min,去除泡沫镍表面的油污。然后将其放入2 mol/L HCl溶液中浸泡20 min以除去泡沫镍表面的氧化层。用无水乙醇以及去离子水进行多次清洗,并将其放入鼓风干燥箱中烘干8 h。具体的工作电极制备方法如下:1)分别将上文所制得的NiCoO2@N-C-X(X=1、2、3)以及NiCoO2作为活性材料,实验用导电炭黑为导电剂,聚四氟乙烯溶液为粘合剂,以m(NiCoO2@N-C-X(X=1、2、3)NiCoO2)∶m(导电炭黑)∶m(聚四氟乙烯溶液)=7∶1∶1的质量比将其混合在表面皿中,并加入少量无水乙醇充分搅拌使其混合均匀;2)取烘干的泡沫镍用分析天平称其质量记为m1,将剪裁好的泡沫镍预留出1 cm×1 cm的有效面积,然后在预留好的有效面积中涂抹1)中所制好的浆料,将涂抹好的泡沫镍放置在坩埚中贴好相对应标签置于鼓风干燥箱中80 ℃恒温烘干 10 h;3)烘干完成后将泡沫镍分别用压片机在 10 MPa的条件下进行多次压平,使活性材料与泡沫镍材料紧密结合;4)然后用无水乙醇多次对压片后的电极片进行清洗,以除去电极片表面多余的原料。将泡沫镍再次置于坩埚中放进鼓风干燥箱以80 ℃烘干12 h,即可分别得到最终参与掺杂以及未参与掺杂的工作电极片;5)称量涂料后泡沫镍的质量并将其记为m2,涂料前后质量之差的70%即为在工作电极片上所涂抹电极材料的质量,大约是2 mg。
m=0.7(m2-m1)
(3)
2.1 样品表征方法
2.1.1 傅里叶红外光谱
傅里叶红外光谱(Fourier transform-infrared spectroscopy,FT-IR)主要用于检测样品在标准中红外区域的吸收光谱,该测试手段被广泛应用于有机化合物的定性及原子基团分析。本次实验的红外光谱分析使用的是上海Nicolet is5型号的傅里叶红外光谱分析仪。
图3为NiCoO2及NiCoO2@N-C-X的IR谱图,如图3a所示,掺杂前后样品的红外光谱有着明显的区别。由于氮碳掺杂还可能引起NiCoO2晶格的畸变和缺陷的形成。并且氮原子的电负性高于氧原子,当氮原子掺入NiCoO2晶格中时,会吸引周围的电子,导致材料电子结构的改变。这种改变影响了化学键的振动频率和强度,从而在红外光谱上产生新的吸收峰或导致原有吸收峰的变化。
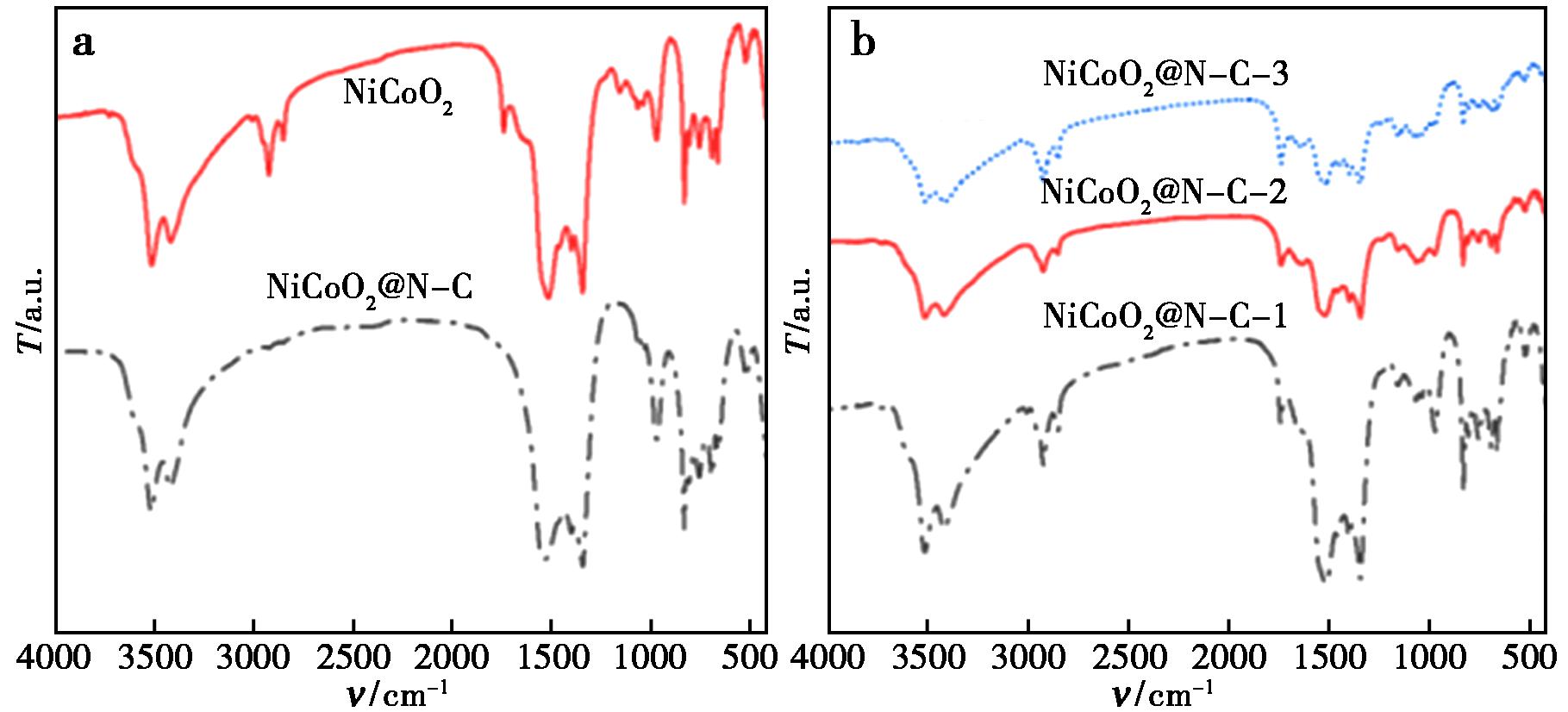
a.NiCoO2及NiCoO2@N-C的红外光谱;b.NiCoO2@N-C-X(X=1、2、3)的红外光谱
图3 傅里叶红外光谱图
Fig.3 Fourier transform-infrared spectroscopy
掺杂后的样品在2 927及1 753 cm-1左右出现了较为明显的吸收峰,分别代表了C—H伸缩振动与C![]() O伸缩振动。通过对比发现NiCoO2@N-C在波数为1 300~1 160 cm-1的低频区出现了较为密集的吸收峰,这个区中出现的吸收峰其中之一代表了C—N单键的伸缩振动与各种弯曲振动,说明经过水热法及退火处理技术成功合成了NiCoO2@N-C。由此可见,在指纹区内微小的结构差异都会得到反映。图3b为不同掺杂质量的NiCoO2@N-C红外光谱图,通过观察可以发现3条光谱吸收峰位置相同,表明这3个样品均氮碳掺杂成功。
O伸缩振动。通过对比发现NiCoO2@N-C在波数为1 300~1 160 cm-1的低频区出现了较为密集的吸收峰,这个区中出现的吸收峰其中之一代表了C—N单键的伸缩振动与各种弯曲振动,说明经过水热法及退火处理技术成功合成了NiCoO2@N-C。由此可见,在指纹区内微小的结构差异都会得到反映。图3b为不同掺杂质量的NiCoO2@N-C红外光谱图,通过观察可以发现3条光谱吸收峰位置相同,表明这3个样品均氮碳掺杂成功。
2.1.2 比表面积测试
比表面积测试(Brunauer-emmett-teller,BET)是分析样品孔体积、平均孔直径以及比表面积的重要表征手段,其中比表面积与样品的形状以及孔隙结构等密切相关,BET也被看做衡量样品特性的重要参数。
以氮气为吸附质,氢气或氦气作为载气,吸附质与载气按照一定比例进行混合,达到指定压力后在经过300 ℃脱气预处理。实验所得相关数据如表1所示,氮碳掺杂后的样品平均孔直径变小、比表面积增大。
表1 NiCoO2与NiCoO2@N-C-X的孔体积、孔径、比表面积
Tab.1 Pore volume,pore diameter and specific surface area of NiCoO2 and NiCoO2@N-C-X
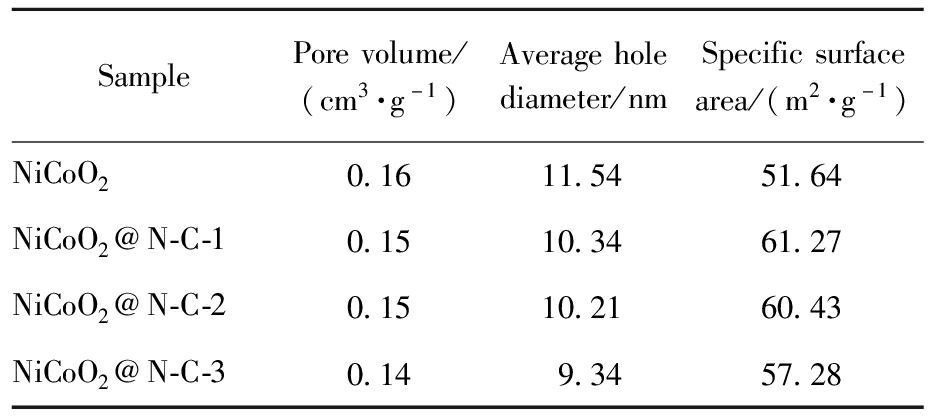
SamplePorevolume/(cm3·g-1)Averageholediameter/nmSpecificsurfacearea/(m2·g-1)NiCoO20.1611.5451.64NiCoO2@N-C-10.1510.3461.27NiCoO2@N-C-20.1510.2160.43NiCoO2@N-C-30.149.3457.28
实验过程中,氮碳原子的引入改变了材料的微观结构,特别是孔隙结构,导致平均孔直径从11.54 nm减小到9.34 nm,而比表面积则从51.64 m2/g增加到61.27 m2/g。这一变化是由于氮碳原子填充了部分原有大孔隙,同时在新位置上形成了更多小孔隙,从而优化了孔隙分布,使得更多表面积得以暴露。从而增强了材料的电化学性能。适当的氮碳掺杂增加了材料的比表面积,为电荷的储存提供了更多的空间。但经过实验研究发现,过度掺杂会导致比表面积降低,从而导致电化学性能的降低。
2.1.3 扫描电子显微镜
SEM常被用来观察产物的微观形貌以及结构。图4展示了NiCoO2@N-C-X在不同放大倍率下的SEM图,测试结果表明样品具有中空海胆状纳米球结构。退火工艺处理后的样品能够更好的维持海胆状纳米球构型。对NiCoO2@N-C-X的微观形貌分析发现NiCoO2@N-C-X在引入黄豆粉末后微观形态大致相同。图4b和4c为NiCoO2@N-C-1的微观形貌,纳米针细而密,没有附着物,结构为标准的中空海胆形状。该物质为碳氮掺杂的最佳产物。如图4f所示,当氮源掺杂质量增加到1.2 g时,NiCoO2@N-C-3的海胆状纳米球上出现了明显的附着物,纳米针随之变粗且出现了明显的节点。这是因为氮源附着在纳米球上过度生长造成了团聚。

a.50 μm;b.2 μm;c.5 μm;d.5 μm;e.10 μm;f.5 μm
图4 NiCoO2@N-C-X的SEM图
Fig.4 SEM diagram of NiCoO2@N-C-X
2.1.4 透射电子显微镜
TEM因其分辨率比SEM更高而常被用来观察样品的超微观结构、观测材料内部微观结构以及形貌特征。
图5a、5b、5c为NiCoO2的TEM图,图5d、5e、5f为NiCoO2@N-C-1的TEM图。从图5a、5d中观察到所制备的样品具有非常明显的中空海胆状纳米球结构,为超级电容器的储存电荷提供了良好的附着平台,缩短了电解质中离子与电子的扩散路径。如图5b、5e所示,NiCoO2以及NiCoO2@N-C-1是由无数纳米针构成,在10 nm以及20 nm的测试条件下观察发现,与图5b、5c相比,图5e、5f的纳米针外层明显被一种包裹层包裹形成核壳结构,这种包裹层是氮碳掺杂层。以上测试结果均与BET、SEM测试所得出的结论相符合。

a.0.5 μm;b.10 nm;c.20 nm;d.0.5 μm;e.10 nm;f.20 nm
图5 NiCoO2及NiCoO2@N-C-1在相同放大倍率下的TEM图
Fig.5 TEM images of NiCoO2 and NiCoO2@N-C-1 at the same magnification
2.1.5 X射线衍射仪
XRD作为一种研究晶体微观结构的表征手段之一而被国内外广泛应用。XRD可以更准确的判断样品的晶体结构。通过与特定晶体的JCPDS标准卡片进行对比,对样品进行定性分析。X射线衍射仪扫描范围为2θ=10°~90°。
如图6所示,NiCoO2在2θ=35.8°、40.3°、62.2°处出现了明显的衍射峰,这些衍射峰分别与NiCoO2的JCPDS标准卡片吻合(JCPDS 10-0188)。NiCoO2@N-C-1的衍射峰与NiCoO2保持一致外,又出现了2个峰强较弱的衍射峰2θ=48.4°和65.5°处,这可以检索到Co(CO3)0.5(OH)0.11H2O(JCPDS 48-0083)。所有的峰相较于标准JCPDS卡片有轻微偏移,这是由于镍钴结合成了金属碳酸盐氢氧化物,但其晶体的结构仍可以保持不变。所有衍射峰强度较高、峰形较窄、密度较大等特点证明该样品具有良好的结晶度。
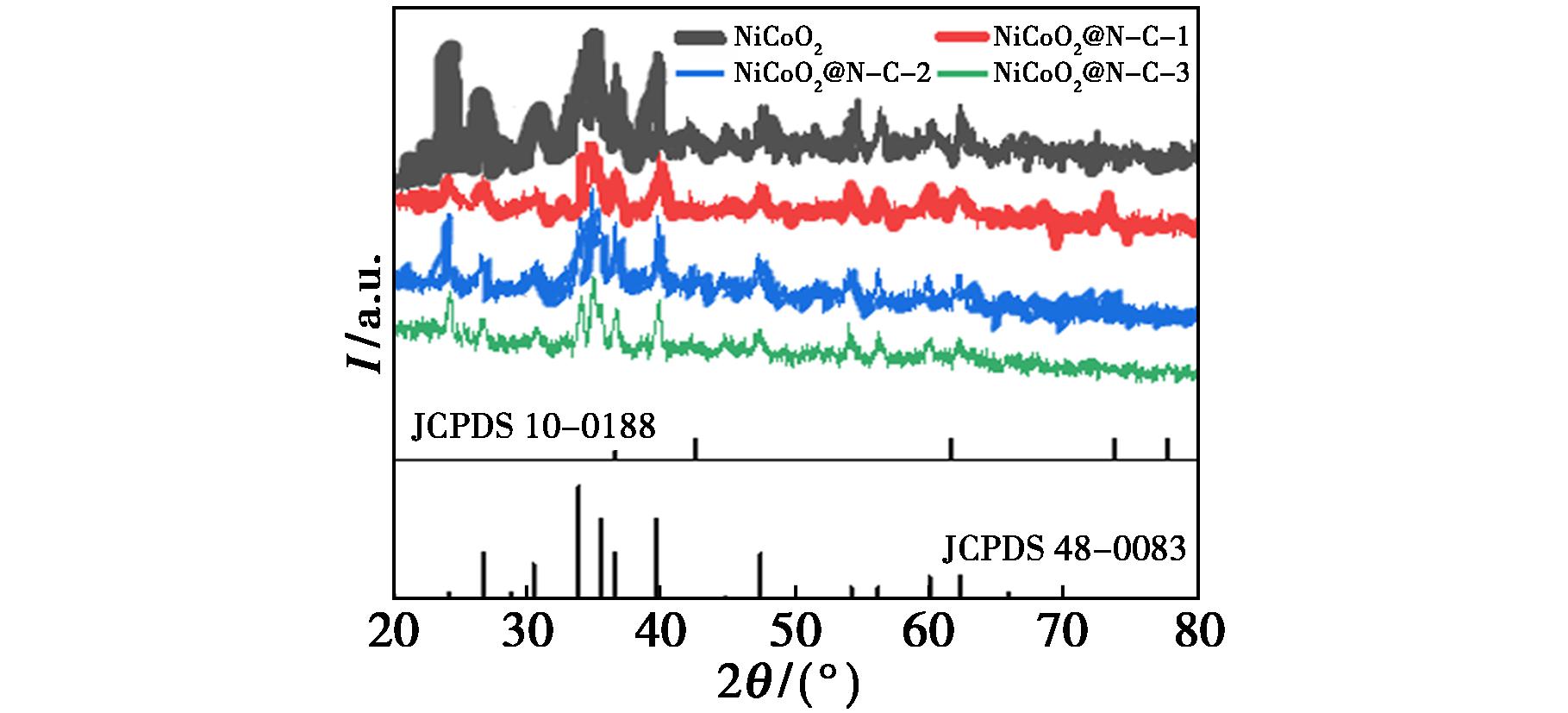
图6 NiCoO2与NiCoO2@N-C-X(X=1、2、3)的XRD图谱
Fig.6 XRD patterns of NiCoO2 and NiCoO2@N-C-X(X=1,2,3)
2.1.6 X射线光电子能谱
XPS是X射线与样品表面发生反应,激发样品表面所包含的原子产生极强光电子,在通过对光电子信息进行处理,即可得到样品中元素的种类、含量和化学环境的相关信息。使用X射线光电子能谱仪对NiCoO2@N-C-X的组成与所含元素氧化态进行深度分析,在测试时保持工作电压为12.5 kV,灯丝电流16 mA,进行多次循环的信号累加。测试结果如图7所示,在全谱中可以清晰的观察到样品中有Ni、Co、O、C、N这5种元素,且它们所含的原子百分比分别为1.73%、1.67%、21.39%、72.13%、3.08%。通过以上数据可以发现Ni、Co元素含量比例接近1∶1。图7b为Ni 2p谱图,其中位于854.8和872.5 eV处的发射峰与Ni2+的特征峰相对应;860.1、878.7 eV处的发射峰归属于Ni3+的特征峰。同理可知,钴也具有4个数值不同的特征峰,而这4个特征峰也分别代表了Co的两种不同价态。所制样品中存在Co3+/Co2+以及Ni3+/Ni2+的混合氧化态,为氧的吸附提供了更多更佳的附着位点,进而可以为不同价态离子之间电子的迁移提供较高的电导率与较好的储能平台。

a.NiCoO2@N-C;b.Ni 2p;c.Co 2p;d.O 1s;e.C 1s;f.N 1s
图7 NiCoO2@N-C的XPS全谱以及各元素拟合分谱
Fig.7 XPS full spectrum of NiCoO2@N-C and fitting spectrum of each element
图7d为O 1s谱图,529.4 eV处的发射峰对应金属-氧键(M—O)的特征峰;532.7 eV处的峰是由NiCoO2@N-C中所包含的OH-基团引起的;在531.0 eV处的峰强最高说明所制备的样品具有低氧配位的缺陷位点,可以为化学反应提供更多更好的附着位点,提高电化学性能。如图7e所示,C 1s能谱中有283.9、284.7以及288.1 eV这3个峰,可分别与C—C、C—N以及C![]() O这3个化学键相对应。C—N键的存在表明过渡金属氧化物中存在氮源掺杂。图7f为N 1s谱图,从右到左依次分成吡啶-N、吡咯-N以及季铵-N这3组特征峰,其中季铵-N的存在将非常有利于电极材料中电子的运动。位于399.1 eV处的发射峰暴露了碳层的缺陷位点,这个缺陷位点也为电荷的储存提供了更多的附着平台。XPS进一步证明了氮源已经成功被分散在NiCoO2表面,这也与前面所运用的多种表征手段得出的结论高一致。
O这3个化学键相对应。C—N键的存在表明过渡金属氧化物中存在氮源掺杂。图7f为N 1s谱图,从右到左依次分成吡啶-N、吡咯-N以及季铵-N这3组特征峰,其中季铵-N的存在将非常有利于电极材料中电子的运动。位于399.1 eV处的发射峰暴露了碳层的缺陷位点,这个缺陷位点也为电荷的储存提供了更多的附着平台。XPS进一步证明了氮源已经成功被分散在NiCoO2表面,这也与前面所运用的多种表征手段得出的结论高一致。
拟合峰面积比与其原子含量相对应,所制备的样品中Ni2+/Ni3+以及Co2+/Co3+的拟合峰面积如表2、3所示,从表中可以看到Ni2+/Ni3+的面积比始终保持在1.04,这表明氮源的掺杂对于样品中Ni的价态并没有明显的影响。然而,Co2+/Co3+在样品中的面积比分别为0.64、0.99、0.86、0.71。测试结果表明,当引入氮源时,Co离子相较于Ni离子更容易被还原成低氧化态,为电子的迁移提供了更多的附着位点和通道。
表2 NiCoO2与NiCoO2@N-C-X的Ni 2p的表面结合能与原子百分比
Tab.2 Surface binding energy and atomic percentage of NiCoO2 and Ni 2p of NiCoO2@N-C-X

SampleNi2+at/%Ni3+at/%Ni2+/Ni3+NiCoO2854.850.93855.649.071.04NiCoO2@N-C-1855.050.93855.949.071.04NiCoO2@N-C-2854.950.93855.849.071.04NiCoO2@N-C-3854,950.93855.649.071.04
表3 NiCoO2与NiCoO2@N-C-X的Co 2p的表面结合能与原子百分比
Tab.3 Surface binding energy and atomic percentage of NiCoO2 and Co 2p of NiCoO2@N-C-X
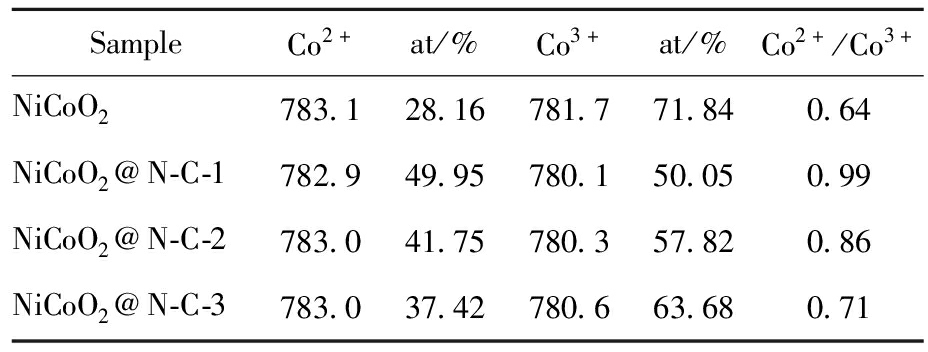
SampleCo2+at/%Co3+at/%Co2+/Co3+NiCoO2783.128.16781.771.840.64NiCoO2@N-C-1782.949.95780.150.050.99NiCoO2@N-C-2783.041.75780.357.820.86NiCoO2@N-C-3783.037.42780.663.680.71
2.2 电化学测试
本文所有涉及的电极材料的电化学测试均利用三电极体系测试,图8为本实验中所采用的电化学工作站示意图。以3 mol/L的KOH溶液为电解液、附着在泡沫镍上的电极材料为工作电极、饱和甘汞电极和铂电极分别为参比电极和对电极。工作电极在进行电化学测试之前需将其放入电解液中浸泡24 h,使电解液能够充分浸润电极材料。
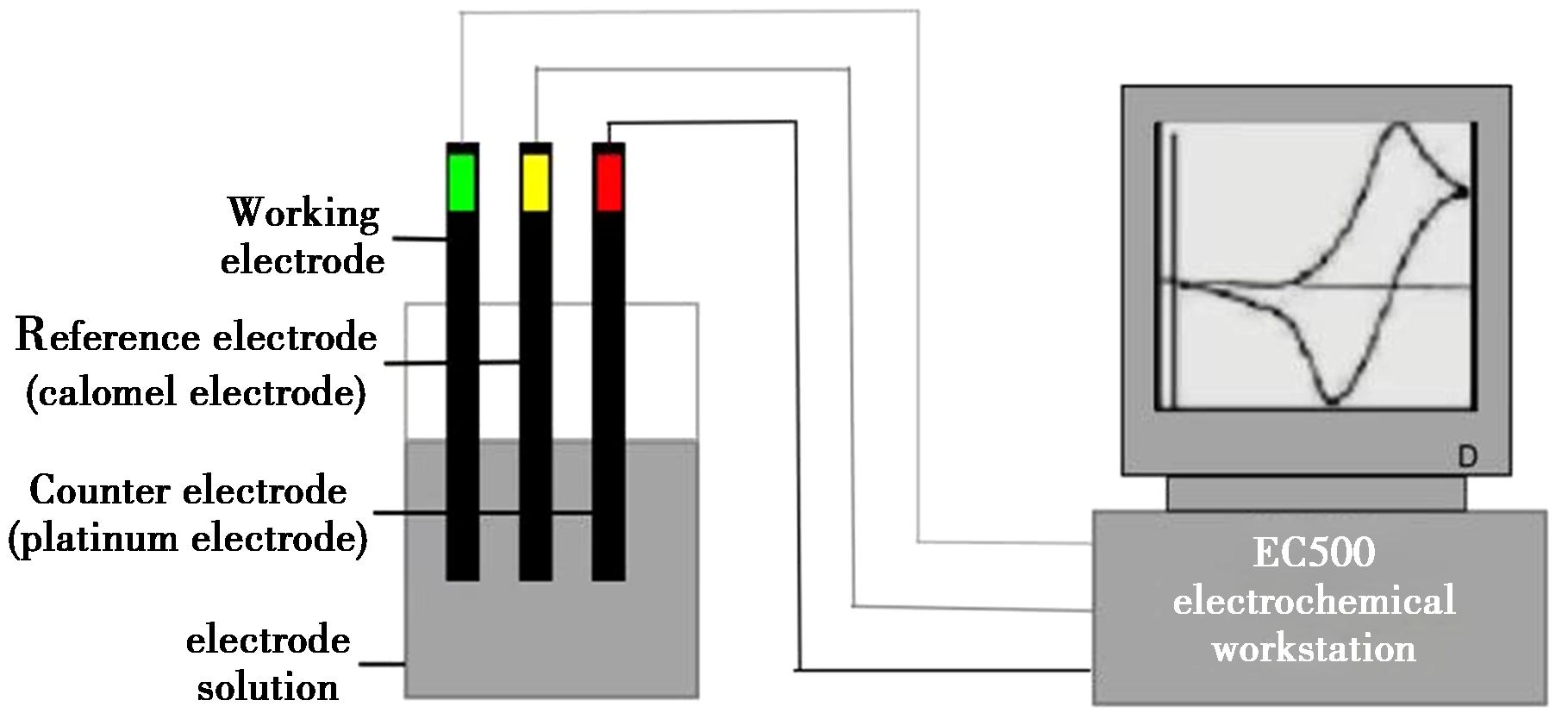
图8 电化学工作站示意图
Fig.8 Schematic diagram of electrochemical workstation
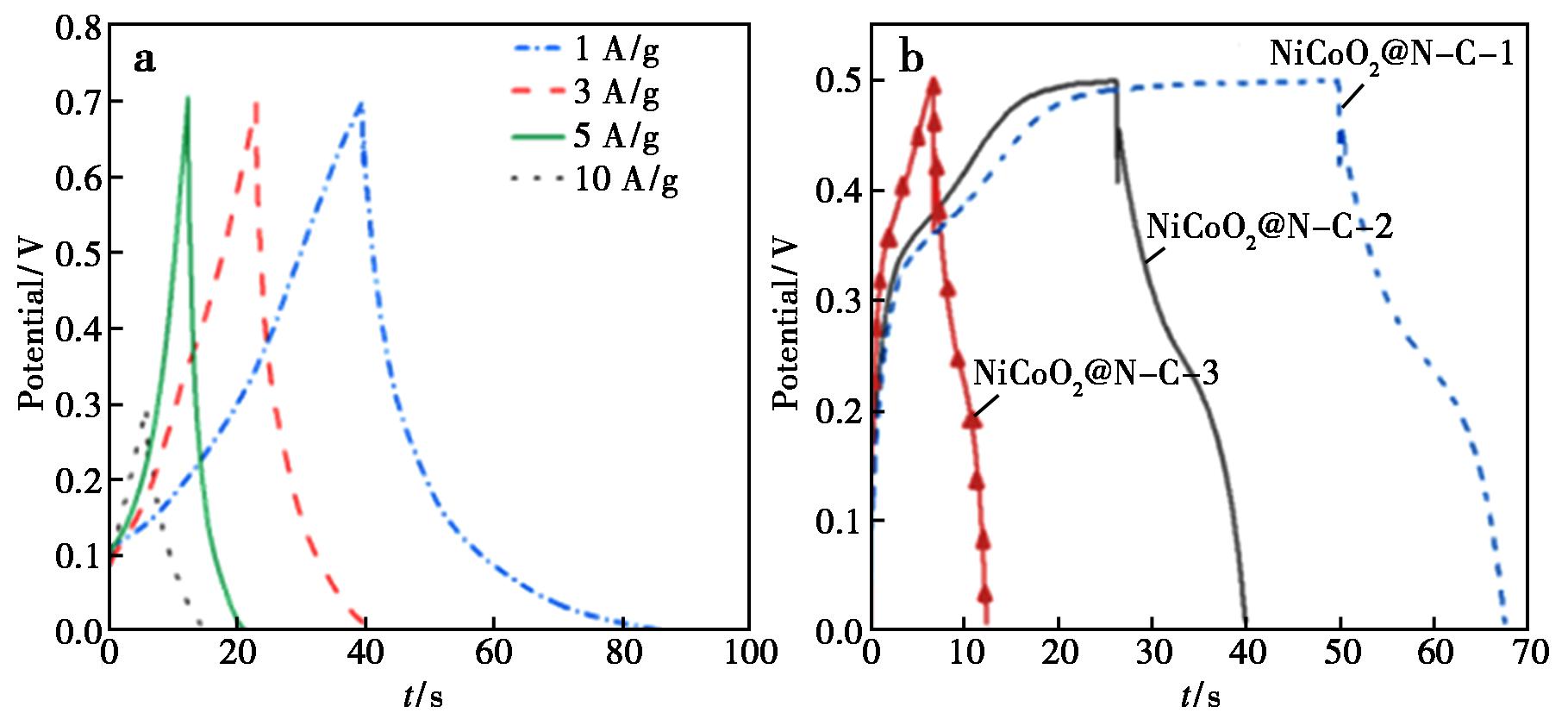
a.NiCoO2在不同电流密度下的GCD;b.NiCoO2@N-C-X(X=1、2、3)在同一电流密度下的GCD曲线
图9 NiCoO2及NiCoO2@N-C-X的GCD曲线
Fig.9 GCD curve of NiCoO2 and NiCoO2@N-C-X
2.2.1 恒流充放电曲线
GCD是以恒电流条件为基准对工作电极进行多次充放电的操作,通过获取电位与时间的变化曲线来探究工作电极的电化学性能。
在GCD曲线中可以观察到氮碳掺杂后的样品具有明显的充放电区间,通过计算得出电流密度为1 A/g时NiCoO2@N-C-X(X=1、2、3)的比电容分别为2 273、1 442、893 F/g。NiCoO2在电流密度分别为0.5、1、3、5、10 A/g条件下比电容分别为678、876、694、416、331 F/g。NiCoO2@N-C-1具有最高的比电容,为工作电极中离子的吸附和电解液中电子的跃迁提供了更多的附着位点。这一结果直接证明了氮碳掺杂对电极材料电化学性能的提升作用。综上所述,对电极材料进行非金属氮碳掺杂会提高其电化学性能,但过度被掺杂层包裹也会导致氮碳过量发生聚合而降低电化学性能,这一测试结果与前文BET、SEM、TEM所得出的结论相符合。
2.2.2 线性扫描伏安法
线性扫描伏安法(Linear sweep voltammetry,LSV)是通过比较施加电位与通过电流之间的变化关系,以此来反映电极的电化学活性。
NiCoO2及NiCoO2@N-C-X这4个样品的LSV曲线如图10所示,从整体上看,无论掺杂与否,所有电极材料的电流都随着电位的移动而呈现明显的加速增长趋势。通过进一步分析发现,在同一电位下,掺杂后样品的电流密度明显高于NiCoO2,表明氮掺杂层的存在提高了电极材料的电化学活性和导电性能。而NiCoO2@N-C-1的电流密度增长幅度最大,NiCoO2@N-C-2与NiCoO2@N-C-3电流密度增长幅度随着氮源掺杂质量的增长而降低。由此推断出过度的黄豆粉末附着在NiCoO2表面会减少电极材料的有效面积,进而导致电极材料中通过的电流减少、可附着位点减少、电化学活性降低影响其储能效果。这一结论与前面GCD的研究结果相吻合。
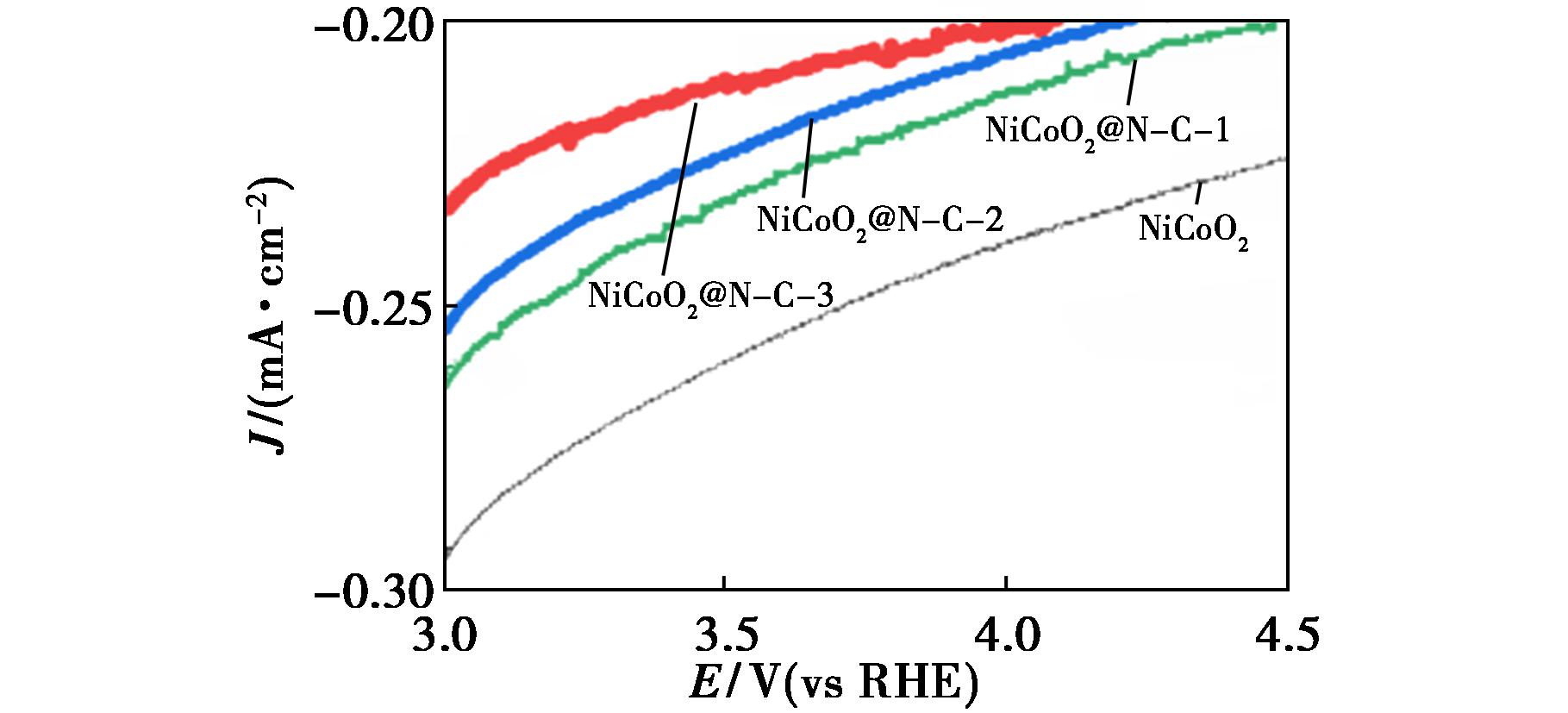
图10 NiCoO2、NiCoO2@N-C-X的LSV图
Fig.10 LSV diagram of NiCoO2 and NiCoO2@N-C-X
2.2.3 交流阻抗测试
交流阻抗(Electrochemical impedance spectroscopy,EIS)是在一定频率的影响下,施加一个微小正弦信号,以此干扰原本稳定的电极测试体系,获取因干扰而产生的有关电流或电位的响应,通过分析样品的Nyquist曲线判断电极材料的电阻信息等。
实验在0.01~100 000 Hz的频率范围及 5 mV的振幅内完成。电化学反应是由电荷的转移以及扩散共同作用,将Nyquist图等效拟合后的效果图如图11所示。在该图中,Nyquist图由高频区和低频区两部分构成。图中X轴的交点代表电阻(Rs)的大小,在高频区半圆直径反应电化学反应中电极与电解质表面电荷转移的电阻,而在低频区直线的斜率则代表了电解质所含的OH-离子在电极中的扩散过程。NiCoO2及NiCoO2@N-C的Rs分别为0.88及0.79 Ω。与NiCoO2相比,参与掺杂的NiCoO2@N-C-X具有较高的斜率。将参与掺杂的样品进行对比发现,相较于其他参与掺杂的样品,NiCoO2@N-C-1的斜率最陡峭,也更加符合理想电极材料的特性,进而证实了氮碳的掺杂有利于提高电极材料的导电与稳定性能。
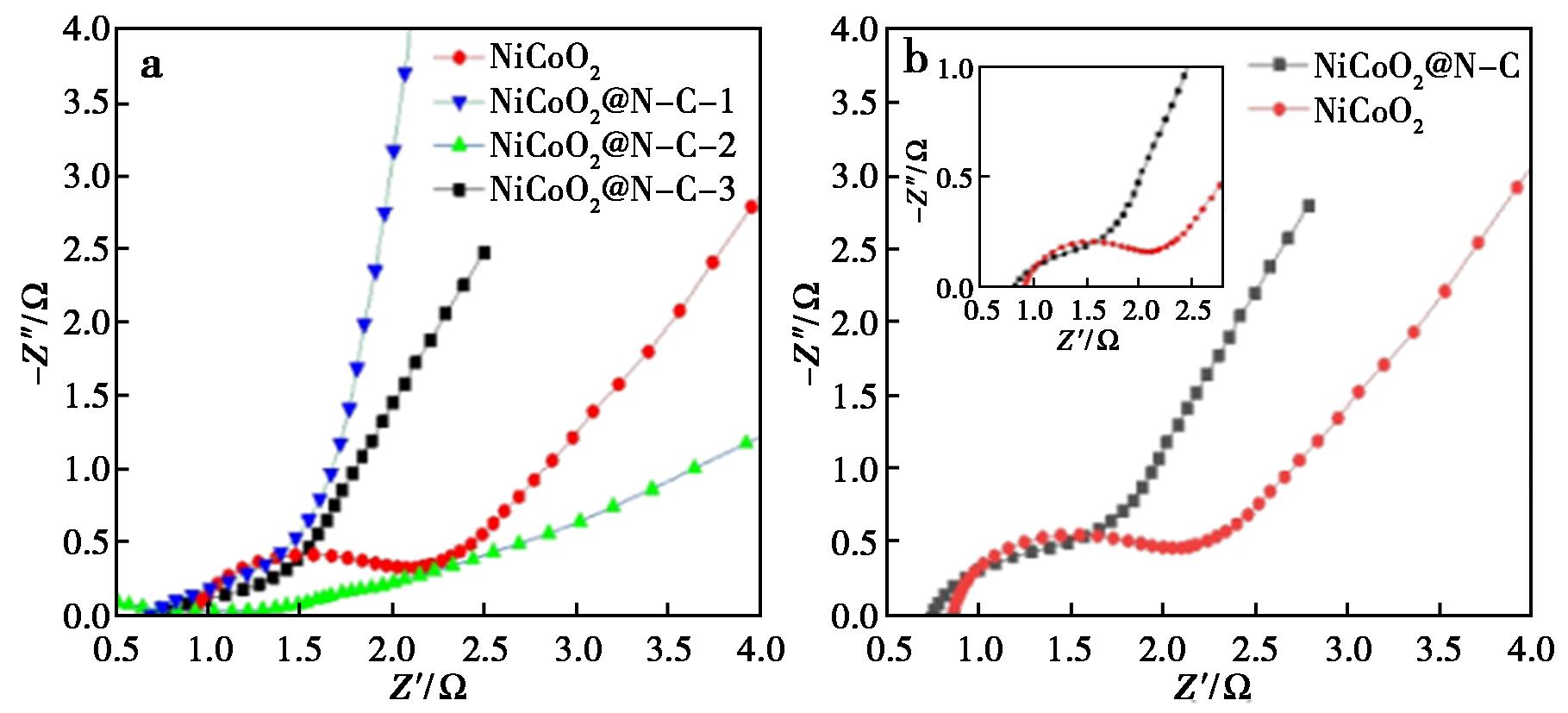
a.NiCoO2、NiCoO2@N-C-1、NiCoO2@N-C-2、NiCoO2@N-C-3;b.NiCoO2@N-C、NiCoO2
图11 NiCoO2以及NiCoO2@N-C-X的Nyquist图
Fig.11 Nyquist diagram of NiCoO2 and NiCoO2@N-C-X
2.2.4 循环伏安及稳定性测试
工作电极扫速为10~100 mV/s条件下的NiCoO2@N-C-1 CV曲线,如图12a所示,可以看出,该曲线呈类矩形的形状,表明工作电极具有良好的电化学双电层电容行为,表现出较高的响应电流和比电容。图12b表明,NiCoO2@N-C-1组装后在电流密度为5 A/g条件下历经20 000次循环后其初始电容保持率为97.8%,表明其具有优异的循环稳定性。
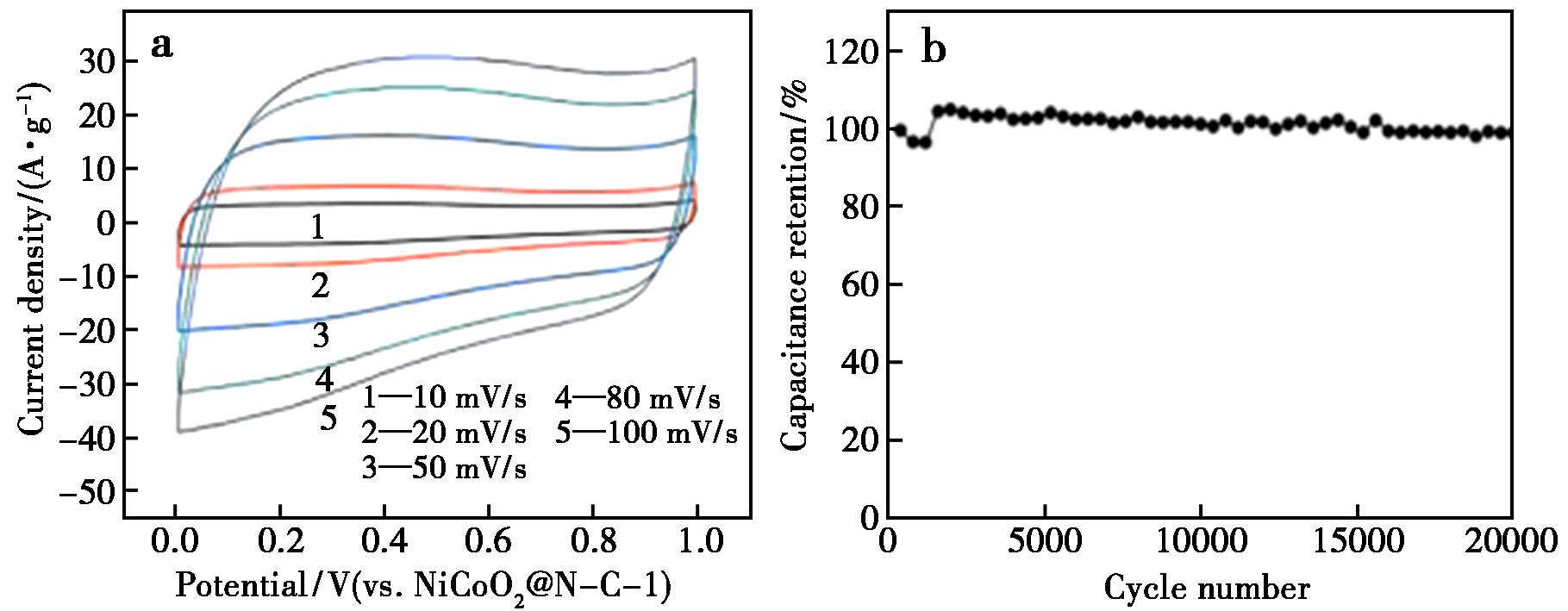
图12 a.NiCoO2@N-C-1的CV图;b.电流密度为5 A/g时NiCoO2@N-C-1的循环稳定性
Fig.12 a.CV diagram of NiCoO2@N-C-1;b.Cyclic stability of NiCoO2@N-C-1 with current density of 5 A/g
本文研究了氮碳掺杂对镍钴基电极材料电化学性能和储能效果的影响。运用多种表征手段和三电极测试体系,得出以下结论。
3.1 本研究所获得的NiCoO2与NiCoO2@N-C-X(X=1、2、3)的结构为中空海胆状纳米球,微粒中Co2+/Co3+、Ni2+/Ni3+为混合氧化态,有更高的导电率和更多的附着位点来储存电荷。对比分析掺杂前后样品的原子百分比推断出Co离子相较于Ni离子更容易被氧化成较低氧化态。
3.2 NiCoO2@N-C-X比NiCoO2具有更明显的充放电平台,可以为工作电极在电解液中的电子转移提供更好的附着位点,提高电极材料的导电性。LSV曲线中表明NiCoO2@N-C-1具有更大的电流密度,EIS测试发现NiCoO2@N-C-1的曲线斜率最大,所以NiCoO2@N-C-1的电化学活性、导电性和稳定性能最好。
3.3 超级电容器中NiCoO2@N-C-1与OH-在工作电极表面发生氧化还原反应增加其活性位点来储存电荷。氮源的适当引入会在一定程度上起到核壳型保护层的作用,这不仅会显著提高电极材料的导电与稳定性能,还能够为工作电极在电解液中的电子跃迁提供更多附着位点增强其储能效果。若过度引入了氮源会使氮源发生团聚、降低电极材料的比表面积,进而导致其电化学性能的衰减。
[1]Joeri R,Daniel H,Volker K,Keywan R,Leon C,Matthew G,Zebedee N,Malte M.Nature,2019,1:357-363.
[2]Kang Q,Lv T,Yuan Y.Sustainability,2021,13(13):7 425.
[3]Rong H,Li J L,Guo Z.Energy,2022,239(15):121 971.
[4]Hu X Y.Research on the Controlled Preparation and Energy Storage Mechanism of Nickel-Cobalt-Based Electrode Materials.Beijing:University of Science and Technology Beijing,2022.
胡小雨.镍钴基电极材料的可控制备与储能机理研究.北京:北京科技大学,2022.
[5]Anjali J,Rajini P A,Ronghua W,Jongmin L.Small,2017,13(11):1 603 102.
[6]Huang S Y,Li S,Ding W,Wang Y.Chem.Reagents,2022,44(5):691-696.
黄思赟,李帅,丁万,王一.化学试剂,2022,44(5):691-696.
[7]Xu F.Preparation of High-Performance Nickel Cobalt-Based Electrode Materials and Construction of Supercapacitors.Nanchang:Nanchang University,2021.
徐芳.高性能镍钴基电极材料的制备与超级电容器的构建.南昌:南昌大学,2021.
[8]Wang T Y,Han N,Jia D D,Li H Q,He X J.Chin.J.Inorg.Chem.,2023,39(2):309-316.
王天云,韩娜,贾德东,李宏强,何孝军.无机化学学报,2023,39(2):309-316.
[9]Dong S H.Research on Nickel Cobalt Layered Double Hydroxide Electrode Materials for Supercapacitors.Qingdao:Qingdao University of Science and Technology,2021.
董世豪.镍钴层状双金属氢氧化物超级电容器电极材料的研究.青岛:青岛科技大学,2021.
[10]An L L,Mi J.Chin.J.Appl.Chem.,2020,37(5):579-586.
安露露,米杰.应用化学,2020,37(5):579-586.
[11]Wan Y C,Zhan J,Chen J.J.Inorg.Mater.,2019,34(2):121-129.
万宇驰,湛菁,陈军.无机材料学报,2019,34(2):121-129.
[12]Mao Z D,Yang C,Hu Q,Sun T.Ship Electr.Technol.,2021,41(4):27-31.
毛振东,杨聪,胡强,孙涛.船电技术,2021,41(4):27-31.
[13]Li A,Wang F,Huang R W,You D,Zhang Y Y,Li X,Zhang Y J.Chem.Reagents,2023,45(9):61-69.
李傲,王飞,黄荣威,游丹,张义永,李雪,张英杰.化学试剂,2023,45(9):61-69.
[14]Shi W M,Liu Y H,Lv X L,Zhang R R,He Y.Micronanoelectron.Technol.,2022,59(11):1 105-1 118.
石文明,刘意华,吕湘连,张瑞荣,何洋.微纳电子技术,2022,59(11):1 105-1 118.
[15]Zou R J,Zhang Z Y,Yuen M F,Hu J Q,Chun S L,Zhang W J.Sci.Rep.,2015,5(1):7 862.
[16]Gi D P,Jung S C,Yun C K.Nano Energy,2015,17(1):17-26.
[17]Wang H,Li J M,Li K,Lin Y P,Chen J M,Gao L J,Nicolosi V,Xu X,Lee J M.Chem.Soc.Rev.,2021,50(1):1 354-1 390.
[18]Wang X D,Zhou H P,Zhang D K,Bi M Y,Feng J J,Chen S J.J.Power Sources,2018,387(31):1-8.
[19]Wang M,Xie Y H,You M Y,Han J,Wang Y Z,Zhu T.Mater.Rep.,2016,30(28):248-252.
王敏,谢元华,由美雁,韩进,王有昭,朱彤.材料导报,2016,30(28):248-252.
[20]Zhai H Y,Zou Z L,Li M Y,Zhang L Y,Zhou W J.Chin.J.Inorg.Chem.,2023,39(4):627-636.
翟好英,邹自力,李明宇,张理元,周文俊.无机化学学报,2023,39(4):627-636.
[21]Sun X W,Bai J,Li C P,Liang H O,Xu T,Sun W Y.Acta Mater.Compositae Sin.,2022,239(4):1-16.
孙兴伟,白杰,李春萍,梁海欧,许瞳,孙炜岩.复合材料学报,2022,239(4):1-16.
[22]Wang L C.Preparation and Capacitance Characteristics of Electrode Materials for flexible Supercapacitors.Tianjin:Tianjin University of Technology,2019.
王龄昌.柔性超级电容器电极材料的制备及电容特性研究.天津:天津理工大学,2019.
[23]Lin Y X.Structural Design of Conductive Polymer Flexible Composite Electrode and Its Application in Supercapacitors.Guangzhou:Guangdong University of Technology,2020.
林迎曦.导电聚合物柔性复合电极的结构设计及其在超级电容器中的应用.广州:广东工业大学,2020.