木贼(Equisetum hyemale)隶属于木贼科木贼属草本植物,其分布范围涵盖亚洲、欧洲、北美洲等地,在我国主要产于华北、华中、华南和西南各省[1]。木贼的入药部位为地上部分,其主要功效是疏散风热、明目退翳,对角膜炎、结膜炎、高血压、鼻衄、疳证、疣等疾病具有较好的治疗作用[2,3]。以往研究多聚焦于木贼提取物的药效考察和药理活性测定,而对其丰富的化学成分知之甚少,研究者很难从“成分-药效-代谢-靶点”多维度阐明木贼的药效物质基础及药理作用机制,进而阻碍了木贼在临床上的推广应用和产品开发。由此可知,在中药的研究开发过程中,化学成分研究是最为基础却又最为关键的步骤之一。因此,快速、准确地鉴定木贼中的化学成分已成为推进木贼临床应用以及药物研发迫切需要解决的难题。常规的化学成分分析主要依赖柱层析分离及核磁波谱鉴定方法,整个过程的分析时间较长、解析难度大、材料消耗多、分离过程中容易丢失含量较少的成分,成分表征受限。与常规的化学成分分析相比,液-质联用技术分析具备分析周期短、灵敏度高、分离度良好以及成分表征更为全面的优点,近年来被广泛应用于中药材及中药复方制剂的化学成分研究[4]。基于此,本研究运用 UPLC-Q-Exactive-Plus-Orbitrap-MS技术快速鉴定木贼的化学成分,为木贼的药效物质基础、作用机制研究及产品开发提供科学依据。
1 实验部分
1.1 主要仪器与试剂
Vanquis型超高效液相色谱仪-Q-Exactive Plus型高分辨质谱仪联用系统(美国Thermo Fisher科技公司);800 C型多用途粉碎机(永康市红太阳机电有限公司);KQ5200 B型高频声波清洗装置(昆山市超声仪器有限公司);SSY-T型超纯净水制备装置(四川水思源环境科技有限公司);EL 204型电子分析天平(瑞士梅特勒-托利多仪器有限公司);XK-16TR型高速离心机(湖南湘科仪器设备公司)。
L-苯丙氨酸、壬二酸、苹果酸、柠檬酸、香豆素对照品(纯度≥98%,批号依次为:wkq22092706、wkq21060402、wkq22100801、wkq23031308、wkq23032810,四川维克奇生物科技有限公司);用于质谱分析的高纯度甲酸(美国Thermo Fisher科技公司);用于质谱分析的高纯度乙腈、甲醇(德国默克公司);用于色谱分析的高纯度乙醇(天津市科密欧化学试剂有限公司);所有用水均为超纯水。
木贼药材采集自贵州省清镇市红枫湖镇右二村,经贵州医科大学贵州省药物制剂重点实验室刘春花副教授鉴别,确定为木贼科植物木贼 Equisetum hyemale的全草,样本(NO.20220703)保存于贵州医科大学贵州省药物制剂重点实验室药效物质基础组。
1.2 实验方法
1.2.1 供试品溶液的制备
取木贼地上部分,晒干后粉碎,过3号筛。精密称取1 g上述粉末,加入25 mL V(乙醇)∶V(水)=1∶1溶液,称定质量,超声振荡(频率 40 kHz,功率240 W)提取60 min,放至室温,用 V(乙醇)∶V(水)=1∶1溶液补足减失的质量,充分混匀后快速抽滤,滤液离心5 min(12 000 r/min),取上清液,即得。
1.2.2 对照品溶液的制备
分别取1.1各对照品适量,精密称定,用 V(乙醇)∶V(水)=1∶1溶液配制成每1 mL含1 mg的对照品储配液,分别精密量取上述各对照品储备液适量予以混合,用V(乙醇)∶V(水)=1∶1溶液稀释成10 μg/mL的混合对照品溶液,离心 5 min(12 000 r/min),取上清液即得。
1.2.3 色谱条件
色谱柱:Hypersil GOLD C18柱(100 mm×2.1 mm,1.9 μm);柱温40 ℃;进样量1 μL;流速0.3 mL/min;流动相为乙腈(B)-0.1%甲酸水溶液(A),0~1 min,5% B;1~15 min,5% B→30% B;15~25 min,30% B→60% B;25~28 min,60% B→95% B;28~30 min,95% B。
1.2.4 质谱条件
采用电喷雾离子源,喷雾电压为3 500 V(正模式)和2 500 V(负模式),鞘气流速为30 mL/min,辅助气流速为10 mL/min,雾化气温度为350 ℃;扫描模式为全扫描+数据依赖二级扫描的正负离子交换模式,扫描范围为100~1 500 m/z,毛细管温度为320 ℃,离子透镜电压为50.0 V,碰撞能梯度为20、40、60 eV,一级分辨率为 70 000,二级分辨率为17 500。
1.2.5 数据分析
将采集的原始数据导入Compound Discoverer 3.1软件进行基线校正、峰校准、去卷积分析等处理,以峰面积阈值80 000、实测值与理论值的偏差小于5、匹配分值不低于80为前置条件,将质谱信息与Thermo Fisher Scientific云端质谱数据库mzCloud(https://www.mzcloud.org/)、PubChem(https://pubchem.ncbi.nlm.nih.gov/)网络数据库、中药成分高分辨质谱本地数据库(Orbitrap Tditional Chinese Medicine Library,OTCML)进行匹配,将匹配结果中化合物的质谱数据逐一与文献[5-34]对比,从而快速鉴定木贼的化学成分。部分化合物的结构通过与对照品的质谱数据加以对比来进一步确认。
2 结果与讨论
2.1 化学成分分析
取1.2.1、1.2.2供试品溶液和混合对照品溶液,按1.2.3、1.2.4色谱-质谱条件进行检测,记录原始数据。采用1.2.5数据分析方法分析化合物结构,共鉴定了70个化合物,包括22个有机酸类、15个氨基酸类、12个生物碱类、7个核苷类、4个糖类、3个黄酮类、2个芳香醛及5个其他成分。木贼供试品在正、负离子模式下的总离子流图见图1,鉴定化合物结果见表1。
表1 木贼的化学成分鉴定结果注
Tab.1 Results of chemical composition identification of Equisetum hyemale
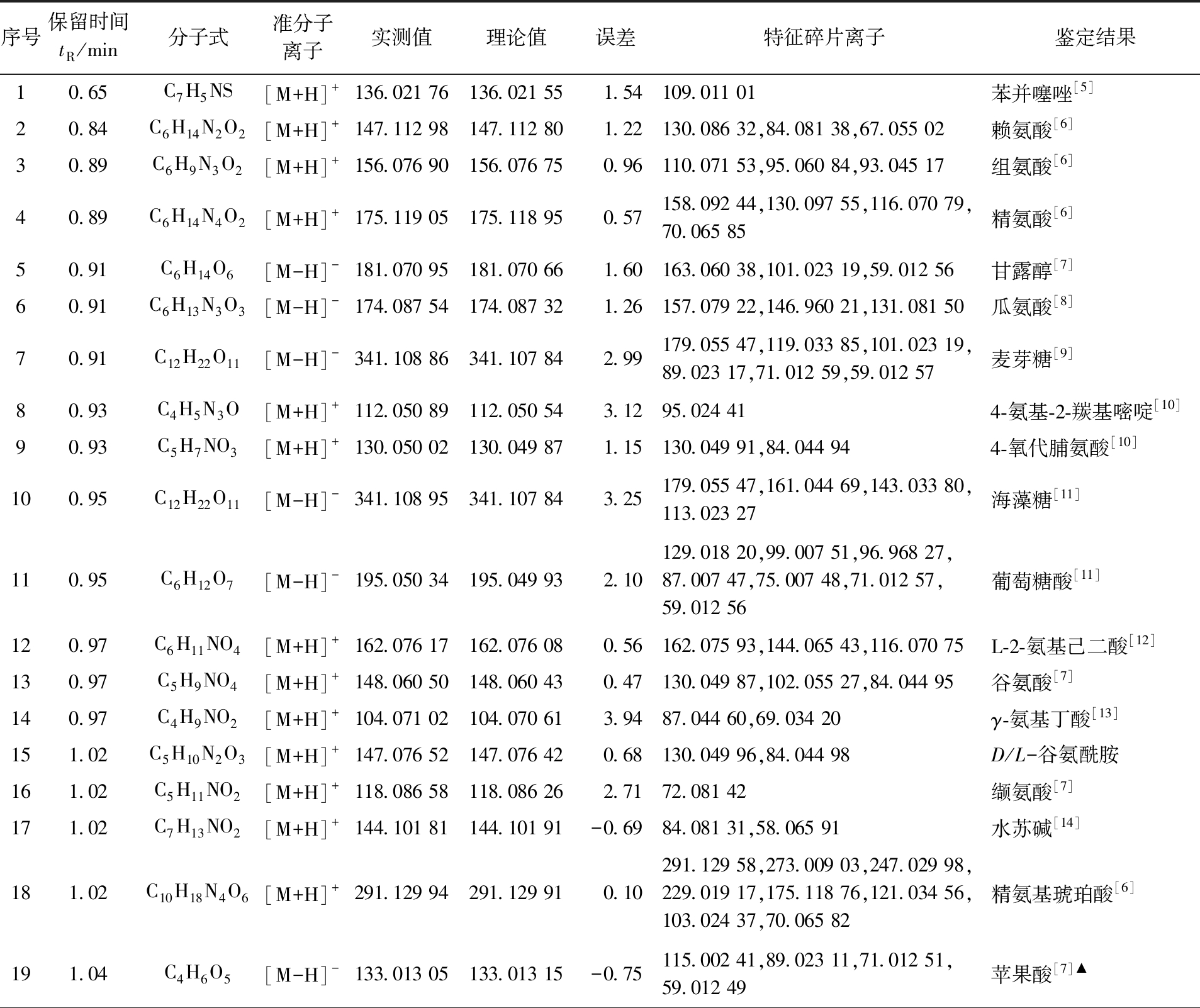
注:▲表示与对照品对照。
序号保留时间tR/min分子式准分子离子实测值理论值误差特征碎片离子鉴定结果10.65C7H5NS[M+H]+136.021 76136.021 551.54 109.011 01苯并噻唑[5]20.84C6H14N2O2[M+H]+147.112 98147.112 801.22130.086 32,84.081 38,67.055 02赖氨酸[6]30.89C6H9N3O2[M+H]+156.076 90156.076 750.96110.071 53,95.060 84,93.045 17组氨酸[6]40.89C6H14N4O2[M+H]+175.119 05175.118 950.57158.092 44,130.097 55,116.070 79,70.065 85精氨酸[6]50.91C6H14O6[M-H]-181.070 95181.070 661.60163.060 38,101.023 19,59.012 56甘露醇[7]60.91C6H13N3O3[M-H]-174.087 54174.087 321.26157.079 22,146.960 21,131.081 50瓜氨酸[8]70.91C12H22O11[M-H]-341.108 86341.107 842.99179.055 47,119.033 85,101.023 19,89.023 17,71.012 59,59.012 57麦芽糖[9]80.93C4H5N3O[M+H]+112.050 89112.050 543.1295.024 414-氨基-2-羰基嘧啶[10]90.93C5H7NO3[M+H]+130.050 02130.049 871.15 130.049 91,84.044 944-氧代脯氨酸[10]100.95C12H22O11[M-H]-341.108 95341.107 843.25179.055 47,161.044 69,143.033 80,113.023 27海藻糖[11]110.95C6H12O7[M-H]-195.050 34195.049 932.10 129.018 20,99.007 51,96.968 27,87.007 47,75.007 48,71.012 57,59.012 56葡萄糖酸[11]120.97C6H11NO4[M+H]+162.076 17162.076 080.56162.075 93,144.065 43,116.070 75L-2-氨基己二酸[12]130.97C5H9NO4[M+H]+148.060 50148.060 430.47130.049 87,102.055 27,84.044 95谷氨酸[7]140.97C4H9NO2[M+H]+104.071 02104.070 613.9487.044 60,69.034 20γ-氨基丁酸[13]151.02C5H10N2O3[M+H]+147.076 52147.076 420.68130.049 96,84.044 98D/L-谷氨酰胺161.02C5H11NO2[M+H]+118.086 58118.086 262.7172.081 42缬氨酸[7]171.02C7H13NO2[M+H]+144.101 81144.101 91-0.6984.081 31,58.065 91水苏碱[14]181.02C10H18N4O6[M+H]+291.129 94291.129 910.10 291.129 58,273.009 03,247.029 98,229.019 17,175.118 76,121.034 56,103.024 37,70.065 82精氨基琥珀酸[6]191.04C4H6O5[M-H]-133.013 05133.013 15-0.75115.002 41,89.023 11,71.012 51,59.012 49苹果酸[7]▲
续表
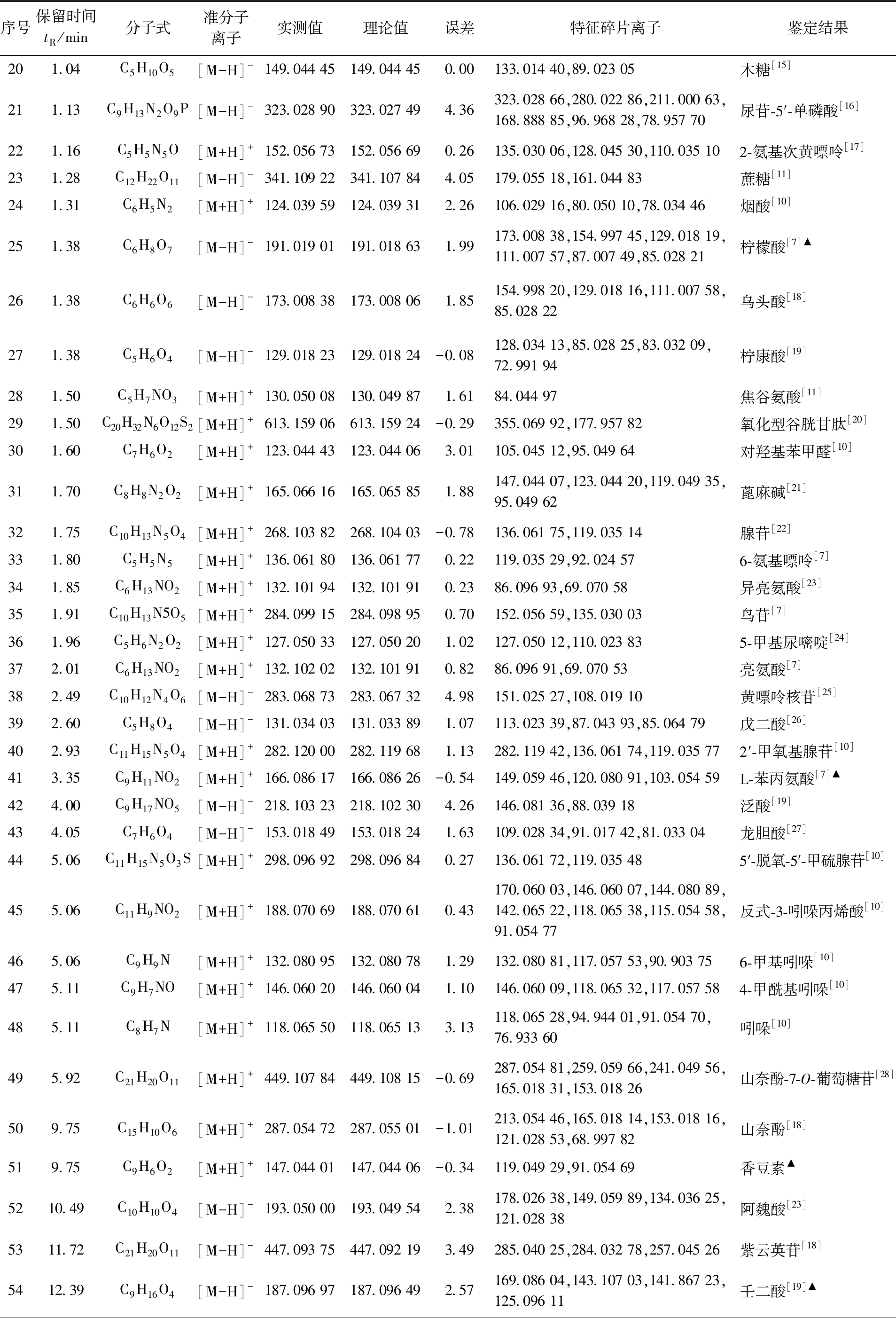
序号保留时间tR/min分子式准分子离子实测值理论值误差特征碎片离子鉴定结果201.04C5H10O5[M-H]-149.044 45149.044 450.00133.014 40,89.023 05木糖[15]211.13C9H13N2O9P[M-H]-323.028 90323.027 494.36323.028 66,280.022 86,211.000 63,168.888 85,96.968 28,78.957 70尿苷-5′-单磷酸[16]221.16C5H5N5O[M+H]+152.056 73152.056 690.26135.030 06,128.045 30,110.035 102-氨基次黄嘌呤[17]231.28C12H22O11[M-H]-341.109 22341.107 844.05179.055 18,161.044 83蔗糖[11]241.31C6H5N2[M+H]+124.039 59124.039 312.26106.029 16,80.050 10,78.034 46烟酸[10]251.38C6H8O7[M-H]-191.019 01191.018 631.99173.008 38,154.997 45,129.018 19,111.007 57,87.007 49,85.028 21柠檬酸[7]▲261.38C6H6O6[M-H]-173.008 38173.008 061.85154.998 20,129.018 16,111.007 58,85.028 22乌头酸[18]271.38C5H6O4[M-H]-129.018 23129.018 24-0.08128.034 13,85.028 25,83.032 09,72.991 94柠康酸[19]281.50C5H7NO3[M+H]+130.050 08130.049 871.6184.044 97焦谷氨酸[11]291.50C20H32N6O12S2[M+H]+613.159 06613.159 24-0.29355.069 92,177.957 82氧化型谷胱甘肽[20]301.60C7H6O2[M+H]+123.044 43123.044 063.01105.045 12,95.049 64对羟基苯甲醛[10]311.70C8H8N2O2[M+H]+165.066 16165.065 851.88147.044 07,123.044 20,119.049 35,95.049 62蓖麻碱[21]321.75C10H13N5O4[M+H]+268.103 82268.104 03-0.78136.061 75,119.035 14腺苷[22]331.80C5H5N5[M+H]+136.061 80136.061 770.22119.035 29,92.024 576-氨基嘌呤[7]341.85C6H13NO2[M+H]+132.101 94132.101 910.2386.096 93,69.070 58异亮氨酸[23]351.91C10H13N5O5[M+H]+284.099 15284.098 950.70152.056 59,135.030 03鸟苷[7]361.96C5H6N2O2[M+H]+127.050 33127.050 201.02127.050 12,110.023 835-甲基尿嘧啶[24]372.01C6H13NO2[M+H]+132.102 02132.101 910.8286.096 91,69.070 53亮氨酸[7]382.49C10H12N4O6[M-H]-283.068 73283.067 324.98151.025 27,108.019 10黄嘌呤核苷[25]392.60C5H8O4[M-H]-131.034 03131.033 891.07113.023 39,87.043 93,85.064 79戊二酸[26]402.93C11H15N5O4[M+H]+282.120 00282.119 681.13 282.119 42,136.061 74,119.035 772′-甲氧基腺苷[10]413.35C9H11NO2[M+H]+166.086 17166.086 26-0.54149.059 46,120.080 91,103.054 59L-苯丙氨酸[7]▲424.00C9H17NO5[M-H]-218.103 23218.102 304.26146.081 36,88.039 18泛酸[19]434.05C7H6O4[M-H]-153.018 49153.018 241.63109.028 34,91.017 42,81.033 04龙胆酸[27]445.06C11H15N5O3S[M+H]+298.096 92298.096 840.27136.061 72,119.035 485′-脱氧-5′-甲硫腺苷[10]455.06C11H9NO2[M+H]+188.070 69188.070 610.43170.060 03,146.060 07,144.080 89,142.065 22,118.065 38,115.054 58,91.054 77反式-3-吲哚丙烯酸[10]465.06C9H9N[M+H]+132.080 95132.080 781.29 132.080 81,117.057 53,90.903 756-甲基吲哚[10]475.11C9H7NO[M+H]+146.060 20146.060 041.10146.060 09,118.065 32,117.057 584-甲酰基吲哚[10]485.11C8H7N[M+H]+118.065 50118.065 133.13 118.065 28,94.944 01,91.054 70,76.933 60吲哚[10]495.92C21H20O11[M+H]+449.107 84449.108 15-0.69287.054 81,259.059 66,241.049 56,165.018 31,153.018 26山奈酚-7-O-葡萄糖苷[28]509.75C15H10O6[M+H]+287.054 72287.055 01-1.01213.054 46,165.018 14,153.018 16,121.028 53,68.997 82山奈酚[18]519.75C9H6O2[M+H]+147.044 01147.044 06-0.34 119.049 29,91.054 69香豆素▲5210.49C10H10O4[M-H]-193.050 00193.049 542.38178.026 38,149.059 89,134.036 25,121.028 38阿魏酸[23]5311.72C21H20O11[M-H]-447.093 75447.092 193.49285.040 25,284.032 78,257.045 26紫云英苷[18]5412.39C9H16O4[M-H]-187.096 97187.096 492.57169.086 04,143.107 03,141.867 23,125.096 11壬二酸[19]▲
续表
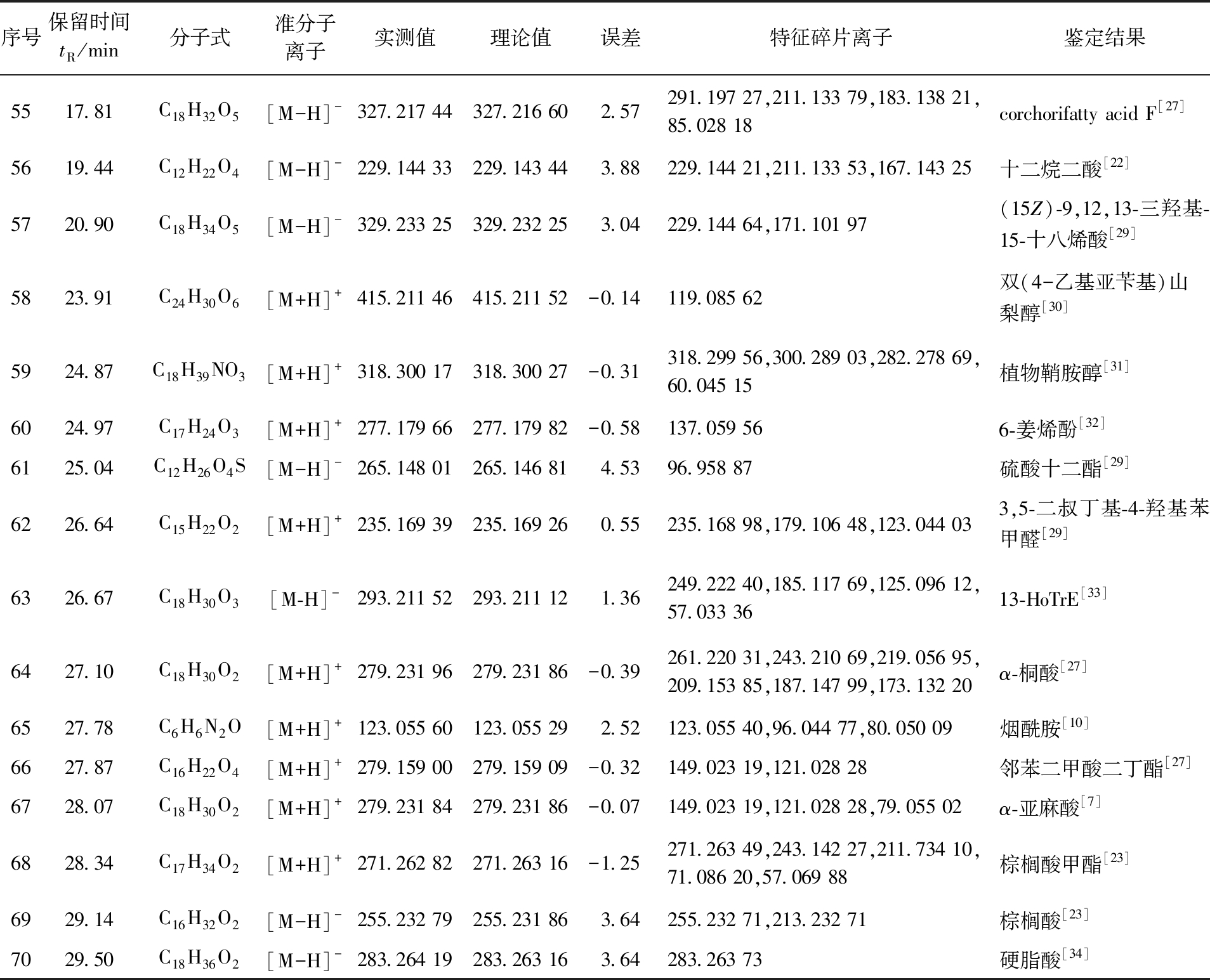
序号保留时间tR/min分子式准分子离子实测值理论值误差特征碎片离子鉴定结果5517.81C18H32O5[M-H]-327.217 44327.216 602.57291.197 27,211.133 79,183.138 21,85.028 18corchorifatty acid F[27]5619.44C12H22O4[M-H]-229.144 33229.143 443.88 229.144 21,211.133 53,167.143 25十二烷二酸[22]5720.90C18H34O5[M-H]-329.233 25329.232 253.04229.144 64,171.101 97(15Z)-9,12,13-三羟基-15-十八烯酸[29]5823.91C24H30O6[M+H]+415.211 46415.211 52-0.14119.085 62双(4-乙基亚苄基)山梨醇[30]5924.87C18H39NO3[M+H]+318.300 17318.300 27-0.31 318.299 56,300.289 03,282.278 69,60.045 15植物鞘胺醇[31]6024.97C17H24O3[M+H]+277.179 66277.179 82-0.58137.059 566-姜烯酚[32]6125.04C12H26O4S[M-H]-265.148 01265.146 814.5396.958 87硫酸十二酯[29]6226.64C15H22O2[M+H]+235.169 39235.169 260.55 235.168 98,179.106 48,123.044 033,5-二叔丁基-4-羟基苯甲醛[29]6326.67C18H30O3[M-H]-293.211 52293.211 121.36 249.222 40,185.117 69,125.096 12,57.033 3613-HoTrE[33]6427.10C18H30O2[M+H]+279.231 96279.231 86-0.39261.220 31,243.210 69,219.056 95,209.153 85,187.147 99,173.132 20α-桐酸[27]6527.78C6H6N2O[M+H]+123.055 60123.055 292.52123.055 40,96.044 77,80.050 09烟酰胺[10]6627.87C16H22O4[M+H]+279.159 00279.159 09-0.32 149.023 19,121.028 28邻苯二甲酸二丁酯[27]6728.07C18H30O2[M+H]+279.231 84279.231 86-0.07149.023 19,121.028 28,79.055 02α-亚麻酸[7]6828.34C17H34O2[M+H]+271.262 82271.263 16-1.25 271.263 49,243.142 27,211.734 10,71.086 20,57.069 88棕榈酸甲酯[23]6929.14C16H32O2[M-H]-255.232 79255.231 863.64 255.232 71,213.232 71棕榈酸[23]7029.50C18H36O2[M-H]-283.264 19283.263 163.64283.263 73硬脂酸[34]
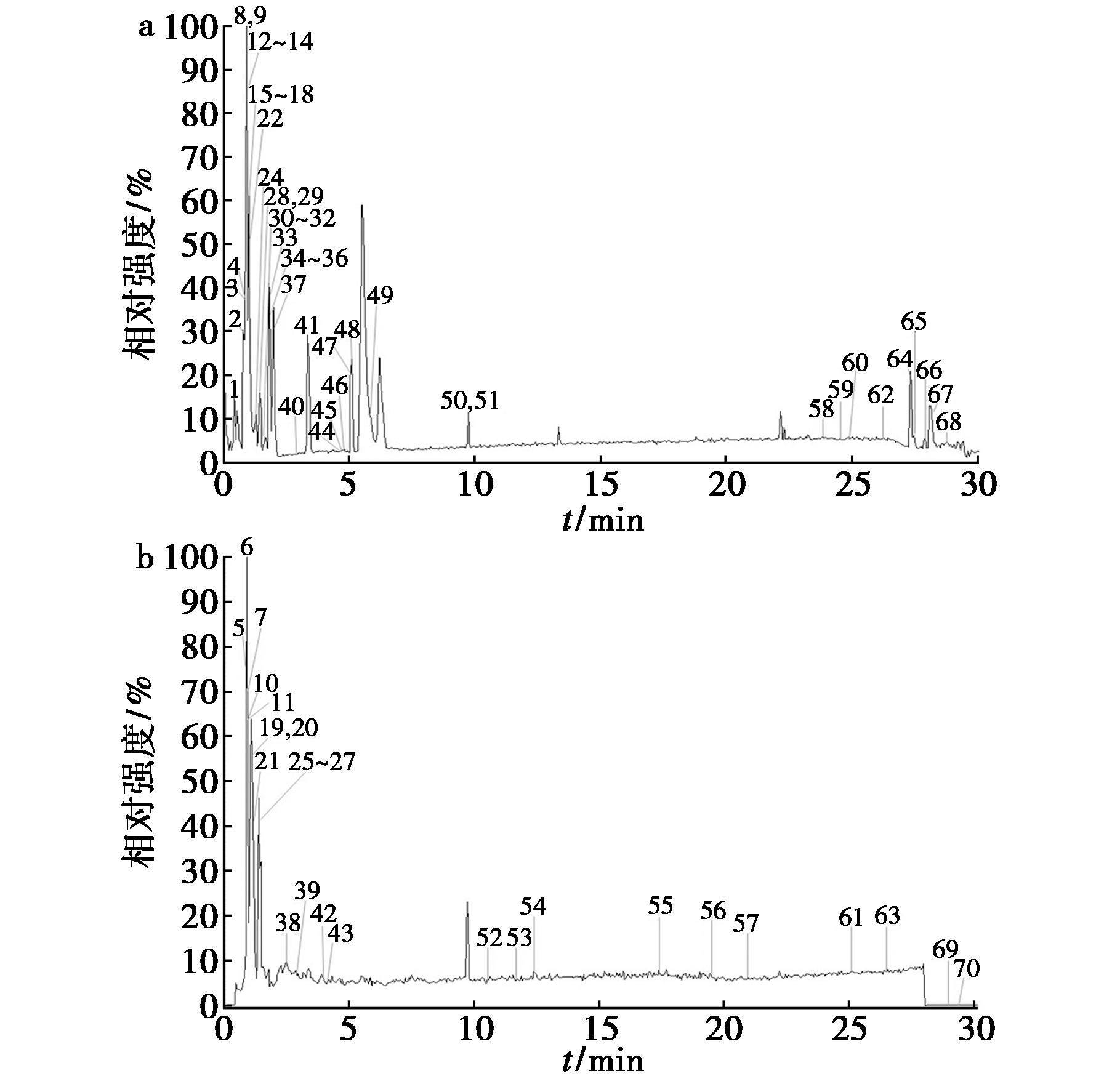
图1 木贼样品在正(a)、负(b)离子模式下的总离子流图
Fig.1 Total ion current diagram of Equisetum hyemale in positive (a) and negative (b) ion mode
2.2 主要成分的裂解规律分析
2.2.1 有机酸类成分
该类成分在高能碰撞下容易丢失中性小分子片段,①芳香酸或芳香酸酯的裂解容易发生在羧基或羧基衍生侧链,常丢失CH2、CH3、COOH、CO2等小分子,羟基取代的芳香环通常不发生裂解。②α断裂、β断裂及i断裂是链状有机酸和有机酸酯的经典断裂方式,从而容易丢失COOH、CH2COOH和CH2小分子片段,同时含有OH的有机酸容易丢失H2O。此外,含有不饱和基团的长链有机酸类化合物的裂解规律相对复杂,可发生重排反应。以阿魏酸(52,tR=10.49 min)、壬二酸(54,tR=12.39 min)和α-桐酸(64,tR=27.10 min)为例。
化合物52:在负离子模式下可见去质子化准分子离子m/z:193.050 00[M-H]-,质谱软件拟合分子式为C10H10O4,m/z:149.059 89[M-H-CO2]-是准分子离子丢失1分子CO2产生的特征碎片离子,接着该碎片离子丢失1分子CH3或1分子C2H4生成碎片离子m/z:134.036 25[M-H-CO2-CH3]-或m/z:121.028 38[M-H-CO2-C2H4]-;准分子离子也可先丢失1分子CH3得到碎片离子m/z:178.026 38[M-H-CH3]-,再失去1分子CO2得到碎片离子m/z:134.036 25[M-H-CH3-CO2]-。该化合物的二级质谱及裂解规律(图2)与文献[23]报道一致,推断为阿魏酸。
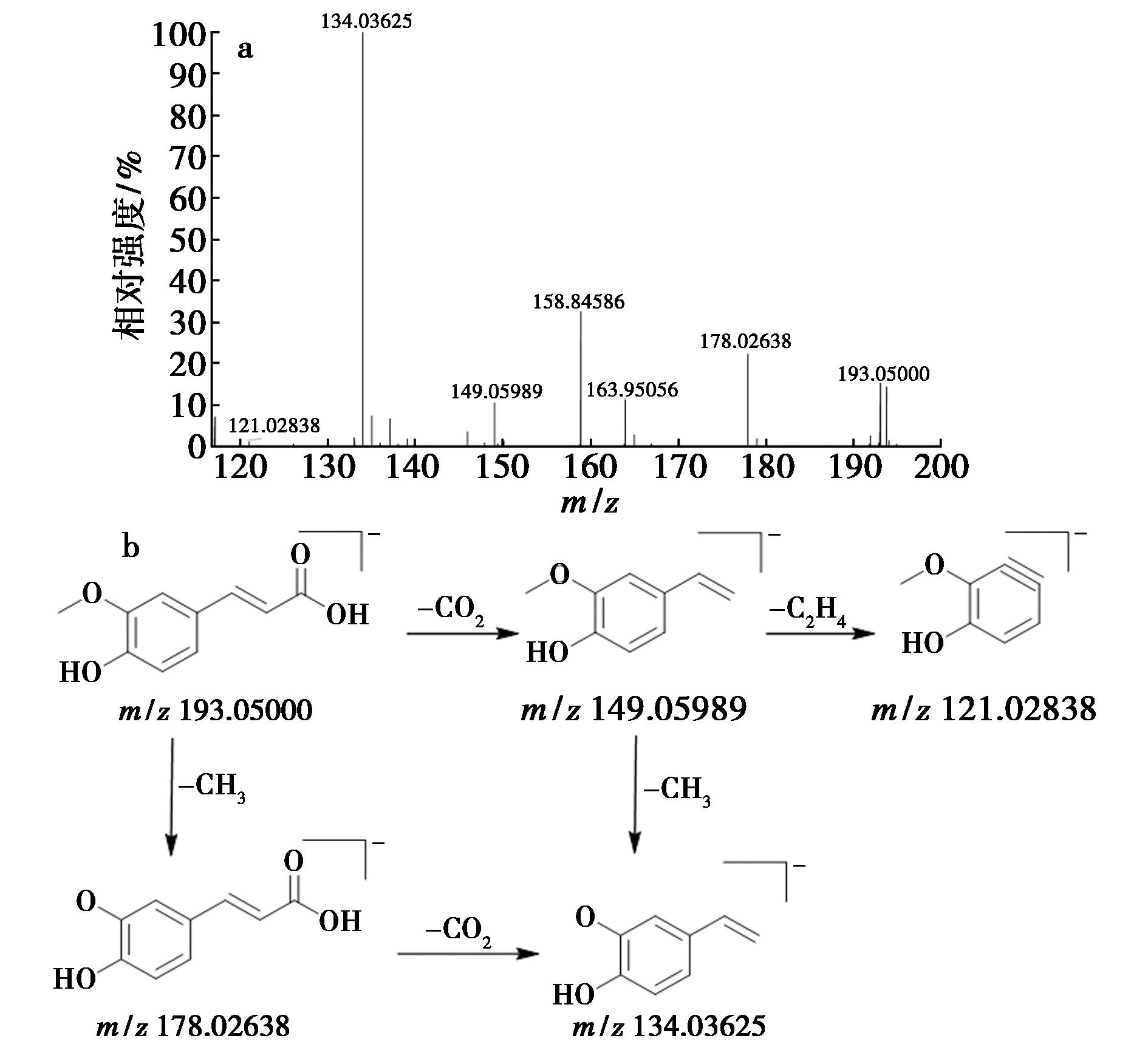
a.MS2图;b.裂解途径
图2 化合物52的质谱图及其裂解途径
Fig.2 Mass spectrum and fragmentation pathways of compound 52
化合物54:在负离子模式下可见去质子化准分子离子m/z:187.096 97[M-H]-,质谱软件拟合分子式为C9H16O4,m/z:169.086 04[M-H-H2O]-、m/z:143.107 03[M-H-CO2]-、125.096 11[M-H-H2O-CO2 or M-H-CO2-H2O]-是准分子离子丢失H2O或CO2分子产生一系列特征碎片离子;同时,该准分子离子可直接脱去1分子HCOOH产生碎片离子m/z:141.867 23[M-H-HCOOH]-。该化合物的二级质谱及裂解规律(图3)与壬二酸对照品以及文献[19]报道一致,推断为壬二酸。
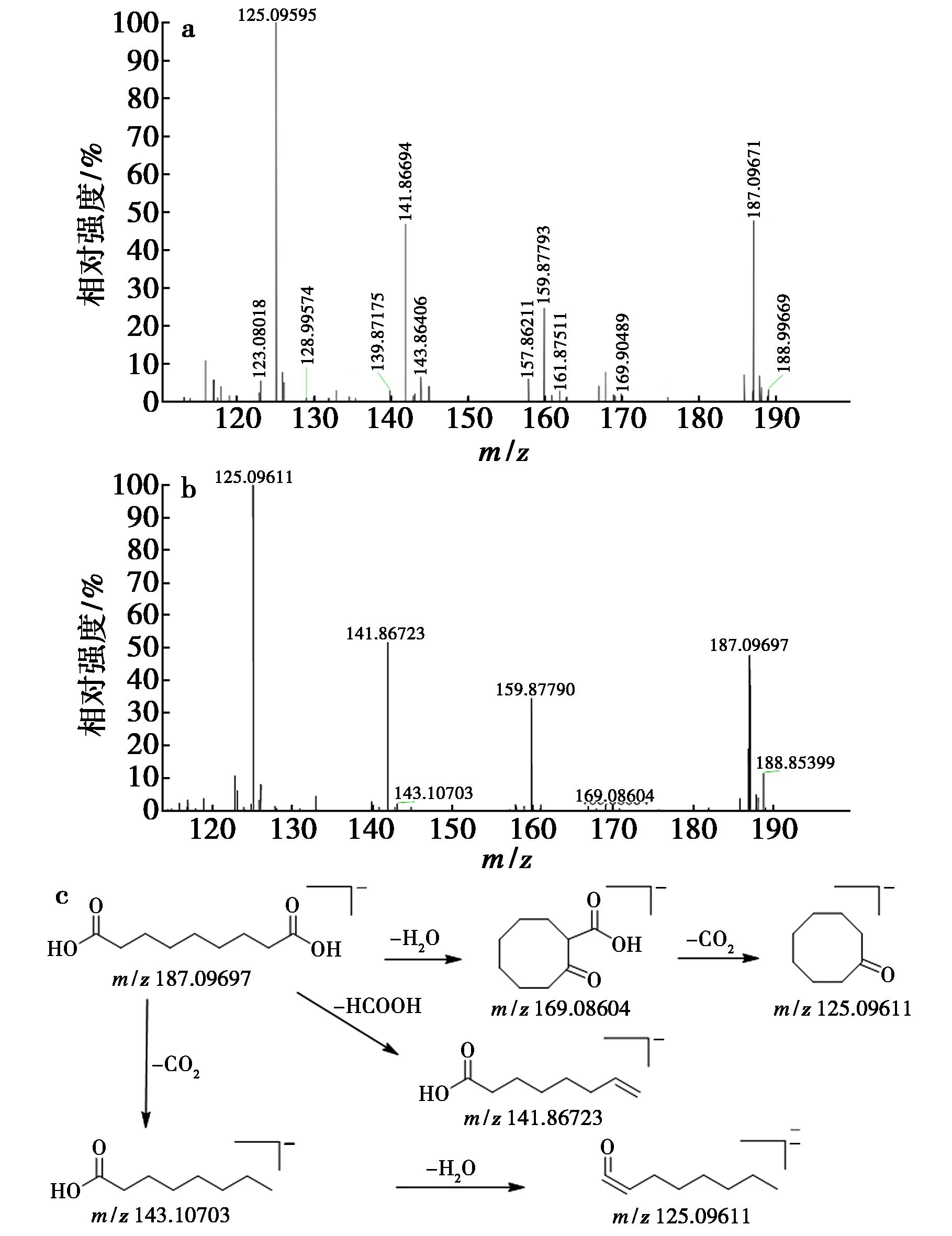
a.壬二酸的MS2图;b.化合物54的MS2图;c.裂解途径
图3 壬二酸、化合物54的质谱图及其裂解途径
Fig.3 Mass spectrum and fragmentation pathways of azelaic acid and compound 54
化合物64的裂解规律:在正离子模式下可见质子化准分子离子m/z:279.231 75[M+H]+,质谱软件拟合分子式为C18H30O2,m/z:209.153 85[M+H-5CH2]+、m/z:219.056 95[M+H-CH2COOH]+、m/z:149.023 27[M+H-CH2COOH-5CH2]+是准分子离子丢失nCH2或CH2COOH分子产生一系列特征碎片离子;该准分子离子也可先后脱去nH2O、nCH2分子产生一系列特征碎片离子m/z:261.220 31[M+H-H2O]+、m/z:243.210 69[M+H-2H2O]+、m/z:187.147 99[M+H-2H2O-4CH2]+、m/z:173.132 20[M+H-2H2O-5CH2]+。该化合物的二级质谱及裂解规律(图4)与文献[27]报道一致,推断为α-桐酸。
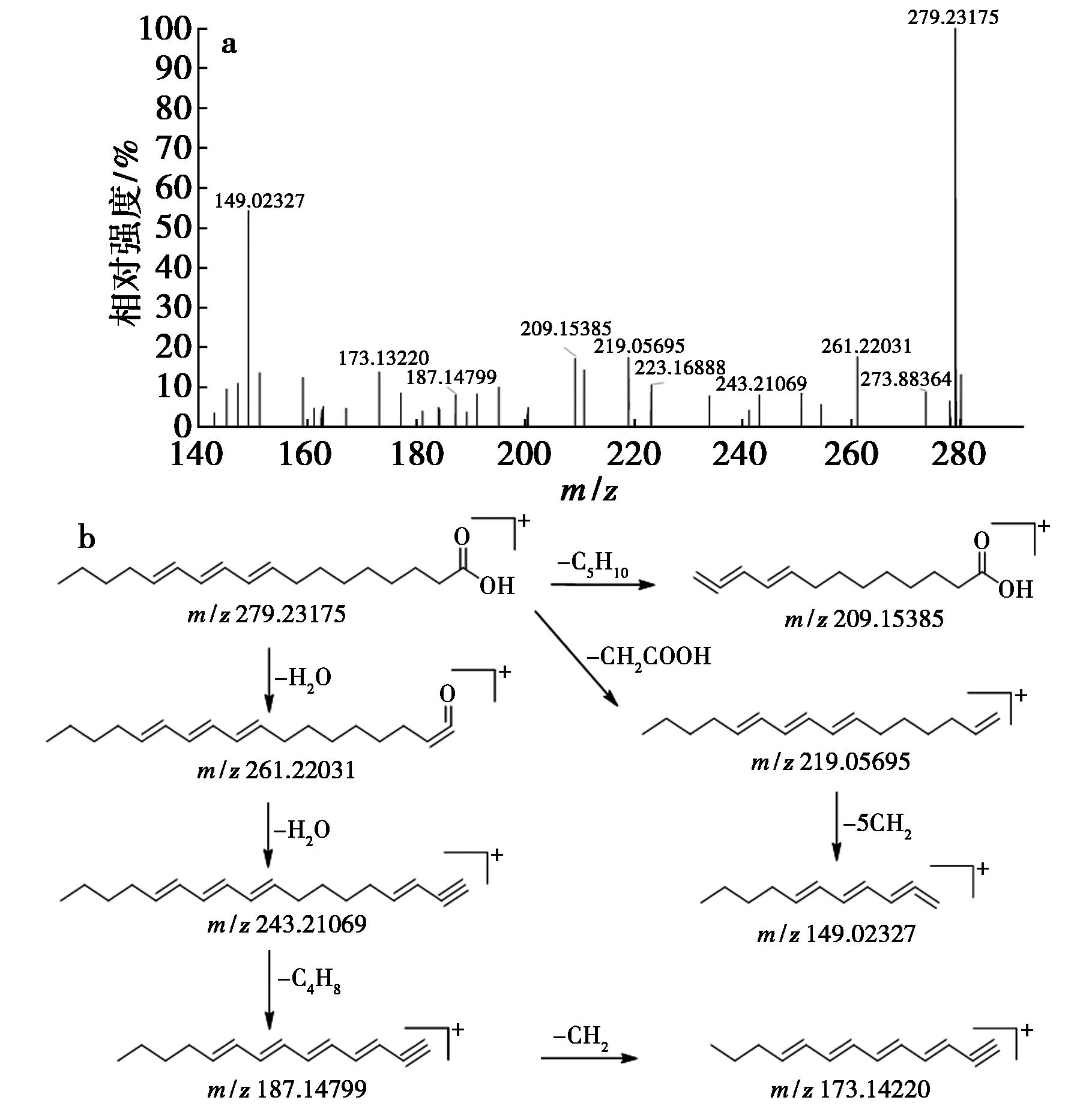
a.MS2;b.裂解途径
图4 化合物64的质谱图及其裂解途径
Fig.4 Mass spectrum and fragmentation pathways of compound 64
2.2.2 氨基酸类成分
该类成分在裂解过程中可能丢失NH3、H2O、CO2及HCOOH等小分子片段。各类型(α-、β-、γ-)氨基酸的裂解方式有所不同,α-氨基酸容易同时脱去HCOOH、NH3分子,β-氨基酸容易脱羧基或者含羧基的长碳链,γ-氨基酸容易先脱羧基再脱氨基。
以L-苯丙氨酸(41,tR=3.35 min)为例:在正离子模式下可见质子化准分子离子为m/z:166.086 17[M+H]+,质谱软件拟合分子式为C9H11NO2,m/z:120.080 91[M+H-COOH]+是准分子离子丢失1分子COOH产生的特征碎片离子;该准分子离子也可先后脱去1分子NH3和1分子COOH生产碎片离子m/z:149.059 46[M+H-NH3]+和m/z:103.054 59[M+H-NH3-COOH]+。该化合物的二级质谱及裂解规律(图5)与L-苯丙氨酸对照品以及文献[7]报道一致,推断为L-苯丙氨酸。
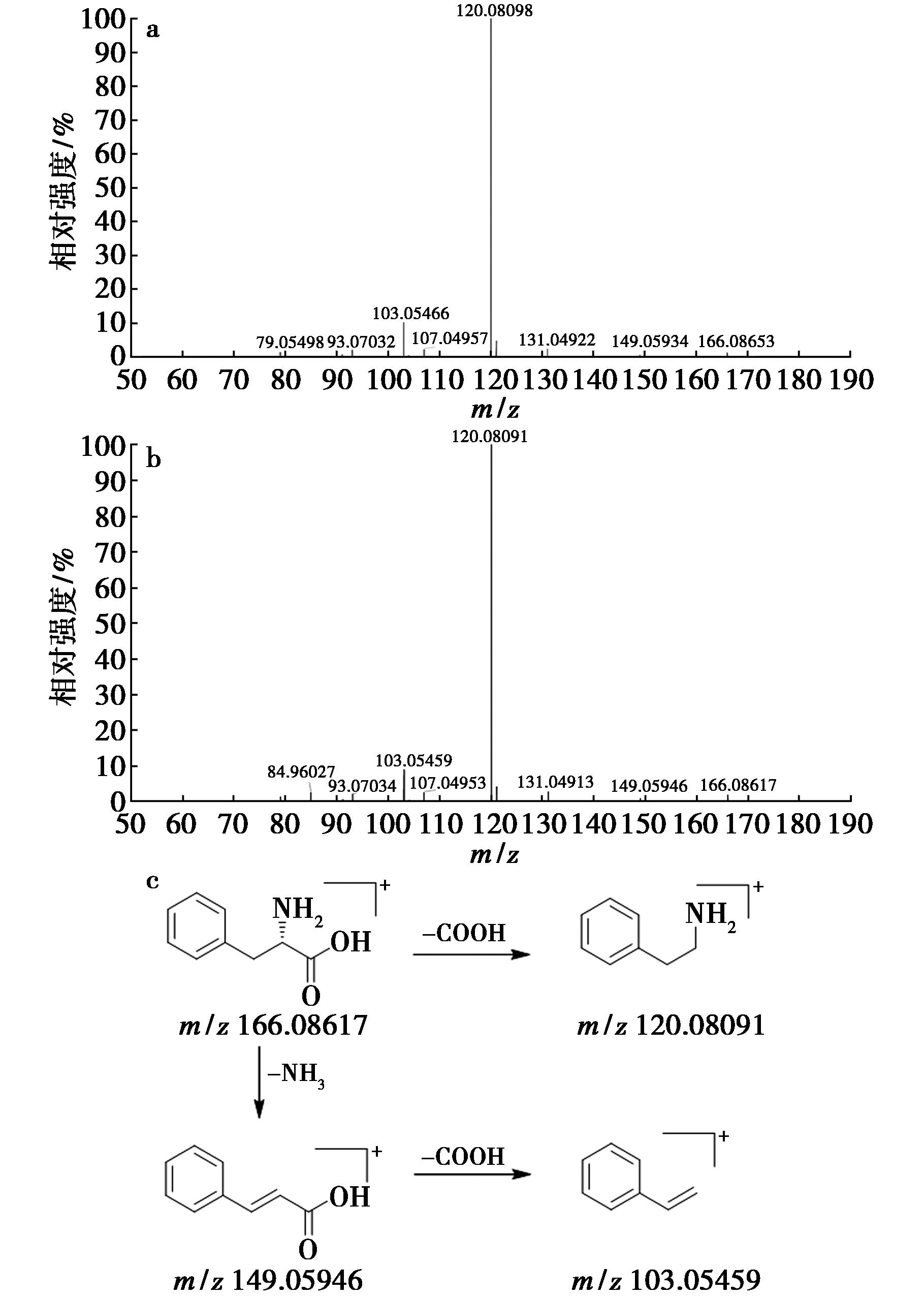
a.L-苯丙氨酸的MS2图;b.化合物41的MS2图;c.裂解途径
图5 L-苯丙氨酸、化合物41的质谱图及其裂解途径
Fig.5 Mass spectrum and their fragmentation pathways of L-phenylalanine and compound 41
2.2.3 生物碱类成分
该类成分根据其母核的不同分为有机胺类、吡咯类、哌啶类、吲哚类、嘌呤及黄嘌呤类等多种类型,不同类型的生物碱裂解方式区别较大,例如有机胺类主要的裂解方式为β裂解,酰胺类主要裂解方式为麦氏重排。但是,分析生物碱裂解特征不难发现,该类成分的裂解具有共同的特征,即容易丢失nH2O、nCH3OH、n(CH2)O、nCO、CHNH2、NO和NH3等中性分子。
以水苏碱(17,tR=1.02 min)为例:在正离子模式下可见质子化准分子离子为m/z:144.101 81[M+H]+,质谱软件拟合分子式为C7H13NO2,m/z:84.081 31[M+H-C4H6O]+、m/z:58.065 91[M+H-C3H10N]+是准分子离子分别丢失1分子C4H6O和1分子C3H10N生成特征碎片离子。该化合物的二级质谱及裂解规律(图6)与文献[14]报道一致,推断为水苏碱。
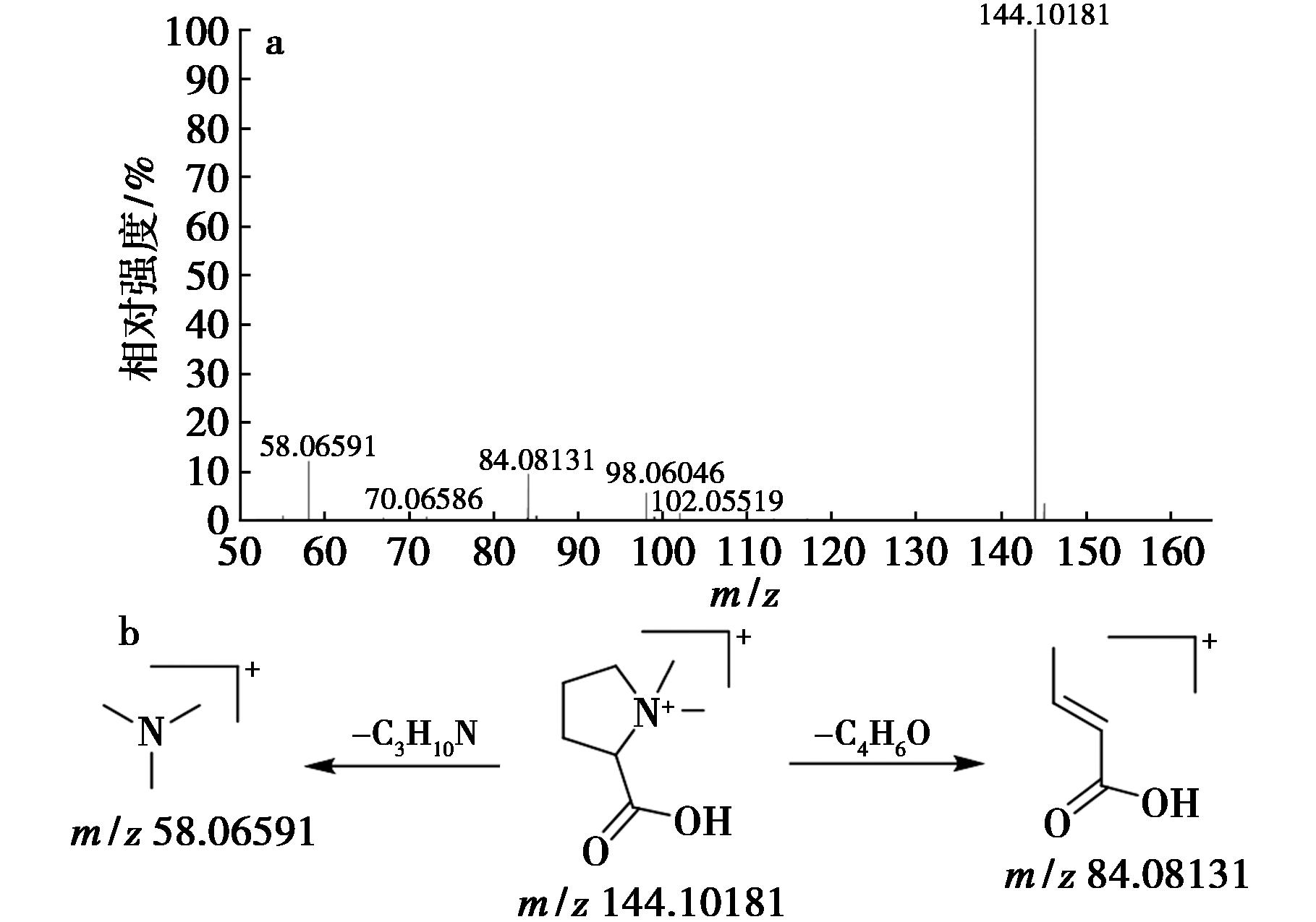
a.MS2图;b.裂解途径
图6 化合物17的质谱图及其裂解途径
Fig.6 Mass spectrum and fragmentation pathways of compound 17
2.2.4 核苷类成分
此类成分由嘌呤或嘧啶苷元与核糖或脱氧核糖进行缩合而成,裂解过程中C—N键容易断裂失去糖基部分,接着嘌呤或嘧啶苷元上的取代基进一步断裂产生NH3等小分子,也可能进一步发生开环反应。
以腺苷(32,tR=1.75 min)为例:在正离子模式下可见质子化准分子离子为m/z:268.103 82[M+H]+,质谱软件拟合分子式为C10H13N5O4,m/z:136.061 75[M+H-C5H8O4]+是准分子离子在裂解过程中发生氮苷键C—N断裂而丢失1分子核糖产生的特征碎片离子,该碎片离子进一步脱去1分子NH3后生成碎片离子m/z:136.061 75[M+H-C5H8O4-NH3]+。该化合物的二级质谱及裂解规律(图7)与文献[22]报道一致,推断为腺苷。
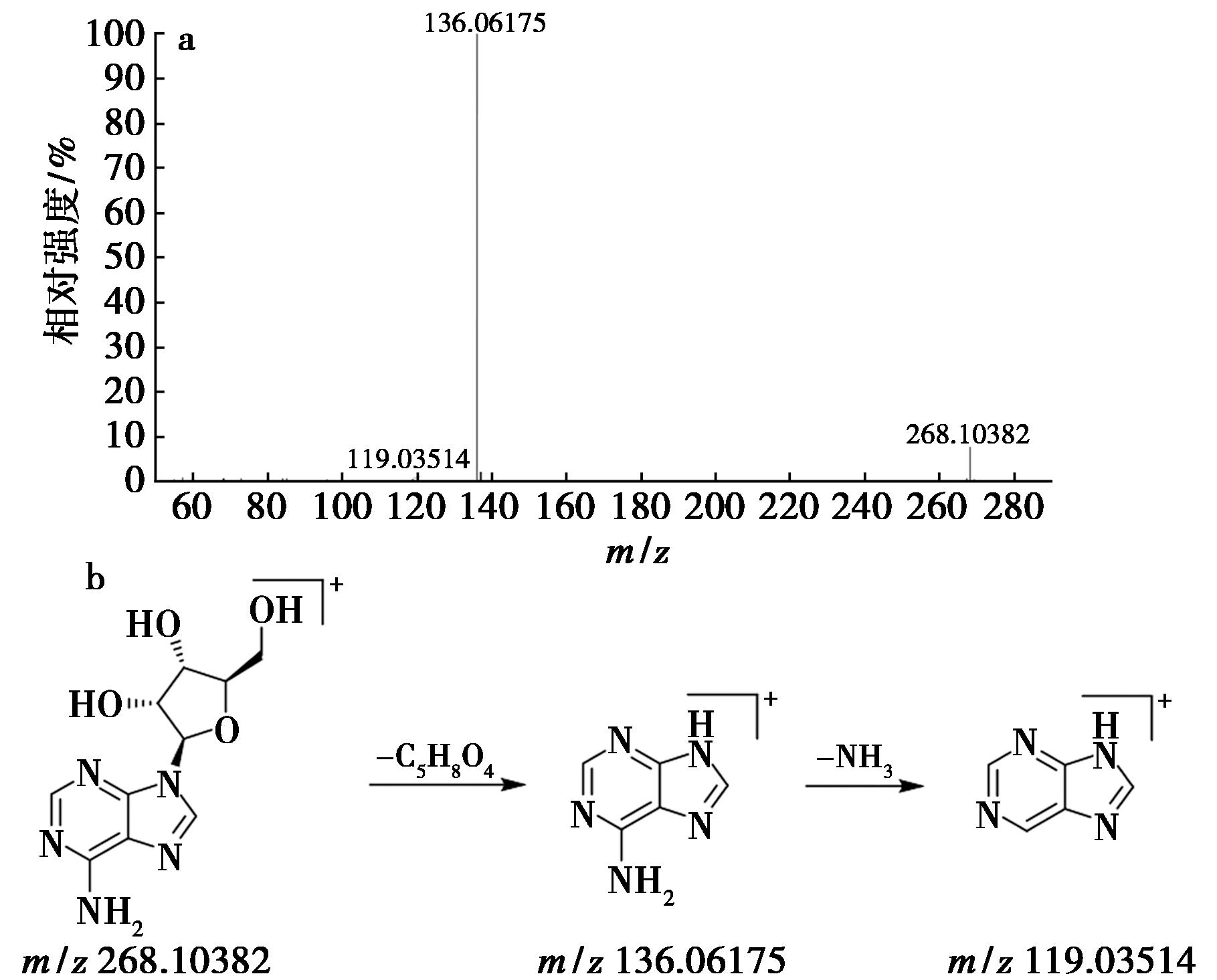
a.MS2图;b.裂解途径
图7 化合物32的质谱图及其裂解途径
Fig.7 Mass spectrum and fragmentation pathways of compound 32
2.2.5 糖类成分
在负离子模式下鉴定了4个糖类化合物,为单糖或低聚糖,因此该研究仅讨论单糖和低聚糖的裂解规律。单糖含多个羟基,裂解过程中容易丢失nH2O、CH2O等分子;低聚糖通常容易发生苷键断裂,得到相应的糖基,糖基可进一步裂解丢失H2O、CH2O、CH3分子。
以海藻糖(10,tR=0.95 min)为例:在负离子模式下可见去质子化准分子离子m/z:341.110 53[M-H]-,质谱软件拟合分子式为C12H22O11,m/z:179.055 47[M-H-C6H11O6]-是裂解过程中氧苷C—O键断裂生成的单糖碎片离子,接着连续丢失H2O分子产生碎片离子m/z:161.044 69[M-H-H2O]-、m/z:143.033 80[M-H-2H2O]-,最后再脱去1分子CH2O生成碎片离子m/z:113.023 27[M-H-2H2O-CH2O]-。该化合物的二级质谱及裂解规律(图8)与文献[11]报道一致,推断为海藻糖。
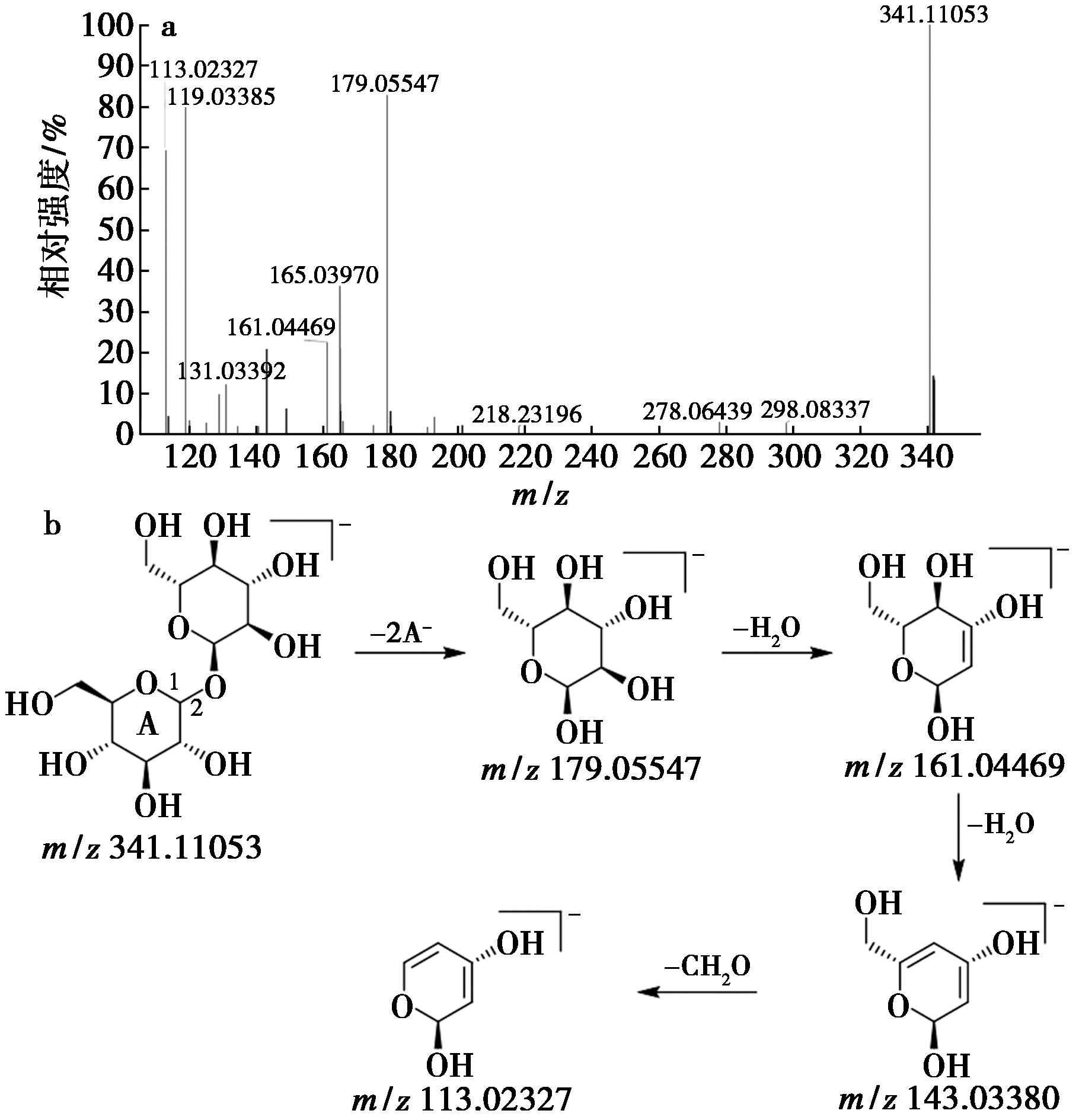
a.MS2图;b.裂解途径
图8 化合物10的质谱图及其裂解途径
Fig.8 Mass spectrum and fragmentation pathways of compound 10
2.2.6 黄酮类成分
该类成分在裂解过程中通常容易发生苷键断裂丢失糖基,苷元部分可能进一步丢失H2O、CO、C3O2等中性小分子,黄酮及异黄酮苷元的C环容易发生逆狄尔斯-阿尔德(Retro Diels-Alder reaction,RDA)裂解。以山奈酚-7-O-葡萄糖苷(49,tR=5.92 min)为例:在正离子模式下可见质子化准分子离子m/z:449.106 08[M+H]+,质谱软件拟合分子式为C21H20O11,m/z:287.054 81[M+H-C6H10O5]+是准分子离子苷键断裂得到的特征碎片离子,进一步发生RDA裂解产生碎片离子 m/z:153.018 26或丢失1分子CO产生碎片离子m/z:259.059 66[M+H-C6H10O5-CO]+。m/z:241.049 56[M+H-C6H10O5-CO-H2O]+或m/z:165.018 31[M+H-C6H10O5-CO-C6H6O]+是碎片离子m/z:259.059 66进一步丢失1分子H2O或1分子C6H6O生成的碎片离子。该化合物的二级质谱及裂解规律(图9)与文献[28]报道一致,推断为山奈酚-7-O-葡萄糖苷。
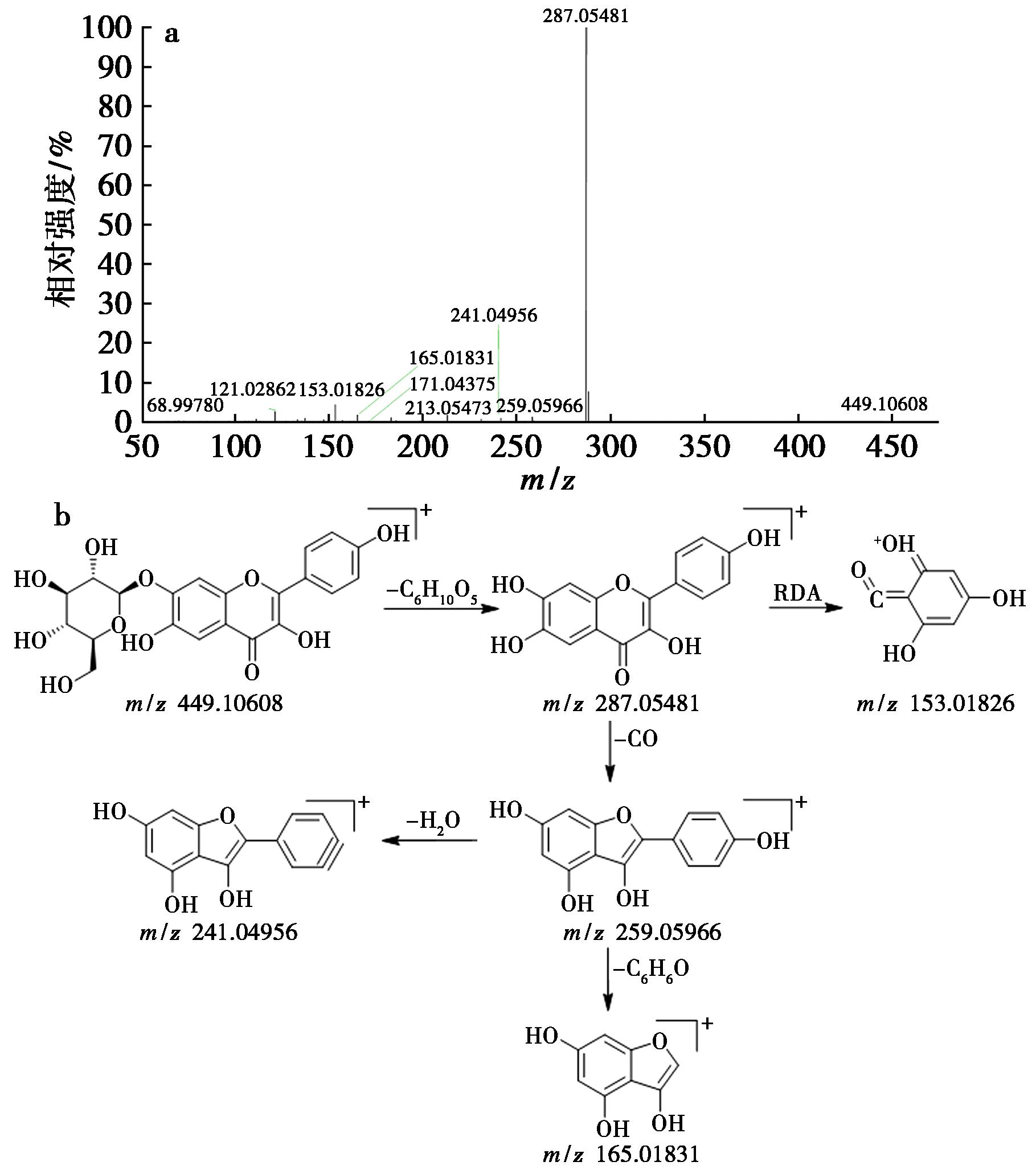
a.MS2图;b.裂解途径
图9 化合物49的质谱图及其裂解途径
Fig.9 Mass spectrum and fragmentation pathways of compound 49
2.2.7 芳香醛类成分
该类成分在裂解过程中主要丢失1分子CO,当芳香环上存在取代基时则可能发生裂解丢失相应的取代基产生H2O、OCH3、CH3等中性分子,芳香环通常不发生裂解。
以对羟基苯甲醛(30,tR=1.60 min)为例:在正离子模式下可见质子化准分子离子m/z:123.055 51[M+H]+,质谱软件拟合分子式为C7H6O2,该准分子离子丢失1分子H2O或1分子CO生成特征碎片离子m/z:105.045 12[M+H-H2O]+或m/z:95.049 64[M+H-CO]+。该化合物的二级质谱及裂解规律(图10)与文献[10]报道一致,推断为对羟基苯甲醛。
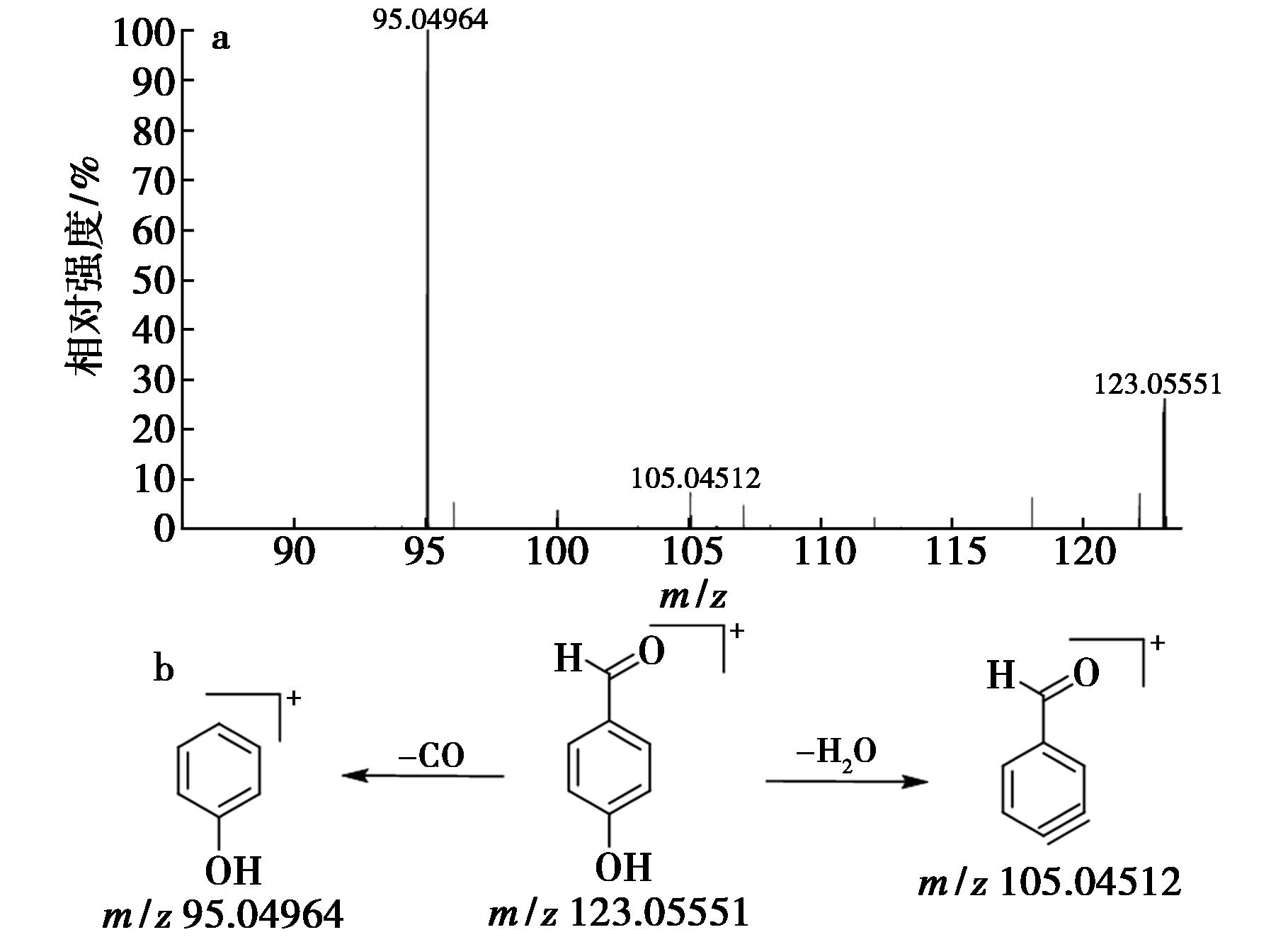
a.MS2图;b.裂解途径
图10 化合物30的质谱图及其裂解途径
Fig.10 Mass spectrum and fragmentation pathways of compound 30
3 结论
本研究首次运用UPLC-Q-Exactive-Orbitrap-MS技术针对木贼的化学成分开展了快速的鉴定,综合分析保留时间、准分子离子、二级质谱特征碎片离子等质谱信息,结合对照品数据及相关文献共鉴定了70个化合物,其中有机酸类、氨基酸类、生物碱类、核苷类成分占比较高,糖类、黄酮类、芳香醛及其他类成分等较少。
化学成分是药用植物产生药效的物质基础,药效是临床应用的重要依据。结合文献报道分析本研究鉴定出的化合物发现,其中包含了多种活性化合物,这些化合物很可能是木贼发挥药效的重要物质。部分有机酸具有显著的抗炎、抗菌、抗病毒、抗氧化活性以及心脑血管疾病预防作用,例如阿魏酸,其能够显著降低猪细小病毒(PPV)的表达,同时降低感染PK-15细胞诱发白细胞介素1β(IL-1β)、白细胞介素6(IL-6)等炎症因子的表达;亚麻酸、棕榈酸等不饱和脂肪酸具有降压、预防心血管疾病的作用,对高血脂、高胆固醇、主动脉内膜的硬化均有显著的调控作用。氨基酸类成分对于维持身体的正常代谢和身体的健康都是必不可少的,木贼中富含多种氨基酸,对人体氨基酸的合成和摄取起着非常重要的作用,例如异亮氨酸,其参与调控胸腺、脾、脑下腺等器官的功能和代谢。生物碱是自然界中发现较早的一类生物活性物质,经过科研人员不断地探索,发现部分生物碱具有抗菌消炎、抗肿瘤、抗血栓等活性,如:水苏碱、烟酰胺。此外,一些核苷和黄酮还显示了抗炎和抗氧化作用。木贼广泛的药理活性可能是各类成分多途径、多靶点协同作用的集中体现。后期课题组将进一步以“成分-药效-代谢-靶点”为切入点,多维模式探讨木贼药效物质基础及作用机制。
综上所述,该方法快速、准确、可靠,鉴定结果在一定程度上弥补了现阶段木贼化学成分研究的不足,为该药材后期药效物质基础、作用机制及产品开发提供参考依据。
[1]Editorial Committee of Flora of China CAS.Flora Reipublicae Popularis Sinicae.Beijing:Science Press,2004:238.中国科学院中国植物志编辑委员会.中国植物志.北京:科学出版社,2004:238.
[2]Chinese Pharmacopoeia Commission.Chinese Pharmacopoeia.1th Volume.Beijing:China Medical Technology Press,2020:64.国家药典委员会.中国药典(第一部).北京:中国医药科技出版社,2020:64.
[3]Pan X,Zhang C H.J.Jilin Med.Univ.,2018,39(3):2 016-2 018.潘旭,张昌浩.吉林医药学院学报,2018,39(3):2 016-2 018.
[4]Yu Y J,Zhou K,Liu D S,Zhu X J,Guo Z H,Yuan S,Shi J.Chem.Reagents,2024,46(10):63-71.于亚娟,周轲,刘东升,朱旭江,郭朝晖,袁松,石晶.化学试剂,2024,46(10):63-71.
[5]Zhang J,Wang T,Men Z Y,Mao H J,Wu Y F.China Environ.Sci.,2020,40(2):851-856.张静,王婷,门正宇,毛洪钧,吴宇峰.中国环境科学,2020,40(2):851-856.
[6]Zhang Y S,Zeng P,Cheng J R,Liu X M,Qiu Y Q,Zhang H N,Zhang Y H.J.Chin.Inst.Food Sci.Technol.,2018,18(6):272-282.张友胜,曾萍,程镜蓉,刘学铭,丘银清,张惠娜,张业辉.中国食品学报,2018,18(6):272-282.
[7]Chen J,Wu H,Liu R H,Zhang C N,Sun Y K.J.Chin.Med.Mater.,2022,45(3):639-646.陈剑,吴昊,刘润花,张晨宁,孙毅坤.中药材,2022,45(3):639-646.
[8]Zhu G H,Pang W,Chen X F,Hu J N.Cent.South Pharm.,2020,18(8):1 344-1 347.朱冠华,庞韦,程学芳,胡娟妮.中南药学,2020,18(8):1 344-1 347.
[9]Song K X.Nanopriming with Green Synthesis of Silver Effects on the Germination and Physiological Characteristics of Alfalfa(Medicago Sativa L.).Xianyang:Northwest Agriculture &Forestry University,2022.宋克晓.绿色合成纳米银引发对紫花苜蓿种子萌发及幼苗生理特性影响研究.咸阳:西北农林科技大学,2022.
[10]Hu H W,Zhao Y Y,Yang T L,Zheng Z X,Peng T,Deng F.Chin.J.Exp.Tradit.Med.Form.,2020,26(7):148-155.胡瀚文,赵永艳,杨天龙,郑振兴,彭腾,邓放.中国实验方剂学杂志,2020,26(7):148-155.
[11]Xu X M.Study on Quality Evalution of Different Species of Tibetan Medicine Berberidis Cortex Based on UPLC-Q-Exactive Orbitrap MS Metabolomics.Chengdu:Chengdu University of Traditional Chinese Medicine,2021.徐鑫梅.基于UPLC-Q-Exactive Orbitrap MS代谢物组学的多基原藏药小檗皮质量评价研究.成都:成都中医药大学,2021.
[12]Hao Z C.Screening and Application of Microorganisms that Inhibit Cyanobacteria Blooms.Tianjin:Tianjin University of Science and Technology,2021.郝忠超.抑制蓝藻水华微生物的筛选与应用.天津:天津科技大学,2021.
[13]Liu N,Tang R Y,She C,Tao T,Min Y H,Li H.Food Ferment.Ind.,2024,50(6):254-259.刘娜,唐睿艺,佘城,陶滔,闵宇航,李航.食品与发酵工业,2024,50(6):254-259.
[14]Liu M S,Yang B P,Yang W L,Cai Y,Wang K H,Peng M D,Chen B Z,Zheng G D.Chin.J.Hosp.Pharm.,2021,41(23):2 395-2 400;2 427.刘梦诗,杨得坡,杨婉玲,蔡轶,王康慧,彭梦蝶,陈柏忠,郑国栋.中国医院药学杂志,2021,41(23):2 395-2 400;2 427.
[15]Zhang J Y.Extraction Technology and Application of Gastrodin and Gastrodia Elata Polysaccharide.Lanzhou:Northwest Normal University,2022.张家义.天麻素和天麻多糖的提取工艺及应用.兰州:西北师范大学,2022.
[16]Feng F.The Molecular Mechanism of Xanthomonas Type Ⅲ Effector AvrAC to Regulate Plant Innate Immunity.Beijing:Tsinghua University,2012.冯锋.黄单胞菌效应蛋白AvrAC调节植物先天免疫的分子机制.北京:清华大学,2012.
[17]Gao H,Xie Y C,Li X Y,Shi G S.Chin.J.Pharm.Anal.,2015,35(9):1 653-1 659.高辉,谢元超,李晓燕,史国生.药物分析杂志,2015,35(9):1 653-1 659.
[18]Yan Y H,Wu T,Chen J,Abdula R,Huang L,Aisa H A.Chin.J.Exp.Tradit.Med.Form.,2021,27(21):156-166.严雅慧,吴涛,陈菊,热依木古丽·阿布都拉,黄磊,阿吉艾克拜尔·艾萨.中国实验方剂学杂志,2021,27(21):156-166.
[19]Li K L,Xiong P,Gong K Y,Peng J,Shi S L,Cai W.Nat.Prod.Res.Dev.,2020,32(2):250-256.李凯琳,熊佩,龚开妍,彭婕,史思林,蔡伟.天然产物研究与开发,2020,32(2):250-256.
[20]Vallverdú-queralt A,Verbaere A,Meudec E,Cheynier V,Sommerer N.J.Agric.Food.Chem.,2015,63(1):142-149.
[21]Chen X H,Jin M C.Chin.J.Health Lab.Technol.,2009,19(10):2 213-2 215;2 269.陈晓红,金米聪.中国卫生检验杂志,2009,19(10):2 213-2 215;2 269.
[22]Cui W H,Deng X L,Wang S Q.Chem.Res.,2023,34(4):313-318.崔维恒,邓晓兰,王思琴.化学研究,2023,34(4):313-318.
[23]Cui W H,Deng X L,Chen C Y.Henan Sci.,2023,41(7):978-984.崔维恒,邓晓兰,陈驰宇.河南科学,2023,41(7):978-984.
[24]Yang M Y.Studies on the Influence of Non-aqueous Medium on the Catalytic Properties of P.fluorescens/A.oryzae Whole-cells and Their Cytotoxicities on the Microbial Cells.Guangzhou:South China University of Technology,2014.杨美艳.非水介质对P.fluorescens/A.oryzae全细胞催化特性与细胞毒性影响的研究.广州:华南理工大学,2014.
[25]Chen J.Screening and Risk Prediction of Metabolic Markers of Thyroid Cancer and Laryngeal Cancer.Hefei:University of Science and Technology of China,2020.陈建.甲状腺癌和喉癌代谢标志物的筛选及其风险预测.合肥:中国科学技术大学,2020.
[26]Zhou W Y,Hu B C,Zhao L R,Liu Z L.J.Chin.Mass Spectrom.Soc.,2009,30(1):31-35.周维友,胡炳成,赵乐荣,刘祖亮.质谱学报,2009,30(1):31-35.
[27]Zhang Y,Deng Q,Wei M,Zhang X.Chin.J.Exp.Tradit.Med.Form.,2021,27(15):91-99.张烨,邓琦,魏敏,张旭.中国实验方剂学杂志,2021,27(15):91-99.
[28]Yang H T.Studies on Characteristic and Analysis of Chemical Components of Aster tataricus and Inhibitory Effect of Friedelan-3beta-ol on Cytochrome P450s in Human Liver Microsome.Shijiazhuang:Hebei Medical University,2016.杨浩天.紫菀化学成分表征与分析及表木栓醇对人肝微粒体CYP450酶抑制作用研究.石家庄:河北医科大学,2016.
[29]Han Z Y,Hu E M,Deng X K,Li Y,Zhang L S,Cao F,Chen J Y,Zhou F J.Sci.Technol.Food Ind.,2021,42(17):16-23.韩忠耀,胡恩明,邓先扩,李燕,张林甦,曹芳,陈建宇,周福军.食品工业科技,2021,42(17):16-23.
[30]Yang L.Qualitative and Quantitative Study on Effective Compounds of Fangji Huangqi Tang Against Adriamycin-induced Nephropathy Based on the Process in Vivo.Taiyuan:Shanxi University,2020.杨柳.基于体内过程的防己黄芪汤干预阿霉素肾病药效成分定性和定量研究.太原:山西大学,2020.
[31]Huang H Y,Kang J L,Yu Y H,Zhao P,Feng S X,Du Y,Li J S.J.Instrum.Anal.,2019,38(1):1-13.黄海英,康俊丽,余亚辉,赵 鹏,冯素香,杜燕,李建生.分析测试学报,2019,38(1):1-13.
[32]Li D Q.J.Anhui Agric.Univ.,2021,48(2):333-338.李东芹.安徽农业大学学报,2021,48(2):333-338.
[33]Rao Y,Huang W P,Feng Y L,Ouyang H,Yang S L.Chin.Tradit.Pat.Med.,2019,41(6):1 455-1 462.饶颖,黄文平,冯育林,欧阳辉,杨世林.中成药,2019,41(6):1 455-1 462.
[34]Liao Q J,Wang X Q,An M Z,Li Y H,Qiao Z W,Zhou H L,Song T F.Liquor Mak.Sci.Technol.,2020,(12):65-70.廖勤俭,王小琴,安明哲,李杨华,乔宗伟,周韩玲,宋廷富.酿酒科技,2020,(12):65-70.