图1 化合物1a的制备
Fig.1 Preparation of compound 1a
重氮化合物作为一类重要的有机合成子,其独特的结构和反应特性使其在有机化学中占据着不可替代的地位。自19世纪末首次发现以来,重氮化合物因其高反应活性和多样化的反应模式而受到广泛关注[1],随着有机合成方法的不断发展,重氮化合物在构建复杂分子结构[2]、合成天然产物和开发新型功能材料等方面发挥着越来越重要的作用[3]。
α-炔基重氮酮自2009年被Davies等[4]首次报道以来,因其双重反应特性:既可作为卡宾前体[5],又可发生Wolff重排生成炔基取代的乙烯酮中间体[6],而受到广泛关注。如2011年,Wang等[7]利用其金属卡宾体性质,报道了一例通过三重金属催化级联反应高效合成苯并稠合二氢呋喃多环化合物的方法。2025年,Zhao等[8]报道了一例铜催化的吲哚C3位选择性C—H官能化/去芳构化串联反应,高效构建吲哚基螺环骨架。其中关键步骤为铜卡宾中间体(来自重氮酮)选择性进攻吲哚C3位后,炔基与吲哚发生分子内5-endo-dig环化,形成螺环骨架。2024年,Ji等[9]利用其Wolff重排后生成的炔基乙烯酮中间体,成功发展了顺序多重重排反应,高立体选择性实现多取代共轭二烯的合成。
重氮化合物的合成至今已发展出许多成熟的方法[10],重氮转移反应[11]、氨基及腙等官能团的重氮化[12,13]、重氮化合物的偶联[14]等。但是对于α-炔基重氮酮的高效合成方法却鲜有报道。Davies等[4]采用预先制备的α-炔基酮通过重氮转移反应,制备相应的α-炔基重氮酮化合物。但该方法存在明显局限性:总产率较低,操作复杂,需要多次调控温度,预先制备的α-炔基酮稳定性较差,无法长时间保存。因此,开发一种高效的模块化合成方法是有必要的。
Weinreb酰胺自1981年问世至今,在构建酮类化合物中发挥着巨大的作用[15],2015年,Shin等[16]首次合成了α-芳基重氮Weinreb酰胺,并应用于不对称Roskamp反应。这类α-芳基重氮Weinreb酰胺的稳定性及反应潜力吸引了我们的关注,基于此,提出了以下策略:通过这类α-芳基重氮Weinreb酰胺进一步与对应的炔基亲核试剂发生酰基化反应,利用Weinreb酰胺的独特性质,一步得到炔基酮化合物,并且重氮基团得到保留,实现α-炔基重氮酮的高效合成。当然,这个策略存在的挑战是,分子中存在两个亲电位点(重氮碳和羰基碳)时,如何对反应位点进行选择性控制。
对此,本文展开了α-炔基重氮酮的高效制备的研究。
ME204E型电子分析天平(瑞士METTLERTOLEDO有限公司);HC-0540A型低温恒温反应浴、SHB-ⅢA型循环式多用真空泵、HC85-1型磁力搅拌器(杭州惠创仪器有限责任公司);RE-2000-1L型旋转蒸发仪(北京莱伯泰科仪器股份有限公司);500 MHz型、600 MHz型核磁共振波谱仪(北京布鲁克科技有限公司)。
4-乙酰氨基苯磺酰基叠氮(p-ABSA)、1,8-二氮杂双环[5.4.0]十一碳-7-烯(DBU)、N,O-二甲基羟胺盐酸盐、1-氯-4-炔基苯、3-氯苯炔、1-炔基-4-氟苯、4-甲氧基苯乙炔、4-乙氧基苯乙炔、(4-溴苯基)乙炔、1-丁基-4-乙炔基苯、4-乙炔基甲苯(上海皓鸿生物医药科技有限公司);正丁基锂(n-BuLi,2.5 mol/L in hexane)、苯乙酰氯、二苄胺、3-溴丙炔,超干乙二醇二甲醚(DME)(安徽泽升科技有限公司);碳酸钾(K2CO3)、无水硫酸钠、乙腈(MeCN)、乙醚、石油醚(PE)、乙酸乙酯(EA)、二氯甲烷(DCM)、氯化铵(NH4Cl)、盐酸(HCl)、甲苯(Tol)、无水乙醇、四氢呋喃(THF)(国药集团化学试剂有限公司)。所用试剂均为分析纯。
从商业供应商处获得的材料无需进一步纯化即可直接使用。溶剂在使用前按照标准程序进行蒸馏。无水四氢呋喃(THF)提前使用钠丝回流处理,使用预涂硅胶的硅胶板(烟台新诺新材料技术有限公司),通过薄层色谱法(TLC)对反应进行监测。在硅胶(粒度为300~400目,中国烟台)上进行柱层析分离,用V(石油醚(PE))∶V(乙酸乙酯(EA))洗脱。
1.2.1 2-重氮-N-甲氧基-N-甲基-2-苯乙酰胺(1a)的合成路线
图1 化合物1a的制备
Fig.1 Preparation of compound 1a
称取27.7 g(200.4 mmol)碳酸钾于烧杯中并加入水配成饱和溶液待用。在装有磁力搅拌子的三颈烧瓶中加入7.23 g(75.0 mmol)N,O-二甲基羟胺盐酸盐和50 mL甲苯(Tol),随后加入6.33 g(50.0 mmol)苯乙酰氯,搅拌下使用滴管缓慢向体系中滴加碳酸钾溶液,并使用洗耳球排气。待体系不再产生气泡且呈碱性时,向体系中缓慢滴加浓盐酸至体系不再产生气泡且呈酸性后,停止滴加浓盐酸并将体系转移至分液漏斗中,水相使用乙酸乙酯(EA)萃取2次,合并的有机相使用无水硫酸钠干燥后旋蒸除去溶剂,得7.18 g淡黄色液体,产率80.1%,所得液体可直接用于下一步反应,无需进一步纯化。
圆底烧瓶中加入转子,称取3.58 g(20.0 mmol)上述所得黄色液体溶于50 mL乙腈(MeCN)中,并加入7.21 g(30.0 mmol) 4-乙酰氨基苯磺酰基叠氮(p-ABSA)。于常温搅拌下缓慢滴加4.57 g(30.0 mmol)1,8-二氮杂双环[5.4.0]十一碳-7-烯(DBU),薄层色谱分析(TLC)监测反应进程,当反应结束后,加入50 mL水淬灭反应并转移至分液漏斗中,水相使用乙醚萃取3次,合并的有机相使用无水硫酸钠干燥后旋蒸除去大部分溶剂后,柱层析分离(V(PE)∶V(EA)=50∶1)得到936.9 mg化合物1a,产率23%。产物核磁数据与文献[16]相一致。
1.2.2 2-(4-氯苯基)-2-重氮-N-甲氧基-N-甲基乙酰胺(1b)的制备
按照文献[17]方法,在1.2.1的条件下制备得到2.35 g化合物1b,产率50%,橙色液体,1HNMR(CDCl3,500 MHz),δ:7.45~7.39(m,2H);7.38~7.33(m,2H);3.71(s,3H);3.28(s,3H)。13CNMR(CDCl3,126 MHz),δ:166.10,131.69,128.89,126.62,125.90,61.17,60.59,53.44,34.08。ESI-MS,m/z:436.118 7[M+Na]+。
1.2.3 α-炔基重氮酮的制备
在无水无氧的氩气保护的25.0 mL Schlenk管中加入0.6 mmol取代苯乙炔并溶解于2.0 mL无水THF中,于-40 ℃下向体系中加入1.2 mmol n-BuLi,并且于该温度反应10 min,后称取对应的0.5 mmol weinreb酰胺重氮化合物溶解于2.0 mL无水THF中后,滴加入体系中并于-40 ℃下反应,TLC检测反应进程。待起始原料全部消耗完后,加入1.0 mL饱和氯化铵溶液淬灭,并用乙醚萃取2次,有机相合并后无需干燥,直接旋蒸走大部分溶剂后柱层析分离(V(PE)∶V(EA)=50∶1)得到对应的α-炔基重氮酮化合物。
1.2.4 产物核磁表征
1-重氮-1,4-二苯基丁-3-炔-2-酮(3a):91.9 mg,产率75%,黄色固体,表征数据与参考文献[9]一致。
4-(4-氯苯基)-1-重氮-1-苯基丁-3-炔-2-酮(3b):89.9 mg,产率64%,黄色固体。1HNMR(CDCl3,600 MHz),δ:7.68~7.20(m,14H)。13CNMR(CDCl3,150 MHz),δ:137.0,133.8,129.03,128.96,118.1,78.4。ESI-MS,m/z:303.029 6[M+Na]+。
1-重氮-4-(4-氟苯基)-1-苯基丁-3-炔-2-酮(3c):79.2 mg,产率60%,橙红色固体。1HNMR(CDCl3,500 MHz),δ:7.65~7.50(t,4H,J=14.9 Hz);7.44(t,2H,J=7.7 Hz);7.28(dd,1H,J=12.9,6.3 Hz);7.09(t,2H,J=8.4 Hz)。13CNMR(CDCl3,125 MHz),δ:164.9(d,J=253.79 Hz),135.0(d,J=8.84 Hz),129.0,127.3,124.9,116.2(d,J=22.36 Hz),115.9,115.8,78.3。
4-(4-溴苯基)-1-重氮-1-苯基丁-3-炔-2-酮(3d):99.2mg,产率61%,橙色固体。1HNMR(CDCl3,600 MHz),δ:7.64~7.26(m,14H)。13CNMR(CDCl3,150 MHz),δ:133.9,132.7,132.0,130.7,129.01,128.98,128.6,125.5,78.4。
4-(3-氯苯基)-1-重氮-1-苯基丁-3-炔-2-酮(3e):121.6 mg,产率62%,黄色固体。1HNMR(CDCl3,600 MHz),δ:7.65~7.29(m,14H)。13CNMR(CDCl3,150 MHz),δ:134.6,132.4,131.0,130.9,130.0,129.1,124.9,121.5,78.6。ESI-MS,m/z:303.029 6[M+Na]+。
1-重氮-4-(4-甲氧基苯基)-1-苯基丁-3-炔-2-酮(3f):93.9 mg,产率68%,红色固体,表征数据与文献[9]一致。
1-重氮-4-(4-乙氧基苯基)-1-苯基丁-3-炔-2-酮(3g):104.4 mg,产率73%,红色固体。1HNMR(CDCl3,600 MHz),δ:7.62~7.57(m,2H);7.51~7.39(m,4H);7.29~7.21(m,1H);6.90~6.83(m,2H);4.04(t,2H,J=10.5 Hz);1.40(t,3H,J=15.0 Hz)。13CNMR(CDCl3,125 MHz),δ:160.98,135.4,134.6,128.9,114.8,63.6,14.6。ESI-MS,m/z:313.094 7[M+Na]+。
1-重氮-1-苯基-4-(对甲苯基)-3-丁炔-2-酮(3h):95.0 mg,产率73%,橙色固体,表征数据与文献[9]一致。
4-(4-丁基苯基)-1-重氮-1-苯基丁-3-炔-2-酮(3i):120.9 mg,产率60%,黄色固体,表征数据与文献[9]一致。
1-(4-氯苯基)-1-重氮基-5-(二苄氨基)戊-3-炔-2-酮(3j):49.7 mg,产率24%,橙黄色液体。1HNMR(CDCl3,500 MHz),δ:7.54(d,2H,J=8.4 Hz);7.41~7.25(m,12H);3.71(s,4H);3.47(s,2H)。13CNMR(CDCl3,125 MHz),δ:130.4,122.7,122.4,122.3,121.9,121.0,60.2,45.9。ESI-MS,m/z:436.118 7[M+Na]+。
1-(4-氯苯基)-1-重氮基-5-(((1S,2R,5S)-2-异丙基-5-甲基环己基)氧基)戊-3-炔-2-酮(3k):18.6 mg,产率10%,橙色液体。1HNMR(CDCl3,500 MHz),δ:7.50(d,2H,J=8.6 Hz);7.38(d,2H,J=8.7 Hz);4.43~4.34(m,2H);3.32~3.20(m,1H);2.25~2.05(m,2H);1.70~1.62(m,2H);1.30~1.19(m,2H);1.00~0.70(m,12H)。13CNMR(CDCl3,125 MHz),δ:168.4,131.7,128.9,126.6,125.9,61.2,60.6,53.5,34.1。ESI-MS,m/z:395.149 7[M+Na]+。
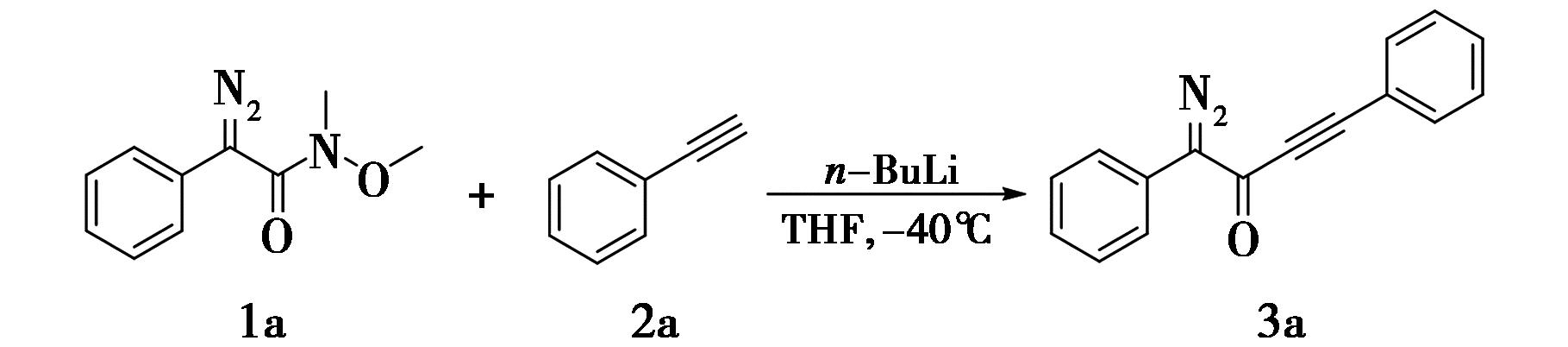
图2 反应初步尝试
Fig.2 Preliminary attempt of the reaction
使用化合物1a与苯乙炔(2a)进行反应的初步尝试,以75%的分离产率得到目标化合物3a,产物核磁数据与文献[9]相一致。
采用模板底物化合物1a和2a进行反应条件的优化。
2.2.1 反应温度的筛选
在标准条件下,对反应的温度进行了筛选,发现在-40 ℃下进行该反应能以75%的分离产率得到目标化合物3a,而在0 ℃下反应时,产率降低至33%,温度降至-20 ℃时,产率降低至27%,温度进一步降低至-60、-78 ℃时,反应无法正常进行。因此以-40 ℃作为反应最优温度进行下一步筛选。
表1 反应温度对反应的影响注
Tab.1 Effect of temperature on the reaction

EntryTemperature/℃Yield of compound 3a1,2)/%10332-20273-40754-60n.r.3)5-78n.r.3)
Note:1)Isolated yield;2)Reaction conditins:0.5 mmol compound 1a,0.6 mmol compound 2a,1.2 mmol n-BuLi in 4.0 mL THF unless other noted;3)no reaction.
2.2.2 溶剂种类的筛选
在确定最后反应温度后,对反应中使用的溶剂进行了筛选,将无水THF更换成无水乙二醇二
表2 溶剂的种类对反应的影响注
Tab.2 Effect of the type of solvent on the reaction

EntrySolventYield of compound 3a1,2)/%1THF752DME583DCM484Et2O25
Note:1)Isolated yield;2)Reaction conditins:0.5 mmol compound 1a,0.6 mmol compound 2a,1.2 mmol n-BuLi in 4.0 mL THF at -40 ℃ unless other noted.
甲醚(DME)后,目标化合物产率下降至58%;更换成无水DCM后,目标化合物产率下降至48%;更换成无水乙醚后,目标化合物产率下降至25%。因此选用无水THF作为反应最优溶剂进行下一步筛选。
2.2.3 碱种类的筛选
在确定最优反应温度和溶剂的种类后,对反应中使用的碱进行了筛选,将n-BuLi更换成LDA后,目标化合物产率下降至42%,而更换成 LiHMDS后,反应无法进行。因此选用n-BuLi为反应的最优碱。
表3 碱的种类对反应的影响注
Tab.3 Effect of the type of base on the reaction

EntryBaseYield of compound 3a1,2)/%1LDA422LiHMDSn.r3)3n-BuLi75
Note:1)Isolated yield;2)Reaction conditins:0.5 mmol compound 1a,0.6 mmol compound 2a,1.2 mmol base in 4.0 mL THF at -40 ℃ unless other noted;3)no reaction.
通过对反应的温度、溶剂的种类、碱的种类的筛选后,确定最优条件为:在无水无氧的氩气保护的25.0 mL Schlenk管中加入0.6 mmol化合物2a并溶解于2.0 mL无水THF中,于-40 ℃下向体系中加入1.2 mmol n-BuLi,并且于该温度反应 10 min,后称取102.5 mg(0.5 mmol)化合物1a溶解于2.0 mL无水THF中后,滴加入体系中并于 -40 ℃下反应,TLC检测反应进程。待化合物1a全部消耗完后,加入1.0 mL饱和氯化铵溶液淬灭,并用乙醚萃取2次,有机相合并后无需干燥,直接旋蒸除大部分溶剂后柱层析分离(V(PE)∶V(EA)=50∶1)得到对应的化合物3a。
在得到最优反应条件后,进行了反应的普适性考察。
以化合物1a为模板底物,考察了苯乙炔上取代基对反应产率的影响。当苯环上连有卤素时,反应均能兼容,且没有监测到取代的苯乙炔对应的锂-卤交换产物3a,但得到的对应α-炔基重氮酮的产率均有所下降(化合物3b~3e,60%~68%),当苯环上连有供电子取代基时,产率相较于标准底物没有明显下降(化合物3f~3h,68%~73%),值得注意的是,当苯环对位连有正丁基时(化合物3i),产率高达80%。
随后,以化合物1b为模板底物进一步考察了
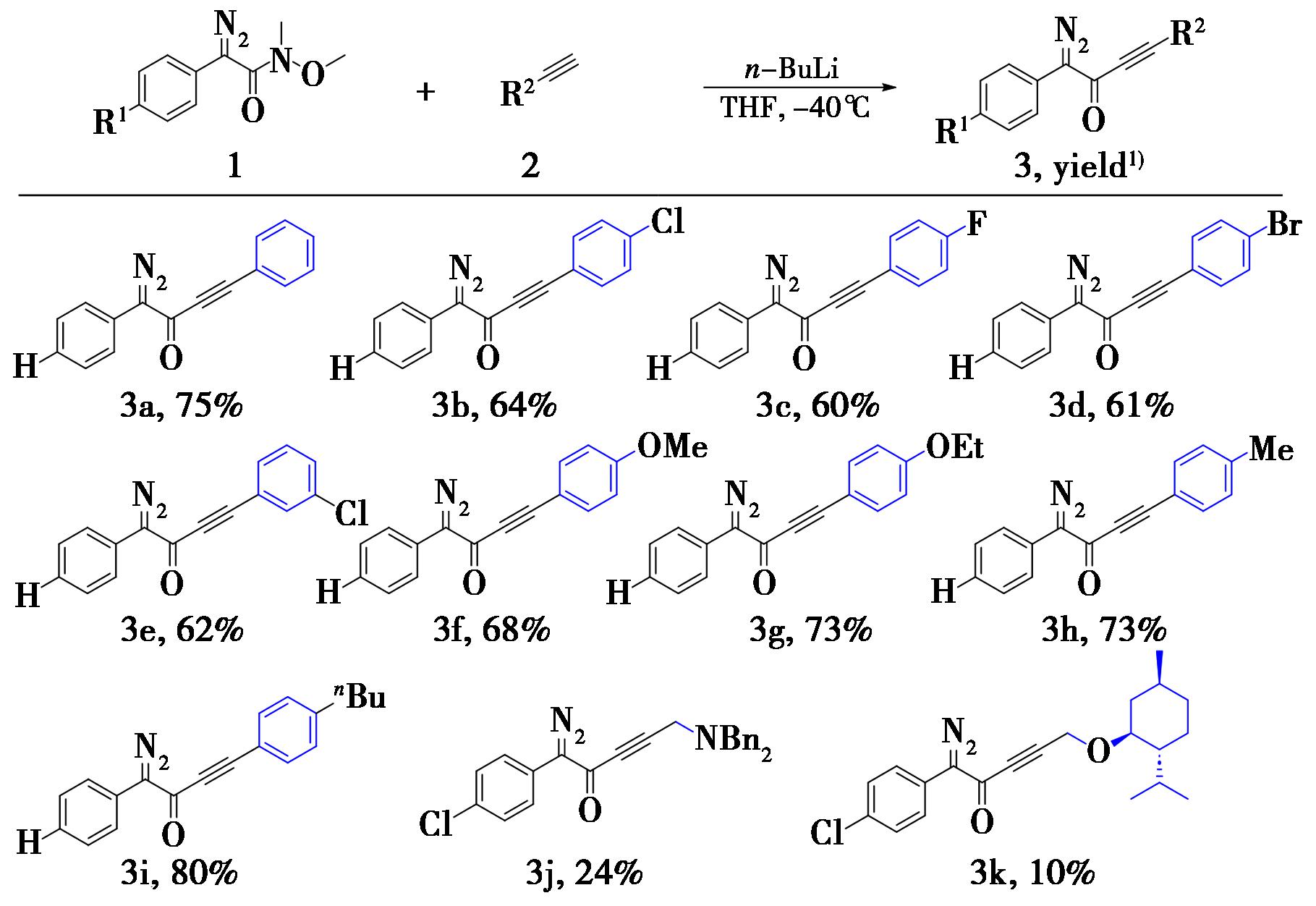
Note:Reaction conditins:0.5 mmol compound 1,0.6 mmol compound 2,1.2 mmol n-BuLi in 4.0 mL THF at -40 ℃ unless other noted;1)Isolated yields.
图3 底物普适性考察
Fig.3 Scope of substrates
炔丙基化合物对该反应的适用性。同时,N,N-二苄基丙-2-炔-1-胺也可以兼容该反应(化合物3j,产率24%)。此外,薄荷醇衍生的炔丙基化合物也能兼容该反应,虽然化合物3k产率较低(产率10%),但是也为各种天然产物的连接带来了机会。
因Weinreb酰胺可简便合成酮类化合物这一特点,设计了以Weinreb酰胺衍生的重氮化合物为重氮前体的策略,成功合成了一系列α-炔基重氮酮化合物。与传统的重氮前体α-炔基酮相比,α-芳基重氮Weinreb酰胺稳定性更佳,便于长时间保存。该策略具有良好的官能团兼容性,同时对于炔丙基重氮酮化合物展现出良好的合成前景,且有一例药物分子薄荷醇衍生的炔烃,也能在该条件下合成相应的α-炔基重氮酮,进一步拓展了α-炔基重氮酮分子库。
[1]Doyle M P,Forbes D C.Chem.Rev.,1998,98:911-936.
[2]Davies H M L,Lian Y J.Acc.Chem.Res.,2012,45:923-935.
[3]Xiao Z,Pu M,Li Y,Yang W,Wang F,Feng X,Liu X.Angew.Chem.Int.Ed.,2025,64:e202 414 712.
[4]Denton J R,Davies H M L.Org.Lett.,2009,11(4):787-790.
[5]Liu X,Li M,Dong K,Peng S,Liu L.Org.Lett.,2022,24:2 175-2 180
[6]Zhegalova N G,Popik V V.J.Phys.Org.Chem.,2011,24:969-975.
[7]Wang H,Denton J R,Davies H M L.Org.Lett.,2011,13(16):4 316-4 319.
[8]Zhao Y,Ji X,Xiao Y,Wu X,Liu L.Chem.Commun.,2025,61:5 162.
[9]Ji X,Shen C,Ni Y,Si Z,Wang Y,Zhi X,Zhao Y,Peng H,Liu L.Angew.Chem.Int.Ed.,2024,63:e202 400 805.
[10]Yuan X,Xu J X.Chem.Reagents,2022,44(2):161-168.
袁鑫,许家喜,化学试剂,2022,44(2):161-168.
[11]Yuan C,Pan Y,Qin Y,Sun W,Lu Y.J.Org.Chem.,2025,90:6 589-6 595.
[12]Cheng G,Cai C,Zhang X,Qiu G,Li S.Synlett,2025,36:1 262-1 266.
[13]Li G,Huang X,Lv J,Zhao X,Yang S,Liu L.Eur.J.Org.Chem.,2024,27:e202 400 899.
[14]Santiago J V,Or owska K,Ociepa M,Gryko D.Org.Lett.,2023,25:6 267-6 271.
owska K,Ociepa M,Gryko D.Org.Lett.,2023,25:6 267-6 271.
[15]Nahm S,Weinreb S M.Tetrahedron Lett.,1981,22(39):3 815-3 818.
[16]Shin S H,Baek E H,Hwang G S,Ryu D H.Org.Lett.,2015,17:4 746-4 749.
[17]Yan J,Zhao W,He Q,Hou J,Zeng H,Wei H,Xie W.Org.Biomol.Chem.,2022,20:2 387.