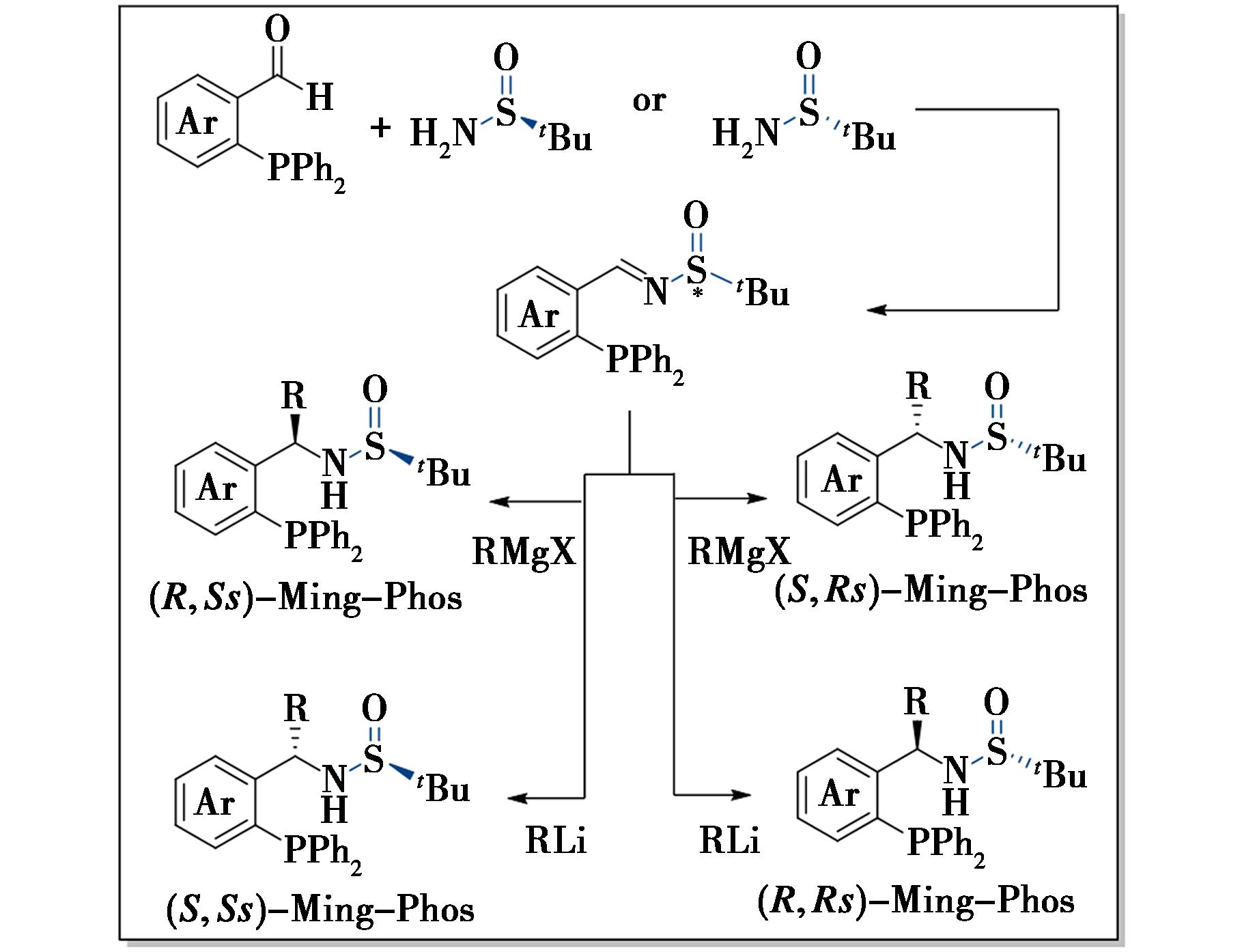
图1 Ming-Phos全构型发散性合成
Fig.1 Enantioselective divergent synthesis of Ming-Phos
过渡金属参与的不对称催化反应,凭借反应条件温和、调控便捷及催化效率高等显著优势,已成为当前有机化学领域中最具吸引力且研究热度极高的方向之一。在过渡金属催化的不对称反应体系中,手性配体作为不对称诱导的核心来源,是实现高对映选择性的关键因素,在反应进程中发挥着不可替代的作用。自20世纪60年代起,手性膦配体作为最早被系统研究的手性配体类别,始终受到化学研究者的高度关注。相较于其他类型配体,其研究深度与广度至今仍处于领先地位,甚至可被视为金属不对称催化领域在该时代发展的典型代表。迄今为止,新型手性膦配体的设计与合成,仍是化学家们在不对称催化研究中投入热情最高、精力最集中的核心方向之一。
Ming-Phos配体(以张展鸣博士命名)是本课题组基于非C2对称性、刚柔并济及兼具软硬配位原子(O、S、N、P原子)的设计理念,成功开发的首类Sadphos(Sulfinamide Phosphine)配体。该配体的合成以商业可得的2-二苯基膦芳基甲醛为起始原料,先与叔丁基亚磺酰胺发生缩合反应生成亚胺,随后经金属试剂对亚胺进行加成反应,通过两步反应即可完成制备,且产物可通过柱层析或重结晶等常规方法便捷分离得到[1]。尤其值得注意的是,可以通过金属试剂的种类和叔丁基亚磺酰胺的构型来调控Ming-Phos配体4种构型的发散性合成(图1)。同时,因其结构多样性突出、修饰位点丰富及易于规模化制备等显著优势,Ming-Phos配体一经报道便受到广泛关注[2]。目前,该配体作为手性配体已成功应用于金、铜、银、钯、铑、镍等过渡金属催化的10余类不对称反应中,并在反应中展现出优异的催化活性与手性诱导能力。本文按照过渡金属的种类,综述了Ming-Phos配体在不对称催化反应以及聚合反应中的应用。

图1 Ming-Phos全构型发散性合成
Fig.1 Enantioselective divergent synthesis of Ming-Phos
鉴于金独特的线性配位几何特性,其中心金属离子通常以sp杂化轨道形成直线型配位键,这种特殊的电子构型和空间排布极大地限制了手性配体对反应立体化学的调控能力,因此涉及金的不对称催化研究长期以来被视为有机合成领域中一项极具挑战性的课题。近几十年来,传统优势配体(包括大位阻手性双膦配体、亚磷酰胺衍生物及少量卡宾配体)的应用已显著推动了金催化不对称转化领域的发展。尽管取得了这些进展,但此领域中,反应范围和底物兼容性方面仍存在明显局限性。因此,设计和开发具有全新骨架结构的手性配体,不仅是突破金催化不对称反应固有挑战的最基础策略之一,更是推动该领域向更广阔应用场景迈进的关键驱动力。这类新型配体需在保持与金高效配位能力的同时,通过精准调控配体的空间位阻效应、电子效应及手性环境,实现对更多反应类型和底物的高效立体化学控制,从而为金催化不对称转化开辟新的研究维度。
在本课题组的前期研究中,使用带有大位阻取代基的(R)-DTBM-MeOBIPHEP和具有较小咬合角的联苯类双膦配体(R)-C1-TunePhos,可实现金催化共轭烯炔酮与硝酮的不对称环加成反应[3]。该反应体系对芳基和环己烯基取代的烯炔酮底物表现出优异的催化性能,但不适用于烷基取代的烯炔酮底物。2014年,Ming-Phos配体的出现解决了该不对称反应的底物限制问题,实现了芳基和烷基共轭烯炔酮底物的高效转化[4]。值得注意的是,本课题组还意外发现一对非对映异构配体可成功调控产物的对映选择性(图2a)[5]。此外,Ming-Phos配体通过共聚反应高效固定在聚苯乙烯上,制备的非均相催化剂不仅保留了与均相催化剂相当的催化活性和对映选择性,还可便捷回收循环使用8次[6]。
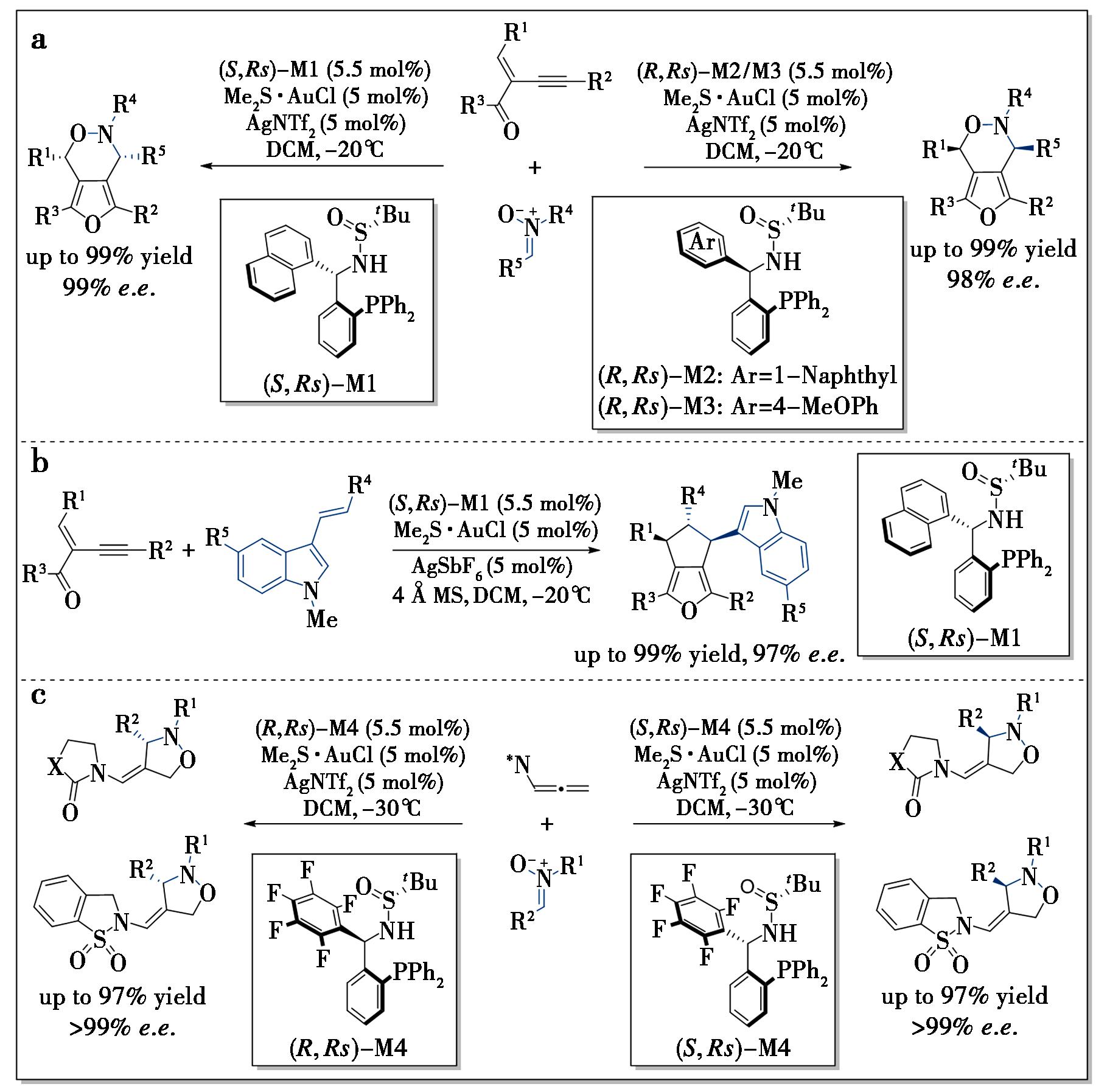
a、b、c分别为烯炔酮与硝酮[5]、烯炔酮与3-苯乙烯基吲哚[7]、N-联烯酰胺与硝酮[8]的不对称环加成反应
图2 Ming-Phos在金催化不对称[3+2]环加成反应中的应用
Fig.2 Application of Ming-Phos in gold-catalyzed asymmetric [3+2] cycloaddition reactions
2018年,本课题组报道了一例以Ming-Phos配体衍生的金催化体系,用于烯炔酮与3-苯乙烯基吲哚的不对称分子间[3+2]环加成反应(图2b)[7]。该转化能以优异收率和高对映选择性构建吲哚基取代的环戊并[c]呋喃——这类结构单元在天然产物及药物分子中广泛存在。研究中的关键发现是水对反应效率具有显著抑制作用,因此需在严格无水条件下进行。该合成方法的特点在于:反应条件温和且操作简便,底物适用范围广泛且起始原料易于获取,同时对非对映选择性和对映选择性展现出优异的调控能力,凸显了其在杂环骨架构建中的合成实用价值。
2022年,本课题组通过易于制备的N-联烯酰胺与硝酮反应合成了具有重要价值的光学活性异噁唑烷。该转化采用新型含氟手性Ming-Phos配体M4,能够以高产率及优异的区域选择性和对映选择性生成环加成产物(图2c)[8]。使用该手性配体的非对映异构体可高选择性地得到相应对映体。机理研究表明,M4中亚磺酰胺部分的N—H键与五氟苯基取代基协同作用,显著提升了对映选择性,这证实了Ming-Phos在该转化中作为多功能配体的作用。值得注意的是,这是将氟效应应用于解决金催化不对称反应中长期存在的挑战,为均相催化中的配体设计拓展了思路与工具。
在2010年,本课题组发现在金催化下烯炔铜与1,3-二苯基异苯并呋喃可发生串联杂环化/[4+3]环加成反应,生成目标非手性氧桥环产物[9]。尽管系统筛选了多种已知手性配体,仅实现了中等的exo/endo选择性。近期研究表明,Ming-Phos配体在此类反应中展现出优异的手性诱导能力,在调控exo/endo比例方面发挥关键作用[10]。该方法能够以良好产率合成手性氧桥多杂环化合物,同时兼具优异的对映选择性和显著的非对映选择性(exo/endo高达50∶1,图3)。
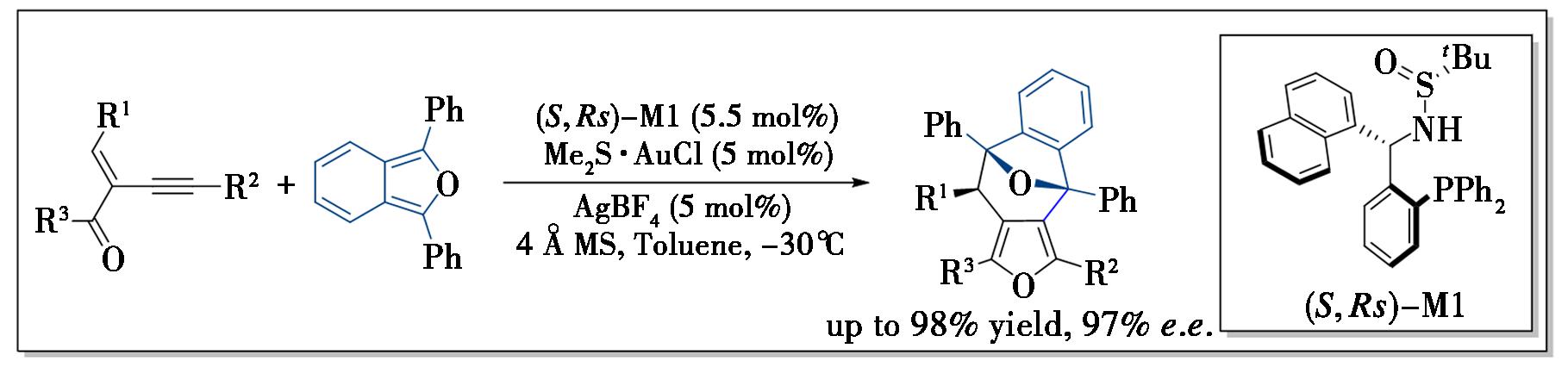
图3 Ming-Phos在金催化不对称[4+3]环加成反应中的应用
Fig.3 Application of Ming-Phos in gold-catalyzed asymmetric [4+3] cycloaddition reactions
多取代吡咯烷类化合物广泛存在于药物、农药、生物碱及催化剂中,过渡金属催化的甲亚胺叶立德与缺电子烯烃的不对称1,3-偶极环加成反应,是合成该类化合物的最直接高效方法之一。然而,合成在C3或C4位带有全碳季碳中心的多取代吡咯烷仍是一项重大挑战。2016年,本课题组利用Ming-Phos衍生的铜催化剂,首次报道了甲亚胺叶立德与β-三氟甲基-β,β-双取代烯酮的高对映选择性[3+2]环加成反应[11]。该方法可规模化制备在C3位具有三氟甲基取代全碳季碳立体中心的高取代吡咯烷,产率良好,非对映选择性>20∶1,对映选择性高达98%。所得环加成产物可转化为醇、高取代2-吡咯啉、N-羟基吡咯烷及双环化合物,且产率高并保留优异的对映选择性(图4a)。值得一提的是,通过X射线衍射成功表征了[M5Cu(CH3CN)]ClO4的单晶结构,结果显示铜与配体的膦原子和氧原子均发生配位。该结构分析证实,Ming-Phos在铜配合物中作为P,O-双齿配体,这与其在金配合物中仅与膦原子相连的单齿配位模式截然不同。
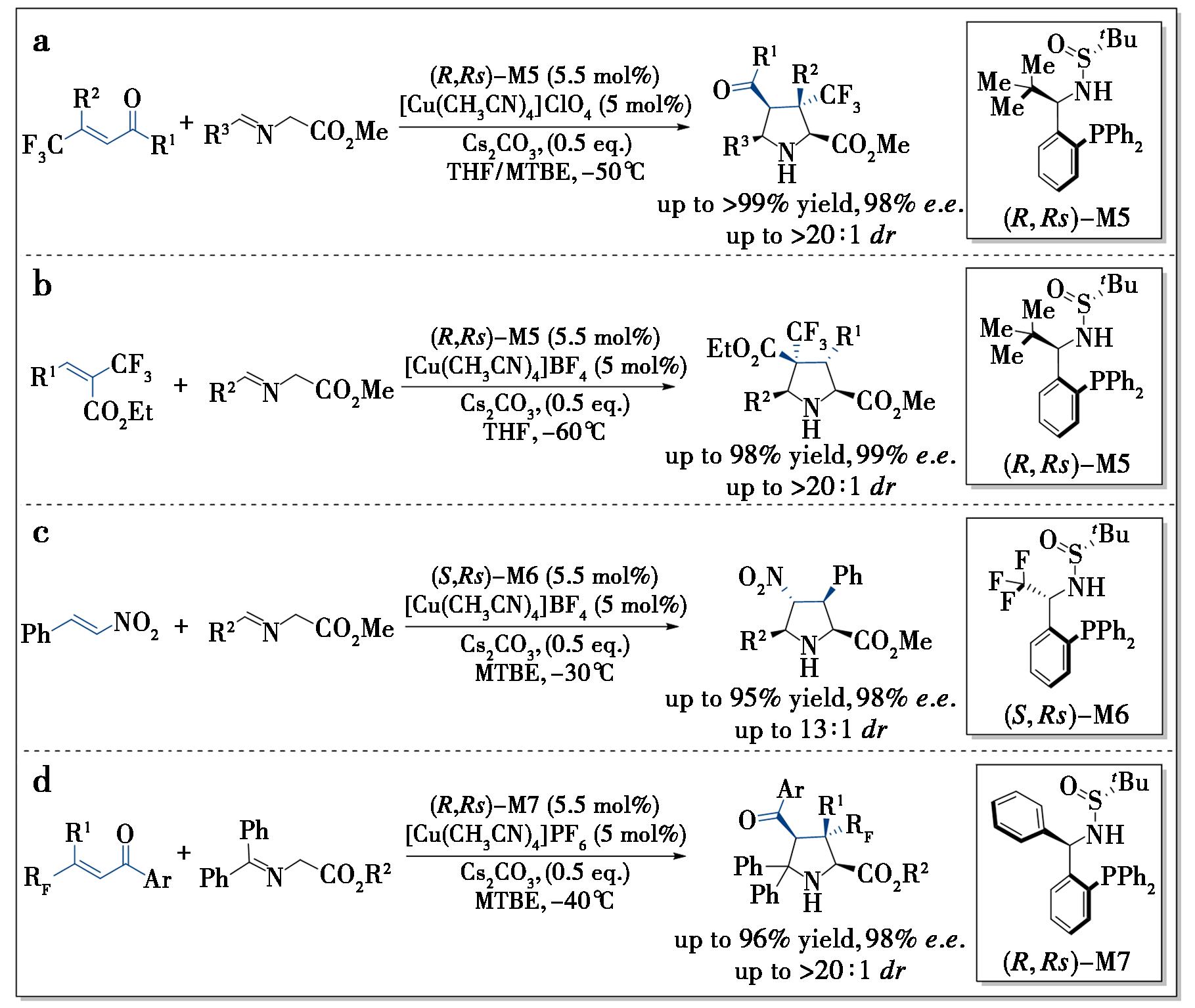
a、b、c、d分别为甲亚胺叶立德与β-三氟甲基-β,β-双取代烯酮[11]、甲亚胺叶立德与α-三氟甲基-α,β-不饱和酯[12]、甲亚胺叶立德与硝基烯烃[13]、甘氨酸酮亚胺与β-三氟甲基-β,β-双取代烯酮[15]的不对称环加成反应
图4 Ming-Phos在铜催化不对称[3+2]环加成反应中的应用
Fig.4 Application of Ming-Phos in copper-catalyzed asymmetric [3+2] cycloaddition reactions
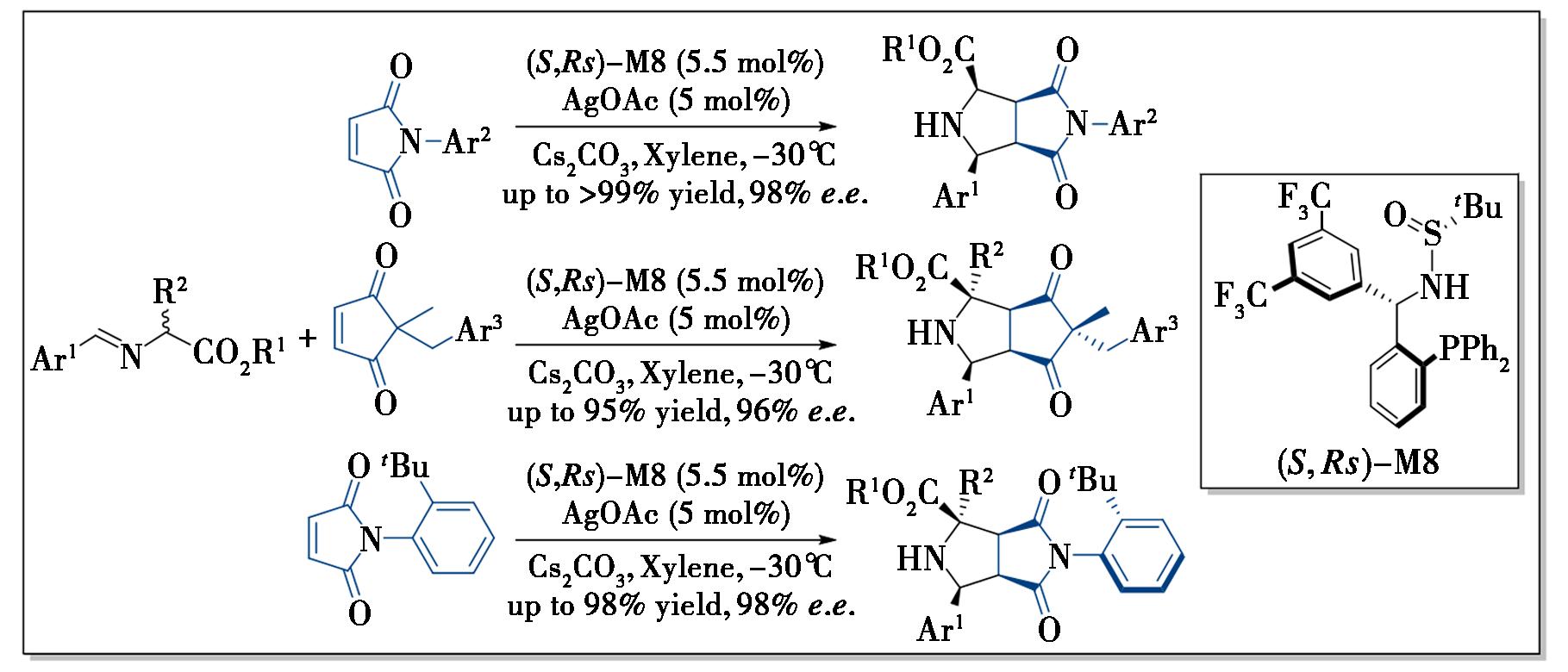
图5 Ming-Phos在银催化不对称[3+2]环加成反应中的应用
Fig.5 Application of Ming-Phos in silver-catalyzed asymmetric [3+2] cycloaddition reactions
其后,本课题组证实了将α-三氟甲基-α,β-不饱和酯用作亲偶极体的可行性。在 Cu(Ⅰ)-Ming-Phos催化体系存在下,这些亲偶体与甲亚胺叶立德反应,可生成在C4位带有三氟甲基取代的全碳季碳立体中心的手性吡咯烷类化合物(图4b)[12]。该反应可放大至克级规模制备高度取代的吡咯烷,且产物的多功能性为衍生化提供了多种可能。机理研究表明,M5的N—H键对提高对映选择性和反应活性起到了重要作用,这可能归因于通过氢键相互作用稳定烯醇中间体,从而有效抑制β-F消除反应。在2020年,本课题组还实现了Cu/Ming-Phos催化的甲亚胺叶立德与硝基烯烃的1,3-偶极环加成(图4c)[13]。值得注意的是,当使用叔丁基取代的M5作为手性配体时,尽管目标产物具有高对映选择性,但非对映选择性仅为4∶1。新设计合成的含三氟甲基的M6配体被证明对该转化中提高非对映选择性起到了关键作用。同年,刘宇等[14]研究者进一步拓展了钯/Ming-Phos催化体系的应用,探索了甲亚胺叶立德与反式三氟甲基烯酮的1,3-偶极不对称环加成反应。
除甲亚胺叶立德外,甘氨酸酮亚胺作为1,3-偶极试剂已被证实可与β-三氟甲基-β,β-双取代烯酮反应,实现具有3个连续立体中心的高官能团化吡咯烷的构建[15]。对市售配体的筛选表明,受空间位阻的影响,迈克尔加成产物为主产物(图4d)。该反应合成环加成产物的关键突破在于使用Ming-Phos配体M7。对照实验表明,烯酮底物中的氟取代基对维持反应活性至关重要。机理研究支持协同反应路径,而非分步的分子间迈克尔加成/分子内曼尼希反应机制。
鉴于高度取代吡咯烷的重要性,开发适用于不对称1,3-偶极环加成反应的新型催化体系(尤其是采用高效简洁手性配体的体系且兼容广谱官能团)始终是研究热点。2019年,本课题组的研究表明,新开发的带有3,5-双(三氟甲基)苯基取代基的Ming-Phos配体M8在银催化不对称[3+2]环加成反应中表现出卓越活性[16]。该反应体系中,甲亚胺叶立德与马来酰亚胺、环戊烯-1,3-二酮及N-(2-叔丁基苯基)马来酰亚胺发生反应,能在温和条件下以良好产率及优异对映选择性,制备多种高官能团化的双环吡咯烷衍生物。
钯催化的Heck型串联反应通过烯烃或炔烃碳钯化生成二价钯中间体,并经多种捕获剂淬灭终止反应。该类反应已被广泛应用于各类环系结构的构建,同时也是复杂分子全合成中实现分子复杂性构建的关键策略[17-21]。
通过烯烃分子内碳钯化反应形成瞬时σ-烷基钯物种以引发交叉偶联反应,已成为合成取代内炔烃的有效策略。然而,受限于底物的外消旋化或配体活性不足,实现此类反应的不对称合成仍颇具挑战性。2020年,本课题组实现了钯催化烯烃与端炔的分子内Heck/Sonogashira反应,成功合成了具有炔丙基取代全碳季碳立体中心的手性苯并稠杂环化合物(图6a)[22]。这一成果的实现依托于所开发的由钯配合物与配体M9构成的高效催化体系。利用该方法,多种N-烯丙基羧酰胺被成功应用,以高对映选择性制得3,4-二氢异喹啉-1(2H)-酮衍生物。值得注意的是,该转化需要使用带有大位阻3,5-二叔丁基苯基的Ming-Phos配体,以戊烷和二氯甲烷的混合体系为溶剂,且无需外加铜作为共催化剂。
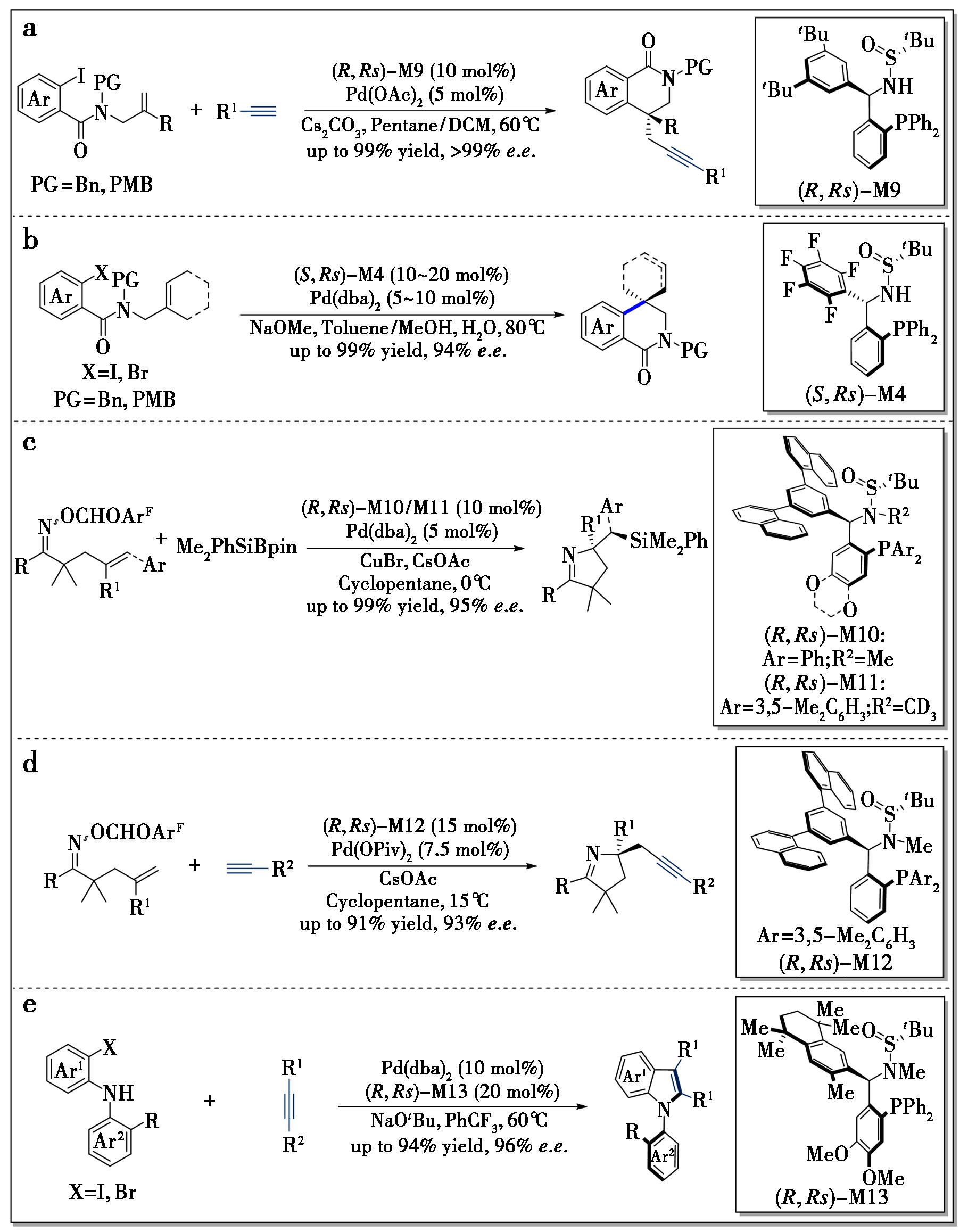
a.烯烃与端炔的分子内不对称Heck/Sonogashira反应[22];b.不对称分子内Heck反应[23];c.不对称Aza-Heck/硅化串联反应[24];d.不对称Narasaka-Heck环化/Sonogashira串联反应[25];e.不对称Larock吲哚合成[26]
图6 Ming-Phos在钯催化不对称Heck反应中的应用
Fig.6 Application of Ming-Phos in palladium-catalyzed asymmetric heck reactions
2021年,通过钯催化的不对称分子内Heck反应,本课题组成功构建了含有季碳手性中心的3,4-二氢-1-(2H)-异喹啉酮(图6b)[23]。该转化由Pd(dba)2与五氟苯取代的配体M4组成的催化体系高效推动,以甲醇钠为碱,甲苯/甲醇混合溶液为溶剂。实验表明,该反应在标准条件下可轻松放大至30 mmol规模,获得超过7 g的目标产物。氮原子上的苄基保护基可通过三氟乙酸顺利脱除,所得酰胺经LiAlH4高效还原后,以高产率得到相应胺类化合物。
过渡金属催化的烯烃不对称双官能团化反应,为复杂手性有机分子的合成提供了强有力的方法支撑。尽管在末端烯烃与环状烯烃的不对称官能团化领域已取得显著进展,但开链内烯烃的对映选择性转化仍面临巨大挑战。这主要归因于两方面:一是两个相邻手性中心的区域选择性与立体选择性难以精确控制;二是内烯烃与过渡金属物种之间的结合亲和力较低。2024年,Chen等[24]利用钯/Ming-Phos催化体系,通过串联Aza-Heck/硅化反应,成功实现了烯烃的对映选择性氨基硅烷化。该反应能够以良好的产率和高对映选择性,制备含有1个季碳或2个连续立体中心的手性吡咯烷(图6c)。DFT计算结果表明,立体诱导作用源于底物片段的芳环与配体中的萘基之间的弱相互作用。
在过去数十年间,链状烯烃的Narasaka-Heck型双官能团化反应已发展为构建杂环骨架的高效策略,但其不对称合成研究却鲜有涉足。2024年,Chen等[25]采用新型Ming-Phos配体M12,在温和反应条件下实现了钯催化烯烃链状肟酯与末端炔烃的对映选择性Narasaka-Heck环化/Sonogashira反应,以优异的产率和对映选择性合成了含季碳立体中心的吡咯啉类化合物(图6d)。研究表明,肟酯底物中的离去基团对反应影响显著,其中2,3,4-三氟苯基取代的底物可使反应取得最优结果。动力学研究显示,转金属化步骤并非该反应的决速步。该反应的可能机理如下:肟酯与零价钯发生氧化加成,随后经分子内Heck环化生成σ-烷基-Pd(Ⅱ)中间体;在醋酸铯作用下,末端炔烃发生去质子化生成炔基阴离子,该阴离子与σ-烷基-Pd(Ⅱ)中间体发生转金属化反应,最终通过还原消除生成目标产物。DFT计算结果表明,底物与配体之间的弱相互作用(尤其是CH—π相互作用)可能是控制反应立体选择性的主要因素。
Larock吲哚合成法作为合成吲哚类化合物最直接且高效的方法之一,自1991年首次报道以来,其不对称版本在构建轴手性N-芳基吲哚方面始终处于空白状态。2022年,本课题组采用钯/M13催化体系,成功实现了首例不对称Larock吲哚合成反应,可高效构建多种轴手性N-芳基吲哚化合物,不仅产率优良,对映选择性更是高达96%(图6e)[26]。动力学研究结合DFT计算证实,炔烃的迁移插入过程为该反应的决速步。进一步的DFT研究表明,配体位阻效应引发的N—C二面角差异,协同非共价相互作用共同参与了反应对映选择性的调控。
轴手性2′-官能化-2-二取代膦基-1,1′-联芳基配体在过渡金属催化的不对称反应中具有极高的应用价值。然而,其合成过程普遍面临手性拆分复杂、合成步骤繁琐及原料昂贵等问题,因此开发相应轴手性及官能化膦酸酯或氧化膦的对映选择性合成方法,一直是化学领域的研究热点。2019年,Qiu等[27]首次将Ming-Phos配体应用于不对称Suzuki偶联反应,成功合成了一系列手性膦酸酯或氧化膦,为轴手性联芳基单氧化膦的合成提供了简便高效的合成途径(图7a)。研究表明,大位阻取代的配体M14可提升反应的对映选择性;碱的碱性对反应影响显著,碱性越强,产物的产率及e.e.值越低,其中使用氢氧化钠或氢氧化钾时,反应几乎无法进行。以磷酸钾作为碱时,反应取得最优结果。
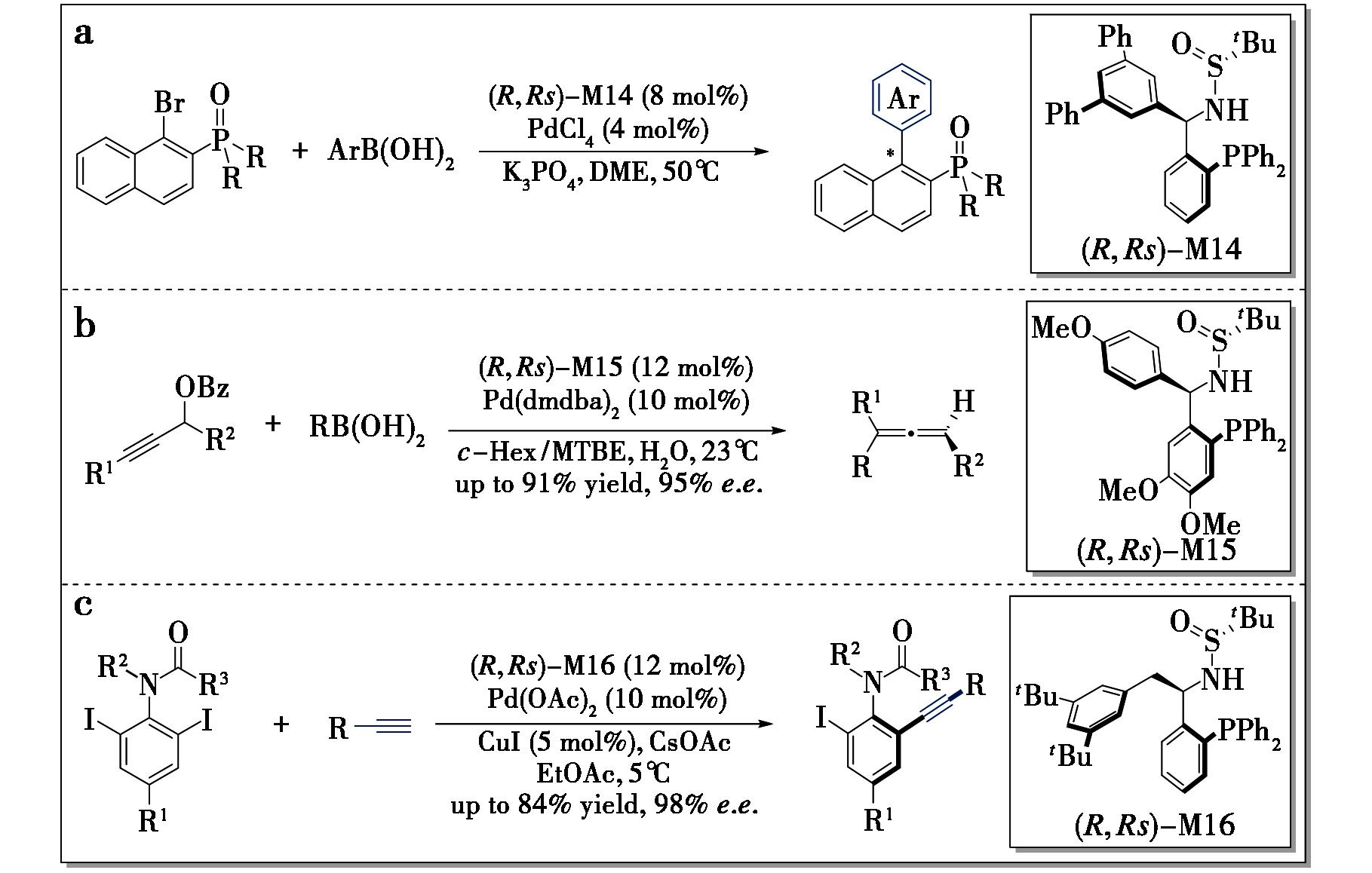
a.不对称Suzuki偶联反应制备轴手性联芳基单氧化膦[27];b.炔丙醇衍生物与有机硼酸的不对称偶联反应[28];c.去对称Sonogashira交叉偶联反应制备轴手性苯胺类化合物[31]
图7 Ming-Phos在钯催化不对称偶联反应中的应用
Fig.7 Application of Ming-Phos in palladium-catalyzed asymmetric coupling reactions
联烯作为一类重要的不饱和烃,因其独特的轴向手性特征而备受有机化学、药物化学及材料科学等领域关注。目前,过渡金属催化炔丙醇衍生物与有机金属试剂的交叉偶联反应已实现外消旋联烯的合成,基于手性转移策略的手性联烯合成研究亦取得显著进展。然而,通过过渡金属催化策略构建手性联烯仍面临关键挑战。2020年,Ma等[28]利用新型Ming-Phos配体M15,成功实现首例钯催化外消旋炔丙醇衍生物与有机硼酸的不对称偶联反应,以高对映选择性合成了系列手性联烯化合物(图7b)。机理研究表明,配体M15中两个手性中心在对映选择性控制中均发挥重要作用。此外,烯基联烯可与N-甲基马来酰亚胺、马来酸酐发生Diels-Alder反应,以优异的对映选择性和非对映选择性构建含有3个连续手性中心的双环/三环化合物,其绝对构型经X射线单晶衍射确证,充分展现了手性联烯在复杂分子合成中的应用潜力。
阻转异构苯胺类化合物作为重要的C-N轴手性分子,其N-端官能团化制备策略已得到广泛研究[29],但通过C-端官能团催化构建该类轴手性结构的进展相对滞后[30]。2022年,本课题组利用Pd-Ming-Phos催化体系,通过去对称Sonogashira交叉偶联反应实现了系列轴手性苯胺类化合物的高效合成(图7c)[31]。研究表明酰基取代基的空间位阻对反应效率起决定性作用,当使用小位阻酰基取代基时,因二取代副产物生成量增加导致产率下降。机理研究证实,原料的去对称化过程与产物的动力学拆分共同赋予反应高对映选择性。稳定性测试显示,产物N—Ar键旋转能垒为28.2 kcal/mol,较低的能垒可能是其易发生外消旋化的重要原因。
手性有机硅烷作为重要的分子骨架,在药物化学与材料科学领域具有广泛应用。尽管化学家已发展多种策略实现手性苄基硅烷的对映选择性合成,但多数转化局限于芳基烷基甲基硅烷,而含有2个空间构型相似芳香环取代的手性二芳基甲基硅烷的高对映选择性合成仍面临显著挑战。本课题组还报道了钯催化N-磺酰腙[32-35]、芳基溴与硅基硼酯的不对称三组分反应,借助Ming-Phos配体高效构建了高对映选择性的二芳基甲基硅烷(图8a)[36]。对照实验证实,钯催化剂是获取手性硅烷的核心要素,而铜盐与4-甲氧基吡啶通过促进Cu-SiMe2Ph物种形成以驱动金属转移过程,对反应效率起决定性作用。N-甲苯磺酰腙的苯基对位取代基电子效应对产率影响显著,强供电子基团取代时几乎无法检测到目标产物。机理研究表明,卡宾配位的钯物种与Cu-SiMe2Ph的金属转移优先于迁移插入,且芳基更易发生迁移插入反应。2023年,Wu等[37]通过密度泛函理论计算深入解析该反应机理,发现Ming-Phos配体在不同基元反应中展现出自适应性,从而优化反应活性与立体选择性。反应中零价钯的氧化加成步骤为决速步骤,随后二价钯中间体的卡宾化反应作为手性决定步骤,其产物立体构型由配体的反位效应与边臂效应协同调控。
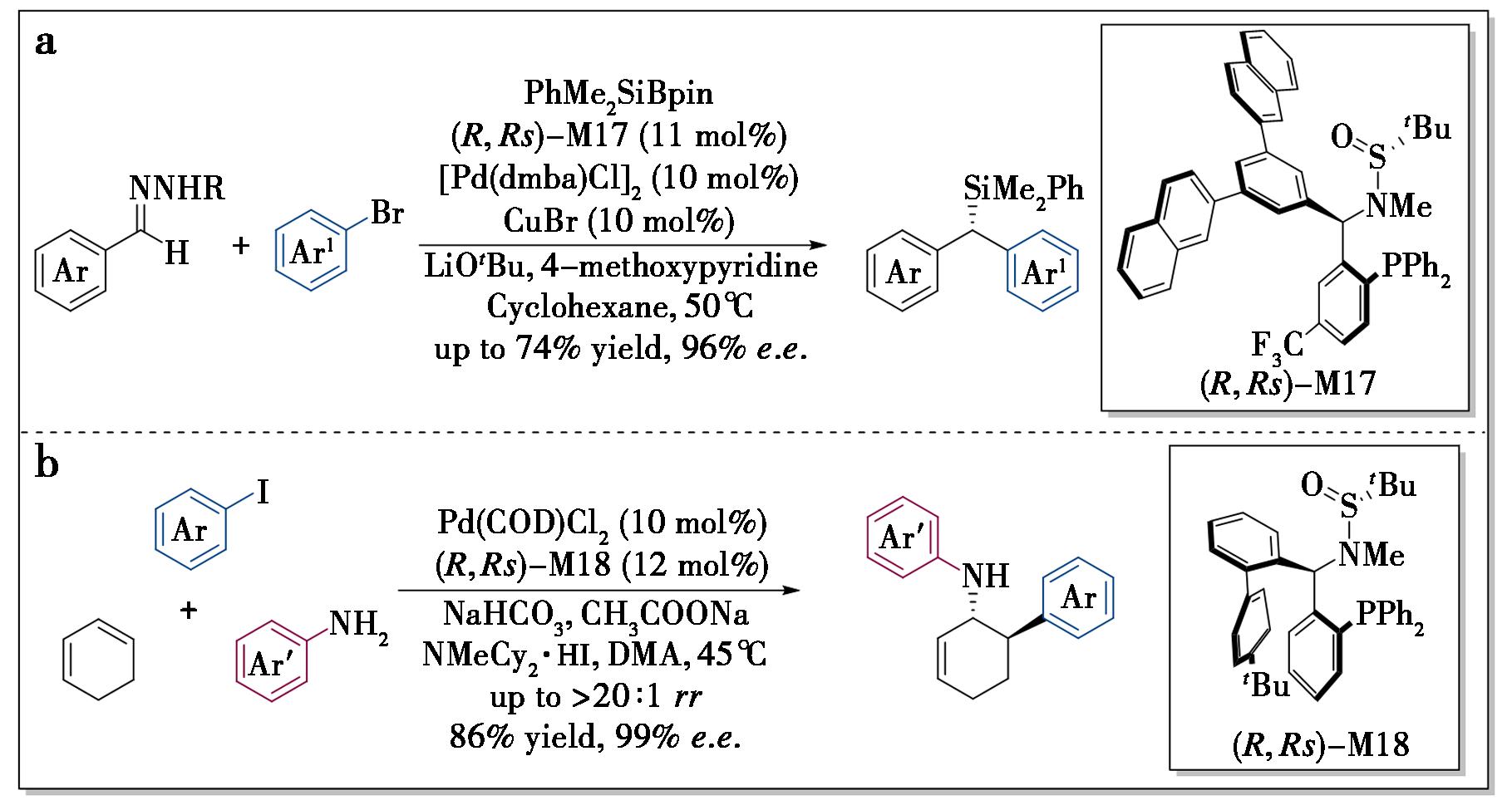
a.钯催化N-磺酰腙、芳基溴与硅基硼酯的不对称三组分反应[36];b.钯催化芳基碘化物、苯胺与1,3-环己二烯的不对称三组分反应[41]
图8 Ming-Phos在钯催化不对称三组分反应中的应用
Fig.8 Application of Ming-Phos in palladium-catalyzed asymmetric three-component reactions
作为一类至关重要的手性环烷基胺,手性环己烯基胺在制药与香料行业中应用广泛,同时亦是多种生物碱合成的关键构建单元[38-40]。尽管钯催化的不对称三组分双烯碳胺化反应可用于构建此类化合物,但相关研究仍处于相对匮乏的状态。这主要归因于该类三组分反应存在多重竞争性副反应,区域选择性的调控(以避免区域异构体生成)以及苯胺可能与催化剂发生竞争性螯合(进而导致对映选择性降低)等问题尚未得到有效解决。2024年,本课题组以芳基碘化物为碳亲电试剂、苯胺为氮亲核试剂,报道了Pd/M18催化的1,3-环己二烯不对称三组分碳胺化反应,为多样化手性环己烯基胺的模块化组装提供了一条高效路径(图8b)[41]。研究表明,添加剂NaHCO3和NMeCy2·HI对反应产率具有显著影响;移除CH3COONa后,反应的对映选择性与区域选择性均受到明显干扰。在苯胺底物适用性考察中发现,电子效应与空间位阻对反应活性的影响尤为显著:带有富电子基团的苯胺可顺利转化为目标产物,而缺电子基团的引入会导致反应效率下降;邻位取代底物的对映选择性优于对位及间位取代底物,且其区域选择性也得到显著提升。此外,机理研究证实,该反应对钯催化剂和苯胺的浓度呈一级反应动力学依赖关系。
硅杂环丁烷(SCBs)与炔烃的不对称扩环反应已成为构建硅手性化合物的重要策略。2024年,本课题组报道了铑催化SCBs与端炔的不对称环化反应,该方法借助新型Ming-Phos配体M19,以优异的对映选择性高效构建了一系列结构多样的手性硅杂环化合物(图9)[42]。研究表明,在Ming-Phos膦配体中引入富电子且空间位阻较大的3,5-二叔丁基苯基基团可显著提升反应的对映选择性。该体系展现出良好的底物适应性与官能团兼容性,产物可通过催化氢化、烯丙基溴化、氧化等反应实现多样化衍生化,进一步转化为多种高附加值手性硅化合物。基于实验结果,本课题组提出了可能的催化循环:Rh(Ⅰ)-M19配合物首先与端炔配位,随后对SCBs发生氧化加成生成五元环铑中间体;炔烃迁移插入形成铑硅杂环庚烯中间体;最后经还原消除释放产物并再生催化剂。该工作不仅为手性硅化合物的合成提供了新方法,也为Ming-Phos配体在不对称催化中的应用开辟了新方向。
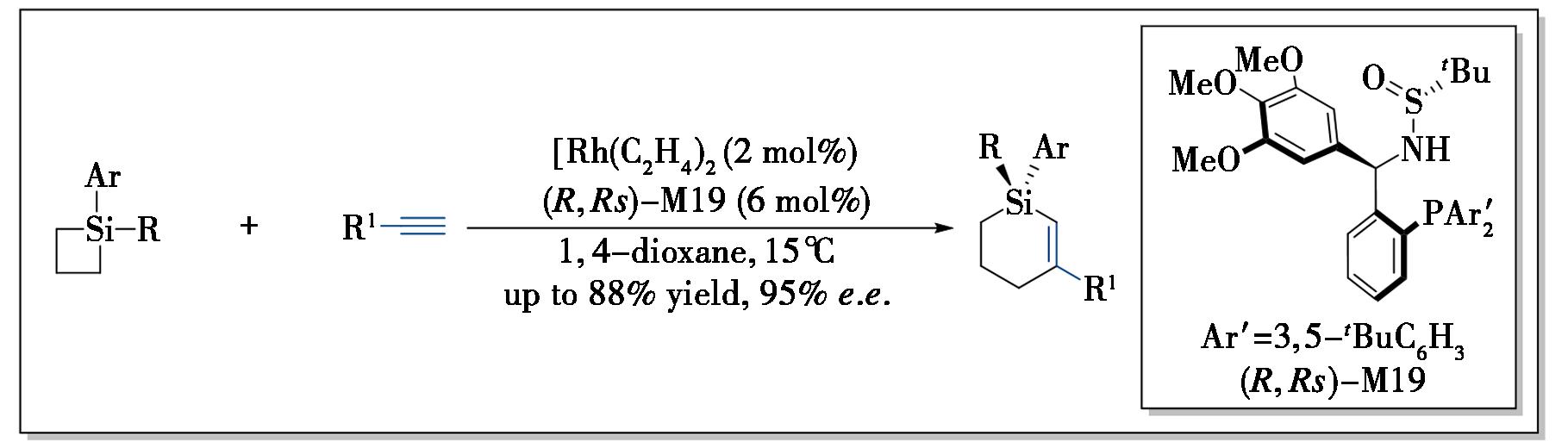
图9 Ming-Phos在铑催化不对称反应中的应用[42]
Fig.9 Application of Ming-Phos in rhodium-catalyzed asymmetric reactions[42]
与单立体中心或1,2-相邻立体中心分子的不对称合成相比,通过单一催化剂同时构建非相邻的1,3-立体中心仍然是一个巨大的挑战。2024年,Kong等[43]以M20为配体,通过镍催化烯烃链状芳基溴化物与α-溴代酰胺的还原环化/交叉偶联反应,高对映选择性和非对映选择性地合成了一系列含1,3-非相邻立体中心的氧吲哚类化合物(图10)。研究表明,二级烷基亲电试剂的选择至关重要,若选用不当,易引发二聚化或自由基加成/环化等副反应。值得关注的是,此前发现的可加速金属还原剂对Ni(Ⅱ)还原的MgCl2,能显著提升该反应的非对映选择性。机理实验证实,反应中存在源自二级烷基亲电试剂的烷基自由基中间体,且排除了烷基锌作为转化关键中间体的可能性。通过X射线单晶衍射分析所制备的镍/Ming-Phos配合物发现,镍与磷、氧原子配位,且该配合物为反应的催化活性物种。作者提出的可能反应机理如下:芳基溴化物与手性Ni(0)物种发生氧化加成,经Zn还原生成芳基镍(Ⅰ)物种;该物种进一步与烯烃发生5-exo环化反应,生成σ-烷基镍(Ⅰ)物种;α-溴代酰胺向生成的Ni(Ⅰ)物种发生单电子转移,形成烷基自由基和Ni(Ⅱ)物种;镁盐通过与2个羰基的相互作用,将Ni(Ⅱ)中间体与烷基自由基连接,促进二者发生分子内重组,形成Ni(Ⅲ)中间体;在过量Zn存在下,Ni(Ⅲ)中间体被还原为Ni(Ⅱ)中间体,随后发生还原消除反应,生成目标产物并再生催化活性 Ni(0)催化剂。

图10 Ming-Phos在镍催化不对称反应中的应用[43]
Fig.10 Application of Ming-Phos in nickel-catalyzed asymmetric reactions[43]
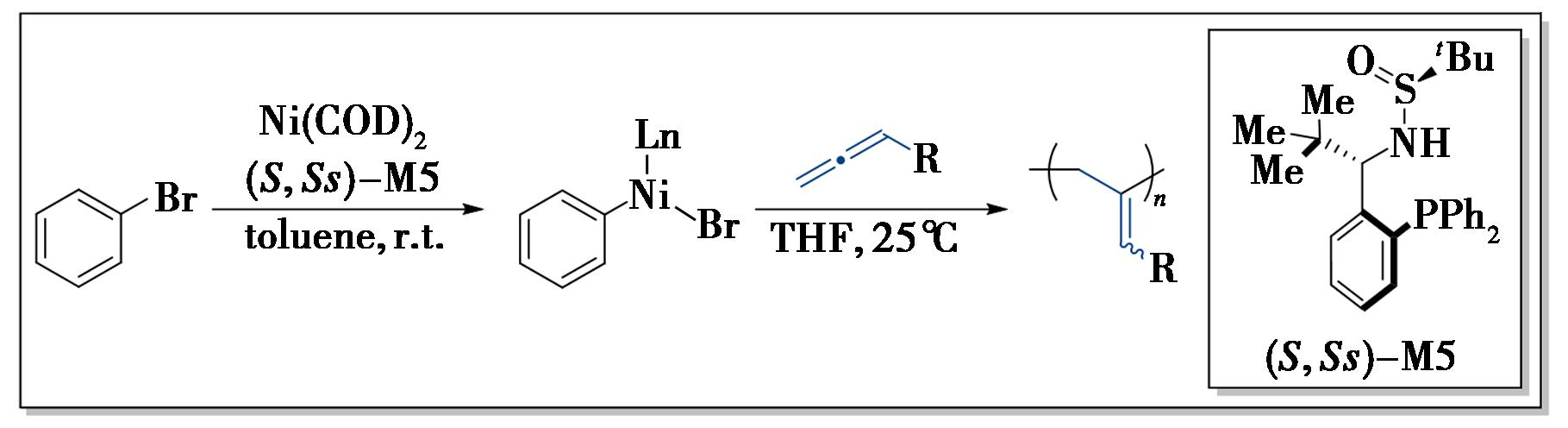
图11 Ming-Phos在镍催化聚合反应中的应用
Fig.11 Application of Ming-Phos in nickel-catalyzed polymerization reactions
聚丙二烯因其主链或侧基含有的不饱和键,成为构建功能材料极具吸引力的合成前体之一。然而,聚丙二烯的高区域选择性合成仍面临挑战。2019年,Wu等[44]开发了一种新型镍(Ⅱ)催化剂,该催化剂以M5为配体,能够高效引发多种丙二烯单体的聚合反应,且反应速率快,具有可控特征。利用该催化剂,可高产率获得结构明确的聚丙二烯,其摩尔质量(Mn)可控,摩尔质量分布(Mw/Mn)较窄。此外,镍(Ⅱ)/M5催化剂对丙二烯单体的累积双键表现出优异的区域选择性,丙二烯单体聚合的2,3-区域选择性高达>99.9%。值得注意的是,以镍(Ⅱ)/M5为引发剂时,含烷基、烷氧基、取代苯基等不同官能团的多种单体均可有效聚合,得到具有更高2,3-区域选择性的聚丙二烯。
自2014年首次报道以来,Ming-Phos配体在多种不对称催化反应中均展现出优异的不对称诱导能力,具体包括金催化的[3+2]环加成反应、[4+3]环加成反应;铜催化的[3+2]环加成反应;银催化的[3+2]环加成反应;钯催化的Heck型反应、交叉偶联反应及三组分反应;铑催化的环化反应;镍催化的还原环化/交叉偶联反应等。此外,该配体在丙二烯聚合反应中亦表现突出。上述研究成果充分证实,Ming-Phos配体在不对称催化及材料聚合领域具有巨大的应用潜力。展望未来,Ming-Phos配体的发展可聚焦于以下核心方向:1)拓展其在廉价金属(如铁、钴、锌等)催化体系中的应用;2)深入探究Ming-Phos配体的动态调控机制;3)利用该配体解决当前对映选择性难以调控的其他反应类型;4)将基于该配体发展的催化体系应用于更多生物活性分子、药物及新材料的合成中。
[1]Hu A,Zhang Z M,Xiao Y,Zhang J L.Org.Synth.,2020,97:262-273.
[2]Li W,Zhang J L.Acc.Chem.Res.,2024,57(4):489-513.
[3]Liu F,Qian D,Li L,Zhao X,Zhang J L.Angew.Chem.Int.Ed.,2010,49(37):6 669-6 672.
[4]Zhang Z M,Chen P,Li W,Niu Y,Zhao X L,Zhang J L.Angew.Chem.Int.Ed.,2014,53(17):4 350-4 354.
[5]Zhou L,Xu B,Ji D,Zhang Z M,Zhang J L.Chin.J.Chem.,2020,38(6):577-582.
[6]Chen M,Zhang Z M,Yu Z,Qiu H,Ma B,Wu H H,Zhang J L.ACS Catal.,2015,5(12):7 488-7 492.
[7]Wang Y,Zhang Z M,Liu F,He Y,Zhang J L.Org.Lett.,2018,20(20):6 403-6 406.
[8]Xu B,Zhang Z M,Han J,Gu G,Zhang J L.Chin.J.Chem.,2022,40(12):1 407-1 412.
[9]Gao H,Wu X,Zhang J L.Chem.Commun.,2010,46:8 764-8 766.
[10]Di X,Wang Y,Wu L,Zhang Z M,Dai Q,Li W,Zhang J L.Org.Lett.,2019,21(9):3 018-3 022.
[11]Zhang Z M,Xu B,Xu S,Wu H H,Zhang J L.Angew.Chem.Int.Ed.,2016,55(21):6 324-6 328.
[12]Xu B,Zhang Z M,Xu S,Liu B,Xiao Y,Zhang J L.ACS Catal.,2017,7(1):210-214.
[13]Zhang R H,Xu B,Zhang Z M,Zhang J L.Acta Chim.Sinica,2020,78(3):245-249.
张荣华,许冰,张展鸣,张俊良.化学学报,2020,78(3):245-249.
[14]Wu L Z,Zhang F Y,Zhang Z T,Shang L,Liu Y.Chin.J.Org.Chem.,2020,40(8):2 460-2 467.
武力左,张峰源,章振涛,尚垒,刘宇.有机化学,2020,40(8):2 460-2 467.
[15]Liu B,Zhang Z M,Xu B,Xu S,Wu H H,Zhang J L.Adv.Synth.Catal.,2018,360(11):2 144-2 150.
[16]Wu Y,Xu B,Liu B,Zhang Z M,Liu Y.Org.Biomol.Chem.,2019,17:1 395-1 401.
[17]Guo H C,Ma J A.Angew.Chem.Int.Ed.,2006,45(3):354-366.
[18]Ping Y,Li Y,Zhu J,Kong W.Angew.Chem.Int.Ed.,2019,58(6):1 562-1 573.
[19]You W,Brown M K.J.Am.Chem.Soc.,2014,136(42):14 730-14 733.
[20]Tong S,Limouni A,Wang Q,Wang M X,Zhu J.Angew.Chem.Int.Ed.,2017,56(45):14 192-14 196.
[21]Yang H,Yang S,Wu X F,Chen F.Green Synth.Catal.,2025,6(1):81-85.
[22]Zhou L,Li S,Xu B,Ji D,Wu L,Liu Y,Zhang Z M,Zhang J L.Angew.Chem.Int.Ed.,2020,59(7):2 769-2 775.
[23]Li S,Chen Q,Zhang Z M,Zhang J L.Green Synth.Catal.,2021,2(4):374-376.
[24]Cao K,Han J,Ye W,Hu D,Ye Z,Yang J,Zhang J L,Chen F.Adv.Sci.,2024,11(34):2 403 470.
[25]Cao K,Han J,Shen H,Yang J,Zhang J L,Chen F.ACS Catal.,2024,14(7):5 305-5 313.
[26]Zhang G,Yang B,Yang J,Zhang J L.J.Am.Chem.Soc.,2022,146(8):5 493-5 501.
[27]Zhang Y,Li Y,Pan B,Xu H,Liang H,Jiang X,Liu B,Tse M K,Qiu L.ChemistrySelect,2019,4(17):5 122-5 125.
[28]Wang H,Luo H,Zhang Z M,Zheng W F,Yin Y,Qian H,Zhang J L,Ma S M.J.Am.Chem.Soc.,2020,142(21):9 763-9 771.
[29]Wang D,Zong J,Wang B,Sun L,Xiao X,Piao H,Ke M,Chen F.Green Synth.Catal.,2025,6(2):211-215.
[30]He Z W,Liang D,Chen J R,Cheng Y,Xiao W J.Green Synth.Catal.,2025,doi:10.1016/j.gresc.2025.03.001.
[31]Yang B,Yang J,Zhang J L.Chin.J.Chem.,2022,40(3):317-322.
[32]Sivaguru P,Pan Y,Wang N,Bi X.Chin.J.Chem.,2024,42(17):2 071-2 108.
[33]Xia Y,Wang J.Chem.Soc.Rev.,2017,46:2 306-2 362.
[34]Liu Z,Sivaguru P,Zanoni G,Bi X.Acc.Chem.Res.,2022,55(12):1 763-1 781.
[35]Liu C,Abdukerem D,Zhu W,Xia K,Mao Z,Abdukader A.Green Synth.Catal.,2024,5(1):62-67.
[36]Yang B,Cao K,Zhao G,Yang J,Zhang J L.J.Am.Chem.Soc.,2022,144(34):15 468-15 474.
[37]Xiao B,Sun T Y,Zhang J L,Wu Y D.Sci.China Chem.,2023,66:2 817-2 827.
[38]Downham R,Ng F W,Overman L E.J.Org.Chem.,1998,63(23):8 096-8 097.
[39]Kwak Y S,Winkler J D.J.Am.Chem.Soc.,2001,123(30):7429-7430.
[40]Tang P,Wang H,Zhang W,Chen F E.Green Synth.Catal.,2020,1(1):26-41.
[41]Wang J,Xu B,Wang Y,Xia G,Zhang Z M,Zhang J L.J.Am.Chem.Soc.,2024,146(31):21 231-21 238.
[42]Sun Y,Zhou K,Ma C,Li Z,Zhang J L.Green Synth.Catal.,2024,5(3):205-210.
[43]Pan Q,Wang K,Xu W,Ai Y,Ping Y,Liu C,Wang M,Zhang J L,Kong W.J.Am.Chem.Soc.,2024,146(22):15 453-15 463.
[44]Kang S M,Xu X H,Xu L,Zhou L,Liu N,Wu Z Q.Polym.Chem.,2019,12:4 822-4 828.