碳量子点(Carbon Quantum Dots,CQDs)是一种零维且具有荧光性能的碳纳米材料,其尺寸一般在1~10 nm之间[1]。因其具有优良的水溶性、生物相容性和低细胞毒性,被广泛应用于分析检测[2]、细胞成像[3]、催化材料[4]等领域,是近年来荧光快速检测研究的热点材料。
铁元素是人体维持代谢功能所必需的重要生命元素,但过量摄入或缺少摄入会导致人体铁中毒或缺铁性贫血[5],从而增加人体内分泌器官功能损害以及心血管疾病的危险[6],故对Fe3+含量的检测在自然水质环境、化工生产、生活食品等方面具有重要意义。
Fe3+的检测方法有多种,如原子吸收光谱法[7]、电感耦合等离子体光谱法[8]、电化学法[9]等,但均存在操作复杂、耗时长等问题。相较之下,灵敏度高、生物相容性好、检测方法简单的荧光检测法具有优势。CQDs作荧光探针因其成本低、操作简便、响应灵敏、选择性好等优点,在检测领域具有较好的应用前景[10,11]。CQDs用于Fe3+检测已有报道[12],然而耐酸型CQDs用于检测Fe3+的研究鲜有报道,因此,研发一种能够在酸性环境快速高效检测Fe3+离子的CQDs具有非常重要的意义[13]。
本文采用一步水热法,以蔗糖为碳源,磷酸二氢铵为氮源及磷源,制备具有亮蓝色荧光的耐酸型氮、磷掺杂CQDs(ART-N,P-CQDs),基于静态猝灭和荧光共振能量转移/内滤效应所引发的荧光猝灭机理,建立了以ART-N,P-CQDs为荧光探针测定Fe3+的方法,可望应用于市面上含铁药品中铁含量的检测。
1 实验部分
1.1 主要仪器与试剂
F-7000型荧光分光光度计(日本株式会社);Lambda 265型紫外分光光度计(美国珀金埃尔默股份有限公司);Tensor 27型傅里叶红外光谱仪(德国Bruker光谱仪器公司);JEM-F200型透射电镜(日本电子株式会社);英国Malvern Zetasizer Nano ZS90型纳米粒度及Zeta电位分析仪(美国DLS公司);FD-1A-50型真空冷冻干燥机(北京博医康实验仪器有限公司);ESCALAB 250Xi型X射线光电子能谱仪(美国Thermo Scientific公司)。
硫酸银、一水合柠檬酸、蔗糖(分析纯,上海润捷化学试剂有限公司);磷酸二氢铵(分析纯,天津市致远化学试剂有限公司);硫酸亚铁、氯化钠、十二水合磷酸氢二钠(分析纯,广东光华科技股份有限公司);九水合硝酸铬、无水硫酸镁、六水合三氯化铁(分析纯,上海阿拉丁生化科技股份有限公司);浓硫酸、浓硝酸、六水合硝酸锌、过氧化氢(分析纯,广州化学试剂厂);无水硫酸铜(分析纯,汕头市西陇化工厂有限公司);硝酸铅(分析纯,山东西亚化学工业有限公司);二水合氯化钴(分析纯,天津市福晨化学试剂厂);二水合氯化钡、六水合硫酸镍、氯化钙(分析纯,天津市大茂化学试剂厂);硫酸汞、硫酸奎宁(分析纯,上海麦克林生化科技股份有限公司)。
1.2 实验方法
1.2.1 ART-N,P-CQDs的制备
称取1.00 g蔗糖溶于25.00 mL去离子水中,然后加入1.00 g磷酸二氢铵,将上述溶液转入50 mL以聚四氟乙烯为衬底的高压反应釜内,在180 ℃的恒温干燥箱内反应6 h。冷却反应釜后,用0.21 μm滤膜过滤其中溶液即为CQDs原液,置于4 ℃冰箱中冷藏备用。
1.2.2 ART-N,P-CQDs的表征
采用UV-Vis和荧光分光光度计对ART-N,P-CQDs的紫外吸收和荧光光谱进行表征;采用 FT-IR表征ART-N,P-CQDs的表面官能团;采用纳米粒度分析仪测定ART-N,P-CQDs的粒径分布;采用TEM对ART-N,P-CQDs进行形貌分析;采用XPS对ART-N,P-CQDs的元素种类和含量进行分析。
1.2.3 荧光量子产率计算
以硫酸奎宁(315 nm激发波长下的QY为54%)为参照物,计算ART-N,P-CQDs荧光量子产率。将硫酸奎宁溶于0.1 mol/L的H2SO4溶液中,通过紫外-可见吸收光谱得到硫酸奎宁和ART-N,P-CQDs的吸光度(吸光度均小于0.1)。然后通过荧光光谱得到对应的荧光积分面积,按下列公式计算其QY。
QYART-N,P-CQDs(%)=QYstd(IART-N,P-CQDs/Istd)
(Astd/AART-N,P-CQDs)(ηART-N,P-CQDs/ηstd)2
(1)
式中,QY为荧光量子产率,%;I为荧光积分面积;A为315 nm激发波长处吸光度;η为溶液折射率,其中水的折射率为1.33,η水/η0.1 mol/L硫酸≈1[14]。
2 结果与讨论
2.1 ART-N,P-CQDs表征及其光学性质
由图1a TEM照片可知制备的ART-N,P-CQDs为较为均匀的球形结构,且具有良好的分散性。对ART-N,P-CQDs的粒径进行统计分析,由图1b可知,经过高斯拟合后得到ART-N,P-CQDs的平均粒径为1.7 nm。
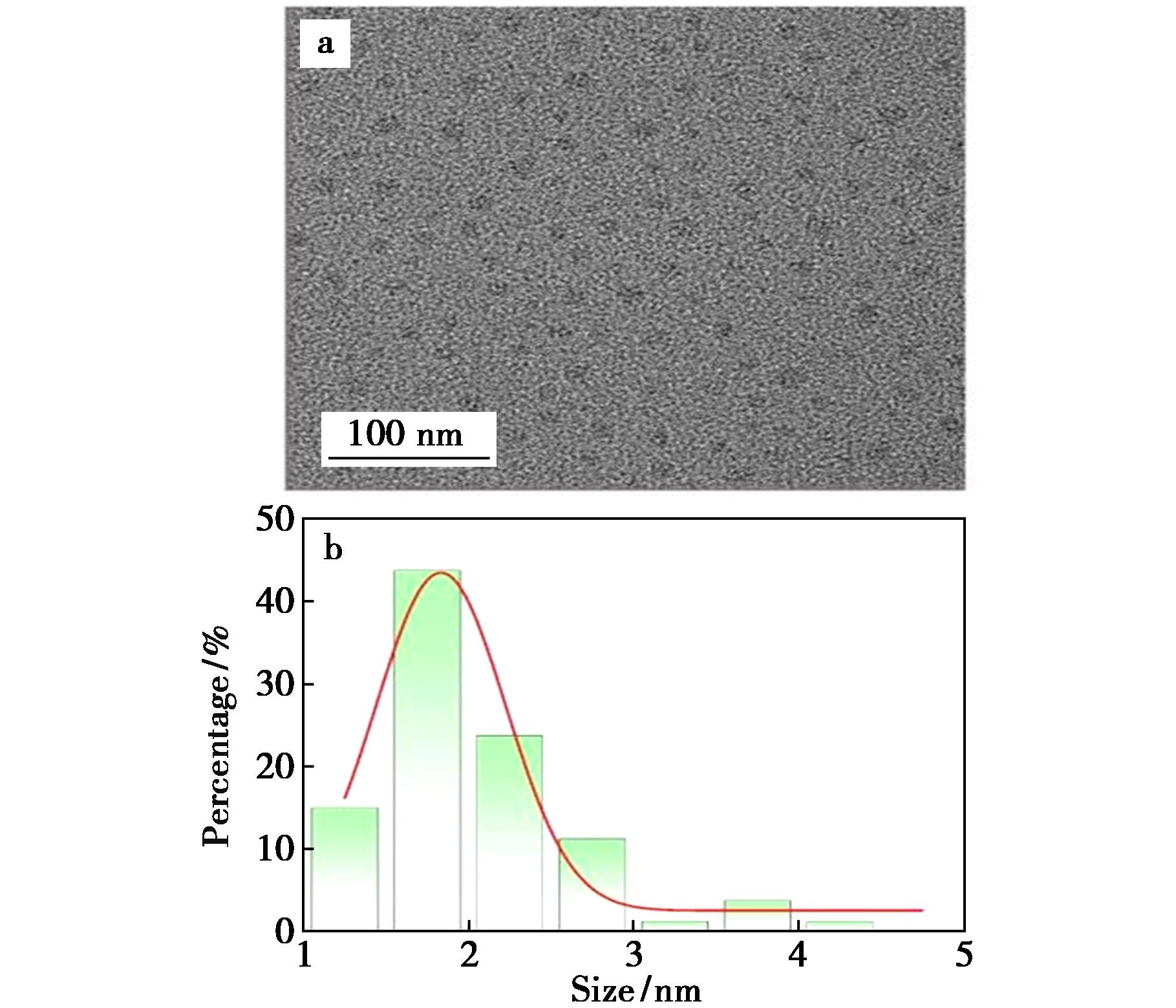
图1 ART-N,P-CQDs的TEM图(a)和粒径分布图(b)
Fig.1 TEM spectra (a) and particle size distribution of ART-N,P-CQDs (b)
由图2激光纳米粒径分析结果可知ART-N,P-CQDs粒径在1~2 nm之间,与上述统计分析结果一致,但其在100 nm处存在的峰可能是由于杂质的存在或纳米颗粒发生集聚所导致。
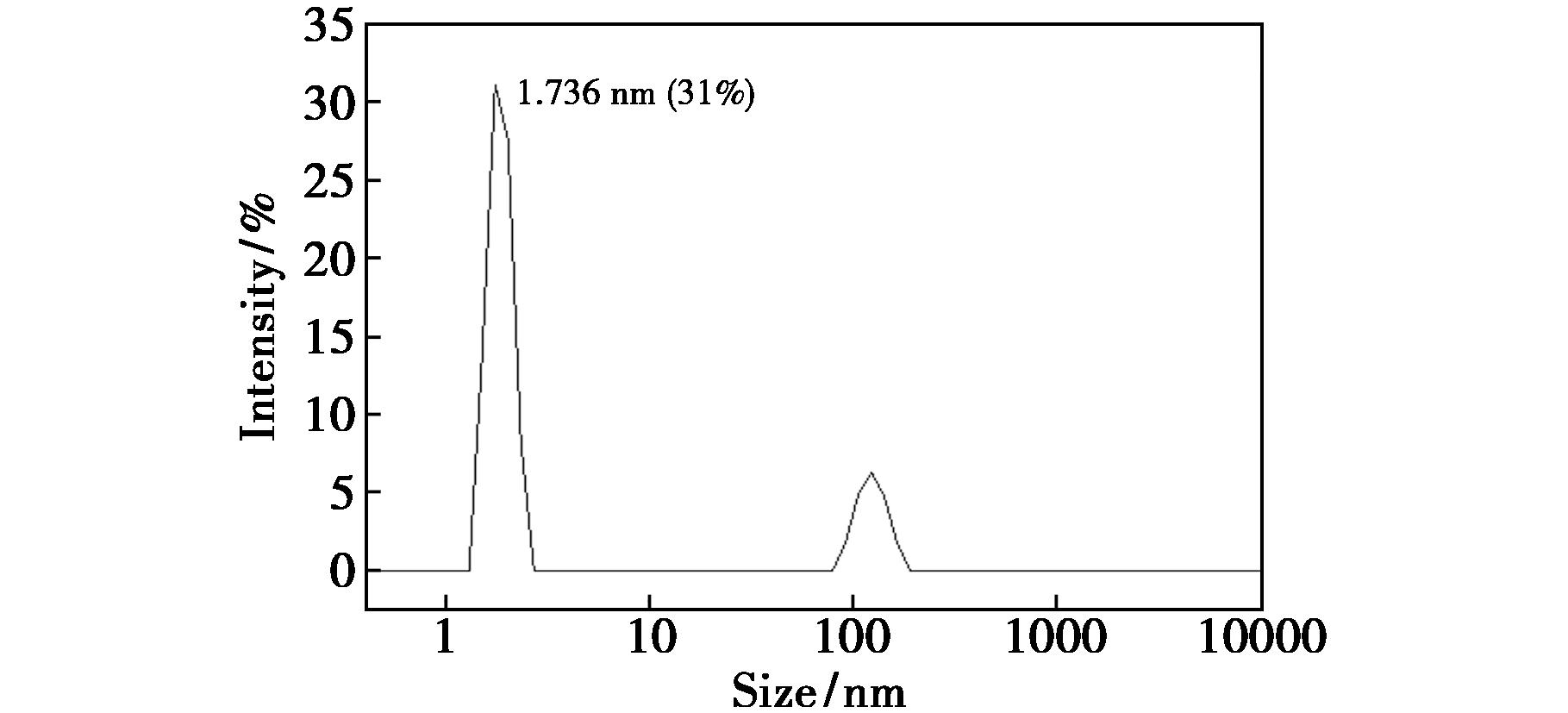
图2 ART-N,P-CQDs的纳米粒径分析图
Fig.2 Particle size distribution of ART-N,P-CQDs
由图3a可知,ART-N,P-CQDs在315 nm激发波长照射下发出蓝色的光[15]。而ART-N,P-CQDs在215和285 nm处具有强烈的紫外吸收峰,330 nm处存在肩峰(图3b)。上述峰是由n-π*和π-π*跃迁引起的吸收峰,说明ART-N,P-CQDs内含有C![]() C和C
C和C![]() O等官能团[16]。
O等官能团[16]。
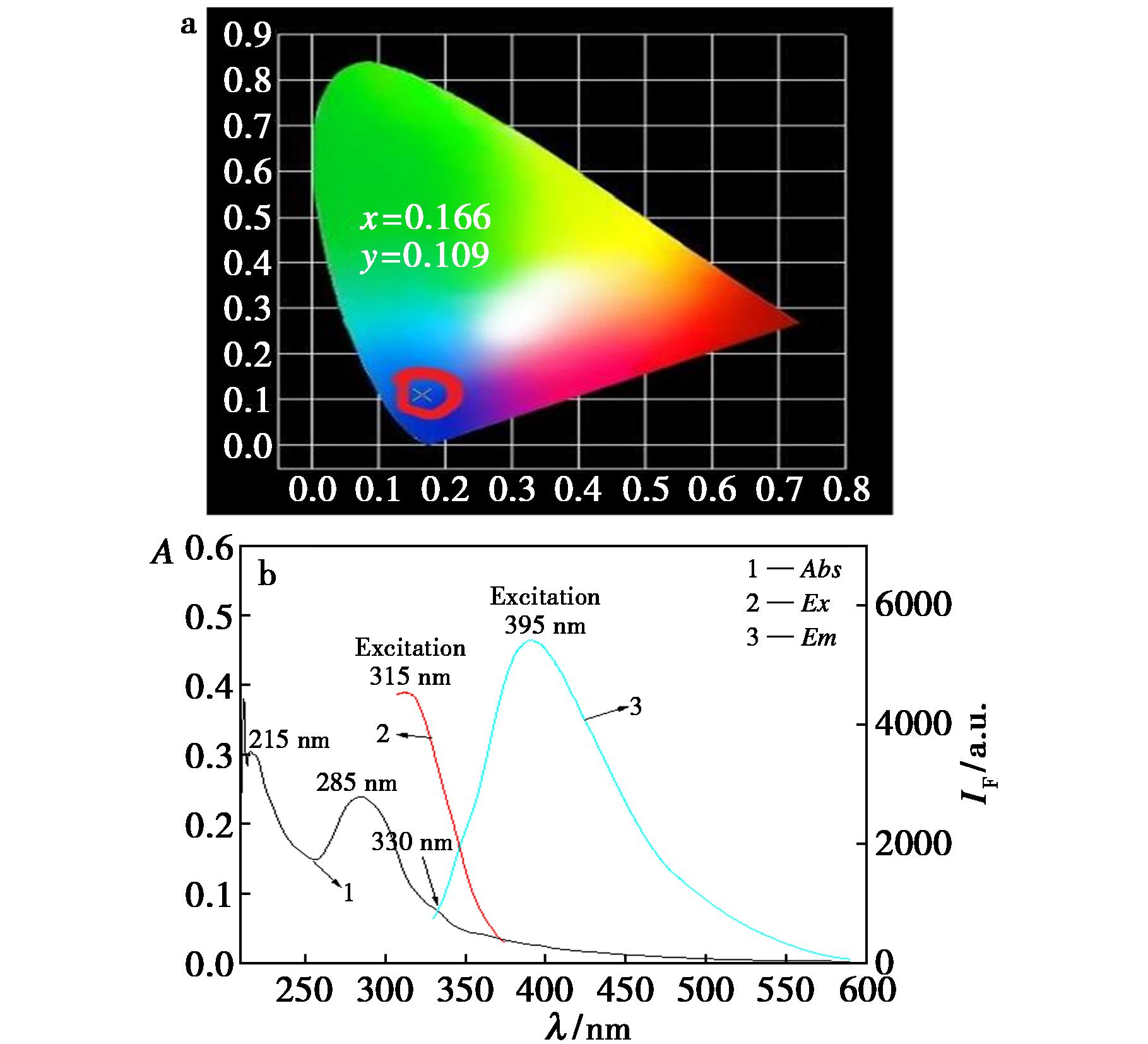
图3 ART-N,P-CQDs的CIE色度图(a)和紫外-荧光光谱图(b)
Fig.3 CIE chromaticity diagram (a) and UV-fluorescence spectra (b) of ART-N,P-CQDs
由图4所示的ART-N,P-CQDs的FT-IR可知,在3 400、3 128 cm-1处为—OH和C![]() C的伸缩振动,2 998、2 864 cm-1为N—H、C—H的伸缩振动,1 716、1 635 cm-1处为
C的伸缩振动,2 998、2 864 cm-1为N—H、C—H的伸缩振动,1 716、1 635 cm-1处为![]() 弯曲振动,1 400 cm-1为C—N的伸缩振动,1 269、1 120、999 cm-1分别为P
弯曲振动,1 400 cm-1为C—N的伸缩振动,1 269、1 120、999 cm-1分别为P![]() O、P—O、C—O—P的伸缩振动,883 cm-1为N—H面外弯曲振动,2 437、540 cm-1为磷酸盐以及胺[17]。上述结果表明ART-N,P-CQDs表面具有不饱和碳结构、含氧基团、含氮基团以及含磷基团。证明氮磷成功掺杂在碳量子点中,且这些亲水性基团使其在水溶液中具有良好的分散性。
O、P—O、C—O—P的伸缩振动,883 cm-1为N—H面外弯曲振动,2 437、540 cm-1为磷酸盐以及胺[17]。上述结果表明ART-N,P-CQDs表面具有不饱和碳结构、含氧基团、含氮基团以及含磷基团。证明氮磷成功掺杂在碳量子点中,且这些亲水性基团使其在水溶液中具有良好的分散性。
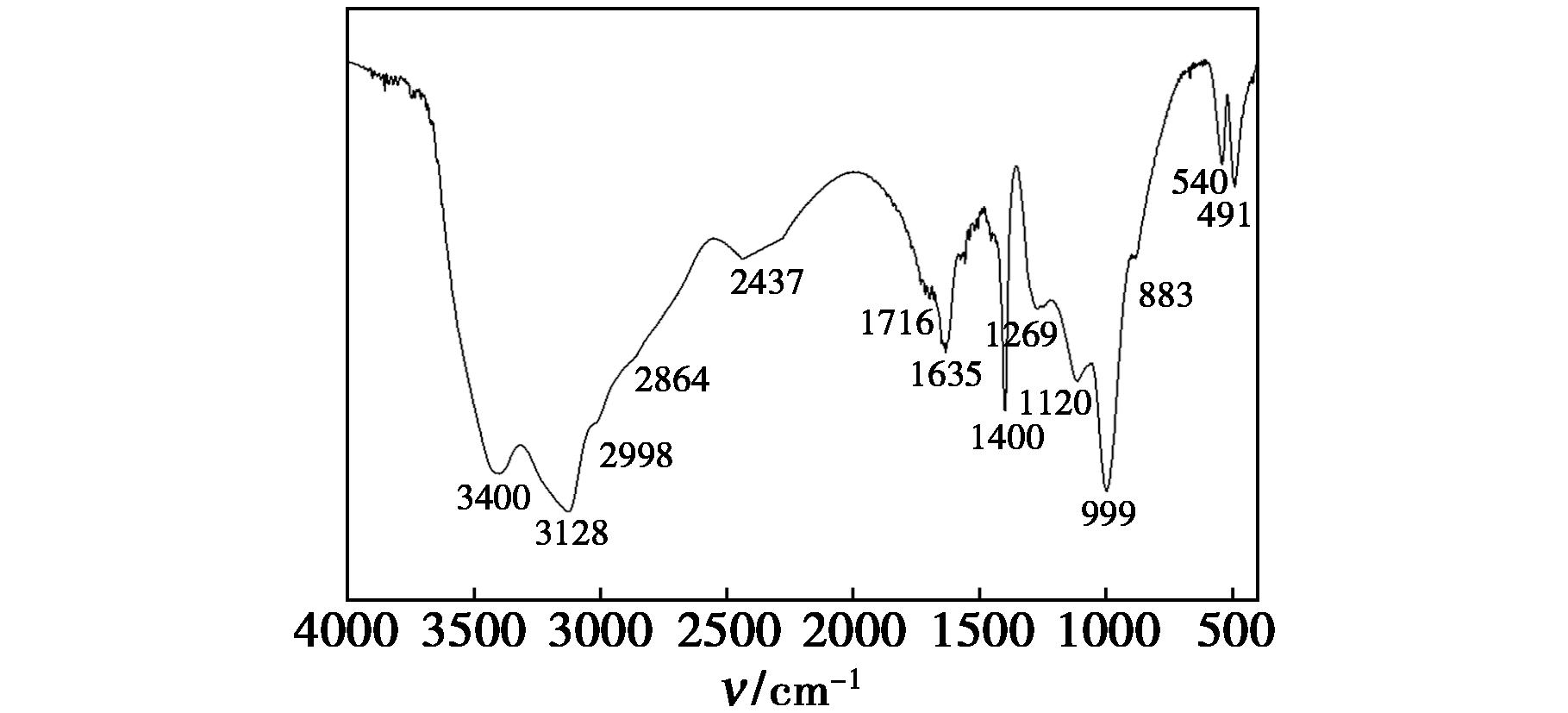
图4 ART-N,P-CQDs的红外光谱图
Fig.4 FT-IR of ART-N,P-CQDs
由图5a可知,ART-N,P-CQDs共有4个不同的峰:C 1s(284.80 eV)、N 1s(400.59 eV)、O 1s(531.88 eV)、P 2p(133.79 eV),表明了ART-N,P-CQDs的表面含有C、O、N、P这4种元素,N和P已经成功掺杂到CQDs中,再由图5b可知,C、O、N、P在其中的占比依次为42.08%、42.78%、5.18%和9.96%。C 1s光谱(图5c)对应![]() (287.78 eV);N 1s光谱(图5d)对应N—H(400.59 eV)、C—N(399.82 eV);O 1s光谱(图5e)对应C—O(530.99 eV)、P—O—P/C—O—C(530.24 eV)、C
(287.78 eV);N 1s光谱(图5d)对应N—H(400.59 eV)、C—N(399.82 eV);O 1s光谱(图5e)对应C—O(530.99 eV)、P—O—P/C—O—C(530.24 eV)、C![]() O(531.88 eV);P 2p光谱(图5f)说明P
O(531.88 eV);P 2p光谱(图5f)说明P![]() O(132.84 eV)、P—O(133.79 eV)的存在[18-20]。
O(132.84 eV)、P—O(133.79 eV)的存在[18-20]。
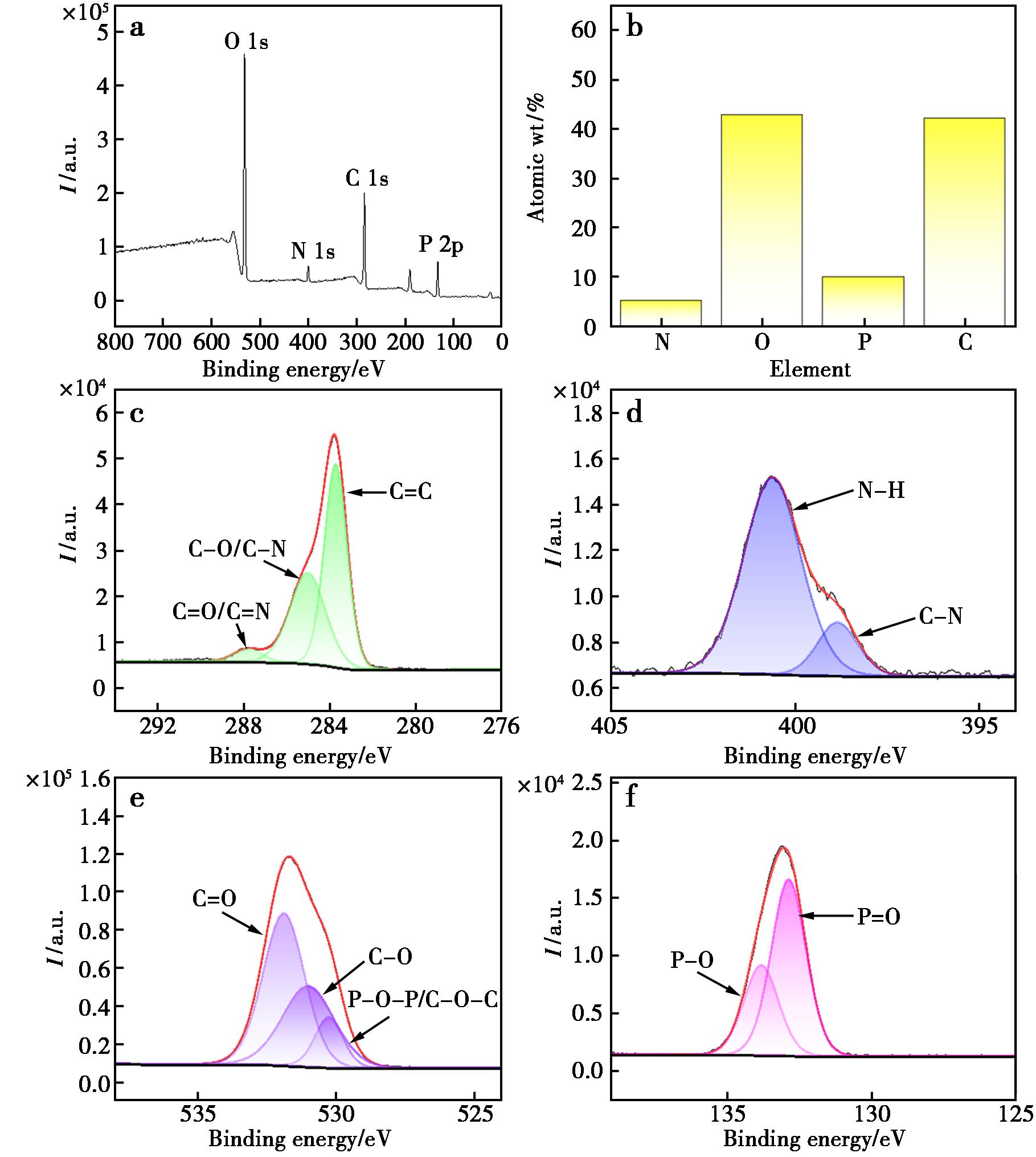
a.XPS全谱图;b.元素含量图;c.C 1s谱图;d.N 1s谱图;e.O 1s谱图;f.P 2p谱图
图5 ART-N,P-CQDs的XPS谱图
Fig.5 XPS spectrum of ART-N,P-CQDs
由图6a和6b可知,λex=315 nm处,ART-N,P-CQDs荧光发射λmax=395 nm,且激发波长在290~330 nm之间,其发射波长不随激发波长变化而改变,由此可推断ART-N,P-CQDs表现出较强的激发独立性。
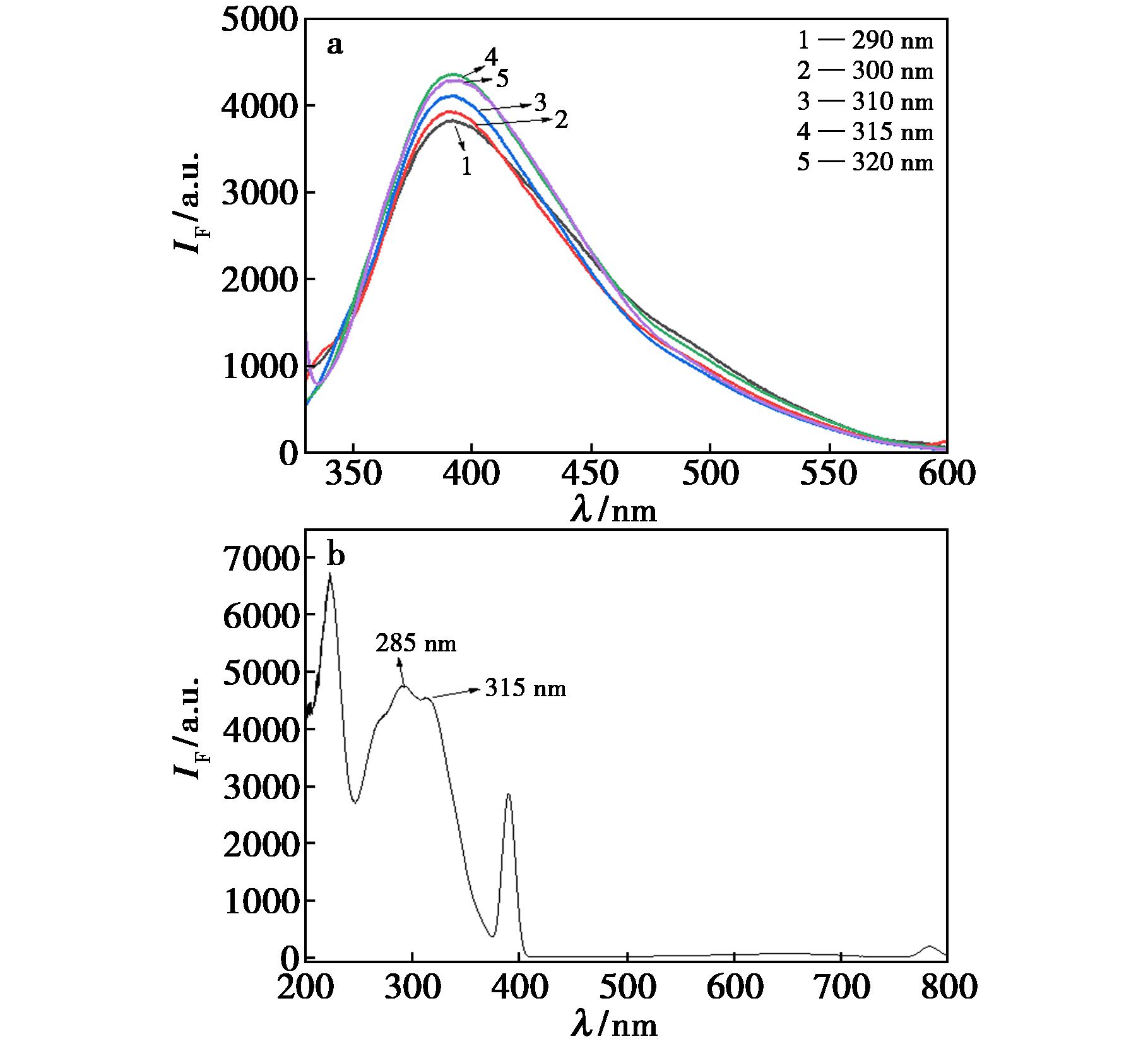
图6 ART-N,P-CQDs的荧光光谱图(a)和激发光谱(b)
Fig.6 Fluorescence spectra (a) and excitation spectra (b) of ART-N,P-CQDs
由图7可知,以硫酸奎宁为参比物质,分别测试ART-N,P-CQDs溶液以及硫酸奎宁溶液在 315 nm处吸光度,并以315 nm为激发波长分别测试其荧光光谱,通过Origin软件对发射峰面积进行积分[21]。基于式(1)对实验数据进行系统计算,得到QYART-N,P-CQDs(%)=54%(9 222.55/113 764)(0.068 1/0.063 3)×12。
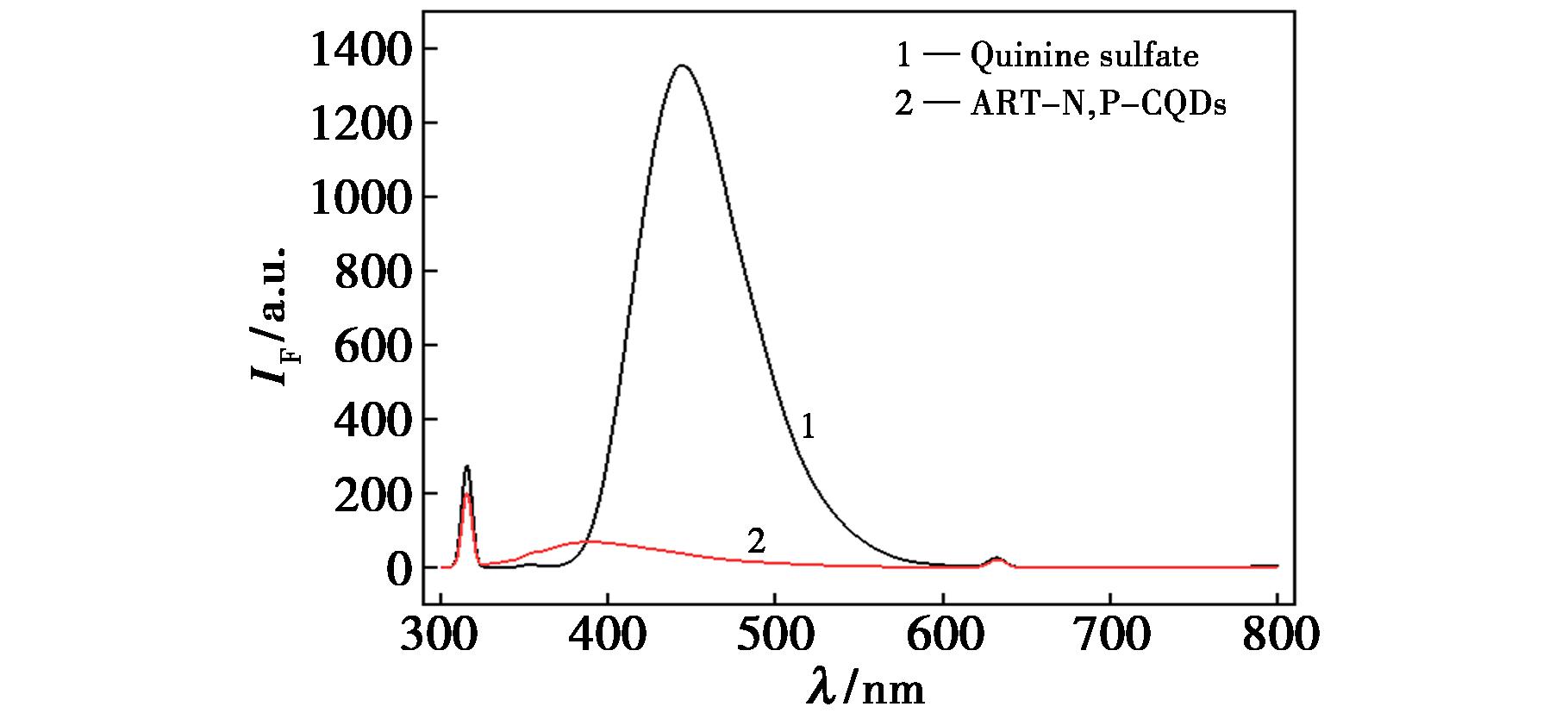
图7 ART-N,P-CQDs和硫酸奎宁的荧光发射图
Fig.7 Fluorescence emission spectra of ART-N,P-CQDs and quinine sulfate
计算结果表明,ART-N,P-CQDs的荧光量子产率为4.7%。
2.2 ART-N,P-CQDs荧光猝灭机理
为了推测Fe3+对ART-N,P-CQDs荧光猝灭机制,通常采用Stern-Volmer方程为依据来判断猝灭机理。Stern-Volmer方程为:
F0/F=1+KSVC=1+Kqτ0C
(2)
式中,F0为未加入Fe3+时ART-N,P-CQDs的荧光强度;F为加入Fe3+时ART-N,P-CQDs的荧光强度;KSV为Stern-Volmer猝灭常数;C为加入Fe3+的浓度;Kq为猝灭过程的速率常数;τ0为无猝灭剂时荧光分子的平均寿命(碳量子点的荧光寿命τ0一般约为1 ns)[22]。
静态猝灭的荧光猝灭常数随温度升高而减小,动态猝灭的荧光猝灭常数随温度升高而增大。由表1可知,随着温度升高,猝灭常数KSV减小,符合静态猝灭的猝灭机理。
表1 不同温度下Fe3+与ART-N,P-CQDs相互作用的Stern-Volmer猝灭常数
Tab.1 Stern-Volmer constants of interaction between Fe3+ and ART-N,P-CQDs at different temperatures

T/℃Linear regression equationKSV/(L·mol-1)Kq/(L·mol-1·s-1)R225F0/F=3.65×103C+0.993 13.65×1033.65×10120.982 635F0/F=3.54×103C+1.0393.54×1033.54×10120.959 355F0/F=2.51×103C+1.0872.51×1032.51×10120.992 6
在静态猝灭中,若猝灭剂存在多个结合位点,可通过Benesi-Hildebrand双对数关系方程lg(F0/F-1)=lgKa+nlgC(其中n为表观结合点数,Ka为表观结合常数),计算结合常数及结合位点数[22]。采用该方程对Fe3+与ART-N,P-CQDs的荧光猝灭数据拟合,其回归方程为:lg(F0/F-1)=1.128lgC-2.689(R2=0.990 7),Ka为2.045×104,n值为1.128>1,表明Fe3+与ART-N,P-CQDs之间结合位点不止一个,且结合力较强[22]。
此外,由图8a可知,加入Fe3+后,ART-N,P-CQDs紫外吸收峰发生了变化,这可能是Fe3+与ART-N,P-CQDs的表面官能团形成了非荧光的基态复合物[23]。由图8b可知,Fe3+的紫外发射光谱与ART-N,P-CQDs的激发,发射光谱存在大面积的重叠,这表明其猝灭机制可能是荧光内滤效应(IFE)或荧光共振能量转移(FRET)。
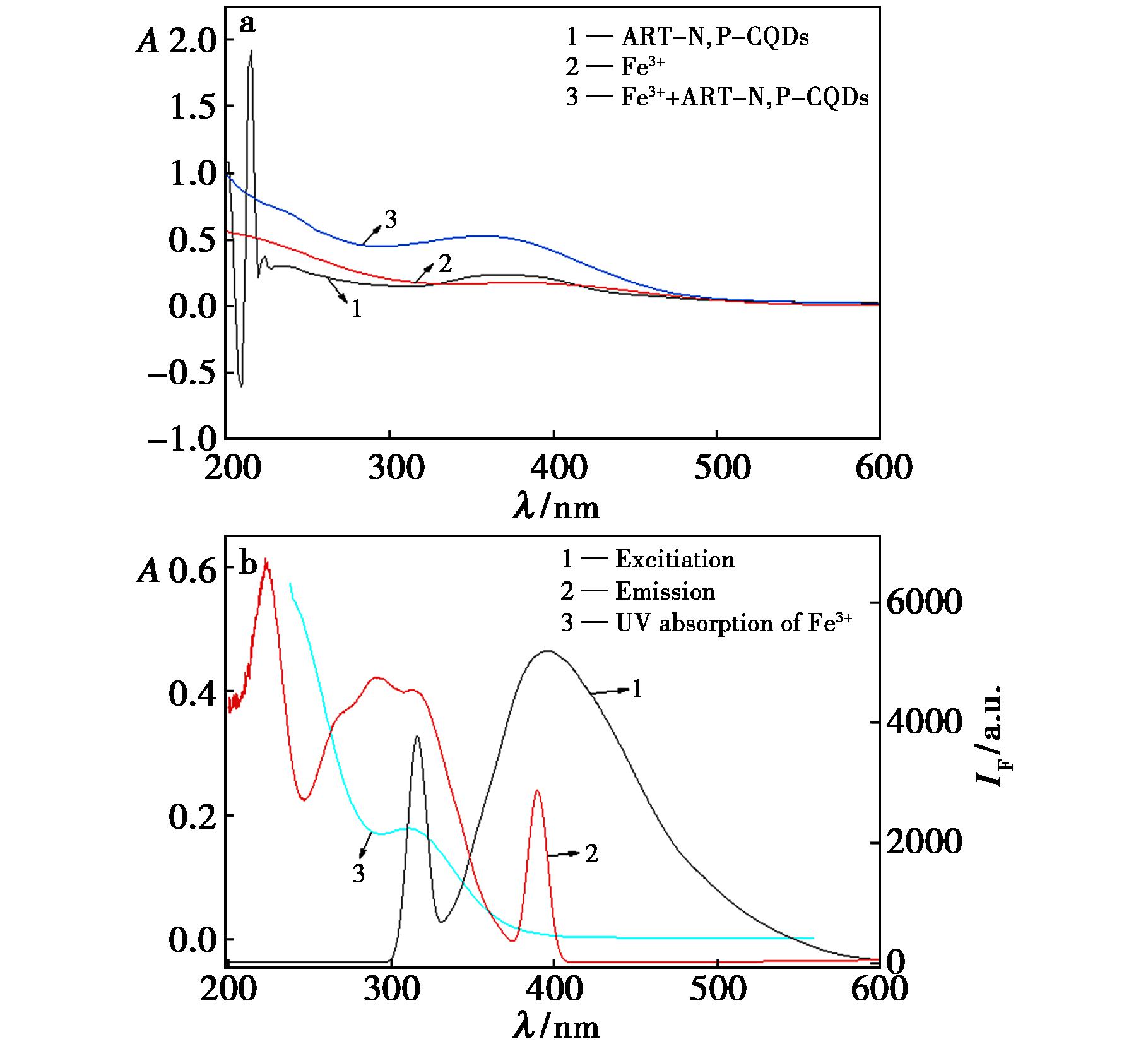
图8 Fe3+、ART-N,P-CQDs及Fe3++ART-N,P-CQDs紫外-可见吸收光谱(a)及ART-N,P-CQDs激发光谱和发射光谱(b)
Fig.8 UV-visible absorption spectra of Fe3+,ART-N,P-CQDs,and Fe3++ART-N,P-CQDs (a) and excitation and emission spectras of ART-N,P-CQDs (b)
2.3 ART-N,P-CQDs的稳定性分析
图9在不同的酸性pH下,ART-N,P-CQDs的荧光强度变化不大,于pH 3的条件下荧光强度更强,因此在酸性条件下仍然适用,这归因于ART-N,P-CQDs表面官能团(羟基、羧基、氨基)的存在,使ART-N,P-CQDs具备酸碱缓冲性能,以此解决耐酸性问题[13]。为防止Fe3+水解,其检测需在酸性条件下进行,因此,该ART-N,P-CQDs适用于Fe3+的检测分析。
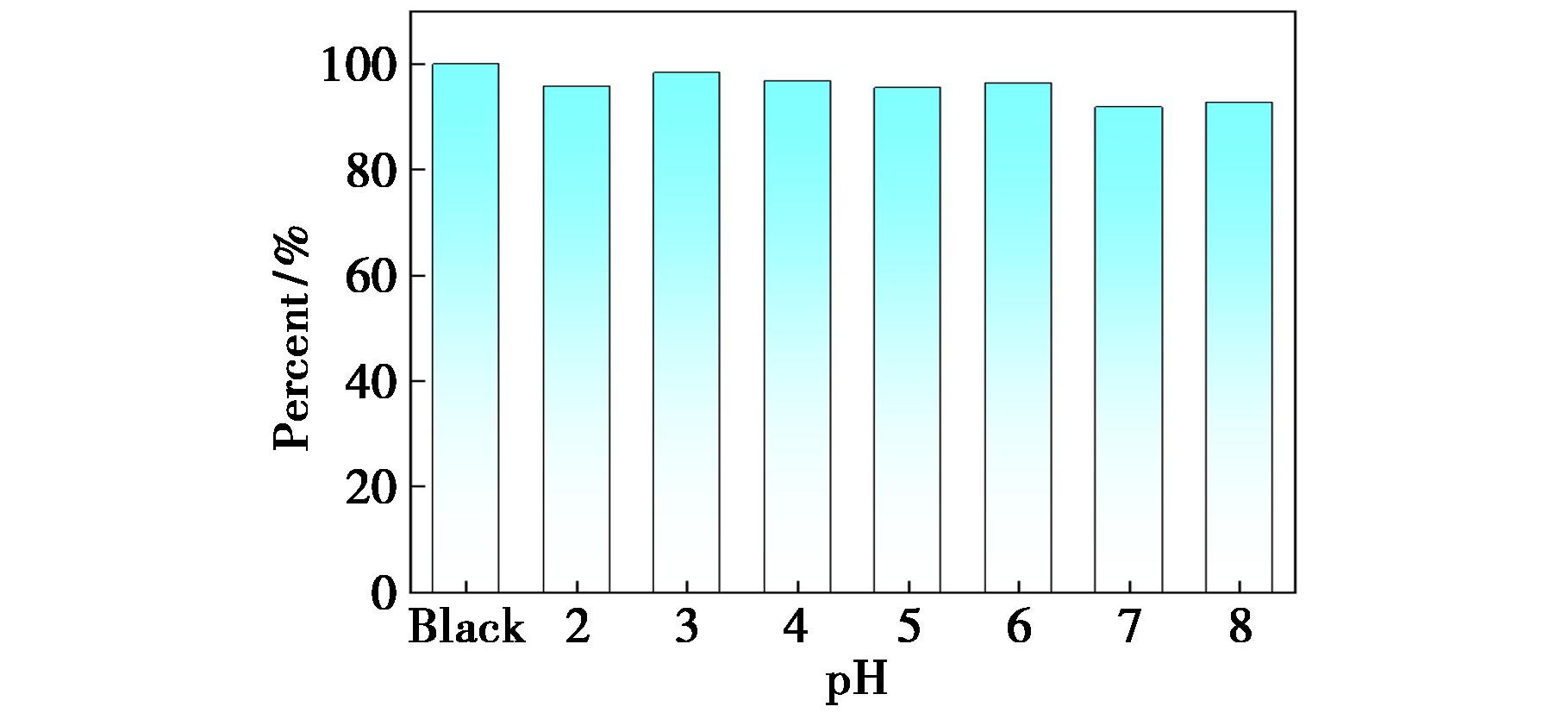
图9 不同pH条件下ART-N,P-CQDs荧光强度
Fig.9 Fluorescence intensity of ART-N,P-CQDs under different pH conditions
由图10可知,在NaCl浓度为0.02~0.25 mol/L范围内,ART-N,P-CQDs的荧光强度变化较小,说明该碳量子点具有一定的抗盐性及抗干扰能力。
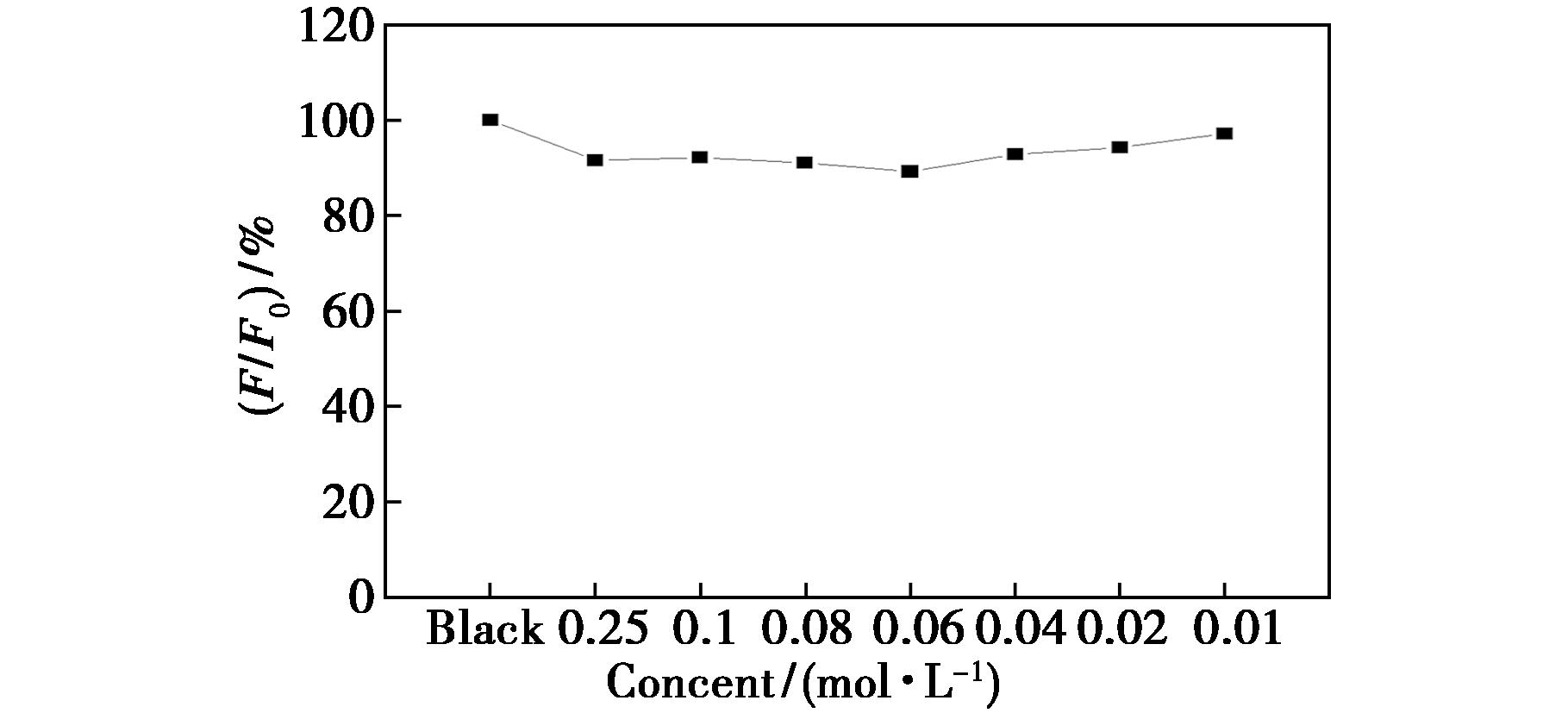
图10 不同离子强度对ART-N,P-CQDs荧光强度影响
Fig.10 Effect of different ionic strengths on the fluorescence intensity of ART-N,P-CQDs
2.4 ART-N,P-CQDs的选择性及抗干扰能力
对多种常见的金属离子(Ag+、Ba2+、Ca2+、Co2+、Cr3+、Fe2+、Fe3+、Hg2+、Mg2+、Ni2+、Pb2+、Zn2+)进行检测,实验结果如图11a所示,100 μmol/L不同金属离子和1 mL/L的ART-N,P-CQDs溶液的猝灭情况,Fe3+对ART-N,P-CQDs的荧光强度有明显的猝灭作用,其余金属离子对ART-N,P-CQDs的荧光强度影响不大,说明Fe3+对ART-N,P-CQDs的猝灭具有选择性。
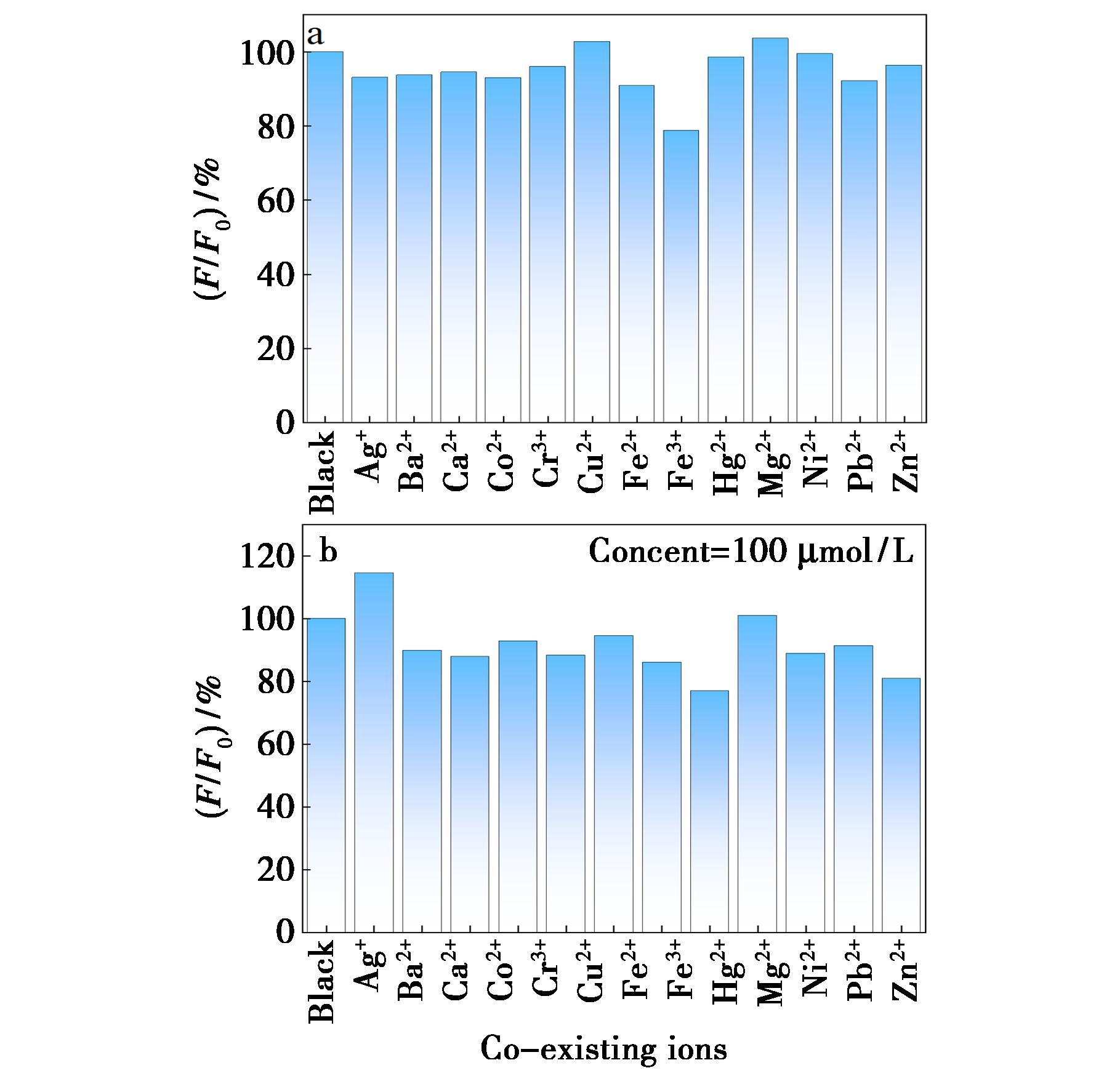
F0和F分别为加入金属离子前后315 nm处测定的荧光强度
图11 金属离子选择(a)和共存离子干扰(b)对ART-N,P-CQDs荧光强度影响
Fig.11 Effect of metal ion selection (a) and coexisting ion interference (b) on fluorescence intensity of ART-N,P-CQDs
ART-N,P-CQDs的抗干扰性能如图11b所示,100 μmol/L不同金属离子和Fe3+离子分别混合1 mL/L的ART-N,P-CQDs溶液的猝灭情况,由图可知,大部分金属离子的加入并未影响Fe3+对ART-N,P-CQDs的荧光强度猝灭,但Ag+和Hg2+对其影响较大,可能是由于Ag+和Hg2+破坏了碳量子点部分官能团所造成的影响[24,25],说明Fe3+对ART-N,P-CQDs的荧光强度猝灭过程具有较好的抗干扰性。
2.5 ART-N,P-CQDs的线性范围与检出限
在ART-N,P-CQDs浓度保持在1 mL/L的情况下,考察不同浓度Fe3+(10~100 μmol/L)对ART-N,P-CQDs荧光强度的影响。通过对F0/F-Concent进行线性拟合可知,Fe3+浓度与ART-N,P-CQDs之间的线性回归方程为F0/F=0.003 64C(Fe3+)+0.990 1(R2=0.994 2),检出限(3σ,n=11)为1.49 μmol/L,表明ART-N,P-CQDs对Fe3+有较好的荧光响应。且与表2的其他材料的检出限相比,该材料具有更好的灵敏度。
表2 本材料和其他材料检出限比较
Tab.2 Comparison of detection limits between ART-N,P-CQDs and other materials
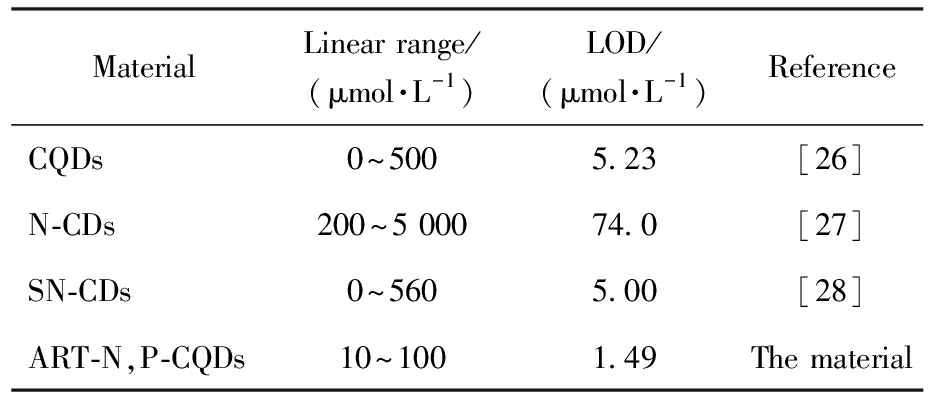
MaterialLinear range/(μmol·L-1)LOD/(μmol·L-1)ReferenceCQDs0~5005.23[26]N-CDs200~5 00074.0[27]SN-CDs0~5605.00[28]ART-N,P-CQDs10~1001.49The material
2.6 补铁药中Fe3+含量检测及加标回收
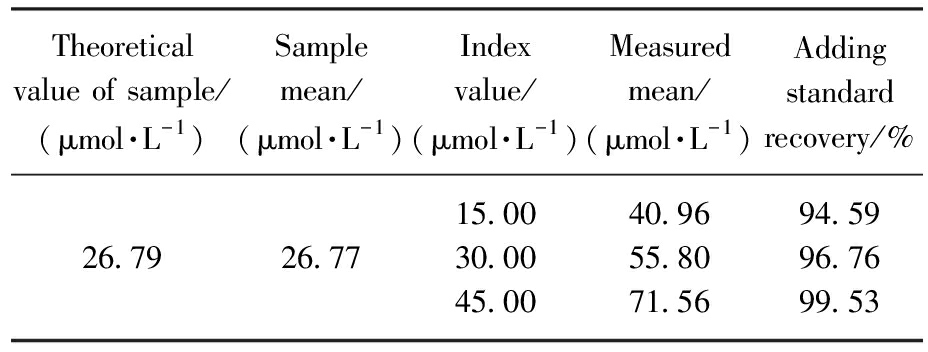
为评价该方法的可靠性,以购买的补铁药为测试对象,调整补铁药至pH 3.0,对其进行加标回收实验(n=3),测得其加标回收率为94.59%~99.53%,测试结果见表3。
表3 加标回收实验结果
Tab.3 Results of recovery test (n=3)
Theoretical value of sample/(μmol·L-1)Sample mean/(μmol·L-1)Index value/(μmol·L-1)Measured mean/(μmol·L-1)Adding standard recovery/%26.7926.7715.0030.0045.0040.9655.8071.5694.5996.7699.53
3 结论
本文以蔗糖为碳源,磷酸二氢铵为氮源和磷源,通过一步水热法制备了具有耐酸性的ART-N,P-CQDs作荧光探针,构建了高灵敏、高选择性的检测Fe3+的荧光分析新方法,探究了体系的荧光猝灭机理为静态猝灭和荧光共振能量转移/内滤效应。该方法实际运用到市面上补铁药片中铁含量的检测,其回收率为94.59%~99.53%,结果令人满意。
[1]Zhang L,Li H D.Chem.Reagents,2023,45(8):94-103.张霖,李宏达.化学试剂,2023,45(8):94-103.
[2]Wang C,Li P,Ding J,Fang Y.Food Sci.Tech.Econ.,2021,46(4):89-95.王超,李彭,丁俭,方勇.粮食科技与经济,2021,46(4):89-95.
[3]Qu J W,Yang S Q,Chen S Y,Hu Y F.Chin.J.Anal.Lab.,2024,43(4):564-571.瞿金为,杨淑琼,陈盛余,胡月芳.分析试验室,2024,43(4):564-571.
[4]Zhang H N,Shan F J,Zhang A J,Chen Y Q.J.Liaoning Uni.Tech.(Nat.Sci.Ed.),2023,43(3):157-163.张慧楠,单凤君,张爱佳,陈玥琪.辽宁工业大学学报(自然科学版),2023,43(3):157-163.
[5]Zuo C Y,Li Q Q,Dai M Z,Fan C Y,Xu Y,Liu G Z,Wang S Y.Chin.J.Inorg.Chem.,2023,39(12):2 301-2 310.左从玉,李琴琴,代明珠,樊琛阳,徐叶,刘光泽,王思雨.无机化学学报,2023,39(12):2 301-2 310.
[6]Ma G S,Zhou M Z.Life Disaster,2020,(1):40-42.马冠生,周明珠.生命与灾害,2020,(1):40-42.
[7]Xing C X,Gu R R,Hu Y X,Lv Y L.Ind.Water Treat.,2023,43(12):162-166.星成霞,顾融融,胡远翔,吕雨龙.工业水处理,2023,43(12):162-166.
[8]Li L N,Su L Y,Jiao Y H,Shen H.Yunnan Geol.,2024,43(2):317-320.李玲娜,苏凌云,焦元海,申焕.云南地质,2024,43(2):317-320.
[9]Ali T A,Mahmoud W H,Mohamed G G.Appli.Organomet.Chem.,2019,33(11):e5 206.
[10]Li Y,Guo H T,Xue M H,Lu S K,Yao B X,Weng W.Chem.Reagents,2020,42(8):893-900.李 ,郭汉涛,薛梅花,卢石孔,姚碧霞,翁文.化学试剂,2020,42(8):893-900.
,郭汉涛,薛梅花,卢石孔,姚碧霞,翁文.化学试剂,2020,42(8):893-900.
[11]Niu J,Wang L Y,Yang E N,Zhang N,Hu P.Chem.Reagents,2020,42(3):221-225.牛静,王利瑶,杨恩暖,张宁,胡鹏.化学试剂,2020,42(3):221-225.
[12]Meng T H,Li C R,Zhao H B,Jiang Y P,Wang H,Yu Y S,Zhong T,Huang X L,Hu X Y.Chin.J.Anal.Lab.,2019,38(7):777-781.孟铁宏,李春荣,赵鸿宾,姜艳萍,王恒,余跃生,钟婷,黄晓玲,胡先运.分析试验室,2019,38(7):777-781.
[13]Zhu Z M,Yan D P,Huang Z H,Zhong X L,Shen Y.Chin.J.Anal.Lab.,2023,42(11):1 508-1 515.朱振茂,严大鹏,黄泽华,钟晓岚,沈赟.分析试验室,2023,42(11):1 508-1 515.
[14]Wang Z H,Zhang Y,Ren L X,Jia J.Chem.Res.App.,2023,35(11):2 561-2 567.王中惠,张漪,任列香,贾晶.化学研究与应用,2023,35(11):2 561-2 567.
[15]Wu X C,Liang W H,Cai C X.Prog.Chem.,2021,33(7):1 059-1 073.吴星辰,梁文慧,蔡称心.化学进展,2021,33(7):1 059-1 073.
[16]Yan L D,Hu Z S,Cheng J X,Zhu Y M,Zhao X F.Chin.J.Lum.,2023,44(12):2 265-2 276.闫立冬,胡朝帅,程俊霞,朱亚明,赵雪飞.发光学报,2023,44(12):2 265-2 276.
[17]Lin L L,Yin Y J,Li Z Y,Xu H J,Hessel V,Ostrikov K K.Chem.Eng.Res.Des.,2022,(178):395-404.
[18]Li Y Y,Shi H M,Feng S L.Chem.Res.Appl.,2021,33(12):2 399-2 404.李影影,时惠敏,冯素玲.化学研究与应用,2021,33(12):2 399-2 404.
[19]Li X Y,Wang C,Li P,Sun X Y,Shao Z Y,Xia J,Liu Q,Shen F,Fang Y.Food Chem.,2023,409:135 243.
[20]Zhao D H,Lv X,Peng W C,Li H H,Zhang J Z,Chen Z Y,Liu X J.Chin.J.Anal.Lab.,1-11[2025-04-06].赵丹华,吕枭,彭伟聪,李华辉,张荩之,陈作义,柳晓俊.分析试验室,1-11[2025-04-06].
[21]Hu R T,Hua H P,Liu F D,Xie R Y,Liu Q Q,Qiu Y X.Guangdong Chem.Ind.,2023,50(2):164-168;175.胡仁涛,华会萍,刘付达,谢睿洋,刘青青,邱燕璇.广东化工,2023,50(2):164-168;175.
[22]Song X L,Hu X P,Liu J,Liu L,Yu Y.Envir.Chem.,2019,38(3):522-530.宋兴良,胡雪萍,刘洁,刘利,于悦.环境化学,2019,38(3):522-530.
[23]Qian W,He L,Pan W S,Chen Y H,Wang H,Liu S L,Chen S J,Liu A P.Chin.J.Lum.,2021,42(11):1 818-1 827.钱玟,何利,潘无双,陈燕华,王惠,刘书亮,陈姝娟,刘爱平.发光学报,2021,42(11):1 818-1 827.
[24]Cheng F C,Zhang S,Zhang L,Sun J P,Wu Y Q.Colloid.Surf.A,2022,636:128 149.
[25]Gontrani L,Bauer E M,Nucara A,Tagliatesta P,Carbone M.Chemosensors,2022,10(9):362.
[26]Ding S,Gao Y,Ni B S,Yang X D.Inorg.Chem.Commun.,2021,130:108 636.
[27]Chin S F,Tan S C,Pang S C,Ng S M.Opt.Mater.,2017,73(11):77-82.
[28]Liu J L,Lan Y W,Peng Y Q,Tan Y F,Liang C F,Wang Y L,Liang X Y.J.Guangxi Uni.(Nat.Sci.Ed.),2020,45(4):876-882.刘锦玲,兰宇卫,彭义琴,谭言芳,梁春凤,王益林,梁信源.广西大学学报(自然科学版),2020,45(4):876-882.