桉烷型倍半萜类化合物(Eudesmane-type sesquiterpenoids)是一类双环倍半萜天然产物的重要代表,通常以十氢萘环为母核,并含有多个氧代官能团,以羟基最为常见,其结构多样性主要取决于环内外羟基和羰基的取代位置等因素(图1)。他们一般具有明显的药理活性[1-14],如抗炎[5,6]、抑制细胞繁殖[7]、抗疟疾[8-10]、抗真菌[11]、神经调节[12]、杀虫[13,14]等。其中如图1所示的O-糖苷化桉烷型倍半萜类化合物Pulisignoside C以及14-Hydroxyisopterocarpolone-11-O-β-D-glucopyran-oside等同样展现出相应的抗疟疾或杀虫等生物活性。
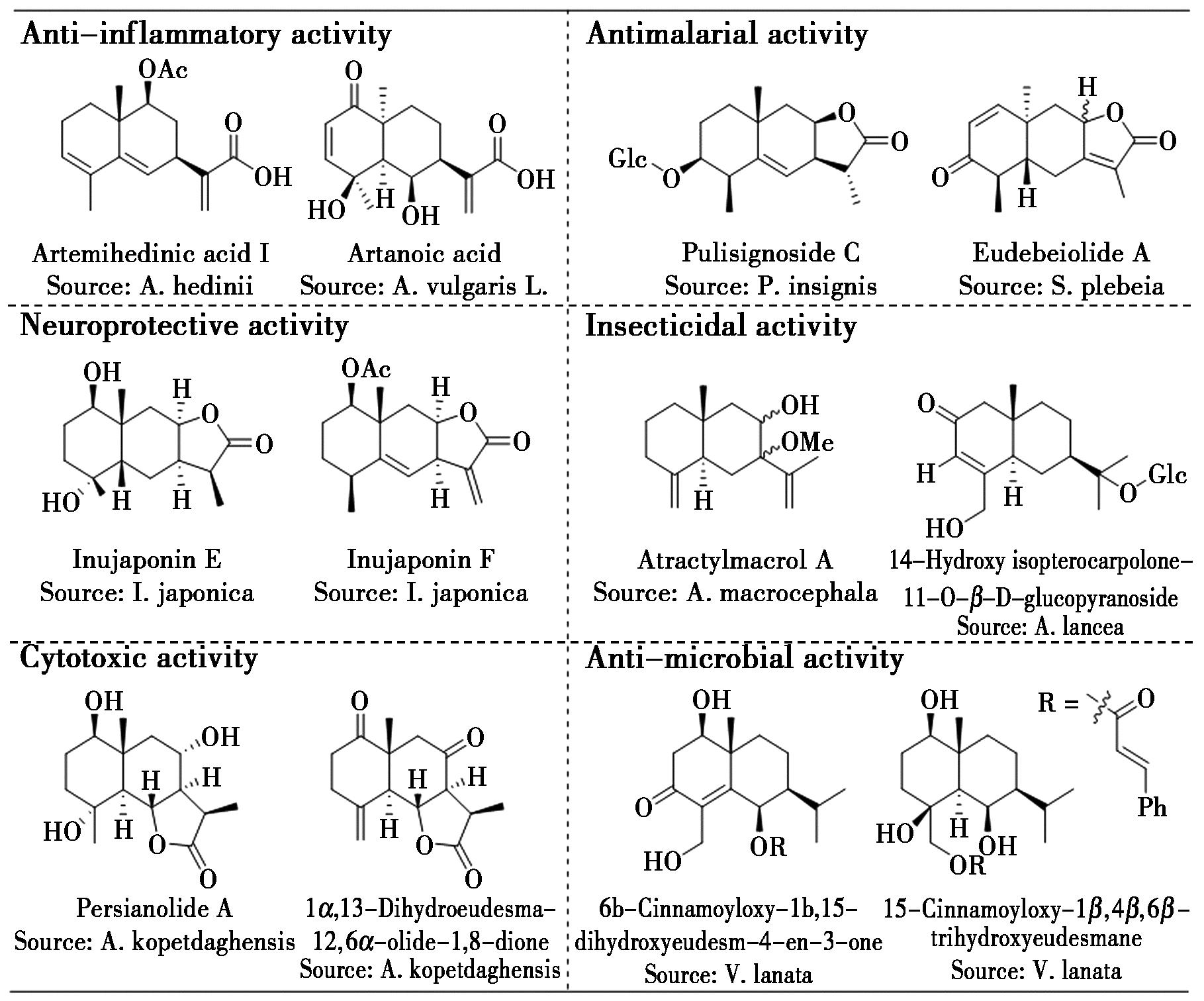
图1 具有生物活性的桉烷型倍半萜类天然产物
Fig.1 Biologically active eudesmane-type sesquiterpenoid natural products
此外,研究表明,桉烷型倍半萜O-糖苷类化合物亦具有重要的抗肿瘤活性。例如,2010年,Xie等[15]从荔枝核中首次分离得到4个桉烷型倍半萜葡萄糖苷类化学成分:荔枝苷A(Litchioside A,1)、荔枝苷B(Litchioside B,2)、Pumilaside A(3)和Funingensin A(4),其中化合物1、2为全新的化学结构,化合物3、4是首次从荔枝核中分离得到的已知化合物(图2)。通过不同肿瘤细胞的活性测试发现:化合物3对人肺腺癌(A549)、肺癌(LAC)、宫颈癌(Hela)和肝癌(Hep-G2)等4种肿瘤细胞株均有很强的体外细胞毒活性,其半数抑制常数IC50值分别为:6.29、2.19、0.012、0.018 μmol/L,显示出广谱的抗肿瘤活性。而化合物4仅对肝癌Hep-G2细胞株有一定的活性(IC50为39.27 μmol/L),但与化合物3的活性相差较大。
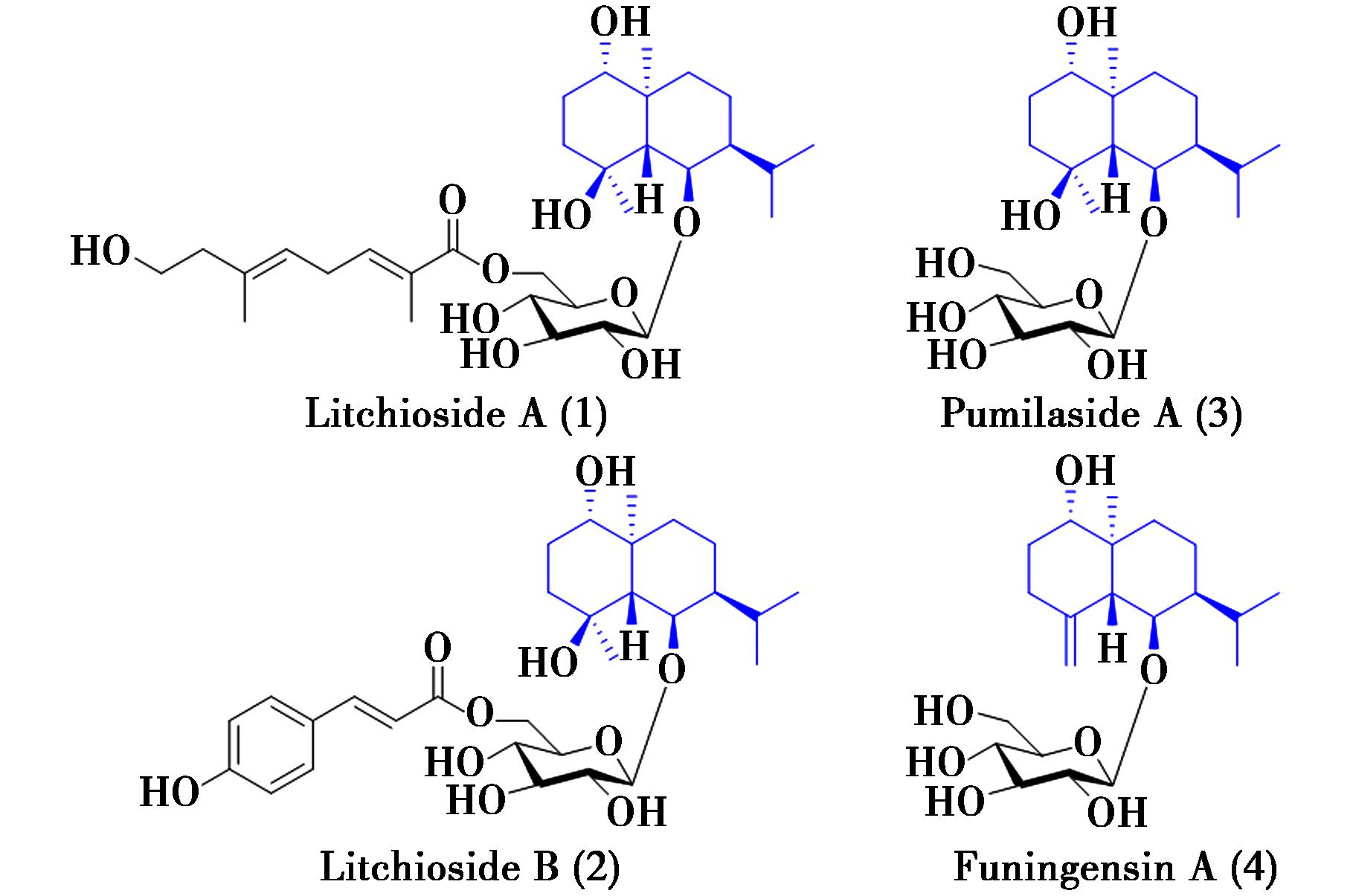
图2 荔枝核中桉烷型倍半萜葡萄糖苷类化学成分
Fig.2 Eudesmane-type sesquiterpene glucoside chemical constituents from lychee seed
最近,Lee等[16]从红紫菀花(Aster koraiensis)中分离出4种倍半萜O-糖苷类化合物,分别命名为Askoseosides A~D(图3)。该研究团队随后通过表皮生长因子(EGF)诱导和佛波醇12-十四酸酯13-乙酸酯(TPA)诱导的细胞转化试验,对这些分离得到的新化合物进行了抗癌活性评估。结果显示,Askosecoside D表现出显著抑制EGF诱导(57.8%)和TPA诱导(67.1%)的集落生长能力。
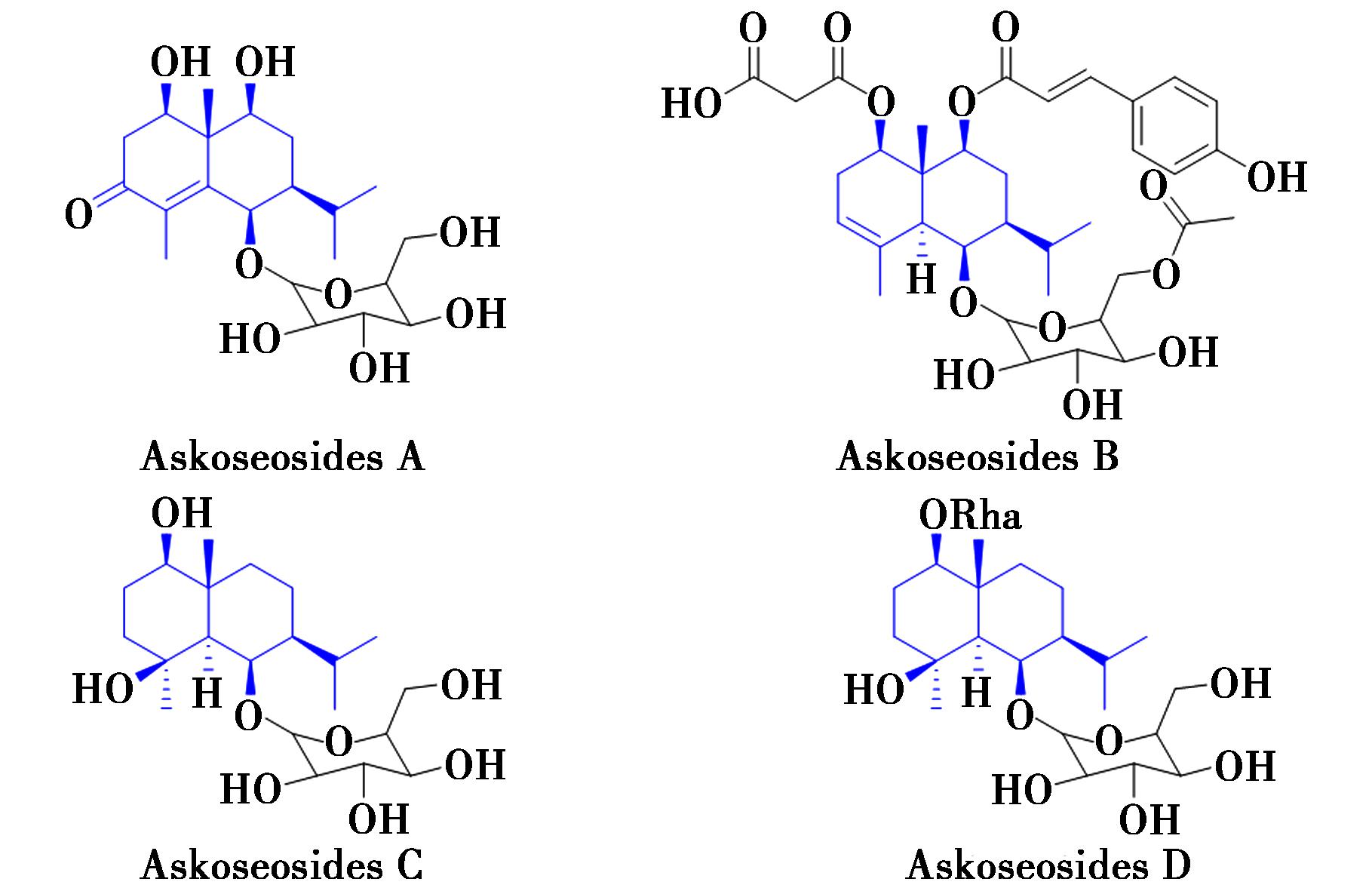
图3 红紫菀花中桉烷型倍半萜糖苷类化学成分
Fig.3 Aucubane-type sesquiterpene glucoside chemical constituents from Aster koraiensis
综上所述,桉烷型倍半萜类天然产物不仅表现出显著的药理活性,还作为许多其他倍半萜化合物的关键生源合成前体或中间体发挥了重要作用。但目前绝大多数具有生物活性的桉烷型倍半萜仍主要依赖于提取分离获得,且缺乏高效的全合成方法,这在很大程度上限制了其进一步的药理研究与应用。桉烷型倍半萜类十氢萘环母核骨架的构筑方法研究已持续近50年,发展出多种独具特色的策略[17-24]。本文通过Diels-alder反应、羰基还原、糖苷化等一系列合成方法,成功构建新型O-糖苷类桉烷型倍半萜衍生物(图4)。
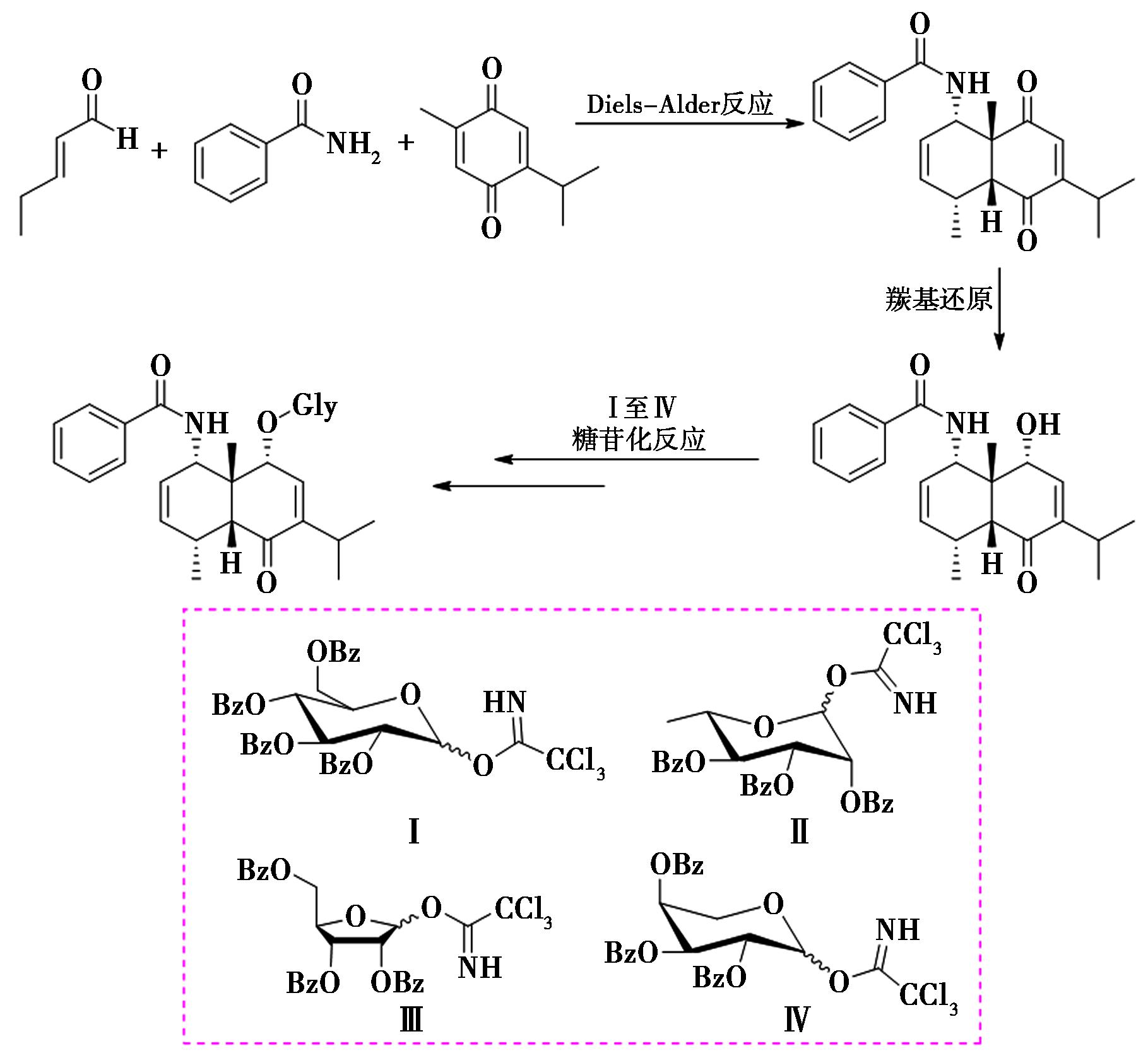
图4 新型糖苷类桉烷型倍半萜衍生物的设计合成
Fig.4 Design and synthesis of novel glycoside eudesmane-type sesquiterpene derivatives
在此基础上,结合现代药理活性测试手段,对所合成的桉烷型倍半萜O-糖苷类化合物进行了初步体外抗肿瘤活性评估,为其在药物开发中的潜在应用提供重要借鉴。
1 实验部分
1.1 主要仪器与试剂
Avance Ⅲ(400或500 MHz)型核磁共振波谱仪(德国布鲁克科技有限公司);Agilent 1290Ⅱ-6470型三重四极杆液质联用仪(安捷伦(中国)科技有限公司);AB-SCIEX-X500R-QTOF型高分辨率液质联用仪(上海爱博才思分析仪器贸易有限公司);XtaLAB AFC12(RINC):Kappa single型X射线晶体衍射仪(日本理学株式会社);SPH-200型氢气发生器(北京中惠普分析技术研究所);HR1200-ⅡB2型生物安全柜(青岛海尔特种电器有限公司);OLYMPUS CKX53型倒置显微镜(北京瑞科中仪科技有限公司);MCO-170AICUVL-PC型二氧化碳培养箱(普和希株式会社);EPOCH12型全波长酶标仪(美国伯腾仪器有限公司);SORVALI ST16型低温高速离心机(赛默飞世尔科技(中国)有限公司);JIMBIO-FIL型细胞技术仪(江苏卓微生物科技有限公司);HRLM-80型高压灭菌锅(青岛海尔生物医疗股份有限公司)。
反式-2-戊烯醛(95%)、百里醌(99%)、对甲苯磺酸(99%)、二异丁基氢化铝(DIBAL-H)(1.5 mol/L in toluene)、吡啶(99.5%)、33% HBr-AcOH溶液(98%)、叔丁基二甲基硅基三氟甲磺酸酯(TBSOTf,98%)、叔丁醇钾(98%)(安徽泽升科技股份有限公司);苯甲酰胺(97%)、α-无水葡萄糖酯(99%)(上海毕得医药科技有限公司);硼氢化钠(98%,上海阿拉丁生化科技股份有限公司);七水合三氯化铈(99.9%)、三氯乙腈(98%)、D-核糖(98%)、alpha-L-鼠李糖一水合物(95%)、L-(+)-阿拉伯糖(98%)(韶远科技(上海)有限公司);苯甲酰氯(99%,上海迈瑞尔生化科技有限公司)。
1.2 合成步骤及化合物结构表征
本文通过如图5所示的合成路线合成得到了中间体1a~4a和4b,以及最终目标产物5a。
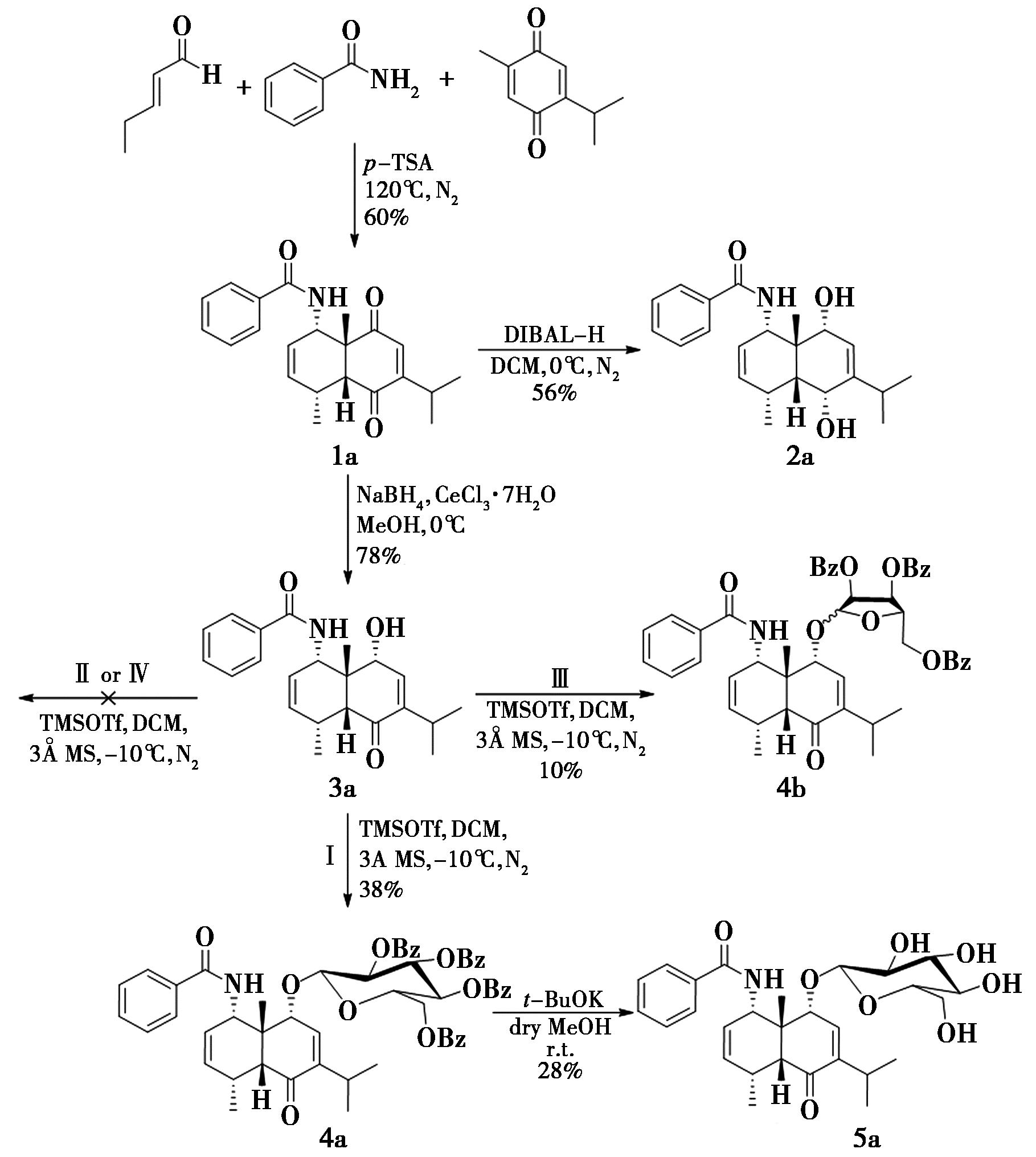
图5 新型糖苷类桉烷型倍半萜衍生物的合成路线
Fig.5 Synthetic routes of novel glycoside eudesmane-type sesquiterpene derivatives
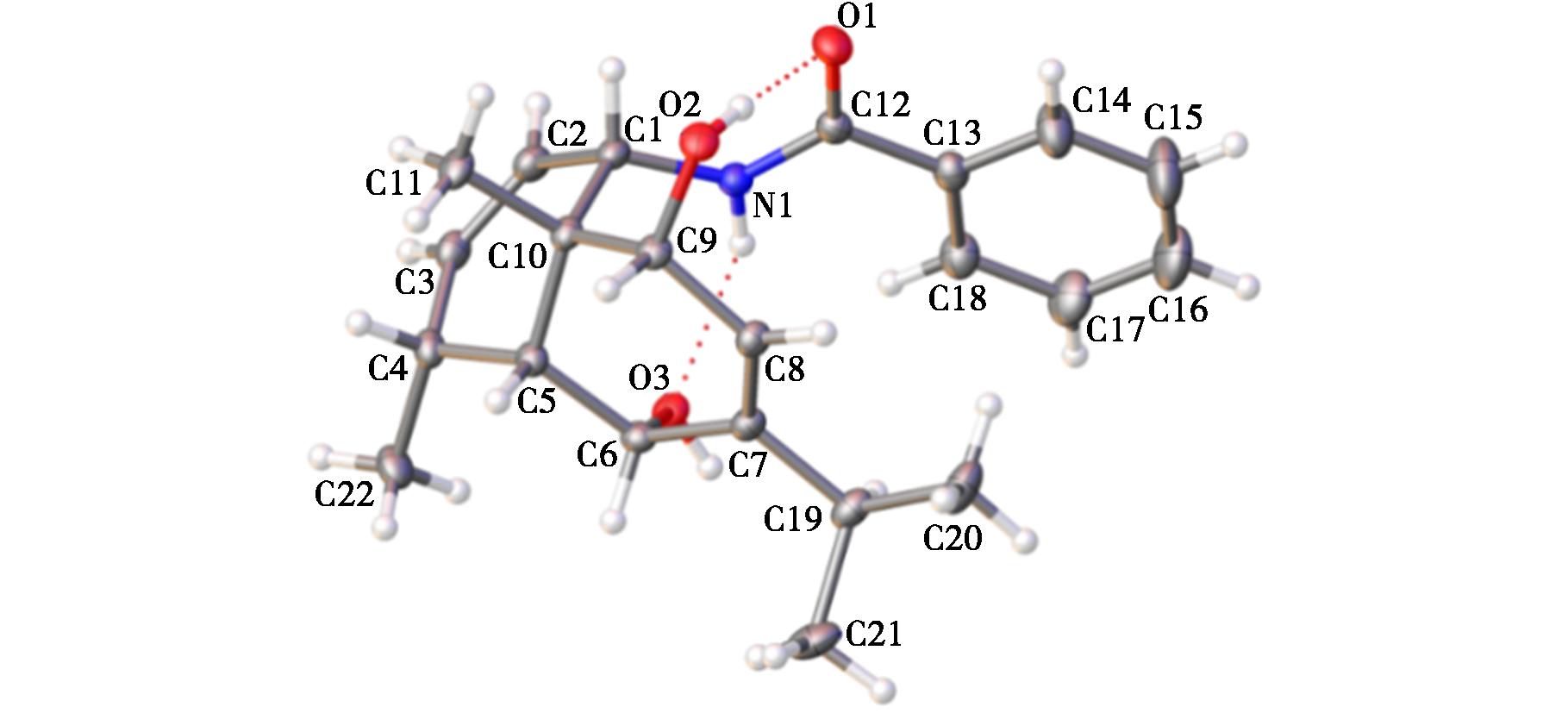
图6 化合物2a单晶结构
Fig.6 Single-crystal structure of compound 2a
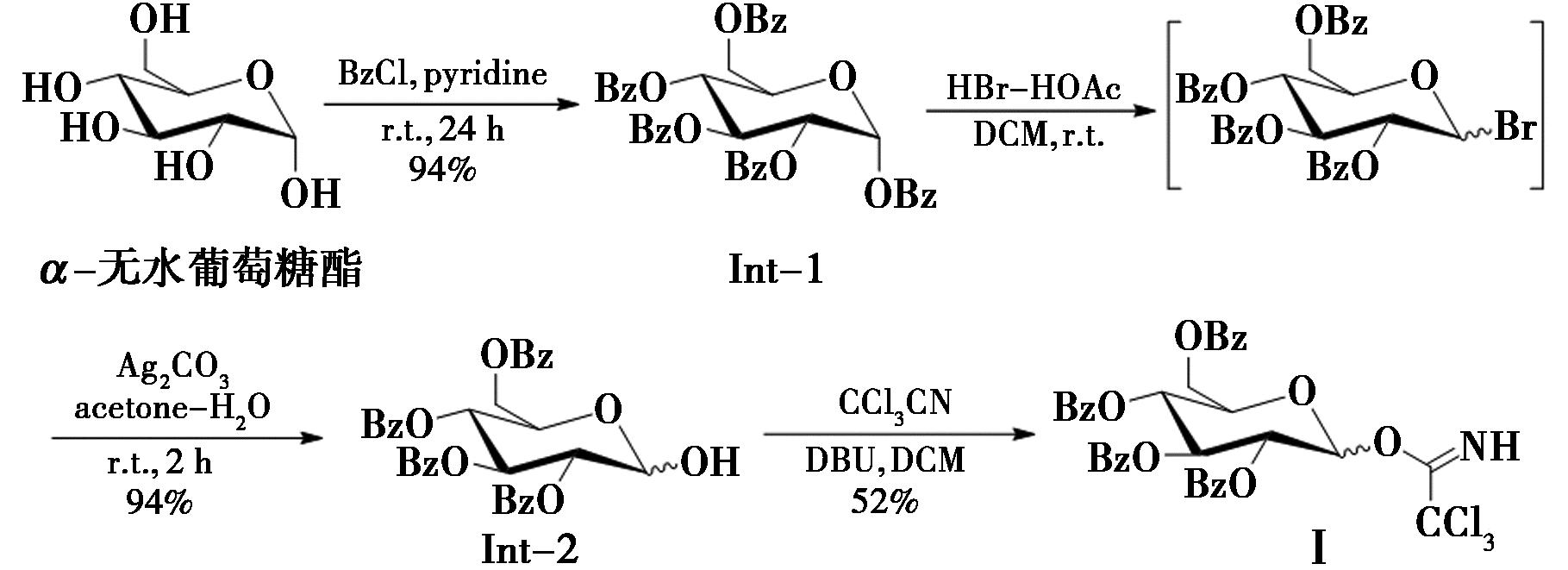
图7 化合物Ⅰ的合成路线
Fig.7 Synthetic routes of compound Ⅰ
1.2.1 中间体化合物1a的合成[18]
在干燥甲苯中加入4.59 mL(45.0 mmol)反式-2-戊烯醛、5.45 g(45.0 mmol)苯甲酰胺、5 g(30.0 mmol)百里醌和258 mg(1.5 mmol,5 mol%)对甲苯磺酸,连接Dean-Stark水分离器,将混合液在120 ℃氮气气流下回流24 h,溶液在旋转蒸发器上浓缩,粗产物用V(石油醚)∶V(乙酸乙酯)=8∶1经硅胶柱层析纯化,得到6.3 g黄色固体1a,产率60%。
1HNMR(CDCl3,500 MHz),δ:7.98(d,1H,J=9.8 Hz);7.83(d,2H,J=7.6 Hz);7.50(dt,3H,J=32.3,7.3 Hz);6.43(s,1H);5.68~5.61(m,2H);4.80(d,1H,J=9.7 Hz);3.26(d,1H,J=8.0 Hz);3.00(p,1H,J=6.8 Hz);2.78(t,1H,J=8.0 Hz);1.45(s,3H);1.13(dd,6H,J=15.3,6.7 Hz);0.88(d,3H,J=7.4 Hz)。LC-MS(ESI),m/z(%):352.1(13.87)[M+H]+,374.1(36.86)[M+Na]+。HR-MS(ESI),C22H25NO3,实测值(计算值),m/z:374.171 9(374.173 2)[M+Na]+。
1.2.2 中间体化合物2a的合成
称取20 mg(0.057 mmol)化合物1a至三颈烧瓶中,加入3 mL无水二氯甲烷,抽充氮气,混合物放置低温反应器降至0 ℃,再用注射器加入300 μL(0.45 mmol) DIBAL-H,保持0 ℃搅拌 1 h,待原料反应完全后加入1 mL甲醇和0.3 mL水进行后处理,减压浓缩除去溶剂,粗产物经硅胶柱层析纯化(V(石油醚)∶V(乙酸乙酯)=8∶1),得到11 mg白色固体2a,产率56%。通过缓慢挥发石油醚/乙酸乙酯混合溶剂,获得化合物2a的四边形方晶。
化合物2a晶体数据:化学式C22H29NO3(M=355.46 g/mol):单斜晶系,空间群P21/c(no.14),a=7.560 24(13) Å,b=13.122 2(3) Å,c=19.274 6(4) Å,β=91.515 5(16),晶胞体积 V=1 911.51(6) Å3,晶胞内分子数Z=4,数据采集温度T=293.15 K,铜靶辐射吸收系数μ(Cu Kα)=0.645 mm-1,计算密度=1.235 g/cm3,衍射点收集情况:公测量13 023个衍射点(8.152≤2θ≤153.078),独立衍射点3 845个(Rint=0.043 8,Rsigma=0.037 4)所有计算均使用这些独立点。结构精修结果R1=0.048 4(I>2σ(I)),wR2=0.152 9(使用全部数据)。
1HNMR(CDCl3,500 MHz),δ:8.54(d,1H,J=9.8 Hz);7.81~7.72(m,2H);7.53~7.42(m,1H);7.36(t,2H,J=7.6 Hz);5.82(d,1H,J=10.0 Hz);5.65(ddd,1H,J=10.0,5.1,3.1 Hz);5.48(d,1H,J=1.9 Hz);4.55(d,1H,J=12.5 Hz);4.30(d,1H,J=4.1 Hz);3.89(dd,1H,J=12.6,2.2 Hz);2.90~2.76(m,1H);2.71(d,1H,J=3.4 Hz);2.30~2.16(m,1H);1.92(s,1H);1.72(t,1H,J=5.4 Hz);1.36~1.30(m,6H);0.88(d,3H,J=7.0 Hz);0.54(d,3H,J=6.8 Hz)。13CNMR(CDCl3,126 MHz),δ:167.14,143.01,134.81,133.76,131.58,128.32,128.03,127.24,126.38,75.46,65.31,46.99,44.28,40.37,29.89,29.17,25.14,22.60,20.27,16.70。LC-MS(ESI),m/z:356.1(30.32)[M+H]+,374.1(27.71)[M+Na]+,354.2(38.0)[M-H]-,390.2(100)[M+Cl]-。HR-MS(ESI),C22H29NO3,实测值(计算值),m/z:354.207 8(354.206 9)[M-H]-。通过加入重水检测氢谱验证δ:2.71(d,1H,J=3.4 Hz)以及δ:1.92(s,1H)应为化合物的两个活泼氢。
1.2.3 中间体化合物3a的合成
将105 mg(0.3 mmol)化合物1a溶于甲醇(14 mL),然后加入223.6 mg(0.6 mmol)氯化铈(Ⅲ)七水合物并搅拌冷却至0 ℃,在0 ℃下分批加入22.8 mg(0.6 mmol) NaBH4,加入完成后,除去冰浴,使混合物逐渐升至室温,待反应完全后,混合物用10 mL冷水淬灭,用乙酸乙酯萃取,饱和食盐水和水洗涤,合并乙酸乙酯层,用无水硫酸钠干燥,过滤,滤液真空浓缩,粗产物用V(石油醚)∶V(乙酸乙酯)=8∶1经硅胶柱层析纯化,得到 83 mg白色固体产物3a,产率78%。
1HNMR(CDCl3,500 MHz),δ:7.65~7.57(m,2H);7.54~7.47(m,1H);7.40(t,2H,J=7.8 Hz);6.22(dd,1H,J=2.4,1.3 Hz);5.99~5.89(m,2H);5.59(ddd,1H,J=10.0,5.3,3.1 Hz);4.45(t,1H,J=2.2 Hz);4.21(ddd,1H,J=8.3,5.1,1.5 Hz);2.71~2.54(m,3H);1.45(d,3H,J=7.4 Hz);1.40(s,3H);0.79(d,3H,J=6.8 Hz);0.48(d,3H,J=6.9 Hz)。13CNMR(CDCl3,126 MHz),δ:203.81,167.50,146.39,140.90,135.90,132.67,132.30,128.65,126.88,122.79,74.95,54.67,51.94,49.08,29.32,26.33,23.72,22.06,19.57,17.18。MS(ESI),m/z:354.1(12.76)[M+H]+,376.1(100)[M+Na]+,352.2(39.66)[M-H]-,388.1(100)[M+Cl]-。HR-MS(ESI),C22H27NO3,实测值(计算值),m/z:376.187 7(376.188 9)[M+Na]+。
1.2.4 全苯甲酰基三氯乙酰亚胺酯糖的合成[25]
将1 g(5.55 mmol)α-无水葡萄糖酯在15 mL无水吡啶中溶解,抽充氮气,置于冰浴冷却至 0 ℃,缓慢加入5.5 mL(47.5 mmol)苯甲酰氯,将混合物转至室温下搅拌过夜,然后用2 mL甲醇淬灭,真空蒸发溶剂,将粗产物溶于乙酸乙酯中,分别用HCl溶液、饱和NaHCO3溶液和食盐水洗涤,真空去除溶剂,粗产物经硅胶柱层析纯化,得到3.51 g白色固体Int-1,产率90%。
同法得到全苯甲酰基鼠李糖、阿拉伯糖和核糖,收率在60%~94%之间。
将0.5 g(0.7 mmol)全苯甲酰基葡萄糖用 5 mL超干二氯甲烷溶解于圆底烧瓶中,再加入 0.5 mL 33% HBr-AcOH溶液室温搅拌10 h。反应完毕后,用饱和NaHCO3溶液和盐水洗涤,用二氯甲烷萃取,浓缩抽干后得到白色固体,无需纯化即可用于下一步反应。将所得粗产物溶于12.5 mL丙酮和0.5 mL水中,然后加入528 mg(1.91 mmol)Ag2CO3,放置室温反应,待原料反应完全后,旋干除去溶剂,用V(石油醚)∶V(乙酸乙酯)=2∶1经硅胶柱层析法纯化,得到279.1 mg,产率94%。将80 mg(0.13 mmol)白色固体Int-2溶于1 mL二氯甲烷中,加入134 μL(1.3 mmol)三氯乙腈和10 μL(0.07 mmol) DBU,混合物放置室温搅拌反应,待反应完全后,通过快速硅胶柱层析法纯化得到49.7 mg白色固体(化合物Ⅰ),产率52%。
同法制得1.78 g全苯甲酰基三氯乙酰亚胺酯鼠李糖(化合物Ⅱ),产率20%、372 mg阿拉伯糖(化合物Ⅲ),产率43%、88 mg核糖(化合物Ⅳ),产率26%。
化合物Ⅰ:白色固体,产率52%。1HNMR(CDCl3,500 MHz),δ:8.64(s,1H);8.07~8.02(m,2H);7.96(ddd,4H,J=8.5,4.9,1.4 Hz);7.90~7.85(m,2H);7.59~7.49(m,3H);7.44(td,3H,J=7.5,5.2 Hz);7.37(t,4H,J=7.8 Hz);7.31(t,2H,J=7.7 Hz);6.84(d,1H,J=3.7 Hz);6.28(t,1H,J=9.9 Hz);5.83(t,1H,J=9.9 Hz);5.62(dd,1H,J=10.2,3.8 Hz);4.71~4.58(m,2H);4.55~4.42(m,1H)。LC-MS(ESI),m/z:761.9(96.16),763.9(100)[M+Na]+。
化合物Ⅱ:白色固体,产率20%。1HNMR(CDCl3,500 MHz),δ:8.83(s,1H);8.11(dd,2H,J=8.3,1.4 Hz);8.06~7.96(m,2H);7.91~7.75(m,2H);7.71~7.60(m,1H);7.57~7.47(m,3H);7.46~7.35(m,3H);7.32~7.25(m,2H);6.49(d,1H,J=1.7 Hz);5.89(dt,2H,J=5.1,3.0 Hz);5.83~5.75(m,1H);4.41(dd,1H,J=9.8,6.2 Hz);1.43(d,3H,J=6.2 Hz)。LC-MS(ESI),m/z:641.9(56.74),643.9(56.65)[M+Na]+。
化合物Ⅲ:白色固体,产率43%。1HNMR(CDCl3,500 MHz),δ:8.64(s,1H);8.17~8.06(m,2H);8.05~7.94(m,2H);7.94~7.81(m,2H);7.68~7.60(m,1H);7.57~7.43(m,4H);7.37(t,2H,J=7.7 Hz);7.30(t,2H,J=7.7 Hz);6.82(d,1H,J=3.2 Hz);6.10~5.95(m,2H);5.94~5.80(m,1H);4.50~4.14(m,2H)。LC-MS(ESI),m/z:627.9(96.26),629.9(100)[M+Na]+。
化合物Ⅳ:白色固体,产率26%。1HNMR(CDCl3,500 MHz),δ:8.84(s,1H);8.03(ddd,4H,J=19.8,8.1,1.4 Hz);7.90~7.85(m,2H);7.58~7.50(m,3H);7.35~7.29(m,6H);6.57(d,1H,J=2.5 Hz);5.92(t,1H,J=3.9 Hz);5.84~5.68(m,2H);4.48(dd,1H,J=13.3,2.2 Hz);4.29(dd,1H,J=13.3,2.9 Hz)。LC-MS(ESI),m/z:627.9(97.38),629.9(100)[M+Na]+。
1.2.5 α-葡萄糖苷衍生物4a的合成
称取14 mg(0.04 mmol)中间体3a和45 mg(0.06 mmol)全苯甲酰基三氯乙酰亚胺酯葡萄糖(化合物Ⅰ)于三颈瓶中,加入3 mL无水二氯甲烷及适量粉末状3 Å分子筛,抽充氮气,混合物降至-10 ℃,加入5 μL(0.028 mmol) TMSOTf保持-10 ℃继续搅拌反应,待反应完全后,用少量三乙胺中和混合物,过滤,用二氯甲烷洗涤滤饼,减压浓缩除去溶剂,经硅胶柱层析纯化(V(石油醚)∶V(乙酸乙酯)=5∶1),得到14 mg白色固体4a,产率38%。
1HNMR(CDCl3,500 MHz),δ:8.06~7.76(m,8H);7.75~7.63(m,2H);7.60~7.19(m,13H);7.18~6.95(m,2H);6.78~6.44(m,1H);6.21(s,1H);5.94(t,1H,J=9.9 Hz);5.67(dt,1H,J=14.6,9.5 Hz);5.56(q,1H,J=9.7 Hz);5.48(dt,1H,J=10.2,2.3 Hz);5.28~5.13(m,1H);4.91~4.81(m,1H);4.72(dd,1H,J=12.2,2.9 Hz);4.61(s,1H);4.53~4.40(m,1H);4.23(ddt,1H,J=17.5,10.1,3.2 Hz);4.19~4.04(m,1H);2.85(dtd,1H,J=14.9,7.7,5.1 Hz);2.74(dd,1H,J=24.7,7.9 Hz);2.67~2.43(m,1H);1.42(d,3H,J=6.1 Hz);1.14(d,3H,J=3.0 Hz);0.95(dd,3H,J=6.9,2.4 Hz);0.91(dd,3H,J=6.9,3.2 Hz)。13CNMR(CDCl3,126 MHz),δ:200.48,168.42,166.09,165.91,165.75,165.65,165.37,165.20,164.67,164.54,149.10,135.36,133.69,133.65,133.45,133.43,133.41,133.38,131.67,130.97,130.92,129.89,129.76,129.73,129.71,129.70,129.53,128.61,128.52,128.48,128.36,127.16,126.95,102.79,97.70,72.98,72.89,72.81,72.78,71.97,70.31,69.36,63.13,63.03,52.92,51.72,39.00,31.27,27.84,26.73,26.33,22.03,21.99,21.38,17.24,16.74。LC-MS(ESI),m/z:932.2(20.27)[M+H]+,954.2(100)[M+Na]+,930.2(7.79)[M-H]-,966.2(100)[M+Cl]-。HR-MS(ESI),C56H53NO12,实测值(计算值),m/z:954.344 5(954.346 5)[M+Na]+。
1.2.6 α-葡萄糖苷衍生物5a的合成
将51 mg(0.45 mmol) t-BuOK加入到85 mg(0.091 mmol)化合物4a、1.5 mL无水甲醇中,室温下搅拌反应1 h后,使用732阳离子交换树脂(H+型)来中和反应混合物,滤液浓缩,经硅胶柱层析纯化(V(二氯甲烷)∶V(甲醇)=20∶1),得 13 mg白色固体5a,产率28%。
1HNMR(CDCl3,500 MHz),δ:7.47~7.32(m,5H);6.13(dt,1H,J=10.2,3.4 Hz);5.70(t,1H,J=9.4 Hz);5.47(d,1H,J=10.0 Hz);4.98(d,1H,J=5.0);4.75(dt,1H,J=10.4,3.5 Hz);4.50(d,1H,J=7.5 Hz);4.39(d,1H,J=7.5 Hz);4.28(d,1H,J=4.2 Hz);4.22~4.12(m,1H);4.03~3.95(m,1H);3.80(d,1H,J=10.6 Hz);3.68(t,1H,J=9.7 Hz);3.56~3.49(m,2H);3.45~3.31(m,1H);3.22~3.04(m,1H);2.59(d,1H,J=73.2 Hz);2.36~2.22(m,1H);2.20~2.06(m,1H);1.98(dq,1H,J=18.7,6.7 Hz);1.37~1.20(m,6H);0.97(dd,3H,J=16.4,6.8 Hz);0.59~0.49(m,3H)。13CNMR(CDCl3,126 MHz),δ:209.71,171.65,136.76,134.60,129.93,128.78,128.54,126.64,126.47,104.26,85.78,69.99,63.64,61.65,57.84,56.60,47.65,46.12,35.94,29.50,29.33,28.37,27.22,20.29,19.09,18.97,17.39。LC-MS(ESI),m/z(%):516.1(44.74)[M+H]+,538.1(100)[M+Na]+,514.2(4.68)[M-H]-,550.2(100)[M+Cl]-。HR-MS(ESI),C28H37NO8,实测值(计算值),m/z:538.240 4(538.241 7)[M+Na]+。
1.2.7 D-核糖苷衍生物4b的合成
称取178.4 mg(0.50 mmol)中间体3a和250.0 mg(0.41 mmol)全苯甲酰基三氯乙酰亚胺酯D-核糖(化合物Ⅲ)于三颈瓶中,加入10 mL无水二氯甲烷及适量粉末状3 Å分子筛,抽充氮气,混合物降至-10 ℃,加入73.6 μL(0.59 mmol)TMSOTf保持-10 ℃继续搅拌反应,待反应完全后,用少量三乙胺中和混合物,过滤,用二氯甲烷洗涤滤饼,减压浓缩除去溶剂,经硅胶柱层析纯化(V(石油醚)∶V(乙酸乙酯)=5∶1),得到51 mg白色固体4b,产率10%。
1HNMR(CDCl3,500 MHz),δ:8.15~8.02(m,6H);7.77(d,2H,J=7.8 Hz);7.36(m,12H);5.92(q,1H,J=5.9 Hz);5.78~5.72(m,1H);5.71~5.64(m,3H);5.56(dt,1H,J=10.1,2.9 Hz);5.52(s,1H);4.90(dd,1H,J=9.8,3.0 Hz);4.51~4.43(m,1H);4.28(t,1H,J=5.8 Hz);4.11(d,1H,J=7.2 Hz);2.93~2.91(m,1H);2.81(d,1H,J=6.9 Hz);2.75~2.66(m,1H);1.28(s,3H);1.18(dd,3H,J=8.0,2.7 Hz);0.97(dd,6H,J=6.9,3.7 Hz)。13CNMR(126 MHz,CDCl3),δ:201.40,166.48,165.91,165.48,165.28,163.55,146.62,133.82,133.64,133.62,133.58,133.55,133.51,133.44,133.23,133.21,129.84,129.80,129.75,129.66,128.55,128.51,128.48,128.43,128.40,128.37,127.21,100.47,95.82,79.57,79.52,79.16,76.21,76.12,72.52,72.42,71.92,71.67,65.81,65.22,64.20,53.72,26.48,22.05,20.73,17.38,14.21。LC-MS(ESI),m/z:798.2(6.84)[M+H]+,820.1(100)[M+Na]+,796.2(23.52)[M-H]-,832.1(100)[M+Cl]-。HR-MS(ESI),C48H47NO10,实测值(计算值),m/z:820.307 4(820.309 8)[M+Na]+。
1.2.8 癌细胞来源
人非小细胞肺癌细胞(A549)、人前列腺癌细胞(DU145)、人宫颈癌细胞(Hela)、人肝癌细胞(HepG2)、人乳腺癌细胞(MCF-7)均来自广西中医药大学广西中药药效研究重点实验室。
1.2.9 MTT法测定化合物的体外抗肿瘤活性
种板:取处于对数生长期的细胞,用胰酶消化后离心,弃去上清液,加入适量的完全培养基,吹打混匀,用移液枪取10 μL至细胞计数仪计数,用完全培养基稀释至5×104个/mL,随即用100 μL排枪将细胞悬液转移至96孔板中,每个孔100 μL,然后将其放置培养箱中培养24 h。
给药:按顺序每孔加入配制好的浓度为100、50、25、12.5、6.25、3.125、1.56、0.78 μmol/L的桉烷型倍半萜衍生物待测液各100 μL,阴性对照组加入等体积的含1% DMSO的相同培养基,每组3个复孔,在含5% CO2培养箱中培养48 h。阳性对照组为阿霉素。
检测:在尽可能避光的环境下,用排枪每孔加10 μL MTT溶液,37 ℃继续孵育4 h,丢弃上清液,每孔加100 μL DMSO,至摇床混匀(15 min),用酶标仪检测OD值,检测波长为490 nm。
数据处理:首先用Excel处理原数据,得到不同浓度的生长抑制率,后用GraphPad Prism 8计算各化合物的IC50值。肿瘤细胞生长抑制率计算公式:生长抑制率(%)=1-(给药组OD值-空白对照组OD值)/(阴性对照组OD值-空白对照组OD值)×100%。
1.2.10 体外抗肿瘤活性测试结果
2 结果与讨论
本文以反式-2-戊烯醛、苯甲酰胺、百里醌作为起始原料,首先通过分子间的Diels-alder反应一锅法合成构建双环骨架1a,然后在中间体1a的基础上,对羰基进行还原实现桉烷型倍半萜骨架的构建及其衍生物的合成。
采用DIBAL-H还原可获得双羰基还原的产物2a,并利用X射线晶体衍射技术对其结构进行了确证。
若采用硼氢化钠和氯化铈七水合物则以良好产率选择性还原C-10位羰基得到化合物3a。由 13CNMR谱中的δ 203.81和δ 167.50可看出该化合物含两个羰基,再结合 1HNMR谱以及 1H-1H COSY谱分析(图8),H-6(δ 4.18)与H-18(δ 9.30),H-9(δ 1.62~1.59)与H-10(δ 4.49~4.41),H-10(δ 4.49~4.41)与H-11(δ 3.89),H-11(δ 3.89)与H-15(δ 1.08)之间存在相关性,考虑到H-10与两个相邻的质子(H-9和H-11)都有相关性且H-11与H-15之间也存在较弱的相关性,以及存在两个羰基的信息,因此可以判断化合物3a的C-7位羰基未被还原为羟基(图9)。
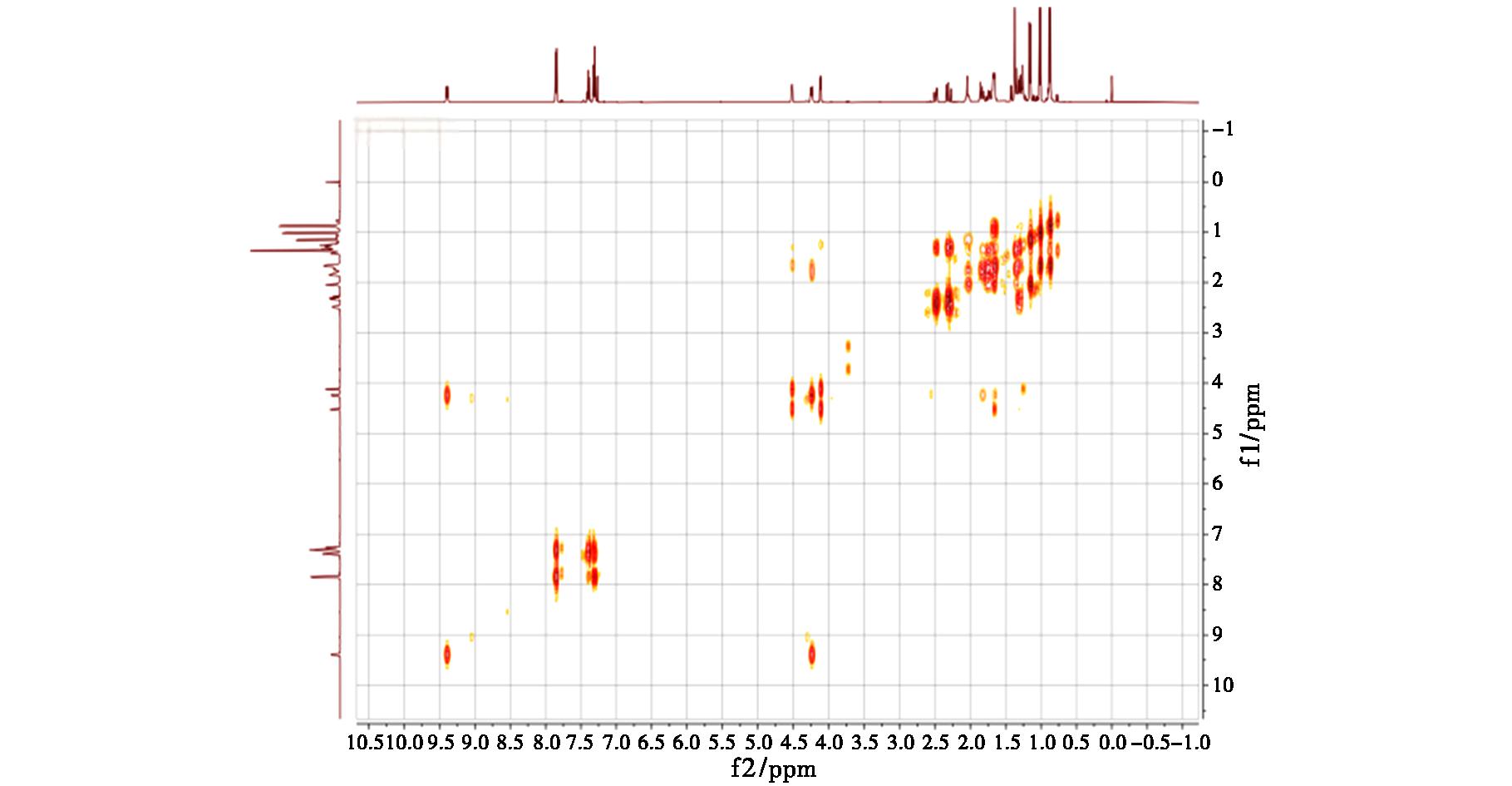
图8 化合物3a 1H-1H COSY谱
Fig.8 1H-1H COSY spectrum of compound 3a
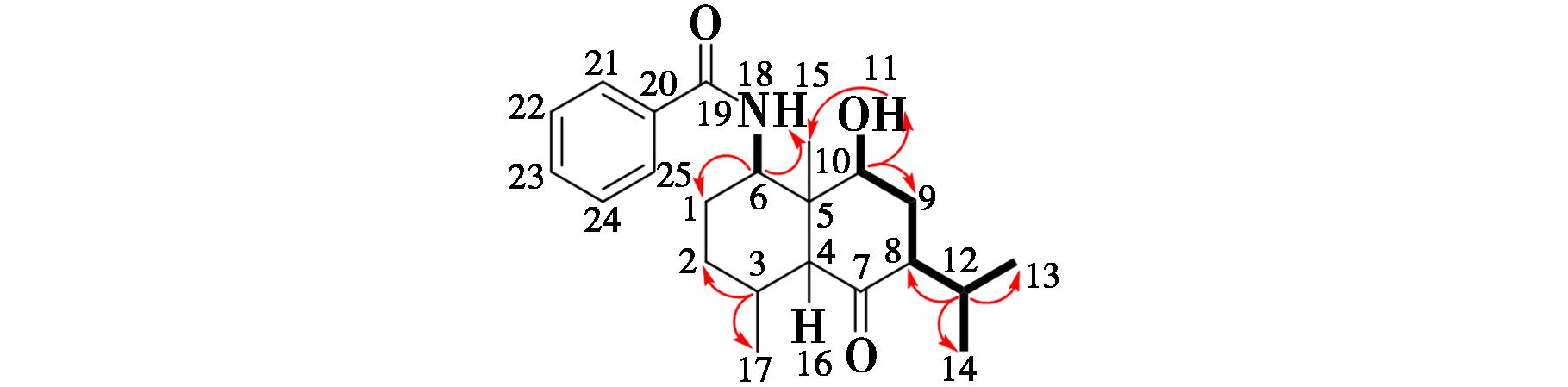
图9 化合物3a的主要 1H-1H COSY相关
Fig.9 Key 1H-1H COSY correlations of compound 3a
本文随后合成了三氯乙酰亚胺酯糖供体Ⅰ~Ⅳ,包括α-葡萄糖、D-核糖、鼠李糖和阿拉伯糖,然后采用Schmidt法对化合物3a的C-10位羟基进行糖苷化修饰,得到桉烷型倍半萜类衍生物。
在合成桉烷型倍半萜糖苷类化合物的过程中,探索了不同的糖供体及其反应效果。使用三氯乙酰亚胺酯葡萄糖(化合物Ⅰ)作为供体,能够得到产物5a。在吡喃糖苷中,由于吡喃糖环的特定构象,糖苷键可以形成α或β构型,核磁共振法是确定吡喃糖苷键构型最常用的方法[26]。在 13CNMR谱中,吡喃糖环上不同碳原子的化学环境会因糖苷键的构型不同而有所区别,表现为不同的化学位移。类似地,在 1HNMR谱中,与糖苷键直接相连的氢原子的化学位移也会因α和β构型的差异而有所不同。例如,在葡萄糖分子中,1-H和2-H之间的耦合常数(1JH-H)是决定糖苷键构型的关键参数。该耦合常数可通过Karplus公式[27]进行计算,并据此推断糖苷键的具体构型。具体而言,当1-H处于直立键时,氢原子指向糖苷键方向,此时糖苷键呈现β构型,其耦合常数JH-H较大(6~8 Hz);而当1-H处于平伏键时,氢原子位于糖苷键侧面,此时糖苷键为α构型,其耦合常数JH-H较小(3~5 Hz)。如图10所示,化合物5a中1′-H(δ 4.50,J1′,2′=7.5 Hz),的核磁共振信号与D-葡萄糖的β构型特征相符,由此可初步推断其糖苷键构型为β构型。此外,化合物5a的碳谱中δ 104.26的信号应归属于β型葡萄糖苷异头位碳,而α型葡萄糖苷异头位碳的化学位移通常<100。值得注意的是,尽管耦合常数是一个重要指标,但在确定糖苷键构型时,除耦合常数(JH-H)之外,亦可参考化学位移(δ)和核Overhauser效应(NOE)等核磁共振(NMR)参数[28]。
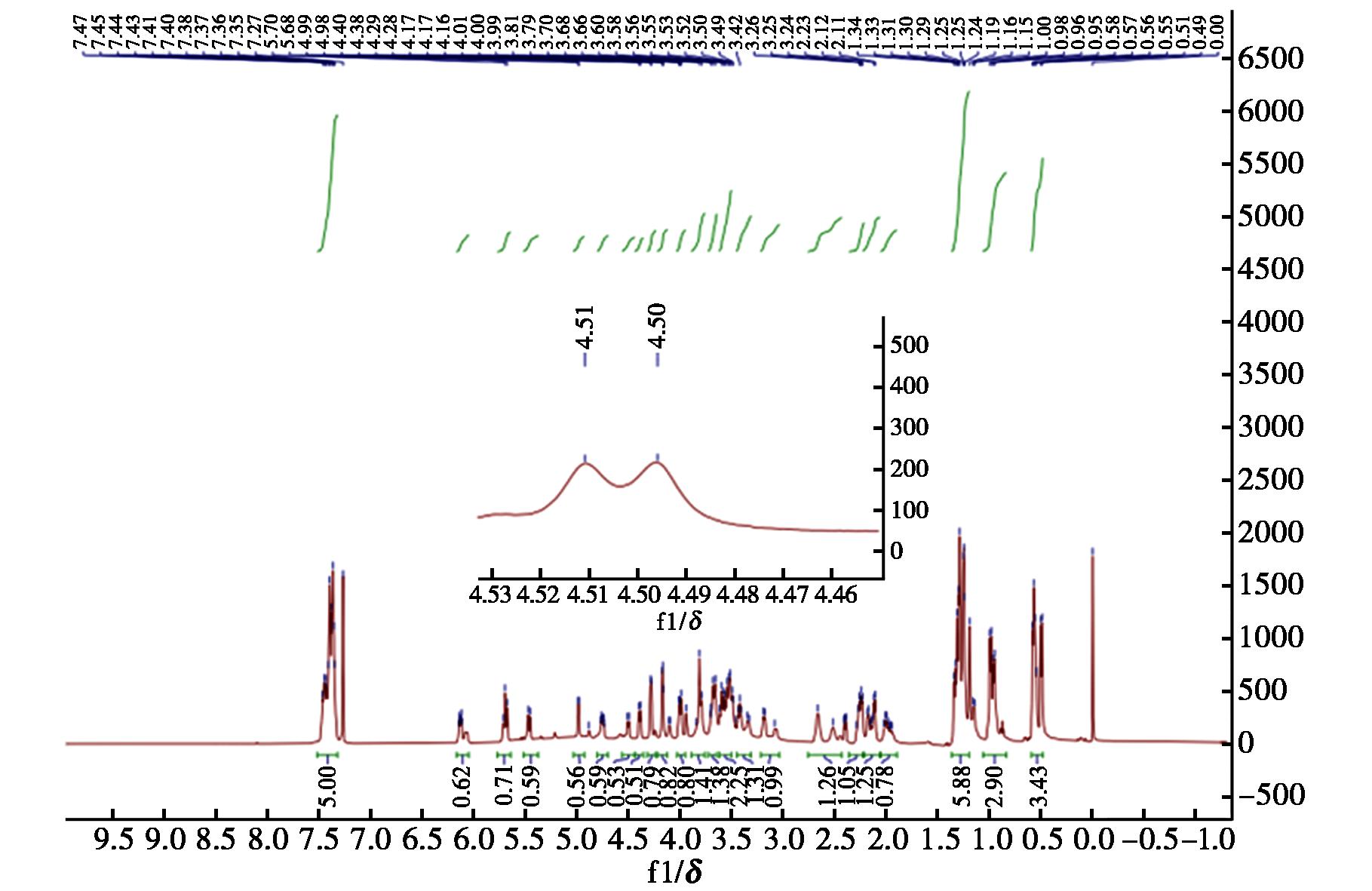
图10 化合物5a的氢谱
Fig.10 1HNMR spectrum of compound 5a
此外,当使用其他三氯乙酰亚胺酯糖供体——D-核糖、阿拉伯糖和鼠李糖时,发现D-核糖作为糖基供体时可以得到D-核糖苷衍生物4b,但产率偏低,而阿拉伯糖和鼠李糖的反应效果不佳,未得到预期产物。这可能是由于这些糖基供体的立体构型、反应活性不适用于使用Schmidt法进行糖苷化反应。
得到目标产物后,本文以阿霉素为阳性对照药,评估了合成的桉烷型倍半萜糖苷类化合物对5种肿瘤细胞系(肺癌细胞A549、前列腺癌细胞DU145、宫颈癌细胞Hela、肝癌细胞HepG2及乳腺癌细胞MCF-7)的抗肿瘤活性,具体结果见表1。对A549、Hela、HepG2和MCF-7这4种肿瘤细胞,化合物表现出了一定的活性,其IC50值范围为94.96~115.7 μmol/L。值得注意的是,化合物4b仅对DU145细胞显示出一定的活性。通过活性数据对比发现,化合物3a对A549、Hela、HepG2和MCF-7这4种肿瘤细胞展现出了较好的抑制作用;而对DU145肿瘤细胞,C-10位糖苷化的化合物4b却明显优于化合物3a。这些结果表明,对于某些肿瘤细胞来说,C-10位的糖苷化修饰并非提高化合物抗肿瘤活性的决定性因素。
表1 化合物1a~5a对不同肿瘤细胞的半数抑制浓度注
Tab.1 Determination of IC50 values of compounds 1a~5a against various cancer cell lines
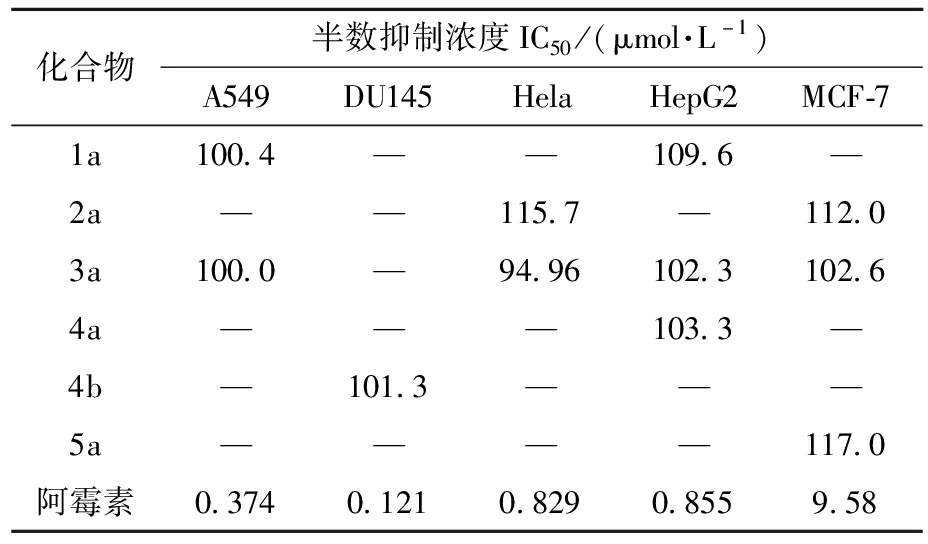
化合物半数抑制浓度IC50/(μmol·L-1)A549DU145HelaHepG2MCF-71a100.4——109.6—2a——115.7—112.03a100.0—94.96102.3102.64a———103.3—4b—101.3———5a————117.0阿霉素0.3740.1210.8290.8559.58
注:“—”表示无活性。
3 结论
本文使用反式-2-戊烯醛、苯甲酰胺和百里醌作为起始原料,通过分子间的Diels-alder反应可以有效地合成桉烷型倍半萜骨架,且产率良好,这为构建桉烷型倍半萜骨架提供了可行的途径。随后,在合成桉烷型倍半萜衍生物的过程中,DIBAL-H可以有效还原化合物1a双环上的两个羰基。此外,通过合理的合成策略,成功制备了三氯乙酰亚胺酯糖基供体,并利用Schmidt糖苷化法将糖基引入到了桉烷型倍半萜骨架上,得到了相应的糖苷类衍生物4a、4b和5a。尽管产率有待提高,但这一研究为桉烷型倍半萜糖苷类衍生物的合成提供了新的途径和思路。
与常用抗癌药物阿霉素相比,化合物1a~5a对多种癌细胞系(包括肺癌、前列腺癌、宫颈癌、肝癌和乳腺癌)中展现出的抑制作用并不显著,但这些结果仍为桉烷型倍半萜类化合物结构优化提供重要参考,并指引进一步探索结构类似或功能相关的化合物。未来的研究方向可能包括尝试其他结构修饰策略,例如调整糖苷键的位置或类型,或去除N-苯甲酰基保护基,以期提高化合物抗癌活性。
[1]Huang H P,Xie Y H,Huang R C,Chen Y L,Deng Y Q,Zhang Z W.Chin.Tradit.Pat.Med.,2024,46(10):3 387-3 392.黄红萍,谢钰航,黄若晨,陈泳乐,邓延秋,张振伟.中成药,2024,46(10):3 387-3 392.
[2]Wu G X,Zhao H Y,Peng C,Liu F,Xiong L.Heliyon,2024,10(15):e35 270.
[3]Zhang H,Sun R R,Liu Y F,Guo X,Li C L,Nan Z D,Jiang Z B.Molecules,2024,29(22):5 483.
[4]Bishayee A,Kavalakatt J,Sunkara C,Johnson O,Zinzuwadia S S,Collignon T E,Banerjee S,Barbalho S M.Food Chem.,2024,457:140 412.
[5]Zhang C,Wen R,Ma X L,Zeng K W,Xue Y,Zhang P M,Zhao M B,Jiang Y,Liu G Q,Tu P F.J.Nat.Prod.,2018,81(4):866-878.
[6]Wang X,Peng X,Tang C P,Zhou S Z,Ke C Q,Liu Y L,Yao S,Ai J,Ye Y.J.Nat.Prod.,2021,84(5):1 626-1 637.
[7]Fattahian M,Ghanadian M,Zolfaghari B,Aghaei M,Zulfiqar F,Khan I A,Ali Z.Phytochemistry,2022,203:113 411.
[8]Wang Q,Mei W L,Dai H F,Tan D G,Zhang J M,Huang S Z.Phytochemistry,2020,38:161-165.
[9]Jang H J,Oh H M,Hwang J,Tkim M H,Lee S,Jung K,Kim Y H,Lee S W,Rho M C.Phytochemistry,2016,130:335-342.
[10]Nhoek P,Chae H S,Kim Y M,Pel P,Huh J,Kim H W,Choi Y H,Lee K,Chin Y W.J.Nat.Prod.,2021,84(2):220-229.
[11]Ramseyer J,Thuerig B,Demieri M,Schärer H J,Oberhänsli T,Gupta M P,Tamm L,Hamburger M,Potterat O.J.Nat.Prod.,2017,80(12):3 297-3 305.
[12]Wu X D,Ding L F,Tu W C,Yang H,Su J,Peng L Y,Li Y,Zhao Q S.Phytochemistry,2016,129:68-76.
[13]Xu K,Feng Z M,Yang Y N,Jiang J S,Zhang P C.Fitoterapia,2016,114:115-121.
[14]Wang S Y,Ding L F,Su J,Peng L Y,Song L D,Wu X D.Phytochemistry,2018,23:127-131.
[15]Xu X Y,Xie H H,Hao J,Jiang Y M,Wei X Y.Food Chem.,2010,122(4):1 047-1 054.
[16]Seo Y H,Kim J Y,Ryu S M,Hwang S Y,Lee M H,Kim N,Son H,Lee A Y,Kim H S,Moon B C,Jang D S,Lee J.Plants,2023,12(8):1 726.
[17]Wender P A,Lechleiter J C.J.Am.Chem.Soc.,1978,100(13):4 321-4 322.
[18]Vieira Y W,Nakamura J,Finelli F G,Brocksom U,Brocksom T J.J.Braz.Chem.Soc.,2007,18(2):448-451.
[19]Zhang Y,Wang P H,Chu Y,Liu M M,Chen G Y,Lu Y P,Ye D Y.Chin.J.Org.Chem.,2012,32(7):1 340-1 343.张宇,王鹏辉,楚勇,刘明明,陈广怡,陆银萍,叶德泳.有机化学,2012,32(7):1 340-1 343.
[20]Ma K Q,Zhang C B,Liu M M,Chu Y,Hu C Q,Ye D Y.Chin.J.Org.Chem.,2012,32(4):781-785.马开庆,张春波,刘明明,楚勇,胡昌其,叶德泳.有机化学,2012,32(4):781-785.
[21]Xu Z J,Liu X Y,Zhu M Z,Xu Y L,Yu Y,Xu H R,Cheng A X,Lou H X.Org.Lett.,2021,23(23):9 073-9 077.
[22]Panigrahi A,Pulukuri K K.ChemRxiv,2024,DOI:10.26434/chemrxiv-2023-3fldg-v4.
[23]Ma K Q,Zhang C B,Liu M M,Chu Y,Zhou L,Hu C Q,Ye D Y.Tetrahedron Lett.,2010,51(14):1 870-1 872.
[24]Gu X D,Dai Y Y,Guo T T,Franchino A,Dixon D J,Ye J X.Org.Lett.,2015,17(6):1 505-1 508.
[25]Peng P,Schmidt R R.Acc.Chem.Res.,2017,50(5):1 171-1 183.
[26]Pei Y H,Hua H M,Li Z L,Chen G.Acta Pharm.Sin.,2011,46(2):127-131.裴月湖,华会明,李占林,陈刚.药学学报,2011,46(2):127-131.
[27]Karplus M.J.Chem.Phys.,1959,30(1):11-15.
[28]Speciale I,Notaro A,Garcia-vello P,Lorenzo F,Armiento S,Molinaro A,Marchetti R,Silipo A,Castro C.Carbohydrate Polym.,2022,277:118 885.