由于免疫抑制剂和广谱抗生素等的大量使用,真菌感染的发生率大幅度上升,已成为一种具有较高致死率的临床常见病[1,2]。14α-去甲基化酶(CYP51)是目前临床上用来治疗真菌感染的主要靶点[3],唑类药物是一类代表性的CYP51抑制剂,是临床上使用最广泛的抗真菌药物[4],一线抗真菌感染的药物(图1)如氟康唑[5]、伏立康唑[6]、伊曲康唑[7]和泊沙康唑[8]等由于大量的应用,耐药性问题日益严重,不能满足临床需求[9,10]。
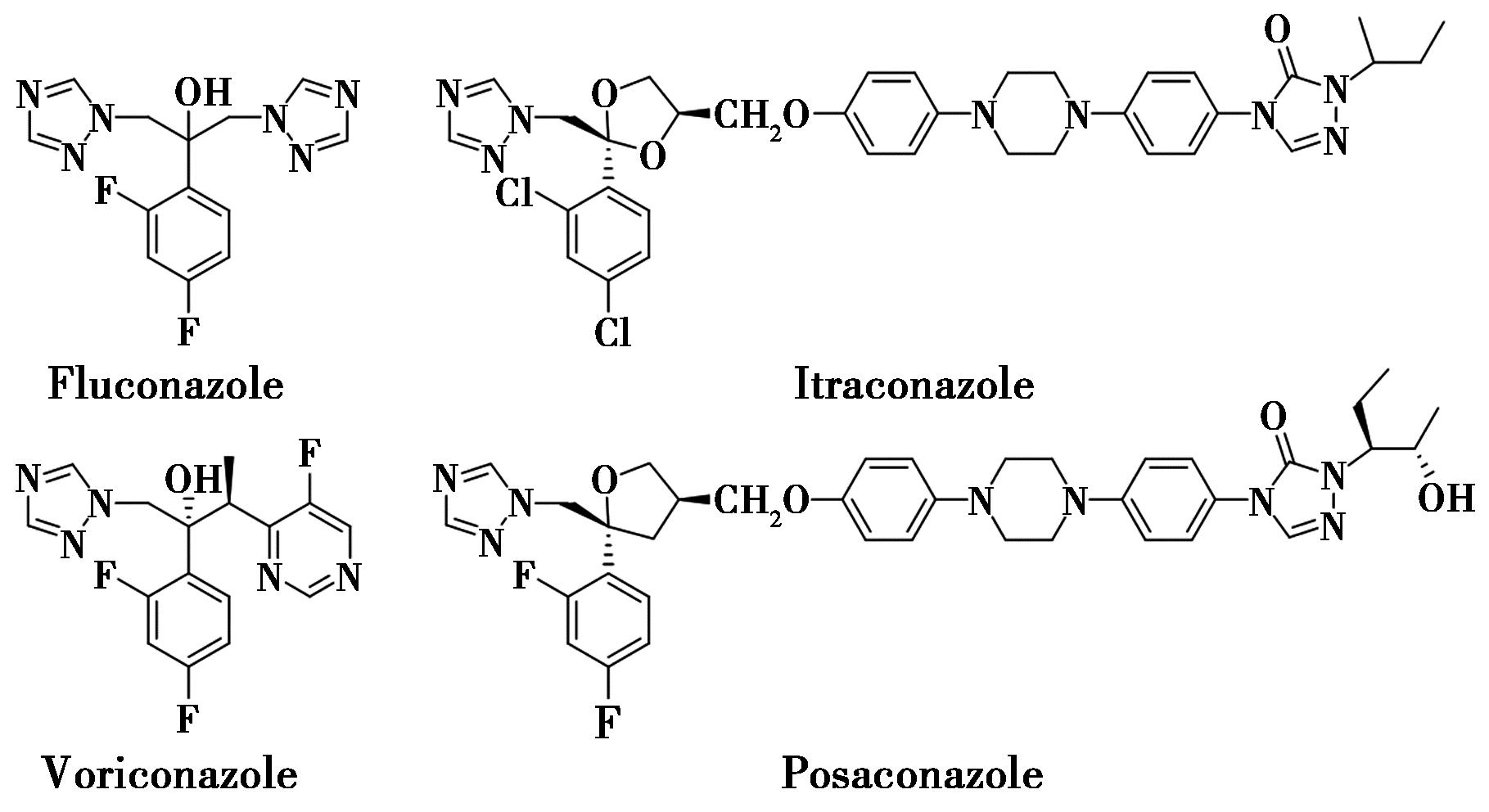
图1 CYP51抑制剂结构
Fig.1 Structures of CYP51 inhibitors
临床上使用的几种非甾体抗炎药(NSAIDs)被发现在体外具有一定的抗真菌能力[11-13]。当它们与唑类药物(CYP51抑制剂)联合使用时,NSAIDs可能会明显提高CYP51抑制剂的抗真菌疗效[14]。值得注意的是,它们甚至在治疗耐药真菌感染方面表现出独特的优势。已证实布洛芬可阻断真菌细胞的外排泵,并与氟康唑有协同抗真菌效果[15,16]。因此,设计含NSAIDs片段的新型药物,发挥其协同抑制的优势,提高抗真菌治疗效果是一个非常好的思路[17,18]。
CYP51底物进出通道是一个狭长的疏水口袋,唑类化合物的侧链与CYP51疏水口袋中的氨基酸相互作用,不同的氢键和疏水性相互作用可能使小分子在提升药效力、逆转耐药性和治愈霉菌感染等方面表现出一定的优势。例如泊沙康唑和伊曲康唑由于具有长侧链结构,不仅能有效抑制念珠菌,对曲霉病和隐球菌也具有较好的抑制效果[19,20]。因此,设计不同类型及长度侧链的唑类CYP51抑制剂是开发新型唑类药物的一个有效途径。
有文献报道含哌嗪片段的唑类化合物表现出良好的抗真菌活性[21,22],因此,保留唑类化合物关键药效团,以哌嗪或者甲基哌嗪为连接片段,以对唑类药物治疗效果具有协同增效作用的NSAIDs片段为侧链,设计合成三氮唑酰胺衍生物,以期发现具有广谱抗真菌活性的CYP51抑制剂。
1 实验部分
1.1 主要仪器与试剂
RQ598型磁力搅拌器(艾卡(广州)仪器设备有限公司);RQ1139型磁力搅拌低温反应浴(深圳勒普拓仪器技术有限公司);ZF-20D型暗箱式紫外分析仪、SHZ-DI型循环真空泵(巩义市予华仪器有限责任公司);RQ691型中压快速纯化制备(天津博纳艾杰尔科技有限公司);Bruker 400 MHz型核磁共振仪(德国Bruker公司);Agilent 1290Ⅱ-6740型三重四极杆液质联用仪(安捷伦(中国)科技有限公司);MS204TS型万分之一天平(梅特勒-托利多仪器(上海)有限公司);N1201B型旋转蒸发仪(上海爱朗仪器有限公司)。
(2S)-2-(4-异丁基苯基)丙酸、(2S)-2-(6-甲氧基萘-2-基)丙酸(上海毕得医药科技有限公司);(S)-1-Boc-2-甲基哌嗪、1-Boc-哌嗪(上海韶远试剂有限公司);石油醚、乙酸乙酯(广州启硕化工有限公司);二氯甲烷、甲醇(广东光华科技股份有限公司);1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐、碳酸氢钠、乙腈、无水硫酸钠(安徽泽升科技股份有限公司),所用试剂均为分析纯。
1.2 实验方法
1.2.1 目标化合物的合成
目标化合物的合成路线如图2所示,以(2S)-1-{4-[(2R,3R)-3-(2,4-二氟苯基)-3-羟基-4-(1,2,4-三氮杂环戊熳-1-基)丁-2-基]哌嗪-1-基}-2-[4-(2-甲基丙基)苯基]丙-1-酮(1e)的合成为例。
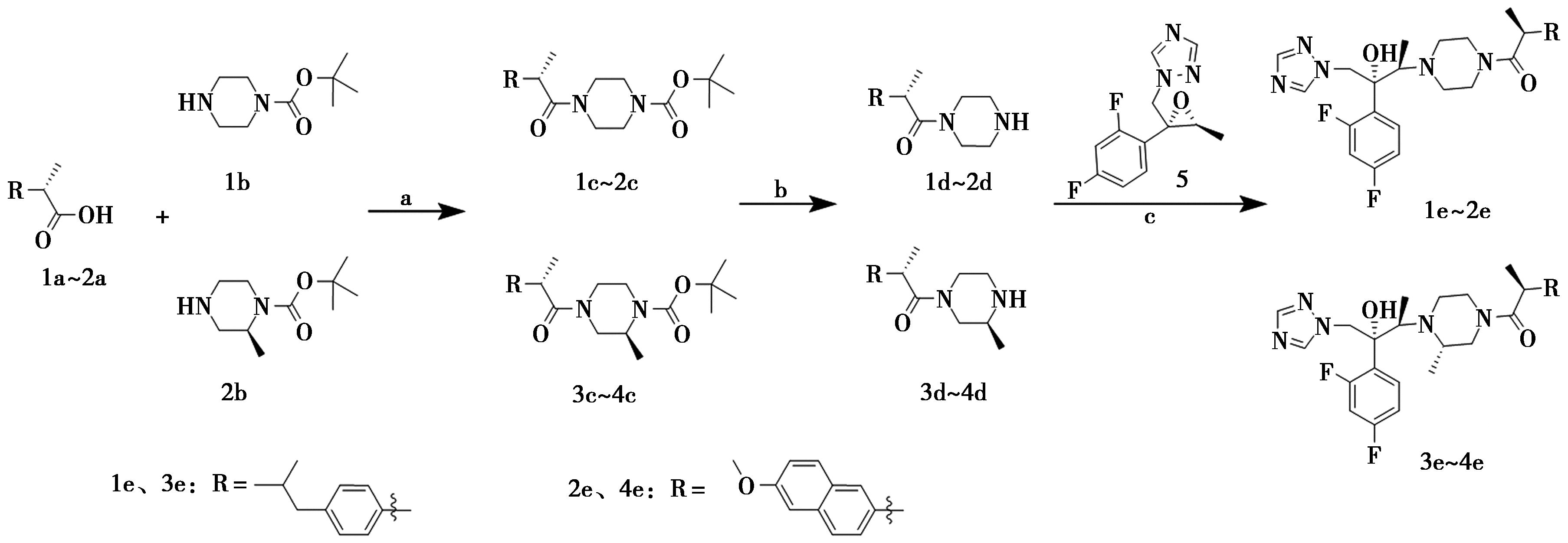
Reagents and conditions:a.EDCI,CH2Cl2,rt,8~12 h,65%~80%;b.4.0 mol/L HCl in 1,4-Dioxane,rt,4 h,60%~70%;c.LiClO4,CH3CN,85 ℃,24 h,45%~60%
图2 目标化合物的合成路线
Fig.2 Synthetic routes of the target compounds
1.2.1.1 4-[(2S)-2-[4-(2-甲基丙基)苯基]丙酰基]哌嗪-1-甲酸-2-甲基丙-2-基酯(1c)的合成
将1.0 g(4.85 mmol)原料(2S)-2-[4-(2-甲基丙基)苯基]丙酸(1a)溶于30 mL无水二氯甲烷,然后加入0.90 g(4.85 mmol)哌嗪-1-甲酸-2-甲基丙-2-基酯(1b)和1.02 g(5.33 mmol)1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(EDCI),室温反应约 10 h。点板监测反应完全,停止搅拌,向反应液中加50 mL水,二氯甲烷萃取(50 mL×3),有机相合并后用30 mL水洗一次,30 mL饱和食盐水洗一次,无水硫酸钠干燥,过滤旋干得粗品,粗品用硅胶柱层析纯化(V(石油醚)∶V(乙酸乙酯)=3∶1),得到1.35 g中间体1c。白色固体,收率71.9%。1HNMR(CDCl3,400 MHz),δ:7.12(q,4H,J=8.2 Hz);3.84(q,2H,J=6.8 Hz);3.52(d,1H,J=11.6 Hz);3.44~3.28(m,4H);3.24~3.13(m,1H);2.78~2.58(m,1H);2.45(d,2H,J=7.2 Hz);1.93~1.79(m,1H);1.51~1.38(m,12H);0.90(d,6H,J=6.6 Hz)。ESI-MS,m/z:375.4[M+H]+。
1.2.1.2 (2S)-2-[4-(2-甲基丙基)苯基]-1-(哌嗪-1-基)丙-1-酮(1d)的合成
将1.3 g(3.47 mmol)原料化合物1c溶于 20 mL(4.0 mol/L)HCl的1,4-二氧六环溶液,室温反应约4 h。点板监测反应完全,停止搅拌,向反应液中加饱和碳酸氢钠溶液调至pH 8~9,乙酸乙酯萃取(50 mL×3),有机相合并后用50 mL水洗一次,50 mL饱和食盐水洗一次,无水硫酸钠干燥,过滤旋干得粗品,粗品用硅胶柱层析纯化(V(二氯甲烷)∶V(甲醇)=20∶1),得到625 mg中间体1d。白色固体,收率65.6%。1HNMR(CDCl3,400 MHz),δ:7.13(d,2H,J=8.1 Hz);7.08(d,2H,J=8.2 Hz);3.87~3.77(m,2H);3.49~3.39(m,1H);3.34(t,2H,J=4.9 Hz);2.88~2.80(m,1H);2.77~2.60(m,2H);2.44(d,2H,J=7.2 Hz);2.32~2.23(m,1H);1.84(dp,1H,J=13.5,6.8 Hz);1.43(d,3H,J=6.9 Hz);0.88(d,6H,J=6.6 Hz)。ESI-MS,m/z:275.4[M+H]+。
1.2.1.3 (2S)-1-{4-[(2R,3R)-3-(2,4-二氟苯基)-3-羟基-4-(1,2,4-三氮杂环戊熳-1-基)丁-2-基]哌嗪-1-基}-2-[4-(2-甲基丙基)苯基]丙-1-酮(1e)的合成
将200 mg(0.80 mmol)原料1-{[(2R)-2-(2,4-二氟苯基)-3-甲基氧杂环丙-2-基]甲基}-1,2,4-三氮杂环戊熳(5)溶于10 mL乙腈,然后加入218.45 mg(0.80 mmol)化合物1d和254.08 mg(2.39 mmol)高氯酸锂,氮气保护下,85 ℃反应约24 h。点板监测反应完全,停止搅拌,将反应液浓缩至干,用20 mL二氯甲烷溶解,过滤取滤液,旋干得粗品,粗品用硅胶柱层析纯化(V(二氯甲烷)∶V(甲醇)=50∶1),得到219 mg目标化合物1e。白色固体,纯度99.54%,收率52.3%。1HNMR(CDCl3,400 MHz),δ:7.81(s,1H);7.68(s,1H);7.36~7.24(m,1H);7.03(q,4H,J=8.1 Hz);6.68~6.60(m,2H);4.77(q,2H,J=14.2 Hz);3.75(q,1H,J=6.8 Hz);3.50~3.14(m,2H);2.85(s,1H);2.65(s,2H);2.36(d,3H,J=7.2 Hz);1.86~1.69(m,4H);1.35(d,3H,J=6.8 Hz);0.80(d,6H,J=6.6 Hz);0.67(d,3H,J=6.5 Hz)。13CNMR(CDCl3,101 MHz),δ:172.29,162.57(dd,J=249.9,12.1 Hz),158.06(dd,J=244.2,11.0 Hz),151.70,144.13,140.19,139.24,130.58(dd,J=9.1,5.9 Hz),129.60,126.95,124.66(d,J=12.0 Hz),111.58(d,2H,J=21.0 Hz),104.54~103.67(m),78.96(d,J=5.3 Hz),64.04,55.88(d,J=6.8 Hz),45.88,44.97,42.91,42.46,30.19,22.32,20.59,6.74。ESI-MS,m/z:526.5[M+H]+。
目标化合物2e、3e和4e的合成参考化合物1e的合成方法。
1.2.1.4 (2S)-1-{4-[(2R,3R)-3-(2,4-二氟苯基)-3-羟基-4-(1,2,4-三氮杂环戊熳-1-基)丁-2-基]哌嗪-1-基}-2-(6-甲氧基萘-2-基)丙-1-酮(2e)的合成
198 mg白色固体,纯度99.47%,收率45.3%。1HNMR(CDCl3,400 MHz),δ:7.80(s,1H);7.67(s,1H);7.61(t,2H,J=8.7 Hz);7.51(s,1H);7.36~7.18(m,2H);7.11~7.01(m,2H);6.70~6.56(m,2H);4.94~4.58(m,2H);3.92(d,1H,J=6.3 Hz);3.83(s,3H);3.67~3.15(m,3H);2.85(d,1H,J=1.4 Hz);2.67(d,2H,J=1.5 Hz);2.36(d,1H,J=2.8 Hz);1.99(s,1H);1.91~1.81(m,1H);1.43(d,3H,J=6.0 Hz);0.64(s,3H)。13CNMR(CDCl3,101 MHz),δ:172.33,162.56(dd,J=250.3,12.0 Hz),158.04(dd,J=245.1,11.7 Hz),157.61,151.60,144.13,137.06,133.45,130.56(dd,J=9.2,6.1 Hz),129.11,127.57,126.05,125.51,124.56(d,J=10.3 Hz),119.08,111.54(d,J=20.2 Hz),105.62,104.44~103.71(m),78.95(d,J=5.6 Hz),64.05,55.89(d,J=6.9 Hz),55.33,45.91,43.21,42.48,20.72,6.83。ESI-MS,m/z:550.6[M+H]+。
1.2.1.5 (2S)-1-[(3S)-4-[(2R,3R)-3-(2,4-二氟苯基)-3-羟基-4-(1,2,4-三氮杂环戊熳-1-基)丁-2-基]-3-甲基哌嗪-1-基]-2-[4-(2-甲基丙基)苯基]丙-1-酮(3e)的合成
312 mg白色固体,纯度99.28%,收率72.6%。1HNMR(CDCl3,400 MHz),δ:7.80(s,1H);7.68(s,1H);7.32~7.23(m,1H);7.13~6.97(m,4H);6.72~6.59(m,2H);4.89~4.58(m,3H);4.49~4.34(m,1H);3.75(dd,1H,J=13.7,6.8 Hz);3.14~2.51(m,5H);2.36(d,2H,J=7.1 Hz);1.84~1.69(m,2H);1.36(d,3H,J=6.8 Hz);1.04(d,1H,J=5.7 Hz);0.90(d,1H,J=6.6 Hz);0.84~0.74(m,8H);0.64(d,J=6.8 Hz,2H)。13CNMR(CDCl3,101 MHz),δ:172.60,162.53(dd,J=249.9,12.2 Hz),158.21(dd,J=245.8,11.8 Hz),151.55,144.19,140.25,139.75,130.49(dd,J=8.7,6.2 Hz),129.59,126.98,124.31(d,J=14.0 Hz),111.54(d,J=20.7 Hz),104.85~103.50(m),79.26(d,J=5.7 Hz),62.36,57.26,55.50(d,J=7.9 Hz),51.98,47.95,45.95,44.89,43.27,42.47,30.22,22.00,20.50,11.16。ESI-MS,m/z:540.6[M+H]+。
1.2.1.6 (2S)-1-[(3S)-4-[(2R,3R)-3-(2,4-二氟苯基)-3-羟基-4-(1,2,4-三氮杂环戊熳-1-基)丁-2-基]-3-甲基哌嗪-1-基]-2-(6-甲氧基萘-2-基)丙-1-酮(4e)的合成
216 mg白色固体,纯度99.25%,收率48.1%。1HNMR(CDCl3,400 MHz),δ:7.84~7.73(m,1H);7.67(s,1H);7.66~7.58(m,2H);7.57~7.47(m,1H);7.30(dd,1H,J=8.4,1.1 Hz);7.27~7.21(m,1H);7.09~7.02(m,2H);6.71~6.60(m,2H);4.90~4.53(m,3H);4.52~4.38(m,1H);3.96~3.88(m,1H);3.83(s,3H);3.07~2.55(m,5H);1.61(s,1H);1.42(d,3H,J=6.8 Hz);1.06(d,1H,J=6.0 Hz);0.99~0.74(m,3H);0.58(d,2H,J=6.5 Hz)。13CNMR(CDCl3,101 MHz),δ:172.68,162.52(dd,J=251.1,11.2 Hz),158.21(dd,J=244.8,11.8 Hz),157.63,151.54,144.20,137.62,133.45,130.52(dd,J=14.6,8.1 Hz),129.07,127.58,125.89,125.44,124.31(d,J=13.1 Hz),119.12,111.52(d,J=20.3 Hz),105.65,104.80~103.38(m),79.12(d,J=6.2 Hz),62.29,56.28(d,J=3.1 Hz),55.31,52.10,47.96,45.93,43.50,42.89,40.40,20.84,11.24。ESI-MS,m/z:564.6[M+H]+。
1.2.2 化合物体外抗真菌活性实验
依据美国临床标准委员会(CLSI)建立的真菌敏感性测试方案(M27-A3)的微量液基稀释法进行操作[23]。
选择标准株:白色念珠菌(Candida albicans) ATCC5314(记为C.alb)、烟曲霉(Aspergillus fumigatus)CGMCC3.7795(记为A.fum)、新型隐球菌(Crytococcus neoformans) CGMCC3.1563(记为C.neo)和氟康唑耐药白色念珠菌:C.alb 901为测试菌株。
将真菌进行传代培养后,收集指数生长末期的真菌细胞,用RPMI-1640培养基稀释至5×103 cfu/mL的浓度,并将100 μL真菌悬浮液接种到96孔微孔板中。将测试化合物溶解在DMSO中作为储备溶液,然后用RPMI-1640培养基稀释备用。向每个孔中加入100 μL的测试化合物,然后将培养板在35 ℃下孵育24 h用于白色念珠菌,72 h用于新型隐球菌,48 h用于烟曲霉。然后用酶标仪于600 nm波长下扫描各孔的吸光度(OD600),MIC80定义为抑制80%以上真菌细胞生长的测试化合物的浓度,所有数据均为3个独立实验的平均值。
1.2.3 分子对接
分子对接是用Discovery Studio 2016完成的,CYP51晶体结构(PDB∶5TZ1)从蛋白质数据库下载。对蛋白质结构进行修饰和调整,删除不需要的水分子和配体,添加极性氢,以CYP51原晶体中的配体结合口袋作为分子对接的活性口袋。小分子是通过Discovery Studio内置的“制备配体”协议和默认参数制备的,利用PyMOL 2.5.0软件进行可视化制图。
2 结果与讨论
2.1 体外抗真菌活性
由表1结果可知,目标化合物对白色念珠菌ATCC5314表现出良好的活性,化合物3e(0.25 μg/mL)优于阳性对照氟康唑(0.5 μg/mL),化合物1e和2e与氟康唑相当。阳性对照药氟康唑(>64 μg/mL)对烟曲霉基本无抑制活性,化合物1e~4e对烟曲霉有着较好的抑制活性,其中以化合物1e和3e活性最好(2.0 μg/mL)。化合物3e(2.0 μg/mL)对新型隐球菌的活性与氟康唑(2.0 μg/mL)相当,对氟康唑耐药白色念珠菌的抗菌实验结果表明化合物1e~4e具有抗耐药性,而对照药氟康唑、伏立康唑在测试浓度下没有表现出抑制活性。总之,化合物1e~4e具有广谱、高效的体外抗真菌作用,且对氟康唑耐药白色念珠菌敏感。
表1 目标化合物抗真菌活性注
Tab.1 Antifungal activity of the target compounds
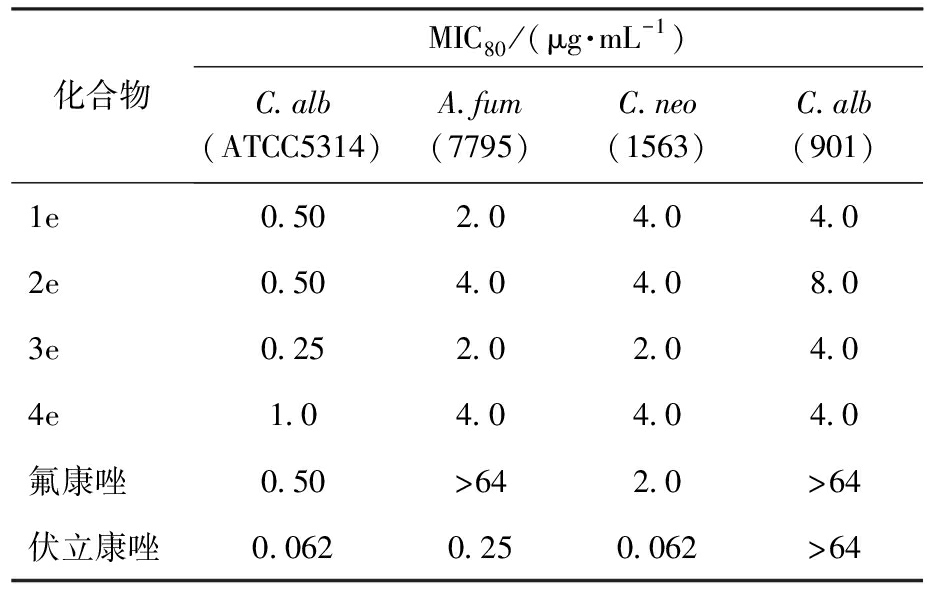
化合物MIC80/(μg·mL-1)C.alb(ATCC5314)A.fum(7795)C.neo(1563)C.alb(901)1e0.502.04.04.02e0.504.04.08.03e0.252.02.04.04e1.04.04.04.0氟康唑0.50>642.0>64伏立康唑0.0620.250.062>64
注:C.alb ATCC5314:白色念珠菌(ATCC5314);C.neo 1563:新型隐球菌(CGMCC3.1563);A.fum 7795:烟曲霉(CGMCC3.7795);C.alb 901:氟康唑耐药白色念珠菌。
2.2 化合物3e与CYP51的分子对接结果
为了阐明目标化合物抗真菌的作用机制,选取化合物3e与白色念珠菌CYP51蛋白(PDB code:5TZ1)进行分子对接,以便更好地了解其抑制CYP51的作用机制(图3)。分子对接结果显示,化合物3e的侧链很好地占据了底物进出通道,并到达通道入口。哌嗪环和Leu376,哌嗪环上的甲基和Leu121、Tyr118、Phe233之间,以及布洛芬片段的丙基链和Leu87、Leu88和Tyr64之间形成疏水相互作用。布洛芬片段的苯环与His377和Phe233形成π-π相互作用,并且哌嗪环氢原子与Met508形成碳氢相互作用。
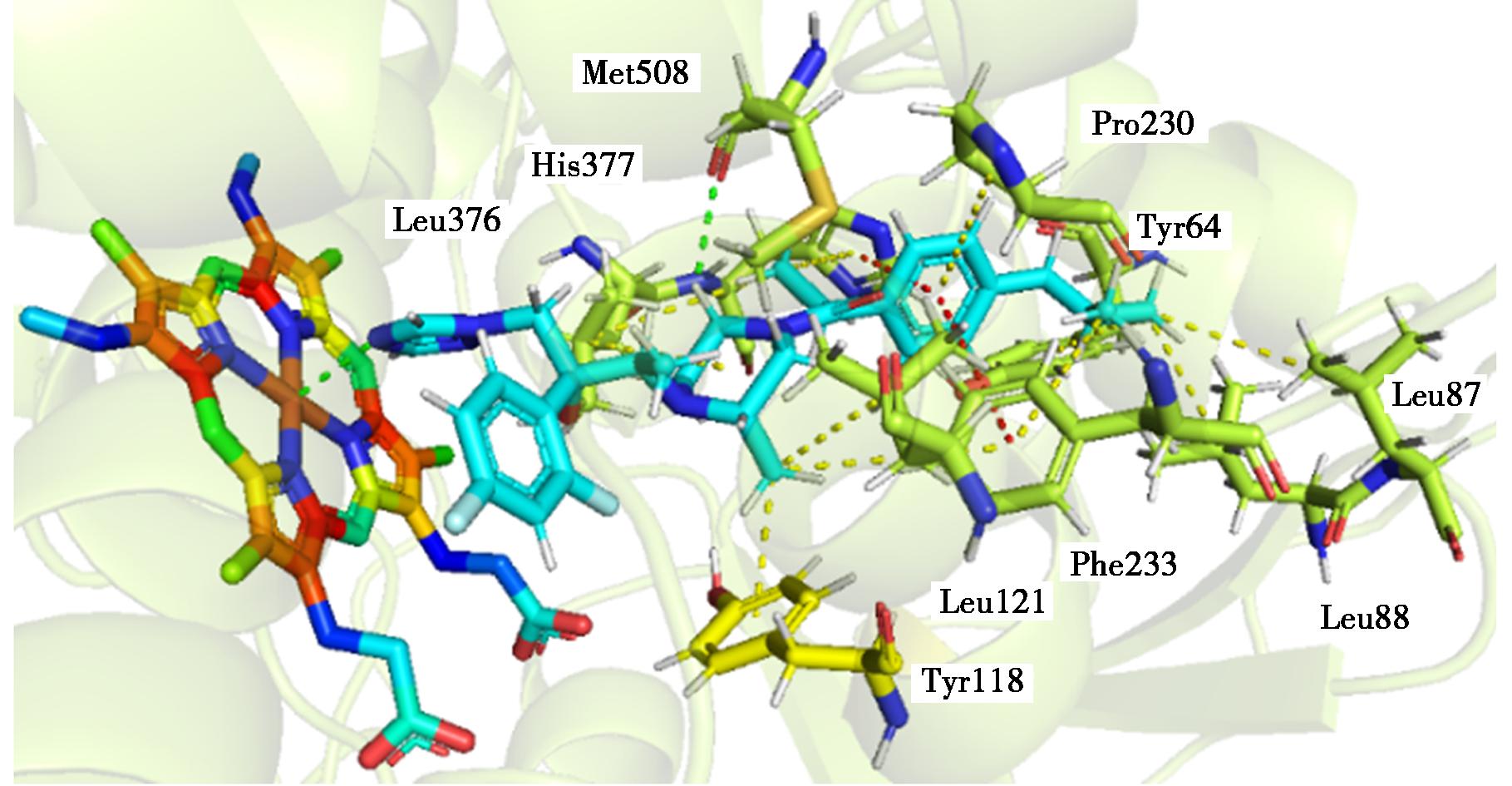
π-π相互作用红色虚线表示;黄色表示疏水相互作用;绿色表示氢键相互作用
图3 化合物3e与CYP51的分子对接结果
Fig.3 Molecular docking results of compound 3e with CYP51
分子蛋白对接结果证实化合物3e的侧链很好地占据了CYP51疏水活性口袋,哌嗪环上的甲基和布洛芬片段的异丙基链与疏水口袋氨基酸残基的疏水相互作用可能是其抗真菌活性较好的原因。但烷基链长度对疏水相互作用的影响尚未得到系统探究,未来可将哌嗪环上的甲基或布洛芬片段的异丙基链替换为不同长度的直链烷基(如乙基、丙基、丁基等)及带有分支的烷基(如异丙基、异丁基等)。分析烷基链长度与分支结构对配体与CYP51疏水口袋结合的影响。例如,当烷基链长度与疏水口袋的空间尺寸高度匹配时,可增加配体与口袋残基的疏水相互作用,进而增强结合稳定性,提升抗真菌活性。
总之,本文证明将NSAIDs活性片段与唑类药物关键药效团相连,可有效发挥抗真菌作用,验证了设计的合理性。
3 结论
本文保留唑类化合物关键药效团,以哌嗪或者甲基哌嗪为连接片段,以对唑类药物治疗效果具有协同增效作用的NSAIDs片段为侧链,设计合成了4个三氮唑酰胺衍生物,其结构经MS、1HNMR、13CNMR确认,经高效液相色谱验纯(纯度>95%)。对合成的目标化合物进行体外抗真菌测试结果显示,4个化合物对白色念珠菌、烟曲霉、新型隐球菌、氟康唑耐药白色念珠菌均表现出了非常好的抑制作用。分子蛋白对接结果证实化合物3e能够很好的结合在CYP51活性口袋,并且形成稳定的结合模式。因此,以哌嗪或者甲基哌嗪作为连接片段,将NSAIDs片段引入唑类药物侧链可以发挥较好的抗真菌作用,本文工作的完成能够为开发新型唑类抗真菌药物提供有价值的参考。
[1]Suleyman G,Alangaden G J.Infect.Dis.Clin.N.Am.,2021,35(4):1027-1053.
[2]Zhang M M,Lei M K,Pang M L,Wang Y Y,Zhou L F,Jiang Y X.Phy.Test.Chem.Anal.part B:Chem.Anal.,2024,60(10):1061-1066.
张萌萌,雷美康,庞明利,王莹莹,周垄芳,蒋永祥.理化检验-化学分册,2024,60(10):1061-1066.
[3]Lepesheva G I,Friggeri L,Waterman M R.Parasitology,2018,145(14):1820-1836.
[4]Peyton L R,Gallagher S,Hashemzadeh M.Drugs Today,2015,51(12):705.
[5]Brion L P,Uko S E,Goldman D L.J.Infect.,2007,54(6):521-529.
[6]Wakie R,Prasad R,Morschhäuser J,Barchiesi F,Borowski E,Milewski S.Mycoses,2007,50(2):109-115.
R,Prasad R,Morschhäuser J,Barchiesi F,Borowski E,Milewski S.Mycoses,2007,50(2):109-115.
[7]Feng W L,Yang J,Pan Y W,Xi Z Q,Qiao Z S,Ma Y.Can.J.Microbiol.,2016,62(2):173-178.
[8]Wang Q Q,Li Y,Cai X,Li R Y,Zheng B,Yang E C,Liang T Y,Yang X Y,Wan Z,Liu W.Antibiotics,2021,10(10):1217.
[9]Quiles-melero I,García-rodríguez J.Rev.Iberoam.De Micología,2021,38(2):42-46.
[10]Ben-ami R,Kontoyiannis D P.Infect.Dis.Clin.N.Am.,2021,35(2):279-311.
[11]Khodavandi A,Alizadeh F,Vanda N A,Karimi G,Chong P P.Pharm.Biol.,2014,52(12):1505-1509.
[12]Urai M,Kaneko Y,Niki M,Inoue M,Tanabe K,Umeyama T,Fukazawa H,Ohno H,Miyazaki Y.J.Infect.Chemother.,2014,20(10):612-615.
[13]Arai R,Sugita T,Nishikawa A.Mycoses,2005,48(1):38-41.
[14]Scott E M,Tariq V N,Mccrory R M.Antimicrob.Agents Chemother.,1995,39(12):2610-2614.
[15]Pina-vaz C,Sansonetty F,Rodrigues A G,Martinez-de-oliveira J,Fonseca A F,Mardh P A.J.Med.Microbiol.,2000,49(9):831-840.
[16]Sharma M,Biswas D,Kotwal A,Thakuria B,Kakati B,Chauhan B S,Patras A.J.Clin.Diagn.Res.,2015,9(1):20-22.
[17]Li C C,Tu J,Han G Y,Liu N,Sheng C Q.Eur.J.Med.Chem.,2022,227:113961.
[18]Mi Z S,Gan B,Yu S H,Guo J N,Zhang C J,Jiang X Y,Zhou T,Su J,Bai R R,Xie Y Y.J.Enzyme Inhib.Med.Chem.,2019,34(1):1489-1497.
[19]Shu Y S,Shi Y P,Yang Y L,Dong Z G,Yi Q Y,Shi H Y.J.Clin.Pharm.Ther.,2022,47(12):1966-1981.
[20]Groll A H.Mycoses,2002,45(S3):48-55.
[21]Thamban C N,Shrestha S K,Ngo H X,Tsodikov O V,Howard K C,Garneau-tsodikova S.J.Med.Chem.,2018,61(1):158-173.
[22]Zhu P H,Zhou T,Chen H,Chen X R,Wang X B,Kong L Y,Yang M H.J.Med.Chem.,2023,66(11):7497-7515.
[23]CLSI M27-Ed4.Reference Method for Broth Dilution Antifungal Susceptibility Testing of Yeasts-Approved Standard,2017-11-30.