随着石油的应用领域日益广泛,污染问题进一步加剧,人们对生存环境的污染问题越来越重视[1]。石油是由烷烃和芳香烃组成的复杂混合物[2],易造成土壤累积污染,被纳入《土壤污染防治行动计划》中,成为土壤环境中重点监测的污染物。根据国家颁布的GB 36600—2018《土壤环境质量 建设用地土壤污染风险管控标准(试行)》[3],石油烃不同碳段会根据理化性质差异具备不同的毒性,如致癌性和非致癌毒性,而芳香烃化合物因分子结构特性更容易产生生态毒性,对环境生物和人类健康同样存在风险[4]。目前,我国土壤污染已从单一污染向复合污染转变,这对污染土壤修复技术提出更高的要求[5]。单一测定土壤总石油烃含量,难以科学、全面、准确地定量反映土壤的污染程度,而以毒性相对较强的芳香烃作为总体石油烃筛选值的取值依据,具有重要的污染评估意义。对土壤样品中脂肪烃和芳香烃进行分离监测,能够更加精准地开展地块调查评估、完成污染风险管控判定,进而针对性地对污染物进行毒性降解与土壤修复处理,切实保障人类健康。
近年来,土壤石油烃中脂肪烃和芳香烃的高效分离已然成为研究热点,国内外学者围绕该方向开展了大量探索性工作。如何燎等[6]对石油烃中芳香烃分离技术进行了探究,总结了芳烃分离技术的选择策略及未来发展方向;王言等[7]则聚焦低共熔溶剂在芳香烃/脂肪烃混合物分离中的应用,通过测试及探究奠定了实验基础。在具体分离技术研究方面,Liu等[8]研发的高效分离膜能够有效分离脂肪烃和芳香烃混合物,具有很大的应用前景,但其成本高,难以实现工业化与常规检测的大规模推广;胥红研[9]采用氧化铝小柱分离土壤柴油段总石油烃中的脂肪烃和芳香烃,操作简便且回收率高,但方法重现性受人员操作影响较大,检测结果难以保证重现性等;此外,HPLC-GC联用法可同时测定土壤及奶粉中脂肪烃和芳香烃,具有溶剂消耗少、正确度高的优势,但对专用的分析仪器要求严苛,在现有常规实验室中难以普及推广应用[10,11];柯润辉等[12]提出的PTV-GC-FID法可定量分析烃类污染残留,操作便捷,但未针对土壤基质的复杂性进行优化,适配性不足;李翔等[13]利用TLC-FID分离测定土壤中石油烃组分,仅适用于沸点>300 ℃的馏分,对低沸点脂肪烃、芳香烃则易造成一定损失;张青春[14]、胡凤玲[15]分别建立的氧化铝层析柱分离法、二氯甲烷液液萃取法,可实现脂肪烃和芳香烃的有效分离,但上述方法适用于环境类水质样品的测定;铁建成等[16]建立加压流体萃取法,提取固体废物中多环芳烃定性定量分析方法,提取效率高,具有一定的参考价值,但针对土壤基质的复杂性,存在基质干扰大、净化效果差等问题。
综上,现有脂肪烃(AH)与芳香烃(ArH)分离技术虽种类较多,但针对土壤复杂基质的专用分离方法仍存在诸多不足,部分方法受仪器成本、基质适配性差等问题,难以满足目前土壤石油烃污染精细检测与风险评估的实际需求。基于此,本文建立一种适用于土壤基质的石油烃中脂肪烃和芳香烃分离分析方法,通过优化前处理工艺与分离条件,解决现有方法在土壤基质中基质干扰大、普适性差、重现性不足、仪器门槛高等问题,实现土壤石油烃中脂肪烃与芳香烃的高效、稳定、精准分离与定量。该方法可为精细评估土壤石油烃中毒性来源提供切实有效的检测手段,为土壤污染地块的精准风险管控提供数据支撑,同时也为土壤基质中烃类化合物的分离纯化研究提供新的借鉴。
1 实验部分
1.1 主要仪器与试剂
TRACE 1300型气相色谱仪(赛默飞世尔科技(中国)有限公司);HPFE 06S型高通量加压流体萃取仪(睿科集团(厦门)股份有限公司);BSA224S型电子天平(赛多利斯科学仪器(北京)有限公司)。
16种多环芳烃标准溶液(1000 μg/mL)、正葵烷标准溶液(100 μg/mL)、正四十烷标准溶液(100 μg/mL)(北京坛墨质检科技股份有限公司);正己烷中31种正构烷烃类(C10~C40)标准溶液(1000 μg/mL)、正己烷(色谱级)、丙酮(色谱级)、二氯甲烷(色谱级)(上海安谱实验科技股份有限公司);SPE硅胶小柱、C18小柱、中性氧化铝小柱(广州科芊实验器材有限公司)。
1.2 校准曲线配制
16种多环芳烃曲线浓度:分别用正己烷稀释标准标液为0、10、25、50、75、100 μg/mL。
正构31种石油烃曲线浓度:分别用正己烷稀释标准标液,配制曲线浓度点为2(总浓度为 62 μg/mL)、10(总浓度为310 μg/mL)、20(总浓度为620 μg/mL)、50(总浓度为1550 μg/mL)、100(总浓度为3100 μg/mL)、300 μg/mL(总浓度为9300 μg/mL);正葵烷标准使用液:用正己烷稀释标准标液为50 μg/mL;正四十烷标准使用液:用正己烷稀释标准标液为50 μg/mL。
1.3 试验方法
1.3.1 样品采集与保存
收集新鲜土壤,4 ℃以下密封冷藏保存。样品采用冷冻干燥方式脱水,经过研磨,将样品处理成1 mm颗粒状。
1.3.2 样品预处理
称取10 g(精确到0.01 g)土壤样品,加入 25 μg多环芳烃标液、50 μg石油烃标液,装入萃取池,加压流体萃取装置加热温度为140 ℃,加压压力为7 MPa,萃取溶剂为V(丙酮)∶V(二氯甲烷)=1∶1,预加热平衡时间10 min,萃取时间 10 min,吹扫时间60 s,萃取流程循环2次。玻璃接收瓶为60 mL,萃取池规格为34 mL。接收瓶接收萃取液,转移到平行浓缩仪浓缩至约1 mL,待净化。依次用10 mL(1 g/6 mL)正己烷活化硅酸镁净化柱,待柱上正己烷近干时,将浓缩液全部转移至净化柱中,开始收集流出液,用约2 mL正己烷洗涤浓缩液收集装置,转移至净化柱,再用 12 mL正己烷淋洗净化柱,收集淋洗液,与流出液合并,浓缩得到的净化液约1 mL,待下一步进行脂肪烃和芳香烃的分离。
1.3.3 分离脂肪烃和芳香烃的影响因素实验
1.3.3.1 分离洗脱压力
量筒量取10 mL正己烷冲洗活化SPE硅胶小柱,弃去洗脱液。取净化液1 mL,加入至活化好的SPE硅胶小柱,分别用常压(AP)、负压(NP)、加压(PP)方式以正己烷洗脱,用比色管接收洗脱液,收集 20 mL,关阀,使得收集于比色管的洗脱液,为第一组分T1(脂肪烃)。取出比色管,装入另一根干净的比色管,缓慢加入35 mL二氯甲烷洗脱,收集于比色管,为第二组分T2(芳香烃)。将以上收集的组分,转移到平行浓缩仪,以对应溶剂润洗比色管3次,浓缩至1 mL,上机分析。
1.3.3.2 分离柱填料种类
分别选取SPE硅胶小柱、C18小柱、中性氧化铝小柱,正己烷活化3种分离柱,弃去洗脱液。取1 mL净化液分别上样,用正己烷在常压下以自然流速进行洗脱,收集20 mL于比色管的洗脱液,为第一组分T1(脂肪烃),取出比色管。装入另一根干净的比色管,缓慢加入35 mL二氯甲烷洗脱,收集于比色管,为第二组分T2(芳香烃)。将以上收集的组分,转移到平行浓缩仪,以对应溶剂润洗比色管3次,浓缩至1 mL,上机分析。
1.3.3.3 洗脱溶剂种类
分别用量筒取10 mL正己烷、正戊烷、异辛烷、正庚烷冲洗SPE硅胶小柱,弃去洗脱液。分别取1 mL净化液上样,以常压下自然流速进行洗脱。分别收集正己烷、正戊烷、异辛烷、正庚烷洗脱液,关阀,为第一组分T1(脂肪烃),取出比色管封口。装入另一根干净的比色管,缓慢加入 35 mL二氯甲烷洗脱,收集于比色管,为第二组分T2(芳香烃)。将以上收集的组分,转移到平行浓缩仪,以对应溶剂润洗比色管3次,浓缩至1 mL,上机分析。
1.4 仪器分析条件
气相色谱仪带有分流/不分流进样口,可程序升温,具有氢火焰离子化检测器。色谱柱为石英毛细管色谱柱,30 m×0.32 mm×0.25 μm,固定相为5%苯基-95%甲基聚硅氧烷。进样口温度为 300 ℃,不分流,初始温度50 ℃,保持2 min,以 40 ℃/min的速率升至230 ℃,以20 ℃/min升至 320 ℃,保持20 min,进样量1 μL,检测器温度 320 ℃,载气流速1.5 mL/min,氢气空气流量为40∶400 mL/min。
1.5 计算结果表示
能够被正己烷等溶剂提取且不被硅酸镁吸附,在气相色谱图上保留时间介于正癸烷(包含)与正四十烷(包含)之间的有机化合物。定性从正癸烷出峰开始,到正四十烷出峰结束连接一条水平基线进行积分。定量以浓度为横坐标,以确定的保留时间窗内总峰面积为纵坐标,建立校准曲线,芳香烃组分以等浓度的16种多环芳烃为代表组分进行定量,脂肪烃组分则以等浓度的31种正构烷烃为代表组分进行定量。
2 结果与讨论
2.1 分离柱洗脱压力
分离柱洗脱采用常压(0.1 MPa)、负压(-0.08 MPa)、加压(0.4 MPa)3种洗脱压力,将浓缩净化液经SPE硅胶小柱洗脱分离,检测结果见图1。常压(0.1 MPa)为最优洗脱压力条件,该条件下土壤中脂肪烃、芳香烃的效果最佳,平均回收率分别达到123%、107%;常压条件下洗脱速度缓慢,洗脱过程接近平推流洗脱模型(平推流模型是指流体在柱内以均匀流速向前推进,可实现组分高效分离),能够有效实现脂肪烃和芳香烃的分离。真空方式形成负压(-0.08 MPa)条件下,脂肪烃和芳香烃的回收率分别为98.0%、75.2%,可有效分离石油烃中脂肪烃和芳香烃,分离效果优于加压(0.4 MPa)条件(脂肪烃和芳香烃的回收率仅57.8%、42.5%)。加压条件下回收率偏低,推测因柱头压力过大导致洗脱流速过快,脂肪烃和芳香烃在SPE硅胶小柱上吸附-解析平衡未充分建立,进而造成洗脱、分离不完全。针对常压下脂肪烃回收率超100%的现象,可能由基质效应(土壤基质中干扰组分与目标物共洗脱)、实验系统误差或仪器响应偏差等因素导致,该现象在土壤等复杂基质的固相萃取检测中较为常见。
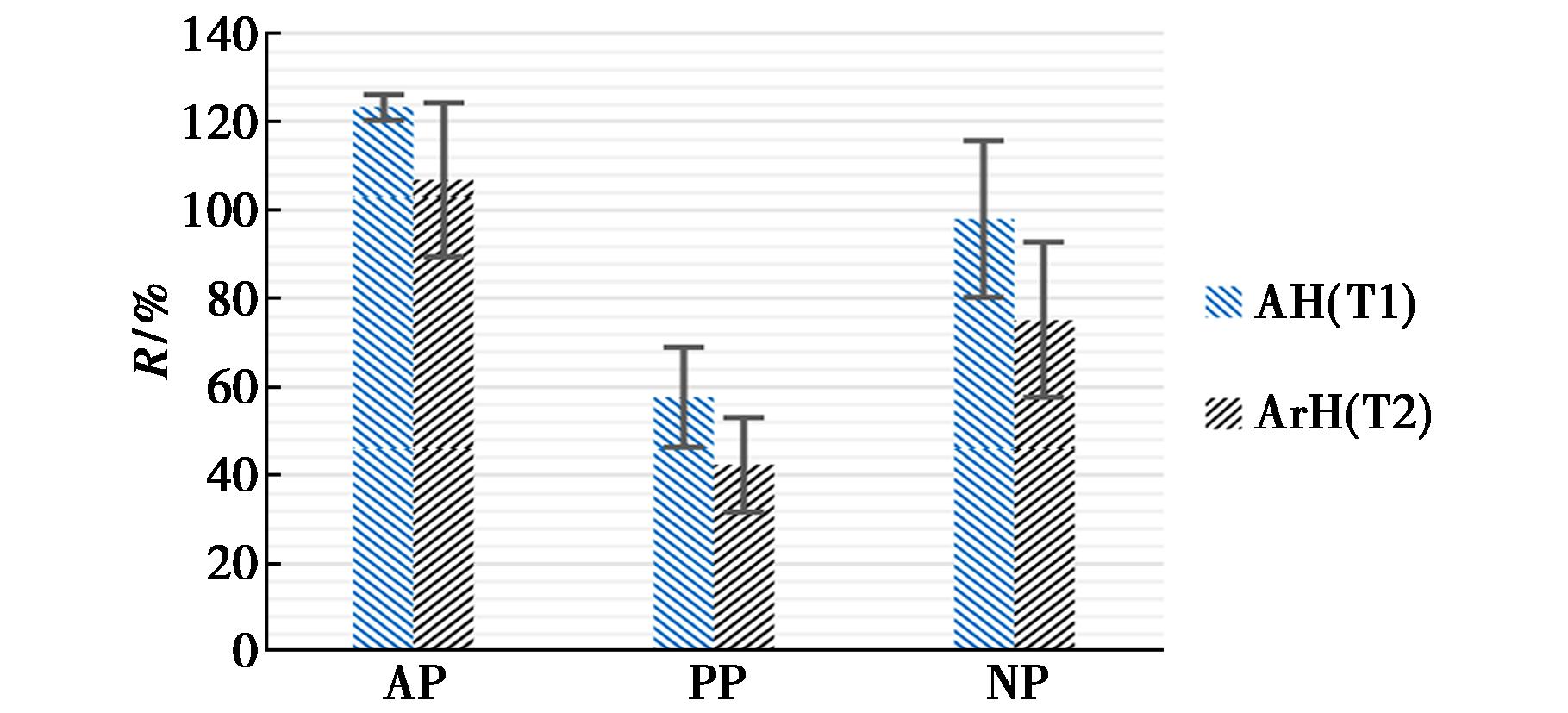
图1 洗脱压力结果影响图
Fig.1 Effect of elution pressure on separation results
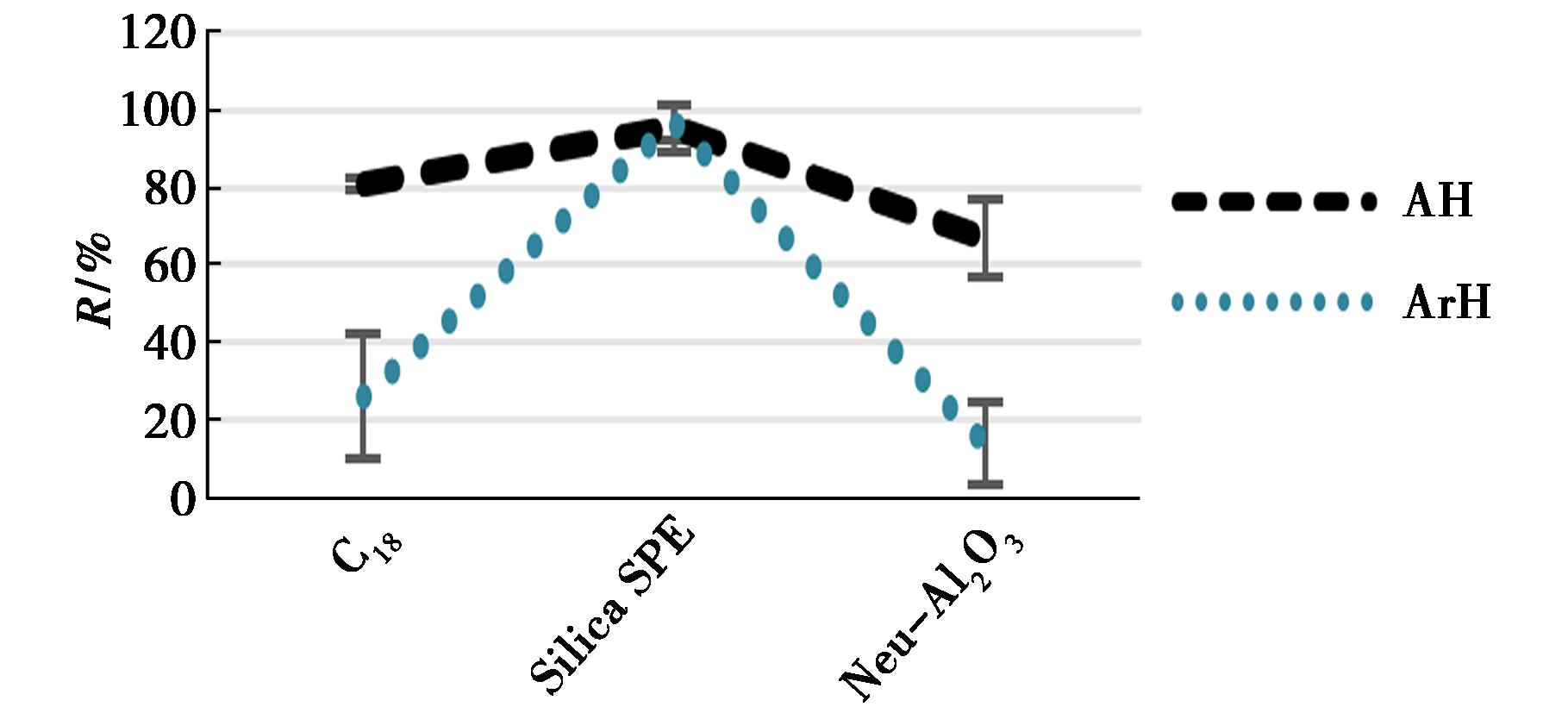
图2 填料类型结果影响图
Fig.2 Effect of packing material types on separation results
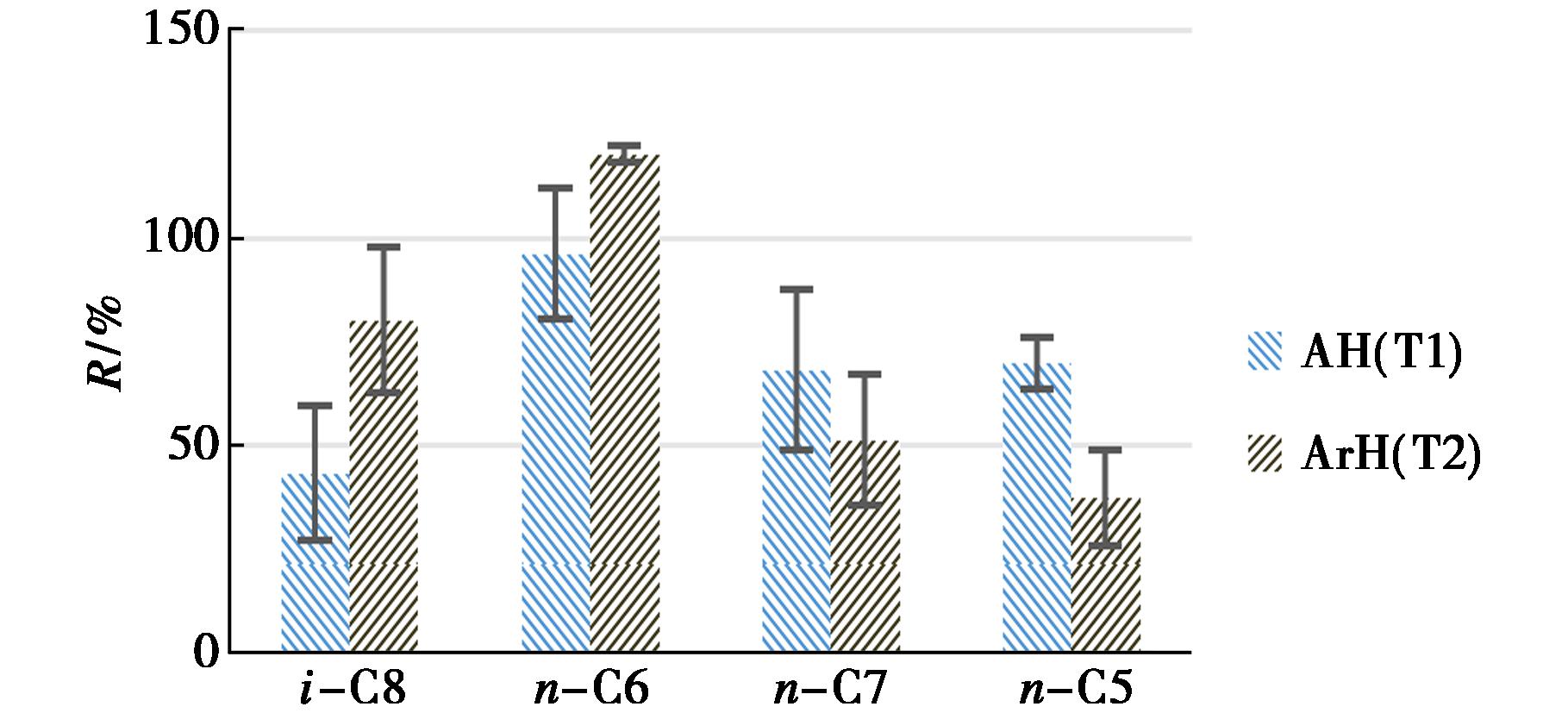
图3 洗脱溶剂结果影响图
Fig.3 Effect of elution solvents on separation results
据SPSS单因素方差分析,结果显示不同分离柱压力对脂肪烃回收率影响存在极显著差异(p<0.01),对芳香烃回收率影响存在显著差异(p<0.05),说明洗脱压力是影响SPE硅胶小柱分离土壤中脂肪烃和芳香烃效果的关键因素。
2.2 分离柱填料种类
土壤石油烃经硅酸镁柱净化去除基质干扰后,采用SPE硅胶小柱、C18小柱、中性氧化铝小柱3种不同填料的固相萃取柱,开展脂肪烃与芳香烃组分的分离实验,结果表明SPE硅胶小柱为最优分离填料。
SPE硅胶小柱可实现石油烃中脂肪烃与芳香烃的有效分离,二者平均回收率分别为95.4%、96.8%。其分离机制主要基于硅胶表面的孔隙吸附作用、表面酸中心作用以及与芳香烃之间π键相互作用差异,从而实现脂肪烃和芳香烃分离。C18小柱对石油烃中的脂肪烃和芳香烃的分离效果不佳,脂肪烃回收率为81.2%,但芳香烃回收率仅26.3%,C18小柱填料以强疏水相互作用为核心保留机制,通过氢键亲和力作用保留目标物,短链烷烃易与C18表面的疏水基团竞争结合,将吸附的芳香烃置换洗脱,导致两组分无法实现完全分离。中性氧化铝小柱同样未能实现脂肪烃和芳香烃的有效分离,中性氧化铝具备碱性特性,可通过物理吸附作用保留烃类物质,且其表面金属阳离子可与芳香烃的π电子体系形成π-阳离子配合作用,增强对芳香烃的吸附;但由于脂肪烃和芳香烃分子极性、疏水性等理化性质相近,二者在中性氧化铝表面的吸附-解吸行为差异较小,难以实现有效分离。
据SPSS单因素方差分析,结果显示不同分离柱填料对脂肪烃回收率影响存在显著差异(p<0.05),对芳香烃回收率影响存在极显著差异(p<0.01),表明填料类型是影响石油烃中脂肪烃与芳香烃分离效果的关键因素。
2.3 洗脱溶剂种类
土壤石油烃经硅酸镁净化柱去除基质干扰后,以正己烷、正戊烷、异辛烷和正庚烷为洗脱溶剂,探讨溶剂极性、粘度和沸点对脂肪烃和芳香烃组分分离洗脱效果的影响。实验结果表明,4种溶剂均能实现石油烃中的脂肪烃和芳香烃的有效分离。溶剂极性排序为正庚烷>异辛烷>正己烷>正戊烷,其中正己烷洗脱效果最优,回收率最高,脂肪烃与芳香烃回收率分别达96.5%、120%。极性偏低的正戊烷-二氯甲烷组合与极性偏高正庚烷-二氯甲烷组合,洗脱芳香烃组分回收率均较低,分别仅为37.7%、51.5%,异辛烷的洗脱结果亦表明了溶剂极性过高或过低均会影响石油烃的分离回收率。
据SPSS分组显著性分析结果显示,不同溶剂体系下芳香烃回收率存在极显著差异(p<0.01);而脂肪烃回收率无显著差异(p=0.1>0.05)。
3 方法质量控制
3.1 校准曲线与检出限
样品分析过程中因柱流失出现基线上升,绘制校准曲线时,各浓度点的总峰面积均扣除柱流失峰面积校正。在实验设定的浓度范围内,脂肪烃和芳香烃的分析方法均表现出良好的线性关系,相关系数均大于0.996;以低浓度出峰点信噪比S/N=10∶1计算方法检出限,其中芳香烃为 1.7 ng、脂肪烃为0.27 ng,该检出限水平可满足检测需求。
表1 芳香烃校准曲线
Tab.1 Calibration curve of aromatic hydrocarbon
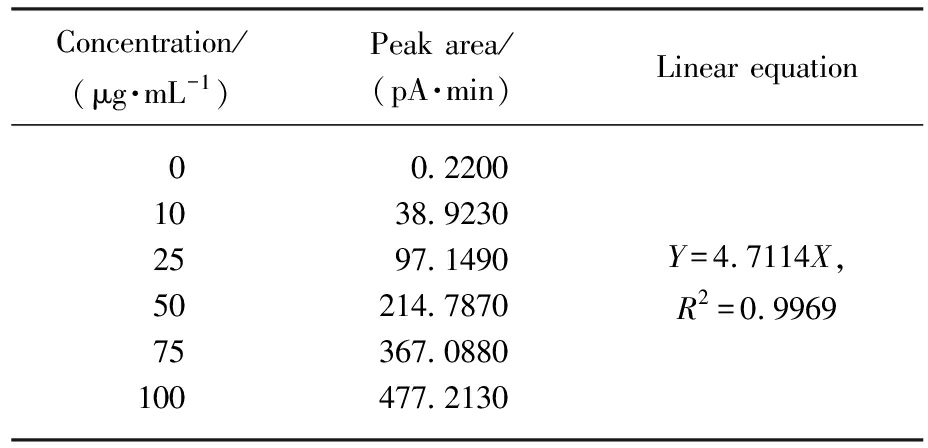
Concentration/(μg·mL-1)Peak area/(pA·min)Linear equation0102550751000.220038.923097.1490214.7870367.0880477.2130Y=4.7114X,R2=0.9969
表2 脂肪烃校准曲线
Tab.2 Calibration curve of aliphatic hydrocarbon
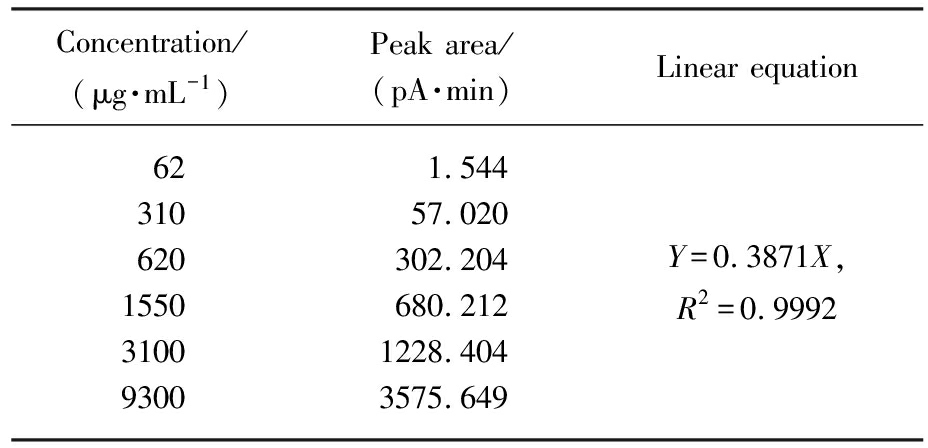
Concentration/(μg·mL-1)Peak area/(pA·min)Linear equation623106201550310093001.54457.020302.204680.2121228.4043575.649Y=0.3871X,R2=0.9992
3.2 方法精密度与回收率
选取石英砂作为本底基质,向其中分别添加50 μg的16种多环芳烃标准溶液、50 μg石油烃标准溶液(对应31种正构烷烃总浓度为1550 μg/mL),经实验前处理流程处理后,所得到目标物结果回收率范围为80.9%~95.3%,相对标准偏差范围为1.11%~11.2%,各项指标均满足分析检测要求。
4 结论
通过系统优化压力、净化与分离填料类型、洗脱溶剂配比等关键参数建立了土壤石油烃中脂肪烃与芳香烃组分的分离纯化的气相色谱分析方法,确定了以丙酮-二氯甲烷混合溶剂为提取试剂、硅酸镁柱净化除杂、SPE硅胶小柱为分离介质、正己烷-二氯甲烷梯度洗脱的技术方案,实现了两类烃类化合物的高效分离与精准定量,具有操作简便、抗基质干扰能力强、分离效果稳定等优势,可满足土壤烃类污染监测、毒性鉴定及风险评估的实际需求。本研究暂未深入探讨不同污染程度土壤样品的前处理参数适配性,后续研究可进一步优化高浓度污染土壤的提取与净化条件,结合GC-MS联用技术实现单体烃的精准定性,同时拓展方法在沉积物、固体废物、地下水等多介质中的应用,为土壤石油烃污染的溯源分析与修复效果评估提供更全面的技术保障。
[1]Mi Y D.China Build.Mater.Sci.Technol.,2015,24(5):92-93.
米亚东.中国建材科技,2015,24(5):92-93.
[2]Chen Y J,Zhang H H,Ma Z H,Wang X Y,Wang J,Xu K.China Resour.Compr.Util.,2025,43(2):139-142.
陈彦君,张怀辉,马祖红,汪新月,王瑾,徐轲.中国资源综合利用,2025,43(2):139-142.
[3]GB 36600—2018.Soil Environmental Quality-Risk Control Standard for Soil Pollution in Construction Land (Trial),2018-08-01.
GB 36600—2018.土壤环境质量 建设用地土壤污染风险管控标准(试行),2018-08-01.
[4]Wei J J,Wang Z S,Tian L,Shao Z G,Nie F,He M.Ecol.Sci.,2025,44(5):280-288.
魏嘉嘉,王占生,田磊,邵志国,聂凡,贺美.生态科学,2025,44(5):280-288.
[5]Feng S,Wu M L,Li Q,Tang S W,Xu H N.Environ.Chem.,2025,44(9):3404-3414.
冯爽,吴蔓莉,李倩,唐诗薇,徐会宁.环境化学,2025,44(9):3404-3414.
[6]He L,Li J,Gao M S,Liu D Y,Zhang Y H,Zhao L,Gao J S,Xu C M.CIESC J.,2025,76(5):1909-1926.
何燎,李俊,高梦舒,刘东阳,张宇豪,赵亮,高金森,徐春明.化工学报,2025,76(5):1909-1926.
[7]Wang Y,Hou Y C,Ren S X,Mo C F,Ji Y A,Wu W Z.China Science Paper Online Excellent Papers,2017,10(1):106-112.
王言,侯玉翠,任树行,么聪菲,纪柚安,吴卫泽.中国科技论文在线精品论文,2017,10(1):106-112.
[8]Liu T,Sun H,Wang X Q,Li J,Zhang Z Q,Wu P,Wang N X,An Q F.Chin.J.Chem.Eng.,2024,69:13-22.
[9]Xu H Y.Guangdong Chem.Ind.,2013,40(12):176-177.
胥红研.广东化工,2013,40(12):176-177.
[10]Li C Q,Jiang J S,Liu L P,Zhao J H,Wu Z Y,Ren Y J.Phy.Test.Chem.Anal.part B:Chem.Anal.,2025,61(2):176-181.
李超群,蒋敬思,刘立平,赵锦华,吴宗源,任颖俊.理化检验-化学分册,2025,61(2):176-181.
[11]Liu L L,Li B N,Yang M Q,Yang M,Wu Y W.Food Ferment.Ind.,2022,48(7):258-263.
刘玲玲,李冰宁,杨梦奇,杨明,武彦文.食品与发酵工业,2022,48(7):258-263.
[12]Ke R H,Yang C Y,Hu X,Xie R L,Yin J J,Song Q H.Chin.J.Anal.Chem.,2018,46(10):1677-1684.
柯润辉,杨春艳,胡雪,谢瑞龙,尹建军,宋全厚.分析化学,2018,46(10):1677-1684.
[13]Li X,Zeng L Y,Wang Q,Cui S Y,Cai L X,Li Y,Bai Z W.Petrol.Process.Petrochem.,2023,54(1):128-134.
李翔,曾令仪,王乾,崔树阳,蔡凌霄,李怿,白正伟.石油炼制与化工,2023,54(1):128-134.
[14]Zhang Q C.Manuf.Autom.,2013,35(1):44-47.
张青春.制造业自动化,2013,35(1):44-47.
[15]Hu F L.Pop.Stand.,2025,(10):148-150.
胡凤玲.大众标准化,2025,(10):148-150.
[16]Tie J C,Liu J,Xiao Y S,Jia L X.Chem.Reagents,2024,46(8):99-106.
铁建成,刘俊,肖远淑,贾丽霞.化学试剂,2024,46(8):99-106.