农药在美国被称之为经济毒剂,在欧洲被称之为农用化学品,在我国,农药是指用于预防、消灭或控制危害农业、林业的病虫草和其他有害生物,以及有目的地调控植物和昆虫生长的化学合成物,或者来源于生物及其他天然物质的一种或几种物质的混合物及其制剂[1]。农药残留(Pesticide Residues)的概念产生于20世纪60年代,通常是指直接或间接使用化学农药以后存在于农作物、生物体和环境中的微量农药单体以及具有独立意义的代谢产物、降解产物和杂质的总和,以每千克样本中有多少毫克(mg/kg)表示。农药能够为农作物的供应带来保证,同时也带来危害健康的农药残留问题[2],农药残留是施药后的必然现象,但如果超过最大残留限量标准,会产生对人畜不良影响或通过食物链对生态系统中的生物造成毒害的风险。
蔬菜、水果中含有人体必需的维生素、膳食纤维和无机盐等[3],是生活必需品也是人们餐桌上必不可少的食材,但为了抑制杂草生长、防止病虫害、调节蔬菜水果的生长发育及提高经济收入,种植过程中不合理使用农药就成了农药残留最大的来源。农药残留的影响和危害具有多面性,长期食用含有农药残留的食品可能引起慢性中毒或者产生致癌、致畸和致突变的效应;另一方面,不合理使用农药尤其是土壤中除草剂的残留会导致药害事故频繁,引起大面积减产甚至绝产,对农业生产造成严重影响;此外,许多国家以农药残留限量作为技术性贸易措施限制农产品食品的进口,保护本国农业生产,给农业、农产品、食品输出国的国际贸易带来巨大的影响[4]。因此,在农产品的农残检测中,准确可靠的检测结果是正确评价和保证食品安全性的先决条件,是国家贸易公平交易的有效凭证。
目前,发达国家农药残留检测技术逐步趋向高技术化、系列化、快速化和便携化,为缩短样品检测周期,样品处理技术近年来发展迅速,与传统前处理技术相比,新型样品前处理技术更加简便快捷,并逐步实现了自动化,与此同时,先进的检测设备和检测技术不断涌现,色谱技术[5]、色谱-质谱联用技术[6]的应用推动农药残留检测技术向着高通量、高灵敏度和高准确度方向发展[7],从而被广泛应用于农残检测的各个领域[8]。其中,QuEChERS前处理技术因快速、简便、低成本等优势被广泛应用[3],2003年,QuEChERS技术由美国科学家Lehotay及德国Anastassiades教授首次提出[3,9],其核心流程包括样品提取、盐析相分离和提取液净化,在多数处理中,QuEChERS技术后常需旋蒸、氮吹等浓缩步骤[10-14]等,在净化后又取2 mL上清液40 ℃或氮吹或旋蒸后复溶上机,易造成目标化合物损失的同时,延长了样品处理时间;检测技术方面,张军忠[14]采用气相色谱-单四极杆质谱仪的SIM模式检测柑橘类水果中的农药残留,证实了气质联用法的高分辨率、高灵敏度和高特异性优势,单四极杆气相色谱-质谱联用仪的选择离子监测(SIM)模式虽可满足常规检测需求,但在复杂基质样品的痕量分析中抗干扰能力有限,而MRM模式[15]具有极强的抗干扰能力,此工作模式能有效地减少了其他离子对其的干扰,降低本底噪音值,具有极强的抗干扰能力以及高灵敏度和高通量离子传输效率等特点,能保证待分析物能被准确定性、定量检测而特别适用于分析基质复杂、干扰因素多且目标化合物含量极低的样品,已为痕量检测的优选方法[16]。
青藏高原地区生态环境特殊,农产品种植体系独特,但针对该区域的多类别农药残留同步检测技术尚属空白,现有检测方法难以适配高原地区果蔬基质特性。近年来,西宁市已构建市-县-乡-基地四级果蔬农残监管检测体系,推行“证码合一”溯源模式,农残合格率稳定在99.7%以上,且常态化开展农残专项整治,但仍面临小散农户用药管控难、基层检测能力不足、省外果蔬溯源链条易断裂等现实挑战,农残超标问题偶有发生,果蔬质量安全保障尚存短板,本研究的开展可精准破解当地监管痛点,兼具显著的现实必要性与针对性。本研究选取的13种农药均为西宁本地果蔬种植常用品类,且是适于气相色谱质谱法检测的化合物,覆盖主要农残类型,契合高原病虫害防控需求与国家监管重点,适配本地检测能力,能精准反映当地监管薄弱环节,为监管优化提供靶向科学支撑。基于此,本研究以青海省西宁市市售果蔬为研究对象,采用改良的前处理技术结合MRM模式,建立13种多类别农药残留的同步检测方法。该方法无需浓缩步骤,可减少目标物损失,且MRM模式通过两级离子筛选显著提升抗干扰能力,实现“高灵敏、广覆盖、强抗扰、快响应”的检测目标。研究成果以低成本、易推广的优势,为青藏高原农产品质量安全与绿色发展提供核心技术支撑,这也是本研究的核心价值与新颖性所在。
1 实验部分
1.1 主要仪器与试剂
8890+7000D型气相色谱-质谱联用仪(带70 eV电子轰击源,配备HP-5MS UI型色谱柱,15 m×250 μm×0.25 μm,带柱中反吹,美国Agilent公司);TDZ5-WS型离心机(最高转速5000 r/min,湖南湘仪实验室仪器开发有限公司);16位强力多管涡旋混匀仪(最高转速3000 r/min,江苏海门市其林贝尔仪器制造有限公司)。
乙腈(色谱纯,美国Merck公司);盐包(4 g硫酸镁、1 g氯化钠、1 g柠檬酸钠、0.5 g柠檬酸氢二钠,分装于15 mL聚丙烯管中)、净化包(150 mg无水硫酸镁、25 mg乙二胺-N-丙基硅烷化硅胶(PSA),分装于15 mL离心管中)(上海安谱实验科技股份有限公司);13种农药混合标准物质(浓度100 μg/mL,带标准物质证书,有效期内,北京坛墨质检科技股份有限公司);实验用水为超纯水,由密理博纯水机制备。
1.2 实验方法
1.2.1 样品采集与前处理
此次研究分别于2024年4月、9月在西宁市五区两县的商店和农贸市场采集当地市售蔬菜共计29份(品种有:莴苣、辣椒、甜椒、黄瓜、苦瓜、结球甘蓝、芦笋、菜心、茄子、芹菜、油麦菜、青花菜等)、水果15份(品种有:草莓、桑葚、蓝莓、杨梅、阳光玫瑰葡萄、猕猴桃、苹果、树莓、桃子等),经过基质固相分散技术处理后对其浸提液用MRM模式检测其中氧乐果、毒死蜱、水胺硫磷、三唑磷、灭线磷、乙酰甲胺磷、甲胺磷、乐果、氯氟氰菊酯、硫丹及其代谢物(α-硫丹、β-硫丹、硫丹硫酸酯)、五氯硝基苯、百菌清等13种农药残留量。
前处理过程见图1。

图1 样品前处理过程
Fig.1 Sample pretreatment process
1.2.2 检测与验证方法
仪器条件和色谱条件:进样口温度280 ℃,不分流进样;前级色谱柱流量1.0 mL/min,后级色谱柱流量1.2 mL/min;进样量1 μL;传输线温度280 ℃;载气为氦气,碰撞气为氮气;升温程序:60 ℃保持1 min,然后以40 ℃/min升温至 120 ℃,再以5 ℃/min升温至310 ℃,保持5 min。
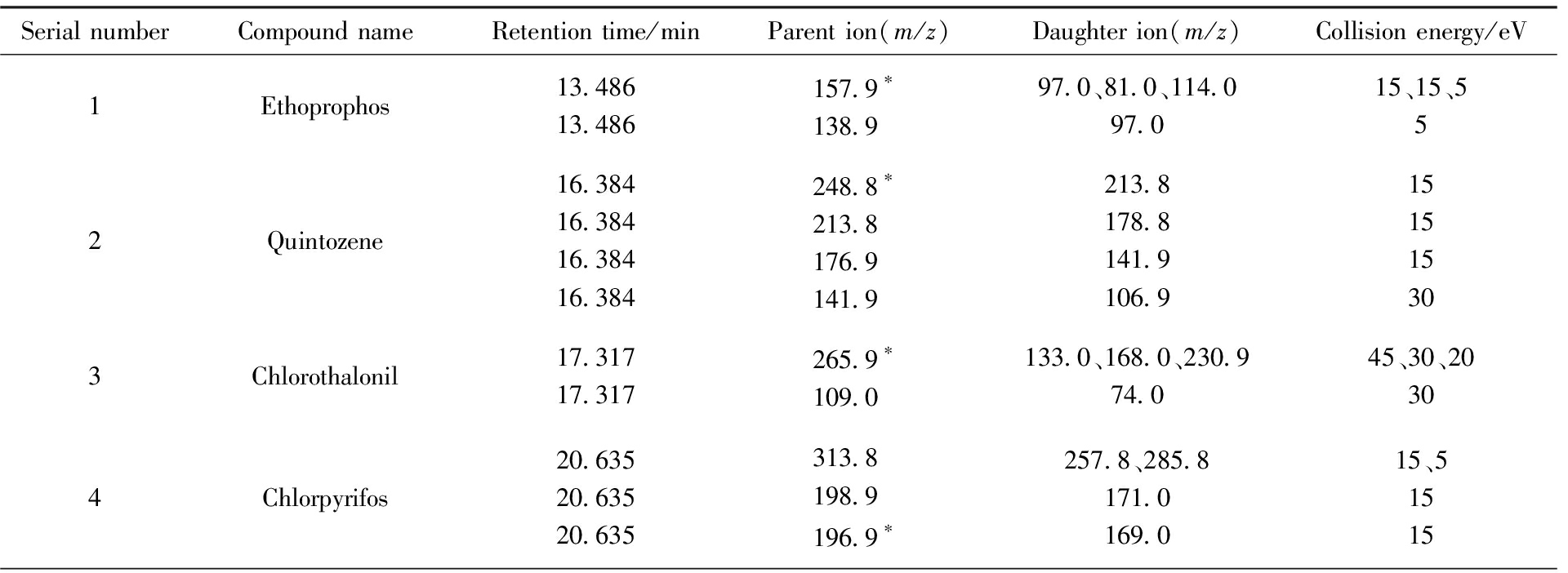
质谱条件:离子源温度230 ℃,四极杆温度150 ℃;离子化能量70 eV;溶剂延迟3 min;扫描模式为MRM模式,各化合物保留时间及特征离子信息见表1。
表1 各化合物保留时间及特征离子信息注
Tab.1 Retention time and characteristic ion information of each compound
Serial numberCompound nameRetention time/minParent ion(m/z)Daughter ion(m/z)Collision energy/eV1Ethoprophos13.48613.486157.9∗138.997.0、81.0、114.097.015、15、552Quintozene16.38416.38416.38416.384248.8∗213.8176.9141.9213.8178.8141.9106.9151515303Chlorothalonil17.31717.317265.9∗109.0133.0、168.0、230.974.045、30、20304Chlorpyrifos20.63520.63520.635313.8198.9196.9∗257.8、285.8171.0169.015、51515
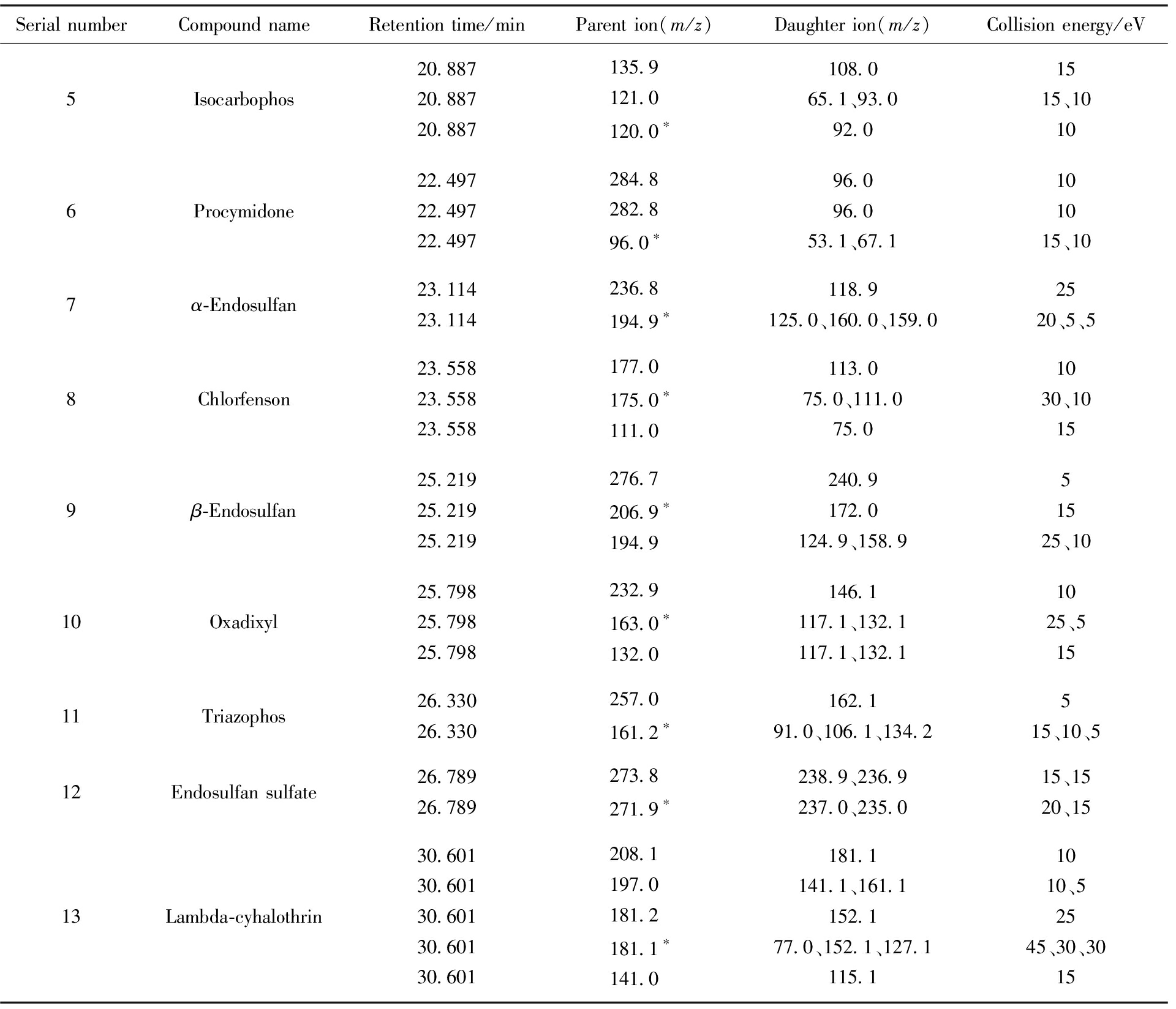
续表
Serial numberCompound nameRetention time/minParent ion(m/z)Daughter ion(m/z)Collision energy/eV5Isocarbophos20.88720.88720.887135.9121.0120.0∗108.065.1、93.092.01515、10106Procymidone22.49722.49722.497284.8282.896.0∗96.096.053.1、67.1101015、107α-Endosulfan23.11423.114236.8194.9∗118.9125.0、160.0、159.02520、5、58Chlorfenson23.55823.55823.558177.0175.0∗111.0113.075.0、111.075.01030、10159β-Endosulfan25.21925.21925.219276.7206.9∗194.9240.9172.0124.9、158.951525、1010Oxadixyl25.79825.79825.798232.9163.0∗132.0146.1117.1、132.1117.1、132.11025、51511Triazophos26.33026.330257.0161.2∗162.191.0、106.1、134.2515、10、512Endosulfan sulfate26.78926.789273.8271.9∗238.9、236.9237.0、235.015、1520、1513Lambda-cyhalothrin30.60130.60130.60130.60130.601208.1197.0181.2181.1∗141.0181.1141.1、161.1152.177.0、152.1、127.1115.11010、52545、30、3015
注:表1中*标注的为定量离子,其余为定性离子。
标准曲线绘制:以苹果基质配制标准工作曲线,浓度点依次为10、20、50、100、200、500 μg/L,采用外标法定量。
方法验证:考察方法的基质效应关系(ME)、线性关系(R2)、检出限(LOD)、精密度(RSD)和回收率,验证结果见表2、表3,典型谱图见图2。
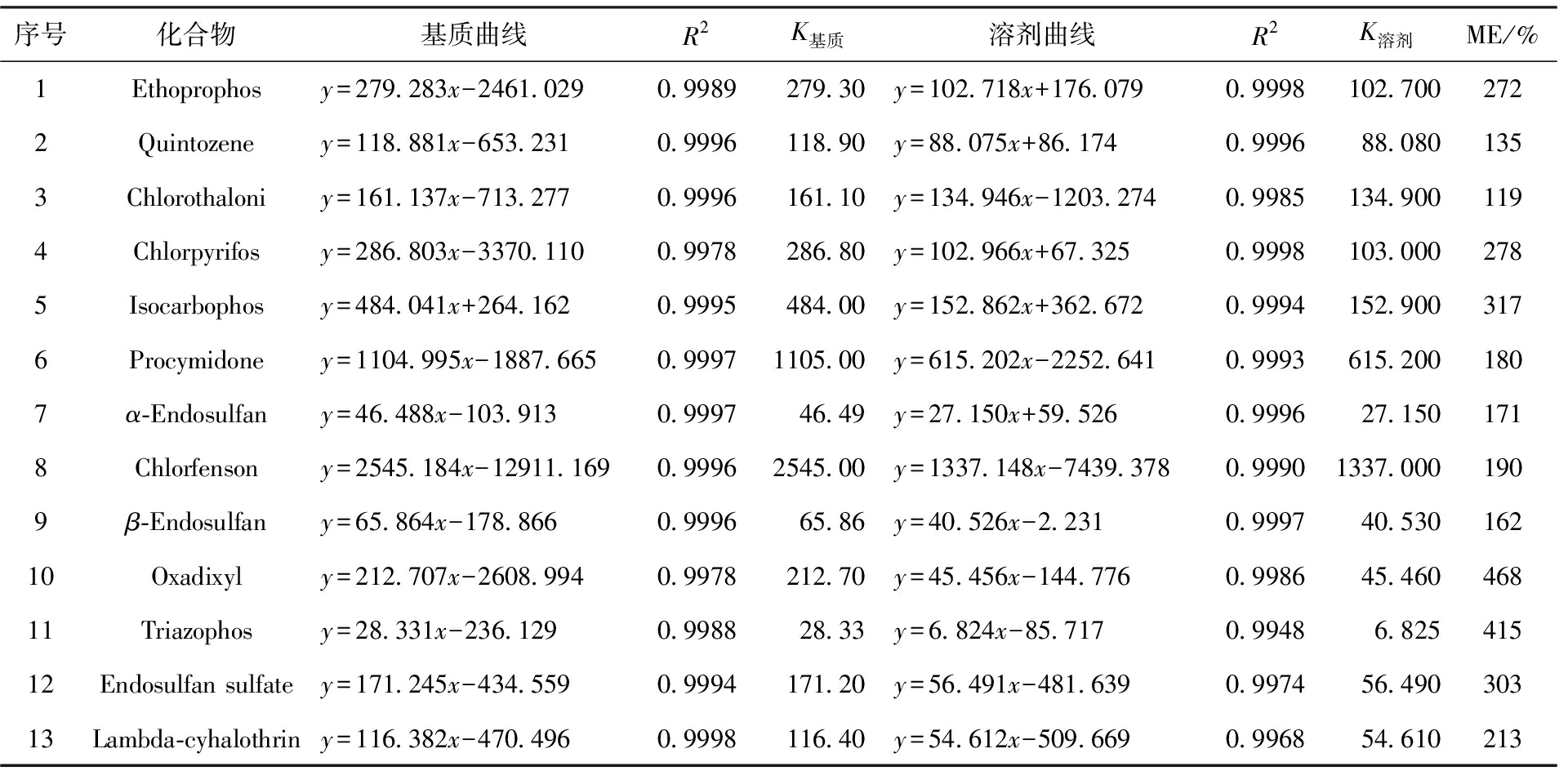
表2 基质效应情况
Tab.2 Results of matrix effects
序号化合物基质曲线R2K基质溶剂曲线R2K溶剂ME/%1Ethoprophosy=279.283x-2461.0290.9989279.30y=102.718x+176.0790.9998102.7002722Quintozeney=118.881x-653.2310.9996118.90y=88.075x+86.1740.999688.0801353Chlorothaloniy=161.137x-713.2770.9996161.10y=134.946x-1203.2740.9985134.9001194Chlorpyrifosy=286.803x-3370.1100.9978286.80y=102.966x+67.3250.9998103.0002785Isocarbophosy=484.041x+264.1620.9995484.00y=152.862x+362.6720.9994152.9003176Procymidoney=1104.995x-1887.6650.99971105.00y=615.202x-2252.6410.9993615.2001807α-Endosulfany=46.488x-103.9130.999746.49y=27.150x+59.5260.999627.1501718Chlorfensony=2545.184x-12911.1690.99962545.00y=1337.148x-7439.3780.99901337.0001909β-Endosulfany=65.864x-178.8660.999665.86y=40.526x-2.2310.999740.53016210Oxadixyly=212.707x-2608.9940.9978212.70y=45.456x-144.7760.998645.46046811Triazophosy=28.331x-236.1290.998828.33y=6.824x-85.7170.99486.82541512Endosulfan sulfatey=171.245x-434.5590.9994171.20y=56.491x-481.6390.997456.49030313Lambda-cyhalothriny=116.382x-470.4960.9998116.40y=54.612x-509.6690.996854.610213
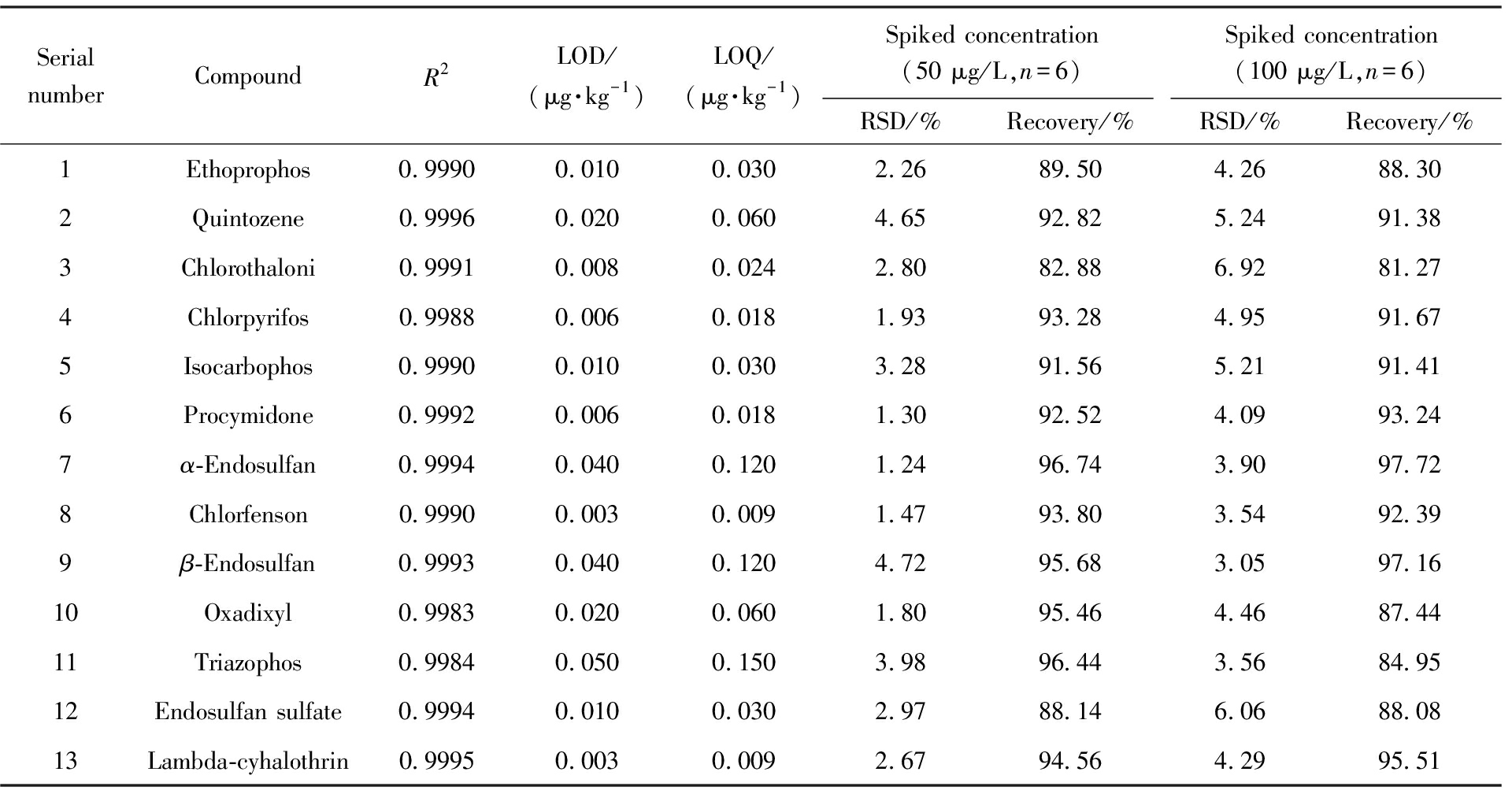
表3 方法验证情况
Tab.3 Method validation results
Serial numberCompoundR2LOD/(μg·kg-1)LOQ/(μg·kg-1)Spiked concentration(50 μg/L,n=6)Spiked concentration(100 μg/L,n=6)RSD/%Recovery/%RSD/%Recovery/%1Ethoprophos0.99900.0100.0302.2689.504.2688.302Quintozene0.99960.0200.0604.6592.825.2491.383Chlorothaloni0.99910.0080.0242.8082.886.9281.274Chlorpyrifos0.99880.0060.0181.9393.284.9591.675Isocarbophos0.99900.0100.0303.2891.565.2191.416Procymidone0.99920.0060.0181.3092.524.0993.247α-Endosulfan0.99940.0400.1201.2496.743.9097.728Chlorfenson0.99900.0030.0091.4793.803.5492.399β-Endosulfan0.99930.0400.1204.7295.683.0597.1610Oxadixyl0.99830.0200.0601.8095.464.4687.4411Triazophos0.99840.0500.1503.9896.443.5684.9512Endosulfan sulfate0.99940.0100.0302.9788.146.0688.0813Lambda-cyhalothrin0.99950.0030.0092.6794.564.2995.51
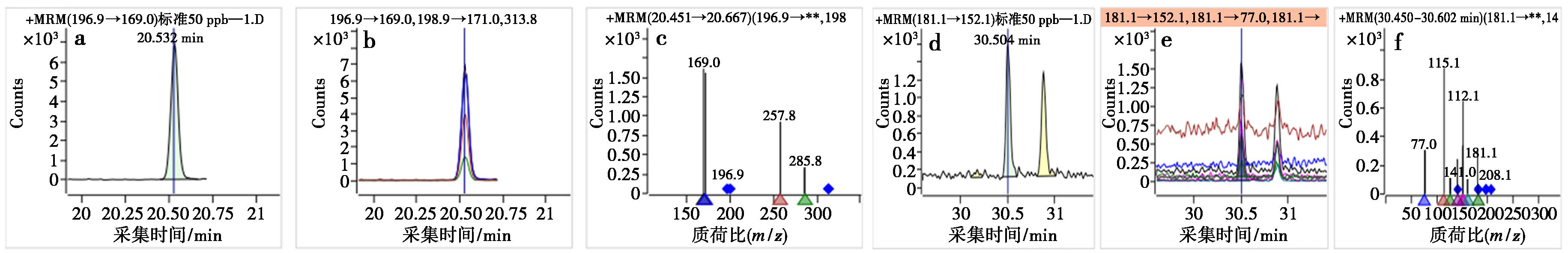
a~c分别为毒死蝉的定量离子对、定性离子对、特征离子质谱图;d~f分别为氯氟氰聚酯的定量离子对、定性离子对、特征离子质谱图
图2 典型谱图
Fig.2 Typical chromatogram
2 结果与讨论
2.1 前处理方法优化
食品中农药残留分析通常需经过样品制备、提取、净化、分离检测和综合分析等步骤,有效的样品前处理是所有步骤的前提,50%的检测误差来源于样品前处理过程[1]。理想的前处理方法应满足萃取完全、净化有效、操作简便、环保安全等要求。传统样品前处理技术如溶剂萃取法、液-液分配法和柱色谱法,存在操作繁琐、耗时较长、溶剂用量大等不足。近年来,固相萃取、固相微萃取、基质固相分散技术及QuEChERS等新型前处理技术得到广泛应用。本研究采用优化的前处理技术,以乙腈为提取剂,结合成品盐包和净化包完成提取与净化。样品经乙腈提取、盐包盐析离心后,取上清液直接加入净化包净化,再次离心后即可吸取上清液上机检测,无需旋蒸、氮吹等浓缩步骤。该改良方法具有以下优势:一是操作简便快速,大幅缩短了前处理周期;二是样品全程处于密闭环境中,有效避免了目标化合物的挥发损失,尤其利于低含量农药残留的检出;三是采用成品盐包和净化包,减少了实验人员操作差异带来的系统误差,提高了方法的重现性;四是净化离心后的直接上样,避免了因氮吹过程中易挥发化合物的损失。方法验证结果显示,13种农药的回收率为81.27%~97.72%,RSD为1.24%~6.92%,表明该前处理方法的提取效率和净化效果良好,可满足检测需求。
2.2 MRM模式检测优势
气相色谱-质谱联用技术通过气相色谱的高效分离与质谱的高灵敏度检测相结合,已成为农药残留检测的核心技术之一。此次MRM模式的核心优化是“特异性离子对的筛选与验证”,在全扫的基础上确定各化合物的母离子,再选择合适的碰撞电压确定各母离子的子离子,得到优化的MRM方法。结合检测结果,两组及以上离子对(母离子→子离子)的选择,确保在复杂果蔬基质中,可更好的准确辨认化合物,使结果更为准确,这也是本文能有效规避基质干扰、保证检测准确性的关键。其次,从表2基质效应的分析情况来看,80%以上化合物的ME(%)>150%,结合基质工作曲线,MRM模式更能有效消除基质成分对目标分析物检测响应的干扰,保证复杂基质样品定量结果的准确性、可靠性与合规性,与结果中81.27%~97.72%的回收率相匹配,另外,选取的离子对经方法验证后,RSD<7%,且检出限低于GB 2763—2021《食品安全国家标准 食品中农药最大残留限量》[17]标准限值(如毒死蜱检出限远低于0.1 mg/kg),结合上述分析,较SIM模式更能满足检测要求。
2.3 结果检测的选择及优化
农药种类繁多,根据防治对象可分为杀虫剂、杀菌剂、除草剂等,根据化学结构可分为有机磷类、有机氯类、拟除虫菊酯类、氨基甲酸酯类等。传统检测方法中,不同类别农药因化学性质差异需采用不同的检测方法和检测器,如有机氯类农药常用电子捕获检测器(ECD)检测,有机磷类农药常用火焰光度检测器(FPD)或氮磷检测器(NPD)检测,拟除虫菊酯类农药可采用ECD或液相色谱法检测。这种“一类一检”的模式操作繁琐、检测效率低、检测成本高,难以满足批量样品多类别农药残留同步筛查的需求。
本研究通过优化色谱和质谱条件,建立了可同步检测13种多类别农药残留的方法,涵盖有机磷类(毒死蜱、水胺硫磷、三唑磷、灭线磷)、有机氯类(α-硫丹、β-硫丹、硫丹硫酸酯、杀螨酯)、拟除虫菊酯类(氯氟氰菊酯)及杀菌剂(腐霉利、五氯硝基苯、百菌清、恶霜灵)。通过优化升温程序和MRM离子对参数,13种农药实现了有效分离,保留时间稳定(表1),无明显干扰峰。方法验证结果显示,所有农药的线性关系良好(R2≥0.9983),精密度和回收率均符合检测标准要求。该方法突破了传统“一类一检”的局限,实现了多类别农药的同步检测,大幅提高了检测效率,降低了检测成本,为批量果蔬样品的农药残留筛查提供了高效可行的技术方案。
3 结论
农药残留问题已成为全球关注的食品安全焦点,不仅威胁人类健康,还影响农产品国际贸易。蔬菜和水果作为日常生活必需品,其农药残留检测是保障食品安全的关键环节。随着我国农药残留最大限量标准的不断严格和相关法规的逐步完善,对农药残留检测技术提出了更高的要求,亟需开发通用性强、准确性高、稳定性好且易于推广的检测方法
本研究围绕建立西宁市果蔬农药残留高效检测方法、提升监管水平的核心目的,采用基质固相分散前处理技术结合气质联用MRM模式,对西宁市五区两县多品类果蔬中13种农药残留进行检测,结合检测结果,对方法关键参数进行回顾性分析,明确方法实用性与可靠性。本方法线性范围为0~5 mg/kg,覆盖果蔬中农药残留常规检出浓度区间,相关系数R2介于0.9983~0.9996之间,表明目标农药浓度与检测响应值线性关联显著,定量准确性强;检出限低至0.003~0.050 μg/kg,定量限为0.009~0.15 μg/kg,具备优异的痕量检测能力,可有效捕捉低含量农药残留;加标浓度50、100 μg/L时,回收率分别达82.88%~96.74%、81.27%~97.72%,精密度分别为1.24%~4.72%、3.05%~6.92%,均符合农药残留检测技术规范,证实方法稳定性与准确性良好。
QuEChERS技术简化了前处理流程,无需浓缩步骤,搭配MRM模式的两级离子筛选优势,有效降低基质干扰,适配西宁多品类果蔬检测需求,成功填补青藏高原地区相关检测技术空白。但本方法仍有局限,仅检测13种农药,且缺乏高浓度点的回收与精密度数据分析,有待后续进一步完善。总之,该方法各项参数表现优良,操作简便、检测高效,为当地农产品质量安全监管提供了核心技术工具,也为我国高原地区农产品绿色发展和国际贸易提供了技术保障,对推动农业可持续发展具有重要意义,未来可进一步扩展检测农药种类、完善MRM离子对数据库,深入研究高原环境对检测方法的影响并优化条件,结合QuEChERS自动样品制备系统实现前处理自动化,提升检测效率。
[1]黄志强.食品中农药残留检测指南.北京:中国标准出版社,2010.
Huang Z Q.Guidelines for Detection of Pesticide Residues in Food.Beijing:China Standards Press,2010.
[2]Chen H Q,Liu J,Lan M Z.Light Ind.Sc.Technol.,2017,33(6):4-6;29.
陈惠琴,刘佳,蓝梦哲.轻工科技,2017,33(6):4-6;29.
[3]Gao R,Zhang W B,Wu Y H,Luan R J,Luan Y J.Phy.Test.Chem.Anal.part B:Chem.Anal.,2024,60(7):668-673.
高冉,张文波,吴义华,栾日坚,栾玉姣.理化检验-化学分册,2024,60(7):668-673.
[4]Sun Z Y,Bao Y,Zhang F L,Su T W.Food Sci.Technol.,2025,50(7):172-174.
孙正阳,包颖,张发玲,苏天伟.食品科技,2025,50(7):172-174.
[5]NY/T 761—2008.Determination of Multiple Residues of Organophosphorus,Organochlorine,Pyrethroid and Carbamate Pesticides in Vegetables and Fruits,2008-04-30.
NY/T 761—2008.蔬菜和水果中有机磷、有机氯、拟除虫菊酯和氨基甲酸酯类农药多残留的测定,2008-04-30.
[6]NY/T 1380—2007.Determination of 51 Pesticide Residues in Vegetables and Fruits-Gas Chromatography-Mass Spectrometry,2007-09-01.
NY/T 1380—2007.蔬菜、水果中51种农药多残留的测定 气相色谱-质谱法,2007-09-01.
[7] Lei D D,Song P Y,Xu Q B,Wang J B,Kong W J.Chin.J.Anal.Lab.,2024,43(10):1505-1512.
雷豆豆,宋鹏悦,徐青斌,王伽伯,孔维军.分析试验室,2024,43(10):1505-1512.
[8]Yang B J.China Food Saf.Mag.,2021,36:90-91.
杨宝娟.食品安全导刊,2021,36:90-91.
[9]Wen X,Tan S H,Lin Q C,Lin X Z,Li X P,Ye S M.J.Anal.Sci.,2024,40(3):323-336.
温馨,谭淑铧,林庆昶,林小贞,黎小鹏,叶少媚.分析科学学报,2024,40(3):323-336.
[10]Xiang W.Cereal Feed Ind.,2025,(6):120-124.
相薇.粮食与饲料工业,2025,(6):120-124
[11]Wang Q.Modern Food,2025,(22):202-204.
王倩.现代食品,2025,(22):202-204
[12]Yan Y.Chin.J.Food Saf.,2023,(15):105-108;114.
闫玉.食品安全导刊,2023,(15):105-108;114
[13]Jing Z,Liu C,Liu X B.Mod.Flour Milling Ind.,2020,34(4):22-25.
景赞,刘超,刘晓碧.现代面粉工业,2020,34(4):22-25.
[14]Zhang J Z.Brand Stand.,2024,(4):7-9.
张军忠.品牌与标准化,2024,(4):7-9.
[15]GB 23200.113—2018.National Food Safety Standard-Determination of 208 Pesticides and Their Metabolites in Plant-Derived Foods-Gas Chromatography-Mass Spectrometry,2018-12-21.
GB 23200.113—2018.食品安全国家标准 植物源性食品中208种农药及其代谢物残留量的测定 气相色谱-质谱联用法,2018-12-21.
[16]Ji Z L.Research on Rapid Screening Method of Multiple Pesticide Residues in Fruits and Vegetables Based on GC-MS/MS Combined with Database.Chengdu:Sichuan Agricultural University,2020.
吉政霖.基于GC-MS/MS结合数据库建立水果和蔬菜中多种农残快筛方法的探究.成都:四川农业大学,2020.
[17]GB 2763—2021.National Food Safety Standard——Maximum Residue Limits for Pesticides in Food,2021-09-03.
GB 2763—2021.《食品安全国家标准 食品中农药最大残留限量》,2021-09-03.