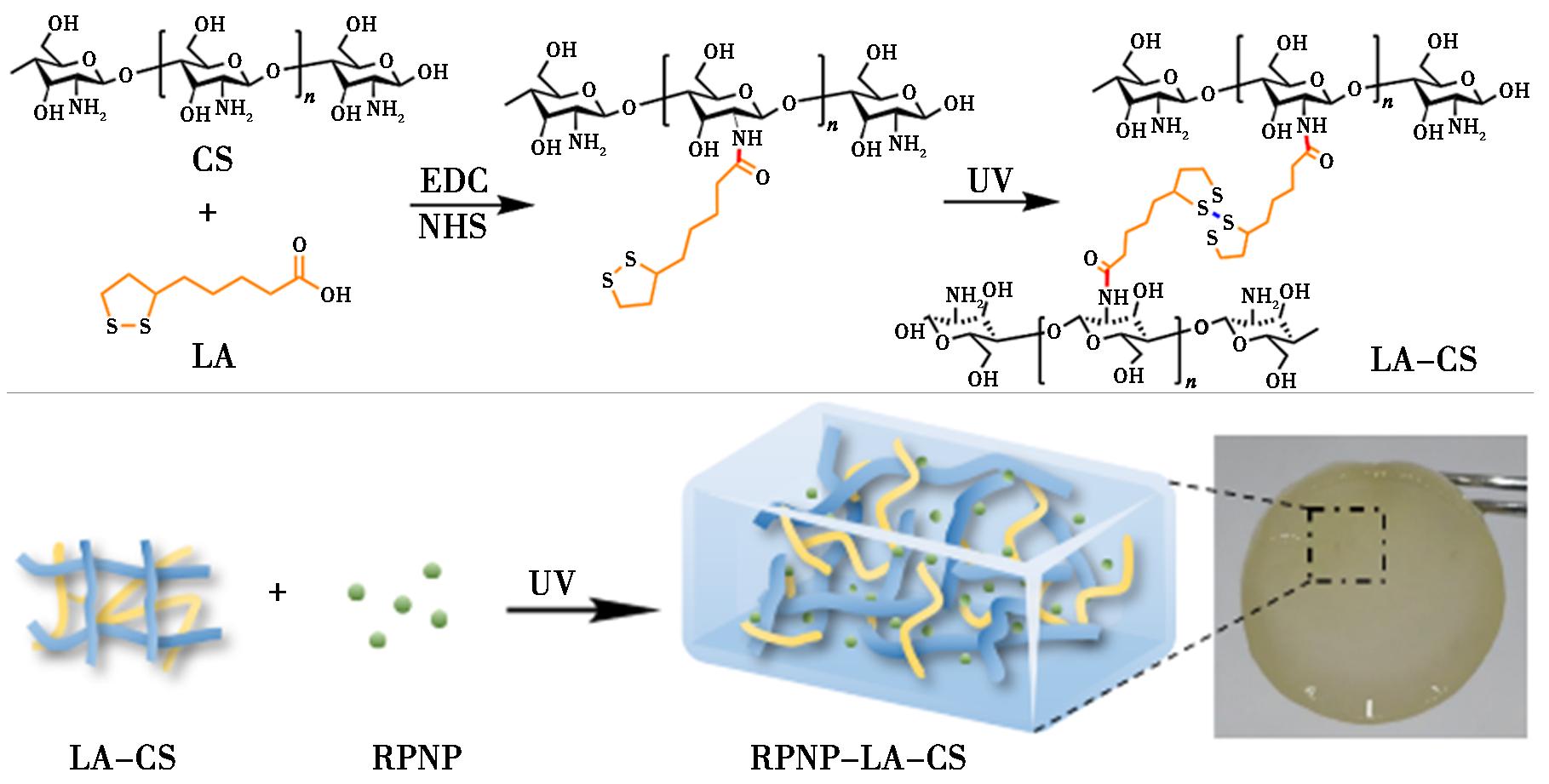
皮肤作为人体最大的保护屏障在维持机体稳态中发挥重要作用,但其易受创伤、微生物感染等外界因素破坏而引发皮肤损伤。伤口愈合是一个多阶段的复杂生物学过程,包括前期止血和炎症反应清除异物,增生、重塑期组织结构恢复[1],但在过程中常出现因感染、持续性炎症反应、坏死组织残留、局部血供不足及生长因子匮乏等问题,阻碍成纤维细胞等迁移与增殖,导致愈合过程延迟甚至失败[2],而通过施加功能性伤口敷料可明显促进愈合进程。其中水凝胶敷料在创面修复领域展现出独特优势,被认为是改善创面愈合的有效策略,其三维交联网络结构不仅能隔离伤口、增加透气性,还可主动维持创面湿性微环境,为细胞增殖、迁移及组织再生提供适宜的生理条件,有利于伤口愈合。以天然多糖如壳聚糖、纤维素、海藻酸钠等为基质的水凝胶,因兼具优异生物相容性、可降解性与功能多样性等特点,在伤口修复领域展现出良好的发展潜力[3,4]。
壳聚糖(CS)来源于天然甲壳素,对人体无毒,降解产物安全,凭借其良好的生物相容性、抗菌止血等活性,在智能药物递送、组织工程支架[5]及新型伤口敷料等领域前景广阔;CS分子链存在丰富的氨基和羟基等官能团,通过进一步改性可获得更广泛的应用[6]。硫辛酸(LA)的双硫五元环结构,可通过双硫键的开环重组而聚结,因此具备动态可逆的交联能力,同时具有抗氧化应激、抗炎特性[7];CS分子可通过氨基与LA的羧基发生酰胺反应获得改性,同时保留接枝分子LA的动态二硫键;此外,LA的改性可增强CS的水溶性,使其更容易溶解和吸收伤口分泌物[8]。Pang等[9]研究将α-硫辛酸改性壳聚糖和黑色素纳米颗粒结合,在紫外光(UV)下形成凝胶,可缓解糖尿病伤口氧化应激,加速血管再生和伤口愈合。
天然植物多糖是从植物中提取的一类重要生物大分子,具有丰富的生物活性和良好的生物相容性,研究表明多糖具有免疫调节、抗肿瘤、抗病毒、抗氧化和降血糖等多种药理学应用[10]。根据《中国植物志》[11]记载,水龙骨来源于蕨类水龙骨属植物水龙骨(Rhizoma polypodiodis nipponicae,RPN)的根茎,具有活血化瘀、治疗跌打损伤的功效。王重娟等[12]采用水提醇沉技术自RPN中分离出酸性杂化多糖,研究发现该多糖可激活巨噬细胞,进而提升免疫抑制小鼠的免疫功能;Batur等[13]发现欧亚水龙骨(Polypodium vulgare L.)提取物通过促进表皮再生和增加血管化而有助于伤口愈合。Parrado等[14]研究证实白绒水龙骨水提物具有抗氧化成分,能中和活性氧、增强内源性抗氧化系统,还可促进DNA修复、调控免疫炎症反应,改善光老化相关的细胞外基质降解。
本研究旨在提取RPNP并验证其抗氧化能力,通过接枝LA来对CS改性,制备RPNP-LA-CS复合水凝胶,进一步研究复合水凝胶的抑菌作用,并探讨其对小鼠背部全皮层损伤修复的促进效果。
1 实验部分
1.1 主要仪器与试剂
SCIENTZ-12N型冷冻干燥机(宁波新芝生物科技股份有限公司);PS-40A型超声波清洗机(东莞市洁康超声波设备有限公司);UV1101型紫外分光光度计(上海天美科学仪器有限公司);Synergy H1型全功能酶标仪(美国伯腾仪器有限公司);Nicolet iN10型傅里叶变换显微红外光谱仪、Pico 21型台式离心机(美国赛默飞世尔科技有限公司);JSM6390LV型扫描电子显微镜(日本电子株式会社)。
水龙骨(安徽锦承药业有限公司);硫辛酸(LA,99%)、壳聚糖(CS,Mw=300000)、水杨酸(C7H6O3,99.5%)、吗啉乙磺酸(MES,99%)、1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(EDC·HCl,98.5%)、N-羟基琥珀酰亚胺(NHS,98%)、2,2-联苯基-1-苦基肼基(DPPH,96%)、2,2-联氮-双(3-乙基苯并噻唑啉)-6-磺酸(ABTS,99%)、Triton-X-100(上海麦克林生化科技股份有限公司);乙酸(C2H4O2)、苯酚(C6H6O,≥99.0%)、过硫酸钾(K2S2O8,≥99.5%)、硫酸亚铁(FeSO4)、铁氰化钾(K3Fe(CN)6,≥99.5%)、三氯乙酸(TCA,≥99.0%)、三氯化铁(FeCl3,≥97.0%)(国药集团化学试剂有限公司)。
1.2 RPNP的提取
RPN根茎洗净晾干后烘干,粉碎后过600目筛。取150 g RPN粉末于提取皿中,按1∶40(g/mL)料液比加入纯水在50 ℃下分两次超声提取,每次2 h,将两次提取液合并,用纱布过滤除渣,使用滤纸再次抽滤后,于50 ℃减压浓缩至200 mL。按照V(浓缩液)∶V(乙醇)=1∶4向浓缩液中加入无水乙醇进行醇沉过夜,抽滤收集沉淀并晾干,待乙醇挥发完全后加入50 mL纯水复溶,采用Sevage法去除粗多糖中的蛋白质,按照V(复溶液)∶V(氯仿)∶V(正丁醇)=25∶5∶1的比例加入溶液,混匀静置30 min,分层后去除下层,留上层继续加入Sevage溶液,重复上述操作4~6次后,用无水乙醇对上层液再次进行醇沉,抽滤后得到沉淀进行冻干即得RPNP。采用苯酚硫酸法测得RPNP多糖含量约为73%。
1.3 RPNP的抗氧化实验
配制6 mg/mL的RPNP母液,梯度稀释为6、3、2、1、0.5、0.25 mg/mL的样品溶液来测定RPNP多糖溶液对DPPH自由基、ABTS+自由基、羟基自由基清除率及总还原力能力,每组样品重复3次,均以Vc溶液作为阳性对照。
1.3.1 DPPH自由基清除实验
参考陈卫等[15]方法,取等量的样品溶液和0.1 mmol/L DPPH的乙醇溶液,37 ℃避光孵育 30 min,取出后测上清液在酶标仪波长为517 nm处的吸光度值,按照式(1)计算清除率。
DPPH自由基清除率(%)=
[A0-(A1-A2)]/A0×100%
(1)
式中,A0为蒸馏水代替样品与DPPH的吸光度,A1为样品实验组吸光度值,A2为乙醇代替DPPH与样品的吸光度。
1.3.2 ABTS+自由基清除实验
参考陈霖虹等[16]方法并稍加修改,7 mmol/L的ABTS溶液与2.45 mmol/L的过硫酸钾溶液等体积混合均匀,避光反应14 h后,用磷酸盐缓冲液稀释,用紫外分光光度计检测在734 nm波长处的吸光度值为0.70±0.02,作为ABTS工作液备用。取2 mL ABTS工作液与60 μL样品溶液混合均匀,室温下孵育6 min后,立即用酶标仪测波长为734 nm处的吸光度值。按照式(1)类似方法计算清除率,其中A0为蒸馏水与ABTS工作液的吸光度,A2为蒸馏水与样品的吸光度。
1.3.3 羟基自由基清除实验
参考周连玉等[17]方法并稍加修改,9 mmol/L FeSO4、水杨酸的乙醇溶液,H2O2溶液按序加入至等量梯度浓度样品溶液中,37 ℃水浴30 min后于离心机中4500 r/min离心10 min,去上清,用酶标仪测波长为510 nm处各组吸光度值。按照式(1)类似方法计算清除率,A0为蒸馏水与水杨酸显色剂的吸光度,A2为蒸馏水与样品的吸光度值。
1.3.4 总还原力实验
RPNP待测梯度溶液配制同上,参考侯敏娜等[18]方法并稍加修改。取1 mL各梯度浓度样品溶液向其中加入1 mL(0.2 mol/L,pH 6.6)磷酸盐缓冲溶液和1 mL 1%的铁氰化钾溶液,混匀后置于50 ℃水浴中,加热20 min后,立即取出向其中迅速加入1 mL 10%的三氯乙酸溶液,8000 r/min离心5 min后取500 μL上清液于离心管中,向其中加入500 μL水和125 μL 0.1%三氯化铁溶液,充分混合均匀,反应10 min后取样于700 nm波长处测OD值,按照式(2)计算总还原力。
总还原力=OD样品-OD空白
(2)
式中,OD空白是用水代替RPNP样品的吸光度值。
1.4 LA-CS、RPNP-LA-CS水凝胶的制备
1.4.1 LA-CS的合成
LA-CS合成方法参考Yang等[19]方法并稍加修改,1 g(4.85 mmol)的LA加入至100 mL pH 5.5的MES-乙醇溶液中,室温下搅拌至完全溶解。随后将14.54 mmol的EDC-HCl添加至LA溶液中,完全溶解后向溶液中加入14.54 mmol的NHS,激活反应3 h;加入4.85 mmol的CS,室温搅拌24 h后于纯水中透析4 d,将透析液冷冻干燥即得LA-CS冻干物。
1.4.2 傅里叶变换衰减全反射红外光谱(ATR-FTIR)分析
为验证CS接枝LA是否成功,对LA-CS冻干物进行傅里叶红外光谱测定分析产物结构,在4000~500 cm-1范围内扫描16次,分辨率为4 cm-1。
1.4.3 LA-CS空白水凝胶、RPNP-LA-CS复合水凝胶的制备
质量分数2% LA-CS溶于6 mg/mL RPNP水溶液中,参考Pang等[9]方法,于紫外光(365 nm波长,60 mW/cm2)下照射30 min制得RPNP-LA-CS复合水凝胶;空白水凝胶则为不添加多糖,质量分数2% LA-CS溶于纯水中紫外光下照射30 min后制得。
1.4.4 LA-CS、RPNP-LA-CS复合水凝胶的理化性质表征
1.4.4.1 扫描电镜观察水凝胶内部截面
为探究复合水凝胶的内部结构特征,将水凝胶冻干后,取冻干物进行纵向切割,贴附于有导电胶的样品台并完成喷金处理,随后置于扫描电镜下观察其微观结构。
1.4.4.2 溶胀率
取适量冻干水凝胶称重并记录为W0,置于0.02 mmol/L、pH 7.4 PBS缓冲液中于2、4、6、12 h后取出用滤纸吸干表面多余水分,称重并记录下重量为W1,按照式(3)计算溶胀率。
溶胀率(%)=(W1-W0)/W0×100%
(3)
1.4.4.3 抑菌实验
为研究水凝胶对金黄色葡萄球菌(S.aureus)(革兰氏阳性菌)和铜绿假单胞菌(P.aeruginosa)(革兰氏阴性菌)两种皮肤伤口处常见条件致病菌的抑菌效果,将50 mg水凝胶冻干物置于紫外灯下照射30 min后,与5 mL稀释后的菌液(浓度为105~107 CFU/mL)于37 ℃恒温振荡(160 r/min)孵育共培养12 h,将共孵育的菌液适当稀释后,取100 μL菌液涂布于LB固体培养基表面,37 ℃恒温培养18~24 h,观察菌落生长情况,并根据式(4)计算抑菌率。
抑菌率(%)=
(对照组菌落数-实验组)/对照组×100%
(4)
1.5 RPNP-LA-CS水凝胶血液相容性研究
取新鲜小鼠血液加入抗凝剂离心(1500 r/min,5 min),取下层血细胞,用PBS反复清洗3次,直至上清液不再显红色,将所得血细胞溶于PBS配制为体积分数5%的血红细胞悬液备用。称取RPNP-LA-CS水凝胶冻干物剪碎,于PBS中溶胀48 h,配制浓度为9、6、3、2、1 mg/mL的水凝胶浸提液。在离心管中加入等体积的浸提液和5%血红细胞悬液,37 ℃下孵育2 h,取出后3000 r/min离心5 min,取上清液置于540 nm处测吸光度值(OD),分别以PBS和Triton-X-100代替浸提液作为阴性对照和阳性对照。以式(5)计算溶血率。
溶血率(%)=(ODs-ODn)/(ODp-ODn)×100%
(5)
式中,ODs、ODn、ODp分别为水凝胶样品、阴性对照组、阳性对照组的吸光度值。
1.6 皮肤全皮层损伤体内动物实验
1.6.1 实验动物及分组
选用8周龄SPF级雄性KM小鼠[许可证号:SCXK(鄂)2020-0018]共18只,由湖北省实验动物研究中心提供。本实验经湖北工业大学科研伦理与科技安全委员会批准(编号:HBUT20250058),实验中对动物的处理方法严格遵守实验动物管理条例。
适应环境后将小鼠随机分为3组:模型组(Model组)、空白水凝胶组(LA-CS组)、载药水凝胶组(RPNP-LA-CS组)。
1.6.2 全皮层损伤动物模型建立及治疗
全皮层损伤动物模型建立方法参考吴燕等[20]方法,在小鼠背部建立1 cm2的全皮层损伤创面。载药水凝胶组小鼠创面覆予RPNP-LA-CS水凝胶;空白水凝胶组则以LA-CS水凝胶覆盖创面;模型组则不予任何水凝胶覆盖创面。
创面愈合情况观察:在术后1、5、10、15 d拍照记录各组小鼠背部伤口愈合情况并分析愈合率和愈合轨迹。15 d处死全部小鼠并取背部创面皮肤固定于组织固定液中,经石蜡包埋切片后,进行苏木精&伊红(H&E)染色,置于显微镜下观察分析。
1.7 统计学分析
实验数据通过Origin和GraphPad Prism 9进行单因素分析(One-way ANOVA),均以平均值±标准差表示,P<0.05即为具有显著性。
2 结果与讨论
2.1 RPNP抗氧化能力测定
RPNP抗氧化能力结果如图2所示,RPNP具有一定的抗氧化能力,且在6~0.25 mg/mL范围内随着浓度的降低,RPNP抗氧化能力降低,在浓度为6 mg/mL时,对DPPH自由基、ABTS+自由基、羟基自由基清除率达到(89.68±0.85)%、(75.49±0.96)%、(64.50±0.96)%,总还原力为1.38±0.03;RPNP对DPPH自由基、ABTS+自由基、羟基自由基的半数抑制浓度(IC50)分别为(1.97±0.22)、(1.86±0.27)、(5.48±0.48)mg/mL。说明RPNP具有广谱自由基清除能力,能有效抵御自由基引起的氧化损伤,避免因自由基积累导致的氧化应激问题,从而减轻炎症反应。
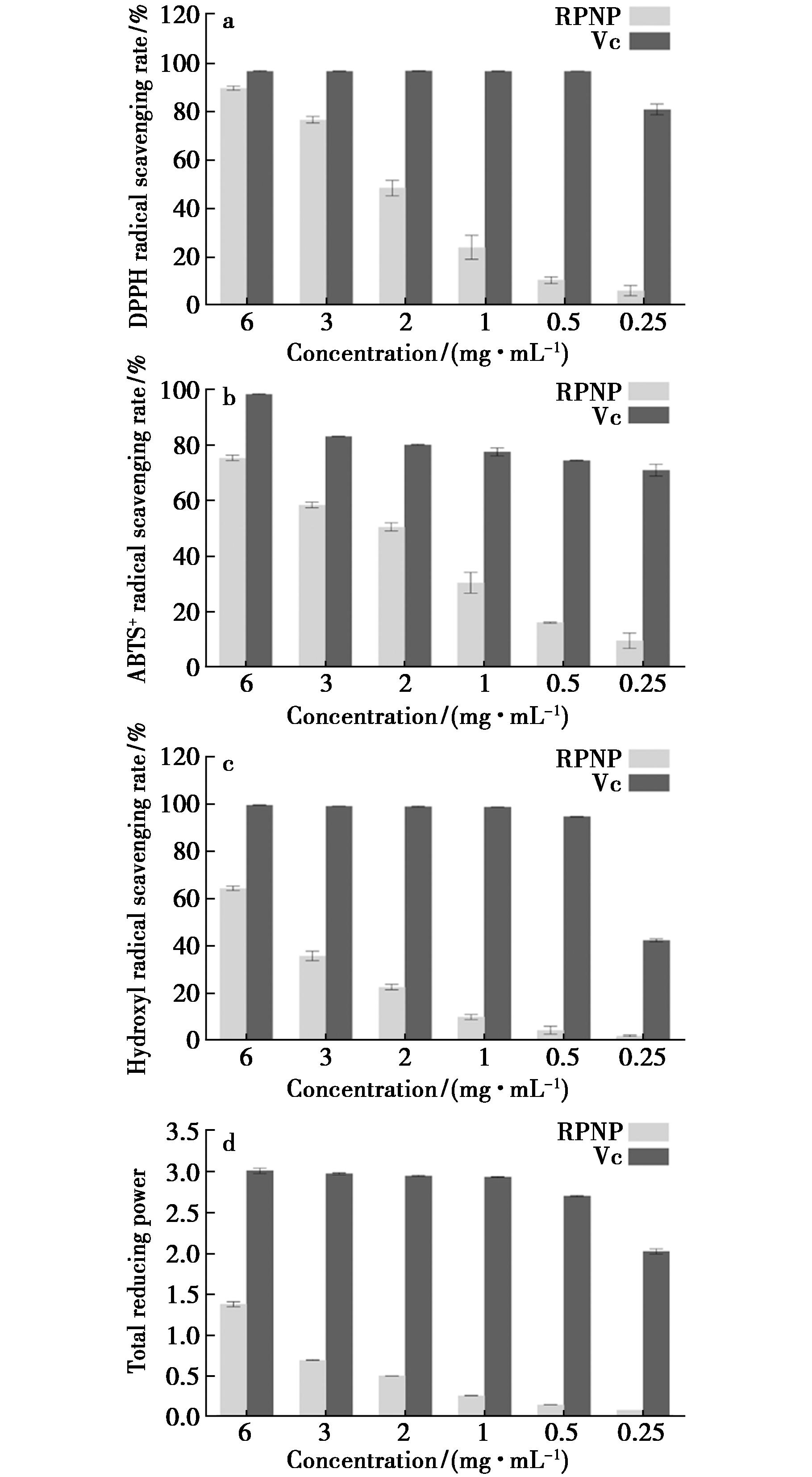
a.各梯度浓度样品对DPPH自由基清除率;b.各梯度浓度样品对ABTS+自由基清除率;c.各梯度浓度样品对羟基自由基清除率;d.各梯度浓度样品总还原力
图2 RPNP对自由基清除能力及还原力
Fig.2 Radical scavenging capacity and total reducing power of RPNP
2.2 LA-CS傅里叶变换衰减全反射红外光谱(ATR-FTIR)分析
LA-CS合成产物经ATR-FTIR检测谱图如图3所示,1692.23 cm-1处为LA羧基C![]() O伸缩振动峰,2925.97 cm-1处为LA的碳链含亚甲基和次甲基的C—H伸缩振动峰,1554.83 cm-1处出现新的吸收峰,为N—H伸缩振动峰,来源于CS的 —NH2基团,1642.09 cm-1处为酰胺的C
O伸缩振动峰,2925.97 cm-1处为LA的碳链含亚甲基和次甲基的C—H伸缩振动峰,1554.83 cm-1处出现新的吸收峰,为N—H伸缩振动峰,来源于CS的 —NH2基团,1642.09 cm-1处为酰胺的C![]() O的伸缩振动峰,是LA与CS脱水缩合生成酰胺键的特征峰[21],由此可推断LA与CS经过酰胺反应成功以酰胺键结合。
O的伸缩振动峰,是LA与CS脱水缩合生成酰胺键的特征峰[21],由此可推断LA与CS经过酰胺反应成功以酰胺键结合。
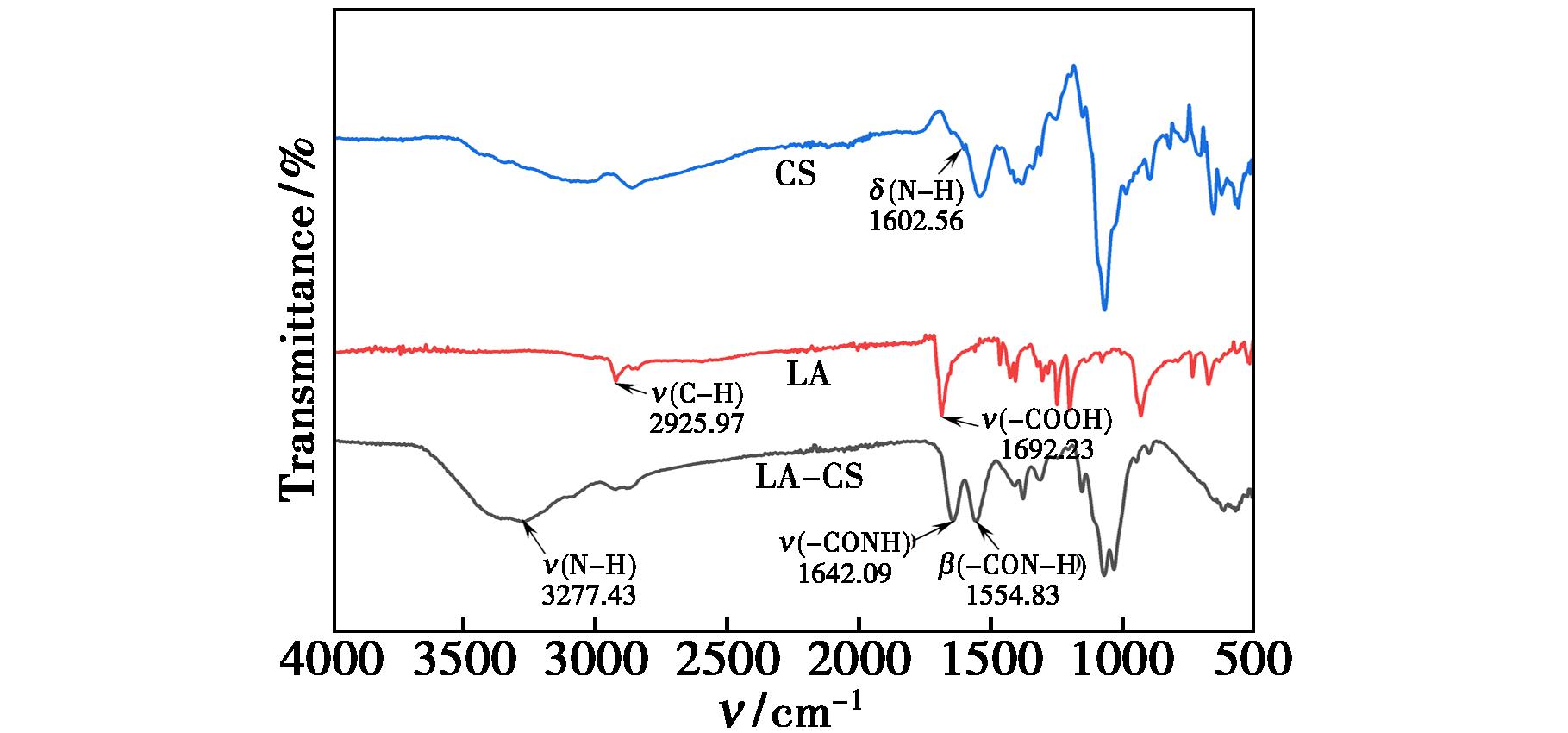
图3 CS、LA、LA-CS的ATR-FTIR谱图
Fig.3 ATR-FTIR spectra of CS,LA,and LA-CS
2.3 RPNP-LA-CS水凝胶的扫描电镜分析
在扫描电镜下观察到水凝胶内部如图4所示,RPNP-LA-CS水凝胶具有疏松多孔状结构,孔隙分布比较均匀,与LA-CS水凝胶相比,RPNP的加入并没有使水凝胶结构塌陷,反而使孔状结构变得更加紧密,这可能是由于RPNP的加入使分子间的氢键、静电相互作用等非共价键作用加强导致。Ye等[22]有类似研究结果,多糖可以在水凝胶网络内的不同尺度上有效地形成氢键,从而显著增强机械性能。

图4 LA-CS(a)与RPNP-LA-CS(b)水凝胶冻干扫描电镜图
Fig.4 Scanning electron microscopy images of freeze-dried LA-CS (a) and RPNP-LA-CS (b) hydrogels
2.4 水凝胶溶胀率
通过水凝胶在PBS体系中的溶胀表现,据此可评估其对伤口渗液的吸收能力,结果见图5,显示该水凝胶具有优良的溶胀特性,能够提供良好伤口修复湿润环境,空白水凝胶溶胀率高于RPNP-LA-CS水凝胶。产生这一因素的原因可能是由于RPNP的加入,使水凝胶结构更加紧密,其孔隙小于空白组水凝胶,导致溶胀率小于空白水凝胶。
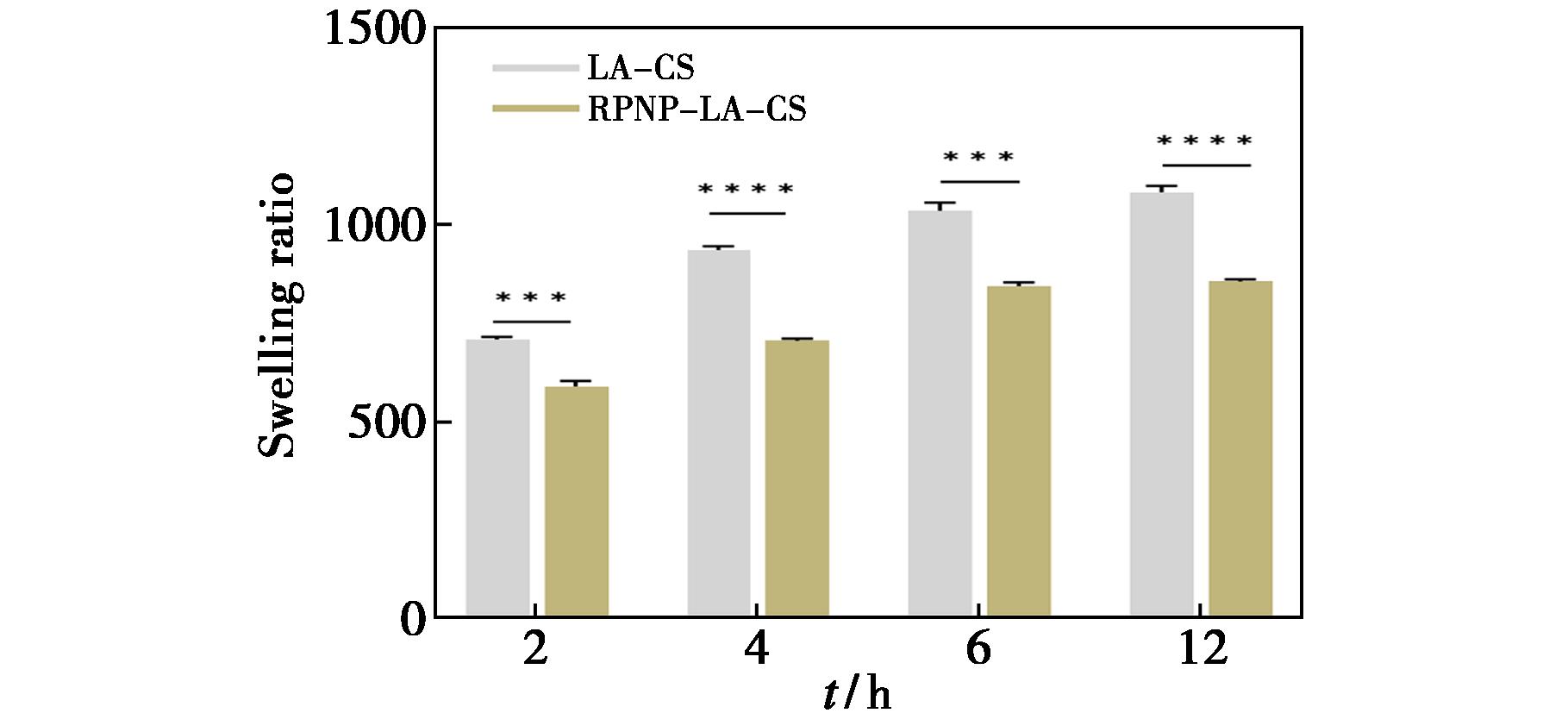
图5 水凝胶溶胀率
Fig.5 Swelling ratio of hydrogels
2.5 水凝胶的抑菌性能
水凝胶对S.aureus和P.aeruginosa的抑菌效果如图6所示,将与水凝胶共孵育12 h的菌液涂布于固体培养基18~24 h后,两种细菌菌落数量均大幅减少,表明细菌生长受到强烈抑制。LA-CS水凝胶对S.aureus的抑菌率可达到(97.53±0.38)%,对P.aeruginosa的抑菌率可达到(96.72±0.29)%;RPNP-LA-CS复合水凝胶对S.aureus的抑菌率可达到(98.38±0.17)%,对P.aeruginosa的抑菌率可达(98.99±0.1)%。RPNP的加入并没有降低LA-CS的抑菌效果,反而增强了抑菌效果;两组水凝胶对两种革兰氏阳性、阴性代表菌均有优异的抑制生长作用,说明水凝胶具有良好的广谱抑菌性能,能有效阻止创面处潜在的细菌感染。
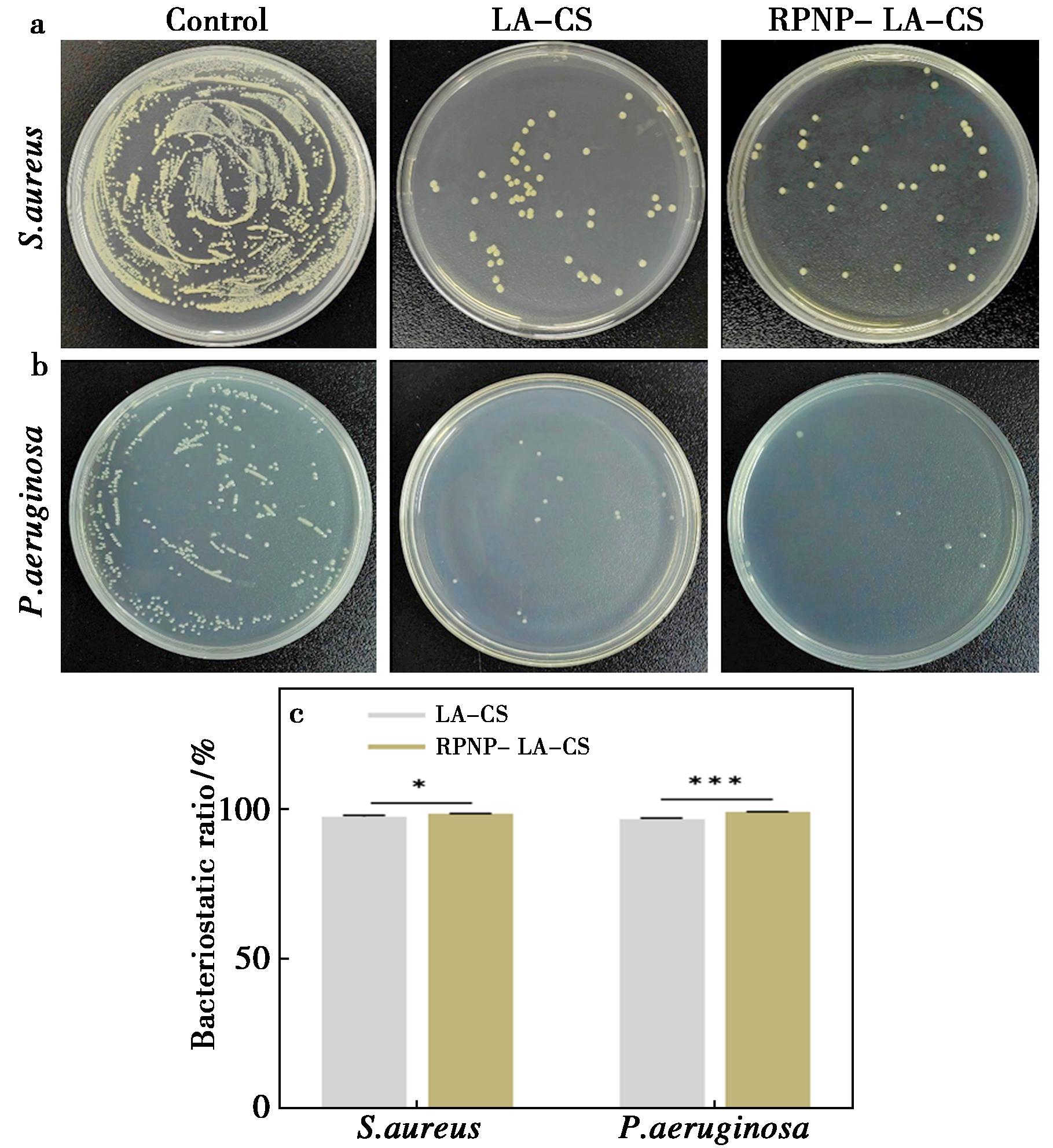
a.LA-CS、RPNP-LA-CS与S.aureus共培养后涂布于固体培养基上的菌落情况;b.与P.aeruginosa共培养后涂布于固体培养基上的菌落情况;c.各组水凝胶对S.aureus和P.aeruginosa的抑菌率
图6 水凝胶抑菌性能
Fig.6 Antibacterial activity of hydrogels
2.6 RPNP-LA-CS水凝胶的溶血率测定
通过体外溶血实验来评估RPNP-LA-CS水凝胶的生物相容性,以溶血率不高于5%作为合格标准。不同浓度的RPNP-LA-CS水凝胶浸提液的溶血率如图7所示,在1~9 mg/mL的范围内,水凝胶溶血率均低于5%,且在浓度为6 mg/mL时,水凝胶浸提液溶血率最低,仅为(0.25±0.06)%,符合材料溶血性能评估标准ASTM F756-17《材料溶血性能评估标准实践》[23](≤5%)的安全要求,结果表明RPNP-LA-CS水凝胶具有良好的血液相容性。
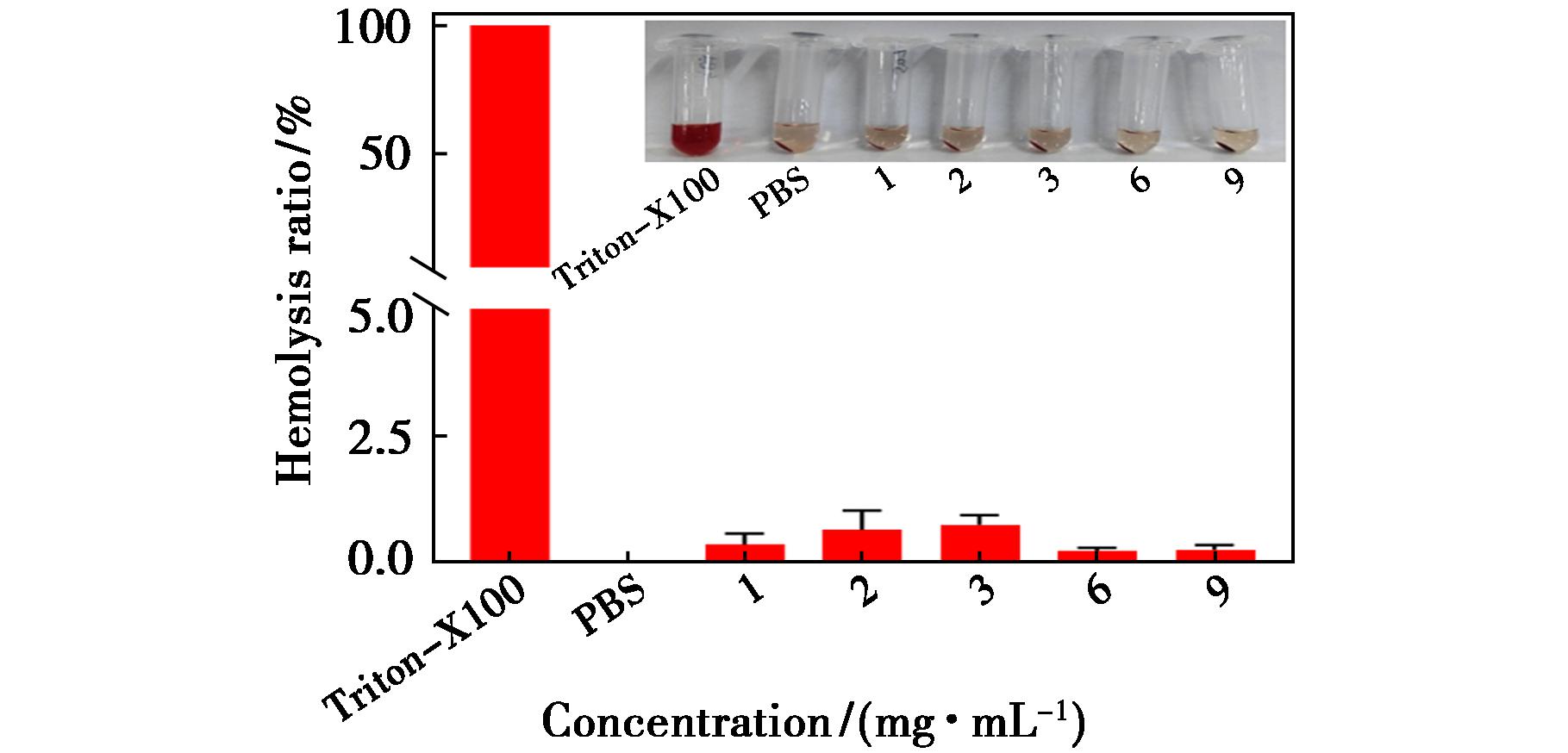
图7 RPNP-LA-CS水凝胶溶血率
Fig.7 Hemolysis ratio of RPNP-LA-CS hydrogels
2.7 伤口愈合率及愈合轨迹
3组小鼠背部创面愈合情况大体图片如图8所示,根据创面形状绘制出伤口愈合轨迹。创面覆予水凝胶组伤口愈合率高于模型组,且RPNP-LA-CS组伤口愈合率更高。在第5 d时,LA-CS和RPNP-LA-CS组小鼠伤口愈合显著高于模型组(P<0.05,P<0.01);在第15 d时RPNP-LA-CS组伤口创面愈合率已经达到(99.73±0.29)%,空白水凝胶组伤口愈合率为(96.37±0.36)%,模型组仅为(89.87±1.54)%,愈合率显著低于两组给予水凝胶组(P<0.0001)。
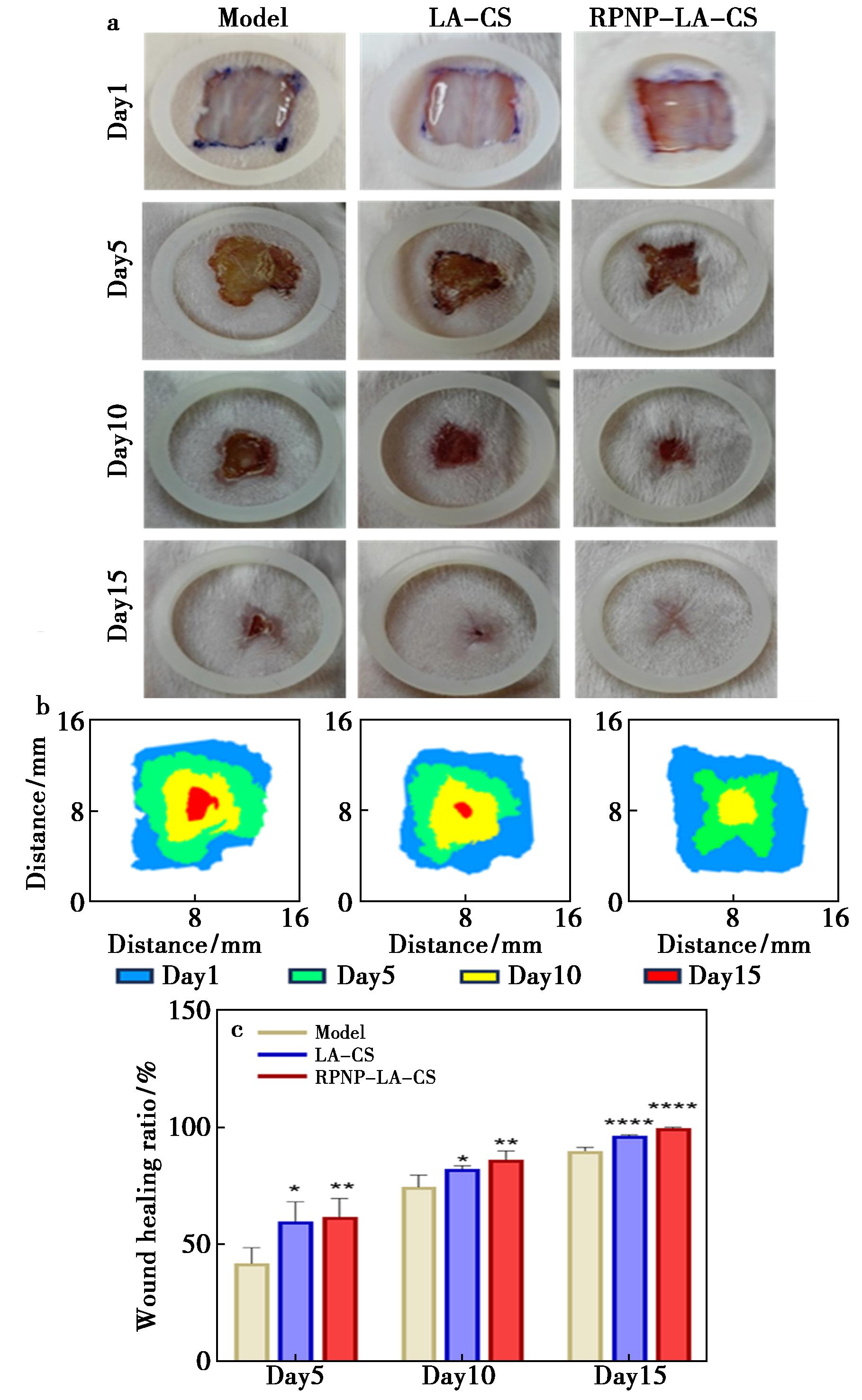
*P<0.05,**P<0.01,****P<0.0001,compared with the model group
图8 各组小鼠不同时间下创面情况(a)、创面愈合轨迹图(b)和各组小鼠伤口愈合率(c)
Fig.8 Wound conditions of mice in each group at different time points (a),wound healing trajectory plot (b),and wound healing ratio of mice (c)
2.8 创面损伤处皮肤组织H&E染色
对术后15 d各组小鼠背部创面部位皮肤组织进行H&E染色,所得结果如图9所示,表皮厚度结果见表1。LA-CS组和RPNP-LA-CS组小鼠创面处皮肤组织修复效果明显优于模型组。模型组小鼠皮肤表皮增厚,且有结痂情况,真皮层与表皮层分离,并有大量炎症细胞浸润,角质层细胞角化不全含有残存的细胞核,新生血管较少,未见毛囊附属器。LA-CS组表皮厚度较为正常,但毛囊结构并未完全恢复,有少量新生血管。与正常小鼠皮肤组织相比,RPNP-LA-CS组皮肤组织可以看到较为完整的表皮、真皮、皮下组织结构,皮脂腺和毛囊等皮肤附属器分布均匀,且表皮厚度趋于正常,说明在较短时间内RPNP不仅促进伤口愈合,还促进创面皮肤组织正常化。
表1 各组小鼠伤口皮肤组织表皮厚度注
Tab.1 Epidermal thickness of the wound skin tissue in mice

组别表皮厚度/μmNormal53.2±5.4Model133.5±30.8####LA-CS91.7±13.4∗∗####RPNP-LA-CS69.2±12.2∗∗∗∗##
注:**P<0.01、****P<0.0001与模型组相比;##P<0.01、####P<0.0001与正常组相比。
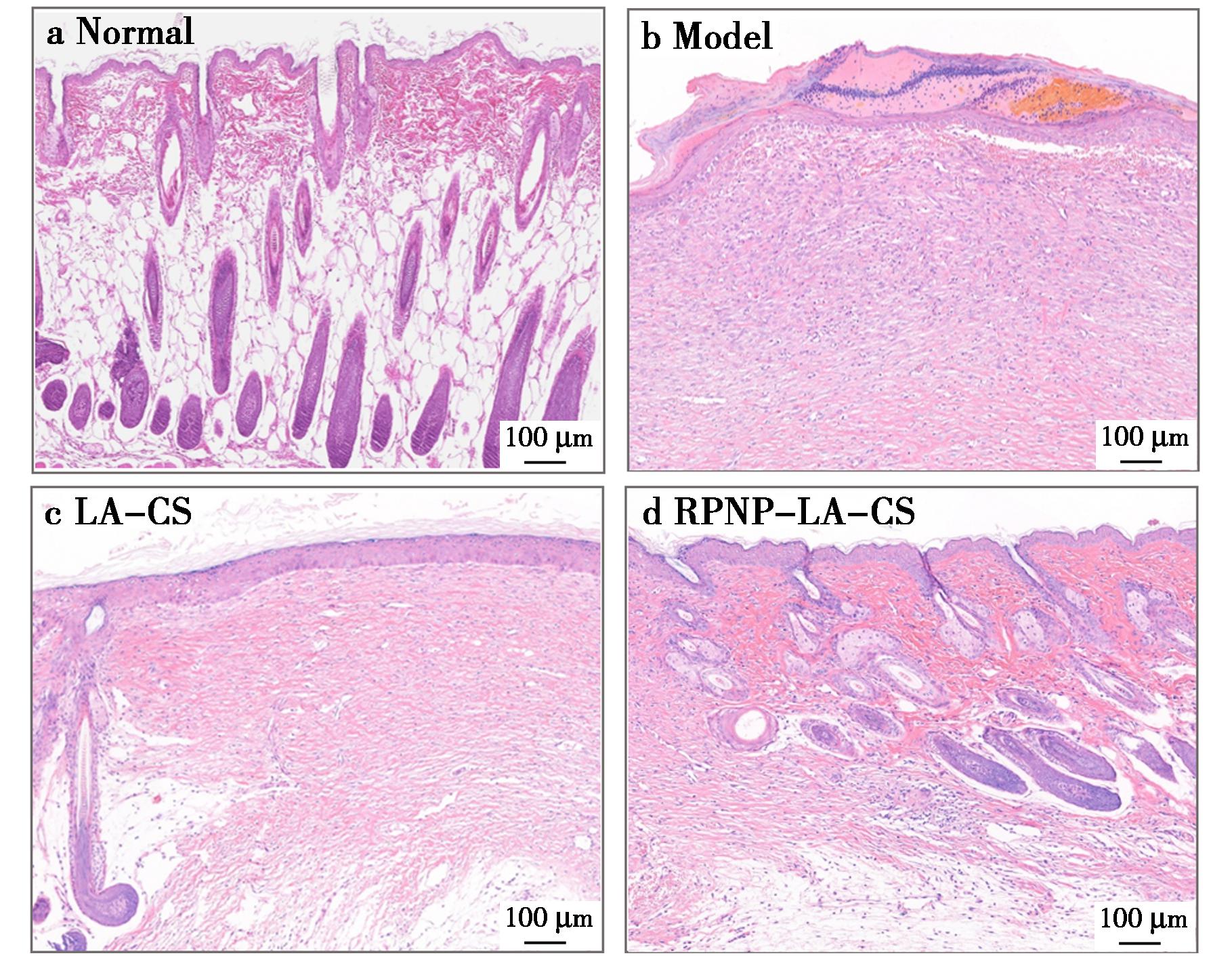
a~d分别为正常小鼠、模型组、LA-CS、RPNP-LA-CS组皮肤组织H&E染色结果图
图9 各组小鼠伤口皮肤组织H&E染色
Fig.9 H&E staining images of the wound skin tissues in mice
天然植物多糖在伤口愈合方面已展现出优越的前景,Yan等[24]利用水提醇沉法从白及中分离白及多糖,并基于氧化白及多糖和聚乙烯醇制备气凝胶敷料,该敷料通过减轻炎症反应、促进血管生成及加速上皮形成来增强伤口愈合;Li等[25]研究表明负载黄芪-三七提取物的羧甲基壳聚糖-海藻酸钠复合水凝胶,能促进小鼠成纤维细胞增殖和胶原沉积,上调血管内皮生长因子的表达,通过多途径协同作用促进全层伤口愈合。Wang等[26]基于天麻多糖构建多功能水凝胶,将其应用于金黄色葡萄球菌感染的小鼠糖尿病创面的修复;结果显示,多功能水凝胶的抗氧化能力优异,对DPPH、ABTS+自由基清除率接近Vc;可降低氧化应激标志物MDA水平,缓解细胞与机体氧化损伤;下调TNF-α、IL-1β等促炎因子,上调IL-10等抗炎因子,抑制TLR4/MyD88/NF-κB信号通路,从而减轻创面炎症浸润,改善创面炎症微环境,促进愈合。在本研究中,RPNP-LA-CS复合水凝胶具有优异的抑菌活性,可能通过清除多种自由基,减轻创面炎症反应等来加快伤口愈合速度,促进损伤皮肤组织毛囊、皮脂腺等结构恢复。
3 结论
本文证实RPNP能够清除多种自由基,具有抗氧化能力。通过形貌、溶胀、生物安全性评价系列实验研究结果表明RPNP-LA-CS复合水凝胶具有三维疏松多孔结构,生物相容性良好,且对金黄色葡萄球菌及铜绿假单胞菌有良好的抑制作用。同时复合水凝胶展示出优异的促进伤口修复效果,能够加快全皮层损伤小鼠皮肤愈合速度,且恢复的皮肤组织结构更加完整。因此,RPNP在皮肤伤口损伤具有良好的应用潜力,同时也为RPN的综合应用提供了新的方向。
[1]Falanga V,Isseroff R R,Soulika A M,Romanelli M,Margolis D,Kapp S,Granick M,Harding K.Nat.Rev.Dis.Primers,2022,8(1):50.
[2]Wang L H,Lu X Y,Wang Y K,Sun L N,Fan X Y,Wang X R,Bai J.Pharmaceutics,2025,17(8):976.
[3]Qi J E,Wang Y Q,Ren J M,Zhang C F,Li X C.Chin.J.Anal.Lab.,2025,44(6):814-820.
齐加恩,王颖倩,任嘉敏,张朝峰,李晓春.分析试验室,2025,44(6):814-820.
[4]Shang Y,Dai M Y,Liu Y,Tian Y,Ma H.J.Dalian Ocean.Univ.,2021,36(2):347-354.
尚悦,代明允,刘鹰,田野,马贺.大连海洋大学学报,2021,36(2):347-354.
[5]Bharathi R,Ganesh S S,Harini G,Vatsala K,Anushikaa R,Aravind S,Abinaya S,Selvamurugan N.Int.J.Biol.Macromol.,2022,222:132-153.
[6]Wang J L,Zhuang S T.J.Clean.Prod.,2022,355:131825.
[7]Luo Z,Liu W G,Cui C Y.Chin.Polym.Bull.,2025,38(12):1789-1806.
雒振,刘文广,崔春燕.高分子通报,2025,38(12):1789-1806.
[8]Wu H,Zhu L,Xie L,Zhou T Y,Yu T B,Zhang Y Z.Int.J.Biol.Macromol.,2024,278:134609.
[9]Pang Z X,Li Q Y,Liu K,Wu X P,Xu H X,Chen Z B,Dai H L.Carbohydr.Polym.,2024,340:122215.
[10]Yu Y,Shen M Y,Song Q Q,Xie J H.Carbohydr.Polym.,2018,183:91-101.
[11]Editorial Committee of Flora of China CAS.Flora reipublicae popularis sinicae.Beijing:Science Press,2000.
中国科学院中国植物志编辑委员会.中国植物志.北京:科学出版社,2000.
[12]Wang C J,Liang Y Q,Xia H Y,Li C H,Zhu Y D,Li Z K.Immunol.J.,2019,35(9):737-743.
王重娟,梁月琴,夏洪颖,李翠红,朱瑜丹,李仲昆.免疫学杂志,2019,35(9):737-743.
[13]Batur S,Ayla S,Sakul A A,Okur M E,Karada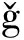 A E,Daylan B,Özdemir E M,Kepil N,Gunal M Y.Medeniyet Med.J.,2020,35(4):315-323.
A E,Daylan B,Özdemir E M,Kepil N,Gunal M Y.Medeniyet Med.J.,2020,35(4):315-323.
[14]Parrado C,Nicolas J,Juarranz A,Gonzalez S.Photochem.Photobiol.Sci.,2020,19(6):831-843.
[15]Chen W,Gu C H,Ye Z W,Xiong L B,Li T,Gao Y J,Chen Q.Chem.Reagents,2024,46(2):67-73.
陈卫,谷彩花,叶兆伟,熊林斌,李涛,郜雅婧,陈琼.化学试剂,2024,46(2):67-73.
[16]Chen L H,Xiao G S,Xu Y J,Wu J J,Yu Y S,Wen J,Zou B,Li L,Chen S P,Fu M Q.Food Ferment.Ind.,2025,51(3):215-224.
陈霖虹,肖更生,徐玉娟,吴继军,余元善,温靖,邹波,李璐,陈树鹏,傅曼琴.食品与发酵工业,2025,51(3):215-224
[17]Zhou L Y,Zhong R,Jiao L,Chen Q H,Zhan Y.Food Res.Dev.,2020,41(15):6-10.
周连玉,钟睿,焦璐,陈启红,展艳.食品研究与开发,2020,41(15):6-10.
[18]Hou M N,Hou S P,Wang J,Peng X J,Xu H Y,Zhao F.Acta Chin.Med.Pharmacol.,2025,53(9):39-44.
侯敏娜,侯少平,王洁,彭修娟,许海燕,赵帆.中医药学报,2025,53(9):39-44.
[19]Yang H H,Lu Y,Bao L L,Liu Y,Liu D Q,Zhong Z M.Int.J.Food Microbiol.,2025,434:111149.
[20]Wu Y,Kou X Y,Wang Y Z,Liu T,Liu X Y,You X Y,Su J T.Chem.Reagents,2023,45(12):26-32.
吴燕,寇先勇,王峣姿,刘同,刘馨月,尤祥宇,苏江涛.化学试剂,2023,45(12):26-32.
[21]Wang X Y,Yao L H,Zhang J,Yu Y Y,Wang P,Wang Q.China Dye.Finish.,2023,49(12):44-48;66.
王馨悦,姚丽华,张静,余圆圆,王平,王强.印染,2023,49(12):44-48;66.
[22]Ye Y H,Niu X,Zheng K,Wan Z M,Zhang W C,Hua Q,Zhu J Y,Qiu Z,Wang S H,Liu H,Renneckar S,Rojas O,Jiang F.Mater.Horiz.,2025,12(6):1878-1890.
[23]ASTM F756-17.Standard Practice for Assessment of Hemolytic Properties of Materials,2025-08-01.
ASTM F756-17.材料溶血性能评估标准实践,2025-08-01.
[24]Yan Q,Long X Y,Zhang P X,Lei W,Sun D Q,Ye X Y.Carbohydr.Polym.,2022,293:119696.
[25]Li J,Li L N,Yu Y,Qin R X,Yu C Y,Chen C,Dong Y M,Tan Y D,Liu Y N,Liu X L.Front.Pharmacol.,2025,16:1526828.
[26]Wang R Y,Qi Y C,Liu W C,Cheng Z Q,Li W,Zhu H Y,Zhao Y,Han J H.Carbohydr.Polym.,2025,367:123983.