在全球范围内,对可再生能源存储以及大规模储能系统的需求正呈现出不断攀升的态势。在此背景下,研发具备低成本、高性能特点的二次电池技术,已然成为当务之急。而锂离子电池的发展满足高安全性、高能量密度和快速充电性能的要求[1]。因此,锂离子电池在便携式电子设备、大型电化学储能以及电动汽车市场占据着主导地位。然而,锂资源存在稀缺性,且地理分布极不均衡,这两个问题使得人们不得不将目光投向其他电化学储能体系,以寻求替代方案[2-5]。钠离子电池则凭借诸多优势进入大众视野。地球上的钠资源极为丰富,成本也相对低廉,并且钠与锂在工作原理和特性方面存在相似之处。基于这些特点,钠离子电池被认为是下一代大规模储能技术的理想替代选择之一[6]。
对钠离子电池而言,正极材料是影响其能量密度、循环寿命以及成本的关键因素[7,8]。在诸多正极材料体系当中,聚阴离子化合物凭借自身稳定的三维结构框架、可灵活调节的工作电压和出色的热稳定性,受到了科研人员的广泛关注[9-12]。Jiang等[13]通过系统的原位/非原位表征证实了钒基聚阴离子材料与三维碳基质复合,能够有效提升锌离子的扩散系数和结构可逆性,从而同时实现材料的高倍率性能和长循环寿命。聚阴离子材料Na3V2(PO4)3(NVP)具有热力学稳定性好、结构开放等特点,被认为是一种极具商业化潜力的钠离子电池正极材料[14]。Shi等[15]利用三维交联导电网络包覆Na3V2(PO4)2F3纳米颗粒的策略,能够有效缓解循环过程中的结构应变,从而显著提升钠离子电池的循环稳定性与结构完整性。聚阴离子材料中的硫酸根(SO4)2-基,尤其是Na2Fe(SO4)2,它借助自身极强的电负性诱导效应,能够产生高于3.0 V(vs.Na+/Na)的Fe2+/Fe3+氧化还原电位。而且,其原料中的铁和硫来源丰富,对环境友好,成本也极为低廉,因此展现出极为可观的应用前景[16]。正因如此,深入探究其晶体结构、电化学特性以及储钠机制,对于推动高性能钠离子电池的研发,有着重要的科学意义和实际应用价值。不过,Na2Fe(SO4)2和不少聚阴离子材料一样,存在本征电子电导率较低的问题。这一问题极大地制约了它在充放电过程中的倍率性能,也使得活性物质无法得到充分利用,进而导致其实际电化学性能,特别是在大电流工作条件下的表现,难以达到理想状态[17-19]。为突破材料导电性方面的限制难题,把材料纳米化以及与碳材料复合,已被证实是极具成效的解决策略。当把材料尺寸缩减至纳米量级时,钠离子和电子在固相中的扩散路径能够显著缩短,可有效弥补材料自身本征导电性欠佳的短板。Mao团队[20]通过精准调控合成条件,成功制备出纳米颗粒、纳米片或者分级多孔结构。这些独特的结构不仅增大了材料的比表面积,还增加了反应活性位点的数量,进而改善了材料的倍率性能。不过,该研究并未深入探究形貌调控对材料导电性会产生怎样的影响,而形貌调控这些因素对于材料的储能性能而言,是极为关键的。Barpanda团队[16]则采用另一种方法,他们通常先将FeSO4·7H2O、Na2SO4等前驱体与葡萄糖、蔗糖、柠檬酸等碳源进行机械球磨或者液相混合处理,随后在惰性气氛的环境下进行热处理,以此合成碳包覆的Na2Fe(SO4)2复合材料。碳包覆技术有着多重积极作用,它不仅可以显著提升材料的电子电导率,还能有效抑制颗粒在循环充放电进程中的团聚与过度生长现象,进而增强材料的倍率性能以及循环稳定性。然而,当前相关研究存在一些不足,比如缺乏对球磨时长、热处理的温度或者时长等关键参数进行系统性优化,也未能构建起这些参数与碳层质量之间的定量关联。Tripathi团队[21]另辟蹊径,他们先将Na2Fe(SO4)2的前驱体与氧化石墨烯等分散液充分混合,接着借助水热/溶剂热过程或者后续的热处理手段,让Na2Fe(SO4)2材料牢牢锚定在石墨烯片层之上。像石墨烯这类材料,不仅为电子传导搭建了高效的通道,而且其自身具备的柔韧性,还能在材料充放电过程中起到缓冲体积变化的作用,进而延长材料的循环使用寿命。不过,现有的这种合成手段存在一定局限性,难以精准把控纳米颗粒的尺寸大小、分布的疏密程度,以及石墨烯片层的堆叠形态。在实际操作中,纳米颗粒很容易出现团聚现象,或者分布得不够均匀;而石墨烯片层也可能会重新堆叠在一起。这些情况都会对复合结构的整体性能产生不利影响。Islam团队[22]尝试了一种新方法,他们通过引入其他金属离子(如Mn2+、Mg2+等)来部分取代材料中的位点。这一操作能够调节材料的晶体结构和电子结构,在某些情况下,还能引入额外的电荷载流子,或者改变能带结构,进而提升材料自身的本征电导率。然而,目前关于提升本征电导率这一说法,缺乏直接测量本征电导率的数据作为有力支撑。引入高导电性的碳基质,能够搭建起高效的电子传输网络,显著提升材料的整体导电性能[23,24]。其中,碳纳米管(CNTs)作为一种一维纳米碳材料,具备优异的导电性、超大的比表面积以及出色的机械稳定性,是构建三维导电网络的理想之选。分散在基体中的CNTs,就如同一张三维网络,又或是无数根微小的栏杆。它们在物理层面阻隔了新生纳米颗粒的迁移、团聚和融合。在颗粒生长过程中,一旦遇到CNTs的阻碍,就无法自由移动合并成更大的颗粒,从而实现了材料的纳米化。通过将碳纳米管均匀地包覆在Na2Fe(SO4)2纳米颗粒表面,CNTs不仅能为电化学反应提供快速的电子通道,还能抑制Na2Fe(SO4)2纳米颗粒在循环过程中的团聚与生长,进而全面提升复合材料的导电性、结构稳定性和电化学性能[25-28]。
基于此,本研究聚焦于设计并打造一种由碳纳米管包覆Na2Fe(SO4)2(NFS)所构成的复合材料。通过优化合成工艺,促使碳纳米管能够均匀地包覆在Na2Fe(SO4)2的表面。随后,对其作为钠离子电池正极材料时的物相结构、微观形态以及电化学性能展开系统性探究。本研究采用这种复合结构设计,有助于解决Na2Fe(SO4)2材料自身导电性不佳的难题,为开发新一代兼具高性能与低成本特性的正极材料,提供全新的思路以及切实可行的实验参考[29-32]。
1 实验部分
1.1 主要仪器与试剂
ST2742B型四探针粉末电阻率测试仪(中国桂林赛瑞科技有限公司);D8 ADVANCE型X射线衍射仪、D8 25X型X射线光电子能谱仪(德国Bruker公司);Verios 5UC型场发射扫描电子显微镜(广州贝拓科学技术有限公司);PMC-1000-AT型电化学工作站(北京申乾科技有限公司);LAND型电池测试系统(中国武汉金诺电子有限公司)。
七水合硫酸亚铁(FeSO4·7H2O)、抗坏血酸(C6H8O6)(分析纯>99.0%,上海麦克林生化科技股份有限公司);无水硫酸钠(Na2SO4,分析纯 >99.0%,上海阿拉丁生化科技股份有限公司);碳纳米管(江苏天奈科技股份公司)。实验所用去离子水由本实验室自制。
1.2 实验方法
1.2.1 Na2Fe(SO4)2材料的制备
如图1所示,依据Na2Fe(SO4)2化学式中各元素的化学计量比,准确称取2.5235 g(17.66 mmol)Na2SO4、4.9391 g(17.66 mmol)FeSO4·7H2O、0.311027 g(1.7766 mmol)抗坏血酸,将称量好的原料置于洁净的烧杯中,加入200 mL去离子水作为溶剂,在室温条件下持续搅拌60 min,直至所有盐类完全溶解,形成均匀、澄清的水溶液。随后,将该溶液转移至磁力加热搅拌器上,在100 ℃的温度范围内加热并持续搅拌,使水分逐渐蒸发,直至体系由溶液转变为粘稠的溶胶,并最终形成湿凝胶。待多余水分基本去除后,将所得固体初步研磨成粉末。并将其在氩气气氛的管式炉中,升温速率为5 ℃/min升温至200 ℃,保温6 h,自然降温到室温。以彻底去除残留水分。获得干燥的Na2Fe(SO4)2前驱体粉末。最后,将此前驱体置于管式炉中,升温速率为5 ℃/min升温至 350 ℃,流速为200 mL/min的氩气气氛保护下烧结6 h,自然降温到室温,完成结晶过程,最终得到目标产物Na2Fe(SO4)2材料。
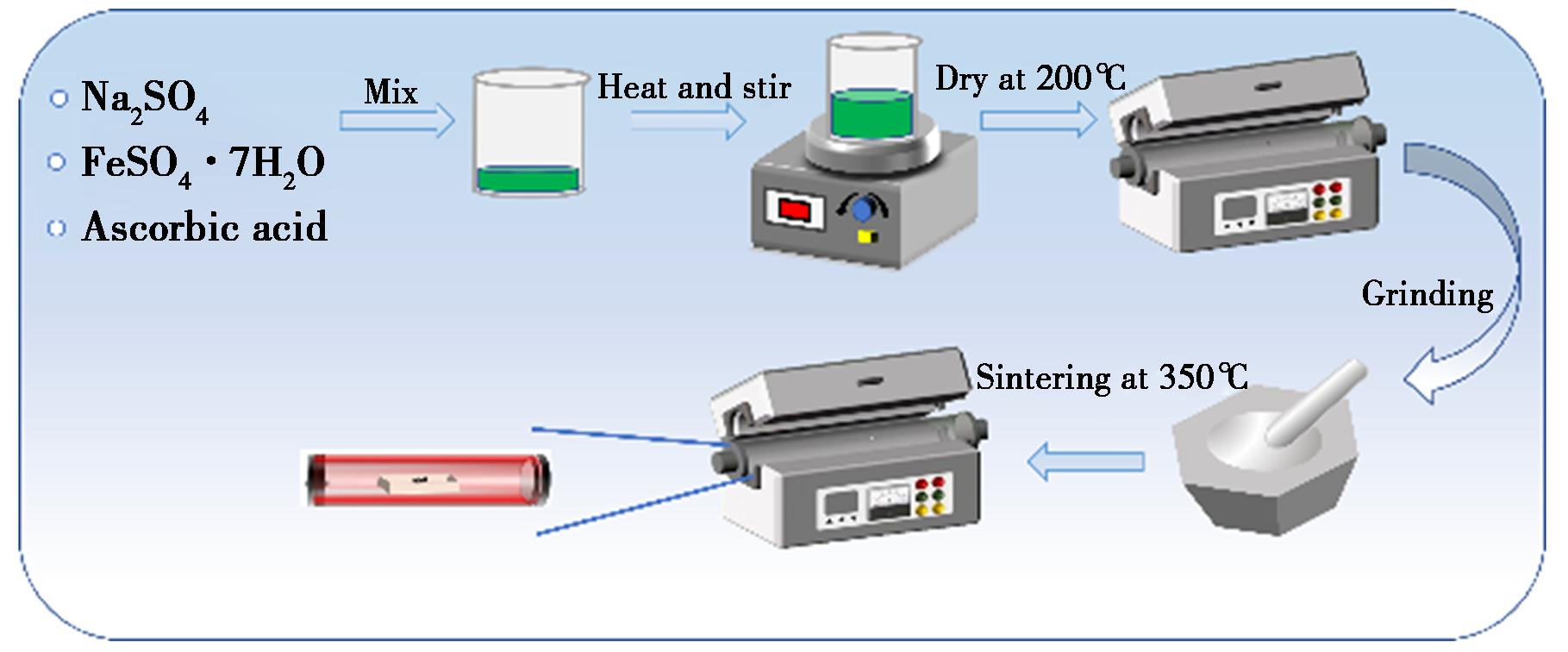
图1 溶胶凝胶法制备Na2Fe(SO4)2材料
Fig.1 Preparation of Na2Fe(SO4)2 material via the sol-gel method
Na2Fe(SO4)2/CNTs材料与上述制备 Na2Fe(SO4)2的方法类似,将上述称量好的盐溶液缓慢倒入已分散好的CNTs悬浮液中,继续搅拌使其充分混合。将混合体系置于磁力加热搅拌器上,在100 ℃下加热并持续搅拌,蒸发多余水分,体系逐渐由溶液转变为含有CNTs的溶胶,并最终形成复合湿凝胶。之后的制备同Na2Fe(SO4)2的过程。最终制得Na2Fe(SO4)2/CNTs复合材料[33]。
1.2.2 表征测试方法
采用以下表征仪器对合成材料的物相、形貌及电化学性能进行系统分析测试:采用X射线衍射仪对材料的晶体结构进行表征。采用Cu Kα辐射源(λ=1.5406 Å),工作电压和电流分别设置为40 kV和40 mA。扫描范围设定为5°至90°(2θ),扫描速度为5°/min。采用场发射扫描电子显微镜观察材料的微观形貌与颗粒尺寸。测试前将少量样品粉末均匀粘附于导电胶上,并在5 kV的加速电压下,于15000和60000倍放大倍数下进行观测。四探针电阻测试采用ST2742B型四探针粉末电阻率测试仪测试材料的电子电导率。将一定质量的粉末样品置于测试腔体中,在7~15 MPa的压力范围内,以1 MPa为步长测量其电阻率随压力的变化关系,以确保测试条件的一致性。电化学测试将所制备的正极材料组装成CR2032型纽扣电池,在室温((25±2) ℃)下进行电化学性能评估。循环伏安(CV)测试使用PMC-1000-AT型电化学工作站,在2.0~4.5 V(vs.Na+/Na)电压窗口内以0.1 mV/s的扫描速率进行。恒电流充放电(GCD)测试使用LAND电池测试系统,在相同的电压窗口内,以0.1 C(1 C=91 mA/g)的电流密度进行循环性能测试。
2 结果与讨论
图2是对Na2Fe(SO4)2前驱体材料进行热重测试,可以发现材料在160 ℃之前的质量损失为7.77%,160~350 ℃时的质量损失为4.57%,分别对应于吸收水和结晶水的去除。结果表明,材料在450 ℃以上分解,失重率为22.25%,这一结果与其他课题组的研究结果一致[19]。
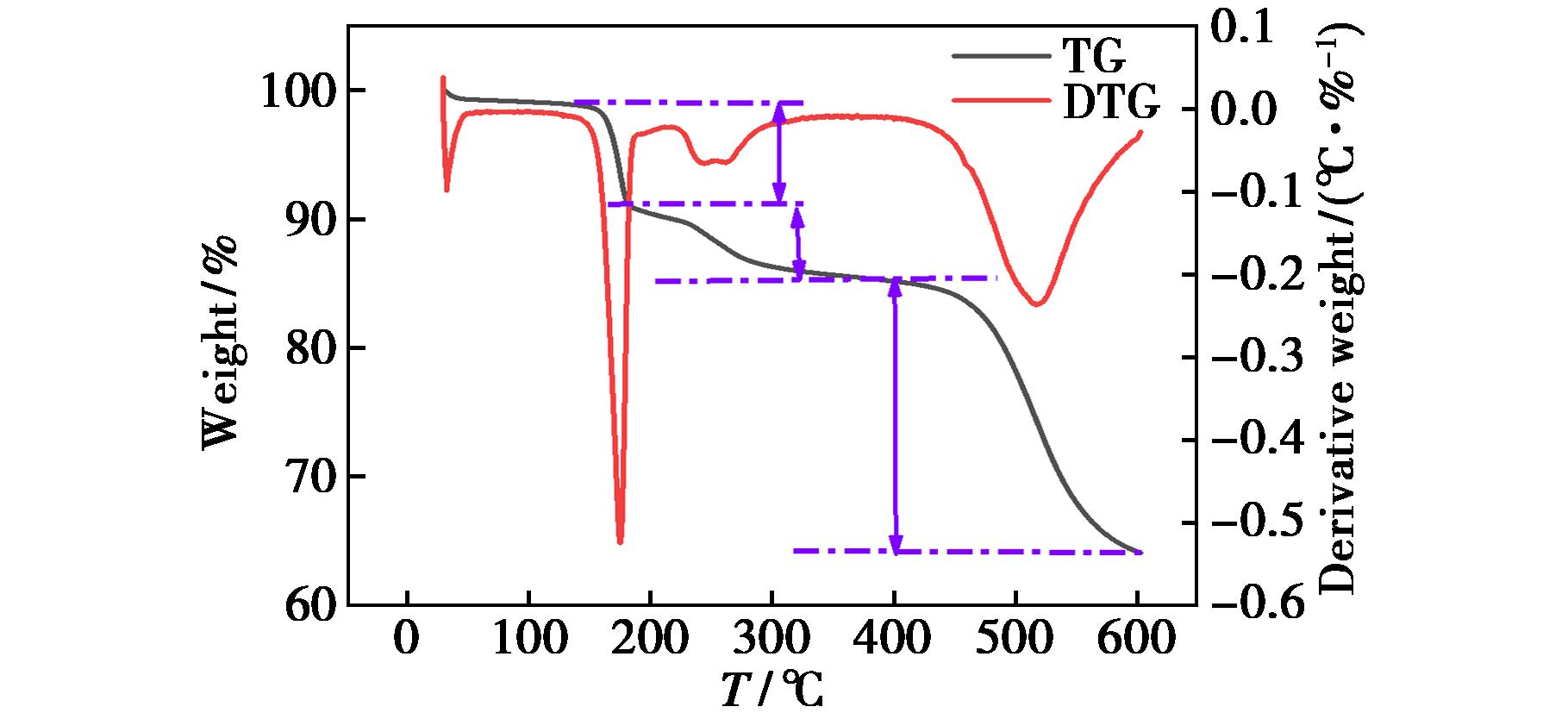
图2 Na2Fe(SO4)2前驱体材料热重测试
Fig.2 Thermogravimetric analysis of Na2Fe(SO4)2 precursor material
图3为Na2Fe(SO4)2与碳纳米管复合形成的Na2Fe(SO4)2/CNTs的XRD图。观察图谱能够发现,这两种材料的主要衍射峰符合Na2Fe(SO4)2的标准卡片(PDF 21-1360),这一结果充分说明目标相已顺利合成。不过,图谱中在特定角度也出现了若干非主相的衍射信号。具体而言,在2θ=10°处存在一个较弱的峰,这大概率是合成过程中产生的微量无定形杂质或者中间相所导致的;在2θ=20°左右的范围,有一个较为明显的衍射峰,这可能与钠离子非化学计量比而产生的微量Na6Fe(SO4)4相关杂相存在关联;而在2θ=30.5°附近出现的肩峰或者独立小峰,则有可能是晶格中局部阳离子有序/无序排列,或者是碳引发的轻微晶格畸变所造成的。值得指出的是,Na2Fe(SO4)2/CNTs图谱中并未观测到CNTs的特征衍射峰。这主要是因为所采用的多壁CNTs结晶度较低,其衍射信号宽化且强度弱;而且CNTs在复合材料中负载量较低,且其微弱衍射信号被主体Na2Fe(SO4)2强烈的结晶衍射峰所掩盖。该现象表明CNTs以高度分散的状态存在于复合材料中,未发生显著团聚,从而有利于构建连续导电网络而不影响活性物质的主体晶体结构。
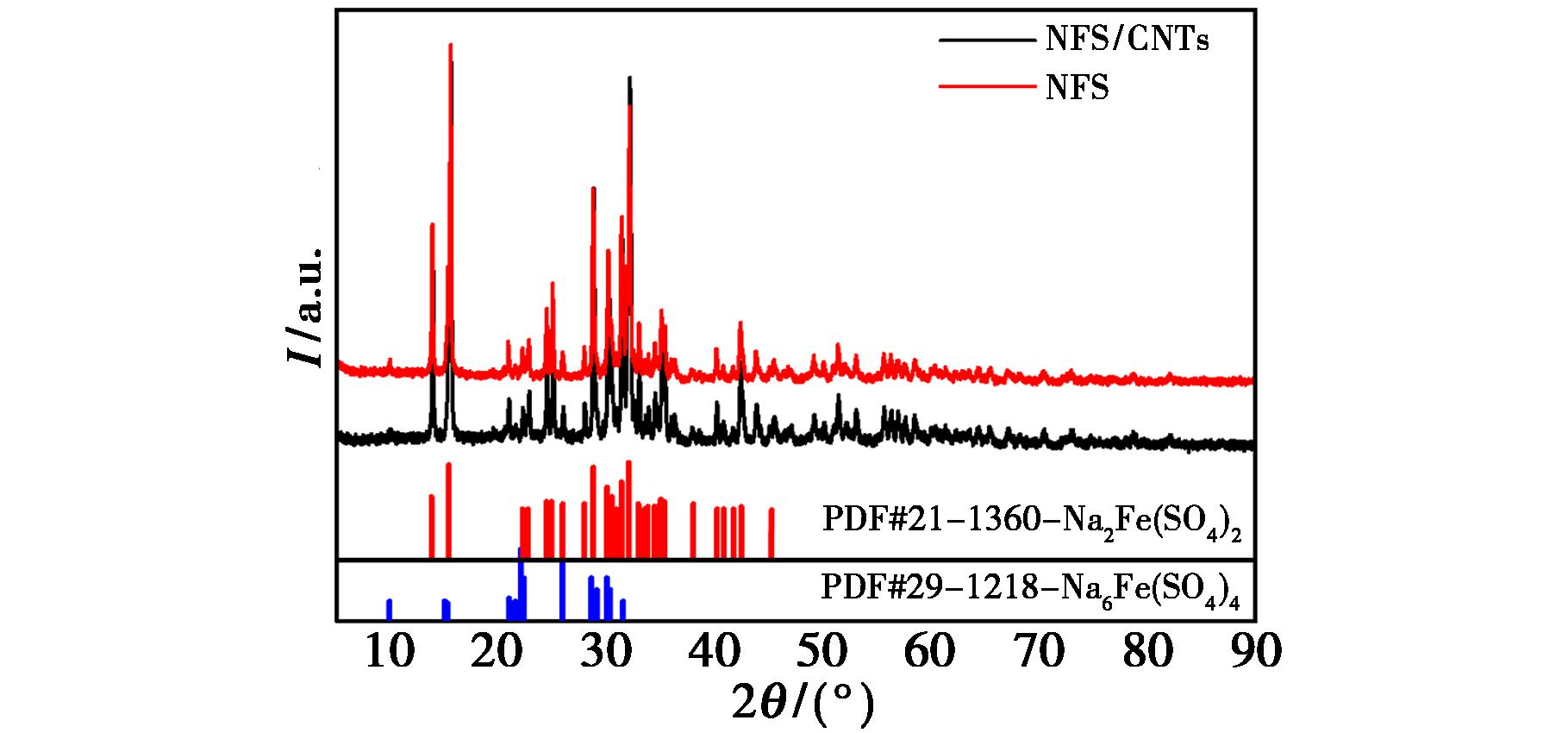
图3 Na2Fe(SO4)2和Na2Fe(SO4)2/CNTs的XRD图
Fig.3 X-ray diffraction patterns of Na2Fe(SO4)2 and Na2Fe(SO4)2/CNTs
利用SEM对材料的微观形貌进行了表征。如图4a所示,从SEM图像中能够观察到,未与碳纳米管复合的Na2Fe(SO4)2样品呈现出不规则的块状形貌。其颗粒尺寸分布范围较大,大致在200 nm~2 μm之间。而且,部分颗粒由于经历了高温处理过程,出现了明显的团聚现象,进而形成了尺寸较大的二次颗粒(图4a)。与之形成鲜明对比的是,加入碳纳米管后的Na2Fe(SO4)2/CNTs复合材料展现出了更为均匀的颗粒分布状态。其颗粒尺寸主要集中在200~500 nm之间(图4c)。通过SEM图像可以清晰地看到,碳纳米管的加入使得材料的粒径有所减小,这也从侧面说明实现了材料的纳米化。此外,在复合材料中还能观察到,碳纳米管在Na2Fe(SO4)2颗粒表面构建起了三维网络结构,这种结构有效地包覆并连接了各个颗粒,从而显著提升了整体材料的电子导电性。为了进一步验证复合材料的元素分布状况,对其进行了EDS面扫描分析(图4e)。分析结果显示,钠(Na)、铁(Fe)、硫(S)、氧(O)以及碳(C)元素在材料中均匀分布。这一结果表明,碳纳米管在复合体系中具有良好的分散性,这有利于构建连续的导电网络,进而改善电极的电化学性能。电极材料的结构完整性是决定其循环稳定性的关键。图4b和4d分别展示了两种电极在5次充放电循环后的SEM图像。从图4b可以观察到,纯Na2Fe(SO4)2颗粒在经历早期的嵌钠/脱钠过程后,出现了明显的破裂与粉化现象,这表明该材料在电化学反应过程中承受了较大的体积应变,导致结构发生不可逆的机械降解。而在同样的循环条件下,Na2Fe(SO4)2/CNTs复合材料(图4d)的颗粒形貌依然保持完整,表面光滑且未观察到明显的微裂纹。结果证明CNTs构建的三维网络结构能够有效缓解循环过程中产生的机械应力,抑制颗粒的粉化与开裂,从而维持电极结构的长期完整性。

图4 Na2Fe(SO4)2材料(a)和Na2Fe(SO4)2/CNTs(c)的SEM图,Na2Fe(SO4)2材料(b)和Na2Fe(SO4)2/CNTs(d)在0.1C倍率下循环5圈后的SEM图,Na2Fe(SO4)2/CNTs中Na、Fe、S、O、C元素分布的EDS能谱图(e)
Fig.4 SEM images of the Na2Fe(SO4)2 material (a) and Na2Fe(SO4)2/CNTs (c);SEM images of the Na2Fe(SO4)2 material (b) and Na2Fe(SO4)2/CNTs (d) after 5 cycles at a rate of 0.1 C;EDS spectra showing the elemental distribution of Na,Fe,S,O,and C in Na2Fe(SO4)2/CNTs(e)
图5是Na2Fe(SO4)2和Na2Fe(SO4)2/CNTs材料CV曲线的对比情况。图5a中,未添加碳纳米管的Na2Fe(SO4)2材料,其CV曲线仅显现出Fe2+/Fe3+这一对氧化还原峰,而且曲线的积分面积相对较小。这一现象表明,该材料自身具备的电化学活性较为有限,在反应过程中出现的极化程度较高。与之形成对比的是,Na2Fe(SO4)2/CNTs复合材料的CV曲线(图5b)有着不同的表现。其中,Fe2+/Fe3+所对应的氧化还原峰明显增强,峰与峰之间的间距有所缩小。这充分说明,由碳纳米管构成的导电网络,有效降低了电极的极化程度,加快了电荷的传输速度以及反应的动力学进程。此外,复合材料的CV曲线面积大幅增大,这与后续在恒电流充放电测试中所观察到的更高放电容量这一趋势相契合。这一结果进一步证实,引入碳纳米管能够提升材料的电化学性能。
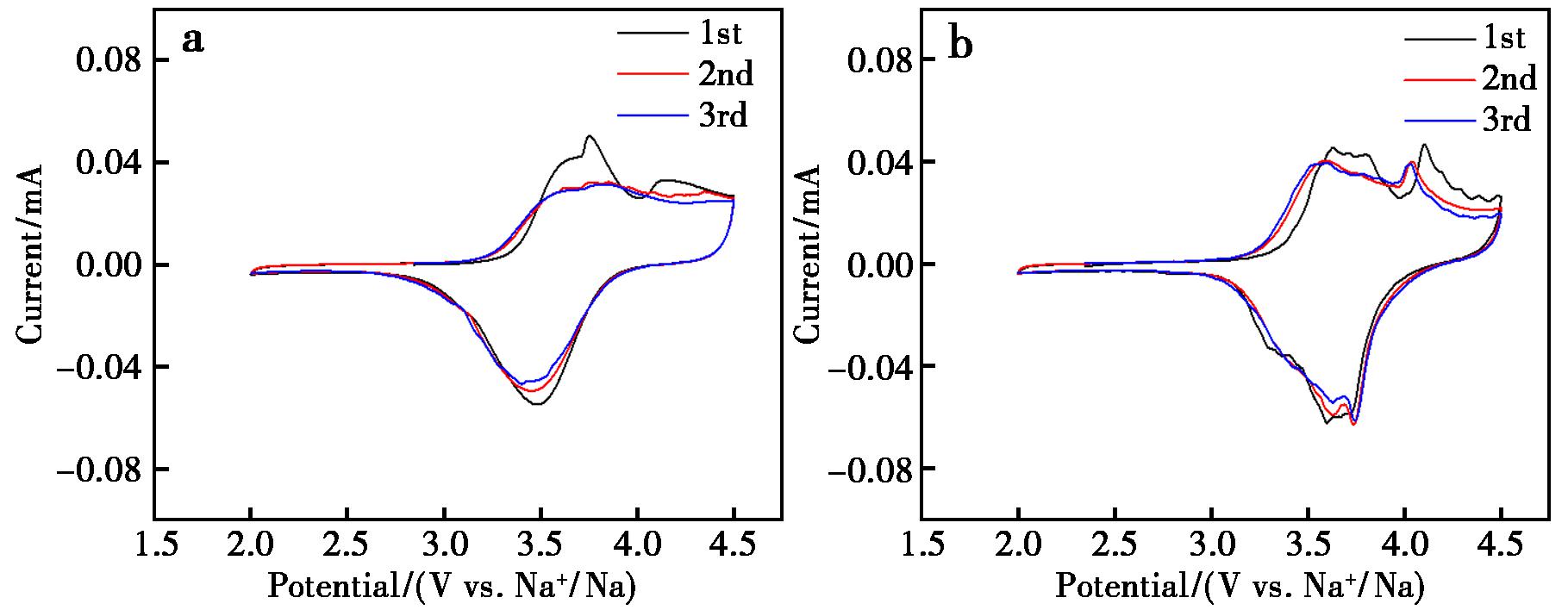
图5 Na2Fe(SO4)2(a)和Na2Fe(SO4)2/CNTs(b)材料的前3圈循环伏安曲线
Fig.5 First three cycles of cyclic voltammetry curves for Na2Fe(SO4)2 (a) and Na2Fe(SO4)2/CNTs material (b)
图6展示了Na2Fe(SO4)2和Na2Fe(SO4)2包覆碳纳米管复合材料的电导率测试数据。实验结果显示,纯相Na2Fe(SO4)2材料的电导率极低,在15 MPa压力下的电导率仅为3.39×10-9 S/cm,这直接表明其自身电子导电能力极弱会严重阻碍电极反应时电荷的传输,成为制约其在钠离子电池等电化学储能领域实际应用的关键阻碍。为有效提升材料的电子导电性,研究采用了碳纳米管包覆的方法,成功制备了Na2Fe(SO4)2/CNTs复合正极材料。电导率测试结果显示,在相同测试条件下,Na2Fe(SO4)2/CNTs材料的电导率达到了9.65×10-3 S/cm,与纯相材料相比,导电性能提高了6个数量级。这主要是因为碳纳米管在活性物质颗粒之间构建起了高效的三维电子导电网络,为电子的快速传输提供了通道,极大地增强了复合电极整体的电子传输动力学。碳纳米管的引入,不仅从根本上改善了材料的导电性,其独特的力学性能和结构特性还可能对电极的结构稳定性起到增强作用。在电池循环过程中,它能够缓冲体积应变,为复合材料后续展现出优异的倍率性能和长循环稳定性奠定了关键的物理基础。需指出的是,纯相Na2Fe(SO4)2自身电子电阻率较高(109 Ω·cm),这是限制其电化学活性的根本因素。而碳纳米管在活性物质颗粒表面及间隙所形成的连续、高导通的网络结构,进一步保障了电子传输的高效性。该网络为电子传输提供了很好的传输路径,使得电极内部的电子能够快速抵达每一个活性颗粒表面,大幅降低了电荷转移阻抗。电化学测试结果(图7)为上述机理提供了直接证据,显著降低的极化过电位反映了改善的电极反应动力学;接近100%的库仑效率表明了高度可逆的钠离子脱嵌过程;而在高倍率下依然可观的比容量,则直观地证明了该材料具备满足快速充放电应用的巨大潜力。
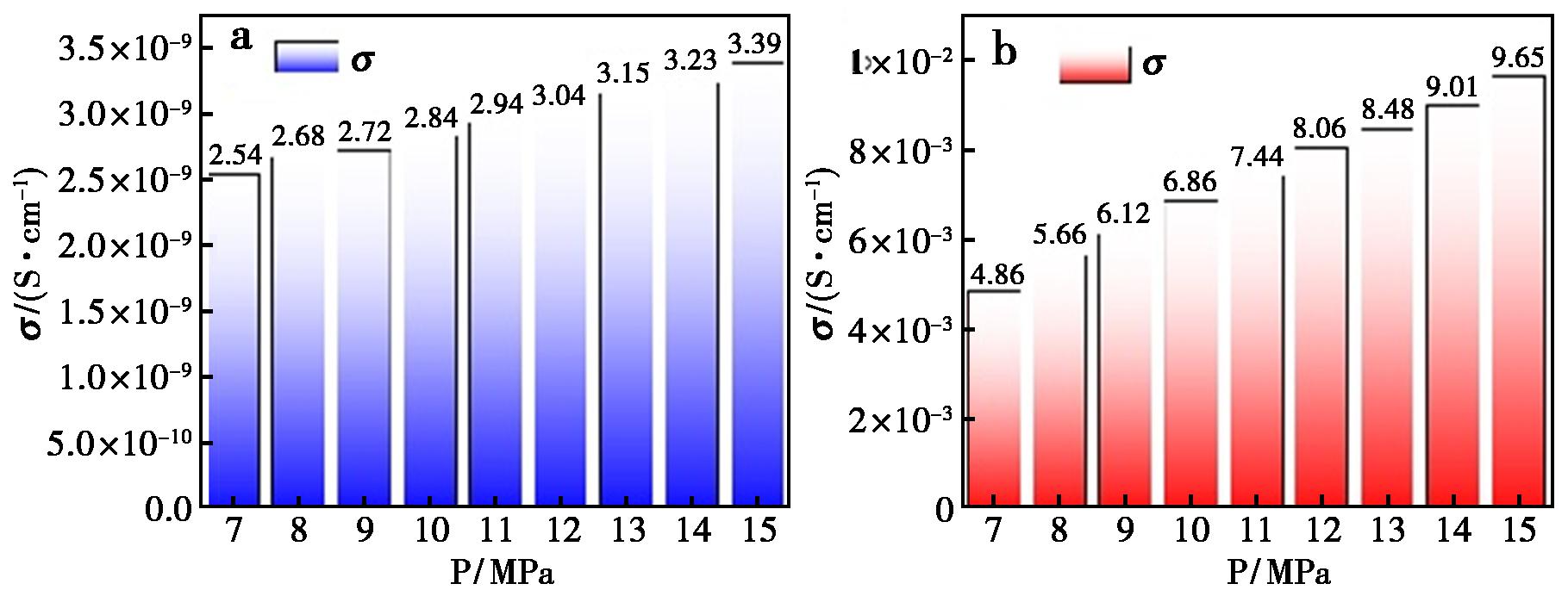
图6 Na2Fe(SO4)2(a)和Na2Fe(SO4)2/CNTs材料(b)的电导率柱状图
Fig.6 Electrical conductivity histograms of Na2Fe(SO4)2 (a) and Na2Fe(SO4)2/CNTs composite material (b)
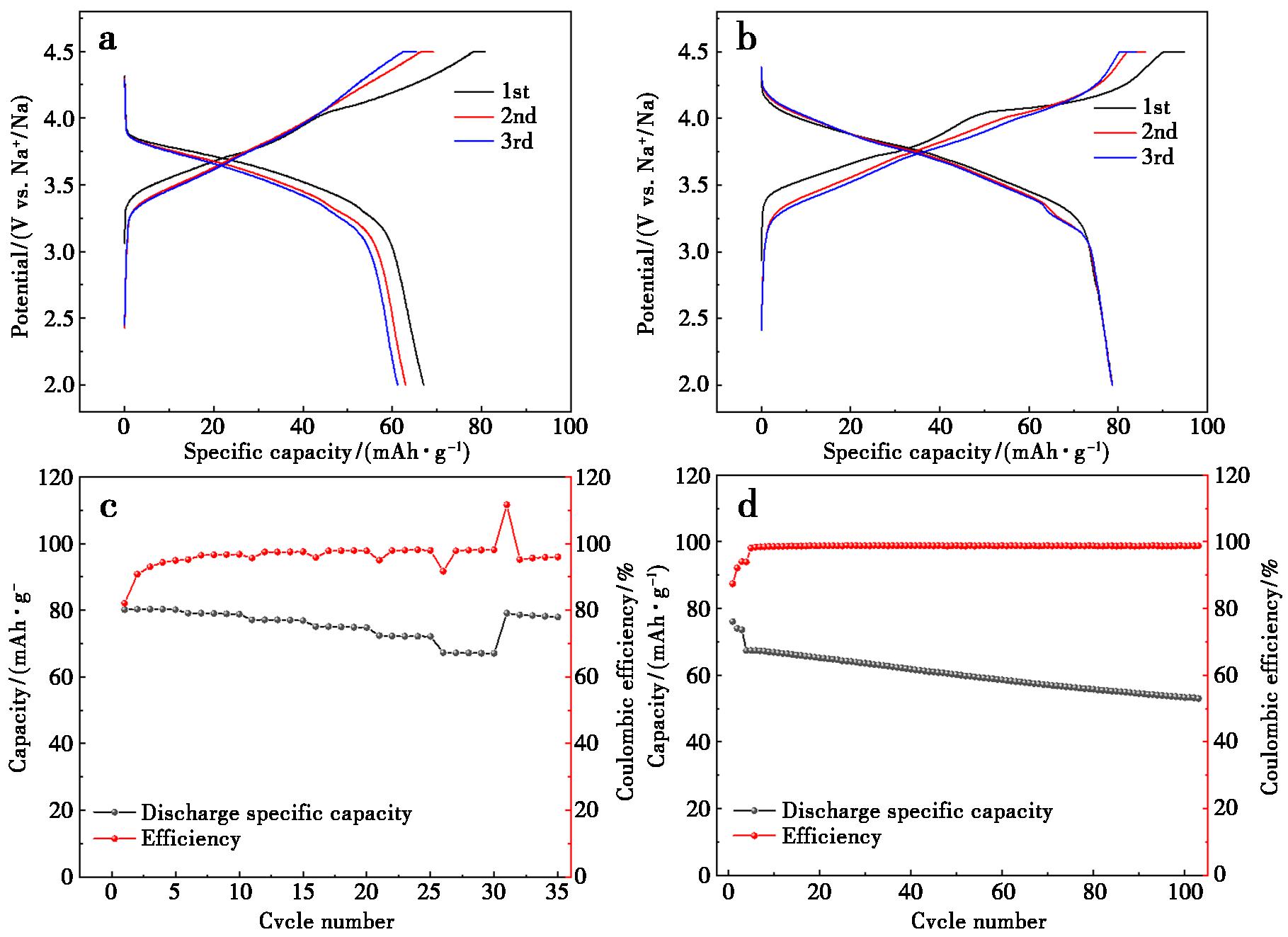
图7 Na2Fe(SO4)2(a)和Na2Fe(SO4)2/CNTs(b)材料的前3圈充放电曲线图;Na2Fe(SO4)2/CNTs材料的倍率性能图(c);Na2Fe(SO4)2/CNTs材料100次循环性能图(d)
Fig.7 First three charge-discharge cycles of Na2Fe(SO4)2 (a) and Na2Fe(SO4)2/CNTs (b) material,Rate performance of Na2Fe(SO4)2/CNTs material(c),Performance of Na2Fe(SO4)2/CNTs material after 100 cycles (d)
图7a和7b分别是Na2Fe(SO4)2及其与Na2Fe(SO4)2/CNTs复合材料在0.1 C(1 C=91 mA/g)电流密度下的前3圈恒电流充放电曲线。纯相Na2Fe(SO4)2的首圈放电比容量为67.06 mAh/g(图7a),其较低的可逆容量主要是因为材料本征电子电导率不足,导致活性物质利用率受限。在后续循环中,该材料表现出较明显的容量衰减,第3圈放电容量下降至61.22 mAh/g,容量保持率为91.3%,表明在钠离子脱嵌过程中可能存在不可逆相变或其它副反应,加剧了容量损失。相比之下,Na2Fe(SO4)2/CNTs复合正极(图7b)的首圈放电比容量显著提升至78.73 mAh/g,证明碳纳米管构建的导电网络有效促进了电子传输,提高了活性材料的电化学利用率。更值得注意的是,该复合材料展现出优异的循环可逆性,第3圈放电容量仍维持在78.68 mAh/g,容量保持率高达99.9%,远优于纯相材料。这表明CNTs的包覆不仅改善了电极的导电性,还有效缓冲了循环过程中的体积应变,抑制了副反应的发生,从而显著提升了材料的结构稳定性与循环性能。图7c为Na2Fe(SO4)2/CNTs在2~4.5 V电压窗口内的倍率性能测试结果。材料在0.1 C倍率下的初始放电容量为80.23 mAh/g。随着电流密度逐步升高至0.2、0.5、1、2及5 C,电极仍表现出良好的倍率特性,在5 C高倍率下容量保持在67.31 mAh/g左右。当电流密度恢复至0.1 C后,容量可恢复至79.09 mAh/g,相当于初始容量的98.57%,说明材料结构在高倍率充放电后仍保持高度可逆,CNTs的引入显著增强了电极的动力学性能与结构稳定性。进一步考察了Na2Fe(SO4)2/CNTs在2~4.5 V宽电压范围内循环100圈的长循环稳定性(图7d)。经过CNTs包覆改性后,材料循环性能得到显著改善,100圈循环后容量保持率达78.7%。此外,复合材料在循环初期表现出较低的容量衰减,说明CNTs的包覆不仅有效提升了电极的循环寿命,也抑制了活性物质在高压下的不可逆分解,减少了初始容量损失。
为了深入研究碳纳米管包覆硫酸铁钠材料前后的钠离子反应动力学的特性,采用电化学阻抗谱(EIS)对电池材料进行了阻抗测试并运用公式(1)[34]进行了扩散系数的计算,结果如表1所示。图8展示了Na2Fe(SO4)2与Na2Fe(SO4)2/CNTs复合材料的EIS图。高频区域的半圆代表电荷转移电阻,低频区域的直线则代表活性材料固相中Na+扩散引起的韦伯阻抗(Warburg)。通过Zview2软件拟合得到的两种正极材料NFS和NFS/CNTs的电荷转移电阻Rct值为1134和347.5 Ω,所拟合的等效电路如图8中的插图所示。
DNa+=0.5R2T2A-2n-4F-4C2σ-2
(1)
表1 NFS和NFS/CNTs电极的电荷转移电阻及钠离子扩散系数
Tab.1 Charge transfer resistance and sodium ion diffusion coefficient of NFS and NFS/CNTs electrodes
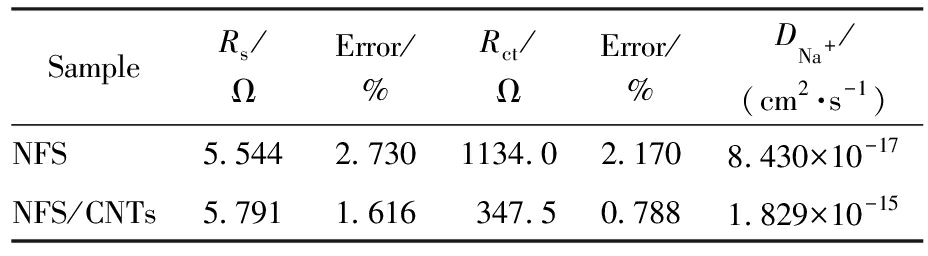
SampleRs/ΩError/%Rct/ΩError/%DNa+/(cm2·s-1)NFS5.5442.7301134.02.1708.430×10-17NFS/CNTs5.7911.616347.50.7881.829×10-15
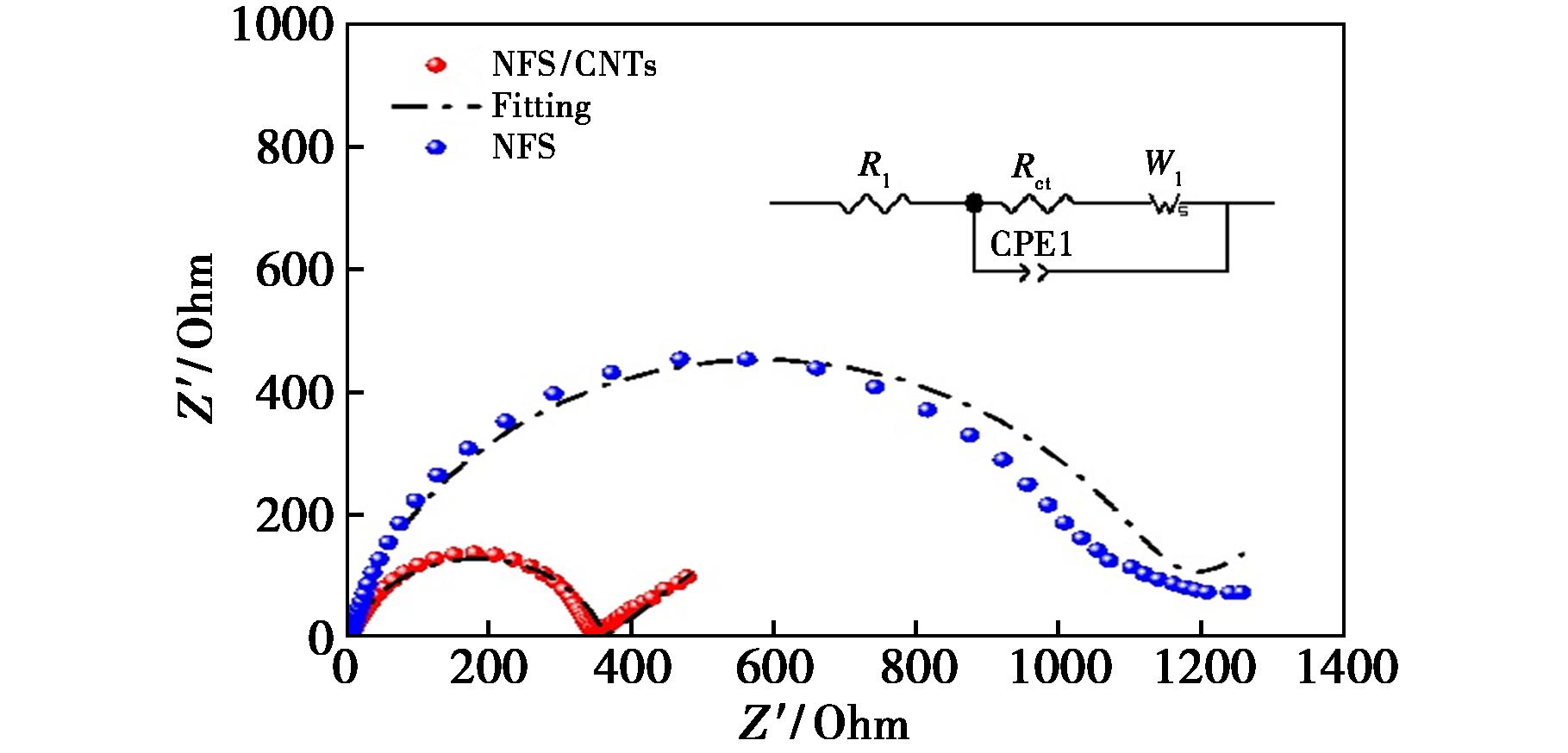
图8 Na2Fe(SO4)2和Na2Fe(SO4)2/CNTs材料的阻抗图
Fig.8 Impedance plots of Na2Fe(SO4)2 and Na2Fe(SO4)2/CNTs materials
式中,A为电极的表面积1.5386 cm2;n为参与电子转移反应的每个分子的电子数(n=1);F为法拉第常数96485;C为Na2Fe(SO4)2电极中钠离子的浓度,可由材料的晶胞体积计算得到0.086 mol/cm3;R为气体常数8.314 J/(K·mol);T为实验的室温298.13 K;σ是 Warburg系数。由阻抗测试得到的低频区实部阻抗与角频率ω-0.5拟合得到的直线斜率K(KNFS/CNTs=35.498,KNFS=164.86)。
由上述公式计算得到的两种正极材料NFS和NFS/CNTs的钠离子扩散系数为8.430×10-17和1.829×10-15cm2/s,说明碳纳米管包覆后材料表现出最低的电荷转移电阻和较快的离子传输速度,减小了钠离子的扩散阻力。表明钠离子扩散加速且嵌钠/脱钠过程中界面副反应减弱。与样品Na2Fe(SO4)2相比,Na2Fe(SO4)2/CNTs的样品Rct值显著减小,表明电荷转移电阻降低,这有利于Na+快速扩散并提升材料的倍率性能。
3 结论
本研究创新性地采用碳纳米管(CNTs)包覆策略,成功制备出具备三维导电网络强化的Na2Fe(SO4)2/CNTs复合正极材料。通过一系列的测试与表征,深入探究了材料的微观结构与电化学性能。结果表明:
3.1 CNTs以高度分散的状态,均匀地包覆在Na2Fe(SO4)2颗粒的表面。这一包覆过程并未改变Na2Fe(SO4)2的主体晶体结构,成功构建起连续的电子传导路径,Na2Fe(SO4)2/CNTs复合材料电导率提升至10-3 S/cm(提高了6个数量级),为电子的快速传输提供了保障。
3.2 电化学性能测试数据证明了该复合材料具有良好的性能。首圈放电比容量由纯相的67.06 mAh/g提高至78.73 mAh/g;在5 C高倍率下仍保持67.31 mAh/g的可逆容量;在2~4.5 V电压窗口循环100圈后容量保持率达78.7%。
3.3 CNTs不仅大幅增强电子/离子传输动力学,还有效抑制颗粒团聚、缓冲体积应变,从而提升了材料的结构稳定性与电化学性能。CNTs包覆策略简单且高效。它能够在不破坏活性物质本征结构的前提下,系统性地改善聚阴离子型正极材料本征电导率低、反应动力学缓慢等问题。这一策略不仅极大地提升了材料的电化学性能,还为其他具有类似低电导特性的电极材料的结构设计与性能优化提供了思路,对推动高性能、低成本钠离子电池正极材料的研发进程具有积极而深远的意义。
[1]Huang L P,Huang Y X,Wang J X,Lin J R,Xu J L,Yin Z J,Wang X,Li M,Shi X Y,Shao L Y,Sun Z P.ACS Appl.Mater.Interfaces,2025,17(38):53659-53669.
[2]Feng W L,Shen T D.Chin.J.Power Sources,2013,37(11):2063-2066.
冯卫良,沈同德.电源技术,2013,37(11):2063-2066.
[3]Ma X H,Yang J W,Ye J.Guangdong Chem.Ind.,2013,40(8):60-61,52.
马晓华,杨建文,叶璟.广东化工,2013,40(8):60-61,52.
[4]Pan M S,Lin Z F,Ge Y L.Shandong Chem.Ind.,2025,54(1):79-81;84.
盘茂森,林泽锋,葛雅莉.山东化工,2025,54(1):79-81;84.
[5]Dong Z,Wei Y H,Jia Y,Qu L.Chin.J.Power Sources,2025,49(6):1111-1117.
董溱,魏远航,贾雨,屈龙.电源技术,2025,49(6):1111-1117.
[6]Duan L L,Duan Y J,You C G.Technol.Dev.Chem.Ind.,2025,55(1):49-53.
段莉莉,段艺杰,游晨光.化工技术与开发,2025,55(1):49-53.
[7]Li L.Preparation and Performance Study of Layered Transition Metal Iron-Based Cathode Materials for Sodium Ion Batteries.Guangzhou:Guangdong University of Technology,2023.
黎伦.钠离子电池层状过渡金属铁基正极材料的制备及性能研究.广州:广东工业大学,2023.
[8]Lin C G.Investigation on P2/O3 Biphase Layered Cathode Materials for Sodium-Ion Batteries.Xiamen:Xiamen University of Technology,2024.
林春钢.P2/O3复合相钠离子电池层状正极材料的研究.厦门:厦门理工学院,2024.
[9]Wang H,Li H,Sun D,Tang Y,Xiang S,Zhang X.Acta Chimica Sinica,2025,83(8):947-961.
[10]Jin Y X,Zhou Q,Zhou L,Gao T,Li Z J,Wang Y,Lu J L.Energy Storage Sci.Technol.,2025,14(11):4184-4198.
金宇玄,周权,周琳,高腾,李子杰,王琰,卢俊龙.储能科学与技术,2025,14(11):4184-4198.
[11]Chen C J,Li J H.Chem.Adhes.,2025,47(5):581-618.
陈婵娟,李建华.化学与粘合,2025,47(5):581-618.
[12]Li X S,Liang J,Cao X,Zhu S Y,Bai Y F,Sun J W,Luo H B,Kong J.Rare Met.,2025,44(5):2871-2899.
[13]Jiang R,Lin J R,Shi X Y,Zheng B T,Huang Q F,Xu J L,Shao L Y,Sun Z P,Zhang Q Q,Hang L F.J.Mater.Chem.A,2025,13:22047-22056.
[14]Shi C L,Muhtar D,Lu X Y,Liu F Q,Lu X,Sun Z P,Guo Z P.Adv.Energy Mater.,2025,15(26):2500448.
[15]Shi C L,Xu J L,Tao T,Lu X Y,Liu G P,Xie F Q,Wu S,Wu Y X,Sun Z P.Small Meth.,2024,8(3):2301277.
[16]Barpanda P,Oyama G,Nishimura S I,Chung S C,Yamada A.Nat.Commun.,2014,5(1):4358.
[17]Wang Y R,Yang Y,Nie Y L,Wang Q,Liu S,Wang Q.J.Energy Storage,2024,83:110629.
[18]Watcharatharapong T,Thienprasert J,Barpanda P,Ahuja R,Chakraborty S.J.Mater.Chem.A,2017,5(41):21726-21739.
[19]Pan W L,Guan W H,Liu S Y,Xu B B,Liang C,Pan H G,Yan M,Jiang Y Z.J.Mater.Chem.A,2019,7(21):13197-13204.
[20]Mao J F,Zhou T F,Zheng Y,Gao H,Liu H K,Guo Z P.J.Mater.Chem.A,2018,6(8):3284-3303.
[21]Tripathi R,Ramesh T N,Ellis B L,Nazar L F.Angew.Chem.Int.Ed.,2010,49(46):8738-8742.
[22]Islam M S,Driscoll D J,Fisher C A J,Slater P R.Chem.Mater.,2005,17(20):5085-5092.
[23]Yang W,Liu Q,Hou L J,Yang Q,Mu D B,Tan G Q,Li L,Chen R J,Wu F.Small,2024,20(5):2306595.
[24]Yang W,Liu Q,Yang Q,Lu S J,Lv H J,Liu T,Li L,Chen R J,Wu F.Nano Energy,2025,141:111075.
[25]Liu Y,Sun C,Ni Q,Sun Z,Li M,Ma S,Jin H B,Zhao Y J.Energy Storage Mater.,2022,53:881-889.
[26]Li M,Sun C,Yuan X Y,Li Y,Yuan Y F,Jin H B,Lu J,Zhao Y J.Adv.Funct.Mater.,2024,34(21):2314019.
[27]Liu X H,Tang L B,Xu Q J,Liu H M,Wang Y G.Electrochim.Acta,2019,296:345-354.
[28]Yin F X,Liu Z J,Zhao Y,Feng Y T,Zhang Y G.Nanomaterials,2017,7(9):253.
[29]Guo J Z,Wan F,Wu X L,Zhang J P.J.Mol.Sci.,2016,32(4):265-279.
郭晋芝,万放,吴兴隆,张景萍.分子科学学报,2016,32(4):265-279.
[30]Yang D Z.Research on Advanced Cathode Materials for Sodium Ion Batteries.Shanghai:Shanghai Jiao Tong University,2016.
杨德志.高性能钠离子电池正极材料研究.上海:上海交通大学,2016.
[31]Wang Q,Jiang Z L,Yu C,Li L P,Li G S.Chin.Chem.Lett.,2025,36(6):110006.
[32]Yao G,Zhang X X,Yan Y L,Zhang J Y,Song K M,Shi J,Mi L W,Zheng J Y,Feng X M,Chen W H.J.Energy Chem.,2020,50:387-394.
[33]Fang Y J,Liu Q,Feng X M,Chen W H,Ai X P,Wang L G,Wang L,Ma Z Y,Ren Y,Yang H X,Cao Y L.J.Energy Chem.,2021,54:564-570.
[34]Wang X Y,Hao H,Liu J L,Huang T,Yu A S.Electrochim.Acta,2011,56(11):4065-4069.