在全球天然药物旺盛需求的背景下,中药材及其制剂的应用不断扩大。中药分析是中药药理、药效研究的基础,同时也是中药质量控制的关键环节之一[1]。但中药成分复杂、来源分散、工艺差异显著、多靶点的复杂体系给中药活性成分检测、质量评价和质量控制带来了挑战。现有色谱、质谱等分析方法在成分确证与定量方面优势突出,但样品前处理、检测周期与设备成本使其难以满足现场检测和生产过程在线监测需求。
拉曼光谱(Raman Spectroscopy,RS)可以反映单一或混合体系的结构特征,能够提供分子特异性强的“指纹”谱峰,在物质的定性和定量分析中起着十分重要的作用[2]。然而,自发拉曼光谱存在信号强度弱的短板[3]。表面增强拉曼光谱(Surface-Enhanced Raman Spectroscopy,SERS)可以通过纳米金属表面局域等离子体热点显著增强拉曼信号,进一步拓展至痕量成分与污染物的快速检测。该技术凭借其分子指纹识别的高特异性、高灵敏度、高准确度、快速无损和不受水分干扰等独特优势脱颖而出[4]。SERS的出现不仅催生了化学和生物学的一个全新的研究领域,而且开辟了作为一种超灵敏分析工具的广泛应用,包括疾病诊断、生物标记物检测、细胞成像和治疗监测[5]。
SERS技术也为中药的安全评价和质量控制提供一个简便、快速、低成本、无损检测的平台。将SERS与高效液相色谱、薄层层析、化学和物理萃取、相萃取等分离技术相结合,可以极大地促进其在中药质量控制中的实际应用[6,7],为中药现代化质量控制提供新的技术路径。本文综述了中药分析面临的挑战、传统方法的局限及SERS在中药分析中的研究进展及应用。
1 表面增强拉曼光谱
1.1 基本原理
拉曼散射源于入射光子与分子的振动/转动自由度发生能量交换,导致散射光频率相对入射光发生偏移,从而形成可表征分子结构与化学键的“振动指纹谱”[8]。拉曼光谱强度一般只有入射激发辐射强度的10-8倍[9],在复杂天然产物中常被荧光背景与谱峰重叠掩盖,限制痕量组分的直接检测[10]。
SERS通过将分析物置于金/银纳米结构的局域表面等离子共振(Local Surface Plasmon Resonance,LSPR)近场,在纳米间隙产生“热点”,可将拉曼信号放大数个数量级以实现痕量检测[11]。增强由电磁机制与化学机制共同决定,包括电磁增强(Electromagnetic Enhancement,EM)与化学增强(Chemical Enhancement,CM),通常以EM为主[12,13],但二者共同决定最终信号的强度和选择性。表面增强拉曼光谱的原理示意图如图1所示。
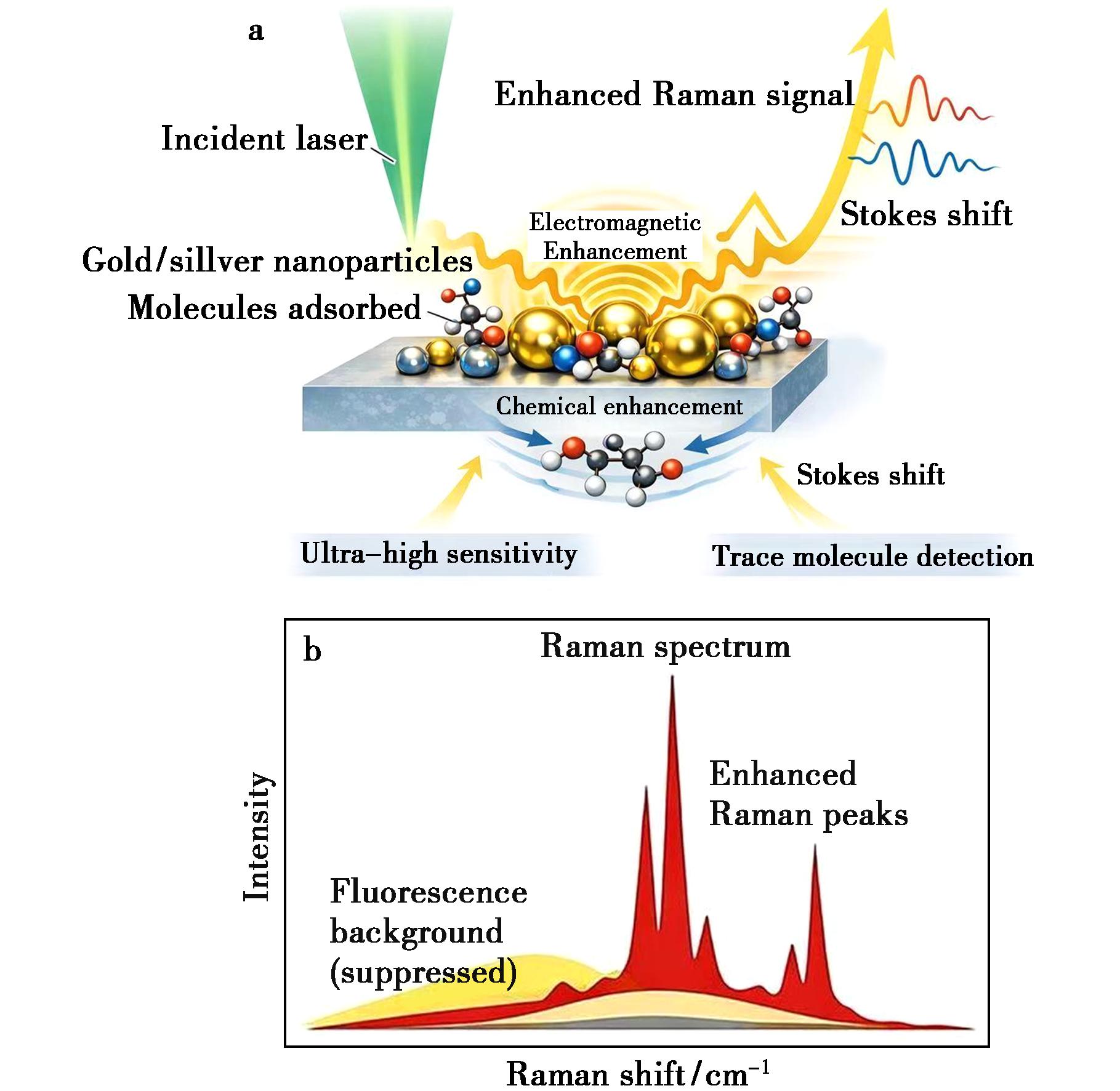
a.Schematic illustration of electromagnetic and chemical enhancement mechanisms in SERS;b.Schematic illustration of the enhancement effect in SERS spectroscopy
图1 表面增强拉曼光谱的原理示意图
Fig.1 Schematic illustration of the principle of surface-enhanced Raman spectroscopy
由于为近场效应,SERS信号对分子-金属距离敏感,复杂基质中常需表面功能化、富集或可控纳米腔以降低基底竞争吸附与批间差的干扰[14,15]。SERS与普通常规拉曼、尖端增强拉曼(Tip-Enhanced Raman Spectroscopy,TERS)存在本质区别:普通拉曼指纹性强但灵敏度低;SERS通过近场放大解决了痕量检测问题;TERS则将增强局域于纳米尺度探针尖端,适用于微区成分分布与界面机理研究[10,16]。
1.2 技术优势与局限性
SERS兼具拉曼的“峰窄-指纹”特性与显著的灵敏度提升,且易与纸基/柔性基底、微流控、富集分离及算法模型集成,从而适应复杂样品的快速指纹筛查与现场检测[17,18]。
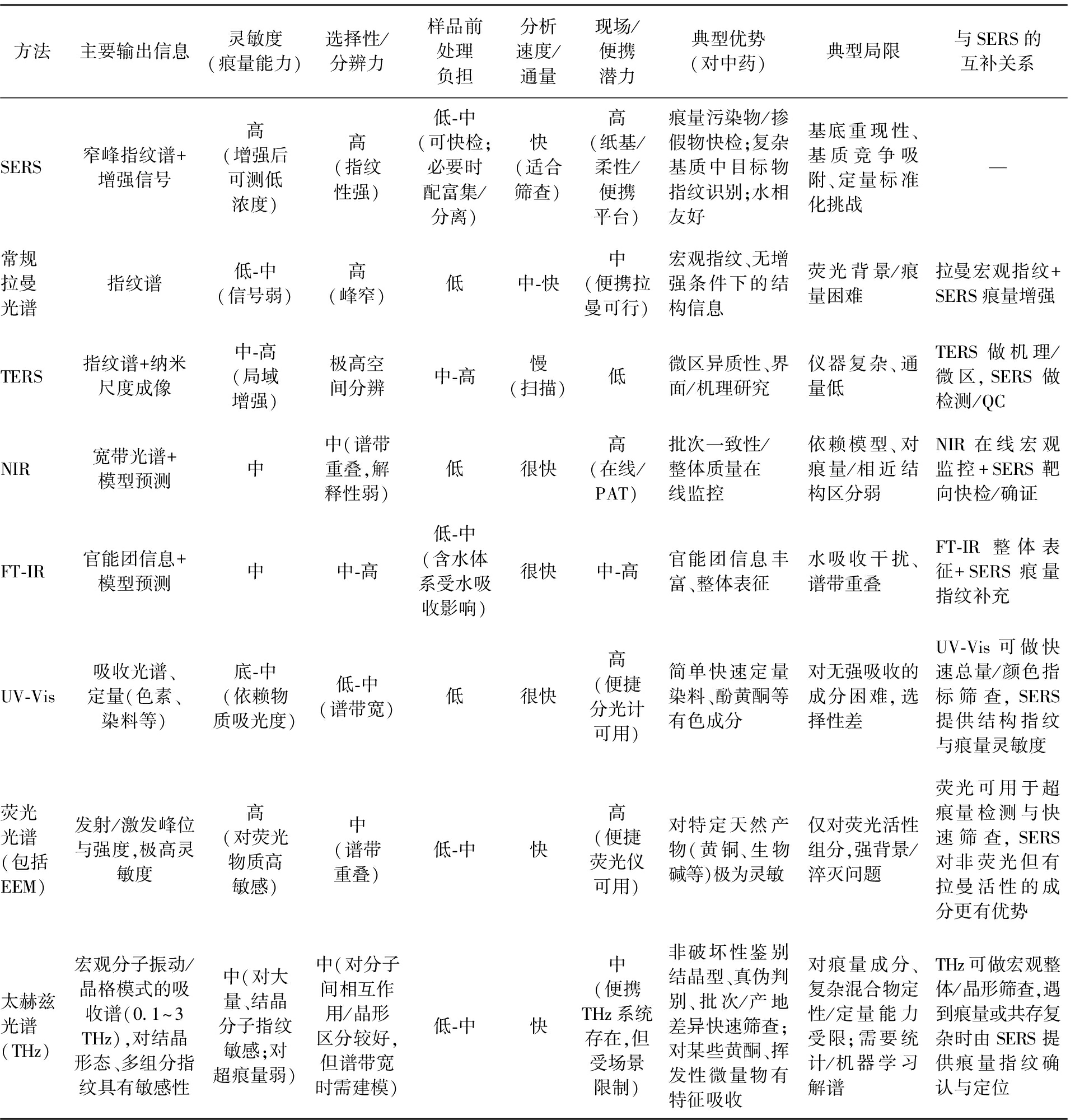
SERS与不同光谱技术比较如表1所示。SERS能较快获得高度指纹性的窄峰光谱并显著提高痕量物检出限,故很适合中药类复杂样品的现场快速筛查[19,20]。相较常规拉曼,SERS在灵敏度和痕量识别上占优;相较TERS,SERS更适合工程化与大样本应用,TERS主要用于纳米尺度机理研究[21];相较近红外光谱(Near-infrared Spectroscopy,NIR)/傅里叶变换红外光谱(Fourier Transform Infrared Spectroscopy,FT-IR),SERS在指纹分辨力与痕量能力上占优,NIR/FT-IR在无损在线与整体性质评估上占优。由于NIR吸收带重叠严重、难以直接解释,因此需要化学计量学手段辅助[22,23],且含水体系对FT-IR会带来显著干扰,而对拉曼光谱干扰较小[24]。二者组合可形成NIR/FT-IR做在线宏观监控,SERS做异常点位的靶向快检的分层质控体系[18];与LC-MS/MS或GC-MS等色谱-质谱联用技术相比,SERS提供快速现场决策能力,而色谱-质谱为法规级的分离、结构确证与准确定量手段。与太赫兹光谱(Terahertz,THz)相比,THz擅长识别药材的晶型、结晶度和批次整体指纹,适合对整批样品进行快速宏观筛查,但对极痕量成分敏感性较差且含水样品有强背景干扰。因此常采用“THz宏观筛查→色谱富集/分离→SERS痕量鉴定→LC-MS验证”的串联策略以发挥互补优势。此外,紫外-可见光谱(UV-Visible Spectrum,UV-Vis)与荧光/激发-发射矩阵(Excitation-Emission Matrix,EEM)等经典光谱法在速度与对特定有色或荧光活性组分的灵敏检测上具有实用性,但选择性和适用性有限。因此未来工作应聚焦于便携一体化读出、减少或免前处理的快速无损检测、可批量生产且重现性高的标准化SERS基底以提升定量可靠性、与NIR/FT-IR及色谱-MS的多模态融合及机器学习判读工作流等。
表1 各光谱分析方法与SERS的对比
Tab.1 Comparative analysis of spectroscopic techniques with SERS
方法主要输出信息灵敏度(痕量能力)选择性/分辨力样品前处理负担分析速度/通量现场/便携潜力典型优势(对中药)典型局限与SERS的互补关系SERS窄峰指纹谱+增强信号高(增强后可测低浓度)高(指纹性强)低-中(可快检;必要时配富集/分离)快(适合筛查)高(纸基/柔性/便携平台)痕量污染物/掺假物快检;复杂基质中目标物指纹识别;水相友好基底重现性、基质竞争吸附、定量标准化挑战—常规拉曼光谱指纹谱低-中(信号弱)高(峰窄)低中-快中(便携拉曼可行)宏观指纹、无增强条件下的结构信息荧光背景/痕量困难拉曼宏观指纹+SERS痕量增强TERS指纹谱+纳米尺度成像中-高(局域增强)极高空间分辨中-高慢(扫描)低微区异质性、界面/机理研究仪器复杂、通量低TERS做机理/微区,SERS做检测/QCNIR宽带光谱+模型预测中中(谱带重叠,解释性弱)低很快高(在线/PAT)批次一致性/整体质量在线监控依赖模型、对痕量/相近结构区分弱NIR在线宏观监控+SERS靶向快检/确证FT-IR官能团信息+模型预测中中-高低-中(含水体系受水吸收影响)很快中-高官能团信息丰富、整体表征水吸收干扰、谱带重叠FT-IR整体表征+SERS痕量指纹补充UV-Vis吸收光谱、定量(色素、染料等)底-中(依赖物质吸光度)低-中(谱带宽)低很快高(便捷分光计可用)简单快速定量染料、酚黄酮等有色成分对无强吸收的成分困难,选择性差UV-Vis可做快速总量/颜色指标筛查,SERS提供结构指纹与痕量灵敏度荧光光谱(包括EEM)发射/激发峰位与强度,极高灵敏度高(对荧光物质高敏感)中(谱带重叠)低-中快高(便捷荧光仪可用)对特定天然产物(黄铜、生物碱等)极为灵敏仅对荧光活性组分,强背景/淬灭问题荧光可用于超痕量检测与快速筛查,SERS对非荧光但有拉曼活性的成分更有优势太赫兹光谱(THz)宏观分子振动/晶格模式的吸收谱(0.1~3 THz),对结晶形态、多组分指纹具有敏感性中(对大量、结晶分子指纹敏感;对超痕量弱)中(对分子间相互作用/晶形区分较好,但谱带宽时需建模)低-中快中(便携THz系统存在,但受场景限制)非破坏性鉴别结晶型、真伪判别、批次/产地差异快速筛查;对某些黄酮、挥发性微量物有特征吸收对痕量成分、复杂混合物定性/定量能力受限;需要统计/机器学习解谱THz可做宏观整体/晶形筛查,遇到痕量或共存复杂时由SERS提供痕量指纹确认与定位
尽管SERS具备显著优势,但仍有一定局限性,如基底/信号重现性差、定量化与校准策略不足、复杂基质干、金属基底稳定性问题以及便携设备与谱库/数据处理标准化欠缺[25]。未来亟需在以下方面实现突破:规模化/标准化SERS基底与性能规范、统一的定量校准与方法学验证规范、与微流控或快速净化技术耦合的一体化便携检测平台、提升金属基底的抗氧化与长期稳定性、开放共享的标准光谱数据库与跨实验室比对体系以推动监管化部署[26-28]。
1.3 数据处理方法
将SERS应用于中药分析的关键是把“复杂基质+荧光背景+基底/热点波动”的原始谱转为可复现、可验证、可迁移的定性/定量结论。流程为:实验设计→预处理→建模→模型转移,并需防范数据泄漏、过拟合与批次漂移[13,19],流程如图2所示。
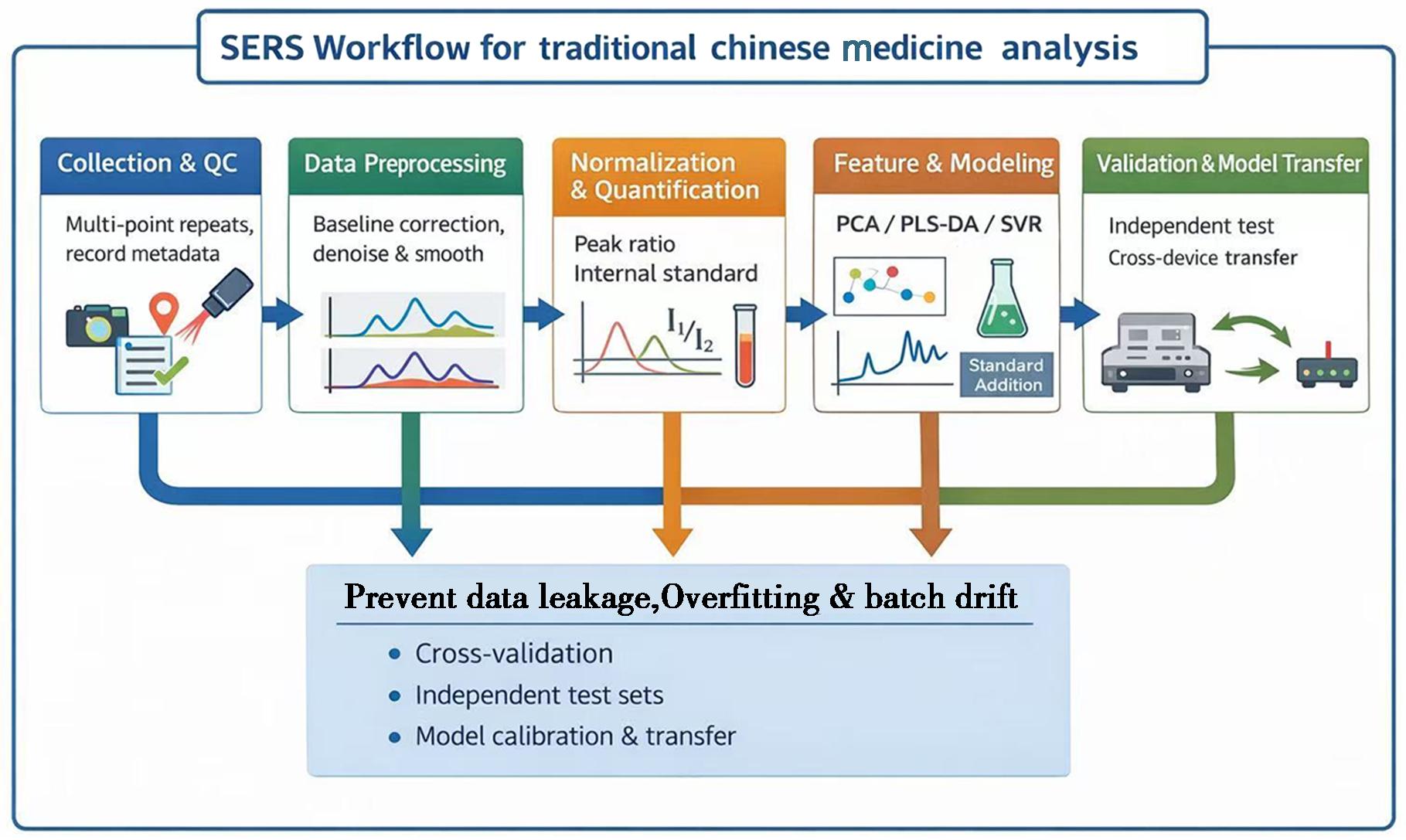
图2 中药分析的SERS数据处理流程图
Fig.2 Flowchart of SERS data processing for traditional Chinese medicine analysis
1.3.1 采集与质控
采集应多点重复并以均值/中位数或分位数汇总,随机化采集顺序,完整记录温湿度、激光功率、积分时间及基底批次等元数据,以便识别与校正系统漂移并支持模型迁移与外部验证[19,24]。
1.3.2 预处理
中药体系最关键的是“基线或荧光”与“强度漂移”的处理。基线校正为先行步骤:常用自适应迭代重加权惩罚最小二乘法进行自动基线拟合与剔除[22]。非对称最小二乘以速度快、参数少适合常规校正[23]。而基于滑动自适应窗口的分段多项式拟合在速度与精度间折中可选[29]。此外需去尖刺、去噪/平滑(如Savitzky-Golay)与波数对齐,但要避免过度平滑,以免改变峰形与峰面积[30]。
1.3.3 归一化与定量策略
SERS强度受热点分布、吸附态与局部环境影响,定量常结合归一化与内标策略:全谱建模可用向量或面积归一化;严格定量宜用峰比、内标或标准加入以增强可追溯性与跨条件一致性[31]。
1.3.4 特征构建与建模
鉴别类任务先用主成分分析技术(Principal Components Analysis,PCA)探索,继而采用偏最小二乘判别分析(Partial Least Squares Discriminant Analysis,PLS-DA)、支持向量机(Support Vector Machine,SVM)、随机森林等分类方法;定量常用偏最小二乘回归(Partial Least Squares Regression,PLSR)、支持向量回归(Support Vector Regression,SVR)。深度学习可直接处理全谱,但需更严格的验证与大样本以防虚高性能[31]。
1.3.5 验证与模型迁移
模型外推性为落地关键。除交叉验证外,应尽量使用独立外部测试集(不同批次/不同日/不同基底)评估性能衰减,并开展跨设备与跨基底的校准与迁移研究,将模型迁移纳入方法学规范以推动应用转化[19]。
2 表面增强拉曼光谱技术在中药分析中的应用
2.1 中药鉴别
2.1.1 真伪鉴别
SERS技术能够敏锐捕捉掺伪物质的特征信号,在打击中药染色、掺假方面效果显著。目前的研究中对于中药的真伪鉴别主要是通过设计功能化基底以此增强识别或者与分离技术联用来消除干扰。前者适合用于现场检测,后者适用于实验室中。张彩虹[32]以Au@Ag NFs为基底,将SERS用于大黄中成药中土大黄苷掺伪的快速定性定量检测。在染色掺假方面,张彬彬等[33]建立薄层色谱法-SERS联用技术检测染色西红花,成功检出多种染料。李丹等[34]建立纸基SERS方法用于鉴别染色红花。Li等[35]构建银纳米颗粒功能化滤纸擦拭纸SERS基底对多种染料具有极低的检测限。Jiang等[36]利用缺陷Cu2O纳米结构实现了草药提取物中苏丹红III选择性检测。Zhang等[37]建立SERS结合机器学习实现了对石斛中金胺O(Auramine O)的精准预测及模型迁移。对于珍贵药材冬虫夏草,孙佳慧等[38]采用SERS结合化学计量学方法可成功将冬虫夏草与3种蛹虫草分为两类。
目前SERS真伪鉴别面临标准谱库缺失的瓶颈,缺乏覆盖常见掺伪物及其结构类似物的标准化SERS指纹数据库。建立标准化SERS谱库,并结合深度学习算法实现未知掺伪物的自动识别,是未来的重点方向。此外,当前研究多集中于单一掺伪物的检测,而实际市场中掺伪往往是多种物质的混合,发展多目标同时识别的方法更具现实意义。
2.1.2 产地与年份鉴别
产地与年份鉴别的本质是捕捉药材次生代谢产物随环境或时间变化的“化学指纹漂移”,SERS的高灵敏度使其能够感知这些细微变化。黄浩等[39]采用拉曼光谱耦合主成分分析-偏最小二乘判别分析对5个产地300批次黄芪饮片建立分类模型,判别准确率高且特异性良好。对陈皮等地理标志药材,吴越等[40]整合非靶标代谢组学与纳米传感技术,开发了双通道荧光可视化传感器,实现了对广陈皮、川陈皮及其他产地的快速鉴别,并开发了便携式纸基传感器,针对白术设计双通道比色传感器,实现白术与苍术及不同产地白术的可视化区分。对于含有荧光成分的药材,Du等[41]开发新型Ag@Cs纳米粒子SERS基底,可明显区分20个样品并基于PCA评价不同来源质量。针对野生与栽培冬虫夏草的区分难题,Liu等[42]采用SERS结合机器学习算法区分野生与栽培冬虫夏草,准确率达98.95%
在年份鉴别方面,杨方等[43]采用SERS技术检测8种储存年份陈皮,金膜-银纳米颗粒基底效果最佳,通过12处的特征峰可区分不同年份,发现储存7年以上陈皮较5年及以下产生新成分。Dai等[44]进一步利用SERS结合PCA-LDA对陈皮年份进行精准分类,发现1607 cm-1处的峰强度与年份呈显著负相关,分类准确率超过90%,为陈皮“陈久者良”的质量评价提供了光谱学证据,检测结果如图3所示。
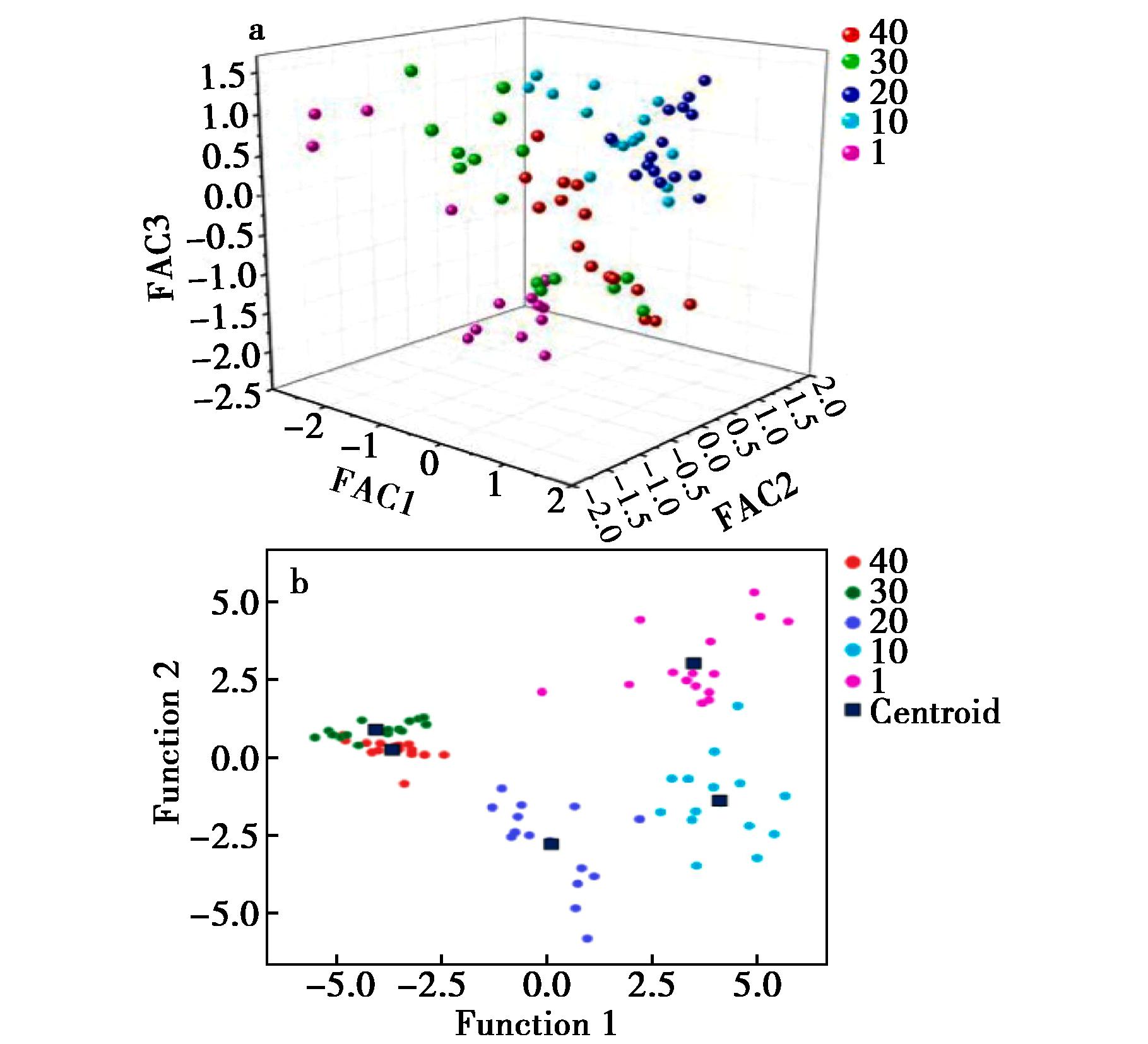
a.3D scatter plot of the PCA scores for the PCR samples in different age groups;b.Scatter plot of PCA-LDA scores for the PCR samples in different age groups.Function 1 or 2 was interpreted as linear discriminant component of 1 or 2
图3 不同储存年限陈皮样品SERS光谱的主成分分析(PCA)[44]
Fig.3 Principal component analysis (PCA) of the SERS spectra of PCR samples with different storage ages[44]
目前的研究中模型验证多通过交叉验证,缺乏独立外部测试集评估。建议未来增加独立外部测试集评估,同时可引入迁移学习技术,将已有模型作为起点,通过少量目标域样本进行微调,降低跨批次、跨仪器的建模成本。
2.2 中药检查
2.2.1 中药内源性毒物快速筛查
中药中的内源性毒性成分是影响其用药安全的关键因素。谈铭等[45]建立了QuEChERS前处理结合SERS快速检测药酒中乌头碱的方法,检测限达10 mg/kg。Lin等[46]开发了Ag-APS纳米颗粒通过酰胺键特异性富集马兜铃酸I,检测限达40 nmol/L,成功检出4种含马兜铃酸中药中的马兜铃酸I残留。通过化学修饰在基底表面引入特异性识别基团,实现对目标毒物的选择性富集。
当前研究多聚焦于单一毒物,实际用药中往往是多种毒物共同存在。未来应发展能够同时捕获和识别多类毒物的多功能SERS基底,另一个值得关注的问题是中药提取物中的大量共存成分可能干扰识别基团与毒物的结合,甚至导致假阴性。建议在方法学验证中增加复杂基质加标回收实验,并采用LC-MS/MS进行结果比对,以客观评估方法的准确性和适用性。
2.2.2 中药外源性污染物检测
外源性污染物检测是SERS在中药安全性评价中应用最为广泛的领域。任菲等[47]针对薏苡仁中黄曲霉毒素G1,建立动态SERS检测方法,检测限5.5 μg/kg。在微生物检测方面,朱晓英[48]构建的功能化纳米材料SERS平台可同时检测6种致病菌,检测限均小于10 CFU/mL。刘艺丹等[49]通过SERS利用4-巯基苯硼酸监测甘草、海藻、黄连饮片霉变过程中微生物数量的动态变化。
中药种植过程中的农药残留是影响其安全性的另一重要问题。Zhang等[50]针对延胡索中氯氰菊酯残留,建立了改良的QuEChERS技术结合SERS方法,利用双波段建立偏最小二乘回归模型,检测限达到0.484 mg/L。储冰妍等[51]对铁皮石斛中多菌灵和甲基托布津进行定性和定量检测,揭示混合农残中的分子竞争效应。Zhu等[52]受荷叶乳突结构启发制备仿生Ag/PDMS柔性透明薄膜,实现对石斛表面农药的原位检测。Meenakshi等[53]将石墨烯-金纳米复合材料涂覆于保鲜膜,检测出积雪草粉末中氯吡虫啉,检测限达0.1 mg/kg。Sun等[54]利用SERS标记技术追踪了纳米农药在人参植株体内的迁移与分布,为评估其安全性提供了新视角。
对于真菌毒素和微生物检测,SERS的灵敏度已可满足限量要求,但实际样品的基质效应往往被低估。建议在方法学验证中增加复杂基质(如不同产地、不同炮制方法的药材)的加标回收实验,并引入质谱法进行结果比对。对于农药残留物的检测,目前多残留同步检测方法尚不成熟,竞争吸附问题的系统解决方案缺失。未来应研究不同农药的吸附行为,构建抗干扰的多残留同步检测平台。
2.2.3 非法添加物的识别
打击中药中非法添加化学药物或漂白剂是保障临床安全的重要任务。胡然等[55]建立了分子印迹聚合物-SERS联用方法检测中药中非法添加的茶碱,检出限低至0.1 μg/L。针对SO2残留,Dong等[56]开发的顶空-薄膜微萃取-SERS联用技术,在25~400 mg/kg范围内呈良好线性关系,检测限为6 mg/kg。Fan等[57]开发Si@Ag@PEI复合膜SERS传感器结合3D打印装置,可在15 min内快速检测SO2,检测限低于药典标准。Lu等[58]开发的比率型SERS传感器配合手持设备,实现了SO2残留的现场定量检测,原理示意图如图4所示。
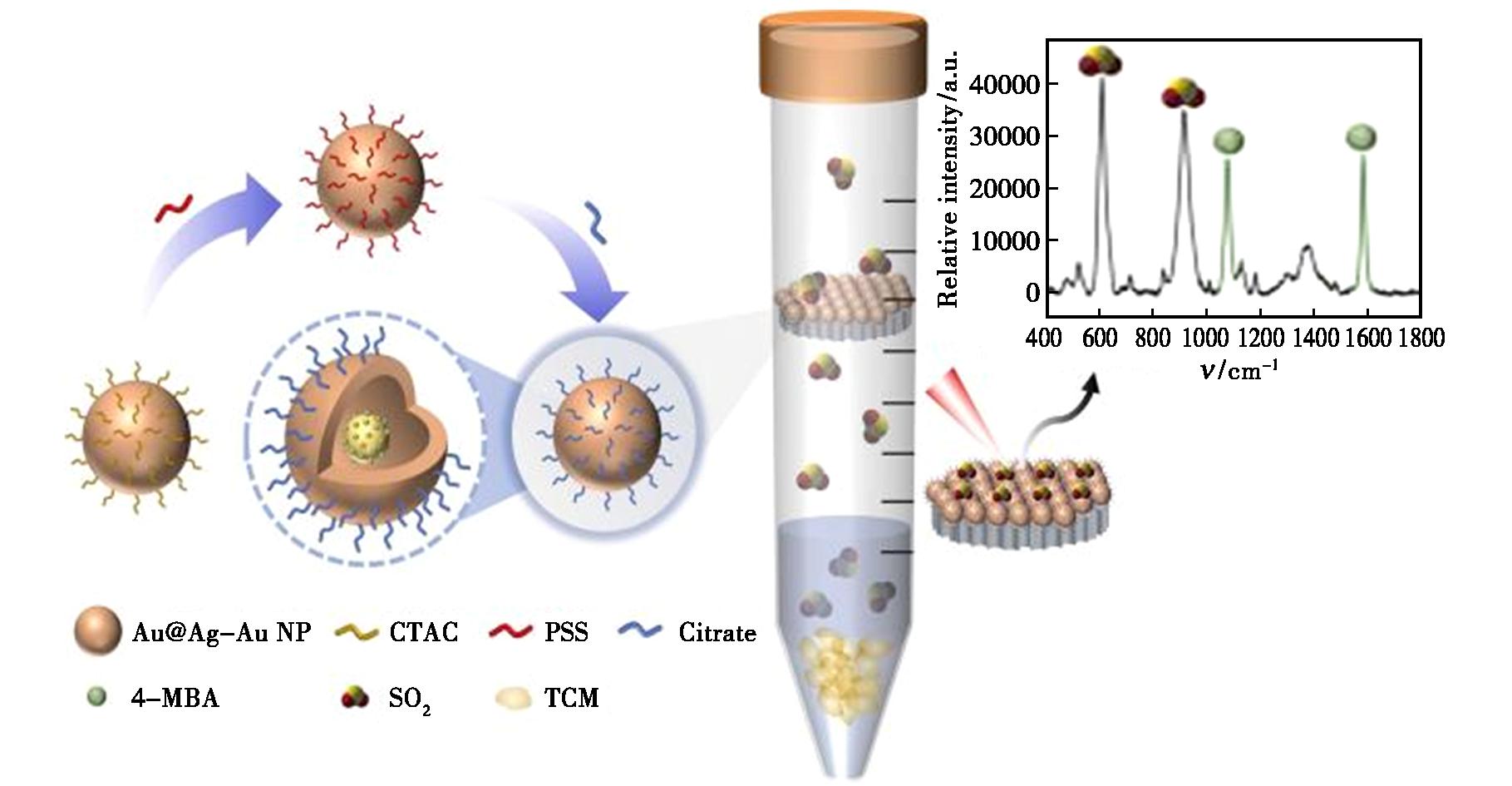
图4 比率型SERS传感器检测中药中SO2的原理示意图[58]
Fig.4 Schematic diagram of rationetric SERS sensor for detecting SO2 in Chinese herbal medicines[58]
目前分子印迹聚合物-SERS联用,从根本上解决SERS基质干扰问题,但分子印迹技术的制备过程繁琐、模板依赖性强,限制了高通量应用。未来可探索虚拟模板印迹技术实现一类物质的广谱识别。
2.3 中药含量检测
2.3.1 中药活性成分检测
SERS技术通过银纳米溶胶、金/银复合基底等增强效应,显著提升了中药复杂体系的检测灵敏度。无需复杂提取,直接对药材粉末或简单提取物进行SERS检测,可获得其独特的化学指纹图谱。Huang[59]等首次实现白术片的SERS快速检测。谭炜[60]等采用银溶胶分析桑皮苷成分,建立了快速检测方法。Zhou等[61]构建Ag@SiO2@Cu@蛾翅光栅状核壳平台,实现大枣皂苷A等皂苷的无标记检测,并结合机器学习算法可区分不同药效物质。采用SERS检测黄芪,可区分药材的不同部位,并检测到皂苷类特征信号[62]。Xie[63]等以黄连为模型鉴定14种生物碱特征峰,明确活性成分在木质部与韧皮部的富集规律。白术[64]、党参[65]药材煎剂的研究揭示了活性成分与纳米基底的电荷转移增强机理。采用SERS技术分析鱼腥草汤剂[66]可获得13个特征峰,而常规拉曼光谱几乎无响应,充分体现SERS对弱散射体系的高灵敏检测优势。胡琰[67]等建立红花注射液SERS快速鉴别法,实现注射液的质量控制。针对基质干扰严重的药材,如对三七粉末及药材水提、醇提物直接检测,所得信号微弱,经薄层色谱法分离后的单一组分可获得理想的SERS光谱,实现皂苷类成分无标化快速鉴别[68]。
SERS在中药活性成分检测中多数研究停留在定性或半定量层面,对检测方法的批间重现性、定量准确性等关键性能指标评估不足,不同研究使用的基底、仪器、参数各异,结果难以直接比较和复现。未来应聚焦于基底标准化推动高活性基底的批量化制备与商业化供应,提升重现性与准确性。
2.3.2 痕量药效物质的检测
通过设计高性能的SERS基底可实现中药微量活性成分的分析。例如设计Au@Ag核壳纳米颗粒结合可控聚集,实现黄连素比色-SERS双模式传感,SERS检测限达0.10 μmol/L,该方法中结构相似的原小檗碱类生物碱无交叉干扰[69]。Yuan等[70]以镍泡沫为模板磁控溅射制备Ag-NF-20基底,实现青蒿素检测限至10-4 ng/mL。基于蜻蜓翅膀模板的Ag@V-Ti@D.W复合基底[71]和DVD光栅的Ag/V-Ti/DVD基底[72],使绿原酸、连翘苷的检测限分别达到10-6和10-7 g/L级别。Cui等[73]设计磁控溅射制备Ag/V-Ti基底,苦杏仁苷检测限低至10-8 g/L,并用机器学习进行分类。
SERS对于痕量物质检测的提升主要是对基底结构的精密可控,且实现了基底工程与算法辅助的深度融合,这也是未来痕量检测的发展方向。同时也应关注基底在复杂基质中性能状况,系统评估基底在真实中药样品中的检测能力。
2.3.3 中药活性成分的定量研究
SERS技术也可以实现中药活性成分的准确定量。Zhao等[74]以小檗碱为模型化合物,结合密度泛函理论计算与液相色谱-质谱进行交叉验证,实现了小檗碱的灵敏、快速、无损定性与定量检测。Li等[75]构建的TiO2@AgNP核壳纳米复合超结构,成功实现对刺五加中4种结构相似黄酮类成分的同时区分与定量,检出限达到10-5~10-6 mol/L,信号与浓度呈现良好线性关系。
目前研究中实现了单一组分定量与多组分同时定量。SERS定量目前最大的挑战是信号重现性问题。未来SERS定量研究应重点关注:(1)内标法的标准化应用,建立强制性的内标校正规范,使不同研究的结果具有可比性;(2)方法学验证的规范化,系统报告检测限、定量限、线性范围、精密度、回收率等指标。
2.4 中药整体质量评价与作用机制研究
2.4.1 中药复方配伍规律研究
SERS技术可为中药复方“君臣佐使”配伍理论提供可视化证据。Zhou等[76]采用SERS结合光栅状基底与机器学习实现中药复方“泽泻-白术汤”的超灵敏检测,对复方及单味药的分类准确率达97.78%,揭示配伍过程中成分相互作用。活血化瘀汤研究发现,全方与分煎药队存在差异,证实复方并非单味药的简单加和,而是发生了成分转化或新物质生成[77]。狼疮Ⅱ号方的分析量化了配伍相互作用:发现了协同、拮抗效应及配伍专属新峰[78]。
SERS通过比较全方与拆方的光谱差异,为配伍规律研究提供了可视化证据。但当前研究多停留在现象描述,未能阐明差异成分的化学本质及其药效关联,未来应实现从表征到机理的深层探索。
2.4.2 中药药效物质的作用机制研究
中药药效物质的筛选与作用机制阐释是中药现代化的核心科学问题,SERS技术凭借其高灵敏度、指纹识别能力的优势,已成为阐明中药药效物质及其作用机制的重要工具。在活性成分筛选方面,Xie等[79]开发HRMR-PM和SERS-PCMP策略研究参芪降糖颗粒与α-葡萄糖苷酶的相互作用,结合SERS标记技术实现靶蛋白结合活性的高通量筛选与定量分析,成功筛选出多种活性成分。在药物-生物大分子相互作用机制解析中。Zhang等[80]采用SERS和荧光光谱研究人参皂苷Rg3与人血清白蛋白相互作用,揭示与人血清白蛋白结合后结构变化,为理解药效差异提供结构基础。Wu等[81]通过多技术联用探讨了石斛酚抑制糖尿病性白内障的分子机制,证实石斛酚通过与醛糖还原酶基因发生结合来发挥作用,石斛酚不仅能抑制醛糖还原酶活性,还可下调其基因表达,为石斛防治糖尿病性白内障提供了更深入的分子药理学依据。SERS技术在药效机制监测方面实现了细胞水平的追踪,Wan等[82]开发了硼酸纳米探针SERS技术,实现了在细胞水平实时监测中药成分对活性氧及信号通路的动态调控,该实时监测策略为中药多靶点、多通路的作用特点提供了有效研究范式,检测示意图如图5所示。
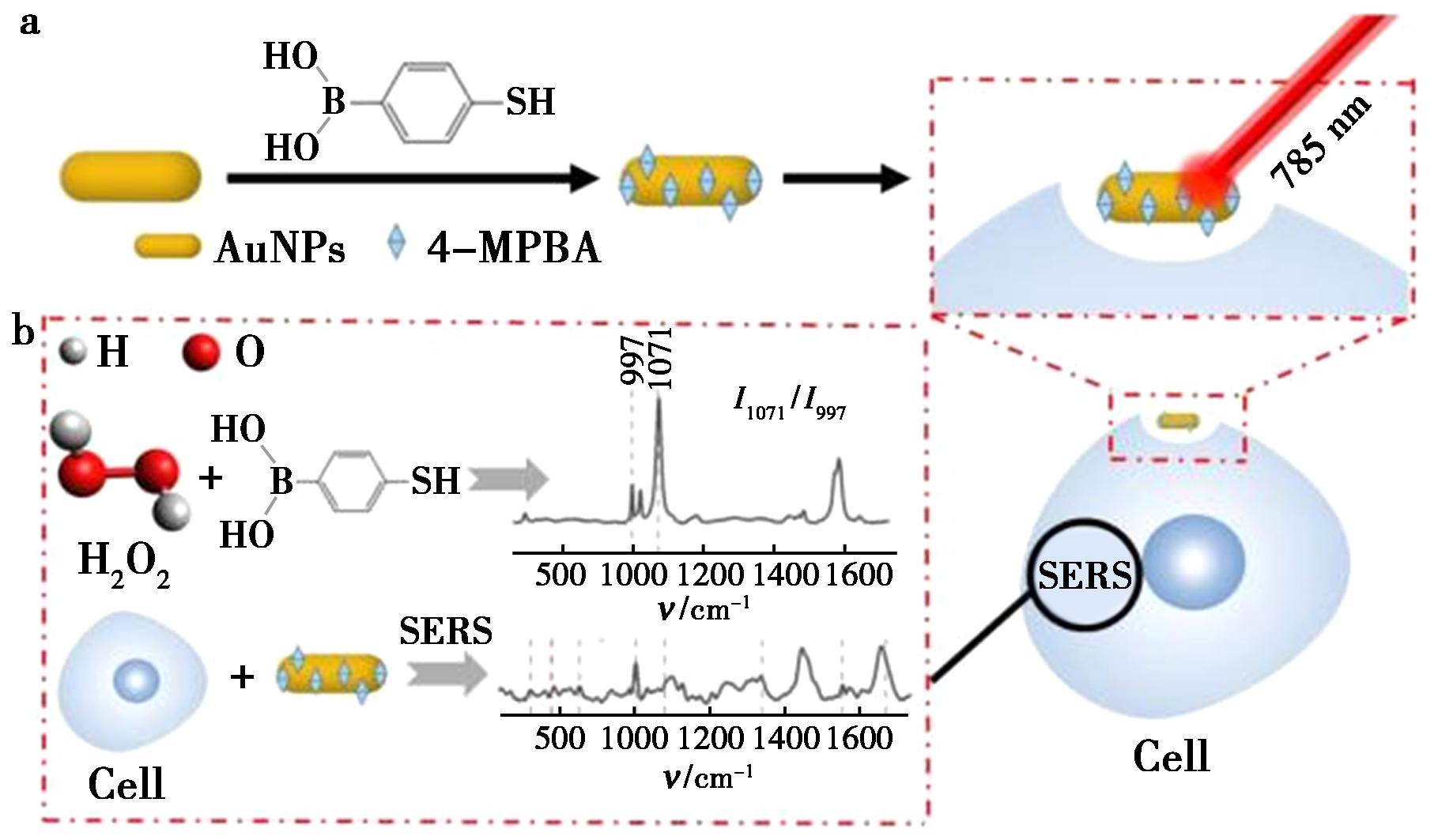
a.Preparation of boronic acid based H2O2 nanoprobe;b.Synergistic effect of SERS detection of PI3K and H2O2
图5 SERS双参数监测纳米探针同时检测人参皂苷Rg3诱导细胞凋亡过程中细胞内ROS和PI3K/Akt通路的示意图[82]
Fig.5 SERS nanoprobe for simultaneous monitoring of intracellular ROS and PI3K/Akt pathway in ginsenoside Rg3-induced apoptosis[82]
SERS机制研究正从体外研究向细胞内研究转变,智能纳米探针实现了多信号时空监测,为阐释中药多靶点作用提供了新手段。但细胞水平检测面临探针稳定性、生物相容性、靶向性三大挑战。未来应开发多功能探针、建立单细胞SERS谱库,深入揭示细胞异质性对药效的影响。
3 总结与展望
本文系统综述了SERS的增强机理、优势、数据处理方式,及其在中药分析领域的研究进展,包括基于其特性对中药活性成分检测、质量安全监控、真伪优劣鉴别、作用机制研究的应用研究进展。
虽然SERS在中药分析中已展现潜力,但离大规模应用仍有诸多现实障碍。未来需要重点突破的方向包括:(1)设计成本低、性质稳定、可批量制备的基底,将热点的随机性转化为可控增强,提升定量重现性至常规分析水平;(2)建立覆盖中药材、饮片、中成药的标准SERS谱库,制定方法学验证规范,推动形成行业或药典标准;(3)深化SERS与其他分析方法的在线联用,结合深度学习算法挖掘弱信号与重叠峰信息构建验证系统,确保方法的可靠性;(4)将SERS融入中药生产体系中,在流通监管环节部署便携式快检,实现从田间到临床全流程的质量监控,最终实现中药的质量安全和精准用药。
[1]Zhang X Y,Tao Y,Xu X F,Li Q,Zhang H X,Jiang S L,Liu Y Q,Yang C,Cheng X L,Li X R,Wei F.Chin.J.Pharm.Anal.,2025,45(4):554-563.
张欣悦,陶冶,徐新房,李千,张海霞,姜水蓝,刘艺淇,杨超,程显隆,李向日,魏锋.药物分析杂志,2025,45(4):554-563.
[2]Su S B,Zhang Y P,Zhang L L,He Z Y,Zhang J L.Chin.J.Exp.Tradit.Med.Formulae,2011,17(8):284-286.
苏松柏,张永萍,张丽丽,贺祝英,张建玲.中国实验方剂学杂志,2011,17(8):284-286.
[3]Zeng M J,Ma W W,Tang Y C.J.J.Anal.Test.,2024,43(1):95-106.
曾敏静,马玮玮,唐浴尘.分析测试学报,2024,43(1):95-106.
[4]Lv J H,Chen J Q,Lv C L.Chin.J.Anal.Chem.,2025,53(6):853-863.
吕建华,陈俊秋,吕长利.分析化学,2025,53(6):853-863.
[5]Lin L L,Alvarez-puebla R,Liz-marz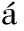 n L M,Trau M,Wang J,Fabris L,Wang X,Liu G K,Xu S P,Han X X,Yang L B,Shen A G,Yang S K,Xu Y K,Liu S C,Huang J A,Li M,Tian L M,Nguyen L B T,Cialla-may D,Stone N,Carney R P,Ji W,Song W,Chen Z,Phang I Y,Henriksen-lacey M,Chen H R,Wu Z Y,Guo H,Ma H,Ustinov G,Mosca S,Gardner B,Long Y T,Popp J,Nie S M,Ling X Y,Ye J.ACS Appl.Mater.Interfaces,2025,17(11):16287-16379.
n L M,Trau M,Wang J,Fabris L,Wang X,Liu G K,Xu S P,Han X X,Yang L B,Shen A G,Yang S K,Xu Y K,Liu S C,Huang J A,Li M,Tian L M,Nguyen L B T,Cialla-may D,Stone N,Carney R P,Ji W,Song W,Chen Z,Phang I Y,Henriksen-lacey M,Chen H R,Wu Z Y,Guo H,Ma H,Ustinov G,Mosca S,Gardner B,Long Y T,Popp J,Nie S M,Ling X Y,Ye J.ACS Appl.Mater.Interfaces,2025,17(11):16287-16379.
[6]Zhang Y,Zhao S J,Zheng J K,He L L.Trac Trends Anal.Chem.,2017,90:1-13.
[7]Yi J,You E M,Hu R,Wu D Y,Liu G K,Yang Z L,Zhang H,Gu Y,Wang Y H,Wang X,Ma H,Yang Y,Liu J Y,Fan F R,Zhan C,Tian J H,Qiao Y,Wang H L,Luo S H,Meng Z D,Mao B W,Li J F,Ren B,Aizpurua J,Apkarian V A,Bartlett P N,Baumberg J,Bell S E J,Brolo A G,Brus L E,Choo J,Cui L,Deckert V,Domke K F,Dong Z C,Duan S,Faulds K,Frontiera R,Halas N,Haynes C,Itoh T,Kneipp J,Kneipp K,Le R E C,Li Z P,Ling X Y,Lipkowski J,Liz-marz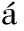 n L M,Nam J M,Nie S M,Nordlander P,Ozaki Y,Panneerselvam R,Popp J,Russell A E,Schlücker S,Tian Y,Tong L M,Xu H X,Xu Y K,Yang L B,Yao J L,Zhang J,Zhang Y,Zhang Y,Zhao B,Zenobi R,Schatz G C,Graham D,Tian Z Q.Chem.Soc.Rev.,2025,54(3):1453-1551.
n L M,Nam J M,Nie S M,Nordlander P,Ozaki Y,Panneerselvam R,Popp J,Russell A E,Schlücker S,Tian Y,Tong L M,Xu H X,Xu Y K,Yang L B,Yao J L,Zhang J,Zhang Y,Zhang Y,Zhao B,Zenobi R,Schatz G C,Graham D,Tian Z Q.Chem.Soc.Rev.,2025,54(3):1453-1551.
[8]Peter F.Bernath.Spectra of atoms and molecules.New York:Oxford University Press,2005:293-317.
[9]Graves P,Gardiner D.Springer,1989,10:23.
[10]Shipp D W,Sinjab F,Notingher I.Adv.Opt.Photon.,2017,9(2):315.
[11]Jones R R,Hooper D C,Zhang L W,Wolverson D,Valev V K.Nanoscale Res.Lett.,2019,14(1):231.
[12]Han X X,Rodriguez R S,Haynes C L,Ozaki Y,Zhao B.Nat.Rev.Meth.Primers,2021,1(1):87.
[13]Chen R,Jensen L.Chem.Phys.Rev.,2023,4(2):021305.
[14]Le R E C,Etchegoin P G.Principles of Surface-Enhanced Raman Spectroscopy.Amsterdam:Elsevier,2009:1-27.
[15]Neng J,Zhang Q,Sun P L.Biosens.Bioelectron.,2020,167:112480.
[16]Höppener C,Aizpurua J,Chen H,Gräfe S,Jorio A,Kupfer S,Zhang Z L,Deckert V.Nat.Rev.Meth.Primers,2024,4(1):47.
[17]Langer J,Aberasturi D J,Aizpurua J,Alvarez-puebla R A,Auguié B,Baumberg J J,Bazan G C,Bell S E J,Boisen A,Brolo A G,Choo J,Cialla-may D,Deckert V,Fabris L,Faulds K,Abajo F J G,Goodacre R,Graham D,Haes A J,Haynes C L,Huck C,Itoh T,Käll M,Kneipp J,Kotov N A,Kuang H,Ling X Y,Maier S A,Mayerhofer T,Moskovits M,Murakoshi K,Nam J M,Nie S,Ozaki Y,Pastoriza-santos I,Popp J,Perez-juste J,Pucci A,Reich S,Ren B,Schlucker S,Schatz G C,Shegai T,Tay L L,Thomas K G,Tian Z Q,Duyne R P,Tuan V D,Wang Y,Willets K A.ACS Nano,2019,14(1):28-117.
[18]Cao Y,Sun Y,Yu R J,Long Y T.Microchim.Acta,2024,191(1):8.
[19]Geraldes C F G C.Molecules,2020,25(23):5547.
[20]Guo S X,Popp J,Bocklitz T.Nat.Protoc.,2021,16(12):5426-5459.
[21]Stiles P L,Dieringer J A,Shah N C,Duyne R P.Annual Rev.Anal.Chem.,2008,1:601-626.
[22]Roggo Y,Chalus P,Maurer L,Lema-martinez C,Edmond A,Jent N.J.Pharm.Biomed.Anal.,2007,44(3):683-700.
[23]Qi W L,Jiang Q Q,Erihem U.Beni Suef Univ.J.Basic Appl.Sci.,2025,14(1):75.
[24]Zhao R,Wang Q S,Wang Y Q,Mei R C,Wang X Y,Chen L X.Trac Trends Anal.Chem.,2025,193:118479.
[25]Sloan-dennison S,Wallace G Q,Hassanain W A,Laing S,Faulds K,Graham D.Nano Convergence,2024,11(1):33.
[26]Fornasaro S,Alsamad F,Baia M,Batista de Carvalho L A E,Beleites C,Byrne H J,Chiadò A,Chis M,Chisanga M,Daniel A,Dybas J,Eppe G,Falgayrac G,Faulds K,Gebavi H,Giorgis F,Goodacre R,Graham D,Manna P,Laing S,Litti L,Lyng F M,Malek K,Malherbe C,Marques M P M,Meneghetti M,Mitri E,Moha ek-grošev V,Morasso C,Muhamadali H,Musto P,Novara C,Pannico M,Penel G,Piot O,Rindzevicius T,Rusu E A,Schmidt M S,Sergo V,Sockalingum G D,Untereiner V,Vanna R,Wiercigroch E,Bonifacio A.Anal.Chem.,2020,92(5):4053-4064.
ek-grošev V,Morasso C,Muhamadali H,Musto P,Novara C,Pannico M,Penel G,Piot O,Rindzevicius T,Rusu E A,Schmidt M S,Sergo V,Sockalingum G D,Untereiner V,Vanna R,Wiercigroch E,Bonifacio A.Anal.Chem.,2020,92(5):4053-4064.
[27]Lu Z X,Wang J,Yan S.Molecules,2026,31(1):191.
[28]Wang C Y,Weng G J,Li J J,Zhu J,Zhao J W.Anal.Chim.Acta,2024,1296:342291.
[29]Zhang Z M,Chen S,Liang Y Z.Analyst,2010,135(5):1138.
[30]Savitzky A,Golay M J E.Anal.Chem.,1964,36(8):1627-1639.
[31]Santos D P,Sena M M,Almeida M R,Mazali I O,Olivieri A C,Villa J E L.Anal.Bioanal.Chem.,2023,415(18):3945-3966.
[32]Zhang C H.Detection of Active Components of Rhubarb and Adulteration of Rhaponiticin Based on Raman Spectroscopy.Hangzhou:China University of Metrology,2024.
张彩虹.基于拉曼光谱的中药大黄活性成分及土大黄苷掺伪的检测研究.杭州:中国计量大学,2024.
[33]Zhang B B,Shi Y,Chen H,Zhu Q X,Lu F.J.Pharm.Pract.,2017,35(3):215-218.
张彬彬,史毅,陈辉,朱青霞,陆峰.药学实践杂志,2017,35(3):215-218.
[34]Li D,Lv D Y,Chen H,Lu F,Chen Q,Chu K D.Chin.J.Pharm.Anal.,2015,35(8):1466-1470.
李丹,吕狄亚,陈辉,陆峰,陈强,褚克丹.药物分析杂志,2015,35(8):1466-1470.
[35]Li D,Zhu Q X,Lv D Y,Zheng B X,Liu Y H,Chai Y F,Lu F.Anal.Bioanal.Chem.,2015,407(20):6031-6039.
[36]Jiang Y X,Cong S,Song G,Sun H Z,Zhang W,Yao W R,Zhao Z G.J.Raman Spectrosc.,2021,52(7):1265-1274.
[37]Zhang L L,Zhang C H,Li W X,Li L,Zhang P,Zhu C,Ding Y F,Sun H W.Foods,2023,12(22):4124.
[38]Sun J H,Feng Y,Wang S,Sheng Y,An L P,Du P G,Sun J B.Chin.J.Pharm.Anal.,2022,42(4):727-733.
孙佳慧,冯源,王珊,盛瑜,安丽萍,杜培革,孙晶波.药物分析杂志,2022,42(4):727-733.
[39]Huang H,Li J,Chen R,Feng S Y,Lin J Q,Huang Z F,Li Y Z,Chen W W,Yu Y,Lin D,Lin J.J.Fuzhou Univ.Nat.Sci.Ed.,2014,42(4):646-652.
黄浩,李洁,陈荣,冯尚源,林居强,黄祖芳,李永增,陈伟炜,俞允,林多,林佳.福州大学学报(自然科学版),2014,42(4):646-652.
[40]Wu Y.A Visual Sensing New Method Study for Identification of Traditional Chinese Medicine Origin and Detection of Sulfur Dioxide Residue.Wuhan:South-central University for Nationalities,2023.
吴越.中药产地鉴别和二氧化硫残留量检测的可视化传感新方法研究.武汉:中南民族大学,2023.
[41]Du M H,Sun Z Q,Xie M Z,Gu S Q,Chen Y C,Wang Q.J.Mater.Chem.C,2023,11(43):15138-15148.
[42]Liu Q H,Tang J W,Ma Z W,Hong Y X,Yuan Q,Chen J,Wen X R,Tang Y R,Wang L.Curr.Res.Food Sci.,2024,9:100820.
[43]Yang F,Zhong Y,Zhou H K,Chu S S,Liu H T.Laser Optoelectron.Prog.,2017,54(3):296-301.
杨方,钟莹,周鸿昆,褚赛赛,刘海涛.激光与光电子学进展,2017,54(3):296-301.
[44]Dai G Y,Wu L X,Zhao J H,Guan Q N,Zeng H S,Zong M,Fu M Q,Du C G.Food Chem.,2023,408:135210.
[45]Tan M,Zhang J.J.China Food,202,17:66-68.
谈铭,张洁.中国食品,2021,17:66-68.
[46]Lin C C,Lin P Y,Han Z Y,Tsai C Y,Beck D E,Hsieh S.Spectrochim.Acta Part A Mol.Biomol.Spectrosc.,2023,300:122918.
[47]Ren F,Yu Z G,Lu F.J.Instrum.Anal.,2021,40(4):612-616.
任菲,于治国,陆峰.分析测试学报,2021,40(4):612-616.
[48]Zhu X Y.Research on Surface Enhanced Raman Spectroscopy(SERS) in Rapid Detection of Pathogenic Bacteria in Traditional Chinese Medicine.Tianjin:Tianjin University of Traditional Chinese Medicine,2022.
朱晓英.表面增强拉曼光谱(SERS)技术在中药致病菌快速检测中的应用研究.天津:天津中医药大学,2022.
[49]Liu Y D,Yan Y L,Ning Y,Wang H X.Chin.Tradit.Pat.Med.,2025,47(8):2791-2795.
刘艺丹,颜月玲,宁滢,王海霞.中成药,2025,47(8):2791-2795.
[50]Zhang H,Nie P C,Xia Z Y,Feng X P,Liu X X,He Y.Molecules,2020,25(18):4081.
[51]Chu B Y.Study on Rapid Detection Technology of Pesticide Residues in Dendrobium officinale Based on Surface-Enhanced Raman Spectroscopy.Hangzhou:Zhejiang University of Technology,2024.
储冰妍.基于表面增强拉曼光谱的铁皮石斛农药残留快速检测技术研究.杭州:浙江工业大学,2024.
[52]Zhu Z D,Shi X Y,Feng Y T,He M,Ye C,Zhou H Y,Zhang M F,Zhang W,Li J H,Jiang C L.Spectrochim.Acta Part A Mol.Biomol.Spectrosc.,2023,288:122211.
[53]Meenakshi M M,Annasamy G,Sankaranarayanan M.Spectrochim.Acta Part A Mol.Biomol.Spectrosc.,2023,299:122878.
[54]Sun W,Yuan Q,Tan M Y.Microchem.J.,2025,212:113493.
[55]Hu R,Lu F,Bian X H,Xu J Y.J.Instrum.Anal.,2017,36(7):902-905;910.
胡然,陆峰,卞筱泓,许激扬.分析测试学报,2017,36(7):902-905;910.
[56]Dong J,Cai L M,Wang S Y,Wang Y R,Chen X.Anal.Lett.,2019,52(8):1236-1246.
[57]Fan B,Wang Y C,Li Z H,Xun D J,Dong J,Zhao X W,Fan X H,Wang Y.Talanta,2022,238:122988.
[58]Lu Y,Mo X F,Zhu G,Huang Y,Wang Y C,Yang Z Z,Gao L Q,Shen G F,Wang Y,Zhao X W.J.Hazard.Mater.,2024,467:133763.
[59]Huang H,Shi H,Feng S Y,Lin J Q,Chen W W,Yu Y,Lin D,Xu Q,Chen R.Laser Phys.,2013,23(1):015601.
[60]Tan W,Hu L S,Liu S P.Shanghai Biomed.Eng.,2013,34(4):226-227.
谭炜,胡林水,刘书朋.生物医学工程学进展,2013,34(4):226-227.
[61]Zhou W Y,Han X,Wu Y J,Shi G C,Xu S Q,Wang M L,Yuan W Z,Cui J H,Li Z L.IEEE Photonics J.,2024,16(4):1-9.
[62]Kong S N,Ou S,Liu Y,Xie M Z,Mei T,Zhang Y S,Zhang J C,Wang Q,Yang B Y.Front.Pharmacol.,2022,13:828449.
[63]Xie M Z,Lu W Y,Gu S Q,Lu J Z,Wu H T,Yao L,Du M H,Zhang J J,Liu Y,Wang Q.Anal.Chim.Acta,2024,1287:342067.
[64]Chen W W,Feng S Y,Lin W S,Chen R,Li Y Z,Lin J Q,Huang R X.Spectrosc.Spectr.Anal.,2009,29(9):2450-2452.
陈伟炜,冯尚源,林文硕,陈荣,李永增,林居强,黄瑞香.光谱学与光谱分析,2009,29(9):2450-2452.
[65]Feng S Y,Chen R,Li Y Z,Chen G N,Lin J Q,Lin W S,Chen W W,Chen J S,Yu Y.Chin.J.Lasers,2010,37(1):121-124.
冯尚源,陈荣,李永增,陈冠楠,林居强,林文硕,陈伟炜,陈杰斯,俞允.中国激光,2010,37(1):121-124.
[66]Chen W W,Lin J,Feng S Y,Huang H,Yu Y,Lin D,Chen R.Opt.Health Care Biomed.Opt.VI,2014,9268:92681B.
[67]Hu Y,Zhang Y.China Pharm.,2015,5:759-761.
胡琰,张雁.中国药师,2015,5:759-761.
[68]Wei C H,Chen J,Xu M L,Qi X Y.J.Jiangsu Univ.Med.Ed.,2015,25(3):263-267;270.
卫程华,陈娟,许曼翎,戚雪勇.江苏大学学报(医学版),2015,25(3):263-267;270.
[69]Gao Y H,Hu Z W,Wu J M,Ning Z,Jian J Y,Zhao T,Liang X C,Yang X J,Yang Z,Zhao Q Y,Wang J P,Wang Z G,Dina N E,Gherman A M R,Jiang Z J,Zhou H B.J.Pharm.Biomed.Anal.,2019,174:123-133.
[70]Yuan W Z,Zhang Z B,Wu Y J,Shi G C,Xu S Q.AIP Adv.,2022,12(10):105101.
[71]Yuan W Z,Han X,Shi G C,Wang M L,Zhou W Y,Cui J H,Liu F Z,Li Z L,Wu Y J,Wang L Y.Opt.Laser Technol.,2024,169:109911.
[72]Yuan W Z,Han X,Shi G C,Wang M L,Zhou W Y,Cui J H,Liu F Z,Li Y J,Li Z L,Wu Y J,Wang L Y.J.Lumin,2023,263:120097.
[73]Cui J H,Han X,Shi G C,Li K H,Yuan W Z,Zhou W Y,Li Z L,Wang M L.Opt.Mater.,2023,143:114170.
[74]Zhao J,Liu Y,Fales A M,Register J,Yuan H,Vo-dinh T.Drug Test.Anal.,2014,6(10):1063-1068.
[75]Li Y L,Li J B,Wang H S,Qi S R,Zhang Z H,Wang Y Q,Wang Y,Ji W.J.Biosensors.2025;15(8):536.
[76]Zhou W Y,Han X,Wu Y J,Shi G C,Xu S Q,Wang M L,Yuan W Z,Cui J H,Li Z L.Heliyon,2024,10(9):e30499.
[77]Chen W W,Liu Y,Shi H,Yu Y,Lin D,Feng S Y,Lin J,Huang H,Chen R.Spectrosc.Spectr.Anal.,2017,37(4):1134-1138.
陈伟炜,刘宇,施红,俞允,林多,冯尚源,林佳,黄浩,陈荣.光谱学与光谱分析,2017,37(4):1134-1138.
[78]Chen Q M.Surface-Enhanced Raman Scattering Spectroscopic Analysis of Compatibility of Lupus Ⅱ Prescription.Guangzhou:Guangzhou University of Chinese Medicine,2021.
陈秋媚.基于表面增强拉曼光谱技术的狼疮Ⅱ号方配伍规律研究.广州:广州中医药大学,2021.
[79]Xie J H,Mao S Y,Zhao Y L,Zhang G M,Yao J C,Guan Y X,Yan J Z,Zhang H.Anal.Chim.Acta,2024,1317:342911.
[80]Zhang W,Bai X Y,Wang Y P,Zhao B,Zhao Y,Hou W,Jin Y P,Zhao D Q.Spectrochim.Acta Part A Mol.Biomol.Spectrosc.,2014,117:210-215.
[81]Wu J,Li X,Wan W C,Yang Q H,Ma W F,Chen D,Hu J M,Chen C O,Wei X Y.J.Ethnopharmacol.,2017,198:255-261.
[82]Wan J H,Cheng W D,Xing X Y,He Y T,Tang P,Feng Y P,Liu S D,Lu X X,Zhong L Y.Biosensors,2023,13(2):212.