随着全球对可持续发展和碳中和战略的日益重视,生物质资源已成为科学研究与产业发展的焦点。作为传统发酵工业白酒酿造的主要固体废弃物,酒糟的再利用已成为不可忽视且亟待解决的挑战。作为酿酒产业副产物的主要组成部分,酒糟产量巨大,根据国家统计局关于白酒产量数据,估算我国每年白酒酒糟产排量超2000万t,其含水率高、酸度大、易腐烂变质,处理不当会严重污染生态环境和极大的资源浪费。因此,推动废弃酒糟的资源化利用,实现变废为宝,不仅能有效解决其长期带来的环境问题,还可为社会创造可观的经济效益。
酒糟作为一种粮食酿造副产物,当前利用方式多集中于直接作为动物饲料[1,2]、生物肥料或生物能源[3-5]等,这些方法由于附加值和利用效率问题,未能充分挖掘酒糟作为一种可再生生物质的内在价值。酒糟中活性成分如蛋白质、糖类、以及多酚物质等的提取也引起广泛关注[6-10],除了这部分占比较少的活性物质,酒糟实质上是一种典型的木质纤维素,这使其具备了转化为高性能生物基材料的巨大潜力[11-13]。木质纤维素中各组分均有各自特点,可针对性设计实现功能化利用,而高效分离是实现高值化转化的前提,但木质纤维素固有的顽固性及其各组分间强烈的分子间相互作用,为其分离和后续利用带来了重大挑战。为此,研究者们探索了多种处理策略,酸水解和碱水解是最常用的两种方法。酸水解更常用于从天然木质纤维中提取纳米纤维素,酸作用于纤维素无定形区的糖苷键使之水解,得到高度结晶的纳米纤维素晶体[14-16],这一方法往往侧重于纤维素的回收,而木质素组分被视为副产物或“黑液”直接排放。相较于酸性环境,碱性条件对C—O键的破坏力较弱,同时能够有效断裂木质素与半纤维素之间的酯键,实现溶出木质素的同时避免木质素进一步缩合,从而保留木质素和纤维素的原始结构,本文采用碱水解法回收酒糟木质纤维素,希望以较高的回收率获得分离彻底的酒糟原木质素和纤维素,为各组分的功能化或高值化利用提供基础支撑。
1 实验部分
1.1 主要仪器与试剂
Nicolet IS10型红外光谱仪(美国赛默飞世尔科技公司);布鲁克AVANCE NEO 400M型核磁共振仪(美国Bruker公司);UV-2700型紫外-可见分光光度计、Shimadzu Class LC-10 system型凝胶渗透色谱仪(日本岛津公司);DX-2800型X-射线粉末衍射仪(丹东浩元仪器有限公司);TGA-550型热重分析仪(美国TA仪器公司);YB-200E型高通量全自动显微成像仪(复纳科学仪器(上海)有限公司)。
实验原料酒糟粉末(四川省宜宾五粮液集团有限公司);α-淀粉酶(分析纯,上海迈瑞尔化学技术有限公司);糖化酶(液化型,106 U/mL,上海阿拉丁生化科技股份有限公司);亚氯酸钠(分析纯,上海阿达玛斯试剂有限公司);试剂乙醇、氢氧化钠、乙酸、浓盐酸、酚酞(分析纯,成都市科隆化学品有限公司)。所用的原料均为市场销售,无需提纯。实验用水为四川省成都浩康科技有限公司纯水机制备的超纯水。
1.2 实验方法
1.2.1 酒糟分离与回收方法
原始酒糟半干粉末使用超纯水、乙醇浸泡洗涤,80 ℃鼓风烘箱中烘干至恒重后,使用粉碎机粉碎。以此为原料进行分离与回收,取20 g酒糟样品中加入200 mL蒸馏水,并于100 ℃预处理 3 h,然后室温冷却至55 ℃以下,加入45 mL 2.5%的α-淀粉酶溶液,于50 ℃恒温磁力搅拌24 h,直到液体部分滴碘溶液不显蓝色。水解完毕后,将水解液煮沸使酶失活,过滤。滤液旋蒸获得固体产物A。滤渣用蒸馏水冲洗3次过滤,固体加入200 mL 0.2%的糖化酶溶液,于50 ℃恒温磁力搅拌24 h,过滤。滤液旋蒸获得固体产物B。滤渣用蒸馏水冲洗3次过滤,滤渣投入0.5 mol/L氢氧化钠溶液,滤渣与溶液质量比为1∶11,于 100 ℃进行恒温水解反应48 h,反应结束后冷却至室温过滤,滤渣用100 mL蒸馏水冲洗2次过滤,并收集滤液。滤液部分用2 mol/L HCl调节至pH 8,用截留分子量为500 Da的透析袋透析 48 h,然后冷冻干燥,得到产物C。滤渣再用蒸馏水冲洗至pH 7,获得固体产物D。
1.2.2 表征/测试方法
1.2.2.1 化学结构分析
采用傅里叶红外分析(FT-IR),将样品与干燥后的KBr混合并压成透明片状,以1 cm-1的分辨率在400~4000 cm-1的范围内对样品扫描64次进行红外光谱分析。使用核磁共振仪(NMR),重水为溶剂,TMS为内标,测试样品 1HNMR。采用紫外-可见分光光度计,在200~800 nm范围内测试溶液吸收峰。采用凝胶渗透色谱测定产物的相对分子质量,以水和乙酸为流动相,流速为 5 mL/min。采用X-射线粉末衍射仪对样品的晶体结构进行表征。测试条件设置Cu Kα辐射(λ=1.5406 Å),40 kV电压40 mA电流,在10°~60°(2θ)的范围内以0.02°的步长和1°/min的扫描速度收集衍射数据。
1.2.2.2 热稳定性分析
采用热重分析仪对回收产物进行热重分析(TGA)。在氮气氛下,升温速率为10 ℃/min,气体流速为50 mL/min,升温范围40~700 ℃。
1.2.2.3 表观形貌表征
采用高通量全自动显微成像仪对样品微观形貌进行表征(SEM)。SEM测试前需要喷金,加速电压为15 kV。
2 结果与讨论
2.1 回收产物分析
酒糟分离及回收的流程如图1所示,对每一阶段所获得的产物进行分析。为研究淀粉酶和糖化酶处理后酒糟成分的变化,对该阶段产物A和产物B进行了结构分析。图2a红外谱图显示产物A中3427 cm-1附近有一个极强且宽的吸收峰,主要是O—H键伸缩振动吸收;2924 cm-1处为亚甲基C—H伸缩振动;1645 cm-1附近的吸收峰为吸附水的H—O—H弯曲振动吸收峰;1456 cm-1附近的弱信号为C—H弯曲振动;1086 cm-1处出现的强信号峰为C—O—H相关的C—O伸缩振动峰;796和607 cm-1附近吸收峰归属为C—C键的伸缩振动和淀粉的骨架模式振动。该阶段获得的淀粉呈现褐色,可能是由于酒糟在经历复杂发酵和高温蒸煮过程中,发生了无法逆转的美拉德反应,1408 cm-1附近的吸收峰对应于羧酸根 —COO-对称伸缩振动,可能来源于褐变过程中氧化产生的酸性基团;1266 cm-1附近的吸收峰为C—O伸缩振动,结合其他信号位置,排除了蛋白质与木质素的存在,推测此为美拉德反应产物的C—N或C—O振动吸收,是褐变产物存在的直接证据,因此该阶段获得的产物是一种淀粉-美拉德色素复合物。
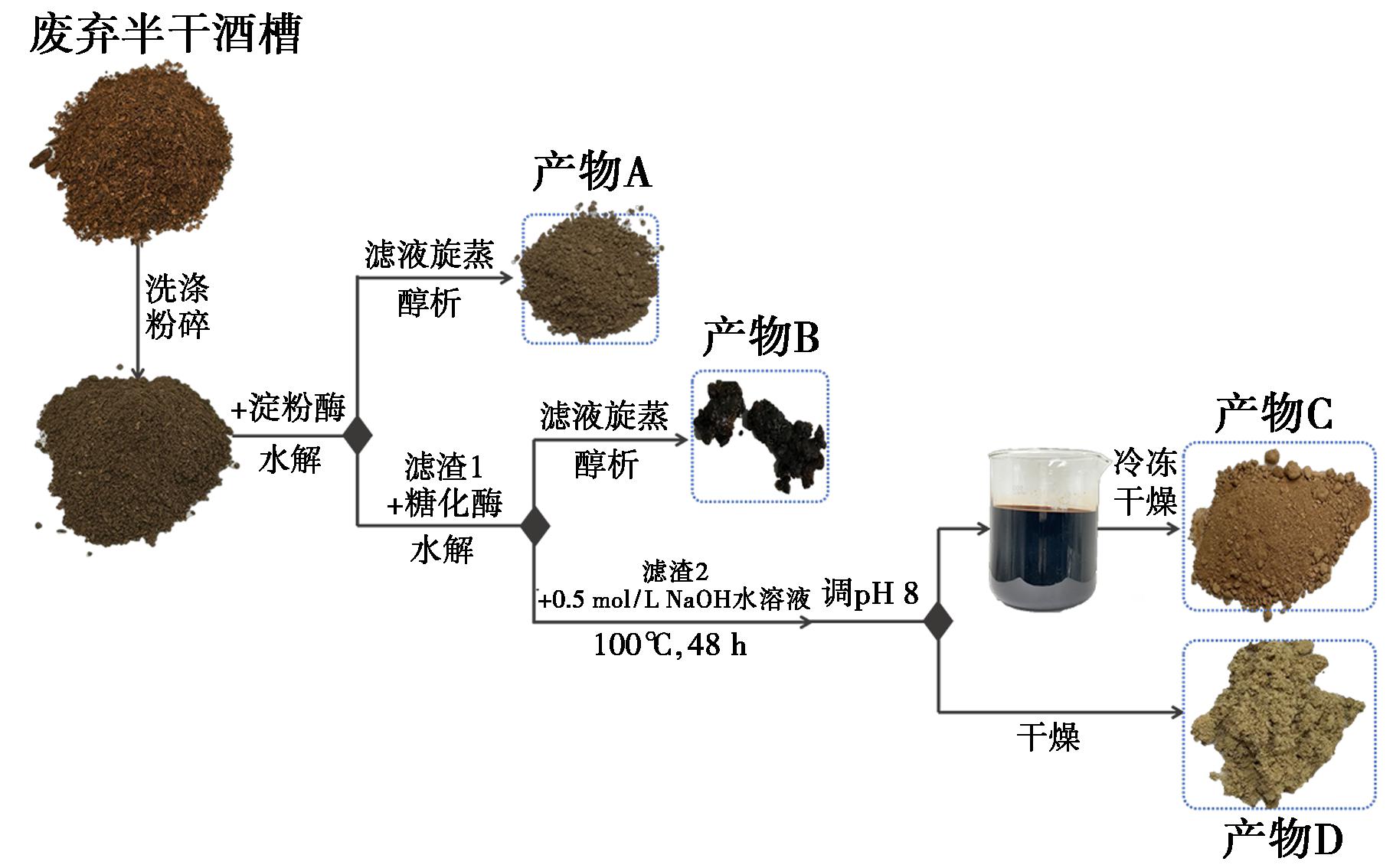
图1 实验流程图
Fig.1 Experimental flow chart
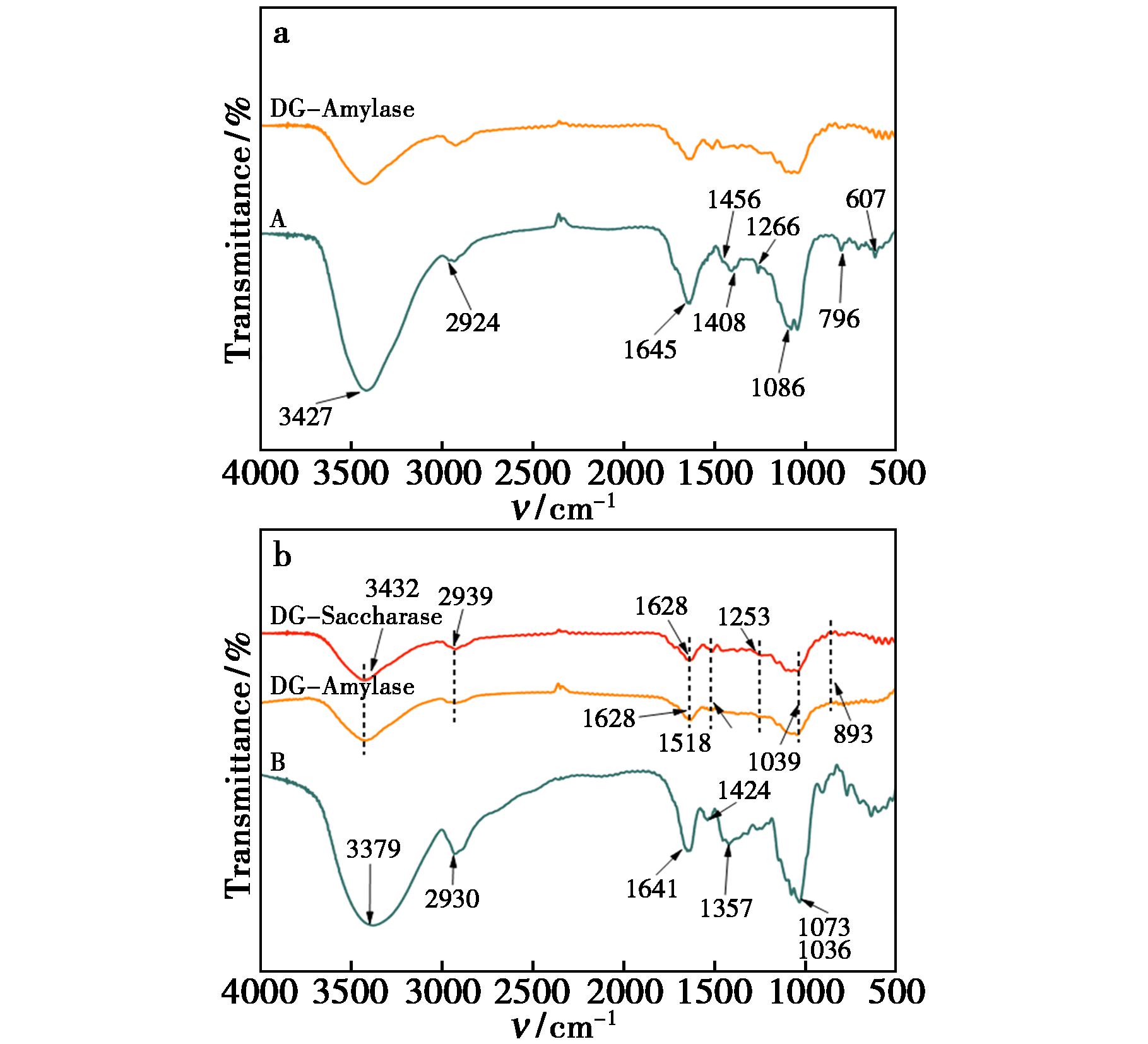
a.淀粉酶处理酒糟后产物A和滤渣1(DG-Amylase)的FT-IR谱图;b.DG-Amylase使用糖化酶处理后产物B和滤渣2(DG-Saccharase)的FT-IR谱图
图2 酒糟用淀粉酶和糖化酶处理后产物FT-IR谱图
Fig.2 FT-IR spectra of distillers′ grains treated with amylase and saccharase
进一步通过糖化酶进行水解处理,以去除未完全水解的淀粉和糖类物质,图2b显示产物B结构中,3379 cm-1附近有一个极强且宽的吸收峰主要是O—H键伸缩振动吸收;1641 cm-1处的吸收峰是吸附水的H—O—H弯曲振动;1424 cm-1处的吸收峰是![]() CH2的弯曲振动吸收峰;在1200~900 cm-1范围内出现了强、宽多重峰,是糖类的特征区域,1357 cm-1最强峰处对应于—CH2—伸缩振动;而在1073、1036 cm-1处的信号,则是醇羟基的变角振动吸收峰,与葡聚糖特征结构完全一致。结果表明,通过淀粉酶和糖化酶的序贯处理,能有效移除酒糟中的淀粉与糖类,为后续木质纤维素组分的分离提供了纯净底物。
CH2的弯曲振动吸收峰;在1200~900 cm-1范围内出现了强、宽多重峰,是糖类的特征区域,1357 cm-1最强峰处对应于—CH2—伸缩振动;而在1073、1036 cm-1处的信号,则是醇羟基的变角振动吸收峰,与葡聚糖特征结构完全一致。结果表明,通过淀粉酶和糖化酶的序贯处理,能有效移除酒糟中的淀粉与糖类,为后续木质纤维素组分的分离提供了纯净底物。
粗木质纤维素经碱性水解后分离获得的产物C和产物D,分别对其进行了结构分析,产物C的红外谱图(图3a)显示3416 cm-1处出现典型 —OH特征峰;2930和2917 cm-1处的信号为甲氧基—OCH3和—OCH2—的伸缩振动。在1220和1086 cm-1处峰值对应芳醚和脂肪醚C—O键(β—O—4键)的伸缩振动;在1596、1514、1408 cm-1处信号对应于芳香环特征吸收;881 cm-1处的吸收峰与芳香环的C—H面外弯曲振动峰,与木质素特征结构完全吻合。此外,在1041、783 cm-1处和1351 cm-1处同时存在明显吸收峰,分别对应木质素中典型的G单元和S单元,且相对峰强表明酒糟S型木质素的丰度高于G型。核磁氢谱中(图3c),δ 8.5和5.4左右发生化学位移为酚羟基和脂肪羟基;在δ 7.5~6.3范围内出现宽峰对应于愈创木酰基单元的芳香族质子峰;δ 4.1~3.3范围内的峰与木质素结构上的甲氧基质子有关,δ 4.8处为D2O溶剂峰,进一步证实了关于木质素结构的分析。将酒糟木质素与商用木质素结构进行对比,红外图(图3d)显示,酒糟回收木质素与商用木质素特征结构一致,紫外图显示(图3e),280~300 nm处出现木质素苯环吸收,和商用碱木质素吸收峰位置完全对应,表明经水解提取获得纯度较高的酒糟木质素。
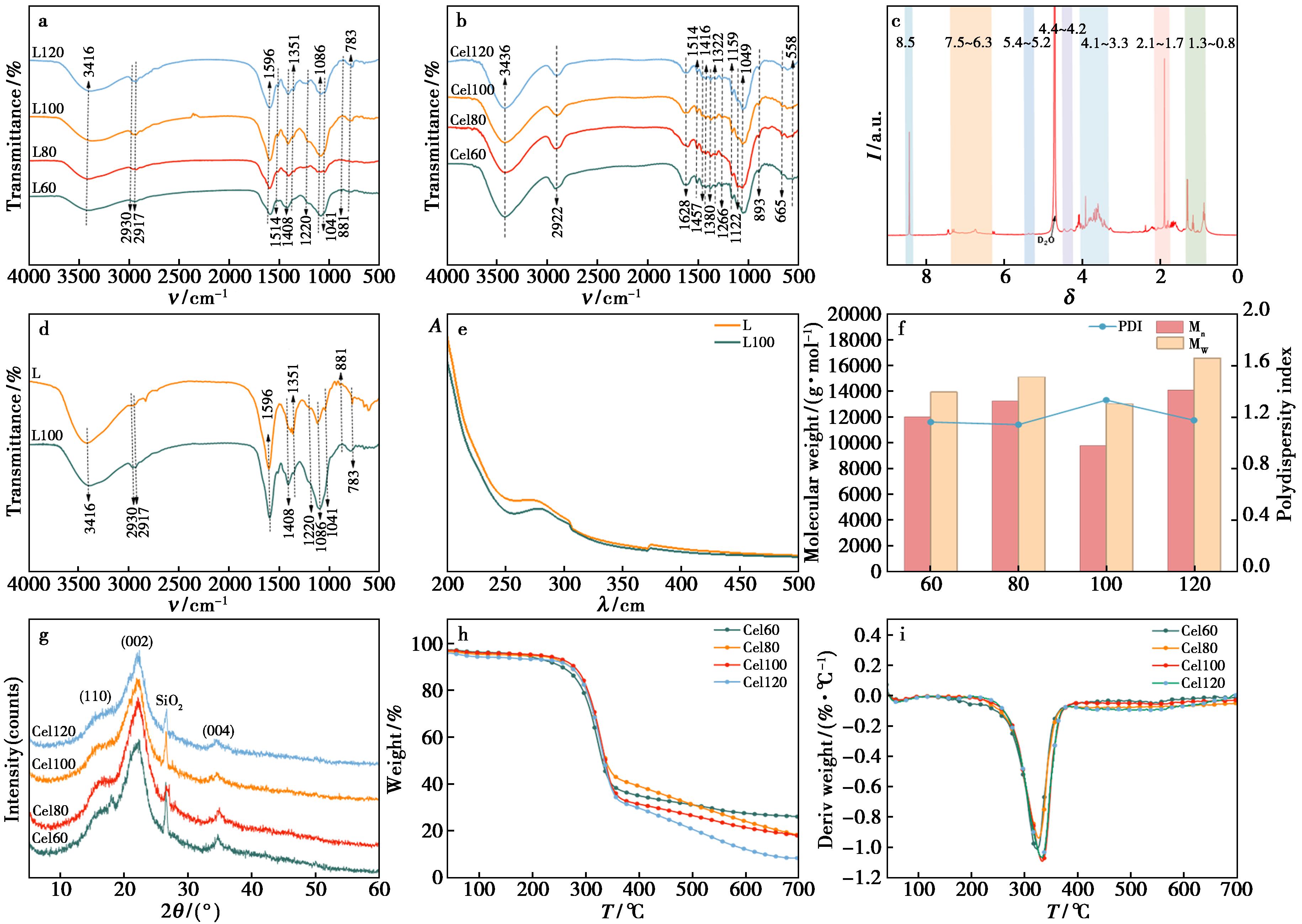
L60、L80、L100和L120为水解温度60、80、100和120 ℃得到的木质素;Cel60、Cel 80、Cel 100和Cel 120为水解温度60、80、100和120 ℃得到的纤维素
a.不同水解温度下酒糟木质素产物的FT-IR谱图;b.不同水解温度下酒糟纤维素产物的FT-IR谱图;c.酒糟木质素的 1HNMR谱图;d.商用木质素和酒糟木质素的FT-IR谱图;e.商用木质素和酒糟木质素的UV-Vis谱图;f.酒糟木质素分子量;g.纤维素的XRD谱图;h.氮气气氛下纤维素组分的TG曲线;i.氮气气氛下纤维素组分的DTG曲线
图3 酒糟在不同水解温度下产物结构表征图
Fig.3 Structure characterization diagrams of distillers′ grains hydrolysis products at different temperatures
图3b显示,产物D在3436 cm-1处出现—OH伸缩振动峰;2922 cm-1处的信号为—OCH3和亚甲基—OCH2—的伸缩振动;1628和1514 cm-1处峰值对应纤维素中的结合水;1457、1416、1380和1322 cm-1处峰值分别对应葡萄糖环—CH2—和 —CH—弯曲振动;1159和1049 cm-1处峰值分别对应纤维素主链上β-1,4-糖苷键的不对称伸缩振动和葡萄糖环上的C—O—H伸缩振动;1266和1122 cm-1对应纤维素中的C—O键振动变形;893 cm-1处峰值对应β-1,4-糖苷键特征峰;665和558 cm-1处葡萄糖环的变形振动,证明该产物D为纤维素。并且未观察到1700 cm-1处半纤维素对应的C![]() O峰,说明粗纤维中半纤维素已去除干净。结果表明,在酶水解基础上,经温和条件下碱性水解即能有效分离并回收获得特征结构理想的酒糟木质素与纤维素。
O峰,说明粗纤维中半纤维素已去除干净。结果表明,在酶水解基础上,经温和条件下碱性水解即能有效分离并回收获得特征结构理想的酒糟木质素与纤维素。
2.2 木质纤维素分离过程分析
2.2.1 温度影响规律
为了探究温度对纤维素和木质素分离效果的影响,分别在60、80、100、120 ℃条件下进行了水解实验,并对回收的纤维素和木质素进行了对比分析。根据不同温度所获得的木质素红外谱图,发现不同温度下的水解处理,均可将木质素从酒糟粗木质纤维素中分离出来,并且根据红外谱图对比(图3a)发现随着温度的升高,木质素结构β-O-4键并未发生显著变化。通过GPC对分子量测试结果显示(图3f,表1),在60~100 ℃范围内所获得的木质素重均分子量Mw分布在理想的中低分子量13 k~16 kDa区间内,且PDI值在1.1~1.4范围内,证明不同温度下提取获得的木质素分子结构保持稳定且分子量分布较窄。当温度提升至120 ℃时,Mw突增至16.6 kDa,分析木质素分子在此温度下可能发生了一定程度的自聚反应。
表1 不同条件下回收木质素的GPC测试结果
Tab.1 GPC test results of recovered lignin under different conditions
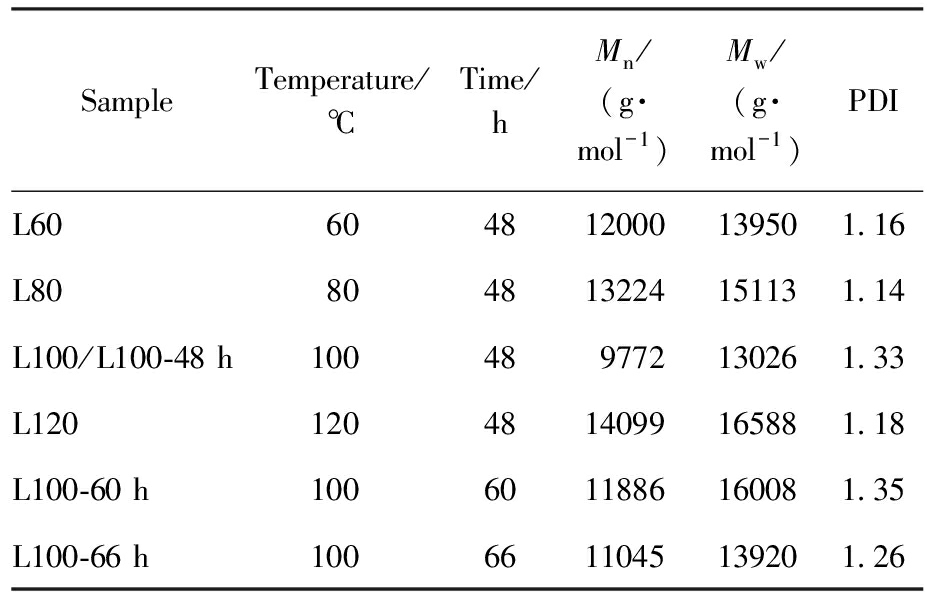
SampleTemperature/℃Time/hMn/(g·mol-1)Mw/(g·mol-1)PDIL60604812000139501.16L80804813224151131.14L100/L100-48 h100489772130261.33L1201204814099165881.18L100-60 h1006011886160081.35L100-66 h1006611045139201.26
不同温度下水解获得纤维素的XRD(图3g)结果显示,在22.6°出现明显强衍射峰,14.8°、16.5°出现可辨的肩峰,这属于典型的纤维素I晶型结构衍射。经计算,60、80、100、120 ℃获得的纤维素结晶度指数分别为35%、43.7%、43.0%、39.5%,相较于原纤维素数值偏低,这主要是酒糟经历了酿造过程的高温/高压蒸煮以及发酵酸性环境,在一定程度上破坏了结晶区的完整性,另外样品中还含有较高比例的高度无序非晶态物质,如残留木质素组分,抬高了无定形背景。就数据变化规律来看,随温度升高其结晶度先升高后降低,这是由于随着碱水解的推进,无定形木质素组分被逐步剥离,继续升高温度至120 ℃碱溶液的有效渗透溶胀作用可能会破坏纤维素氢键网络。以上结果证明,通过碱水解处理能够有效分离出结构稳定的木质素和纤维素,且在100 ℃内温度变化对回收产物原始结构特征影响较小。
对回收纤维素进行了热稳定性和残炭率进行分析(图3h、3i)。700 ℃的残余质量显示,60 ℃所获样品的残炭率高达25%,这是由于其保留了较多的木质素组分,与上述分离效率结果吻合。随着水解温度升高至80、100和120 ℃,残炭率依次降至18%、17%和8%。这一趋势表明,较高的处理温度能更有效地去除酒糟中的木质素组分。因此,为实现木质素的高效剥离,60 ℃水解处理分离效率有限,100 ℃及以上则更为有效。对两组分的表观状态及SEM形貌分析(图4)显示,不同温度下获取的木质素形貌存在较大差异且存在规律性的变化,随着温度升高,木质素组分颜色变深,100 ℃木质素呈现较为均匀的颗粒状,继续升温至120 ℃时木质素将呈现明显的聚集态,结合上述GPC结果,进一步说明高温将不利于木质素分子的稳定性。与此同时,纤维素组分随着温度升高变得更为松散、颜色变淡,纤维素组分逐渐从复合物变为较干净的纤维素纤维。综合分析,木质素和纤维素的分离效率随温度提升逐渐提升,100 ℃是相对最佳的温度条件。

L60、L80、L100和L120为水解温度60、80、100和120 ℃得到的木质素;Cel 60、Cel 80、Cel 100和Cel 120为水解温度60、80、100和120 ℃得到的纤维
a.酒糟在不同水解温度处理后产物木质素和纤维的数码照片;b.酒糟在不同水解温度处理后产物木质素和纤维的SEM图像
图4 酒糟在不同水解温度处理后产物的数码照片及SEM图像
Fig.4 Digital photos and SEM images of hydrolysis products of distillers′ grains at different temperatures
2.2.2 时间影响规律
以上在100 ℃较佳温度条件下经48 h获得了结构理想的木质素组分,但纤维素组分中仍残留有一定量的木质素组分,为进一步深入对纤维素和木质素的分离,将100 ℃获得的纤维素组分置于相同反应体系延长时间至60和66 h进行二次分离回收。对获得的木质素组分和纤维素组分进行结构分析,其红外谱图(图5a、5b)显示,特征峰位置以及相对峰强无显著变化,说明随反应时间的延长,木质素和纤维的特征官能团并未发生明显破坏。GPC测试结果(图5c,表1)表明,随着处理时间延长至60和66 h,与48 h阶段获得的产物相比,木质素重均分子量基本保持在13 k~16 kDa范围内,且PDI值稳定维持在1.3左右,进一步证明碱水解方法对木质素提取具有良好的稳定性。而纤维素组分的热稳定性分析结果显示(图5e、5f),48、60和66 h回收纤维素组分的初始分解温度分别为210、166和253 ℃,出现先降低后升高的趋势,这可能是由于反应进程的推进,60 h的长时间反应导致纤维素分子链发生一定程度的水解降解,产生了稳定性较差物质;而当时间继续延长至66 h,更充分的反应可能去除了纤维中的无定形区及残留的、热稳定性较差的水解物,使回收纤维素纯度提高,从而提升了其初始热稳定性。残炭率的变化直接反映了纤维素在高温热解过程中的石墨化能力。水解60 h的样品残炭率达22%,可能是适度的水解在去除无定形区的同时,保留了足够的分子链长度以形成交联网络。而当水解时间延长至66 h时,残炭率急剧下降至8%,这可能是纤维素在这一过程中发生分子链断裂与聚合度降低,从而削弱了其形成稳定炭骨架的能力。
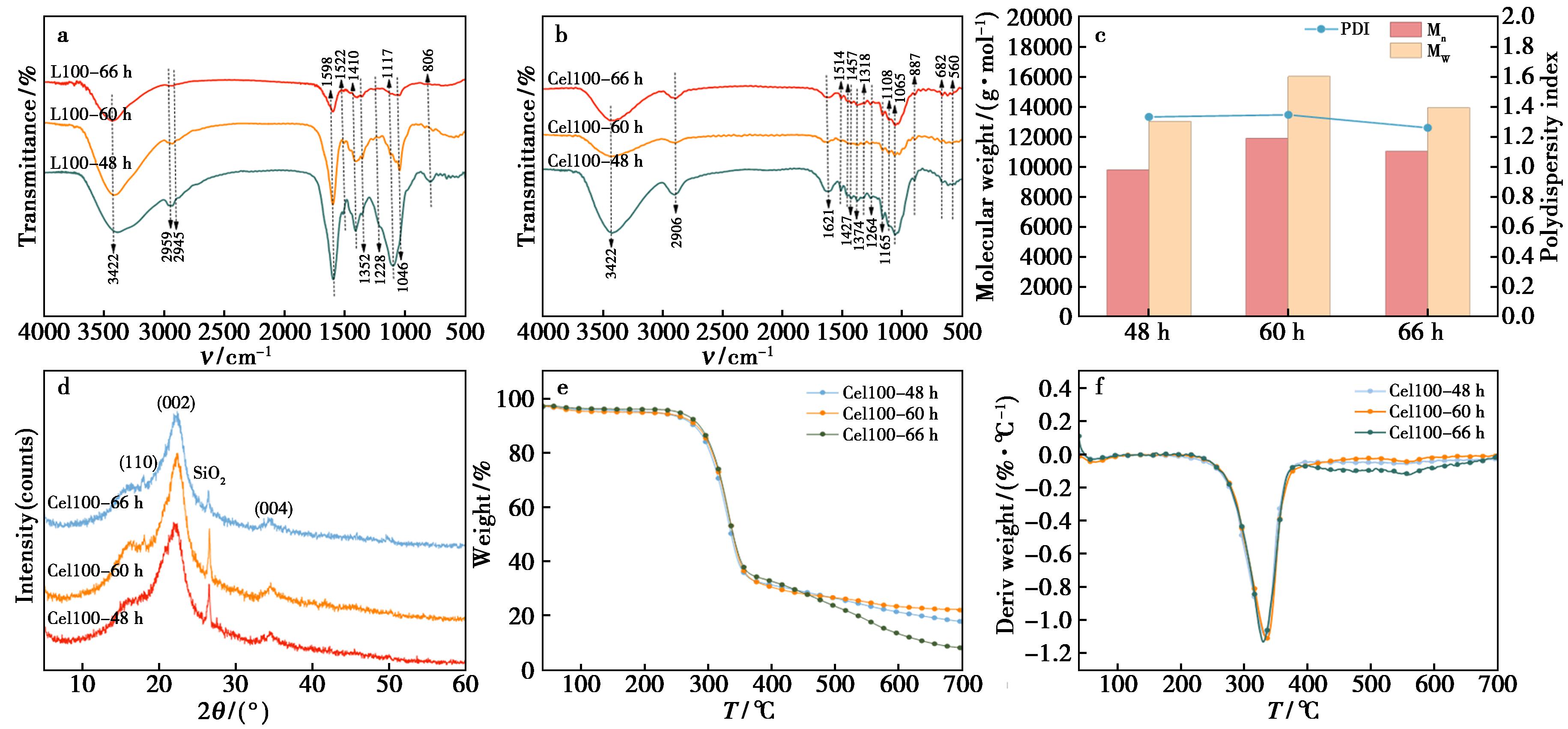
a.酒糟在100 ℃下不同水解时间处理后产物木质素的FT-IR的谱图;b.纤维的FI-IR的谱图;c.木质素分子量;d.纤维素的XRD谱图;e.氮气气氛下纤维素的TGA;f.氮气气氛下纤维素的DTG曲线
图5 酒糟在100 ℃下不同水解时间处理后产物的结构表征
Fig.5 Structural characterization of hydrolysis products of distillers′ grains treated at 100 ℃ for different durations
SEM(图6)结果表明,反应时间延长可促进木质素的进一步溶出。溶出的木质素分子经乙醇析出时,由于其分子特殊的富苯环结构,通过π-π作用和氢键力等分子间力进行高度有序的自组装,形成分布均匀、结构致密的球形。然而长时间的水解将不可避免地破坏纤维素原始结构。对比纤维素形貌,48 h阶段获得的纤维素组分仍以成束的状态呈现,随反应时间延长,样品中呈现更显著的单根纤维,这归因于碱性环境持续破坏纤维束间相互作用,从而导致宏观纤维结构的解离。

L100-48 h、L100-60 h和L100-66 h为100 ℃水解时间48、60和66 h得到的木质素;Cel 100-48 h、Cel 100-60 h和Cel 100-66 h为100 ℃水解时间48、60和66 h得到的纤维
a.酒糟在100 ℃下不同水解时间处理后产物木质素SEM图像;b.产物纤维的SEM图像
图6 酒糟在100 ℃下不同水解时间处理后产物的SEM图像
Fig.6 SEM images of hydrolysis products of distillers′ grains treated at 100 ℃ for different durations
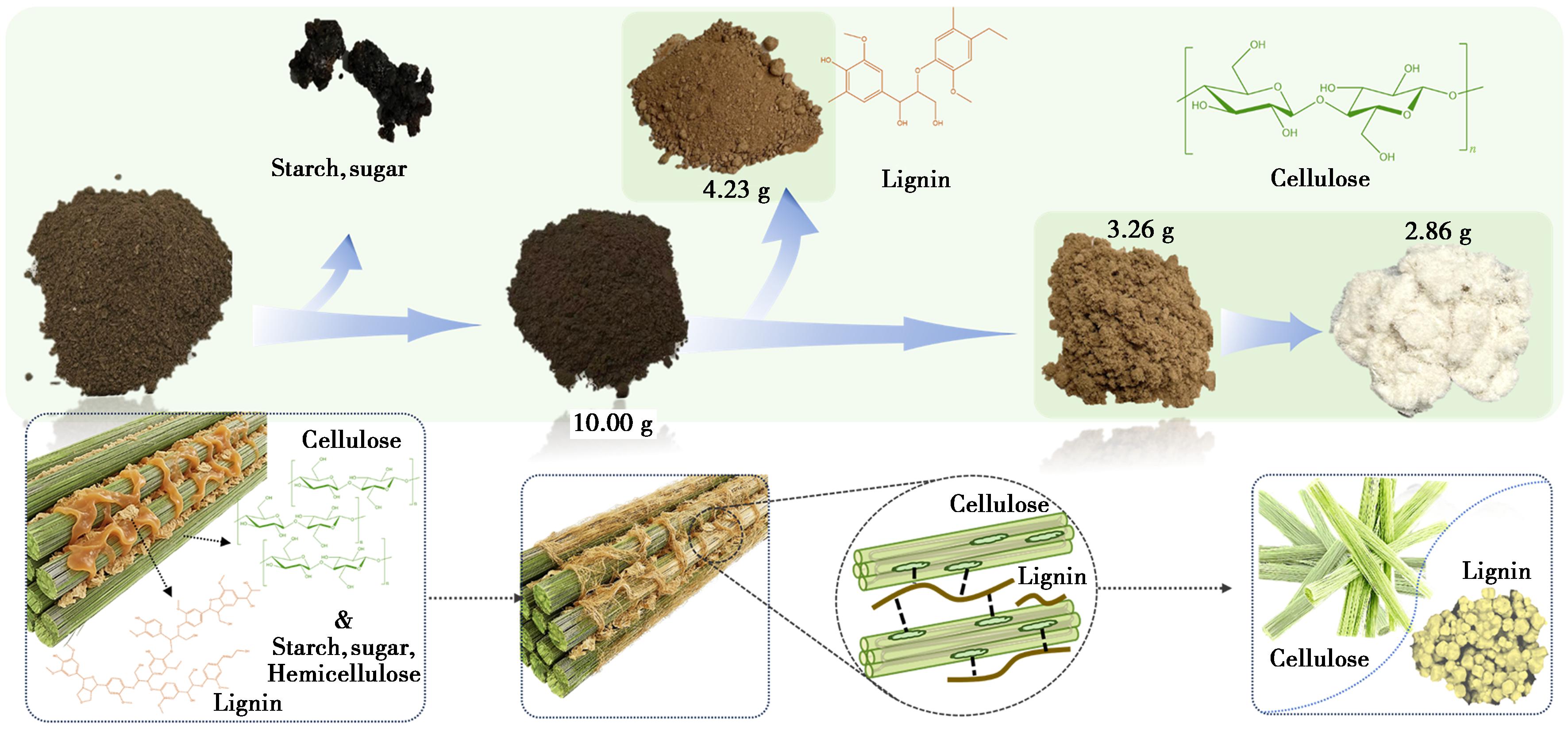
图7 酒糟回收过程与机制示意图
Fig.7 Schematic diagram of the process and mechanism of distillers′ grains recovery
基于回收原木质素和纤维素结构的目的,避免组分过度降解,100 ℃、48 h即可达到稳定且较佳的分离效率与回收效果。基于水解后所得木质素产物的质量,与底物(酶解处理后的产物)质量进行对比,计算得到木质素的一步水解产率为42.3%。进一步分析了底物中木质素总含量,通过氧化降解的方式(置于2%亚氯酸钠水溶液中并调节至pH 4.6,于80 ℃反应6 h)进一步处理纤维素组分,彻底去除剩余顽固木质素,定量酒糟木质纤维素中木质素总含量为46.3%。据此,可以推算一步水解获得的木质素回收率可达到91.4%。同时,基于成分分析,排除残留木质素的质量占比,获得87.7%纯度的结晶性保持完好的原纤维素。
3 结论
本研究成功建立了一种基于酶预处理与碱水解相结合的分离方法,用于从酒糟中高效提取高质无损木质素和纤维素。通过系统优化水解温度与时间,在100 ℃、0.5 mol/L NaOH体系中反应48 h,单组分回收率达91.4%,所得木质素分子量集中分布于13 kDa,是作为粘接剂以及树脂的理想分子量,为其高值化循环利用提供了良好的结构基础。纤维素纯度达87.7%,结晶度保持良好,呈现清晰干净的原纤维结构。该方法在常压、温和条件下实现了木质纤维素组分的无损分离,为酒糟的高值化利用提供了可靠的技术支撑,具有潜在的环境与经济效益。
[1]Spowart P R,Richeson J T,Crawford D M,Samuelson K L.Appl.Anim.Sci.,2022,38(2):118-128.
[2]Zynda H M,Copelin J E,Rebelo L R,Weiss W P,Wilken M,Lee C.J.Dairy Sci.,2022,105(10):8054-8068.
[3]Luo X,Liu Y H,Lei L Y,Shen J L,Zhang Q,Wang Y P,Ruan R,Cui X.Bioresour.Technol.,2023,386:129496.
[4]Zhao A M,Lv J W,Chen Q L,Xie Y,Cao Y,Jiang C Y,Ao X Q.Int.J.Hydrog.Energy,2021,46(1):314-323.
[5]Chen J,Zhang M Y,Liu X Z,Xiao X,Zhang L H.Energy Conserv.,2023,42(6):40-44.
陈娟,张明阳,刘新辙,肖学,张林华.节能,2023,42(6):40-44.
[6]Fonseca Y A,Gurgel L V A,Baêta B E L,Dragone G,Mussatto S I.J.Clean.Prod.,2023,416:137966.
[7]Liu X G,Chang R,Zhou Z L,Ren Q X,Shen C H,Lan Y,Cao X N,Mao J.J.Funct.Foods,2023,108:105722.
[8]Nayak N,Bhujle R R,Nanje-gowda N A,Chakraborty S,Siliveru K,Subbiah J,Brennan C.Heliyon,2024,10(10):e30921.
[9]Xu S H,Liu H B,He C L,Li L L,Yan X H.Chem.Reagehts.,2022,44(1):32-38.
许世浩,刘宏炳,何晨露,黎玲玲,燕雪花.化学试剂,2022,44(1):32-38.
[10]Garcia-castello E M,Conidi C,Cassano A.Sep.Purif.Technol.,2024,336:126183.
[11]Li M C,Li H,Li C,Fu Y S,Li J,Li D Q.Chem.Reagents,2025,47(8):45-51.
李美婵,李贺,李灿,付泳盛,李君,李德强.化学试剂,2025,47(8):45-51.
[12]Cheng G G,Zeng F J,Liu X Y,Yang Q N,Wei S Z,Huang Q.Int.J.Biol.Macromol.,2025,306:141458.
[13]Iswanto A H,Lee S H,Hussin M H,Hamidon T S,Hajibeygi M,Manurung H,Solihat N N,Nurcahyani P R,Lubis M A R,Antov P,Savov V,Kristak L,Kawalerczyk J,Osvaldov L M,Farid S,Selvasembian R,Fatriasari W.Int.J.Biol.Macromol.,2024,283:137714.
L M,Farid S,Selvasembian R,Fatriasari W.Int.J.Biol.Macromol.,2024,283:137714.
[14]Wang X J,Feng X,Chen G X,Lin B F,Qi H S.Ind.Crops Prod.,2022,187:115391.
[15]Yang J Y,Yu Q F,Li M F.Bioresour.Technol.,2023,384:129365.
[16]Zhu P,Feng L Y,Ding Z J,Bai X C.Int.J.Mol.Sci.,2022,23(18):10764.