低氧激活前药(HAP)是一种重要的肿瘤靶向治疗策略,在肿瘤低氧区域可被高表达的还原酶激活,释放具有细胞毒性的药物,从而发挥靶向抗肿瘤作用[1,2]。HAP主要包括氮氧化物、醌、硝基化合物和金属配合物[3]。其中,醌类化合物常见于天然或合成的抗癌和抗菌剂,可通过一步两电子或两步一电子的机制还原为氢醌。醌氧化还原酶1(NQO1)是催化醌类化合物体内还原反应的主要生物酶,其作用机制主要是以还原型黄素腺嘌呤二核苷酸(FADH2)作为辅助因子催化醌的双电子还原[4]。NQO1主要位于细胞的胞质溶胶中,也存在于细胞核、内质网、细胞膜和线粒体以及细胞外[5-8]。NQO1在某些癌症肿瘤组织如甲状腺、肾上腺、乳腺、卵巢、结肠和非小细胞肺癌中过表达[9,10],使其成为开发抗肿瘤药物和前药的理想靶标[10-13]。NQO1能够选择性的在肿瘤低氧条件下将醌还原为对应的酚,从而导致抗肿瘤药物的释放。
三甲基锁醌丙酸(Q3PA),分子结构如图1所示,是一类代表性的醌类HAP,能够在NQO1的触发下释放具有抗肿瘤活性的药效团。Mendoza等[4]开发了一种可被NQO1还原激活的醌丙酸触发基团,醌环上取代基的变化能够显著影响催化反应中的米氏常数和催化效率等。Q3PA还被应用于抗肿瘤前药和荧光探针的设计中。Zhang等[14]将Q3PA与5-氟尿嘧啶(5-FU)连接合成了一种新型HAP用于癌症靶向治疗,该化合物比传统5-FU类药物表现出更高的抗肿瘤活性和安全性。Qu等[15]将Q3PA与鬼臼毒素(PPT)连接合成的一种新型化合物能够在NQO1的作用下释放PPT,从而靶向性的杀死肿瘤细胞。康普瑞汀A4(CA4)是一种有效的微管蛋白抑制剂,将其与Q3PA连接所形成的化合物对缺氧暴露下的A549和HepG2细胞表现出显著毒性[16]。Park等[17]合成了一种由Q3PA连接聚己内酯和聚乙二醇的共聚物,将其通过自组装形成纳米胶束用于阿霉素的靶向递送。上述研究报道的化合物均具有醌丙酸的“三甲基锁”结构,在NQO1催化下,醌被还原为酚,继而引发快速内酯化和一系列多米诺分解反应,最终释放出活性药物。尽管Q3PA在一系列临床前研究中表现出了良好的肿瘤低氧激活响应性,然而到目前为止,尚未见关于NQO1催化Q3PA还原机理的研究,其低氧响应机制尚不明确。因此,本文对NQO1催化Q3PA还原的反应机理进行了深入探讨,以期为设计开发新型的低氧靶向性醌类抗肿瘤药物提供理论依据。
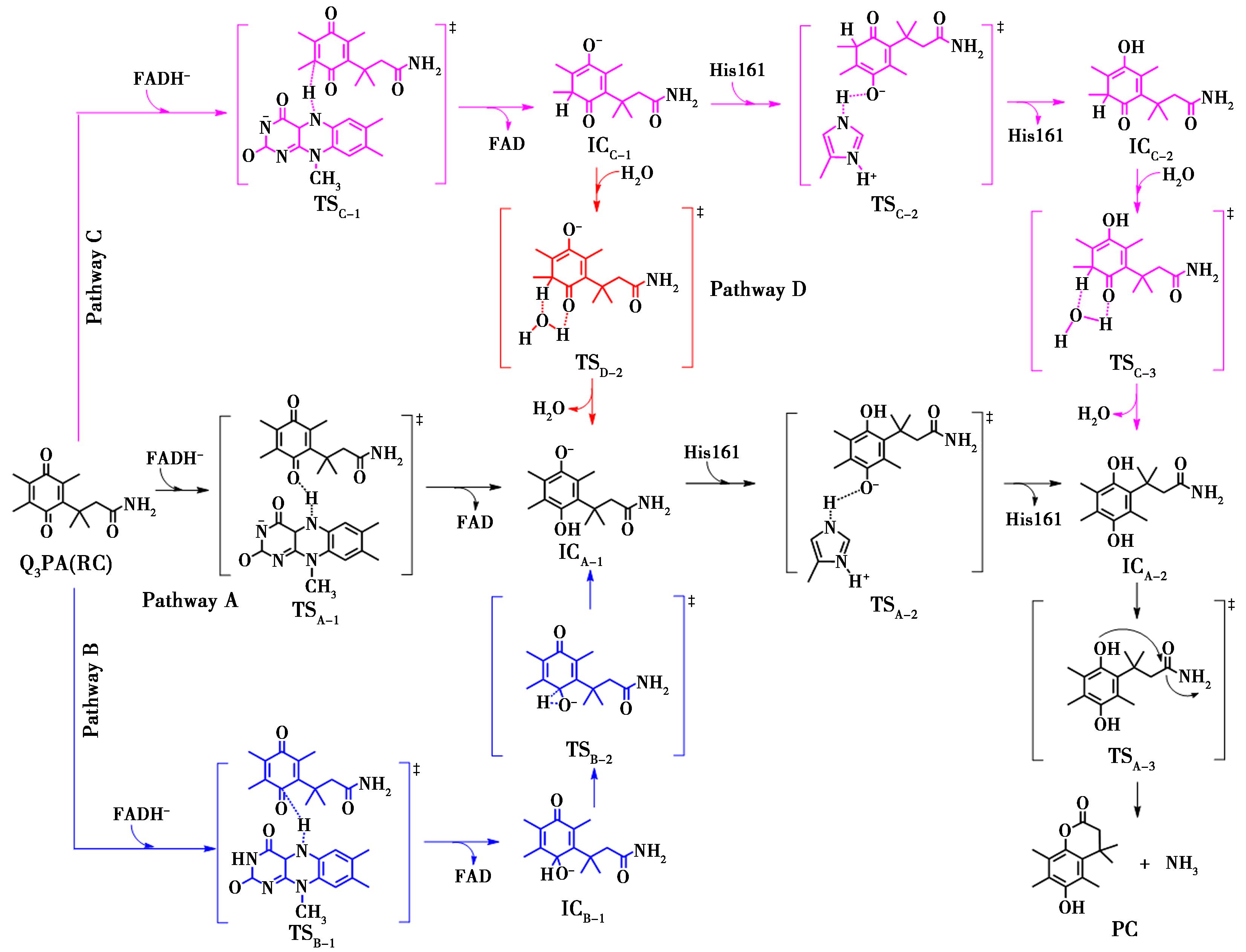
途径A:RC→TSA-1→ICA-1→TSA-2→ICA-2→TSA-3→PC;途径B:RC→TSB-1→ICB-1→TSB-2→ICA-1→TSA-2→ICA-2→TSA-3→PC;途径C:RC→TSC-1→ICC-1→TSC-2→ICC-2→TSC-3→ICA-2→TSA-3→PC;途径D:RC→TSC-1→ICC-1→TSD-2→ICA-1→TSA-2→ICA-2→TSA-3→PC
图1 NQO1中FADH-介导的Q3PA双电子还原假设机理
Fig.1 Hypothesis mechanism of FADH- mediated two electron reduction of Q3PA in NQO1
1 模型及计算方法
以辅酶FADH2和Q3PA为计算模型,探讨了NQO1中辅酶FADH2介导的Q3PA双电子还原机理。根据以往的研究[18-20],为了简化计算模型以节约计算成本,将FADH2分子结构中异咯嗪环上的磷酸尾链用甲基替代,并将异咯嗪环羟基上的质子用酪氨酸残基(Tyr155)脱去使其成为FADH-。Q3PA经FADH-介导的双电子还原假设机理如图1所示,共包括4条反应路径。Q3PA首先被FADH-还原为Q3PA半醌阴离子(ICA-1);然后进一步被组氨酸残基还原,生成对氢醌结构(ICA-2);最后经过分子内环化形成内酯(PC),导致药物的释放。在整个反应过程中,第一步由FADH-提供2个电子和1个质子(2e-/1H+),第二步由组氨酸残基提供1个质子,一共经过了2e-/2H+的转移。
所有反应物、中间体、过渡态和产物的结构均采用密度泛函(DFT)M062X方法[21],在6-31+G(d,p)水平上进行几何结构优化;并在相同水平上计算振动频率,均得到无虚频的稳定结构或有唯一虚频的过渡态结构。为模拟催化Q3PA发生还原反应的NQO1酶活性中心的蛋白环境,采用了SMD溶剂模型,以氯苯和乙腈为溶剂,在更高精度的SMD-M062X/6-311+G(3df,2p)水平上计算了各驻点的单点能。上述计算均使用Gaussian16程序完成。
在分子对接中,首先将底物在M062X/6-31+G(d,p)水平上进行结构优化,得到无虚频的稳定结构后,与NQO1晶体结构(PDB ID:1DXO)进行分子对接。所有对接均使用GOLD 5.2软件包,选择导向模式,移除NQO1蛋白中的水分子并补全氢原子,选择酶活性口袋中FADH2异咯嗪环的N5作为对接中心,设置10 Å球形区域为活性口袋边界。采用“GoldScore”作为打分函数,选用细胞色素P450模式进行对接。对接结果的分子结构采用PyMOL软件进行可视化。
2 结果与讨论
2.1 Q3PA双电子还原机理
如图1所示,Q3PA经FADH-催化的双电子还原机理包括4条可能的反应路径。简单来说,2e-/1H+由FADH-异咯嗪环的N5分别经途径A、B和C向Q3PA的羰基氧原子、α碳原子或β碳原子传递;或者在生成中间体ICC-1后,再通过途径D发生H2O介导的质子转移。各路径最终均经过最后一步分子内环化形成目标产物。图2为在M062X/6-31+G(d,p)水平上优化得到的Q3PA双电子还原路径中涉及的过渡态结构及相关参数。
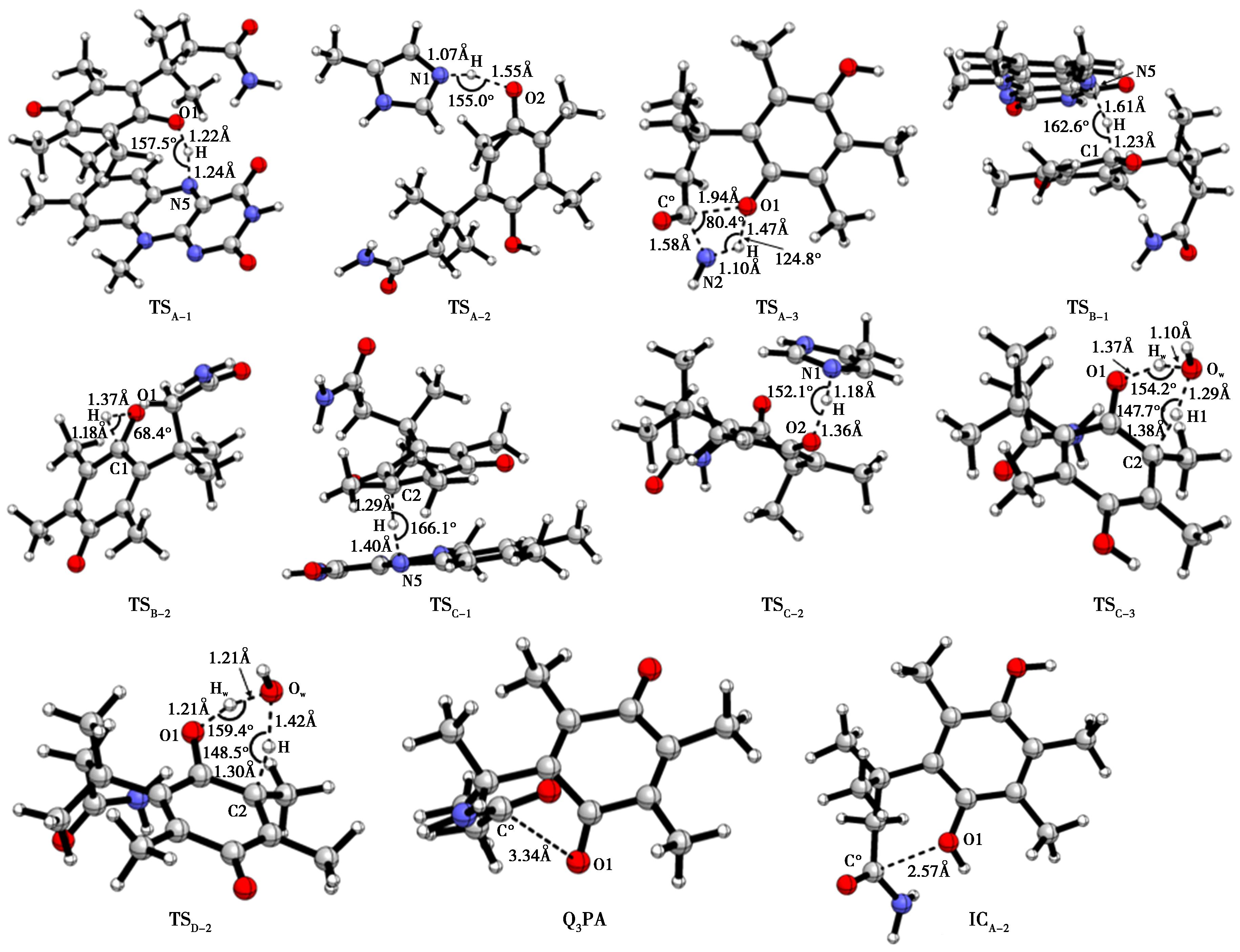
图2 M062X/6-31+G(d,p)水平上优化得到Q3PA双电子还原反应的过渡态结构与主要参数
Fig.2 Optimized structures and parameters of TSs in reduction of Q3PA double electron calculated at M062X/6-31+G(d,p) theoretical level
途径A中,FADH-异咯嗪环N5位的H向Q3PA的氧原子发生转移,该步骤经历过渡态TSA-1并且在1266.73i cm-1处有唯一虚频,振动模式对应N5—H键的断裂与H—O1键的形成,得到中间体ICA-1,本步的反应能垒为10.57 kcal/mol(文中所提及的能量均为气相中计算所得的数值)。N5—H键长由RC中的1.02 Å增加到TSA-1中的1.24 Å,H—O1键长由TSA-1中的1.22 Å缩短至ICA-1中的0.98 Å,键角N5—H—O1为157.5°。接下来,组氨酸残基(His161)继续向中间体ICA-1进行1H+的传递,组氨酸残基N1位的H传递至中间体ICA-1另一侧的羰基氧原子上,该步骤经历过渡态TSA-2并在455.98i cm-1处有唯一的虚频,振动模式对应N1—H键的断裂与H—O2键的形成,本步的反应能垒为15.49 kcal/mol。N1—H键长由ICA-1中的1.02 Å增加到TSA-2中的1.07 Å,H—O2键长由TSA-1中的1.55 Å缩短至ICA-2中的0.99 Å,键角N1—H—O2为155.0°。
途径B共经历了4步反应,与途径A不同的是,反应物经历了两步反应生成半醌阴离子中间体(即途径A中的ICA-1)。在生成ICA-1后,途径B与途径A经历了相同的反应历程,因此,仅对途径B中的前两步进行讨论。该途径的前两步经历了两个过渡态TSB-1和TSB-2,这两个过渡态均具备唯一的虚频,分别是440.83和1621.59i cm-1。其中,第一步反应为FADH-异咯嗪环N5位的H向Q3PA的羰基α碳原子发生转移,过渡态振动模式对应N5—H键的断裂与H—C1键的形成;第二步反应为中间体ICB-1的异构化,H原子由C1原子转移至O1,振动模式对应C1—H键的断裂与H—O1键的形成。两步的反应能垒分别为36.60和43.04 kcal/mol,可见反应物经途径B生成ICA-1的能垒明显高于途径A(仅为10.57 kcal/mol),这表明途径B在动力学上明显不如途径A有利。此外,通常认为酶催化反应体系的能垒一般低于30 kcal/mol[22],因此反应物也几乎不可能通过途径B发生反应。
途径C经历的反应历程与途径A和B有比较明显的差异,除了最后一步内脂化反应,前期的2e-/1H+转移机制完全不同于途径A和B。因此,对途径C经过3步反应生成对氢醌结构(即ICA-2)的过程进行详细探讨。FADH-异咯嗪环N5位的H向Q3PA的羰基β碳原子发生转移,该步骤经历过渡态TSC-1(唯一虚频1204.88i cm-1)生成中间体ICC-1。接下来,组氨酸残基(His161)向中间体ICC-1传递1个氢质子至ICC-1另一侧的羰基氧原子上生成中间体ICC-2,该步骤经历过渡态TSC-2(唯一虚频864.8i cm-1)。第三步为ICC-2经水分子介导的氢转移,即C2位的H1原子通过水分子的氢桥键转移至O1位,生成中间体ICA-2。该步骤经历过渡态TSC-3并在1595.48i cm-1处有唯一的虚频。该步骤也计算了未经水分子介导的直接分子内氢转移机制,但获得的反应能垒高达52.56 kcal/mol,这明显高于正常的酶催化反应能垒,因此在后续氢转移反应中均采用了水分子介导的机制。水不仅可以作为反应物和酶的良好分散介质,还能在催化过程中充当辅助因子,协助质子转移[23-25]。这3步反应的能垒分别为26.24、2.82和29.53 kcal/mol,可见虽然第二步反应的能垒极低,但是由于第一步和第三步的能垒明显高于途径A生成ICA-2的能垒,因此途径C也不如途径A具有能量上的优势。
途径D与途径A和C相近,其第一步与途径C完全相同,即2e-/1H+由FADH-向Q3PA转移生成中间体ICC-1。然后,ICC-1经水分子介导发生分子内的氢转移,即C2位的H1原子通过水分子形成的氢桥键转移至O1位,生成中间体ICA-1。该步骤经历过渡态TSD-2并在1693.55i cm-1处有唯一的虚频,振动模式对应C2—H1键和OW—HW键的断裂,以及H1—OW键与HW—O1键的形成。本步的反应能垒为26.15 kcal/mol。此后的反应途径与途径A完全相同,故不再予赘述。可见,与途径A和C相比,途径D经历的唯一不同步骤(即第二步的分子内氢迁移反应)的活化能也明显高于途径A的两步反应能垒,因此也不如途径A有利。
Q3PA经过上述4条途径均生成了对氢醌结构,即中间体ICA-2。通过分子结构可以看出,ICA-2分子中C1位上的羟基氧原子比Q3PA中C1位的羰基氧原子更加靠近酰胺基的碳原子(如图2所示,ICA-2中O1…Cα距离为2.57 Å,Q3PA中O1…Cα距离为3.34 Å),而且3个甲基之间的相对空间位置也较还原之前更为拥挤。这些结构特征都导致了ICA-2分子的快速内酯化,从而使得酰胺键发生断裂并释放出氨基上连接的活性药效团。该步骤经历过渡态TSA-3并在653.69i cm-1处有唯一的虚频,振动模式对应Cα—N2键的断裂与Cα—O1键的形成,O1—H键的断裂与N2—H键的形成。本步的反应能垒为30.96 kcal/mol。
比较上述各还原反应路径,第一步均为2e-/1H+转移,在优化得到的3个过渡态(TSA-1、TSB-1和TSC-1)中,反应物的醌环均以相对平行的空间位置堆叠于FADH-异咯嗪环的上方,可推测此种反应模式有利于FADH-中N5的离域与醌环中O的离域发生轨道重叠,从而在FADH-中的N5位和醌环之间发生2e-/1H+的转移。文献中有关醌环也是以相对平行的空间位置堆叠于FADH-异咯嗪环上方的。例如,Zhang等[16]使用NQO1晶体结构(PDB ID:3JSX)来探究CA-4和NQO1之间的潜在结合模式,发现CA-4的醌环结构平行于FADH-异咯嗪环上方的;Liu等[26]将雷公藤甲素(TP)与Q3PA连接合成出CX-23,将其与NQO1晶体对接也证明了这一点。各途径的势能曲线如图3所示,各驻点的相对能量列于表1。从表1所示M062X/6-31+G(d,p)水平上气相中各驻点的相对能量值分析可知,各路径第一步的羟基化反应(TSA-1、TSB-1、TSC-1)为吸热反应,其中TSA-1的反应能垒为10.57 kcal/mol,而TSB-1与TSC-1的反应能垒分别为36.60和26.24 kcal/mol,后者能垒较高,表明在第一步的还原过程中,FADH-中N5位和醌环中O原子之间更容易发生2e-/1H+的耦合转移。而在第二步的组氨酸残基质子化过渡态(TSA-2、TSC-2)均为放热反应,其中TSA-2的反应能垒为15.49 kcal/mol,而TSC-2的反应能垒为2.82 kcal/mol,后者能垒较低,表明反应TSC-2更容易发生。在路径B中设计了互变异构化反应TSB-2,但其能垒高达43.04 kcal/mol,能垒较高,不容易发生反应。在路径C经过过渡态TSC-1生成中间体ICC-1后,经过过渡态TSD-2,由H2O作为质子转移通道生成羟基化产物ICA-1的反应能垒是26.15 kcal/mol,高于过渡态TSA-1的反应能垒,表明中间体ICA-1的生成更倾向于经过路径A。在生成中间体ICC-2后经过过渡态TSC-3由H2O介导质子转移,其能垒为29.53 kcal/mol,高于过渡态TSA-2的能垒,表明ICA-2更倾向于通过路径A中的过渡态TSA-2生成。结果表明,虽然过渡态TSC-2的能垒比过渡态TSA-2的能垒低12.67 kcal/mol,但是路径A中的过渡态TSA-1的能垒比过渡态TSC-1的能垒低15.67 kcal/mol且只需要两步反应。总体来说,路径A为Q3PA双电子还原的优势路径,过渡态TSA-3为其控速步骤,反应能垒为30.96 kcal/mol。为了模拟酶体系中的反应环境,采用SMD隐式溶剂模型在氯苯和乙腈两种不同介质中计算了各驻点的能量,结果表明在溶剂中反应的能量变化趋势与气相中是一致的。
表1 FADH-介导的Q3PA还原反应的相对能量(E)、焓(H)和吉布斯自由能(G)注
Tab.1 Relative energies (E),enthalpies (H) and Gibbs free energies (G) for the reduction of Q3PA mediated by FADH- (kcal/mol)
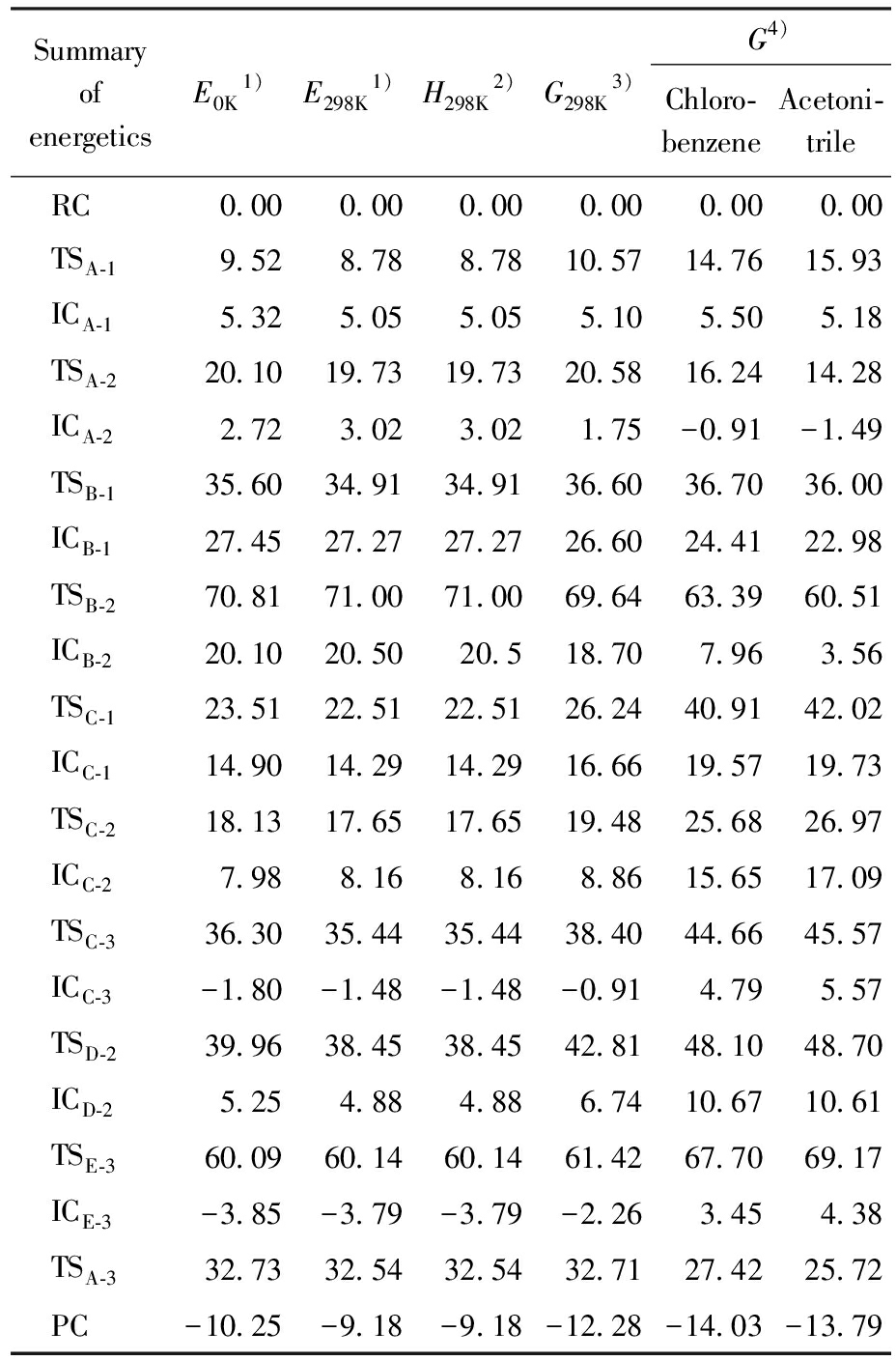
Summary of energeticsE0K1)E298K1)H298K2)G298K3)G4)Chloro-benzeneAcetoni-trileRC0.000.000.000.000.000.00TSA-19.528.788.7810.5714.7615.93ICA-15.325.055.055.105.505.18TSA-220.1019.7319.7320.5816.2414.28ICA-22.723.023.021.75-0.91-1.49TSB-135.6034.9134.9136.6036.7036.00ICB-127.4527.2727.2726.6024.4122.98TSB-270.8171.0071.0069.6463.3960.51ICB-220.1020.5020.518.707.963.56TSC-123.5122.5122.5126.2440.9142.02ICC-114.9014.2914.2916.6619.5719.73TSC-218.1317.6517.6519.4825.6826.97ICC-27.988.168.168.8615.6517.09TSC-336.3035.4435.4438.4044.6645.57ICC-3-1.80-1.48-1.48-0.914.795.57TSD-239.9638.4538.4542.8148.1048.70ICD-25.254.884.886.7410.6710.61TSE-360.0960.1460.1461.4267.7069.17ICE-3-3.85-3.79-3.79-2.263.454.38TSA-332.7332.5432.5432.7127.4225.72PC-10.25-9.18-9.18-12.28-14.03-13.79
注:1)在M062X/6-31+G(d,p)水平上计算的气相中各驻点相对能量;2)在M062X/6-31+G(d,p)水平上计算的气相中各驻点的焓;3)在M062X/6-31+G(d,p)水平上计算的气相中各驻点的吉布斯自由能;4)在SMD-M062X/6-311+G(3df,2p)//M062X/6-31+G(d,p)水平上计算的不同溶剂模型中各驻点的吉布斯自由能。
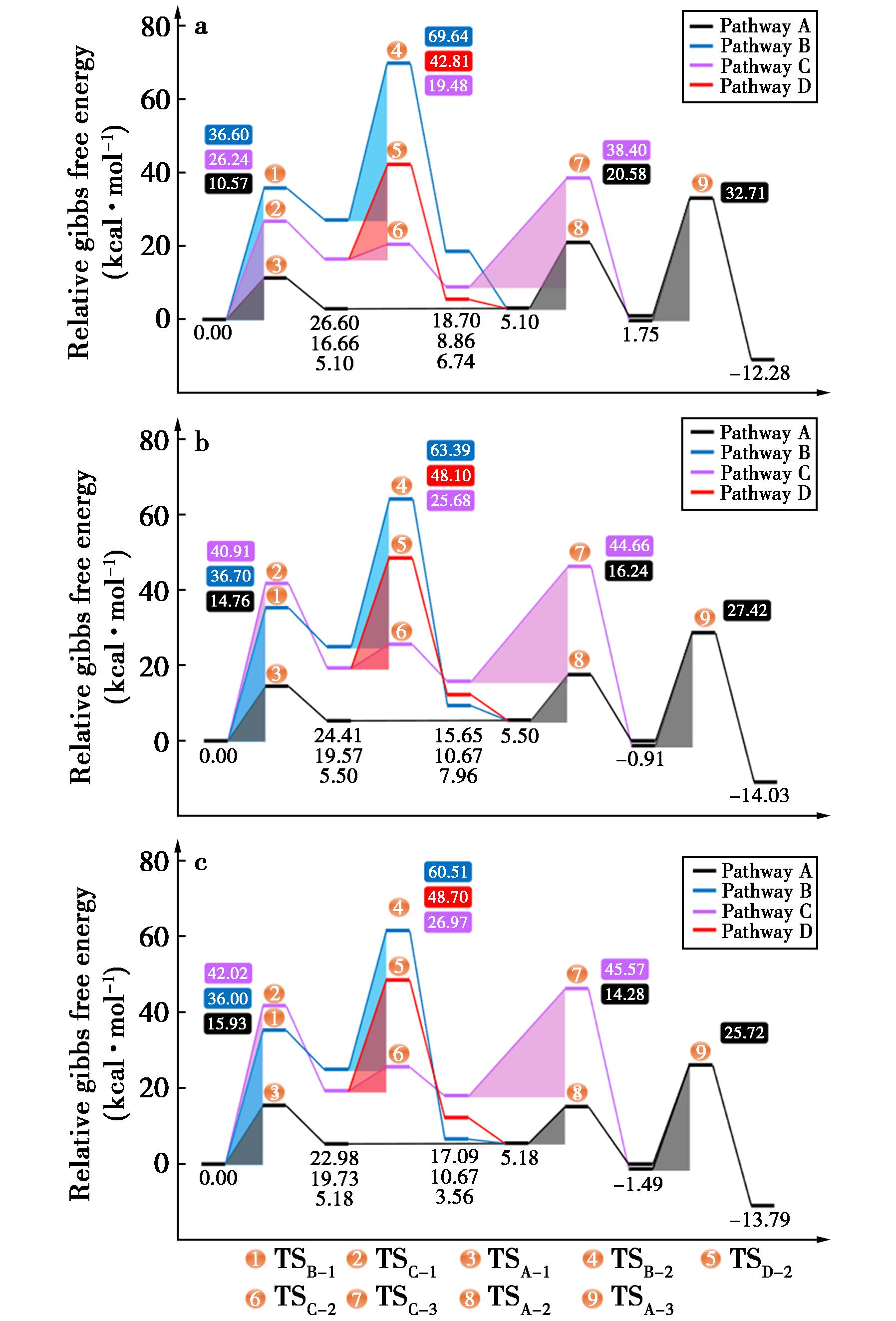
a.气相条件下的势能曲线;b.氯苯溶剂中的势能曲线;c.乙腈溶剂中的势能曲线
图3 M062X/6-311+G(3df,2p)//M062X/6-31+G(d,p)水平计算所得FADH-介导Q3PA还原反应势能曲线
Fig.3 Energy profile of the reduction of Q3PA mediated by FADH- calculated at M062X/6-311+G(3df,2p)//M062X/6-31+G(d,p) theoretical level
2.2 Q3PA与NQO1蛋白的相互作用
图4为经分子对接得到的Q3PA与NQO1的复合物结构。结果表明,Q3PA进入了NQO1蛋白的活性口袋,底物对苯醌部分平行于FADH2的异咯嗪环,形成了π-π堆积。Q3PA两侧的羰基和酪氨酸残基(Tyr126和Tyr128)分别形成了一个氢键,酪氨酸残基芳香环与配体疏水区域形成疏水夹心结构,协同氢键作用进一步稳定了配体在酶活性中心的结合。FADH2与配体的紧密接触有利于调节电子传递路径,或通过空间位阻效应影响底物进入活性位点的取向,从而参与催化反应的调控[27]。值得注意的是,Q3PA与FADH2异咯嗪环的N5位距离3.5 Å。Fraaije等[28]报导在配体与黄素的异咯嗪环发生π-π堆积时,还原位点通常距离黄素的N5位3.5 Å左右,这与本文分子对接得到的结果相吻合。
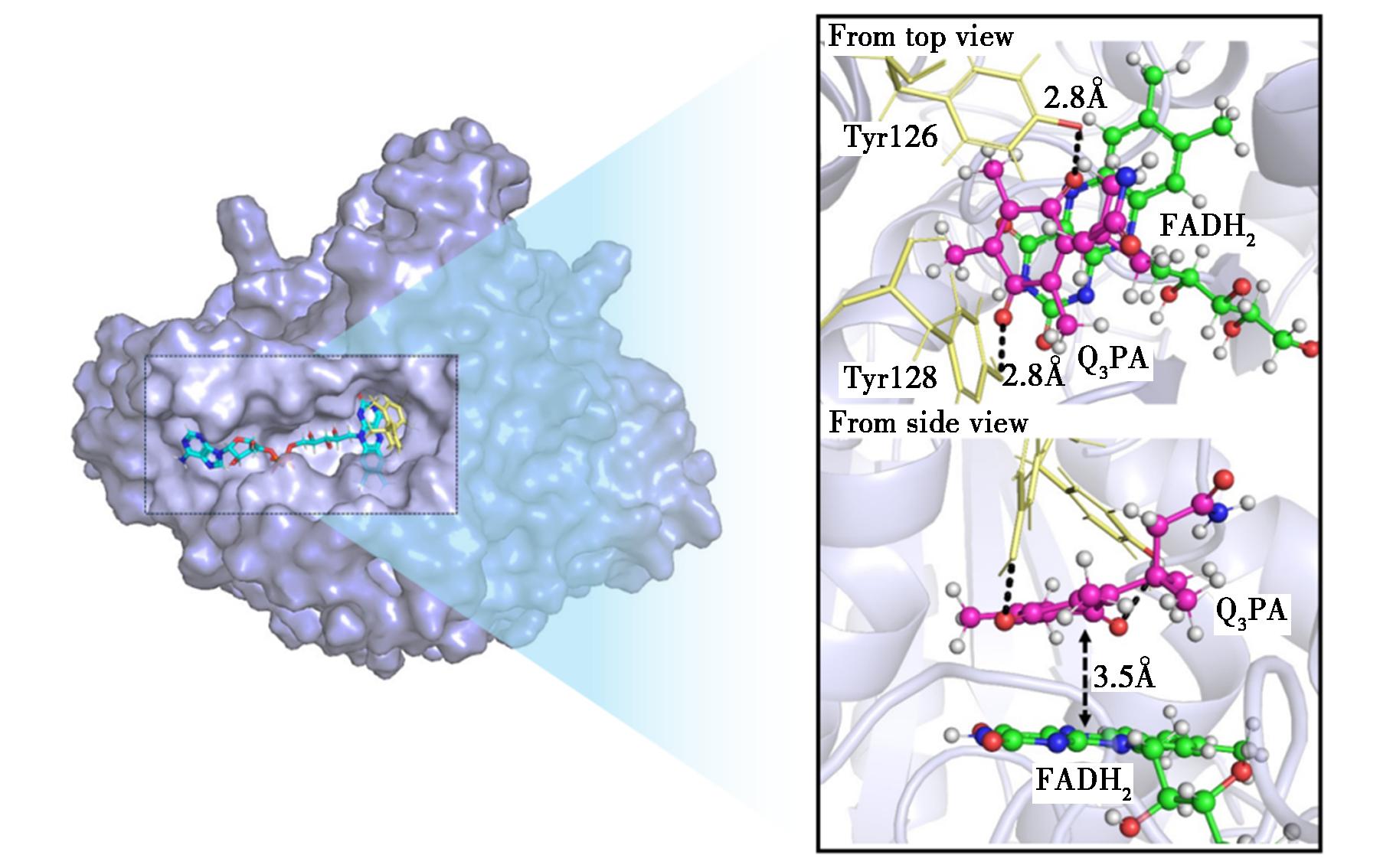
右图为从分子对接的俯视图与侧视图,其中Q3PA用紫色显示,与配体形成氢键的残基用黄色显示,FADH2用绿色显示,氢键相互作用用黑色虚线表示,距离以Å为单位
图4 Q3PA与NQO1酶分子对接的结构
Fig.4 Structure of molecular docking of Q3PA and NQO1 enzyme
Q3PA-NQO1复合物活性中心底物、氨基酸残基及辅酶之间相互作用的二维模型分析如图5a所示。除了上文中提到的形成了2个氢键,底物与酶活性中心之间还存在多种相互作用:Tyr126与Q3PA之间存在Pi-sigma相互作用;FADH2不仅与Q3PA形成π-π堆积,还与其形成烷基相互作用;此外,多个氨基酸残基与底物形成烷基相互作用,包括Pro68、Trp105、Phe106、Tyr128、His161和Phe178。本文还对Q3PA与NQO1活性中心的疏水相互作用进行了分析。如图5b所示,辅酶FADH2与底物之间存在明显的疏水相互作用,已有研究表明FADH2的异咯嗪环被His161、Tyr126和Tyr128等残基包裹,通过疏水作用维持其在疏水口袋中的结合[14]。多个氨基酸残基参与了与底物之间的疏水相互作用,包括Trp105、Phe106、Tyr126、Tyr128、His161和Phe178。这些残基中的苯环结构常通过π-π堆积和疏水作用参与稳定局部构象。总之,上述这些结构特点确保了底物能够稳定的结合于酶活性中心,进而与辅酶相互靠近并发生多步还原反应。
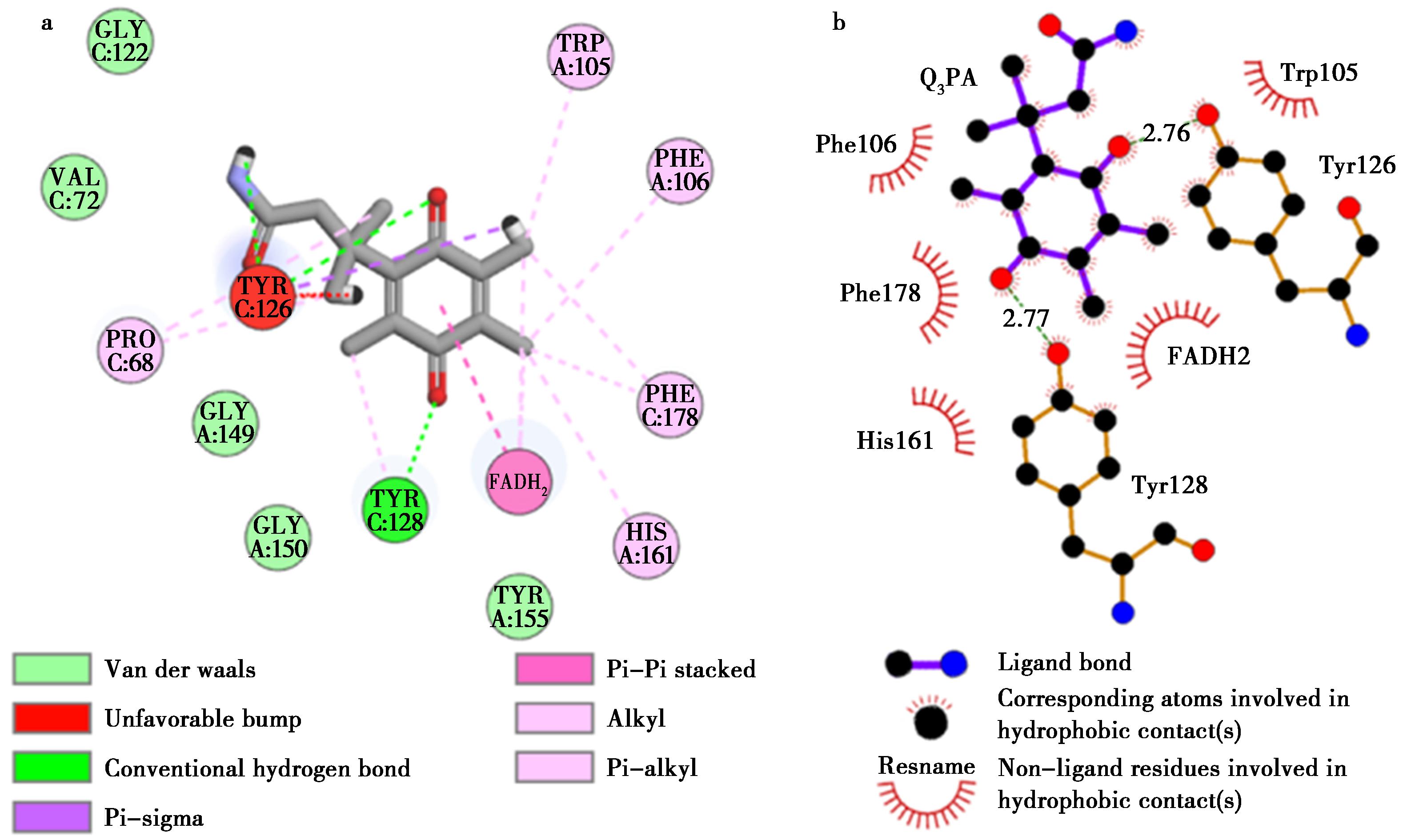
图5 Q3PA与NQO1酶的二维模型分析图(a)和Q3PA与NQO1酶的疏水相互作用分析图(b)
Fig.5 2D model analysis of Q3PA and NQO1 enzyme (a) and hydrophobic interaction analysis of Q3PA and NQO1 enzyme (b)
3 结论
本文对NQO1催化Q3PA还原的机制进行了研究。首先,采用DFT方法探讨了Q3PA在辅酶FADH2的作用下最终还原为相应的对氢醌结构并通过内酯化释放氨气的反应机理,明确了反应过程中的分子结构和能量变化趋势。结果表明,Q3PA首先接受来自FADH2的2e-/1H+生成半醌中间体ICA-1,然后对侧醛基接受来自组氨酸残基的1H+生成对氢醌中间体ICA-2,最后经过内酯化反应生成产物。然后,通过分子对接探讨了Q3PA与NQO1酶蛋白之间的相互作用,发现底物与酶活性中心通过氢键、输水相互作用、π-π堆积等形成了紧密结合的复合物。总之,本文为阐明以Q3PA为响应基团的HAP的靶向作用机制提供了理论依据,对设计开发新型靶向性抗肿瘤药物具有参考价值。
[1]Hunter F W,Wouters B G,Wilson W R.Br.J.Cancer,2016,114(10):1071-1077.
[2]Anduran E,Dubois L J,Lambin P,Winum J Y.Expert Opin.Ther.Pat.,2022,32(1):1-12.
[3]Yu C S,Ouyang H G,Hu B,Weng Z B,Li Y Y.Prog.Pharm.Sci.,2012,36(2):65-72.
余长顺,欧阳洪贵,胡斌,翁志斌,李玉艳.药学进展,2012,36(2):65-72.
[4]Mendoza M F,Hollabaugh N M,Hettiarachchi S U,Mccarley R L.Biochemistry,2012,51(40):8014-8026.
[5]Navarro F,Arroyo A,Martín S F,Bello R I,Cabo R,Burgess J R,Navas P,Villalba J M.BioFactors,1999,9(2/3/4):163-170.
[6]Siegel D,Mcguinness S M,Winski S L,Ross D.Pharmacogenetics,1999,9(1):113-122.
[7]Winski S L,Koutalos Y,Bentley D L,Ross D.Cancer Res.,2002,62(5):1420-1424.
[8]Siegel D,Ross D.Free.Radic.Biol.Med.,2000,29(3/4):246-253.
[9]Jamieson D,Wilson K,Pridgeon S,Margetts J P,Edmondson R J,Leung H Y,Knox R,Boddy A V.Clin.Cancer Res.,2007,13(5):1584-1590.
[10]Danson S,Ward T H,Butler J,Ranson M.Cancer Treat.Rev.,2004,30(5):437-449.
[11]Colucci M A,Couch G D,Moody C J.Org.Biomol.Chem.,2008,6(4):637-656.
[12]Volpato M,Abou-zeid N,Tanner R W,Glassbrook L T,Taylor J,Stratford I,Loadman P M,Jaffar M,Phillips R M.Mol.Cancer Ther.,2007,6(12):3122-3130.
[13]Weerapreeyakul N,Anorach R,Khuansawad T,Yenjai C,Isaka M.Chem.Pharm.Bull.,2007,55(6):930-935.
[14]Zhang X,Li X,Li Z H,Wu X S,Wu Y,You Q D,Zhang X J.Org.Lett.,2018,20(12):3635-3638.
[15]Qu Y,Zhang C,Ma X,Gao Y H,Liu J,Wu L Q.Bioorg.Med.Chem.,2020,28(24):115821.
[16]Zhang C,Qu Y,Ma X,Li M P,Li S,Li Y,Wu L Q.Bioorg.Chem.,2020,103:104200.
[17]Park J,Jo S,Lee Y M,Saravanakumar G,Lee J,Park D,Kim W J.ACS Appl.Mater.Interfaces,2021,13(7):8060-8070.
[18]Curtolo F,Arantes G M.J.Chem.Inf.Model.,2020,60(12):6282-6287.
[19]Song J C,Zheng D W,Wang S B,Wang J J,Sun G H,Zhang N,Zhao L J,Zhong R G.Chem.Reagents,2022,44(11):1598-1604.
宋佳宸,郑大威,王圣博,王娇娇,孙国辉,张娜,赵丽娇,钟儒刚.化学试剂,2022,44(11):1598-1604.
[20]Wang S B,Wang J J,Ren T,Sun G H,Zhang N,Zhao L J,Zhong R G.Chem.Reagents,2023,45(9):29-37.
王圣博,王娇娇,任婷,孙国辉,张娜,赵丽娇,钟儒刚.化学试剂,2023,45(9):29-37.
[21]Goerigk L,Grimme S.Phys.Chem.Chem.Phys.,2011,13(14):6670.
[22]Huang W J,Gherib R,Gauld J W.J.Phys.Chem.B,2012,116(30):8916-8929.
[23]Isaev A N.Russ.J.Phys.Chem.,2003,77(11):1821-1826.
[24]Voehringer-martinez E,Hernandez-soto H.Science,2007,316(5825):691-691.
[25]Liu K R,Badamdorj B,Yang F,Janik M J,Antonietti M.Appl.Catal.B Environ.,2022,316:121641.
[26]Liu M L,Song W,Du X,Su J T,Dong K,Chen Y,Peng Z H.ACS Med.Chem.Lett.,2018,9(12):1253-1257.
[27]Dourado D F A R,Swart M,Carvalho A T P.Chem,2018,24(20):5246-5252.
[28]Fraaije M W,Mattevi A.Trends Biochem.Sci.,2000,25(3):126-132.