Al3+是生物圈中第三丰富的金属元素(其含量为8.3%),在食品包装、炊具、制药等领域具有广泛应用[1,2]。然而,人类活动中铝的过度使用会导致游离铝离子释放到环境和生物体内,导致铝在土壤和地表水中累积,从而引发阿尔茨海默病、帕金森病、痴呆症等疾病[3,4]。根据世界卫生组织(WHO)的声明,人类每日可耐受的铝(Al3+)摄入量约为3~10 mg[5-7]。因此,确定环境中Al3+及生物系统中铝含量的检测方法对于人类生命和环境科学研究至关重要。与原子吸收光谱法(AAS)、电感耦合等离子体质谱法(ICP-MS)等检测仪器相比,荧光检测技术因选择性好、灵敏度高、操作简便和实时检测等特点,得到科研工作者广泛关注,特别是在生物医学和环境科学领域已得到应用[8-12]。因此,设计出一种制备成本低、灵敏度高、选择性好的Al3+荧光探针仍然非常重要[13-21]。萘作为一种结构简单的双环芳香化合物,常存在于煤焦油中,具有一定的刺激性气味。萘结构最早是在1819年,被苏格兰化学家Alexzander garden所发现;1826年,Michael Faraday第一次报道其分子式为C10H8[22];近年来,科学家发现萘衍生物具有多种拮抗作用,包括抗肿瘤、抗菌、抗炎、抗病毒、抗高血压等[23]。
2017年,Chen等[24]报道了一种激发态分子内质子转移(ESIPT)和聚集诱导发光(AIE)荧光探针,其在溶液和活细胞中可以比率型检测Al3+。2024年,Gan等[25]报道了一种简单的Al3+和F-荧光探针,可以应用于检测茶叶植物组织中的Al3+。2019年,Zhai等[26]报道了一种可以调控ESIPT效应的金属Mg有机骨架(Mg-MOF)材料,相比较于Ga3+、In3+、Fe3+、Cr3+、Ca2+和Mg2+等金属离子,该材料对Al3+表现出独特检测能力,其检测限为28 nmol/L。2018年,Velmurugan等[27]开发了一种双萘基荧光探针用于Ni2+和Al3+离子的双通道检测。Ni2+和Al3+离子的感测通过两种途径进行:(ⅰ)通过阻止光致电子转移过程而产生的荧光开启响应;(ⅱ)通过分子内电荷转移过程而发生的红移荧光富集。上述研究工作对Al3+荧光探针的发展起到关键作用,但这些研究工作仍然存在结构合成复杂的问题[28,29]。
萘衍生物是一种新型的荧光探针,其结构基于双苯基环具有共轭特性。此外,萘具有良好的可塑性,可以通过改变萘环上取代基对其进行修饰,从而实现对其光学性质的调控。尽管Al3+荧光探针被广泛研究,但在结构和性能上仍然需要改进。作为一种新型的荧光探针,萘衍生物在荧光成像方面具有出色的性能,例如成本低廉、稳定性良好、结构可塑性强、发光性能优异以及量子效率高等。
本文设计筛选了两种易于合成的萘碳酰腙化合物L1和L2(图1),探针L1在V(乙醇)∶V(HEPES buffer)=3∶7(pH 7.4)体系中对Al3+表现出高的选择性、抗干扰性和低检测限,为Al3+的的荧光检测提供新的检测工具,为萘碳酰腙荧光探针的设计提供新的依据。此外,探针L1还可以检测活细胞中Al3+浓度。
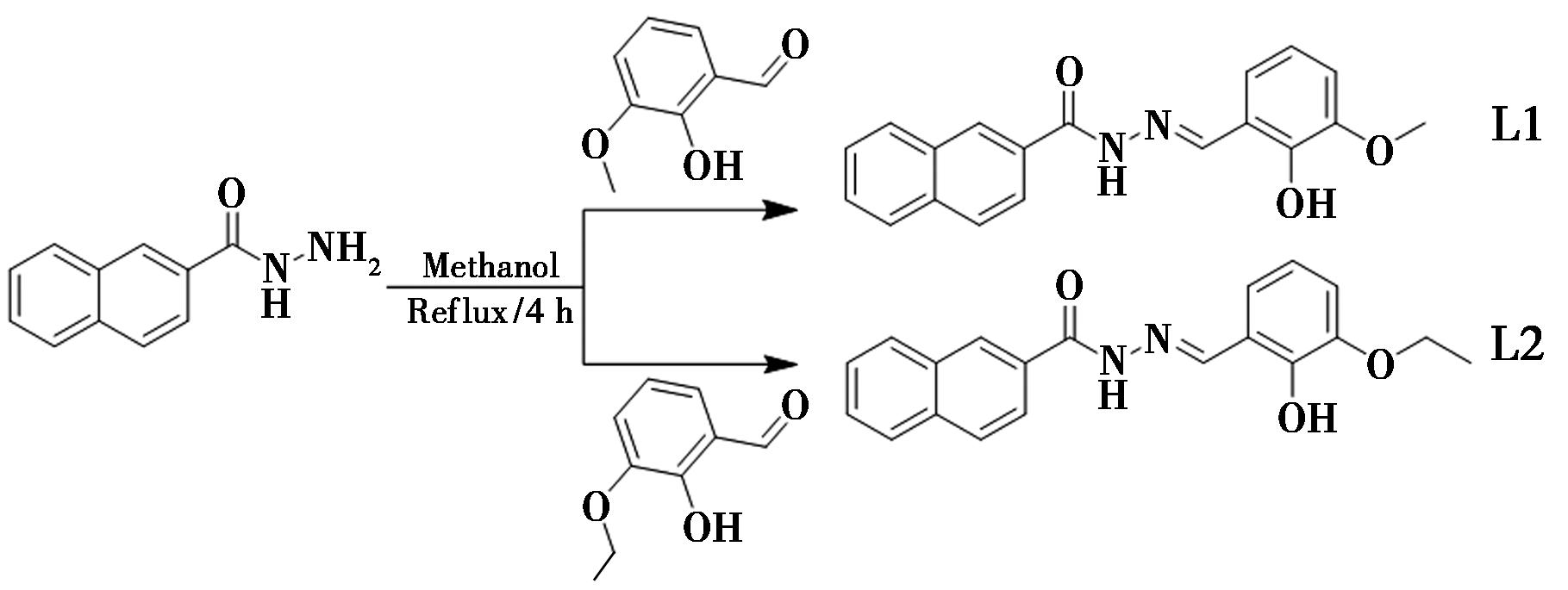
图1 探针L1和L2的合成路线
Fig.1 Synthetic route of probe L1 and L2
Bruker micrOTOF-Q Ⅱ型质谱仪、Bruker AVANCE Ⅲ-400型核磁共振波谱仪(德国布鲁克公司);Hitachi F-4500型荧光光谱仪(日本日立公司);X-4型显微熔点仪(北京泰克仪器有限公司)。
所有阳离子盐均以氯化物盐的形式购买自上海阿拉丁生化科技股份有限公司。
在50 mL圆底烧瓶中加入0.186 g(1 mmol) 2-萘甲酰肼和0.152 g(1 mmol)邻香草醛,另外加入15 mL甲醇作为溶剂,回流搅拌4 h。反应完成后减压除去溶剂,得到黄色沉淀,过滤,用冰冻乙醇洗涤3次,在冷的甲醇中重结晶得到黄色固体,产率:83%,m.p.115~117 ℃。1HNMR(DMSO-d6,400 MHz),δ:12.27(s,1H);11.00(s,1H);8.72(s,1H),8.58(s,1H);8.07(d,2H,J=7.2 Hz);8.02(d,2H,J=7.6 Hz);7.64(s,2H);7.18(d,1H,J=8.0 Hz);7.05(d,1H,J=7.6 Hz);6.89(m,1H);3.83(s,3H)。ESI-MS:m/z:343.1072。
探针L2的合成方法和探针L1的合成方法相同,产率:86%,m.p.104~106 ℃。1HNMR(DMSO-d6,400 MHz),δ:12.27(s,1H);11.00(s,1H);8.71(s,1H);8.58(s,1H);8.01~8.10(m,4H);7.66(s,2H);7.18(d,1H,J=7.6 Hz);7.02(d,1H,J=7.6 Hz);6.86(m,1H);4.07(s,2H);1.36(s,3H)。ESI-MS:m/z:357.1208。
探针L1和L2(10 μmol/L)的荧光光谱在 V(乙醇)∶V(HEPES buffer)=3∶7(pH 7.4)溶液中测定,采用1 cm石英比色皿。氯化物盐Na+、K+、Ag+、Mg2+、Ca2+、Al3+、Cr3+、Mn2+、Fe2+、Fe3+、Co2+、Ni2+、Cu2+、Zn2+、Cd2+、Ba2+、Hg2+和Pb2+作为金属离子(1.0×10-2 mol/L),采用蒸馏水溶解。荧光滴定实验,不同量的Al3+和0.1 mL(200 μmol/L)的L1混合,用V(乙醇)∶V(HEPES buffer)=3∶7(pH 7.4)稀释定容。激发波长Ex为380 nm,发射波长Em为400~800 nm。
荧光探针L1和L2在380 nm波长激发时表现出弱荧光发射,如图2a所示。在溶液中,游离探针分子本身存在光诱导电子转移(Photoinduced Electron Transfer,PET)效应而产生较弱的荧光。然而,当10 μmol/L探针L1和L2在V(乙醇)∶V(HEPES buffer)=3∶7(pH 7.4)溶液中添加Al3+会导致体系在558和553 nm处出现显著的荧光增强。在理想状态下,其他金属离子如Na+、K+、Ag+、Mg2+、Ca2+、Cr3+、Mn2+、Co2+、Ni2+、Zn2+、Cd2+、Ba2+、Hg2+、Pb2+几乎未显示出显著的光谱变化。如图2b所示,展示了探针L1和L2对Al3+的择优性。只有Fe2+、Fe3+和Cu2+引起了淬火效应,该现象归因于3种金属自身固有的磁性。在Al3+存在的条件下,探针L1产生了最显著的蓝色荧光响应,表明探针L1对Al3+具有优异的荧光选择性。
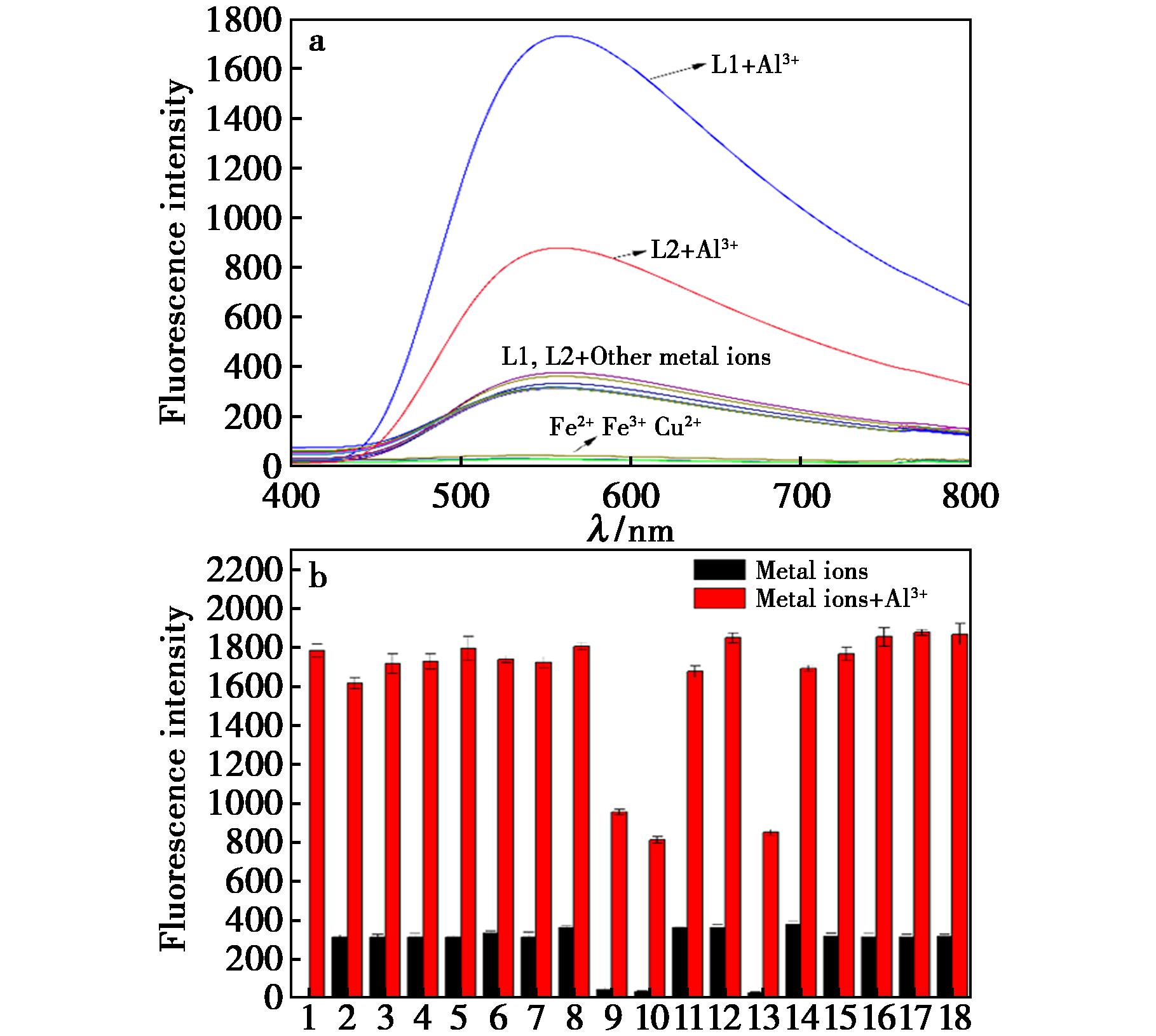
1~18:Na+、K+、Ag+、Mg2+、Ca2+、Al3+、Cr3+、Mn2+、Fe2+、Fe3+、Co2+、Ni2+、Cu2+、Zn2+、Cd2+、Ba2+、Hg2+和Pb2+
图2 a.探针L1和L2分别加入各种分析物后的荧光发射光谱;b.探针L1与Al3+和其它阳离子作用后的发射强度变化
Fig.2 Fluorescence emission spectra of probe L1 and L2 in the presence of various analytes;b.Emission intensity changes of probe L1 with Al3+ and other cations
竞争实验探究了在V(乙醇)∶V(HEPES buffer)=3∶7(pH 7.4)溶液中10 μmol/L探针L1对Al3+的抗干扰能力,如图2b所示。在Al3+存在的作用下,加入其它竞争离子,测量其荧光强度。探针L1在558 nm处的荧光发射强度当加入竞争离子时没有变化;当体系加入Al3+时,激发波长为 380 nm,荧光强度引起显著提升。该研究结果表明,探针L1对Al3+具有良好选择性,即便其他干扰离子存在的情况下也不受影响。
为了进一步研究10 μmol/L荧光探针L1在V(乙醇)∶V(HEPES buffer)=3∶7(pH 7.4)溶液中对Al3+的检测能力,开展了荧光滴定实验,如 图3所示。游离的探针L1在380 nm处表现出微弱的荧光发射,当加入Al3+后,化学传感器L1在558 nm处的荧光显著增强。在紫外灯照射下,观察到荧光从微弱荧光变为蓝色荧光。探针L1荧光强度与Al3+(0~0.5 μmol/L)浓度之间存在线性关系(R2=0.9925)。通过Benesi-Hildebrand方程计算得出探针L1对Al3+的结合常数为1.50×105(mol/L)-1,其最低检测限(LOD)为47.3 nmol/L(3σ/κ),σ代表10次探针荧光值标准偏差,κ代表L1荧光强度与Al3+浓度线性曲线斜率。
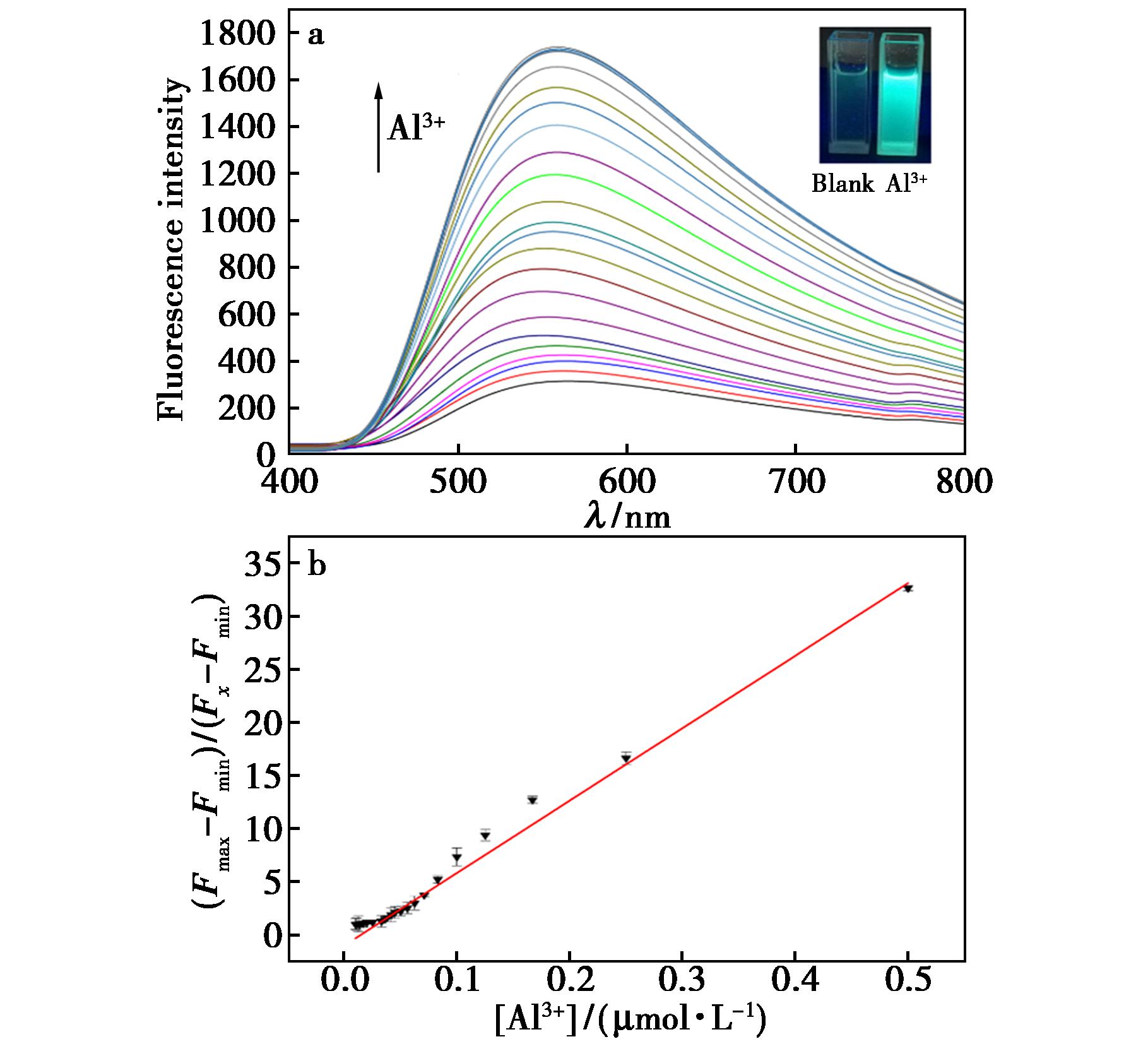
图3 a.探针在加入0~50 μmol/L Al3+后的荧光发射图(插图:在365 nm光线下,颜色发生变化);b.Al3+浓度在0~0.5 μmol/L范围内558 nm处探针L1变化线性图
Fig.3 a.Fluorescence emission spectroscopy of probe L1 after addition of 0~50 μmol/L Al3+(λex=380 nm);inset:emission color change under 365 nm light;b.Fluorescence intensity of probe L1 at 558 nm as a function of Al3+ concentration from 0 to 0.5 μmol/L
探针L1、L2和L1-Al3+的能量优化轨道通过高斯09 B3LYP/6-31G(d,p)进行计算,如图4所示。DFT理论计算发现最高占有轨道(HOMO)-(最低未占有轨道)LUMO的轨道能量差为3.18 eV,其值低于探针L1的能量差(4.57 eV)。理论计算研究结果表明,探针分子对金属Al3+恰好匹配,导致分子螯合,从而实现对Al3+的高选择性荧光增强响应。探针L1和L2的LUMO和HOMO的电子密度分布在萘碳酰腙上,而L1-Al3+的LUMO和HOMO的电子密度则转移到了亚胺基团。理论计算的结果预测了探针L1与Al3+的结合模式,并且与实验结果一致。
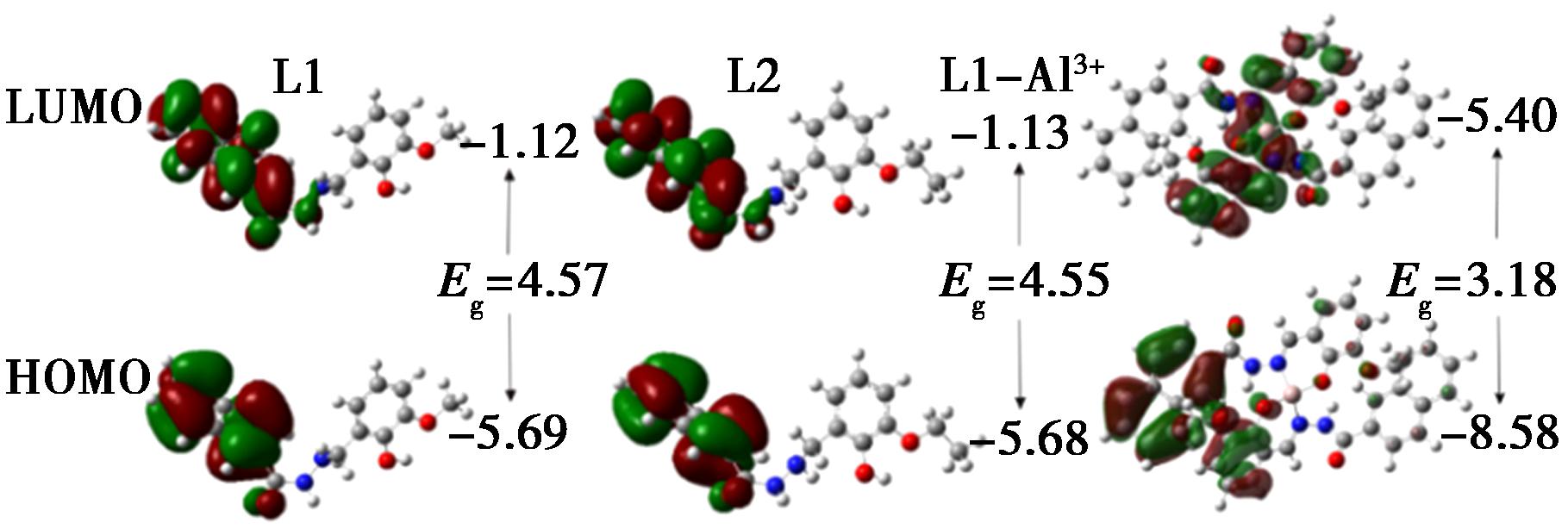
图4 DFT理论计算的探针L1、L2和L-Al3+的HOMO/LUMO能量轨道
Fig.4 Optimized structures and HOMO/LUMO of probe L1,L2 and complex L1-Al3+ by DFT calculation
为了探究探针L1和Al3+的结合模式,通过Job’s Pot研究。10 μmol/L探针L1与Al3+浓度比分别为:0∶10、1∶9、2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1和10∶0的V(乙醇)∶V(HEPES buffer)=3∶7(pH 7.4)溶液。探针L1与Al3+的总浓度保持在10 μmol/L。在发射波长为558 nm处,当Al3+的物质的量比为0.30时,其荧光发射强度达到最大,如图5所示。该研究结果表明探针L1与Al3+的结合比为2∶1,形成稳定的配合物。通过高分辨质谱研究,ESI-MS在CH3OH中的ESI-MS为665.232,与Job’s Pot实验一致。探针L1和L1-Al3+在DMSO-d6溶液中通过 1HNMR被研究。其中亚胺信号(—CH![]() N—)在δ 11.2处和羟基信号(—OH)在δ 12.1处。当加入Al3+之后,羟基信号(—OH)消失,亚胺信号(—CH
N—)在δ 11.2处和羟基信号(—OH)在δ 12.1处。当加入Al3+之后,羟基信号(—OH)消失,亚胺信号(—CH![]() N—)移动到δ 10.2处,如图7所示。该结果表明Al3+与探针L1的结合导致探针L1中一个酚羟基—OH的脱质子化,上述实验结果与理论计算结果保持一致,其检测机理为光诱导电子转移(PET)进程和 —C
N—)移动到δ 10.2处,如图7所示。该结果表明Al3+与探针L1的结合导致探针L1中一个酚羟基—OH的脱质子化,上述实验结果与理论计算结果保持一致,其检测机理为光诱导电子转移(PET)进程和 —C![]() N—异构化行为,机理示意图如图6所示。
N—异构化行为,机理示意图如图6所示。
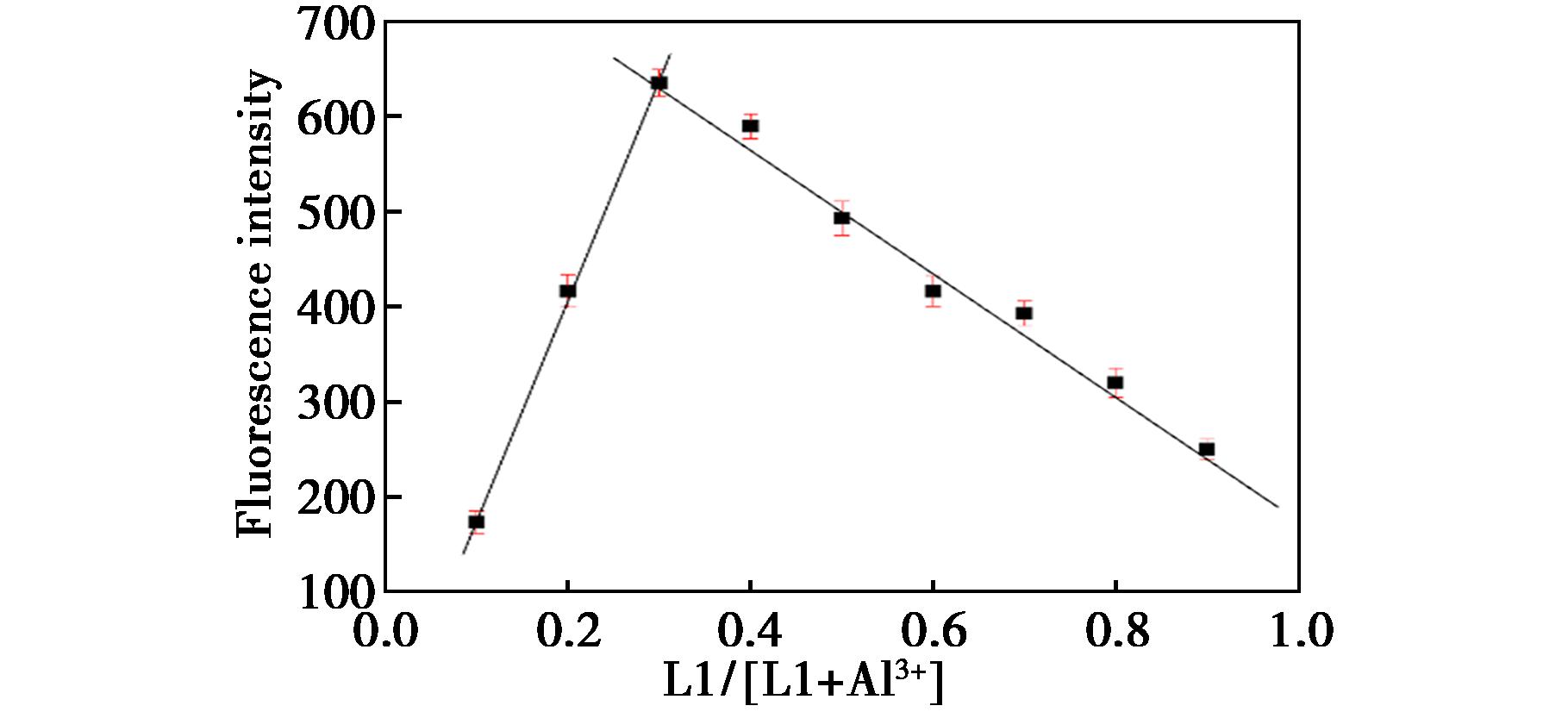
图5 探针L1和Al3+的Job’s Pot曲线图
Fig.5 Job’s Pot of probe L1 and Al3+
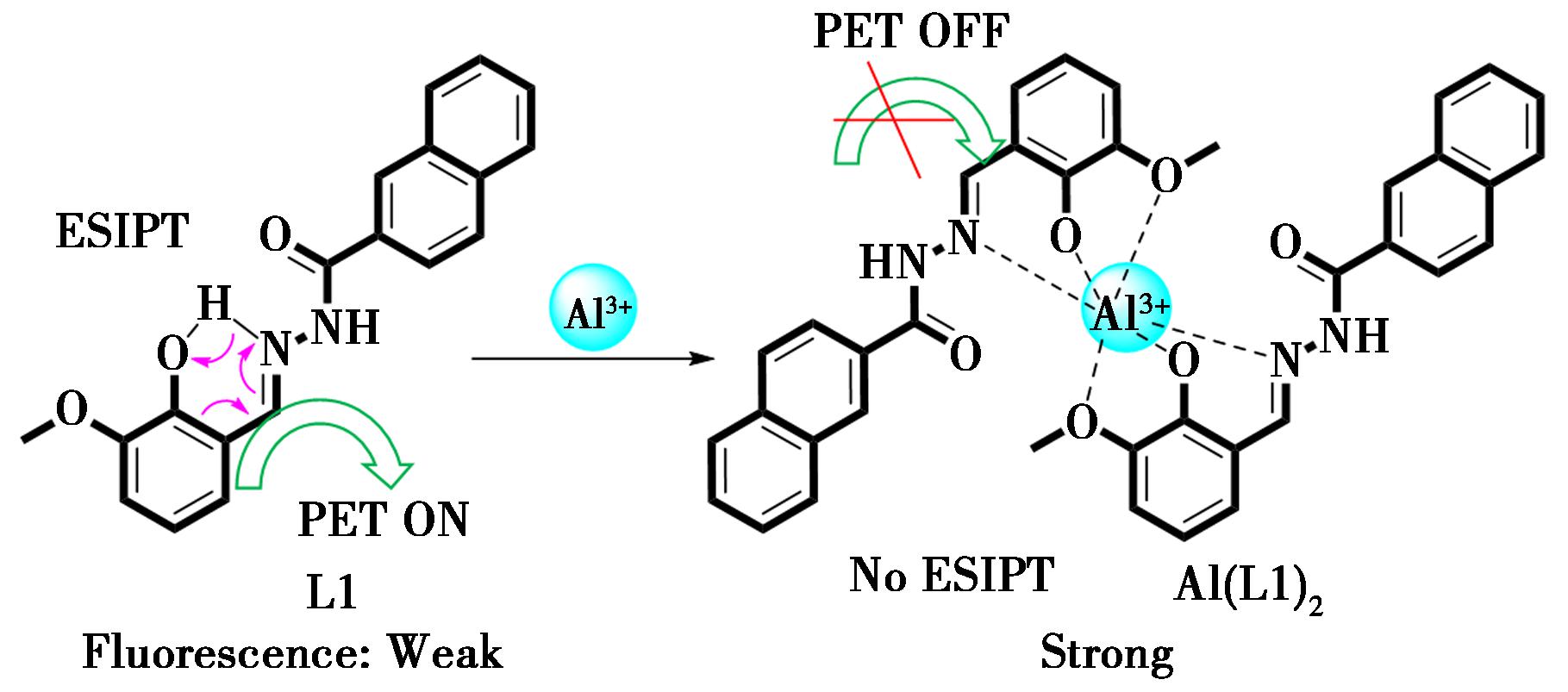
图6 探针L1识别Al3+的荧光增强机理
Fig.6 Fluorescence enhancement mechanism for probe L1 to recognize Al3+
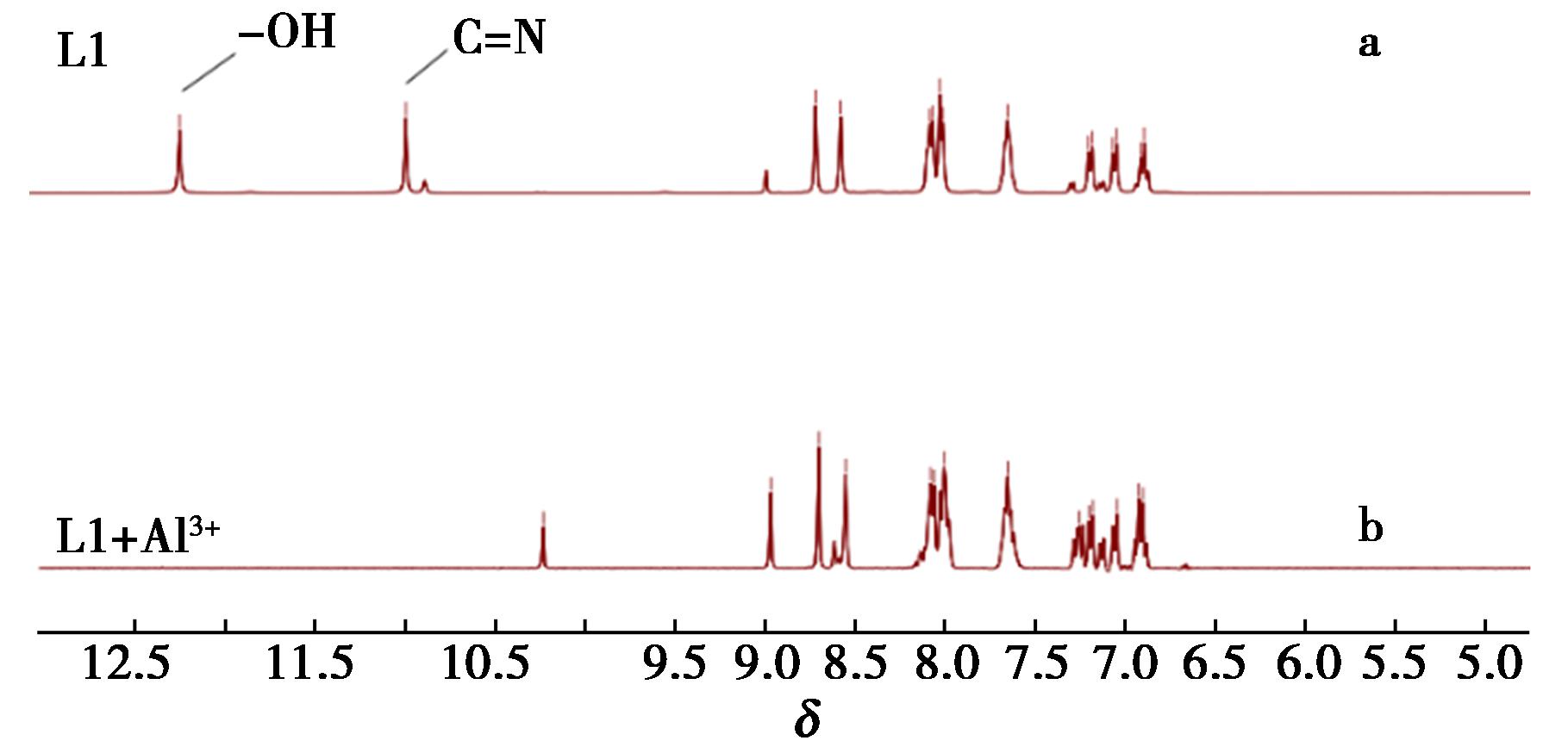
图7 a.探针L1(a)、L1+AlCl3(10 μmol/L)(b)的 1HNMR谱图
Fig.7 1HNMR spectrum of probe L1(a) and L1+AlCl3(10 μmol/L)(b)
可逆性是荧光化学传感器的重要性能。因此,该实验研究了荧光探针L1的荧光可逆性检测性能,以评估探针L1的可重复使用性能。如图8所示,研究了10 μmol/L探针L1在V(乙醇)∶V(HEPES buffer)=3∶7(pH 7.4)溶液中对Al3+的可回收性。当L1-Al3+溶液中加入EDTA后,L1-Al3+溶液的荧光强度已降至接近游离探针L1的荧光发射强度。该研究结果表明,EDTA可以将溶液中L1-Al3+复合物中的Al3+解析出来,通过滴加Al3+和EDTA,荧光信号表现出“ON-OFF-ON”模式循环3次,实现探针L1的可重复利用。
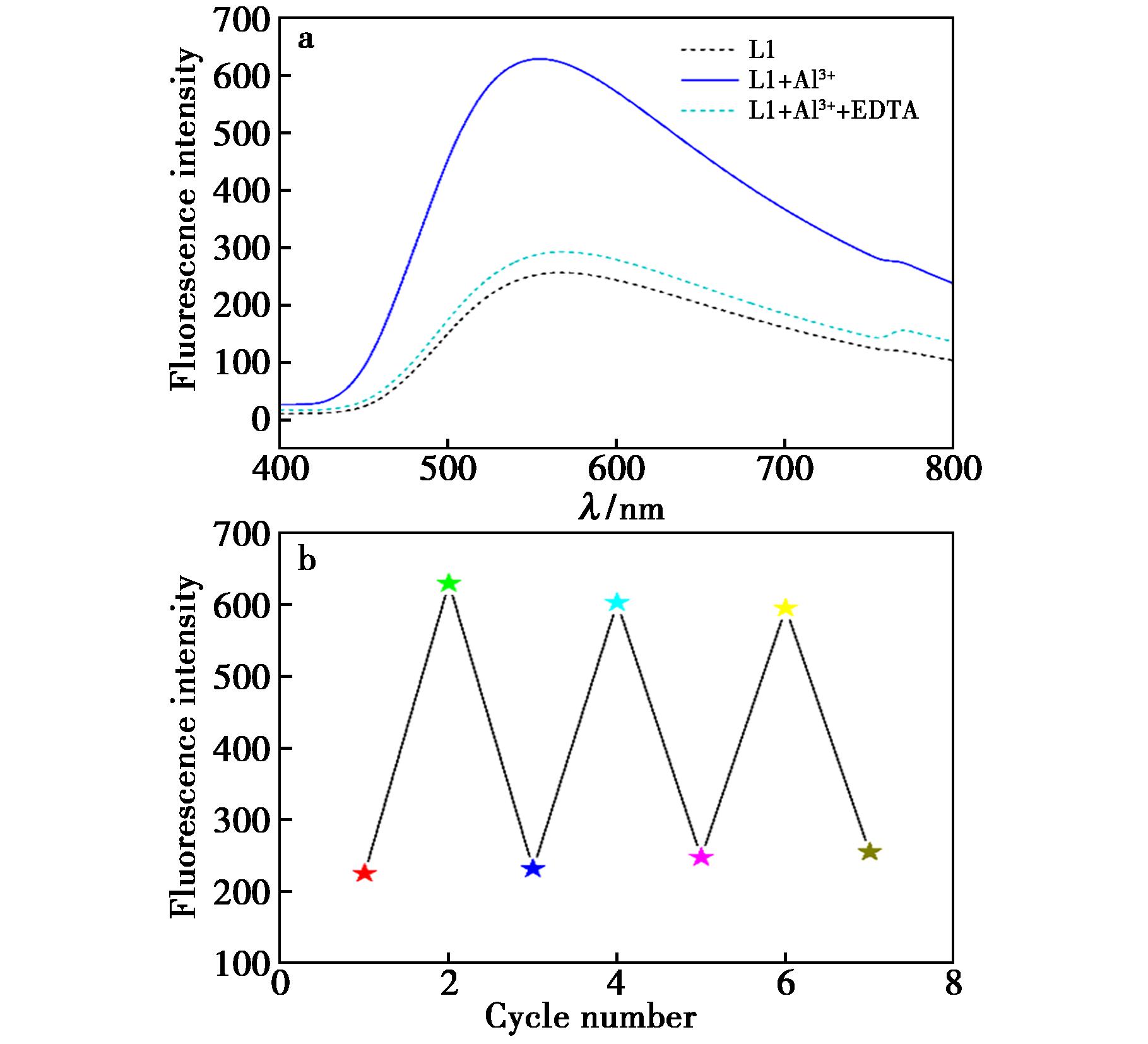
图8 a.探针L1、L1+Al3+和L1+Al3++EDTA的荧光发射强度;b.在EDTA存在的情况下,L1+Al3+在558 nm处荧光发射循环3次,激发波长为380 nm的荧光强度
Fig.8 a.Fluorescence emission spectroscopy of probe L1,L1+Al3+and L1+Al3++EDTA;b.Fluorescence intensity of L1+Al3+ in the presence of EDTA for three cycles at 558 nm,excitation at 380 nm
为了检测探针L1在生物实验中的应用,通过HeLa细胞研究了探针L1在细胞内检测Al3+荧光成像性能,如图9所示。HeLa细胞37 ℃下用 20 μmol/L探针L1孵育30 min,通过荧光显微成像技术发现探针本身表现出微弱的荧光。当HeLa细胞用20 μmol/L探针L1孵育30 min,然后用50 μmol/L Al3+孵育30 min。发现细胞呈现出明亮的蓝色荧光,其激发波长为405 nm。该研究结果说明,探针L1具有良好的细胞穿透性,其容易进入细胞核内,可以用于细胞内Al3+的分析检测。
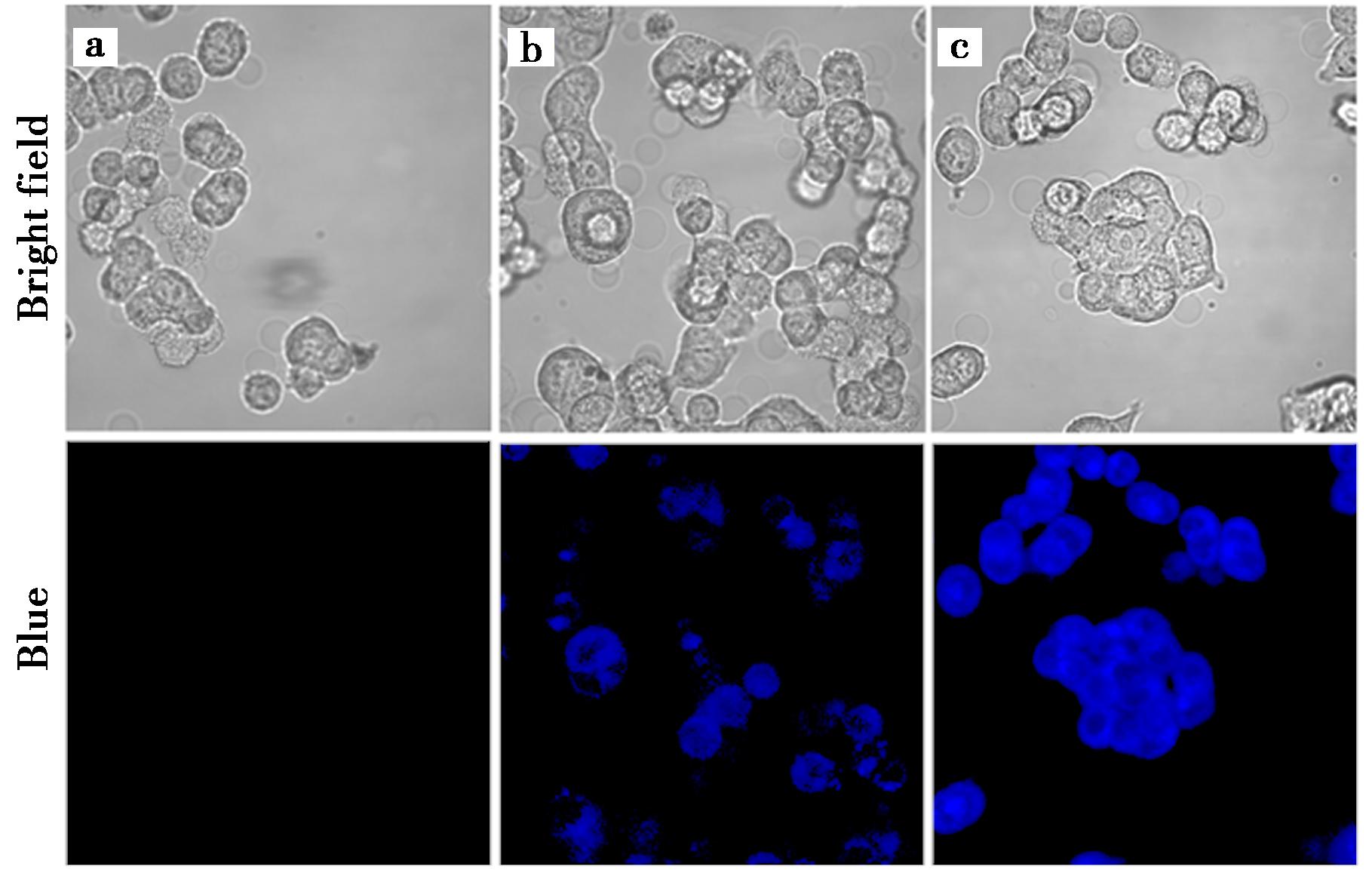
a.没有加探针;b.L1孵育;c.Al3++L1孵育
图9 HeLa细胞荧光成像图
Fig.9 Fluorescence confocal imaging of HeLa cells
该研究工作合成了两种基于萘碳酰腙的荧光探针L1和L2,用于选择性地Al3+检测。研究发现,荧光探针L1对Al3+在V(乙醇)∶V(HEPES buffer)=3∶7(pH 7.4)溶液具有高选择性和高灵敏性,表现出荧光增强和蓝色荧光,其检测限低至47.3 nmol/L。研究证实末端CH3O-取代的结构比CH3CH2O-取代的结构具有更高选择性。通过滴加Al3+和EDTA,荧光信号出现“ON-OFF-ON”模式循环3次,实现探针的重复应用。探针L1在Hela细胞具有良好的细胞通透性,可以用于细胞中Al3+的成像检测。该研究工作为设计萘碳酰腙类高选择性Al3+荧光探针提供了一种新模版。
[1]Tavakoli O,Yoshida H.Environ.Sci.Technol.,2005,39(7):2357-2363.
[2]Alstad N E W,Kjelsberg B M,Vøllestad L A,Lydersen E,Poléo A B S.Environ.Pollut.,2005,133(2):333-342.
[3]Fuge R,Perkins W.Environ.Geochem.Health,1991,13(2):56-65.
[4]Cannon J R,Greenamyre J T.Toxicol.Sci.,2011,124(2):225-250.
[5]Barceló J,Poschenrieder C.Environ.Exp.Bot.,2002,48(1):75-92.
[6]Chan J,Dodani S C,Chang C J.Nat.Chem.,2012,4(12):973-984.
[7]Guo Z Q,Park S,Yoon J,Shin I.Chem.Soc.Rev.,2014,43(1):16-29.
[8]Liu X G,Qiao Q L,Tian W M,Liu W J,Chen J,Lang M J,Xu Z C.J.Am.Chem.Soc.,2016,138(22):6960-6963.
[9]Kim H R,Kumar R,Kim W,Lee J H,Suh M,Sharma A,Kim C H,Kang C,Seung Kim J.Chem.Commun.,2016,52(44):7134-7137.
[10]Qiao Y S,Yuan Y Y,Dong Y L,Huang C F,Wang H Y.Chin.J.Anal.Lab.,2023,42(8):1056-1060.乔亚森,袁莹莹,董亚蕾,黄传峰,王海燕.分析试验室,2023,42(8):1056-1060.
[11]Jin X L,Wu S P,She M Y,Jia Y F,Hao L K,Yin B,Wang L Y,Obst M,Shen Y H,Zhang Y M,Li J L.Anal.Chem.,2016,88(22):11253-11260.
[12]Zhang J D,Yang Y,Xue K X,Ding M J,Xia Z R.Chem.Reagents,2024,46(10):35-43.张继东,杨垚,薛凯茜,丁美娟,夏曾润.化学试剂,2024,46(10):35-43.
[13]Diao Q P,Ma P Y,Lv L L,Li T C,Sun Y,Wang X H,Song D Q.Sens.Actuat.B Chem.,2016,229:138-144.
[14]Kumar A,Chae P S.Anal.Chim.Acta,2017,958:38-50.
[15]Al-saeedi A,Aydin D,Alici O.Spectrochim.Acta Part A Mol.Biomol.Spectrosc.,2023,294:122532.
[16]Ou Z Q,Wang M X,Zhang Z Y,Liang J Q,Tang J W,Lei X L,Yang L T,Liu H,Ma L J.Microchem.J.,2023,195:109386.
[17]Zhao L X,He X L,Xie K B,Hu J J,Deng M Y,Zou Y L,Gao S,Fu Y,Ye F.Spectrochim.Acta Part A Mol.Biomol.Spectrosc.,2023,285:121882.
[18]Gao C Y,Shao Y X,Bao X Y,Li P,Yang Y.Chem.Reagents,2025,47(12):77-82.高超颖,邵雨昕,包晓英,李鹏,杨杨.化学试剂,2025,47(12):77-82.
[19]Zhang J D,Yang Y,Zhang J,She W.Chin.J.Org.Chem.,2024,44(4):1337-1342.张继东,杨垚,张杰,厍伟.有机化学,2024,44(4):1337-1342.
[20]Jiang X J,Zhu R G,Wang S F,Chen Y Y,Fu D Y,Lin L.Chem.Reagents,2017,39(6):643-646.姜秀娟,朱荣贵,王寿峰,陈依依,付大友,林莉.化学试剂,2017,39(6):643-646.
[21]Liao Y H,Wang S,Feng H J,Chen G Y,Song Y,Wu L Y,He W Y.Chin.J.Anal.Lab.,2024,43(5):660-668.廖元淏,王帅,冯华杰,陈光英,宋媛,吴禄勇,何文英.分析试验室,2024,43(5):660-668.
[22]Smith C.Notes Rec.R.Soc.Lond.,1992,46(2):317-323.
[23]Ang W,Chen G,Xiong L,Chang Y,Pi W Y,Liu Y Y,Li C L,Zheng J J,Zhou L X,Yang B,Deng Y,Yang S Y,Luo Y F,Wei Y Q.Eur.J.Med.Chem.,2014,82:263-273.
[24]Chen Y H,Wei T W,Zhang Z J,Chen T T,Li J,Qiang J,Lv J,Wang F,Chen X Q.Ind.Eng.Chem.Res.,2017,56(43):12267-12275.
[25]Hu D D,Bu Y C,Liu M X,Bai F Q,Li J J,Li L C,Cai H M,Gan X P.Anal.Methods,2024,16(45):7781-7788.
[26]Li Y P,Zhu X H,Li S N,Jiang Y C,Hu M C,Zhai Q G.ACS Appl.Mater.Interfaces,2019,11(12):11338-11348.
[27]Velmurugan K,Prabhu J,Raman A,Duraipandy N,Kiran M S,Easwaramoorthi S,Tang L J,Nandhakumar R.ACS Sustainable Chem.Eng.,2018,6(12):16532-16543.
[28]Roy K,Biswas S,Basu D,Das P K.Anal.Chem.,2025,97(32):17650-17658.
[29]Antony E,Ganesan N,Srinivasan K,Paul S P M,Abiram A,Parvatham K,Kannan V R,Nandhakumar R.New J.Chem.,2025,49(34):14787-14800.