共价有机笼(COCs)是一类由有机小分子通过共价键连接而成的离散型三维笼状结构,其特征在于内部具有精确定义的空腔以及可调控的分子通道[1-3]。随着动态共价化学(DCC)理论的完善及高效成键策略的发展,COCs的构筑方法不断成熟,使其在过去十余年中迅速发展为功能有机材料研究的重要前沿方向[4,5]。相较于传统多孔材料,如金属有机框架(MOFs)、共价有机框架(COFs)以及依赖非共价相互作用构筑的超分子笼,COCs兼具结构规整性与分子离散性,展现出一系列独特优势:其空腔尺寸与拓扑结构可通过构筑单元的几何特征实现精确调控;共价骨架赋予其较高的化学稳定性;同时,笼体整体可在分子层面进行功能化修饰,并通常具备良好的溶液可加工性[2,4,6]。这些特性使COCs成为研究分子识别、客体包合、分离纯化及催化等领域的重要平台[7-11]。
在药学相关研究中,COCs展现出区别于传统多孔材料的独特应用潜力。通过合理设计,COCs的空腔尺寸及孔口化学环境可实现“结构契合”的主-客体识别模式,从而有利于对特定药物分子的高选择性包载[1,2]。此外,COCs通常具有较好的溶解性与分散性,使其在生物体系中更易于加工与递送[12-14]。与此同时,笼体表面可引入多样化官能团,为其进一步的生物修饰提供了高度可控的化学基础,有助于提升其生物相容性、靶向能力或刺激响应特性[15-17]。基于上述优势,COCs已逐步发展为集药物递送、生物成像和生物传感于一体的多功能平台材料[2,13,18,19]。
鉴于COCs在医药相关领域的快速发展,有必要对其药学应用潜能进行系统梳理与总结。本综述旨在概述近年来COCs在药物递送、生物成像及生物传感等方面的代表性研究进展,重点探讨其结构特征如何驱动不同应用场景下的功能表现,并进一步分析其在实际生物体系中面临的关键挑战,包括生物稳定性、体内药代动力学行为以及规模化制备等问题。最后,对COCs在药学与生物医学领域的未来发展方向进行展望。
1 共价有机笼的结构设计与合成
1.1 合成策略
共价有机笼的构筑依赖于可控的成键方式与组装路径,而动态共价化学无疑是当前最核心的策略。DCC通过可逆共价键的不断断裂与重组实现“错误修复”,使构筑单元在溶液中自发趋向热力学最稳定、几何构型最合理的笼状结构[20]。在众多可逆成键模式中,亚胺缩合因条件温和、反应速度快和结构多样性高而最为广泛使用[21-24];硼酸酯键则依赖硼酸与二醇之间的快速、可控可逆反应,从而在脱水条件下实现高刚性的笼体结构[25,26];而二硫键、缩醛等半可逆键则在保持一定可逆性的同时提高了笼体在极性溶剂或生物条件下的稳定性[27-29]。除可逆键外,不可逆键形成(如Sonogashira偶联、Suzuki偶联、Yamamoto偶联)也逐渐用于笼体的最终“锁定”,即在预组装后用牢固键固定构型,以获得在体内条件下具有更高化学稳定性的药用笼体[30-33]。
除了经典的可逆自组装之外,模板辅助策略在近年来受到越来越多关注[34,35]。利用金属离子、阴离子或客体分子等作为空间模板,可有效预组织构筑单元的取向,从而提高笼体形成的立体选择性与产率[36-38]。模板不仅能帮助解决因构型竞争而导致的产物分布复杂的问题,还能诱导形成热力学路径难以直接获得的拓扑结构[39,40]。Yusaf等[41]通过动态共价化学的组分混排策略结合还原反应,合成了外围带有明确数量炔基单元的胺基有机笼,并利用铜催化的叠氮-炔烃环加成(CuAAC)活性金属模板(AMT)法,成功构建了[2]-、[3]-、[4]-有机笼轮烷(图1)。该研究首次实现了机械互锁单元在有机笼上的精准引入,为多孔有机共价笼的后合成功能化提供了新颖高效的策略。
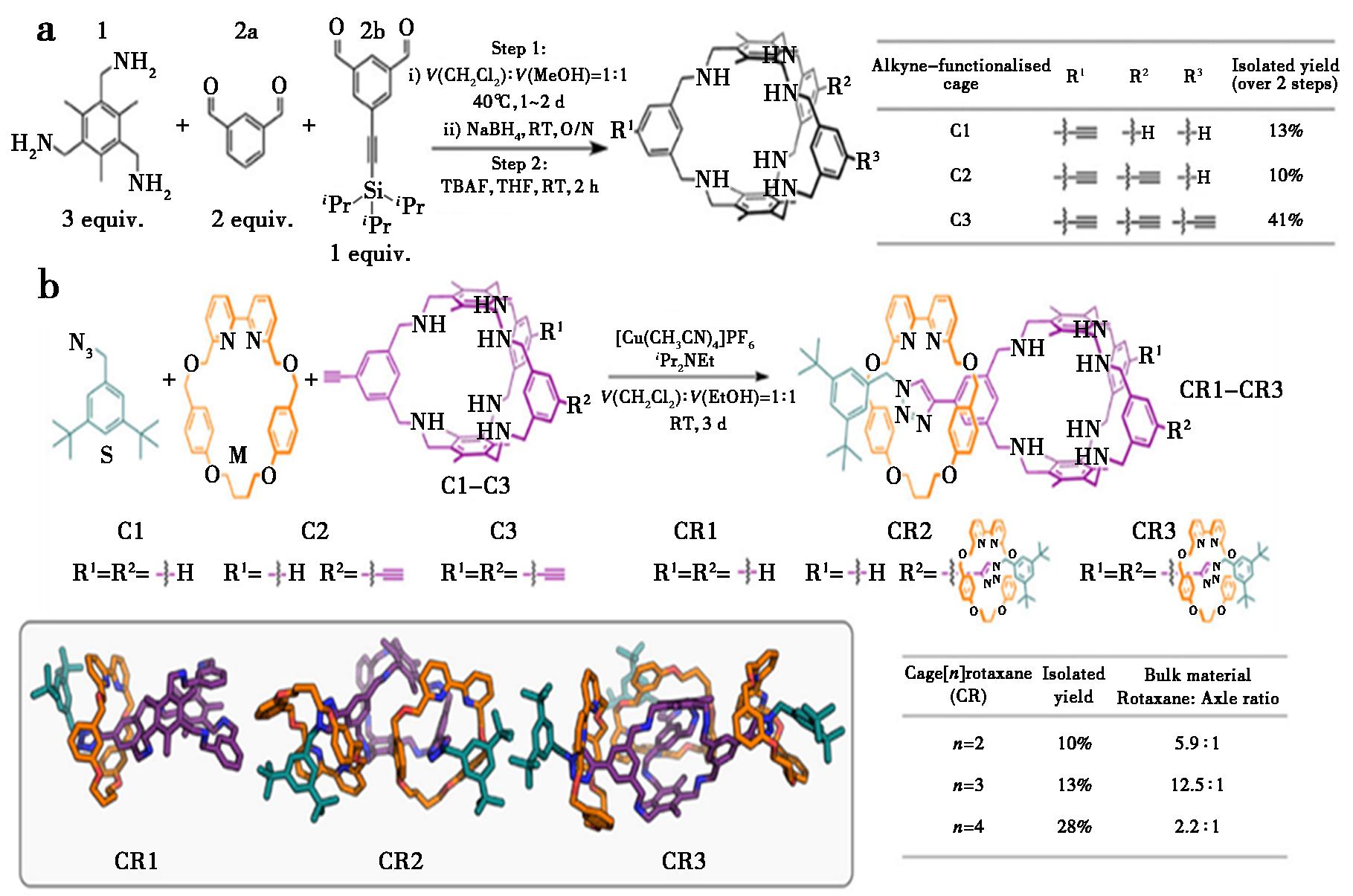
a.合成炔基功能化共价有机笼C1~C3;b.采用CuAAC-AMT方法合成笼[n]轮烷(CR1~CR3)
图1 AMT法精准引入笼上机械互锁单元[41]
Fig.1 Precise introduction of mechanically interlocked units onto organic cages via the active metal template (AMT) approach[41]
此外,动力学控制策略也为构筑非经典笼体提供了可能。通过调节稀释度、反应速率、溶剂极性或催化剂浓度,可在一定条件下偏向动力学产物,从而获得结构独特的笼体[5,24,42-44]。动力学与热力学的协同调控,使COCs的结构空间进一步扩展,为药物递送、成像和生物传感等应用提供了多样化的结构基础[45]。
随着合成策略在实验室层面的成熟,COCs的规模化制备成为其走向实际应用的关键环节。目前,COCs的合成多依赖动态共价自组装(如亚胺缩合)实现“纠错—成笼”过程,实验室合成往往需要较高稀释度以抑制寡聚/聚合副反应[46];放大时混合与传质/传热不均易造成局部浓度升高,从而带来副产物增加、产率下降与批间重现性变差[47]。此外,多组分反应可能产生结构相近的副产物或动态组分交换混合物,使纯化过程对制备色谱或反复结晶依赖度较高,溶剂消耗与成本压力在放大时更为突出[46,48]。对于具有固态孔隙的笼体材料,晶型与分子堆积还会影响孔结构与性能一致性,进一步增加了工程化制备与质量控制难度[49,50]。
针对上述放大瓶颈,研究者已开始发展具有工程放大潜力的工艺路线。其一,连续流合成将部分亚胺笼的构筑由批式转移至流动体系,在更稳定的传热传质条件下提升过程可控性与可重复性[46];其二,机械化学连续化(如双螺杆挤出,TSE)已用于经典多孔有机笼CC3的连续制备,显著降低溶剂用量并提升时空产率,为规模化提供了示范[51];其三,面向晶体多孔材料的过程强化(如高压均质化,HPH等)也体现出通过“成核—晶化”工程化调控来实现大规模制备与结构一致性控制的潜力[50,52]。综合来看,规模化制备仍需在“高浓度成笼效率—分离纯化—晶型/孔结构一致性—质量标准”全链条层面持续优化,并推动合成策略从实验室方法论向可放大的工艺工程融合,以真正释放COCs在生物医学等领域的应用潜力。
1.2 结构与性质调控
COCs的结构特征具有高度可调性,可针对特定药物或生物体系进行精准设计。通过调整构筑单元的几何特性、键连角度与骨架刚性,可实现笼体空腔尺寸与孔口直径的精确控制[53,54]。空腔大小和孔径分布直接决定了笼体对药物分子的包载能力、选择性以及扩散行为,是COCs用于药物递送和分子识别的核心结构参数[53]。同时,笼体内外的官能化位点可通过单体设计或后合成修饰进行调控,从而调节其亲疏水性、分子识别环境和生物相容性[55]。此外,笼体的整体溶解性与分散性可以通过修饰亲水基团、改变骨架柔性或引入离子性侧链来调控,这对其在水相、生理条件和细胞环境中的应用尤为重要[15,56,57]。
值得强调的是,COCs作为离散分子,不同于传统MOFs或COFs的晶态固体框架,其在溶液中的自组装特性赋予其独特优势[48]。许多COCs在溶液中可以单分子、可逆聚集体或超分子组装体形式存在,这些行为为药物包载、释放及生物介导的刺激响应提供了更多可能[3]。例如,某些笼体在水溶液中可通过疏水效应形成胶束状纳米结构,从而提高疏水药物的溶解度[13];另一些则能保持离散实体特性,通过精准的主-客体作用选择性捕获药物分子[12,15,57]。理解并调控其溶液行为,是推动COCs走向药物化学应用的重要前提[10]。
1.3 生物相关修饰策略
为使COCs适应生物体系并实现靶向递送或特定响应,对其进行生物功能化修饰是关键步骤。PEG化是最常见的策略之一,引入聚乙二醇链段可显著提高COCs的水溶性、血液循环时间及免疫逃逸能力[17,58,59]。对于需要主动靶向的应用,可在笼体表面修饰叶酸、RGD肽、小分子配体或抗体片段,以实现与肿瘤细胞或特定生物标志物的高亲和力结合[60-62]。
此外,引入pH、ROS、光敏基团或酶切肽序列等响应性官能团,能使笼体在特定生物环境中触发药物释放或结构变化。例如,pH响应笼体可在肿瘤微环境中快速解离并释放药物[13,63,64];含氧化还原敏感键的笼体能在细胞内高谷胱甘肽浓度下解笼[65];而光敏组分则可在光照条件下激活成像或治疗功能[66,67]。通过这些功能化修饰,COCs不仅具备良好的生物相容性和稳定性,还能进一步集成药物递送、生物成像及高灵敏度生物传感等多功能于一体[15]。
总体而言,结构调控、合成策略与生物修饰的协同设计,使COCs成为具有高度可编程性和应用潜力的分子平台。
2 用于药物递送的共价有机笼
COCs凭借其离散分子结构、精确定义的空腔、优异的溶液加工性及可定制的化学环境,已成为药物递送领域中新兴且极具潜力的载体体系[3,68]。与传统纳米材料不同,COCs的笼状构型使其能在分子尺度上实现药物的精准包载与释放调控,并通过骨架设计与表面修饰在生物体系中维持稳定、可控的行为[64,69]。本文将从包载机制、刺激响应、典型应用及生物安全性等方面总结最新进展,并探讨当前的关键挑战与发展趋势。
2.1 药物包载机制
COCs的药物包载行为主要依赖其空腔内部的化学环境、孔口尺寸以及表面官能团的相互作用方式[68,70]。作为离散笼状结构,COCs的内部空腔通常具备特定的刚性构象和电子性质,因此可以通过分子识别实现对药物分子的选择性包载[10]。
在常见的作用模式中,π-π堆积是包载芳香性药物(如蒽环类抗癌药DOX)的主要驱动力[71]。COCs的芳香骨架能够提供稳定的π面,使药物结构获得热力学上的结合优势;与此同时,笼体内部的氢键位点可进一步增强结合稳定性,尤其适用于含羟基、酰胺或酚羟基的药物。对带电药物而言,静电作用与库伦吸引可以显著提高结合效率,例如带正电的蛋白酶抑制剂或抗癌药可与阴离子功能化笼体形成稳固配位[70]。
得益于精确构筑的空腔尺寸,COCs在主-客体识别中展现出优于传统纳米材料的选择性[72]。例如,一些尺寸敏感笼体能够区分结构相似的药物分子,实现“尺寸筛选”式的选择性装载[73]。该特性不仅增强了包载效率,也使COCs在多重药物体系中具备潜在的可控释放与协同递送能力。
2.2 控释与刺激响应释放系统
COCs的另一个重要优势是可以通过结构设计实现精确的药物释放调控。由于笼体结构可通过动态键、响应性基团或后修饰实现可控开合,其药物释放方式通常包括环境敏感型、自溶解型和结构重构型[14,55,64,74,75]。
在刺激响应策略中,pH触发的释放机制应用最为广泛。带有亚胺或硼酸酯键的COCs在弱酸性条件下可发生部分裂解,从而在癌症微环境或溶酶体内部实现加速药物释放[13,64]。对于含有氧化还原敏感基团(如二硫键)的笼体,高谷胱甘肽(GSH)浓度可诱导其结构解离,实现细胞内选择性释放[76]。另一方面,酶敏感性策略也受到关注,通过引入酯键、肽序列或可切割连接臂,可使笼体在癌细胞中过表达的酶(如MMPs、cathepsin B)作用下实现“开笼”式释放[77,78]。
此外,光敏和ROS(活性氧)响应型COCs近年来受到关注,特别是在联合光动力治疗与药物治疗的体系中[60]。光敏单元可以通过可控激发实现药物的空间-时间精准释放,而ROS响应结构则适用于炎症微环境和肿瘤组织[60]。总体而言,这些刺激响应模式赋予COCs以高度可控和智能化的药物释放能力,显著提升其在精准治疗中的应用前景[79,80]。
2.3 实例与性能比较
近年来,多种COCs已成功用于小分子药物与抗癌药物的包载与递送研究。蒽环类药物DOX是最常用的模型药物之一,其平面芳环结构与笼体内部的π面高度匹配,通常可获得高包载效率(常见可达20~40 wt%)[81]。例如,某些亚胺型笼体在水溶条件下可自发吸附DOX,并在酸性条件下快速释放,表现出优于自由药物的细胞摄取与杀伤效应。Badji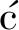 等[82]首次报道了在生理pH水溶液中稳定存在的大型共价有机笼,该研究通过后合成修饰制备了水溶性共价篮状笼CBC-11(图2a),其在生理pH水溶液中可自组装为250 nm结晶纳米颗粒。CBC-11以非协同方式结合多达4个伊立替康或多柔比星(DOX)抗肿瘤药物分子(对应图2b、2c所示的[124⊂CBC-11]和[134⊂CBC-11]),形成稳定复合物,且对HCT 116细胞的IC50>100 μmol/L,生物相容性良好,为抗癌药物封存与递送提供了新型纳米载体。
等[82]首次报道了在生理pH水溶液中稳定存在的大型共价有机笼,该研究通过后合成修饰制备了水溶性共价篮状笼CBC-11(图2a),其在生理pH水溶液中可自组装为250 nm结晶纳米颗粒。CBC-11以非协同方式结合多达4个伊立替康或多柔比星(DOX)抗肿瘤药物分子(对应图2b、2c所示的[124⊂CBC-11]和[134⊂CBC-11]),形成稳定复合物,且对HCT 116细胞的IC50>100 μmol/L,生物相容性良好,为抗癌药物封存与递送提供了新型纳米载体。
a.共价篮状笼(Covalent basket cages,CBC)的合成示意图;方框内为含硫醚侧链模型化合物最稳定构象的能量最小化结构;b.能量最小化的[124⊂CBC-11]复合物的范德华表面示意图(OPLS4);c.能量最小化的[134⊂CBC-11]复合物的范德华表面示意图(OPLS4)
图2 CBC的合成路线和124⊂CBC-11、134⊂CBC-11的示意图[82]
Fig.2 Synthetic route of covalent CBC and representation of 124⊂CBC-11,134⊂CBC-11[82]
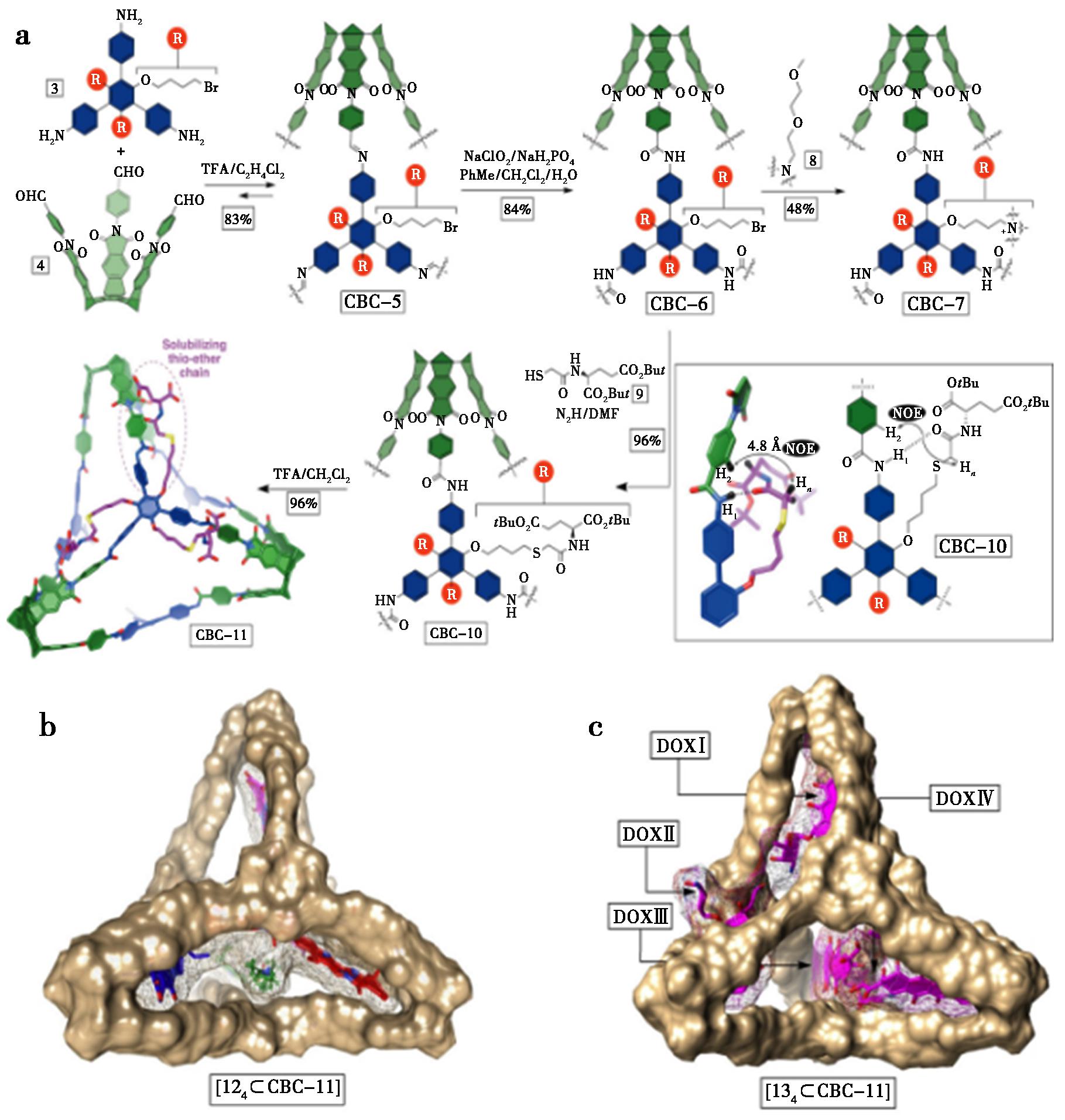
紫杉醇(PTX)等强疏水性药物也可通过疏水驱动与笼体内部的非极性环境实现高效包载,从而显著改善其水溶性和生物利用度。Yuan等[13]首次将多孔有机共价笼用作紫杉醇(PTX)的纳米载体,如图3所示,通过接枝RH40表面活性剂合成了PTX@POC@RH40纳米胶囊。该胶囊包封率超98%、稳定性优异,兼具pH响应性与缓释特性,可提升药物生物利用度和肿瘤靶向性,在4T1乳腺癌模型中展现出更强的抗肿瘤效果且毒性更低,为精准肿瘤治疗提供了新型刺激响应型纳米递送平台。
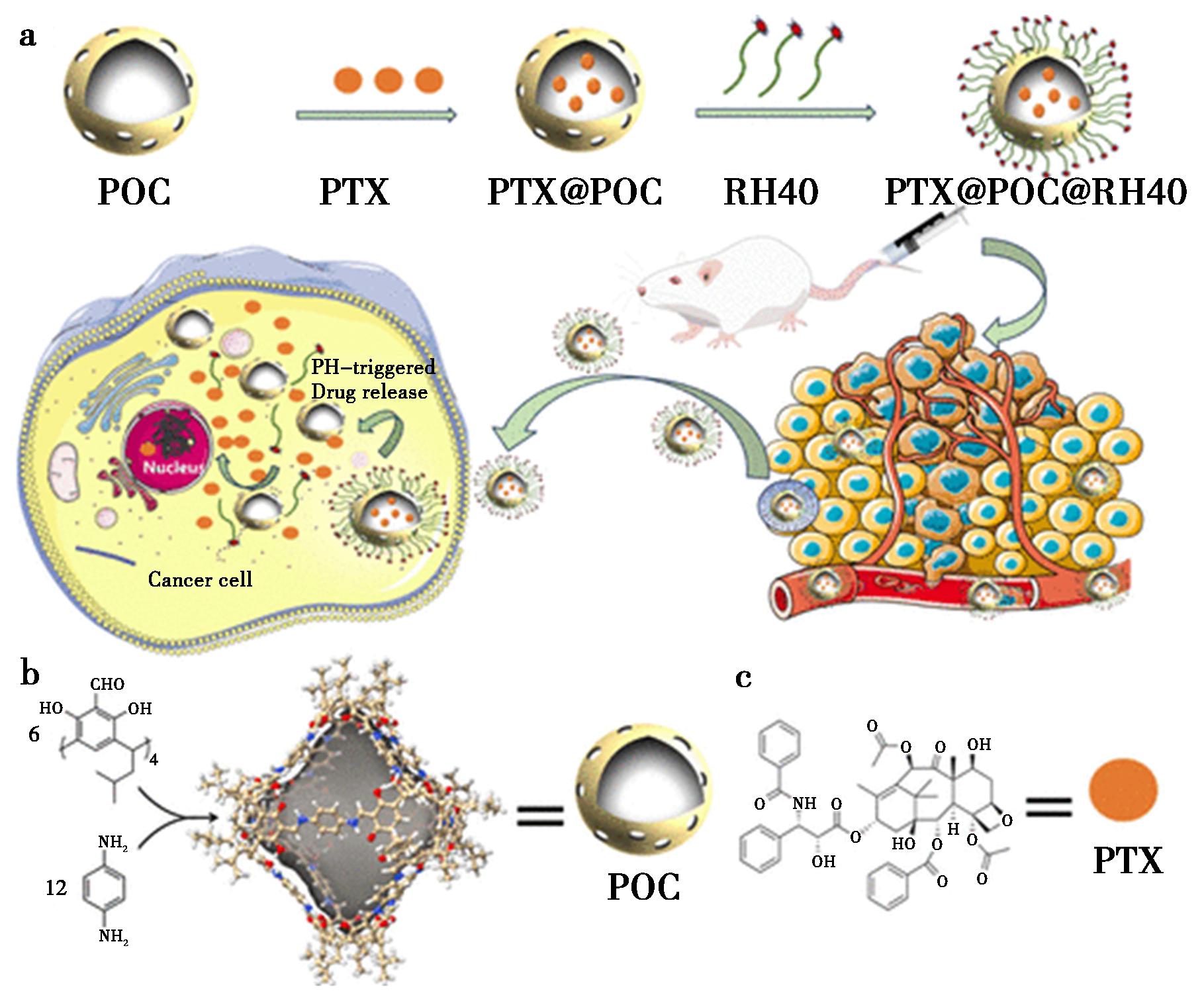
a.多孔有机笼作为pH响应型抗癌药物载体用于肿瘤精准治疗的示意图;b.[6+12]型杯[4]间苯二酚芳烃基多孔有机笼的设计与合成;c.紫杉醇的化学结构
图3 多孔有机笼(POC)作为pH响应型抗肿瘤药物递送体系用于精准肿瘤治疗的示意图[13]
Fig.3 Schematic diagram of POC as pH-responsive anticancer drug deliver for precise tumor therapy[13]
Liu等[70]通过还原质子化修饰CC3笼,构建了Pt-in-(HR)CC3封装体系,利用物理限域作用使Pt纳米簇(~1.7 nm)均匀分散,规避了传统化学保护的活性位点遮挡问题,显著提升水溶性与生物相容性(图4)。该体系在放疗中表现出优异增敏效果,体外联合4 Gy放疗时癌细胞凋亡率达31%,体内可显著抑制肿瘤生长且低毒无器官损伤。其机制通过促进活性氧生成、抑制癌细胞迁移及诱导凋亡实现协同抗肿瘤。该研究验证了共价笼在放疗增敏药物递送中的核心价值,为生物医学与材料化学交叉提供新范式,且封装策略可拓展至多元客体分子。
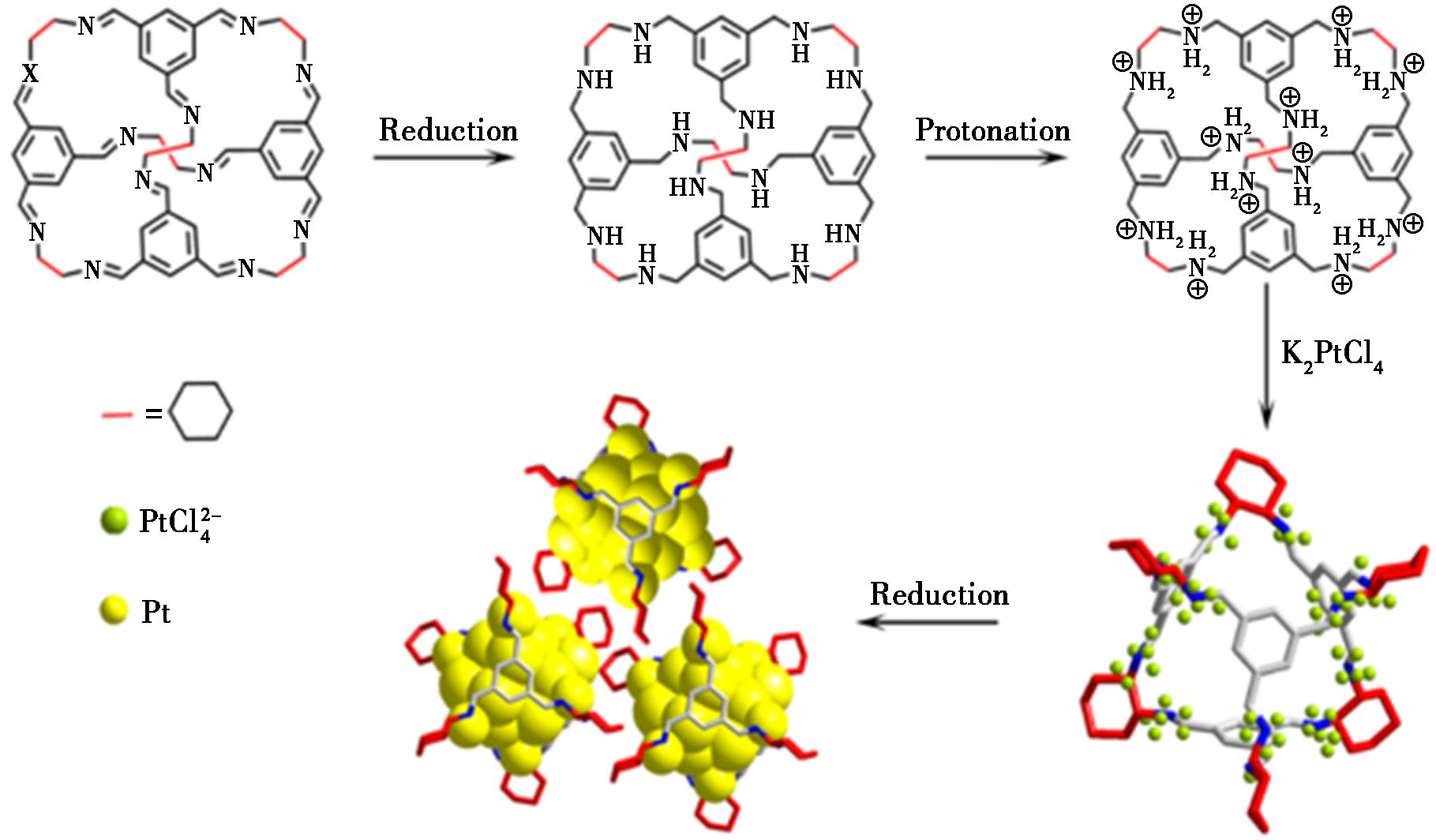
图4 Pt-in-(HR)CC3的合成路线示意图[70]
Fig.4 Synthetic scheme of Pt-in-(HR)CC3[70]
但COCs的缺点也值得注意,例如空腔体积有限,可能限制大分子药物的装载[54];部分笼体在强水相条件下稳定性不足;规模化合成成本较高[51,57]。这些因素提醒研究者在未来需要进一步优化合成、提高稳定性并开发更大尺寸或柔性笼体。Li等[83]通过席夫碱反应,以棱柱状三胺分子共价笼为C3对称节点、对苯二甲醛为C2连接体,合成了新型笼基共价有机框架材料Cage-COF-TT。该材料呈棕色粉末状,具有高结晶度、大比表面积(672 m2/g)和良好热稳定性(高达400 ℃),且在0~500 μg/mL浓度范围内对正常小鼠细胞(L929)和人肝细胞(L-02)无明显细胞毒性。作为药物载体,其对布洛芬(IBU)、5-氟尿嘧啶(FLU)和卡托普利(CAP)的负载量分别达0.22、0.25和0.30 g/g,在模拟体液中52 h内药物释放率均超93%,缓释性能优于传统COF和MOF材料,为生物医学领域药物递送系统的开发提供了新方案,如图5所示。
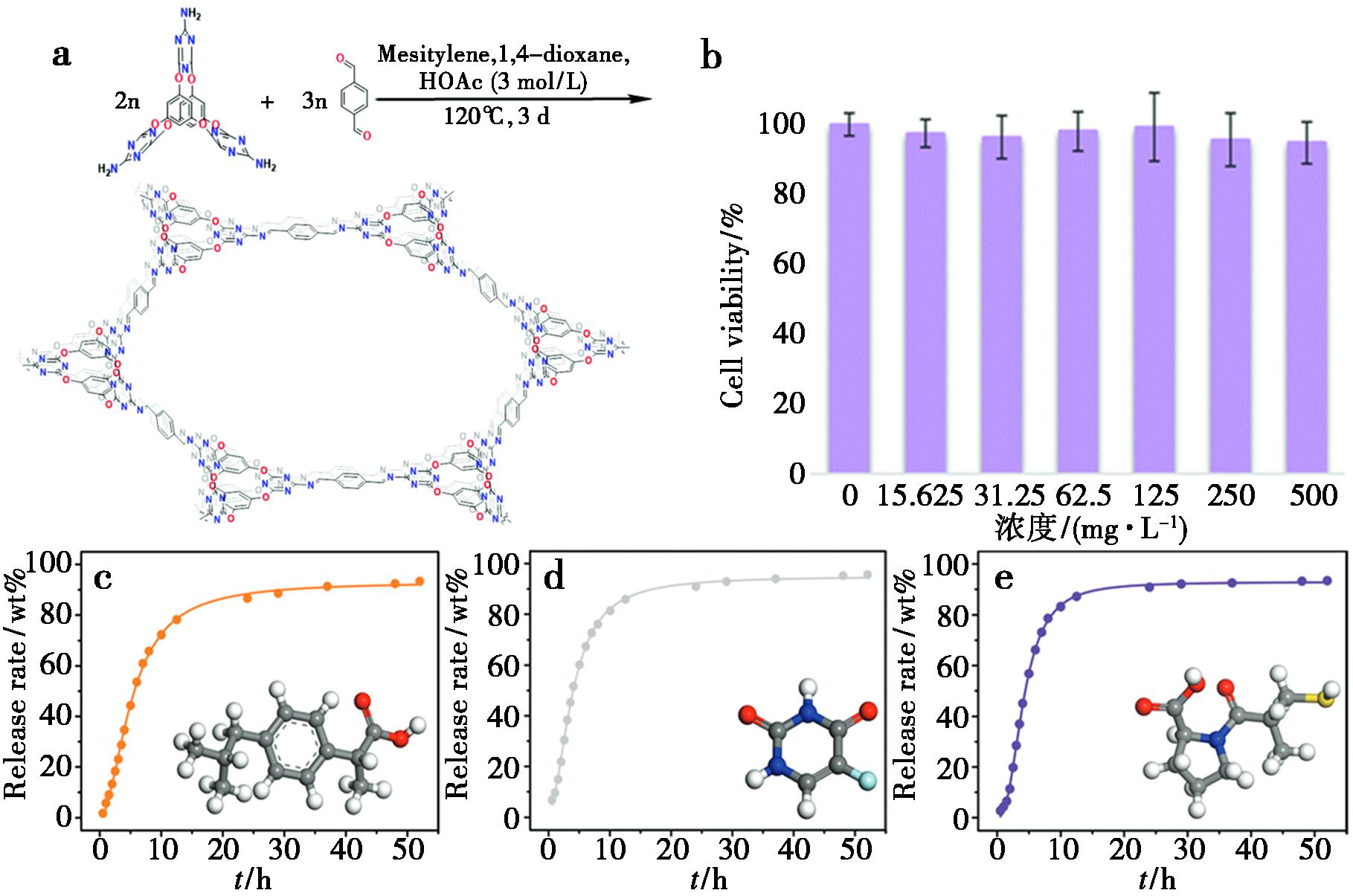
a.笼基共价有机框架材料Cage-COF-TT的合成路线示意图;b.采用MTT法检测Cage-COF-TT在不同浓度(自左至右分别为0、15.625、31.25、62.5、125、250和500 μg/mL)下对人正常肝细胞L-02的细胞存活率;c.负载布洛芬(IBU)的Cage-COF-TT的药物释放曲线,插图为IBU的化学结构式;d.负载5-氟尿嘧啶(FLU)的Cage-COF-TT的药物释放曲线,插图为FLU的化学结构式;e.卡托普利(CAP)的标准曲线;插图为CAP的化学结构式
图5 Cage-COF-TT的合成及细胞毒性和药物包载实验结果[83]
Fig.5 Synthesis,cytotoxicity and drug loading experimental results of Cage-COF-TT[83]
为更直观地比较上述代表性COCs药物递送体系的关键性能,将其主要参数归纳于表1。
表1 代表性COCs在药物递送中的性能对比
Tab.1 Performance comparison of representative COCs in drug delivery
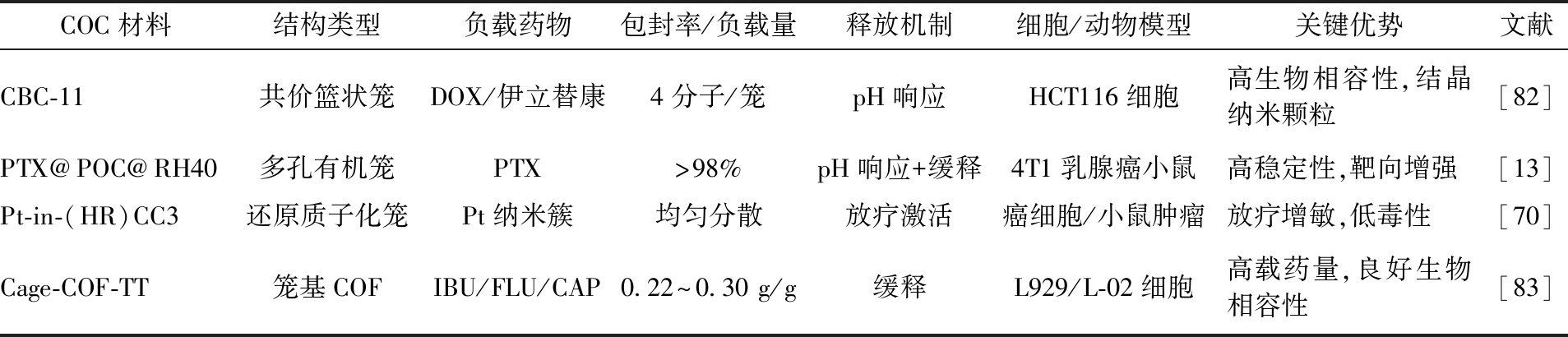
COC材料结构类型负载药物包封率/负载量释放机制细胞/动物模型关键优势文献CBC-11共价篮状笼DOX/伊立替康4分子/笼pH响应HCT116细胞高生物相容性,结晶纳米颗粒[82]PTX@POC@RH40多孔有机笼PTX>98%pH响应+缓释4T1乳腺癌小鼠高稳定性,靶向增强[13]Pt-in-(HR)CC3还原质子化笼Pt纳米簇均匀分散放疗激活癌细胞/小鼠肿瘤放疗增敏,低毒性[70]Cage-COF-TT笼基COFIBU/FLU/CAP0.22~0.30 g/g缓释L929/L-02细胞高载药量,良好生物相容性[83]
2.4 生物安全性与代谢研究进展
在药物递送体系中,载体的生物安全性是决定其临床转化潜力的关键因素。目前已有多项研究表明,COCs在细胞与小动物模型中整体表现出良好的生物相容性[2,4,13]。由亚胺键或酰胺键构筑的有机笼通常呈现较低的细胞毒性,其表面进一步引入聚乙二醇(PEG)或带电基团后,可有效降低非特异性蛋白吸附与免疫系统识别,从而改善其体内稳定性与循环行为[2,6]。血液相容性研究亦显示,经过合理表面修饰的COCs在血清环境中能够保持结构稳定,并表现出较低的溶血率与凝血影响,提示其在静脉给药场景中的潜在应用价值[13,59]。
在体内代谢与清除方面,COCs的生物行为通常与其尺寸、疏水性及表面官能团密切相关。已有研究指出,尺寸较小且亲水性较好的有机笼结构更倾向于经肾脏途径实现快速清除,而粒径较大或疏水性增强的笼体则更易被肝脏代谢系统或网状内皮系统(Reticuloendothelial system,RES)摄取[13,82,84]。此外,含有动态共价键(如亚胺键)的笼体在体内环境中可能发生部分断裂,从而以小分子或低聚体形式排出;相比之下,不可逆共价笼结构则更依赖于代谢酶介导的降解过程或缓慢的体内清除途径[4,6]。然而,目前针对COCs的系统性药代动力学行为、长期体内分布以及慢性毒性评价仍较为有限,这在一定程度上制约了其进一步向临床应用转化[60,84]。
深入理解COCs的体内命运需从其多层级结构特征入手,“键型稳定性-尺度形态-表面化学”共同决定了其代谢与清除路径。首先,键型稳定性是代谢行为的化学基础,依赖动态可逆键(如亚胺)的笼体,在水相或生理环境中可能发生键交换或断裂,降解为小分子或低聚体,从而改变清除方式[85];相比之下,通过“锁定”策略构筑的稳定笼体(如将亚胺还原为酰胺,或使用肼腙键等),则因更高的水相稳定性,更可能以完整或缓慢降解的形式经历体内转运[57,86]。其次,尺度与组装形态主导其生物分布,离散笼体与其纳米组装体的命运迥异[70]。例如,PEG化卟啉纳米笼(porSMNPs,图10)具有约11.3 h的较长血液循环时间,体现了“表面修饰+纳米尺度”对药代行为的精准调控[59];而以表面活性剂实现纳米化的体系(如PTX@POC@RH40),则能显著提高药物体内暴露,改变分布与清除动力学[13]。最后,在表面化学与粒径的层面,亲水性提升、PEG化与电中性化通常可降低蛋白吸附并延长循环时间;而过大的水动力学尺寸易被单核吞噬系统(MPS/RES)捕获,以肝胆途径清除,若将尺寸控制在肾小球滤过阈值附近,则有望实现快速肾清除[87]。
总体而言,目前针对不同结构COCs的系统药代与长期归趋数据仍较匮乏。未来有必要在统一实验框架下,开展对比性的体内分布、代谢产物鉴定与排泄通路研究,从而建立可预测的“化学结构-物理形态-表面性质-体内命运”构效关系,为设计安全、高效、可控的COCs递送系统提供根本依据。
3 用于生物成像的共价有机笼
共价有机笼凭借其精确可控的分子结构、可溶液加工性以及可按需嵌入多种光学或磁性基团的能力,近年来逐渐成为生物成像材料的重要新平台[88]。与传统无机纳米探针(如量子点、金属氧化物纳米颗粒)相比,COCs具备无金属骨架、可降解、表面易修饰等优势,能够在维持成像灵敏度的同时降低长循环与生物蓄积的潜在风险[89]。其分子级定义的空腔和外围功能位点使得光学基团、顺磁金属离子及药物分子能够以可预测方式协同集成,为构建多模态成像与诊疗一体化系统提供了独特结构基础[90]。
3.1 荧光及光学成像
在光学成像领域,COCs的优势首先体现在其可通过结构设计实现固有的荧光或增强已嵌入的发光基团性能。一些研究通过在笼体构筑单元中引入蒽、咔唑、四苯乙烯(Tetraphenylethylene,TPE)等发光模块,使笼体本身具备强荧光或聚集诱导发光(AIE)特性[91,92]。AIE机制尤其适用于笼体结构,因为笼体的刚性环境能够有效限制内旋转,从而显著提升量子产率。此外,笼体内部空腔为荧光基团提供了相对疏水和空间受限的微环境,有助于抑制淬灭并实现环境敏感型成像。通过对笼表结构进行极性调控或者引入目标识别基团(如肽、叶酸),光学笼探针已实现对肿瘤细胞、线粒体或特定生物标志物的选择性成像[16]。
值得注意的是,四苯乙烯(TPE)作为一类聚合基聚集诱导发光(AIE)骨架材料,凭借简便的合成工艺与优异的荧光量子产率,已成为该领域备受青睐且极具影响力的核心构筑单元[66,93-95]。Dong等[96]针对多孔有机笼(POCs)在生物成像中因疏水刚性结构导致的聚集诱导猝灭(ACQ)问题,开发了聚集诱导发光(AIE)活性POCs。如图6所示,以四苯乙烯(TPE)为核心,通过NaBH4还原亚胺键得到柔性R-TPE-cage,再经质子化修饰获得高亲水性R(+)-TPE-cage。该材料具有优异的温度和粘度刺激响应性,100~200 nm的纳米尺寸使其近水溶性且易穿透细胞,生物相容性良好。在HeLa、MCF-7等多种细胞系中,R(+)-TPE-cage展现出高效成像性能,3 h细胞摄取率达93.15%,还可通过主客体作用封装银纳米颗粒,为生物成像与药物递送提供了新策略,拓展了POCs的生物应用场景。
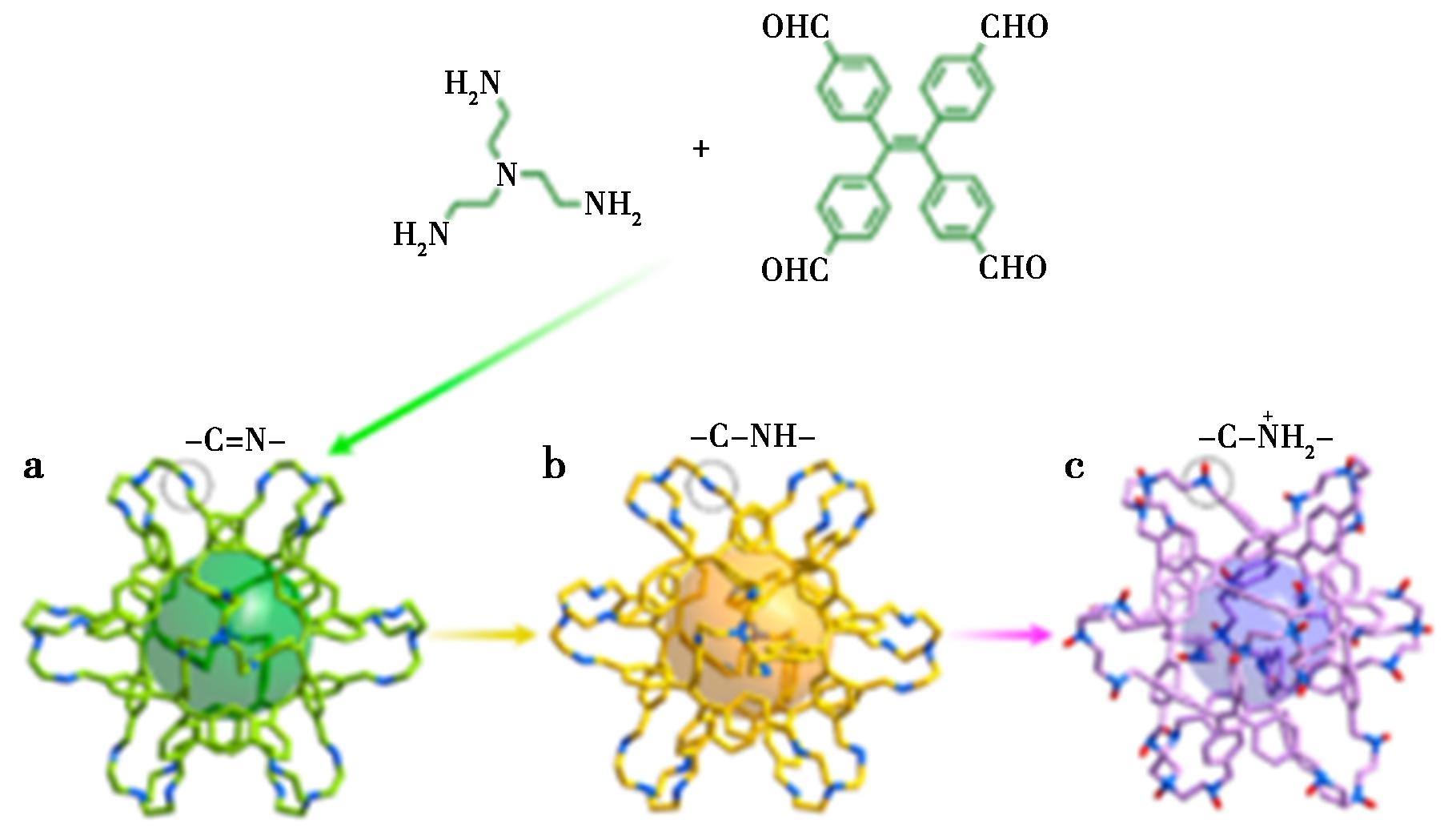
图6 TPE-cage(a)、R-TPE-cage(b)和R(+)-TPE-cage(c)的合成路线[96]
Fig.6 Synthetic routes of TPE-cage (a),R-TPE-cage (b),and R(+)-TPE-cage (c)[96]
Pérez-m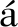 rquez等[18]开发了首个针对3-硝基酪氨酸(NT,肾病关键标志物)的TPE基荧光超分子传感器Cage B(图7)。该传感器通过两步硫醇-迈克尔点击反应合成,TPE单元在笼体中因旋转受限产生强荧光,NT与笼体高亲和力结合后引发静态荧光淬灭,在人体血清中检测限达23 μmol/L,且无其他生物分析物干扰,覆盖慢性肾病患者NT生理浓度,为肾脏损伤临床评估提供了简便高效的新工具。
rquez等[18]开发了首个针对3-硝基酪氨酸(NT,肾病关键标志物)的TPE基荧光超分子传感器Cage B(图7)。该传感器通过两步硫醇-迈克尔点击反应合成,TPE单元在笼体中因旋转受限产生强荧光,NT与笼体高亲和力结合后引发静态荧光淬灭,在人体血清中检测限达23 μmol/L,且无其他生物分析物干扰,覆盖慢性肾病患者NT生理浓度,为肾脏损伤临床评估提供了简便高效的新工具。
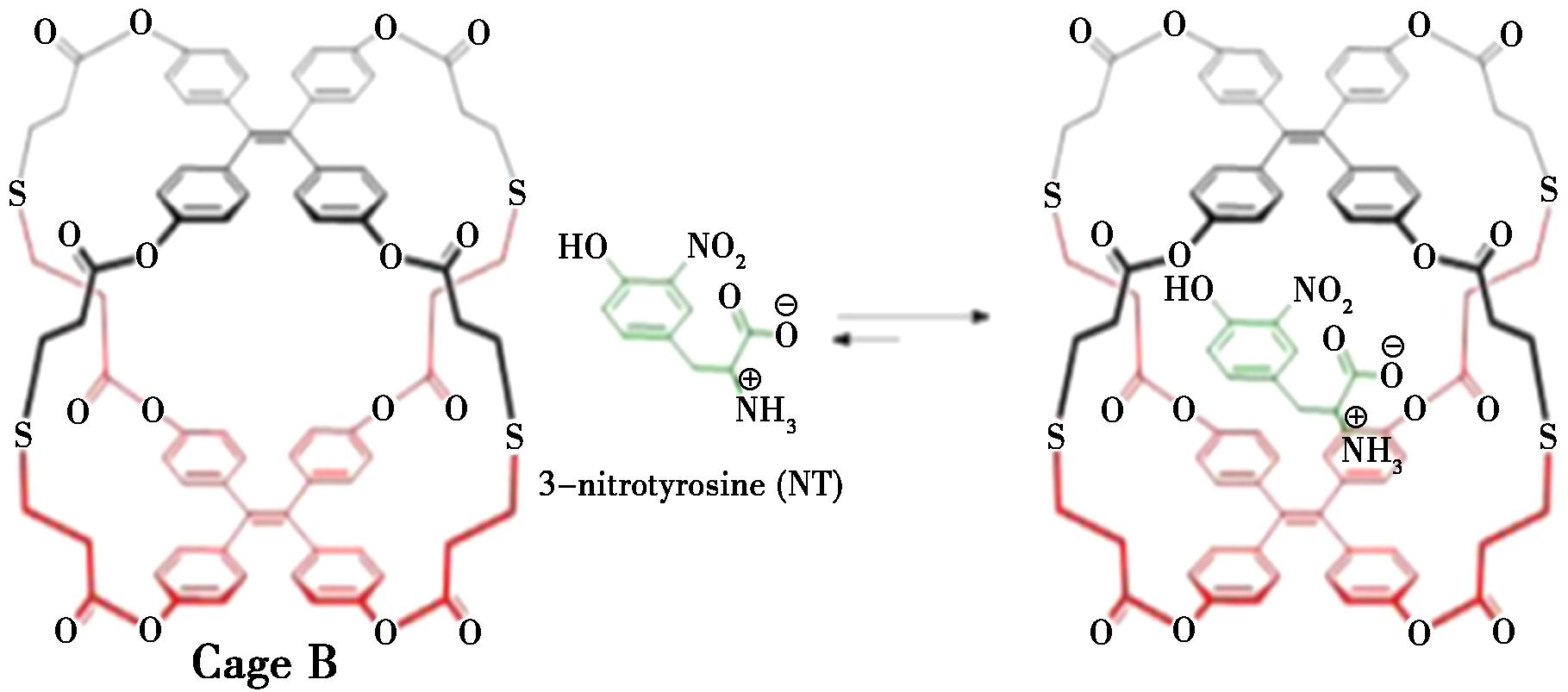
图7 NT在Cage B内部的超分子结合示意图[18]
Fig.7 Supramolecular binding of NT inside Cage B[18]
除了基于TPE的COCs荧光探针外,还有含其他荧光基团(如酚羟基、2,1,3-苯并噻二唑等)的COCs被报道用于生物成像[19,97]。Alimi等[19]开发了应用于生物医学成像的[2+3]型互变异构有机笼OC1。该探针借助酚羟基介导的烯醇-酮互变异构与氢键作用(图8),兼具高生物相容性(IC50>500 μg/mL)、强细胞渗透性(摄取率86.4%)与优异光稳定性(72 h荧光保留),可通过被动扩散精准靶向线粒体(皮尔逊相关系数0.9751),性能显著优于商用探针Mito tracker RedFM。对比实验证实羟基与互变异构是其核心优势,为新型细胞器靶向荧光探针的理性设计提供了重要理论支撑与实践思路。
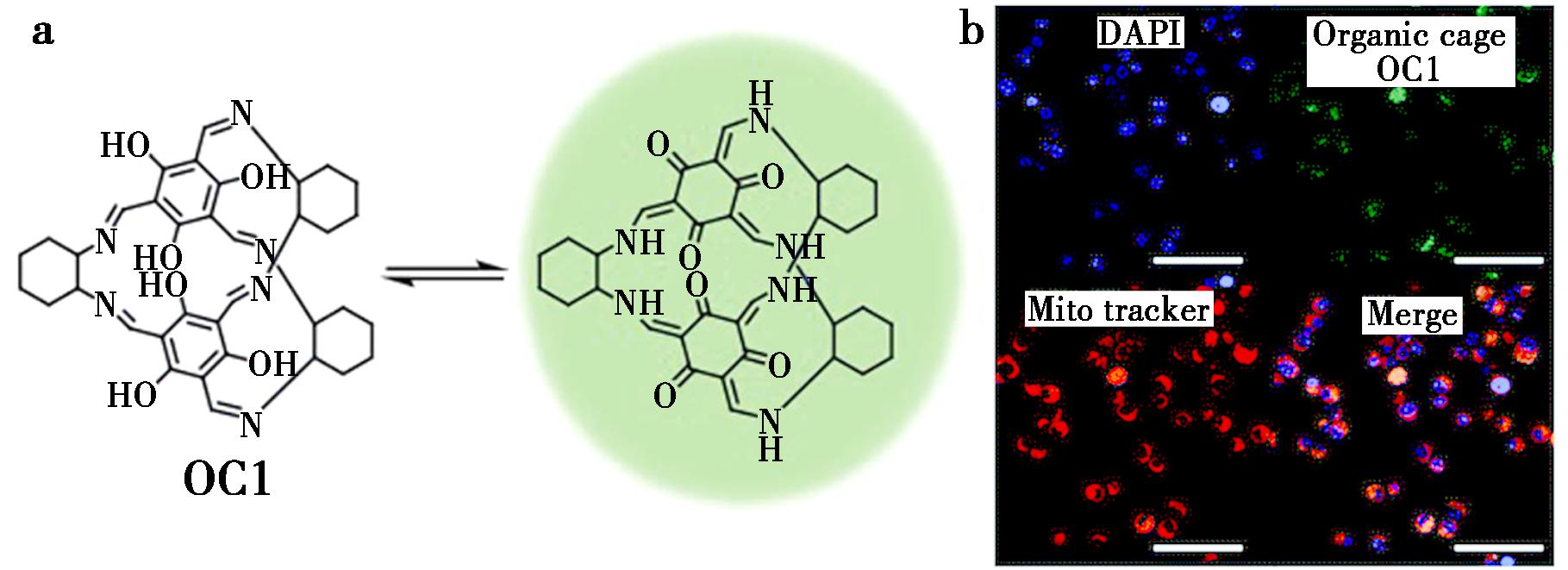
a.OC1的互变异构形式示意图;b.MCF-7细胞与OC1(250 μg/mL)孵育3 h后的活细胞成像结果,显示OC1(激发/发射波长约495/519 nm)与商业线粒体探针Mito tracker RedFM(激发/发射波长约581/644 nm)在线粒体中的摄取及共定位情况,比例尺为50 μm
图8 OC1的互变异构形式和用OC1孵育的MCF-7细胞的活细胞成像结果[19]
Fig.8 Tautomeric forms of OC1 and live cell imaging of MCF-7 cells incubated with OC1[19]
3.2 磁共振与放射成像
在磁共振与放射成像方向,COCs的结构可用于稳定金属离子并避免其游离状态的毒性。例如,基于亚胺或酰胺骨架构建的笼体可作为配体骨架,将Gd3+、Mn2+等顺磁金属离子以明确配位数和空间构型牢固固定,实现高弛豫率和低泄漏风险。与传统小分子MRI造影剂相比,COCs能通过调节笼体尺寸与外层疏水性显著延长循环时间,提高成像窗口[98,99]。
Godart等[99]聚焦共价笼分子在MRI领域的创新应用,通过12步反应合成了基于环三藜芦烃(CTV)的高功能化半隐烷(Hemicryptophane)共价笼HC1。如图9所示,该笼状分子由CTV单元与三(2-氨基乙基)胺(tren)通过含2-羟基间苯二甲酰胺的连接体构建,具C3对称性且在碱性介质中水溶性良好,其多重配位位点为金属离子配合提供了结构基础。将HC1与Gd(Ⅲ)离子配合得到Gd(Ⅲ)@HC1复合物,该共价笼基复合物在2.35T磁场、297 K条件下的纵向弛豫率达46.7 mmol-1·s-1是商用MRI造影剂Dotarem的82.7倍,且在T1加权成像中信号随浓度升高显著增强,造影效果高效。该研究首次实现半隐烷共价笼与f-过渡金属的配合,证实了共价笼分子通过空间限制调控金属离子弛豫性能的优势,为设计高性能MRI造影剂提供了新路径,也拓展了共价笼在生物医学成像领域的应用潜力。
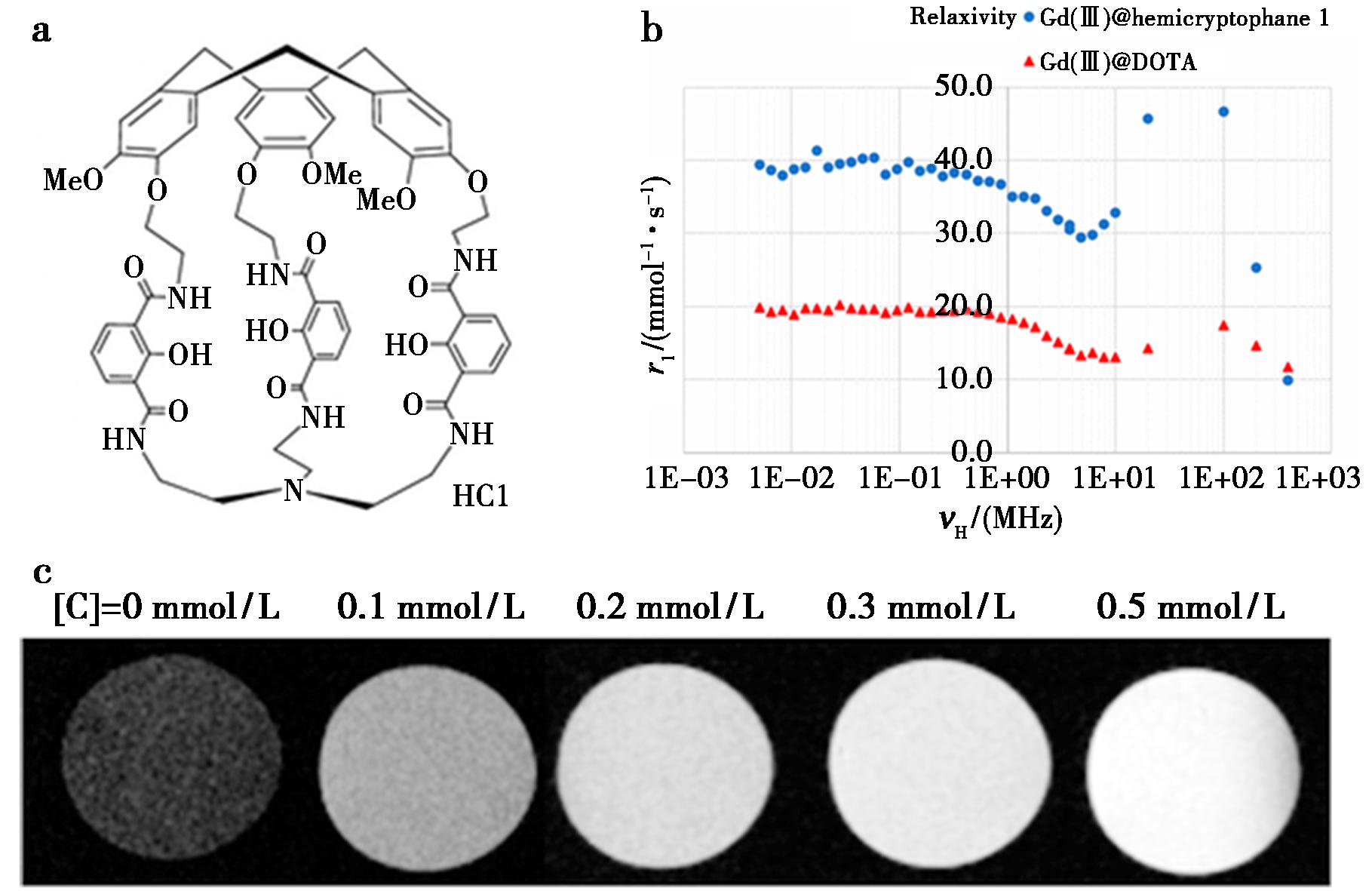
a.半隐烷共价有机笼HC1的结构示意图;b.Gd(Ⅲ)@Hemicryptophane HC1(蓝色圆点)与Gd(Ⅲ)@DOTA(红色三角)溶液中水质子纵向弛豫率(1Hr1)随 1H Larmor频率变化的对比;c.不同浓度半隐烷-Gd(Ⅲ)溶液的T1加权MRI图像(自左至右浓度分别为0、0.1、0.2、0.3和0.5 mmol/L)
图9 HC1的结构和Gd(Ⅲ)@HC1的MRI实验结果[99]
Fig.9 Structure of HC1 and the MRI experimental results of Gd(Ⅲ)@HC1[99]
此外,笼体的结构定义性使得每个笼单位可精确携带固定数目的金属离子,有利于建立剂量—信号之间的可靠关系[100,101]。利用笼体包载或稳定放射性核素实现PET/SPECT成像的研究也在兴起,且由于COCs良好的生物相容性,可进一步降低放射性探针的非特异性分布。
Yu等[59]通过模板导向策略,经卟啉单体预组装、烯烃复分解反应及模板脱除合成卟啉纳米笼,再经12条聚乙二醇(PEG)链酰胺化修饰,构建了卟啉纳米笼嵌入的单分子纳米颗粒(porSMNPs)。如图10a、10b所示,该制剂粒径适配增强渗透滞留效应(EPR),致密PEG冠层提升水溶性与生物相容性,赋予其11.3 h的长血液循环时间。卟啉纳米笼经 64Cu配位标记实现PET成像(图10c、10d),血清螯合稳定性超99.2%,24 h肿瘤摄取率达4.8% ID/g,48 h仍维持有效聚集。
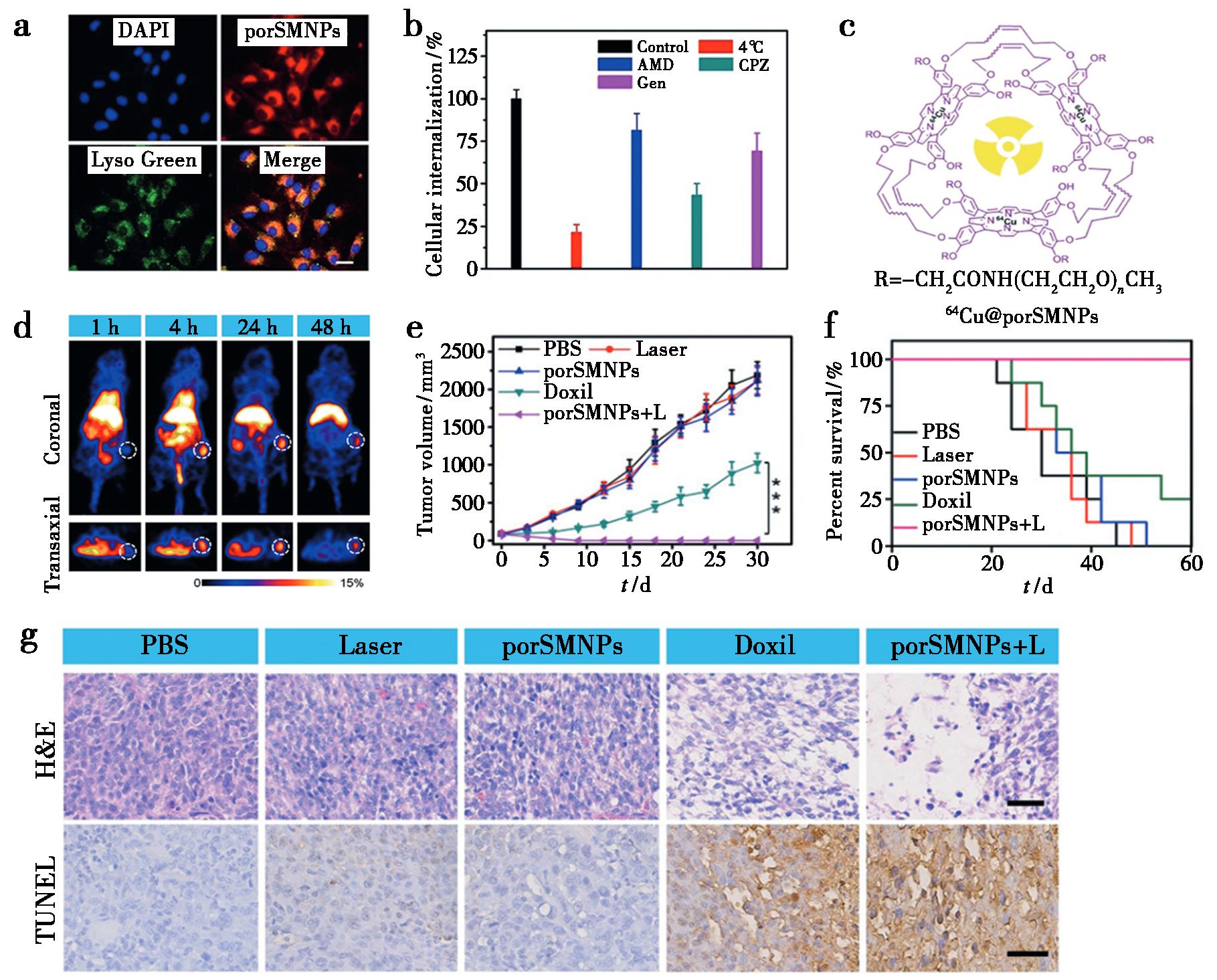
a.U87MG细胞与porSMNPs共孵育8 h后的共聚焦激光扫描显微镜(CLSM)图像,比例尺为50 μm;b.采用不同抑制剂探究porSMNPs细胞摄取机制的实验结果;c.porSMNPs的 64Cu放射性标记示意图;d.U87MG荷瘤小鼠静脉注射 64Cu@porSMNPs后1、4、24和48 h的PET成像结果,白色圆圈标示肿瘤位置;e.不同处理组的肿瘤生长抑制曲线(n=8,***P<0.001);f.不同处理组荷瘤小鼠的生存率(n=8);g.不同处理组肿瘤组织的H&E和TUNEL染色结果,比例尺为200 μm
图10 porSMNPs的结构、生物相容性和诊疗一体化[59]
Fig.10 Structure,biocompatibility and theranostics of porSMNPs[59]
3.3 多模态成像与诊疗一体化
得益于其可同时加载光学探针、金属离子与治疗分子,COCs在构建多模态成像和诊疗一体化系统方面表现尤为突出。一些研究报道通过将AIE发光基团与化疗药物共同嵌入笼体,同时在外围引入MRI金属配位位点,从而实现“光学+MRI”双模态成像,并可实现药物释放的实时监控[96]。在肿瘤模型中,这类“多功能笼”不仅能够在体内精确定位肿瘤,并通过光热、化疗或光动力治疗等方式实现可视化治疗[102,103];还能利用笼体的响应性结构(如pH或酶敏感键)实现成像信号与治疗激活的时序耦合,提高治疗效率并降低副作用[13,78]。由COFs/MOFs在体内多存在可控性不足或溶解性差的问题,可溶性COCs在这类高端应用中的优势逐渐凸显。
Yang等[60]近期开发了一种基于卟啉衍生共价有机笼(PC)的多功能纳米平台DOX@PC@PEG-FA,为COCs在多模态成像及诊疗一体化领域的应用提供了典型范例。如图11所示,该平台通过共价组装将卟啉单元与三胺单体构建为立方笼状结构,1.5 nm3空腔可高效负载化疗药物DOX(负载量0.1 mg/mg PC),锰金属化后形成的MnPC具有优异的T1加权MRI成像性能(r1=6.68 mmol-1·s-1),实现肿瘤靶向成像与治疗过程监测。其核心优势在于通过空间限域效应抑制卟啉π-π堆积,使单线态氧量子产率提升19%,同时共价键赋予平台pH 2~13的广谱稳定性。体外实验显示,该平台可协同化疗与光动力治疗,DOX@PC@PEG-FA+L组对4T1细胞的杀伤率达90.8%;体内实验中,肿瘤体积仅增长0.16倍,抑制率94%,且生物安全性良好(溶血率<5%,主要器官无病理损伤)。该研究证实,COCs凭借结构可设计性、高稳定性及多功能集成能力,能够突破传统载体局限,为构建精准、高效的诊疗一体化纳米系统提供新路径,显著拓展了COCs在生物医学领域的应用前景。
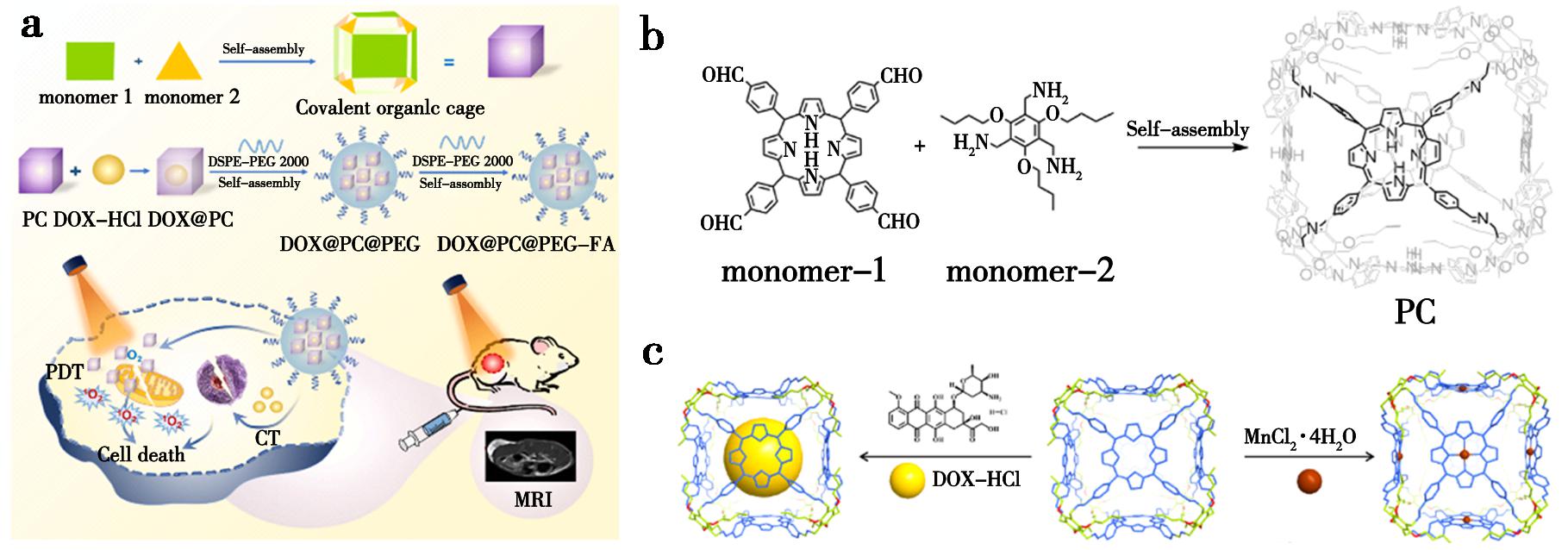
a.DOX@PC@PEG-FA用于MRI引导下化疗-光动力治疗一体化的示意图;b.通过亚胺缩合反应由单体1和单体2合成共价有机笼PC的示意图;c.PC与DOX-HCl通过主-客体作用制备DOX@PC,以及PC经金属化反应制备MnPC的过程示意
图11 DOX@PC@PEG-FA的制备并用于MRI引导下化疗-光动力治疗一体化[60]
Fig.11 Preparation of DOX@PC@PEG-FA for integrated MRI with chemo-photodynamic therapy[60]
图10提到的porSMNPs,其刚性结构抑制光敏剂π-π堆积,大幅提升单线态氧生成效率,光动力治疗(PDT)活性优异,如图10e~10g所示。体内实验中,porSMNPs联合激光可完全消融U87MG肿瘤,凋亡率达90.6%且无复发,无全身毒性,中位生存期超60 d,相比临床药物多柔比星展现更优诊疗效能,为癌症精准诊疗提供极具转化潜力的一体化制剂[59]。
为系统对比各类COCs成像探针的特点与性能,将代表性体系总结于表2。
表2 代表性COCs在生物成像与诊疗中的性能与应用
Tab.2 Performance and applications of representative COCs in bioimaging and theranostics

COC材料成像模式信号单元/机制关键性能参数靶向/功能应用模型文献R(+)-TPE-cage荧光成像TPE单元,聚集诱导发光(AIE)高亲水性,温度/粘度响应细胞穿透HeLa、MCF-7等细胞系[91]Cage B荧光传感/成像TPE单元,结合诱导荧光淬灭对3-硝基酪氨酸检测限达23 μmol/L特异性识别NT(肾病标志物)人体血清[18]OC1荧光成像酚羟基介导的烯醇-酮互变异构光稳定性高,线粒体靶向线粒体靶向MCF-7细胞[19]Gd(Ⅲ)@HC1磁共振成像(MRI)Gd(Ⅲ)配合纵向弛豫率r1=46.7 mmol-1·s-1高性能造影剂T1加权成像测试[99]
续表

COC材料成像模式信号单元/机制关键性能参数靶向/功能应用模型文献porSMNPsPET成像/荧光64Cu标记卟啉笼/光动力治疗血液循环t1/2≈11.3 h,肿瘤摄取4.8% ID/g长循环,EPR效应U87MG肿瘤模型[59]DOX@PC@PEG-FAMRI引导化疗-光动力治疗Mn-卟啉笼/负载DOX(化疗)r1=6.68 mmol-1·s-1,单线态氧量子产率提升19%叶酸靶向,pH响应4T1乳腺癌模型[60]
总体而言,共价有机笼已在生物成像领域显示出独特的结构可设计性和生物应用潜力。从光学、磁共振到放射成像,再到多模态诊疗平台,COCs通过其精确定义的结构与可控的功能化方式,为构建高灵敏度、安全性高、可集成多功能的成像探针提供了新的架构基础。未来发展重点将聚焦于提高成像深度、实现更高的信号—噪声比、开发可降解且代谢明确的笼体骨架,并推动其在动物乃至临床研究中的转化应用。
4 用于生物传感的共价有机笼
4.1 分子识别原理
COCs凭借其高度定义的分子空腔、可设计的内表面化学以及优异的溶液分散性,近年来已成为一类具有突出优势的新型生物传感平台[104]。与传统的金属纳米颗粒、量子点或金属有机框架相比,COCs在空间选择性、结构均一性和生物环境稳定性方面更具可控性,尤其适合构建对小分子代谢物、离子乃至生物大分子具有高亲和力与高选择性的分子识别体系[3,105,12]。
共价有机笼依赖其分子尺度的中空结构提供精确匹配的结合腔体,使其能够通过氢键、π-π堆积、疏水作用或静电相互作用选择性捕获特定分析物[31,106]。通过在笼体内表面引入定制化功能基团(如氨基、羧基、硼酸基、冠醚、肽序列等),可进一步增强识别的方向性和亲和力,实现对ATP、葡萄糖、金属离子或活性氧等关键生物信号分子的精准结合[15,12,107-111]。与传统的超分子笼相比,COCs的kDa级分子量及可控溶解性使其在血液、胞质或胞外微环境中均能保持稳定而不发生大尺度聚集,从而确保识别行为的可靠性[13]。
4.2 荧光与比色传感机制
COCs的结构刚性和可控的基团嵌入能力,使其能够有效调控光学响应过程[96]。许多研究利用笼体的AIE基元、扩展π共轭结构或金属配位单元实现分析物诱导的荧光增强、淬灭或光谱位移[112-114]。例如,含TPE单元的COCs在受分析物结合时会发生构象限制或电子密度改变,从而导致显著的荧光变化[93];而基于硼酸基修饰的笼体能够通过与二醇类物质(如葡萄糖)形成可逆共价键,实现比色或荧光信号的定量化输出[115]。此外,不同于金属纳米材料的比色法通常源于表面等离子体效应且对颗粒聚集状态与介质折射率较敏感,COCs的比色/光谱响应更多来自分子内电子跃迁或主-客体相互作用诱导的电荷转移,因此在需要避免纳米颗粒聚集干扰的应用场景中更具可控性[116,117]。
Qin等[118]通过还原M2(Lα)3(Lβ)2型金属笼,成功制备出具有聚集诱导发光(AIE)特性的共价有机笼C1、C2,其中C2的仲胺活性点位可与氯甲酸苄酯发生酰胺化反应,从而后修饰得到量子产率更高(29.7%)的C3,如图12所示。以这些共价笼为能量供体、尼罗红为受体构建的人工捕光系统,其能量转移效率高(最高76%),天线效应同样较高(最高20)。且该系统在脱卤反应中表现出优异光催化活性,C3-NiR体系产率达67.8%,且底物耐受性良好。该研究整合了金属笼与共价笼的优势,为发光共价笼在捕光和光催化领域的发展提供了新策略。
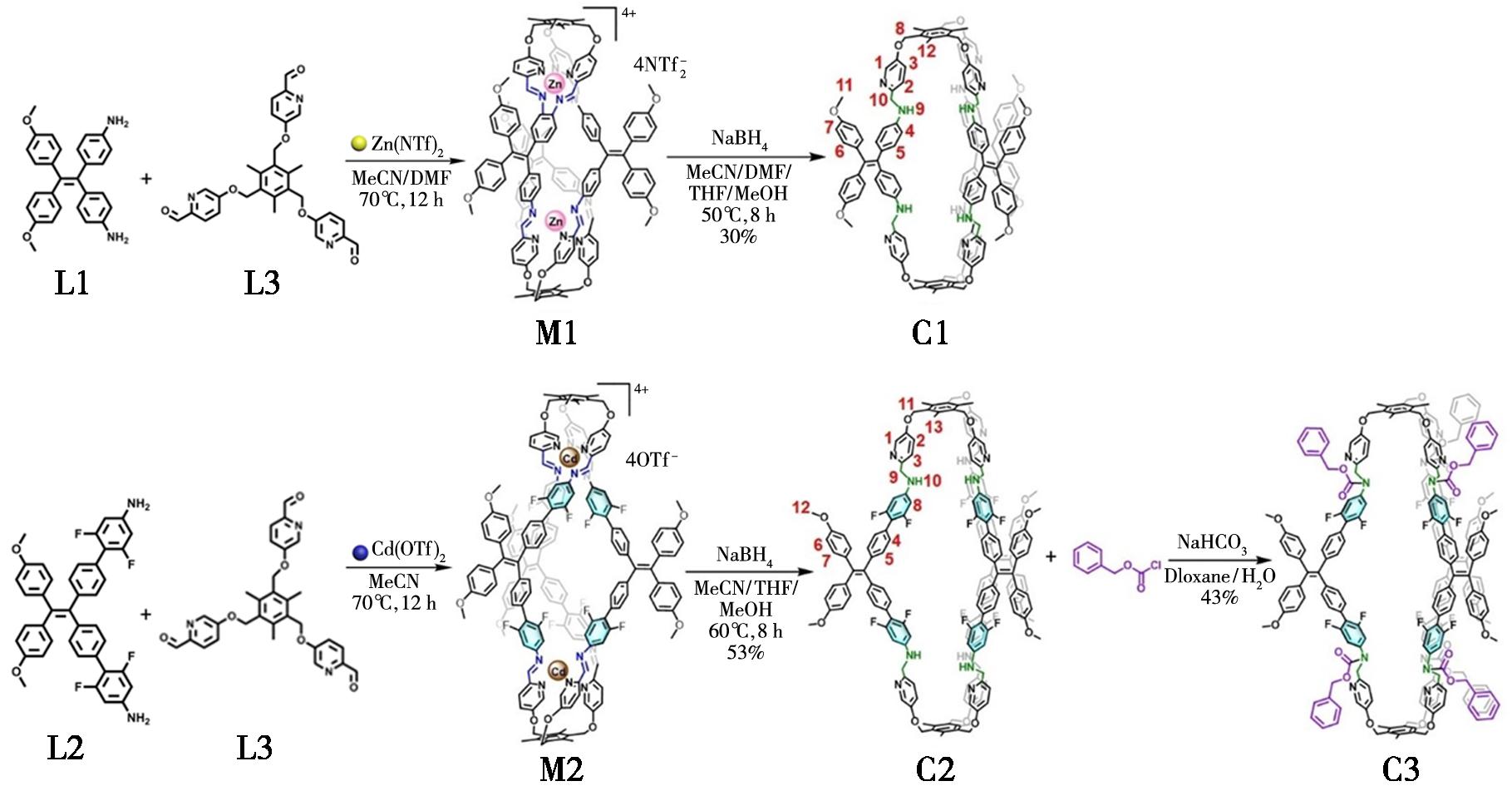
图12 共价有机笼C1和C3的合成路线[118]
Fig.12 Synthetic routes of covalent organic cages C1 and C3[118]
4.3 应用于活体或细胞水平传感的进展
随着COCs的生物相容性与功能化策略不断优化,其在细胞水平的传感验证也在加速推进。已有研究报道多类有机笼荧光探针用于监测重要生理相关分子,例如,ROS响应型有机笼探针可通过氧化诱导的骨架/电子结构变化触发荧光增强或比率信号变化,实现对细胞内氧化应激(如次氯酸,HClO)的成像分析[108,109]。另一方面,得益于笼体内部精确定义的结合空腔与多点非共价相互作用,一些水溶性共价有机笼被用于ATP等高丰度代谢物的识别与检测[15]。此外,基于笼体与金属离子之间的配位/电荷转移相互作用,有机笼荧光体系还能实现对Cu2+等关键金属离子的选择性检测,表现出较好的灵敏度与抗干扰能力[117]。相较于一般小分子探针,有机笼作为离散分子主体,在细胞成像中可呈现更高的光稳定性与更可控的细胞内行为,从而有助于提升信号持续性与成像信噪比[19]。
值得注意的是,利用COCs这一特性,Zhang等[119]针对抗生素耐药性加剧的全球健康危机,设计合成了新型多夹层阳离子共价有机笼Pyrgos[n]cages(n=1~4)。如图13所示,该系列材料通过光催化溴化与笼形成反应制备,具有高密度均匀分布正电荷、高刚性及高稳定性等结构特性,其抗菌效率随夹层数(1~3)增加提升超100倍,其中P-3表现最优。Pyrgos[n]cages采用“破坏细菌膜电位+结合DNA”的双重靶向机制,对金黄色葡萄球菌、耐甲氧西林金黄色葡萄球菌(MRSA)等革兰氏阳性菌展现强效杀菌活性,可同时清除胞内与胞外耐药菌,且能抑制细菌耐药进化(MIC变化仅2倍)。体内外实验验证其低细胞毒性,在小鼠皮肤感染模型中可快速杀菌并促进伤口愈合,为耐药菌感染治疗提供了创新策略与分子基础。针对该材料与DNA的结合机制,分子对接验证显示Pyrgos[n]cages与DNA的结合以沟槽结合(Groove binding)为主(非插入结合),依赖3类相互作用,即①疏水作用:笼体的苯环结构与DNA沟槽内的疏水区域形成疏水堆积;②氢键:笼体咪唑鎓基团的氢原子与DNA碱基对的氧/氮原子形成氢键;③π-π堆积:笼体芳烃的C—H键与DNA碱基的芳香环发生π-π相互作用。而Pyrgos[n]cages表面均匀分布的正电荷,与DNA骨架磷酸基团的负电荷形成静电引力,为结合提供基础驱动力。
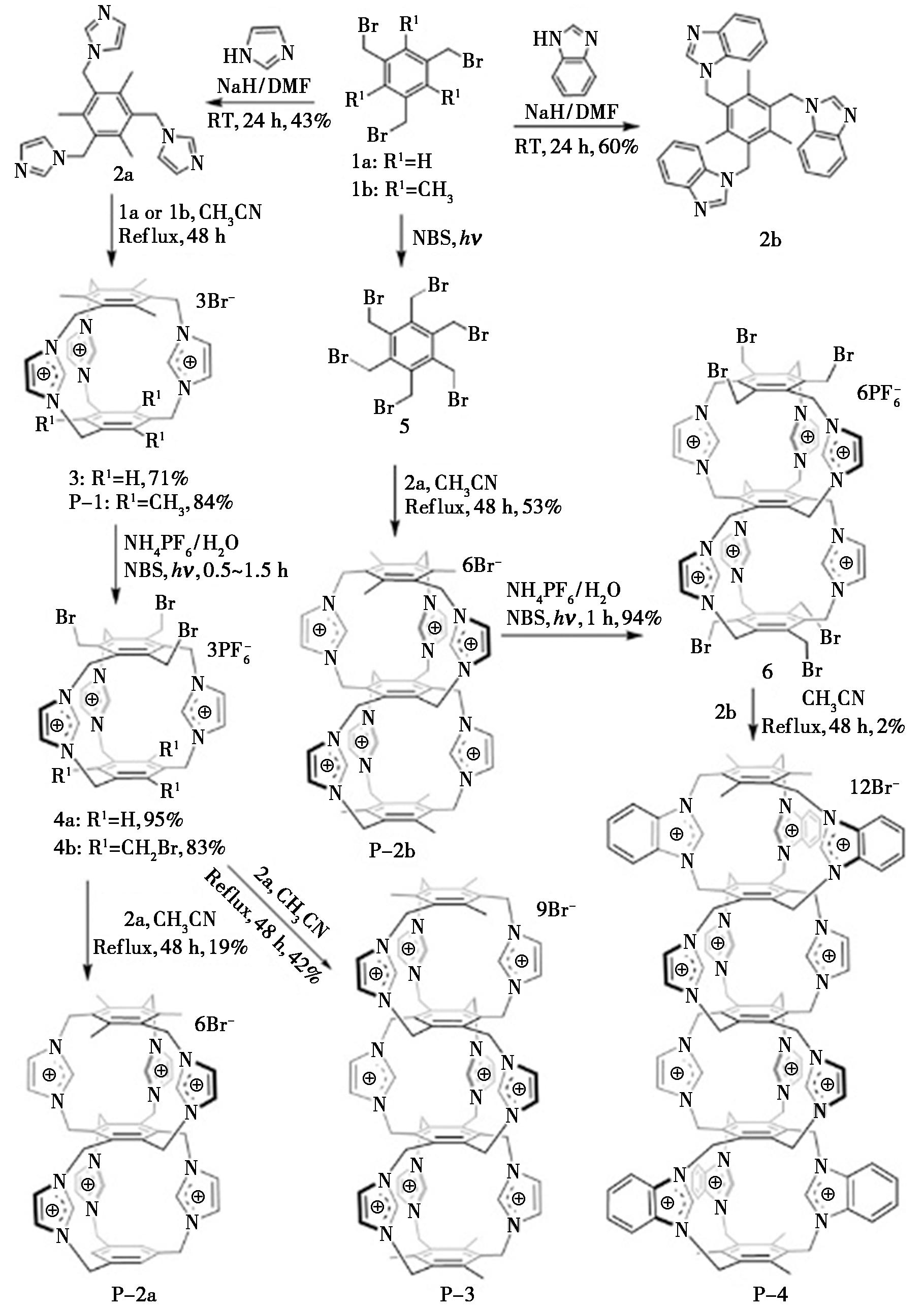
图13 Pyrgos[1]笼(P-1)、Pyrgos[2]笼(P-2a和P-2b)、Pyrgos[3]笼(P-3)及Pyrgos[4]笼(P-4)的合成路线(室温条件)[119]
Fig.13 Synthetic routes of Pyrgos[1]cage (P-1),Pyrgos[2]cages (P-2a and P-2b),Pyrgos[3]cage (P-3),and Pyrgos[4]cage (P-4).room temperature[119]
4.4 与其他纳米传感材料比较
从更广的技术比较角度来看,共价有机笼(COCs)与其他纳米传感材料(如MOFs、COFs、量子点及金属纳米簇等)相比,展现出显著的差异化优势。MOFs/COFs虽然具有较大的孔体积和丰富的功能位点,但其结构在水介质中可能存在稳定性不足的问题,且材料形貌和粒径分布对合成条件较为敏感,不易获得具有明确分子结构定义的传感单元[120-122]。金属纳米材料尽管信号强度较高,但其应用常伴随潜在生物毒性风险以及难以精确调控的表面反应行为[123,124]。相比之下,COCs以离散小分子结构为基本单元,能够在分子尺度上精确调控功能基团密度、荧光中心空间分布及整体立体构型,同时具备更好的溶解性、生物相容性及相对可预测的体内行为[13,53]。这些特性使COCs在构建兼具高选择性、高灵敏度且较好生物相容性的传感体系方面表现出独特优势。
总体而言,共价有机笼正在生物传感领域逐步形成一条由分子识别机制设计、光学响应模式调控到细胞乃至生物体系验证构成的系统化研究路径。其离散分子结构、精确定义的结合空腔以及高度可调的化学环境,使主-客体相互作用与信号转导过程之间能够建立清晰的结构-功能关联,为实现高选择性和高灵敏度的生物传感提供了可靠基础[15,19,109]。
面向未来,通过引入动态或可裂解的化学键,构建具备环境触发降解或潜在生物代谢能力的笼体骨架,有望进一步提升其在生物体系中的安全性与可控性[13,125];同时,结合多重识别位点或多通道光学输出,发展可对多参数生物信号实现并行响应的多功能笼传感器,将有助于复杂生理状态的综合解析[109]。此外,随着对生物相容性、体系稳定性及信号可靠性认识的不断深化,推动共价有机笼从概念验证走向疾病相关模型检测与早期诊断应用,有望成为该领域的重要发展方向。
5 结论
共价有机笼(COCs)凭借独特优势,在药物递送、生物成像及生物传感等生物医学领域展现出广阔应用前景,但从基础研究迈向规模化实际应用仍面临多重挑战。核心瓶颈集中于4方面:分子设计与可控合成的精准性不足、复杂生物环境中的结构稳定性欠佳、体内行为与毒理学特征尚未明确阐明,以及功能集成与跨学科耦合的深度不够。
展望未来,随着合成化学、计算模拟、机器学习辅助设计及单分子表征、先进成像等技术的协同进步,有望快速构建兼具精准形貌、可预测功能与高生物相容性的COCs。其中,人工智能在反应路线规划、结构稳定性预测及药物结合能评估中的应用,将显著加速COCs的设计-验证-优化循环。在反应路线规划方面,计算机辅助合成规划(CASP)工具已能够基于反应数据库输出可行的逆合成拆解与路线候选,为COCs构筑单元筛选、关键官能团引入与后修饰步骤提供“可合成性约束”,从而减少“算得出、做不出”的无效设计[126,127]。在结构稳定性预测方面,针对多孔有机笼已出现面向大规模虚拟笼库的机器学习模型,可快速预测“形状保持性(Shape persistence)”、孔腔尺寸等与孔隙保持密切相关的关键性质,用于优选更可能在溶液/固态维持内在空腔的候选结构[128]。更进一步,若将路线规划与自动化/连续化合成平台结合,可形成“设计—合成—表征—再学习”的闭环迭代,加速材料优化与工艺放大验证[129]。
长远来看,开发可降解、自修复或功能动态调节的“智能笼体”,将推动COCs在精准医学、疾病早筛、可视化治疗及生物电子接口等领域发挥关键作用。
总体而言,COCs正从结构化学基础研究向生命健康应用领域快速跨越。其基于分子尺度工程的精确定义性、功能可编程性及良好生物集成潜力,使其成为药物科学与生物材料领域极具吸引力的前沿方向。随着跨学科合作的深入与技术体系的成熟,COCs有望逐步实现从实验室研究到实际应用的转化,为下一代医疗诊断与治疗平台提供高度可控且安全的材料基础。
[1]Tozawa T,Jones J T A,Swamy S I,Jiang S,Adams D J,Shakespeare S,Clowes R,Bradshaw D,Hasell T,Chong S Y,Tang C,Thompson S,Parker J,Trewin A,Bacsa J,Slawin A M Z,Steiner A,Cooper A I.Nat.Mater.,2009,8(12):973-978.
[2]Hasell T,Cooper A I.Nat.Rev.Mater.,2016,1(9):16053.
[3]Hasell T,Chong S Y,Jelfs K E,Adams D J,Cooper A I.J.Am.Chem.Soc.,2012,134(1):588-598.
[4]Mastalerz M.Angew.Chem.Int.Ed.,2010,49(30):5042-5053.
[5]Schick T H G,Rominger F,Mastalerz M.J.Org.Chem.,2020,85(21):13757-13771.
[6]Jones J T A,Hasell T,Wu X F,Bacsa J,Jelfs K E,Schmidtmann M,Chong S Y,Adams D J,Trewin A,Schiffman F,Cora F,Slater B,Steiner A,Day G M,Cooper A I.Nature,2011,474(7351):367-371.
[7]He A,Jiang Z W,Wu Y,Hussain H,Rawle J,Briggs M E,Little M A,Livingston A G,Cooper A I.Nat.Mater.,2022,21(4):463-470.
[8]Bishop B,Huang S F,Chen H X,Yu H J,Long H,Shen J S,Zhang W.Chin.Chemical Lett.,2024,35(11):109966.
[9]Bhandari P,Mukherjee P S.ACS Catal.,2023,13(9):6126-6143.
[10]Mont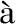 -gonz
-gonz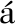 lez G,Martínez-m
lez G,Martínez-m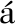
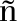 ez R,Martí-centelles V.Targets,2024,2(4):372-384.
ez R,Martí-centelles V.Targets,2024,2(4):372-384.
[11]Ahmad R I,Wang F,Siddiqui R,Zhang M Y,Zhou W,Cai X,He Q.Coord.Chem.Rev.,2025,535:216648.
[12]Zhuang S Y,Wu G,Sun J D,Zhang J S,Xing J B,Wu Y,Wang H,Li Z T,Zhang D W.Org.Chem.Front.,2024,11(2):414-421.
[13]Deng Y P,Du Z H,Du S F,Li N,Wang W J,Su K Z,Yuan D Q.ACS Appl.Bio Mater.,2024,7(11):7535-7543.
[14]Ghaffar A,Asif M B,Mahmood J,Yavuz C T.ACS Mater.Lett.,2025,7(3):1070-1076.
[15]Maji S M,Samanta J,Natarajan R.Chem.,2024,30(15):e202303596.
[16]Zhao Z M,Ukidve A,Kim J,Mitragotri S.Cell,2020,181(1):151-167.
[17]Liu X Y,Fang R J,Feng R,Li Q S,Su M Q,Hou C L,Zhuang K W,Dai Y L,Lei N,Jiang Y B,Liu Y Z,Ran Y P.Drug Resist.Updat.,2022,65:100887.
[18]Pérez-m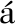 rquez L A,Perretti M D,García-rodríguez R,Lahoz F,Carrillo R.Angew.Chem.Int.Ed.,2022,61(28):e202205403.
rquez L A,Perretti M D,García-rodríguez R,Lahoz F,Carrillo R.Angew.Chem.Int.Ed.,2022,61(28):e202205403.
[19]Al K D,Dey A,Alimi L O,Piwoński H,Habuchi S,Khashab N M.Chem.Sci.,2022,13(24):7341-7346.
[20]Rowan S J,Cantrill S J,Cousins G R L,Sanders J K M,Stoddart J F.Angew.Chem.Int.Ed.,2002,41(6):898-952.
[21]Corbett P T,Leclaire J,Vial L,West K R,Wietor J L,Sanders J K M,Otto S.Chem.Rev.,2006,106(9):3652-3711.
[22]Ro S,Rowan S J,Pease A R,Cram D J,Stoddart J F.Org.Lett.,2000,2(16):2411-2414.
[23]Quan M L C,Cram D J.J.Am.Chem.Soc.,1991,113(7):2754-2755.
[24]Fisher S,Huang H H,Sokoliuk L,Prescimone A,Fuhr O,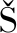 olomek T.J.Org.Chem.,2025,90(12):4158-4166.
olomek T.J.Org.Chem.,2025,90(12):4158-4166.
[25]Christinat N,Scopelliti R,Severin K.Angew.Chem.Int.Ed.,2008,47(10):1848-1852.
[26]Mastalerz M.Acc.Chem.Res.,2018,51(10):2411-2422.
[27]Alfonso I.Chem.Commun.,2016,52(2):239-250.
[28]Collins M S,Carnes M E,Nell B P,Zakharov L N,Johnson D W.Nat.Commun.,2016,7(1):11052.
[29]Orrillo A G,Furlan R L E.Angew.Chem.Int.Ed.,2022,61(26):e202201168.
[30]Kajiyama K,Tsurumaki E,Wakamatsu K,Fukuhara G,Toyota S.ChemPlusChem,2021,86(5):716-722.
[31]Zhao X,Cui H Y,Guo L L,Li B,Li J,Jia X S,Li C J.Angew.Chem.Int.Ed.,2024,63(47):e202411613.
[32]Sato H,Blemker M A,Hellinghausen G,Armstrong D W,Nafie J W,Roberts S T,Krische M J.Chem.,2019,25(37):8719-8724.
[33]Ni Y,Gordillo-g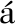 mez F,Pe
mez F,Pe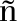 a A M,Nan Z H,Li Z T,Wu S F,Han Y,Casado J,Wu J S.J.Am.Chem.Soc.,2020,142(29):12730-12742.
a A M,Nan Z H,Li Z T,Wu S F,Han Y,Casado J,Wu J S.J.Am.Chem.Soc.,2020,142(29):12730-12742.
[34]Anderson S,Anderson H L,Sanders J K M.Acc.Chem.Res.,1993,26(9):469-475.
[35]Northrop B H,Aricó F,Tangchiavang N,Badji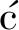 J D,Stoddart J F.Org.Lett.,2006,8(18):3899-3902.
J D,Stoddart J F.Org.Lett.,2006,8(18):3899-3902.
[36]Dale E J,Vermeulen N A,Thomas A A,Barnes J C,Jurí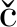 ek M,Blackburn A K,Strutt N L,Sarjeant A A,Stern C L,Denmark S E,Stoddart J F.J.Am.Chem.Soc.,2014,136(30):10669-10682.
ek M,Blackburn A K,Strutt N L,Sarjeant A A,Stern C L,Denmark S E,Stoddart J F.J.Am.Chem.Soc.,2014,136(30):10669-10682.
[37]Ding H M,Wu X J,Zeller M,Xie Y P,Wang C.J.Org.Chem.,2015,80(18):9360-9364.
[38]Zhang W Y,Zhang M Y,Liu Q,He Q.Chem.Lett.,2025,54(11):upaf197.
[39]Chakraborty D,Modak R,Howlader P,Mukherjee P S.Chem.Commun.,2021,57(33):3995-3998.
[40]Carpenter J P,McTernan C T,Greenfield J L,Lavendomme R,Ronson T K,Nitschke J R.Chem.,2021,7(6):1534-1543.
[41]Yusaf Z Z,Egleston B D,Avci G,Jelfs K E,Lewis J E M,Greenaway R L.Chem.,2025,31(35):e202501014.
[42]Yang Z Z,Lehn J M.J.Am.Chem.Soc.,2020,142(35):15137-15145.
[43]Benke B P,Kirschbaum T,Graf J,Gross J H,Mastalerz M.Nat.Chem.,2023,15(3):413-423.
[44]Pausch T,Martínez Mestre P,Zapata F,Mix A,Schmidt B M.Chem.Sci.,2025,16(29):13221-13228.
[45]Avellaneda A,Valente P,Burgun A,Evans J D,Markwell-heys A W,Rankine D,Nielsen D J,Hill M R,Sumby C J,Doonan C J.Angew.Chem.Int.Ed.,2013,52(13):3746-3749.
[46]Briggs M E,Slater A G,Lunt N,Jiang S,Little M A,Greenaway R L,Hasell T,Battilocchio C,Ley S V,Cooper A I.Chem.Commun.,2015,51(98):17390-17393.
[47]Zhu G H,Liu Y,Flores L,Lee Z R,Jones C W,Dixon D A,Sholl D S,Lively R P.Chem.Mater.,2018,30(1):262-272.
[48]Jiang S,Jones J T A,Hasell T,Blythe C E,Adams D J,Trewin A,Cooper A I.Nat.Commun.,2011,2(1):207.
[49]Little M A,Chong S Y,Schmidtmann M,Hasell T,Cooper A I.Chem.Commun.,2014,50(67):9465-9468.
[50]Lucero J M,Jasinski J B,Song M,Li D S,Liu L L,Liu J,De Yoreo J J,Thallapally P K,Carreon M A.Inorg.Chim.Acta,2020,501:119312.
[51]Egleston B D,Brand M C,Greenwell F,Briggs M E,James S L,Cooper A I,Crawford D E,Greenaway R L.Chem.Sci.,2020,11(25):6582-6589.
[52]Liu X L,Wang A,Wang C P,Li J L,Zhang Z Y,Al-Enizi A M,Nafady A,Shui F,You Z F,Li B Y,Wen Y B,Ma S Q.Nat.Commun.,2023,14(1):7022.
[53]Hong S,Rohman M R,Jia J T,Kim Y,Moon D,Kim Y,Ko Y H,Lee E,Kim K.Angew.Chem.Int.Ed.,2015,54(45):13241-13244.
[54]Lucero J,Crawford J M,Osuna C,Carreon M A.CrystEngComm,2019,21(34):5039-5044.
[55]Mao Q Q,Yang S Y,Zhang J J,Liu Y H,Liu M.Adv.Sci.,2024,11(45):2408494.
[56]Konopka M,Cecot P,Harrowfield J M,Stefankiewicz A R.J.Mater.Chem.C,2021,9(24):7607-7614.
[57]Yang M,Qiu F L,El-sayed E M,Wang W J,Du S F,Su K Z,Yuan D Q.Chem.Sci.,2021,12(40):13307-13315.
[58]Kim K P,Cha J D,Jang E H,Klumpp J,Hagens S,Hardt W D,Lee K Y,Loessner M J.Microb.Biotechnol.,2008,1(3):247-257.
[59]Yu G C,Cen T Y,He Z M,Wang S P,Wang Z T,Ying X W,Li S J,Jacobson O,Wang S,Wang L,Lin L S,Tian R,Zhou Z J,Ni Q Q,Li X P,Chen X Y.Angew.Chem.Int.Ed.,2019,58(26):8799-8803.
[60]Xin L H,He W,Huang K K,Li W C,Yang H,Yang S P,Jiao J J.Chem.Eng.J.,2025,526:171229.
[61]Benyettou F,Khair M,Prakasam T,Varghese S,Matouk Z,Alkaabi M,Pena-s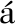 nchez P,Boitet M,Abdulhalim R,Sharma S K,Ghemrawi R,Thomas S,Whelan J,Pasricha R,Jagannathan R,G
nchez P,Boitet M,Abdulhalim R,Sharma S K,Ghemrawi R,Thomas S,Whelan J,Pasricha R,Jagannathan R,G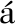 ndara F,Trabolsi A.ACS Appl.Mater.Interfaces,2024,16(42):56676-56695.
ndara F,Trabolsi A.ACS Appl.Mater.Interfaces,2024,16(42):56676-56695.
[62]Ohradanova-repic A,Nogueira E,Hartl I,Gomes A C,Preto A,Steinhuber E,Mühlgrabner V,Repic M,Kuttke M,Zwirzitz A,Prouza M,Suchanek M,Wozniak-knopp G,Horejsi V,Schabbauer G,Cavaco-paulo A,Stockinger H.Nanomed.Nanotechnol.Biol.Med.,2018,14(1):123-130.
[63]Guo Z X,Kong W X,Zhou L Y,He Y,Ma L,Liu G H,Liu Y T,Jiang Y J.ACS Catal.,2025,15(5):3955-3966.
[64]Kirchner P H,Schramm L,Ivanova S,Shoyama K,Würthner F,Beuerle F.J.Am.Chem.Soc.,2024,146(8):5305-5315.
[65]Ling H,Shu H Z,Zhang M X,Liang W C,Li Y W,Li L Y,Zhang L,Huang S Q,Liu H X,Ren S J.ACS Appl.Mater.Interfaces,2025,17(48):65509-65518.
[66]Konopka M,Cecot P,Ulrich S,Stefankiewicz A R.Front.Chem.,2019,7:503.
[67]Dong S Q,Han Y,Tong Z K,Wang J F,Zhang Y S,Li A S,Gopalakrishna T Y,Tian H K,Chi C Y.Chem.Sci.,2024,15(24):9087-9095.
[68]Yang X C,Ullah Z,Stoddart J F,Yavuz C T.Chem.Rev.,2023,123(8):4602-4634.
[69]Yang M,Su K Z,Yuan D Q.Chem.Commun.,2024,60(76):10476-10487.
[70]Liu H,Duan X H,Lv Y K,Zhu L L,Zhang Z X,Yu B,Jin Y X,Si Y N,Wang Z Y,Li B J,Peng P.Chem.Eng.J.,2021,426:130872.
[71]Duan H H,Li Y W,Li Q F,Wang P P,Liu X R,Cheng L,Yu Y,Cao L P.Angew.Chem.Int.Ed.,2020,59(25):10101-10110.
[72]Chen L J,Reiss P S,Chong S Y,Holden D,Jelfs K E,Hasell T,Little M A,Kewley A,Briggs M E,Stephenson A,Thomas K M,Armstrong J A,Bell J,Busto J,Noel R,Liu J,Strachan D M,Thallapally P K,Cooper A I.Nat.Mater.,2014,13(10):954-960.
[73]Ning G H,Cui P,Sazanovich I V,Pegg J T,Zhu Q,Pang Z F,Wei R J,Towrie M,Jelfs K E,Little M A,Cooper A I.Chem.,2021,7(11):3157-3170.
[74]Zhu G H,Hoffman C D,Liu Y,Bhattacharyya S,Tumuluri U,Jue M L,Wu Z L,Sholl D S,Nair S,Jones C W,Lively R P.Chem.,2016,22(31):10743-10747.
[75]Zhu W,Yu H,Luo Y,Chen S,Zheng X.ChemRxiv,2021,doi:10.26434/chemrxiv-2021-rbblr.
[76]Wen H Y,Dong H Q,Xie W J,Li Y Y,Wang K,Pauletti G M,Shi D L.Chem.Commun.,2011,47(12):3550.
[77]Cazzaniga G,Zambra M,Bongiolo S,Prpi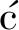 H,Fasola E,Arrigoni F,Piarulli U,Gazzola S.ACS Omega,2025,10(36):41783-41798.
H,Fasola E,Arrigoni F,Piarulli U,Gazzola S.ACS Omega,2025,10(36):41783-41798.
[78]Sullivan H L,Liang Y F,Worthington K,Luo C,Gianneschi N C,Christman K L.Biomacromolecules,2023,24(11):4695-4704.
[79]Zhang Y Y,Tian S D,Huang L P,Li Y N,Lu Y,Li H Y,Chen G P,Meng F L,Liu G L,Yang X L,Tu J S,Sun C M,Luo L.Nat.Commun.,2022,13(1):4553.
[80]Li W Y,Kan J L,Wan J J,Li Y A,Song T,Wang B,Guan Q,Zhou L L,Dong Y B.Chem.Commun.,2023,59(36):5423-5426.
[81]Mont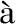 -gonz
-gonz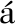 lez G,Bastante-rodríguez D,García-FErn
lez G,Bastante-rodríguez D,García-FErn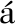 ndez A,Lusby P J,Martínez-m
ndez A,Lusby P J,Martínez-m
 ez R,Martí-centelles V.Chem.Sci.,2024,15(26):10010-10017.
ez R,Martí-centelles V.Chem.Sci.,2024,15(26):10010-10017.
[82]Liyana G V W,Ward C,Wang H,Holbrook J H,Sekera E R,Cui H G,Hummon A B,Badji J D.Angew.Chem.Int.Ed.,2023,62(33):e202306722.
J D.Angew.Chem.Int.Ed.,2023,62(33):e202306722.
[83]Li M,Peng Y,Yan F,Li C G,He Y Q,Lou Y,Ma D X,Li Y,Shi Z,Feng S H.New J.Chem.,2021,45(6):3343-3348.
[84]Jia Z,Hu D Y,Su Y Y,Li H Q,Zhang J J,Ji H,Zou Y,Hong S,Liu M.ACS Appl.Mater.Interfaces,2025,17(49):67351-67360.
[85]Ghosh C,Ali L M A,Bessin Y,Clément S,Richeter S,Bettache N,Ulrich S.Org.Biomol.Chem.,2024,22(7):1484-1494.
[86]Andrews K G,Christensen K E.Chem.,2023,29(26):e202300063.
[87]Soo C H,Liu W H,Misra P,Tanaka E,Zimmer J P,Itty I B,Bawendi M G,Frangioni J V.Nat.Biotechnol.,2007,25(10):1165-1170.
[88]Dou W T,Yang C Y,Hu L R,Song B,Jin T X,Jia P P,Ji X L,Zheng F,Yang H B,Xu L.ACS Mater.Lett.,2023,5(4):1061-1082.
[89]Mahata K,Frischmann P D,Würthner F.J.Am.Chem.Soc.,2013,135(41):15656-15661.
[90]Guan Y M,Gao H,Xu W B,Su P Y,Zhou T X,Xie T Z,Wang M J,Luo H G,Wang P S.RSC Adv.,2025,15(20):15476-15479.
[91]Luo J D,Xie Z L,Lam J W Y,Cheng L,Tang B Z,Chen H Y,Qiu C F,Kwok H S,Zhan X W,Liu Y Q,Zhu D B.Chem.Commun.,2001(18):1740-1741.
[92]Li Y W,Dong Y H,Cheng L,Qin C Y,Nian H,Zhang H Y,Yu Y,Cao L P.J.Am.Chem.Soc.,2019,141(21):8412-8415.
[93]Feng H T,Yuan Y X,Xiong J B,Zheng Y S,Tang B Z.Chem.Soc.Rev.,2018,47(19):7452-7476.
[94]Zhao J,Zhou Z X,Li G F,Stang P J,Yan X Z.Natl.Sci.Rev.,2021,8(6):nwab045.
[95]Zheng X J,Zhu W C,Zhang C,Zhang Y,Zhong C,Li H,Xie G H,Wang X J,Yang C L.J.Am.Chem.Soc.,2019,141(11):4704-4710.
[96]Dong J Q,Pan Y T,Yang K W,Yuan Y D,Wee V,Xu S D,Wang Y X,Jiang J W,Liu B,Zhao D.ACS Nano,2022,16(2):2355-2368.
[97]Fakim A,Maatouk B I,Maiti B,Dey A,Alotaiby S H,Moosa B A,Lin W B,Khashab N M.Adv.Healthc.Mater.,2024,13(26):2401117.
[98]Zamberlan F,Lesbats C,Rogers N J,Krupa J L,Pavlovskaya G E,Thomas N R,Faas H M,Meersmann T.ChemPhysChem,2015,16(11):2294-2298.
[99]Godart E,Long A,Rosas R,Lemercier G,Jean M,Leclerc S,Bouguet-bonnet S,Godfrin C,Chapellet L L,Dutasta J P,Martinez A.Org.Lett.,2019,21(7):1999-2003.
[100]Amendola V,Alberti G,Bergamaschi G,Biesuz R,Boiocchi M,Ferrito S,Schmidtchen F P.Eur.J.Inorg.Chem.,2012,2012(21):3410-3417.
[101]Alberto R,Bergamaschi G,Braband H,Fox T,Amendola V.Angew.Chem.Int.Ed.,2012,51(39):9772-9776.
[102]Yu G C,Yu S,Saha M L,Zhou J,Cook T R,Yung B C,Chen J,Mao Z W,Zhang F W,Zhou Z J,Liu Y J,Shao L,Wang S,Gao C Y,Huang F H,Stang P J,Chen X Y.Nat.Commun.,2018,9(1):4335.
[103]Yin P L,Sun D M,Deng Y C,Zhu X Y,Wang Y F,Yang J H,Feng X S.Theranostics,2024,14(12):4861-4873.
[104]Dai C,Gu B,Tang S P,Deng P H,Liu B.Anal.Chim.Acta,2022,1192:339376.
[105]Ren H M,Liu C,Yang W,Jiang J Z.Dyes Pigm.,2022,200:110117.
[106]Song H X,Guo Y J,Zhang G R,Shi L L.Int.J.Mol.Sci.,2023,24(24):17541.
[107]Zhang S Y,Kochovski Z,Lee H C,Lu Y,Zhang H M,Zhang J,Sun J K,Yuan J Y.Chem.Sci.,2019,10(5):1450-1456.
[108]Xu Y,Dai C,Xu Z F.Spectrochim.Acta Part A Mol.Biomol.Spectrosc.,2026,346:126928.
[109]Dai C,Xu Y,Liu B,Gu B.Microchem.J.,2024,204:110967.
[110]Rios P,Carter T S,Mooibroek T J,Crump M P,Lisbjerg M,Pittelkow M,Supekar N T,Boons G J,Davis A P.Angew.Chem.Int.Ed.,2016,55(10):3387-3392.
[111]Tromans R A,Samanta S K,Chapman A M,Davis A P.Chem.Sci.,2020,11(12):3223-3227.
[112]Kumari C,Kumar A.RSC Adv.,2025,15(51):43366-43376.
[113]Feng F D,Peng Y X,Zhang L,Huang W.Dyes Pigm.,2021,194:109657.
[114]Zhang Z,Bai Q X,Zhai Z R,Long Q W,Han E M,Zhao H,Zhou C W,Lin H B,Zhang W,Ning G H,Xie T Z,Wang P S,Wu T.Nat.Commun.,2024,15(1):7261.
[115]Maatouk A,Rossel T,Therrien B.Inorganics.,2025,13(1):1-14.
[116]Storhoff J J,Lazarides A A,Mucic R C,Mirkin C A,Letsinger R L,Schatz G C.J.Am.Chem.Soc.,2000,122(19):4640-4650.
[117]Dai C,Qian H L,Yan X P.J.Hazard.Mater.,2021,416:125860.
[118]Qin Y,Ling Q H,Wang Y T,Hu Y X,Hu L R,Zhao X L,Wang D,Yang H B,Xu L,Tang B Z.Angew.Chem.Int.Ed.,2023,62(36):e202308210.
[119]Zhang Y,Luo M M,Shi X L,Li A M,Zhou W,Yin Y Y,Wang H,Wong W L,Feng X X,He Q.Sci.Adv.,2024,10(30):eadp4872.
[120]Chong S Y.IUCrJ,2016,3(6):391-392.
[121]Safy M E A,Amin M,Haikal R R,Elshazly B,Wang J J,Wang Y M,Wöll C,Alkordi M H.Chem.,2020,26(31):7109-7117.
[122]Li X L,Zhang C L,Cai S L,Lei X H,Altoe V,Hong F,Urban J J,Ciston J,Chan E M,Liu Y.Nat.Commun.,2018,9(1):2998.
[123]Carnovale C,Bryant G,Shukla R,Bansal V.ACS Omega,2019,4(1):242-256.
[124]Wan J L,Wang J H,Liu T,Xie Z X,Yu X F,Li W H.Sci.Rep.,2015,5(1):11398.
[125]Schick T H G,Lauer J C,Rominger F,Mastalerz M.Angew.Chem.Int.Ed.,2019,58(6):1768-1773.
[126]Coley C W,Rogers L,Green W H,Jensen K F.ACS Cent.Sci.,2017,3(12):1237-1245.
[127]Bennett S,Szczypiński F T,Turcani L,Briggs M E,Greenaway R L,Jelfs K E.J.Chem.Inf.Model.,2021,61(9):4342-4356.
[128]Turcani L,Greenaway R L,Jelfs K E.Chem.Mater.,2019,31(3):714-727.
[129]Coley C W,Thomas D A III,Lummiss J A M,Jaworski J N,Breen C P,Schultz V,Hart T,Fishman J S,Rogers L,Gao H Y,Hicklin R W,Plehiers P P,Byington J,Piotti J S,Green W H,Hart A J,Jamison T F,Jensen K F.Science,2019,365(6453):eaax1566.