兽药被广泛用于治疗或预防动物疾病[1,2]。然而,部分商家非法加入β-受体激动剂[3,4],或超标加入喹诺酮类[5,6]、四环素类等抗生素,进而导致肉、蛋、奶等食品中兽药残留超标,严重危害人体健康。尽管我国出台多项国家标准GB 29692—2013《牛奶中喹诺酮类药物残留量的测定 高效液相色谱法》[7]、GB/T 21312—2007《动物源性食品中14种喹诺酮药物残留检测方法液相色谱-质谱/质谱法》[8]等,但检测方法普遍存在回收率低,前处理耗时长,重复性差等问题,这是因为动物源性食品基质复杂,且肉、蛋、奶中存在的磷脂类杂质会干扰液相-质谱(LC-MS)分析的灵敏度和精度。此外,磷脂类物质易在仪器进样口和色谱柱上不断富集,大大降低了液相[9,10]和质谱[11-13]系统的寿命,维护成本增加。
基于此,针对食品基质中磷脂的净化处理具有重要的现实意义。据文献报道,吸附磷脂的材料有3类,第一类是硅胶基质材料[14,15],常用的氨丙基、氨基或二醇基修饰的硅胶,此类正相SPE材料,对磷脂类化合物的选择性普遍不高。赵琪等[16]制备了一种氨基化磁性空心复合硅基材料分离食用油中的磷脂,制备工艺繁琐,使用原料种类多达十余种,不适合产业化。第二类是聚合物基质[17,18],Herrero-martinez等[19]采用甲基丙烯酸与乙二醇二甲基丙烯酸酯共聚制备的分子印迹微球来吸附磷脂,此种分子印迹可循环使用,对模板分子磷脂酰胆碱(PC)的选择性高于90%,但分子印迹操作步骤多,模板分子不易洗脱,批次间重复性差;第三类是金属氧化物材料[20],董文琪[21]研究了25种纳米金属氧化物(MeONPs)对二棕榈酰磷脂酰胆碱的吸附效果,证明了主要吸附机理是MeONPs与磷脂上的磷酸基团相互作用。但金属氧化物材料受颗粒大小的限制,吸附效率都不高,会产生重金属污染。亟需开发一种去磷脂效率高、成本低廉、易生产放大的固相萃取填料,以此更好地推广和普及对复杂食品基质中的兽残监测。
本文制备了一种极性和非极性共存的双亲性材料,即在硅胶表面修饰十八烷基三氯硅烷(Octadecyltrichlorosilane,OTS),硅胶表面残留硅醇基可与磷脂分子的极性部分相互作用,键合的长链烷烃又能与磷脂化合物的疏水烷烃相互作用,从而牢牢吸附磷脂,可应用于食品检测的样品前处理中。结合HPLC/MS/MS的检测,对鸡蛋、全脂牛奶、鸡肉、猪肉等多种食品基质中的磷脂去除率和鸡蛋中的19种β-受体激动剂、喹诺酮抗生素的兽残加标回收率进行测试。
1 实验部分
1.1 主要仪器与试剂
Equinox型半微量分析天平(英国艾德姆衡器有限公司);FW30型顶置搅拌器(德国弗鲁克有限公司);Mastersizer 3000型激光粒度仪(英国马尔文帕纳科公司);ASAP 2460型全自动比表面及孔隙度分析仪(美国Micromeritics Instrument公司);PE QSightTM 220型液相质谱联用仪(配有电喷雾离子源(ESI),美国珀金埃尔默仪器有限公司);Sigma 300型扫描电镜(德国Carl Zeiss公司);Elementar Unicube型有机元素分析仪(德国 Elementar公司)。
超纯硅胶60(40~63 μm,瑰椒聚上海科技发展有限公司);硅胶-2(色谱级,55~70 μm)、硅胶-3(色谱级,35~45 μm)(青岛信利达硅胶有限公司);硅胶-4(色谱级,40~63 μm,青岛海湾精细化工有限公司);十八烷基三氯硅烷(分析纯,上海阿拉丁生化科技股份有限公司);甲苯、乙醇(色谱级,上海安谱实验科技股份有限公司);9种β-受体激动剂类药物混标、10种喹诺酮类药物混标(1 μg/g)、L-α-磷脂酰胆碱标准品(PC,99.5%)、神经鞘磷脂标准品(SM,99.5%)、磷脂酰乙醇胺标准品(PE,99.5%)(上海安谱璀世标准技术服务有限公司);Waters Oasis PRiME HLB(3 cc/60 mg,美国沃特世公司)。
1.2 实验方法
1.2.1 PPR材料的制备
500 mL三口烧瓶中加入150 mL甲苯,开启机械搅拌,转速为250 r/min,加入50 g硅胶。以1 mL/min的速度滴加10 mL OTS,滴加完毕,升温至60 ℃,计时,3 h后结束反应。待产物冷却至室温,过滤,滤饼用150 mL甲苯、甲醇各洗涤2次,60 ℃真空干燥6 h,记作PPR。
1.2.2 PPR柱制备方法
取3 mL空柱管中装入下筛板,然后称取200 mg(精确至0.0001 g)的PPR填料于下筛板上,装入上筛板,压紧,使填料紧实,平整。
1.3 固相萃取前处理方法
1.3.1 去磷脂测试的前处理方法
全脂牛奶:取1.0 g全脂牛奶加入15 mL离心管,加入4 mL含有0.2%甲酸的乙腈,涡旋振荡混合10 min后,离心(4000 r/min)10 min,待净化。
鸡蛋液、鸡肉、猪肉:分别取2.0 g均质后的食品基质于50 mL离心管中,加入10 mL含0.2%甲酸的V(乙腈)∶V(水)=80∶20溶液,涡旋振荡混合10 min后,离心(4000 r/min)10 min,待净化。
净化:取上述离心后的上清液直接过PPR小柱,收集过柱液后,在45 ℃氮吹条件下吹干,加入1 mL的V(乙腈)∶V(水)=50∶50复溶,复溶后超声5 min,用0.22 μm的尼龙滤器过滤后待检测。未净化样制备:上述基质提取后不经过PPR柱净化,直接过0.22 μm的尼龙滤器待检测。
去磷脂率的计算公式:分别取上述基质的未净化样溶液、样品净化溶液注入仪器中,记录磷脂峰面积,按照公式(1)进行计算:
X=(1-A0/A)×100%
(1)
式中:X为SPE柱的去磷脂效率,%;A为基质样品未经SPE柱净化的所有磷脂峰面积总和;A0为基质样品经SPE柱净化后的所有磷脂峰面积总和。
1.3.2 兽残加标回收率前处理方法
取2.0 g均质后的鸡蛋试样于50 mL离心管中,加入一定体积的β-受体激动剂类和喹诺酮类兽药混合标准品,加入10 mL含0.2%甲酸的 V(乙腈)∶V(水)=80∶20溶液,涡旋振荡混合 10 min后,离心(4000 r/min)10 min,待净化。
净化:取离心后的加标基质的提取液,过PPR柱,收集过柱液后,在45 ℃氮吹条件下吹干。浓缩定容:将过柱液在45 ℃氮吹条件下吹至近干。加入1 mL初始比例流动相进行复溶,用0.22 μm的尼龙滤器过滤后待检测。
空白基质溶液标:取相同质量的样品,不加标准品经过上述提取净化步骤,氮吹后加入等体积β-受体激动剂类和喹诺酮类兽药混合标准品,1 mL初始比例流动相进行复溶,用0.22 μm的尼龙滤器过滤后待检测。
基质加标回收率参照公式(2)计算:
P=[(A2-A1)/A3]×100%
(2)
式中:P为兽残回收率;A2为基质加标样品对应兽残的峰面积;A1为基质空白样品对应兽残的峰面积;A3为空白基质溶液标对应兽残的峰面积。
1.4 HPLC-MS/MS检测条件
1.4.1 磷脂检测条件
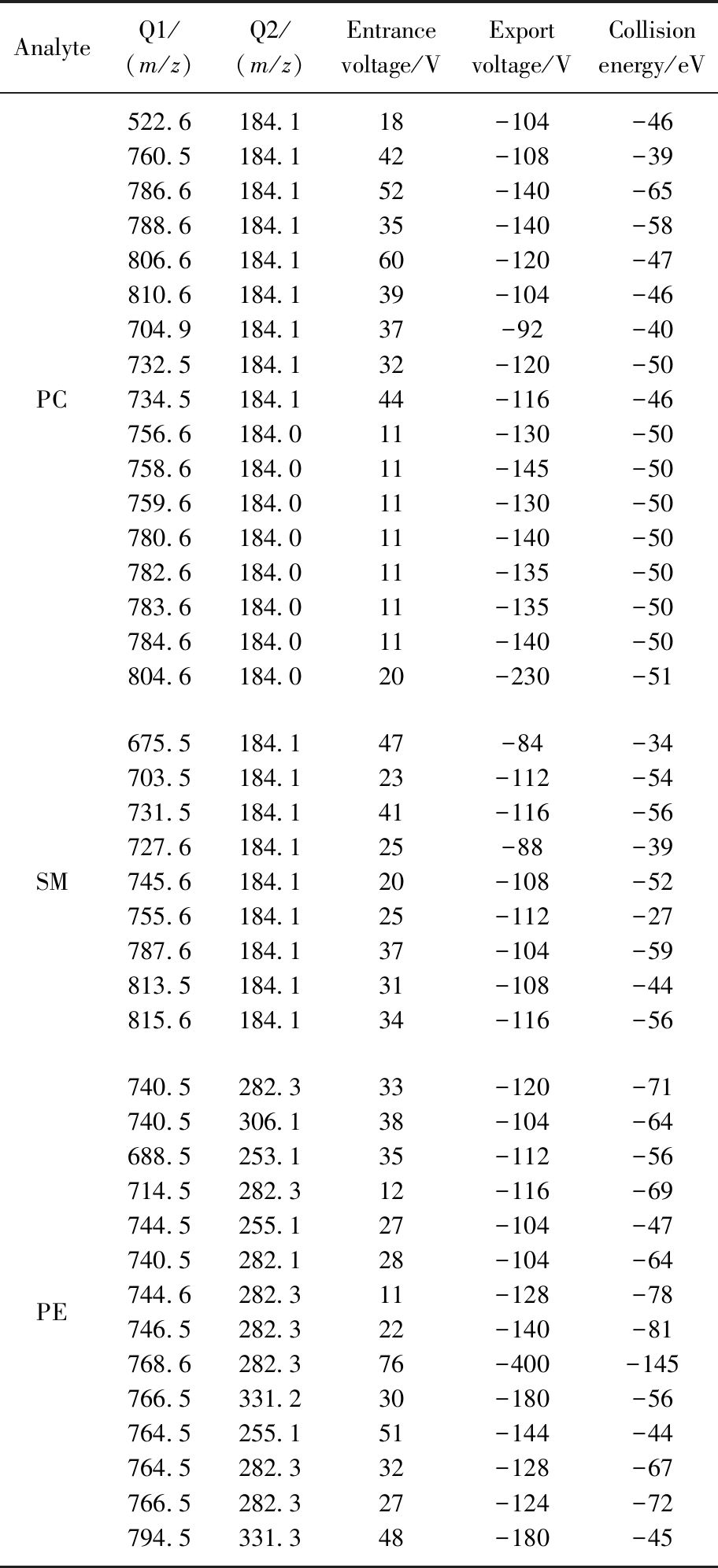
液相色谱条件:进样量:10 μL;Athena C18色谱柱(2.1 mm×50 mm×1.8 μm);柱温:40 ℃;流动相A为V(甲酸)∶V(乙腈)=0.1∶99.9,流动相B为甲醇;流速:0.3 mL/min;梯度条件:0~1 min(V(流动相A)∶V(流动相B)=60∶40),1~5 min(V(流动相A)∶V(流动相B)=40∶60),5~8 min(V(流动相A)∶V(流动相B)=2∶98),8~10 min(V(流动相A)∶V(流动相B)=60∶40);质谱条件:离子源:ESI+;采集方式:MRM;反吹干燥气:60;质谱接口加热温度:320 ℃;雾化气:80;ESI喷雾电压:5500 V;离子源温度:300 ℃。定性离子:神经鞘磷脂(SM)、磷脂酰胆碱(PC)和磷脂酰乙醇胺(PE)3大类,见表1。
表1 SM、PC、PE 3类磷脂的定性、定量离子参数
Tab.1 Qualitative and quantitative ion parameters of three types of phospholipids:SM,PC,and PE
AnalyteQ1/(m/z)Q2/(m/z)Entrance voltage/VExport voltage/VCollision energy/eVPC522.6760.5786.6788.6806.6810.6704.9732.5734.5756.6758.6759.6780.6782.6783.6784.6804.6184.1184.1184.1184.1184.1184.1184.1184.1184.1184.0184.0184.0184.0184.0184.0184.0184.01842523560393732441111111111111120-104-108-140-140-120-104-92-120-116-130-145-130-140-135-135-140-230-46-39-65-58-47-46-40-50-46-50-50-50-50-50-50-50-51SM675.5703.5731.5727.6745.6755.6787.6813.5815.6184.1184.1184.1184.1184.1184.1184.1184.1184.1472341252025373134-84-112-116-88-108-112-104-108-116-34-54-56-39-52-27-59-44-56PE740.5740.5688.5714.5744.5740.5744.6746.5768.6766.5764.5764.5766.5794.5282.3306.1253.1282.3255.1282.1282.3282.3282.3331.2255.1282.3282.3331.33338351227281122763051322748-120-104-112-116-104-104-128-140-400-180-144-128-124-180-71-64-56-69-47-64-78-81-145-56-44-67-72-45
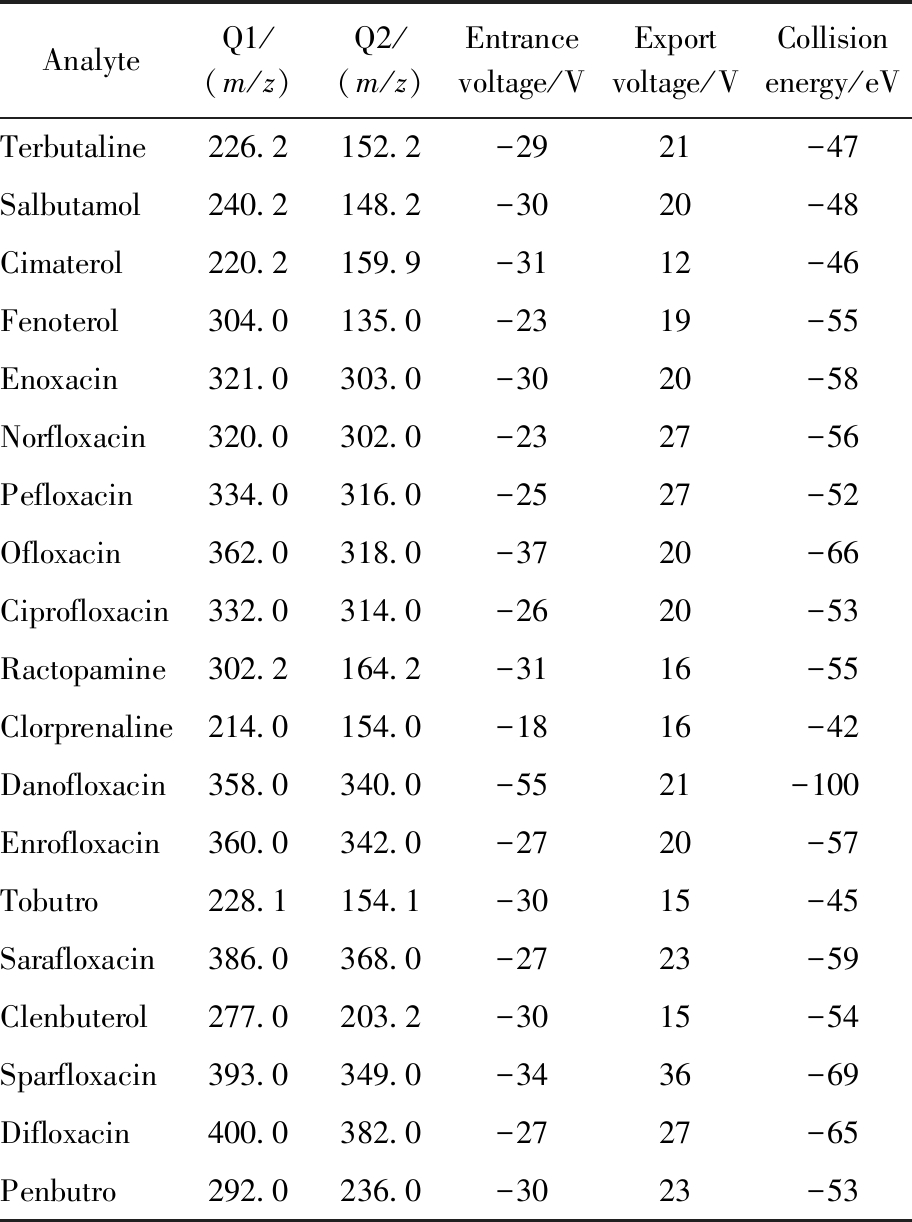
表2 兽残化合物的定性、定量离子参数
Tab.2 Qualitative and quantitative ion parameters of veterinary drug residues
AnalyteQ1/(m/z)Q2/(m/z)Entrance voltage/VExport voltage/VCollision energy/eVTerbutaline226.2152.2-2921-47Salbutamol240.2148.2-3020-48Cimaterol220.2159.9-3112-46Fenoterol304.0135.0-2319-55Enoxacin321.0303.0-3020-58Norfloxacin320.0302.0-2327-56Pefloxacin334.0316.0-2527-52Ofloxacin362.0318.0-3720-66Ciprofloxacin332.0314.0-2620-53Ractopamine302.2164.2-3116-55Clorprenaline214.0154.0-1816-42Danofloxacin358.0340.0-5521-100Enrofloxacin360.0342.0-2720-57Tobutro228.1154.1-3015-45Sarafloxacin386.0368.0-2723-59Clenbuterol277.0203.2-3015-54Sparfloxacin393.0349.0-3436-69Difloxacin400.0382.0-2727-65Penbutro292.0236.0-3023-53
1.4.2 兽残检测条件
液相色谱条件:进样量:10 μL;色谱柱:Acquity UPLC BEH C18色谱柱(2.1 mm×50 mm,1.7 μm);柱温:40 ℃;流动相A:乙腈溶液,流动相B:甲醇,V(甲酸)∶V(5 mmol/L乙酸铵溶液)=0.1∶99.9;流速:0.4 mL/min;梯度条件:0~2.5 min(V(流动相A)∶V(流动相B)=5∶95),2.5~4 min(V(流动相A)∶V(流动相B)=95∶5),4~5 min(V(流动相A)∶V(流动相B)=5∶95)。
质谱条件:离子源:ESI+/ESI-;采集方式:MRM;毛细管电压:3.5 kV;离子源温度:150 ℃;脱溶剂气温度:600 ℃;脱溶剂气流速度:1000 L/h;锥孔气:150 L/h;碰撞其流速:0.15 mL/min。
2 结果与讨论
2.1 硅胶种类对去磷脂性能的影响
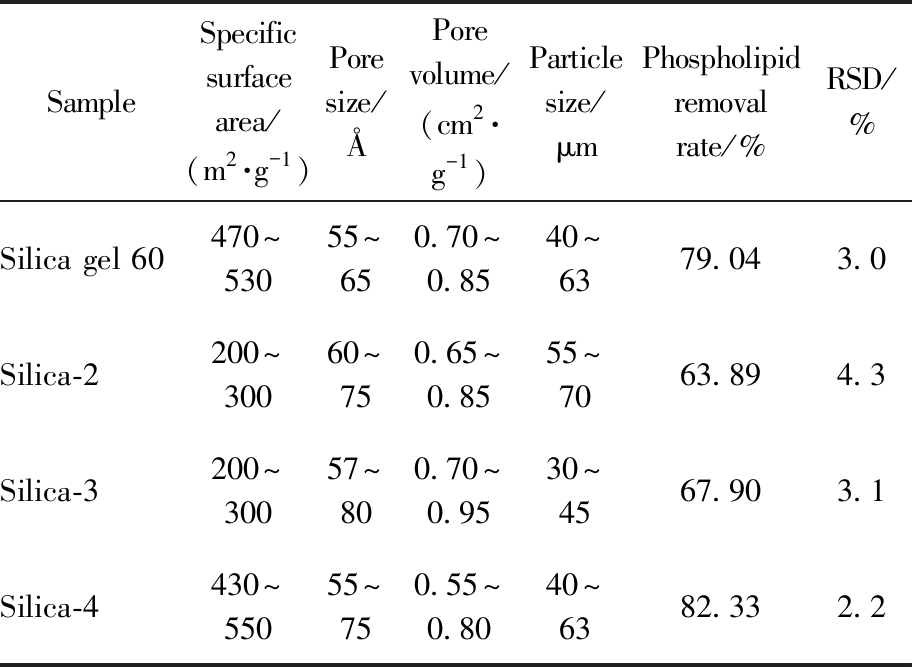
固相萃取是通过目标物与填料的相互作用来实现对目标物的吸附和分离[22]。选取了4种不同的硅胶基球,考察不同物理指标的硅球对磷脂净化效率的影响(测试方法参考1.3.1,制备方法参考1.2.1,以鸡蛋为基质)。由表3可知,硅胶基质的比表面积越大,其与目标物的接触面积越大,活性位点越多,则吸附能力越强,去磷脂效果越好。考虑到硅胶-4的价格更低,综合性能和成本,选择硅胶-4作为进一步的优化实验。
表3 不同硅胶对PPR填料去磷脂率的影响
Tab.3 Effect of silica gel on the phospholipid removal rate of PPR (n=6)
SampleSpecific surface area/(m2·g-1)Pore size/ÅPore volume/(cm2·g-1)Particle size/μmPhospholipid removal rate/%RSD/%Silica gel 60470~53055~650.70~0.8540~6379.043.0Silica-2200~30060~750.65~0.8555~7063.894.3Silica-3200~30057~800.70~0.9530~4567.903.1Silica-4430~55055~750.55~0.8040~6382.332.2
2.2 功能单体种类对去磷脂性能的影响
功能单体是SPE填料的关键组成部分,实验选取正辛基三氯硅烷(n-Octyltrichlorosilane,OTCS)、十二烷基三甲氧基硅烷(n-Dodecyltrimethoxysilane,DTMS)、十六烷基三甲氧基硅烷(Hexadecyltrimethoxysilane,HTMS)、OTS、三十烷基三氯硅烷(Triacontyltrichlorosilane,TTCS)作为功能单体,考察不同功能单体修饰的PPR材料对鸡蛋去磷脂率的影响。通过图1可知,当功能单体为OTS时,材料的去磷脂率最好。这可能是因为磷脂分子的一端由两个脂肪酸链组成,这些脂肪酸链的长度通常在14~24个碳原子之间,最常见的长度是16个碳和18个碳,因此OTS修饰的PPR材料去磷脂率最好。
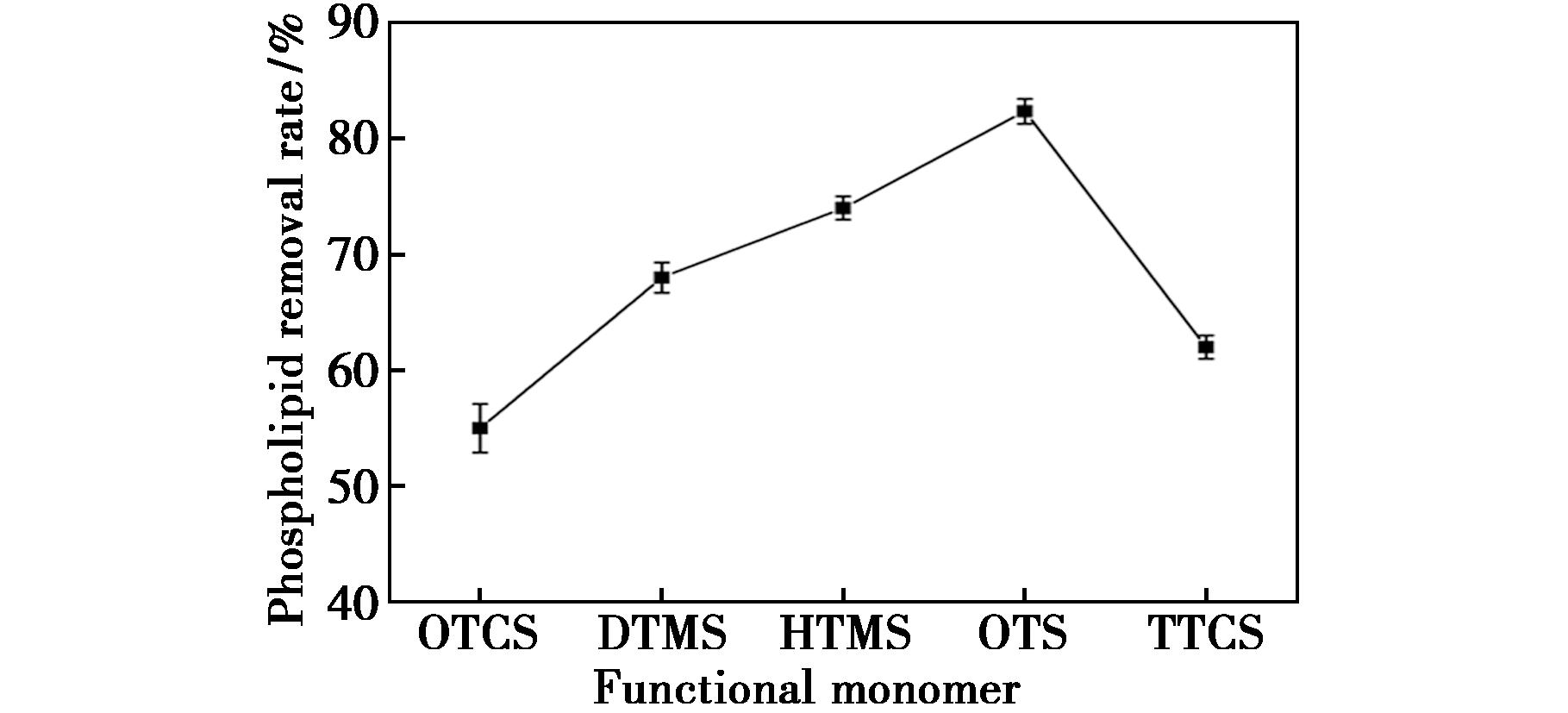
图1 功能单体种类对填料去磷脂率的影响
Fig.1 Influence of functional monomer types on the phospholipid removal rate of filler
2.3 功能单体用量对去磷脂性能的影响
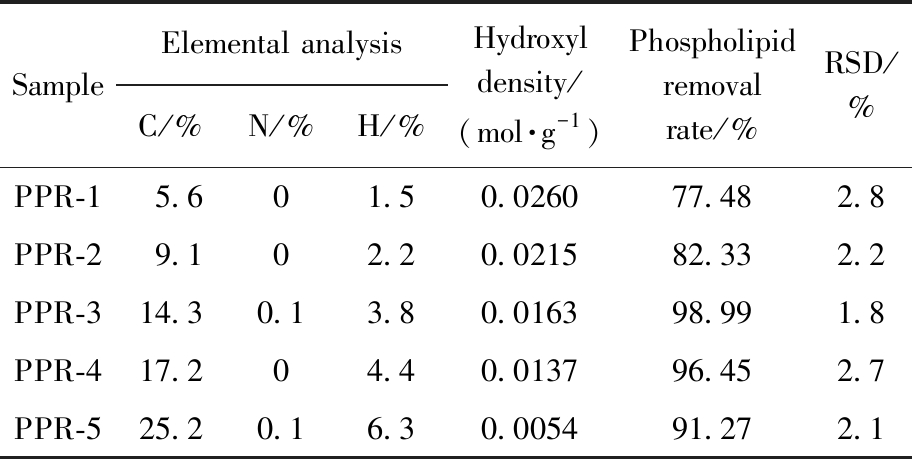
功能单体(OTS)的含量直接影响填料表面的官能团密度,从而影响去磷脂效率。改变OTS用量(5、10、15、20、25 mL)制备了一系列PPR材料。由表4元素分析结果可知,随OTS加入量提高,材料的碳含量升高,表明功能单体OTS已成功键合到硅胶表面。PPR填料在鸡蛋中的磷脂去除能力结果如表4和图2所示。结果表明,随着功能单体用量的增加,去磷脂率呈现出先上升后下降的趋势。其原因在于,对于磷脂的吸附,需要依赖非极性作用力和极性作用力。只有在非极性与极性作用力达到合理平衡时,材料才能对磷脂表现出较理想的选择性与吸附能力。因此,当硅胶表面的碳含量为14.3%,羟值密度在0.0163 mol/g左右时,PPR-3填料的极性与非极性作用力处于较适宜的匹配范围,从而其去磷脂率高达98.99%。综上,选择PPR-3的工艺为最终制备工艺。
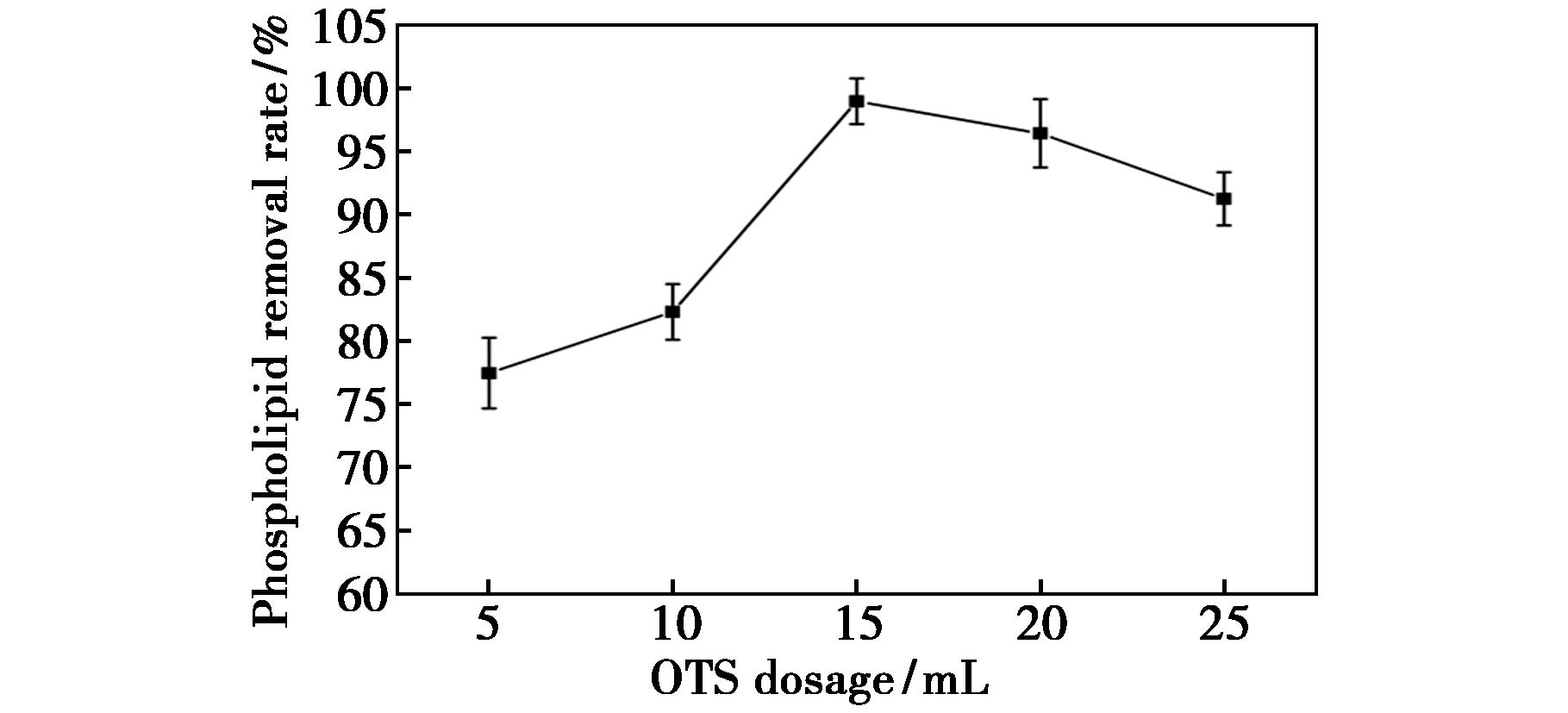
图2 OTS用量对去磷脂率的影响
Fig.2 Effect of OTS dosage on phospholipid removal rate
表4 元素分析、羟值密度及去除磷脂率
Tab.4 Elemental analysis,hydroxyl density,and phospholipid removal rate (n=6)
SampleElemental analysisC/%N/%H/%Hydroxyl density/(mol·g-1)Phospholipid removal rate/%RSD/%PPR-15.601.50.026077.482.8PPR-29.102.20.021582.332.2PPR-314.30.13.80.016398.991.8PPR-417.204.40.013796.452.7PPR-525.20.16.30.005491.272.1
2.4 PPR材料的表征
2.4.1 红外光谱表征
通过FT-IR对OTS、裸硅胶、PPR填料进行表征。图3曲线1为OTS的红外谱图,2923、2853 cm-1处的两个峰分别对应于—CH2—基团的不对称和对称伸缩振动,1464 cm-1处对应—CH2—基团的弯曲振动;曲线2为裸硅胶的红外谱图,其中3600~3250 cm-1为硅胶表面Si—OH的伸缩振动峰,1645 cm-1处为Si—OH的弯曲振动峰,1100 cm-1处为Si—O—Si的反对称伸缩振动;曲线3为PPR的红外谱图,与裸硅胶相比,在2935、2861 cm-1两处出现—CH2—基团的不对称和对称伸缩振动,1470 cm-1处出现—CH2—基团的弯曲振动峰,表明OTS成功修饰到硅胶表面。
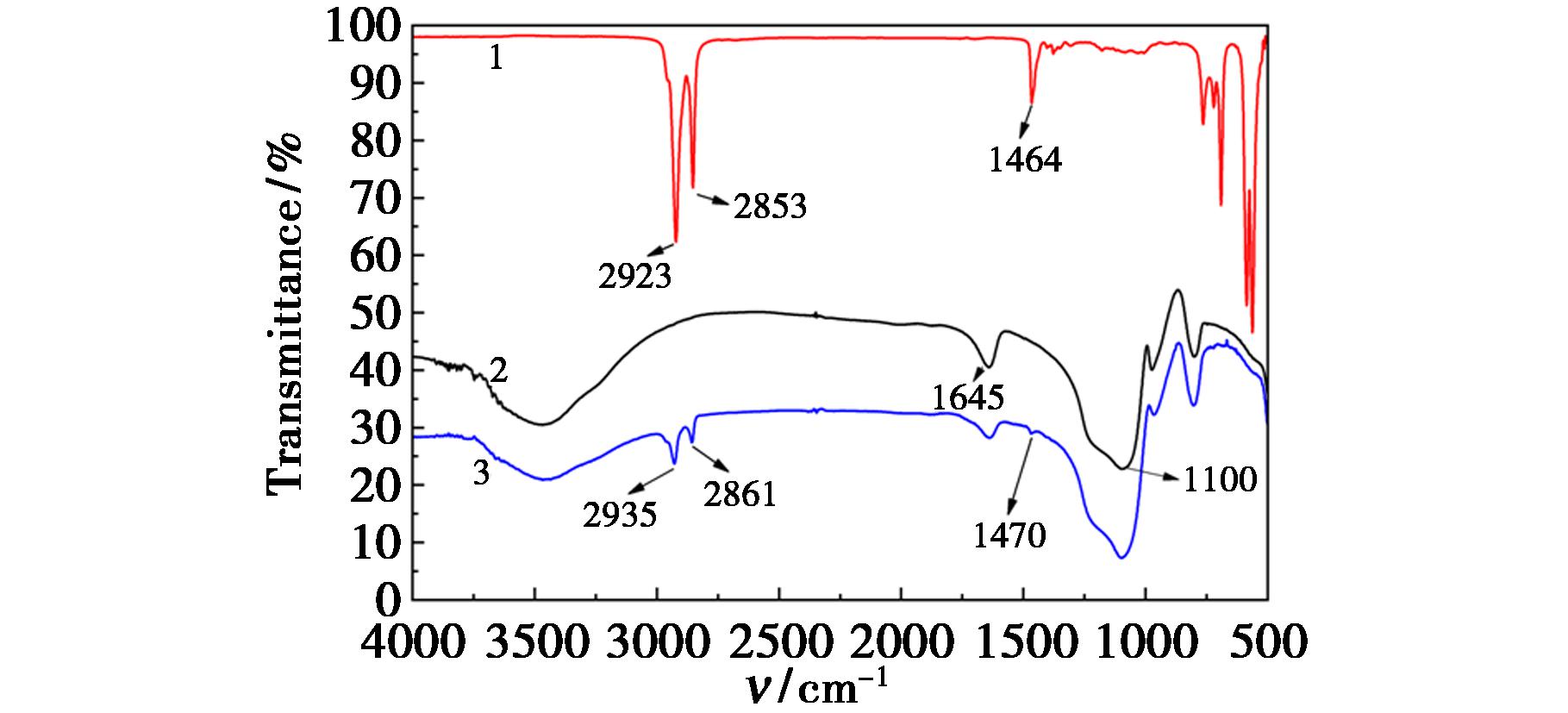
1.OTS;2.硅胶;3.PPR
图3 红外谱图
Fig.3 Infrared spectrum
2.4.2 扫描电子显微镜(SEM)、粒径分析
对OTS修饰前后的裸硅胶与PPR填料进行表面形貌分析(图4),可以看出,硅胶在经OTS接枝改性前后,其整体表面结构变化并不明显。两者均呈现出边缘轮廓略不规则、表面略显粗糙的特征,此外,两类材料的粒径均集中在50~70 μm区间内,分布较为集中,表明改性过程并未造成颗粒破碎或明显的聚集。图5显示PPR材料的粒径呈单峰分布,均一性较好,有利于前处理操作时的过柱流速稳定。

a.硅胶;b.PPR
图4 SEM图
Fig.4 SEM images
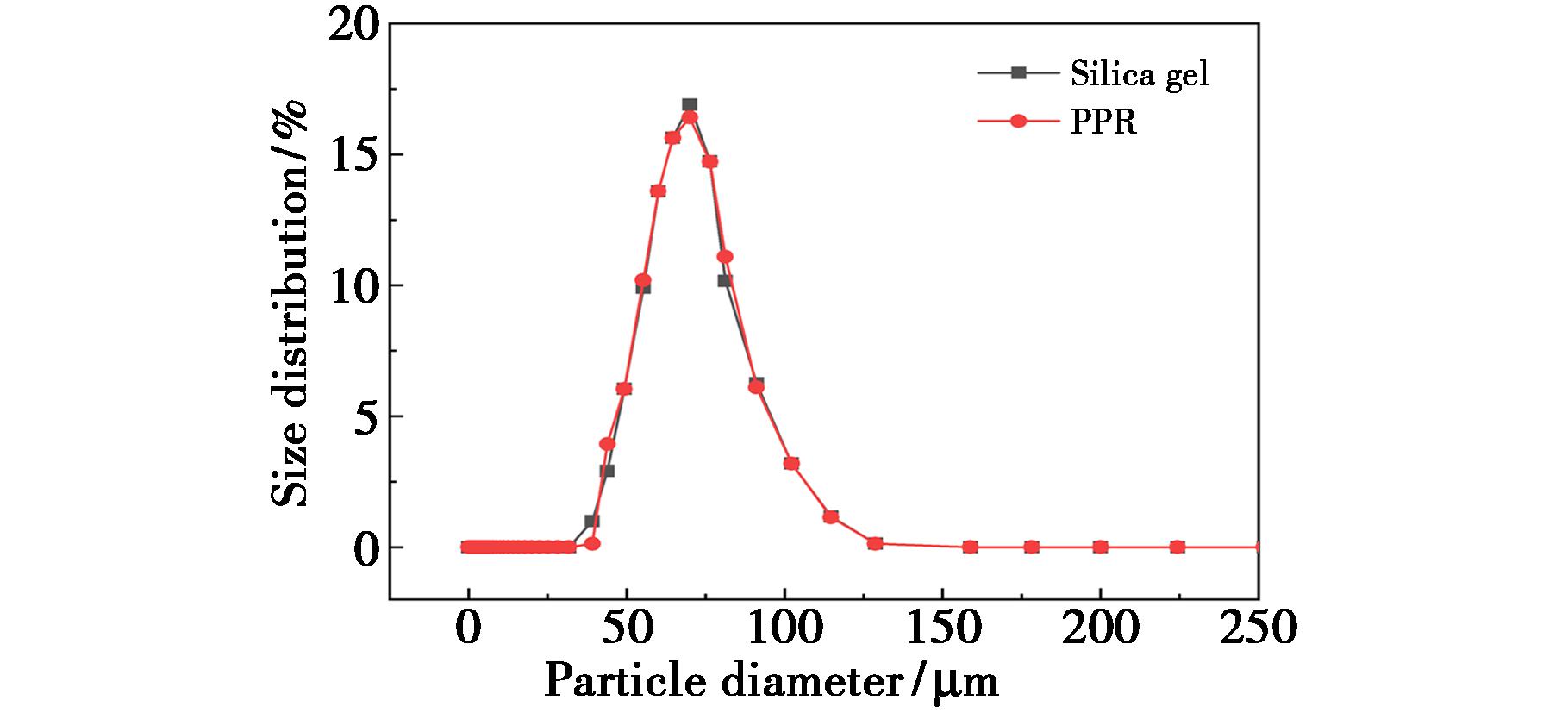
图5 硅胶和PPR材料的粒径分布
Fig.5 Particle size distribution of Silica gel and PPR
2.4.3 N2等温吸附-脱附分析
通过N2等温吸附-脱附曲线对OTS修饰前后的材料进行分析。如图6a所示,裸硅胶和PPR材料的N2等温吸附-脱附曲线类似,吸附量随相对压力增加而增加,当P/PO在0.5~0.9范围内,材料对N2的吸附量增加,出现明显的H1滞后环,表明材料中存在介孔结构[23]。图6b的孔径分布表明,PPR材料相对裸硅胶,孔体积、孔径略有降低,这是因为硅胶表面修饰OTS后,OTS占据了部分孔径内的空间,造成孔体积、孔径的下降。
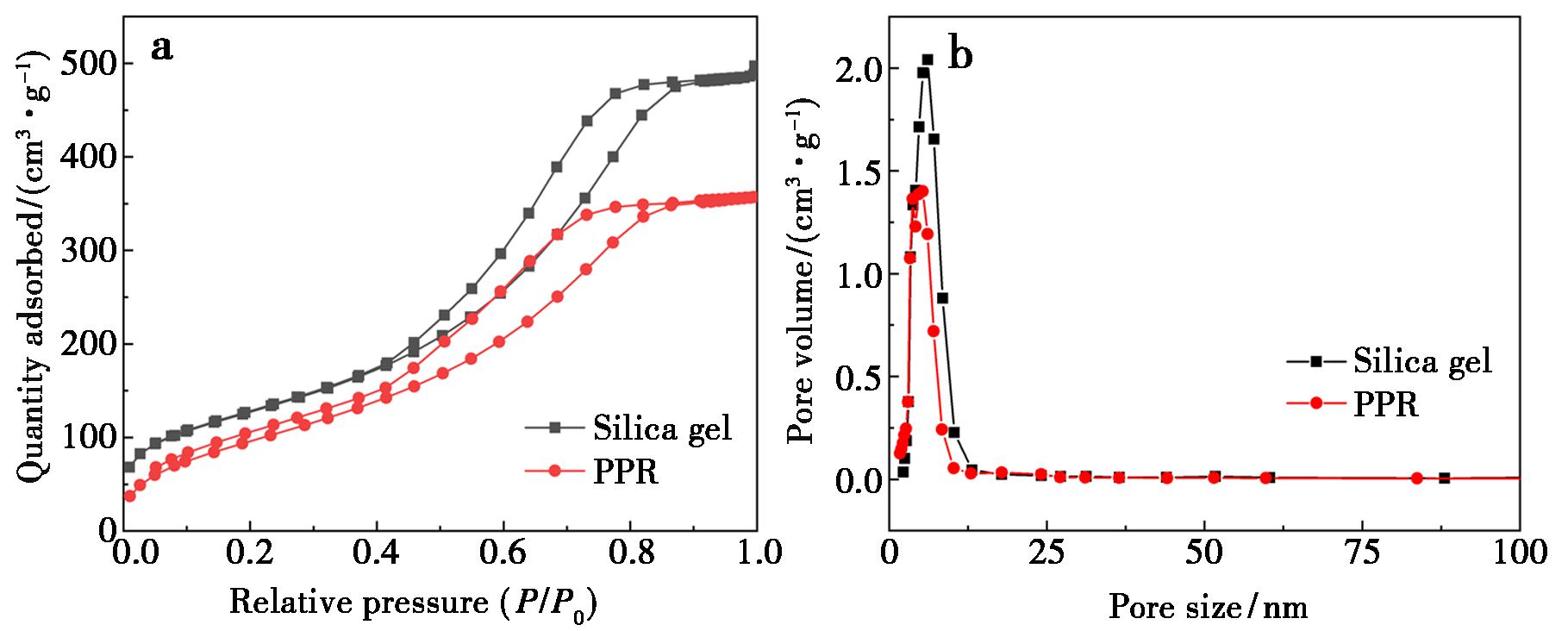
图6 a.N2等温吸附-脱附曲线;b.孔径分布曲线
Fig.6 a.N2 isothermal adsorption-desorption curve;b.Pore size distribution curve
2.5 PPR填料的去磷脂应用性能评价
PPR填料对鸡蛋中的磷脂去除效果如图7所示。可以看到,未经净化时,磷脂峰信号明显偏高。经PPR柱和PRiME HLB柱处理后,磷脂峰显著降低。结合表5可知,PPR小柱对鸡蛋、全脂牛奶、鸡肉、猪肉4种食品基质中的磷脂净化率为98.58%~99.91%,PRiME HLB柱磷脂去除率为94.09%~99.64%,两者在去磷脂性能上相当。
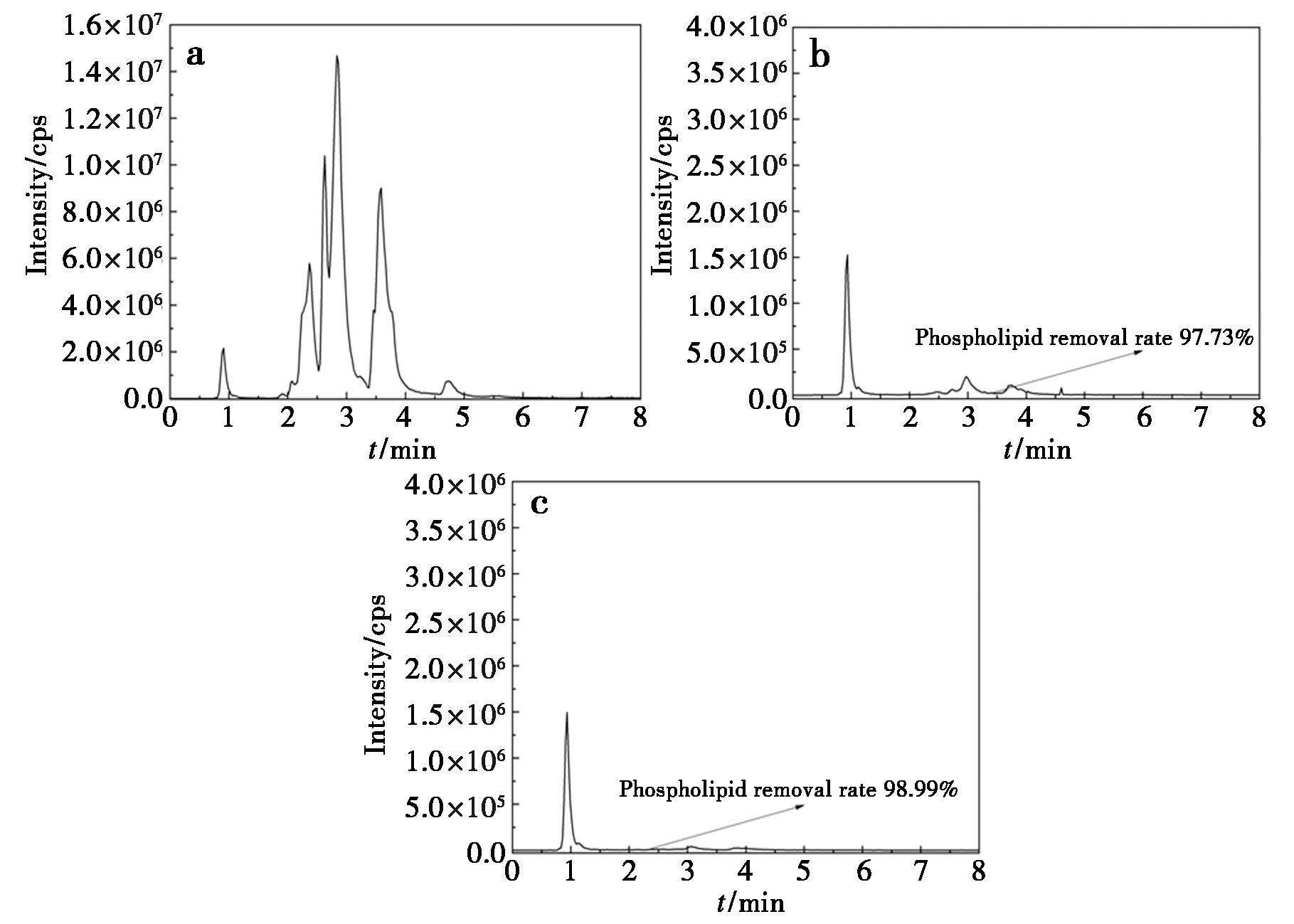
a.未经SPE柱净化;b.PRiME HLB柱净化;c.PPR柱净化
图7 色谱图
Fig.7 Chromatograms
表5 磷脂净化率
Tab.5 Purification rates of phospholipids (n=6)
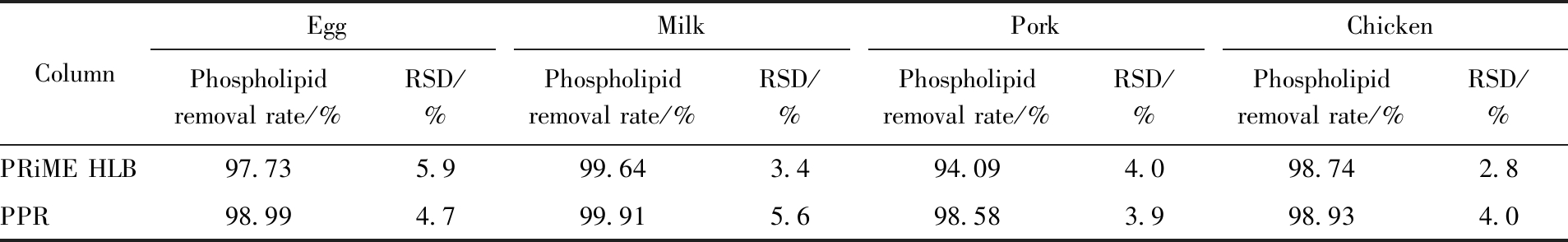
ColumnEggMilkPorkChickenPhospholipid removal rate/%RSD/%Phospholipid removal rate/%RSD/%Phospholipid removal rate/%RSD/%Phospholipid removal rate/%RSD/%PRiME HLB97.735.999.643.494.094.098.742.8PPR98.994.799.915.698.583.998.934.0
2.6 兽残分析方法的评价
PPR柱去除基质中的磷脂类杂质后,还需要考察兽残加标回收率能否满足相关法规要求,防止PPR柱对兽残检测产生干扰。
2.6.1 定量限及线性考察
配制10、50、100、200、300、500 ng/mL共6个质量浓度水平的兽残标准曲线浓度点,以目标物浓度为横坐标,响应值(峰面积)为纵坐标,绘制标准曲线,进行线性回归分析。结果如表6所示,在10~500 ng/mL的浓度范围内19种兽药残留具有良好的线性关系,线性相关系数R2>0.999。
表6 线性回归方程及线性范围
Tab.6 Linear regression equations and linear ranges (n=6)
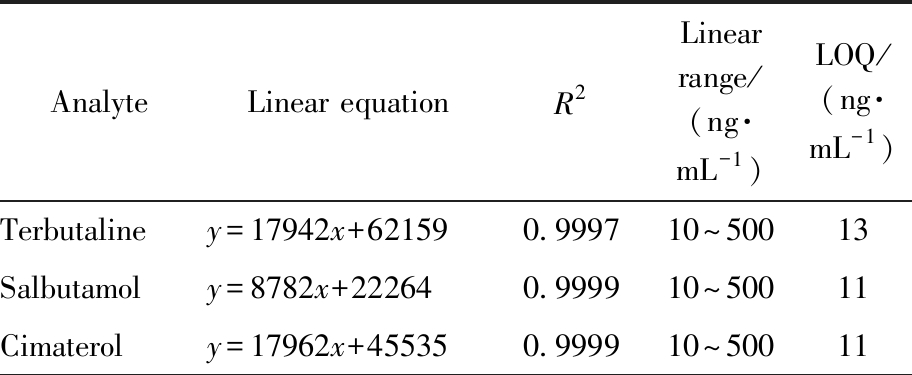
AnalyteLinear equationR2Linear range/(ng·mL-1)LOQ/(ng·mL-1)Terbutaliney=17942x+621590.999710~50013Salbutamoly=8782x+222640.999910~50011Cimateroly=17962x+455350.999910~50011
续表
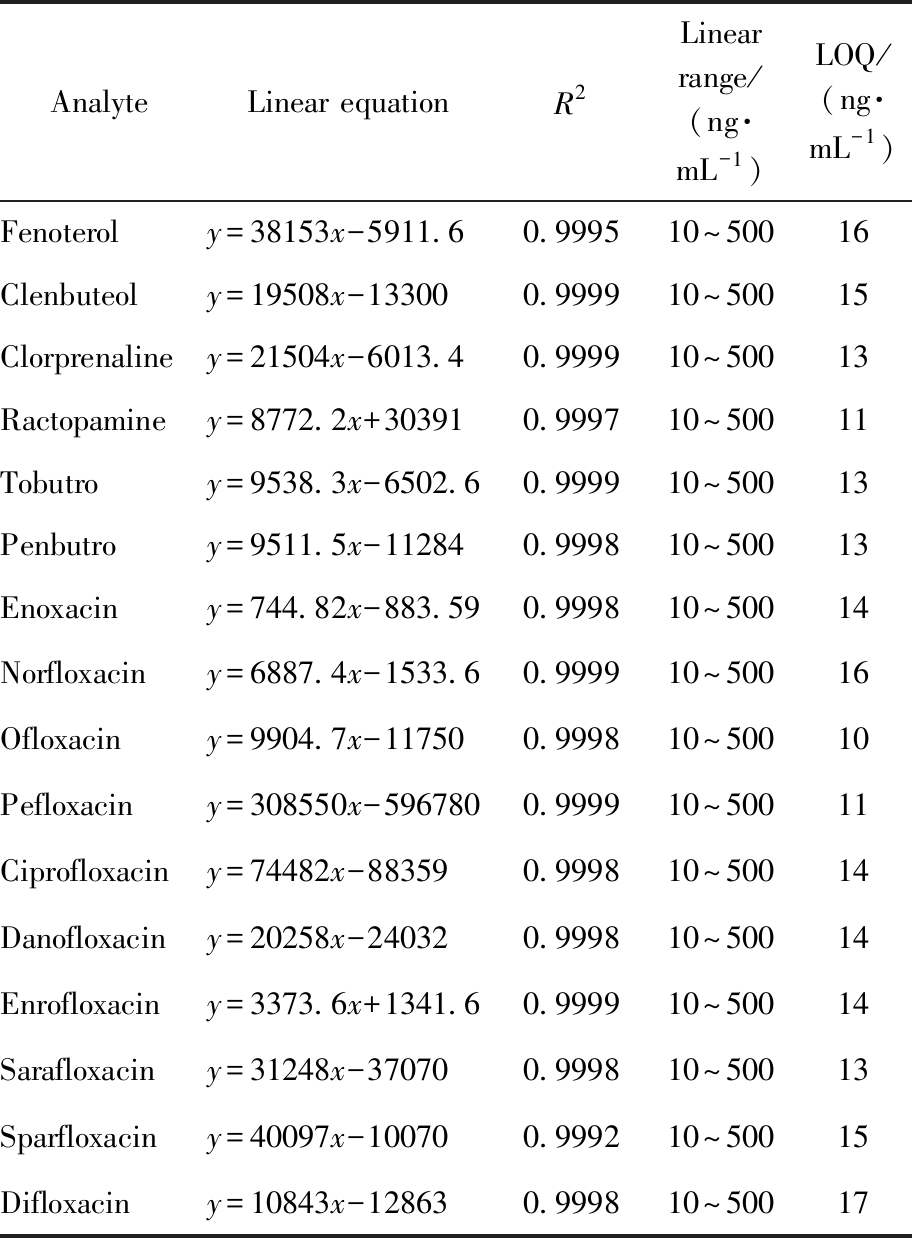
AnalyteLinear equationR2Linear range/(ng·mL-1)LOQ/(ng·mL-1)Fenoteroly=38153x-5911.60.999510~50016Clenbuteoly=19508x-133000.999910~50015Clorprenaliney=21504x-6013.40.999910~50013Ractopaminey=8772.2x+303910.999710~50011Tobutroy=9538.3x-6502.60.999910~50013Penbutroy=9511.5x-112840.999810~50013Enoxaciny=744.82x-883.590.999810~50014Norfloxaciny=6887.4x-1533.60.999910~50016Ofloxaciny=9904.7x-117500.999810~50010Pefloxaciny=308550x-5967800.999910~50011Ciprofloxaciny=74482x-883590.999810~50014Danofloxaciny=20258x-240320.999810~50014Enrofloxaciny=3373.6x+1341.60.999910~50014Sarafloxaciny=31248x-370700.999810~50013Sparfloxaciny=40097x-100700.999210~50015Difloxaciny=10843x-128630.999810~50017
2.6.2 基质效应的考察
采用样本处理后加入法考察基质效应。基质效应的计算方法为:空白基质溶液标与纯溶剂标响应值的差/纯溶剂标响应值。若基质效应在±20%之间,则表明基质效应不影响定量结果的准确性[24]。
基于上述方法,PPR和PRiME HLB柱在鸡蛋中的基质效应,结果见表7。结果显示两款SPE柱对鸡蛋中的19种β-受体激动剂和喹诺酮类目标物的基质效应均在±20%以内,表明该前处理方法无明显基质效应。
表7 各化合物的基质效应
Tab.7 Matrix effects of each compound (n=6)
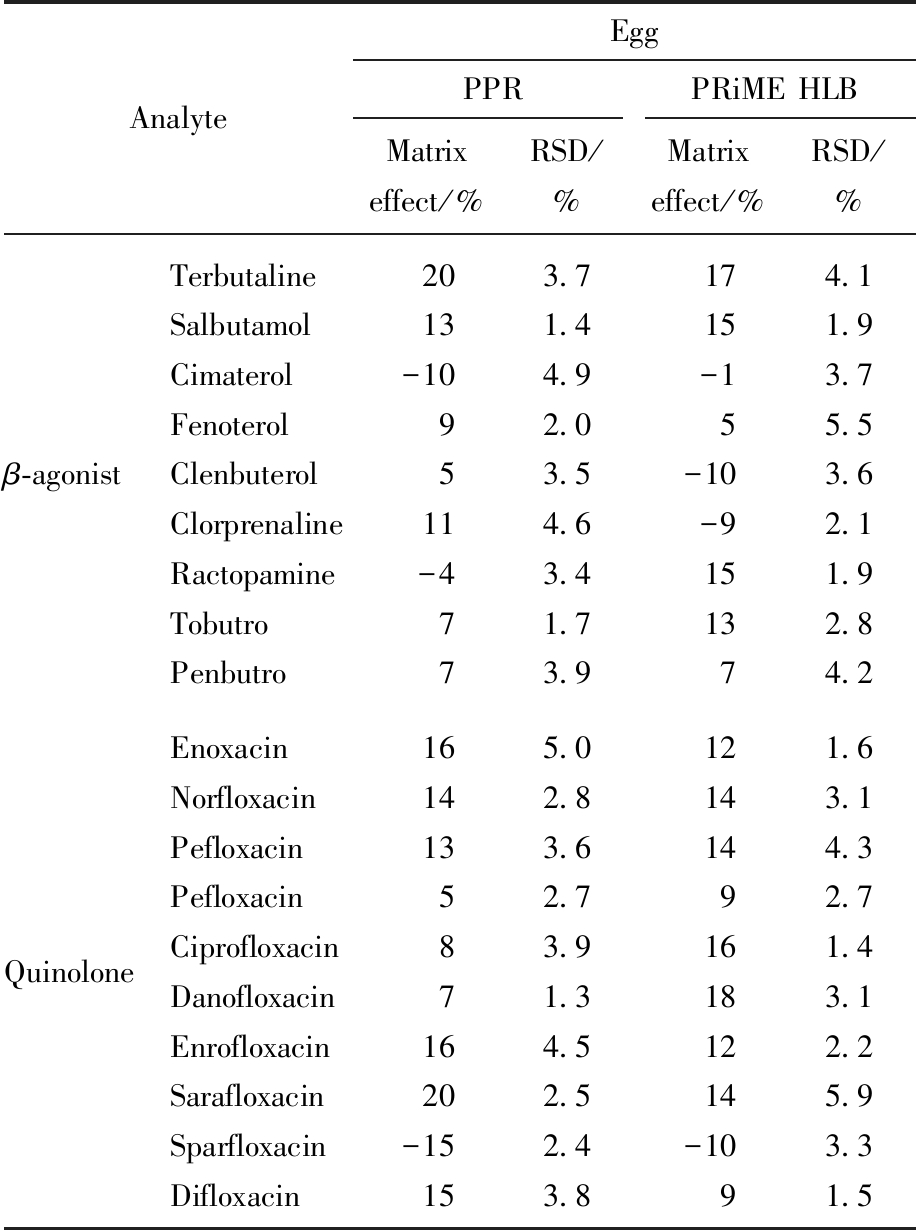
AnalyteEggPPRPRiME HLBMatrix effect/%RSD/%Matrix effect/%RSD/%β-agonistTerbutalineSalbutamolCimaterolFenoterolClenbuterolClorprenalineRactopamineTobutroPenbutro2013-109511-4773.71.44.92.03.54.63.41.73.91715-15-10-9151374.11.93.75.53.62.11.92.84.2QuinoloneEnoxacinNorfloxacinPefloxacinPefloxacinCiprofloxacinDanofloxacinEnrofloxacinSarafloxacinSparfloxacinDifloxacin1614135871620-15155.02.83.62.73.91.34.52.52.43.8121414916181214-1091.63.14.32.71.43.12.25.93.31.5
2.6.3 加标回收率的考察
设置低、中、高3个浓度水平考察PPR柱对19种兽残的加标回收率(加标浓度为50、200、500 ng/mL),并与PRiME HLB柱对比。结果表明(表8),PPR柱对鸡蛋基质中19种β-受体激动剂和喹诺酮类兽残加标回收率为81.0%~102.3%,相对标准偏差为1.4%~8.2%;PRiME HLB柱的加标回收率为80.5%~104.3%,相对标准偏差在3.1%~9.4%,证明PPR柱可与商品化去磷脂柱对标。
表8 19种β-受体激动剂和喹诺酮类兽残的回收率
Tab.8 Recovery rates of 19 β-receptor agonists and quinolone residues (n=6)
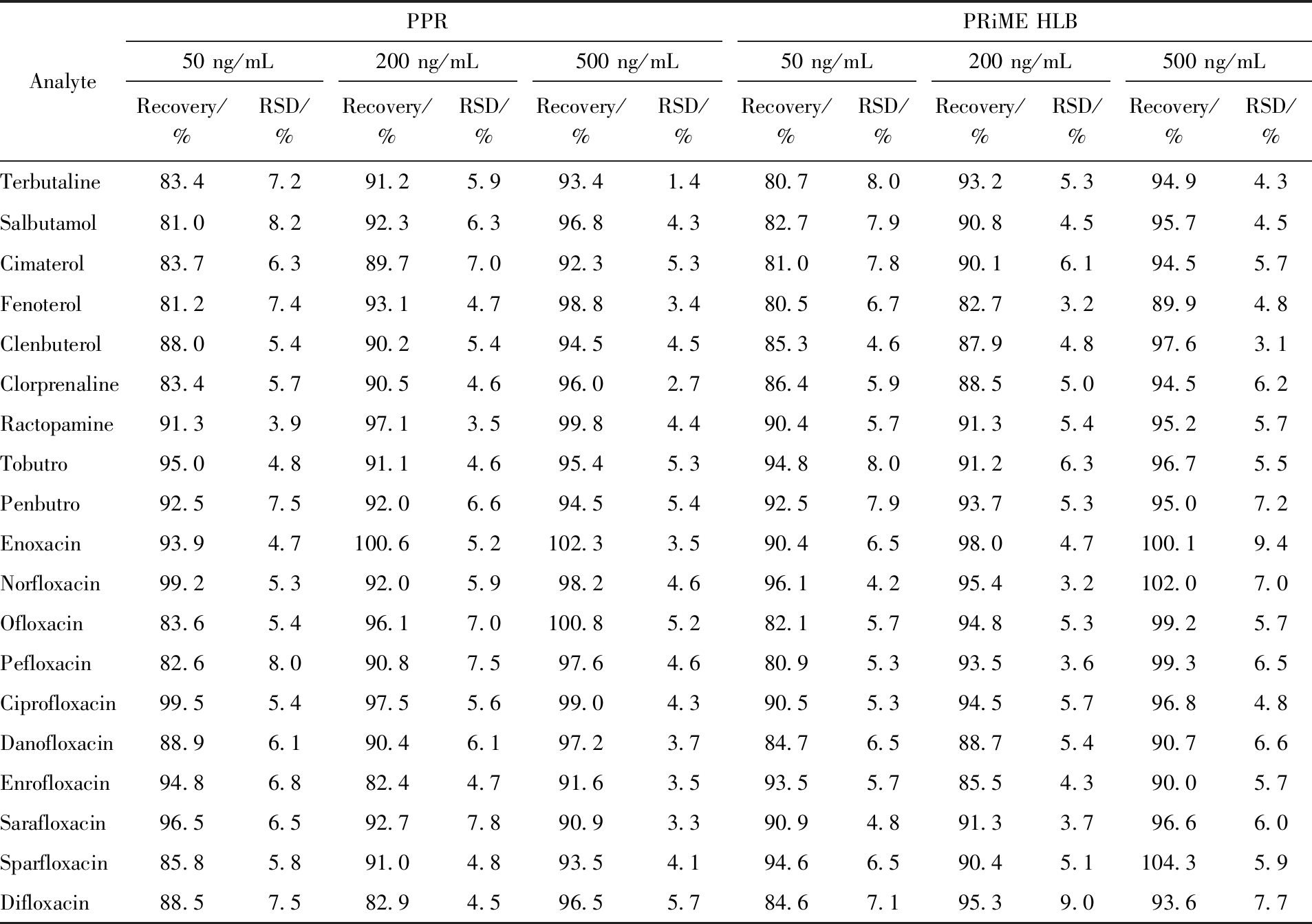
AnalytePPRPRiME HLB50 ng/mL200 ng/mL500 ng/mL50 ng/mL200 ng/mL500 ng/mLRecovery/%RSD/%Recovery/%RSD/%Recovery/%RSD/%Recovery/%RSD/%Recovery/%RSD/%Recovery/%RSD/%Terbutaline83.47.291.25.993.41.480.78.093.25.394.94.3Salbutamol81.08.292.36.396.84.382.77.990.84.595.74.5Cimaterol83.76.389.77.092.35.381.07.890.16.194.55.7Fenoterol81.27.493.14.798.83.480.56.782.73.289.94.8Clenbuterol88.05.490.25.494.54.585.34.687.94.897.63.1Clorprenaline83.45.790.54.696.02.786.45.988.55.094.56.2Ractopamine91.33.997.13.599.84.490.45.791.35.495.25.7Tobutro95.04.891.14.695.45.394.88.091.26.396.75.5Penbutro92.57.592.06.694.55.492.57.993.75.395.07.2Enoxacin93.94.7100.65.2102.33.590.46.598.04.7100.19.4Norfloxacin99.25.392.05.998.24.696.14.295.43.2102.07.0Ofloxacin83.65.496.17.0100.85.282.15.794.85.399.25.7Pefloxacin82.68.090.87.597.64.680.95.393.53.699.36.5Ciprofloxacin99.55.497.55.699.04.390.55.394.55.796.84.8Danofloxacin88.96.190.46.197.23.784.76.588.75.490.76.6Enrofloxacin94.86.882.44.791.63.593.55.785.54.390.05.7Sarafloxacin96.56.592.77.890.93.390.94.891.33.796.66.0Sparfloxacin85.85.891.04.893.54.194.66.590.45.1104.35.9Difloxacin88.57.582.94.596.55.784.67.195.39.093.67.7
3 结论
本文制备了一种双亲性去磷脂材料,通过极性与非极性作用力对磷脂类目标物产生特异性吸附。工艺优化后,PPR材料可对鸡蛋、全脂牛奶、鸡肉、猪肉4种基质的磷脂净化率达到98.58%~99.91%;对鸡蛋中19种β-受体激动剂和喹诺酮类兽残加标回收率及相对标准偏差均与市场进口产品性能相当。易制备、低成本的PPR填料在兽药残留的低成本、精准、快速检测中有着广泛的应用潜力。
[1]Chen X Y,Wu T,Pan Y H,Liu Y,Liu Y Q,Li A J.Food Ind.,2024,45(11):305-307.陈秀英,吴桐,潘艳慧,刘瑜,刘宇奇,李爱军.食品工业,2024,45(11):305-307.
[2]Chen B,Guan B B,Shi M,Jiang L H,He X C,Chen Y.Food Ind.,2021,42(3):322-327.陈彬,管彬彬,石敏,蒋林惠,何薛纯,陈煜.食品工业,2021,42(3):322-327.
[3]Liu C,Jing Z,Song Y H.Food Drug,2025,27(2):180-185.刘超,景赞,宋宇航.食品与药品,2025,27(2):180-185.
[4]Li K Q,Xiao Z G,Luo X Z.China Food Saf.Mag.,2024,(18):87-89;93.李夸巧,肖植国,罗小珍.食品安全导刊,2024,(18):87-89;93.
[5]Liu C,Li J J,Wu X Y,Chen Y Q,Shi P Y,Song J,Dai Q.Food Sci.,2024,45(4):289-299.
[6]Ruan Q Y,Jin S Y.Modern Food Sci.Technol.,2025,(4):200-203.阮乔楹,金少月.现代食品,2025,(4):200-203.
[7]GB 29692—2013.Determination of Quinolone Drug Residues in Milk-High Performance Liquid Chromatography,2013-09-16.GB 29692—2013.牛奶中喹诺酮类药物多残留的测定 高效液相色谱法,2013-09-16.
[8]GB/T 21312—2007.Determination of 14 Quinolone Residues in Animal Derived Foods-LC-MS/MS Method,2007-10-29.GB/T 21312—2007.动物源性食品中14种喹诺酮药物残留检测方法 液相色谱-质谱/质谱法,2007-10-29.
[9]Yan F L,Li Y Z.J.Food Saf.Qual.,2024,15(24):51-56.颜方亮,李玉珍.食品安全质量检测学报,2024,15(24):51-56.
[10]Liu J,Li L,Li L,Wu Z S,Jing X.Chin.J.Anal.Lab.,2024,43(8):1094-1101.刘瑾,李利,李莉,吴祖森,荆旭.分析试验室,2024,43(8):1094-1101.
[11]Deng Y X,Wu H Y,Xu X Z,Zhao H H,Tan Z J,Zhen G C.Food Sci.,2025,46(1):218-226.
[12]Rudt E,Faist C,Schwantes V,Konrad N,Wiedmaier-czerny N,Lehnert K,Topman-rakover S,Brill A,Burdman S,Hayouka Z,Vetter W,Hayen H.Anal.Bioanal.Chem.,2024,416(25):5513-5525.
[13]Wu K,Wu Y T,Zhao J,Zhou Y B.Phys.Test.Chem.Anal.Part B Chem.Anal.,2024,60(1):60-66.吴坤,吴玉田,赵君,周贻兵.理化检验-化学分册,2024,60(1):60-66.
[14]Wu S T,Schoener D,Jemal M.Rapid Commun.Mass Spectrom.,2008,22(18):2873-2881.
[15]Takeda H,Takeuchi M,Hasegawa M,Miyamoto J,Tsugawa H.Anal.Chem.,2024,96(43):17065-17070.
[16]ZL202010769607.1.Zhao Q,Li J,Wang S M,Zhou M.2022-06-24.ZL202010769607.1.赵琪,李健,王诗淼,周沫.2022-06-24.
[17]He X Y,Han R,Li G Z,Wang Z Z,Chen G,Gu L H.Acta Materiae Compositae Sinica,2022,39(2):544-558.何晓英,韩锐,李光照,王中最,陈刚,古良鸿.复合材料学报,2022,39(2):544-558.
[18]He C,Li J,Li Y,Wang B Y,Liu J W,Wu K.Food Ind.,2024,45(11):43-49.何冲,李俭,李媛,王博宇,刘家玮,吴坤.食品工业,2024,45(11):43-49.
[19]Ten-doménech I,Martínez-pérez-cejuela H,Lerma-garcía M J,Simo-alfonso E F,Herrero-martinez J M.Microchimica Acta,2017,184(9):3389-3397.
[20]Liu L Y.Research on Phospholipid Removal Based on Polyanion Metal Ions and Its Application in Bioanalysis.Changsha:Central South University,2023.柳兰玉.基于聚阴离子—金属离子的磷脂去除研究及其在生物分析中的应用.长沙:中南大学,2023.
[21]Dong W Q.Prediction Models for Adsorption Capacity of Metal Oxide Nanoparticles for Lipids.Dalian:Dalian University of Technology,2022.董文琪.纳米金属氧化物对脂质吸附能力的定量预测模型.大连:大连理工大学,2022.
[22]Lou X Y.Study on Modification and Application of New Hydrophilic-Lipophilic Composite Solid Phase Extraction Packing.Tianjin:Tianjin University of Technology,2022.娄鑫玉.新型亲水—亲油复合型固相萃取填料的改性及其应用研究.天津:天津理工大学,2022.
[23]Toncón-leal C F,Villarroel-rocha J,Silva M T P,Braga T P,Sapag K.Adsorption,2021,27(7):1109-1122.
[24]Feng Y Y,Tian Y,Yin L H,Ning B M.Chin.J.New Drugs,2024,33(24):2656-2664.冯媛媛,田冶,尹利辉,宁保明.中国新药杂志,2024,33(24):2656-2664.