由病原微生物引起的传染性疾病至今仍是全球公共卫生领域面临的重大挑战。尽管抗生素(如大环内酯类、氨基糖苷类等)的发现与广泛应用曾有效控制了感染性疾病的传播,但长期过度使用导致细菌通过质粒水平转移、外排泵过表达、药物靶点修饰及细胞壁通透性改变等多种机制产生耐药性,致使传统抗生素的临床效能日益下降[1-3]。与此同时,新型抗生素的研发面临周期长、投入高及经济效益低等多重制约,难以跟上耐药菌的快速演变。因此,开发不依赖于传统作用机制、能够有效克服现有耐药屏障的新型杀菌材料,已成为抗感染研究领域的迫切需求[4,5]。
银纳米颗粒(Ag NPs)作为一种广谱抗菌剂,因其良好的生物相容性、缓释特性及对多种病原微生物(包括革兰氏阳性菌、阴性菌、耐药菌和真菌等)的强大杀伤能力而备受关注。其抗菌机制主要依赖于在生理环境中持续释放的Ag+与活性氧(ROS)的协同作用:Ag+能够多靶点破坏细胞膜完整性并干扰代谢过程,而ROS则进一步引起蛋白质、脂质及核酸的氧化损伤,共同导致微生物死亡[6,7]。理论上,粒径<6 nm的Ag NPs因具有更高的比表面积与反应活性,可进一步增强杀菌效果,并有望通过肾小球滤过实现体内快速清除[8]。然而,超小尺寸Ag NPs易发生团聚,不仅会导致活性下降,还可能因体内蓄积引发潜在的银离子或重金属毒性。因此,如何有效维持其分散性与稳定性,仍是当前研究的关键难点。
铁氧体纳米材料因其良好的生物相容性、可降解性及多模式抗菌潜力而被视为理想的载体候选。其表面富含的Fe2+等活性位点可赋予材料类酶催化性能,在有氧介质中可生成强氧化性羟基自由基(·OH),破坏细菌结构与生物膜[8,9]。已有研究表明,通过引入Cu2+等掺杂金属构建复合铁氧体(如CuFe2O4),可利用其较高的还原电势促进Fe3+/Fe2+循环,显著提升·OH的生成效率,从而增强杀菌性能[10]。基于此,将Ag NPs与铜掺杂铁氧体进行复合,理论上可实现性能的协同增强:一方面,铁氧体基底可作为载体有效抑制Ag NPs的团聚,提高其结构稳定性与生物安全性;另一方面,两者之间的电子耦合效应有望促进界面电子转移,共同增强ROS的生成能力,从而实现对广谱细菌及耐药菌的高效协同杀伤。然而,目前关于Ag NPs与Cu掺杂铁氧体复合材料在抗菌领域的系统研究仍较为缺乏,其协同增强机制尚待深入探索。
为此,本研究以CuFe2O4为载体,通过表面氨基化修饰及吸附策略将超小粒径Ag NPs均匀负载于其表面,成功构建了CuFe2O4@Ag纳米复合材料。利用TEM、XPS、EDS及XRD等表征手段系统分析了材料的微观形貌、元素组成与晶体结构;并以大肠杆菌(E.coli)、金黄色葡萄球菌(S.aureus)及耐甲氧西林金黄色葡萄球菌(MRSA)为对象,系统评价了该复合材料的杀菌性能及其作用机制。结果表明,CuFe2O4@Ag具备显著的广谱杀菌能力,可通过释放金属离子与ROS协同破坏细菌细胞壁结构,导致内容物外泄,最终引发细菌死亡。该复合材料在医疗器械表面防护及抗感染材料领域展现出重要的潜在应用价值。
1 实验部分
1.1 主要仪器与试剂
Glacios 2 Cryo-TEM型透射电子显微镜(TEM)、Thermo Kalpha型X射线光电子能谱仪(XPS)(美国赛默飞世尔科技公司);Quantax75型能量色散X射线光谱仪(EDS,德国布鲁克纳米公司);TK-XRD-201型X射线衍射仪(XRD,中国北京泰坤工业设备有限公司);EPR200M型电子顺磁共振波谱仪(EPR,中国国仪量子技术(合肥)股份有限公司);Zetasizer Nano Zs90型Zeta电位分析仪(英国马尔文帕纳科公司);Sigma 300型扫描电子显微镜(SEM,德国卡尔蔡司公司);IX73型荧光倒置显微镜(日本奥林巴斯公司)。
氯化铁(FeCl3,99%)、氯化铜(CuCl2,99%)、3-氨丙基三甲氧基硅烷(APTMS,98.3%)、柠檬酸钠(Na3C6H5O7,99%)、硝酸银(AgNO3,99.8%)、硼氢化钠(NaBH4,99%)、氯化钠(NaCl,99.3%)、碘化丙啶(PI,99%)、乙二醇(DEG,98%)、异丙醇(IPA,99%)、无水乙醇(CH3CH2OH,98.3%)、结晶紫(安耐吉(上海)医药化学有限公司);磷酸盐缓冲溶液(PBS,pH 7.4)、5,5-二甲基-1-吡咯啉-N-氧化物(DMPO,99%)、2,2,6,6-四甲基哌啶-1-氧自由基(TEMP,99%)(上海阿拉丁生化科技股份有限公司);酵母浸粉、琼脂、胰蛋白胨(北京奥博星生物技术有限责任公司)。
大肠杆菌(E.coli BNCC 133264)、金黄色葡萄球菌(S.aureus BNCC 186335)和耐甲氧西林金黄色葡萄球菌(MRSA ATCC 43300)由中国科学院微生物研究所提供。
1.2 合成方法
1.2.1 CuFe2O4的制备
采用水热法合成CuFe2O4纳米颗粒。将 2.4 mmol FeCl3与1.2 mmol CuCl2溶于20 mL乙二醇中,超声处理30 min使其充分溶解。随后加入1.2 g醋酸钠(NaAc)与0.2 g柠檬酸钠,继续超声混合1 h。将混合溶液转移至25 mL聚四氟乙烯内衬的高压反应釜中,于200 ℃反应10 h。反应结束后,所得黑色产物依次用超纯水和无水乙醇交替洗涤3次,于60 ℃真空干燥箱中干燥12 h,得到CuFe2O4粉末[11]。
1.2.2 CuFe2O4-NH2的制备
取100 mg CuFe2O4纳米颗粒,分散于50 mL异丙醇中,超声30 min。随后加入1 mL 3-氨丙基三甲氧基硅烷,于82 ℃回流搅拌12 h。反应结束后,通过磁分离收集产物,并分别用乙醇和去离子水洗涤3次,于60 ℃真空干燥,得到氨基化修饰的CuFe2O4-NH2载体[12]。
1.2.3 Ag溶胶的制备
将0.0732 g柠檬酸钠与0.0378 g AgNO3溶于1 L超纯水中,配制为银盐-柠檬酸钠混合溶液。另配制50 mL(10 mmol/L)NaBH4溶液作为还原剂。取100 mL上述混合溶液置于250 mL锥形瓶中,在匀速搅拌下逐滴加入3 mL NaBH4溶液,随后超声处理10 min,获得均匀的Ag纳米溶胶[12]。
1.2.4 CuFe2O4@Ag的制备
采用吸附-负载法制备CuFe2O4@Ag复合材料。取10 mg CuFe2O4-NH2粉末分散于10 mL蒸馏水中,加入10 mL新制Ag溶胶,超声处理 30 min后静置陈化20 min,使Ag纳米颗粒充分吸附于载体表面。该吸附-陈化过程重复6次以确保负载充分。最终产物分别用超纯水和乙醇洗涤3次,于60 ℃真空干燥箱中干燥备用。
1.3 杀菌活性评价
以E.coli、S.aureus及MRSA为供试菌株,采用最小抑菌浓度(MIC)测定、菌落计数法及滤纸片扩散法系统评价材料的杀菌性能。所有实验器皿与培养基均经121 ℃高压蒸气灭菌处理。实验前,将菌株活化至指数生长期,采用生理盐水调整菌悬液浓度至1×106 CFU/mL。在杀菌机制研究中,材料使用浓度设定为2倍最小抑菌浓度(2×MIC),所有培养过程均在37 ℃恒温条件下进行。滤纸片扩散法中使用直径7 mm的圆形滤纸片,每组实验设置6个平行重复,实验数据采用统计学方法进行分析处理[13]。
1.3.1 最小抑菌浓度法
在96孔板中依次加入含梯度浓度材料的液体LB培养基100 μL,随后每孔接种5 μL菌悬液(终浓度约为5×104 CFU/孔)。将96孔板置于 37 ℃恒温培养箱中静置培养12 h后,观察并记录各孔细菌生长情况,以无明显浑浊生长的最低药物浓度判定为最小抑菌浓度(MIC)。
1.3.2 菌落计数法
将菌液与材料在37 ℃条件下共孵育不同时间间隔后,采用磁分离移除复合材料,取5 μL上清液均匀涂布于固体LB平板表面。将平板置于37 ℃恒温培养箱中培养12 h后,统计各平板上的菌落形成单位数量,评估材料在不同时间点对细菌存活率的影响。
1.3.3 滤纸片扩散法
将80 μL菌悬液均匀涂布于固体LB培养基表面,将无菌滤纸片(直径7 mm)平贴于培养基表面。随后在每个滤纸片上滴加5 μL不同浓度的材料溶液,置于37 ℃恒温培养箱中培养12 h后,精确测量并记录各组杀菌圈直径。
1.4 杀菌机制研究
1.4.1 PI染色分析
将CuFe2O4@Ag材料与菌悬液在黑暗条件下共孵育25 min,随后通过磁分离移除材料。菌体经PBS缓冲液洗涤3次后,重悬于含碘化丙啶(PI)的染色液中,避光染色10 min。最后使用荧光倒置显微镜观察并记录细菌的PI荧光信号,以评估细胞膜完整性[14]。
1.4.2 细胞膜电位分析
将CuFe2O4@Ag与菌悬液共培养25 min后,经磁分离去除材料,收集菌体并重悬于适量PBS中。使用Zeta电位分析仪测定细菌表面电位的变化,以表征材料对细菌细胞膜表面电荷的影响[15]。
1.4.3 胞内成分泄漏分析
将CuFe2O4@Ag与菌悬液反应25 min后,先通过磁分离移除材料,再将菌液在14000 r/min条件下离心10 min。取上清液,分别通过紫外吸收法(260 nm)检测核酸类物质的泄漏情况[11],以及通过ICP-MS分析K+、Ca2+、Mg2+等金属离子的外泄浓度;沉淀菌体经硝酸-过氧化氢体系消解后,用于测定胞内残留金属离子含量,综合评价材料对细菌膜通透性的影响[15]。
2 结果与讨论
2.1 材料的表征
2.1.1 形貌分析
利用透射电子显微镜(TEM)对纳米材料在合成过程中的尺寸与形貌进行了表征。结果显示,CuFe2O4呈单分散球形结构,粒径约为(155±25)nm(图1a)。在CuFe2O4@Ag复合材料中(图1b),可观察到单分散的核壳结构,其表面均匀分布有粒径为(5.63±0.14)nm的银纳米颗粒(图2a),表明将Ag负载在CuFe2O4表面有助于提高纳米Ag的稳定性。高分辨TEM图像(图1c、1d)显示,0.204 nm的晶格条纹间距对应于面心立方结构银的(200)晶面,而0.207 nm的晶格条纹则归属于CuFe2O4的(220)晶面。EDS及元素 Mapping分析表明(图1e),CuFe2O4@Ag材料中含有C、N、O、Cu、Fe和Ag元素,其原子百分比分别为68.07%、1.38%、22.62%、6.39%、0.65%和0.89%(图2b、2c)。其中,C、N和O元素主要来源于修饰于CuFe2O4表面的硅烷偶联剂,Ag纳米颗粒则均匀分布于载体表面。

a、b.CuFe2O4和CuFe2O4@Ag的TEM;c、d.CuFe2O4@Ag高分辨TEM;e.CuFe2O4@Ag的能量色散X射线光谱Mapping图谱
图1 CuFe2O和CuFe2O4@Ag的TEM和Mapping图像
Fig.1 TEM and Mapping images of CuFe2O and CuFe2O4@Ag
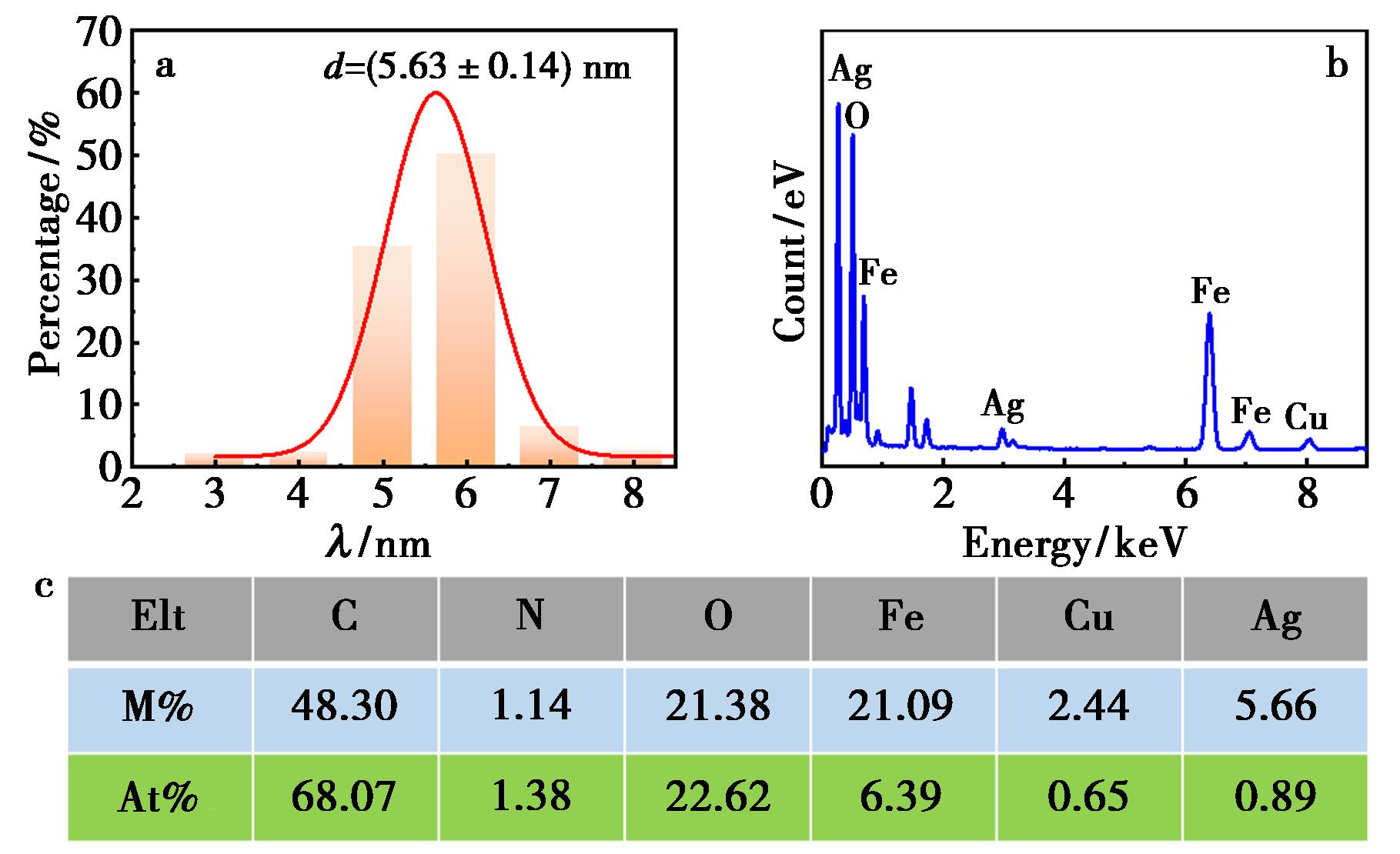
a.纳米Ag的粒径分布;b、c.EDX图谱和元素含量
图2 纳米Ag的粒径分布和CuFe2O4@Ag的EDX图谱和元素含量
Fig.2 Particle size distribution of Ag and EDX spectrum and element content of CuFe2O4@Ag
2.1.2 元素组成
为进一步探究CuFe2O4@Ag材料的元素化学状态及表面组成,进行了X射线光电子能谱(XPS)分析。XPS全谱确认材料中含有C、Ag、N、O、Fe和Cu元素(图3a),与EDS结果一致。各元素的高分辨XPS谱图显示:N 1s(284.8 eV)的结合能可归属为3-氨丙基三甲氧基硅烷中的相应元素(图3e);位于368.27和374.22eV的谱峰分别对应于单质银的Ag 3d5/2和Ag 3d3/2能级(图3b);O 1s在530.8 eV处的信号来源于CuO和Fe3O4中的O2-物种(图3f);Fe 2p谱中位于709.9、718.6和724.0 eV的结合能分别对应Fe3O4中Fe2+与Fe3+的贡献(图3d);Cu 2p3/2在933.54 eV处的峰可归属为Cu0,而Cu 2p1/2在953.7 eV以及位于943.46和940.68 eV的卫星峰则表明Cu2+的存在(图3c),后者可能源于Cu0在空气中发生的电子转移反应[14]。综上,XPS分析表明该复合材料中主要含有Fe3O4、Cu0、CuO和Ag0物相。
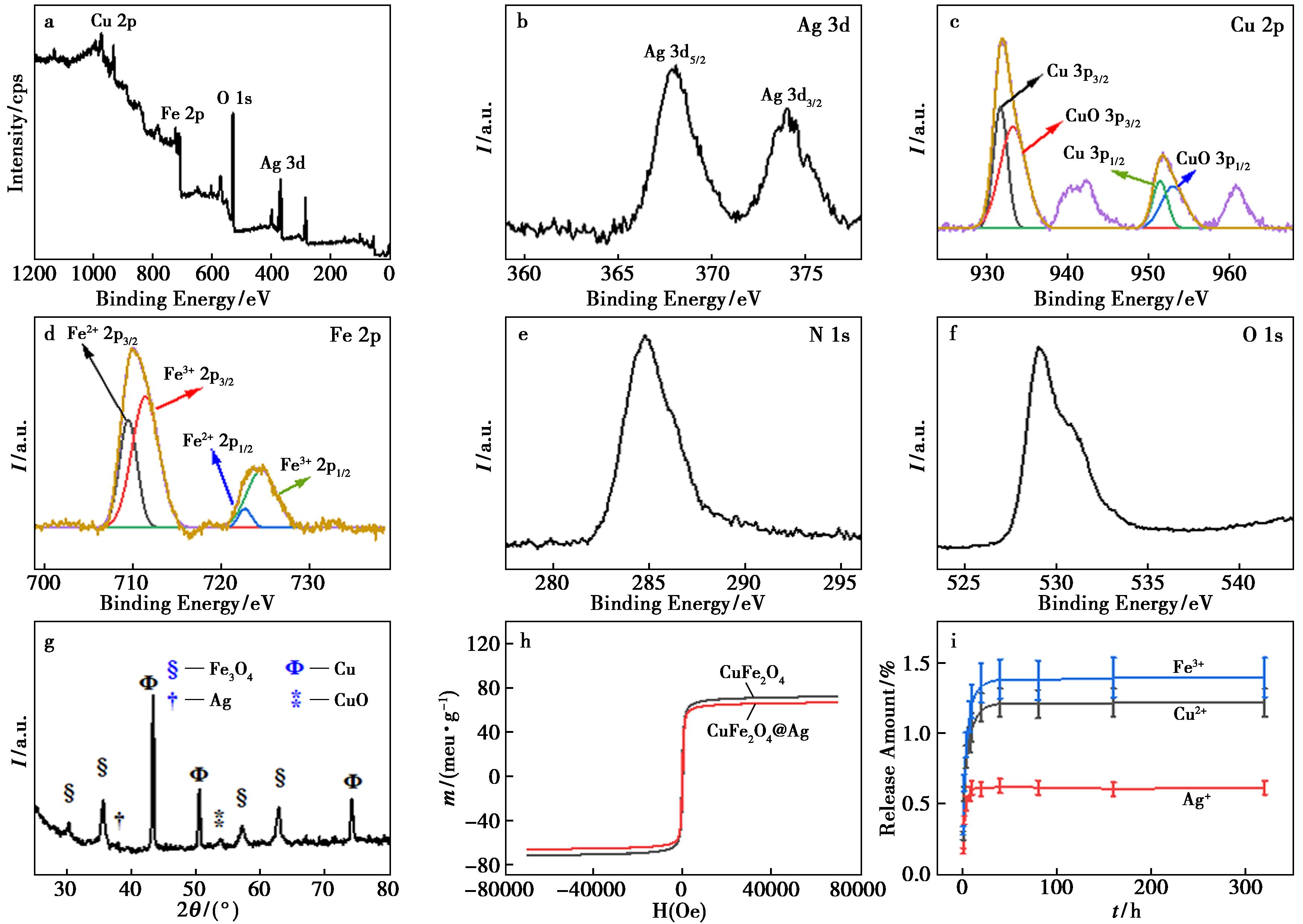
a.CuFe2O4@Ag的XPS图谱;b~f.Ag 3d、Cu 2p、Fe 2p、N 1s、O 1s的XPS图谱;g、h.CuFe2O4@Ag的XRD和VSM图谱;i.CuFe2O4@Ag离子释放
图3 CuFe2O4@Ag的XPS、XRD、VSM图谱以及离子释放
Fig.3 XPS,XRD,VSM spectra and the ion release of CuFe2O4@Ag
2.1.3 晶型分析
为进一步确定制备材料的晶体结构,CuFe2O4@Ag的XRD图谱如图3g所示,在衍射峰2θ=38.9°对应面心立方Ag晶格常数a=4.91Å(JCPDS 4-0783)的(111)位面,衍射峰30.28°、35.85°、57.30°、62.57°对应尖晶型Fe3O4[16],晶格常数为a=8.396 Å的(220)、(311)、(511)和(440)位面(JCPDS 19-0629),在53.48°处的衍射峰对应单斜相的CuO(020)位面(JCPDS 05-0661)[17],在2θ值为43.30°、50.43°、74.13°处的衍射峰可归因于立方相Cu的(111)、(200)和(220)晶面的位面,晶格常数a=3.615 nm(JCPDS 65-9743)。通过XRD表明,CuFe2O4@Ag中含有尖晶型Fe3O4,面心立方相的Ag,单斜相的CuO和立方相Cu。
2.1.4 性质分析
为研究材料的磁性能及离子释放行为,在室温-10000~10000 Oe的外加磁场范围内,通过振动样品磁强计(VSM)对其进行了表征(图3h)。磁滞回线显示,CuFe2O4和CuFe2O4@Ag的饱和磁化强度(Ms)分别为71.56和67.32 emu/g。CuFe2O4@Ag的磁饱和强度略有下降,归因于非磁性的Ag纳米颗粒负载于Fe3O4@Cu@CuO表面所产生的磁性稀释效应。尽管如此,VSM结果仍表明CuFe2O4@Ag具备较强的磁性。通过ICP-MS分析其离子释放行为发现,该材料在室温下可释放Fe3+、Cu2+和Ag+离子(图3i),释放速率在10 h内较快,于45 h左右逐渐达到平衡,释放量顺序为Fe3+>Cu2+>Ag+,该趋势可能与各金属元素的氧化还原电势差异有关。图4a的Nyquist图显示,CuFe2O4@Ag复合材料的中频区圆弧直径显著<纯CuFe22O4,其电荷转移电阻(Rct)从纯相的32.5降至12.8 kΩ·cm2,表明Ag纳米颗粒的引入大幅提升了界面的电荷转移动力学。为进一步探究CuFe2O4@Ag在介质中产生活性氧(ROS)的能力,进行了电子顺磁共振(EPR)测试。结果显示,与对照组相比,加入CuFe2O4@Ag后在谱图中出现了强度比为1∶2∶2∶1的·OH特征信号(图4b),并同时检测到1∶1∶1的 1O2特征峰(图4c),证实该材料在介质中能够有效产生·OH和 1O2。
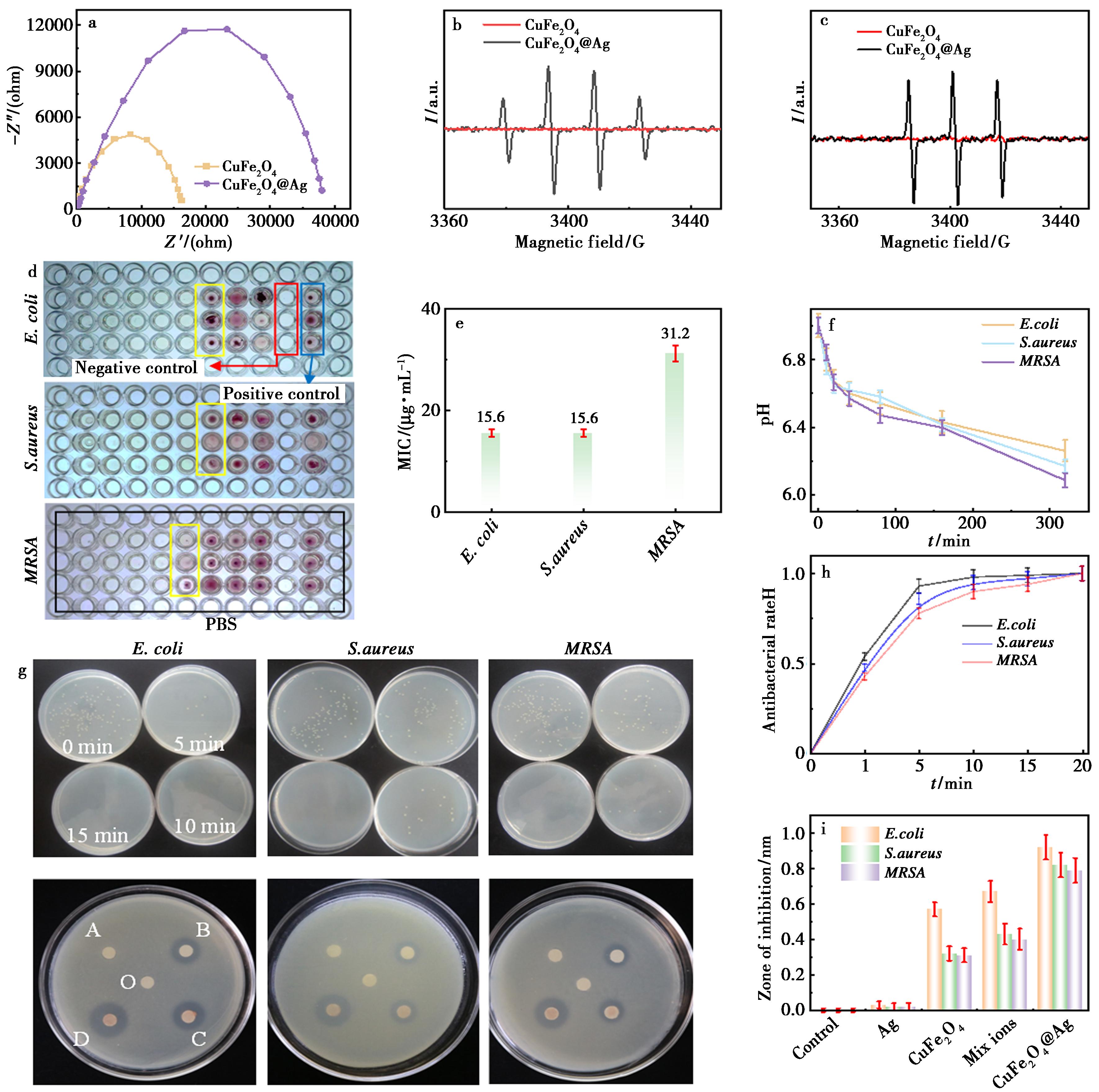
a.CuFe2O4及CuFe2O4@Ag复合材料的电化学阻抗谱分析;b、c.CuFe2O4@Ag的EPR图谱;d、e.MIC杀菌结果;f.E.coli、S.aureus和MRSA在不同时间间隔孵育过程中体系的pH变化;g.菌落计数和滤纸片扩散分析(O:H2O,A:Ag,B:CuFe2O4,C:混合离子,D:CuFe2O4@Ag);h、i.菌落计数法和和滤纸片扩散结果对应的数据
图4 CuFe2O4@Ag杀菌成分组成和杀菌性能
Fig.4 Bactericidal component composition and performance of CuFe2O4@Ag
2.2 杀菌活性
为评估CuFe2O4@Ag的杀菌性能,首先通过最小抑菌浓度(MIC)测定进行分析。结果显示(图4d、4e),CuFe2O4@Ag对大肠杆菌(E.coli)、金黄色葡萄球菌(S.aureus)和耐甲氧西林金黄色葡萄球菌(MRSA)的MIC值分别为15.6、15.6和31.2 μg/mL。图4f证实,孵育期间,细菌代谢的增强使培养介质的pH从中性(pH 7)降至微酸性,为纳米颗粒发生类芬顿反应提供了触发条件。进一步采用菌落计数法评估其杀菌动力学(图4g、4h),发现在作用15 min后,3种菌株均未见菌落形成,表明该材料在15 min内即可达到完全杀菌效果,因此确定其最佳杀菌时间为15 min。
CuFe2O4@Ag通过层层组装法制备,并在有氧条件下可产生活性氧物种(如·OH和 1O2)以及金属离子(Fe3+、Ag+、Cu2+)。为探究各组分在杀菌过程中的作用,以单一组分及其混合组为参照,利用滤纸片扩散法进行评价。在2×MIC浓度下,单独Ag组分未表现出明显杀菌活性;而与CuFe2O4及多阳离子组(Fe3++Ag++Cu2+)相比,CuFe2O4@Ag对E.coli、S.aureus和MRSA均展现出更强的杀菌效果,其中多阳离子组分对杀菌活性的贡献尤为显著(图4i)。以上结果说明,CuFe2O4@Ag的杀菌作用主要源于多阳离子与活性氧的协同作用,且多阳离子发挥主导作用。
2.3 杀菌机制探讨
从细菌结构特征来看,革兰氏阳性菌具有较厚的肽聚糖层及少量磷壁酸,而革兰氏阴性菌则肽聚糖层较薄且富含脂多糖。这些结构成分中所含的![]() 等官能团使细菌表面普遍呈负电性[18]。此外,细胞膜内侧维持的负电位对维持离子通道功能与能量代谢至关重要。CuFe2O4@Ag在溶液中可释放大量金属离子并产生活性氧,金属离子通过静电吸引或强配位作用结合于细菌细胞壁的关键蛋白,改变其二级结构,从而导致细菌死亡;而ROS则凭借强氧化性破坏磷脂双分子层,引起细胞壁损伤。
等官能团使细菌表面普遍呈负电性[18]。此外,细胞膜内侧维持的负电位对维持离子通道功能与能量代谢至关重要。CuFe2O4@Ag在溶液中可释放大量金属离子并产生活性氧,金属离子通过静电吸引或强配位作用结合于细菌细胞壁的关键蛋白,改变其二级结构,从而导致细菌死亡;而ROS则凭借强氧化性破坏磷脂双分子层,引起细胞壁损伤。
为进一步验证材料的杀菌机制,采用红色荧光染料碘化丙啶(PI)对细菌死亡率进行评价。荧光倒置显微镜图像显示(图5a),对照组中仅见少量红色荧光斑点,主要为正常衰老致死的细菌;而经CuFe2O4@Ag处理后的E.coli、S.aureus和MRSA样品中均出现大量红色球状荧光区域,表明材料可引起细菌膜的严重损伤,导致细胞彻底死亡。
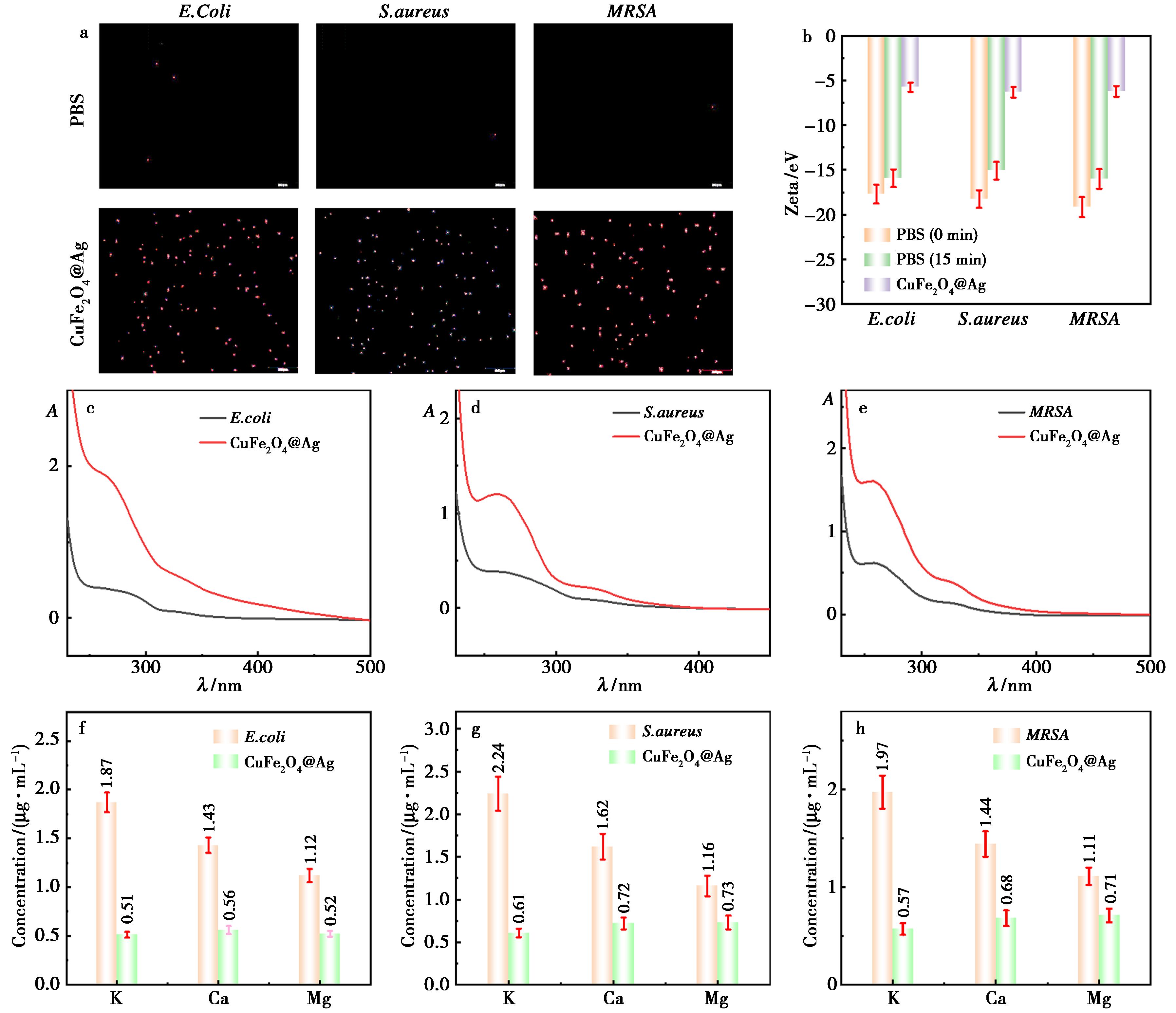
a.CuFe2O4@Ag对E.coli,S.aureus和MRSA的PI染色分析;b.Zeta电势分析;c~h.CuFe2O4@Ag对E.coli、S.aureus和MRSA的核酸泄露和金属离子泄露分析
图5 CuFe2O4@Ag对E.coli,S.aureus和MRSA的杀菌机制结果
Fig.5 Antibacterial mechanism results of CuFe2O4@Ag on E.coli,S.aureus and MRSA
为探究CuFe2O4@Ag对E.coli、S.aureus及MRSA表面负电位环境的破坏作用,对其Zeta电位进行了测定。结果显示(图5b),对照组中3种菌株的初始Zeta电位分别为-17.72、-18.26和-19.18 mV,培养15 min后略升至-15.93、-15.10和-16.01 mV。而经CuFe2O4@Ag处理15 min后,其Zeta电位分别显著升高至-5.76、-6.32和-6.22 mV。该变化可归因于CuFe2O4@Ag与细菌细胞壁表面带负电的官能团发生结合,中和了其表面电荷,从而引起Zeta电位上升。
细菌细胞内含物(如DNA、RNA、核苷酸等)在260 nm附近具有特征性的紫外吸收峰。当细胞膜完整性遭到破坏时,这些物质会泄漏到上清液中,导致上清液在260 nm处的吸光度显著升高。通过紫外-可见分光光度法(UV-Vis)在 260 nm处检测吸光度变化,发现经CuFe2O4@Ag处理15 min后,该波长处的吸光度显著增强,表明细菌细胞内含物大量泄漏(图5c~5e)。进一步采用电感耦合等离子体质谱法(ICP-MS)测定细菌经CuFe2O4@Ag处理后胞内K+、Ca2+、Mg2+的泄漏情况(图5f~5h)。对照组中E.coli、S.aureus和MRSA的K+浓度分别为1.87、2.24和1.97 μg/mL,Ca2+浓度分别为1.43、1.62和 1.44 μg/mL,Mg2+浓度分别为1.12、1.16和 1.11 μg/mL,表明其细胞膜完整性及离子调节功能正常。而经CuFe2O4@Ag处理后,3种细菌胞内K+浓度分别降至0.51、0.61和0.57 μg/mL,Ca2+浓度分别降至0.56、0.72和0.68 μg/mL,Mg2+浓度分别降至0.52、0.73和0.71 μg/mL。实验组离子浓度显著低于对照组,说明CuFe2O4@Ag破坏了细菌细胞壁结构,增强了细胞膜通透性,导致胞内关键离子外流,最终引起细菌死亡。
3 结论
3.1 以CuFe2O4为载体,通过表面氨基化修饰后,将超小粒径的纳米Ag负载在载体表面合成CuFe2O4@Ag。通过TEM、XRD、XPS等表征分析可知,核壳型CuFe2O4@Ag中Ag粒径约为6 nm,含有尖晶型Fe3O4,面心立方相的Ag,单斜相的CuO和立方相Cu。
3.2 大肠杆菌(E.coli)、金黄色葡萄球菌(S.aureus)和耐甲氧西林金黄色葡萄球菌(MRSA)为模式菌株,研究了CuFe2O4@Ag的杀菌活性和杀菌效率,MIC值依次为15.6、15.6和31.2 μg/mL。在2×MIC时,与菌液作用15 min时,杀菌率均达到99.99%以上。
3.3 杀菌机理结果表明CuFe2O4@Ag可释放金属离子和ROS,通过静电吸引和氧化作用显著破坏细胞壁中细菌生存的负电位差的完整性,改变膜通透性,致使核酸和细胞质泄露而达到杀菌效果。
[1]Huang J S,Hotta C I,Leandro J.Water Res.,2025,285:124103.
[2]Luo X,Xiao J W,Yang Q M,Lu X L,Huan Q J,Ai X J,Li B,Sun L,Chen L.Chin.Chem.Lett.,2025,36(1):109684.
[3]Liu S,Yang S,Blazekovic B,Li L,Zhang J D,Wang Y.Engineering,2024,38:13-26.
[4]Li X,Hao Y,Teng D,Mao R Y,Yang N,Wang J H.Chem.Eng.J.,2025,525:170733.
[5]Chen L,Zhang J Y,Jiang X S,Zhang B,Sun Y N,Zhao K,Yao B H,Tang Y F,Tan Q C,Wu Z X.Mater.Today Bio.,2025,35:102419.
[6]Vu N N,Tran B,Ladhari S,Saidi A,Assadi A A,Nguyen T P.Chem.Eng.J.,2025,524:169720.
[7]Xia X,Wu Y D,Hao Q,Xie L X,Liang Y J,Liu K.J.Hazard.Mater.,2025,493:138416.
[8]Castrop H,Schießl I M.Acta Physiol.,2017,219(3):546-555.
[9]Bibi M,Abbas M S,Ahmad N,Muhammad B,Iqbal Z,Rana U A,Khan S U.Compos.Part B-Eng.,2017,114:139-148.
[10]Zhang T,Zhu H B,Croué J P.Environ.Sci.Technol.,2013,47(6):2784-2791.
[11]Guo S B,Isah M B,Hu R L,Guo Z S,Wei X D,Liu Z F,Ji X H,Dias A C P,Zhang X Y.ACS Appl.Mat.Interf.,2025,17(27):38859-38873.
[12]Wang J W,Qiang R R,Miao Q W,Hu R L,Chen H H,Guo S B,Liu Z F.Appl.Surf.Sci.,2025,684:161908.
[13]Guo S B,Liu X,Chen H H,Wang J W,Qiao Y M,Zhang T L,Ji X H,Han H,Liu Z F,Bai Y,Tang J.J.Hazard.Mat.,2024,476:135149.
[14]Guo S B,Liu X,Chen H H,Qiao Y M,Liu Z F,Zhang D,Ting G,Ji X H,Han H,Zhang T L.J.Environ.Chem.Eng.,2024,12(5):113441.
[15]Wang J W,Fang X,Chen H H,Yang J P,Qiu Y,Qiang R R,Guo Z S,Liu Q H,Zhou X L,Liu Z F,Guo S B.Colloid.Surf.A,2024,683:133076.
[16]Guo S B,Zhang D,Qiao Y M,Xu H T,Jiufu Lu J F,Liu Z F,Shi J,Ji X H,Zhang T L.Arabian J.Chem.,2024,17(2):105524.
[17]Shi J,Zheng J L,Liang B,Song F M,Wang J,Guo S B,Ge H G,Gao Y H,Zhang T L.Colloids Surf.A Physicochem.Eng.Aspects,2023,668:131402.
[18]Liu Z F,Guo S B,Fang X,Shao X Z,Zhao Z P.RSC Adv.,2022,12:19856-1986.