苯并呋喃类化合物是一类重要的苯并稠杂环化合物,其独特的结构赋予了多样的活性,使其在药物研发、农药创制和材料科学等领域具有核心价值[1-3],被用于治疗心律失常、痛风、病毒感染、细菌感染等。因此,该类化合物受到了科学家们的密切关注,并且开发了一系列高效的合成方法[4-7]。此外,苯并呋喃骨架本身也是一种极其重要的合成子,是构建众多复杂功能分子的关键砌块[8-10]。在众多的苯并呋喃类化合物中,2,3-二取代苯并呋喃同样表现出优异的生物活性。然而,由于合成难度比无取代或者单取代苯并呋喃更高,目前其相关合成方法的报道相对较少,且部分反应条件较为苛刻。例如Suresh等[11]于2019年报道了碱促进下邻羟基肉桂酸酯或邻羟基查尔酮可与γ-溴代巴豆酸酯的反应,合成了2,3-二取代苯并呋喃类化合物。然而,该策略需使用高沸点溶剂N-甲基吡咯烷酮(NMP),并在120 ℃的高温下进行,反应条件较为苛刻,后处理过程中反应溶剂不易去除。因此,发展条件温和、操作简便的合成方法具有重要研究价值与必要性。基于本课题组在碱促进下α,β-不饱和酮[12-14]、γ-溴代巴豆酸酯[15-17]参与的串联反应等方面的研究兴趣和研究基础。设想2,3-二取代苯并呋喃类化合物可由方便易得的邻羟基查尔酮与γ-溴代巴豆酸酯在碱促进下高效构建。通过实验的不断尝试并实现了上述设想。在此,本文报道了一种碱促进下邻羟基查尔酮与γ-溴代巴豆酸酯的一锅多步串联反应,高效合成一系列2,3-二取代苯并呋喃类化合物。
1 实验部分
1.1 主要仪器与试剂
ME204E型电子分析天平(瑞士METTLER-TOLEDO有限公司);PL-MD-5型溶剂纯化系统(北京逸峰科技有限公司);ZNCL-B型智能磁力搅拌器(巩义市予华仪器有限责任公司);EYELA SB-1100型旋转蒸发仪(上海埃朗仪器有限公司);SHZ-D(Ⅲ)型循环水式多用途真空泵(郑州市亚荣仪器有限公司);ZF-1A型三用紫外分析仪(上海骥辉分析仪器有限公司);GZX-9240MBE型数显鼓风干燥箱(上海博讯实业有限公司医疗设备厂);DZF-6020型真空干燥箱(上海一恒科学仪器有限公司);Bruker AV 400 MHz型核磁共振谱仪(瑞士Bruker公司)。
邻羟基苯甲醛、γ-溴代巴豆酸甲酯(上海皓鸿生物医药科技有限公司);二异丙基乙胺(DIPEA)、1,8-二氮杂双环[5.4.0]十一碳-7-烯(DBU)、N,N-二甲基甲酰胺(DMF)、二甲亚砜(DMSO)(上海麦克林生化科技股份有限公司);碳酸铯(上海毕得医药科技股份有限公司);盐酸、碳酸钾、氢氧化钠、氢氧化钾、乙腈、无水乙醇、无水硫酸钠(国药集团化学试剂有限公司);石油醚(PE)、乙酸乙酯(EA)、二氯甲烷(DCM)、丙酮(Acetone)、四氢呋喃(THF)(武汉欣申试化工科技有限公司)。所用试剂均为分析纯,所用溶剂在使用前通过溶剂纯化系统处理。
从供应商处购买的材料无需进一步纯化即可直接使用。使用硅胶板(GF254,青岛谱科分离材料有限公司)进行薄层色谱法(TLC)监测。通过硅胶(粒度为200~300目,青岛海洋化工有限公司)进行柱色谱法分离。用V(石油醚(PE))∶V(乙酸乙酯(EA))∶V(二氯甲烷(DCM))洗脱。
1.2 实验方法
1.2.1 邻羟基查尔酮(1a)的合成路线
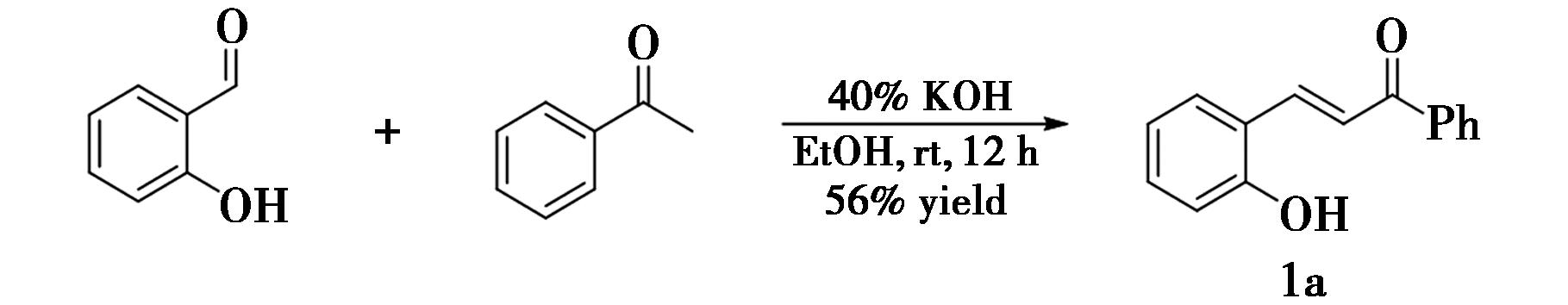
图1 邻羟基查尔酮(1a)的制备
Fig.1 Preparation of o-hydroxychalcone (1a)
圆底烧瓶中加入磁子,依次加入30 mL乙醇、266.5 mg(2.2 mmol)邻羟基苯甲醛、240.3 mg(2.0 mmol)苯乙酮,然后缓慢加入4.0 mL(40%)KOH。混合物在室温下搅拌12 h。反应完成(由TLC监测)后,混合物缓慢加入1 mol/L HCl,将反应液pH调节至中性,过滤后在真空中干燥,得到336.4 mg产物邻羟基查尔酮,产率56%,黄绿色固体。产物的核磁数据与文献[18]相一致。
1.2.2 (E)-4-[2-((E)-3-氧代-3-苯基丙-1-烯-1-基)苯氧基]丁-2-烯酸甲酯的合成(3a′)的制备圆底烧瓶中加入磁子,依次加入1.0 mL乙腈、22.4 mg(0.1 mmol)邻羟基查尔酮、32.6 mg(0.1 mmol)碳酸铯,然后缓慢加入17.9 mg(0.1 mmol)γ-溴代巴豆酸甲酯,混合物在室温下搅拌2 h。反应完成(由TLC监测)后,混合物加入饱和氯化铵溶液,乙酸乙酯萃取、分液、无水硫酸钠干燥、合并有机相,减压除去溶剂,经柱层析分离(V(PE)∶V(EA)=20∶1)得到29.0 mg化合物3a′,产率90%,黄色固体。1HNMR(CDCl3,400 MHz),δ:8.17(d,1H,J=15.9 Hz);8.04(d,2H,J=7.2 Hz);7.70(d,1H,J=7.6 Hz);7.64(d,1H,J=15.9 Hz);7.60(d,1H,J=7.2 Hz);7.53(t,2H,J=7.4 Hz);7.42~7.35(m,1H),7.16(dt,1H,J=15.8,4.0 Hz);7.06(t,1H,J=7.5 Hz);6.91(d,1H,J=8.3 Hz);6.23(d,1H,J=15.8 Hz),4.84(dd,2H,J=4.0,1.6 Hz),3.79(s,3H)。13CNMR(CDCl3,100 MHz),δ:191.1,166.4,157.0,142.1,140.0,138.4,132.6,131.7,129.3,128.61,128.55,124.3,123.3,122.1,121.6,112.4,66.9,51.8。HRMS(ESI),C20H18O4Na+,实测值(计算值),m/z:345.1097(345.1091)[M+Na]+。
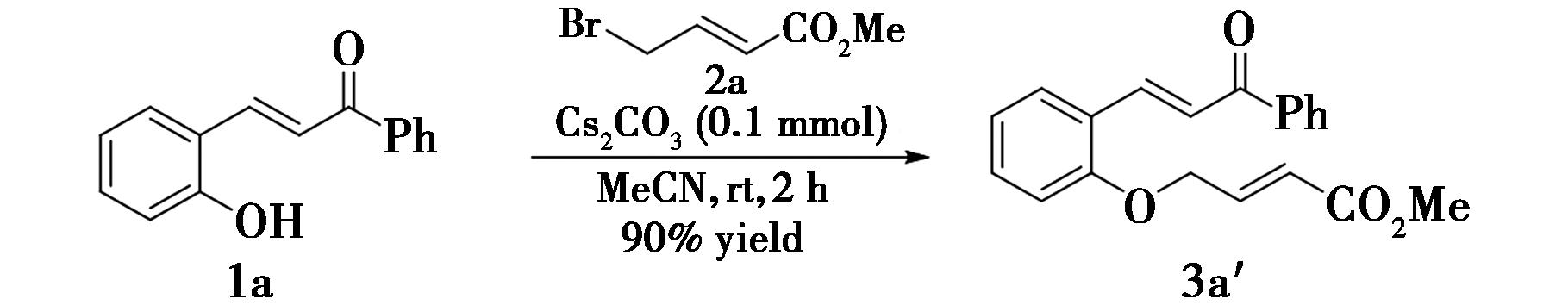
图2 化合物3a′的制备
Fig.2 Preparation of compound 3a′
1.2.3 (E)-3-[3-(2-氧代-2-苯乙基)-2,3-二氢苯并呋喃-2-基]丙烯酸甲酯的合成(3a″)的制备圆底烧瓶中加入磁子,依次加入1.0 mL乙腈、32.2 mg(0.1 mmol)化合物3a′、32.6 mg(0.1 mmol)碳酸铯,混合物在室温下搅拌12 h。反应完成(由TLC监测)后,混合物缓慢加入饱和氯化铵溶液,乙酸乙酯萃取、分液、无水硫酸钠干燥、合并有机相,减压除去溶剂,经柱层析分离(V(PE)∶V(EA)=20∶1)得到28.9 mg化合物3a″,产率89%,黄色固体。1HNMR(CDCl3,400 MHz),δ:7.96~7.90(m,2H);7.63~7.56(m,1H);7.50~7.44(m,2H);7.22~7.15(m,2H);6.96~6.86(m,3H);6.18(dd,1H,J=15.7,1.6 Hz);5.61(ddd,1H,J=8.6,5.3,1.7 Hz);4.36(td,1H,J=8.6,6.1 Hz);3.76(s,1H);3.64(s,3H);3.29(dd,2H,J=7.2,4.9 Hz)。13CNMR(CDCl3,100 MHz),δ:198.3,166.2,158.7,142.8,136.6,133.6,129.5,129.0,128.8,128.2,124.6,123.1,121.3,110.1,83.9,51.8,41.1,40.2。HRMS(ESI),C20H18O4Na+,实测值(计算值),m/z:345.1097(345.1103)[M+Na]+。
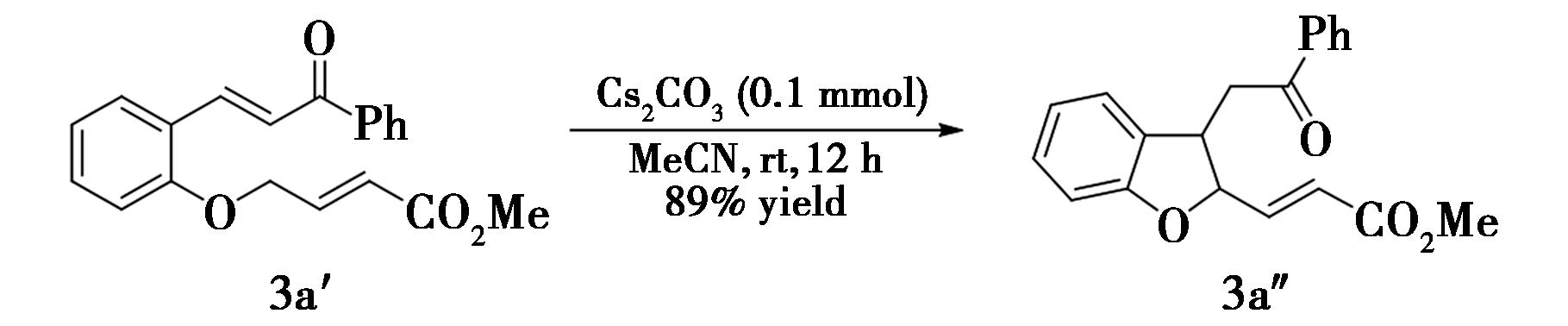
图3 化合物3a″的制备
Fig.3 Preparation of compound 3a″
1.2.4 2,3-二取代苯并呋喃(3)的制备
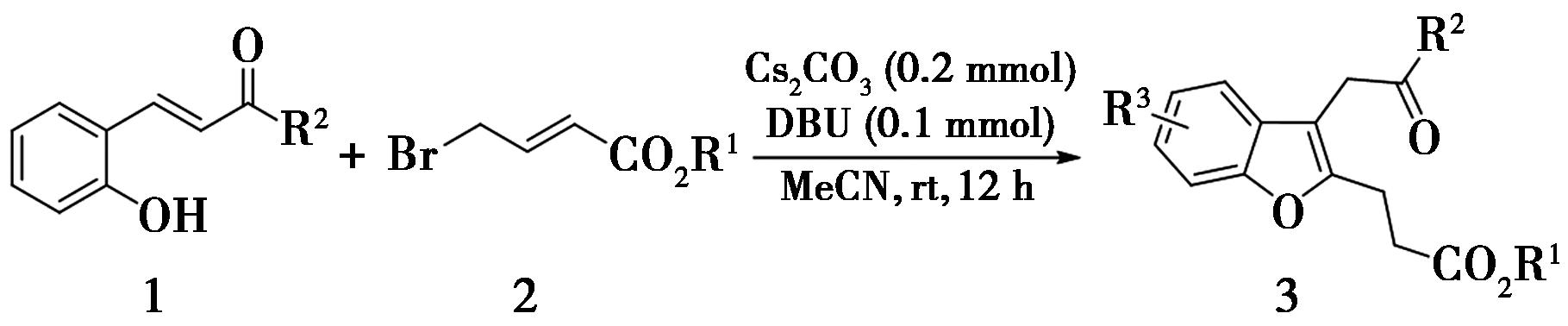
图4 2,3-二取代苯并呋喃的制备
Fig.4 Preparation of 2,3-disubstituted benzofuran
将0.1 mmol邻羟基查尔酮、1.0 mL乙腈、0.2 mmol Cs2CO3加入到反应管中后,再加入0.15 mmol γ-溴代巴豆酸酯,在室温下反应,通过TLC监测到原料消耗完后加入0.1 mmol DBU,继续搅拌12 h。将反应液中和后,减压除去溶剂,经柱层析分离(V(PE)∶V(EA)∶V(DCM)=20∶1∶1)得到2,3-二取代苯并呋喃(3)。
1.2.5 产物核磁表征
3-((3-2-氧代-2-苯乙基)-1-苯并呋喃-2-基)丙酸甲酯(3a)的合成:28.7 mg,产率89%,黄色固体。1HNMR(CDCl3,400 MHz),δ:8.13~8.02(m,2H);7.64~7.56(m,1H);7.53~7.46(m,2H);7.44~7.35(m,2H);7.25~7.14(m,2H);4.34(s,2H);3.66(s,3H);3.09(t,2H,J=7.4 Hz);2.78(d,2H,J=7.4 Hz)。13CNMR(CDCl3,100 MHz),δ:196.3,172.9,154.1,153.8,136.5,133.3,129.2,128.7,128.3,123.7,122.5,119.2,110.9,108.7,51.8,33.7,32.1,22.0。HRMS(ESI),实测值(计算值),C20H18O4Na+,m/z:345.1097(345.1104)[M+Na]+。
3-((3-2-氧代-2-苯乙基)-1-苯并呋喃-2-基)丙酸乙酯(3b)的合成:26.2 mg,产率78%,黄色固体。1HNMR(CDCl3,400 MHz),δ:8.16~8.00(m,2H);7.66~7.56(m,1H);7.54~7.46(m,2H);7.43~7.33(m,2H);7.25~7.12(m,2H);4.34(s,2H);4.12(q,2H,J=7.1 Hz);3.09(t,2H,J=7.4 Hz);2.75(t,2H,J=7.4 Hz);1.23(t,3H,J=7.1 Hz)。13CNMR(CDCl3,100 MHz),δ:196.3,172.5,154.1,154.0,136.5,133.3,129.2,128.7,128.3,123.7,122.4,119.2,110.8,108.6,60.6,33.8,32.4,22.0,14.1。HRMS(ESI),C21H20O4Na+,实测值(计算值),m/z:359.1254(359.1247)[M+Na]+。
3-((3-2-氧代-2-苯乙基)-1-苯并呋喃-2-基)丙酸苄酯(3c)的合成:22.3 mg,产率56%,黄色固体。1HNMR(CDCl3,400 MHz),δ:8.07(dd,2H,J=8.4,1.4 Hz);7.64~7.57(m,1H);7.54~7.46(m,2H);7.45~7.38(m,2H);7.36~7.28(m,5H);7.26~7.15(m,2H);5.12(s,2H);4.31(s,2H);3.13(t,2H,J=7.3 Hz);2.85(t,2H,J=7.3 Hz)。13CNMR(CDCl3,100 MHz),δ:196.3,172.2,154.0,153.7,136.5,135.7,133.3,129.1,128.6,128.5,128.3,128.2,128.1,123.6,122.4,119.2,110.8,108.7,66.4,33.7,32.3,22.0。HRMS(ESI),C26H22O4Na+,实测值(计算值),m/z:421.1410(421.1415)[M+Na]+。
3-((3-2-(4-甲氧基苯基)-2-氧代乙基)-1-苯并呋喃-2-基)丙酸甲酯(3d)的合成:28.5 mg,产率81%,黄色固体。1HNMR(CDCl3,400 MHz),δ:8.05(d,2H,J=8.8 Hz);7.39(dd,2H,J=7.6,1.4 Hz);7.24~7.14(m,2H);7.01~6.94(m,2H);4.28(s,2H);3.87(s,3H);3.66(s,3H);3.09(t,2H,J=7.4 Hz);2.77(t,2H,J=7.4 Hz)。13CNMR(CDCl3,100 MHz),δ:194.8,172.9,163.6,154.0,153.7,130.6,129.6,129.2,123.6,122.4,119.3,113.8,110.8,109.0,55.5,51.7,33.4,32.1,22.0。HRMS(ESI),C21H20O5Na+,实测值(计算值),m/z:375.1203(375.1206)[M+Na]+。
3-((3-2-(3-三氟甲基)-2-氧代乙基)-1-苯并呋喃-2-基)丙酸甲酯(3e)的合成:31.2 mg,产率80%,黄色固体。1HNMR(CDCl3,400 MHz),δ:8.32(s,1H);8.25(d,1H,J=7.8 Hz);7.85(d,1H,J=7.8 Hz);7.64(t,1H,J=7.8 Hz);7.44~7.33(m,2H),7.25~7.15(m,2H);4.37(s,2H);3.65(s,3H);3.09(t,2H,J=7.4 Hz);2.78(t,2H,J=7.4 Hz)。13CNMR(CDCl3,100 MHz),δ:195.0,172.8,154.1,154.0,137.0,131.5,131.2,129.7(q,J=3.7 Hz),129.4,128.9,125.2(q,J=3.9 Hz),123.9,122.6,121.0(q,J=246.4 Hz),119.1,111.0,108.2,51.8,34.0,32.0,22.0。19FNMR,(CDCl3,376 MHz),δ:-62.8。HRMS(ESI),C21H20O5Na+,实测值(计算值),m/z:413.0974(413.0971)[M+Na]+。
3-(3-(2-(萘-2-基)-2-氧代乙基)-1-苯并呋喃-2-基)丙酸甲酯(3f)的合成:24.5 mg,产率66%,黄色固体。1HNMR(CDCl3,400 MHz),δ:8.64(s,1H);8.10(dd,1H,J=8.6,1.8 Hz);8.00(dd,1H,J=8.1,1.4 Hz);7.96~7.87(m,2H);7.68~7.54(m,2H);7.50~7.37(m,2H);7.26~7.14(m,2H);4.48(s,2H);3.67(s,3H);3.14(t,2H,J=7.4 Hz);2.80(t,2H,J=7.4 Hz)。13CNMR(CDCl3,100 MHz),δ:196.2,172.9,154.1,153.9,135.6,133.8,132.5,130.0,129.6,129.2,128.6,127.8,126.9,124.0,123.7,122.5,119.3,110.9,108.9,51.8,33.8,32.1,22.0。HRMS(ESI),C24H20O4Na+,实测值(计算值),m/z:395.1254(395.1249)[M+Na]+。
3-(3-(2-(噻吩-2-基)-2-氧代乙基)-1-苯并呋喃-2-基)丙酸甲酯(3g)的合成:30.2 mg,产率92%,黄色固体。1HNMR(CDCl3,400 MHz,),δ:7.92~7.84(m,1H);7.70~7.61(m,1H);7.49~7.33(m,2H);7.25~7.12(m,3H);4.26(s,2H);3.66(s,3H);3.13(t,2H,J=7.4 Hz);2.79(t,2H,J=7.4 Hz)。13CNMR(CDCl3,100 MHz),δ:189.2,172.9,154.0,143.5,134.0,132.3,129.0,128.2,123.7,122.5,119.3,110.8,108.6,51.8,34.5,32.1,22.0。HRMS(ESI),C18H16O4SNa+,实测值(计算值),m/z:351.0662(351.0668)[M+Na]+。
3-(3-(2-氧丙基)-1-苯并呋喃-2-基)丙酸甲酯(3h)的合成:22.2 mg,产率85%,黄色固体。1HNMR(CDCl3,400 MHz),δ:7.47~7.32(m,2H);7.26~7.15(m,2H);3.73(s,2H);3.66(s,3H);3.07(t,2H,J=7.3 Hz);2.78(t,2H,J=7.3 Hz);2.19(s,3H)。13CNMR(CDCl3,100 MHz),δ:205.5,172.7,154.0,153.8,128.8,123.8,122.6,119.0,110.9,108.6,51.8,38.8,32.0,29.1,21.7。HRMS(ESI),C15H16O4Na+,实测值(计算值),m/z:283.0941(283.0950)[M+Na]+。
3-(6-甲基-3-(2-氧代-2-苯乙基)-1-苯并呋喃-2-基)丙酸甲酯(3i)的合成:20.8 mg,产率62%,黄色固体。1HNMR(CDCl3,400 MHz),δ:8.13~8.02(m,2H);7.66~7.57(m,1H);7.52(dd,2H,J=8.4,7.0 Hz);7.37~7.28(m,2H);7.17(dd,1H,J=8.6,2.0 Hz);4.32(s,2H);3.65(s,3H);3.07(t,2H,J=7.4 Hz);2.76(t,2H,J=7.4 Hz)。13CNMR(CDCl3,100 MHz),δ:195.8,172.7,155.5,152.5,136.4,133.5,130.7,128.8,128.3,128.1,123.9,119.0,111.8,108.6,51.8,33.5,32.0,22.0。HRMS(ESI),C21H20O4Na+,实测值(计算值),m/z:359.1254(359.1252)[M+Na]+。
3-(5-氯-3-(2-氧代-2-苯乙基)-1-苯并呋喃-2-基)丙酸甲酯(3j)的合成:23.2 mg,产率65%,黄色固体。1HNMR(CDCl3,400 MHz),δ:8.10~8.01(m,2H);7.63~7.55(m,1H);7.48(dd,2H,J=8.4,6.8 Hz);7.26~7.18(m,2H);7.04~6.97(m,1H);4.31(s,2H);3.66(s,3H);3.07(t,2H,J=7.4 Hz);2.75(t,2H,J=7.4 Hz);2.43(s,3H)。13CNMR(CDCl3,100 MHz),δ:196.4,172.9,154.5,153.1,136.6,133.9,133.2,128.7,128.3,126.6,123.8,118.7,111.1,108.5,51.8,33.9,32.2,22.0,21.6。HRMS(ESI),C20H17O4ClNa+,实测值(计算值),m/z:379.0708(379.0709)[M+Na]+。
2 结果与讨论
2.1 反应初步尝试
图5 2,3-二取代苯并呋喃化合物的合成
Fig.5 Synthesis of 2,3-disubstituted benzofuran
使用邻羟基查尔酮(1a)与γ-溴代巴豆酸酯(2a)为模版底物进行反应的初步尝试,并以89%的分离产率得到目标化合物2,3-二取代苯并呋喃3a。
2.2 反应条件的优化
采用模板底物化合物1a和2a进行反应条件的优化。
2.2.1 碱种类的筛选
如表1所示,在室温下,乙腈作为溶剂,首先对常用碱的种类进行了筛选,例如K2CO3、Cs2CO3、NaOH、KOH、DIPEA和DBU等,其中K2CO3和Cs2CO3作碱时,只能以痕量得到2,3-二取代苯并呋喃(3a),主要得到的副产物是2,3-二取代二氢苯并呋喃(3a″)。当分别使用NaOH和KOH作碱时,能够分别以35%和21%得到目标产物3a。随后进行了有机碱的筛选,当碱为DBU时能以68%的产率得到目标产物3a,明显高于其他碱所获得的化合物产率,因此以DBU作为最优的碱进行下一步条件筛选。
表1 碱种类的筛选注
Tab.1 Screening of the type of base
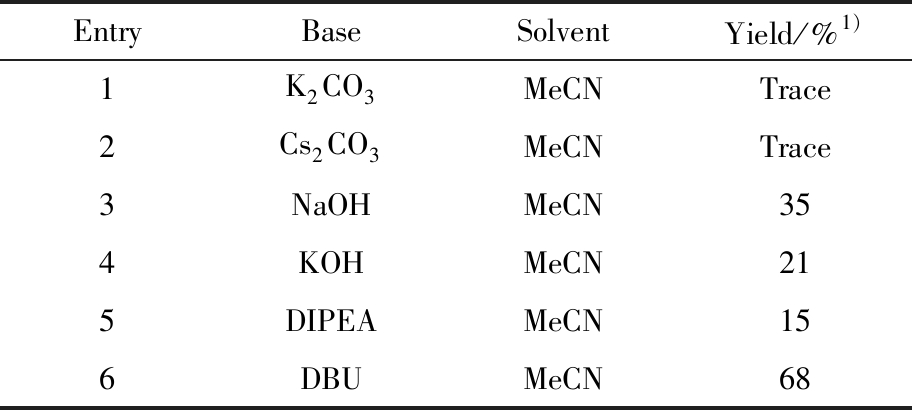
注:Unless otherwise stated,all reactions were performed with 0.1 mmol compound 1a,0.15 mmol compound 2a,and base in 0.2 mmol (1.0 mL)MeCN at room temperature for 12 h;1):Isolated yield.
EntryBaseSolventYield/%1)1K2CO3MeCNTrace2Cs2CO3MeCNTrace3NaOHMeCN354KOHMeCN215DIPEAMeCN156DBUMeCN68
2.2.2 溶剂种类的筛选
如表2所示,当确定选择DBU作为碱后,随后对有机溶剂进行了筛选,例如Acetone、DMSO、DMF、THF和EtOH等。通过实验结果发现,使用MeCN作溶剂时,产物3a的产率(68%)最高。因此,选用MeCN作为反应最优溶剂进行下一步筛选。
表2 溶剂种类的筛选注
Tab.2 Screening of the type of solvent
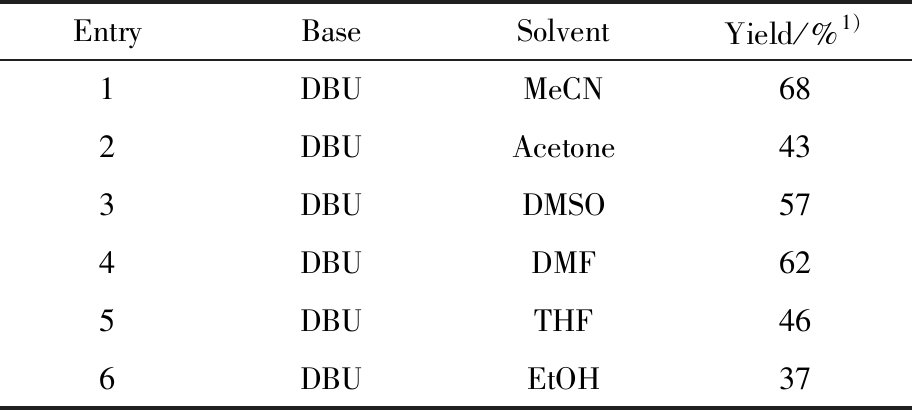
注:Unless otherwise stated,all reactions were performed with 0.1 mmol compound 1a,0.15 mmol compound 2a,and 0.2 mmol DBU in the 1.0 mL specified solvent at room temperature for 12 h.1):Isolated yield.
EntryBaseSolventYield/%1)1DBUMeCN682DBUAcetone433DBUDMSO574DBUDMF625DBUTHF466DBUEtOH37
2.2.3 混合碱种类的筛选
通过碱和溶剂的筛选,确定了以DBU作为碱、乙腈作为溶剂时,目标产物3a的分离产率可达到68%。通过控制实验发现,当使用Cs2CO3作为碱时,以89%的产率得到2,3-二取代二氢苯并呋喃(3a″)。进一步机理研究表明,2,3-二取代二氢苯并呋喃(3a″)在DBU的作用下能够高效转化为2,3-二取代苯并呋喃(3a),且此转化步骤是提升整体反应效率的关键路径。基于此发现,对碱的协同使用进行了当量优化(表3)。最终确定的最佳条件为:0.2 mmol Cs2CO3,0.1 mmol DBU。在双碱体系下,反应实现了最高的产率。故确定混合碱的种类为Cs2CO3和DBU。
表3 混合碱种类筛选注
Tab.3 Screening of the type of mixed bases
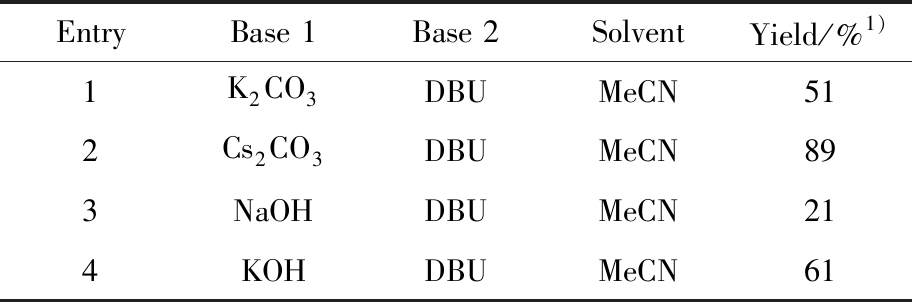
注:Unless otherwise stated,all reactions were performed with 0.1 mmol compound 1a,0.15 mmol compound 2a,and 0.2 mmol Cs2CO3 in 1.0 mL MeCN at room temperature.After the consumption of compound 1a was detected by reaction monitoring,0.1 mmol DBU was added and the mixture was stirred for an additional 12 h.1):Isolated yield.
EntryBase 1Base 2SolventYield/%1)1K2CO3DBUMeCN512Cs2CO3DBUMeCN893NaOHDBUMeCN214KOHDBUMeCN61
通过对关键反应碱的种类、溶剂的种类、混合碱的种类的筛选后,确定最优条件为:室温下,将0.1 mmol邻羟基查尔酮(1a)、1.0 mL乙腈、0.2 mmol Cs2CO3加入到反应管中,再加入0.15 mmol γ-溴代巴豆酸酯(2a),反应监测(TLC)到原料消耗完后加入0.1 mmol DBU,在室温下搅拌12 h。然后将反应液中和后,减压除去溶剂,经柱层析分离(V(PE)∶V(EA)∶V(DCM)=20∶1∶1)后得到目标产物3a。
2.3 反应的普适性考察
在确定最佳反应条件的基础上,进一步探索了反应在邻羟基查尔酮(1)与γ-溴代巴豆酸酯(2)的底物适用性。结果表明(图6),当γ-溴代巴豆酸酯的酯基为甲酯、乙酯、苄酯时,反应均能以中等到优异的产率获得目标产物3,无论是烷基酯或芳基酯都未对反应产生明显影响。随后更换了不同的邻羟基查尔酮,不同的取代基对反应没有产生明显影响,无论是芳基(4-甲氧基苯基、3-三氟甲基苯基、萘、噻吩)还是烷基(甲基)均能以中等至优秀产率获得相应的目标产物。如图6所示的10个2,3-二取代苯并呋喃化合物,均通过本方法合成得到。
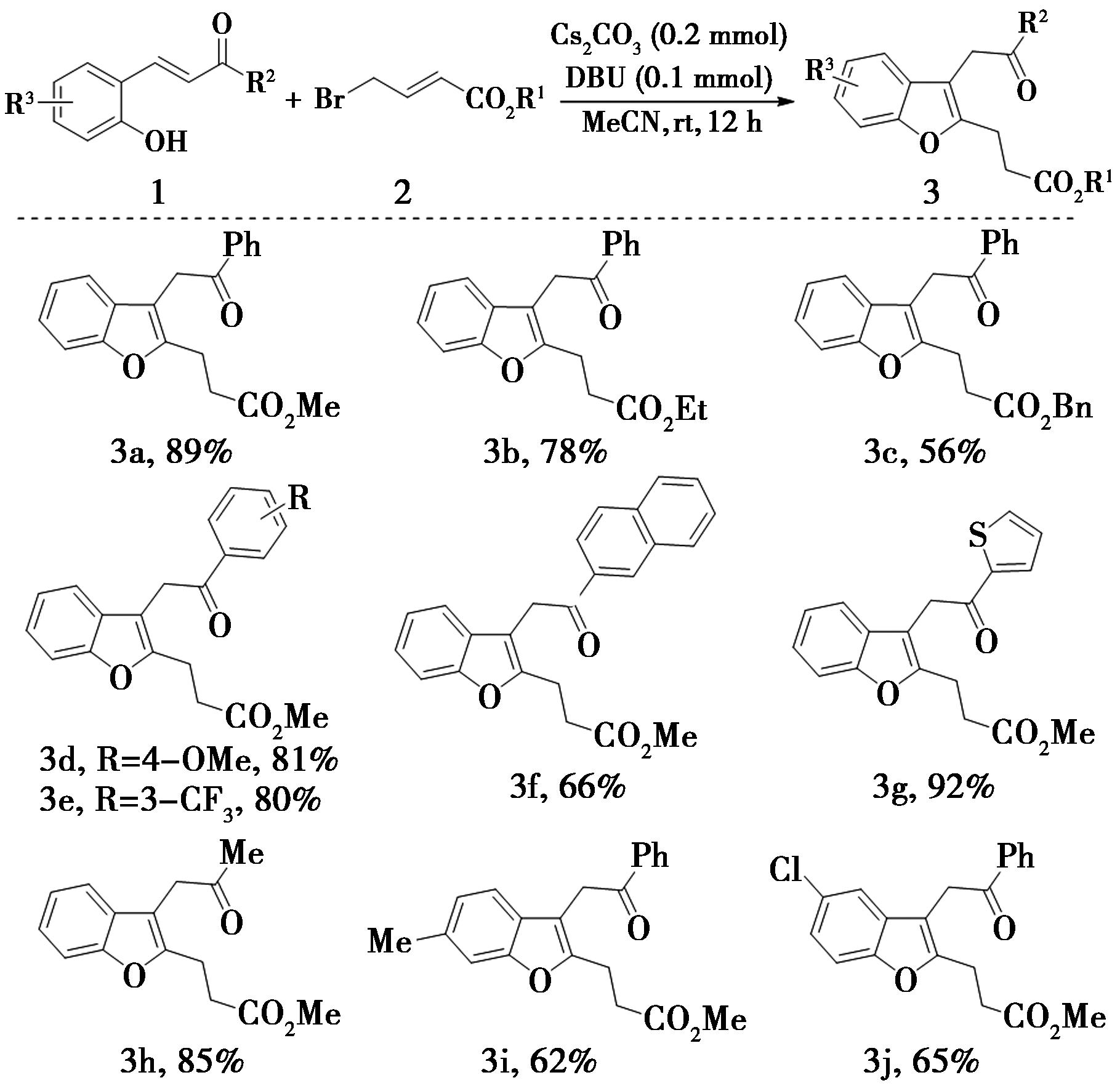
图6 底物普适性考察
Fig.6 Scope of substrates
2.4 苯并呋喃类化合物的合成机理探究
2.4.1 控制实验
通过控制实验对反应的机理进行研究(图7)。首先,以0.1 mmol邻羟基查尔酮(1a)与0.1 mmol γ-溴代巴豆酸甲酯(2a)为模板反应,在0.1 mmol Cs2CO3的作用下,以90%的产率获得化合物3a′(式1),该化合物是通过邻羟基查尔酮中的羟基氧对γ-溴代巴豆酸酯进行SN2取代反应所产生。该中间体3a′在0.1 mmol Cs2CO3的作用下,发生分子内烯丙基迈克尔加成反应,以89%的产率获得2,3-二取代二氢苯并呋喃(3a″,式2)。此外,该化合物3a″在DBU作用下,发生烯键移位,生成2,3-二取代苯并呋喃(3a,式3)。上述控制实验说明化合物3a′和3a″可能是反应过程中的中间体。
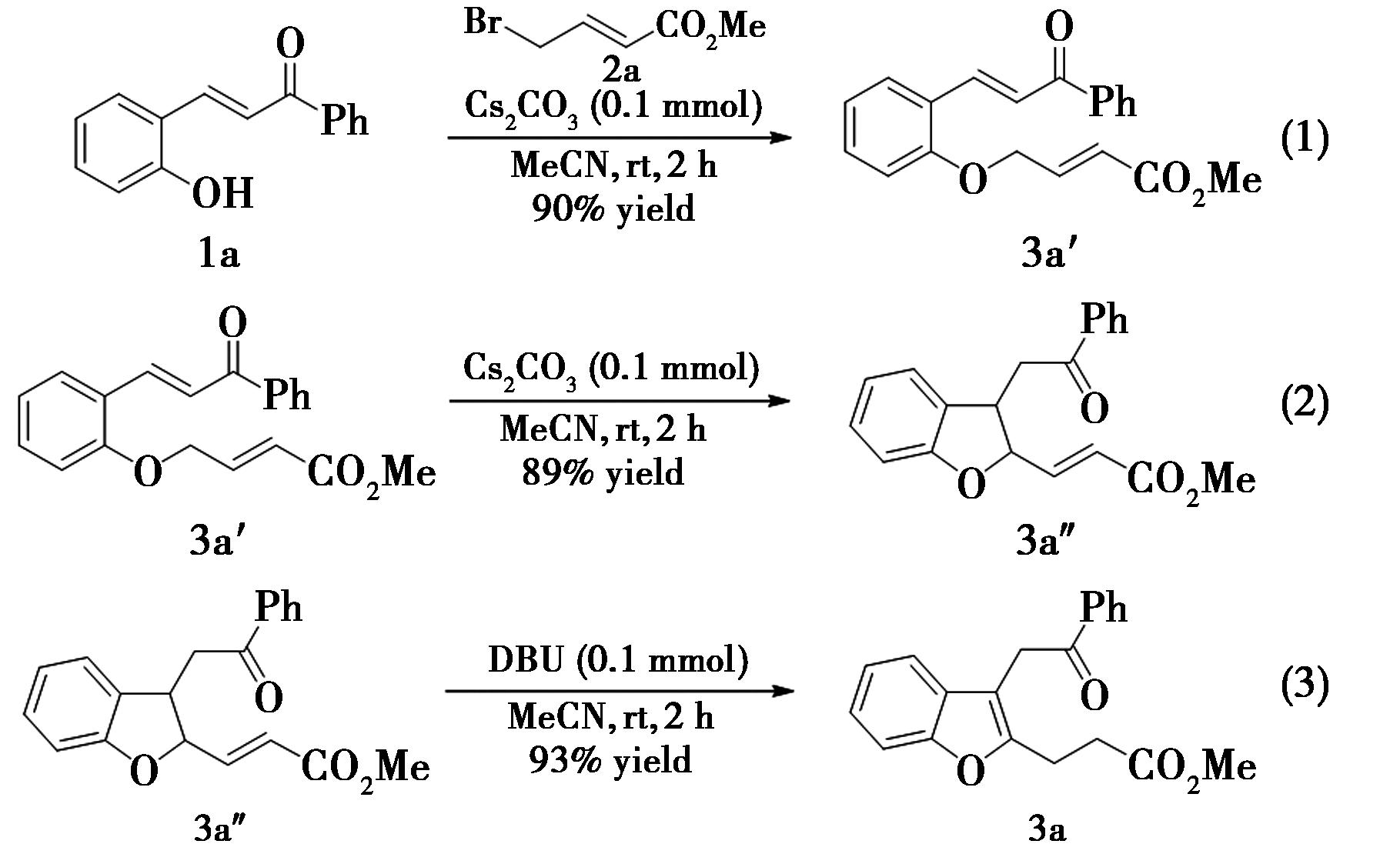
图7 控制实验
Fig.7 Control experiments
2.4.2 苯并呋喃化合物的机理推测
根据文献[19]和上述控制实验的结果,本文提出了相应的可能反应机理(图8)。首先,羟基查尔酮1a在Cs2CO3的介导下去质子化,形成氧负离子中间体Int-1,该中间体与γ-溴代巴豆酸甲酯2a发生SN2取代反应,生成化合物3a′。随后,化合物3a′在另一分子Cs2CO3的介导下去质子化,形成烯丙基负离子中间体Int-2。该中间体发生分子内烯丙基迈克尔加成反应,生成2,3-二取代二氢苯并呋喃(3a″)。最后,化合物3a″在DBU的介导下,发生烯键的移位,形成最终的芳构化产物3a。
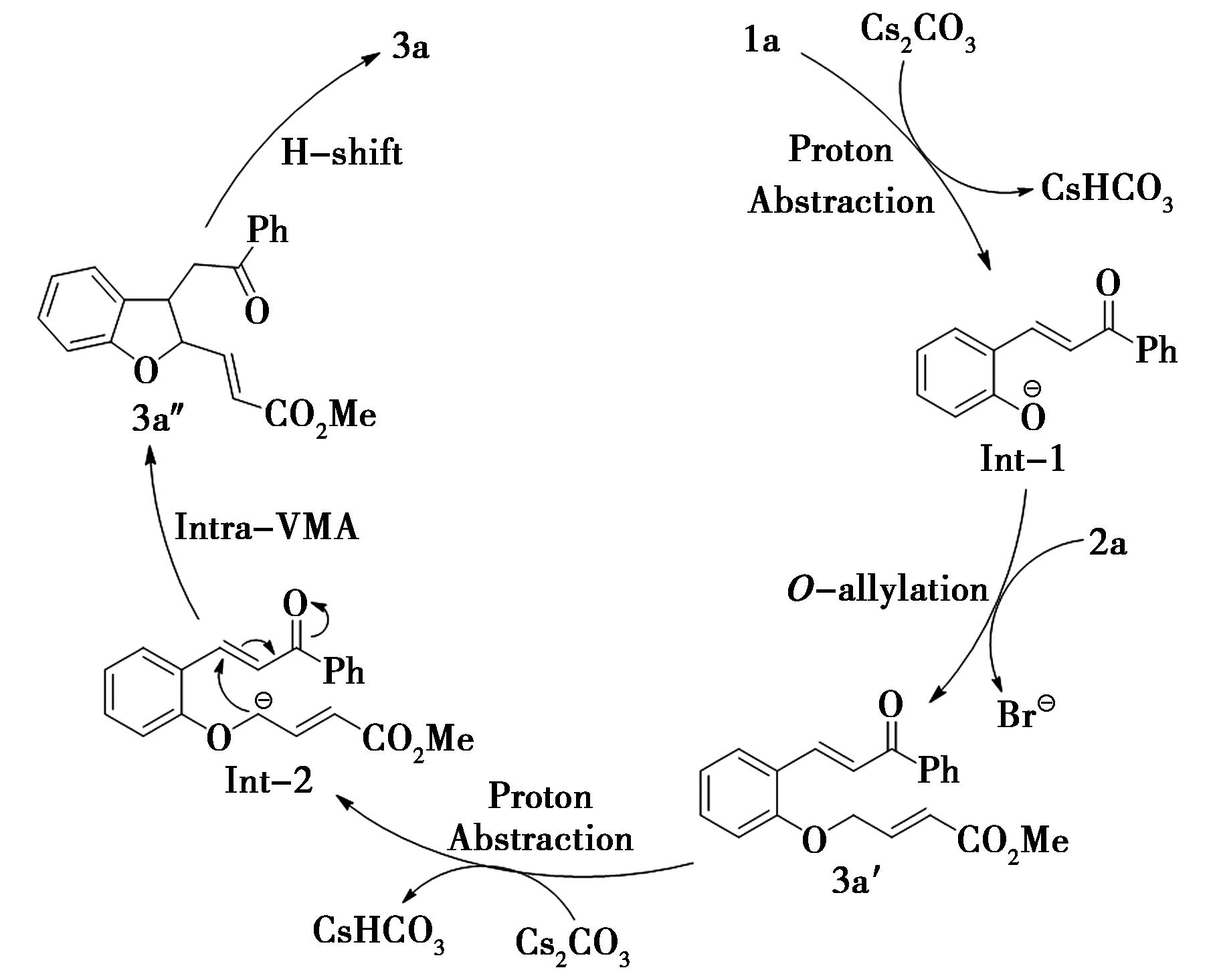
图8 可能的反应机理
Fig.8 Possible reaction mechanism
3 结论
本文报道了一种双碱协同促进下邻羟基查尔酮与γ-溴代巴豆酸酯发生串联反应高效合成 2,3-二取代苯并呋喃类化合物的方法。该合成方法可以在室温条件下进行,取代基对反应无明显影响,普适性良好,底物拓展测试合成的10个目标化合物,产率中等到优秀,为苯并呋喃的合成提供新的方法。合成的2,3-二取代苯并呋喃类化合物为相关生物活性测试提供了物质保障。
[1]Guo H F,Shao H Y,Yang Z Y,Xue S T,Li X,Liu Z Y,He X B,Jiang J D,Zhang Y Q,Si S Y,Li Z R.J.Med.Chem.,2010,53(4):1819-1829.
[2]Radadiya A,Shah A.Eur.J.Med.Chem.,2015,97:356-376.
[3]Zhou Z Y,Sun L Q,Han X Y,Wang Y J,Xie Z S,Xue S T,Li Z R.J.Med.Chem.,2023,66(3):1742-1760.
[4]Dwarakanath D,Gaonkar S L.Asian J.Org.Chem.,2022,11(8):e202200282.
[5]Jin R W,Wang L J,Song Y,Liu X P,Wang J W,Li Z X.Chin.J.Org.Chem.,2024,44(9):2742-2759.靳瑞文,王连杰,宋跃,刘小培,王俊伟,李中贤.有机化学,2024,44(9):2742-2759.
[6]Kushwaha P,Chandra R.Chem.Eur.J.,2025,31(71):e02690.
[7]Liu B,Xi X X,Tong H J,Du M,Zhang Y M.Chem.Reagents,2019,41(1):102-106.刘斌,席孝贤,仝红娟,杜漠,张彦民.化学试剂,2019,41(1):102-106.
[8]Yu J H,Huang L B.ChemCatChem,2023,15(22):e202300986.
[9]Wang Z,Xu P W,Guo S M,Daniliuc C G,Studer A.Nature,2025,642(8066):92-98.
[10]Shi C Q,Wang E H,Zhang Y X,Ma T Y,Zhang R C,Huang H,He Y,Peng Q,Feng Z.CCS Chem.,2025,DOI:10.31635/ccschem.025.202505855.
[11]Harish B,Subbireddy M,Obulesu O,Suresh S.Org.Lett.,2019,21(6):1823-1827.
[12]Chen G,Nie G J,Li L X,Fu J,Yao H,Huang N Y,Wang N Z.Org.Chem.Front.,2025,12(7):2212-2218.
[13]Hu Y,Cai Y F,Liu Y F,Xiong D,Yao H,Li L X,Cao Z Y,Huang N Y,Wang N Z.Chin.J.Chem.,2025,43(17):2181-2186.
[14]Liu Y F,Chen Y,Deng C,Yao H,Li L X,Wang L,Huang N Y,Wang N Z.Org.Lett.,2025,27(41):11503-11509.
[15]Tan M T,Zheng Y P,Zhang S,Yao H,Yan X,Zhao X,Liu M G,Huang N Y,Wang N Z.Org.Lett.,2024,26(43):9203-9209.
[16]Xiong D,Zhang S,Li Z Y,Yao H,Li L X,Huang N Y,Wang N Z.J.Org.Chem.,2025,90(17):5838-5844.
[17]Xiong D,Wang L S,Qu X X,Chen Y,Li L X,Yao H,Huang N Y,Wang N Z.Chem.Commun.,2026,62(4):1045-1057.
[18]Rouh H,Liu Y X,Katakam N,Pham L,Zhu Y L,Li G G.J.Org.Chem.,2018,83(24):15372-15379.
[19]Han X,Ye L W,Sun X L,Tang Y.J.Org.Chem.,2009,74(9):3394-3397.