肝脏作为人体代谢的核心器官,其功能的完整性与机体健康息息相关[1]。然而,在肝脏外科领域,如肝叶切除、肝移植等临床情境中,一种被称为“肝缺血再灌注损伤”(Hepatic Ischemia-Reperfusion Injury,HIRI)的病理过程,已成为影响手术成败与患者预后的关键制约因素[2]。HIRI并非简单的血流中断与恢复,而是一个涉及多分子、多细胞、多通路的复杂级联反应[3]。据统计,HIRI可导致13%的肝切除患者出现术后肝功能不全,并在肝移植中引起早期移植物功能衰竭,严重威胁患者生命[4,5]。
1 肝缺血再灌注损伤病理进展分析
1.1 肝缺血再灌注损伤的病理进程
肝缺血再灌注损伤可分为缺血期与再灌注期两个连续阶段,整个过程是从功能异常逐步发展到结构损伤的连续恶化过程[6]。
其典型过程始于缺血期—因血流阻断导致的组织氧合与营养供应中断,细胞被迫转向无氧代谢,引发ATP耗竭、细胞内酸中毒及离子稳态失衡。更为关键的是紧随其后的再灌注期,尽管血氧与营养物质得以恢复,但这一过程却如同“双刃剑”,会引发更为剧烈的氧化应激爆发、钙超载、线粒体功能障碍、无菌性炎症反应及多种形式的程序性细胞死亡,最终导致肝细胞大量凋亡或坏死,肝功能严重受损[7-10]。
1.2 肝缺血再灌注损伤生物标志物与荧光探针
深入探究HIRI的分子机制,其核心在于一系列关键生物活性分子的动态失衡。例如,ROS的爆发是再灌注损伤重要标志物[11-14],它们攻击脂质、蛋白质和DNA,直接造成细胞结构破坏。线粒体作为细胞的能量工厂和凋亡调控中心,其DNA损伤、代谢物的紊乱[15-17],也在HIRI进程中扮演重要角色。同时,细胞内微环境参数的改变,也是损伤程度的重要指标。这些生物标志物通常具有浓度低、寿命短的特点[18],导致传统的HIRI临床诊断方法,如CT或MRI影像学检查,存在明显局限性[19]。近年来,荧光探针技术在生物医学检测领域取得了革命性进展。凭借其分子量小、膜透性强等特点[20],能够深入组织内部,实现对关键生物分子的活体动态监测,为疾病的早期预警、机制研究与疗效评估提供了强有力的工具[21]。
综上所述,HIRI始于缺血期的能量代谢障碍,并在再灌注期通过氧化应激爆发进一步扰动细胞内微环境、干扰能量代谢稳态、影响气体信号分子平衡,并激活炎症与细胞死亡通路,形成复杂的损伤网络。针对这些关键环节,各类荧光探针已被开发并应用于可视化解析HIRI机制(图1)。本综述将系统阐述不同荧光探针的响应机制,总结近年来针对HIRI各类生物标志物所开发的探针及其在体外与体内成像中的应用进展[22-24],以期为该领域的后续研究提供清晰的参考方向。
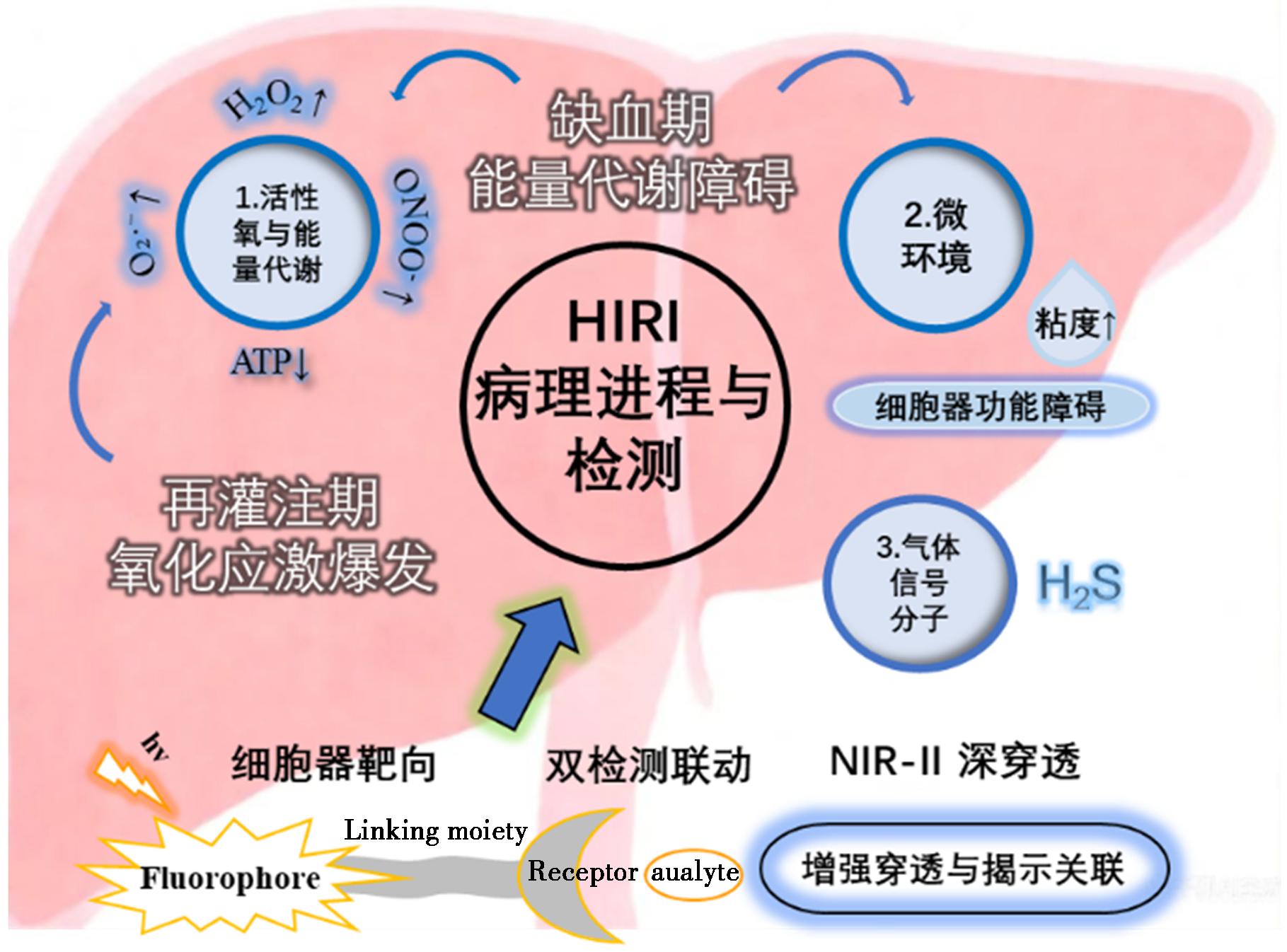
图1 HIRI病理进程与关键生物标志物检测
Fig.1 Pathological progression of HIRI and detection of key biomarkers
2 针对HIRI关键生物标志物的探针研究进展
2.1 活性氧物种与能量代谢检测探针
活性氧(ROS)的爆发与能量代谢紊乱是 HIRI进程中两个紧密耦合的核心事件。再灌注初期,大量分子氧的涌入导致超氧阴离子![]() 过氧化氢(H2O2)等[25]活性氧物种的爆发性生成,对细胞造成损伤。同时,缺血期已耗竭的ATP在再灌注期恢复有限,而线粒体功能障碍又进一步加剧了能量危机。线粒体DNA(mtDNA)作为能量合成的遗传基础,其损伤也与ROS密切相关。因此,开发能检测ROS或能量代谢物,乃至同时监测两者的探针,对于揭示HIRI机制至关重要。
过氧化氢(H2O2)等[25]活性氧物种的爆发性生成,对细胞造成损伤。同时,缺血期已耗竭的ATP在再灌注期恢复有限,而线粒体功能障碍又进一步加剧了能量危机。线粒体DNA(mtDNA)作为能量合成的遗传基础,其损伤也与ROS密切相关。因此,开发能检测ROS或能量代谢物,乃至同时监测两者的探针,对于揭示HIRI机制至关重要。
2.1.1 靶向细胞器的可逆![]() 检测探针
检测探针
这类探针通常以咖啡酸等邻苯二酚衍生物作为![]() 的可逆响应基团,通过氧化还原循环实现动态监测,并连接特定靶向基团以实现细胞器定位。
的可逆响应基团,通过氧化还原循环实现动态监测,并连接特定靶向基团以实现细胞器定位。
2013年,Tang等[26]就已经关注到![]() 在 HIRI中的关键作用,开发具有单/双光子成像能力的可逆荧光探针1(图2a)。在
在 HIRI中的关键作用,开发具有单/双光子成像能力的可逆荧光探针1(图2a)。在![]() 存在时,邻苯二酚被氧化为苯醌结构,荧光显著增强;加入还原剂后,苯醌被还原为邻苯二酚,荧光恢复至基线,实现可逆循环。该探针成功应用于肝细胞、斑马鱼及小鼠模型中,实现了缺血再灌注等生理病理过程中
存在时,邻苯二酚被氧化为苯醌结构,荧光显著增强;加入还原剂后,苯醌被还原为邻苯二酚,荧光恢复至基线,实现可逆循环。该探针成功应用于肝细胞、斑马鱼及小鼠模型中,实现了缺血再灌注等生理病理过程中![]() 波动的动态、可逆、可视化监测,这一研究为HIRI氧化应激机制提供了动态可视化的直接证据,也为后续可逆荧光探针在活性氧相关病理机制研究中的应用奠定了坚实的基础。
波动的动态、可逆、可视化监测,这一研究为HIRI氧化应激机制提供了动态可视化的直接证据,也为后续可逆荧光探针在活性氧相关病理机制研究中的应用奠定了坚实的基础。
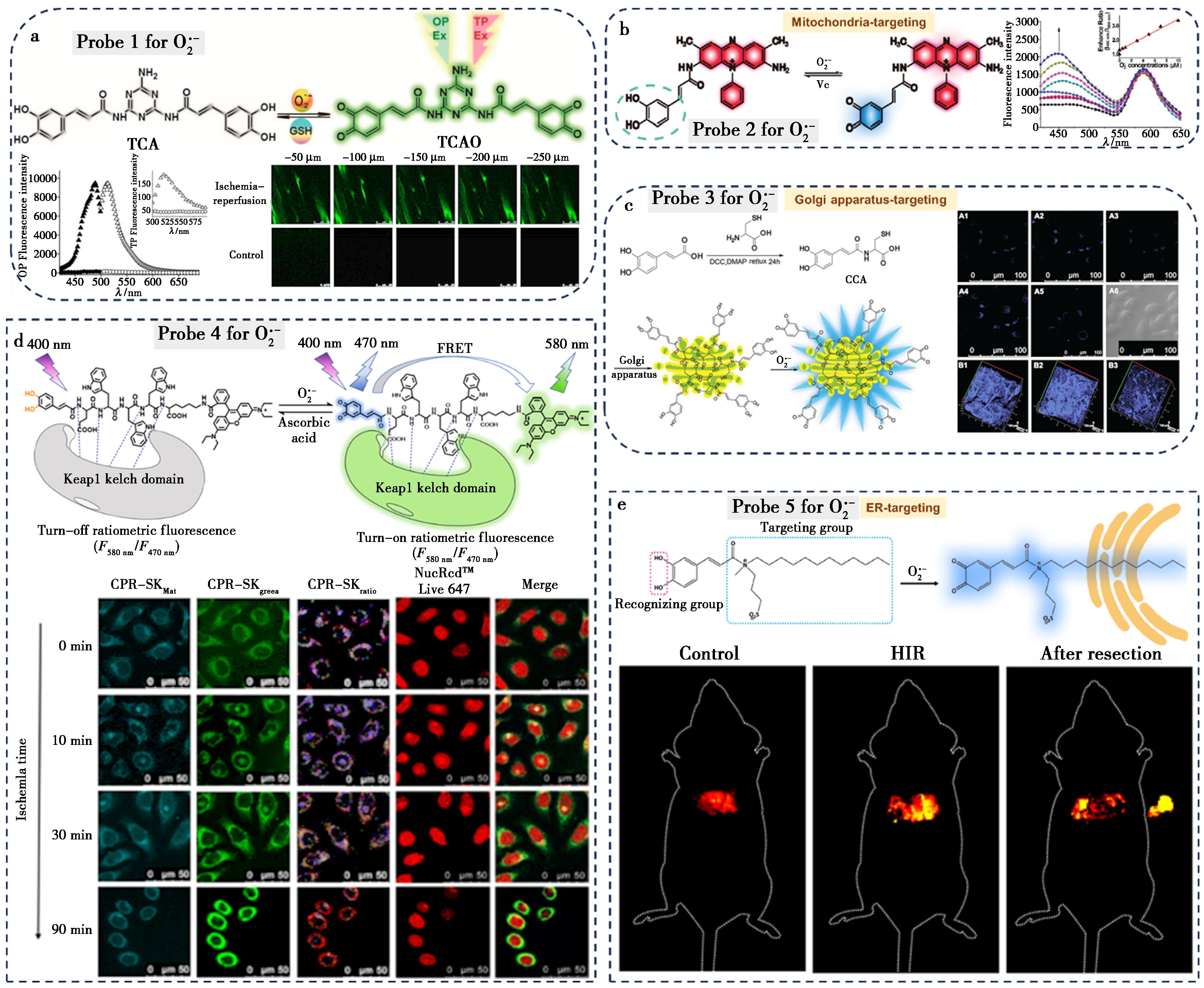
a.探针1为早期开发的单/双光子可逆探针[26];b.探针2靶向线粒体,实现比率成像[27];c.探针3靶向高尔基体[28];d.探针4靶向Keap1蛋白[29];e.探针5靶向内质网[30]
图2 用于检测![]() 的代表性荧光探针1~5化学结构化学结构及细胞器靶向策略
的代表性荧光探针1~5化学结构化学结构及细胞器靶向策略
Fig.2 Chemical structures and organelle-targeting strategies of representative reversible fluorescent probes 1~5 for superoxide anion ![]() detection
detection
2019年,Tang等[27]继续以咖啡酸作为![]() 响应基团,设计并构建了一种可用于活细胞及活体水平对线粒体
响应基团,设计并构建了一种可用于活细胞及活体水平对线粒体![]() 进行可逆成像的双光子荧光比率探针2(图2b)。在
进行可逆成像的双光子荧光比率探针2(图2b)。在![]() 氧化下发生荧光增强(450 nm)而藏红T荧光(590 nm)不变,且在线粒体膜电位变化时仍能稳定工作。借助该探针与细胞质
氧化下发生荧光增强(450 nm)而藏红T荧光(590 nm)不变,且在线粒体膜电位变化时仍能稳定工作。借助该探针与细胞质![]() 探针DHE的联合成像,研究首次在HIRI模型中发现线粒体来源的
探针DHE的联合成像,研究首次在HIRI模型中发现线粒体来源的![]() 可通过电压依赖性阴离子通道(VDAC)转运至细胞质,导致乌头酸酶失活并加剧肝损伤;进一步提出联合抑制VDAC通道与提升Mn-SOD活性可有效缓解HIRI损伤。该工作不仅阐明了一种新的
可通过电压依赖性阴离子通道(VDAC)转运至细胞质,导致乌头酸酶失活并加剧肝损伤;进一步提出联合抑制VDAC通道与提升Mn-SOD活性可有效缓解HIRI损伤。该工作不仅阐明了一种新的![]() 转运分子机制,也为HIRI的防治提供了新的策略与成像工具。
转运分子机制,也为HIRI的防治提供了新的策略与成像工具。
2019年,Tang等[28]再次聚焦于细胞器靶向,设计并构建了一种可用于活体水平对高尔基体![]() 进行实时、可逆成像的双光子荧光探针3(图2c)。在
进行实时、可逆成像的双光子荧光探针3(图2c)。在![]() 存在时,探针荧光显著增强(490 nm),并表现出良好的可逆性。研究首次发现HIRI过程中高尔基体内
存在时,探针荧光显著增强(490 nm),并表现出良好的可逆性。研究首次发现HIRI过程中高尔基体内![]() 水平显著升高,并与caspase-2表达上调及细胞凋亡增强相关。
水平显著升高,并与caspase-2表达上调及细胞凋亡增强相关。
2022年,Tang等[29]设计并构建了一种可用于活细胞水平对细胞内氧化还原状态进行成像的荧光探针4(图2d)。该探针以咖啡酸作为![]() 的响应单元,以四肽序列(EWWW)作为Keap1蛋白的靶向单元,并通过酰胺键与罗丹明B荧光团连接。
的响应单元,以四肽序列(EWWW)作为Keap1蛋白的靶向单元,并通过酰胺键与罗丹明B荧光团连接。![]() 存在时,蓝色荧光(470 nm)增强及绿色荧光(580 nm)显著增强。同时,探针通过 EWWW序列特异性锚定Keap1蛋白,实现对其亚细胞定位的实时示踪。该探针成功应用于HIRI细胞模型中氧化还原状态的动态分析揭示HIRI损伤中,
存在时,蓝色荧光(470 nm)增强及绿色荧光(580 nm)显著增强。同时,探针通过 EWWW序列特异性锚定Keap1蛋白,实现对其亚细胞定位的实时示踪。该探针成功应用于HIRI细胞模型中氧化还原状态的动态分析揭示HIRI损伤中,![]() 与Keap1的关系。2023年,Tang等[30]设计并开发了一种新型可逆荧光探针5(图2e),特异性靶向内质网(ER)可逆检测
与Keap1的关系。2023年,Tang等[30]设计并开发了一种新型可逆荧光探针5(图2e),特异性靶向内质网(ER)可逆检测 ![]() 探针结合了ER靶向基团与
探针结合了ER靶向基团与 ![]() 可逆响应基团,在活细胞及小鼠模型中实现了ER内
可逆响应基团,在活细胞及小鼠模型中实现了ER内 ![]() 的实时荧光成像。研究发现,在HIRI过程中,ER内
的实时荧光成像。研究发现,在HIRI过程中,ER内 ![]() 水平显著升高,且其来源主要与NADPH氧化酶4有关。研究揭示了一条由ER
水平显著升高,且其来源主要与NADPH氧化酶4有关。研究揭示了一条由ER ![]() 介导的NOX4-SERCA2b-caspase 4信号通路。
介导的NOX4-SERCA2b-caspase 4信号通路。
以上这些探针在特异性靶向、灵敏度、可逆性及功能设计上各有卓越表现,但其发射波长均较短,组织穿透能力弱,限制了其在深层组织活体成像中的应用,主要用于细胞、浅层组织或离体器官成像。且仍缺乏能够同时多种关键生物标志物进行监测的手段,阻碍了对HIRI病理机制的深入理解。
2.1.2 近红外与多响应ROS检测探针
近红外(特别是NIR-Ⅱ区)荧光探针和多响应探针代表了该领域的重要发展方向,它们分别致力于解决活体成像深度与对比度的难题,以及揭示复杂生物分子间的交互关系。近红外荧光探针利用更长波长的发射光,有效减少了生物组织的光子散射和自发荧光干扰,从而显著提升了活体成像的穿透深度和信噪比[31]。
随着研究不断深入,2018年,Chen等[32]设计了一种可用于活细胞及活体水平对线粒体![]() 进行比率成像的近红外荧光探针6(图3a)。该探针以近红外七甲川菁染料为荧光信号单元,三氟甲磺酰胺为
进行比率成像的近红外荧光探针6(图3a)。该探针以近红外七甲川菁染料为荧光信号单元,三氟甲磺酰胺为![]() 响应基团,通过亲脂性三苯基膦阳离子实现线粒体靶向。在
响应基团,通过亲脂性三苯基膦阳离子实现线粒体靶向。在![]() 作用下发生酰胺键断裂,吸收峰从762蓝移至606 nm,发射峰从 790 nm蓝移至742 nm,基于双通道荧光强度比实现
作用下发生酰胺键断裂,吸收峰从762蓝移至606 nm,发射峰从 790 nm蓝移至742 nm,基于双通道荧光强度比实现![]() 的定量检测。探针成功应用于细胞缺血再灌注模型,再灌注阶段线粒体
的定量检测。探针成功应用于细胞缺血再灌注模型,再灌注阶段线粒体![]() 爆发性增加,其程度与细胞凋亡指标(Ca2+超载、凋亡蛋白表达等)正相关。同时也实现了在小鼠HIRI过程中
爆发性增加,其程度与细胞凋亡指标(Ca2+超载、凋亡蛋白表达等)正相关。同时也实现了在小鼠HIRI过程中![]() 的动态监测,并验证了缺血预适应与后适应可显著降低
的动态监测,并验证了缺血预适应与后适应可显著降低![]() 爆发,减轻肝损伤。2019年,Chen等[33]继续深入近红外荧光探针的研究,设计了一种可以在HIRI模型中用于检测H2O2的近红外比率型荧光探针7(图3b)。该探针基于七甲川花菁荧光骨架,通过酯键共价连接硼酸酯识别单元构建而成。探针在与H2O2反应后发生显著光谱变化:最大吸收峰从780 nm蓝移至605 nm,荧光发射在758 nm处增强、在806 nm处减弱,形成可用于定量检测的比率型信号(F758/F806)。随着再灌注过程的延长,荧光探针在发射光谱中表现出806 nm处的荧光信号减少和758 nm处的荧光信号增加,肝细胞和小鼠HIRI模型中的荧光信号比大幅上升,实现了线粒体呼吸链与缺血再灌注过程中H2O2波动的可视化。
爆发,减轻肝损伤。2019年,Chen等[33]继续深入近红外荧光探针的研究,设计了一种可以在HIRI模型中用于检测H2O2的近红外比率型荧光探针7(图3b)。该探针基于七甲川花菁荧光骨架,通过酯键共价连接硼酸酯识别单元构建而成。探针在与H2O2反应后发生显著光谱变化:最大吸收峰从780 nm蓝移至605 nm,荧光发射在758 nm处增强、在806 nm处减弱,形成可用于定量检测的比率型信号(F758/F806)。随着再灌注过程的延长,荧光探针在发射光谱中表现出806 nm处的荧光信号减少和758 nm处的荧光信号增加,肝细胞和小鼠HIRI模型中的荧光信号比大幅上升,实现了线粒体呼吸链与缺血再灌注过程中H2O2波动的可视化。
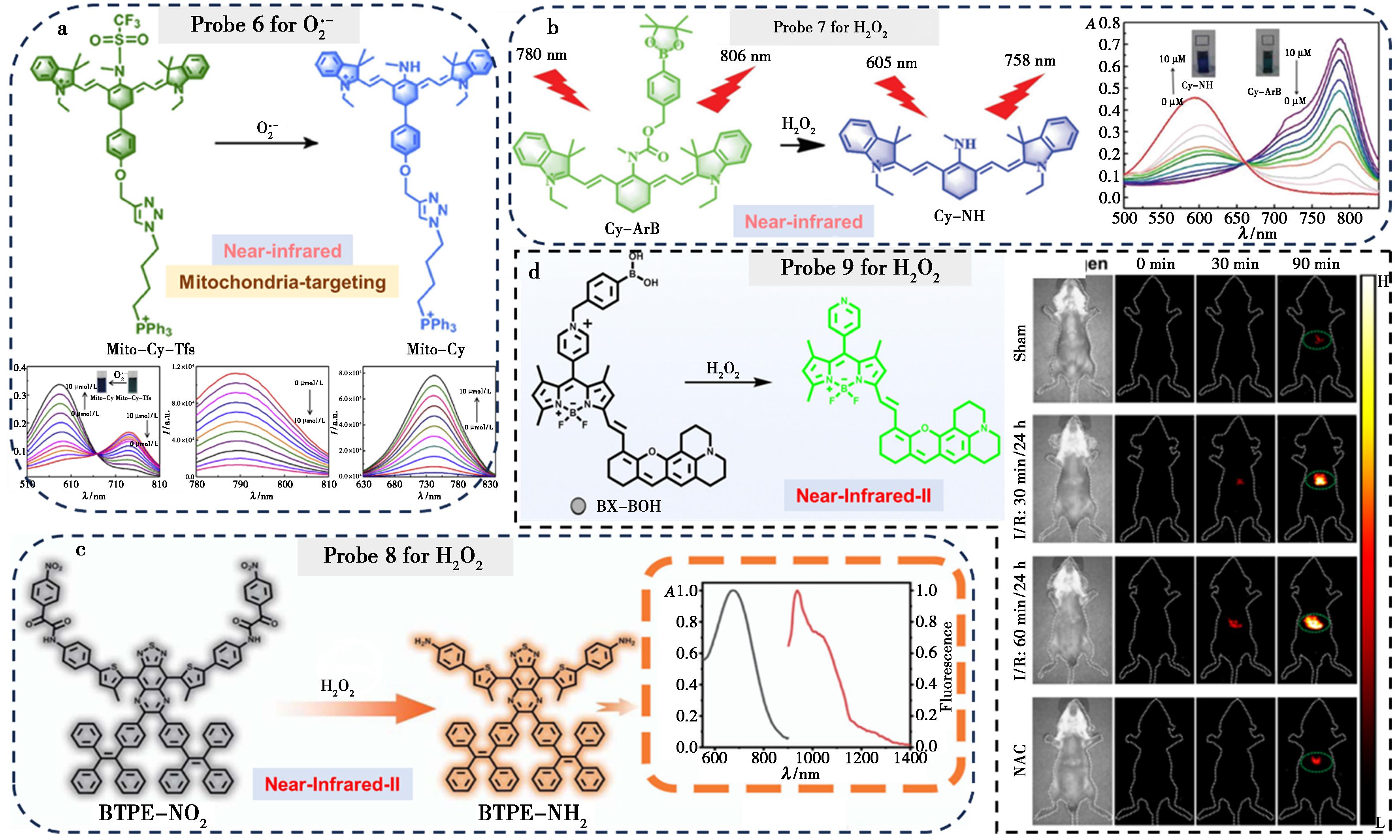
a.探针6为线粒体靶向的![]() 比率型近红外探针[32];b.探针7为H2O2比率型近红外探针[33];c.探针8为H2O2激活的NIR-Ⅱ荧光/光声双模态探针[34];d.探针9为NIR-Ⅱ荧光/光声双模态探针[21]
比率型近红外探针[32];b.探针7为H2O2比率型近红外探针[33];c.探针8为H2O2激活的NIR-Ⅱ荧光/光声双模态探针[34];d.探针9为NIR-Ⅱ荧光/光声双模态探针[21]
图3 近红外及多响应型荧光探针6~9化学结构与靶向策略
Fig.3 Chemical structures and targeting strategies of near-infrared and near-infrared and multiresponsive fluorescent probes 6~9
2021年,Chen等[34]设计了一种可在间质性膀胱炎及肝缺血再灌注损伤等模型中对H2O2进行激活型双模态成像的近红外二区探针8(图3c)。该探针以苯并噻二唑为核心,通过引入硝基苯氧乙酰胺作为H2O2响应基团与荧光淬灭单元。进一步经两亲性聚合物包裹,形成水分散性好、生物相容性高的纳米颗粒。在疾病部位H2O2作用下,探针激活并释放出强NIR-Ⅱ荧光发射(950~1200 nm)及光声信号,实现高对比度的NIR-Ⅱ荧光成像与多光谱光声断层扫描双模态成像。该探针成功应用于小鼠模型中药物性肝损伤、肝缺血再灌注损伤及间质性膀胱炎的精准诊断与病灶三维定位,展现出优异的激活特异性、深层组织穿透能力及高信噪比成像性能。
2023年,Zeng等[21]报道了一种可在HIRI模型中对H2O2进行激活型双模态成像的纳米探针9(图3d)。该探针以BODIPY型NIR-Ⅱ染料为核心,引入甲基苯基硼酸酯作为H2O2响应基团,并利用季铵化吡啶的强吸电子效应实现荧光猝灭。探针进一步以牛血清白蛋白为基质进行包覆,形成水分散性良好、生物相容性高的纳米颗粒。在肝损伤区域病理水平H2O2作用下,硼酸酯被切割,季铵化吡啶转变为中性吡啶,探针激活并产生显著的NIR-Ⅱ荧光信号和光声信号,实现高对比度的NIR-Ⅱ荧光成像与多光谱光声断层扫描双模态成像。该探针成功应用于小鼠HIRI损伤模型的早期检测与损伤程度评估,并可通过抗氧化剂预处理验证其信号特异性,展现良好的H2O2可视化能力。
多响应探针则通过集成多个识别单元,能够同时或顺序响应两种及以上生物标志物,为解析HIRI等复杂病理过程中的分子网络提供新的工具。
2019年,Tang等[35]设计合成第一个![]() 双色双光子荧光探针10(图4a)。该探针结合咖啡酸作为
双色双光子荧光探针10(图4a)。该探针结合咖啡酸作为![]() 可逆响应基团与Cy5作为ONOO-响应基团,在单波长(800 nm)双光子激发下实现蓝/红双通道荧光信号同步输出。研究首次在HIRI模型中观察到线粒体
可逆响应基团与Cy5作为ONOO-响应基团,在单波长(800 nm)双光子激发下实现蓝/红双通道荧光信号同步输出。研究首次在HIRI模型中观察到线粒体![]() 与ONOO-的协同升高。进一步通过蛋白质组学分析,发现ONOO-可使精氨酸酶1的3个酪氨酸残基发生硝化修饰,导致其活性降低;而精氨酸酶1的抑制又进一步促进ONOO-生成,形成恶性循环,加剧细胞内氧化还原失衡与HIRI损伤。
与ONOO-的协同升高。进一步通过蛋白质组学分析,发现ONOO-可使精氨酸酶1的3个酪氨酸残基发生硝化修饰,导致其活性降低;而精氨酸酶1的抑制又进一步促进ONOO-生成,形成恶性循环,加剧细胞内氧化还原失衡与HIRI损伤。
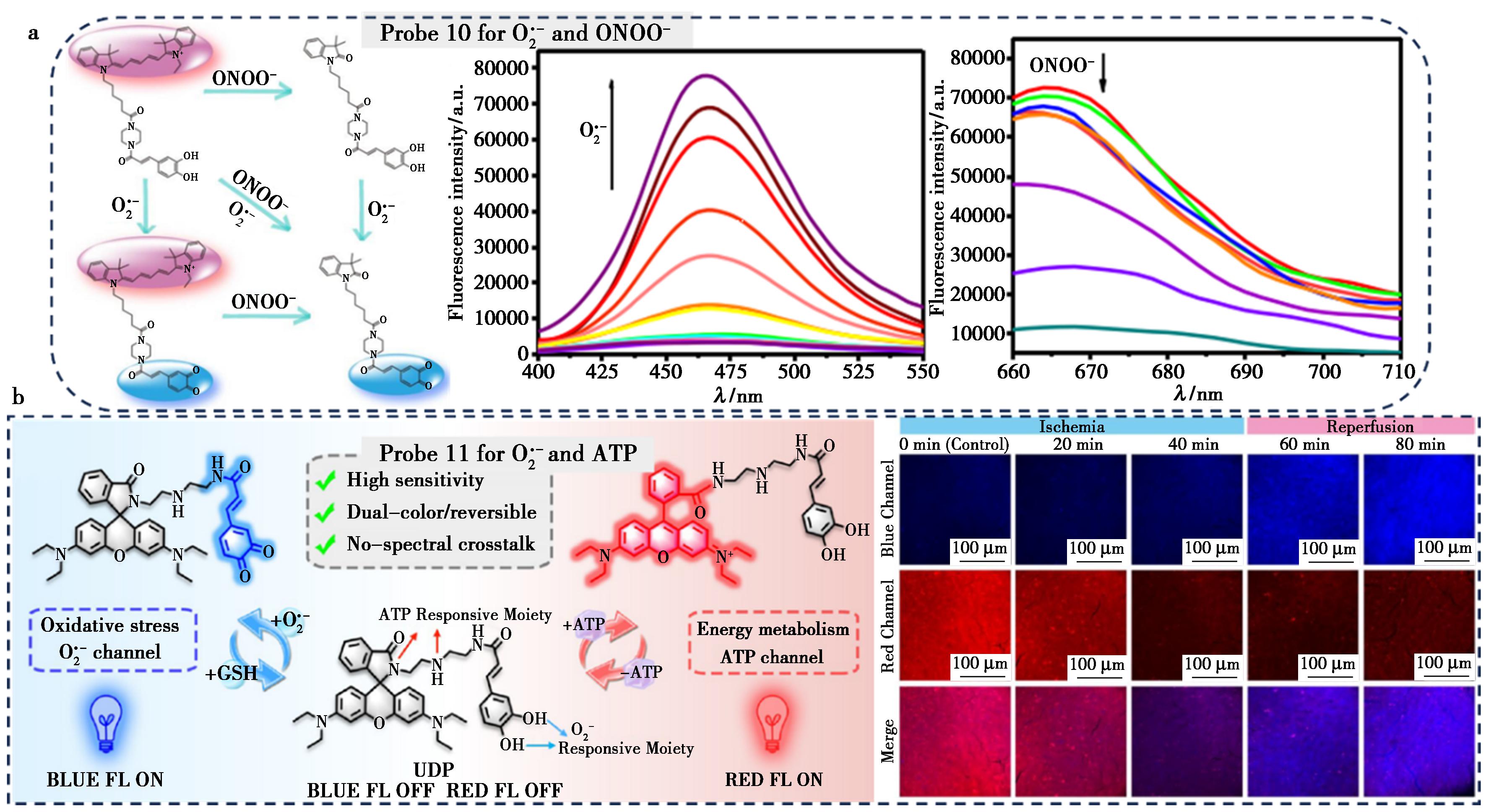
a.探针10为![]() 双色双光子荧光探针[35];b.探针11为
双色双光子荧光探针[35];b.探针11为![]() 可逆双色成像探针[37]
可逆双色成像探针[37]
图4 用于HIRI多生物标志物同步成像的双响应荧光探针10、11化学结构与靶向策略
Fig.4 Chemical structures and targeting strategies of dual-response fluorescent probes 10,11 for simultaneous imaging of multiple biomarkers in HIRI
ATP的消耗是HIRI的一个重要标志[36]。消耗ATP会诱导细胞内钙超载,并导致一系列病理事件,例如线粒体通透性转换孔开放,促进细胞凋亡。要精确解析损伤的进程,就需要捕捉ATP在细胞中的动态过程。
2023年,Tang等[37]设计了一种可用于活体水平对![]() 和ATP进行可逆双色成像的荧光探针11(图4b)。该探针以咖啡酸和罗丹明螺内酰胺分别作为
和ATP进行可逆双色成像的荧光探针11(图4b)。该探针以咖啡酸和罗丹明螺内酰胺分别作为![]() 和ATP的识别单元。借助该探针,研究首次原位可视化HIRI过程中肝细胞及小鼠肝脏内
和ATP的识别单元。借助该探针,研究首次原位可视化HIRI过程中肝细胞及小鼠肝脏内![]() 爆发与ATP耗竭的时空协同变化,并观察到再灌注期ATP的轻微恢复。首次揭示了HIRI中一条由
爆发与ATP耗竭的时空协同变化,并观察到再灌注期ATP的轻微恢复。首次揭示了HIRI中一条由![]() 触发的信号通路:过量
触发的信号通路:过量![]() 氧化修饰SDH的关键氨基酸残基→导致SDH失活→降低线粒体NADH水平→抑制线粒体ATP合成→最终导致胞内ATP耗竭。该工作不仅从分子层面阐明了氧化应激与能量代谢紊乱之间的关联与协同作用机制。
氧化修饰SDH的关键氨基酸残基→导致SDH失活→降低线粒体NADH水平→抑制线粒体ATP合成→最终导致胞内ATP耗竭。该工作不仅从分子层面阐明了氧化应激与能量代谢紊乱之间的关联与协同作用机制。
2.1.3 能量代谢检测探针
线粒体作为细胞的“能量工厂”,其功能的完整性与代偿能力是决定细胞命运的关键。缺血期,线粒体氧化磷酸化功能衰竭ATP合成骤减;再灌注期,功能失调的线粒体又成为活性氧爆发的主要源头,并通过凋亡因子等途径,启动细胞的不可逆损伤程序。因此,线粒体功能的代偿与失代偿,直接决定了肝细胞在HIRI中的命运。
2021年,Tang等[38]设计了线粒体靶向荧光探针12(图5a),在活体水平上监测mtDNA的动态变化。该探针通过吡啶鎓基团实现对线粒体膜的靶向,与mtDNA结合后产生荧光信号。研究首次在HIRI损伤模型中实时、动态地观察到了 mtDNA损伤随着HIRI进程而恶化,证实了该过程是由ROS爆发所介导,进而揭示了ROS→mtDNA损伤这一在HIRI损伤中的关键信号通路。同时建立了一种药物筛选平台,成功筛选出两种对HIRI损伤具有显著保护作用的潜在药物。该工作为理解mtDNA相关疾病机制及开发新型治疗策略提供了重要见解。
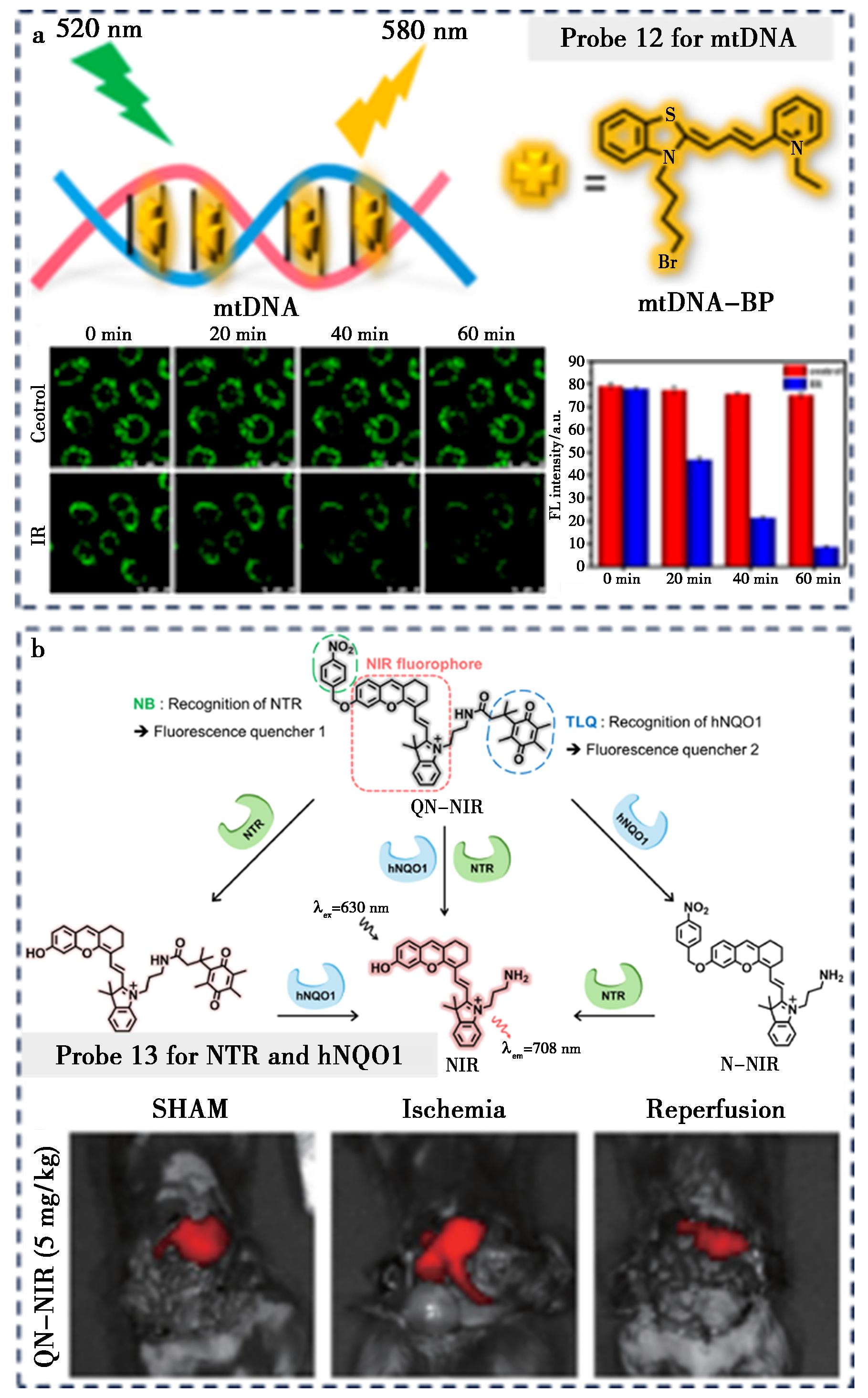
a.探针12为线粒体靶向的mtDNA荧光探针[38];b.探针13为双酶激活近红外荧光探针[39]
图5 针对HIRI能量代谢标志物的荧光探针12、13化学结构与靶向策略
Fig.5 Chemical structures and targeting strategies of fluorescent probes 12,13 targeting energy metabolism biomarkers in HIRI
之前的研究主要集中在检测HIRI过程中产生的ROS与线粒体的损伤上,但对以缺氧为特征的缺血性损伤的特异性检测仍处于探索之中。
2025年,Hong等[39]开发了一种可用于活体水平对肝缺血进行实时、特异性成像的双酶激活近红外荧光探针13(图5b)。该探针以半花菁为近红外荧光团,通过引入TLQ和NB两个响应基团,分别靶向缺氧相关还原酶hNQO1和硝基还原酶。正常条件下,探针的荧光被有效淬灭;而在缺血缺氧条件下,hNQO1和NTR的活性上调,依次或同时切割TLQ与NB基团,产生近红外荧光响应。双酶激活策略有效降低了背景干扰,实现了高信噪比的成像。在细胞水平,探针成功监测了CoCl2诱导的缺氧状态下hNQO1/NTR活性的上调,并通过抑制剂和CRISPR切割实验证实了其双酶依赖的激活机制;在活体小鼠肝缺血模型中,实现了缺血阶段的特异性成像,并能有效区分缺血与再灌注损伤。该研究为基于缺氧酶标志物的疾病检测与干预策略开辟了新途径。该类探针通过集成多个识别单元,实现了对复杂病理网络中关键分子的同步监测。
2.2 微环境参数检测探针
物理微环境是反映细胞功能状态、评估损伤程度的重要指标[40]。其中,粘度与细胞器功能障碍及组织损伤进展密切相关。损伤期间,氧化还原平衡紊乱不仅攻击生物大分子,还影响亚细胞器的结构与功能[41]。线粒体功能障碍可导致其基质粘度升高,ATP合成受阻[42]。溶酶体粘度增加则会削弱自噬能力,导致毒性物质堆积[43,44]。因此,检测肝细胞内特定细胞器的粘度变化,对于早期识别损伤组织、揭示损伤机制具有重要意义。
2022年,Tang等[45]开发了一种基于溶酶体粘度激活的近红外二区(NIR-Ⅱ)荧光探针14(图6a),用于HIRI的精准导航。该探针采用刚性花菁染料设计,通过限制分子内旋转实现粘度响应性荧光增强(13倍),在864 nm处具有显著的NIR-Ⅱ发射。研究揭示了HIRI中的ROS-丙二醛(MDA)-组织蛋白酶B信号通路,并证实溶酶体粘度是HIRI精确成像的理想生物标志物。
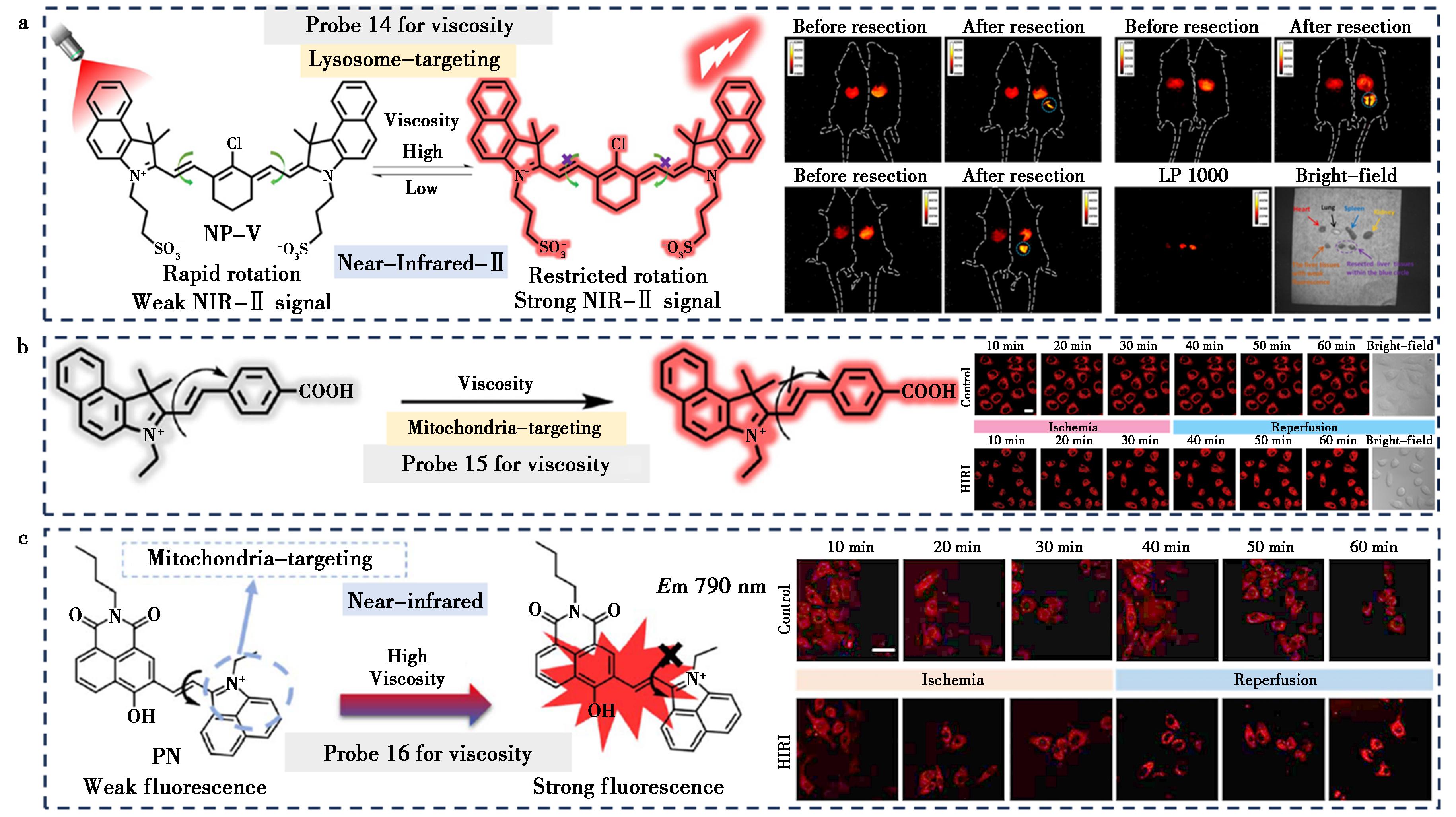
a.探针14为溶酶体靶向的NIR-Ⅱ粘度激活荧光探针[45];b.探针15为线粒体靶向粘度敏感荧光探针[46];c.探针16为基于ICT机制的近红外线粒体粘度探针[47]
图6 用于检测HIRI微环境粘度变化的荧光探针14~16化学结构与靶向策略
Fig.6 Chemical structures and targeting strategies of fluorescent probes 14~16 for detecting changes in microenvironmental viscosity HIRI
2023年,Xie等[46]开发了一种用于HIRI细胞模型中检测粘度的线粒体靶向荧光探针15(图6b)。该探针基于2,3,3-三甲基-3H-吲哚结构,通过引入4-羰基苯甲醛基团,在粘度升高时表现出约21倍的荧光增强。探针成功用于检测药物刺激下细胞内线粒体粘度的变化,实现了对HIRI期间线粒体粘度的实时成像。与DCFH-DA的共成像研究发现HIRI过程中线粒体内ROS的增加与线粒体粘度的升高密切相关。
2024年,Chen等[47]开发了一种基于ICT机制的新型近红外探针16(图6c),用于监测HIRI过程中线粒体粘度的动态变化。该探针以1,8-萘酰亚胺衍生物为供体,苯并[c,d]吲哚盐为电子受体,在粘度升高时表现出32倍的荧光增强。研究证实其能够检测制霉菌素诱导的活细胞粘度变化,并成功应用于HIRI细胞与小鼠模型的实时成像。结果表明,探针通过区分正常与损伤肝细胞的线粒体粘度差异,为HIRI的早期识别提供依据。
该类探针通过粘度诱导的分子内旋转受限或ICT效应实现荧光增强,为HIRI早期诊断及细胞器功能障碍研究提供工具。
2.3 气体信号分子检测探针
低浓度的H2S在一定程度上可以通过减少氧化应激和改善能量代谢来保护线粒体[48]免受HIRI的影响,增强细胞生物能,反之则加速损伤。
2024年,Fang等[49]设计了线粒体靶向、H2S激活型荧光探针17(图7a),用于在活体水平上对线粒体H2S原位成像。该探针采用基于萘的D-π-A分子结构,其芳香基叠氮单元作为H2S特异性响应基团,吡啶鎓阳离子则同时作为线粒体靶向单元和荧光淬灭的电子受体。与H2S反应后,释放出具有强分子内电荷转移特性的荧光团,从而在602 nm处产生明显的荧光。研究在HIRI中,首次实现了对线粒体H2S动态变化的原位追踪,发现H2S水平在缺血期升高,而在再灌注期下降。
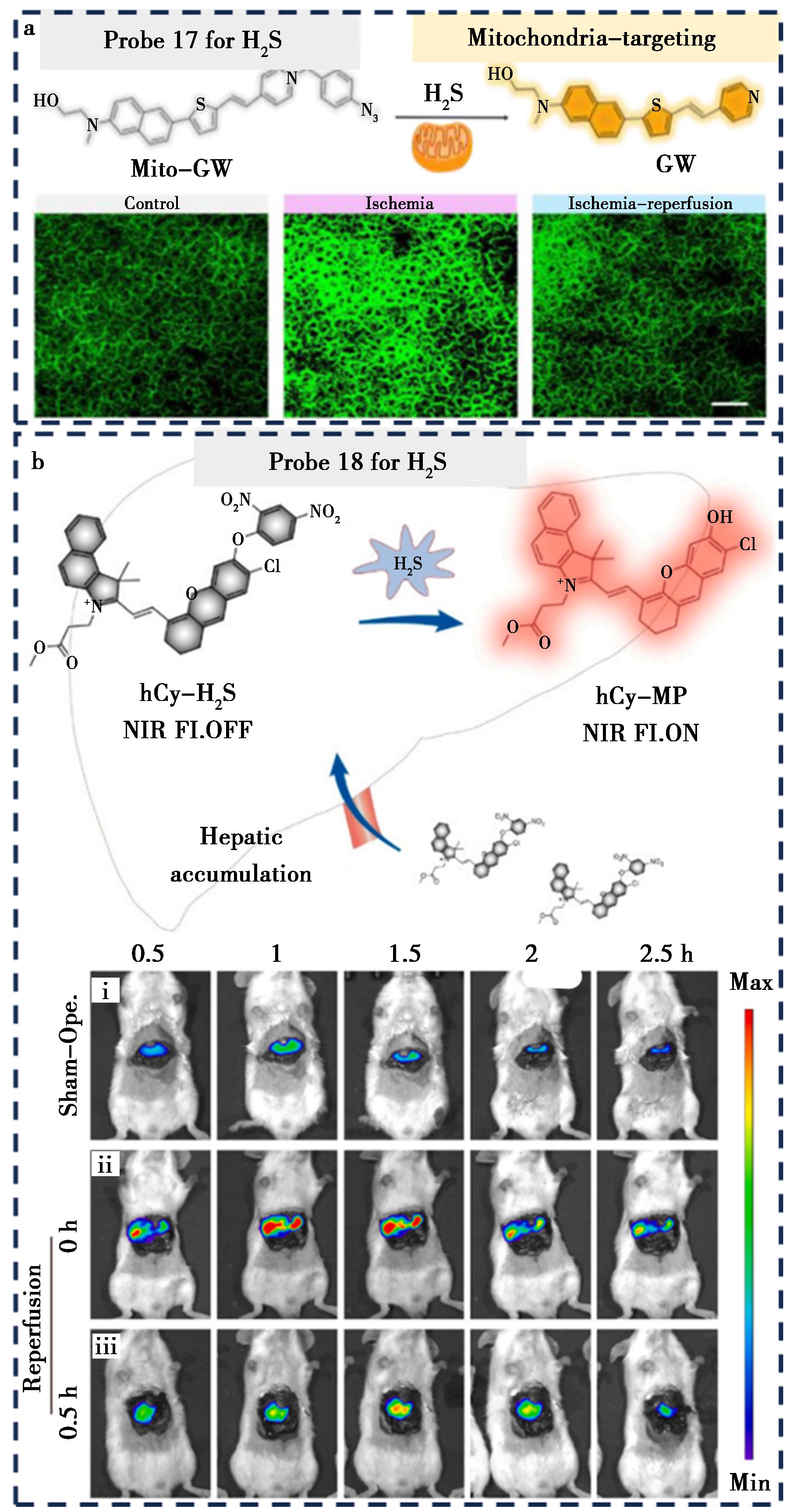
a.探针17为线粒体靶向H2S激活荧光探针[49];b.探针18为肝脏富集型近红外H2S荧光探针[50]
图7 用于检测气体信号分子硫化氢(H2S)的荧光探针17、18化学结构与靶向策略
Fig.7 Chemical structures and targeting strategies of fluorescent probes 17,18 for detecting the gas signaling molecule hydrogen sulfide (H2S) in HIRI
2025年,Xiong等[50]设计一种可用于活体水平对肝组织中H2S成像的近红外荧光探针18(图7b)。该探针以半菁染料hCy-MP为信号单元,通过2,4-二硝基苯醚作为H2S响应基团,在H2S作用下DNP被切断释放出发光基团,实现近红外荧光信号的显著增强。探针因其疏水性结构在肝脏中优先富集,研究在HIRI小鼠模型中实现了H2S水平的动态监测,并发现H2S在缺血阶段上调、再灌注阶段被大量消耗的现象。H2S检测探针不仅可用于揭示HIRI的病理机制,还有望用于未来HIRI保护药物的体内药效评价。
3 结论
本综述系统总结了针对HIRI关键生物标志物(如活性氧物种、能量代谢、微环境参数及气体信号分子等)所开发的各类荧光探针,阐述了其设计策略、响应机制及在细胞、动物模型中的应用成果。这些探针不仅实现了对HIRI病理过程中关键信号的实时、原位成像,还揭示了氧化应激与能量代谢紊乱之间的关联、细胞器特异性损伤机制以及气体信号分子的动态调节规律,为研究者提供对HIRI病理机制更全面的理解。
尽管该领域已取得重要进展,但仍面临探针可逆性不足、组织穿透深度有限、多参数检测能力薄弱以及临床转化难度大等挑战。未来,通过发展新型可逆响应机制、近红外二区、多通道联合检测,荧光探针有望在HIRI的早期诊断、机制研究、药物开发及临床治疗中发挥更加关键的作用,最终推动HIRI诊治向精准化、可视化方向发展。
[1]Trefts E,Gannon M,Wasserman D H.Curr.Biol.,2017,27(21):R1147-R1151.
[2]Zhai Y,Petrowsky H,Hong J C,Busuttil R W,Kupiec-weglinski J W.Nat.Rev.Gastroenterol.Hepatol.,2013,10(2):79-89.
[3]Eltzschig H K,Eckle T.Nat.Med.,2011,17(11):1391-1401.
[4]Hammond J S,Guha I N,Beckingham I J,Lobo D N.Br.J.Surg.,2011,98(9):1188-1200.
[5]Abt P L,Desai N M,Crawford M D,Forman L M,Markmann J W,Olthoff K M,Markmann J F.Ann.Surg.,2004,239(1):87-92.
[6]Guan Y,Yao W F,Yi K,Zheng C X,Lv S X,Tao Y,Hei Z Q,Li M Q.Small,2021,17(23):2007727.
[7]Lorenzen J M,Batkai S,Thum T.Free.Radic.Biol.Med.,2013,64:78-84.
[8]Zulihumaer R.Standard Living,2025,9:106-108.祖丽胡玛尔·热依木.标准生活,2025,9:106-108.
[9]Blaustein M P,Lederer W J.Physiol.Rev.,1999,79(3):763-854.
[10]Vander H M G,Cantley L C,Thompson C B.Science,2009,324(5930):1029-1033.
[11]Fang B,Wang L M,Li H Q,Zhang J X,Ding Y,Li P P,Peng B,Bai H,Li L.Sci.China Chem.,2025,68(1):297-307.
[12]Lee J,Mun S J,Shin Y,Lee S,Son M J.Arch.Pharm.Res.,2022,45(6):390-400.
[13]Li W,Shen Y,Gong X Y,Zhang X B,Yuan L.Anal.Chem.,2021,93(49):16673-16682.
[14]Mun S J,Ryu J S,Lee M O,Son Y S,Oh S J,Cho H S,Son M Y,Kim D S,Kim S J,Yoo H J,Lee H J,Kim J,Jung C R,Chung K S,Son M J.J.Hepatol.,2019,71(5):970-985.
[15]Yao S K,Wu Z L,Zhang Y M,Yang T,Yuan H,Ding W Z,He W J,Guo Z J,Chen Y C.CCS Chem.,2025,7(2):596-609.
[16]Sanderson T H,Reynolds C A,Kumar R,Przyklenk K,Hüttemann M.Mol.Neurobiol.,2013,47(1):9-23.
[17]Armstrong P W,Boden W E.Ann.Intern.Med.,2011,155(6):389-391.
[18]Dhalla N S,Panagia V,Singal P K,Makino N,Dixon I M C,Eyolfson D A.J.Mol.Cell.Cardiol.,1988,20:3-13.
[19]Ippolito D,Inchingolo R,Grazioli L,Drago S G,Nardella M,Gatti M,Faletti R.World J.Gastroenterol.,2018,24(23):2413-2426.
[20]Wang H,Wen N,Li P,Xiu T C,Shang S Q,Zhang W,Zhang W,Qiao J N,Tang B.Talanta,2024,270:125532.
[21]Zeng Z,Chen J J,Sun L H,Zeng F,Wu S Z.Chem.Commun.,2023,59(5):571-574.
[22]Guo Q Y,Liu A J,Huang Y H,Ding J Y,Ding J J,Wang L M,Ding Y,Peng B,Li L,Fang B,Jiang S,Bai H.Chin.Chem.Lett.,2025,36(12):110943.
[23]Jing X Y,Han S,Yang Y,Lai Y B,Lin W Y.Coord.Chem.Rev.,2025,534:216607.
[24]Wu L L,Li Z L,Wang K,Groleau R R,Rong X D,Liu X T,Liu C Y,Lewis S E,Zhu B C,James T D.J.Am.Chem.Soc.,2025,147(11):9001-9018.
[25]Dickinson B C,Chang C J.Nat.Chem.Biol.,2011,7(8):504-511.
[26]Zhang W,Li P,Yang F,Hu X F,Sun C Z,Zhang W,Chen D Z,Tang B.J.Am.Chem.Soc.,2013,135(40):14956-14959.
[27]Zhang W,Su D,Li P,Zhang J,Liu J H,Wang H,Zhang W,Tang B.Chem.Commun.,2019,55(72):10740-10743.
[28]Zhang W,Zhang J,Li P,Liu J H,Su D,Tang B.Chem.Sci.,2019,10(3):879-883.
[29]Zhang W,Zhou C M,Li P,Liu J H,Wang X,Zhang W,Wang H,Tang B.Anal.Chem.,2022,94(36):12352-12359.
[30]Zhang W,Fan W J,Wang X,Li P,Zhang W,Wang H,Tang B.Anal.Chem.,2023,95(21):8367-8375.
[31]Liu M,Ma Z C,Liu H,Tian Z Y.Infrared,46(11):36-63.刘明,马哲骋,刘恒,田志远.红外,46(11):36-63.
[32]Han X Y,Wang R,Song X Y,Yu F B,Lv C J,Chen L X.Biomaterials,2018,156:134-146.
[33]Xu R F,Wang Y,You H Y,Zhang L W,Wang Y Q,Chen L X.Analyst,2019,144(8):2556-2564.
[34]Chen J J,Chen L Q,Wu Y L,Fang Y C,Zeng F,Wu S Z,Zhao Y L.Nat.Commun.,2021,12(1):6870.
[35]Zhang W,Liu J H,Li P,Wang X,Bi S M,Zhang J,Zhang W,Wang H,Tang B.Biomaterials,2019,225:119499.
[36]Fukunaga N,Ribeiro R V P,Bissoondath V,Billia F,Rao V.Transplant.Proc.,2022,54(8):2357-2363.
[37]Liu J H,Zhang W,Wang X,Ding Q,Wu C C,Zhang W,Wu L L,James T D,Li P,Tang B.J.Am.Chem.Soc.,2023,145(36):19662-19675.
[38]Zhang W,Bi S M,Li P,Liu J H,Zhou C M,Wang X,Zhang W,Wang H,Tang B.Anal.Chem.,2021,93(14):5782-5788.
[39]Hong S J,Lee H,Lee E J,Kim M,Ryu H J,Koo J H,Lee M H.ACS Sens.,2025,10(8):6074-6083.
[40]Tang Y,Kong W N,Zhao J W,Chen Y,Liu L,Zhang G Y.Ultrasound.Med.Biol.,2020,46(9):2464-2471.
[41]Glantzounis G K,Salacinski H J,Yang W X,Davidson B R,Seifalian A M.Liver Transplant.,2005,11(9):1031-1047.
[42]Chen B C,Mao S M,Sun Y Y,Sun L Y,Ding N,Li C D,Zhou J.Chem.Commun.,2021,57(36):4376-4379.
[43]Devany J,Chakraborty K,Krishnan Y.Nano Lett.,2018,18(2):1351-1359.
[44]Wang L,Xiao Y,Tian W M,Deng L Z.J.Am.Chem.Soc.,2013,135(8):2903-2906.
[45]Liu J H,Zhang W,Zhou C M,Li M M,Wang X,Zhang W,Liu Z Z,Wu L L,James T D,Li P,Tang B.J.Am.Chem.Soc.,2022,144(30):13586-13599.
[46]Xie D C,Ma W C,Wang C,Zhang W P,Ding Z Y.Chem.Commun.,2023,59(8):1030-1033.
[47]Chen X,Jiang Z L,Wang Z Y,He F L,Fu M L,Xie Z D,Hu J F.RSC Adv.,2024,14(16):11151-11156.
[48]Paul B D,Snyder S H,Kashfi K.Redox Biol.,2021,38:101772.
[49]Fang B,Yang J Q,Wang L M,Li H Q,Guo J Y,Zhang J X,Guo Q Y,Peng B,Liu K D,Xi M M,Bai H,Fu L,Li L.Chin.Chem.Lett.,2024,35(6):108913.
[50]Xiong S Q,Liang W E,Chen X Q,Zhang Y,Bian Y N,Su D D.Sens.Actuat.B Chem.,2025,441:138012.