天然产物因其高度演化的结构差异性与固有的多维化学复杂性,成为探索生物作用机制和药物创新不可替代的资源库。据统计,约49%的已上市药物来源于天然产物或其衍生物[1],如抗疟药物青蒿素[2]、抗癌药物紫杉醇[3]、免疫抑制剂环孢菌素[4]等。随着现代科学技术的发展,如AI驱动的高通量筛选、合成生物学突破、微流控培养技术等,天然产物的研究正在持续地更新和发展,而对其进行结构解析和鉴定,是了解其构效关系,进而实现结构修饰与改造的先决条件。
目前,已有许多方法应用于天然产物的结构鉴定,例如核磁共振[5]、质谱[6]、近红外光谱[7]和圆二色光谱[8]等,但它们通常不能为复杂结构提供全面和直接的信息,特别是具有多个手性中心的分子。单晶X射线衍射(Single crystal X-ray diffraction,SCXRD)是一种公认的确定精确结构及绝对构型信息的可靠方法,通过测定单晶的晶体结构可以了解晶体中原子的三维空间排列、获得有关键长、键角、扭角、分子构型和构象、分子间相互作用和堆积等大量微观信息,研究其规律、从而进一步阐明化合物的性质[9]。然而,该方法在实际应用中具有一定的局限性:首先,培养出高质量的单晶是进行SCXRD的必要条件,对培养环境、操作人员的知识储备及分析经验有着较高要求;其次,因天然产物的结构多样性、获取量的有限性等客观因素,很多化合物难以成功培养出高质量的单晶。因此,单晶培养的成功率极大地制约着SCXRD在天然产物结构鉴定中的应用范围。
近年来,已经发展出各种基于分子间特异性相互作用的、创新型辅助结晶策略来突破这种限制,例如晶体海绵(Crystalline sponge,CS)法、结晶伴侣(Crystallization chaperone,CC)法等。这些策略利用氢键、卤素键、C-H-O、C-H-π和π-π堆积、范德华力或者静电作用等相互作用来限制客体分子的热运动,通过与主体(框架)相互作用,客体分子得以长程有序地排列,进而形成适合SCXRD分析的晶体[10]。其中,晶体海绵法使用多孔框架材料实现客体分子在主体孔道中的定向排列;而结晶伴侣法则采用非固有通道材料与难以单独结晶的有机分子实现共结晶。
1 晶体海绵法
2013年,Inokuma等[11]首次提出了一种无需样品自身结晶来制备单晶的方法,该方法使用类似于海绵的固有多孔晶体框架,从溶液中吸收客体分子并使其定向排列,通过蒸发溶剂,最终形成客体有序的包合物,通过SCXRD分析准确测定客体分子结构,称为晶体海绵法(图1a)。其中金属有机框架(Metal-organic framework,MOF)作为传统CSM的核心,具有双互穿结构的三维配位网络,是由金属离子(簇)与有机配体通过配位键连接而成的晶态多孔框架材料[12]。
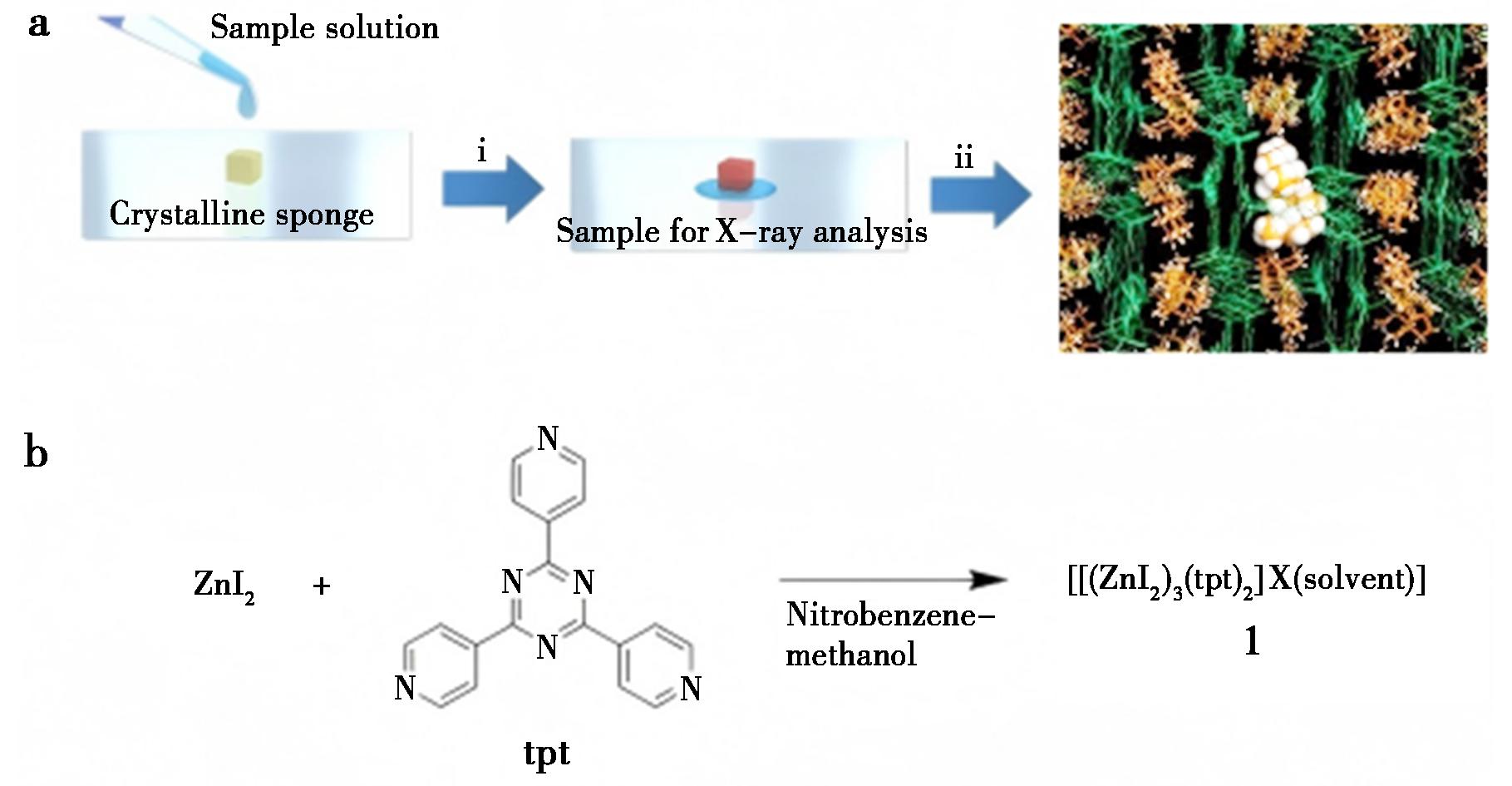
图1 a.晶体海绵法的示意图;b.ZnI2-tpt的制备[12]
Fig.1 a.Schematic representation of the CS method;b.Preparation of ZnI2-tpt[12]
1.1 初代晶体海绵
2002年,Biradha等[13]首先合成制备了基于锌的MOF晶体海绵:{[(ZnI2)3(tpt)2]·x(solvent)]}n[tpt=2,4,6-tris(4-pyridyl)-1,3,5-triazine](图1b)。研究发现该MOF具有弹簧一样(Spring-like)的柔性孔道,在其孔道内,客体分子能通过π-π堆积、氢键等作用被识别,并且在客体分子的吸附和脱附过程中MOF仍保持晶态。2014年,Inokuma等[14]率先将该晶体海绵的实验程序标准化:室温下在tpt的PhNO2溶液和ZnI2的MeOH溶液的液面分层处生长晶体7 d,之后将得到的晶体在50 ℃的环己烷中浸泡7 d以交换强结合的PhNO2,最后将晶体置于目标客体分子的CH2Cl2溶液中50 ℃缓慢挥发2 d,利用溶剂挥发驱动客体进入晶体孔道,从而得到可用于SCXRD解析的晶体。
Urban等[15]将ZnI2-tpt浸泡在含目标客体的溶液中,通过蒸发溶剂,筛选出适合进行X射线衍射的晶体,确定了海洋天然产物elatenyne的绝对构型,解决了其因伪对称结构导致的长期结构确证的争议。Wada等[16]将ZnI2-tpt浸泡在红藻(Laurencia pacifica)的甲醇粗提物中,成功解析了prepacifenol、laurinterol、deoxyprepacifenol、johnstonol、pacifenol、2,10-dibromo-3-chlorochamigran-7-en-9-ol等6种倍半萜的结构。Matsuda等[17]采用ZnI2-tpt与核磁共振相结合的方法,实现了复杂的萜类海洋天然产物asttellifadiene的结构解析(图2)。
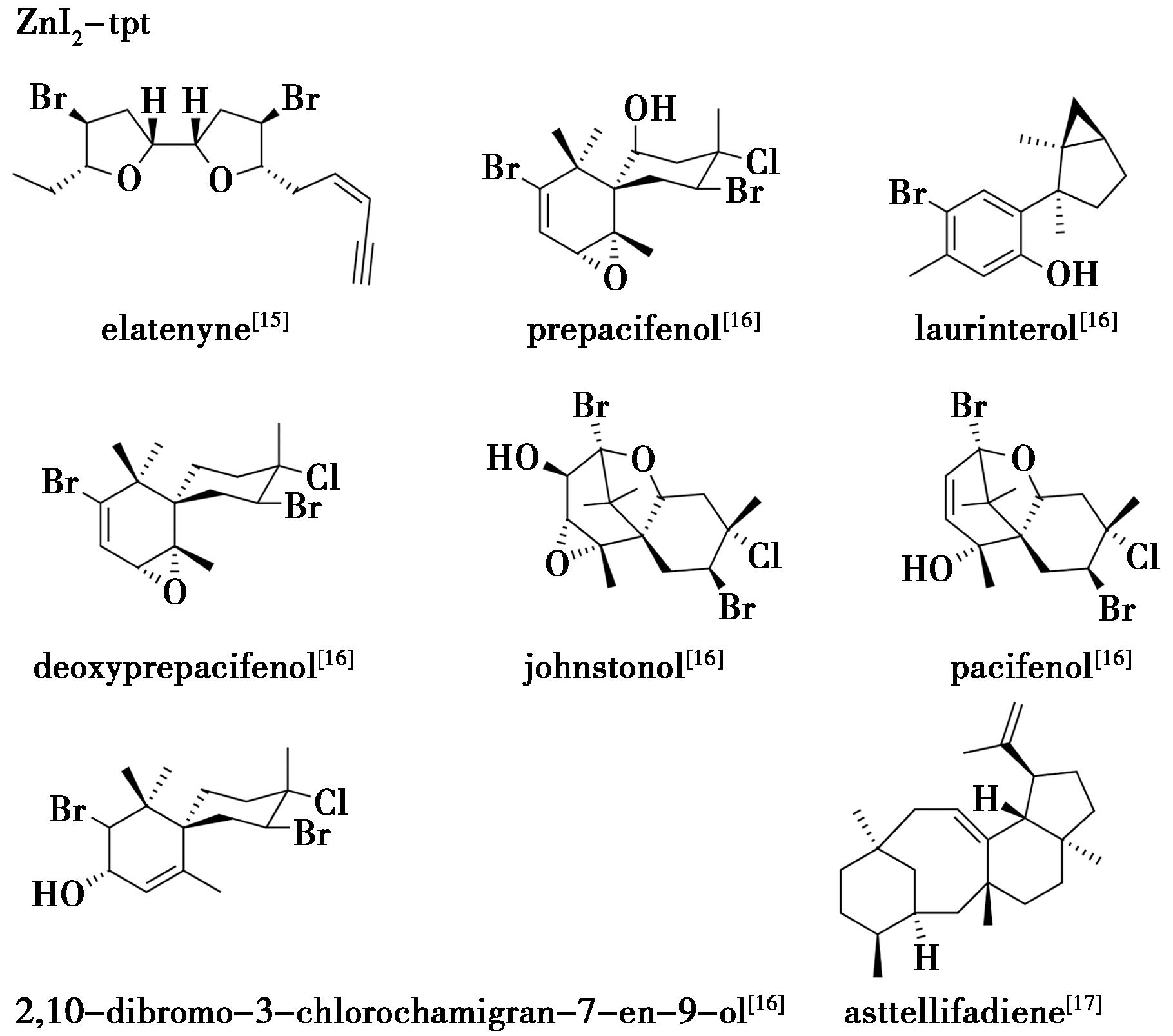
图2 ZnI2-tpt-天然产物结晶实例[15-17]
Fig.2 Crystallization examples of ZnI2-tpt with natural products[15-17]
Zigon等[18]将晶体海绵法与气相色谱相结合,实现了α-蒎烯、薄荷醇、新薄荷醇、薄荷酮、异薄荷酮、薄荷呋喃、桉树脑的结构确证。Li等[19]通过同步辐射结合晶体海绵,以及质谱与核磁共振联用,成功确定了asarinin的绝对构型。Inokuma等[11]建立了高效液相色谱与晶体海绵相结合的方法,仅使用5 μg的miyakosyne A样品就成功地解析了其分子骨架中的多个手性中心的构型(图3)。
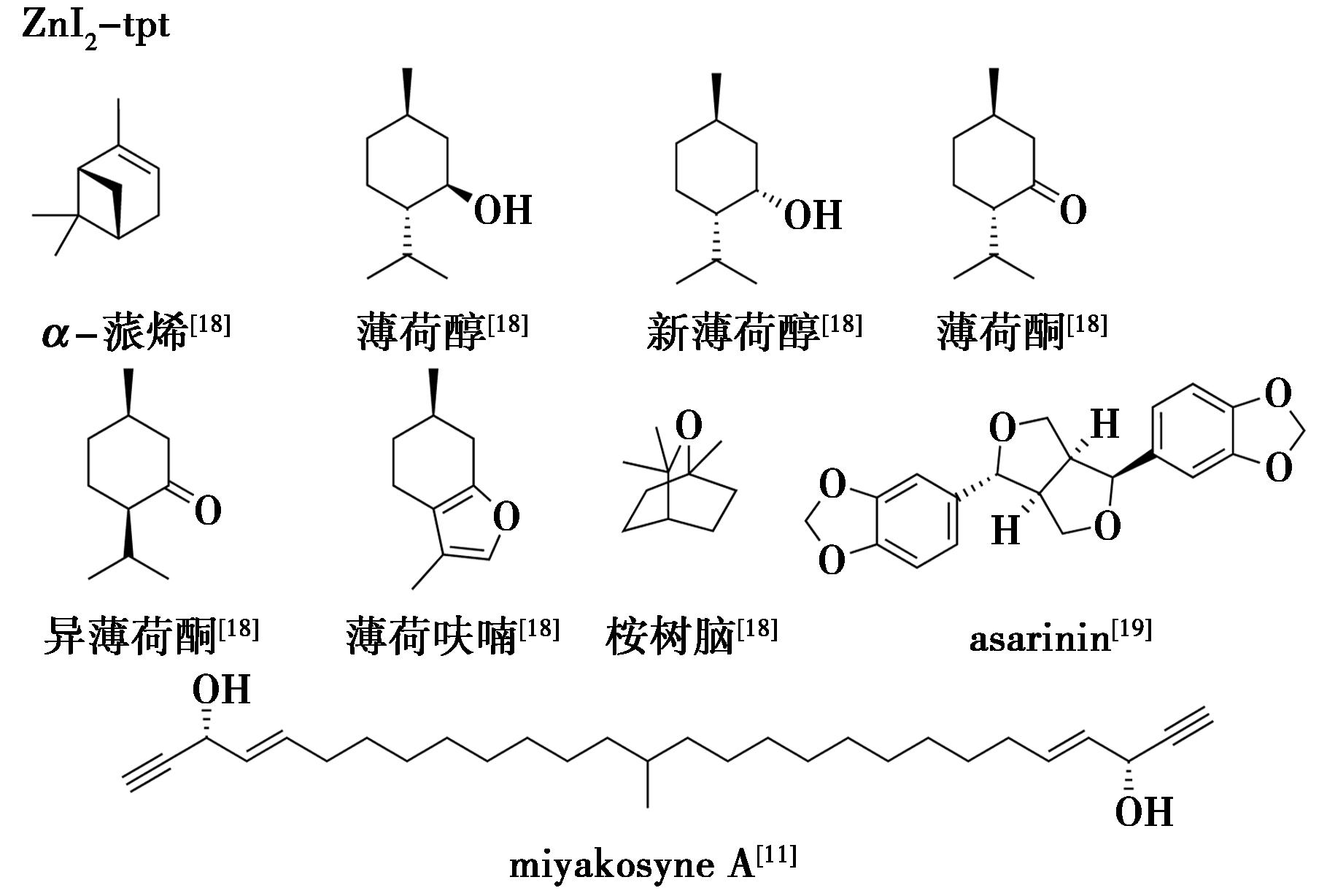
图3 ZnI2-tpt-天然产物结晶实例[11,18,19]
Fig.3 Crystallization examples of ZnI2-tpt with natural products[11,18,19]
Hoshino等[20]从稀有放线菌(Streptoalloteichus tenebrarius)中分离得到一种新型的具有硝基芳基侧链的γ-吡喃酮类化合物tenebrathin并通过将其与ZnI2-tpt结合,阐明了化学结构。Habib等[21]采用ZnI2-tpt包合萜烯类化合物,如香叶醇、法尼醇、β-突厥酮等,并进一步实现了结构确证(图4)。
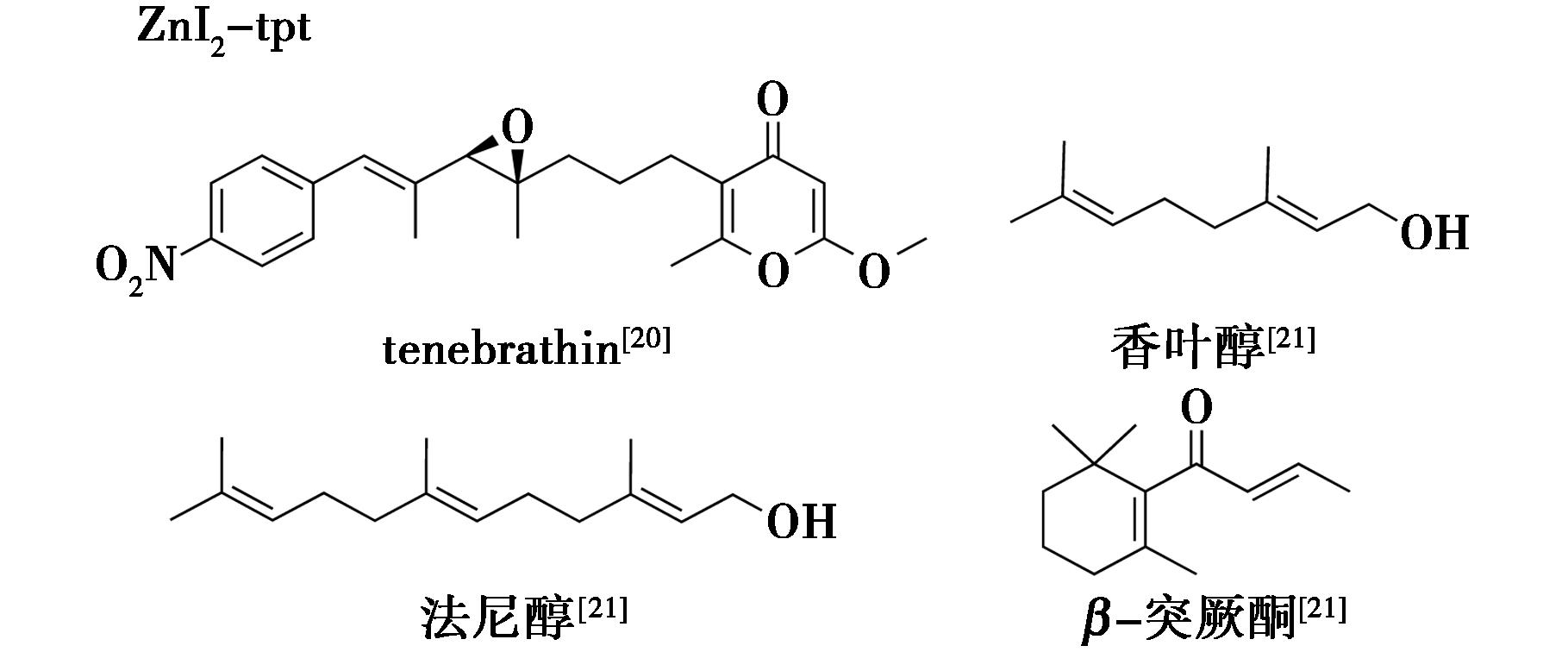
图4 ZnI2-tpt-天然产物结晶实例[20,21]
Fig.4 Crystallization examples of ZnI2-tpt with natural products[20,21]
1.2 初代晶体海绵的改进
2016年,Hoshino等[22]对晶体海绵的制备、孔道溶剂交换、客体分子浸泡、数据收集和晶体学分析等步骤进行了改进和优化,取得了相应进展。如在浸泡步骤中,获得较高的客体分子位点占有率尤为重要,因此,需对每个客体样品优化浸泡的关键参数(例如温度、时间、浓度、溶剂)。当标准条件不适用时,可采用高通量方法;X射线数据收集方面,通过在高角度区域收集更多的衍射点,客体分子的数据完整度和质量得到了显著改善;对主体框架中最灵活的ZnI2部分和填充剩余空隙的溶剂进行适当的无序处理,对于获得更好的精修数据质量也很重要。这项研究通过精细优化实验和数据处理流程,为其能够提供高质量数据奠定了基础。
在MOF合成方法和包合溶剂改进等方面,Ramadhar等[23]用CHCl3代替PhNO2合成ZnI2-tpt,该方法避免了暴露溶剂的交换且无需加热,将合成时间从14 d缩短到仅3 d,显著缩短了实验周期,后续使用同步辐射仪解决了数据质量和空间群确定问题,实现了反式茴香脑、愈创木薁、(1R,2S,5R)-乙酸薄荷酯的结构解析。2017年,Ramadhar等[24]用甲基叔丁基醚作为客体包合溶剂,成功确定了(E)-1,2-二苯乙烯、香草醛和(+)-青蒿素的化学结构(图5)。
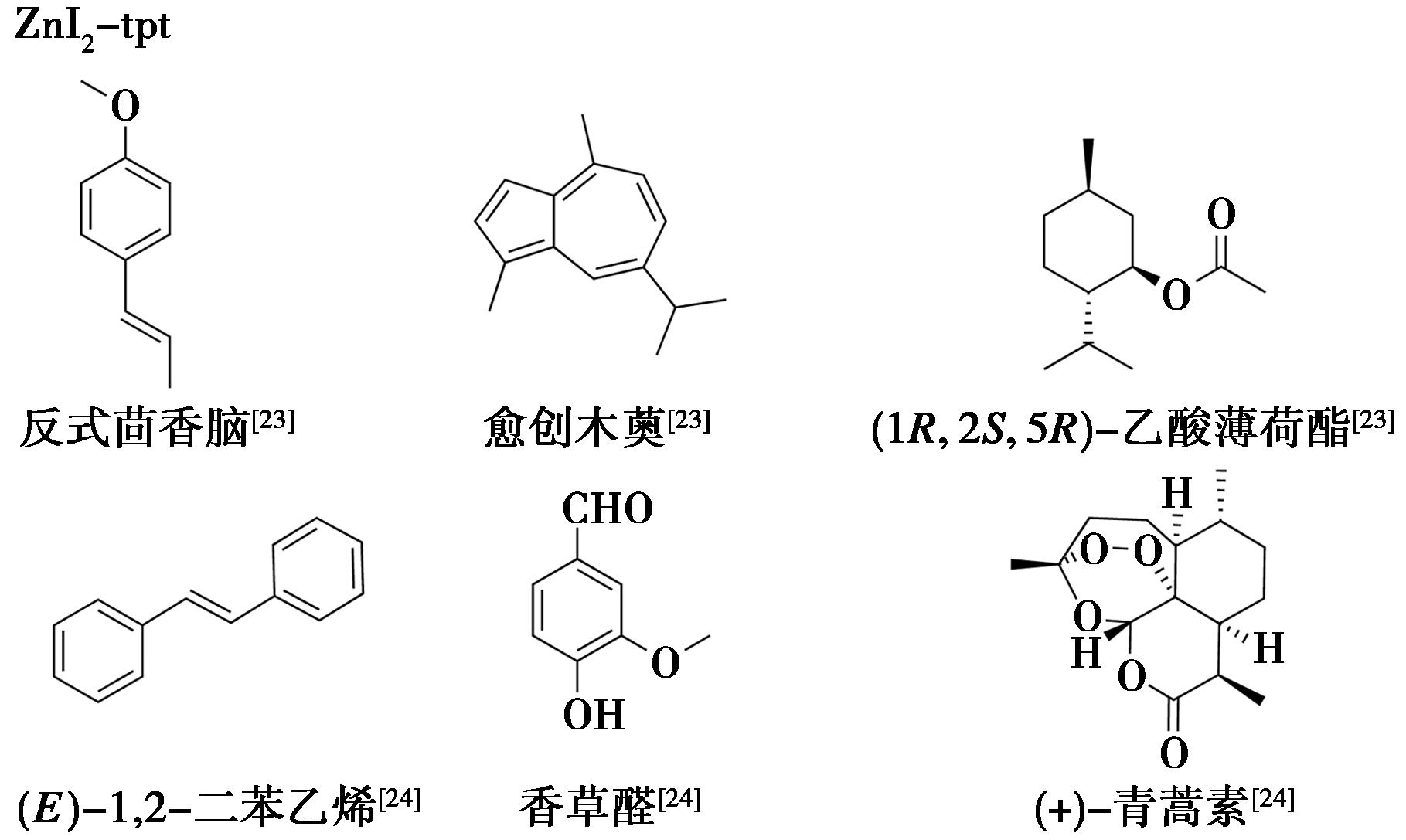
图5 ZnI2-tpt-天然产物结晶实例[23,24]
Fig.5 Crystallization examples of ZnI2-tpt with natural products[23,24]
Ramadhar等[25]还用Cl原子和Br原子代替I原子,改变MOF的金属封端配体,合成了ZnCl2-tpt与ZnBr2-tpt。这种选择较弱衍射信号的卤素原子来构建MOF,目的就是为了最大化客体分子的衍射信号贡献。这是一种“牺牲”晶体本身的质量,以换取对客体分子更清晰、更精确观测的方法。结果表明该方法在数据处理上降低了精修时间,提高了结构解析的精度与速度。Jung等[26]采用ZnI2-tpt和ZnCl2-tpt,实现了对(+)-germacrene D-4-ol及其降解产物(+)-τ-杜松醇、(-)-δ-杜松烯、(+)-τ-缪罗醇、(+)-α-杜松醇的结构分析(图6)。
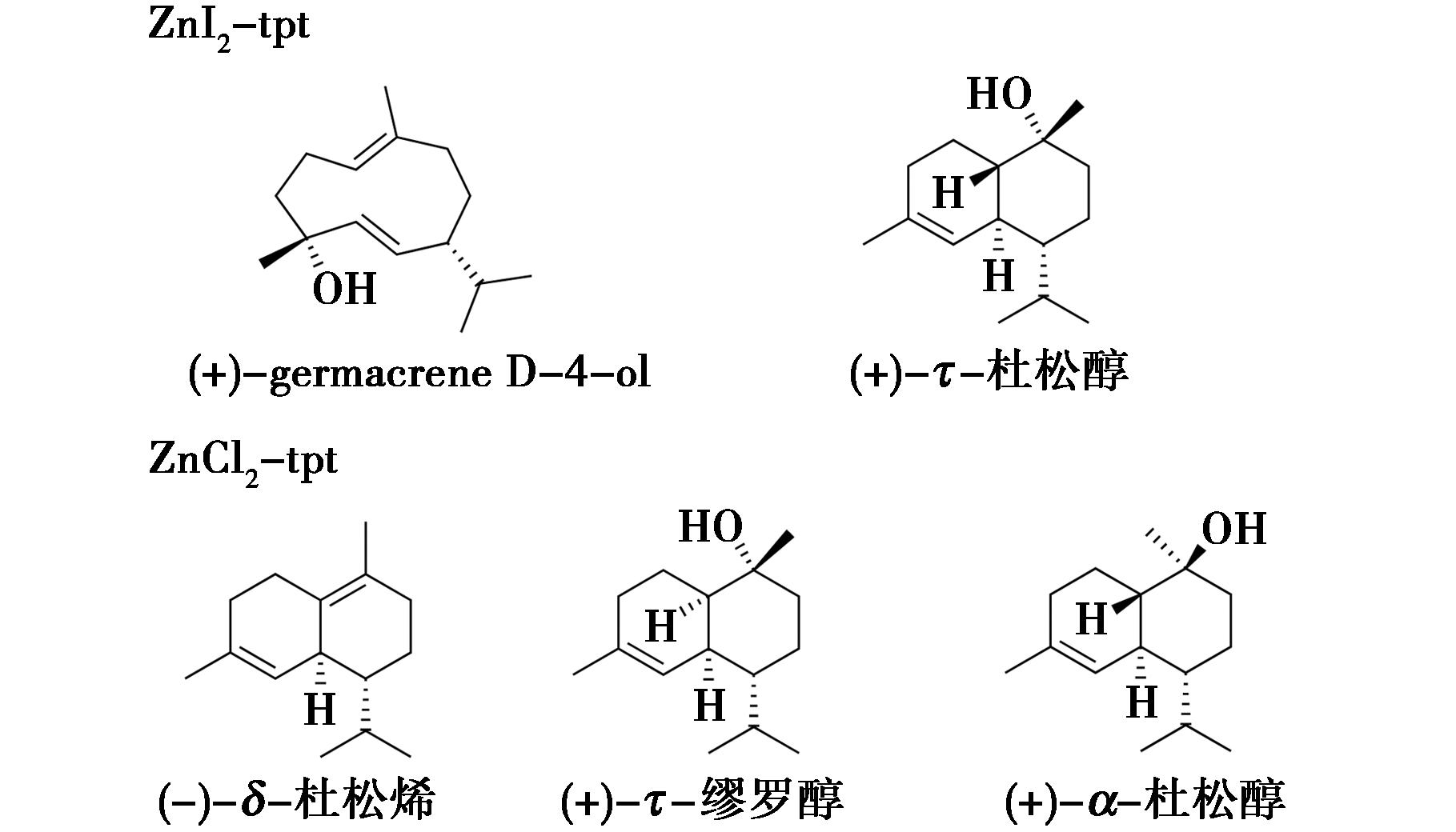
图6 ZnI2-tpt和ZnCl2-tpt-天然产物结晶实例[26]
Fig.6 Crystallization examples of ZnI2-tpt and ZnCl2-tpt with natural products[26]
Kai等[27]从真菌(Collimonas fungivorans)中分离出了一类具有烯-三炔结构单元的新型多氧代十六烷酸类衍生物collimonins A和collimonins B,通过采用ZnCl2-tpt与光谱、化学相结合的方法,成功解析了其化学结构。Morishita等[28]采用振动圆二色谱和ZnCl2-tpt相结合的方法,确定了真菌(Aspergillus oryzae)中的12元大环内酯化合物phaseolide A的结构。Hara等[29]从细菌(Nocardia carnea)的提取物中分离出一种新型具有三环碳骨架结构的二萜类化合物carneadiol,通过使用晶体海绵并结合光谱分析,确定了 carneadiol的绝对构型(图7)。
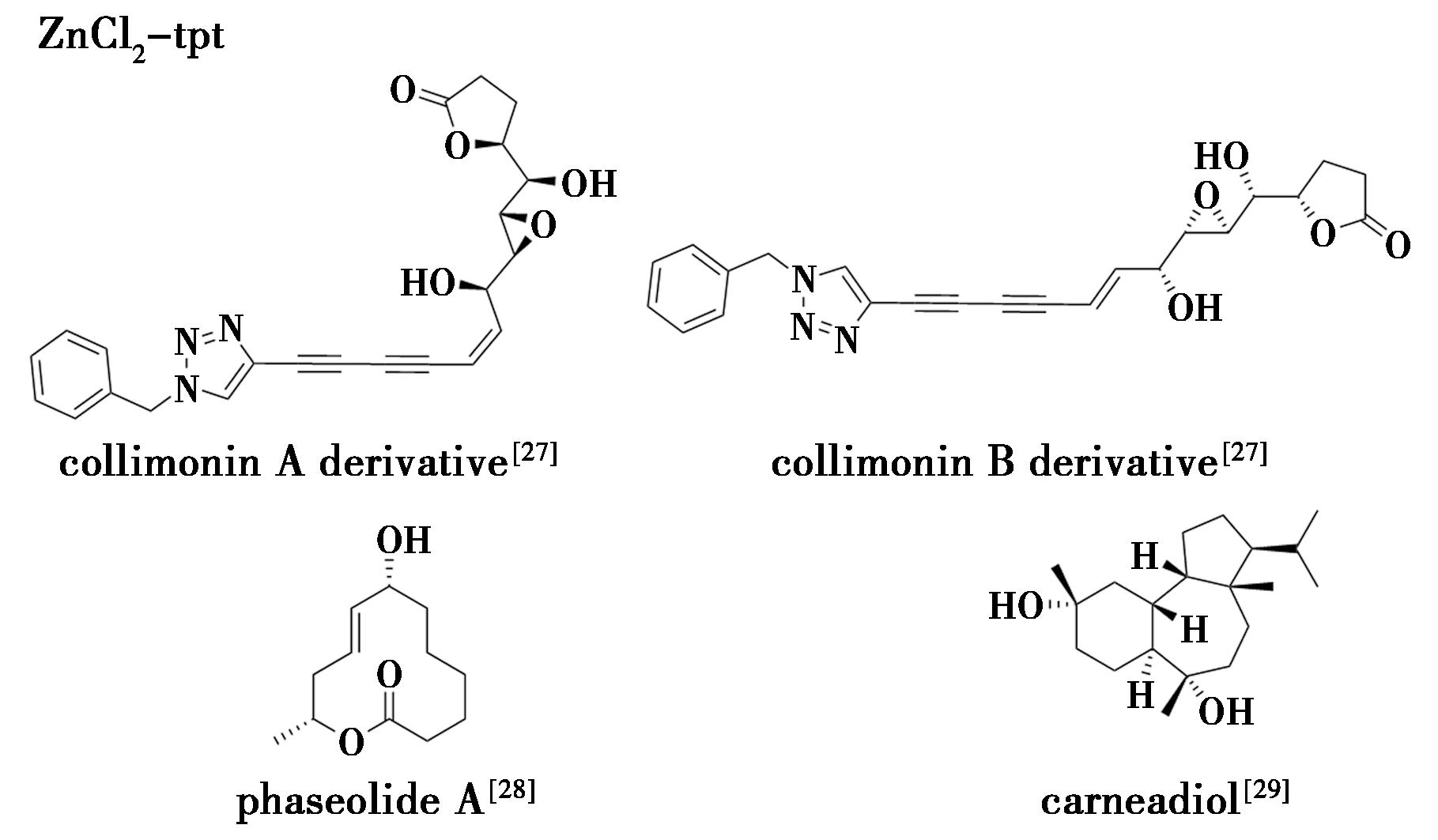
图7 ZnCl2-tpt-天然产物结晶实例[27-29]
Fig.7 Crystallization examples of ZnCl2-tpt with natural products[27-29]
Taniguchi等[30]成功地解析了使啤酒产生苦味的13种转化产物的结构(化合物5~17)。具体是将粗转化产物经过高效液相色谱快速分离后,再分别与ZnCl2-tpt结合,通过缓慢挥发溶剂,获得了高质量的晶体(图8)。
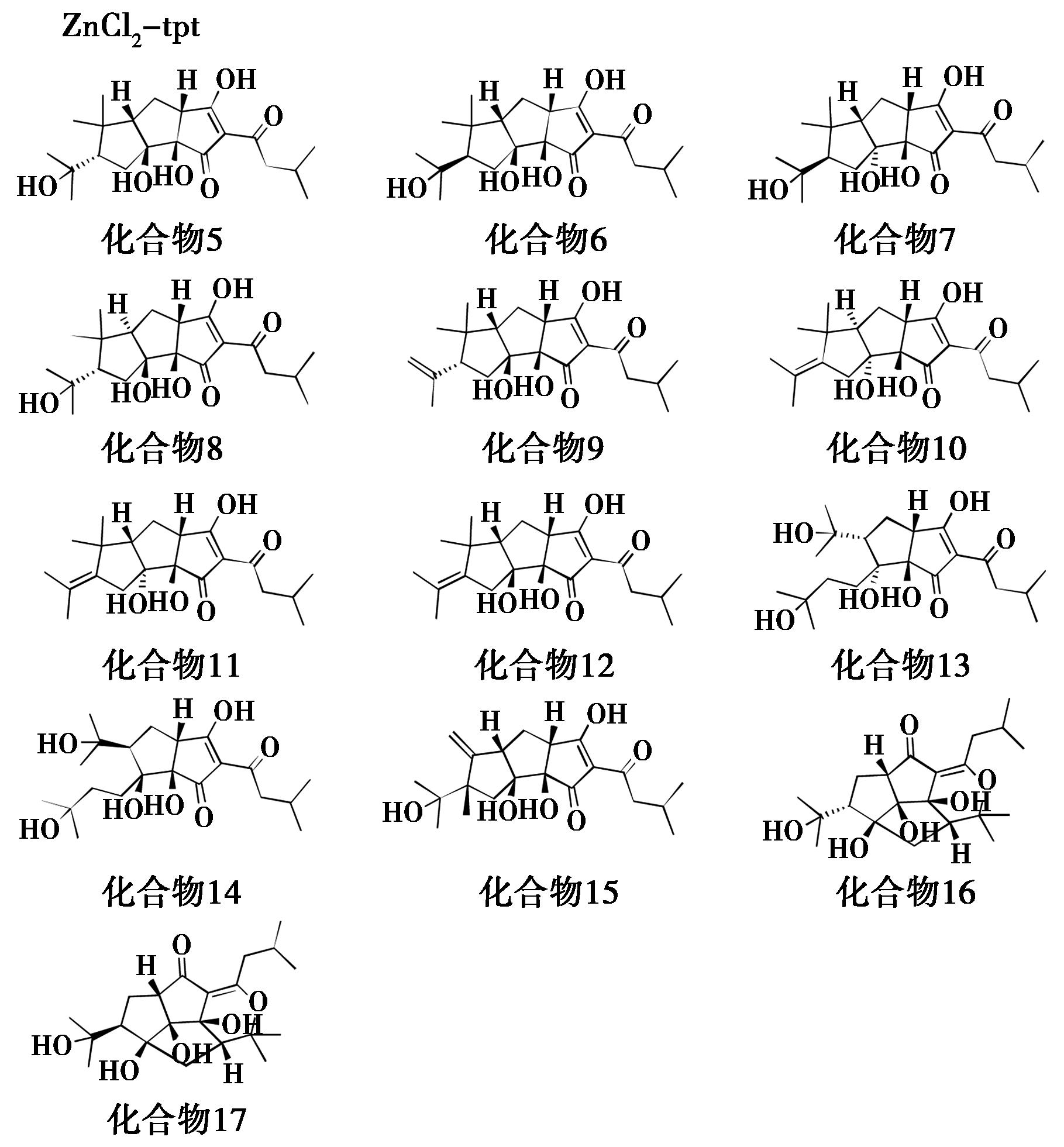
图8 ZnCl2-tpt-天然产物结晶实例[30]
Fig.8 Crystallization examples of ZnCl2-tpt with natural products[30]
2021年,Wada等[31]使用丙酮、乙酸乙酯和丁酮代替环己烷,成功解析了胆固醇、(20S)-羟基胆固醇、(22R)-羟基胆固醇、(22S)-羟基胆固醇、表雄酮、石胆酸、鹅脱氧胆酸、胆酸等结构(图9)。
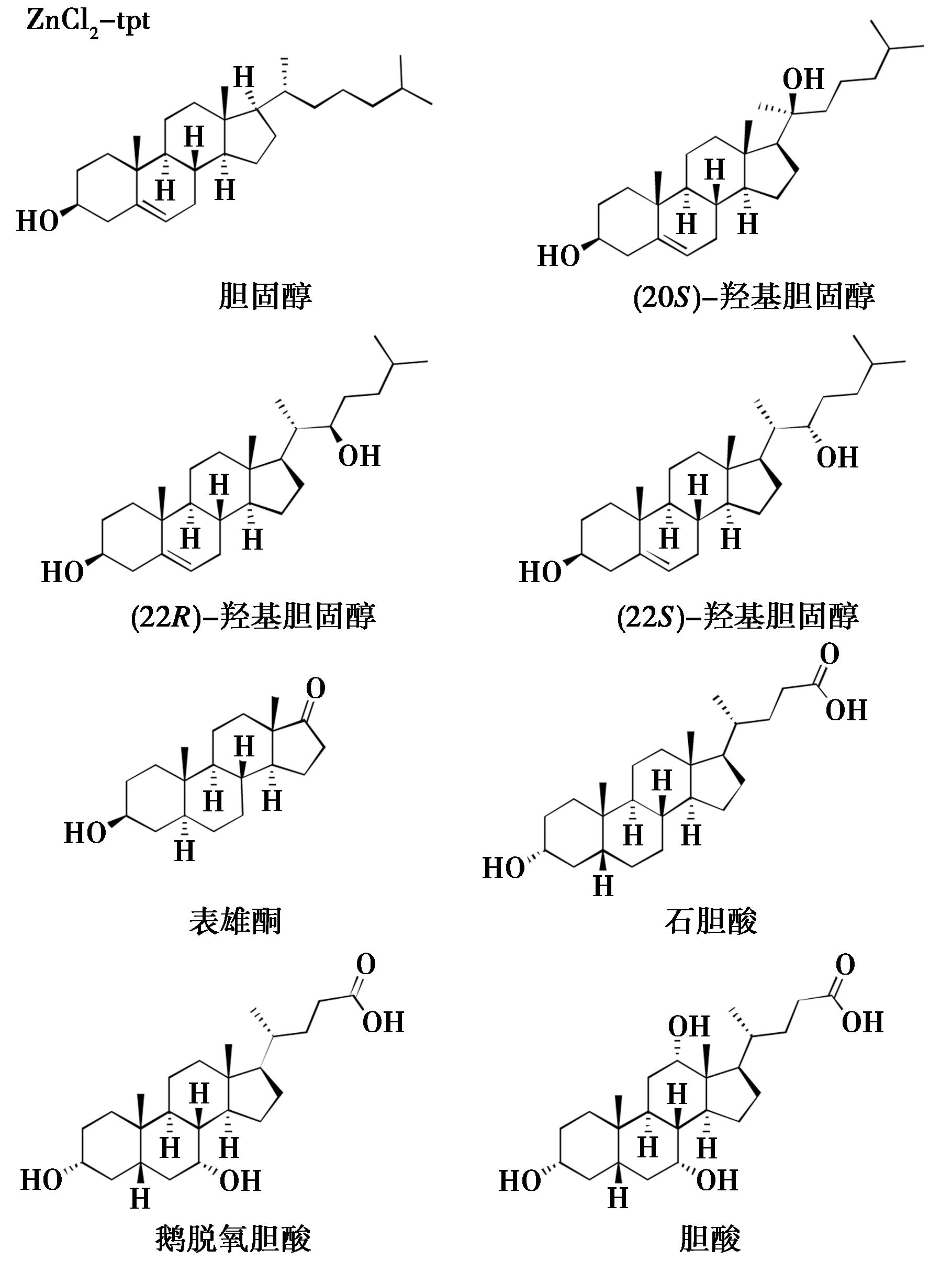
图9 ZnCl2-tpt-天然产物结晶实例[31]
Fig.9 Crystallization examples of ZnCl2-tpt with natural products[31]
Gu等[32]通过高效液相色谱分离富集得到目标成分,随后采用ZnBr2-tpt作为主体框架,成功区分了顺式细辛醚与反式细辛醚双键构型的差异以及香芹酚和百里香酚羟基取代位置的差异(图10)。
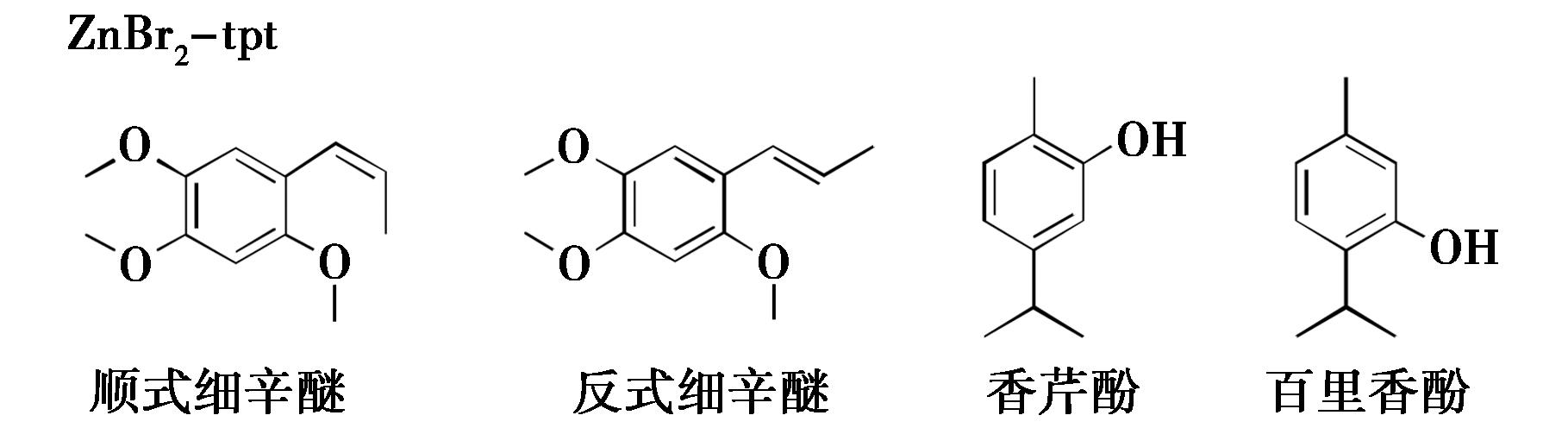
图10 ZnBr2-tpt-天然产物结晶实例[32]
Fig.10 Crystallization examples of ZnBr2-tpt with natural products[32]
2025年,Yoshida等[33]通过采用小楔角同步辐射晶体学技术,将晶体海绵尺寸缩小至1~10 μm范围,显著提升了结构解析的准确性,甚至实现了对纳克级(约3 ng)微量样品的分析。此外,2025年,Huang等[34]在DEF中合成了一个六氮杂环的金属有机框架:[ZrFMOF,Zr6(μ3-O)8(COO)8(H2O)8(DEF)7]。该框架由芴基羧酸与ZrOCl2构成,且具有两个不同的空腔。ZrFMOF通过空腔中存在的弱相互作用以3种不同的结合模式实现了包括藜芦醇、丁香酚、邻氨基苯甲酸甲酯在内的12种化合物的结构测定(图11)。
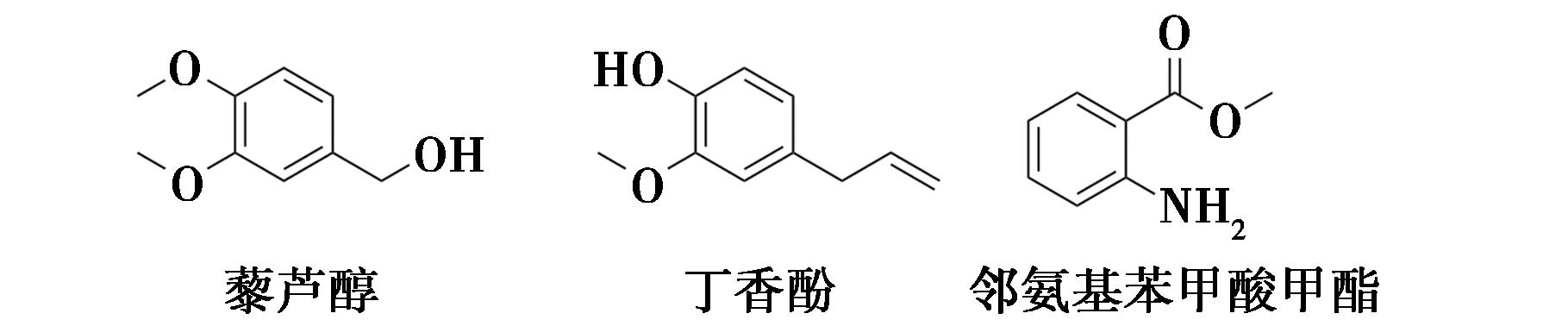
图11 ZrFMOF-天然产物结晶实例[34]
Fig.11 Crystallization examples of ZrFMOF with natural products[34]
ZrFMOF在使用前无需活化,包合客体时不涉及溶剂交换,展现出了很强的实用性[35]。
1.3 适用于手性客体的晶体海绵
2016年,Lee等[36]成功合成了两个手性MOF-520,由次级结构单元SBU(SBU=Al8(μ-OH)8(HCOO)4(-COO)12)和BTB(BTB=1,3,5-benzenetribenzoate)连接体构成(图12)。该方法的核心原理在于:BTB连接体在构筑三维网络时形成螺旋手性排列,为客体分子的绝对构型测定提供了一个内在的、可靠的参考基准。MOF-520次级结构单元上的甲酸配体可被含氧官能团(如羧酸、醇、酚)去质子化后的阴离子取代,使客体分子通过配位键直接锚定在框架上。此举大幅降低了客体的热运动自由度,即使在低占有率下也能实现高精度的结构解析。研究成功测定了染料木素的结构,并精确区分了赤霉素单双键等微小差异。该方法还利用框架的手性空腔实现了对映异构体的选择性结晶,直接确定了茉莉酸分子的绝对构型,为CS法拓展了新方向(图13)。
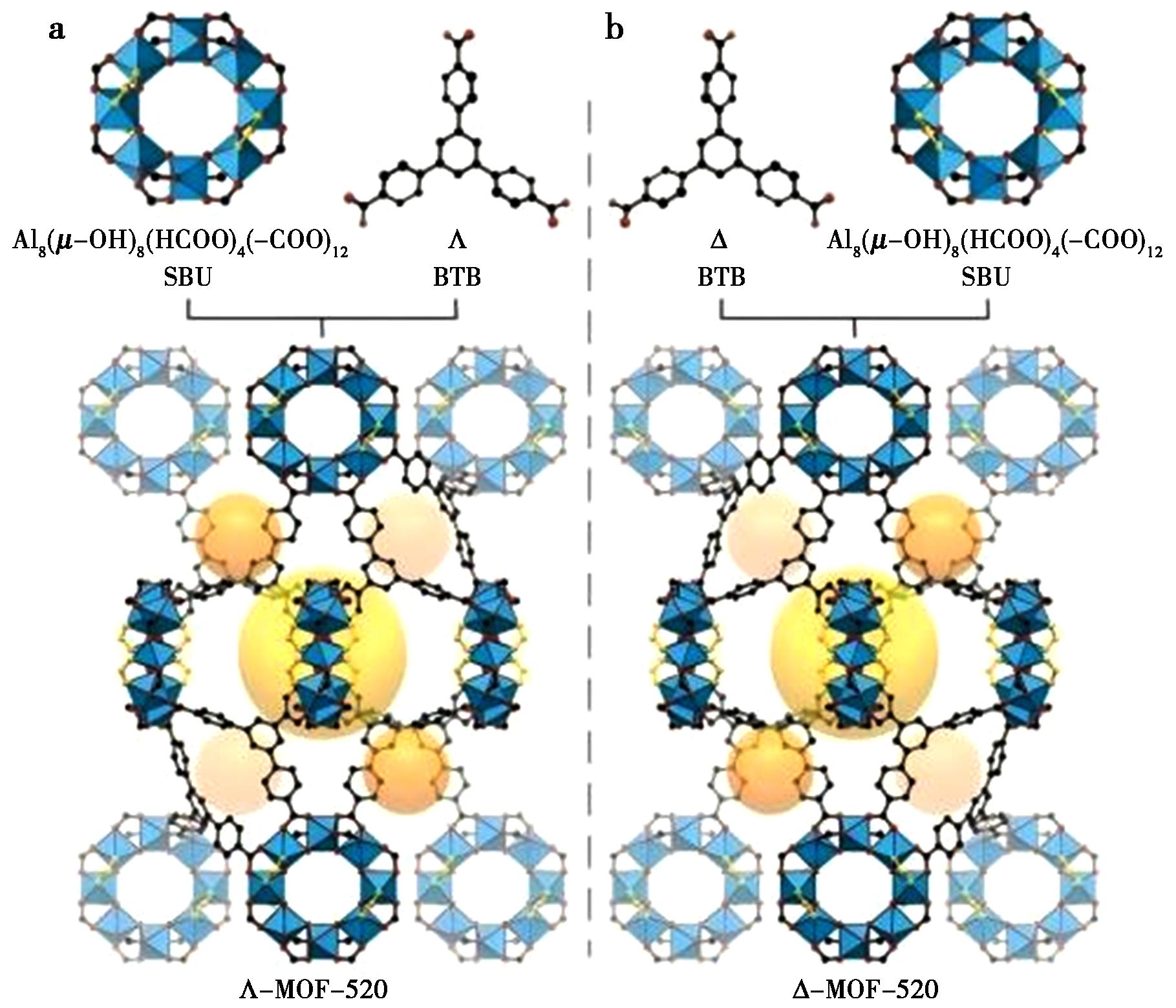
a.Λ-MOF-520;b.Δ-MOF-520
图12 MOF-520对映体及其次级结构单元的结构[36]
Fig.12 Structures of MOF-520 enantiomorphs and their secondary structural units[36]
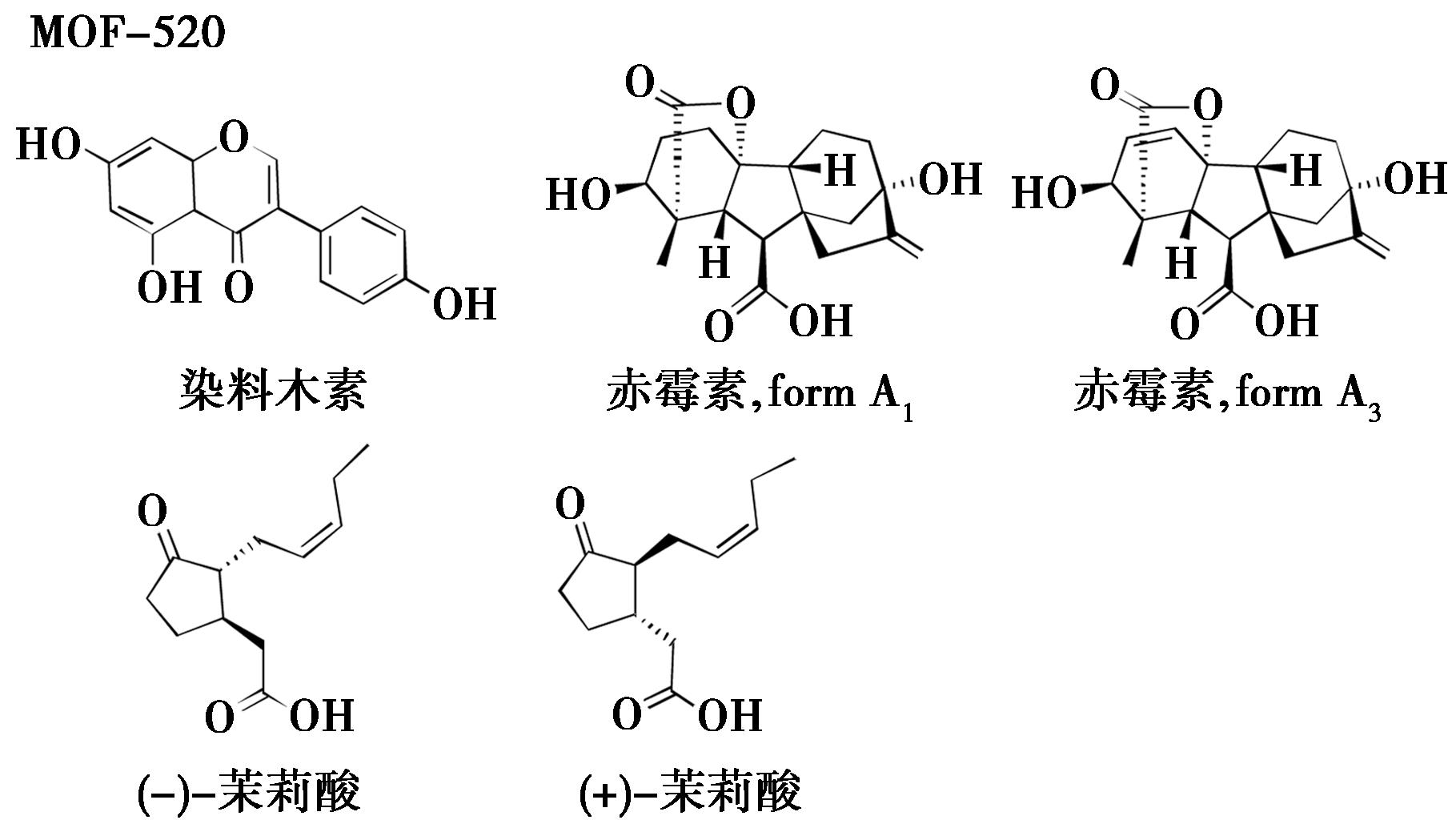
图13 MOF-520-天然产物结晶实例[36]
Fig.13 Crystallization examples of MOF-520 with natural products[36]
2017年,Zhang等[37]合成了一种手性晶体海绵:CMOM-3S[Co2(man)2(bpy)3](OTf)2(man=R/S-mandelate;bpy=4,4′-bipyridine),手性配体S-扁桃酸或R-扁桃酸(man)是结构中的手性来源,决定了材料对手性客体的识别偏好;桥联配体为4,4′-联吡啶(bpy),将金属中心连接起来,扩展形成三维网络;平衡阴离子为三氟甲磺酸根(OTf),用于平衡骨架的正电荷,同时其较大的体积和独特的化学性质(含F、O原子)对孔道尺寸、表面化学及主客体相互作用至关重要。CMOM-3S可同时作为手性色谱固定相(Chiral stationary phase,CSP)和手性晶体海绵(Chiral crystalline sponge,CCS)发挥作用,并能够在没有对映体标准品的情况下,实现对映异构体的分离和鉴别(图14)。2020年,Zhang等[38]将平衡阴离子替换为四氟硼酸根,得到CMOM-2S,优化了孔道的尺寸、形状和表面化学(特别是氢键位点);还使用不同位点氯代或甲基化的R-扁桃酸衍生物作为手性源,得到CMOM-11R~CMOM-41R,微调了手性孔洞内壁的立体化学环境和空间位阻。2023年,Deng等[39]又报道了一种新型手性晶体海绵CMOM-5[Ni(SIDEC)(bipy)(H2O)][NO3],手性配体使用天然手性分子S-吲哚啉-2-羧酸,该配体与镍离子形成一维手性棒状构筑单元,再通过 4,4′-联吡啶连接,形成一个均手性阳离子三维网络。CMOM-5的框架是自适应的,当不同的手性客体进入后,框架会适当调整其孔道形状和尺寸,以最优方式容纳客体。该研究成功解析了扁桃酸甲酯的晶体结构(图15)。
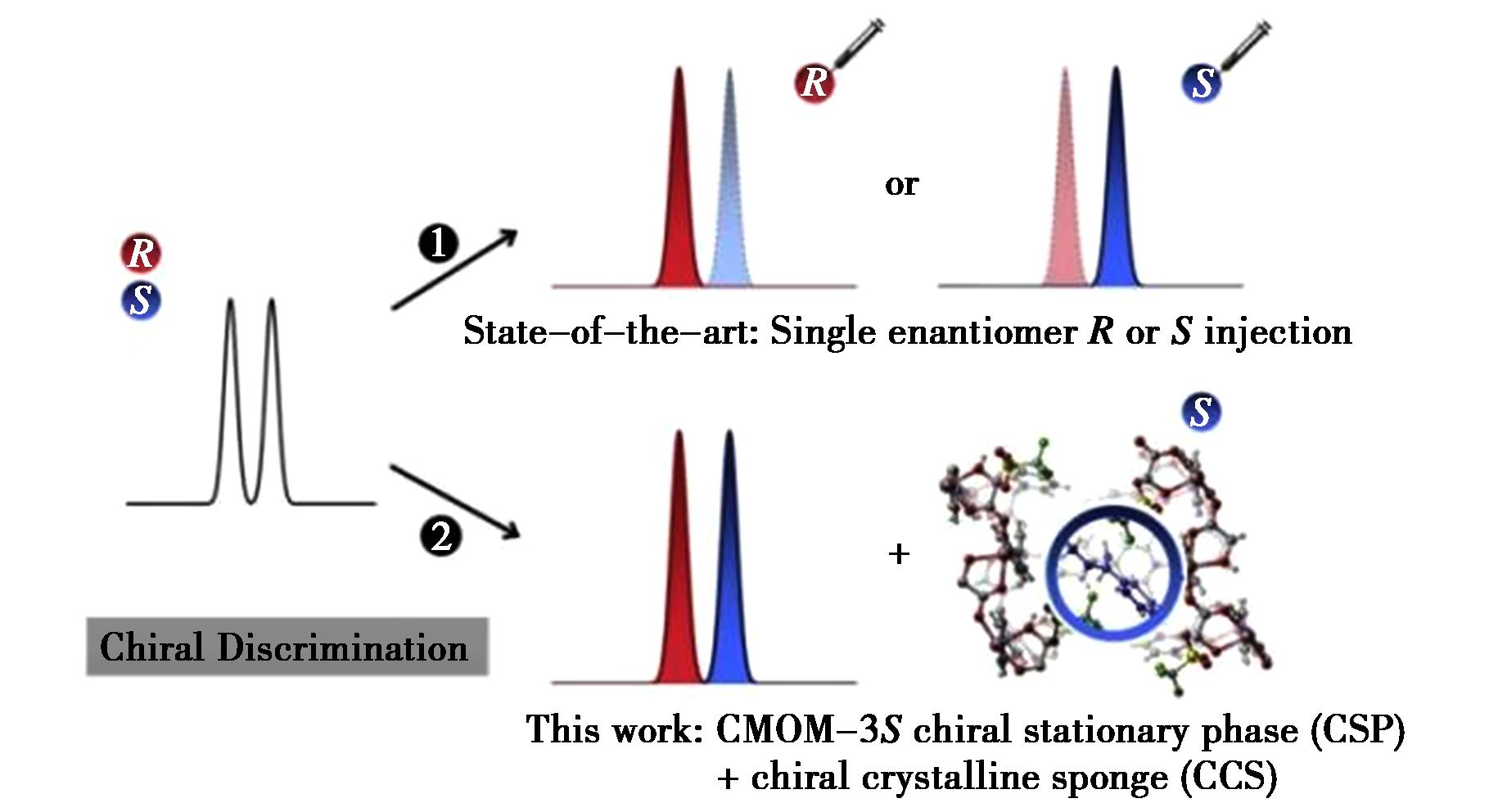
图14 方法1需使用对映体的标准品来确定绝对构型,基于CMOM-3S的方法2则无需使用标准品[37]
Fig.14 Method 1 requires the use of enantiomeric standards to determine the absolute configuration,whereas Method 2 based on CMOM-3S does not require the use of standards[37]
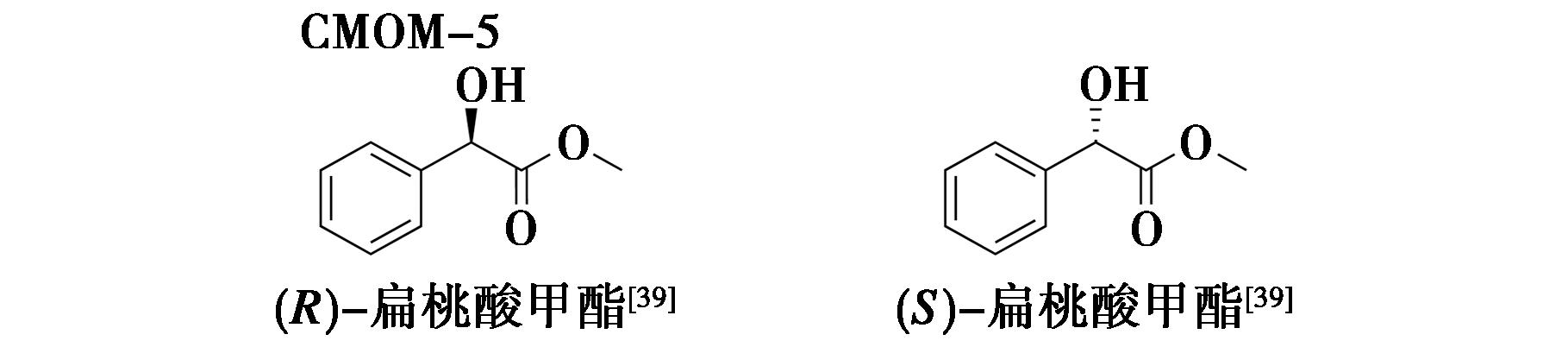
图15 CMOM-5-天然产物结晶实例[39]
Fig.15 Crystallization examples of CMOM-5 with natural products[39]
1.4 适用于长链烷基的晶体海绵(含“分子捕手”)
含有长烷基链结构单元的分子在天然产物中十分常见。这些分子由较长的碳链组成,通常具有较强柔性而难以结晶,常规的单晶培养方法对其并不适用。虽然传统的晶体海绵法可以使其进入金属有机框架的孔道中,但存在制备过程繁琐、对目标分子选择性差的情况,影响这一类分子的单晶解析的精度和准确度。
Tu等[40]设计的BTB-MOF-24是由H3BTB连接体和[Fe3(CO2)6(DMF)2]∞棒状次级结构单元构筑而成,形成了一种具有狭窄通道和位于BTB3-连接体间的不对称三明治型空腔,空腔有两种不同的尺寸:3.4 Å(A位点)和6.0 Å(A′位点)(图16)。这些空腔与狭窄的通道共同构成了主体结构,这种不对称形状对于固定客体分子至关重要。独特的不对称三明治空腔能够像“分子夹”一样,通过C-H-π和π-π等相互作用,与客体分子的骨架发生作用。这种作用能显著降低柔性客体分子的热运动自由度,使其在空腔中有序排列,如对柔性长链分子的吸附和结构确定可在9 h内完成,无需或仅需施加极少的约束即可完成全部的结构精修。BTB-MOF-24的核心创新在于其不对称三明治空腔的设计,能够以微量样品和极短时间,实现对角鲨烯和DHA乙酯等长链柔性分子的高精度结构解析(图17)。
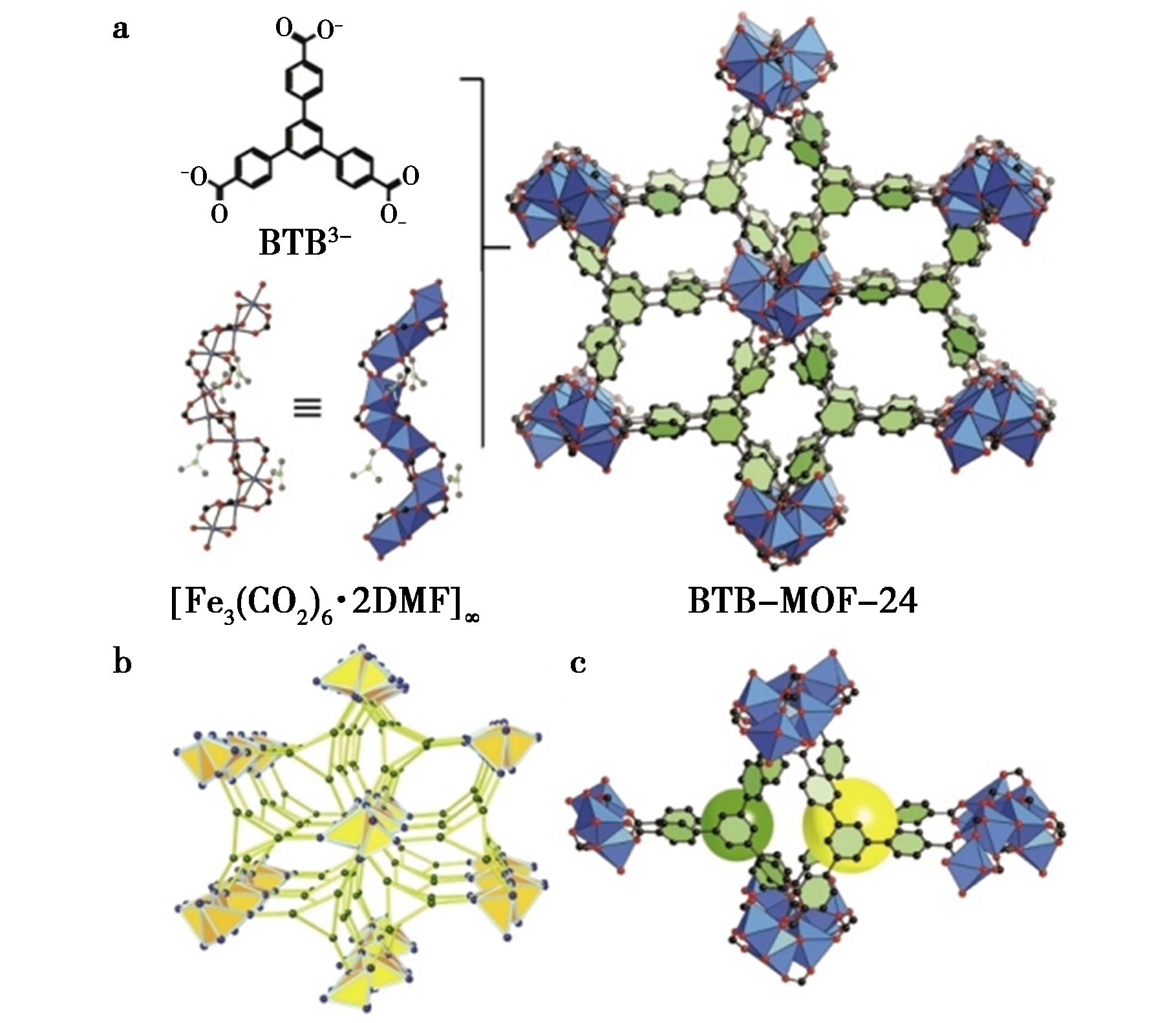
图16 a.BTB-MOF-24的合成过程;b.BTB-MOF-24的基本结构示意图;c.BTB3-连接体之间分别存在3.4 Å(绿色球体,A位点)和6.0 Å(黄色球体,A′位点)的不对称空腔[40]
Fig.16 a.Synthesis process of BTB-MOF-24;b.Representation of the underlying architecture of BTB-MOF-24;c.Asymmetric cavities of 3.4 Å(green sphere,site A) and 6.0 Å(yellow sphere,site A′) between the BTB3- linkers[40]
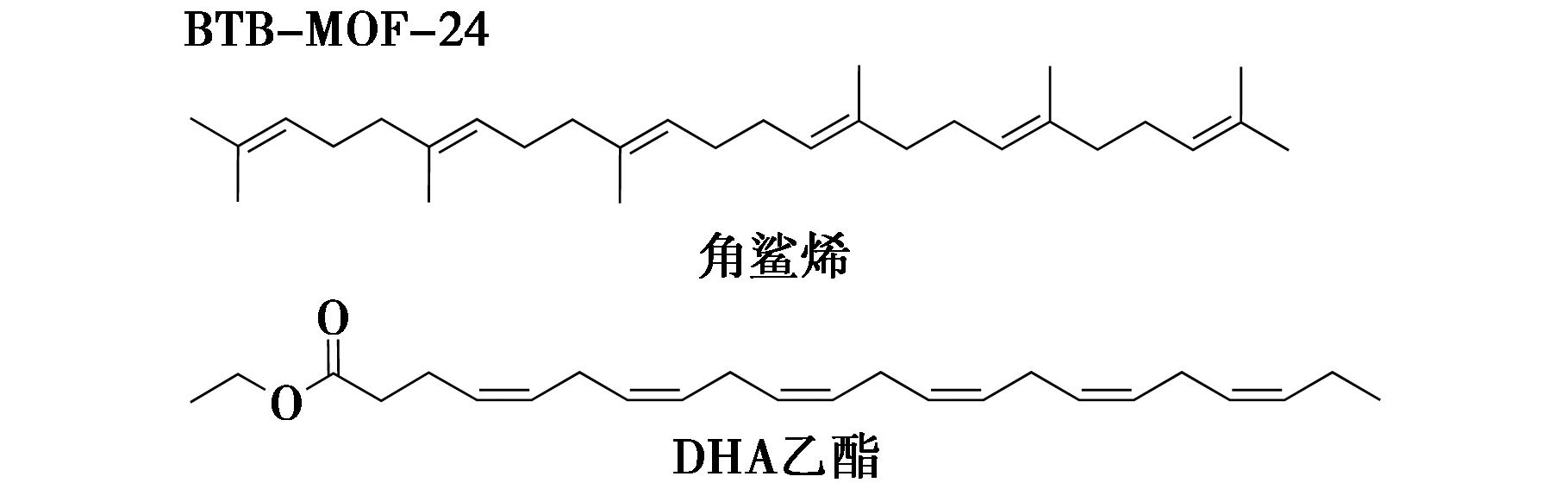
图17 BTB-MOF-24-天然产物结晶实例[40]
Fig.17 Crystallization examples of BTB-MOF-24 with natural products[40]
2025年,针对含有长烷基链结构单元的分子,Wu等[41]提出了一种创新的“超分子对接”策略,采用“分子捕手”,即超大环金属有机框架,实现对长烷基链化合物的特异性识别,并成功构建了单晶结构。该团队首先制备了含柱芳烃EtP5BPPy、H4L1分子和Zn(NO3)2·6H2O的混悬液,随后加入冰醋酸,混悬液超声处理后滤过,加热48 h后冷却至室温,得到了适合SCXRD分析的EtP5-MOF-2主体单晶。将EtP5-MOF-2主体单晶浸泡在少量含客体的溶剂中,室温放置10 min,随后收集用于衍射的单晶(图18)。SCXRD结果显示,长烷基链化合物通过C-H-O、C-H-π和C-H-S等相互作用稳定在EtP5亚基的空腔中;这种“超分子对接”方法通过主-客体识别,能够促进客体分子快速整合到框架中,不需要复杂且耗时的溶剂交换过程。该研究成功测定了48种含烷基链分子的结构,包括二氢茉莉酮、6-戊基-δ-己内酯、11-十六碳烯醛、棕榈酸6-甲基庚酯、棕榈油酸甲酯、芥酸甲酯等(图19)。不仅如此,该方法还适用于混合物中目标分子的结构鉴定,不需进行纯化。
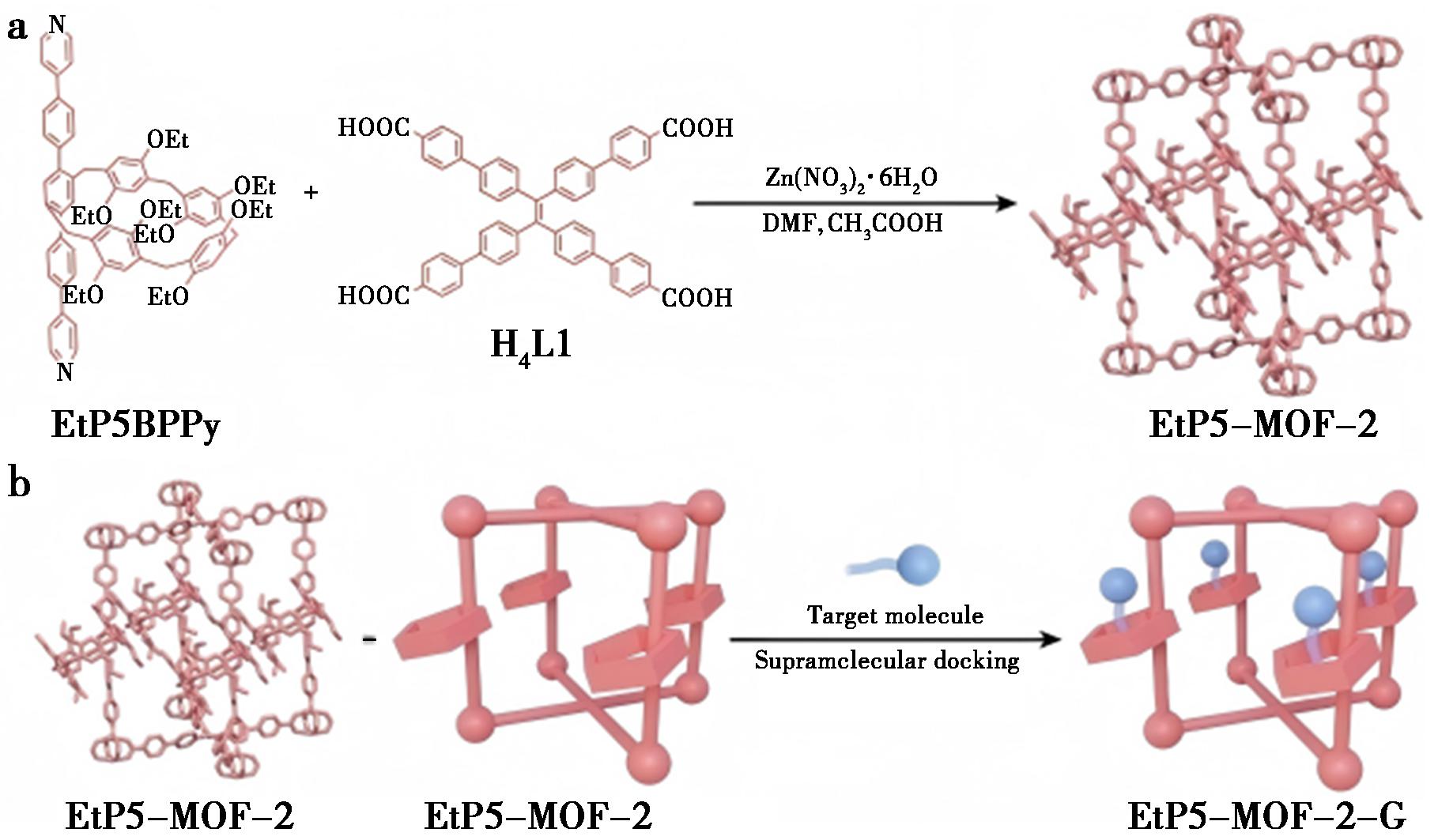
图18 a.EtP5BPPy柱芳基和H4L1分子制备EtP5-MOF-2的示意图;b.超分子对接过程的模型图[41]
Fig.18 a.Schematic diagram of preparing EtP5-MOF-2 using the pillararene-based strut EtP5BPPy and H4L1 motifs;b.Model diagram of the supramolecular docking process[41]
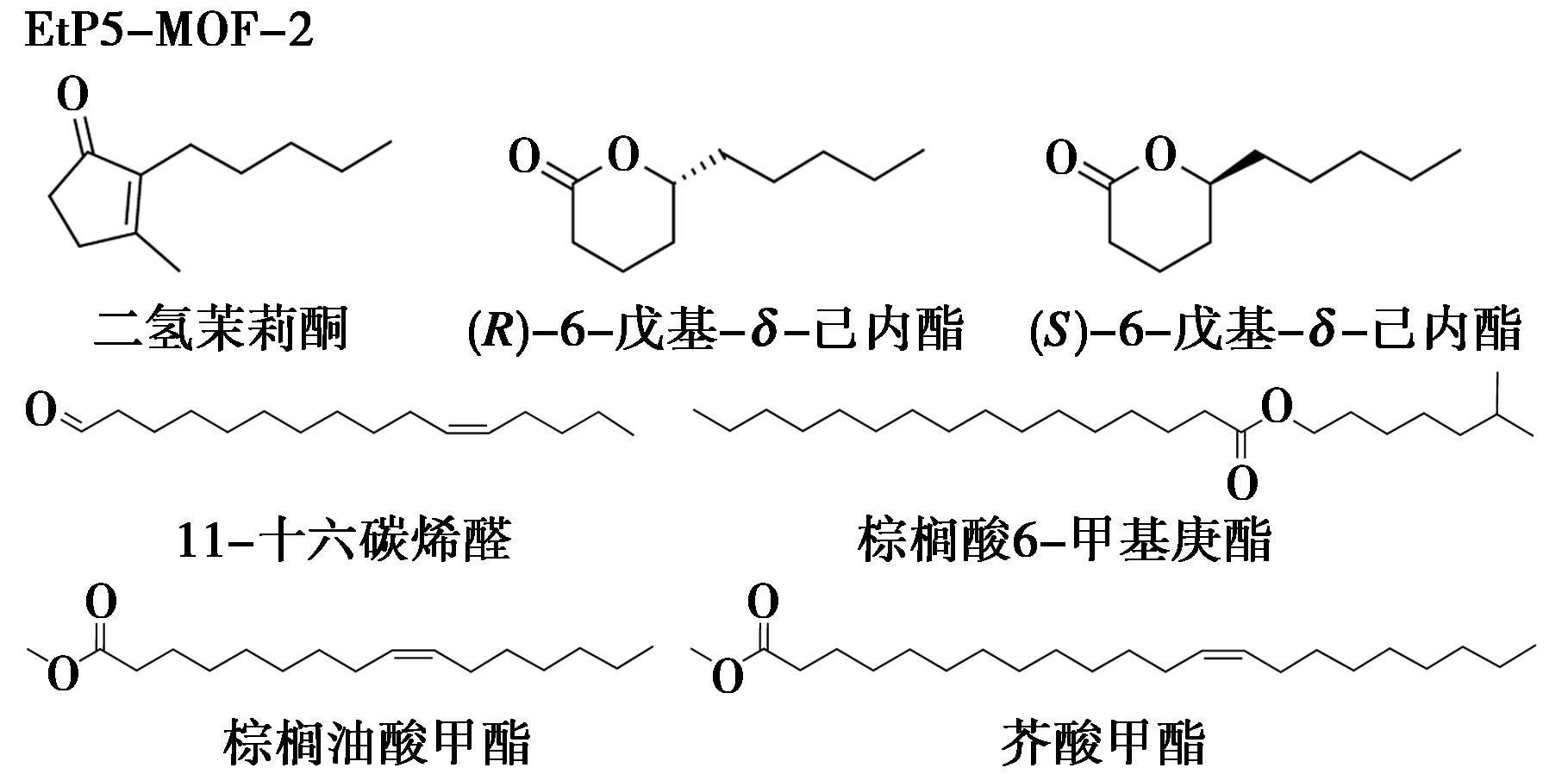
图19 EtP5-MOF-2-天然产物结晶实例[41]
Fig.19 Crystallization examples of EtP5-MOF-2 with natural products[41]
1.5 适用于亲水性客体的晶体海绵
2025年,He等[42]针对当前晶体海绵仍存在客体分子占有率低、亲水性分子难以进入疏水性孔道等问题,构建出新一代晶体海绵。其基本组件是具有高对称性的离散型配位笼,如八面体形的M6L4笼(具Td对称性),诱导剂为平面芳香族聚磺酸阴离子,被称为“粘贴”阴离子(如芘-1,3,6,8-四磺酸盐,具D2h对称性)。当带正电的配位笼与“粘贴”阴离子在结晶过程中结合时,两者之间的几何对称性不匹配破坏了配位笼本身的高对称性。这迫使晶体以低对称性空间群生长。低对称性的堆积方式避免了高对称性晶体中常见的对称元素,从而防止了客体分子的无序,并形成了可供客体分子进出的通道(图20)。低对称性结晶是与初代海绵最根本的区别,是解决客体无序问题的关键。具体操作有两种方法:方法A(结晶后吸附),先合成空的晶体海绵,再将其浸泡在客体溶液中吸附客体;方法B(结晶前包封),先在溶液中形成主客体复合物,再诱导其与“粘贴”阴离子共结晶。该方法可用于绝对构型确定,低对称性空间群与主体中的重原子相结合,能够通过Flack参数可靠地确定手性客体的绝对立体构型。另外,空腔的洞口和通道允许对两亲性分子进行“部分包封”-疏水部分进入笼内,亲水部分伸出笼外并通过氢键等作用固定,进一步将可分析化合物的范围扩展至中等尺寸的药物分子,如甘氨胆酸、地高辛、洋地黄皂苷、莫能菌素等药物分子(图21)。
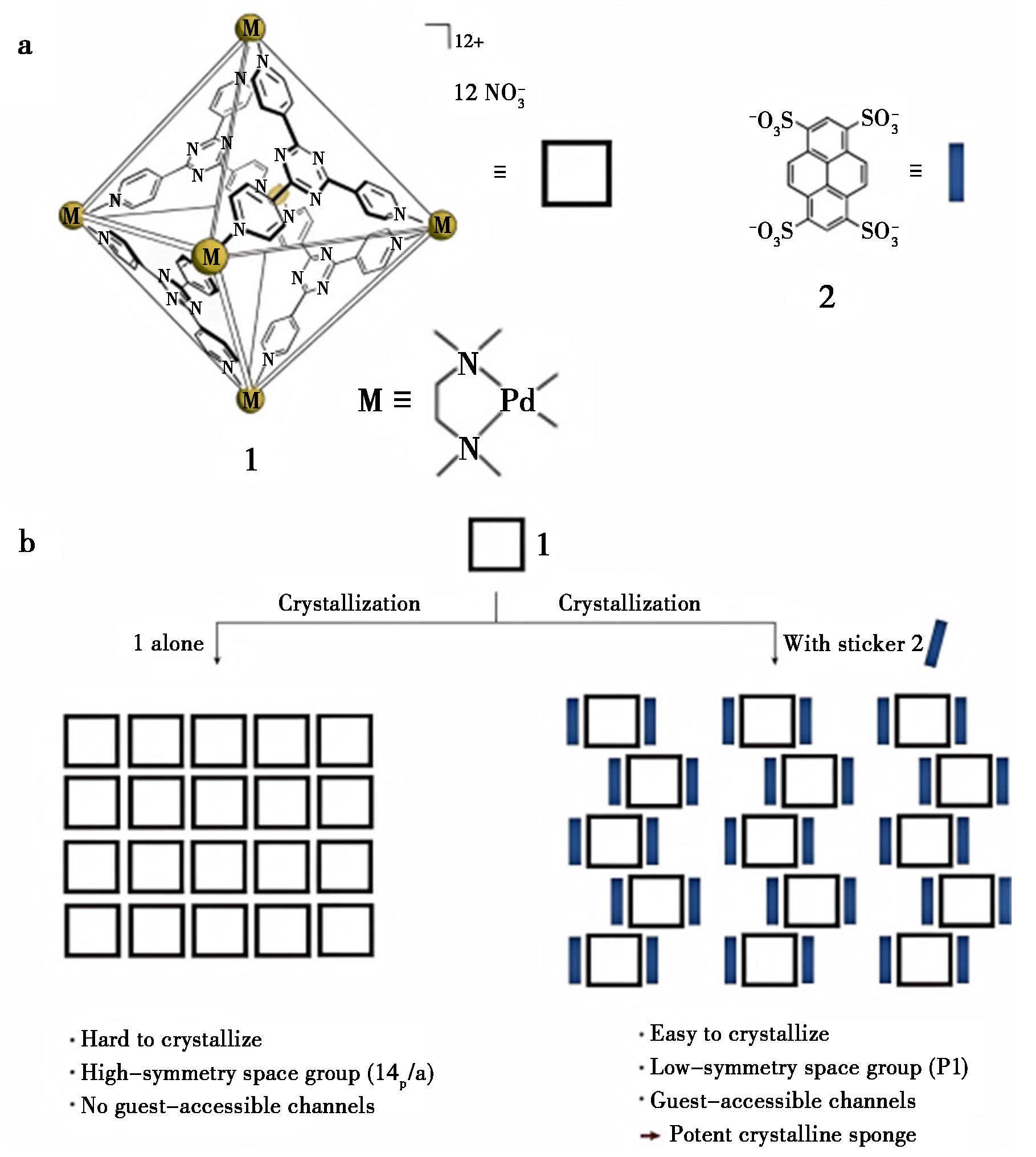
图20 a.配位笼112+和“粘贴”阴离子24-的化学结构;b.“粘贴”诱导配位笼结晶成CS[42]
Fig.20 a.Chemical structures of coordination cage 112+ and sticker anion 24-;b.Sticker-induced crystallization of a coordination cage into a CS[42]
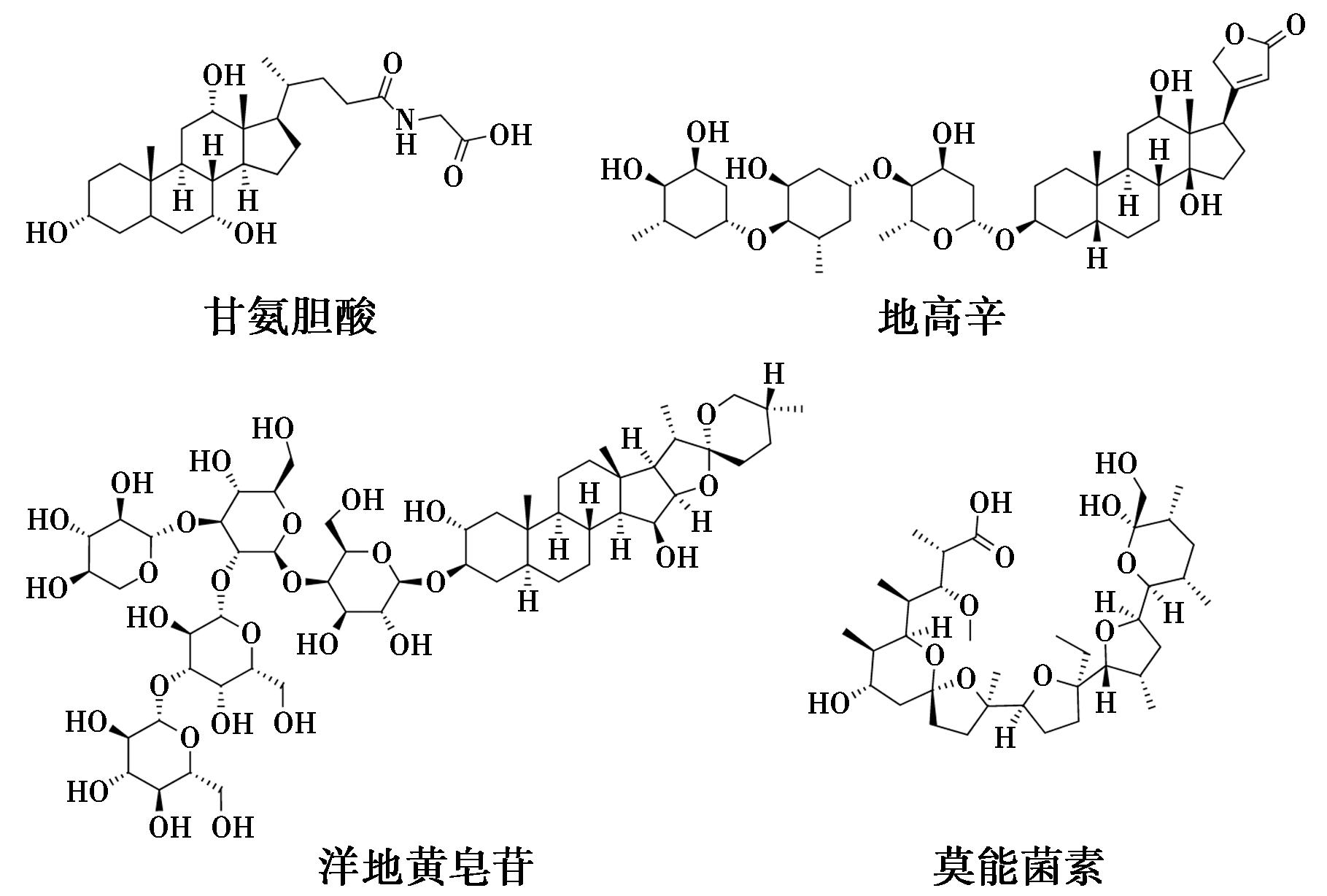
图21 M6L4配位笼-天然产物结晶实例[42]
Fig.21 Crystallization examples of M6L4 coordination cages with natural products[42]
1.6 适用于亲核化合物的晶体海绵
对于生物碱等亲核性化合物来说,很难使用传统的晶体海绵法进行分析。针对这一问题,Nakagawa等[43]报道了一种新型金属有机框架APF-80。该框架是由CoBr2、3-吡啶基、4-吡啶基混合取代的六氮杂苯烯配体(344-TPHAP)和 1,4-苯二羧酸在DMA溶液中反应合成的。其中Co2+中心存在两个彼此相邻开放的金属位点,这种双开放的位点可以通过与Co2+形成配位键,使得APF-80对含氮、氧、硫等亲核基团的化合物表现出优异的兼容性(图22)。此外,APF-80还结合了水介导的氢键网络,为客体捕获提供了多重作用位点。研究成功实现了咖啡因、尼古丁、奎宁、奎宁丁、金雀花碱、吴茱萸次碱等生物碱的结构确定,扩大了晶体海绵法可分析化合物的范围(图23)。
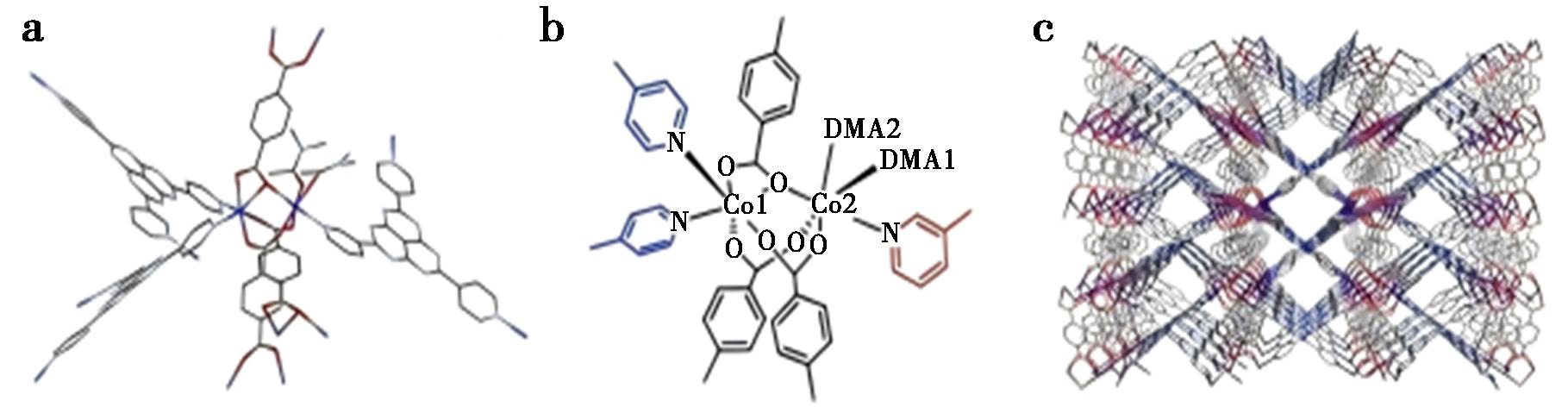
图22 a.Co2+配体和周围配体的结构;b.Co2+配体的化学表示,红色和蓝色分别代表3-吡啶基和4-吡啶基团;c.APF-80沿a轴的三维结构[43]
Fig.22 a.Structure of the Co2+ dimer and the surrounding ligands;b.Chemical representation of the Co2+ dimer,red and blue colors respectively show 3-pyridyl and 4-pyridyl groups;c.View of the three-dimensional structure of APF-80 along the a-axis[43]
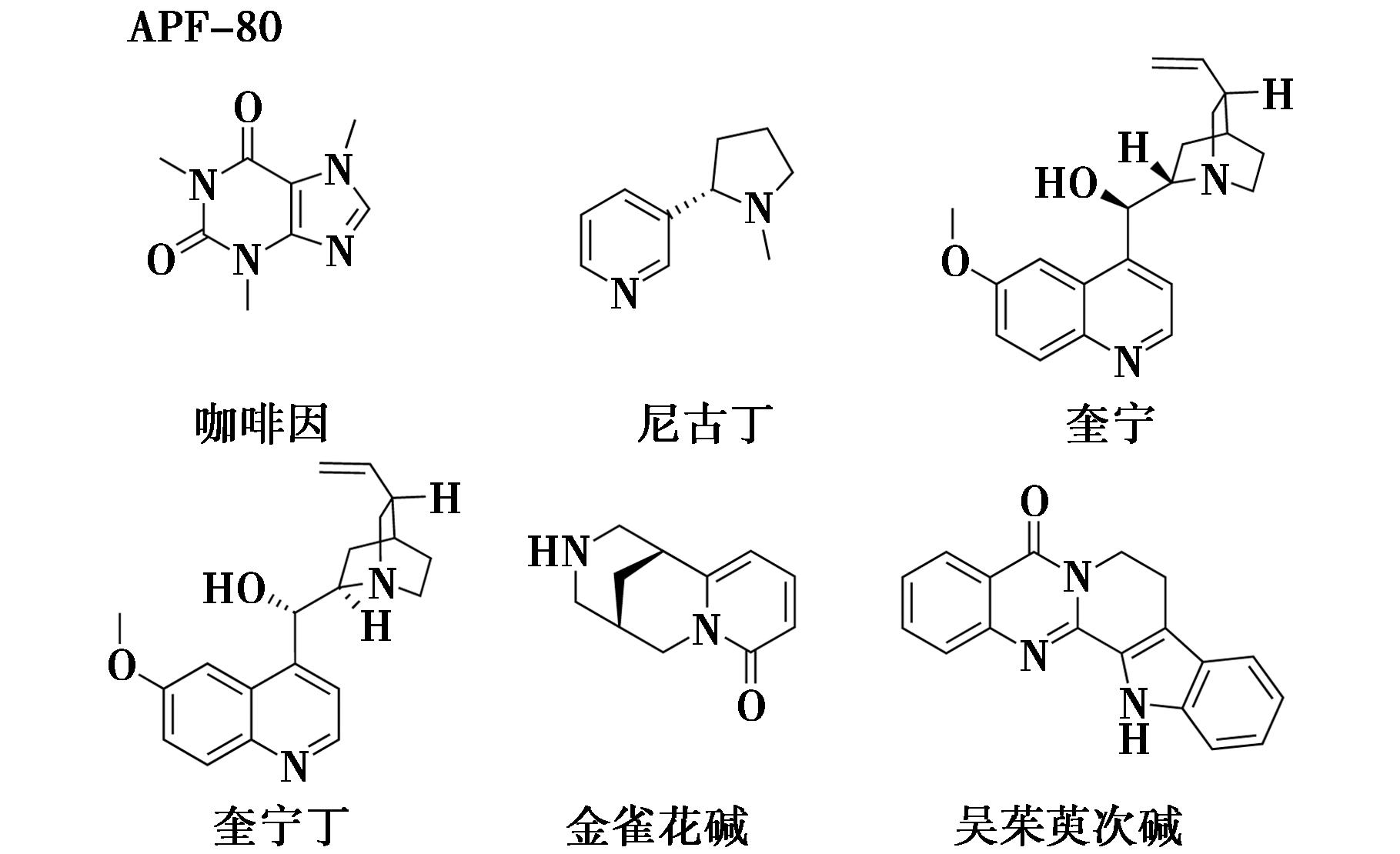
图23 APF-80-天然产物结晶实例[43]
Fig.23 Crystallization examples of APF-80 with natural products[43]
2 结晶伴侣法
近年来,柔性框架或适应性孔隙成为材料科学和分子识别的重要研究领域。与MOFs相比,非固有通道的灵活框架具有自适应孔径的优势,使其能够更好地容纳和封装客体分子。采用非固有通道结构的框架材料与有机分子形成共晶的结晶伴侣法,在天然产物结构确定中展现出独特优势。一般可采用液体扩散、缓慢蒸发结晶、降温等方式来获得客体分子与结晶伴侣共晶体。根据主体分子的不同,可分为:具有自适应孔隙的金刚烷类衍生物(Tetraaryladamantanes,TAAs),具有高适应性和耐用性的环状三核Ag(I)吡唑盐配合物,具有半开放和可调节空腔的分子夹,具有独特空腔结构的大环衍生物和具有柔性氢键的主体框架材料等。
2.1 基于金刚烷衍生物的TAAs
以四芳基金刚烷为代表的结晶伴侣是一类高度对称的刚性化合物,其分子结构中存在4个芳香族基团,可帮助客体化合物在金刚烷主体间隙中实现长程有序的排列,继而形成高质量的共晶体。
2015年,Schwenger等[44]开发了金刚烷类衍生物的结晶伴侣法,通过合成4种四芳基取代的金刚烷类衍生物,观察到只有1,3,5,7-四(2,4-二甲氧基苯基)金刚烷(TDA)具有容纳客体分子的能力,并且通过简单的溶剂处理或再结晶即可实现客体分子的释放。2017年,Alexandre等[45]发现TDA的同系物1,3,5,7-四(2,4-二乙氧基苯基)金刚烷(TEO)不仅具有包合分子的能力,还可以形成高负载的晶体结构,更有利于分子储存。2020年,Casco等[46]还发现TDA与TEO能够封装多种客体分子,并稳定这些客体分子以阻止副反应的发生,因而提出了封装有机晶体(Encapsulation organic crystals,EnOCs)的概念,并将EnOCs与超过100种的小分子共结晶,通过SCXRD确定了它们的结构,正式地将EnOCs应用于有机小分子绝对构型的测定[47]。
为扩大客体分子的适用范围和种类,Krupp等[48]进一步合成了1,3,5,7-四(2-溴-4-甲氧基苯基)金刚烷(TBro,图24a)。通过在母核上引入Br原子,不仅加强了主体与亲脂性化合物的相互作用,同时Br原子产生的异常散射,也提高了α-蛇麻烯、麝香酮等结构确证结果的准确度。该团队以TDA、TEO和TBro作为结晶伴侣,在与柠檬烯、香芹酮、α-侧柏酮、芳樟醇、丁香酚、苯乙醇等52种不同客体化合物进行共结晶试验时(图25),发现其中88%的化合物形成了共晶,77%的化合物得到了高分辨率的结构数据。基于这一成果,Krupp等[48]创新性提出了“光谱-共结晶耦合方法”(Spectroscopy cum crystallization,SCC),他先将尼古丁溶解在CD2Cl2中进行核磁共振光谱分析,然后在核磁管中加入TEO,溶解后作为结晶伴侣,在氮气中挥发溶剂,16 h后将获得的共晶体进行了X射线晶体学分析,成功地解析了尼古丁的绝对构型(图24b)。
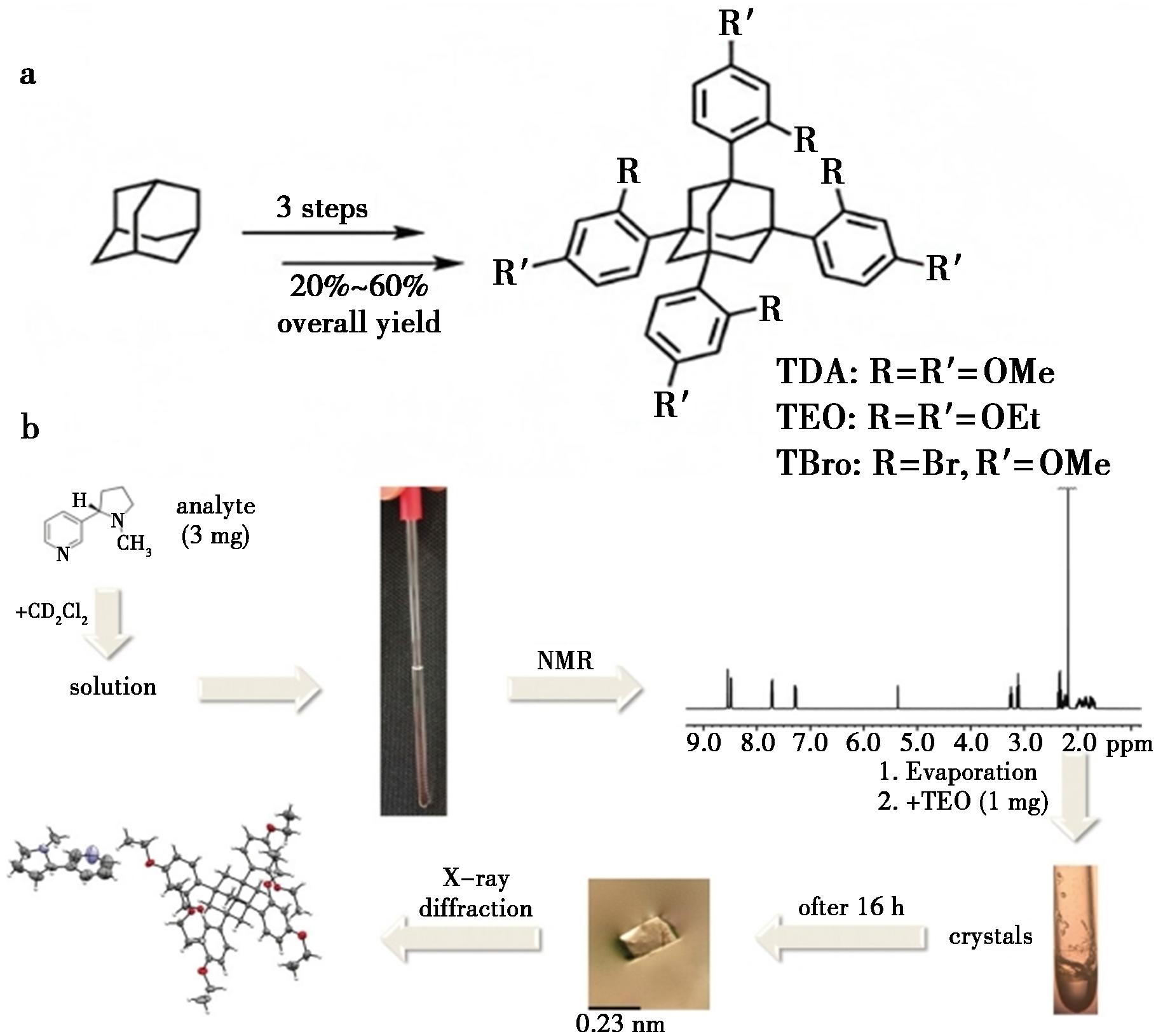
图24 a.TDA、TEO和TBro的结构图;b.SCC方法的示意图[48]
Fig.24 a.Structural analysis of TDA,TEO and TBro;b.Schematic diagram of the SCC method[48]
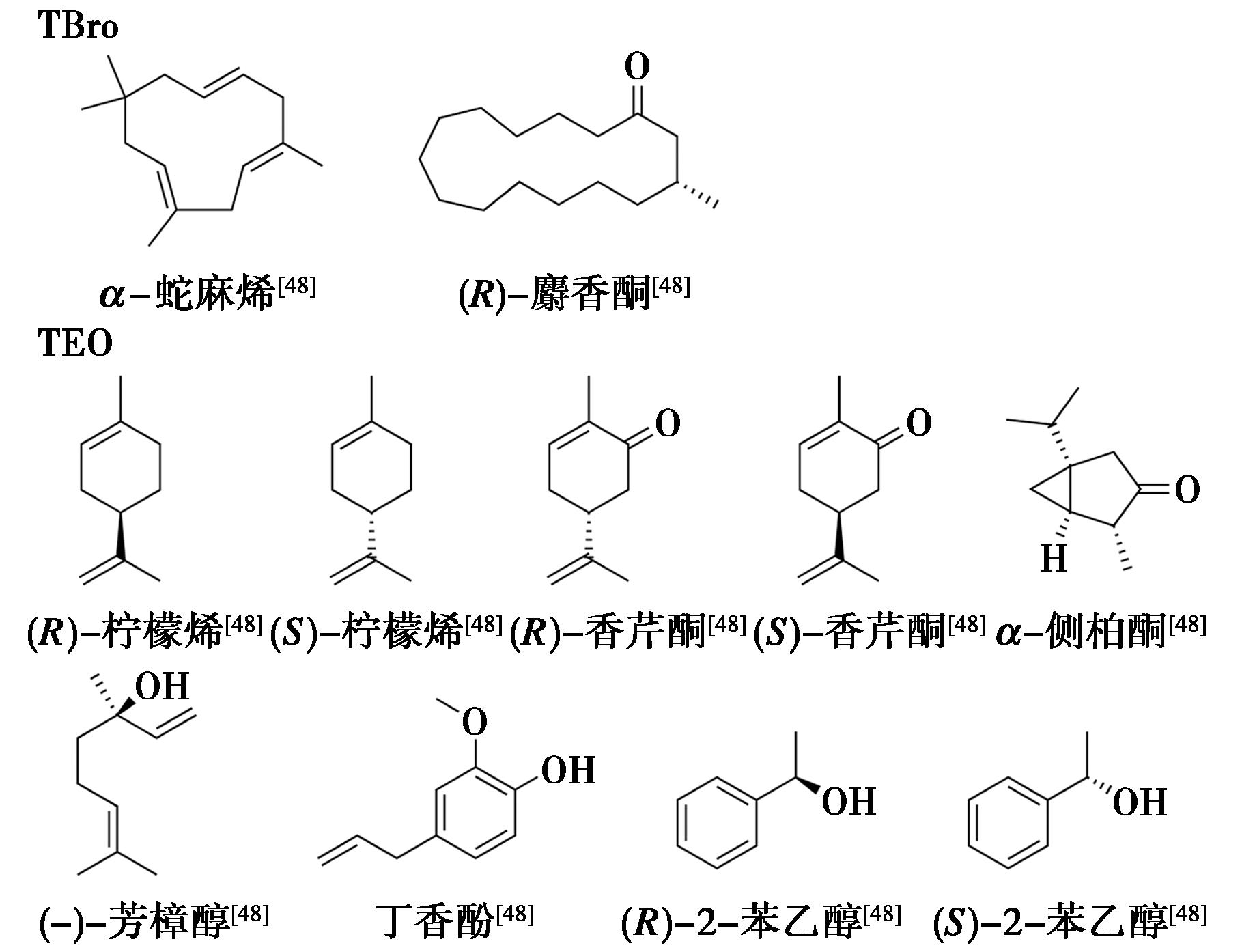
图25 TEO和TBro-天然产物结晶实例[48]
Fig.25 Crystallization examples of TEO and TBro with natural products[48]
此外,Li等[49]在2023年开发并合成了一种基于蒽环的结晶伴侣1,3,5,7-四(4-(10-甲氧基蒽-9-基)苯基)金刚烷(TMAPA),采用氯苯和四氢呋喃作为辅助溶剂将难以自行结晶的油性有机分子与TMAPA结合以形成共晶。通过在结构中引入蒽环,增加了金刚烷4个取代基的臂长,提高了捕获客体分子的成功率(图26)。该团队尝试将乙酸香叶酯、乙酸松油酯、苯甲醚、橙花醇等56种油性有机分子与TMAPA共结晶(图27),成功获得了47种高分辨率共晶体结构数据,充分证明了TMAPA主体对各类油性化合物的适用性。
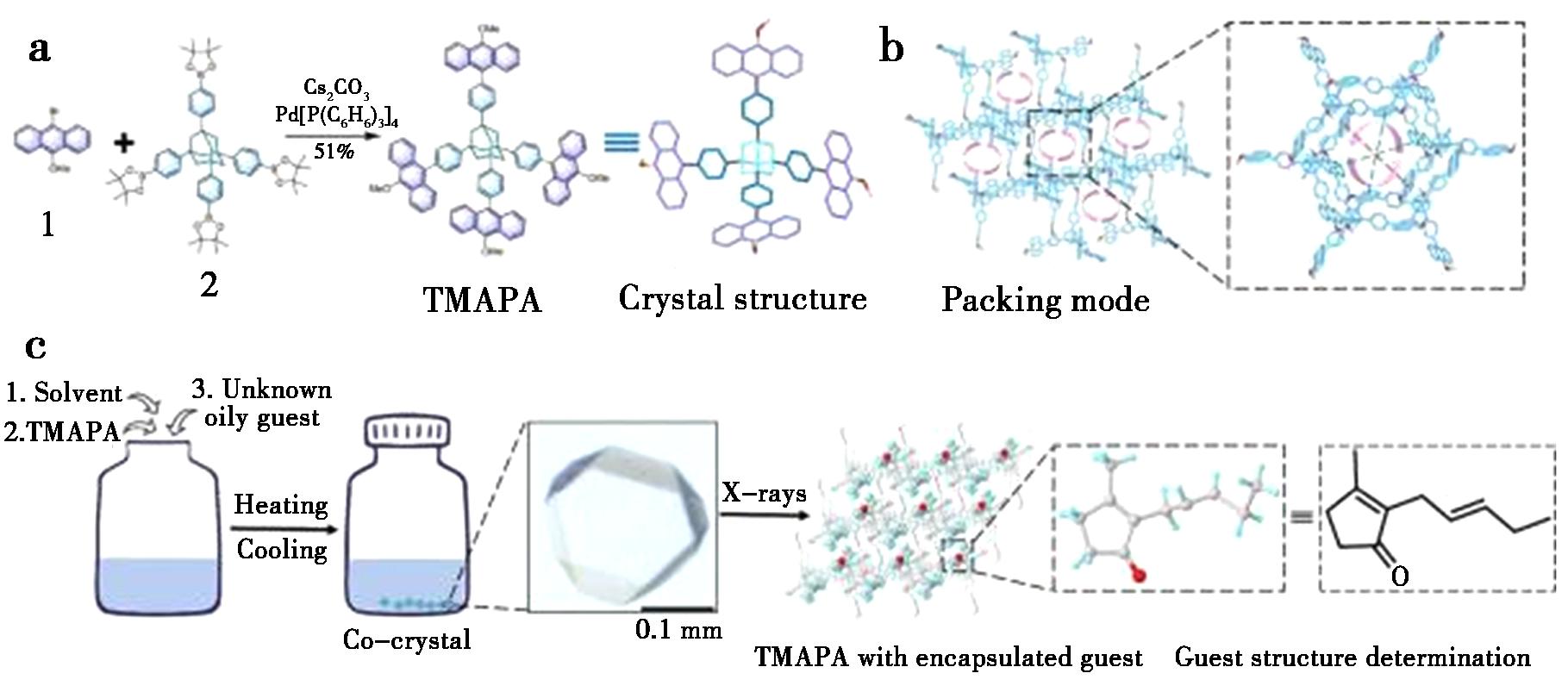
图26 a.TMAPA的合成和晶体结构;b.TMAPA的堆积模型;c.溶剂辅助共结晶方案[49]
Fig.26 a.Synthesis and crystal structure of TMAPA;b.Packing model of TMAPA;c.Solvent-assisted co-crystallization scheme[49]
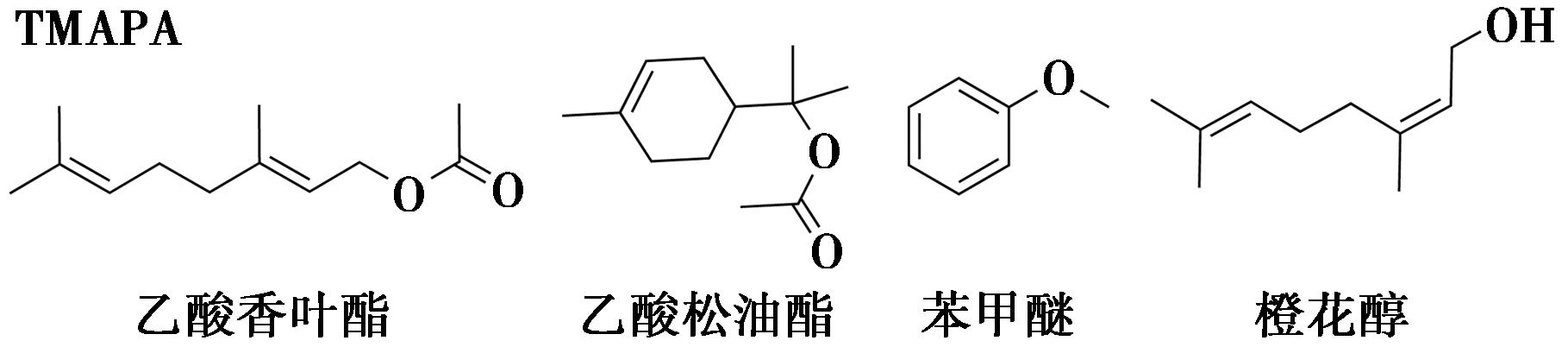
图27 TEO和TBro-天然产物结晶实例[49]
Fig.27 Crystallization examples of TEO and TBro with natural products[49]
2024年,Berking等[50]成功地合成了一种新型的氟化结晶伴侣1,3,5,7-四(2-氟-4-甲氧基苯基)金刚烷(TFM)用于解析柔性较强的无环化合物(如三烯烃、醛、醇、脂肪酸、倍半萜类和萜烯类等),研究实现了月桂烯、(R)-香茅醛、(R)-乙酸香茅酯、正癸醛、乙酸金合欢酯、(7R,11R)-乙酸植醇酯等柔性化合物的结构解析(图28)。与TDA、TEO、TBro相比,TFM的合成方法更为简便,形成的晶体结构分辨率更高,并且有利于形成促进晶体生长、提高晶体稳定性、辅助晶体表征的溶剂化物。但在尝试包封甾醇类化合物角鲨烯(分子量411 g/mol)时发现,由于长脂肪链的摆动导致共晶体中的客体存在严重无序,这是目前TAAs能够包封分子量的上限(图29)。
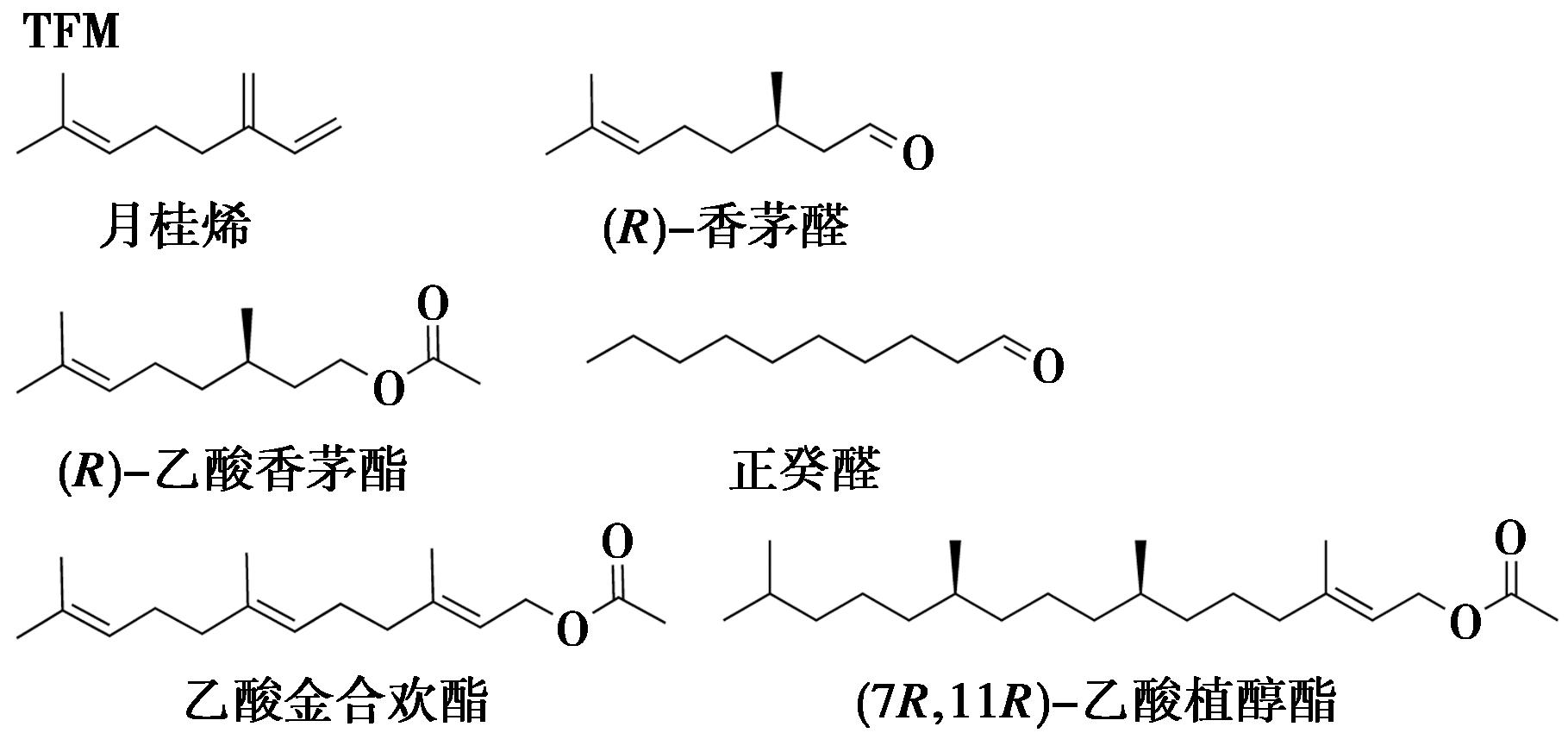
图28 TFM-天然产物结晶实例[50]
Fig.28 Crystallization examples of TFM with natural products[50]
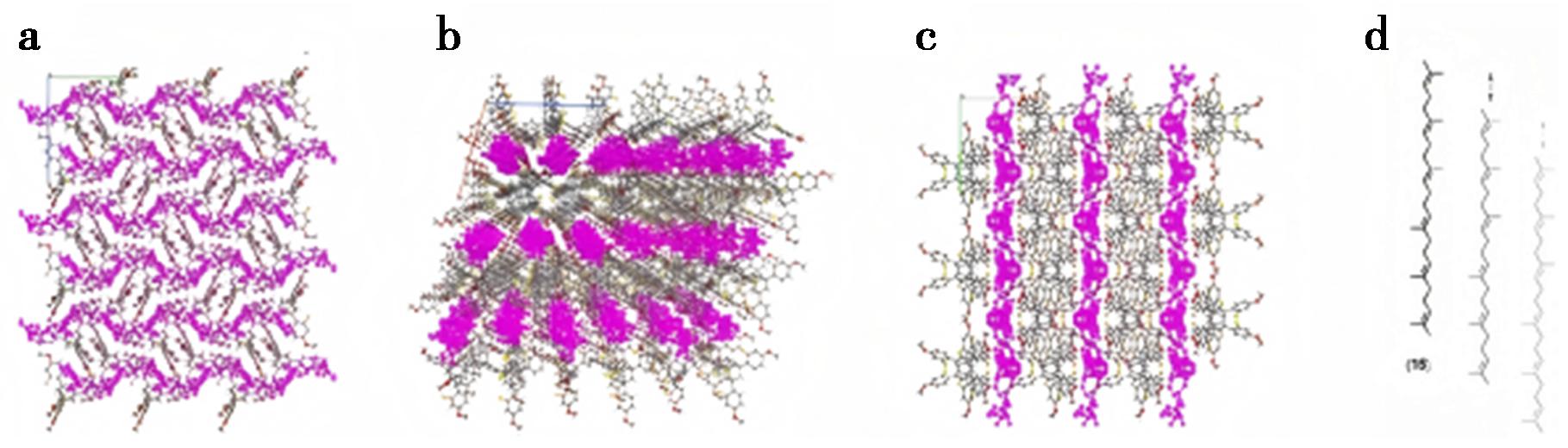
a.沿晶胞a轴方向视图;b.沿晶胞b轴方向视图;c.沿晶胞c轴方向视图;d.角鲨烯的化学结构
图29 TFM与角鲨烯的晶体堆积[50]
Fig.29 TFM crystallized with squalene[50]
2.2 基于环状三核配合物的Ag3Pz3
环状三核配合物(Cyclic trinuclear complexes,CTCs)是由3个单价金属阳离子和3个桥联杂环配体构成的平面配位化合物。它们是多功能的超分子配体,可以提供与各种客体的超分子相互作用的位点。由于CTCs的π-酸性/碱性可以通过改变金属阳离子、桥接配体和配体上的取代基来进行调节,这些特征可以促进其与天然产物分子结合进而确证客体结构。2023年,Song等[51,52]开发合成了一类高度氟化的环状三核Ag(I)吡唑盐配合物(Ag3[3,5-(CF3)2Pz]3,Ag3Pz3)(图30a)。Ag3Pz3通过其平面九元Ag3N6金属环的强π-酸性,使其能够与具有富电子基团的化合物稳定结合。通过引入三氟甲基不仅提高了Ag3Pz3在常规溶剂(如环己烷、二氯甲烷、乙腈和甲醇等)中的溶解度,而且能够与结合分子发生多重C—H…F的相互作用,进一步降低了所结合客体分子的热运动自由度。另外,Ag原子的异常散射,也提高了手性分子绝对构型鉴定的准确度。
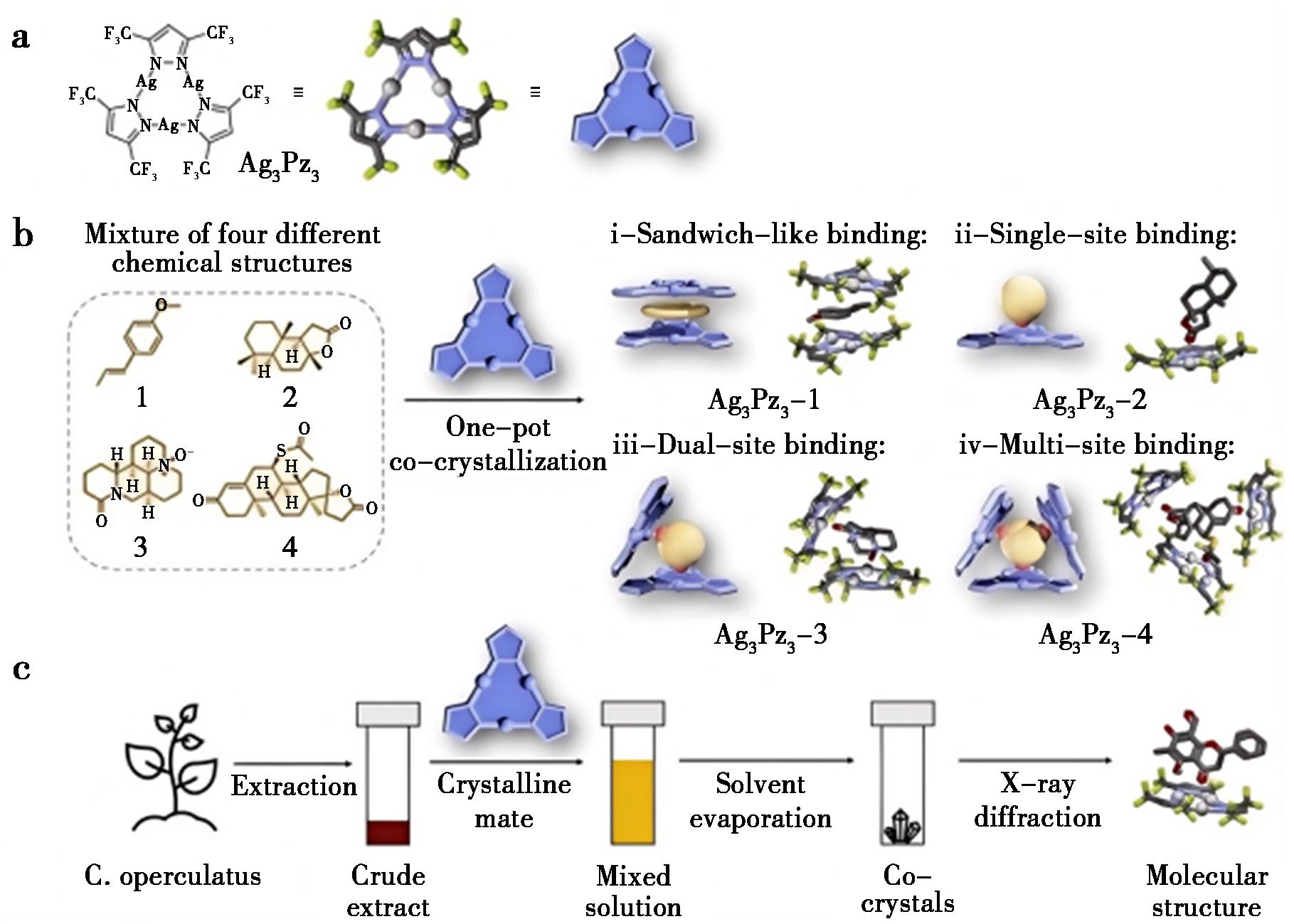
图30 a.Ag3Pz3的化学结构和晶体结构;b.在Ag3Pz3的共晶体中观察到的4种相互作用模式;c.水翁花粗提物与Ag3Pz3共结晶的工作流程[52]
Fig.30 a.Chemical and crystal structures of Ag3Pz3;b.Four interaction patterns identified within Ag3Pz3cocrystals;c.Workflow for the cocrystallization of Cleistocalyx operculatus crude extract with Ag3Pz3[52]
Ag3Pz3具有高度适应性,能够根据客体大小、形状和电子富集位点调整堆积模式。具有平面结构的含氧的有机分子通常都以三明治状的结合模式嵌入进两个平行的Ag3Pz3之间,相比之下,具有非平面结构的含氧的有机分子,因其含有的酮羰基或酯羰基具有较强的Lewis碱性,可优先与Ag3N6金属环的π-酸形成单位点、双位点或多位点的结合模式(图30b)。研究发现,在形成的共晶体中,有机分子与Ag3Pz3之间的平面距离小于Ag原子与C原子VDW半径之和,表现出很强的酸碱相互作用;并且,研究人员基于Hirshfeld划分的独立梯度模型进一步得出晶体结构中存在着强烈的范德华相互作用及显著的静电势吸引作用的结论,这些相互作用在一定程度上提高了晶体结构的稳定性。
Song等[51]将Ag3Pz3直接用于混合物中有机分子的结构解析和天然产物的粗提物中目标客体的分离与结构解析,如将Ag3Pz3溶解于水翁花(Cleistocalyx operculatus)的粗提物中,在室温下缓慢蒸发溶剂,获得了4种晶胞参数不同的晶体,成功表征了水翁花提取物中5种成分的化学结构(化合物26~30),其中包括2个新的黄酮类化合物(图31),极大地提高了混合物分离和结构鉴定的速度(图30c)[52]。
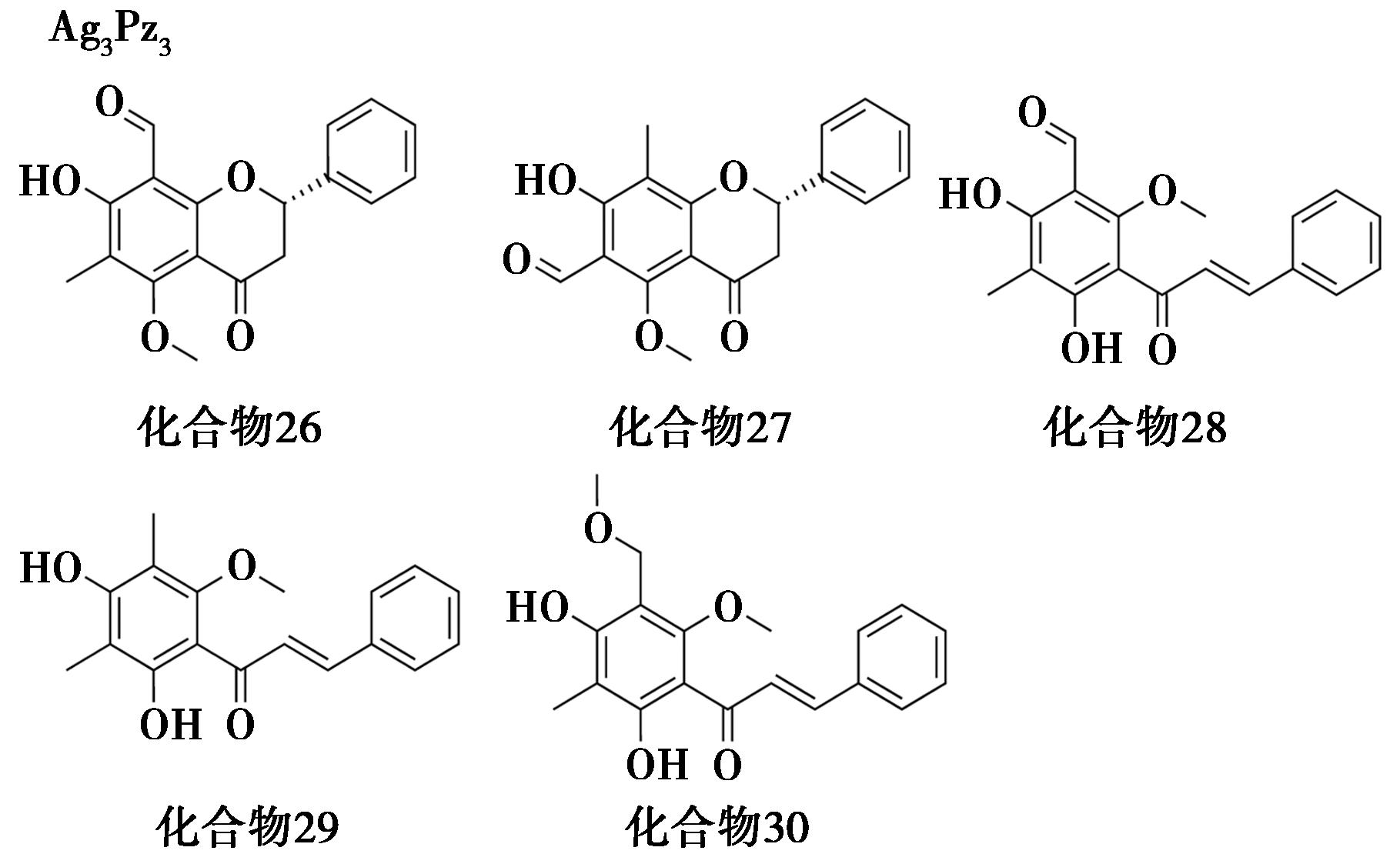
图31 Ag3Pz3-水翁花粗提物中化学成分结晶实例[51]
Fig.31 Crystallization examples of Ag3Pz3 with chemical components in the crude extract of Cleistocalyx operculatus[51]
然而,CTCs也存在一定的局限性。首先,具有强氧化或还原电位的客体可能损害CTCs的结构(如抗坏血酸或间氯过氧苯甲酸)[51];其次,以Ag3Pz3为代表的CTCs主要结合平面或含氧客体,对缺乏富电子基团的化合物结合能力较弱或不结合;另外,非手性的Ag3Pz3无法区分对映异构体。因此,为进一步的完善CTCs的功能,可尝试调节CTCs的酸碱性或在配体上引入手性取代基,以扩大其应用范围。
2.3 基于甘脲衍生物的分子夹
2020年,Liu等[53]合成了甘脲类分子夹,因其具有半开放、刚性的空腔,在不同溶剂中会形成多通道堆积结构,为液态分子的结构确证提供了新的方法。两个蒽基团作为分子夹的“臂”,环醚作为间隔基,因结构中含有羰基富电子基团,可通过电子转移与缺电子的客体分子形成稳定的共晶体,这些特性使分子夹在不同溶剂中形成多通道堆积结构,从而适应不同大小的客体分子。为验证分子夹的“夹取”能力,团队选取了六氟苯、均三甲苯、2,6-二异丙基苯胺和乙基邻氨基苯甲酸酯液体分子,结果均在共晶体结构观察到了液体分子通过C-H-π、C-H-O和π-π堆叠等分子间特异性相互作用被固定在分子夹的腔内或外部(图32)。然而,在尝试封装较大分子量的棕榈油酸时,未能得到共晶。由于共晶的形成依赖于分子夹的开放腔体和多通道堆积结构,对于大体积、大分子量的液态分子仍有一定局限性。
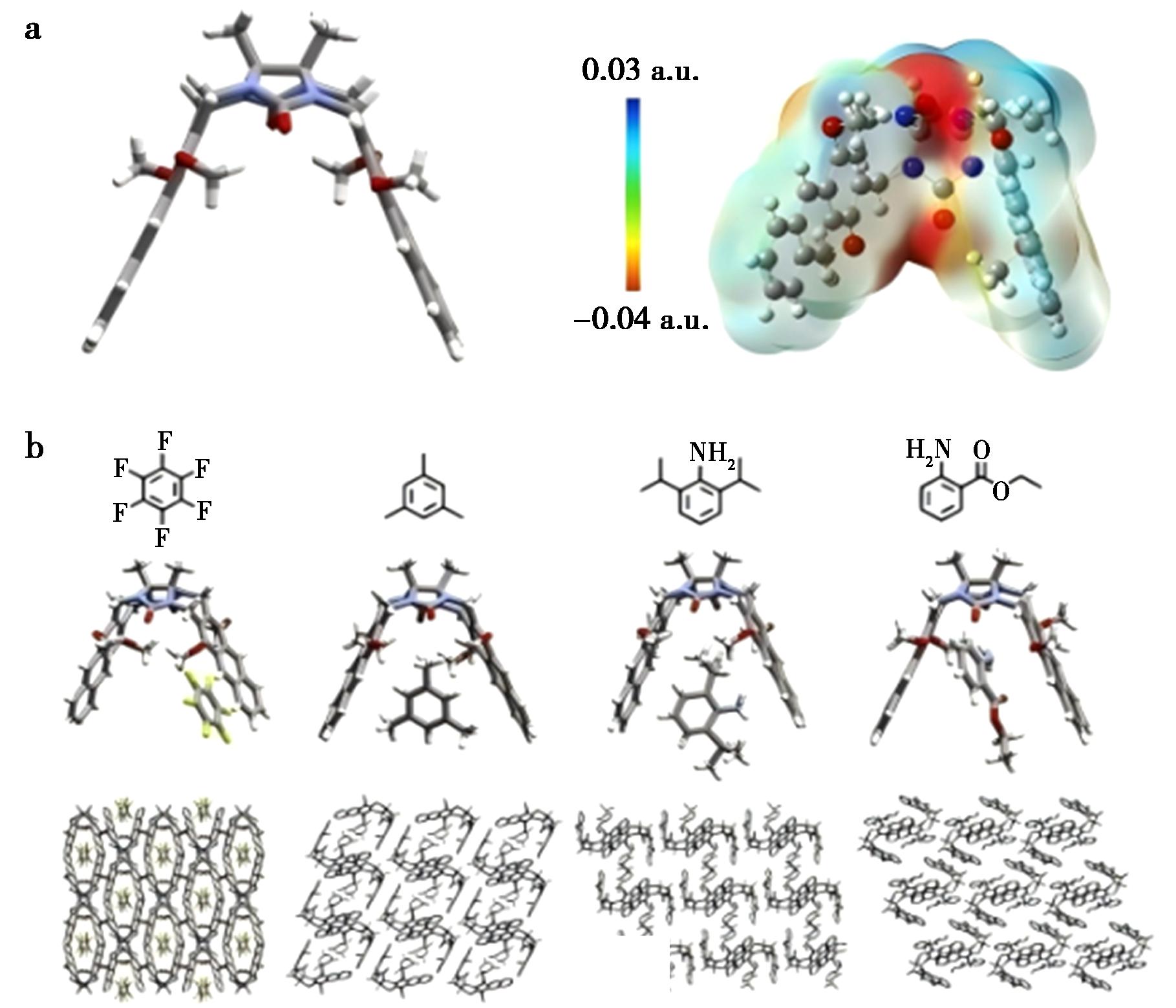
图32 a.分子夹的晶体结构和静电势表面;b.六氟苯、均三甲苯、2,6-二异丙基苯胺、乙基邻氨基苯甲酸酯的化学结构、晶体结构和堆积结构[53]
Fig.32 a.Crystal structure and electrostatic potential surface of the molecular clip;b.Chemical structure,crystal structure and packing structure of hexafluorobenzene,mesitylene,2,6-diisopro pylaniline,ethyl anthranilate[53]
2.4 大环衍生物
大环分子是超分子系统的重要组成部分,具有独特的空腔结构。特别是磷酸化大环,因其结构中存在刚性、易自结晶的基团,如苯、萘、蒽及菲等,这些特性使其能够作为主体分子,通过非共价键相互作用,选择性地结合和识别特定类型的客体分子并且辅助其结晶,通过SCXRD实现结构测定。
Pinalli等[54]报道了3种四磷酸盐空腔体(Tiiii[H,CH3,CH3],H1)、(Tiiii[C3H7,CH3,C2H5],H2)和(Tiiii[C3H6Py+Cl-,CH3,C2H5],H3),这3种空腔体在甲醇和水两种溶剂中通过阳离子-偶极和氢键等不同的分子间相互作用选择性地结合并封装丙氨酸、亮氨酸、丝氨酸等15种氨基酸分子,尤其是大环H1具有封装各种氨基酸盐酸盐的能力(图33)。
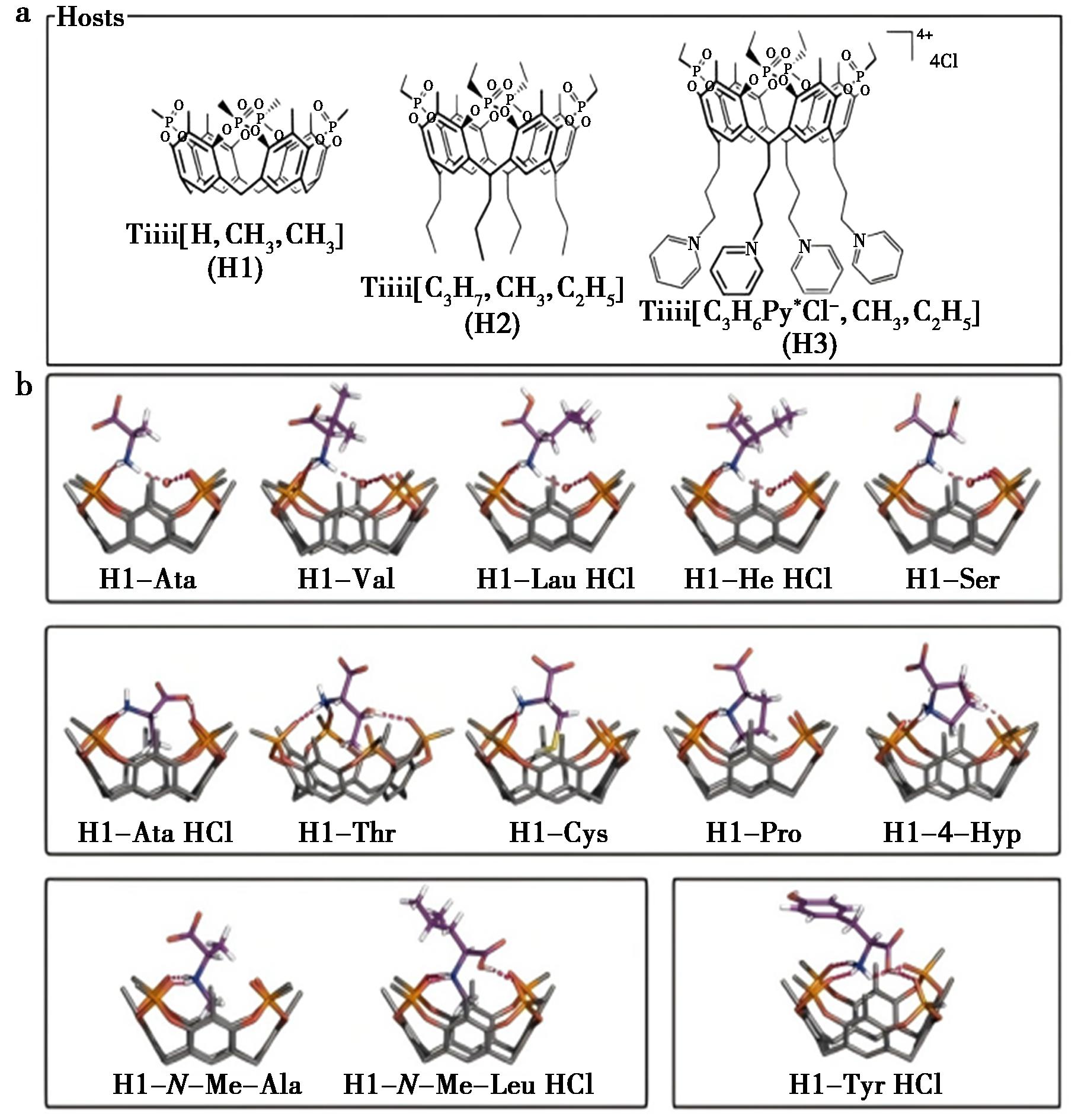
图33 a.3种四膦酸盐空穴(H1,H2,H3)的结构;b.H1与13个氨基酸盐酸盐配合物的晶体结构侧视图[54]
Fig.33 a.Structure of three tetraphosphonate cavitands (H1,H2,H3);b.Side views of the molecular structures of H1 with 13 amino acid hydrochloride complexes[54]
Jiao等[55]开发了一种新型的环磷酰胺衍生物CTX[P(O)Ph](图34),因其具有丰富氢键供体、磷氧双键提供的负电势表面以及富电子的空腔,这类结构能够有效的捕获油性客体分子并实现有序地排列。此外,P原子的异常散射提高了手性客体分子绝对构型确定的准确度。该研究团队利用CTX[P(O)Ph]实现了肉桂醛、丁香酚、丁香酚、覆盆子酮等油性客体分子的结构解析(图35)。然而,CTX[P(O)Ph]的有限空腔限制了其与较大的客体分子的相互作用。因此,Li等[56]在2,7-OH-F[3]A1的中间环引入桥联的苯基氧化膦基团,合成了具有更大空腔与更多电荷结合位点的F[3]A1-[P(O)Ph]3。
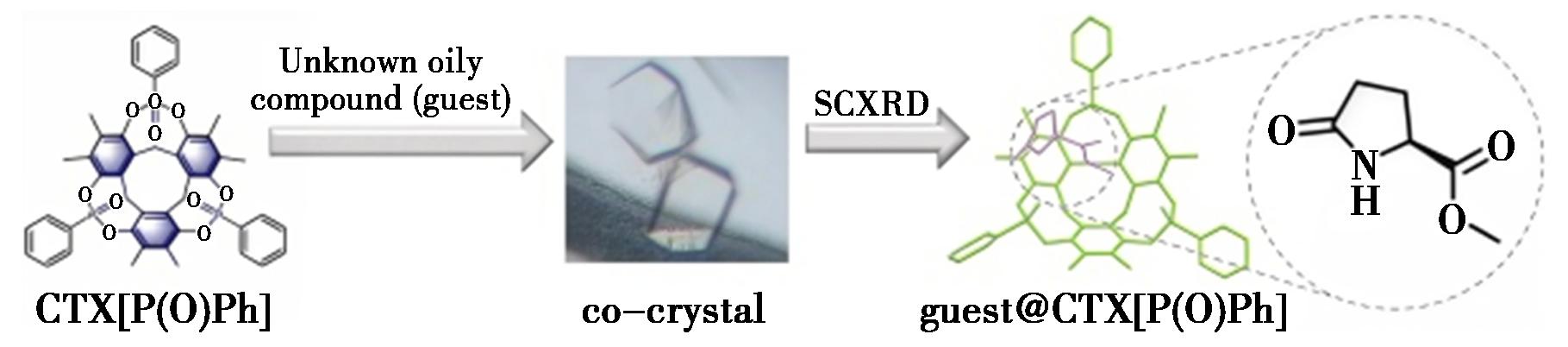
图34 CTX[P(O)Ph]与油性化合物的结晶示意图[55]
Fig.34 Schematic diagram of the crystallization of CTX[P(O)Ph] with oily compounds[55]
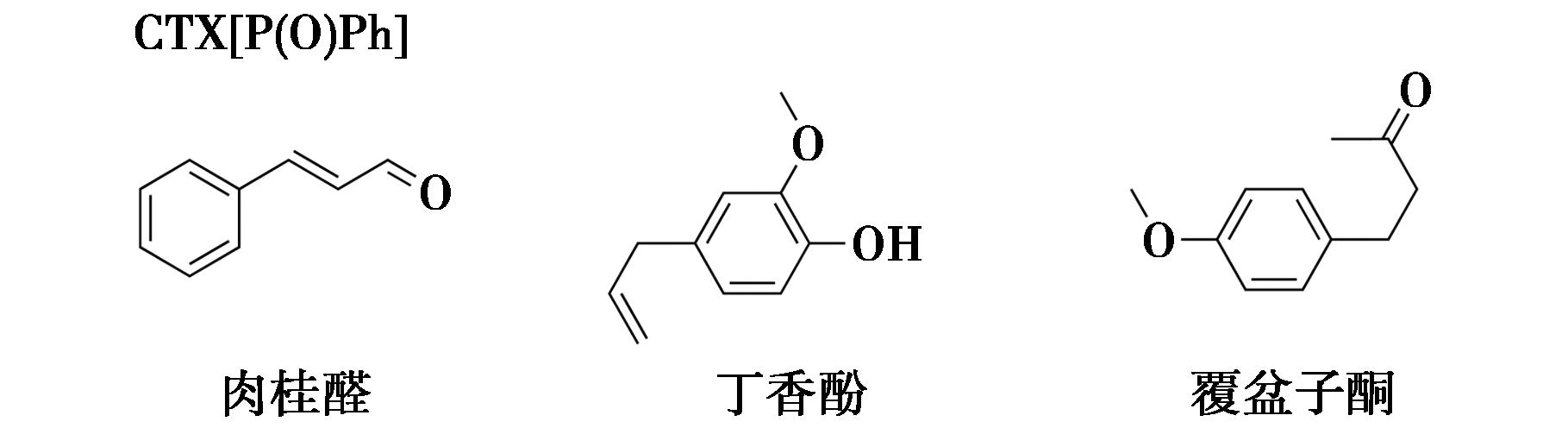
图35 CTX[P(O)Ph]-天然产物结晶实例[55]
Fig.35 Crystallization examples of CTX[P(O)Ph] with natural products[55]
2.5 氢键有机框架
1994年,Russell等[57]报道了基于胍离子-有机磺酸硫离子的二维氢键网络框架[Guanidinum cations(G,C(NH2)3+,GS)和Organomonosulfonate anions(S,RSO3-)],该网络框架具有灵活的N—H…O—S氢键构成的层链状结构(图36a),通过其收缩封装客体分子,GS降低了客体分子的无序概率,并实现了100%的客体占有率。其框架结构和晶体排列会因有机单磺酸盐的结构、客体分子尺寸与形状的不同而变化。主体框架中硫原子的异常散射也提高了手性分子绝对构型确定的准确度。
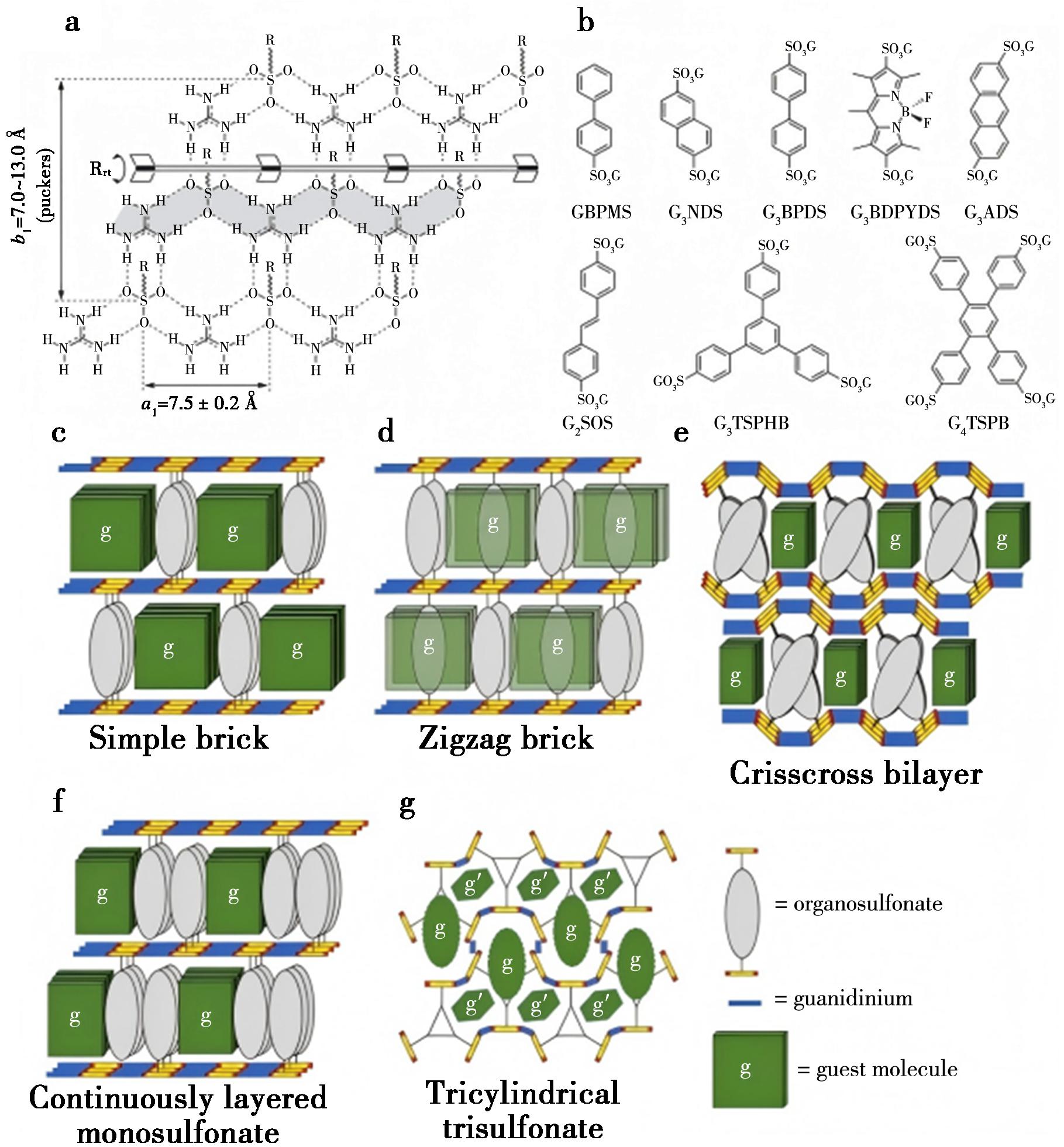
图36 a.由氢键构成的层链状结构的GS示意图;b.GS框架结构中使用的代表性有机磺酸胍;c~e.二磺酸胍架构:简单砖状结构、锯齿形砖状结构、交错双分子层;f.单磺酸胍的连续多层架构;g.G3TSPHB作为主体三圆柱形架构[58]
Fig.36 a.Schematic of a quasi-hexagonal GS sheet highlighting the hydrogen-bonded hinge mechanism;b.Representative organic sulfonated guanidines used in the GS framework structure;c~e.Disulfonated guanidine architectures:simple brick structure,zigzag brick structure,staggered double molecular layers;f.Continuous multi-layer architecture of monosulfonated guanidine;g.G3TSPHB as the main three-cylinder architecture[58]
GS主体框架可根据胍与有机磺酸盐的化学计量比分为单磺酸胍、二磺酸胍、多磺酸胍。通常情况下,单磺酸胍更易形成包合物[58]。研究发现,氢键主体框架能够适应不同客体分子,灵活地调整其在晶格中的堆积模式,呈现出多种结构,包括简单砖状结构、锯齿形砖状结构、交错双分子层、连续多层、三圆柱形结构等(图36c~36g)。
Russell利用GS、晶体海绵法以及改进的晶体海绵法对愈创木酚和2,6-二异丙胺的结构解析进行比较。结果发现,3种方法分别在24 h内、数周及10 d内获得了适合SCXRD分析的晶体。该团队还利用具有快速、精准结合客体分子能力的GS主体框架(图36b),在室温下缓慢挥发培养得到了薁、(+)-香紫苏内酯、屈螺酮、孕酮、乙酸橙花酯等晶体包合物(图37)。此外,Dillon等[59]报道的一种新型GS主体-环己烷单磺酸胍(GCHMS)能与不同形状、尺寸和化学性质的客体形成包合物,并呈现出“架构异构”现象。该现象源于有机磺酸基团在GS片层上具有可变的投影拓扑结构,从而产生多种框架异构体。与先前使用的芳基单磺酸胍盐相比,GCHMS在包封脂肪族客体时展现出更广泛的适用性。通过SCXRD分析,这些采用传统方法难以结晶的有机化合物的绝对构型均获得了高精度的结构解析数据。
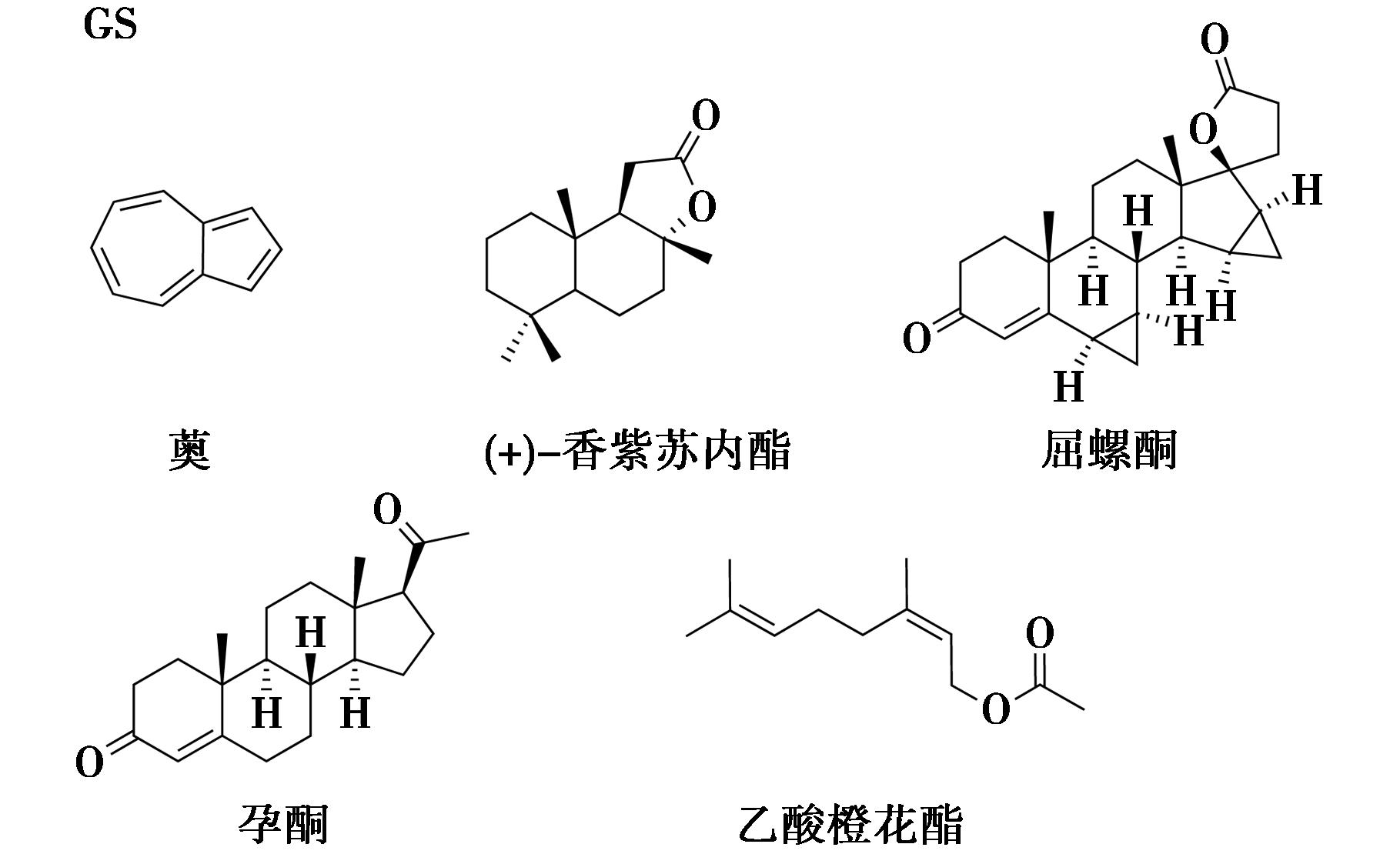
图37 GS-天然产物结晶实例[58]
Fig.37 Crystallization examples of GS with natural products[58]
Brummel等[60]将GS框架概念拓展至有机硫酸盐(R-OSO3-),设计合成了作为新型氢键有机框架的有机硫酸胍盐。Chaudhry等[61,62]开发出具有晶格可预测性的![]() 框架,该框架通过1,3,6,8-芘四磺酸四钠盐(Na4·PYR)与胍(G)结合获得。基于稳固的π-π堆积与氢键作用,
框架,该框架通过1,3,6,8-芘四磺酸四钠盐(Na4·PYR)与胍(G)结合获得。基于稳固的π-π堆积与氢键作用,![]() 框架成功包封了咖啡因等活性成分。
框架成功包封了咖啡因等活性成分。
3 展望与讨论
获得天然产物晶体结构对分析药物构效关系和加速药物开发至关重要,然而传统SCXRD在获得高质量晶体方面具有一定的挑战性。因此,创新型的结晶辅助策略—晶体海绵法和结晶伴侣法,在确定天然产物绝对构型方面展现出了独特优势,并且随着研究的深入,不断扩大了这些方法的应用范围。首先,晶体海绵的固有多孔框架结构提供了与油状及柔性等客体分子相互作用的位点,使其得到稳定排列,进而实现精确结构的鉴定;结晶伴侣可根据客体分子的大小、形状,自适应地调整框架结构,通过主客体间的相互作用,有效地限制客体分子热运动的自由度,保证结构确证的可靠性。其次,研究人员针对“特定”分子“定制”性地开发出合适的主体框架,扩大了天然产物结构研究的分析范围。例如,设计出了手性MOF材料以准确结合具有不同类型的多手性天然产物;合成出了以Ag原子为核心的环状三核配合物,将结构分析范围由简单的有机分子延伸到复杂的天然产物。值得注意的是,主客体相互作用的分析和可视化对于理解结晶层和客体之间的结合原理是十分必要的。研究人员可通过 Hirshfeld划分的独立梯度模型,既能够精确分析分子间相互作用的强弱,又能清楚地理解主客体之间的作用机制。
为进一步提高晶体培养的成功率、结构分析的效率与准确度,未来的研究方向将继续集中在技术和方法的融合上。例如,晶体结构预测(Crystal structure prediction,CSP)技术,通过计算模拟给定化学成分的稳定或亚稳态晶体结构,降低晶体缺陷,从而减少试错成本。它还具有识别多晶型物、预测晶体堆积的能力,使得其在单晶培养上具有广泛的应用;此外,人工智能(AI)和机器学习相结合,通过自动化、智能化地改变结晶过程,可以显著减少单晶生长和结构解析的时间,并可能为分析复杂天然产物的结构提供新的方案。值得注意的是,药物共晶已被成功证明能够提高药物活性成分的生物利用度,改善其药动学及药效学性质。这些先进的技术和方法将推动晶体学的发展,为天然产物及药物分子的结构解析不断提供新视角,更推动药物创新领域实现新突破。
[1]Newman D J,Cragg G M.J.Nat.Prod.,2016,79(3):629-661.
[2]Tu Y Y.Nat.Med.,2011,17(10):1217-1220.
[3]Wani M C,Taylor H L,Wall M E,Coggon P,McPhail A T.J.Am.Chem.Soc.,1971,93(9):2325-2327.
[4]Hansson M J,Elmér E.Neurotherapeutics,2023,20(6):1482-1495.
[5]Seco J M,Qui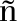 o
o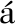 E,Riguera R.Chem.Rev.,2004,104(1):17-118.
E,Riguera R.Chem.Rev.,2004,104(1):17-118.
[6]Kind T,Fiehn O.Bioanal.Rev.,2010,2(1/2/3/4):23-60.
[7]Czarnecki M A,Morisawa Y,Futami Y,Ozaki Y.Chem.Rev.,2015,115(18):9707-9744.
[8]Zhang A H,Tan R X.J.Int.Pharm.Res.,2015,42(6):734-737.张爱华,谭仁祥.国际药学研究杂志,2015,42(6):734-737.
[9]Bunaciu A A,Udri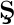 tioiu E G,Aboul-enein H Y.Crit.Rev.Anal.Chem.,2015,45(4):289-299.
tioiu E G,Aboul-enein H Y.Crit.Rev.Anal.Chem.,2015,45(4):289-299.
[10]Li H,Chen R N,Lu Y,Jiang J L,Lin C,Wang L Y.Coord.Chem.Rev.,2025,538:216712.
[11]Inokuma Y,Yoshioka S,Ariyoshi J,Arai T,Hitora Y,Takada K,Matsunaga S,Rissanen K,Fujita M.Nature,2013,495(7442):461-466.
[12]Zigon N,Duplan V,Wada N,Fujita M.Angew.Chem.Int.Ed.,2021,60(48):25204-25222.
[13]Biradha K,Fujita M.Angew.Chem.,2002,114(18):3542-3545.
[14]Inokuma Y,Yoshioka S,Ariyoshi J,Arai T,Fujita M.Nat.Protoc.,2014,9(2):246-252.
[15]Urban S,Brklja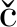 a R,Hoshino M,Lee S,Fujita M.Angew.Chem.Int.Ed.,2016,55(8):2678-2682.
a R,Hoshino M,Lee S,Fujita M.Angew.Chem.Int.Ed.,2016,55(8):2678-2682.
[16]Wada N,Kersten R D,Iwai T,Lee S,Sakurai F,Kikuchi T,Fujita D,Fujita M,Weng J K.Angew.Chem.Int.Ed.,2018,57(14):3671-3675.
[17]Matsuda Y,Mitsuhashi T,Lee S,Hoshino M,Mori T,Okada M,Zhang H P,Hayashi F,Fujita M,Abe I.Angew.Chem.Int.Ed.,2016,55(19):5785-5788.
[18]Zigon N,Kikuchi T,Ariyoshi J,Inokuma Y,Fujita M.Chem.,2017,12(10):1057-1061.
[19]Li K,Yang D S,Gu X F,Di B.Fitoterapia,2019,134:135-140.
[20]Hoshino S,Mitsuhashi T,Kikuchi T,Wong C P,Morita H,Awakawa T,Fujita M,Abe I.Org.Lett.,2019,21(16):6519-6522.
[21]Habib F,Tocher D A,Press N J,Carmalt C J.Microporous Mesoporous Mater.,2020,308:110548.
[22]Hoshino M,Khutia A,Xing H Z,Inokuma Y,Fujita M.IUCrJ,2016,3(2):139-151.
[23]Ramadhar T R,Zheng S L,Chen Y S,Clardy J.Acta Crystallogr.Sect.A Found.Adv.,2015,71(1):46-58.
[24]Ramadhar T R,Zheng S L,Chen Y S,Clardy J.CrystEngComm,2017,19(31):4528-4534.
[25]Ramadhar T R,Zheng S L,Chen Y S,Clardy J.Chem.Commun.,2015,51(56):11252-11255.
[26]Jung Y,Mitsuhashi T,Kageyama K,Kikuchi T,Sato S,Fujita M.Chem,2024,30(39):e202400512.
[27]Kai K J,Sogame M,Sakurai F,Nasu N,Fujita M.Org.Lett.,2018,20(12):3536-3540.
[28]Morishita Y,Sonohara T,Taniguchi T,Adachi K,Fujita M,Asai T.Org.Biomol.Chem.,2020,18(17):3392.
[29]Hara Y,Nakamura A,Manome T,Takaya A,Takahashi H,Ban S,Yaguchi T,Ishibashi M.J.Nat.Med.,2025,79(2):435-440.
[30]Taniguchi Y,Kikuchi T,Sato S,Fujita M.Chem.,2022,28(2):e202103339.
[31]Wada N,Kageyama K,Jung Y,Mitsuhashi T,Fujita M.Org.Lett.,2021,23(23):9288-9291.
[32]Gu X F,Zhao Y,Li K,Su M X,Yan F,Li B,Du Y X,Di B.J.Chromatogr.A,2016,1474:130-137.
[33]Yoshida S,Baba S,Mizuno N,Nakamura Y,Sato S,Fujita M.J.Am.Chem.Soc.,2025,147(27):23917-23922.
[34]Huang W P,Liu J C,Wang F,Xu W,Tao Z M,Middleton D A,Liu C D,Qin S Q,Ye W C,Jiang R W.Inorg.Chem.Front.,2025,12(9):3531-3544.
[35]Cai F,Su X Y,Huang W P,Yuan B,Liu J C,Lai J,Jiang R W.Chem.Reagents,2025,47(11):32-41.蔡放,苏晓昀,黄伟平,袁博,刘金长,赖娟,江仁望.化学试剂,2025,47(11):32-41.
[36]Lee S,Kapustin E A,Yaghi O M.Science,2016,353(6301):808-811.
[37]Zhang S Y,Yang C X,Shi W,Yan X P,Cheng P,Wojtas L,Zaworotko M J.Chem.,2017,3(2):281-289.
[38]Zhang S Y,Fairen-jimenez D,Zaworotko M J.Angew.Chem.Int.Ed.,2020,59(40):17600-17606.
[39]Deng C H,Song B Q,Lusi M,Bezrukov A A,Haskins M M,Gao M Y,Peng Y L,Ma J G,Cheng P,Mukherjee S,Zaworotko M J.Cryst.Growth Des.,2023,23(7):5211-5220.
[40]Tu T N,Scheer M.Chem.,2023,9(1):227-241.
[41]Wu Y T,Shi L,Xu L,Ying J L,Miao X H,Hua B,Chen Z J,Sessler J L,Huang F H.Nature,2025,640(8059):676-682.
[42]He W,Yu Y K,Iizuka K,Takezawa H,Fujita M.Nat.Chem.,2025,17(5):653-662.
[43]Nakagawa T,Wada Y,Chan B,Baba T C,Hanaya K,Koseki Y,Asano R,Aoki K,Usov P M,Kawano M.J.Am.Chem.Soc.,2025,147(32):29013-29025.
[44]Schwenger A,Frey W,Richert C.Chem,2015,21(24):8781-8789.
[45]Alexandre P E,Schwenger A,Frey W,Richert C.Chem,2017,23(38):9018-9021.
[46]Casco M E,Krupp F,Grätz S,Schwenger A,Damakoudi V,Richert C,Frey W,Borchardt L.Adsorption,2020,26(8):1323-1333.
[47]Rami F,Nowak J,Krupp F,Frey W,Richert C.Beilstein J.Org.Chem.,2021,17:1476-1480.
[48]Krupp F,Frey W,Richert C.Angew.Chem.,2020,132(37):16009-16013.
[49]Li H,Jiao J M,Xie W,Zhao Y,Lin C,Jiang J L,Wang L Y.ACS Mater.Lett.,2023,5(10):2673-2682.
[50]Berking T,Hartenfels J,Lenczyk C,Santiso-quinones G,Frey W,Richert C.Angew.Chem.Int.Ed.,2024,63(27):e202402976.
[51]Song J G,Zheng J,Wei R J,Huang Y L,Jiang J,Ning G H,Wang Y,Lu W G,Ye W C,Li D.Chem.,2024,10(3):924-937.
[52]Dobson J T F,Kurz H,Nitschke J R.Chem.,2024,10(4):1038-1040.
[53]Liu Y Z,Chen P P,Shi B B,Jiao T Y,Ju H Q,Liu P R,Huang F H.Org.Chem.Front.,2020,7(5):742-746.
[54]Pinalli R,Brancatelli G,Pedrini A,Menozzi D,Hern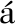 ndez D,Ballester P,Geremia S,Dalcanale E.J.Am.Chem.Soc.,2016,138(27):8569-8580.
ndez D,Ballester P,Geremia S,Dalcanale E.J.Am.Chem.Soc.,2016,138(27):8569-8580.
[55]Jiao J M,Li H,Xie W,Zhao Y,Lin C,Jiang J L,Wang L Y.Chem.Sci.,2023,14(41):11402-11409.
[56]Li H,Li Z J,Lin C,Jiang J L,Wang L Y.Nat.Commun.,2024,15(1):5315.
[57]Russell V A,Etter M C,Ward M D.J.Am.Chem.Soc.,1994,116(5):1941-1952.
[58]Li Y T,Tang S S,Yusov A,Rose J,Borrfors A N,Hu C T,Ward M D.Nat.Commun.,2019,10(1):4477.
[59]Dillon A M,Yusov A,Chaudhry M T,Newman J A,Demkiw K M,Woerpel K A,Lee A Y,Ward M D.Cryst.Growth Des.,2024,24(8):3483-3490.
[60]Brummel B R,Lee K G,McMillen C D,Kolis J W,Whitehead D C.Org.Lett.,2019,21(23):9622-9627.
[61]Chaudhry M T,Newman J A,Lee A Y.Chem.,2024,30(33):e202400957.
[62]Chaudhry M T,Newman J A,Lee A Y,Patel A.Chem.,2024,30(68):e202402958.